Анемия снижение количества гемоглобина (Hb) в единице объема крови, чаще при одновременном уменьшении числа эритроцитов (или общего объема эритроцитов). Терми
| Анемия – снижение количества гемоглобина (Hb) в единице объема крови, чаще при одновременном уменьшении числа эритроцитов (или общего объема эритроцитов). Термин анемия без детализации не определяет конкретного заболевания, а указывает на изменения в анализах крови, выявленные лабораторными методами. Это наиболее частый гематологический синдром. Как известно, синдром – это комплекс симптомов, объединенных единым патогенезом. |
В патогенезе нарушений, возникающих при анемии, ведущую роль играет нарушение оксигенации клеток различных органов и систем. Как следствие тканевой гипоксии возникают нарушение клеточного метаболизма и метаболический ацидоз. Раньше других на гипоксию реагирует ЦНС. Клинически эти патологические процессы проявляются в виде анемического синдрома, который наблюдается при многих заболеваниях и некоторых состояниях. Так его возникновение может быть связано с кровопотерей различного генеза. Он встречается при внутренних и инфекционных заболеваниях, онкологических процессах. Снижение общего количества гемоглобина и эритроцитов также наблюдается при некоторых физиологических состояниях, например, при беременности и лактации, в период усиленного роста, у лиц, занимающихся профессиональным спортом и др.
Так как анемия это всегда синдром какого-либо заболевания или состояния, то строго классифицировать анемию невозможно. Все попытки создать универсальную патогенетическую, этиологическую или иную классификацию анемии не увенчались успехом. В практической работе чаще всего используют так называемые классифицирующие критерии: морфология эритроцитов, степень насыщения эритроцитов гемоглобином, степень регенерации эритроцитов, количество ретикулоцитов, концентрация гемоглобина, патогенетические факторы и др.
^ Морфология эритроцитов. Размер эритроцита в норме составляет 7-8 мкм. В соответствии с этим выделяют микроцитарные (средний диаметр менее 6,7 мкм), макроцитарные (средний диаметр более 9,5 мкм) и нормоцитарные анемии.
^ Степень насыщения эритроцитов гемоглобином. Среднее содержание НЬ в эритроците, в норме составляет 27—33 пикограмма (пг).
В повседневной практике наиболее доступный метод определения содержания НЬ в эритроцитах может служить определение цветового показателя (ЦП). В норме значение цветового показателя (указывающего на содержании НЬ в эритроцитах) — 0,8—1,0 (нормохромия эритроцитов), при значении цветового показателя менее 0,8 говорят об их гипохромии, при цветовом показателе более 1,0 — о гиперхромии. Способ расчета ЦП будет приведен ниже.
Возможно сочетание двух вышеназванных критериев, например гипохромные микроцигарные анемии, нормохромные нормоцитарные анемии.
^ Степень регенерации эритроцитов определяют по количеству ретикулоцитов в периферической крови и по этому значению оценивают эффективность эритропоэза. В норме количество ретикулоцитов в крови — 0,5—1,5% (5-15%).
^ Количество ретикулоцитов — индикатор работы красного ростка костного мозга. При их увеличении речь идёт о напряжённом эритропоэзе (гемолитические анемии, железодефицитные анемии). При их уменьшении говорят о неэффективном эритропоэзе (апластические анемии, витамин В12-дефицитиые анемии, лейкозы).
^ Ретикулоцитарный криз — повышение содержания ретикулоцитов в ответ на успешное лечение железодефицитной и витамин В12-дефицитной анемий.
Концентрация гемоглобина. В зависимости от уровня НЬ различают лёгкую степень анемии (НЬ от 80 до 100 г/л), среднюю степень (НЬ от 60 до 80 г/л), тяжёлую степень (НЬ ниже 60 г/л).
^ Патогенетические факторы. Это связь возникновения анемии с нарушением кровообразования, кровопотерей (постгеморрагические) и избыточным кроверазрушением (гемолитические). Возможно сочетание этиологических факторов.
Несмотря на объективность всех приведенных показателей, объединить их в одной классификации не представляется возможным, так как одна и также анемия одновременно может быть представлена в нескольких рубриках. Поэтому сегодня для практической работы наиболее удобно использовать предложенную еще М.П. Кончаловским (1915), в последствии несколько модифицированную, классификацию анемий. Почти вековой опыт её использования в клинике позволяет считать, что она наиболее удачная из всех предложенных классификаций, хотя и не идеальна.
Эта классификация дает возможности клиницисту в каждом конкретном случае определить причину анемии. Необходимо учитывать, что при некоторых заболеваниях в основе развития анемии лежат сложные, комбинированные патогенетические механизмы.
( М.П. Кончаловский, И.А. Кассирский, Г.А.Алексеев)
- Анемии вследствие кровопотери
- Острая постгеморрагическая анемия
- Хроническая постгеморрагическая анемия
- Анемия вследствие нарушенного кровообразования
- Железодефицитная анемия
- В12-дефицитная анемия
- Фолиеводефицитная анемия
- Анемия обусловленная дефицитом белков
- Гипо- и апластические анемии
- Анемии обусловленные дефицитом других факторов (кобальт, медь, др.)
- Анемии вследствие повышенного кроверазрушения – гемолитические.
- Анемии обусловленные внутриэритроцитарными факторами (эритроцитопатии, энзимопатии)
- Анемии обусловленные внеэритроцитарными факторами
Анализ представленной классификации позволяет выявить достаточно много «слабых мест». Так железодефицитная анемия, самая частая анемия в практике семейного врача, одновременно находится в двух рубриках – анемия вследствие кровопотери (хроническая постгеморрагическая анемия) и анемия вследствие нарушенного кровообразования. Кроме того, в этой классификации фактически не учитываются такие показатели как гипер-, нормо- или гиперхромность; микро – или макроцитоз и др. А, как известно, оценка этих показателей часто является определяющим компонентом в диагностике анемий. Тем не менее, эта классификация наиболее проста в применении и не требует сложных гематологических исследований.
Безусловно, есть ситуации, которые требуют использования несколько более сложного варианта этой классификации. Так в ряде случаев анемия может быть вызвана не только нарушением синтеза гемма (гипохромные микроцитарные): железодефицитные анемии, анемии, связанные с нарушением синтеза или утилизации порфиринов, но и вызванные нарушением синтеза глобина: количественные (талассемии) и качественные (аномальные гемоглобины — гемоглобинопатии). Следует также помнить о существовании диформных и триформных анемиях, когда в качестве этиологического фактора выступает 2-3 причины.
Некоторые авторы предлагают выделять анемии со сложным патогенезом. Это анемии при инфекционных и воспалительных заболеваниях, ожоговая анемия и т.д.
В данном методическом пособии мы коснемся лишь одного вида анемий – железодефицитных. Но кроме этого вопроса, нам показалось важным, рассмотреть более широко проблему нарушения обмена железа.
Почему проблема железодефицитной анемии сегодня столь актуальна?
Интерес к той или иной проблеме в медицине связан, как правило, с распространенностью заболевания (состояния) в популяции.
На долю ЖДА приходится 85% всех анемий, ею страдает 20% населения планеты, ЛДЖ – имеют 30% населения планеты. В динамике ЛДЖ и /или ЖДА имеется два пика. 1-й пик ЖДА и ЛДЖ приходится на период детства — 20-25% (из них 43% — дети младше 4-х лет), а 2-й пик ЖДА и ЛДЖ – беременность. В определенной мере распространенность связывают с экономическим положением страны, так в Северной Америке ЛДЖ и ЖДА обнаруживается у 8% населения, в Африке – у 44% населения, а в Юго-Восточной Азии – у 70% населения.
Скрининг практически здоровых детей из социально защищенных семей выявил дефицит железа в США – у 12% детей, в Англии – у 15%, в Северном Квебеке – у 58%. Неожиданным был и тот факт, что среди обследованных детей мальчики составляли 57,6%, традиционно считалось, что ЛДЖ чаще встречается у девочек. При этом дефицит железа выявлен у 27% обследованных детей белой расы в, а у детей из африканских семей – в 40% случаев.
Остановимся на проблеме железодефицитных заболеваний и состояний. Но, прежде всего, несколько слов о терминологии. С медицинской (биологической) точки могут быть выделены элементы, которые называются незаменимыми. Эссенциальными (незаменимыми) микроэлементами на современном этапе развития науки считаются Fe, Cu, Zn, Mn, Se, Mo, Сг, I, Со, F, для которых доказаны проявления синдромов истинного дефицита у человека. Наряду с этими микроэлементами, по данным P. Aggett (1985), для некоторых животных незаменимыми являются As, В, Вг, Li, Ni, Si, V и др. А.П. Авцын (1983) разработал концепцию и классификацию патологических процессов, вызванных дефицитом, избытком или дисбалансом микроэлементов в организме, и предложил для них объединяющее название «микреэлементозы».
С другой стороны среди всех ионов выделяют электролиты, которые определяют ионную силу состава биологических жидкостей (внеклеточной жидкости и ионного состава цитозоля). Это натрий, калий, хлориды и бикарбонат.
Все другие ионы имеют либо регуляторное значение, либо составляют основу определенных тканей и структур. Кальций и фосфор в костной ткани; фосфор фосфолипидов биологических мембран, железо эритроцитов, микроэлементы как активные компоненты структур активного центра ферментов и витаминов.
^ ОБМЕН ЖЕЛЕЗА И ЕГО НАРУШЕНИЯ
Из всех металлов, жизненно важных для человека, железо наиболее распространено и играет первостепенную роль во многих биохимических реакциях. Это жизненно важный металл, поступающий в организм человека с пищей. В нем нуждаются все живые существа на земле, кроме семейства Lactobacillus
Находясь в комплексе с порфирином и будучи включенным в структуру соответствующего белка, железо не только обеспечивает связывание и высвобождение кислорода, но и принимает участие в ряде жизненно важных окислительно-восстановительных процессов. Поскольку неорганическое железо высокотоксично, в его ассимиляции, транспорте и депонировании задействованы весьма специфичные процессы. Обмен железа в организме жестко регулируются, но при нарушении этих механизмов может возникнуть либо его дефицитом, либо его избыток.
На долю железа приходится лишь 0,0065 % массы тела (3- 5 г). Оно входит в состав комплексных соединений. Подразделяется на клеточное и внеклеточное. Клеточные соединения железа имеют различное строение, обладают характерной только для них функциональной активностью и играют важную биологическую роль. К ним относятся:
— гемопротеины, структурным элементом которых является гем (гемоглобин, миоглобин, цитохромы, каталаза, пероксидаза);
— железосодержащие ферменты негеминовой группы (сукцинат-дегидрогеназа, ацетил-КоА-дегидрогеназа, НАДН2-цитохром с-редуктаза, ксантиноксидаза, аконитаза), ферритин, гемосидерин и ряд других соединений железа.
К внеклеточным соединениям относится железосвязывающий белок — трансферрин.
Наиболее важным соединением, в который входит 60—70 % (2,7 г) железа организма, является гемоглобин — это дыхательный пигмент крови, содержащийся в эритроцитах, выполняет газотранспортную функцию. Гемоглобина состоит из белковой части — глобина и небелковой — гема, в котором двухвалентный ион железа связан с протопорфирином. Молекула гемоглобина содержит 0,34 % железа.
Миоглобин — дыхательный белок сердечной и скелетных мышц — содержится 3—5 % всего железа организма. Основная функция миоглобина — транспорт кислорода через клетку, регуляция его содержания в мышце и депонирование. Молекула миоглобина содержит 0,34 % железа, состоит из гема и полипептидной цепи, включающей 153 аминокислотных остатка.
На долю железосодержащих ферментов приходится 0,1—0,2 % (6-8 мг) всего железа организма. Они содержатся во всех клетках, но главным образом в митохондриях. Цитохромы и цитохромоксидаза осуществляют перенос электронов, поэтому железо, которое входит в их состав, постоянно меняет валентность. Каталаза и пероксидаза катализируют реакции с пероксидом водорода. Ферменты с негеминовым железом также локализованы в митохондриях, участвуют в цикле трикарбоновых кислот, окислительном фосфорилировании и транспорте электронов на конечном этапе окисления. Следовательно, изменения содержания железа в организме может вызвать изменения не только эритропоэза, но и многих других функций.
Эритропоэз осуществляется под контролем эритропоэтина. Но на его активность оказывают влияние катехоламины, стероидные гормоны, гормоны щитовидной железы, гормон роста и циклические нуклеотиды и др. Следовательно, состояние эритропоэза находится под воздействием многих факторов. В норме уровень гемоглобина, количество эритроцитов и многие другие показатели находятся в достаточно жестких физиологических рамках.
При патологии показатель объема крови не вполне отражает изменение массы эритроцитов. Так, например, создается ложное впечатление о повышении уровня гемоглобина и гематокрита на фоне резкого снижения объема плазмы, которое наблюдается при кровотечениях, обширных ожогах, выраженном диурезе, а также при других тяжелых формах обезвоживания организма. В противоположность этому кажущееся снижение гематологических показателей регистрируют у больных с увеличенным объемом крови при беременности или застойной сердечной недостаточности.
Гематологические показатели для лиц разного возраста в норме приведены в приложении. У женщин детородного возраста эти параметры на 10 % ниже, чем у мужчин. У лиц, находящихся в высокогорных районах, показатели более высокие и до некоторой степени находятся в пропорциональной зависимости от высоты над уровнем моря. Исходя из предлагаемых норм, анемию можно определить как снижение более чем на 10 % средних значений гематологических показателей для лиц определенного пола. Однако, поскольку в норме изменения уровня гемоглобина достигают этого предела, подтвердить умеренно выраженную анемию бывает не просто.
Для диагностики железодефицитных состояний разной степени прибегают к помощи разнообразных лабораторных методов исследования. У взрослых железодефицитное состояние развивается поэтапно, и для каждого этапа характерны определенные изменения лабораторных данных. В самом начале уменьшаются запасы железа, что, однако, не сопровождается уменьшением количества железа, предназначенного для эритропоэза.
Лабораторные критерии ЖДА можно представить следующим образом:
- Низкий цветовой показатель;
- Гипохромия эритроцитов, микроцитоз;
• Снижение содержания сывороточного железа; - Повышение общей железосвязывающей способности;
• Снижение содержания ферритина.
Сразу же можно предположить, что при наличии «слабой» лаборатории не все перечисленные показатели могут быть получены.
Вместе с тем важнейшим лабораторным признаком, позволяющим предположить железодефицитный характер анемии, является низкий цветовой показатель. Он отражает содержание гемоглобина в эритроците и является расчетной величиной. Зная число эритроцитов в крови и содержание в ней гемоглобина, можно вычислить, в какой мере им насыщен каждый эритроцит. Для вычисление цветового показателя следует утроенное число граммов Нв (гемоглобин выражается в г/л) на первые три цифры числа эритроцитов.
Пример: Нв – 145г/л х 3 : 450 (первые три цифры числа эритроцитов) = 0,96. Следует помнить, что цветовой показатель больше 1 может быть только при макроцитозе. Перенасыщения гемоглобином не бывает. Нормальный эритроцит насыщен им до предела.
Поскольку при ЖДА нарушен синтез гемоглобина из-за недостатка железа, но продукция эритроцитов в костном мозге снижается незначительно, то рассчитываемый цветовой показатель всегда ниже 0,85, (все ЖДА являются гипохромными). При использовании в лабораторной практике современных анализаторов имеется возможность непосредственного определения среднего содержания гемоглобина в одном эритроците, обозначающегося латинской абревиатурой МСН (в норме 27 — 35 рд). При гипохромных анемиях эритроциты гипохромные, из-за недостатка Нв в центре имеется широкое просветление. При этом они по форме напоминает бублик или кольцо (анулоцит). Кроме того, в мазке крови больных ЖДА часто встречаются микроциты, в которых содержание гемоглобина меньше, чем в эритроцитах обычного размера. В мазке периферической крови при ЖДА, кроме микроцитоза, может быть выявлен анизоцитоз и пойкилоцитоз, т.е. эритроциты неодинаковой величины и различной формы. Количество сидероцитов (эритроциты с гранулами железа, выявляемого при специальной окраске) резко снижено по сравнению с нормой, вплоть до полного их отсутствия.
Содержание ретикулоцитов в крови, как правило, в пределах нормы, за исключением случаев выраженной кровопотери при соответствующей патологии (обильные носовые и маточные кровотечения) или в первые дни лечения препаратами железа, когда отмечается увеличение их числа. Количество лейкоцитов и тромбоцитов обычно не изменено, но может наблюдаться тромбоцитоз, исчезающий после коррекции ЖДА.
Таким образом для правильной диагностики ЖДА необходимо иметь не только количественные показатели «красной» крови, но и описание качественных изменений эритроцитов (при их наличии).
Морфологическое исследование костного мозга для диагностики ЖДА малоинформативно и может иметь значение лишь при специальной окраске на железо и подсчете сидеробластов (эритроидные клетки костного мозга с гранулами железа), количество которых у больных ЖДА значительно снижено.
В аспирате костного мозга, окрашенном Prussian blue, выявляют заметное уменьшение или даже отсутствие запасов железа в макрофагах на фоне снижения уровня сывороточного ферритина.
^ Подходы к обследованию больного с анемией
Приступая к обследованию больного анемией, следует исходить из правила, что для подтверждения диагноза необходимо использовать минимум лабораторных тестов и процедур. Как и при других заболеваниях, первостепенное значение имеют подробный анамнез и тщательный осмотр больного.
К примеру, если из семейного анамнеза становится известно о наследовании определенного доминирующего признака, то это убедительно свидетельствует в пользу первичного наследственного сфероцитоза. При выявлении сердечного шума и спленомегалии у больного с анемией повышается вероятность подострого бактериального эндокардита. Подобные ситуации в практике семейного врача довольно редки.
Чаще он встречаются с ЖДА вызванными кровотечениями. При этом кровопотери, как правило, не значительны, поэтому только при целенаправленном изучении данного вопроса можно их обнаружить. Это «малые», но длительно существующие кровопотери. Многие больные с ними свыклись и не расценивают их как патологию. Наиболее часто это кровотечения: маточные (метроррагии, полименорея, гиперменорея), желудочно-кишечные (геморроидальные, кишечные, пищеводные, желудочное), носовые, десневые, из мочевыводящих путей. Особое место занимают кровотечения в полости (гематорокс, гемоперикардиум, гемоперитонеум), эндомериоз, так как реутилизации железа при этом не происходит.
Кровопотери относятся к наиболее важным причинам развития железо-дефицитных состояний у взрослого человека. У женщин детородного возраста менструальные кровотечения ответственны за большинство случаев этих состояний. Следует знать, что при приеме противозачаточных эстроген-эрогестероно-вых пилюли, менструальные кровопотери невелики, тогда как применение внутриматочных спиралей их увеличивает.
У взрослого мужчины самой частой причиной железодефицитного состояния бывают желудочно-кишечные кровотечения. В обследовании этих больных первостепенное значение имеет анализ кала на скрытую кровь. Поскольку желудочно-кишечные кровотечения бывают интермиттирующими, исследования кала на скрытую кровь необходимо проводить многократно в течение продолжительного периода. Пептические язвы, диафрагмальная грыжа, дивертикулез и рак служат наиболее частыми причинами этих кровотечений. Нередко скрытую кровь в кале выявляют при геморрое или у лиц, принимающих салицилаты, однако кровотечения при этом редко бывают значительными. Почти у 15 % пациентов с желудочно-кишечным кровотечением выявить его источники не удается даже с помощью тщательного исследования. В странах тропического пояса основной причиной кровотечений у больных служат глистные инвазии, особенно анкилостомоз. Иногда при наследственной телеангиэктазии или геморрагическом диатезе кровотечения происходят из многочисленных участков желудочно-кишечного тракта. При тромбоцитопении, качественных изменениях тромбоцитов и при болезни Виллебранда желудочно-кишечные кровотечения более часты, нежели при дефиците факторов свертывания крови.
Регулярное донорство чревато прогрессивным уменьшением резервов железа в организме, а у менструирующих женщин при этом может развиться истинный железодефицитный эритропоэз. Истощение запасов железа усиливается по мере учащения эпизодов сдачи крови.
Второй причиной, часто сочетающейся с первой, является недостаточное поступление железа с пищей и/или снижение его всасывания (воспалительные процессы в желудочно-кишечном тракте, удаление части кишечника и др.). Кроме того, причиной нарушения всасывания может быть изменение всасывания железа – синдром мальабсорбции.
Могут быть выявлены группы риска по железодефицитным анемиям или латентному дефициту железа .
Потребность в железе увеличивается в период роста, в подростковом возрасте и при беременности. В США дефицит железа выявляют у 10 % детей дошкольного возраста, пик его частоты приходится на возраст 1—2 года. Увеличенная потребность в железе детского организма не может быть удовлетворена детским питанием, в котором преобладают молоко и злаковые, но мало мяса и овощей. Количество железа в этой диете невелико, а его ассимиляция может быть затруднена из-за присутствия железосвязывающих анионов, особенно фосфатов. В связи с этим детское питание следует обогащать железом. В подростковом возрасте дефицит железа может быть обусловлен нерегулярным режимом питания и недостаточным пережевыванием пищи. В период беременности плод потребляет из организма женщины около 500 мг железа, даже если у нее уже развилось железодефицитное состояние. Потребность организма в железе при беременности увеличивается примерно в три раза. Большинство беременных с профилактической целью должны принимать препараты железа в виде его солей. Если подобная профилактика не проводится, то частота развития железодефицитных состояний у беременных увеличивается более чем на 50 %.
Анемия вследствие недостаточного поступления железа в организм чаще всего развивается у представителей популяций, в диете которых очень невелико количество животных белков. Уже упоминалось о причинах недостаточного потребления железа детьми и подростками. У представителей низких социальных слоев населения и пожилых потребление железа с пищей находится на субоптимальном уровне из-за материальных трудностей, отсутствия зубов, безразличия к образу жизни.
Процессы всасываемости железа могут снижаться при многих заболеваниях. Это может быть частичная или полной гастрэктомия, когда нарушаются процессы ассимиляции пищевого железа, в результате чего пища с большей скоростью проходит те участки кишечника, в которых в основном всасывается железо. Ахлоргидрия также сопровождается снижением его всасывания. У больных с хронической диареей или мальабсорбцией также развивается недостаточность железа, особенно при вовлечении в процесс двенадцатиперстной и проксимальных отделов тонкой кишки. Иногда железодефицитная анемия служит предвестником нетропической спру (целиакия).
Всасывание железа зависит от:
- Характера пищи
- Состояния и функциональной активности ЖКТ, печени, желчного пузыря и поджелудочной железы
- Потребностей организма (у детей всасывание железа при его дефиците снижено, а у взрослых — повышено)
- Величиной депонированного железа
- Состоянием эритропоэза
Третья причина — повышенный расход железа, что наблюдается при беременности, лактации, ускоренном росте, у лиц, занимающихся профессиональным спортом и др.
У некоторых, очень немногих, больных дефицит железа может быть обусловлен нарушением поступления в эритроидные клетки-предшественники железа, связанного с трансферрином. Это может быть врожденным состоянием или оно обусловлено образованием аутоантител к рецепторам трансферрина.
Если суммировать все вышеизложенное, то причинами ЖДА и ЛДЖ может быть объяснена:
- Низким социально-экономическим уровнем жизни населения
- Недостаточностью средств, выделяемых на профилактики и раннюю диагностику ЛДЖ, адекватную коррекцию пищевых дефицитов Fe
- Современным напряженным образом жизни
- Экологической ситуацией
- Ростом общей заболеваемости
При этом выделяют внешние и внутренние причины ЛДЖ и ЖДА. Внешние причины:
- Алиментарный фактор – наиболее значимая внешняя причина абсолютного ДЖ (социально-экономические условия, вегетарианство, религиозные обычаи, особенности национальной кухни)
- Извращение вкусовых пристрастий (в Германии употребляют большое кол-во продуктов, содержащих крахмал, а это формирует дефицит Fe, Zn, K)
ЖДС
— раннее детство (высокие темпы роста)
— пубертатный период (усиленная учебная или производственная нагрузка, дисфункция эндокринной системы, месячные)
— период беременности и лактация
— профессиональный спорт (повышение потребностей в Fe)
Все вышеперечисленные факты следует активно выяснять и учитывать при сборе, как анамнеза заболевания, так и анамнеза жизни.
При изучении жалоб больного следует помнить, что независимо от этиологии анемии всегда имеется анемический синдром (разной степени выраженности), связанный с гипоксемией и гипоксией органов и тканей. Это такие симптомы как: слабость, головокружение, одышка, боли в области сердца, обморочные состояния, тахикардия, гипотония, мелькание “мушек” перед глазами, сонливость днем, плохое засыпание ночью, тяжесть в эпигастральной области, ухудшение аппетита, метеоризм, раздражительность, плаксивость, снижение памяти и внимания.
При дефиците железа нарушается деятельность ЦНС, в частности, изменяется активность: левой гемисферы, затылочных долей обеих гемисфер, центров оптической памяти, центров отвечающих за поля зрения, сенсорного поля левого полушария.
Это проявляется:
- Снижением интеллектуальной и двигательной способности (прямой и отсроченный эффект)
- Ухудшением показателей развития и познавательных функций у младенцев
- Появлением стойких поведенческих отклонений и умственной заторможенности у детей и подростков
У детей нарушение оксигенации ЦНС может вызвать:
- Склонность к изоляции
- Снижение фона положительных эмоций, удовольствия и восхищения
- Осторожность в поступках,
- Нерешительность, быструю утомляемостью,
Такие дети отличаются меньшей любознательностью и детской игривостью, а также рассеянностью внимания к занятиям.
У взрослых дефицит железа и недостаточное обеспечение кислором головного мозга может проявляться утомляемостью, снижением работоспособности, социальной и трудовой дезадаптацией, у них часты депрессия и психологические проблемы.
Не следует забывать, что дефицит железа оказывает прямое воздействие на активность головного мозга, и тогда у человека появятся:
- Забывчивость
- Рассеянность
- Приступы мигрени (особенно в утренние часы)
- Периоды подавленность
Вторая группа симптомов связана с сидеропенией (недостаточное содержание железа в организме). Это так называемый сидеропенический синдром. Он проявляется:
- Пристрастие к запахам (ацетон, бензин)
- Снижение аппетита
- Употребление в пищу – земли (геофагия), крахмал (амилофагия), мела, сырого мяса, сырого теста, сырых макаронных изделий, льда (пагофагия)
- Ногти уплощены, становятся ложкообразными (койлонихии),, теряют блеск, имеется поперечная исчерченность легко ломаются.
- Кожа сухая, слегка шелушится, плохо загорает
- Анулярный стоматит (эрозии в углах рта — заеды)
- Дисфагия. Она наступает при длительном и выраженном дефиците у больного вследствие истончения слизистой оболочки части пищевода, которая расположена ниже перстневидного хряща гортани (симптом Пламмера— Винсона)
- Атрофический глоссит
- Ломкость волос
- Недержание мочи
- Императивные позывы на мочеиспускание
- Субфебрилитет
- Кариес
- Мышечные боли
Сидеропенический синдром (тканевой дефицит железа) может быть представлен в виде четырех основных группы органов, в которых проявления гипосидероза выявлены максимально:
- Кожные покровы, придатки кожи и слизистые (сухость, поражение волос и ногтей)
- Желудочно- кишечный тракт (снижение и извращение аппетита, дисфагия, запоры или диарея, глоссит, жжение языка, эзофагит, в желудке — дистрофические изменения клеток слизистой оболочки)
- Нервная система (повышенная утомляемость, шум в ушах, головокружение, головные боли, снижение интеллектуальных возможностей)
- Сердечно сосудистая система (тахикардия, диастолическая дисфункция)
Таким образом, используя все вышеперечисленные жалобы, мы можем составить своеобразный «портрет» больного ЖДА. Этот «портрет» будет не полным, если мы не вспомним «бледную немощь» — pica chlorotica, яркое описание проявлений дефицита железа у девочек-подостков. Для них характерна зеленоватая окраска кожи (ювенильный хлороз)
Г.А. Даштаянц предложил выделять три уровня проявлений анемий.
Первый – неспецифические проявления гемической гипоксии. Они не связаны с этиологическим фактором, это такие симптомы как: слабость, снижение работоспособности, учащение сердцебиения, головокружение, обмороки.
Второй – специфические клинические проявления. Они зависят от вида анемии. Бледность кожи в сочетании с тканевым дефицитом железа (сидеропенический синдром – это железодефицитная анемия. Если бледность кожных покровов сочетается с глосситом, проявлением фуникулярного миелеза – то это Анемия Аддисон-Бирмера (В12-дефицитная анемия.
Третий признак – специфические изменения показателей крови:
— гопохромно-микроцетарная анемия, гипоферремия – жнлнзоднфицитная анемия
— гиперхромно-макроцитарная анемия с гиперферремией — мегалобластная анемия
— микросфероцитоз с овалоцитозом — хроническая гемолитическая анемия
— мегалобластный эритроцитоз – В12-дефицитная анемия.
Безусловно представление о клиническом статусе больного с анемией зависит от основного заболевания, а также от формы анемии (острая или хроническая).
Степень выраженности симптомов зависит и от ряда других факторов. При быстром развитии анемии времени для полного развития компенсаторных процессов недостаточно и у больного симптомы могут быть более выражены, чем при постепенном развитии анемии той же степени. Кроме того, жалобы больного могут зависеть от местного сосудистого заболевания. К примеру, стенокардия, перемежающая хромота или преходящая ишемия мозга могут обостряться при развитии, анемии.
Анемия средней тяжести может протекать бессимптомно. При этом пациента может беспокоить не мотивированная усталость, одышка и сердцебиение, особенно после физической нагрузки.
При тяжелой форме анемии симптоматика часто сохраняется даже у больного, находящегося в состоянии покоя, он не может переносить физические нагрузки. Если концентрация гемоглобина становится менее 75 г/л, то минутный сердечный выброс в покое заметно повышается по мере увеличения как частоты сердечных сокращений (ЧСС), так и ударного объема. Больной способен осознавать это состояние гипердинамии сердца и предъявлять жалобы на сердцебиения и учащенный пульс. Симптомы сердечной недостаточности могут развиться в том случае, если резерв миокарда исчерпан.
Известно, что симптоматика при тяжелой форме анемии распространяется и на другие системы органов. Больной часто жалуется на головокружение и головные боли, шум в ушах вплоть до обморока. Многие больные становятся раздражительными, страдают бессонницей, с трудом концентрируют свое внимание. Поскольку кровоток в коже снижен, у больного может развиться гиперчувствительность к холоду. Симптоматику со стороны желудочно-кишечного тракта, например анорексию, диспепсию и даже тошноту, а также дисфункцию толстого кишечника в первую очередь следует отнести за счет шунтирования крови, минующей сосудистое русло внутренних органов. У женщин обычно нарушается менструальный цикл, что проявляется как аменореей, так и обильными кровотечениями. Мужчины могут жаловаться на импотенцию или утрату либидо.
Бледность кожи это основной признак анемий. Однако следует помнить, что его информативность ограничена другими факторами, определяющими цвет кожи. Так, у разных индивидов значительно варьирует толщина и структура кожи. Кроме того, в ней может изменяться кровоток. В зависимости от расположения сосудов и типа микроциркуляции возможно появление желтоватого болезненного оттенка кожи даже у здорового человека, в то время как у больных анемией она может приобретать красноватый оттенок в связи с приливом в момент возбуждения или после него. Другим важным фактором, определяющим цвет кожи, служит концентрация меланина в эпидермисе. Светлокожие выглядят бледными, даже если они не страдают анемией, и, наоборот, у очень смуглого человека довольно трудно распознать бледность кожи. И, наконец, приобретенные нарушения меланиновой пигментации (болезнь Аддисона, гемохроматоз) или желтуха могут маскировать бледность кожных покровов. Однако даже у темнокожих анемию можно заподозрить по цвету ладонных поверхностей или слизистой оболочки полости рта, ногтевого ложа и конъюнктивы век. Цвет кожи на сгибах ладонной поверхности считают информативным признаком. Если по бледности они одинаковы с окружающей кожей, то уровень гемоглобина у больного, как правило, составляет менее 70 г/л.
Развитию бледности кожных покровов при анемии содействуют два фактора, один из которых — это, несомненно, уменьшение концентрации гемоглобина в крови, поступающей в сосуды кожи и слизистых оболочек, а другой — это шунтирование крови в обход сосудов кожи и других периферических тканей, способствующее усиленному кровоснабжению жизненно важных органов. Перераспределение кровотока представляет собой один из важных механизмов компенсации анемии.
Из других клинических признаков, ассоциирующихся с анемией, следует отметить тахикардию, значительные колебания пульсового давления и гипердинамику предсердия. Систолический шум изгнания довольно часто слышен над предсердиями, особенно над легочной артерией. Венозный шум может определяться над сосудами шеи. После коррекции анемии эта симптоматика исчезает. Больные с гемолитической анемией часто иктеричны, у них определяют сплено-мегалию, иногда развиваются поверхностные кожные изъязвления над таранной костью.
источник
АНЕМИЯ (малокровие), группа заболеваний, при которых в крови уменьшается содержание эритроцитов и/или гемоглобина, что приводит к гипоксии. Анемия может возникать в результате кровотечения (постгеморрагическая анемия), нарушения кровообразования (железодефицитная анемия, пернициозная анемия, гипопластическая анемия, апластическая анемия), повышенного кроверазрушения (гемолитическая анемия и гемоглобинопатия).
Для облегчения диагностики анемии кроме стандартных анализов по определению гемоглобина, эритроцитов проводится еще ряд дополнительных исследований, которые рассмотрены ниже.
| Норма, мкм 3 | Повышенный объем эритроцитов | Пониженный объем эритроцитов |
| мужчины: 80 — 94 |
женщины:
81 — 99
- макроцитарные и мегалобластические анемии (дефицит витамина В12, фоллиевой кислоты)
- анемии, которые могут сопровождаться макроцитозом (гемолитические анемии, болезни печени, миелодиспластические синдромы)
- микроцитарные анемии (железодефицитные анемии, талассемии, сидеробластические анемии)
- анемии, которые могут сопровождаться микроцитозом (гемолитические анемии, гемоглобинопатии)
MCV (mean corpuscular volume — средний корпускулярный объем) — средняя величина объема эритроцитов, измеряемая в кубических микрометрах или фемтолитрах (fl), рассчитывается по формуле (в гематологических анализаторах MCV вычисляется делением суммы клеточных объемов на число эритроцитов):
Показатель MCV в основном используется для характеристики типа анемии:
- MCV 100ft (эритроциты характеризуются как макроциты) — макроцитарные и мегалобластные анемии (фолиеводефицитная анемия, B12-дефицитная анемия).
Кроме вышесказанного, изменения показателя MCV могут дать полезную информацию о нарушениях водно-электролитного баланса: повышенное значение MCV говорит о гипотоническом характере нарушений; пониженное значение MCV — о гипертоническом характере нарушений.
| Норма | Повышенное содержание гемоглобина | Пониженное содержание гемоглобина |
| 27-31 пг |
|
|
MCH — это показатель степени насыщения эритроцита гемоглобином, рассчитываемый по формуле:
MCH самостоятельного значения не имеет, и всегда рассматривается вкупе с MCV, MCHC, цветовым показателем. На основании значений этих показателей различают три вида анемий: нормохромные анемии, гипохромные анемии, гиперхромные анемии.
| Норма | Повышенная концентрация гемоглобина | Пониженная концентрация гемоглобина |
| 33-37% 20,4-22,9 ммоль/л |
|
|
MCHC — показатель насыщенности эритроцитов гемоглобином, рассчитываемый по формуле:
MCHC используется для дифференциальной диагностики анемий: сниженный MCHC (нарушение синтеза гемоглобина) — гипохромные железодефицитные анемии; повышенный MCHC — гиперхромные анемии. Кроме этого, MCHC позволяет диагностировать характер нарушений водно-электролитного баланса.
RDW (red cell distribution with — мера различия эритроцитов по объему) рассчитывается по формуле:
RDW выше нормы означает гетерогенность популяции эритроцитов или наличие в пробе крови нескольких популяций эритроцитов (после переливания крови).
Классификация анемий по показателям RDW, MCV
- Гомогенные анемии (RDW-норма):
- Микроцитарные анемии (MCV-занижен): бета-талассемия, хронические заболевания;
- Нормоцитарные анемии (MCV-норма):острая кровопотеря, гемолитическая анемия вне криза, хронические заболевания;
- Макроцитарные анемии (MCV-завышен):болезни печени, апластическая анемия.
- Гетерогенные анемии (RDW-завышено):
- Микроцитарные анемии (MCV-занижен): дефицит железа;
- Нормоцитарные анемии (MCV-норма):дефицит железа и витамина, гемоглобинопатия, миелодиспластический синдром, миелофиброз;
- Макроцитарные анемии (MCV-завышен): дефицит фолиевой кислоты и витамина B12, гемолитический криз, агглютинация эритроцитов, лейкоцитоз выше 50·10 9 /л.
ЦП отражает относительное содержание гемоглобина в эритроците. ЦП клинически аналогичен MCH и коррелирует с MCV.
- ЦП 1,1 (гиперхромия) — зависит только от увеличения объема эритроцита (но не от повышенного насыщения эритроцита гемоглобином), поэтому всегда сочетается с макроцитозом:
- мегалобластные анемии (дефицит фолиевой кислоты и витамина B12);
- гипопластические анемии (гемобластозы, диссеминации злокачественных новообразований);
- многие хронические гемолитические анемии;
- сидеробластные анемии (при миелодиспластическом синдроме);
- острые постгеморрагические анемии;
- анемии, сопутствующие циррозу печени, при гипотиреозе, приеме цитостатиков, контрацептивов, противосудорожных лекарственных препаратов.
В значительной мере диагностику анемий облегчает правильная трактовка морфологических изменений эритроцитов:
источник
В клинической практике особенно важное значение придается изучению морфологического и биохимического состава периферической крови, с помощью которых можно получить представление о количественном и качественном составе форменных элементов крови, изучить состав плазмы, содержание в ней продуктов азотистого обмена, липидного, пигментного, углеводного и минерального.
Общий клинический анализ крови складывается из определения гематокрита, СОЭ, уровня гемоглобина, ОРЭ,определения цветного показателя, подсчета форменных элементов крови и выведения лейкограммы.
СОЭ — скорость оседания эритроцитов является одним из наиболее важных клинических показателей крови. СОЭ имеет диагностическое и прогностическое значение, но не является специфическим признаком какого-либо заболевания. СОЭ зависит от вязкости плазмы, размеров и формы форменных элементов. Ускорение СОЭ наблюдается при:
— заболеваниях, сопровождающихся воспалительными процессами,
— парапротеинемии (миелома, атипичные лейкозы),
— анемиях (кроме микросфероцитарной и дрепаноцитной)
Замедление СОЭ наблюдается при:
— сердечно-сосудистой патологии (полицитемия и повышение концентрации углекислого газа)
— гипофибриногенемия (ДВС-синдром, поражение паренхимы печени),
— желтухе, увеличении содержания желчных кислот и желчных пигментов в плазме,
— приеме салицилатов, хлорида кальция.
Гематокрит – общий объем эритроцитов, дающее представление о процентном соотношении между плазмой и форменными элементами.
Объем эритроцитов увеличивается при:
-дегидратации (токсикозы, рвота, поносы),
-недостаточности коры надпоченчников
Объем эритроцитов уменьшается при:
Цветной показатель – показатель степени насыщенности эритроцитов гемоглобином. В зависимости от ЦП, анемии делятся на гипохромные (ЦП меньше 0,85), нормохромные (ЦП= 0.85 – 1,15), гиперхромные (ЦП более 1,15).
Резистентность эритроцитов (ОРЭ)– осмотическая резистентность эритроцитов,это свойство эритроциов противостоять повряждающим факторам (химическим, механическим и т.д.)Резистентность эритроцитов снижается при:
— нарушение функции селезенки.
Резистентность эритроцитов повышается при:
— гипохромных микроцитарных анемиях(железодефицитная).
Гемоглобин – основной дыхательный пигмент, хромопротеин, обеспечивающий ткани кислородом.Снижение уровня гемоглобина (гипохромемия) наблюдается при:
— анемиях различного генеза.
Увеличение уровня гемоглобина (гиперхромемия ) в крови наблюдается при :
— значительных физических нагрузках и стрессе,
— относительное увеличение при гемоконцентрации ,
Эритроциты – красные безъядерные форменные элементы крови, участвующие в газообмене, поддержание КЩС, в гликолизе и т.д.
Эритроцитоз – увеличение количества эритроцитов в кровеносном русле.
— у животных, обитающих в высокогорных местностях.
— сердечная недостаточность, пороки сердца,
— эмфизема легких, пневмосклероз,
— эндокринные нарушения(болезнь Аддисона, тетания)
Патологический относительный (мнимый в результате гипогидратации):
-профузный понос и обильная рвота,
Пойкилоцитоз – изменение формы эритроцитов (стоматоциты, сфероциты, акантоциты, дакриоциты, дрепаноциты и т.д.)
Анизоцитоз(анизохромия) – изменение в окраске эритроцитов (менее интенсивная у гипохромных, более интенсивная у гипохромных) – является неблагоприятным признаком острой или обострения хронической анемии.
Лейкоциты — белые клетки крови, включают в себя агранулоциты (лимфоциты и моноциты) и гранулоциты (базофилы, нейтрофилы, эозинофилы).
Лейкоцитоз – повышение общего количества лейкоцитов в крови наблюдается:
— в коматозных состояниях (уремическаяч, диабетическая, печеночная),
— заболеваниях системы кроветворения.
— лимфогранулематозе и лейкозах,
— после обильных кровопотерь,
— в результате введения некоторых лекарственных веществ(камфара, адреналин. инсулин),
Лейкопения – уменьшение общего числа лейкоцитов в крови наблюдается при:
-некоторых инфекционных заболеваниях (бруцеллез, септический эндокардит),
-функциональные заболевания ЦНС.
Процентное соотношение отдельных лейкоцитов.
Эозинофилия –увеличение количества эозинофилов в крови является своеобразной реакцией организма на поступление чужеродного белка и гистамина. Эозинофилы выполняют антигистаминную, антитоксическую фагоцитарную функции.
Эозинофилия отмечается при:
-паразитарных заболеваниях (глистные инвазии, лямблиоз)
-лечении антибиотиками и сульфаниламидами,
—заболеваниях системы крови,
Эозинопения и анэнозинофилия — уменьшение количества или полное отсутсвие эозинофилов в крови ,встречается при :-
— на высоте некоторых острых инфекций,
Лимфоцитоз- увеличение количества лимфоцитов в крови, делится на :
-физиологический лимфоцитоз(после приема пищи, физической нагрузки) и
— патологический лимфоцитоз(при инфекционных заболеваниях, в период выздоровления после острой инфекции, анемии, гипофункции яичников).
Лимфопения- понижение количества лимфоцитов в крови наблюдается при:
Моноцитоз — увеличение количества моноцитов в крови наблюдается при:
-острых инфекционных заболеваниях
-хроническом течении инфекции,
Моноцитопения- уменьшение моноцитов в крови, отмечается при:
-тяжелых септических процессах,
Базофилия — увеличение количества базофилов в крови. Базофилы содержат в своих гранулах важнейшие медиаторы тканевого обмена (гепарин, гистамин) и участвуют в аллергических, анафилактических реакциях, а также в процессе свертывания крови.
Дегенеративные изменения в клетках (лейкоцитах).
Дегенеративные изменения проявляются:
-в виде токсической зернистости нейтрофилов,
-дегенеративные нарушения в ядре (гиперсегментированное ядро), кариолизис — разрушение ядра.
Дегенеративные изменения лейкоцитов в большой степени характерны для:
Свертывающая и антисвертывающая системы крови.
Свертывание крови является защитной реакцией организма, предохраняющей его от кровопотери. Процесс свертывания крови регулируется нервной и эндокринной системами. Текучесть крови предотвращает слипание клеток и позволяет им легко перемещаться по сосудам. Свертываемость и текучесть, взаимодействуя между собой, образуют надежную систему гемостаза.
Система гемостаза обеспечивается следующими факторами:
1.Сосудистый- с одной стороны, эндотелий сосудов выделяет в кровь вещества, не позволяющие клеткам крови слипаться и прилипать к стенкам сосудов, а с другой- при повреждении сосудов выделяются вещества, способствующие тромбообразованию.
2.Тромбоцитарный — за счет деятельности тромбоцитов.
Тромбоциты (кровяные пластинки)- самые маленькие клеточные элементы крови. Участвуют в процессе свертывания крови. Общее количество тромбоцитов подвержено значительным суточным колебаниям.
Существуют различные способы подсчета: в камере, в мазках
Снижение числа тромбоцитов – тромбоцитопения – наблюдается:
— при инфекционных заболеваниях
— при ионизирующем воздействии
Повышение числа тромбоцитов (тромбоцитоз) наблюдается:
— в послеоперационном периоде,
— при злокачественных опухолях.
3.Плазменные факторы свертывания.
— V11 — проконвертин (тромботропин)
— V111 -антигемофильный глобулин (АГГ)
— 1X -плазменный компонент тромбопластина (ПКТ)
— X111 -фибринолизирующий фактор
Плазменные факторы объединяются в следующие группы:
1.Коагуляционная система(свертывающая)-способствует свертыванию крови.
2.Антикоагуляционная система (противосвертывающая) — предотвращает самопроизвольное тромбообразование.
3.Фибринолитическая — расщепляет и удаляет фибрин из кровотока.
Коагулограмма является комплексом лабораторных тестов, дающих представление о состоянии системы свертывания крови, антикоагуляции и фибринолиза. Среди тестов есть простые ( ориентировочные) — позволяющие выявить грубые сдвиги, и уточняющие , которые более детально характеризуют механизм имеющихся нарушений.
К методам исследования сосудисто-тромбоцитарного гемостаза относятся:
-определение числа тромбоцитов,
-определение адгезионной и агрегационной способности тромбоцитов.
-исследование реакции кровяного сгустка и другие.
Время кровотечения (ВК) –интервал между временем прокола мякоти пальца и остановкой кровотечения.В норме остановка кровотечения наступает через 2-3 минуты от момента прокола и дает представление о функции тромбоцитов.
Удлинение времени кровотечения наблюдается при:
— длительном приеме антикоагулянтов
— Наряду с подсчетом тромбоцитов определяют адгезию тромбоцитов-свойство прилипать к поврежденной поверхности стенки сосуда.
— Индекс адгезивности в норме –20-50%.
— Снижение индекса свидетельствует об уменьшении адгезивной способности и наблюдается при:
Агрегация тромбоцитов — способность тромбоцитов соединятся .Спонтанная агрегация в норме-0-20%.Повышение агрегационной способности тромбоцитов отмечается при:
Снижение агрегационной способности отмечается:
Определение ретракции кровяного сгустка- процесс сокращения ,уплотнения и выделения сыворотки крови сгустком плсде образования фибрина под действием белка,содержащегося в тромбоцитах.
В норме индекс ретракции –48-64 %.
Индекс ретракции — отношение объема выделенной сыворотки к объему взятой крови. Его снижение бывает при тромбоцитопениях
К методам исследования коагуляционного гемостаза относятся:
— определение тромбинового времени
— определение количества фибриногена
— активированное частичное тромбопластиновое время (АЧТВ)
— определение толерантности плазмы.
Время свертывания — интервал между взятием крови и появлением в ней сгустка фибрина.
Норма для венозной крови –5-1-минут.
Норма для капиллярной крови: начало-30 секунд-2 мин., окончание 3-5 мин.
Увеличение времени свертывания крови происходит при гипокоагуляции за счет недостатка ряда плазменных факторов свертывания или действия антикоагулянтов. Наблюдается при заболеваниях печени.
Уменьшение времени свертывания отмечаетсяза за счет гиперкоагуляции при массивных кровотечениях
Тромбиновое время-время, за которое происходит превращение фибриногена в фибрин.
В норме тромбиновое время равно 15-18 секундам.Увеличение тромбинового времени отмечается при:
— врожденной недостаточности фибриногена.
Этот показатель служит контролем при лечении гепарином и фибринолитиками.
Фибриноген — белок синтезирующийся в печени и под действием X111 фактора, превращающийся в фибрин.
Норма фибриногена в крови –2-4 г/л.
Увеличение фибриногена свидетельствует о повышении свертываемости и риске образования тромбов.
| П О К А З А Т Е Л Ь | Лошадь | КРС | Овца | Коза | Свинья | Собака | Кошка |
| рН | 7,2-7,5 | 7,35-7,5 | 7,3 — 7,4 | 7,35-7,5 | 7,35-7,5 | 7,3-7,6 | 7,3-7,6 |
| Плотность | 1,046-1,059 | 1,052 | 1,051 | 1,051 | 1,046-1,054 | 1,051-1,062 | 1,052 |
| Гематокрит | 30,7% | 24-48% | 32% | 38 % | 32-47% | 50,4 % | 24-45% |
| Время свертывания (мин.) | 15 — 30 | 8 — 10 | 4 — 8 | 4 — 8 | 10 — 15 | 4 — 8 | 1 — 2 |
| Резистентность эритроцитов ( в NaCl) | 0,36-0,58 | 0,44-0,62 | 0,44-0,6 | 0,45-0,60 | 0,38-0,46 | 0,42-0,58 | 0,46-0,6 |
| СОЭ ( мм/ ч) | 40-70 | 0,5- 1,5 | 0,8 | 0,8 | 2 — 9 | 2 — 6 | |
| Гемоглобин (г% (ед.Сали) | 8 — 14 | 9 — 12 | 7 — 11 | 10 — 15 | 9 — 11 | 11-17 (60-80) | 10 — 14 |
| ЦП | 0,8 — 1,2 | 0,7 – 1,1 | 0,5 – 0,7 | 0,7 – 1,1 | 0,8 – 1,0 | 0,8 – 1,2 | 0,7 – 1,1 |
| СГЭ ( пг) | 17 — 20 | 16,5-18,5 | 10 — 13 | 16 — 18 | 16 — 19 | 19 — 23 | 17 — 20 |
Форменные элементы
| Форменные элементы | Лошадь | КРС | Овца | Коза | Свинья | Собака | Кошка |
| Эритроциты (млн./мм куб) | 6,0 – 9,0 | 5,0-7,5 | 7,0 – 12,0 | 12,0- 18,0 | 6,0 – 7,5 | 5,2-8,4 | 6,6 – 9,4 |
| Лейкоциты (тыс./ мм куб.) | 7,0- 12,0 | 4,5-12,0 | 6,0 – 14,0 | 8,0 – 17,0 | 8,0– 16,0 | 8,5-10,5 | 10,0-20,0 |
| Тромбоциты (тыс. мм куб) | 100-600 | 260-700 | 150 — 200 | 150- 300 | 200-500 | 200-600 | 300-700 |
Лейкограмма
| Вид животного | Б | Э | Нейтрофилы | Л | М | Профиль крови | ||
| Ю | П | С | ||||||
| Лошадь | 0 — 1 | 1 — 4 | 0 — 1 | 3 — 6 | 45 — 62 | 25 -44 | 2 — 4 | Нейтрофильный |
| КРС | 0 — 2 | 3- 20 | 0 — 1 | 2 — 5 | 20 — 35 | 40-75 | 2 -7 | Лимфоцитарный |
| Овца | 0 — 1 | 4 — 12 | 0 — 2 | 3 — 6 | 35 — 45 | 40 — 50 | 2 — 5 | Лимфоцитарный |
| Коза | 0 — 1 | 3 — 12 | 1 — 5 | 29 — 38 | 47 — 64 | 1 — 2 | Лимфоцитарный | |
| Свинья | 0 — 1 | 1 — 4 | 0 — 2 | 2 — 4 | 40 — 48 | 40 — 50 | 2 — 6 | Лимфоцитарный |
| Собака | 0 — 1 | 2 — 9 | 1 — 6 | 40 — 71 | 21 — 40 | 1 — 5 | Нейтрофильный | |
| Кошка | 0 — 1 | 2 — 8 | 0 — 1 | 3 — 9 | 40 — 45 | 36 — 51 | 1 — 5 | Лимфоцитарный |
1.Эритроциты ( млн./мм куб.) Х= эритроциты в 5 бол.кв.*4000*200(развед)
( 5 бол.кв. = 80 малым кв.) 80
2.Лейкоциты ( тыс. / мм куб.) Х= лейкоциты в 100б.кв. * 4000 * 20
(100бол.кв.=1600 малым) 1600
3.Тромбоциты (тыс. / мм куб.) Х= тромбоциты на 1000 эр-ов*норма эр-ов
ЦП – показатель степени насыщения эритроцитов гемоглобином.
ЦП = Найденное кол-во Нв * Норма эр-ов
Норма Нв * Найденное кол-во эр-ов
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Для студента самое главное не сдать экзамен, а вовремя вспомнить про него. 9658 — 

193.124.117.139 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
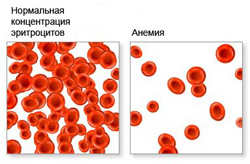
Эритроциты формируются в красном костном мозге из белковых фракций и небелковых компонентов под воздействием эритропоэтина (синтезируется почками). Эритроциты в течение трех дней обеспечивают транспорт, главным образом, кислорода и углекислого газа, а также питательных веществ и продуктов метаболизма от клеток и тканей. Срок жизни эритроцита сто двадцать дней, после чего он разрушается. Старые эритроциты накапливаются в селезенке, где утилизируются небелковые фракции, а белковые поступают в красный костный мозг, участвуя в синтезе новых эритроцитов.
Вся полость эритроцита наполнена белком, гемоглобином, в состав которого входит железо. Гемоглобин придает эритроциту красную окраску, а также помогает ему переносить кислород и углекислый газ. Его работа начинается в легких, куда эритроциты поступают с током крови. Молекулы гемоглобина захватывают кислород, после чего обогащенные кислородом эритроциты направляются сначала по крупным сосудам, а затем и по мелким капиллярам к каждому органу, отдавая клеткам и тканям необходимый для жизни и нормальной деятельности кислород.
Анемия ослабляет способность организма к газовому обмену, за счет сокращения числа эритроцитов нарушается транспортировка кислорода и углекислого газа. Вследствие этого у человека могут наблюдаться такие признаки анемии как чувство постоянной усталости, упадок сил, сонливость, а также повышенная раздражительность.
Анемия является проявлением основного заболевания и не является самостоятельным диагнозом. Многие болезни, включая инфекционные заболевания, доброкачественные или злокачественные опухоли могут быть связаны с анемией. Именно поэтому анемия является важным признаком, который требует проведения необходимых исследований для выявления основной причины, которая привела к ее развитию.
Тяжелые формы анемии вследствие тканевой гипоксии могут привести к серьезным осложнениям, таким как шоковые состояния (например, геморрагический шок), гипотония, коронарная или легочная недостаточность.
- по механизму развития;
- по степени тяжести;
- по цветному показателю;
- по морфологическому признаку;
- по способности костного мозга к регенерации.
| По патогенезу анемия может развиться вследствие кровопотери, нарушения образования эритроцитов или из-за их выраженного разрушения. По механизму развития выделяют:
|
- потеря крови (острые или хронические кровотечения);
- повышенное разрушение эритроцитов (гемолиз);
- уменьшенное производство эритроцитов.
Также следует заметить, что в зависимости от вида анемии причины ее возникновения могут отличаться.
Факторы, влияющие на развитие анемии
- гемоглобинопатии (изменение строения гемоглобина наблюдается при талассемии, серповидноклеточной анемии);
- анемия Фанкони (развивается вследствие имеющегося дефекта в кластере белков, которые отвечают за восстановление ДНК);
- ферментативные дефекты в эритроцитах;
- дефекты цитоскелета (клеточный каркас, располагающийся в цитоплазме клетки) эритроцита;
- врожденная дизэритропоэтическая анемия (характеризуется нарушением образования эритроцитов);
- абеталипопротеинемия или синдром Бассена-Корнцвейга (характеризуется нехваткой бета-липопротеина в клетках кишечника, что ведет к нарушению всасываемости питательных веществ);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (вследствие нарушения клеточной мембраны эритроциты принимают шарообразную форму).
- дефицит железа;
- дефицит витамина B12;
- дефицит фолиевой кислоты;
- дефицит аскорбиновой кислоты (витамин С);
- голодание и недоедание.
Хронические заболевания и новообразования
- почечные заболевания (например, туберкулез печени, гломерулонефрит);
- заболевания печени (например, гепатит, цирроз);
- заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, атрофический гастрит, неспецифический язвенный колит, болезнь Крона);
- коллагеновые сосудистые болезни (например, системная красная волчанка, ревматоидный артрит);
- доброкачественные и злокачественные опухоли (например, миома матки, полипы в кишечнике, рак почек, легких, кишечника).
- вирусные заболевания (гепатит, инфекционный мононуклеоз, цитомегаловирус);
- бактериальные заболевания (туберкулез легких или почек, лептоспироз, обструктивный бронхит);
- протозойные заболевания (малярия, лейшманиоз, токсоплазмоз).
Ядохимикаты и медикаментозные средства
- неорганический мышьяк, бензол;
- радиация;
- цитостатики (химиотерапевтические препараты, используемые для лечения опухолевых заболеваний);
- антибиотики;
- нестероидные противовоспалительные средства;
- антитиреоидные препараты (снижают синтез гормонов щитовидной железы);
- противоэпилептические препараты.
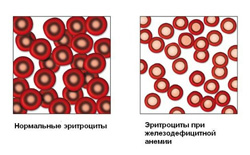
Для железодефицитной анемии характерно снижение эритроцитов, гемоглобина и цветового показателя.
Железо — это жизненно важный элемент, участвующий во многих метаболических процессах организма. У человека с весом семьдесят килограмм запас железа в организме составляет примерно четыре грамма. Данное количество поддерживается благодаря сохранению баланса между регулярными потерями железа из организма и его поступлением. Для поддержания равновесия суточная потребность железа составляет 20 – 25 мг. Большая часть поступающего железа в организм затрачивается на его нужды, остальное депонируется в виде ферритина или гемосидерина и при необходимости расходуется.
Нарушение поступления железа в организм
- вегетарианство вследствие неупотребления белков животного происхождения (мясо, рыба, яйца, молочные продукты);
- социально-экономическая составляющая (например, недостаточно денег для полноценного питания).
Нарушение усвоения железа
Всасывание железа происходит на уровне слизистых желудка, поэтому такие заболевания желудка как гастриты, язвенная болезнь или резекция желудка приводят к нарушению всасывания железа.
Повышенная потребность организма в железе
- беременность, в том числе многоплодная беременность;
- период лактации;
- подростковый возраст (за счет быстрого роста);
- хронические заболевания, сопровождающиеся гипоксией (например, хронический бронхит, пороки сердца);
- хронические нагноительные заболевания (например, хронические абсцессы, бронхоэктатическая болезнь, сепсис).
Потери железа из организма
- легочные кровотечения (например, при раке легких, туберкулезе);
- желудочно-кишечные кровотечения (например, язва желудка и двенадцатиперстной кишки, рак желудка, рак кишечника, варикозное расширение вен пищевода и прямой кишки, неспецифический язвенный колит, глистные инвазии);
- маточные кровотечения (например, преждевременная отслойка плаценты, разрыв матки, рак матки или шейки матки, прервавшаяся внематочная беременность, миома матки);
- почечные кровотечения (например, рак почек, туберкулез почек).
Питание при анемии
В питании железо делится на:
- гемовое, которое поступает в организм с продуктами животного происхождения;
- негемовое, которое поступает в организм с продуктами растительного происхождения.
Следует заметить, что гемовое железо усваивается в организме значительно лучше, нежели негемовое.
Количество железа на сто миллиграмм
Продукты питания
животного
происхождения
- печень;
- язык говяжий;
- мясо кролика;
- индюшатина;
- гусиное мясо;
- говядина;
- рыба.
- 9 мг;
- 5 мг;
- 4,4 мг;
- 4 мг;
- 3 мг;
- 2,8 мг;
- 2,3 мг.
Продукты питания растительного происхождения
- сушеные грибы;
- свежий горох;
- гречка;
- геркулес;
- свежие грибы;
- абрикосы;
- груша;
- яблоки;
- сливы;
- черешня;
- свекла.
- 35 мг;
- 11,5 мг;
- 7,8 мг;
- 7,8 мг;
- 5,2 мг;
- 4,1 мг;
- 2,3 мг;
- 2,2 мг;
- 2,1 мг;
- 1,8 мг;
- 1,4 мг.
При соблюдении диеты также следует увеличить потребление продуктов, содержащих витамин C, а также белок мяса (они повышают усвояемость железа в организме) и снизить потребление яиц, соли, кофеина и кальция (они уменьшают всасываемость железа).
Медикаментозное лечение
При лечении железодефицитной анемии больному параллельно с диетой назначается прием препаратов железа. Данные лекарственные средства предназначены для восполнения дефицита железа в организме. Они выпускаются в виде капсул, драже, инъекций, сиропов и таблеток.
Доза и длительность лечения подбирается индивидуально в зависимости от следующих показателей:
- возраста пациента;
- степени тяжести заболевания;
- причины, вызвавшей железодефицитную анемию;
- на основе результатов анализов.
Препараты железа принимаются за один час до еды или через два часа после приема пищи. Данные лекарственные средства нельзя запивать чаем или кофе, так как снижается всасываемость железа, поэтому их рекомендуется запивать водой или соком.
Принимать внутрь по одному грамму три – четыре раза в сутки.
Принимать по одной таблетке в день, с утра за тридцать минут до приема пищи.
Принимать по одной таблетке один – два раза в день.
Данные препараты рекомендуется назначать совместно с витамином C (по одной таблетке один раз в день), так как последний увеличивает всасываемость железа.
Препараты железа в виде инъекций (внутримышечных или внутривенных) применяются в следующих случаях:
- при тяжелой степени анемии;
- если анемия прогрессирует, несмотря на принимаемые дозы железа в виде таблеток, капсул или сиропа;
- если у больного имеются заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, неспецифический язвенный колит, болезнь Крона), так как принимаемый препарат железа может усугубить имеющееся заболевание;
- перед оперативными вмешательствами с целью ускоренного насыщения организма железом;
- если у пациента имеется непереносимость препаратов железа при их приеме внутрь.
Хирургическое лечение
Хирургическое вмешательство производится при наличии у больного острого или хронического кровотечения. Так, например, при желудочно-кишечном кровотечении может применяться фиброгастродуоденоскопия или колоноскопия с выявлением области кровотечения и последующей его остановкой (например, удаляется кровоточащий полип, коагулируется язва желудка и двенадцатиперстной кишки). При маточных кровотечениях, а также при кровотечениях в органах, находящихся в брюшной полости, может применяться лапароскопия.
При необходимости больному может быть назначено переливание эритроцитарной массы для восполнения объема циркулирующей крови.

В норме витамин В12 поступает в организм с пищевыми продуктами. На уровне желудка В12 связывается с продуцируемым в нем белком, гастромукопротеидом (внутренний фактор Касла). Данный белок защищает поступивший в организм витамин от негативного воздействия микрофлоры кишечника, а также способствует его усвоению.
Комплекс гастромукопротеид и витамин В12 доходит до дистального отдела (нижний отдел) тонкого кишечника, где происходит распад этого комплекса, всасывание витамина В12 в слизистый слой кишечника и дальнейшее поступление его в кровь.
Из кровяного русла данный витамин поступает:
- в красный костный мозг для участия в синтезе эритроцитов;
- в печень, где происходит его депонирование;
- в центральную нервную систему для синтеза миелиновой оболочки (покрывает аксоны нейронов).
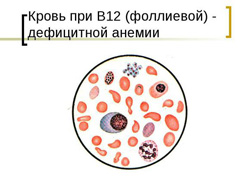
Клиническая картина В12 и фолиево-дефицитной анемии основывается на развитии у больного следующих синдромов:
- анемический синдром;
- желудочно-кишечный синдром;
- невралгический синдром.
| |
Данные симптомы развиваются вследствие атрофических изменений слизистого слоя ротовой полости, желудка и кишечника. |
|
- снижение уровня эритроцитов и гемоглобина;
- гиперхромия (выраженная окраска эритроцитов);
- макроцитоз (увеличенный размер эритроцитов);
- пойкилоцитоз (различная форма эритроцитов);
- при микроскопии эритроцитов выявляются кольца Кебота и тельца Жолли;
- ретикулоциты снижены или в норме;
- снижение уровня лейкоцитов (лейкопения);
- повышение уровня лимфоцитов (лимфоцитоз);
- снижение уровня тромбоцитов (тромбоцитопения).
В биохимическом анализе крови наблюдается гипербилирубинемия, а также снижение уровня витамина В12.
При пункции красного костного мозга выявляется повышение мегалобластов.
Больному могут быть назначены следующие инструментальные исследования:
- исследование желудка (фиброгастродуоденоскопия, биопсия);
- исследование кишечника (колоноскопия, ирригоскопия);
- ультразвуковое исследование печени.
Данные исследования помогают выявить атрофические изменения слизистой оболочки желудка и кишечника, а также обнаружить заболевания, которые привели к развитию В12-дефицитной анемии (например, злокачественные образования, цирроз печени).
Все больные госпитализируются в отделение гематологии, где проходят соответствующее лечение.
Питание при В12-дефицитной анемии
Назначается диетотерапия, при которой увеличивается потребление продуктов, богатых витамином В12.
Суточная норма витамина В12 составляет три микрограмма.
Количество витамина В12 на сто миллиграмм
Медикаментозное лечение
Медикаментозное лечение назначается больному по следующей схеме:
- В течение двух недель больной ежедневно получает по 1000 мкг Цианокобаламина внутримышечно. За две недели у пациента исчезает неврологическая симптоматика.
- В течение последующих четырех – восьми недель больной получает по 500 мкг ежедневно внутримышечно для насыщения депо витамина В12 в организме.
- Впоследствии больной пожизненно получает внутримышечные инъекции один раз в неделю по 500 мкг.
Во время лечения одновременно с Цианокобаламином больному могут назначить прием фолиевой кислоты.
Больной В12-дефицитной анемией должен пожизненно наблюдаться у гематолога, гастролога и семейного врача.
Фолиевая кислота (витамин B9) является водорастворимым витамином, который отчасти продуцируется клетками кишечника, но в основном должен поступать извне для восполнения необходимой для организма нормы. Суточная норма фолиевой кислоты составляет прием 200 – 400 мкг.
В пищевых продуктах, а также в клетках организма фолиевая кислота находится в форме фолатов (полиглутаматы).
Фолиевая кислота играет большую роль в организме человека:
- участвует в развитии организма во внутриутробном периоде (способствует формированию нервной проводимости тканей, кровеносной системы плода, предупреждает развитие некоторых пороков развития);
- участвует в росте ребенка (например, в первый год жизни, в период полового созревания);
- влияет на процессы кроветворения;
- совместно с витамином В12 участвует в синтезе ДНК;
- препятствует образованию тромбов в организме;
- улучшает процессы регенерации органов и тканей;
- участвует в обновлении тканей (например, кожи).
Абсорбция (всасывание) фолатов в организме осуществляется в двенадцатиперстной кишке и в верхнем отделе тонкого кишечника.
При фолиеводефицитной анемии у больного наблюдается анемический синдром (такие симптомы как повышенная утомляемость, сердцебиение, бледность кожных покровов, снижение работоспособности). Неврологический синдром, а также атрофические изменения слизистой оболочки ротовой полости, желудка и кишечника при данном виде анемии отсутствуют.
Также у больного может наблюдаться увеличение размеров селезенки.
При общем анализе крови наблюдаются следующие изменения:
- гиперхромия;
- снижение уровня эритроцитов и гемоглобина;
- макроцитоз;
- лейкопения;
- тромбоцитопения.
В результатах биохимического анализа крови наблюдается снижение уровня фолиевой кислоты (менее 3 мг/мл), а также повышение непрямого билирубина.
При проведении миелограммы выявляется повышенное содержание мегалобластов и гиперсегментированных нейтрофилов.
Питание при фолиеводефицитной анемии играет большую роль, больному необходимо ежедневно потреблять продукты, богатые фолиевой кислотой.
Следует заметить, что при любой кулинарной обработке продуктов фолаты разрушаются приблизительно на пятьдесят процентов и более. Поэтому для обеспечения организма необходимой суточной нормой продукты рекомендуется употреблять в свежем виде (овощи и фрукты).
| Продукты питания | Наименование продуктов | Количество железа на сто миллиграмм |
| Продукты питания животного происхождения |
|
|
| Продукты питания растительного происхождения |
|
|
Медикаментозное лечение фолиеводефицитной анемии включает прием фолиевой кислоты в количестве от пяти до пятнадцати миллиграмм в сутки. Необходимую дозировку устанавливает лечащий врач в зависимости от возраста пациента, тяжести течения анемии и результатов исследований.
Профилактическая доза включает прием одного – пяти миллиграмм витамина в сутки.
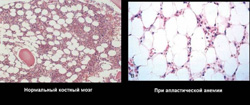
Апластическая анемия может быть врожденной или приобретенной.
Клинические проявления апластической анемии зависят от степени выраженности панцитопении.
При апластической анемии у больного наблюдаются следующие симптомы:
- бледность кожных покровов и слизистых;
- головная боль;
- учащенное сердцебиение;
- одышка;
- повышенная усталость;
- отеки на ногах;
- десневые кровотечения (вследствие снижения уровня тромбоцитов в крови);
- петехиальная сыпь (красные пятна на коже маленьких размеров), синяки на коже;
- острые или хронические инфекции (вследствие снижения уровня лейкоцитов в крови);
- изъязвления орофарингеальной зоны (поражается слизистая полости рта, язык, щеки, десна и глотка);
- желтушность кожных покровов (симптом поражения печени).
При биохимическом анализе крови наблюдается:
- повышение сывороточного железа;
- насыщение трансферрина (белок, переносящий железо) железом на 100%;
- повышение билирубина;
- повышение лактатдегидрогеназы.
При пункции красного мозга и последующем гистологическом исследовании выявляются:
- недоразвитие всех ростков (эритроцитарный, гранулоцитарный, лимфоцитарный, моноцитарный и макрофагальный);
- замещение костного мозга жировым (желтый костный мозг).
Среди инструментальных методов исследований больному может быть назначено:
- ультразвуковое исследование паренхиматозных органов;
- электрокардиография (ЭКГ) и эхокардиография;
- фиброгастродуоденоскопия;
- колоноскопия;
- компьютерная томография.
При правильно подобранном поддерживающем лечении состояние пациентов с апластической анемией существенно улучшается.
При лечении апластической анемии больному назначаются:
- иммунодепрессивные препараты (например, Циклоспорин, Метотрексат);
- глюкокортикостероиды (например, Метилпреднизолон);
- антилимфоцитарный и антитромбоцитарный иммуноглобулины;
- антиметаболиты (например, Флударабин);
- эритропоэтин (стимулирует образование эритроцитов и стволовых клеток).
Немедикаментозное лечение включает:
- трансплантацию костного мозга (от совместимого донора);
- переливание компонентов крови (эритроциты, тромбоциты);
- плазмаферез (механическое очищение крови);
- соблюдение правил асептики и антисептики с целью предотвращения развития инфекции.
Также при тяжелом течении апластической анемии больному может понадобиться хирургическое лечение, при котором производится удаление селезенки (спленэктомия).
В зависимости от эффективности проводимого лечения у больного при апластической анемии может наблюдаться:
- полная ремиссия (затухание или полное исчезновение симптомов);
- частичная ремиссия;
- клиническое улучшение;
- отсутствие эффекта от лечения.
|
|
|
|

Гемолитическая анемия может развиться вследствие наследственных или приобретенных заболеваний.
По локализации гемолиз может быть:
- внутриклеточным (например, аутоиммунная гемолитическая анемия);
- внутрисосудистым (например, переливание несовместимой крови, диссеминированное внутрисосудистое свертывание).
У пациентов с легкой степенью гемолиза уровень гемоглобина может быть нормальным, если производство эритроцитов соответствует темпу их разрушения.
Преждевременное разрушение эритроцита может быть связано со следующими причинами:
- внутренними мембранными дефектами эритроцитов;
- дефектами структуры и синтеза белка гемоглобина;
- ферментативными дефектами в эритроците;
- гиперспленомегалией (увеличение размеров печени и селезенки).
Наследственные заболевания могут вызвать гемолиз в результате отклонений мембраны эритроцита, ферментативных дефектов и отклонений гемоглобина.
Существуют следующие наследственные гемолитические анемии:
- энзимопатии (анемии, при которых наблюдается недостаток фермента, дефицит глюкозо-6-фосфатдегидрогеназы);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (эритроциты неправильной шарообразной формы);
- талассемия (нарушение синтеза полипептидных цепей, входящих в строение нормального гемоглобина);
- серповидно-клеточная анемия (изменение строения гемоглобина приводит к тому, что эритроциты принимают серпообразную форму).
Приобретенные причины гемолитической анемии включают иммунные и не иммунные нарушения.
Иммунные нарушения характеризуются аутоиммунной гемолитической анемией.
Не иммунные нарушения могут быть вызваны:
- ядохимикатами (например, пестициды, бензол);
- лекарственными средствами (например, противовирусные препараты, антибиотики);
- физическим повреждением;
- инфекциями (например, малярия).
Гемолитическая микроангиопатическая анемия приводит к производству фрагментированных эритроцитов и может быть вызвана:
- дефектным искусственным сердечным клапаном;
- диссеминированным внутрисосудистым свертыванием;
- гемолитическим уремическим синдромом;
- тромбоцитопенической пурпурой.
Симптомы и проявления гемолитической анемии разнообразны и зависят от вида анемии, степени компенсации, а также от того, какое лечение получал больной.
Следует заметить, что гемолитическая анемия может протекать бессимптомно, а гемолиз выявляться случайно во время обычного лабораторного тестирования.
При гемолитической анемии могут наблюдаться следующие симптомы:
- бледность кожи и слизистых;
- ломкость ногтей;
- тахикардия;
- учащение дыхательных движений;
- снижение артериального давления;
- желтушность кожных покровов (из-за увеличения уровня билирубина);
- на ногах могут наблюдаться язвы;
- гиперпигментация кожи;
- желудочно-кишечные проявления (например, боль в животе, нарушение стула, тошнота).
Следует заметить, что при внутрисосудистом гемолизе у больного наблюдается дефицит железа из-за хронической гемоглобинурии (наличие гемоглобина в моче). Вследствие кислородного голодания нарушается сердечная функция, что приводит к развитию у пациента таких симптомов как слабость, тахикардия, одышка и стенокардия (при тяжелой форме анемии). Из-за гемоглобинурии у больного также наблюдается потемнение мочи.
Длительный гемолиз может привести к развитию желчных камней вследствие нарушения обмена билирубина. При этом пациенты могут жаловаться на боль в животе и бронзовый цвет кожи.
В общем анализе крови наблюдается:
- снижение уровня гемоглобина;
- снижение уровня эритроцитов;
- увеличение ретикулоцитов.
При микроскопии эритроцитов выявляется их серпообразная форма, а также кольца Кебота и тельца Жолли.
В биохимическом анализе крови наблюдается повышение уровня билирубина, а также гемоглобинемия (увеличение свободного гемоглобина в плазме крови).
Также необходимо сдать анализ мочи на выявление наличия гемоглобинурии.
При пункции костного мозга наблюдается выраженная гиперплазия эритроцитарного ростка.
Существует много видов гемолитической анемии, поэтому лечение может отличаться в зависимости от причины, вызвавшей анемию, а также от типа гемолиза.
При лечении гемолитической анемии больному могут назначаться следующие препараты:
- Фолиевая кислота. Профилактическая доза фолиевой кислоты назначается, потому что активный гемолиз может потреблять фолат и впоследствии привести к развитию мегалобластоза.
- Глюкокортикостероиды (например, Преднизолон) и иммунодепрессанты (например, Циклофосфан). Данные группы препаратов назначаются при аутоиммунной гемолитической анемии.
- Переливание эритроцитарной массы. Больному индивидуально подбираются отмытые эритроциты, так как существует высокий риск разрушения перелитой крови.
Спленэктомия
Спленэктомия может быть первоначальным вариантом в лечении некоторых типов гемолитической анемии, таких как, например, наследственный сфероцитоз. В других случаях, например, при аутоиммунной гемолитической анемии, спленэктомия рекомендуется тогда, когда другие методы лечения потерпели неудачу.
Терапия препаратами железа
При гемолитической анемии применение препаратов железа в большинстве случаев противопоказано. Это связано с тем, что уровень железа при данной анемии не снижается. Однако если у больного наблюдается постоянная гемоглобинурия, то происходит существенная потеря железа из организма. Поэтому при выявлении дефицита железа пациенту может быть назначено соответствующее лечение.
Проявления анемии будут зависеть от следующих факторов:
- какое количество крови было потеряно;
- с какой скоростью происходит кровопотеря.
Симптомами постгеморрагической анемии являются:
- слабость;
- головокружение;
- бледность кожных покровов;
- сердцебиение;
- одышка;
- тошнота, рвота;
- сечение волос и ломкость ногтей;
- шум в ушах;
- мелькание мушек перед глазами;
- жажда.
При острой кровопотере у больного может развиться геморрагический шок.
Выделяют четыре степени геморрагического шока.
источник