Анемия — тип заболеваний крови, которые включены в список МКБ 10. Заключается в более низких значениях гемоглобина, эритроцитов и их последствий.
Анемия — это болезни разнообразной этиологии, проявляющиеся в аномальном расщеплении эритроцитов. Эритроциты продуцируются в костном мозге и циркулируют в крови около 120 дней. Существует много причин, приводящих к значительному сокращению времени их выживания и к образованию анемии.
Заболевание делится на классификации в соответствии с этиологическими факторами на наследственные и приобретенные гемолитические анемии.
Наследственные заболевания включают:
- дефекты клеточной мембраны эритроцитов;
- аномалии ферментов, необходимых для правильных метаболических процессов в эритроцитах;
- патологии, связанные с гемоглобином.
- аутоиммунные процессы;
- тромбоз;
- диссеминированная внутрисосудистая коагуляция;
- инфекции (например, малярия);
- хронические заболевания, такие как сифилис, заболевания печени и почек;
- гиперспленизм (увеличение селезенки с сопровождающимся увеличением распада эритроцитов).
Врожденные показатели выявляются в молодом возрасте. Аутоиммунные формы чаще всего затрагивают пожилых людей. У людей с тяжелой болезнью часто нет клинических симптомов в течение длительного времени. Врожденные и приобретенные гемолитические анемии проявляются разными симптомами.
Общие симптомы анемии обычно возникают при падении гемоглобина ниже 8,5 г/дл, или когда анемия развивается достаточно быстро, поэтому организм неспособен адаптироваться. К ним относятся:
- слабость, легкая утомляемость;
- ухудшение концентрации и внимания;
- боль, головокружение;
- тахикардия;
- одышка;
- бледность кожи и слизистых оболочек.
Кроме того, существуют симптомы, которые помогают диагностировать наследственную анемию у детей, то есть желтуху с различной степенью тяжести, возникающую в периоды сильной эрозии эритроцитов.
Вторым характерным симптомом является увеличение селезенки и печени из-за разрушения эритроцитов и чрезмерного накопления железа в клетках этих органов.
Наследственные гемолитические анемии у детей являются заболеванием, вызванным иммунной реакцией между антителами матери и антигенами плодной крови. Это называется серологическим конфликтом, который возникает, когда мать имеет систему антигена Rh (-) крови, а ребенок — Rh (+).
Апластическая анемия является относительно редким типом этой группы заболеваний. Выявляется у 2-6 человек на миллион. Характеризуется нарушением производства клеток крови в костном мозге, специальной ткани, заполняющей внутреннюю часть костей. Выделяют желтый костный мозг, состоящий из жировой ткани, и красный костный мозг, который отвечает за продуцирование как красных кровяных телец (эритроцитов), так и белых кровяных клеток (лейкоцитов), тромбоцитов.
У детей внутренность костей заполнена красным костным мозгом. По прошествии лет она заменяется желтым костным мозгом, а производство клеток крови происходит только в плоских костях.
У людей, страдающих апластической анемией, обнаруживается гипоплазия костного мозга. При врожденной железодефицитной анемии присутствует только дефицит эритроцитов, а гипоплазия костного мозга приводит не только к недостаточному количеству эритроцитов, но и лейкоцитов и тромбоцитов. Вышеуказанные нарушения связаны с характерными симптомами.
Симптомы апластической анемии могут возникать внезапно или медленно, в течение недель или даже месяцев. Врожденная анемия у детей может развиваться в хроническую форму. Она способна привести к смерти пациента.
Можно выделить две группы причин, приводящих к развитию апластической анемии — унаследованные и приобретенные причины. Врожденные апластические анемии появляются в 25% случаев, диагностированных у детей.
Анемия Даймонда-Блекфена — это врожденная гипопластическая анемия, которая обычно проявляется в младенчестве.
Примерно у 30% пациентов наблюдаются другие врожденные аномалии, особенно верхних конечностей, черепно-лицевых областей, сердца и урогенитального тракта.
Хотя большинство патологий являются случайными, приблизительно 10-25% — семейные, причем многие из них демонстрируют аутосомно-доминантное наследование.
Показатели лейкоцитов и тромбоцитов нормальны или немного уменьшены. Точная причина не ясна, но существует расстройство биогенеза рибосом.
Является одной из редких групп генетических заболеваний, известных как наследственные синдромы отказа работы костного мозга.
Примерно у 25% пораженных детей существует ошибка в гене, называемым рибосомным белком S19 (RPS19). Имеются данные об участии ряда других генов.
Тяжесть симптомов варьируется, но часто различна и опасна для жизни.
Обычно это проявляется в первые несколько месяцев жизни, когда у маленького ребенка развивается тяжелая гипопластическая макроцитарная анемия. У некоторых детей может не развиться анемия до позднего детства.
Физические аномалии присутствуют у 50% пораженных детей. Существует широкий диапазон серьезных отклонений. Многие дети очень малы для своего возраста.
источник
Существует очень много возможных причин развития анемии.
Иногда анемия возникает в результате определенных хронических заболеваний, таких как рак или болезни почек.
Для таких больных лечение анемии – это составная часть лечения их основного заболевания.
Но анемия может также быть вызвана рядом генетических вариаций, которые передаются из поколения в поколение. Гены, половину которых мы получаем от отца, а половину от матери, кодируют абсолютно все функции нашего организма, и кроветворение в том числе.
Как и все остальные процессы в человеческом теле, продукция красных кровяных телец проходит в несколько этапов, в которых участвуют сотни разных молекул. Если на любом из этих этапов что-то пойдет не так, как задумано природой, созревание красных кровяных телец может нарушиться, и возникнет анемия.
То, как организм усваивает из пищи железо и витамины, очень важно для правильной продукции клеток крови. Если тело не в состоянии усвоить, к примеру, железо, то будет нарушен синтез гемоглобина, и наши эритроциты не смогут доставлять достаточно кислорода клеткам. Нарушение всасывания нутриентов – это первый из возможных механизмов наследственной анемии. Но, как вы увидите дальше, он далеко не единственный.
Анемия представляет собой состояние, при котором снижается содержание пигмента гемоглобина в крови, а также уменьшается количество эритроцитов. Основной проблемой при анемии является недостаточное снабжение тканей кислородом, что сказывается на состоянии практически всех органов и систем, особенно нервной системы.
У больных анемией может возникать слабость, чрезмерная утомляемость, головокружения, раздражительность, одышка, ускоренное сердцебиение, бледность кожи и слизистых, ломкость ногтей и другие симптомы. У некоторых больных отмечается странная тяга к несъедобным вещам, таким как лед, бумага или глина. Возникают проблемы в сексуальной сфере. Ухудшается способность воспринимать информацию и решать интеллектуальные задачи. Падает иммунитет и, как следствие, человек чаще страдает инфекционными заболеваниями.
Врачи обычно сосредотачиваются на распространенных типах анемии, вызванных дефицитом железа, старением, перенесенными операциями и хроническими болезнями, включая рак, диабет, воспалительные заболевания кишечника, болезни почек, болезни сердца, гепатит, ВИЧ/СПИД, ревматоидный артрит и другие. Эти типы анемии хорошо известны, и можно встретить массу информационных ресурсов, посвященных таким проблемам, особенно в англоязычном интернете.
Можем обрадовать англоязычных пользователей, перечислив для них наиболее известные на Западе группы и фонды, которые предоставляют очень качественную информацию об анемиях, в том числе наследственных:
• Американская ассоциация серповидноклеточной анемии (The American Sickle Cell Anemia Association).
• Международная федерация талассемии (Thalassaemia International Federation).
• Международный фонд наследственной геморрагической телеангиэктазии (Hereditary Hemorrhagic Telangiectasia Foundation International).
• Фонд анемии Даймонда-Блекфена (Diamond Blackfan Anemia Foundation).
• Фонд анемии Кули (Cooley’s Anemia Foundation)
• Фонд исследования анемии Фанкони (Fanconi Anemia Research Fund).
• Фонд синдрома Швахмана-Даймонда (Shwachman-Diamond Syndrome Foundation).
Реже встречаются наследственные анемии, которые вызваны генетическими сбоями на разных этапах производства красных кровяных телец. Эти заболевания могут приводить к синтезу «неправильных» эритроцитов или гемоглобина, к быстрому уничтожению эритроцитов в крови (гемолизу) и др. Ниже вы найдете список основных генетических заболеваний, приводящих к анемии:
1. Серповидноклеточная анемия.
Серповидноклеточная анемия представляет собой генетическое заболевание, при котором красные кровяные тельца имеют аномальную форму полумесяца или буквы «С». Эти аномальные эритроциты не справляются со своими функциями, и пребывают в кровеносном русле всего 10-20 суток вместо положенных для здоровых клеток 120 дней. Организм постоянно синтезирует новые клетки, но анемия развивается из-за короткого периода жизни эритроцитов. Заболеванию наиболее подвержены люди африканского происхождения.
Талассемия – это заболевание, при котором организм неправильно синтезирует некоторые протеины, необходимые для «сборки» гемоглобина. Умеренная или тяжелая анемия может стать результатом отсутствия тех или иных протеинов, в зависимости от этого талассемия подразделяется на несколько видов. Талассемию можно лечить постоянными переливаниями крови или трансплантацией костного мозга. Болезнь характерна для выходцев из средиземноморских стран.
Анемия Фанкони относится к заболеваниям, при которых костный мозг не может производить и эритроциты, и другие типы клеток крови (лейкоциты и тромбоциты). Это приводит к анемии, которая лечится трансплантацией костного мозга. У таких больных зачастую обнаруживаются другие врожденные дефекты, а также повышенная восприимчивость к различным типам рака (острый миелобластный лейкоз, рак головы и шеи, рак пищевода, рак вульвы, анальный рак и другие). Этот диагноз часто ставят детям в возрасте 10-15 лет, но анемия Фанкони может быть впервые обнаружена и в зрелом возрасте.
4. Анемия Даймонда-Блекфена.
Анемия Даймонда-Блекфена – это редкое заболевание, для которого характерен дефект синтеза красных кровяных телец в костном мозге. Анемия Даймонда-Блекфена может развиться в любом возрасте, но обычно ее диагностируют в течение первого года жизни. При этом заболевании также присутствуют некоторые физические дефекты и аномалии черт лица. У больных относительно высокий риск острого миелобластного лейкоза.
5. Синдром Швахмана-Даймонда (SDS).
Этот синдром, нечасто встречающийся в отечественной литературе, является генетическим нарушением синтеза белых и красных кровяных телец в костном мозге и пищеварительных ферментов поджелудочной железы. Пониженная продукция клеток крови ведет к постоянным инфекциям и анемии. Симптомы начинают проявляться уже в возрасте 4-6 месяцев: замедленный рост, диарея, проблемы с кормлением. Со стороны поджелудочной железы наблюдаются нарушения, напоминающие муковисцидоз. Болезнь диагностируется в первые годы жизни ребенка.
6. Нарушения мембраны эритроцитов.
Эти заболевания вызывают нестабильность клеточной структуры и появление красных кровяных телец аномальной формы. Самая известная из этих патологий – наследственный микросфероцитоз, или болезнь Минковского-Шоффара. При этой болезни эритроциты имеют необычную сферическую форму и быстро разрушаются. Это заболевание характерно для людей родом из Северной Европы.
Наследственный эллиптоцитоз сопровождается образованием большого количества овальных эритроцитов. Болезнь чаще встречается у людей африканского или средиземноморского происхождения.
Наследственный стоматоцитоз – третья форма, для которой характерно образование эритроцитов со светлой областью посередине (похожие на рот, откуда и название болезни). У этих клеток нарушен транспорт натрия и калия через оболочку. Тяжесть анемии бывает разной, некоторые больные могут вообще не иметь никаких жалоб.
7. Дефицит глюкозо-6-фосфатдегидрогеназы.
Дефицит фермента G6PD – это наследственное заболевание, при котором в организме не вырабатывается важный энзим, защищающий клетки крови от разрушения химикатами и лекарственными веществами. Дефицит G6PD – это самый распространенный на планете ферментный дефицит, которым страдает более 400 миллионов человек, преимущественно из Африки, Азии и Средиземноморья. У таких людей в ответ на инфекцию, токсины или лекарства может развиться гемолиз – массовое разрушение красных кровяных телец.
8. Наследственная геморрагическая телеангиэктазия.
Наследственная геморрагическая телеангиэктазия (НГТ) – это состояние, при котором у больных часто возникают кровотечения в местах неправильного соединения вен и артерий. В результате повторяющейся потери крови, в основном из желудка и кишечника, у них развивается анемия.
Перечисленные выше болезни – это лишь часть из возможных генетических причин анемии. Люди с любым заболеванием, которое ухудшает работу костного мозга или влияет на всасывание витамина В12 или железа в пищеварительном тракте, также могут страдать анемией.
К таким болезням можно отнести:
• Врожденный дискератоз.
• Врожденные дизэритропоэтические анемии.
• Врожденные синдромы мальабсорбции витамина В12.
Из заболеваний, которые затрагивают обмен железа, можно отметить гемохроматоз. Эта болезнь не является причиной анемии. При гемохроматозе организм усваивает намного больше железа, чем ему необходимо. В результате избыток железа откладывается в органах и тканях, повреждая их. Гемохроматоз – это одно их самых частых генетических заболеваний. На изучении этого заболевания в США специализируется некоммерческая организация Iron Disorders Institute.
Поскольку наследственные анемии обусловлены определенными нарушениями в генах, существует много надежных способов поставить диагноз. Наличие анемии и других характерных симптомов могут навести врача на мысль, что у вас одно из этих заболеваний. Генетический анализ расставит все точки над «i». Чтобы помочь врачу в этой работе, вы должны как можно больше сообщить ему о состоянии здоровья ваших родственников.
Для этого вам неплохо бы иметь семейную медицинскую историю – систематизированные записи о здоровье всех родных.
источник
Железодефицитная анемия – клинико-гематологический синдром, обусловленный недостатком железа в организме человека, что влечет нарушение нормального синтеза гемоглобина и гипоксию тканей.
Патология широко распространена. По статистическим данным, у 8-10% женщин детородного возраста диагностируется железодефицитная анемия, а у 30% женщин – латентный дефицит железа. В раннем детском возрасте признаки железодефицитной анемии выявляются у каждого второго ребенка. В структуре всех анемий на долю железодефицитной приходится 90%.
В основе развития железодефицитной анемии лежит отрицательный баланс обмена железа. К этому могут приводить разные факторы, но чаще всего причиной дефицита железа становится хроническая кровопотеря:
- кровотечения из геморроидальных узлов или анальных трещин;
- дисфункциональные маточные кровотечения;
- обильные менструации;
- желудочно-кишечные кровотечения (из эрозий и язв слизистой оболочки желудка или кишечника).
Другие причины кровопотери:
- гельминтозы;
- гемосидероз легких;
- геморрагические диатезы (болезнь Виллебранда, гемофилия);
- гемоглобинурия;
- обширные травмы и операции;
- частая сдача крови (донорство).
Нередко железодефицитная анемия развивается и у пациентов с хронической почечной недостаточностью, находящихся на программном гемодиализе.
При железодефицитных состояниях происходит снижение активности IgA; в результате у пациентов зачастую возникают кишечные и респираторные инфекции.
Недостаток железа в организме также может сформироваться в результате недостаточного поступления его из пищи по следующим причинам:
- низкий уровень жизни;
- вегетарианство;
- соблюдение диеты, ограничивающей употребление мясных продуктов;
- анорексия;
- искусственное вскармливание детей грудного возраста, особенно при позднем введении прикорма.
Ряд заболеваний и патологических состояний органов пищеварительной системы может приводить к нарушению всасывания железа и развитию железодефицитной анемии:
- гастерэктомия;
- состояние после резекции тонкой кишки;
- синдром мальабсорбции;
- хронический энтерит;
- гипоацидный гастрит;
- кишечные инфекции.
Железодефицитная анемия развивается и у пациентов, страдающих хроническими гепатитами или циррозом печени. В данном случае нарушается транспорт железа из депо.
Железодефицитная анемия может также появиться на фоне повышенной потребности в железе (в период полового созревания, беременности либо лактации) или при значительных потерях этого элемента (при онкологических, инфекционных заболеваниях).
В зависимости от причины железодефицитные анемии делятся следующим образом:
- алиментарные;
- постгеморрагические;
- связанные с нарушением транспорта железа, недостаточностью его резорбции или повышенным расходом;
- обусловленные врожденным (исходным) дефицитом железа.
По степени выраженности лабораторных и клинических признаков железодефицитные анемии бывают:
- легкими (гемоглобин выше 90 г/л);
- средней тяжести (гемоглобин от 70 до 90 г/л);
- тяжелыми (гемоглобин менее 70 г/л).
Железодефицитная анемия легкой степени в большинстве случаев протекает без-каких либо клинических проявлений или с минимальной их выраженностью. Тяжелая форма сопровождается развитием гематологического, сидеропенического и циркуляторно-гипоксического синдромов.
В течении железодефицитной анемии выделяют несколько стадий:
- Предлатентный железодефицит – истощается депонированное железо, гемоглобиновые и транспортные запасы сохранены.
- Латентный железодефицит – происходит снижение запасов содержащегося в плазме крови транспортного железа.
- Собственно железодефицитная анемия – истощение всех метаболических запасов железа (эритроцитарного, транспортного и депонированного).
В клинической картине железодефицитной анемии выделяют синдромы:
- циркуляторно-гипоксический;
- сидеропенический;
- астеновегетативный.
Возникающие на фоне железодефицитной анемии циркуляторно-гипоксические нарушения ухудшают течение сопутствующих заболеваний сердечно-сосудистой и дыхательных систем.
Развитие циркуляторно-гипоксического синдрома обусловлено нарушением синтеза гемоглобина, в результате чего страдает транспорт кислорода и развивается тканевая гипоксия. Клинически это проявляется:
- общей слабостью;
- сонливостью;
- головокружениями;
- шумом в ушах;
- преходящими обмороками;
- учащенным сердцебиением;
- повышенной чувствительностью к низкой температуре;
- одышкой, возникающей при физических нагрузках, а при тяжелой анемии – и в состоянии покоя.
Механизм развития сидеропенического синдрома связан с дефицитом железосодержащих тканевых ферментов (цитохромов, пероксидазы, каталазы). Недостаток названных ферментов становится причиной наблюдаемых на фоне железодефицитной анемии трофических расстройств со стороны слизистых оболочек и кожных покровов. Признаки сидеропенического синдрома:
- сухость кожи;
- деформация, повышенная ломкость и поперечная исчерченность ногтей;
- выпадение волос;
- атрофический гастрит;
- дисфагия;
- ангулярный стоматит;
- глоссит;
- искажения вкуса (желание употреблять в пищу несъедобные предметы, например глину или зубной порошок);
- дизурические расстройства;
- диспепсия;
- мышечная слабость.
Астеновегетативный синдром характеризуется эмоциональной лабильностью, повышенной раздражительностью, ухудшением памяти, снижением работоспособности.
Клиническая картина железодефицитной анемии у детей неспецифична, преобладает один из следующих синдромов:
- Астеновегетативный. Связан с кислородным голоданием тканей нервной системы. Проявляется снижением мышечного тонуса и задержкой психомоторного развития ребенка. При тяжелой степени железодефицитной анемии и отсутствии необходимой терапии возможна интеллектуальная недостаточность. К другим проявлениям астеновегетативного синдрома относят энурез, обморочные состояния, головокружение, раздражительность и плаксивость.
- Эпителиальный. Характеризуется изменениями со стороны кожи и ее придатков. Кожные покровы становятся сухими, в области коленей и локтей развивается гиперкератоз, волосы теряют блеск и активно выпадают. Часто развиваются хейлит, глоссит, ангулярный стоматит.
- Диспепсический. Снижается аппетит вплоть до полного отказа от еды, наблюдаются неустойчивость стула (поносы, чередующиеся с запорами), вздутие живота, дисфагия.
- Сердечно-сосудистый. Развивается на фоне тяжелой железодефицитной анемии и проявляется одышкой, снижением артериального давления, тахикардией, шумами в сердце и дистрофическими изменениями в миокарде.
- Синдром иммунодефицита. Характеризуется немотивированным повышением температуры до субфебрильных значений. Дети подвержены респираторным кишечным инфекциям с тяжелым и (или) затяжным течением.
- Гепатолиенальный. Наблюдается на фоне выраженной железодефицитной анемии, особенно сочетающейся с другими видами анемий или рахитом. Проявляется увеличением размеров печени и селезенки.
В раннем детском возрасте признаки железодефицитной анемии выявляются у каждого второго ребенка.
Диагностика состояния, а также определение степени его тяжести осуществляются по результатам лабораторных исследований. Для железодефицитной анемии характерны следующие изменения:
- снижение содержания гемоглобина в крови (норма для женщин – 120–140 г/л, для мужчин – 130–150 г/л);
- пойкилоцитоз (изменение формы эритроцитов);
- микроцитоз (наличие в крови аномально маленьких по своим размерам эритроцитов);
- гипохромия (цветовой показатель – менее 0,8);
- снижение концентрации сывороточного железа (норма для женщин – 8,95–30,43 мкмоль/л, для мужчин – 11,64–30,43 мкмоль/л);
- уменьшение концентрации ферритина (норма для женщин – 22–180 мкг/л, для мужчин – 30–310 мкг/л);
- уменьшение насыщения трансферрина железом (норма – 30%).
Для эффективного лечения железодефицитной анемии важно установить причину, ее вызвавшую. С целью обнаружения источника хронической кровопотери показано проведение:
- ФЭГДС;
- рентгенографии желудка с контрастированием;
- колоноскопии;
- ирригоскопии;
- ультразвукового исследования органов малого таза;
- исследования кала на скрытую кровь.
По статистическим данным, у 8-10% женщин детородного возраста диагностируется железодефицитная анемия, а у 30% женщин – латентный дефицит железа.
В сложных диагностических случаях выполняют пункцию красного костного мозга с последующим гистологическим и цитологическим исследованием полученного пунктата. Значительное снижение в нем сидеробластов свидетельствует о наличии железодефицитной анемии.
Дифференциальная диагностика проводится с другими видами гипохромных анемий (талассемией, сидеробластной анемией).
Принципы терапии железодефицитной анемии:
- устранение источника хронической кровопотери;
- коррекция рациона;
- восполнение недостатка железа.
Важную роль играет диетотерапия. В рацион включают язык, печень, мясо кролика, баранину, говядину, телятину – продукты, богатые гемовым железом. Для улучшения всасывания железа из желудочно-кишечного тракта необходимы аскорбиновая, янтарная и лимонная кислоты, которые в большом количестве содержатся в свежих фруктах и ягодах. Исключают шоколад, молоко, соевый протеин, чай, кофе, поскольку они ингибируют всасывание железа.
Но только лишь диетой восполнить уже образовавшийся дефицит железа невозможно. Пациенты с железодефицитной анемией проходят заместительную терапию ферропрепаратами длительным курсом (не менее 2-2,5 месяцев).
При тяжелой форме железодефицитной анемии и выраженном циркуляторно-гипоксическом синдроме возникают показания к проведению гемотрансфузии.
Возникающие на фоне железодефицитной анемии циркуляторно-гипоксические нарушения ухудшают течение сопутствующих заболеваний сердечно-сосудистой и дыхательных систем.
При железодефицитных состояниях происходит снижение активности IgA; в результате у пациентов зачастую возникают кишечные и респираторные инфекции.
На фоне длительного течения тяжелой формы железодефицитной анемии у больных может развиться миокардиодистрофия.
Прогноз благоприятный при условии своевременной коррекции дефицита железа и устранения причины развития анемии.
Профилактика железодефицитной анемии включает:
- полноценное рациональное питание;
- ежегодный контроль содержания гемоглобина в крови;
- своевременное устранение источников хронической кровопотери;
- профилактический прием препаратов железа лицами из группы риска.
Видео с YouTube по теме статьи:
Образование: окончила Ташкентский государственный медицинский институт по специальности лечебное дело в 1991 году. Неоднократно проходила курсы повышения квалификации.
Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
источник
Железодефицитная анемия – это патологическое состояние, характеризующееся снижением количества гемоглобина и эритроцитов из-за недостатка железа в организме, а также трофическими расстройствами (нарушениями структуры тканей). Гемоглобин — это железосодержащий белок крови, основной функцией которого является перенос кислорода от легких к тканям, а от тканей к легким он переносит углекислый газ.
Все симптомы железодефицитной анемии объединены в два синдрома (устойчивая совокупность симптомов, возникающих по единой причине).
Анемический синдром:
- общая слабость;
- снижение работоспособности;
- головокружение;
- обморочные состояния (помрачение сознания);
- шум в ушах;
- мелькание « мушек» перед глазами;
- одышка (учащенное дыхание) и ускоренное сердцебиение при незначительной физической нагрузке.
Сидеропенический синдром.
- Поражение эпителия (тканей, покрывающих все тело и выстилающих полые органы) любой локализации.
- Поражение эпителия желудочно-кишечного тракта:
- трещины в углах рта;
- затруднения при глотании сухой и твердой пищи;
- жжение и боли в языке, возникающие спонтанно или после еды, сглаженность сосочков языка (сидеропенический глоссит);
- зубы теряют блеск, быстро разрушаются, несмотря на самый тщательный уход за ними;
- непостоянные тупые ноющие боли в эпигастральной области (в середине верхней части живота).
- Поражение кожи и ее придатков (волосы, ногти):
- сухая кожа с множественными микротрещинами (особенно кисти рук, передняя поверхность голеней);
- ногти — повышается ломкость ногтей, поперечная исчерченность, ложкообразные вдавления (койлонихии – « корявые ногти»);
- волосы — выпадение волос, сухость и ломкость волос, преждевременная седина.
- Извращение вкуса (в виде желания есть мел, известь, уголь, глину, сырую крупу) и извращение обоняния (пристрастие к необычным запахам – ацетона, керосина, красок, фекалий).
- Нарушение деятельности сфинктеров (круговых мышц, замыкающих какое-либо отверствие: заброс пищи из желудка в пищевод, беталепсия (недержание мочи и кала при кашле, смехе, натуживании, поднимании ноги на ступеньку)).
- Поражение эпителия желудочно-кишечного тракта:
С учетом уровня гемоглобина (особого вещества эритроцитов (красных клеток крови), переносящего кислород) железодефицитная анемия, как и другие формы анемий, может быть тяжелой, средней и легкой степени.
- Легкая степень: концентрация гемоглобина 90-110 г/л (то есть граммов гемоглобина на 1 литр крови).
- Средняя степень: содержание гемоглобина 70-90 г/л.
- Тяжелая степень: уровень гемоглобина менее 70 г/л.
В норме уровень гемоглобина в крови:
- у женщин – 120-140 г/л;
- у мужчин – 130-160 г/л;
- у новорожденных – 145-225 г/л;
- у детей 1 мес. – 100-180 г/л;
- у детей 2 мес. – 2 лет. – 90-140 г/л;
- у детей 2-12 лет – 110-150 г/л;
- у детей 13-16 лет – 115-155 г/л.
Вместе с тем клинические признаки тяжести анемии (симптомы гипоксического характера (недостатка кислорода)) не всегда соответствуют степени тяжести анемии по лабораторным критериям. Поэтому предложена классификация анемий по степени выраженности клинических симптомов.
По клиническим проявлениям выделяют пять степеней тяжести анемий.
- Легкая степень анемии — без клинических проявлений.
- Умеренная степень анемии:
- быстрая утомляемость;
- слабость;
- недомогание;
- пониженная концентрация внимания;
- бледность видимых слизистых и ногтевых лож.
- Тяжелая степень анемии:
- одышка при умеренной или незначительной нагрузке;
- головная боль, головокружение;
- учащенное сердцебиение (аритмия);
- шум в ушах;
- нарушение сна (например, затрудненное засыпание, частые пробуждения ночью);
- снижение аппетита, изменения пищевых пристрастий в виде отказа от ранее любимой еды;
- извращение аппетита (поедание мела, грязи, красок и др.) и обоняния (нравятся резкие запахи бензина, красок, лаков);
- бледность видимых слизистых и ногтевых лож, кожных покровов;
- повышенная чувствительность к холоду — пациент постоянно мерзнет;
- развиваются воспаления языка (глосситы), губ (хейлит);
- истонченные, исчерченные, ломкие ногти;
- частые простудные заболевания.
- Анемическая прекома:
- одышка в состоянии покоя без каких-либо нагрузок;
- прогрессирующая слабость, сонливость;
- психические расстройства (галлюцинации, депрессивный синдром);
- кожа и слизистые оболочки резко бледные с синюшным оттенком;
- тахикардия (учащенное сердцебиение).
- Анемическая кома:
- низкое артериальное (кровяное) давление;
- рвота;
- тахипноэ (учащенное поверхностное дыхание);
- потеря сознания;
- непроизвольное мочеиспускание;
- отсутствие рефлексов на конечностях (то есть реакции в ответ на раздражение: например, перестает определяться разгибание конечности при ударе молоточком в зонах близкого расположения нервов под кожей или сгибание пальцев ног при проведении пальцем по подошве).
- Низкий запас железа при рождении:
- недоношенные дети;
- дети, рожденные от матерей с железодефицитной анемией;
- дети из многоплодной беременности (одновременное вынашивание двух и более плодов);
- дети от матерей с кровотечением в последние месяцы беременности или во время родов.
- Алиментарные факторы (нарушение поступления железа с пищей и всасывания железа в кишечнике).
- Вегетарианство (употребление только растительной пищи).
- При однообразной диете с повышенным содержанием жиров и углеводов.
- Наследственные нарушения транспорта железа (снижение активности ферментов, переносящих железо из полости кишечника в кровь).
- Нарушения всасывания железа вследствие патологии желудочно-кишечного тракта:
- удаление желудка или его части;
- рак желудка;
- удаление части кишечника;
- хронический панкреатит (воспаление поджелудочной железы);
- муковисцидоз (наследственное заболевание, которое характеризуется поражением всех органов, вырабатывающих слизь (печень, поджелудочная железа, железы слизистой кишечника, дыхательная система, потовые и слюнные железы);
- целиакия (генетическая болезнь, при которой белок глютен вызывает повреждение слизистой тонкого кишечника, и нарушается процесс всасывания);
- энтеропатии (невоспалительные хронические заболевания кишечника, вызванные недостатком ферментов в кишечнике или дефектами строения кишечной стенки) и др.
- Хронические потери крови различного генеза (происхождения):
- во внешнюю среду, наиболее часто – кровотечения из желудочно-кишечного тракта (из дивертикула Меккеля (врожденная патология тонкой кишки в виде слепого выпячивания стенки кишечника), при язве и эрозии (дефект слизистой оболочки) желудка и 12-перстной кишки, варикозном расширении вен слизистой желудка и кишечника). Повторные, даже необильные, кровопотери постепенно приводят к анемии вследствие истощения в организме запасов железа, необходимого для образования гемоглобина (особого вещества эритроцитов (красных клеток крови), переносящего кислород). Суточное поступление в организм железа с пищей невелико, примерно 11-28 мг, причем всасывается из него около 1-3 мг, то есть приблизительно столько же, сколько содержится в 15 мл крови. Поэтому ежедневная потеря этого и даже меньшего количества крови неминуемо приводит к сокращению запасов железа в организме и возникновению железодефицитной анемии;
- во внутреннюю среду без реутилизации (повторного использования) железа — изолированный гемосидероз легких (хроническое заболевание легких, проявляющееся повторными кровоизлияниями в альвеолы – пузырьки с воздухом).
- Повышенное потребление железа — при опухолевом росте любой локализации.
Врач гематолог поможет при лечении заболевания
- Анализ анамнеза заболевания и жалоб (когда (как давно) появились общая слабость, одышка, головокружение, колющие боли в грудной клетке и др.; с чем пациент связывает возникновение этих симптомов).
- Анализ анамнеза жизни (есть ли у пациента какие-либо хронические заболевания, отмечаются ли наследственные (передаются от родителей к детям) заболевания, имеет ли пациент вредные привычки, принимал ли длительно какие-нибудь препараты, выявлялись ли у него опухоли, контактировал ли он с токсическими (отравляющими) веществами).
- Общий осмотр (определяется цвет кожных покровов (возможна бледность); пульс может быть учащенным, артериальное (кровяное) давление — сниженным).
- Анализ крови. Может определяться снижение количества эритроцитов (красных клеток крови, норма 4,0-5,5х10 9 /литр), уменьшение уровня гемоглобина (особого соединения внутри эритроцитов, переносящего кислород, норма 130-160 г/л). Цветной показатель (отношение уровня гемоглобина, умноженного на 3, к первым трем цифрам количества эритроцитов) снижается (в норме этот показатель 0,86-1,05).
- Биохимический анализ крови:
- снижение уровня сывороточного железа (сыворотка – это жидкая часть крови);
- повышение уровня ОЖСС (общая железосвязывающая способность сыворотки);
- снижение уровня насыщения трансферрина (белка крови, основного переносчика железа) железом;
- снижение уровня ферритина (сложный белок, в котором запасается железо).
- Исследование костного мозга, полученного при помощи пункции (прокалывания с извлечением внутреннего содержимого) кости, чаще всего грудины (центральной кости передней поверхности грудной клетки, к которой крепятся ребра), выполняется в некоторых случаях для оценки кроветворения и выявления характера анемии.
- Трепанобиопсия (исследование костного мозга в его соотношении с окружающими тканями) выполняется при взятии на исследование столбика костного мозга с костью и надкостницей, обычно из крыла подвздошной кости (область таза человека, расположенная наиболее близко к коже), с помощью специального приборы – трепана. Наиболее точно характеризует состояние костного мозга.
- Электрокардиография (ЭКГ). Определяется увеличение частоты сердечных сокращений, нарушение питания мышцы сердца, реже – нарушения ритма сердца.
- Возможна также консультация терапевта.
- Устранение причин, вызывающих развитие анемии, является очень важным фактором при лечении.
- Режим дня: активный образ жизни, ежедневные прогулки на свежем воздухе.
- Диетотерапия:
- употреблять больше пищи с высоким содержанием белка (например: творог, мясо, рыба, яичный белок, печень, почки и др.);
- ограничить употребление жиров (жирных сортов мяса, птицы, рыбы, сала, жирных колбас), отдавать предпочтение легкоусвояемым жирам (сливочное, подсолнечное, соевое, оливковое масло);
- ограничить употребление молока (не более 0,5 л в сутки) и крепкого чая, так как они препятствуют всасыванию железа в кишечнике;
- количество углеводов не ограничивается, рекомендуются блюда из различных круп (например: каши, пудинги), сахара, меда, варенья, бобовых, изделий из муки, овощей, фруктов, ягод;
- употребление повышенного количества витаминов группы В и С: витаминами группы В богаты дрожжи, печень, почки, бобовые, яичные желтки, мясо, рыба, молоко, творог, отруби (рисовые, пшеничные); витамина С (аскорбиновой кислоты) много в салате, зеленом луке, капусте, зернах сои;
- употреблять достаточное количество железосодержащих продуктов (например: свиная и говяжья печень, говяжий язык, мясо кролика и индейки, крупы – гречневая, овсяная, ячневая, пшено, черника, персики; икра рыб, особенно осетровых).
- Обязательное назначение препаратов железа: в первые три месяца лечения анемии — в лечебных дозах, в последующем – в профилактических. Препараты железа назначают внутрь между приемами пищи, запивая свежими фруктовыми соками или водой, нельзя запивать молоком.
- В тяжелых случаях анемии назначают препараты железа в инъекциях внутримышечных или внутривенных, переливание эритроцитарной массы (эритроцитов донора).
Прогноз при своевременной диагностике и адекватном лечении благоприятный.
Осложнения.
- Нарушение психоэмоционального состояния:
- снижается память;
- нарушается концентрация внимания;
- появляется раздражительность.
- Анемическая кома (утрата сознания с отсутствием реакции на внешние раздражители вследствие недостаточного поступления кислорода к головному мозгу в результате значительного или быстро развившегося снижения количества эритроцитов (красных клеток крови)).
- Ухудшение состояния внутренних органов, особенно при наличии хронических заболеваний (например, сердца, почек и др.).
- Гемоглобин содержится в эритроцитах – это красные клетки крови.
- В норме в организме здорового взрослого человека содержится 4-5 г железа.
- Железодефицитная анемия встречается очень часто и составляет 4/5 всех анемий (снижение в крови уровня гемоглобина).
ИНФОРМАЦИЯ ДЛЯ ОЗНАКОМЛЕНИЯ
Необходима консультация с врачом
Педиатрия — учебник для медицинских вузов,. П. Шабалов, 2003г.
- Низкий запас железа при рождении:
- недоношенные дети;
- дети, рожденные от матерей с железодефицитной анемией;
- дети из многоплодной беременности (одновременное вынашивание двух и более плодов);
- дети от матерей с кровотечением в последние месяцы беременности или во время родов.
- Алиментарные факторы (нарушение поступления железа с пищей и всасывания железа в кишечнике):
- дети на искусственном вскармливании;
- позднее введение прикорма (позже 5-6 месяцев);
- вегетарианство (употребление только растительной пищи);
- избыток цельного молока в рационе ребенка (более 0,5 л. в сутки);
- при однообразной диете с повышенным содержанием жиров и углеводов.
- Наследственные нарушения транспорта железа (снижение активности ферментов, переносящих железо из полости кишечника в кровь).
- Нарушения всасывания железа вследствие патологии желудочно-кишечного тракта:
- удаление желудка или его части;
- рак желудка;
- удаление части кишечника;
- хронический панкреатит (воспаление поджелудочной железы);
- муковисцидоз (наследственное заболевание, характеризуется поражением всех органов, вырабатывающих слизь (печень, поджелудочная железа, железы слизистой кишечника, дыхательная система, потовые и слюнные железы);
- целиакия (генетическая болезнь, при которой белок глютен вызывает повреждение слизистой тонкого кишечника и нарушается процесс всасывания);
- энтеропатии (невоспалительные хронические заболевания кишечника, вызванные недостатком ферментов в кишечнике или дефектами строения кишечной стенки) и др.
- Хронические потери крови различного генеза (происхождения):
- во внешнюю среду, наиболее часто – кровотечения менструальные и из желудочно-кишечного тракта (из дивертикула Меккеля (врожденная патология тонкой кишки в виде слепого выпячивания стенки кишечника), при язве и эрозии (дефект слизистой оболочки) желудка и 12-перстной кишки, варикозном расширении вен слизистой желудка и кишечника). Повторные, даже необильные, кровопотери постепенно приводят к анемии вследствие истощения в организме запасов железа, необходимого для образования гемоглобина (особого вещества эритроцитов – красных клеток крови – переносящего кислород). Суточное поступление в организм железа с пищей невелико, примерно 11-28 мг, причем всасывается из него около 1-3 мг, т.е. приблизительно столько же, сколько содержится в 15 мл крови. Поэтому ежедневная потеря этого и даже меньшего количества крови неминуемо приводит к сокращению запасов железа в организме и возникновению железодефицитной анемии;
- во внутреннюю среду без реутилизации (повторного использования) железа: изолированный гемосидероз легких (хроническое заболевание легких, проявляющееся повторными кровоизлияниями в альвеолы – пузырьки с воздухом), эндометриоз (разрастание внутренней оболочки матки внутри других органов).
- Повышенное потребление железа:
- при беременности (300 мг железа уходит на потребности плода, 150 мг содержится в плаценте, от 100 до 250 мг теряется в родах из-за кровопотери);
- при лактации (100-200 мг железа выходит с молоком за период кормления);
при интенсивном росте организма (преимущественно в подростковом периоде, особенно в сочетании с интенсивными физическими нагрузками – юные спортсмены), при опухолевом росте любой локализации.
- Выбрать подходящего врача гематолог
- Сдать анализы
- Получить от врача схему лечения
- Выполнить все рекомендации
источник
Железодефицитная анемия – синдром, обусловленный недостаточностью железа и приводящий к нарушению гемоглобинопоэза и тканевой гипоксии. Клинические проявления представлены общей слабостью, сонливостью, пониженной умственной работоспособностью и физической выносливостью, шумом в ушах, головокружениями, обморочными состояниями, одышкой при нагрузке, сердцебиением, бледностью. Гипохромная анемия подтверждается лабораторными данными: исследованием клинического анализа крови, показателей сывороточного железа, ОЖСС и ферритина. Терапия включает лечебную диету, прием препаратов железа, в некоторых случаях – трансфузию эритроцитарной массы.
Железодефицитная (микроцитарная, гипохромная) анемия – анемия, обусловленная нехваткой железа, необходимого для нормального синтеза гемоглобина. Её распространенность в популяции зависит от половозрастных и климатогеографических факторов. По обобщенным сведениям, гипохромной анемией страдает около 50% детей раннего возраста, 15% женщин репродуктивного возраста и около 2% мужчин. Скрытый тканевой железодефицит выявляется практически у каждого третьего жителя планеты. На долю микроцитарной анемии в гематологии приходится 80–90% всех анемий. Поскольку железодефицит может развиваться при самых различных патологических состояниях, данная проблема актуальна для многих клинических дисциплин: педиатрии, гинекологии, гастроэнтерологии и др.
Ежесуточно с потом, калом, мочой, слущенными клетками кожи теряется около 1 мг железа и примерно столько же (2-2,5 мг) поступает в организм с пищей. Дисбаланс между потребностями организма в железе и его поступлением извне или потерями способствует развитию железодефицитной анемии. Железодефицит может возникать как при физиологических условиях, так и в результате ряда патологических состояний и быть обусловлен как эндогенными механизмами, так и внешними воздействиями:
Чаще всего анемия вызывается хронической потерей крови: обильными менструациями, дисфункциональными маточными кровотечениями; желудочно-кишечными кровотечениями из эрозий слизистой желудка и кишечника, гастродуоденальных язв, геморроидальных узлов, анальных трещин и др. Скрытая, но регулярная кровопотеря отмечается при гельминтозах, гемосидерозе легких, экссудативном диатезе у детей и др.
Особую группу составляют лица с болезнями крови — геморрагическими диатезами (гемофилией, болезнью Виллебранда), гемоглобинурией. Возможно развитие постгеморрагической анемии, вызванной одномоментным, но массивным кровотечением при травмах и операциях. Гипохромная анемия может возникать вследствие ятрогенных причин — у доноров, часто сдающих кровь; пациентов с ХПН, находящихся на гемодиализе.
К факторам алиментарного порядка относятся анорексия, вегетарианство и следование диетам с ограничением мясных продуктов, плохое питание; у детей — искусственное вскармливание, позднее введение прикорма. Снижение абсорбции железа характерно для кишечных инфекций, гипоацидного гастрита, хронического энтерита, синдрома мальабсорбции, состояния после резекции желудка или тонкой кишки, гастрэктомии. Значительно реже железодефицитная анемия развивается вследствие нарушения транспортировки железа из депо при недостаточной белково-синтетической функции печени – гипотрансферринемиях и гипопротеинемиях (гепатитах, циррозе печени).
Ежедневная потребность в микроэлементе зависит от пола и возраста. Наиболее высока необходимость в железе у недоношенных, детей раннего возраста и подростков (в связи с высокими темпами развития и роста), женщин репродуктивного периода (в связи с ежемесячными менструальными потерями), беременных (в связи с формированием и ростом плода), кормящих мам (в связи с расходом в составе молока). Именно эти категории являются наиболее уязвимыми в отношении развития железодефицитной анемии. Кроме того, повышение потребности и расхода железа в организме наблюдается при инфекционных и опухолевых заболеваниях.
По своей роли в обеспечении нормального функционирования всех биологических систем железо является важнейшим элементом. От уровня железа зависит поступление кислорода к клеткам, протекание окислительно-восстановительных процессов, антиоксидантная защита, функционирование иммунной и нервной систем и пр. В среднем содержание железа в организме находится на уровне 3-4 г. Более 60% железа (>2 г) входит в состав гемоглобина, 9% — в состав миоглобина, 1% — в состав ферментов (гемовых и негемовых). Остальное железо в виде ферритина и гемосидерина находится в тканевом депо – главным образом, в печени, мышцах, костном мозге, селезенке, почках, легких, сердце. Примерно 30 мг железа непрерывно циркулирует в плазме, будучи частично связанным основным железосвязывающим белком плазмы – трансферрином.
При развитии отрицательного баланса железа мобилизуются и расходуются запасы микроэлемента, содержащиеся в тканевых депо. На первых порах этого бывает достаточно для поддержания адекватного уровня Hb, Ht, сывороточного железа. По мере истощения тканевых резервов компенсаторно увеличивается эритроидная активность костного мозга. При полном истощении эндогенного тканевого железа его концентрация начинает снижаться в крови, нарушается морфология эритроцитов, уменьшается синтез гема в гемоглобине и железосодержащих ферментов. Страдает кислородтранспортная функция крови, что сопровождается тканевой гипоксией и дистрофическими процессами во внутренних органах (атрофический гастрит, миокардиодистрофия и др.).
Железодефицитная анемия возникает не сразу. Вначале развивается предлатентный железодефицит, характеризующийся истощением только запасов депонированного железа при сохранности транспортного и гемоглобинового пула. На этапе латентного дефицита отмечается уменьшение транспортного железа, содержащегося в плазме крови. Собственно гипохромная анемия развивается при уменьшении всех уровней метаболических запасов железа – депонированного, транспортного и эритроцитарного. В соответствии с этиологией различают анемии: постгеморрагические, алиментарные, связанные с повышенным расходом, исходным дефицитом, недостаточностью резорбции и нарушением транспорта железа. По степени выраженности железодефицитные анемии подразделяются на:
- Легкие (Нb 120-90 г/л). Протекают без клинических проявлений или с их минимальной выраженностью.
- Среднетяжелые (Нb 90-70 г/л). Сопровождаются циркуляторно-гипоксическим, сидеропеническим, гематологическим синдромами умеренной степени выраженности.
- Тяжелые (Нb
Циркуляторно-гипоксический синдром обусловлен нарушением синтеза гемоглобина, транспорта кислорода и развитием гипоксии в тканях. Это находит свое выражение в ощущении постоянной слабости, повышенной утомляемости, сонливости. Пациентов преследует шум в ушах, мелькание «мушек» перед глазами, головокружения, переходящие в обмороки. Характерны жалобы на сердцебиение, одышку, возникающую при физической нагрузке, повышенную чувствительность к низким температурам. Циркуляторно-гипоксические нарушения могут усугублять течение сопутствующей ИБС, хронической сердечной недостаточности.
Развитие сидеропенического синдрома связано с недостаточностью тканевых железосодержащих ферментов (каталазы, пероксидазы, цитохромов и др.). Этим объясняется возникновение трофических изменений кожных покровов и слизистых оболочек. Чаще всего они проявляются сухостью кожи; исчерченностью, ломкостью и деформацией ногтей; повышенным выпадением волос. Со стороны слизистых оболочек типичны атрофические изменения, что сопровождается явлениями глоссита, ангулярного стоматита, дисфагии, атрофического гастрита. Может возникать пристрастие к резким запахам (бензина, ацетона), искажение вкуса (желание есть глину, мел, зубной порошок и пр.). Признаками сидеропении также служат парестезии, мышечная слабость, диспепсические и дизурические расстройства. Астеновегетативные нарушения проявляются раздражительностью, эмоциональной неустойчивостью, снижением умственной работоспособности и памяти.
Поскольку в условиях железодефицита IgA теряет свою активность, больные становятся подвержены частой заболеваемости ОРВИ, кишечными инфекциями. Пациентов преследует хроническая усталость, упадок сил, снижение памяти и концентрации внимания. Длительное течение железодефицитной анемии может привести к развитию миокардиодистрофии, распознаваемой по инверсии зубцов Т на ЭКГ. При крайне тяжелом железодефиците развивается анемическая прекома (сонливость, одышка, резкая бледность кожи с цианотичным оттенком, тахикардия, галлюцинации), а затем – кома с потерей сознания и отсутствием рефлексов. При массивной стремительной кровопотере возникает гиповолемический шок.
На наличие железодефицитной анемии может указывать внешний вид больного: бледная, с алебастровым оттенком кожа, пастозность лица, голеней и стоп, отечные «мешки» под глазами. При аускультации сердца обнаруживается тахикардия, глухость тонов, негромкий систолический шум, иногда – аритмия. С целью подтверждения анемии и определения ее причин проводится лабораторное обследование.
- Лабораторные тесты. В пользу железодефицитного характера анемии свидетельствует снижение гемоглобина, гипохромия, микро- и пойкилоцитоз в общем анализе крови. При оценке биохимических показателей отмечается снижение уровня сывороточного железа и концентрации ферритина (60 мкмоль/л), уменьшение насыщения трансферрина железом (
- Инструментальные методики. Для установления причины хронической кровопотери должно быть проведено эндоскопическое обследование ЖКТ (ЭГДС, колоноскопия,), рентгенодиагностика (ирригоскопия, рентгенография желудка). Обследование органов репродуктивной системы у женщин включает УЗИ малого таза, осмотр на кресле, по показаниям — гистероскопию с РДВ.
- Исследование пунктата костного мозга. Микроскопия мазка (миелограмма) показывает значительное снижение количества сидеробластов, характерное для гипохромной анемии. Дифференциальная диагностика направлена на исключение других видов железодефицитных состояний — сидеробластной анемии, талассемии.
К основным принципам терапии железодефицитной анемии относятся устранение этиологических факторов, коррекция рациона питания, восполнение железодефицита в организме. Этиотропное лечение назначается и проводится специалистами гастроэнтерологами, гинекологами, проктологами и др.; патогенетическое – гематологами. При железодефицитных состояниях показано полноценное питание с обязательным включением в рацион продуктов, содержащих гемовое железо (телятины, говядины, баранины, мяса кролика, печени, языка). Следует помнить, что усилению ферросорбции в ЖКТ способствуют аскорбиновая, лимонная, янтарная кислота. Ингибируют всасывание железа оксалаты и полифенолы (кофе, чай, соевый протеин, молоко, шоколад), кальций, пищевые волокна и др. вещества.
Вместе с тем, даже сбалансированная диета не в состоянии устранить уже развившийся недостаток железа, поэтому больным с гипохромной анемией показана заместительная терапия ферропрепаратами. Препараты железа назначаются курсом не менее 1,5-2-х месяцев, а после нормализации уровня Hb проводится поддерживающая терапия в течение 4-6 недель половинной дозой препарата. Для фармакологической коррекции анемии используются препараты двухвалентного и трехвалентного железа. При наличии витальных показаний прибегают к гемотрансфузионной терапии.
В большинстве случаев гипохромная анемия подается успешной коррекции. Однако при неустраненной причине железодефицит может рецидивировать и прогрессировать. Железодефицитная анемия у детей раннего и младшего возраста может вызывать задержку психомоторного и интеллектуального развития (ЗПР). В целях профилактики железодефицита необходим ежегодный контроль параметров клинического анализа крови, полноценное питание с достаточным содержанием железа, своевременная ликвидация источников кровопотери в организме. Следует учитывать, что лучше всего усваивается железо, содержащееся в мясе и печени в форме гема; негемовое железо из растительной пищи практически не усваивается – в этом случае оно сначала должно восстановиться до гемового при участии аскорбиновой кислоты. Лицам групп риска может быть показан профилактический прием железосодержащих препаратов по назначению специалиста.
источник
Анемия. Виды анемий: железодефицитная, гемолитическая, В12 дефицитная, апластическая. Причины, диагностика, степени анемии.
Анемия или пониженное количество гемоглобина в крови, а в просторечии – «малокровие». Практически каждый человек хотя бы один раз сталкивался с такой формулировкой, особенно женщины. Что же означает этот пугающий термин? Почему возникает данное состояние организма? Чем опасна анемия? Как вовремя распознать её на начальных этапах?
Анемия – это патологическое состояние организма, при котором наблюдается снижение количества гемоглобина и эритроцитов ниже нижних границ нормы. Причем уменьшение содержания гемоглобина является обязательным признаком анемии, в отличие от снижения количества эритроцитов. То есть снижение концентрации гемоглобина при анемии есть всегда, а снижение количества эритроцитов может и не быть. Однако в некоторых случаях при анемии выявляются патологические формы эритроцитов (не двояко – вогнутые).
Анемия – это не самостоятельное заболевание, а следствие основной патологии, потому, выявление сниженного уровня эритроцитов и гемоглобина, требует проведения тщательной диагностики для выявления причины!
Гидремия – разжижение крови.
Такое состояние возможно при поступлении в кровоток тканевой жидкости при схождении отека, обильном питье. Гидремия – это псевдоанемия.
Сгущение крови
Сгущение крови может происходить вследствие потери жидкой части крови, что происходит при сильном обезвоживании. Обезвоживание наблюдается в результате сильной рвоты, поноса, обильного потения. Однако в этом случае за счет сгущения крови количество гемоглобина и эритроцитов может быть в пределах нормальных значений. В таких ситуациях говорят о наличии скрытой анемии.
Специфические и неспецифические признаки анемии – что относится к ним?
В первую очередь рассмотрим, как же проявляется анемия. Существуют неспецифические проявления и специфические. Неспецифические проявления называются так, потому что эти признаки общие для всех видов анемий. Специфические же проявления строго индивидуальны и характерны только для каждого конкретного вида анемии.Сейчас мы рассмотрим только неспецифические проявления, а специфические укажем при рассмотрении видов анемий.
Итак, к неспецифическим признакам анемий, относят следующие симптомы:
- бледность кожи и слизистых оболочек
- слабость
- головокружение
- шум в ушах
- головные боли
- быстрая утомляемость
- сонливость
- одышка
- анорексия (патологическая потеря аппетита или отвращение к пище)
- нарушение сна
- нарушения менструального цикла вплоть до полного прекращения менструаций (аменореи)
- импотенция
- тахикардия (увеличение частоты сердечных сокращений)
- шумы в сердце (усиление сердечного толчка, систолический шум на верхушке сердца)
- сердечная недостаточность
- при снижении количества гемоглобина менее 50 г/л возможно развитие ацидоза (закисление крови)
- снижение содержания гемоглобина ниже нормальных показателей
- снижение содержания эритроцитов ниже нормы
- изменение цветного показателя
- изменение содержания лейкоцитов и тромбоцитов
Виды анемий – постгеморрагическая, гемолитическая, дефицитная и гипопластическая
Анемии могут вызываться совершенно разными причинами, поэтому принято все анемии делить по различным признакам, в том числе по причинам, их вызывающим. Согласно причинам (патогенезу) выделяют три вида анемии: постгеморрагические, гемолитические и связанные с нарушением кровообразования (дефицитные и гипопластические). Что это значит? Разберем подробнее.
Постгеморрагические анемии связаны с острой или хронической кровопотерей (кровотечение, ранение).
Гемолитические – развиваются в связи с усиленным разрушением эритроцитов.
Дефицитные анемии вызваны недостатком витаминов, железа или других микроэлементов, которые необходимы для кроветворения.
Гипопластические анемии – это самый тяжелый вид анемий и связан он с нарушением кроветворения в костном мозгу.
- По степени тяжести. Существует три степени тяжести анемии – легкая, средняя и тяжелая в зависимости от содержания гемоглобина и эритроцитов в крови:
| Степень тяжести | Гемоглобин, г/л | Эритроциты, Т/л | ||||||||||||||||||||||
| Легкая | > 100 г/л | > 3 Т/л | ||||||||||||||||||||||
| Средняя | 100 – 66 г/л | 3 – 2 Т/л | ||||||||||||||||||||||
| Тяжелая | 1,05) и гипохромные (ЦП 8,0 микрон) и мегалобластные (СДЭ > 9,5 микрон). Нормоцитарные анемии характеризуются нормальным диаметром эритроцитов, микроцитарные – уменьшенным диаметром эритроцитов, а макроцитарные и мегалобластные связаны с увеличением диаметра эритроцитов. К нормоцитарным анемиям относят – острую постгеморрагическую и большинство гемолитических анемий; к микроцитарным – железодефицитную анемию, микросфероцитоз и хроническую постгеморрагическую анемию. Макроцитарные анемии – это гемолитическая болезнь новорожденных, фолиево дефицитная анемии. Мегалоцитарная – В12 дефицитнаяанемия.
Мы рассмотрели, на какие типы, и по каким признакам классифицируют анемии. Перейдем к рассмотрению, как проявляются отдельные виды анемий, какие изменения при этом наблюдаются в крови и в организме человека в целом.
Симптомы острой постгеморрагической анемии, картина крови Симптомами острой постгеморрагической анемии являются такие признаки: бледность, резкое головокружение, обмороки, частый пульс, холодный пот, снижение температуры тела, иногда рвота. Потеря крови более 30% от исходного уровня является критической и опасна для жизни. Диагностика постгеморрагической острой анемии В крови увеличивается количество ретикулоцитов более 11%, также появляются «незрелые» эритроциты и эритроциты с измененной формой клетки. Со стороны лейкоцитов наблюдается увеличение их общего количества выше 12 Г/л, а в лейкоцитарной формуле идет сдвиг влево. В последующие два месяца после острой кровопотери происходит восстановление показателей эритроцитов и гемоглобина. Однако восстановление количества эритроцитов и содержания гемоглобина связано с расходованием фонда железа в организме и может повлечь за собой развитие железодефицита. Поэтому в период восстановления после кровопотери необходимо соответствующее питание, то есть в рационе должны быть продукты с высоким содержанием железа (например, гранаты, гречка, печень и т.д.). Принципы лечения острой постгеморрагической анемии Лечение острой постгеморрагической анемии должно проводиться в условиях стационара и быть направлено на восстановление количества циркулирующей крови, количества форменных элементов крови и поддержание этих показателей. В первую очередь необходимо остановить кровотечение. Затем в зависимости от количества кровопотери применяют переливание крови, эритроцитарной массы и кровезаменителей. Симптомы хронической постгеморрагической анемии Симптомы хронической постгеморрагической анемии такие же, как при железодефицитной анемии. Какие же это симптомы? Итак, признаками хронической постгеморрагической анемии являются: кожа «алебастрового» оттенка (очень белая, бледная), извращение обоняния (непереносимость запахов или, наоборот, тяга к каким-либо запахам), изменение вкуса, одутловатость лица, пастозность голеней, ломкость волос и ногтей, сухость, шершавость кожи. Также возможно образование койлонехий – истонченных и уплощенных ногтей. Помимо этих внешних признаков возможно появление одышки, тошноты, головокружения, учащения пульса, слабости, утомляемости, субфебрильной температуры (до 37° С) и прочее. Из-за дефицита железа могут проявляться нарушения со стороны желудочно-кишечного тракта – кариес, глоссит, сниженная кислотность желудочного сока, а также непроизвольное мочеиспускание при смехе, потливость. Диагностика хронической постгеморрагической анемии В крови при хронической постгеморрагической анемии появляются слабо окрашенные эритроциты маленького размера, овальные эритроциты, снижено общее количество лейкоцитов, а в лейкоцитарной формуле наблюдается незначительный лимфоцитоз. В сыворотке крови концентрация железа ниже нормы – 9,0 мкмоль/л, также ниже нормального содержание меди, кальция, витаминов А, В, С, но, однако, повышена концентрация цинка, марганца и никеля в крови. Причины хронической постгеморрагической анемии Почему же возникает такое состояние – хроническая постгеморрагическая анемия? Причины этого явления следующие:
Лечение хронической постгеморрагической анемии Именно в силу причин, приводящих к развитию хронической постгеморрагической анемии, при лечении этого состояния, прежде всего, необходимо устранить причину хронической кровопотери.Затем необходимо сбалансированное питание, содержащее продукты с высоким содержанием железа, фолиевой кислоты и витаминов. В случае тяжелой анемии необходимо принимать препараты железа (сорбифер, феррум-лек) в виде таблеток или инъекций, препараты фолиевой кислоты, витамин В12 в виде таблеток или в виде инъекций. Наиболее эффективными препаратами для восстановления уровня железа в организме являются таблетированные препараты, которые выпускаются различными фирмами. В силу этого в аптеках представлен широкий выбор препаратов железа. При выборе препарата необходимо обращать внимание на содержание железа в одной таблетке и биологическую доступность данного препарата. Препараты железа необходимо принимать совместно с аскорбиновой кислотой и фолиевой кислотой, поскольку в такой комбинации происходит наилучшее усвоение железа. Однако при выборе препарата и дозы необходимо обязательно проконсультироваться с врачом. Гемолитические анемии – это группа анемий, при которых процессы разрушения эритроцитов преобладают над процессами их производства. Иными словами разрушение эритроцитов происходит быстрее, чем образуются новые клетки, взамен разрушенных. Гемолитические анемии могут быть наследственными и приобретенными. Наследственные гемолитические анемии это:
Симптомы гемолитических анемий Общим признаком всех гемолитических анемий является желтуха. Желтуха появляется вследствие того, что при разрушении эритроцитов выделяется в кровь большое количество билирубина, который и приводит к данному симптому. Помимо желтухи имеются следующие признаки, общие для всех гемолитических анемий – увеличение печени и селезенки, увеличение концентрации билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев». В связи с тем, что наиболее широкое распространение среди наследственных гемолитических анемий имеют серповидно – клеточная анемия и талассемия, более подробно рассмотрим именно их.
Серповидно – клеточная анемия вызвана тем, что синтезируется молекула гемоглобина с дефектом. Такие дефектные молекулы гемоглобина собираются в веретенообразные кристаллы (тактоиды), которые растягивают эритроцит, придавая ему серповидную форму. Такие серповидные эритроциты мало пластичны, повышают вязкость крови и закупоривают мелкие кровеносные сосуды. Кроме этого своими острыми концами такие эритроциты протыкают друг друга и разрушаются. Симптомы серповидно–клеточной анемии Серповидно – клеточная анемия внешне проявляется следующими признаками:
Диагностика серповидно–клеточной анемии В анализе крови сниженное количество гемоглобина (50 – 80 г/л) и эритроцитов (1 – 2 Т/л), увеличение ретикулоцитов до 30% и более. В мазке крови видны серповидные эритроциты и эритроциты с тельцами Жолли и кольцами Кабо. Лечение серповидно-клеточной анемии Основной принцип лечения данного вида анемии –это недопущение гемолитических кризов. Данный эффект достигается тем, что человек избегает гипоксических состояний – присутствия в разреженном воздухе, в местах с низким содержанием кислорода и прочее. Используют переливание эритроцитарной массы или кровезаменителей.
Талассемия возникает вследствие нарушения скорости образования гемоглобина. Такой незрелый гемоглобин не стабилен, в результате чего он выпадает в эритроцитах в виде включений – телец, а весь эритроцит приобретает внешний вид мишеневидной клетки. Талассемия – это тяжелое наследственное заболевание, которое невозможно вылечить, а можно лишь облегчить ее проявления. Симптомы талассемии
Диагностика талассемии В крови обнаруживаются мишеневидные эритроциты, увеличенное количество ретикулоцитов, снижение концентрации гемоглобина до 20 г/л, а эритроцитов до 1 Т/л. Также наблюдаются уменьшение количества лейкоцитов и тромбоцитов. Итак, мы рассмотрели основные виды наследственных гемолитических анемий, которые передаются от родителей к детям. Перейдем к рассмотрению приобретенных гемолитических анемий, которые возникают вследствие наличия провоцирующего фактора. Приобретенные гемолитические анемии, иммунные и не иммунные анемии Прежде всего, необходимо отметить, что приобретенные гемолитические анемии могут развиваться при участии иммунной системы (иммунные) или без ее участия (не иммунные). К анемиям, развивающимся при участии иммунной системы, относятся вирусная, сифилитическая анемия и гемолитическая болезнь новорожденных. Не иммунные гемолитические анемии – это болезнь Маркиафавы – Микелли, а также анемии, возникшие вследствие длительной маршевой ходьбы, отравления алкоголем, кислотами, солями тяжелых металлов, ядами змей, насекомых и грибов. При ожогах, составляющих более 20% поверхности тела, недостатке витамина Е и малярии, также развивается не иммунная гемолитическая анемия.
Лечение этих видов анемии, как правило, не требуется. Гемолитическая болезнь новорожденного, причины развития, симптомы заболевания, степени тяжести.
В настоящее время проводится профилактика гемолитической болезни новорожденных путем отслеживания наличия антител у матери. Если у матери выявляются антитела, то лечение проводят в стационаре. При этом производят вливание антирезусных иммуноглобулинов. Признаки не иммунных гемолитических анемий, лабораторные симптомы Не иммунные гемолитические анемии имеют следующие признаки – желтуха,увеличенные печень и селезенка,повышенная концентрация билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев».В картине крови отмечается наличие эритроцитов различной формы и размеров, ретикулоцитоз до 30% и выше, сниженное количество лейкоцитов и тромбоцитов. Такие анемии сами по себе не требуют отдельного и особенного лечения, так как в первую очередь необходимо убрать фактор, вызывающий эту анемию (яды змей, соли тяжелых металлов и т.д.). Анемии, вызванные нарушением кровообразования, делятся на две большие группы – дефицитные анемии и гипопластические. Дефицитные анемии связаны с дефицитом необходимых для кроветворения элементов. К дефицитным анемиям относят – железодефицитную анемию, железорефрактерную анемию, В12 – дефицитную и фолиево дефицитную. Гипопластические анемии вызваны гибелью клеток – предшественниц в костном мозгу. Гипопластические анемии могут быть наследственными (анемия Фанкони, анемия Эстрена – Дамешика, анемия Блекфэрна — Даймонда) и приобретенными. Приобретенные гипопластические анемии развиваются либо сами по себе вследствие неизвестной причины, либо на фоне имеющегося заболевания — лучевой болезни, инфекций, повреждений иммунитета. Для большинства людей больший интерес представляют дефицитные анемии, которые могут возникнуть практически у каждого человека. Поэтому наиболее подробно остановимся именно на этом виде анемий.
Причины железодефицитной анемии Железодефицитная анемия возникает в следующих случаях:
Симптомы железодефицитной анемии Клинически железодефицитная анемия проявляется тремя основными синдромами – гипоксическим, сидеропеническим и анемическим. Что это за синдромы? Чем характеризуется каждый из них?Синдром – это устойчивая совокупность симптомов. Итак, гипоксический синдром характеризуется одышкой, головными болями, шумом в ушах, быстрой утомляемостью, сонливостью и тахикардией; анемический синдром выражается в уменьшении содержания количества эритроцитов и гемоглобина. Сидеропенический синдром напрямую связан с уменьшением количества железа в организме и проявляется так: нарушение питания кожи, ногтей, волос – кожа «алебастрового» оттенка, сухость и шершавость кожи, ломкие волосы и ногти. Затем присоединяетсяизвращение вкуса и обоняния (желание есть мел, вдыхать запах мытых бетонных полов и т.д.). Возможно появление осложнений со стороны желудочно-кишечного тракта – кариеса, дисфагии, снижения кислотности желудочного сока, непроизвольного мочеиспускания (в тяжелых случаях), потливости. Диагностика железодефицитной анемии В крови наблюдается снижение содержания гемоглобина до 60 – 70 г/л, эритроцитов до 1,5 – 2 Т/л, также снижено количество или вовсе отсутствуют ретикулоциты. Появляются эритроциты различных форм и размеров. Концентрация сывороточного железа ниже нормы. Лечение железодефицитной анемии В основе лечения железодефицитной анемии лежат принципы устранения причины ее возникновения – лечение заболеваний желудочно – кишечного тракта, а также введение сбалансированного пищевого рациона. В диете должны присутствовать продукты с высоким содержанием железа (печень, мясо, молоко, сыр, яйца, злаки и т.д.). Однако главным средством восстановления количества железа в организме на начальном этапе являются лекарственные препараты железа. В большинстве случаев такие лекарства назначают в виде таблеток. В тяжелых случаях прибегают к внутримышечным или внутривенным инъекциям. В лечении данной анемии используют, например, такие препараты: сорбифер, феррум-лек, тардиферон, тотема и другие. Выбор различных лекарственных средств, в том числе комбинированных, очень широк. При выборе необходимо консультироваться с врачом. Обычно, суточная доза для профилактики и лечения анемии легкой степени составляет 50-60 мг железа, для лечения анемии средней тяжести – 100-120 мг железа в сутки. Лечение анемии тяжелой степени проводят в стационаре и применяют препараты железа в виде инъекций. Затем переходят на таблетированные формы. Препараты железа вызывают потемнение стула, однако в данной ситуации это нормально.Если препарат железа вызывает неприятные ощущения в желудке, то его необходимо заменить.
Железорефрактерную анемию также называют сидеробластной или сидероахристической. Железорефрактерная анемия развивается на фоне нормального содержания железа в сыворотке крови и недостатка ферментов, которые участвуют в синтезе гемоглобина. То есть основная причина железорефрактерной анемии – нарушение процессов «усвоения» железа. Симптомы железорефрактерной анемии, что такое гемосидероз? Проявляется железорефрактерная анемия одышкой, головными болями, головокружением, шумом в ушах, быстрой утомляемостью, сонливостью, нарушениями сна и тахикардией. Из-за высокого содержания железа в крови тканях наблюдается гемосидероз.Гемосидероз – это отложение железа в органах и тканях вследствие его избытка. При гемосидерозе развивается недостаточность сердечно – сосудистой системы вследствие отложения железа в сердечной мышце, сахарный диабет, поражение легких и увеличиваются размеры печени и селезенки. Кожа приобретает землянистый оттенок. Диагностика железорефрактерной анемии, что такое сидеробласты? Цветной показатель крови снижен до 0,6 – 0,4, присутствуют эритроциты различных форм и размеров, количество гемоглобина и эритроцитов ниже нормы. Имеются изменения и в костном мозгу – появляются клетки – сидеробласты. Сидеробласты – это клетки, имеющие вокруг ядра венчик из железа. В норме таких клеток в костном мозгу 2,0 – 4,6%, а при железорефрактерной анемии их количество может доходить до 70%. Лечение железорефрактерной анемии Лечения, которое смогло бы устранить ее совсем, на сегодняшний день нет. Возможно применение заместительной терапии – вливание эритроцитарной массы и кровезаменителей.
Во-первых, что такое В12? В12 – это витамин, который имеет также название цианкобаламин. Цианкобаламин содержится в основном в продуктах животного происхождения – мясо, печень, почки, молоко, яйца, сыр. Уровень витамина В12 необходимо постоянно поддерживать употреблением соответствующих продуктов, поскольку происходят его естественные физиологические потери с калом и желчью. Причины В12 дефицитной анемии Итак, В12 – дефицитная анемия – это анемия, возникающая вследствие недостаточности витамина В12. Недостаток витамина В12 может быть вызван недостаточным его поступлением с пищей или нарушением его усвоения в желудочно-кишечном тракте. Недостаточное поступление цианкобаламина с пищей возможно у строгих вегетарианцев. Также недостаток В12 может проявиться при повышении потребности в нем у беременных женщин, кормящих матерей, раковых больных. Неусвоение витамина В12, поступающего с пищей в достаточном количестве, происходит при заболеваниях желудка, тонкого кишечника (дивертикулы, глисты) и лечении противосудорожными средствами или оральными контрацептивами. Симптомы В12 дефицитной анемии Симптомы проявления В12 – дефицитной анемии характеризуются нарушениями в центральной нервной системе и желудочно-кишечном тракте. Итак, рассмотрим эти две большие группы симптомов:
Диагностика В12 дефицитной анемии В системе крови происходит переход на мегалобластический тип кроветворения. Это означает, что в крови появляются гигантские эритроциты с укороченным сроком жизни, ярко окрашенные эритроциты без просветления в центре, грушевидные и овальные эритроциты с тельцами Жолли и кольцами Кабо. Также появляются гигантские нейтрофилы, уменьшается количество эозинофилов (вплоть до полного отсутствия), базофилов и общего количества лейкоцитов. В крови повышена концентрация билирубина, в связи с чем, может наблюдаться легкая желтушность кожи и склер глаз. Лечение В12 дефицитной анемии В первую очередь необходимо вылечить заболевания желудочно-кишечного тракта и наладить сбалансированное питание, с достаточным содержанием витамина В12. Применение курса инъекций витамина В12 быстро нормализует кроветворение в костном мозгу, а далее необходимо постоянное, регулярное поступление с пищей достаточного количества витамина В12.
Симптомы фолиеводефицитной анемии При фолиево дефицитной анемии страдает желудочно-кишечный тракт, поэтому и проявления данной анемии связаны с нарушениями работы желудочно-кишечного тракта. Наблюдается появление повышенной чувствительности к кислой пище, глоссита, трудностей глотания, атрофии слизистой желудка, увеличения размеров печени и селезенки. Лечение фолиеводефицитной анемии Для лечения данного вида анемии применяют таблетки фолиевой кислоты и нормализуют рацион питания, в котором должны быть продукты, содержащие достаточное количество фолиевой кислоты.
Симптомы гипопластических анемий Гипопластические анемии могут быть наследственными или приобретенными, однако все подвиды данного типа анемий характеризуются одинаковыми проявлениями. Рассмотрим эти симптомы:
Причины, вызывающие развитие гипопластической анемии Какие же причины способны вызывать подобное поражение костного мозга? Наследственные анемии, соответственно, передаются по наследству, а вот приобретенные? Все факторы, способные приводить к развитию гипопластической анемии, делятся на экзогенные (внешние) и эндогенные (внутренние). В таблице приведены основные экзогенные и эндогенные причины, способные вызвать развитие гипопластической анемии.
Принципы лечения гипопластических анемий Лечение гипопластических анемий находится строго в компетенции врача – гематолога. Могут применяться различные методы стимулирования кроветворения, или пересадка костного мозга. Итак, мы рассмотрели все основные виды анемий. Конечно, их гораздо больше, однако мы не можем объять необъятное. При появлении каких-либо признаков анемии необходимо своевременно обратиться к врачу. И регулярно сдавать анализ крови на содержание гемоглобина. источник |


 Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.
Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.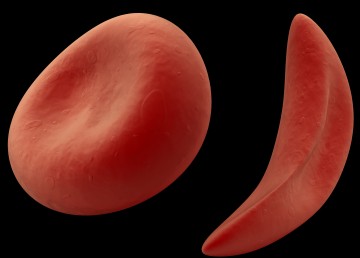 Причины серповидно–клеточной анемии
Причины серповидно–клеточной анемии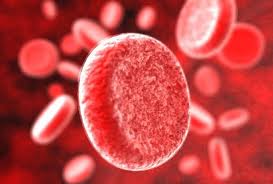 Талассемия – причины заболевания
Талассемия – причины заболевания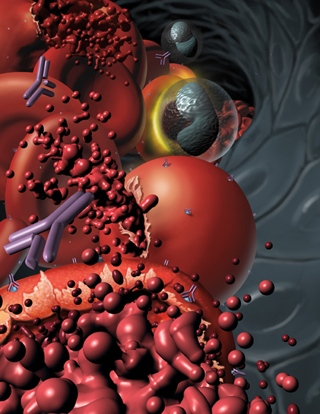 Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы.
Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы.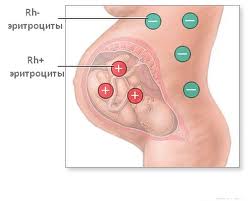 Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.
Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.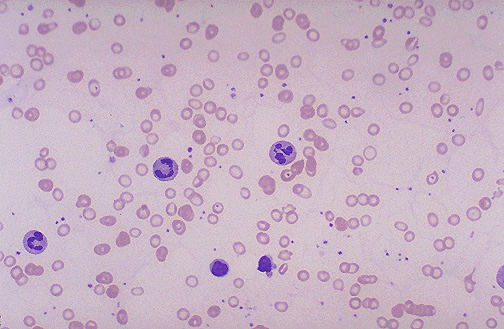 Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты.
Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты. Причина железорефрактерной анемии
Причина железорефрактерной анемии Что такое В12? Где содержится этот витамин?
Что такое В12? Где содержится этот витамин? Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12.
Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12. Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.
Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.