Недоношенные дети зачастую значительно отстают в физическом развитии, а также подвержены дефициту жизненно важных витаминов и микроэлементов. А потому такие дети находятся в группе риска появления анемического расстройства. Анемия у недоношенных новорожденных – это одна из наиболее часто встречающихся патологий. И некоторые формы анемии могут нести непосредственную угрозу для жизни ребенка.
Основным фактором, которые провоцирует возникновение анемии, является недостаток в организме железа, фолатов, витамина Е и витаминов группы В. Данное расстройство было обнаружено и описано еще в 50-х годах прошлого века. Тогда было выделено несколько промежутков, которые характеризируют анемию у недоношенных детей. Состояние при анемии обозначается ранней, промежуточной и поздней фазой.
Ранняя анемия недоношенных имеет достаточно сложный механизм развития. Развитие заболевания происходит на первом месяце жизни практически у половины детей, которые родились раньше срока. Основной причиной появления такого расстройства считается задержка образования красных кровяных телец и недостаточная функциональная зрелость костного мозга, вызванная преждевременным появлением на свет.
С восьмой недели диагностируется промежуточная фаза прогрессирования анемического расстройства у ребенка, на которую указывает появление ретикулоцитов в периферической крови, что не характерно для обычного состояния. При этом уровень гемоглобина не понижается, однако в дефиците находится запас железа. Образование эритроцитов, как правильно, ниже необходимого.
Уже начиная с 16 недели, в организме ребенка фиксируется критическое истощение запасов железа, что в результате приводит к появлению гипохромных эритроцитов. Такое явление указывает на развитие железодефицитной анемии, при которой значительно падает уровень гемоглобина в крови. Такой процесс характеризует позднюю анемию недоношенных младенцев.

- Сниженная продолжительность жизни кровяных телец.
- Особенности в обмене витаминов и микроэлементов.
- Недостаточное содержание железа.
Лечение анемии недоношенных на ранней стадии развития в большинстве случаев не требуется, поскольку она отражает процесс развития. На ранней стадии детям необходимо обеспечить полноценное и сбалансированное питание, в особенности обратить внимание на поступление фолиевой кислоты, витаминов Е и витаминов группы В. Переливание крови проводится только в редких случаях, обычно такая процедура не требуется.
Лечение детей с поздней анемией заключается в правильной тактике выживания. Она заключается в необходимом питании, прогулках на свежем воздухе, гимнастических и массажных процедурах, профилактике других заболеваний. Также назначается прием железосодержащих препаратов. Длительность их приема зависит от тяжести расстройства. При неэффективности препаратов показана госпитализация.
Профилактика анемии заключается в проведении лечебно-профилактических мер различных инфекционных заболеваний, лечении позднего токсикоза беременных и соблюдении сбалансированного рациона питания. Эффективной профилактической мерой выступает естественное вскармливание ребенка. Также детям рекомендуется давать витамин Е, фолиевую кислоту и железосодержащие препараты в первые месяцы жизни.
источник
У недоношенных детей организм еще окончательно не созрел. Поэтому он не приспособлен к самостоятельному существованию. Качественный и количественный состав крови у таких детей будет отличаться рядом особенностей. Даже при условии нормального развития, отсутствия заболеваний у недоношенных детей развивается анемия.
У детей, рожденных раньше срока, уровень гемоглобина и число эритроцитов может быть таким же, как и у доношенных малышей. Реже отмечается снижение или, наоборот, повышение этих показателей. В течение первых двух месяцев жизни происходит стремительное снижение количества гемоглобина в крови. Скорость этого процесса намного выше у недоношенных детей, чем у доношенных. Вследствие этого развивается состояние, характерное для детей, появившихся на свет раньше срока. В медицине оно называется анемией недоношенных детей.
В настоящее время существует несколько теорий возникновения анемии у недоношенных детей. Основные из них предполагают такие причины:
• недостаток в организме ребенка железа, которое необходимо для синтеза гемоглобина. Установлено, что это не единственная причина заболевания. Часто при введении препаратов железа в первые недели жизни ребенка не дают положительных результатов
• нарушения обмена веществ в организме
• сниженные запасы железа в организме
• анемия у матери
• стремительный прирост массы тела ребенка в первые месяцы жизни. Этот фактор приводит к повышенным потребностям железа
• недостаточность ферментов, которые участвуют в синтезе гемоглобина
• повышенный уровень билирубина в крови, что приводит к усиленному распаду эритроцитов
• временная функциональная недостаточность костного мозга — главного органа, где вырабатываются эритроциты
• врожденные заболевания, в особенности сепсис
• патологии, приобретенные впервые месяцы жизни недоношенного ребенка: рахит, пневмония, инфекционные заболевания
• неправильное и нерациональное питание ребенка, позднее введение прикорма и докорма. Пища, содержащая недостаточное количество белков и витаминов нередко усиливает проявления анемии у недоношенных детей
• неблагоприятные гигиенические условия
• недостаток свежего воздуха
• неблагоприятная экологическая обстановка
При нормальном протекании беременности, правильном развитии всех внутренних органов и систем у любого недоношенного малыша будут отмечаться признаки анемии разной степени.
Начинается активное проявление симптомом заболевания в конце первого — начале второго месяца жизни ребенка. Пик анемии отмечается, как правило, в 3-4-месячном возрасте. Если обеспечить правильный уход за малышом, а также придерживаться диетических норм, применять эффективные лекарственные препараты проявления заболевания полностью исчезают в возрасте 6-7 месяцев.
Важно! Если анемия у недоношенного ребенка сохраняется дольше 7 месяцев, тогда следует искать другие причины заболевания, не связанные с преждевременным появлением ребенка на свет.
Основной признак анемии — снижение в крови уровня гемоглобина и количества эритроцитов. Это приводит к ухудшению снабжения организма ребенка кислородом. Развиваются проявления гипоксии — кислородного голодания. От этого страдают все органы и системы: сердечно-сосудистая, дыхательная, нервная система, которые крайне чувствительны к нехватке кислорода в крови ребенка. Проявления таких нарушений могут быть следующие:
• учащенное сердцебиение. Это компенсаторная реакция, благодаря которой к органам и тканям поступает большее количество крови и улучшается снабжение кислородом
• увеличение размеров сердца из-за постоянных перегрузок
• характерные изменения на кардиограмме
• гипоксия миокарда
• учащение дыхания, одышка. При легкой степени анемии этот признак появляется только при нагрузке. При более тяжелых формах анемии одышка развивается в состоянии покоя
• поверхностное, неглубокое дыхание
• повышенная возбудимость ребенка
• угнетенное состояние малыша
• апатия
• отсутствие реакций на внешние раздражители при тяжелых формах анемии
• ухудшение или полная потеря аппетита
• бледность кожных покровов
• бледность слизистых оболочек
• увеличение селезенки в размерах при гемолитической анемии, связанной с усиленным распадом эритроцитов
• снижение уровня железа в анализе крови при железодефицитной анемии
• частые срыгивания
• сухость кожи
• нарушения стула
• отек лица и конечностей при тяжелых формах анемии
• отставание в физическом и умственном развитии
• повышенная склонность к инфекционным и воспалительным заболеваниям
Проявления заболевания будут отличаться в зависимости от степени заболевания, а также типа анемии.
Анемия у недоношенных детей
Независимо от типа анемии у недоношенных детей лечение всегда длительное и комплексное. Выбор метода коррекции состояния ребенка полностью зависит от типа и степени анемии.
Этот метод лечения анемии у недоношенных детей используют достаточно часто в первый месяц после рождения. Как правило, малыши очень хорошо переносят эту процедуру. Переливание крови или эритроцитарной массы значительно улучшает состав красной крови — повышает количество эритроцитов и гемоглобина. В большинстве случаев гемотрансфузии назначают при снижении уровня гемоглобина у недоношенного ребенка ниже 130 г/л в первую неделю жизни, что сопровождается серьезными нарушениями со стороны дыхания, а также работы сердца и центральной нервной системы. Основные опасности и побочные эффекты переливания крови:
• риск заражения такими заболеваниями, как ВИЧ, цитомегаловирусная инфекция и т.д.
• отторжение чужеродной крови
• нарушения электролитного равновесия крови
• избыток в сосудистом русле жидкости, которая поступает с вводимой кровью
У детей, родившихся раньше срока, наиболее частая форма анемии в возрасте после двух месяцев — железодефицитная. Основные лекарственные средства, используемые для лечения таких детей — препараты железа.
Важно! Чем меньше вес ребенка, тем раньше следует начинать лечение. Дозы препарата должны быть бόльшими.
Препараты железа детям назначаются внутрь в дозировке 5-7 мг на 1 килограмм веса в сутки между приемами пищи до нормализации уровня гемоглобина в крови. В дальнейшем 1,5-2 месяца принимают препарат железа в половинной дозе. Около 2 лет проводят плановую профилактику анемии недоношенных средствами, которые подберет врач. Повышает эффективность применение препаратов железа с аскорбиновой кислотой и витамином Е. При уровне гемоглобина 100 г/л и выше препараты железа не применяют.
Важно! Препараты железа нельзя запивать молоком!
Препараты железа в форме инъекций назначают только в следующих случаях:
• непереносимость препаратов железа
• нарушения в желудке и кишечнике
Основные побочные эффекты препаратов железа:
• боли в животе
• запор
• понос
• тошнота
• болезненность инъекций
Лечение разного типа анемий комплексное, что требует назначения разных групп лекарственных средств. С этой целью фармацевтическая промышленность выпускает комбинированные средства, которые содержат железо с фолиевой кислотой, витамином В12 и другими витаминами.
Витамины в лечении анемии
Наиболее часто детям с признаками анемии назначают витамины группы В, в особенности В12, а также фолиевую и аскорбиновую кислоту, рыбий жир. Все эти вещества повышают всасывание железа, улучшают обмен веществ в организме ребенка, участвуют в синтезе гемоглобина.
Диетотерапия в лечении анемии
Для новорожденных малышей единственный продукт питания — материнское молоко или адаптированная молочная смесь. Поэтому качественное улучшение состава пищи для детей, страдающих анемией, заключается в том, что нужные и ценные витамины, белки и микроэлементы (железо) вводятся дополнительно. Проводится такая терапия сначала в условиях отделения для новорожденных строго по медицинским показаниям в соответствии с массой тела ребенка и степенью анемии. По мере взросления ребенка ему назначают раннее введение прикорма, богатого витаминами, минералами, микроэлементами и белками. Эти вещества незаменимы в процессе синтеза эритроцитов и образования гемоглобина в крови растущего организма.
Важно! Вылечить анемию только с помощью диеты невозможно. Также, как и прием лекарственных средств без нормализации питания часто не оказывает должного эффекта. Только комплексный подход к проблеме анемии недоношенных детей дает продолжительный результат.
Эффективные меры профилактики следующие:
• назначение беременным во 2 и 3 триместре препаратов железа или витаминных комплексов, содержащих железо
• применение препаратов железа кормящими матерями
• детям, рожденным раньше срока, с трехмесячного возраста обязательно назначают препараты железа в дозе 2 мг/кг в сутки. Минимальная продолжительность приема — 3 месяца
• в течение двух лет, а иногда и дольше, контроль показателей крови 1 раз в квартал
• контроль за рационом беременных и кормящих женщин. Важно следить за тем, чтобы в меню присутствовали продукты, богатые железом
• назначение детям препаратов на основе рыбьего жира
Прогноз анемии недоношенных детей благоприятный. Средствами и методами современной медицины заболевание успешно лечится. Рациональное питание, прием лекарственных средств и регулярный контроль за показателями крови — составляющие здоровья вашего ребенка.
источник
Анемия является одной из наиболее частых патологий у детей раннего возраста. Около 20% доношенных детей страдают данным заболеванием, а среди недоношенных на первом году жизни анемия развивается практически у всех. При этом тяжесть анемии тем выше, чем меньше гестационный возраст ре6енка. В первые месяцы жизни у недоношенных детей с очень низкой массой тела при рождении (менее 1500 г) и гестационным возрастом менее 30 нед. тяжелая анемия, требующая переливание эритроцитарной массы, составляет до 90%.
Выделяют раннюю и позднюю анемии недоношенных.
Ранняя анемия недоношенных — это выраженная форма физиологической анемии новорожденных. Она развивается к концу первого-началу второго месяца жизни, имеет нормохромно-нормоцитарный тип и является гипорегенераторной анемией в результате транзиторной гипопродукции эндогенного эритропоэтина.
В последние годы изменился взгляд на патогенез ранней анемии недоношенных. Основные звенья в патогенезе РАН: дефицит гемопоэтических факторов (железа, фолиевой кислоты, белка) и недостаточность гуморального фактора — эритропоэтина (ЭП), ответственного за эритропоэз в организме, повышенный гемолиз эритроцитов, особенность типов гемоглобина, физиологическая гемодилюция, лабораторные потери и другие факторы.
Регуляция эритропоэза осуществляется эритропоэтином по принципу обратной связи. Интенсивность его обусловлена уровнем эритропоэтина в крови, физиологическим стимулом продукции которого является гипоксия. Внутриутробно он продуцируется в печени, которая сохраняет за собой эту функцию (в меньшей степени) как после рождения, так и на протяжении всей последующей жизни. После рождения основным органом, продуцирующим эритропоэтин (до 90%), являются почки. Процесс перехода начинается с 32-й недели гестации. Это объясняется тем, что печеночные О2-рецепторы менее чувствительны к гипоксии и реагируют на уровень рО2, равный 25-30 мм Hg (кислородное насыщение крови при этом составляет 50-60%), что защищает плод в условиях относительной гипоксии от избыточной полицитемии.
Частота развития и тяжесть клинического течения РАН обратно пропорциональна сроку гестации и массе тела при рождении. Степени тяжести РАН, соответствующие общепринятой классификации по А. И. Хазанову, следующие: I степень — колебания гемоглобина в пределах 100-85 г/л; II степень — 84-70 г/л; III степень — ниже 70 г/л.
Основными клиническими симптомами РАН являются: увеличение частоты сердечных сокращений и частоты дыхания, появление функционального систолического шума, усиление бледности кожных покровов, снижение двигательной активности, мышечного тонуса и суточной прибавки массы тела. Все эти клинические симптомы у здоровых недоношенных новорожденных можно рассматривать как включение компенсаторных механизмов организма в ответ на снижение количества клеток — переносчиков кислорода. У детей с кардио-респираторными проблемами эти симптомы являются угрожающими. Нужно помнить, что компенсаторные возможности у недоношенных детей ограничены ввиду общей незрелости организма и наличия сопутствующей пери- и постнатальной патологии.
Одним из основных методов лечения ранней анемии недоношенных до настоящего времени остаются гемотрансфузии. Наиболее часто для гемотрансфузий используется донорская эритроцитарная масса. Показаниями для переливаний эритроцитарной массы при анемии недоношенных являются: снижение гемоглобина ниже 130 г/л и гемотокрита ниже 0,4 в период ранней адаптации (первые 7 дней жизни) в сочетании с тяжелыми нарушениями дыхания и сердечной деятельности. Широкое использование гемотрансфузий у недоношенных детей сопряжено хотя и с невысоким, но существенным риском. Это прежде всего возможность передачи с трансфузиями вирусных инфекций (ВИЧ, ЦМВ), возможны также перегрузки сосудистого русла жидкостью, развития состояния «трансплантант против хозяина», электролитного дисбаланса. В настоящее время ведется поиск альтернативных путей решения этой проблемы. Одной из них является применение рекомбинантного человеческого эритропоэтина (Эпоэтин бета), полученного с помощью методов генной инженерии и внедренного в клиническую практику во всех возрастных группах.
Данные о том, что эритропоэтин является главным фактором в регуляции фетального и неонатального эритропоэза и что РАН характеризуется временной остановкой синтеза эндогенного эритропоэтина, дают возможность использования рекомбинантного эритропоэтина (Эпоэтин бета) у этой категории детей, обеспечивая не только хорошую терапевтическую эффективность, но и являясь физиологическим методом терапии.
Необходимо подчеркнуть, что одновременно с введением Эпоэтин бета, в результате активации эритропоэза, а также для достижения лучшего терапевтического эффекта, возрастает необходимость в адекватной обеспеченности белком и назначении препаратов железа (от 2 до 6 мг/кг/день), особенно у недоношенных детей, так как у них ограничен запас железа, а при его недостатке действие Эпоэтин бета снижается. Введение Эпоэтин бета повышает утилизацию клетками костного мозга железа из железосодержащих препаратов.
Снижение потребности в продуктах аллогенной крови и предупреждение осложнений, связанных с ними, является важным преимуществом включения Эпоэтин бета в терапевтический комплекс для профилактики и лечения ранней анемии недоношенных. Этот метод биологически безопасен и экономически доступен, что дает основание рекомендовать его для применения в неонатологической практике при выхаживании недоношенных детей, особенно гестационного возраста Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
источник
Основные причины железодефицитной анемии у недоношенных детей. Терапия. Данные проведенных исследований.
Н.М. Пясецкая, Т.А.Орлова, Национальная медицинская академия последипломного образования им. П.Л.Шупика, кафедра неонатологии
Институт прикладных проблем физики и биофизики НАН Украины, г. Киев
Для детей, родившихся преждевременно, харак-терной особенностью постнатального периода яв-ляется выраженное снижение уровня гемоглобина и количества эритроцитов с развитием с 3-го меся-ца жизни анемии недоношенных, которая носит же-лезодефицитный характер.
Непосредственной причиной железодефицитной анемии (ЖДА) у детей раннего возраста является развитие дефицита железа в организме, на степень выраженности которого влияет, как обеспеченность плода железом внутриутробно, так и обеспечен-ность новорожденного железом после рождения (экзогенное поступление железа в составе грудного молока или смесей и утилизация железа из эндо-генных запасов). Единственным источником железа для плода является кровь матери, поэтому, преж-девременные роды лишают новорожденного значи-тельного количества железа, наиболее интенсив-ный переход которого происходит в последнем триместре беременности.
Частота возникновения ЖДА у недоношенных де-тей составляет 50-100 % и зависит от:
- степени недоношенности ребенка (гестацион-ный возраст);
- состояния первоначального депо железа;
- интенсивности роста недоношенного ребенка;
- наличия перинатальных кровопотерь и их объем;
- характера вскармливания и патологии пост-натального периода;
- своевременности и качества профилактики анемии препаратами железа;
- состояния ферментных систем, участвующих в активном всасывании железа;
- длительности проводимой эритропоэтиноте-рапия (ЭПО-терапия), способствующей быст-
- рому истощению запасов железа и другие факторы.
Достижения последних десятилетий в области экс-периментальной гематологии, молекулярной био-логии и генетики расширили представления о фи-зиологии эритропоэза плода и новорожденного, что позволило расширить представления и о механиз-ме развития ЖДА у недоношенных детей.
Целью исследований является усовершенствова-ние антианемического комплекса путем изучения основных патогенетических механизмов развития дефицита железа и ЖДА у недоношенных детей разного гестационного возраста.
Для достижения поставленной цели в динамике первых 2-3 месяцев жизни под наблюдением нахо-дилось 297 недоношенных новорожденных геста-ционного возраста (ГВ) 26-35 нед, которые находи-лись в клинике «ОХМАТДЕТ» г. Киева.
Для изучения основных звеньев развития дефици-та железа и ЖДА у недоношенных детей определя-ли:
1) основные показатели красной крови (Hb, RBC, Ht), эритроцитарные индексы (MCV, MCH, MCHC, RDW);
2) регенераторную активность костного мозга путем подсчета ретикулоцитов (RTC);
3) структурно-качественное состояние эритро-цитов (электронная микроскопия и определение проницаемости эритроцитарных мембран — ПЭМ;
4) функциональное состояние гемоглобина по содержанию активного гемоглобина (Hbакт) и неак-тивного (HbD), содержащего дериваты гемоглобина (MetHb, SHb, HbCO) по модифицированному мето-ду, разработанного в Киевском НИИ Гематологии и переливания крови;
5) активность процессов липопероксидации по содержанию в крови полного спектра продуктов ПОЛ: первичных, вторичных и конечных. Изучали гептановую фазу липидных экстрактов, состоящую в основном из нейтральных липидов, и изопропа-нольную, в которую в большей степени экстрагиру-ются фосфолипиды;
6) показатели обмена негемового железа, ис-пользуя методы, разработанные на количествен-ной спектроскопии электронного спинового резо-нанса (ЭСР) (Михайлик О.М., Дудченко Н.А., 2000): индекс железа в форме депонирующих его белков – ферритина/гемосидерина) ; концентра-цию железа в составе трансферрина ; концентрацию белка трансферрина , степень насыщения трансферрина железом . Кон-центрацию железа трансферрина, ассоциированно-го с клетками крови , рассчитывали, ис-пользуя показатели в цельной крови и плазме крови с учетом гематокрита (): . Спек-тры электронного спинового резонанса регистриро-вали для прессованных цилиндрических образцов диаметром около 2 мм, используя спектрометр EPA-10 mini spectrometer (Санкт-Петербург, Рос-сия).
FeФт
Статистическую обработку материала проводили на персональном компьюторе IBM Pentium с ис-пользованием программ Statgraf (V.2.6., USA) и STATISTICA (фирмы StartSoft Inc., USA), интегри-рованной системы для комплексного статистиче-ского анализа и обработки данных в среде Windows. Для определения критериев достоверно-сти разницы статистических совокупностей исполь-зовали критерии Стьюдента (t-тест). Различия счи-тались достоверными при р 0,05), у детей ГВ 31-29 нед — с 89,16 % до 93,8 % (р Нажмите для комментария
Для отправки комментария вам необходимо авторизоваться.
Для отправки комментария вам необходимо авторизоваться
источник
Анемия (малокровие) — заболевание или патологическое состояние, при котором в крови резко падает уровень гемоглобина и количество эритроцитов. Болезнь распространена как в детском возрасте, так и у взрослых. Тканевая гипоксия, вызванная анемией, приводит к задержке развития, частым болезням ребенка.
Анемия у детей в 40% случаев диагностируется до трех лет. В раннем возрасте малыши особенно чувствительны к воздействию внешних факторов, влияющих на гемопоэз.
Новорожденный младенец делает первые самостоятельные вздохи и начинает продуцировать эритроциты. На стадии плода он был полностью зависим от материнских клеток крови. Они доставляли необходимый кислород и выводили шлаки. Установлено, что до полугода дети еще сохраняют запасы гемоглобина, железа, полученные от матери, но во втором полугодии жизни вся надежда только на «собственное производство».
Второй по опасности период жизни — подготовка и половое созревание (пубертатный). Организм ребенка требует много витаминов и «строительных» материалов. Педиатры обнаруживают до 30% анемий у юношей 12-16 лет, девушек – 11-15.
В таблицах приведена зависимость уровня эритроцитов и гемоглобина от возраста ребенка.
| Возраст | Количество эритроцитов (х 10 12 в литре крови) |
| сразу после рождения и до седьмого дня жизни | 4 – 6,6 |
| две недели | 3,6 – 6,2 |
| 1 месяц | 3,0 – 5,4 |
| 2 – 6 месяцев | 2,7 – 4,9 |
| 1 год | 3,6 – 4,9 |
| 3 – 12 лет | 3,5 – 4,7 |
| после 13 | 3,6 – 5,6 |
| Возраст | Уровень гемоглобина в г/л |
| 2 недели | 134 — 198 |
| 1 месяц | 107 — 171 |
| полгода | 110 — 141 |
| год | 113 — 141 |
| 2 – 5 лет | 110 — 140 |
| до 12 лет | 120 – 150 |
| подростковый период | 120 – 166 (юноши), 115 – 153 (девушки) |
Таблицы демонстрируют снижение накоплений у 6-месячного ребенка.
Педиатры заметили, что дети, находящиеся на грудном вскармливании, болеют малокровием значительно реже, чем «искусственники». Это происходит из-за качественного состава материнского молока. В нем содержится полноценный набор веществ для образования гемоглобина (медь, железо, белки, витамины).
В старшем возрасте дети нуждаются в микроэлементах (никель, кобальт, марганец, медь, железо), достаточном содержании белка в пище. Отсутствие мясных продуктов, овощей, фруктов приводит к нарушению гемопоэза, формированию дефицитных анемий. Особенно чувствителен организм к недостатку витаминов группы В, фолиевой кислоты, С.
У доношенного годовалого ребенка возможно возникновение алиментарной (нарушение вскармливания) и алиментарно-инфекционной анемии (последствия респираторных заболеваний, отитов, ринитов).
В дошкольном возрасте причиной может стать глистная инвазия (аскаридоз), перенесенные инфекционные заболевания, болезни кишечника с нарушением всасывательной способности.
В подростковом возрасте анемия сопутствует отравлению алкоголем, курению, употреблению наркотиков.
Классификация детских анемий построена на зависимости от причины и вызванных морфологических изменениях клеток эритробластного ряда.
Постгеморрагические — вызваны острой или длительной хронической кровопотерей, возникают при травмах, оперативных вмешательствах.
Анемии, связанные с нарушением продуцирования эритроцитов , блокадой эритроцитарного ростка. Они подразделяются на несколько видов:
- гипохромные железодефицитные анемии у детей;
- анемии с нормальным уровнем железа наследственные и приобретенные (сидероахрестические, вызванные низким уровнем порфиринов);
- мегалобластические, включая В12 и фолиеводефицитную;
- приобретенные и наследственные апластические и гипопластические анемии, связанные с общим угнетением кроветворения.
Группа гемолитических анемий по механизму образования связана с усилением разрушения эритроцитов, отставанием синтеза новых клеток от потребности (гемоглобинопатии, ферментопатии, гемолитическая болезнь новорожденных, аутоиммунные процессы).
Принято выделять 3 стадии в развитии болезни:
- прелатентный период — характеризуется истощением железа в тканях, снижением процессов усвоения из пищи в связи с ферментативной недостаточностью, при этом уровень гемоглобина в крови нормальный;
- латентный (скрытый) — снижается количество запасов железа в депо и в сыворотке крови;
- стадия выраженных клинических проявлений — значительно снижен гемоглобин и эритроциты, имеется клиническая симптоматика гипоксии тканей.
Симптомы анемии группируются в синдромы по характеру поражения определенных органов и систем. Они могут проявляться вместе или иметь преимущественные признаки, зависят от степени поражения гемопоэза в каждом отдельном случае. Наиболее типичны для уровня снижения гемоглобина до 80 г/л и ниже.
- Эпителиальный — бледная кожа, слизистые, ушные раковины, при осмотре ребенка кожу называют «прозрачной» из-за хорошо просвечивающихся кровеносных сосудов, наблюдается шелушение и пигментация, ломкость ногтей, стоматит во рту, отказ от еды, у малыша до года частые срыгивания, понос, наклонность к рвоте, у более старших детей — извращение вкуса (расковыривают стену и едят известку, мел, землю).
- Астеноневротический — дети отстают в речевом и психическом развитии, раздражительны, плохо спят, наблюдается энурез (ночное неконтролируемое мочеиспускание), в старшем возрасте вялые, не успевают делать задания в школе, отличаются повышенной утомляемостью, жалуются на частые головные боли, головокружения.
- Поражение сердечно-сосудистой системы — склонность к пониженному давлению, беспокоят сердцебиения, тахикардия, постоянно холодные руки и стопы, при аускультации определяется приглушенность тонов сердца, возможен шум.
- Дефицит иммунитета — проявляется в частых простудных заболеваниях, кишечных инфекциях, длительном периоде восстановления, плохом заживлении царапин и мелких ранок.
- Гепатолиенальный — поражение печени и селезенки обнаруживается при обследовании по повышенному уровню билирубина, нарушенному составу белков и ферментов, увеличению размеров.
Окончательная диагностика с определением лабораторных признаков позволяет установить конкретный вид анемии, степень тяжести и стадию болезни.
В общем анализе крови определяется сниженное содержание гемоглобина и эритроцитов, гипохромия.
- при легкой степени — показатели гемоглобина колеблются от 90 до 110 г/л, количество эритроцитов снижается до 3,5х 10 12 /л;
- при 2 степени (средней) — показатели изменяются, соответственно, 70–90 и 2,5х 10 12 и ниже;
- для 3 (тяжелой) степени — характерны сниженный гемоглобин ниже 70, эритроциты менее 2,5х 10 12 .
Биохимические тесты позволяют определить количество сывороточного железа, уровень насыщенности трансферрина, концентрацию ферритина в сыворотке, билирубин.
При необходимости проводятся исследования на содержание конкретных витаминов в крови.
Для диагностики апластических и мегалобластных анемий имеется необходимость в проведении пункции и исследовании костного мозга.
Анемия у недоношенных детей подразделяется на такие виды:
- ранняя – возникает на первом-втором месяце жизни малыша;
- поздняя – на третьем-четвертом месяце.
На развитие ранней формы оказывают влияние такие факторы:
- родовые травмы головы;
- предшествующие инфекционные заболевания матери накануне родов;
- нарушения в питании, вызвавшие дефицит белка и микроэлементов в последние 2 месяца.
Анемию рассматривают как физиологичную для некоторых доношенных детей. Ребенок отличается бледностью, другие проявления отсутствуют. В крови обнаруживают нормо- или гиперхромию.
При поздней форме – сниженное количество железа.
Лечить такие виды анемии нужно с помощью обеспечения покрытия необходимого дефицита в организме матери.
Железодефицитная анемия у детей выявляется по сниженному уровню:
- гемоглобина;
- цветового показателя;
- сывороточного железа (менее 120 мкмоль/л);
- насыщения плазмы трансферрином (менее 25%);
- сывороточного ферритина (менее 30 нг/л).
На фоне повышения железосвязывающих способностей сыворотки – до 60 мкмоль/л и выше.
Определяется положительный эффект от применения препаратов железа на 7-10 день лечения.
Для терапии необходимо дифференциальная диагностика с атипичными формами (сидероахрестическими, диморфными), гипохромными анемиями.
Сидероахрестическая анемия вызвана дефектами строения гемоглобина, при котором железо не захватывается эритроцитом. Лабораторно определяется достаточный уровень железа и трансферрина в крови, а способность связывать железо низкая. В лечении препараты железа не нужны.
Диморфные анемии связаны с одновременным дефицитом железа, витамина В12, фолиевой кислоты, белков, других микроэлементов. Часто выявляются при вскармливании ребенка козьим молоком. В клинике преобладает отставание в развитии, геморрагические высыпания, увеличение селезенки (реже печени).
В анализах крови: резкое падение эритроцитов, лейкоцитоз, наличие мегалоцитов, снижение гемоглобина и железа.
Пиридоксиндефицитная анемия — редкая форма, связанная с недостатком витамина В6, что нарушает синтез гема. В крови снижено количество эритроцитов, они гипохромны, но уровень железа даже повышен. Препараты железа в терапии не показаны.
Талассемия — наследственное заболевание, приводящее к анемии из-за нарушения синтеза белка, встречаются другие генетические синдромы (даунизм, аномалии костей, зубов). Признаки проявляются в 2–8 лет. Клиническое течение в виде кризов с лихорадкой, пигментацией кожи, переломами костей скелета. В крови – ретикулоцитоз, эритробласты, повышен билирубин, сывороточное железо, железо определяется в моче.
Представителем гемолитических анемий является наследственное заболевание — болезнь Минковского-Шоффара (микросфероцитоз). Из-за высокой проницаемости оболочки эритроцитов они становятся сферическими, разрушаются селезенкой как чужеродные клетки. Возникает в любом возрасте, но чаще выявляется у детей.
Клинически проявляется выраженной желтухой при удовлетворительном состоянии ребенка. Протекает с обострениями и ремиссиями. Кроме общих для всех анемий симптомов, существует типичная зависимость самочувствия от холода (наступает спазм сосудов рук и ног), происходит пожелтение кожи и склер, периодически наблюдается темная моча. Со временем проявляются последствия заболевания — трофические язвы на стопах и голенях, не поддающиеся терапии.
Лечение анемии у детей зависит от вида малокровия, степени тяжести заболевания. Кроме лекарственных препаратов, обязательно уделяется внимание режиму и питанию.
Ежедневно следует предусмотреть пребывание больного ребенка на воздухе. Прогулки лучше совершать в парке или лесу, где воздух насыщен кислородом. Рекомендуется даже для школьников устраивать дневной сон.
Диета ребенка до года с малокровием должна кроме грудного молока своевременно подключать соки, тертые овощи и фрукты, мясное пюре. При искусственном вскармливании подбираются молочные смеси, обогащенные железом и микроэлементами.
В старших возрастных группах нельзя забывать о пользе продуктов из печени, говядины, морской рыбы, о бобовых (фасоль, чечевица), о приправах из свежей зелени. Фрукты и овощи лучше давать в сыром виде в салатах, свежих соках.
Применяются по показаниям препараты железа: Гемофер, Ферроплекс, Конферон и другие. Они обязательно сочетаются с комплексными витаминами, антиоксидантами.
При В12 -дефицитной анемии назначают внутримышечные инъекции витамина и фолиевую кислоту внутрь. Если малокровие вызвано нарушенной всасываемостью из кишечника, для ребенка важно нормализовать стул. В терапии возможно применение ферментов, растительных препаратов.
Если заболевание выявлено у ребенка своевременно и организовано правильное питание и лечение, то возможно полное выздоровление.
Профилактика железодефицитной анемии у детей начинается с ведения беременности матери, соблюдения правильного режима и организации полноценного питания. Для новорожденного необходимо материнское молоко. Это самое нужное средство предупреждения малокровия. Мамы с детьми должны больше гулять, высыпаться.
Если при беременности имелась анемия, то врач должен наблюдать малыша в группе повышенного риска. Возможно, придется перенести часть прививок на более поздние сроки.
В школьном периоде жизни нельзя разрешать ребенку употребление фастфуда, большого количества сладостей. Лучше положить в ранец яблоко или грушу. Дома зимой варить компот из сухофруктов, летом включать в питание свежие ягоды.
В некоторых случаях по назначению врача рекомендуются профилактические дозы препаратов железа короткими курсами. Нельзя забывать про опасность анемии при жалобах ребенка на усталость, головную боль, неуспеваемость по школьной программе. Дети гораздо сильнее реагируют на все поражающие факторы, чем взрослые. В какую сторону изменится внутренний баланс организма — укрепление защиты или болезнь — зависит от взрослых членов семьи.
источник
У детей анемии встречаются часто, и самая распространенная среди них — железодефицитная, в раннем возрасте ее выявляют у детей. При недостаточном поступлении или избыточных потерях железа, при нарушении его всасывания, в крови снижается содержание гемоглобина.
Не стоит относиться к анемии как к несерьезному заболеванию, которое «пройдет само». Она ухудшает самочувствие ребенка, с напряжением начинают работать многие органы и системы, но особенно чувствителен к недостаточному снабжению кислородом растущий головной мозг малыша.
Железо имеет важное значение для организма человека: оно участвует в транспорте кислорода ко всем тканям и углекислого газа от них, в восстановлении поврежденных тканей, входит в состав многих ферментов и белков, поддерживает нормальную работу иммунитета.
В растущем организме железо расходуется не только на компенсацию его потерь и образование гемоглобина (он транспортирует кислород), но и на создание дополнительных запасов для роста.
Этот микроэлемент накапливается в организме будущего малыша на протяжении всей беременности, поступая через плаценту от матери. Поэтому важно, чтобы у самой беременной женщины не было проявлений железодефицитной анемии. Большая часть запасов железа внутриутробно накапливается у плода в течение последнего триместра. Недоношенные дети не успевают получить достаточный запас этого элемента, и после рождения у них довольно быстро формируется железодефицитное состояние.
После рождения железо поступает в организм с пищей. В грудном молоке железа содержится меньше, чем например, в коровьем или козьем, но благодаря особому белку лактоферрину всасывается оно намного лучше, поэтому доступность железа из грудного молока выше. Кроме того, лактоферрин связывает не всосавшееся в кишечнике железо, тем самым препятствуя размножению условно-патогенных бактерий.
В первые 5 месяцев жизни здоровому малышу бывает достаточно запасов железа, которые сформировались внутриутробно. Но из-за быстрого обмена веществ к 6 месяцам они истощаются. Железа, которое поступает с грудным молоком, становится недостаточно, и уже продукты прикорма начинают играть роль в восполнении его дефицита.
Железо содержится в разных продуктах, но из пищи растительного происхождения оно всасывается намного хуже, чем из животных продуктов. И советы употреблять в больших количествах яблоки, гранаты, гречку не оправданы, потому что форма, в которой содержится железо в них, усваивается из кишечника плохо, несмотря на его большое процентное содержание. Рыба, печень и мясо в свою очередь улучшают всасывание этого микроэлемента из злаков, овощей и фруктов. Молоко, чай, каши из злаков затрудняют усвоение железа из-за содержащихся в них фитатов, фосфатов, кальция и танина. В присутствии аскорбиновой кислоты и фруктозы скорость всасывания железа возрастает. Важно также, чтобы пища содержала достаточное количество белка.
Причинами дефицита железа у ребенка могут быть:
- патология беременности, при которой нарушается поступление железа к плоду (токсикозы, угроза прерывания, заболевания или анемия матери во время беременности);
- недоношенность, многоплодие;
- кровопотеря в родах, ранняя перевязка пуповины;
- раннее искусственное вскармливание, вскармливание коровьим или козьим молоком, несбалансированное питание малыша;
- повышенные темпы роста (у недоношенных, детей с большой массой тела при рождении, во втором полугодии и на втором году жизни);
- кровотечения (в том числе у части девочек в период становления менструального цикла) или нарушение всасывания в кишечнике (хронические энтериты, наследственные синдромы).
Анемия возникает не сразу, в ее развитии выделяют ряд последовательных стадий. Сначала истощаются запасы железа в тканях — так называемый прелатентный дефицит железа. Он не имеет никаких внешних признаков, но у детей, в отличие от взрослых, железо начинает хуже всасываться из кишечника. Лабораторно подтвердить это можно только с помощью сложных специальных процедур, не предназначенных для повседневной практики.
Вторая стадия — латентный (скрытый) дефицит, когда кроме тканевых запасов истощается и транспортируемое белками крови железо, содержание гемоглобина и эритроцитов все еще не изменено. Эту стадию можно распознать лабораторно и по ряду незначительных симптомов. В биохимическом анализе крови снизится содержание сывороточного железа и повысится железосвязывающая способность сыворотки. В этот период ребенок быстро и легко утомляется, становится раздражительным и капризным, у него может снизиться аппетит.
Третья стадия — непосредственно сама железодефицитная анемия, развивается, когда исчерпаны все запасы железа в организме. Изменения будут уже и в общем анализе крови — уровень гемоглобина становится ниже 110 г/л, возможно небольшое снижение эритроцитов, они становятся разной формы и размеров, слабо окрашиваются красителями. В крови остается сниженным уровень сывороточного железа, повышена железосвязывающая способность сыворотки.
Патологические симптомы касаются практически всех органов и систем. Ребенок может жаловаться на слабость, он плохо переносит физическую нагрузку, часто капризничает и плачет. Кожа становится бледной, сухой, волосы — тусклыми и ломкими. У каждого третьего ребенка в возрасте до 3 лет, страдающего анемией, наблюдается извращение вкуса, обоняния и аппетита — им начинает нравиться запах бензина, выхлопных газов, мыла, дети начинают отдавать предпочтение острой, соленой или кислой пище, а иногда едят несъедобные вещества — мел, глину, крахмал, лед.
Слизистая оболочка рта при анемии становится более сухой и ранимой, в тяжелых случаях возможны воспалительные изменения на деснах, губах, языке, зубы чаще поражаются кариесом. Изменения касаются также сердечно-сосудистой, мочевыделительной, нервной систем, желудочно-кишечного тракта. У детей с анемией снижается иммунитет, и они начинают часто болеть кишечными или респираторными инфекциями.
Из-за дефицита железа усиливается всасывание свинца, который содержится в выхлопных газах автомобилей, в промышленных выбросах предприятий крупных городов. Это неблагоприятно влияет на растущий организм, может привести к изменениям интеллекта, поведения, а также заболеваниям крови и почек.
По содержанию гемоглобина выделяют три степени тяжести анемии: легкая, если гемоглобин в пределах 83 — 110 г/л, средней тяжести при гемоглобине 66 — 82 г/л и тяжелая, если гемоглобин ниже 66г/л. Пропорционально гемоглобину в крови снижается содержание эритроцитов.
Важно правильно организовать режим дня — ребенок должен проводить на свежем воздухе не меньше 3 часов в день. Исследования показали, что в таком случае гемоглобин образуется быстрее. Такой же эффект оказывают массаж и лечебная гимнастика.
Кормящей матери необходимо сбалансированно питаться, чтобы в молоко попадало достаточное количество железа. Рацион ребенка постарше тоже должен быть полноценным: содержать достаточно животного белка, а также свежих овощей и фруктов.
Важное правило: если дефицит железа уже сформировался, то восполнить его без железосодержащих препаратов, только одной диетой, невозможно.
Для лечения детям чаще всего назначают лекарства в виде сиропа или каплей внутрь, врач рассчитает необходимую дозу и курс препарата. Первый раз лекарство лучше дать в половинной дозе, чтобы исключить индивидуальную непереносимость. Если после приема лекарства появляются тошнота, рвота, боли в животе, запор или понос, врач или уменьшит дозу, или заменит препарат. В течение 7- 10 дней дозу постепенно доводят до полной. Как правило, лечение довольно длительное, не меньше 3 недель, проходит под регулярным контролем уровня гемоглобина, ретикулоцитов и эритроцитов в крови. После нормализации цифр гемоглобина препараты железа принимают еще некоторое время, чтобы восполнить его запас в тканях. В комплексном лечении также используют витамины с микроэлементами (медь, кобальт, никель, марганец).
Во время лечения железо может окрашивать стул ребенка в черный цвет. Запивать лекарство лучше фруктовым соком, на который у ребенка нет аллергии — содержащийся в нем витамин С улучшает всасывание железа. А молоко, чай, напротив, ухудшают.
Если анемия обнаружена у малыша с инфекционным заболеванием, восполнять дефицит железа с помощью лекарств начинают только после выздоровления. Такая анемия может быть просто результатом перераспределения запасов железа в организме.
источник
Анемия у детей в большинстве случаев оказывается железодефицитной и обуславливается дефицитом железа в организме, возникающим ввиду нарушений его поступления с пищей, усвоения в кишечнике или излишних потерь.
Возникновению анемии, в большинстве случаев, предшествует возникновение скрытого недостатка железа, который рассматривается как функциональное нарушение и выражается уменьшением резервного запаса железа в организме и понижением его уровня в тканях, при этом — отсутствием анемии.
Главная причина железодефицитной анемии, по ВОЗ — это несбалансированная диета, бедная железом. Значительно реже железодефицитная анемия у детишек развивается из-за различных кровотечений, (такая анемия называется — хроническая постгеморрагическая, или из-за глистных инвазий (в регионах с низкой культурой).
- Недостаток железа в организме ребеночка при его рождении.
- Недостаток железа ввиду несбалансированной диеты.
- Увеличение потребности организма ребеночка в железе из-за активного роста.
- Потеря железа организмом, превышающая физиологическую потерю.
К алиментарно-зависимым факторам анемии у детей можно отнести
- Недостаток железа в употребляемой пище.
- Пониженная всасываемость железа в ЖКТ.
- У детишек до года причиной анемии может быть возрастание потерь железа ввиду мелких кровотечений в ЖКТ, вызванных преждевременным прикормом детей кефиром и коровьим молоком.
У подростков мужского пола причиной анемии- могут быть разные болезни ЖКТ: язвенное кровотечение, полипоз, ангиоматоз или опухоль ЖКТ, неспецифический язвенный колит, Меккелев дивертикул, кровотечения из геморроидальных вен.
У девочек-подростков и девушек главной причиной постгеморрагической ЖДА являются маточные кровотечения, а болезни ЖКТ отодвигаются на второй план. Половые различия следует учесть при определении причин ЖДА.
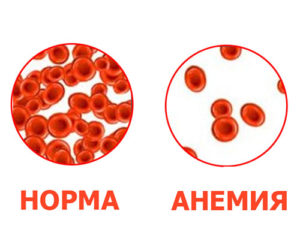
- Уменьшение уровня гемоглобина — Hb (ниже 110 г/л).
- Небольшое понижение числа эритроцитов (меньше 3,8 × 1012/л).
- Уменьшение цветового показателя (меньше 0,85).
- Возрастание скорости оседания эритроцитов (СОЭ, больше 10-12 мм/ч).
- Пониженное или нормальное число ретикулоцитов (10-20‰).
- Кроме этого, лаборант отмечает морфологические особенности эритроцитов — пойкилоцитоз и анизоцитоз.
В общих анализах крови, проводимых с помощью автоматического анализатора крови, кроме изменения указанных выше показателей, меняется серия эритроцитарных индексов.
Уменьшается средний объем эритроцита (mean corpuscular volume — MCV, меньше 80 фл),
Среднее содержание Hb в эритроците (mean corpuscular hemoglobin — MCH, меньше 26 пг),
Средний уровень Hb в эритроците (mean corpuscular hemoglobin concentration — MCHC, меньше 320 г/л),
Увеличивается степень анизоцитоза эритроцитов (red cell distribution width — RDW, больше 14%).
В биохимических анализах крови обращают внимание на
Понижение количества железа в сыворотке крови — СЖ (меньше 12,5 мкмоль/л).
Возрастание общей железосвязывающей способности сыворотки — ОЖСС (больше 69 мкмоль/л).
Уменьшение процента насыщения трансферрина железом — НТЖ (менее 17%).
Понижение количества сывороточного ферритина СФ (меньше 30 нг/мл или мкг/л).
Сейчас стало возможным определять растворимые трансферриновые рецепторы, концентрация их при дефиците железа возрастает (более 2,9 мкг/мл).
- Устранить причину, вызвавшую болезнь (скорректировать питание, выявить и устранить источник кровопотери).
- Возместить недостающее железо организму.
- Назначаются железосодержащие лекарства, т.к. возмещение недостатка железа в организме другими методами невозможно.
- Используются в первую очередь железосодержащие лекарства для внутреннего применения.
- Дозы железосодержащих лекарств подбираются индивидуально с учетом возраста больного, его массы и плана лечения.
- Продолжительность лечения должна быть при анемиях первой (легкой) ст. — 3 мес, при анемиях второй (средней) ст. 4,5 мес, и при анемиях третьей (тяжёлой) степени — полгода.
- В процессе лечения должны восполниться резервы железа в депо, что можно определить по нормализации уровня сывороточного ферритина.
- Необходим обязательный контроль эффективности лечения железосодержащими лекарствами.
В РФ терапию ЖДА проводят по Протоколу «Железодефицитная анемия» утвержденному МЗ России от 22.10.2004г.
В терапии ЖДА у детишек есть особенности, которые учитываются в терапевтических протоколах. Например, назначение детям до 3х лет солевых железосодержащих лекарств в дозировках 5-8 мг/кг веса в день, как это рекомендует протокол, приводит к токсическим явлениям у некоторых детей. Поэтому, детям до 3х лет рекомендуемая ежедневная дозировка железосодержащих лекарств 3 мг/кг, детишкам после 3х лет — 5 мг/кг.
 Железодефицитная анемия у детей Лекарства для приёма внутрь
Железодефицитная анемия у детей Лекарства для приёма внутрь
Железосодержащие лекарства для терапии ЖДА можно условно подразделить на ионные-солевые (двухвалентные) и лекарства на основе гидроксид полимальтозного комплекса (трёхвалентные).
К препаратам 2х валентного железа относятся актиферрин, сорбифер, ферроплекс, фенюльс.
К препаратам 3х валентного железа на основе гидроксид полимальтозного комплекса относятся: мальтофер, феррум-лек, железо полимальтозное, ферри.
Современные научные исследования доказывают, что эффект от препаратов 2х и 3х валентоного железа в лечении ЖДА одинаков.
- Частые передозировки и иногда отравления лекарством из-за неконтролируемости организмом пассивного всасывания железа.
- Вступление в реакцию с прочими лекарствами и едой.
- Характерный привкус металла во рту после приёма лекарства.
- Коричневая или фиолетовая окраска десен и эмали зубов, как правило проходящая со временем, в редких случаях стойкая.
- Высокий процент отказов родителей от лечения (до трети приступивших к лечению).
Большей части побочных эффектов нет у препаратов трёхвалентного железа на основе гидроксид полимальтозного комплекса
- Они безопасны.
- Риск передозировок, интоксикаций, отравлений отсутствует.
- Не дают окрашивания десен и зубов.
- Не имеют металлического привкуса.
- Хорошо переносятся.
- Не вступают во взаимодействие с прочими лекарствами и продуктами.
- Обладают антиоксидантными свойствами.
- Пациенты реже отказываются от лечения.
Парентеральные (внутривенные и внутримышечные) железосодержащие лекарства применяются тогда, когда есть противопоказания к назначению железосодержащих лекарств для внутреннего приема или они не дают эффекта.
- Тяжелых формах ЖДА (на сегодняшний день они встречаются редко, менее чем у 3% больных анемией).
- Аллергии на пероральные железосодержащие лекарства.
- Неэффективности железосодержащих лекарств для приема внутрь.
- Наличии у детей язвы желудка или 12-перстной кишки или операций на ЖКТ в прошлом.
- Хронические болезни кишечника у пациента (болезнь Крона язвенный колит).
- Хронические болезни почек (в преддиализный и диализный периоды) если они отягощаются анемией.
- Наличие противопоказаний к переливанию эритроцитной массы.
- Наличие необходимости скорого насыщения организма железом.
Внутримышечно или внутривенно препараты железа, как правило делают, 1-3 раза в неделю. При терапии парентеральными железосодержащими лекарствами нельзя превышать общий дефицит железа, который можно рассчитать по формуле Ганзони.
Общий дефицит железа, мг = Масса тела больного, кг × (Hb (норма), г/л — Hb больного, г/л) × 0,24 + Депо железа, мг.
Коэффициент 0,24 = 0,0034 × 0,07 × 1000:
содержание железа в Hb — приблизительно 0,34%;
объем крови — 7% массы тела;
1000 — перевод граммов в миллиграммы.
Депо железа у пациентов с массой тела:
менее 35 кг — 15 мг/кг, целевая концентрация Hb — 130 г/л;
более 35 кг — 500 мг, целевая концентрация Hb — 150 г/л.
В этой формуле учитывается железо в депо, которое составляет более трети общего количества железа в организме. Понижение резервов железа в депо можно определить по количеству сывороточного ферритина.
Возможны побочные эффекты при введении железа парентерально местные (жжение, зуд) и общие (аллергические). При парентеральном введении железа требуется наблюдение за больным, применение тестовой дозы лекарства до начала терапии, точный расчет дозы лекарства.
Чтобы лечение парентеральными железосодержащими препаратами стало безопасным и эффективным для ребенка следует выполнять следующие принципы лечения
- Применять современные парентеральные железосодержащие лекарства с низкой токсичностью, без возможных анафилактических реакций, представляющих угрозу для жизни ребеночка.
- Определить общий дефицит железа в организме ребенка до начала лечения.
- Прекратить терапию после того, как общий дефицит железа в организме восполнится, для того чтобы избежать перенасыщения железом опасного для ребенка.
- Соблюдать технику внутримышечных инъекций и внутривенных инфузий железосодержащих лекарств.
- Строго соблюдать инструкцию к парентеральным препаратам железа, если рекомендуется ввести пробную дозу до начала терапии.
- Терапию следует проводить в интервале безопасных доз, т. к. побочные эффекты парентеральных железосодержащих лекарств дозозависимы.
- Ретикулоцитарная реакция: к концу первой, началу второй недели с начала терапии железосодержащими лекарствами число ретикулоцитов увеличивается на 2-3% или 20-30‰ если сравнивать с их числом до лечения.
- Увеличение уровня Hb к концу месяца терапии на 10 г/л и гематокрита на 3% если сравнивать с начальными цифрами до лечения.
- Купирование проявлений анемии через 1-1,5 мес с начала лечения.
- Восполнение дефицита железа в тканях в депо через 3-6 мес с начала терапии, что можно определить по нормализации уровня СФ (более 30 нг/мл).
- Неправильная постановка диагноза железодефицитная анемия у детей.
- Неадекватная доза железосодержащих лекарств.
- Недостаточная продолжительность терапии ЖДА.
- Невыполнение назначений врача родителями ребенка.
- Наличие у ребенка трудностей всасывания железа в ЖКТ.
- Непереносимость ребенком выбранного лекарства.
Если диагноз ЖДА поставлен верно, то эффект от терапии препаратами железа обязательно будет. Если нет ретикулоцитарной реакции, которая характеризует первый эффект от лечения, и нет возрастания уровня Hb на 10 г/л и гематокрита на 3% после месяца терапии, то нужно прекратить прием лекарств и обдумать диагноз, т. к., существует вероятность, что у ребенка — не ЖДА.
Устойчивость ЖДА к терапии железосодержащими лекарствами часто вызвана неправильно подобранной дозой или анемия не имеет ничего общего с недостатком железа.
Недавно описана новая форма ЖДА, называемая железорефрактерной (iron-refractory iron deficiency anemia — IRIDA). Она наследуется по аутосомно-рецессивному типу. Терапия IRIDA железосодержащими лекарствами для приёма внутрь неэффективна, некоторый эффект получается при использовании парентеральных железосодержащих лекарств.
При ЖДА, в большинстве случаев, нет показаний для переливаний эритроцитной массы. Даже в тяжелых случаях, ЖДА успешно лечится пероральными, внутримышечными или внутривенными железосодержащими лекарствами. Риски от переливания эритроцитной массы для борьбы с ЖДА значительно превышает пользу от него.

Ежесуточные потребности взрослого в железе — 1-2 мг, ребеночка — 0,5-1,2 мг. Стандартный суточный рацион питания содержит от 5 до 15 мг железа. В ЖКТ усваивается 10-15% железа из пищи.
Главные пищевые источники железа — это продукты, содержащие гемовое железо: мясо (говядина, баранина, курятина), рыба, творог. Важнее не содержание железа в продукте, а его биодоступность. Негемовое железо, из растительных продуктов: овощей, фруктов, злаков обладает низкой биодоступностью, т.е. из этих продуктов железо хуже всасывается.
Для всасывания железа нужны некоторые условия: аскорбиновая кислота улучшает всасываемость железа, а танин, имеющийся в чае, или фитаты, которые есть в некоторых продуктах, уменьшают её. При ЖДА усвоение железа в 12-перстной кишке значительно увеличивается.
Для профилактики ЖДА американская академия педиатрии рекомендует следующее
- Здоровые доношенные детишки до 4х месяцев обладают достаточными резервами железа в организме.
- После 4х месяцев, если ребеночек вскармливается только грудью, ему необходимы препараты железа в дозировке 1 мг/кг в день, из-за малого содержания железа в материнском молоке — до введения прикорма.
- Для детишек на смешанном вскармливании — рекомендации аналогичны.
- Детишки, вскармливающиеся адаптированными молочными смесями получают с пищей достаточно железа и дополнительного назначения им железосодержащих лекарств не требуется.
- Цельное коровье молоко не рекомендуется давать детишкам до года.
- Детишкам от 6-12 мес требуется 11 мг железа ежедневно, его они должны получить с питанием. В прикорм нужно включать красное мясо и овощи богатые железом.
- Дети 1-3 лет нуждаются в 7 мг железа в день, в их рационе обязательно должно быть красное мясо, овощи, богатые железом и фрукты, богатые аскорбиновой кислотой.
- Все дети, родившиеся до срока, находящиеся на грудном или смешанном вскармливании, требуют назначения им железосодержащих лекарств в дозах не меньше 2 мг/ кг в день с 1 месяца жизни до введения прикорма.
- А недоношенных и маловесных детишек, вскармливающихся искусственно нужно кормить обогащенными железом молочными смесями.
- Дети из социально-неблагополучных семей, семей с низким доходом.
- Недоношенные дети или дети с низким весом при рождении.
- Дети, которых кормят только грудью после 4-месячного возраста без прикорма или приема ребенком препаратов железа.
- Дети, которых кормят до года цельным коровьим молоком или пищей бедной железом.
- Недостаточность питания, задержка роста и веса.
- Увеличенные потребности в железе, обусловленные состоянием организма.
Диспансерное наблюдение за детьми и подростками с ЖДА осуществляется в нашей стране на протяжении 1-го года со дня постановки диагноза.
Проводится контроль самочувствия и общего состояния ребенка. Общий анализ крови контролируется ежемесячно, после нормализации показателей — 1 раз в 3 месяца. Перед снятием ребена с диспансерного учета назначают общий анализ крови, который должен быть нормальным
Проф. прививки деткам с ЖДА разрешены. Для их проведения не требуется нормализация уровня Hb. Проф прививки детей с нетяжелыми анемиями проводятся по календарю т.к. число иммунных клеток у таких детей достаточное.
Это всё про анемия у детей. Желаю Вам здоровья!
источник

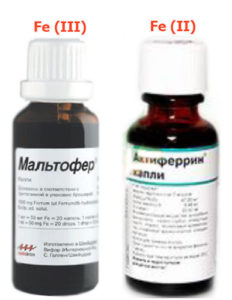 Железодефицитная анемия у детей Лекарства для приёма внутрь
Железодефицитная анемия у детей Лекарства для приёма внутрь