Суточная потребность в витамине В12 составляет 3-5 мкг, а запасы данного витамина в печени настолько велики, что даже при прекращении поступления кобаламина в организм признаки его дефицита появятся не ранее, чем через 2-3 года. Тем не менее, диета играет определенную роль в процессе лечения заболевания, особенно когда запасы витаминов В12 в организме снижаются.
Причинами снижения запасов витамина В12 в организме могут быть:
Заболевания печени. Такие заболевания, как цирроз и рак печени, приводят к уменьшению количества нормальных клеток органа, и замещению их соединительной тканью, которая неспособна депонировать витамин В12. В результате запасы данного витамина в организме снижаются, а при нарушении его поступления признаки заболевания могут появляться в более ранние сроки.
Беременность. В данном случае матери необходимо обеспечивать витамином В12 не только свой, но и быстро развивающийся организм ребенка, поэтому суточная потребность в витамине В12 может увеличиваться на 50%, а в случае многоплодной беременности – еще больше. В нормальных условиях (при отсутствии заболеваний печени) запасов кобаламина в организме достаточно, чтобы покрыть потребности матери и плода в данном веществе. Однако при частых беременностях запасы кобаламина могут истощаться, особенно если у матери имеются какие-либо заболевания печени, поэтому беременным женщинам особенно важно потреблять достаточное количество этого витамина с пищей.
Пациентам необходимо обязательно питаться правильно и сбалансировано, чтобы в меню находилось достаточное количество витаминных и минеральных веществ, а также белков. Желательно отказаться от продуктов, способных раздражать слизистые оболочки органов желудочно-кишечного тракта. Крайне важную роль играет отказ от потребления алкоголя и от самых разных вредных продуктов. Пациентам показано еще и ограничение потребления жиров.
Диета предполагает, что в рационе должно присутствовать много продуктов, богатых витамином В12. К таковым в первую очередь относятся субпродукты, представленные говяжьей, свиной и куриной печенью, а также сердцем, почками и пр. Необходимо обязательно включить в свой рацион рыбу и морепродукты, разные виды мяса, к примеру, крольчатину, говядину, баранину и свинину. Также стоит есть еще и яичный желток, и разные сыры, и кисломолочные продукты.
Содержание витамина В12 в некоторых продуктах питания
Печень говяжья — 60 мкг
Печень свиная — 30 мкг
Печень куриная — 16 мкг
Скумбрия -12 мкг
Мясо кролика — 4,3 мкг
Говядина — 2,6 мкг
Морской окунь — 2,4 мкг
Свинина — 2 мкг
Треска — 1,6 мкг
Карп — 1,5 мкг
Куриное яйцо — 0,5 мкг
Сметана — до 0,4 мкг
Полезные продукты при анемии
— мясо, сливки, масло – содержат аминокислоты, белки;
— свекла, морковь, фасоль, горох, чечевица, кукуруза, помидоры, рыба, печень, овсяная каша, абрикосы, пивные и пекарские дрожжи – содержат необходимые для процесса кроветворения микроэлементы;
— зеленые овощи, салаты и зелень, зерновые завтраки – содержат достаточное количество фолиевой кислоты;
— вода из минеральных источников с слабоминерализованным железосульфатно-гидрокарбонатномагниевым составом вод, что способствует всасыванию железа в ионизированной форме организмом;
— дополнительно обогащенные железом пищевые продукты (кондитерские изделия, хлеб, детское питание и т. д.);
— мед – способствует усвояемости железа;
— сок сливы – содержит до 3 мг железа в одном стакане.
Кроме этого, рекомендуется употребление земляники, малины, винограда, бананов, орехов, лука, чеснока, сока яблок, ананаса, айвы, абрикоса, вишни, калины, березы.
Кабачки, патиссоны, салат, помидоры, сок с них в соединении с соком моркови, картошки содержит необходимые для лечения анемии элементы.
Опасные и вредные продукты при анемии
Следует ограничить употребление жиров, молока, мучных сдобных изделий, чая, кофе, кока-колы
Исключить из рациона блюда, которые содержат рассол и уксус (они разрушительно влияют на кровь).
Опасным для здоровья и жизни есть употребление алкоголя при анемии (особенно крепких напитков и суррогатных заменителей). Спиртные напитки способствуют патологическим процессам при течении анемии, возникновению осложнений в виде синдрома нарушения свертываемости крови.
Цель назначения: улучшить состояние питания организма, повысить его защитные силы, усилить восстановительные процессы в пораженном органе.
Общая характеристика: диета повышенной энергоценности с преимущественным увеличением содержания белков, особенно молочных, витаминов, минеральных веществ (кальций, железо и др.), умеренным увеличением количества жиров и углеводов.
Кулинарная обработка и температура пищи обычные.
Химический состав и энергоценность: белки – 110–130 г (60 % животные), жиры – 100–120 г (20–25 % растительные), углеводы – 400–450 г; энергетическая ценность 12,6–14,2 МДж (3000–3400 ккал); натрия хлорид – 15 г, свободная жидкость – 1,5 л.
Режим питания: 5 раз в день.
Рекомендуемые продукты и блюда .
1. Пшеничный и ржаной хлеб и различные мучные изделия (пирожки печеные, бисквиты, сдоба и др.).
3. Различные виды мяса, птицы и рыбы, исключая очень жирные, в любой кулинарной обработке. Печень, мясопродукты (колбаса, ветчина, сосиски), рыбопродукты (сельди, балыки, икра, консервы – шпроты, сардины и др.); нерыбные морепродукты.
4. Молочные продукты в полном ассортименте с обязательным включением творога и сыра.
5. Яйца – в разном приготовлении.
6. Жиры: сливочное, растительное масла в натуральном виде, топленое – для приготовления блюд.
7. Разная крупа (особенно гречневая, овсяная), макаронные изделия. Бобовые, хорошо разваренные, в виде пюре.
8. Овощи, фрукты, ягоды – в любой кулинарной обработке, но частью обязательно сырые.
9. Различные закуски, особенно лиственные и овощные салаты.
10. Соусы – мясной красный, молочный бешамель, сметанный, молочно-яичный и др.
11. Пряности – в умеренном количестве.
12. Различные сладкие блюда, мед, варенье и др.
13. Напитки – любые, обязательно овощные и фруктовые соки, отвар шиповника и пшеничных отрубей.
Исключают: очень жирные сорта мяса и птицы, бараний, говяжий и кулинарные жиры; острые и жирные соусы, торты и пирожные с большим количеством крема.
• 1-й завтрак: салат из свежей капусты с яблоками со сметаной, омлет, каша овсяная молочная, чай с молоком;
• 2-й завтрак: сыр, чай;
• обед: борщ на мясном бульоне со сметаной, курица жареная с отварным рисом, компот;
• полдник: отвар шиповника;
• ужин: зразы мясные, фаршированные луком и яйцом, морковное пюре, запеканка из гречневой крупы с творогом, чай;
• на ночь: кефир.
источник
Если анализы крови показывают низкий гемоглобин, появились слабость и одышка, скорее всего, у вас анемия. А вот какая — железодефицитная или дефицитная по витамину В12 — должен выяснить врач по результатам обследований. Чем отличаются две разные анемии и почему не стоит самостоятельно пить препараты железа, рассказывает кардиолог Антон Родионов.
Что делать, если по результатам анализов выявлена железодефицитная анемия?
Лечить! Здесь надо запомнить очень важную вещь: если анемия уже развилась, то в организме есть тяжелый дефицит железа, и только изменением диеты восполнить этот железодефицит невозможно. Обязательно нужно обратиться к врачу и принимать лекарственные препараты железа.
Выбрать конкретный препарат вам поможет врач. В большинстве случаев достаточно приема препарата в таблетках. При тяжелой анемии, хронических воспалительных заболеваниях или плохой переносимости препараты железа вводят внутривенно. А вот внутримышечно препараты железа вводить нежелательно, вероятность осложнений такого лечения весьма высока, от этого метода введения в мире уже отказываются.
И еще одно очень важное соображение по поводу лечения. Принимать препараты железа нужно не просто до нормализации гемоглобина, а еще хотя бы два месяца дополнительно, чтобы пополнить тканевые запасы.
Но иногда препараты железа плохо переносятся!
Действительно, иногда препараты железы приводят к развитию побочных эффектов со стороны желудочно-кишечного тракта (запоры или понос, тошнота, боль в животе, металлический привкус во рту).
Если у вас наблюдаются подобные побочные эффекты, не нужно прекращать прием препаратов. Обратитесь к своему врачу, возможно, он порекомендует уменьшить дозу препарата или поменять препарат.
Важно знать, что препараты железа могут окрашивать стул в черный цвет, в данном случае это не признак желудочно-кишечного кровотечения, а нормальная реакция кишечного содержимого на взаимодействие с железом.
Как питаться при железодефицитной анемии?
Еще раз напомню, что если анемия уже есть, то диета — не основное лечение, а дополнение к таблеткам. Только диета — это для тех, у кого анемии еще нет, но есть факторы риска. Итак, смотрим, в каких продуктах много железа, а в каких совсем мало.
Содержание железа в продуктах
Впрочем, не надо думать, что орехи и овсянка могут полностью заменить мясо. Дело в том, что здесь указано абсолютное содержание железа в продуктах, но всасывается оно далеко не полностью. Например, из мяса всасывается около 20% железа, а из растительных продуктов — только 5–10%.
И наконец, обратите внимание, что красный цвет продуктов совершенно не гарантирует высокого содержание железа. До слез умиляет желание накормить человека, сдавшего кровь на донорском пункте, свекольным салатом, гранатом и напоить красным вином со словами: «Тебе надо гемоглобин восстанавливать». Нет в этих продуктах железа, почти совсем нет.
Можно ли полечиться от анемии самостоятельно? Лекарства же в аптеке свободно продаются.
Нежелательно. Лечение анемии в жизни может оказаться не самым простым занятием, а в статье я не могу описать всех нюансов диагностики и сложностей в лечении. Не говоря уж о том, что мало просто принимать препараты железа — надо понять причину анемии и как-то попытаться на нее воздействовать.
А теперь — о самом интересном, о чем не знают даже многие врачи. Поговорим о дефиците железа без анемии.
Вы уже помните, что железо в организме нужно не только для того, чтобы участвовать в образовании гемоглобина. В частности, железо служит вспомогательным элементом (коферментом) в процессе образования эпителиальных тканей.
Но организм полагает, что все же главная функция железа состоит в транспортировке кислорода, поэтому, когда общий уровень железа в организме снижается, то гемоглобин берет его «в долг» из тканей. Создается ситуация, когда анемии еще нет (гемоглобин нормальный), а в тканях железа мало.
Клинически это проявляется так:
- Повышенная утомляемость
- Частые простуды, боли в горле
- Субфебрилитет (постоянная температура 37,1–37,4 °С)
- Выпадение волос и ломкость ногтей
- Извращение аппетита (хочется есть мел, землю, лед)
- Синдром беспокойных ног (ощущение дискомфорта в ногах, особенно в ночные часы)
Нередко такие пациенты годами ходят по врачам, сдают тысячи ненужных анализов, главным образом, «на иммунитет», принимают тонны иммуномодуляторов, витаминов и разных «улучшайзеров» без всякого эффекта, а надо всего-то сделать анализы на железо и ферритин и восполнить тканевые запасы железа. Значимым считают снижение уровня ферритина —>
Какая еще анемия бывает?
Мы поговорили о железодефицитной анемии, на долю которой приходится подавляющее большинство всех случаев снижения гемоглобина, но есть и другие формы анемии, которые лечат совершенно по-другому. Именно поэтому до установления причины анемии просто так вслепую пить таблетки нельзя. Более того, поспешное лечение может «смазать картину» и впоследствии затруднить постановку правильного диагноза.
Если в анализе крови помимо низкого гемоглобина, снижения уровня эритроцитов и гематокрита мы видим повышение цветового показателя (>1,05) или увеличение среднего количества гемоглобина в эритроците и объема эритроцита (MCH и MCV), то, скорее всего, речь идет об анемии, связанной с дефицитом витамина В12. Этот витамин необходим для созревания эритроцитов, его недостаток приводит к появлению крупных клеток крови, которые достаточно быстро разрушаются.
Причин дефицита В12 довольно много — это прежде всего различные заболевания желудочно-кишечного тракта, начиная с атрофического гастрита, заканчивая перенесенными операциями на желудке и кишечнике, но самая частая причина — это выработка антител, которые нарушают всасывание этого витамина в желудке. У людей старшего возраста эта болезнь развивается довольно часто.
Какие бывают симптомы В12-дефицитной анемии?
Помимо симптомов собственно анемии при В12-дефицитной анемии нередко развивается поражение нервной системы. Появляется покалывание в кистях рук и стопах, снижается чувствительность в ногах и руках, возникают спазмы мышц, мышечная слабость, «мышечная медлительность» (пациенты описывают это так: «Хочу сделать шаг, а нога выполняет его с задержкой на пару секунд. «).
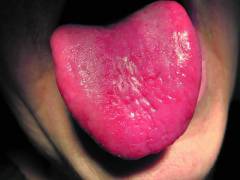
Иногда развивается воспаление языка, проявляющееся чувством жжения и увеличением его размеров, дискомфортом в горле. Это состояние часто путают с фарингитом, рефлюксной болезнью, в результате чего больные безуспешно лечатся у отоларингологов и гастроэнтерологов.
Какие анализы надо сдавать для подтверждения В12-дефицитной анемии?
Помимо клинического анализа крови нужно сдать кровь на витамин В12 (цианокобаламин) и гомоцистеин. При этом заболевании уровень В12 будет значительно снижен, а гомоцистеин, наоборот, повышен. Кроме того, в общем анализе крови может снижаться уровень лейкоцитов и тромбоцитов.
Как лечить В12-дефицитную анемию?
Если в лечении железодефицитной анемии еще иногда допустима какая-то самодеятельность, то дефицит В12 — дело очень серьезное, и лечить такую анемию может только врач.
Для восполнения недостатка витамина его вводят в инъекциях, сначала ежедневно, затем раз в неделю, потом, после стабилизации состояния, один раз в месяц. К сожалению, в России препараты В12 в таблетках отсутствуют. Имеющиеся в аптеках поливитамины или комплексы, в состав которых входят витамины группы В, категорически не подходят для лечения.
Как правило, причину дефицита В12 раз и навсегда устранить не удается, поэтому лечение должно быть пожизненным. Нельзя бросать лечение при нормализации гемоглобина, в этом случае через несколько месяцев все вернется назад.
Можно ли профилактически принимать витамины группы В для того, чтобы не было анемии?
Здоровому человеку — не нужно и бессмысленно. Дело в том, что витамин В12 в инъекциях — это серьезный лекарственный препарат, который можно использовать строго по показаниям. А безрецептурные поливитамины из аптеки с витаминами В — это почти пустышки.
А еще есть другие, более редкие формы анемии, разобраться в которых под силу только специалисту-гематологу. Поэтому не занимайтесь, пожалуйста, самодеятельностью и в случае серьезных отклонений в анализах ступайте к врачу.
А если гемоглобин высокий, что делать?
Высокий гемоглобин — визитная карточка спортсменов и курильщиков. В этих случаях он может доходить до 180 г/л и даже немного выше. С этим делать ничего не надо, разве что курильщикам надо бросить курить.
А вот если у вас ни с того ни с сего уровень гемоглобина составляет 200 г/л и более, это серьезный повод для обращения к гематологу.
источник
Раньше B12-дефицитную анемию (болезнь Аддисона – Бирмера) называли злокачественным малокровием или пернициозной анемией. Первым, кто заявил о существовании такой болезни и описал данный вариант, был врач из Англии Томас Аддисон, и произошло это еще в 1855 году. Позже немец Антон Бирмер сообщил о заболевании в более подробной форме, но случилось это лишь 17 лет спустя (1872). Однако ученый мир признал первенство за Аддисоном, поэтому по предложению французского врача Армана Труссо, патология стала называться именем автора, то есть, болезнью Аддисона.
Прорыв в изучении этого тяжелого недуга случился уже в 20 годах прошлого века, когда американские врачи Джордж Уипл, Уильям Мёрфи и Джордж Майнот на основе своих исследований заявили, что недуг поддается лечению, если в рационе больного будет присутствовать сырая печень. Они доказали, что В12-дефицитная анемия – врожденная несостоятельность желудка в выделении веществ, обеспечивающих всасывание витамина B12, за что в 1934 году были награждены Нобелевской премией по физиологии и медицине.
В настоящее время мегалобластную анемию, связанную с недостатком цианокобаламина (витамина В12), мы знаем, как В12-дефицитную анемию, а комбинированную форму, обусловленную дефицитом и витамина B12, и фолиевой кислоты (витамина B9), как В12-фолиеводефицитную анемию.
Как отмечено выше, В12-дефицитная и В12-фолиеводефицитная анемии входят в группу мегалобластных анемий, для которых характерно снижение продукции ДНК, что, в свою очередь, влечет нарушение пролиферации клеток, способных к быстрому делению. Это – клетки:
- Костного мозга;
- Кожных покровов;
- Слизистых оболочек;
- Желудочно-кишечного тракта.
Среди всех быстропролиферирующих клеток, гемопоэтические (кроветворные) проявляют наибольшую склонность к ускоренному размножению, поэтому симптомы малокровия стоят в числе первых клинических проявлений данных мегалобластных анемий. Нередки случаи, когда, помимо анемии (снижение уровня эритроцитов и гемоглобина), наблюдаются другие признаки гематологической патологии, например, уменьшение количества кровяных пластинок – тромбоцитов (тромбоцитопения), нейтрофильных лейкоцитов (нейтропения, агранулоцитоз), а также моноцитов и ретикулоцитов.
кровь при B12-дефицитной анемии
Почему эти варианты малокровия так взаимосвязаны и в чем их разница? Дело в том, что:
- Присутствие и непосредственное участие витамина В12 весьма необходимо для образования активной формы фолиевой кислоты, которая, в свою очередь, очень нужна для продукции тимидина – важного компонента ДНК. Данное биохимическое взаимодействие при участии всех необходимых факторов позволяет в полной мере обеспечить нормальное образование клеток крови и клеток ЖКТ (желудочно-кишечный тракт);
- На витамин В12 возложены и другие задачи – при его участии распадаются и синтезируются отдельные жирные кислоты (ЖК). При недостаточном содержании цианокобаламина данный процесс нарушается, и в организме начинает накапливаться вредная, убивающая нейроны, метилмалоновая кислота, а вместе с этим снижается продукция миелина – вещества, которое образует миелиновую оболочку, несущую электроизолирующую функцию для нервных клеток.
Что касается фолиевой кислоты, то распад ЖК в ее участии не нуждается и при ее недостатке нервная система не страдает. Мало того – если пациенту, имеющему дефицит В12 в качестве лечения прописать фолиевую кислоту, то непродолжительное время она будет стимулировать эритропоэз, но лишь до тех пор, пока она не окажется в избытке. Излишнее количество препарата заставит работать весь присутствующий в организме В12, то есть, даже тот, который был предназначен для обеспечения распада ЖК. Безусловно, к добру такая ситуация не приводит – еще больше поражаются нервные ткани, развиваются глубокие дегенеративные изменения спинного мозга с потерей двигательных и чувствительных функций (комбинированный склероз, фуникулярный миелоз).
Таким образом, недостаток витамина В12, наряду с нарушением пролиферации кроветворных клеток и развитием анемии, оказывает негативное воздействие на нервную систему (НС), в то время, как дефицит фолиевой кислоты влияет лишь на деление гемопоэтических клеток, но на здоровье нервной системы не отражается.
Цианокобаламин из продуктов питания, попавших в ЖКТ, всасывается с помощью так называемого, внутреннего фактора (ВФ). Вот как это происходит:
- В желудке В12 всасываться с внутренним фактором, как считали раньше, не спешит, он находит протеин-R и соединяется с ним, чтобы в виде комплекса «Vit B12 + protein-R» направиться в 12-перстную кишку и уже там, под воздействием протеолитических ферментов, расщепиться;
- В 12-перстной кишке цианокобаламин освобождается от протеина-R и в свободном состоянии встречается с прибывшим туда внутренним фактором, вступает с ним во взаимодействие и образует другой комплекс – «Vit B12 + ВФ»;
- Комплекс «Vit B12 + ВФ» направляется в тощую кишку, находит рецепторы, предназначенные для внутреннего фактора, соединяется с ними и всасывается;
- После всасывания цианокобаламин «садится» на транспортный белок транскобаламин II, который доставит его в места основной деятельности или в депо для создания запаса (костный мозг, печень).
Очевидно, почему такое большое значение уделяется внутреннему фактору, ведь если с ним все в порядке, то почти весь цианокобаламин, поступивший с пищей, благополучно попадет по месту назначения. В противном случае (при отсутствии ВФ) – только 1% витамина В12 методом диффузии просочиться сквозь кишечную стенку и тогда человек не получит нужного ему количества такого важного витамина.
Суточная потребность организма в цианокобаламине составляет от 3 до 5 мкг, а в запасе его находится от 4 до 5 граммов, стало быть, можно подсчитать, что, если полностью исключить поступление витамина В12 (например, при гастрэктомии), то запасы иссякнут через 3-4 года. А вообще, запас витамина B12 рассчитан на 4-6 лет, в то время как фолиевая кислота при отсутствии поступления исчезнет через 3-4 месяца. Отсюда можно сделать вывод, что дефицит В12 при беременности не грозит, если до того его уровень был в норме, а вот фолиевая кислота, если женщина не употребляла сырых фруктов и овощей, вполне способна упасть ниже допустимого предела и создать дефицитное состояние (развитие фолиеводефицитной анемии).
Витамин В12 содержится в продуктах животного происхождения, фолиевая кислота – почти во всех продуктах питания, однако цианокобаламин замечательно переносит термическую обработку в течение длительного времени и сохраняется для поступления в организм, чего нельзя сказать о фолиевой кислоте – после 15-минутного кипячения от этого витамина не останется и следа…
Недостаток цианокобаламина может быть вызван следующими причинами:
- Низким поступлением с пищей витамина В12 (когда человек по собственной инициативе или в силу других причин недополучает продукты, несущие организму цианокобаламин: мясо, печень, яйца, молочные продукты), либо полным переходом на вегетарианство (в пище растительного происхождения витамин В12 трудно найти);
- Нарушением секреции внутреннего фактора, обусловленным атрофией слизистой, которая формируется по причине наследственной предрасположенности, воздействия токсических веществ, влияния антител и развития атрофического гастрита в результате этого. Подобные последствия подстерегают пациента в случае полного удаления желудка (гастрэктомия), в то время как потеря только части органа оставляет секрецию нетронутой;
- Отсутствием рецепторов, в которых нуждается внутренний фактор с целью своего связывания, что происходит при поражающей все отделы ЖКТ болезни Крона, дивертикулах и опухолях тонкой кишки, туберкулезе и резекции подвздошной кишки, кишечном инфантилизме (целиакии), хроническом энтерите;
- Конкурентным поглощением цианокобаламина в ЖКТ гельминтами или микроорганизмами, которые интенсивно размножаются после наложения анастомозов;
- Расстройством внешнесекреторной функции поджелудочной железы и следствием этого – нарушением расщепления протеина-R, что препятствует связыванию витамина В12 с внутренним фактором;
- Довольно редкой, полученной по наследству, аномалией – понижением уровня транскобаламина и нарушением перемещения цианокобаламина в костный мозг.
С витамином В9 все намного проще: он содержится почти во всех продуктах, замечательно всасывается в здоровом кишечнике и не испытывает нужды ни в каком внутреннем факторе. А проблемы возникают, если:
- Рацион в силу разных обстоятельств пациента крайне скуден;
- Человек, страдающий нервной анорексией, преднамеренно отказывается от еды;
- Возраст пациента расценивается, как пожилой;
- Алкоголик «трясется» от абстинентного синдрома при длительном запое (не до полноценной еды – она не лезет);
- Имеет место синдром нарушенного кишечного всасывания (заболевания ЖКТ: болезнь Крона, целиакия, опухоли кишечника и др.) – основная причина В12-фолиеводефицитной анемии;
- Увеличивается потребность в фолиевой кислоте, что бывает при беременности, некоторых кожных заболеваниях (псориаз, дерматит), нарушении утилизации (алкоголизм, врожденные болезни обмена фолатов).
Кстати, недостаток витамина В9 не так уж редко наблюдается у людей, которые вынуждены длительно принимать противосудорожные препараты, в том числе, фенобарбитал, поэтому данный факт следует учитывать при назначении подобной терапии.
Коль описываемые состояния относят к анемиям, то, само собой разумеется, что для них будут характерны все симптомы малокровия:
- Быстрое наступление усталости даже при минимальной физической активности, слабость, снижение работоспособности;
- Эпизоды потемнения в глазах;
- Склонность к гипотонии (снижение артериального давления);
- Нарушение дыхания (желание ускорить шаг или другие движения вызывают одышку);
- Периодические головные боли, часто кружится голова;
- Нередко отмечается нарушение ритма (тахикардия);
- Кожные покровы бледные, отдают легкой желтизной (субиктеричность);
- В полости рта развиваются проблемы с характерными для глоссита признаками: сосочки атрофированы, поверхность языка – лакированная, язык распухает и болит;
- Возможно увеличение печени и селезенки;
- Отечность нижних конечностей;
- Частый стул, который, впрочем, может чередоваться с запорами;
- Заметное снижение аппетита и, соответственно, веса.
Ввиду того, что при недостатке цианокобаламина имеет место триада синдромов (поражения крови, ЖКТ и нервной системы), а при дефиците фолиевой кислоты страдания нервной системы не отмечаются, следующие симптомы, свидетельствующие о вовлечении в патологический процесс нервной системы, будет относиться только к В12-дефицитному состоянию:
- Фуникулярный миелоз (дегенеративная патология спинного мозга), который по выраженности не коррелирует с клиническими проявлениями анемии;
- Периферическая полинейропатия с мышечной слабостью, расстройством чувствительности и снижением сухожильных рефлексов;
- В иных случаях на почве анемии наблюдаются депрессивные состояния, нарушение памяти, редко – психические расстройства.
Следует отметить, что В12- и фолиеводефицитные состояния быстро прогрессирующим течением не отличаются и на симптомы не особо богаты. Заболевания до недавнего времени были отнесены к патологии преклонного возраста, правда, в последние годы наметилась тенденция к «омоложению» – такого рода анемии стали встречаться у молодых людей.
Клинически проявляющаяся иктеричность склер и желтушность кожи – признаки, которые дают основание незамедлительно отправить пациента в лабораторию, где и начинается диагностика фолиево- и В12-дефицитных состояний.
Первый этап лабораторных исследований заставляет заподозрить мегалобластную анемию:
- Общий анализ крови (ОАК) – типичный для подобных состояний: пониженный уровень эритроцитов и гемоглобина, тромбоцитопения, нейтропения с полисегментированностью, ЦП обычно выше 1, макроцитоз, пойкилоцитоз, анизоцитоз, в эритроцитах – тельца Жолли, кольца Кебота;
- Повышенные значения билирубина за счет несвязанной фракции в биохимическом анализе крови (БАК).
Учитывая, что похожую картину периферической крови может давать другая гематологическая патология (гипопластические и апластические состояния, гемолитическая анемия, лейкоз), больному в обязательном порядке назначают пункцию спинного мозга, в котором находят мегалобласты (характерный признак В12-дефицитной анемии), гигантских размеров мегакариоциты и клетки гранулоцитарного ряда.
Как правило, после лабораторных тестов (или параллельно с ними) пациента ждет «страшная процедура» – фиброгастроскопия (ФГС), по данным которой видно, что слизистая оболочка желудка атрофирована.
Между тем, дальнейшая диагностика В12-дефицитной анемии требует ее отмежевания от малокровия, связанного с недостатком витамина В9. Очень важно тщательно собрать анамнез пациента: изучить его образ жизни и питания, досконально выявить симптомы, исследовать состояние сердечно-сосудистой и нервной системы, но уточнение диагноза все же требует лабораторных исследований. И здесь следует отметить, что в любом случае дифференциальная диагностика этих двух анемий сложна для обычных лабораторий, ведь создается необходимость определения количественных значений витаминов, однако:
- Микробиологический метод далек от совершенства и дает только приблизительные результаты;
- Радиоиммунологические исследования недоступны жителям деревень и маленьких городов, поскольку проведение анализа требует участия современного оборудования и высокочувствительных реагентов, которые являются привилегией больших городов.
В таком случае для дифференциальной диагностики был бы полезен анализ мочи, определяющий в ней количество метилмалоновой кислоты: при В12-дефицитной анемии ее содержание заметно увеличивается, тогда как при фолиеводефицитном состоянии уровень остается неизменным.
Лечение недостатка фолиевой кислоты преимущественно ограничивается назначением таблетированных форм витамина В9 в дозе 5-15 мг/сутки. Правда, если диагноз фолиеводефицитной анемии все же остается под вопросом, то целесообразно начать лечение с внутримышечного введения цианокобаламина. Однако наоборот – нельзя, ведь при В12-дефицитной анемии применение фолиевой кислоты еще больше усугубит ситуацию.
Что касается лечения В12-дефицитной анемии, то оно основано на трех принципах:
- В полной мере насытить организм цианокобаламином, чтобы и на выполнение функциональных обязанностей хватило и в запас отложилось;
- За счет поддерживающих доз постоянно пополнять запасы;
- По возможности стараться не допустить развития анемического состояния.
Само собой разумеется, что главным в лечении недостатка В12 будет назначение цианокобаламина с учетом изменений со стороны крови и выраженности неврологической симптоматики, если она имеет место.
- Обычно лечение начинается с внутримышечного введения цианокобаламина в дозе 500 мкг каждый день и оксикобаламина – 1000 мкг через день;
- Если имеет место выраженные симптомы поражения нервной системы (фуникулярный миелоз), то доза В12 увеличивается до 1000 мкг (каждый день), а, кроме этого, добавляется по 500 мкг аденозилкобаламина в таблетках, который в обмене участие принимает, но на кроветворение не влияет;
- Появление в анализе крови гипохромии красных клеток крови на фоне лечебных мероприятий или в случае смешанных форм болезни (В12- + железодефицитная анемия) является основанием для назначения препаратов железа;
- К переливанию эритроцитной массы прибегают в особых случаях: если явно обозначились признаки кислородного голодания головного мозга и симптомы анемической энцефалопатии, имеет место прогрессирующая сердечная недостаточность и при подозрении на развитие анемической комы – очень опасного для жизни пациента состояния;
- Одновременно назначается терапевтическое воздействие на факторы, которые, возможно, стали причиной дефицита витамина В12, с такой целью проводится: дегельминтизация (препараты и дозы зависят от вида гельминтов), лечение заболеваний желудочно-кишечного тракта, хирургическая операция при раке желудка, нормализация кишечной флоры, разрабатывается диета, предусматривающая достаточное поступление витамина B12 в организм.
Буквально через несколько дней от начала терапии производится контрольный подсчет ретикулоцитов – ретикулоцитарный криз будет свидетельством, что тактика лечения выбрана правильно.
После того, как состояние крови будет признано нормальным, пациента переводят на поддерживающую терапию: сначала каждую неделю, а потом каждый месяц больному вводят 500 мкг В12, а, кроме этого, раз в полгода назначают 2-3 недельный курс витаминотерапии (поддерживающее лечение витамином В12).
источник
Анемия – это клинико-гематологический синдром или заболевание, для которого характерно уменьшение уровня гемоглобина и (или) эритроцитов в единице объема крови. Эксперты ВОЗ определили критерием анемии для женщин уровень гемоглобина 120 г/л и менее (121–145 г/л в норме), для мужчин – 130 г/л и менее (131–164 г/л в норме).
Дефицит железа является серьезной медико-социальной проблемой во всех странах. Наиболее подверженные дефициту железа группы населения (дети, подростки, беременные и женщины детородного возраста) определяют будущее каждой страны.
В России распространенность железодефицитной анемии(ЖДА) колеблется от 12 до 18 %, но среди женщин этот показатель может достигать 20-40 % и более (М.И. Лосева, Т.И. Поспелова, 2002).
ЖДА относится к группе анемий, возникающих в результате дефицитного эритропоэза, чаще всего при потере крови или недостаточном поступлении и всасывании железа.
Главной функцией железа является перенос кислорода к тканям. Помимо этого железо участвует в пролиферации клетки, продукции и уничтожении кислородных радикалов (антиоксидантная функция). Недостаток этого микроэлемента ведет к уменьшению умственных и познавательных способностей, предрасполагает к частым инфекциям (М.И. Лосева, 1988; Dallman, 1987;Wacter, 1989).
Обмен железа в организме представляет собой четко организованный процесс. Все освободившееся при распаде гемоглобина и железосодержащих ферментов железо утилизируется. Потери железа с калом, мочой, волосами, слущенным эпителием кожи и слизистой пищеварительного тракта составляют 1 мг/сут. Восполняются потери железа из пищи, при этом 1 мг/сут покрывает потребности взрослого человека, 1,5-2 мг – женщины репродуктивного возраста и 3 мг – беременной женщины и в период лактации.
Большую часть всасывающегося железа составляет гемовое железо гемоглобина и миоглобина, которое находится в мясе, рыбе, печени, яйцах. В этих продуктах доля усвояемого железа составляет 10-20 %. Негемовое железо содержится в продуктах растительного происхождения и оно менее доступно (доля усвояемого железа – 6 %).
Основное место всасывания железа – двенадцатиперстная кишка и начальные отделы тощей кишки. После всасывания железо связывается с транспортным белком трансферрином, который доставляет железо к эритрокариоцитам костного мозга, ретикулоэндотелиальным клеткам и во все ткани организма для синтеза ферментов – цитохромоксидаз. Железо попадает в митохондрии, где происходит синтез гема из железа и протопорфирина. В эритрокариоцитах синтезируется ферритин, который необходим для удаления из клетки избытка железа, не вошедшего в гемоглобин, и его депонирования. Больше всего ферритина в эритробластах, базофильных нормоцитах и в макрофагах.
Частые, даже небольшие кровопотери (кровотечения из ЖКТ, носовые кровотечения, маточные кровотечения, почечные кровотечения и т.д.).
Нарушение всасывания железа при патологии ЖКТ (резецированный желудок, хронический панкреатит, язвенная болезнь, гастрит, язвенный колит, резекция тонкого кишечника).
Недостаточное поступление железа с пищей при условии общего дефицита питательных веществ, дефицита в рационе мяса, рыбы, растительных продуктов.
Повышенная потребность в железе: период беременности, лактации, активное занятие спортом, быстрый рост организма.
Нарушение реутилизации железа при разрушении эритроцитов.
Анкилостомидоз (глистная инвазия анкилостомой).
Использование препаратов, тормозящих всасывание железа (антациды, препараты кальция, крепкие напитки – чай, кофе, свежие молокопродукты).
Патология печени (хронический гепатит, цирроз), ахлоргидрия, дисбактериоз кишечника.
Нарушение синтеза транспортного белка – трансферритина (наследственное или приобретенное заболевание с нарушением белковообразовательной функции печени).
Врожденный дефицит железа.
При длительном лечении эритропоэтином: с увеличением эритропоэза возрастает потребность в железе.
Анемический синдром, обусловленный гемической гипок-сией: бледность кожных покровов и слизистых, быстрая утомляемость, слабость, сонливость, одышка при физической нагрузке. Головокружение и потемнение в глазах, головные боли и сниженная работоспособность. Усиление болей в сердце при патологии сердца.
Сидеропенический синдром вследствие тканевого дефицита железа: ломкость волос, ногтей, исчерченность ногтей, койлонихии, сухость кожи, извращение вкуса (pica chlorotica), проявляющееся в непреодолимом желании есть малосъедобные вещи: мел, глину, песок, зубной порошок, сырое тесто и т.п. Пристрастие к необычным запахам: бензина, керосина, газетной бумаги, ацетона, лаков и др. Атрофия слизистой языка, пищевода (сухость во рту, разрушение зубов, глоссит, афтозный стоматит).
Висцеральный синдром – структурные и функциональные изменения различных органов. Со стороны ЖКТ – субатрофический и атрофический гастрит, эрозивно-язвенные поражения, дисфагия, синдром раздраженного кишечника; со стороны сердечно-сосудистой системы: склонность к артериальной гипертонии, НЦД, анемическая миокардиодистрофия; со стороны ЦНС: гипоксическая энцефалопатия (снижение памяти, нарушение сна). Задержка полового и физического развития.
Синдром вторичного иммунодефицита: частые аденовирусные инфекции, хронизация воспалительных процессов; глубокая и стойкая депрессия продукции интерферонов лейкоцитами, снижение IgА (в 1,3 раза) иIgМ.
Лабораторная диагностика. Характерно снижение гемоглобина до 120 г/л и менее у женщин и до 130 г/л и менее у мужчин. Цветовой показатель всегда снижен до 0,8-0,6 (в норме 0,86-1,05). В мазке крови выявляются гипохромные эритроциты со склонностью к микроцитозу, анизоцитозу и пойкилоцитозу. Уровень ретикулоцитов чаще нормален или снижен, редко наблюдается повышение до 2-5 % в первое время после значительной кровопотери. Наблюдается тенденция к лейкопении.
Пунктат костного мозга, как правило, не изменен.
Содержание сывороточного железа (СЖ) по сравнению с нормой (12,5-30,4 мкмоль/л) снижается. Общая железосвязывающая способность сыворотки крови (ОЖСС) повышается (при норме 30,6-84,6 мкмоль/л). Снижается ферритин сыворотки крови (в норме 70-140 мкг/л у мужчин и 35-70 мкг/л у женщин). Коэффициент насыщения трансферрина (КНТ) железом снижается (в норме 25-40 %).
Современные лабораторные методы позволяют выделить 3 степени развития ЖДА.
Прелатентный (Iстепень) дефицит железа, для которого характерно уменьшение запасов железа в костном мозге и тканях (снижается ферритин сыворотки).
При IIстепени – латентном дефиците железа развивается железодефицитный эритропоэз. Начинается снижение уровня гемоглобина, СЖ, увеличивается ОЖСС, снижается КНТ.
При IIIстепени развивается ЖДА различной степени выраженности. Все вышеописанные показатели достигают критических значений.
Для установления причины ЖДА прежде всего исключают кровопотерю, главным образом из ЖКТ. Для выявления кровопотери из ЖКТ используются следующие методы: 1) визуальная оценка – выявление черного стула (мелены). Для ее появления кровопотеря должна составлять 100-120 мл в сутки и более; 2) реакция Грегерсена на скрытую кровь обычно положительна при кровопотере более 12-20 мл в сутки; 3) определение кровопотери после введения больному эритроцитов, меченных радиоактивным хромом – проба Пфасмана. Она выявляет кровопотерю менее 15 мл в сутки. Наиболее часто причиной кровопотери являются язвенные и опухолевые поражения различных отделов ЖКТ, для установления которых используется весь арсенал современных методов исследования (ультразвуковых, эндоскопических, рентгенологических, включая компьютерную томографию, и др.).
Основные принципы терапии и профилактики ЖДА
Достижение полной клинической и гематологической ремиссии с помощью препаратов железа (лучше пероральных) в сочетании с витаминами В1, В2, В6, С и соблюдения диеты, богатой протеинами, микроэлементами, природными антиоксидантами (мясо, рыба, печень, яйца, ягоды, овощи).
Проведение поддерживающей терапии при сохраняющемся источнике кровотечения.
Ликвидация причины, вызвавшей дефицит железа, источника кровотечения.
Контроль эффективности лечебных мероприятий каждые 3-4 недели. Исследование СЖ, ОЖСС, КНТ, ферритина – до лечения, на 7-14-й день после отмены препаратов, затем 1-2 раза в год.
Динамическое наблюдение за больными ЖДА не менее 3 лет.
Медикаментозное лечение ЖДА
Проводится преимущественно пероральными препаратами железа. Выбор препарата определяется содержанием в нем элементарного железа (Fe 2+ ) и хорошей переносимостью.
Суточная и курсовая дозы препарата рассчитывается с учетом уровня СЖ и содержания элементарного железа (Fe 2+ ) в капсуле (таблетке). При содержании:
СЖ – 10-12 мкмоль/л, суточная доза Fe 2+ – 23-25 мг. Курсовая доза – 1355 мг. Курс лечения – 1,5-2 месяца.
СЖ – 8 мкмоль/л, суточная доза Fe 2+ – 46-51 мг. Курсовая доза – 3100-3200 мг. Курс лечения – 2-2,5 месяца.
СЖ – менее 8 мкмоль/л, суточная доза Fe 2+ – 70-80 мг. Курсовая доза – 6500-7000 мг. Курс лечения – 3 месяца и более.
Наиболее часто используемые препараты для лечения ЖДА приведены в табл. 46.
Содержание железа в препарате и их дозировка
Содержание Fe 2+ в 1 таблетке
(раствор для приема внутрь)
Показания для парентерального введения препаратов железа:
Непереносимость всех пероральных препаратов.
Нарушение всасывания (язвенный колит, энтерит).
Язвенная болезнь желудка и двенадцатиперстной кишки.
Тяжелая анемия и жизненная необходимость быстрого восполнения дефицита железа.
Количество ампул на курс лечения рассчитывается по формуле: А = К × (166,7 – D) × 0,004, где К – масса тела больного, кг,D– исходный уровень гемоглобина, г/л. Используют препараты феррум-лек, феррлицит (в 5 мл раствора 100 мг железа) для внутривенного введения и феррум-лек, эктофер (в 2 мл раствора 100 мг железа) для внутримышечного применения. Обычно они вводятся по 1 ампуле ежедневно или через день.
Переливание крови проводится только по жизненным показаниям.
Витамин В12— и фолиеводефицитная анемииотносятся к группе анемий, возникающих в результате неэффективного эритропоэза с нарушением созревания всех трех ростков кроветворения.
При участии витамина В12(его кофермента метилкобаламина) образуется активная форма фолиевой кислоты, которая необходима для синтеза тимидина, входящего в состав ДНК. Таким образом, витамин В12и фолиевая кислота принимают участие в синтезе ДНК, а также в делении дифференцирующихся клеток костного мозга и ЖКТ. В связи с этим при В12-дефицитной анемии подавляется не только нормальный (нормобластический) тип эритропоэза, но также миелоидный и мегакариоцитарный ростки, что приводит к лейкопении и тромбоцитопении. Нарушение синтеза ДНК приводит к задержке клеточного деления, избыточному накоплению гемоглобина в эритроцитах и увеличению их размера – макроцитозу. Некоторые гиперхромные эритроциты достигают в размере 11-12 мкм и более – такие эритроциты называются мегалоцитами. Эритропоэз в основном идет аномальным путем с образованием аномальных молодых эритроцитов, содержащих ядро, – мегалобластов. Таким образом формируются характерные гематологические признаки В12-дефицит-ной анемии – мегалобластический тип кроветворения, макроцитоз с избыточным содержанием гемоглобина в эритроцитах, что дает увеличение цветового показателя.
Витамин В12(его кофермент аденозилкобаламин) необходим также для нормального обмена жирных кислот. При дефиците витамина В12обмен жирных кислот нарушается, образуются пропионовая и метилмалоновая кислоты, токсичные для нервной ткани и приводящие к развитию фуникулярного миелоза.
Обмен витамина В12и фолиевой кислоты в организме
Витамин В12из пищевых продуктов (мясо, яйца, сыр, молоко, почки) попадает в желудок, где связывается с белком – протеином-R. Далее этот комплекс поступает в двенадцатиперстную кишку, где под влиянием протеолитических ферментов поджелудочной железы происходит его расщепление. Одновременно в кишечник поступает внутренний фактор (фактор Касла), вырабатываемый в желудке, который связывается с витамином В12. Комплекс витамина В12с внутренним фактором присоединяется к рецепторам кишечника для внутреннего фактора и всасывается. После всасывания витамин В12связывается с транспортным белком транскобаламиномII, который переносит его в костный мозг на нужды кроветворения и в печень, где он депонируется. Суточная потребность в витамине В12– 3-5 мкг, запас витамина – 3-5 г, поэтому для истощения запаса витамина В12и развития клинической картины анемии требуется от 3 до 12 лет.
Фолиевая кислота содержится в организме в количестве 5-20 мг, и ее запасы при нарушении поступления могут истощиться за 4 месяца. Суточная потребность в витамине составляет 100-200 мкг. Она увеличивается при беременности и гемолитических анемиях. Фолиевая кислота содержится в значительном количестве в овощах и фруктах. Правда, 50 % ее разрушается при кулинарной обработке. Всасывается фолиевая кислота в верхнем отделе тонкой кишки.
нарушение секреции фактора Касла слизистой оболочкой желудка вследствие аутоиммунного атрофического гастрита или гастроэктомии (главная причина);
поражение тонкой кишки, отсутствие рецепторов к внутреннему фактору вследствие глютеновой энтеропатии или хронического энтерита;
конкурентное поглощение витамина В12в кишечнике широким лентецом или микробами (синдром слепой петли);
полное исключение из рациона продуктов животного происхождения (алиментарная недостаточность);
нарушение внешнесекреторной функции поджелудочной железы, в результате чего комплекс витамина В12с протеином-Rне расщепляется;
редкий наследственный дефект – снижение количества транскобаламина II;
у новорожденных – вскармливание козьим молоком, которое содержит малое количество фолиевой кислоты;
длительный прием противосудорожных препаратов, оральных контрацептивов, некоторых туберкулостатиков;
беременность при плохом питании, злоупотреблении алкоголем, а также в случае, если беременная женщина страдает наследственной или приобретенной формой гемолитической анемии;
нарушение кишечного всасывания вследствие массивной резекции тонкого кишечника, при синдроме слепой петли, целиакии;
наследственно обусловленное изолированное нарушение всасывания фолиевой кислоты.
Анемический синдром. Постепенно появляются признаки усталости, сниженной работоспособности, слабость, сердцебиение и одышка при физической нагрузке. Больные имеют характерный внешний вид: одутловатость, пастозность лица с бледно-желтым оттенком кожи, небольшая желтушность склер.
Синдром желудочно-кишечных нарушений: атрофия слизистой желудка с соответствующей клинической картиной, подтвержденная гистологически; атрофический десквамативный глоссит (характерны участки десквамации эпителия и атрофии нитевидных сосочков – малиновый, «лакированный» язык).
Фуникулярный миелоз, связанный с нарушением обмена жирных кислот. Наиболее ранними симптомами поражения нервной системы являются парестезии и нарушения чувствительности с постоянными легкими болевыми ощущениями, ощущение холода, онемение в конечностях, чувство ползанья мурашек. Нередко наблюдаются признаки мышечной слабости. В первую очередь страдают нижние конечности. Поражение чаще симметричное. Руки поражаются редко. При глубоком поражении нарушается вибрационная и глубокая чувствительность. Иногда у больных появляются психические нарушения, бред, слуховые и зрительные галлюцинации. В самых тяжелых случаях наблюдается кахексия, арефлексия, стойкие параличи нижних конечностей (псевдотабиес).
Для фолиеводефицитной анемии не характерна одутловатость лица. Сравнительно часто наблюдается иктеричность склер. Нет неврологических нарушений. Глоссит наблюдается крайне редко.
Лабораторная диагностика. Изменения в общем анализе крови, биохимических анализах и в костном мозге при В12— и фолиеводефицитной анемиях схожи.
В анализе крови наблюдаются анемия, тромбоцитопения и нейтропения. Уровень ретикулоцитов чаще снижен. Цветовой показатель больше 1. Определяется макроцитоз с наличием мегалоцитов, анизоцитоз, пойкилоцитоз, базофильная пунктуация эритроцитов. В эритроцитах обнаруживаются остатки ядра – тельца Жолли и кольца Кебота.
Характерным для этих анемий является полисегментированность нейтрофилов. Если в норме нейтрофил содержит 3-4 сегмента, то при В12— или фолиеводефицитной анемии – 5-6.
Желтушность кожных покровов и иктеричность склер при этих анемиях обусловлена увеличением в крови билирубина за счет его непрямой фракции вследствие гемолиза макро- и мегалоцитов. При этом увеличена селезенка, реже – печень.
В стернальном пунктате выявляется резкое раздражение красного ростка, преобладание эритроидных клеток над миелоидными с наличием мегалобластов.
В моче определяется высокая концентрация метилмалоновой кислоты, что характерно только для В12-дефицитной анемии в отличие от фолиеводефицитной.
Основные принципы терапии и профилактики В12— и фолиеводефицитной анемий
Основным методом лечения является применение препаратов витамина В12. С этой целью используют цианкобаламин (500 мкг/сут ежедневно) или гидроксикобаламин (1 мг/сут через день). Все препараты вводятся парентерально. Длительность курса терапии – 4-6 недель.
К концу первой недели лечения обязательно контролируют уровень ретикулоцитов. Обнаружение большого числа ретикулоцитов (20-50 %) на фоне стабильного уровня гемоглобина указывает на эффективность терапии.
С целью профилактики рецидива В12-дефицитной анемии в последующем пожизненно ежемесячно вводят препараты витамина В12 – цианкобаламин или гидроксикобаламин по 500 мкг, или же проводят двух-трехнедельные курсы поддерживающей терапии (10-14 инъекций) 1-2 раза в год.
При выраженных клинических проявлениях фуникулярного миелоза используют высокие дозы цианокобаламина (1000 мкг/сут) в сочетании с аденозилкобаламином (500 мкг/сут внутримышечно), который, не влияя на костномозговое кроветворение, участвует в обмене жирных кислот в нервной ткани.
Лечебная доза фолиевой кислоты составляет 5-15 мг/сут. Она оказывается достаточной даже в случае нарушенного всасывания фолиевой кислоты. При выявлении фолиеводефицитной анемии во время беременности или кормления следует назначить ту же дозу препарата, а после нормализации эритропоэза доза может быть уменьшена до 1 мг/сут на весь период беременности и кормления.
источник
Данное заболевание крови встречается у 0,1% всего населения, однако среди пожилых людей данный показатель повышается до 1%. Чаще болеют женщины, причем развитие дефицита витамина В12 обычно связано с беременностью и может самостоятельно исчезать после рождения ребенка.
Интересные факты
- Дефицит витамина В12 отмечается у 10% людей в возрасте старше 70 лет, однако не у всех из них развиваются клинические проявления В12 дефицитной анемии.
- Ни одно животное или растение на земле не способно синтезировать витамин В12.
- Витамин В12 вырабатывается исключительно микроорганизмами (бактериями), обитающими в конечном отделе пищеварительного тракта животных и человека, однако он неспособен попасть в кровоток, так как его всасывание происходит в тощей кишке, которая расположена в начальных отделах кишечника.
Образование эритроцитов начинается еще на ранних стадиях эмбрионального развития. Первые клетки крови у эмбриона образуются из мезенхимы (особой эмбриональной ткани) в конце 3 недели беременности. По мере роста и развития выделяются основные органы, которые обеспечивают кроветворение.
Основными кроветворными органами являются:
- Печень – выполняет кроветворную функцию с 6 недели внутриутробного развития и до рождения ребенка.
- Селезенка – участвует в процессе кроветворения с 12 недели внутриутробного развития и до рождения ребенка.
- Красный костный мозг – начинает выполнять кроветворную функцию с 12 недели внутриутробного развития и является единственным кроветворным органом после рождения ребенка.
Образование эритроцитов происходит из так называемых полипотентных стволовых клеток (ПСК). В организме человека имеется около 40 тысяч ПСК, которые образуются в периоде внутриутробного развития. Они содержат ядро, в котором располагается ДНК (дезоксирибонуклеиновая кислота), регулирующая процессы клеточного деления и дифференцировки (приобретения клеткой специфической функции). Кроме ядра в стволовых клетках имеется множество других структур (органелл), которые нужны для обеспечения процессов их жизнедеятельности и размножения.
Молекула ДНК человека имеет форму двух нитей, спирально перекрученных между собой. Каждая нить состоит из множества особых химических соединений – нуклеозидов. Нуклеозиды могут соединяться друг с другом в различных комбинациях, от чего в конечном итоге и зависит вид клетки, ее форма, состав и выполняемые ею функции. Другими словами, любые проявления живой клетки зависят от того, какие нуклеозиды и в какой последовательности будут взаимодействовать в каждой определенной молекуле ДНК.
Уникальной особенностью ПСК является то, что под действием различных регуляторных факторов они могут превращаться в любую клетку крови — эритроцит (обеспечивающий транспорт газов), тромбоцит (отвечающий за остановку кровотечений), лейкоцит или лимфоцит (выполняющие защитные функции).
Процесс роста и развития эритроцитов регулируется эритропоэтином – особым веществом, которое вырабатывается почками, если ткани организма испытывают недостаток в кислороде (кислородное голодание). Эритропоэтин активирует образование эритроцитов в красном костном мозге, в результате чего увеличивается их количество в периферической крови, что улучшает доставку кислорода к органам и тканям организма. Устранение кислородного голодания на тканевом уровне уменьшает продукцию эритропоэтина, что приводит к уменьшению синтеза эритроцитов.
Процесс дифференцировки (образования эритроцита из стволовой клетки) можно представить следующим образом:
- Полипотентная стволовая клетка через несколько промежуточных делений превращается в клетку-предшественницу эритропоэза, которая также содержит ядро и органеллы.
- Под воздействием эритропоэтина клетка-предшественница эритропоэза начинает активно делиться, при этом в ней происходит ряд структурных и функциональных изменений — она в несколько раз уменьшается в размерах, теряется ядро и большинство органелл (следовательно, и способность к дальнейшему размножению) и накапливает гемоглобин.
- Все описанные выше процессы происходят в красном костном мозге, а их результатом является образование ретикулоцитов (незрелых форм эритроцитов). За сутки в костном мозге образуется около 3 х 10 9 ретикулоцитов, которые выделяются в периферический кровоток. Они содержат некоторые органеллы и способны в небольших количествах образовывать гемоглобин.
- В течение 24 часов происходит полная утрата всех оставшихся органелл, в результате чего формируется зрелый эритроцит.
Для образования эритроцитов необходимы:
- Железо – включается в состав гемоглобина, являясь основным микроэлементом, обеспечивающим транспорт кислорода в организме.
- Витамин В12 (кобаламин) – принимает участие в образовании ДНК.
- Витамин В9 (фолиевая кислота) – также участвует в процессе образования ДНК.
- Витамин В6 (пиридоксин) – участвует в процессе образования гемоглобина.
- Витамин В2 (рибофлавин) – участвует в процессе дифференцировки эритроцитов.
Конечным этапом эритропоэза является зрелый эритроцит. Он не содержит ядра, практически полностью лишен органелл и не способен делиться. Его красный цвет обусловлен наличием железа, входящего в состав гемоглобина, который заполняет почти все внутреннее пространство клетки (в каждом эритроците содержится от 250 до 400 миллионов молекул гемоглобина, что равняется 25 – 40 пикограммам).
Эритроцит имеет форму уплощенного двояковогнутого диска с более толстыми краями и углублением в центре. Внутренняя поверхность его клеточной мембраны выстлана специальным белком – спектрином, который отвечает за поддержание формы клетки. Диаметр клетки равен в среднем 7,5 – 8,3 мкм.
Перечисленные особенности строения позволяют эритроциту видоизменяться и проходить через мельчайшие кровеносные сосуды организма, диаметр которых в 2 – 3 раза меньше диаметра самих эритроцитов, возвращаясь после этого к первоначальной форме (благодаря наличию спектрина).
Эритроциты не способны передвигаться самостоятельно и транспортируются в организме с током крови. Наружные поверхности их мембран обладают определенным отрицательным зарядом, в результате чего отталкиваются друг от друга, от остальных клеток крови и от стенок сосудов (которые также заряжены отрицательно). Это обеспечивает поддержание всех клеток крови во взвешенном состоянии, предотвращая их слипание и образование сгустков.
Средний срок жизни эритроцитов составляет 120 дней, в течение которых они циркулируют в крови, выполняя свои функции. Так как данные клетки практически лишены органелл, их способности к устранению повреждений (неизменно возникающих в процессе циркуляции в организме) довольно ограничены.
С течением времени эритроциты несколько уменьшаются в объеме (однако количество гемоглобина в них остается прежним), клеточная мембрана утрачивает эластичность и способность видоизменяться. Кроме того, наружная поверхность мембран старых эритроцитов теряет свой отрицательный заряд. Результатом этих процессов является уменьшение прочности и изменение формы красных клеток крови, что способствует их разрушению.
Разрушение эритроцитов (гемолиз) происходит:
- в селезенке;
- в сосудистом русле.
Разрушение эритроцитов в селезенке (внутриклеточный гемолиз)
Селезенка является основным органом, в котором разрушается до 90% эритроцитов, а также других клеток крови. Этому процессу способствует наличие большого количества так называемых синусоидных капилляров, имеющих в своей стенке небольшие отверстия. Эритроциты при прохождении через такие капилляры выходят из них и проходят через узкие щели в ткани селезенки (диаметр которых составляет 0,5 – 0,7 мкм). Старые или деформированные клетки не способны пройти через эти щели, поэтому задерживаются в них и разрушаются специальными клетками – макрофагами, которые находятся в данном органе в большом количестве.
При разрушении эритроцита железо, входящее в состав гемоглобина, высвобождается в кровоток, связывается с особым транспортным белком трансферрином и переносится в костный мозг, где вновь используется для образования эритроцитов. Оставшийся гемоглобин в результате нескольких химических реакций превращается в билирубин (несвязанную фракцию) – вещество желтого цвета, которое выделяется в кровоток при разрушении эритроцитов. Билирубин транспортируется в печень, где связывается с глюкуроновой кислотой, образуя связанную фракцию билирубина, которая включается в состав желчи и выводится из организма с калом.
Разрушение эритроцитов в сосудистом русле (внеклеточный гемолиз)
Данный термин подразумевает разрушение эритроцитов (и других клеток крови) непосредственно в просвете кровеносных сосудов. Примерно 10% эритроцитов разрушается путем внеклеточного гемолиза. Гемоглобин, попадающий при этом в кровоток, связывается с особым белком плазмы – гаптоглобином. Образующийся комплекс переносится в селезенку и разрушается ее макрофагами.
Организм человека не в состоянии синтезировать витамин В12, поэтому его количество полностью зависит от поступления с пищей (преимущественно животного происхождения).
Всасывание кобаламина происходит в кишечнике и только в присутствии особого фермента – внутреннего фактора Касла, который вырабатывается париетальными клетками слизистой оболочкой желудка. Поступающий с пищей витамин В12 связывается с данным ферментом в желудке. Образовавшийся комплекс взаимодействует (в присутствии ионов кальция) со специфическими рецепторами клеток слизистой оболочки тощей кишки (являющейся частью тонкого кишечника), в результате чего кобаламин переносится в кровоток, а внутренний фактор Касла остается в просвете кишечника.
Попавший в кровоток витамин В12 связывается со специальным транспортным белком – транскобаламином I или II и в таком виде доставляется в костный мозг, где принимает участие в процессе кроветворения, и в печень, являющуюся местом его депонирования. Важно отметить, что в клетки организма витамин В12 может попасть, только находясь в комплексе с транскобаламином II.
При сбалансированном питании и прочих нормальных условиях в кишечнике ежедневно всасывается 30 – 50 мкг витамина В12. Он депонируется в печени, которая у взрослого человека может содержать до 3 – 5 миллиграмм витамина. Если учесть, что суточная потребность организма в нем составляет 3 – 5 мкг, то становится понятным, почему первые признаки В12 дефицитной анемии начинают появляться не ранее чем через 2 – 3 года после нарушения процессов поступления кобаламина в организм.
Недостаток витамина В12 приводит к нарушению синтеза ДНК во всех клетках организма. В первую очередь это проявляется в тканях, в которых процессы клеточного деления происходят наиболее интенсивно — в кроветворной ткани и в слизистых оболочках.
Попавший в клетку кобаламин превращается в одну из двух активных форм:
- Дезоксиаденозилкобаламин (ДА-В12). Участвует в образовании жирных кислот. При их недостатке в организме поражается нервная система.
- Метил-кобаламин (метил-В12). Принимает активное участие в процессе образования компонентов ДНК, а именно в синтезе тимидина – одного из пиримидиновых нуклеозидов. Недостаток витамина В12 в организме приводит к остановке синтеза данного нуклеозида, в результате чего образуется структурно неполноценная молекула ДНК. Она быстро разрушается, что делает невозможным дальнейшее деление и дифференцировку клеток. Кроме того, метил-В12 также необходим для образования миелина, из которого состоят оболочки нервных волокон. При недостатке данного вещества нарушается проведение нервного импульса по нервам, что может проявляться разнообразными неврологическими симптомами.
Нарушение синтеза ДНК в процессе кроветворения происходит в начальных стадиях эритропоэза, в результате чего дальнейшее развитие эритроцитов становится невозможным. Образующиеся при этом кроветворные клетки (называемые мегалобластами) имеют большие размеры (10 – 20 мкм), содержат остатки разрушенного ядра и множество органелл, а также большое количество гемоглобина. Большинство из них разрушается прямо в костном мозге – развивается так называемый неэффективный эритропоэз. Те мегалобласты, которые все-таки выделяются в кровоток, неспособны выполнять транспортную функцию и при первом же прохождении через селезенку задерживаются и разрушаются в ней.
Важно отметить, что при недостатке витамина В12 в костном мозге нарушается образование не только эритроцитов, но и других клеток – лейкоцитов и тромбоцитов. Обычно эти изменения выражены менее значительно, чем дефицит эритроцитов, однако при длительном течении заболевания и отсутствии адекватного лечения может развиться панцитопения – клинический синдром, характеризующийся недостатком всех клеточных элементов в крови.

Причинами развития дефицита витамина В12 являются:
- недостаточное поступление с пищей;
- нарушение всасывания в кишечнике;
- повышенное использование витамина В12 в организме;
- наследственные заболевания, нарушающие обмен витамина В12.
Как было сказано ранее, организм человека неспособен самостоятельно синтезировать кобаламин, поэтому он должен присутствовать в потребляемой пище. Растения не содержат витамин В12, поэтому единственным его источником являются продукты животного происхождения — мясо, рыба, кисломолочные продукты и так далее. В нормальных условиях данные продукты включены в рацион почти каждого человека, поэтому дефицита витамина В12 не развивается.
Причинами недостаточного поступления витамина В12 с пищей могут быть:
- нарушение питания;
- хронический алкоголизм.
Нарушение питания
Одной из частых причин дефицита кобаламина в организме может быть вегетарианство. Вегетарианцами называется определенная группа людей, которые полностью отказались не только от мяса, но и от всех продуктов животного происхождения (яиц, рыбы, молока, сливочного масла и других). Так как данные продукты являются единственным источником кобаламина, вполне логично, что в скором времени у таких людей может развиться дефицит витамина В12 в организме.
Кроме вегетарианцев риск развития В12 дефицитной анемии повышен у бедных слоев населения, которые из-за недостатка средств не могут позволить себе употребление достаточного количества продуктов животного происхождения.
Хронический алкоголизм
Употребление больших доз алкоголя препятствует взаимодействию кобаламина с внутренним фактором Касла, а также повреждает слизистую оболочку желудка, нарушая выработку данного фактора париетальными клетками. Результатом этого становится резкое уменьшение количества кобаламина, поступающего в кровь.
Кроме того, длительное злоупотребление алкогольными напитками может привести к развитию таких заболеваний как алкогольный гепатит и цирроз. Результатом этого является уменьшение запасов кобаламина в печени, что снижает компенсаторные возможности организма при нарушении поступления данного витамина с пищей.
В данном случае с пищей поступает достаточное количество кобаламина, однако нарушены процессы его транспортировки из просвета кишечника в кровь.
Причинами нарушения всасывания витамина В12 могут быть:
- нарушение образования внутреннего фактора Касла;
- поражение тонкого кишечника;
- паразитарные инфекции.
Нарушение образования внутреннего фактора Касла
Как уже говорилось, наличие данного фактора является необходимым условием для всасывания витамина В12. При его недостатке поступающий с пищей кобаламин не способен пройти через слизистую оболочку кишечника и полностью выделяется с калом.
Причинами недостатка внутреннего фактора Касла могут быть:
- Атрофический гастрит. Данное заболевание характеризуется атрофией (уменьшением размеров и снижением функциональной активности) всех клеток слизистой оболочки желудка, что приводит к снижению или полному прекращению синтеза внутреннего фактора Касла париетальными клетками.
- Аутоиммунный гастрит. Характеризуется нарушением деятельности иммунной (защитной) функции организма, в результате чего собственные клетки начинают восприниматься как чужеродные, к ним образуются специфические антитела, которые их разрушают. При аутоиммунном гастрите антитела могут образовываться как к париетальным клеткам слизистой оболочки желудка, так и к самому фактору Касла.
- Рак желудка. Это опухолевое заболевание, в процессе которого происходит неконтролируемый рост и размножение опухолевых клеток, что приводит к постепенному разрушению и вытеснению париетальных клеток слизистой оболочки.
- Удаление желудка. Лечение некоторых заболеваний (прободной язвы, рака) заключается в частичном или полном удалении желудка, что приводит к уменьшению либо полному исчезновению париетальных клеток и, следовательно, к уменьшению количества образующегося внутреннего фактора Касла.
- Врожденный дефицит внутреннего фактора Касла. Данное заболевание передается по наследству и характеризуется дефектом гена, ответственного за образование этого фактора, что приводит к нарушению его секреции железами желудка.
Поражение тонкого кишечника
Всасывание витамина В12 происходит в тощей кишке. Различные повреждения данного отдела тонкого кишечника могут привести к нарушению процессов всасывания в нем.
Причинами поражения тощей кишки могут быть:
- Воспалительные заболевания (энтериты). Воспалению тонкого кишечника могут способствовать инфекции желудочно-кишечной системы, пищевые отравления, различные аллергии. При длительном течении воспалительных процессов происходит атрофия клеток слизистой оболочки кишечника, что делает невозможным всасывание кобаламина.
- Опухоли. Опухоли кишечника, по описанному ранее механизму, могут приводить к разрушению его слизистой оболочки.
- Удаление тонкой кишки (из-за опухоли или по другой причине).
Паразитарные инфекции
Исследованиями последних лет установлено, что более чем у 90% населения в кишечнике обитают различные паразиты (глисты). Им, как любым живым организмам, для роста и развития требуются определенные питательные вещества, в том числе и витамины. Некоторые глисты (например, широкий ланцет, вызывающий развитие дифиллоботриоза) могут достигать огромных размеров, в результате чего практически весь витамин В12, поступающий с пищей, не всасывается, а потребляется паразитом.
Как упоминалось ранее, взрослому человеку необходимо всего лишь 3 – 5 мкг кобаламина в сутки. Однако при определенных условиях и заболеваниях потребность в данном витамине может значительно увеличиваться.
Причинами усиленного использования витамина В12 в организме могут быть:
- Беременность. В развивающемся плоде процессы роста и деления клеток происходят максимально интенсивно, что увеличивает потребность матери в витамине В12 в несколько раз.
- Гипертиреоз. Данное заболевание характеризуется увеличенным образованием и поступлением в кровоток гормонов щитовидной железы (трийодтиронина и тироксина). Это приводит к повышению обмена веществ в организме, что характеризуется усилением процессов клеточного деления во многих органах и требует больших количеств кобаламина.
- Злокачественные опухоли. Злокачественный процесс характеризуется неконтролируемым и непрерывным размножением опухолевой клетки, в результате чего образуется множество ее копий. При массивных опухолях большая часть кобаламина может потребляться опухолевой тканью, в результате чего другие органы будут испытывать недостаток в данном витамине.
Это довольно большая группа патологических состояний, характеризующаяся нарушением образования определенных веществ, которые в норме обеспечивают всасывание и утилизацию кобаламина в организме.
Нарушение обмена витамина В12 может быть обусловлено:
- Наследственным дефицитом транскобаламина II. Заболевание наследуется по аутосомно-рецессивному типу, то есть ребенок будет болеть только в том случае, если оба родителя страдали данным заболеванием (либо являлись его бессимптомными носителями). Характеризуется уменьшением образования или полным отсутствием транскобаламина II в организме. В этом случае количество витамина В12 в крови нормальное или даже увеличенное, однако он не может попасть в клетки организма, в результате чего развивается клиническая картина В12 дефицитной анемии.
- Синдромом Имерслунд-Гресбека. Данное заболевание также передается по аутосомно-рецессивному типу и характеризуется нарушением всасывания витамина В12 в кишечнике. Механизм этого процесса окончательно не установлен, так как секреция и взаимодействие внутреннего фактора Касла с кобаламином происходят нормально, и никаких органических поражений тонкого кишечника не наблюдается. Предполагается нарушение транспортных систем в клетках слизистой оболочки тощей кишки.
- Нарушением использования витамина В12 в клетках. Как говорилось ранее, в клетках организма кобаламин превращается в метил-кобаламин и дезоксиаденозилкобаламин. Эти процессы требуют наличия определенных веществ (ферментов), при отсутствии которых использование витамина В12 клетками становится невозможным.

Заболевание развивается медленно и в начальных стадиях характеризуется неспецифическими симптомами – слабостью, повышенной утомляемостью. С течением времени состояние пациента ухудшается, а проявления дефицита витамина В12 становятся более явными.
Основные клинические проявления В12 дефицитной анемии обусловлены:
- нарушением образования клеток крови;
- поражением пищеварительной системы;
- поражением нервной системы.
В результате нарушения процесса кроветворения в циркулирующей крови снижается количество эритроцитов. Это ухудшает транспорт газов в организме и приводит к кислородному голоданию всех тканей и органов.
Нарушение кроветворения проявляется:
- Бледностью и желтушностью кожи и слизистых оболочек. Розоватый цвет кожи и слизистых оболочек обусловлен белково-пигментным комплексом – гемоглобином, входящим в состав эритроцитов. При В12 дефицитной анемии бледность развивается постепенно, усиливаясь в течение нескольких месяцев. Кроме того, из-за усиленного разрушения эритроцитов (происходящего в костном мозге и в селезенке), в кровь выделяется большое количество пигмента билирубина, который придает коже и слизистым оболочкам желтоватый оттенок.
- Учащенным сердцебиением. Если организм испытывает недостаток в кислороде – активируются определенные защитные реакции, одной из которых является увеличение частоты сердечных сокращений (ЧСС). Это приводит к увеличению объема крови, проходящей через каждый орган за единицу времени, что улучшает доставку кислорода.
- Болями в сердце. Увеличение частоты сердечных сокращений улучшает доставку кислорода ко всем органам. Однако само сердце при этом выполняет большую работу и получает меньше кислорода, что может привести к появлению колющих болей в груди, которые могут распространяться в область левого плеча и живота.
- Непереносимостью физических нагрузок. При физических нагрузках увеличивается потребность мышц в энергии, которая образуется только при достаточном количестве поступающего кислорода. В нормальных условиях эти потребность восполняются за счет увеличения частоты сердечных сокращений. Однако при В12 дефицитной анемии ЧСС и так увеличена, что усугубляется нарушенной транспортной функцией эритроцитов, в результате чего физические нагрузки различной интенсивности приводят к быстрой утомляемости, появлению чувства нехватки воздуха, головокружениям или потере сознания.
- Головокружениями и частыми обмороками. Данные симптомы являются признаками выраженного дефицита эритроцитов в крови, когда головной мозг начинает испытывать недостаток в кислороде.
- Появлением «мушек» перед глазами. Это обусловлено недостаточным кровоснабжением сетчатки глаза (которая весьма чувствительна к кислородному голоданию) и стекловидного тела, что приводит к нарушению в них обмена веществ, ухудшению остроты зрения и появлению перед глазами маленьких темных пятен в форме колец, молний, ниточек и др.
- Увеличением селезенки. Большие эритроциты, попадающие в кровоток, задерживаются в капиллярах селезенки, закупоривая их. Это приводит к скоплению большого количества клеток крови в органе и увеличению его в размерах.
Поражение желудочно-кишечной системы является наиболее ранним признаком дефицита витамина В12 в организме, что обусловлено интенсивным клеточным делением в слизистых оболочках полости рта, желудка, кишечника. При нарушении данных процессов быстро развиваются атрофические изменения и нарушение функции органов.
Поражение пищеварительной системы может проявляться:
- Нарушением пищеварения. Процесс пищеварения полностью зависит от нормального функционирования слизистых оболочек полости рта, желудка и кишечника. В них располагается множество желез, выделяющих особые пищеварительные соки, которые способствуют переработке пищевых продуктов. При недостаточности данных соков пища не проходит должной обработки, в результате чего нарушаются процессы всасывания питательных веществ, витаминов, микроэлементов.
- Неустойчивым стулом. В результате нарушения процессов пищеварения пища может дольше задерживаться в желудке или в кишечнике, приводя к вздутию живота, изжоге, запорам, которые могут чередоваться с диареей (поносом).
- Снижением аппетита. Появляется в результате снижения секреции желудочного сока атрофированной слизистой оболочкой желудка.
- Снижением массы тела. Является результатом снижения аппетита и нарушения пищеварения.
- Изменением цвета и формы языка. Поверхность языка образована огромным множеством мелких ворсинок, называемых сосочками. При В12 дефицитной анемии происходит атрофия слизистой оболочки языка, то есть постепенное уменьшение и исчезновение всех сосочков. В результате язык становится гладким, ярко-малинового цвета.
- Нарушением вкуса. Человек чувствует вкус различных продуктов благодаря наличию множества вкусовых рецепторов, расположенных в слизистой оболочке языка (преимущественно в сосочках). Следствием ее поражения является снижение или полная утрата вкусовых ощущений. Кроме того, у человека может появляться различные вкусовые отклонения – он может испытывать отвращение к различным продуктам питания (например, к мясу, рыбным изделиям и т. д.).
- Частыми инфекциями ротовой полости. Слизистая оболочка ротовой полости играет важную защитную роль, предотвращая рост и развитие патогенной микрофлоры. При ее атрофии увеличивается частота инфекционных заболеваний полости рта, может развиваться глоссит (воспаление языка), гингивит (воспаление десен).
- Болью и жжением в полости рта. Возникает в результате атрофических изменений слизистой оболочки и поражения нервных окончаний ротовой полости.
- Болью в животе после еды. Нормальная слизистая оболочка желудка выполняет защитную функцию, предохраняя желудок от агрессивного воздействия пищевых продуктов. При нарушении процессов клеточного деления повышается риск ее воспаления (развития гастрита) и образования язв, что может проявляться режущими болями в животе, усиливающимися после приема пищи (особенно острой, грубой, плохо обработанной).
Поражения нервной системы при дефиците витамина В12 обусловлены участием кобаламина в образовании миелиновых оболочек, которые являются составной частью большинства нервных волокон организма и обеспечивают передачу нервного импульса по ним. При нарушении образования миелина происходит повреждение и склероз (замещение рубцовой тканью) нервных клеток и нервных волокон, что может проявляться всевозможными неврологическими нарушениями (в зависимости от того, какие нервы были поражены).
Наиболее опасным считается поражение головного мозга, являющегося центром всей нервной системы, и спинного мозга, который представляет собой совокупность нервных волокон, идущих от головного мозга ко всем органам и тканям организма и в обратном направлении.
Симптомами поражения нервной системы при В12 дефицитной анемии могут быть:
- Нарушение чувствительности. Одно из первых проявлений поражения нервной системы. Чувствительность может нарушаться в любых участках тела, однако это наиболее заметно, когда поражаются пальцы рук, запястья. Больной человек может не ощущать прикосновение, тепло, холод и даже боль. Чаще поражение носит двусторонний характер и без соответствующего лечения постоянно прогрессирует.
- Парестезии. Один из видов нарушения чувствительности, характеризующийся онемением, покалыванием, «ползанием мурашек» в определенной области кожи.
- Атаксия. Данный термин подразумевает нарушение согласованной работы мышц. Это может проявляться нарушением равновесия, неуклюжестью и несогласованностью движений рук и ног, туловища.
- Снижение мышечной силы. Чтобы мышца сокращалась, необходимо поступление достаточного количества нервных импульсов из головного мозга. Кроме того, даже в покое головной мозг постоянно посылает к мышцам небольшое количество импульсов, что обеспечивает поддержание мышечного тонуса. При поражении спинного мозга импульсы не могут достичь мышц, в результате чего происходит их атрофия (уменьшение массы и размеров). При отсутствии своевременного лечения данное состояние может прогрессировать и привести к параличу – полной утрате способности выполнять произвольные движения.
- Нарушение процессов дефекации и мочеиспускания. Развиваются при длительном недостатке витамина В12 в организме и могут проявляться задержкой или, наоборот, недержанием кала и/или мочи (в зависимости от того, какие участки спинного мозга поражены).
- Нарушения психики. Является одним из наиболее неблагоприятных (в прогностическом плане) симптомов заболевания и характеризуется поражением коры головного мозга. Выраженность психических расстройств варьирует в зависимости от пораженного участка и выраженности склеротических изменений и может проявляться как бессонницей, незначительным ухудшением памяти или легкой депрессией, так и тяжелыми психозами, судорогами, галлюцинациями.
При В12 дефицитной анемии неврологические симптомы появляются в определенной последовательности — вначале происходит симметричное поражение ног, затем живота и туловища. В более поздних стадиях в процесс вовлекаются пальцы рук, плечевой пояс, шея, может поражаться область лица и головы. В последнюю очередь появляются психические расстройства.
Диагностикой и лечением В12 дефицитной анемии занимается врач-гематолог, который, при необходимости, может привлекать других специалистов (гастролога, невролога).
Процесс диагностики В12 дефицитной анемии включает:
- общий анализ крови;
- биохимический анализ крови;
- пункцию костного мозга;
- установление причины В12 дефицитной анемии.
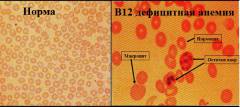
Целью данного исследования является определение клеточного состава периферической крови, а также детальное исследование полученного материала под микроскопом, что позволяет выявить отклонения в размерах, форме или составе клеток в крови.
Забор крови для анализа
Процедуру производит медсестра в специальном процедурном кабинете. Кровь берется утром, натощак. За 2 – 3 часа до сдачи анализа рекомендуется исключить курение и тяжелые физические нагрузки.
Для клинического анализа кровь могут брать:
- Из пальца (капиллярную). Капиллярную кровь берут из кончика пальца руки. Вначале с целью дезинфекции медсестра обрабатывает палец пациента ватой, смоченной в 70% спирте. После этого скарификатором (тонкой одноразовой стерильной пластинкой, которая заточена с обеих сторон) делается прокол кожи на глубину 2 – 4 мм. Первая появившаяся капля крови удаляется ватным тампоном, после чего в специальную промаркированную стеклянную трубку набирается несколько миллилитров крови. По окончании процедуры к месту прокола на 2 – 3 минуты прикладывается ватный тампон, пропитанный спиртом.
- Из вены. Кровь обычно берут из вен локтевой области, которые наиболее хорошо определяются под кожей. Если определить расположение вены в данной области не удается, кровь можно взять из любой другой вены. Пациент садится на стул и кладет руку на его спинку таким образом, чтобы локтевой сустав оказался в разогнутом состоянии. Медсестра накладывает тугой жгут на область плеча и определяет местоположение вены. Локтевая область дважды обрабатывается ватой, смоченной в спирте, после чего одноразовой стерильной иглой, присоединенной к шприцу, производится прокол вены и забор нескольких миллилитров крови. Потом игла извлекается, а к месту прокола на 5 – 7 минут прикладывается пропитанный спиртом ватный тампон.
Микроскопическое исследование
Для определения формы и размеров различных клеток в исследуемой крови, одну или несколько капель переносят на специально стекло, окрашивают специальными красителями и исследуют в световом микроскопе. Таким же способом можно подсчитать примерное содержание клеток в исследуемом образце.
Нормальный размер эритроцитов – 7,5 – 8,3 мкм. При микроскопическом исследовании они определяются как клетки красного цвета, одинаковых размеров, кольцевидной формы, не содержащие ядра или других включений.
При дефиците витамина В12 в костном мозге образуются мегалобласты. Часть из них сразу разрушается, а остальные поступают в кровоток.
При В12 дефицитной анемии микроскопическая картина периферической крови характеризуется:
- Пойкилоцитозом – наличием эритроцитов различной формы.
- Анизоцитозом – наличием эритроцитов различных размеров.
- Макроцитозом – наличием эритроцитов, увеличенных в диаметре (более 8,5мкм).
- Внутриклеточными включениями – в эритроцитах определяются остатки разрушенного ядра и некоторые органеллы.
- Гиперхромией – эритроциты имеют более выраженную окраску, чем в норме (что обусловлено большой концентрацией гемоглобина и отсутствием сужения в центре клетки).
Исследование в гематологическом анализаторе
В большинстве современных лаборатории имеются специальные гематологические анализаторы, которые позволяют в довольно короткие сроки получить точную информацию о количестве клеточных элементов в исследуемой крови, а также некоторые другие показатели.
| Исследуемый показатель | Что обозначает | Норма | Изменения при В12 дефицитной анемии |
| Данный показатель более точно отображает средние размеры эритроцитов в исследуемой крови, так как оценивает большее количество клеток, чем то, которое исследует врач при обычной микроскопии. | 75 – 100 кубических микрометров (мкм 3 ). | 100 – 110 мкм 3 и более. | |
| Концентрация эритроцитов (RBC) | В результате усиленного разрушения эритроцитов в костном мозге и в селезенке количество их в периферической крови будет снижено. | Мужчины (М): 4,0 – 5,0 х 10 12 /л. | Менее 4,0 х 10 12 /л. |
| Женщины (Ж): 3,5 – 4,7 х 10 12 /л. | Менее 3,5 х 10 12 /л. | ||
| Концентрация тромбоцитов (PLT) | При в12 дефицитной анемии нарушается образование не только эритроцитов, но и остальных клеток крови. | 180 – 320 х 10 9 /л. | Менее 180 х 10 9 /л. |
| Концентрация лейкоцитов (WBC) | Лейкоциты выполняют защитную функцию. В норме их концентрация увеличивается при различных инфекциях. При дефиците витамина В12 образование лейкоцитов нарушается, и их количество в крови может быть уменьшено даже при тяжелых инфекционных заболеваниях. | 4,0 – 9,0 х 10 9 /л. | Менее 4,0 х 10 9 /л. |
| Концентрация ретикулоцитов (RET) | При дефиците витамина В12 кроветворение в костном мозге неэффективно, клетки не созревают до стадии ретикулоцитов, в результате чего их количество в крови будет снижено. | М: 0,24 – 1,7%. | Может быть в несколько раз ниже нормы. |
| Ж: 0,12 – 2,05%. | |||
| Общий уровень гемоглобина (HGB) | При В12 дефицитной анемии количество эритроцитов снижено, однако концентрация гемоглобина в каждом из них увеличена, что может поддерживать общий уровень гемоглобина в крови на нормальном уровне. | М: 130 – 170 г/л. | Может быть нормальным или слегка сниженным. |
| Ж: 120 – 150 г/л. | |||
| Средняя концентрация гемоглобина в эритроцитах (MCHC) | Дает более точную информацию о насыщении эритроцитов гемоглобином, так как не учитывается объем плазмы, в которой находятся клетки крови. | 320 – 360 г/л. | Более 400 г/л. |
| Среднее содержание гемоглобина в одном эритроците (MCH) | Определяется посредством деления уровня гемоглобина на количество эритроцитов (вычисления производятся гематологическим анализатором автоматически). | 27 – 33 пикограмм (пг). | Более 35 пг. |
| Гематокрит (Hct) | Данный показатель выражается в процентах и определяет долю клеточных элементов в общем объеме крови. | М: 42 – 50%. | Снижен из-за значительного уменьшения количества эритроцитов в крови. |
| Ж: 38 – 47%. | |||
| Цветовой показатель (ЦП) | Характеризует степень насыщения эритроцитов гемоглобином — чем его больше, тем выше будет цветовой показатель. | 0,85 – 1,05. | Более 1,1. |
| Скорость оседания эритроцитов (СОЭ) | Так как наружные поверхности эритроцитов заряжены отрицательно, они отталкиваются друг от друга, что препятствует их склеиванию. Суть определения СОЭ заключается в склеивании эритроцитов в крови и оседании их на дно пробирки под действием силы тяжести. Скорость данного процесса зависит от концентрации клеток в крови — чем их меньше, тем слабее они отталкиваются друг от друга, и тем быстрее будет СОЭ. | М: 3 – 10 мм/час. | Более 15 мм/час. |
| Ж: 5 – 15 мм/час. | Более 20 мм/час. |
Данное исследование позволяет определить наличие растворенных в крови веществ (белков, ферментов, витаминов и других). Практически любое заболевание (в том числе и В12 дефицитная анемия) характеризуется увеличением или снижением концентрации различных веществ в крови, что позволяет судить о выраженности патологического процесса и степени повреждения внутренних органов, а также контролировать эффективность проводимого лечения.
Кровь для биохимического исследования берется из вены (подготовка пациента и методика забора материала были описаны выше), после чего в специальной пробирке направляется в лабораторию.
| Исследуемый показатель | Что обозначает | Норма | Изменения при В12 дефицитной анемии |
| Содержание кобаламина в крови | Обычно заболевание характеризуется снижением уровня витамина В12. Однако в некоторых случаях (при нарушениях обмена кобаламина в организме) концентрация данного витамина в крови будет увеличена, несмотря на клинические проявления В12 дефицитной анемии, поэтому данный показатель необходимо оценивать, учитывая данные других анализов. | 200 – 900 пг/мл. |
|
| Уровень метилмалоновой кислоты в крови | Данное вещество участвует в процессах жизнедеятельности клеток. Для его использования необходимо наличие активной формы кобаламина (ДА-В12), в отсутствии которой метилмалоновая кислота не может использоваться клетками организма, в результате чего ее концентрация в крови повышается. | 73 – 270 нмоль/мл. | Значительно выше нормы. |
| Уровень гомоцистеина в крови | Гомоцистеин – аминокислота, которая участвует в образовании вещества метионина, входящего в состав миелиновых оболочек нервных клеток. Этот процесс также требует присутствия активной формы кобаламина (метил-В12). При его недостатке количество свободного гомоцистеина в плазме крови повышается. | 5 – 16 мкмоль/л. | Значительно выше нормы. |
| Концентрация билирубина (несвязанной фракции). | Уровень несвязанного билирубина может повышаться при массивном разрушении мегалобластов в красном костном мозге и в селезенке. | 4,5 – 17,1 мкмоль/л. | Может быть увеличен в несколько раз, особенно при длительном течении заболевания. |
| Концентрация сывороточного железа | При интенсивном разрушении эритроцитов и их предшественников из них выделяется большое количество железа. В нормальных условиях оно используется для синтеза новых эритроцитов, однако при В12 дефицитной анемии данный процесс нарушен, в результате чего концентрация железа в крови может повышаться. | М: 17,9 – 22,5 мкмоль/л. | Может повышаться при длительном течении заболевания. |
| Ж: 14,3 – 17,9 мкмоль/л. |
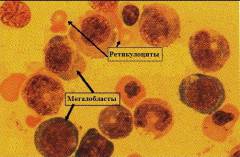
Обычно костный мозг берут из грудины. Процедура выполняется только специально обученным врачом в условиях стерильной операционной. Место пункции дважды обрабатывается 70% спиртовым или йодным раствором. После этого специальным шприцем с полой иглой, установленной под прямым углом к грудине, прокалывают кожу и надкостницу и продвигают иглу на 1 – 2 см в вещество кости. Убедившись, что игла находится в полости кости, производится забор нескольких миллилитров костного мозга, который имеет вид густого, желтовато-красно вещества. Полученный материал направляется в лабораторию для микроскопического исследования.
При В12 дефицитной анемии в костном мозге определяется увеличение клеточных элементов (преимущественно за счет предшественников эритроцитов). Клетки увеличены в размерах, содержат слишком большое количество гемоглобина (по сравнению с нормой). Также отмечается нарушение созревания мегакариоцитов (предшественников тромбоцитов) и промиелоцитов (предшественников лейкоцитов).
При подтверждении диагноза не менее важным моментом является выявление его причины, так как ее устранение (если оно возможно) может привести к излечению пациента.
Для выявления причины В12 дефицитной анемии используется:
- Оценка рациона пациента. Уточняется, как питается пациент, потребляет ли достаточное количество животных продуктов, как часто употребляет алкогольные напитки.
- Фиброгастродуоденоскопия (ФГДС). Метод исследования внутренней поверхности желудка и начального отдела кишечника посредством введения специальной трубки с видеокамерой на конце. Позволяет выявить атрофию слизистой, наличие рака или язвы.
- Биопсия слизистой оболочки желудка и/или кишечника. Подразумевает прижизненное взятие кусочка ткани слизистой оболочки и исследование его клеточного строения. Позволяет выявить атрофические процессы, а также различить доброкачественные и злокачественные опухоли.
- Анализ кала на яйца гельминтов (глистов). С помощью данного метода можно установить само наличие паразитов, а также определить их чувствительность к различным противопаразитарным препаратам, что позволит назначить максимально эффективное лечение.
- Определение специфических антител. В крови могут определяться антитела к внутреннему фактору Касла либо к париетальным клеткам слизистой оболочки, которые его продуцируют.
- Оценка функции печени. Определяется уровень печеночных ферментов в крови, проводится ультразвуковое исследование (УЗИ) органа.
- Определение уровня гормонов щитовидной железы в крови. При их увеличении потребление кобаламина организмом возрастает, что со временем может привести к развитию В12 дефицитной анемии.
Суть медикаментозной терапии данного недуга заключается в ведении витамина В12 извне. Поступив в организм, кобаламин быстро включается в процессы кроветворения, что приводит к устранению симптомов анемии в довольно короткие сроки.
Показаниями к началу лечения витамином В12 являются:
- подтвержденный (лабораторно) диагноз В12 дефицитной анемии;
- концентрация кобаламина в плазме крови менее 220 пг/мл;
- выраженная клиническая картина анемии (даже при более высокой концентрации кобаламина в крови).
Способ применения и дозировка
В большинстве случаев препарат витамина В12 (цианокобаламин) вводится внутримышечно. Прием внутрь (в виде таблеток) допускается, если достоверно установлено, что причиной дефицита витамина является недостаточное его количество в пище, а общее состояние организма не критично (легкое снижение показателей крови, отсутствие неврологических проявлений).
Лечение начинают с внутримышечного введения 500 – 1000 мкг цианокобаламина 1 раз в сутки. Минимальный курс лечения – 6 недель, после чего переходят на поддерживающую терапию. Дозировка препарата на данном этапе лечения зависит от причины и выраженности дефицита витамина В12 в организме. Обычно назначается внутримышечное введение 200 – 400 мкг цианокобаламина 2 – 4 раза в месяц. Поддерживающая терапия может проводиться пожизненно.
Контроль эффективности лечения
В период лечения рекомендуется сдавать общий анализ крови 2 – 3 раза в неделю.
Первым признаком эффективности терапии, а также достоверным подтверждением диагноза является «ретикулоцитарный криз», возникающий на 3 – 5 день после начала введения витамина В12 в организм. Данное состояние характеризующийся резким увеличением количества ретикулоцитов в крови (в 10 – 20 раз), что свидетельствует о начале нормального кроветворения в косном мозге.
В течение 1 – 1,5 месяцев происходит постепенная нормализация состава периферической крови, ослабление неврологических проявлений, нормализация работы пищеварительной системы, что свидетельствует об эффективности проводимого лечения. На этапе поддерживающей терапии рекомендуется ежемесячное проведение общего анализа крови и определение уровня кобаламина в крови.
Суть метода заключается в переливании пациенту крови или, чаще, отдельной эритроцитарной массы. Переливание крови является опасной процедурой, поэтому данный метод используется только при угрожающих жизни состояниях.
Показаниями к переливанию эритроцитов при В12 дефицитной анемии являются:
- Тяжелая анемия – уровень гемоглобина менее 70 г/л;
- Анемическая кома – потеря сознания, обусловленная выраженным нарушением доставки кислорода к мозгу.
Перед началом процедуры проводятся тесты на совместимость крови донора и реципиента (того, кому переливается кровь), после чего в одну из больших вен организма вводится катетер, через который переливается эритроцитарная масса. Так как данная процедура сопряжена с риском развития множества побочных реакций, в течение всего периода переливания крови в палате должен присутствовать врач.
При подтвержденном диагнозе В12 дефицитной анемии одновременно с переливанием донорских эритроцитов начинают внутримышечное введение витамина В12. Переливание крови следует прекратить как можно раньше, как только устранено угрожающее жизни состояние.
Как говорилось ранее, суточная потребность в витамине В12 составляет 3 – 5 мкг, а запасы данного витамина в печени настолько велики, что даже при прекращении поступления кобаламина в организм признаки его дефицита появятся не ранее, чем через 2 – 3 года. Тем не менее, диета играет определенную роль в процессе лечения заболевания, особенно когда запасы витаминов В12 в организме снижаются.
Причинами снижения запасов витамина В12 в организме могут быть:
- Заболевания печени. Такие заболевания как цирроз и рак печени, приводят к уменьшению количества нормальных клеток органа, и замещению их соединительно тканью, которая неспособна депонировать витамин В12. В результате запасы данного витамина в организме снижаются, а при нарушении его поступления признаки заболевания могут появляться в более ранние сроки.
- Беременность. В данном случае матери необходимо обеспечивать витамином В12 не только свой, но и быстро развивающийся организм ребенка, поэтому суточная потребность в витамине В12 может увеличиваться на 50%, а в случае многоплодной беременности – еще больше. В нормальных условиях (при отсутствии заболеваний печени) запасов кобаламина в организме достаточно, чтобы покрыть потребности матери и плода в данном веществе. Однако при частых беременностях запасы кобаламина могут истощаться, особенно если у матери имеются какие-либо заболевания печени, поэтому беременным женщинам особенно важно потреблять достаточное количество этого витамина с пищей.
| Наименование продукта | Содержание витамина В12 в 100г продукта |
| Печень говяжья | 60 мкг |
| Печень свиная | 30 мкг |
| Печень куриная | 16 мкг |
| Скумбрия | 12 мкг |
| Мясо кролика | 4,3 мкг |
| Говядина | 2,6 мкг |
| Морской окунь | 2,4 мкг |
| Свинина | 2 мкг |
| Треска | 1,6 мкг |
| Карп | 1,5 мкг |
| Куриное яйцо | 0,5 мкг |
| Сметана | до 0,4 мкг |

С тех пор как в лечении В12 дефицитной анемии начали применять внутримышечное введение цианокобаламина прогноз для жизни и здоровья пациентов значительно улучшился. При соблюдении режима приема препарата люди могут доживать до глубокой старости без каких-либо проявлений заболевания.
источник
