Боль в груди — одна из самых частых причин обращения за врачебной помощью. Причина боли в груди может быть ясной, но часто бывает атипичной. Случаи, когда пациенты жалуются на боль в груди, представляют наибольшие трудности для диагностики.
Дифференциально-диагностический ряд в таких случаях чрезвычайно широк и включает, в том числе, заболевания, представляющие непосредственную угрозу жизни, такие как инфаркт миокарда с подъемом и без подъема сегмента ST, нестабильную стенокардию, тромбоэмболию легочной артерии и расслаивающую аневризму аорты.
Расслаивающая аневризма аорты (РАА) представляет достаточно сложную проблему в плане первичной диагностики. Причиной этого является как низкая частота данной патологии, так и большая вариабельность клинических проявлений.
Без применения кардиохирургических методов в ранние сроки заболевания прогноз крайне неблагоприятен, а двухнедельная выживаемость не превышает 20 % , поэтому своевременная диагностика РАА является важнейшей задачей.
Под термином «расслаивающая аневризма аорты» подразумевают внезапное образование вследствие различных причин дефекта интимы аорты с последующим проникновением крови через этот дефект в дегенеративно измененную срединную оболочку, образованием гематомы и продольным расслоением стенки аорты.
Расслоение (диссекция) происходит преимущественно в дистальном, реже в проксимальном отделе. Гематома может развиваться по ходу аорты и закупоривать одну из ее ветвей, начиная от ветвей дуги аорты и заканчивая кишечными артериями.
Ретроградная диссекция может поражать коронарные артерии. Чаще вовлекается правая коронарная артерия. Ретроградное расслоение может привести к нарушению прочности одной или нескольких створок аортального клапана и его недостаточности.
Ложный канал располагается в наружной половине средней оболочки аорты. Наружная его стенка составляет всего четверть первоначальной толщины стенки аорты. Это является причиной частых разрывов аорты у больных с расслаивающей аневризмой.
Разрыв аневризмы дуги аорты происходит чаще всего в полость средостения, разрыв нисходящей аорты — в левую плевральную полость, брюшной аорты — в забрюшинную клетчатку. Так как париетальный перикард прикрепляется к восходящей части аорты, непосредственно проксимальнее места отхождения плечеголовного ствола, разрыв любого отдела восходящей части аорты может привести к тампонаде перикарда.
Классификации расслаивающих аневризм аорты обычно основаны на локализации проксимального разрыва внутренней оболочки аорты и протяженности расслоения стенки аорты. Поскольку разрыв внутренней оболочки аорты может теоретически произойти в любом сегменте и быть множественным, варианты расслоения аорты весьма разнообразны.
Однако на практике разрыв внутренней оболочки чаще всего происходит в передней стенке восходящей части аорты на границе проксимальной и средней трети, а также в начальном сегменте нисходящей части аорты дистальнее русла левой подключичной артерии.
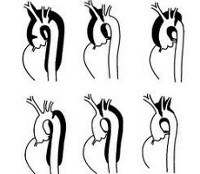
Именно на этом принципе основана простая и широко распространенная Стэндфордская классификация, согласно которой выделяют несколько типов расслоения:
- тип А — разрыв интимы находится в восходящей аорте с поражением дуги или нисходящей аорты, или без них;
- тип В — надрыв находится в нисходящей аорте, при этом расслоение распространяется проксимально и дистально.
Для определения прогноза болезни и выработки консервативной и оперативной тактики в клинике применяется модификация классификации М. DeBakey:
- тип I — разрыв внутренней оболочки локализуется в восходящей части аорты, а расслоение ее стенок распространяется до брюшной части аорты;
- тип II — разрыв внутренней оболочки локализуется в восходящей части аорты, расслоение заканчивается слепым мешком проксимальнее плечеголовного ствола;
- тип III — разрыв внутренней оболочки аорты локализуется в начальном отделе нисходящей части грудной аорты дистальнее устья левой подключичной артерии.
Классификация расслаивающей аневризмы аорты
Согласно другой классификации, выделяют пять классов диссекции аорты.
- К 1-му классу относят классическое расслоение аорты с формированием ложного и истинного ходов без образования сообщения между ними,
- к 2-му— интрамуральную гематому или кровоизлияние,
- к 3-му — пенетрирующее изъявление атеросклеротической бляшки стенки аорты вследствие надрыва ее капсулы,
- к 4-му — небольшие ограниченные или частичные диссекции аорты с образованием выпячивания ее стенки
- к 5-му — ятрогенные или посттравматические диссекции аорты (например, расслоение аорты проведенным в нее для катетеризации сердца катетером).
Классификация диссекций аорты по L. G. Svensson и соавт.
Разрыв интимы, являющийся началом расслаивающей аневризмы, обнаруживается в восходящей части аорты примерно в 70 % случаев. В 10 % случаев его находят в дуге, в 20 % — в нисходящей части грудной аорты. В редких случаях наблюдается надрыв интимы брюшной аорты.
Диссекция (расслоение) аорты может быть острой (до 2 недель) и хронической (более 2 недель).
Распространенность РАА оценивается в среднем как 1 на 10 000 госпитализированных (однако значительная часть больных погибает на догоспитальном этапе). Данная патология является причиной 1,1 % случаев внезапной смерти и 3-4 % случаев всех внезапных смертей от сердечно-сосудистых заболеваний; выявляется в 1 случае на 400 аутопсий.
К предрасполагающим факторам расслоений аорты относятся заболевания и состояния, сопровождающиеся кистозной дегенерацией медии:
- длительно существующая артериальная гипертензия,
- врожденные дефекты соединительной ткани (синдромы Марфана, Элерса — Данлоса, Тернера),
- поликистозная болезнь почек,
- пожилой возраст (60-70 лет);
- врожденные пороки сердца (коарктация аорты, бикуспидальный или одностворчатый клапан);
- атеросклероз аорты;
- беременность;
- травма грудной клетки,
- сильное физическое и эмоциональное напряжение;
- системные васкулиты (особенно часто гранулематозный, гигантоклеточный артериит);
- химические и токсические воздействия (наркотики, например, кокаин);
- ятрогенные причины.
Наиболее частыми симптомами при РАА являются внезапное начало боли с молниеносным достижением максимальной интенсивности, локализация боли в грудной клетке, боль в спине. Боль описывается пациентами как очень интенсивная или нестерпимая, самая сильная боль, которую они когда-либо испытывали, боль острая или рвущая.
У значительной части пациентов могут наблюдаться те или иные изменения сегмента ST или зубца Т.
При проксимальном типе расслоения может выслушиваться шум аортальной регургитации.
Как при проксимальном, так и при дистальном типе расслоения может определяться асимметрия пульса (снижение его наполнения или отсутствие) и артериального давления на верхних или нижних конечностях.
У части пациентов могут выявляться те или иные неврологические нарушения.
Относительно редко встречается вторичный (чаще всего задненижний) инфаркт миокарда, связанный с распространением расслоения на устье коронарной артерии.
К заболеваниям, имеющим сходную с РАА клиническую картину, относятся:
- острый коронарный синдром;
- аортальная недостаточность без диссекции (расслоения);
- аневризма аорты без диссекции (расслоения);
- костно-мышечные;
- перикардит;
- опухоль средостения;
- плеврит;
- тромбоэмболия легочной артерии;
- холецистит.
Наличие РАА можно подозревать, если у пациента имеется боль; боль в сочетании с обмороком (синкопе); боль в сочетании с симптомами сердечной недостаточности; боль в сочетании с симптомами поражения ЦНС (инсульт); сердечная недостаточность без болевого синдрома; симптомы поражения ЦНС (инсульт) без болевого синдрома; изменения на рентгенограмме органов грудной клетки без болевого синдрома; отсутствие пульса без болевого синдрома.
Согласно рекомендациям рабочей группы Европейского общества кардиологов, для подтверждения диагноза, уточнения типа расслоения (локализация, протяженность), диагностики и уточнения тяжести аортальной недостаточности и диагностики экстравазации (периаортальная или медиастинальная гематома, плевральный или перикардиальный выпот) предпочтение следует отдавать трансторакальной ЭхоКГ с последующей трансэзофагеальной ЭхоКГ и внутрисосудистым УЗИ, мультиспиральной компьютерной томографии или магнитно-резонансной томографии.
Ангиография может проводиться для определения анатомического субстрата при планируемом чрескожном вмешательстве у гемодинамически стабильных и нестабильных пациентов, но не рутинно. Рентгенография грудной клетки не дает дополнительной информации.
Ниже представлены начальные лечебно-диагностические мероприятия, которые следует проводить при подозрении на РАА в соответствии с рекомендациями группы экспертов Европейского общества кардиологов.
- Сбор детального анамнеза и полный осмотр (при возможности).
- Обеспечение венозного доступа, анализы крови (ОАК, КФК, тропонин I (Т), Д-димер, гематокрит, липиды).
- Мониторирование артериального давления и ЭКГ.
- Снижение систолического артериального давления, предпочтительно β-адреноблокаторы (пропранолол, метопролол, эсмолол), при противопоказаниях — антагонисты кальция.
- При тяжелой артериальной гипертензии дополнительно вазодилататоры.
- Трансторакальная (трансэзофагеальная) ЭхоКГ.
Всем пациентам с расслаивающей аневризмой аорты показано хирургическое лечение.
Представляем клинический пример прижизненной диагностики РАА на основании особенностей течения заболевания и клинической картины.
Пациентка А., 59 лет. Жалоб в момент поступления нет. Ранее сердечно-сосудистых заболеваний не переносила.
Впервые за 3 дня до обращения в стационар возникла колющая, пронизывающая боль умеренной интенсивности в области сердца и между лопатками без связи с физической нагрузкой и движением, усиливавшаяся при пальпации, сохранялась несколько часов после самостоятельного приема анальгетиков. Повторный подобный приступ развился накануне поступления в стационар.
Консультирована неврологом, высказано предположение о вертеброгенной торакалгии. Проведена ЭКГ, выявлены изменения (отрицательные зубцы Т в отведениях III и aVF), по поводу которых пациентка направлена в стационар с диагнозом: «ИБС. Заднедиафрагмальный инфаркт миокарда».
При объективном обследовании обращал на себя внимание умеренно интенсивный диастолический шум, выслушивавшийся над аортой и по правому краю грудины.
С учетом острого характера и длительности боли в грудной клетке в сочетании с выявленными признаками аортальной недостаточности, предположительно остро развившейся (не было сведений о существовавшем ранее пороке сердца, границы сердца в пределах нормы, отсутствовали признаки хронической сердечной недостаточности) было высказано предположение о наличии РАА восходящего отдела аорты.
Пациентка была госпитализирована в ОРИТ, где планировалось начать инфузию эсмолола, провести трансторакальную и, при необходимости, трансэзофагеальную ЭхоКГ.
Через 10 мин после поступления больная внезапно потеряла сознание, диагностировано прекращение кровообращения (электромеханическая диссоциация). Реанимационные мероприятия безуспешны.
Диагноз: «Расслаивающая аневризма восходящей аорты. Гемоперикард. Тампонада сердца».
При патологоанатомическом исследовании было обнаружено непротяженное расслоение восходящей аорты с надклапанным разрывом и кровоизлиянием в полость перикарда.
П. В. Долотовская, И. В. Грайфер, С. В. Ефремов, Н. В. Фурман
источник
Расслаивающая аневризма аорты – внезапное образование дефекта внутренней оболочки стенки аорты с последующим проникновением потока крови в дегенеративно-измененный средний слой, образованием внутристеночной гематомы и продольным расслоением стенки аорты.
Тип I — разрыв внутренней оболочки локализуется в восходящей части аорты, а расслоение её стенок распространяется до брюшной части. Патологический процесс имеет два варианта:
а) расслоение стенки заканчивается слепым мешком в дистальных отделах аорты;
б) имеется второй – дистальный разрыв аорты (дистальная фенестрация).
Тип II — разрыв внутренней оболочки локализуется в восходящей части аорты, расслоение заканчивается слепым мешком проксимальнее плечеголовного ствола.
Тип III — разрыв внутренней оболочки локализуется в начальном отделе нисходящей части грудной аорты дистальнее устья левой подключичной артерии. Процесс расслоения имеет 4 варианта:
а) заканчивается слепым мешком выше диафрагмы;
б) заканчивается слепым мешком в дистальных отделах брюшной части аорты;
в) направлено не только дистально, но и распространяется ретроградно на дугу и восходящую часть аорты, заканчиваясь слепыми мешками;
г) распространяется на брюшную часть аорты с развитием дистальной фенестрации.
Принято считать, что основной причиной расслоения стенки аорты является артериальная гипертензия, поскольку 84% больных имеют повышенные цифры артериального давления. Однако артериальная гипертензия и гемодинамические особенности различных сегментов аорты могут привести к подобным изменениям только при дегенеративных изменениях ее средней оболочки, мышечных и эластических ее структур. Последнее может быть вызвано различными этиологическими факторами: атеросклерозом, фиброзной дисплазией, идиопатическим медионекрозом, генетическим дефектом эластических структур (болезнь Марфана), гормональными изменениями в них, характерными для последнего триместра беременности. В последние годы в связи с развитием ангиографии и методов баллонной дилатации выделяют еще одну группу расслаивающих аневризм аорты и ее ветвей — ятрогенные аневризмы.

При разнообразных процессах в аорте этиологические факторы повышения артериального давления и дегенеративных изменений средней оболочки имеют различное значение. Так, например, расслаивающая аневризма при беременности, болезни Кушинга, феохромоцитоме в основном обусловлено «кризовыми» подъемами артериального давления. Расслоение при коарктации, так же как и при атеросклерозе, обусловлено обычно и высоким артериальным давлением, и дегенеративными изменениями стенки аорты. У больных моложе 40 лет расслоение аорты чаще всего обусловлено врожденными и генетическими изменениями в стенке аорты, нежели нарушениями гемодинамики. Ятрогенные причины повреждения сосудистой стенки (при ангиографии, баллонной дилатации, канюляции аорты при проведении ИК или введении кардиоплегического раствора) зависят только от технических погрешностей и не связаны ни с уровнем давления, ни с дегенеративными изменениями стенки кровеносного сосуда.
Выделяют три основных фактора:
- расслоение артериальной стенки;
- развитие обширной внутристеночной гематомы;
- сдавление или отрыв многочисленных ветвей аорты, снабжающих кровью жизненно важные органы (миокард, головной или спинной мозг, почки), с последующей их ишемией.
Возможны несколько вариантов течения расслоения артериальной стенки:
- ложный просвет полностью заполняется тромбом и при отсутствии симптомов компрессии соседних органов может наступить «самоизлечение»;
- расслоение стенки прекращается на том или ином уровне с неизмененной стенкой, однако всегда имеется опасность расширения ложного просвета с последующим разрывом наружных стенок аорты;
- при расслоении стенки аорты может произойти вторичный — дистальный — разрыв внутренней оболочки сосуда с образованием дистальной фенестрации. Вторая фенестрация снижает «напряженность» внутристеночной гематомы и прекращает процесс более дистального расслоения. Однако это важно только в период острой стадии развития процесса. В хронической стадии фактор сохранения кровотока по ложному просвету аорты всегда создает опасность увеличения его размеров и разрыва, даже в случае устранения проксимальной фенестрации оперативным путем;
- больной может умереть либо вследствие разрыва стенки аорты и внутреннего кровотечения, либо вследствие острой окклюзии магистральных артерий, снабжающих кровью миокард, мозг, почки, органы брюшной полости.
Симптомы расслоения сосудистой стенки разнообразны и могут имитировать практически все сердечно-сосудистые, а также неврологические, урологические заболевания. Клиническая картина обусловлена локализацией первичной фенестрации аорты и протяженностью процесса расслоения. Расслоение — процесс динамический и при более или менее продолжительном наблюдении за больным в финальной стадии болезни клиническая картина может значительно отличаться от первоначальной.
Процесс может иметь три формы течения:
- острую (до 2 суток);
- подострую (до 2-4 недели);
- хроническую (месяцы и даже годы).
В анамнезе обычно отмечается артериальная гипертензия. Наиболее частым симптомом расслоения аорты является боль настолько интенсивная, что нередко вызывает коллаптоидное состояние. Падение артериального давления приостанавливает процесс расслоения аорты, что несколько снижает интенсивность болей и стабилизирует общее состояние больных. Волнообразное течение болезни вновь приводит к повышению артериального давления и продолжению расслоения стенки аорты. При этом характер болевого синдрома по своей первичной локализации и иррадиации в значительной степени меняется.
При II типе расслоения боль обычно локализуется за грудиной и имитирует острый инфаркт миокарда. Эта ситуация особенно часто наблюдается в тех случаях, когда расслоение в действительности распространяется на корень аорты и способствует компрессии коронарных артерий. Болевой синдром действительно имеет коронарный генез. При дальнейшем расслоении аорты I типа боль «перемещается» в межлопаточную область, а затем постепенно «спускается» по позвоночнику в поясничную область.
При аневризмах III типа первоначально боль локализуется в межлопаточной области. Больные сравнивают ее с кинжальным ударом в спину. Боль иррадиирует в левую руку, левую половину грудной клетки, распространяется на поясницу. При распространении процесса расслоения на брюшную часть аорты при аневризмах I и III типа боль появляется в области эпигастрия, гипогастрия или же локализуется в поясничной области. При ретроградном расслоении аневризм III типа боль может носить загрудинный инфарктоподобный характер и иррадиировать в шею, что обусловлено расслоением дуги аорты. Значительно реже расслоение аорты протекает с малоинтенсивными болями. У ряда больных расслоение аорты протекает практически асимптомно и первыми признаками болезни являются симптомы ишемии головного или спинного мозга, аортальной недостаточности, ишемии почек, органов пищеварения и нижних конечностей. Нередко первым признаком расслоения бывает развитие пульсирующего образования в животе, трактующееся как аневризма брюшной части аорты.
Расслоение ветвей дуги и нисходящей грудной и брюшной отделов аорты может сопровождаться: 1) острой, а затем хронической ишемией головного или спинного мозга; 2) острой ишемией органов пищеварения; 3) стабильной вазоренальной гипертензией или инфарктом почки; 4) острой ишемией нижних конечностей. В связи с этим больным могут ставить самые различные диагнозы — инсульт, тромбоз мезентериальных сосудов, почечная колика, тромбоэмболия бифуркации аорты; и госпитализировать их в стационары различного профиля.
При остром развитии болезни и прорыве аневризмы в полость перикарда, плевральную полость или забрюшинное пространство первыми клиническими признаками могут быть боль и типичная картина внутреннего кровотечения.
Симптомы компрессии соседних органов, характерные для истинных аневризм грудной части аорты, могут развиваться и при расслаивающих аневризмах аорты. При аневризмах II типа нередко отмечаются симптомы венозной гипертензии головы, шеи, верхних конечностей, связанные со сдавлением верхней полой вены. При аневризмах I типа с расслоением дуги аорты могут появляться симптомы, связанные с компрессией трахеи, левого бронха (одышка, стридор, частые пневмонии) и возвратного нерва (осиплость голоса, сухой кашель).
В некоторых случаях клиническая картина при расслаивающей аневризме грудного отдела аорты имеет сходство с клинической картиной инфаркта миокарда, а при расслаивании брюшного отдела аорты — с картиной почечной колики. Начало боли при расслаивании аневризмы аорты обычно острое, внезапное, тогда как при острой коронарной недостаточности боль может нарастать постепенно. Большое значение имеет локализация боли: при расслаивающей аневризме аорты боль редко иррадиирует в руки, и локализация боли может меняться с постепенным движением боли по спине, вдоль позвоночника по ходу расслоения аорты; постепенно болевые ощущения могут распространяться в нижние отделы живота и малый таз.
При истинной почечной колике обычно характерны дизурические явления и другие симптомы. Доказательством наличия расслаивающей аневризмы аорты служит и появление вслед за болью симптомов, связанных с распространением расслоения аорты в области отхождения магистрального сосуда или нескольких сосудов (асимметрия пульса на верхних и нижних конечностях, гемипарез, параплегия или инсульт, боль в поясничной области, гематурия, отек мошонки). Известны и разнообразные «периферические сосудистые маски» заболевания (по типу синдрома Такаясу), а также «пневмонические», желудочно-кишечные (по типу острого живота).
Типичны острое начало болезни, указания в анамнезе на артериальную гипертензию, имеются внешние признаки болезни Марфана. При стандартном осмотре более чем у половины больных отмечается асимметрия пульсации и уровня артериального давления на верхних и нижних конечностях. В ряде случаев пульс не определяется; отмечаются признаки острой или хронической ишемии. Чаще снижение пульса и давления отмечается на левых конечностях. При перкуссии может определяться расширение средостения вправо или влево. Аускультативно над восходящей частью аорты при I-II типе расслоения аорты выслушивается систолический шум. Почти у половины таких больных отмечаются признаки аортальной недостаточности — диастолический шум и снижение уровня диастолического артериального давления. В ряде случаев над областью сердца выслушивается шум трения перикарда. При распространении расслоения на нисходящую часть аорты систолический шум может определяться сзади в межлопаточной области и паравертебрально слева в поясничной области. При этом шум выслушивается над брюшной частью аорты и в области эпигастрия. Выявление пульсации сонных артерий и систолического шума над ними позволяет определить вовлечение в процесс ветвей дуги аорты. Важным для постановки диагноза аневризм I и III типа с распространением расслоения на брюшную часть аорты является пальпаторное определение ее пульсации, которая может быть усилена. Аорта при пальпации расширена, мягкая на ощупь, податлива за счет увеличения в основном ложного просвета. Могут определяться и большие ложные аневризмы брюшной части, обычно неотделимые от реберной дуги.
Результаты электрокардиографии служат в основном двум целям: установить или исключить острый инфаркт миокарда (данный диагноз ставится практически у 90% больных с расслоением аорты). Если имеются признаки острого инфаркта миокарда, данные ЭКГ обязательно необходимо сопоставить с данными рентгенографии органов грудной клетки, поскольку расширение тени восходящей части аорты позволяет предположить у больного расслаивающую аневризму I-II типа с вовлечением в процесс устьев коронарных артерий. Кроме того, признаки острой коронарной недостаточности определяют как тактику подготовки больного к операции при наличии расслоения аорты, так и ее характер.
Фонокардиография подтверждает данные аускультации и позволяет зафиксировать у больного развитие аортальной недостаточности. Объемная сфигмография и ультразвуковая допплерография позволяют выявить «заинтересованность» магистральных артерий конечностей, уточнить распространенность процесса, особенности кровоснабжения головного мозга, а также вовлечение в процесс, расслоение сонных и позвоночных артерий.
Большое значение в диагностике расслаивающих аневризм грудной части аорты имеет рентгенологический метод. Практически у всех больных выявляется расширение тени верхнего средостения. Расширение восходящей части аорты лучше фиксируется в левой косой проекции. В той же проекции хорошо видна и тень нисходящей части аорты. Расширение ее тени наблюдается, у 50% больных с I типом расслоения и у 100% больных с III типом расслоения. При этом отмечаются неровность контуров нисходящей части аорты и деформация ее тени. Рентгенологически может выявляться жидкость в полости перикарда и в плевральной полости, причем даже в хронической стадии процесса. Для уточнения диагноза большую роль имеет динамическое рентгенологическое исследование.
Эхокардиография позволяет достаточно четко фиксировать двойной просвет восходящей аорты, а также состояние аортального клапана и наличие перикардиального выпота при угрожающем разрыве аорты.
Высокими информативными возможностями обладает в диагностике расслаивающих аневризм и компьютерная томография с одновременным введением рентгеноконтрастного вещества. Она позволяет дифференцировать тромбоз обычной аневризмы грудной части аорты от тромбоза ложного просвета при ее расслоении.
Заключительным методом диагностики является тотальная аортография. Ее особенности заключаются в том, что при трансфеморальном доступе катетер в ряде случаев не попадает в истинный просвет аорты, в связи с чем информативность метода значительно снижается. В подобных случаях лучше использовать трансаксиллярный доступ справа. Цель ангиографического исследования — определить точное место проксимальной фенестрации, протяженность расслоения, «заинтересованность» ветвей аорты и наличие или отсутствие дистальной фенестрации. Не все ангиографические признаки расслоения аорты могут быть получены в 100% случаев. Наиболее достоверный признак — расширение и деформация тени аорты. Этот признак позволяет диагностировать проксимальный уровень расслоения и его протяженность. Частым признаком (примерно у 75% больных) является одновременное контрастирование истинного и ложного просветов аорты. Чаще удается фиксировать ложный просвет в нисходящей части аорты. Истинный просвет аорты нередко значительно сужен. В 10-15% случаев ложный просвет может быть тромбирован, причем вероятность тромбоза возрастает в дистальном направлении. Однако наличие в этом сегменте стенозирования истинного просвета свидетельствует о тромбировании ложного просвета. Истинный просвет обычно носит спиралеобразный ход в нисходящей части аорты, что характерно для расслоения. У некоторых больных при аортографии фиксируется четкая разделительная полоса — отслоенная внутренняя оболочка — между истинным и ложным просветом. Уровень проксимальной фенестрации обычно определяется наличием сброса рентгеноконтрастного вещества в резко расширенный ложный просвет. В ряде случаев этот сброс не удается фиксировать, и по контуру истинного просвета аорты выявляется лишь небольшой дефект наполнения.
Одним из признаков расслоения является отрыв ветвей дуги и брюшной части аорты от истинного просвета. Если ветви аорты контрастируются одновременно с контрастированием истинного просвета, то это свидетельствует об их нормальном отхождении. Если контрастирование запаздывает или вообще отсутствует, следует думать об их отрыве. В подобных случаях необходимо дополнить исследование контрастированием ложного просвета аорты. Во-первых, это четче позволит определить размеры ложного просвета, степень его тромбоза и, во-вторых, выявить проходимость отходящих от ложного просвета ветвей аорты. При ангиографии корня аорты удается фиксировать регургитацию контрастного вещества из аорты в левый желудочек, что свидетельствует о той или иной степени аортальной недостаточности. Это осложнение обнаруживается примерно у 50% больных с расслоением восходящей части аорты. При II типе расслоения подобная недостаточность встречается в 2 раза чаще, чем при I типе.
При естественном течении расслаивающих аневризм грудной части треть больных погибает в течение первых суток, только 10% доживает до 3 месяцев с момента возникновения заболевания. 80% больных, переживших острую и подострую стадии болезни, остаются живы в течение 1-3 лет. Все больные с развитием проксимальной фенестрации в восходящей части аорты погибают в течение первого месяца болезни.
Хирургическое лечение более эффективно у больных с расслоением аорты I-II типа, консервативное при III типе.
При консервативном ведении: основной причиной смерти больных с I-II типом расслоения является тампонада сердца, менее частая причина — окклюзия магистральных ветвей аорты. У больных с III типом расслоения основной причиной смерти является кровотечение в левую плевральную полость и почечная недостаточность. Последняя развивается не только в результате окклюзии почечных артерий из-за расслоения брюшного отдела, но и воздействия проводимой гипотензивной терапии.
В настоящее время при остром расслоении грудной части аорты наиболее рациональным является дифференцированный подход к тактике лечения в зависимости от типа расслоения и развития осложнений. Лекарственная терапия показана больным с различными типами расслоения аорты как начальный этап лечения, до момента проведения аортографии и обеспечения оперативного лечения. Срочная операция необходима при угрожающем разрыве аневризмы, прогрессирующем расслоении, выраженной аортальной недостаточности, при образовании мешковидной аневризмы, а также при неэффективности проводимой терапии, не снимающей болевого синдрома, и при «неуправляемой» гипертензии. Показанием к операции является также наличие крови в перикарде или плевральной полости.
Лекарственная терапия в острой и подострой стадиях болезни рекомендуется больным с III типом расслоения, пациентам с предполагаемым I типом расслоения, но при стабильном течении процесса, больным с высокими факторами риска (обычно старше 50 лет), а также в тех случаях, когда место фенестрации не удается выявить на аортограмме и при отсутствии контрастирования ложного канала. Следует также придерживаться консервативного метода лечения при ее эффективности у больных, у которых с момента расслоения прошло более 14 дней. Основной целью лекарственной терапии являются предотвращение прогрессирования расслоения аорты и нормализация гемодинамики и гомеостаза. Для этого проводится управляемая гипотензия. Необходимы постоянный контроль за уровнем артериального давления, диуреза, мониторирование ЭКГ. Каждые 12 часов проводится рентгенологический контроль грудной клетки с целью выявления динамики размеров аневризмы и наличия жидкости в плевральных полостях и перикарде. Как показывает опыт, риск операций, производимых в хронической стадии процесса при стабилизации гемодинамики и гомеостаза, а также вследствие укрепления наружных слоев аорты в сегменте расслоения, значительно уменьшается, чем в острой и подострой стадиях.
- к основным целям лечения относят снижение АД и сократимости миокарда;
- желаемый уровень систолического АД – 100-120 мм рт. ст. или самый низкий уровень, не вызывающий ишемии сердца, головного мозга и почек у страдающих гипертонией;
- для быстрого снижения высокого АД прибегают к внутривенной инфузии нитропруссида натрия или нитроглицерина при обязательном одновременном применении β-блокатора;
- для быстрого снижения сократимости миокарда производят внутривенное введение β-блокаторов в возрастающей дозе до достижения ЧСС 50–60 в минуту;
- обеих целей можно добиться при помощи лабетолола (10 мг внутривенно в течение 2 минут, далее 20-80 мг каждые 10-15 мин до максимальной дозы 300 мг, в качестве поддерживающей меры – инфузии 2-20 мг в минуту);
- при противопоказаниях к β-блокаторам можно использовать антагонисты кальция, замедляющие ритм сердца (верапамил, дилтиазем);
- прием короткодействующих препаратов нифедипина внутрь или под язык может привести к быстрому снижению АД даже в рефрактерных случаях, однако сопряжено с риском возникновения рефлекторной тахикардии, по-видимому, эти средства не следует назначать без предварительного введения β-блокатора;
- при вовлечении в расслоение артерий почек для снижения АД наиболее эффективным может быть внутривенное введение ингибитора ангиотензин–превращающего фермента (эналаприл 0,625 — 5 мг каждые 4 – 6 ч);
- при клинически значимой гипотонии необходимо быстрое внутривенное введение жидкости; в рефрактерных случаях проводится инфузия прессорных агентов (предпочтительнее — норадреналина; допамин применяется только в низких дозах для стимуляции мочеотделения).
Тем не менее хирургическое лечение показано больным с I-II типом расслоения сразу же после стабилизации гомеостаза в связи с непредсказуемым развитием осложнений. Помимо указанных признаков угрожающих осложнений, важным симптомом для решения вопроса о срочной операции являются симптомы острой окклюзии ветвей аорты, снабжающих кровью жизненно важные органы (мозг, почки, висцеральные органы). При угрозе разрыва аорты операция показана по витальным показаниям. Для больных с III типом расслоения операцию чаще следует производить в хронической стадии процесса, преимущественно у больных не старше 50 лет, при аневризме только грудной части аорты либо мешковидных аневризмах брюшной части аорты, сочетающихся с болевым синдромом, при синдроме хронической ишемии органов пищеварения, вазоренальной гипертензии и ишемии нижних конечностей.
При тяжелых сопутствующих заболеваниях у больных пожилого возраста следует предпочесть лекарственную терапию, если она эффективна.
Техника операций при расслаивающих аневризмах I-II типа аналогична таковой при обычных аневризмах восходящей части аорты. При наличии расслоения аорты швы накладывают так, чтобы ликвидировать ложный просвет в ее стенке. Операции направлены на устранение проксимальной фенестрации в аорте. При развитии острой аортальной недостаточности восходящую часть аорты протезируют с помощью специального «кондуита», содержащего протез клапана. Для лучшей герметизации швов дистального анастомоза можно использовать специальный клей, заливаемый между расслоенными слоями сосудистой стенки.
При расслоении I типа, симптомах ишемии мозга вследствие окклюзии ветвей дуги аорты показано одновременное протезирование восходящей части и ее дуги с имплантацией брахиоцефальных сосудов в протез или их протезирование. При симптомах, характерных для расслоения брюшной части аорты и ее ветвей, не исчезающих и даже усугубляющихся после устранения проксимальной фенестрации расслоения, вторым этапом показана операция на брюшной части и ее ветвях. Второй этап операции направлен обычно на резекцию больших ложных аневризм брюшной части, а также на реваскуляризацию почек, органов брюшной полости и нижних конечностей.
При расслаивающих аневризмах III типа устранение только проксимальной фенестрации с протезированием грудного отдела следует считать радикальной при ограниченном участке поражения, не переходящем на брюшную часть аорты. Если расслоение распространяется на брюшную часть аорты, то устранение ложного просвета при протезировании грудной части аорты приводит часто к ишемии почек вследствие редукции кровотока по ложному просвету, от которого чаще отходит левая почечная артерия. Современная тактика при подобных операциях должна заключаться в одномоментной реконструкции всей нисходящей части и ее магистральных ветвей. Метод операции при этом по доступу к аорте и условиям ее проведения практически не отличается от такового при аневризме грудной и брюшной частей аорты, но требует некоторой детализации. В грудной части межреберные артерии обычно не вовлечены в процесс расслоения, так как ложный просвет расположен по переднелатеральной стенке аорты. В брюшной части ложный просвет в 85% случаев располагается слева. Именно поэтому левая почечная артерия значительно чаще отходит от ложного просвета аорты, чем правая. Устья висцеральных артерий могут быть вовлечены в процесс расслоения, но чаще отходят от истинного просвета. Они обычно расположены близко друг к другу и поэтому могут быть имплантированы в протез на одной площадке.
Сосуд пережимают и рассекают в продольном направлении. Внутреннюю оболочку между истинным и ложным просветом иссекают на всем протяжении. Площадку с межреберными артериями вшивают в окно протеза по задней его поверхности. По описанному методу на площадке имплантируют ветви брюшной части аорты. Отдельно вшивают на площадке устье левой почечной артерии. В случаях острого расслоения в связи со слабостью стенок аорты производится устранение проксимальной фенестрации аорты.
Учитывая, что кровоснабжение спинного мозга в основном осуществляется через артерию Адамкевича, которая чаще всего расположена на уровне Х-XI грудного позвонка, можно использовать несколько видоизмененный метод сохранения кровотока по спинномозговым ветвям. Четыре-пять пар верхних межреберных артерий можно перевязать. Из площадки нижнего сегмента грудного отдела с устьями межреберных артерий на уровне VIII-XII грудных позвонков создается слепой канал, открытый в просвет аорты. Именно в этом месте накладывается дистальный анастомоз протеза с аортой. В тех случаях, когда винтообразный ход расслоения грудной аорты выглядит таким образом, что нижние межреберные и верхние поясничные артерии, а также чревный ствол и верхняя брыжеечная артерия отходят от истинного просвета аорты, радикальную коррекцию аневризмы грудной и брюшной частей аорты производят одномоментно. При этом можно раздельно протезировать грудную часть аорты с целью ликвидации ложного просвета и проксимальной фенестрации, а затем произвести резекцию аневризмы брюшной части с протезированием и реваскуляризацией почек.
источник
Расслаивающая аневризма аорты – дефект внутренней оболочки аневризматически расширенной аорты, сопровождающийся образованием гематомы, продольно расслаивающей сосудистую стенку с формированием ложного канала. Расслаивающая аневризма аорты проявляется внезапной интенсивной болью, мигрирующей по ходу расслоения, подъемом артериального давления, признаками ишемии сердца, головного и спинного мозга, почек, внутреннего кровотечения. Диагноз расслоения сосудистой стенки основан на данных ЭхоКГ, КТ и МРТ грудной/брюшной аорты, аортографии. Лечение осложненной аневризмы включает интенсивную медикаментозную терапию, резекцию поврежденного участка аорты с последующей реконструктивной пластикой.
Расслаивающая аневризма аорты – продольное расслоение стенки аорты в дистальном или проксимальном направлении на различном протяжении, обусловленное разрывом ее внутренней оболочки и проникновением крови в толщу дегенеративно-измененного среднего слоя. Расширение аорты при расслаивании ее стенки может носить умеренный характер или отсутствовать, поэтому расслаивающую аневризму аорты часто называют расслоением аорты.
Большинство аневризм локализуются в наиболее гемодинамически уязвимых зонах аорты: около 70% — в восходящем отделе в нескольких сантиметрах от аортального клапана, 10% случаев – в дуге, 20% — в нисходящем отделе аорты дистальнее устья левой подключичной артерии. Расслаивающая аневризма в кардиологии относится к угрожающим жизни состояниям с риском массивного кровотечения при разрыве аорты или острой ишемии жизненно важных органов (сердца, мозга, почек и др.) при окклюзии магистральных артерий. Обычно расслоение аневризмы аорты возникает в возрасте 60-70 лет, у мужчин в 2-3 раза чаще, чем у женщин.
Причинами патологии являются заболевания и состояния, приводящие к дегенеративным изменениям мышечных и эластичных структур средней оболочки аорты (медиа). Пожилой возраст пациентов (старше 60-70 лет), травмы грудной клетки, III триместр беременности у женщин старше 40 лет считаются факторами риска расслоения аневризмы аорты. К основным причинам относятся:
- Стабильно повышенное АД. Основной риск расслоения аорты связан с длительной артериальной гипертензией (70-90% случаев), сопровождающейся гемодинамическим напряжением и хронической травматизацией аорты.
- Наследственные дефекты соединительной ткани. Расслаивающая аневризма может развиваться как осложнение синдромов Марфана, Тернера, Элерса-Данлоса.
- Болезни сердца и сосудов. В группе риска — пациенты с аортальными пороками, коарктацией аорты, выраженным атеросклерозом аорты, системными васкулитами.
- Перенесенные кардиохирургические операции и манипуляции. В ранний и поздний послеоперационный период после хирургических вмешательств на сердце и аорте (протезирования аортального клапана, резекции аорты) существует повышенный риск расслаивания аневризм. Ятрогенные расслаивающие аневризмы связаны с техническими погрешностями при выполнении аортографии и баллонной дилатации, канюляции аорты для обеспечения искусственного кровообращения.
Первичным патогенетическим звеном в большинстве случаев является надрыв интимы с последующим образованием внутристеночной гематомы. Примерно в 10% случаев расслаивающую аневризму аорты может инициировать кровоизлияние в медиа при спонтанном разрыве капилляров, разветвляющихся в стенке аорты. Распространение интрамуральной гематомы в пределах медиа обычно сопровождается последующим разрывом интимы, но может происходить без него (в 3-13% случаев). В редких случаях расслоение аорты может наблюдаться при пенетрации атеросклеротической язвы.
Согласно классификации ДеБейки, определяют 3 типа расслоения:
- I – надрыв интимы в восходящем сегменте аорты, расслоение распространяется до грудного и брюшного отделов;
- II – место надрыва и расслоение ограничено восходящим отделом аорты,
- III – надрыв интимы в нисходящей аорте, расслоение может распространяться до дистальных отделов брюшной аорты, иногда ретроградно на дугу и восходящую часть.
Стэнфордская классификация выделяет расслаивающие аневризмы аорты типа A — с проксимальным расслоением, затрагивающим ее восходящий отдел, и типа B — с дистальным расслоением дуги и нисходящей части аорты. Тип A характеризуется более высокой частотой развития ранних осложнений и высокой догоспитальной летальностью. По течению расслаивающие аневризмы аорты могут быть острыми (от нескольких часов до 1-2 дней), подострыми (от нескольких дней до 3-4 недель) и хроническими (несколько месяцев).
Клиническая картина заболевания обусловлена наличием и протяженностью расслоения аорты, внутристеночной гематомой, сдавлением и окклюзией ветвей аорты, ишемией жизненно важных органов. Различают несколько вариантов развития расслаивающей аневризмы аорты: образование обширной непрорвавшейся гематомы; расслоение стенки и прорыв гематомы в просвет аорты; расслоение стенки и прорыв гематомы в окружающие аорту ткани; разрыв аорты без расслоения стенки.
Для расслаивающей аневризмы аорты характерно внезапное начало с имитацией симптомов различных сердечно-сосудистых, неврологических, урологических заболеваний. Расслоение аорты проявляется резким нарастанием раздирающей, нестерпимой боли с широкой областью иррадиации (за грудиной, между лопатками и по ходу позвоночника, в эпигастральной области, пояснице), мигрирующей по ходу расслоения. Отмечается повышение артериального давления с последующим спадом, асимметрия пульса на верхних и нижних конечностях, обильное потоотделение, слабость, синюшность, двигательное беспокойство. Большая часть больных с расслаивающей аневризмой аорты умирает от развития осложнений.
Неврологическими проявлениями патологии могут служить ишемическое поражение головного или спинного мозга (гемипарез, параплегия), периферическая нейропатия, нарушения сознания (обморок, кома). Расслаивающая аневризма восходящей аорты может сопровождаться ишемией миокарда, сдавлением органов средостения (появлением охриплости, дисфагии, одышки, синдрома Горнера, синдрома верхней полой вены), развитием острой аортальной регургитации, гемоперикарда, тампонады сердца. Расслоение стенок нисходящей грудной и брюшной части аорты выражается развитием тяжелой вазоренальной гипертензии и острой почечной недостаточности, острой ишемии органов пищеварения, мезентериальной ишемии, острой ишемии нижних конечностей.
При подозрении на расслаивающую аневризму аорты необходима срочная и точная оценка состояния больного. Основными методами диагностики, позволяющими визуализировать поражение аорты, являются рентгенография грудной клетки, ЭхоКГ (трансторакальная и чреспищеводная), УЗДГ, МРТ и КТ грудной/брюшной аорты, аортография.
- Рентгенография грудной клетки. Выявляет признаки спонтанного расслоения аорты: расширение аорты и верхнего средостения (в 90% случаев), деформацию тени контуров аорты или средостения, наличие плеврального выпота (чаще слева), снижение или отсутствие пульсации расширенной аорты.
- ЭхоКГ. Трансторакальная или чреспищеводная эхокардиография помогают определить состояние грудной аорты, выявить отслоившийся лоскут интимы, истинный и ложный каналы, оценить состоятельность аортального клапана, распространенность атеросклеротического поражения аорты.
- Томография. Выполнение КТ и МРТ при расслаивающей аневризме аорты требует стабильного состояния больного для транспортировки и проведения процедуры. КТ применяют для обнаружения интрамуральной гематомы, пенетрации атеросклеротических язв грудного отдела аорты. МРТ позволяет без использования внутривенного введения контрастного вещества точно определить локализацию разрыва интимы, направление расслоения по направлению кровотока в ложном канале, оценить вовлеченность основных ветвей аорты, состояние аортального клапана.
- Аортография. Является инвазивным, но высокочувствительным методом исследования расслаивающей аневризмы аорты; позволяет увидеть место начального надрыва, локализацию и протяженность расслоения, истинный и ложный просветы, наличие проксимальной и дистальной фенестрации, степень состоятельности аортального клапана и коронарных артерий, целостность ветвей аорты.
Необходимо проводить дифференциальную диагностику расслаивающей аневризмы аорты с острым инфарктом миокарда, окклюзией мезентеральных сосудов, почечной коликой, инфарктом почки, тромбоэмболией бифуркации аорты, острой аортальной недостаточностью без расслоения аорты, нерасслаивающей аневризмой грудной или брюшной аорты, инсультом, опухолью средостения.
Больных с осложненной аневризмой аорты экстренно госпитализируют в отделение кардиохирургии. Консервативная терапия показана при любых формах заболевания на начальном этапе лечения с целью остановки прогрессирования расслоения сосудистой стенки, стабилизации состояния больного. Проводится:
- Интенсивная терапия. Направлена на купирование болевого синдрома (путем введения ненаркотических и наркотических анальгетиков), выведение из шокового состояния, снижение артериального давления. Проводится мониторинг гемодинамики, сердечного ритма, диуреза, ЦВД, давления в легочной артерии. При клинически значимой гипотонии важно быстрое восстановление ОЦК за счет внутривенной инфузии растворов.
- Медикаментозное лечение. Является основным у большинства больных с неосложненными расслаивающими аневризмами типа B (с дистальным расслоением), при стабильном изолированном расслоении дуги аорты и стабильном неосложненном хроническом расслоении. При неэффективности проводимой терапии, прогрессировании расслоения и развитии осложнений, а также больным с острым проксимальным расслоением стенки аорты (типа A) сразу же после стабилизации состояния показано экстренное оперативное вмешательство.
- Оперативное лечение. При расслаивающей аневризме аорты выполняют резекцию поврежденного участка аорты с надрывом, удаление интимального лоскута, ликвидацию ложного просвета и восстановление иссеченного фрагмента аорты (иногда одномоментную реконструкцию нескольких ветвей аорты) методом протезирования или сближения концов. В большинстве случаев операция выполняется в условиях искусственного кровообращения. По показаниям осуществляют вальвулопластику или протезирование аортального клапана, реимплантацию коронарных артерий.
При отсутствии лечения расслаивающей аневризмы аорты летальность высокая, в течение первых 3 месяцев может достигать 90%. Послеоперационная выживаемость при расслоении типа A составляет 80%, типа B – 90%. Долгосрочный прогноз в целом благоприятный: десятилетняя выживаемость составляет 60%. Профилактика формирования расслаивающей аневризмы аорты заключается в контроле за течением сердечно-сосудистых заболеваний. Предупреждение расслоения аорты включает наблюдение кардиолога, мониторинг артериального давления и уровня холестерина крови, периодическое УЗДГ или УЗДС аорты.
источник
Расслаивающая аневризма аорты (dissection of the aorta) возникает, когда кровь из просвета аорты попадает внутрь ее стенки, образуя т.н. ложный канал и распространяясь по ее ходу на различную длину. Это состояние возникает остро и является жизнеугрожающим. Без лечения 25% пациентов умирают в течение 24 часов, 50% — в течение 48 часов и 1 год проживают только 10%.
На современном этапе развития медицины благодаря совершенствованию методов диагностики и лечения расслаивающая аневризма аорты превратилась из практически абсолютно фатального процесса в патологию с 75% 5-летней выживаемостью.
До сих пор широко используется оригинальная классификация расслоения аорты по DeBakey, выделяющая три ее типа:
Основываясь на различиях в клиническом течении и прогнозе, Daily предложил альтернативную классификацию, выделяющую следующие два типа расслоения аорты: Тип А — расслоение,
вовлекающее восходящую аорту (тип I и II по DeBakey). Тип В — расслоение, ограниченное нисходящей аортой (тип III по DeBakey). Расслоение считается острым, если со времени его возникновения прошло менее двух недель, хроническим — если более двух недель.
Ведущим проявлением острого расслоения аорты является внезапный приступ очень интенсивной боли в груди (в 90% случаев). Наиболее часто боль локализуется по передней поверхности грудной клетки и иррадиирует в межлопаточное пространство. Если боль ограничивается передней поверхностью грудной клетки, наиболее вероятно расслоение восходящей аорты, и если боль локализуется только в спине, наиболее вероятно расслоение нисходящей аорты.
Расслоение аорты клинически может также проявляться синкопальными состояниями, острой сердечной недостаточностью, обычно обусловленной тампонадой сердца, или острой недостаточностью аортального клапана, ДВС синдромом. Помимо того, могут наблюдаться разнообразные ишемические синдромы как следствие нарушения кровообращения по скомпрометированным расслоением артериям. Например, инфаркт миокарда, острая ишемия головного мозга, почечная недостаточность, реноваскулярная гипертензия, ишемия спинного мозга, обусловленная сдавлением передней спинномозговой артерии с моторным и сенсорным дефицитом, ишемия кишечника, ишемия конечностей, отсутствие или ослабление пульса на конечностях. Физикальное обследование
При помощи простых методов физикального обследования можно выявить повышение артериального давления, характерное для многих пациентов с расслаивающей аневризмой аорты. В случае острой сердечной недостаточности, в т.ч. при тампонаде сердца, выявляются снижение артериального давления, тахикардия, повышение центрального венозного давления, растяжение шейных вен, парадоксальный пульс. Отсутствие или ослабление пульса, которое является критерием расслоения аорты, при расслоении восходящей аорты наблюдается у 50 % пациентов, а при расслоении нисходящей аорты — у 10-15 %.
Аортальная недостаточность обнаруживается у большинства пациентов с расслоением восходящей аорты. Реже ретроградное распространение расслоения дуги или нисходящей аорты может вовлекать аортальный клапан, но в целом, она указывает на начало расслоения в восходящей аорте. Если острая значительная аортальная регургитация приводит к левожелудочковой недостаточности, увеличения пульсового давления, обычно ассоциированного с хронической аортальной недостаточностью не наблюдается. Наружный разрыв расслаивающей аневризмы в левую плевру обуславливает тупость при перкуссии легких и ослабление дыхательных шумов.
Неврологический дефицит в виде гемиплегии может быть обусловлен скомпрометированностью сонных артерий, и в виде параплегии — передней спинномозговой артерии. Значительная ишемия конечностей проявляется потерей глубоких сухожильных рефлексов, анестезией и параличом.
Общепринятым механизмом расслоения аорты считается проникновение крови из ее просвета в медию через разрыв в интиме. Поперечно ориентированный разрыв интимы в 61% случаев обнаруживается в точке, расположенной на несколько сантиметров выше аортального клапана, в 16% — между отхождением левой подключичной артерии и ligamentum arteriosum. Менее типичными местами разрыва интимы являются нисходящая аорта (9%), дуга аорты (8%) и брюшная аорта (2%).
Признается также возможность развития расслоения аорты после образования первичного кровоизлияния в медию из vasa vasorum уже со вторичным разрывом интимы. Этот механизм считают ответственным в 4% случаев обнаружения гематомы внутри стенки аорты, однако без нарушения целостности интимы. Разрыв интимы не находят также в 13% случаев расслоения нисходящей грудной или брюшной аорты. При этом какого-либо патологического процесса, ответственного за развитие разрыва интимы или кровоизлияния в медию, не находят.
Атеросклероз не оказался четким этиологическим фактором расслоения аорты и относительно его роли в нем до сих пор существуют разногласия. С одной стороны, место наиболее частого и тяжелого атеросклеротического поражения — брюшная аорта является участком самого редкого возникновения расслоения аорты, а разрывы интимы в участке аорты, пораженном атеросклерозом, обнаруживаются менее чем в 5% случаев. С другой стороны, Wilson и Hutchins, обнаружившие незначительное, но достоверное преобладание атеросклеротического поражения у пациентов с расслаивающей аневризмой против контрольной группы лиц, не исключают даже в этих случаях его вероятной роли в расслоении.
Патологические процессы в медии (некроз, эластиновая фрагментация и фиброз) изучались гистологическими методами в нормальной аорте вне признаков внешнего поражения, у пожилых людей, пациентов с аортальным стенозом, при синдроме Марфана и расслаивающей аневризме аорты. Достоверного преобладания этих процессов при расслаивающей аневризме аорты не было выявлено, хотя при ней они и были выражены значительнее. Пузырный медионекроз (cystic medionecrosis) у пациентов моложе 40 лет с расслаивающей аневризмой аорты в классической работе Schlatmann и Becker оказался единственным процессом, частота встречаемости которого не увеличивалась с возрастом. Однако альтернативное мнение существует и по этому поводу, так как другим исследователям удалось показать прогрессирование пузырного медионекроза с возрастом и при артериальной гипертензии. Хотя пузырный медионекроз часто встречается при синдроме Марфана, у некоторых пациентов с расслоением аорты при синдроме Марфана пузырного медионекроза нет.
На особом месте стоят ятрогенные причины расслоения — катетеризация сердца, установка системы для внутриаортальной баллонной контрпульсации через бедренную артерию, выполнение баллонной ангиопластики для устранения коарктации аорты. Сердечно-сосудистые оперативные вмешательства являются редкой причиной расслоения аорты. По данным Массачусетского центрального госпиталя США они наблюдаются в 0,16% случаев (24 случая на 14 877 операций), но по данным клиники Mayo этот процент может достигать 11,6%. Третей по частоте встречаемости причиной расслоения аорты после АГ и двустворчатого аортального клапана выступают кардиохирургические вмешательства.
На современном этапе принят следующий подход к лечению пациентов с острой расслаивающей аневризмой аорты. Все пациенты с диагнозом острой расслаивающей аневризмы аорты госпитализируются в реанимационное отделение специализированной кардиохирургической клиники, где начинается медикаментозная терапия, и оцениваются показания к экстренному оперативному вмешательству.
Целью медикаментозной терапии является предотвращение дальнейшего расслоения и наружного разрыва аорты. Пациентам без острой левожелудочковой недостаточности рекомендуется снизить сократимость миокарда, частоту сердечных сокращений и артериальное давление до минимально возможных значений, когда еще обеспечивается перфузия жизненно важных органов, и находятся под контролем мочеотделение и функции центральной нервной системы. Классической медикаментозной комбинацией для этой цели считается внутривенная инфузия нитропруссида натрия с b-адреноблокатором (пропранолол, эсмолол, лабеталол). Одновременное назначение этих препаратов является обязательным, т.к. нитропруссид увеличивает миокардиальную сократимость, которая нежелательна, нивелируемую b-адреноблокатором. Триметафан также эффективно снижает артериальное давление и сократимость миокарда, но по причине развивающейся к нему тахифилаксии считается препаратом второго порядка. При противопоказаниях к b-адреноблокаторам (бронхиальная астма) могут быть использованы внутривенные формы блокаторов кальциевых каналов (нифедипин), хотя по этому поводу в литературе существует мало данных.
Второй целью медикаментозной терапии на дооперационном этапе является адекватное обезболивание. Боли при расслаивающей аневризме аорты очень интенсивные и требуют введения наркотических анальгетиков. Некупирующиеся боли считаются признаком продолжающегося расслоения и являются показанием к экстренному оперативному вмешательству.
Параллельно с проводимой медикаментозной терапией требуется оценить показания к экстренному оперативному лечению. Этими показаниями считаются следующие: расслоение восходящей аорты, острая сердечная недостаточность, признаки наружного разрыва (гемоперикард, гемоторакс), нарушение кровотока по ветвям аорты, признаки прогрессирования расслоения (некупирующаяся боль, увеличение размеров аневризмы). Первой особенностью операций расслаивающих аневризмах аорты является то, что они экстренные, так как каждый час их отсрочки увеличивает вероятность гибели пациента. На подготовку пациента, как правило, времени практически не остается. При I типе расслоения, не требующем протезирования дуги аорты, и II типе выполняются следующие операции.
Операция Бенталла заключается в иссекании аортального клапана, протезировании аортального клапана и восходящей аорты (со стороны интимы) одним комбинированным протезом с ре-имплантацией коронарных сосудов в протез. В случае минимальной аортальной недостаточности или когда удается сохранить клапан путем пластической операции, выполняется супракоронарное протезирование восходящей аорты.
Обе операции длительные, трудоемкие и выполняются в условиях искусственного кровообращения. Для них типичны большие кровопотери. Особо тщательно при этих операциях требуется проводить защиту миокарда,
используя стандартные солевые кардиоплегические растворы и альтернативные методики кардиоплегии — кровяная и с перфтораном. Пациент олаждается до температуры 24-260С, что в сочетании с большой кровопотерей и длительным искусственным кровообращением дает большое число осложнений после операции, в том числе развитие ДВС синдрома. При вовлечении в расслоение дуги аорты (I тип) выполняется ее протезирование с ре-имплантацией сосудов головы и шеи (плечеголовной ствол, левая общая сонная, левая подключичная). При этом используется полная остановка кровообращения (cardiac arrest) и ретроградная перфузия головного мозга через внутренние яремные вены. В этих условиях одной из главных задач является защита головного мозга, что достигается общей глубокой гипотермией до 12-140С и применением препаратов, снижающих потребность головного мозга в кислороде (пропофол, седуксен). Длительная перфузия, полная остановка кровообращения и ретроградная перфузия неблагоприятным образом сказываются на функциях центральной нервной системы, приводя к различным осложнениям в послеоперационном периоде, от незначительной энцефалопатии до глубокой комы и отека мозга. Для коррекции этих состояний используют симптоматическую терапию, подобную к медикаментозной защите головного мозга при операциях с ретроградной перфузией.
При коррекции расслоения нисходящей грудной аорты (Ш тип расслоения) выполняется протезирование нисходящей грудной аорты с ре-имплантацией межреберных сосудов в протез. Это самые тяжелые операции. Их особенностью является наложение шунта в обход места протезирования аорты с полной остановки кровообращения на время его наложения с ретроградной перфузией головного мозга и также гипотермией до 12-140 С. Для обеспечения хирургического доступа (боковой, а не срединный, как в предыдущих случаях), выполняется однолегочная интубация, требуется защита головного мозга, как в предыдущем случае, плюс органов грудной и брюшной полости, кровоснабжаемых из выделенного участка аорты.
источник