Согласно общепринятым стандартам под аневризмой понимают локальное либо распространенное расширение артерии, превышающее более чем в 1,5 раза (на 2 см и более) его нормальный диаметр или близлежащий участок сосуда.
В зависимости от локализации выделяют следующие виды аневризм:
Восходящего отдела и дуги аорты.
По этиологии аневризмы делятся на:
а) невоспалительные (атеросклеротические; трaвматические, возникающие вследствие повреждения сосудистой стенки при колото-резаных либо пулевых ранениях);
б) воспалительные (развивающиеся при сифилисе, неспецифическом аортоартериите, а также микотические).
встречаются при коарктации аорты, синдроме Марфана, кистозном медионекрозе или болезни Эйдгеймера, синдроме Ehlers-Danlos.
В зависимости от формы аневризмы разделяют на:
По морфологии различают аневризмы:
1.Истинные (сохранены все слои сосудистой стенки).
Ложные (стенка сформирована соединительно-тканной капсулой, образованной вследствие выхода крови за пределы сосуда).
Расслаивающие (проникающие между слоями аорты).
В зависимости от клинического течения выделяют аневризмы:
По клиническим проявлениям аневризмы разделяют на:
Осложненные (расслоение стенки, разрыв).
Аневризмы грудной аорты (АГА) и торакоабдоминальной локализации представляют собой наиболее сложную в хирургическом плане и опасную по своим последствиям сосудистую патологию. Согласно данным литературы, 2-летняя выживаемость неоперированных больных с подобным заболеванием не превышает 25%, а 5-летняя — 13%, при этом более половины летальных исходов обусловлено разрывом аневризмы. Хотя достоверных данных о зависимости частоты разрыва АГА от ее размеров нет, достаточно точно установлено, что в сравнении с аневризмами брюшной аорты (АБА) риск этот значительно выше.
Основные причины развития АГА — дегенеративные процессы врожденного (синдром Марфана, коарктация аорты) либо приобретенного (артериальная гипертензия, атеросклероз) характера, изменяющие структуру и свойства мышечного, эластического и коллагенового компонентов стенки аорты. Возможны два варианта возникновения и прогрессирования АГА: с формированием аневризма-тического мешка веретенообразной или мешковидной формы; с расслоением (диссекцией) стенки аорты.
Большинство АГА протекают скрыто, поэтому первые симптомы появляются нередко достаточно поздно: при начавшемся расслоении стенки аорты либо разрыве аневризмы. Один из наиболее постоянных признаков этой патологии — боль, которая локализуется за грудиной, в области сердца, между лопаток, иррадиирует в шею. У отдельных лиц, страдающих данной патологией, отмечают одышку, сухой кашель, иногда охриплость голоса. Сосудистые шумы выявляют у 70% больных. Более чем у половины пациентов диагностируют артериальную гипертензию и ИБС. Неспецифичность всех перечисленных проявлений болезни делает проблематичным своевременное распознавание АГА на основе клинической симптоматики.
Традиционное рентгенологическое исследование органов грудной клетки позволяет у 30–48% больных заподозрить аневризму по следующим признакам: отклонение пищевода при контрастировании его Ba2SO4, расширение тени аорты и средостения, кальциноз стенки аневризмы.
Ультразвуковая диагностика АГА имеет меньшее в сравнении с распознаванием АБА значение. Более достоверную информацию дают ангиография, КТ и ЯМРТ. Они позволяют определить локализацию и размеры аневризмы, распространенность парааортальной гематомы, дифференцировать ложный и истинный просветы аорты при ее диссекции.
Наиболее информативным методом диагностики АГА считается чреспищеводная либо трансторакальная эхокардиография, чувствительность и специфичность этой неинвазивной процедуры достигает 88–98%.
Лечение АГА — хирургическое. Заключается оно в иссечении аневризмы и восстановлении кровотока путем реконструктивной операции или замещения аорты протезом. В связи с большим числом магистральных ветвей, отходящих от аорты к жизненно важным органам в этом отделе, и необходимостью сохранения данных ветвей и восстановления в них кровотока, вмешательства при аневризмах этой локализации считаются одними из самых травматичных.
Оперативные доступы. В зависимости от локализации патологического процесса применяют продольную (срединную) и поперечную (с двусторонней торакотомией) стернотомию, боковую торакотомию в четвертомпятом межреберье слева, торакофрено-люмботомию, тотальную срединную стернолапаротомию.
Операцию проводят в условиях искусственного кровообращения, умеренной фармакологической гипотонии либо временного обходного шунтирования.
источник
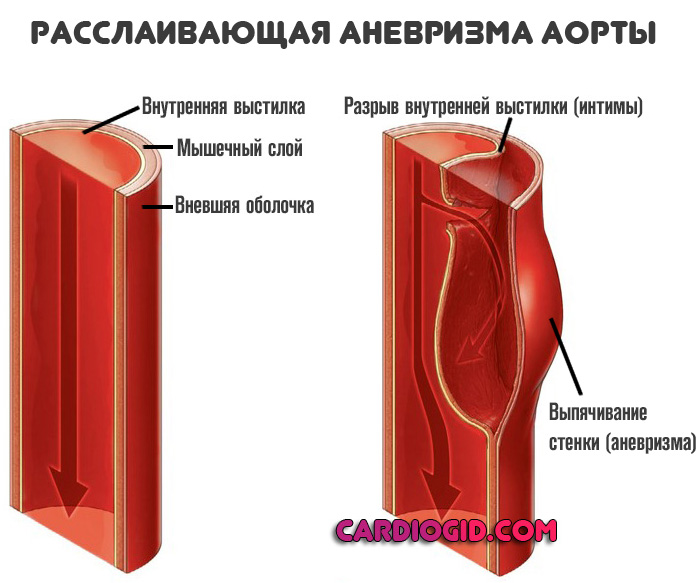
Расслаивающая аневризма аорты – внезапное образование дефекта внутренней оболочки стенки аорты с последующим проникновением потока крови в дегенеративно-измененный средний слой, образованием внутристеночной гематомы и продольным расслоением стенки аорты.
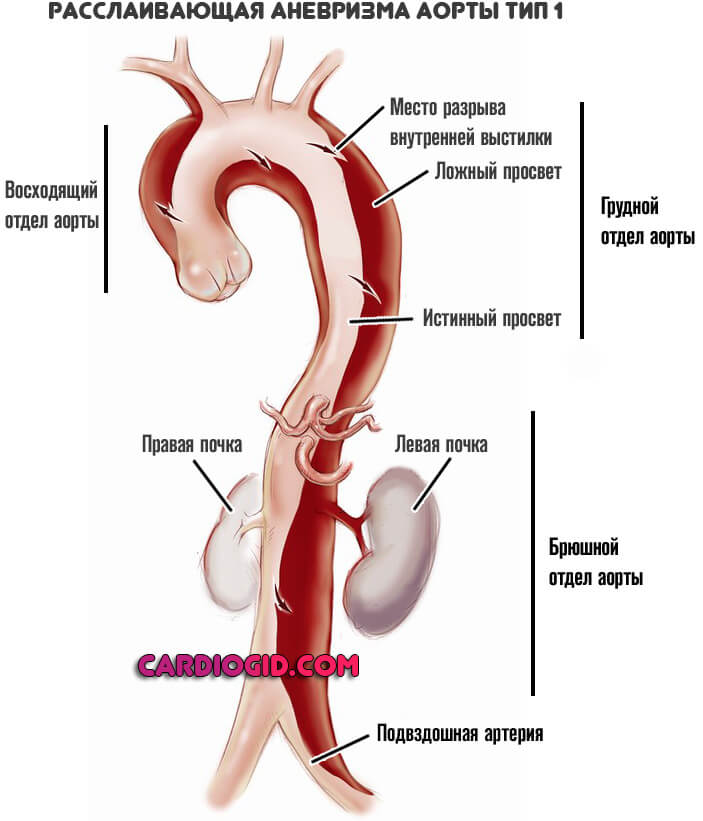
Тип I — разрыв внутренней оболочки локализуется в восходящей части аорты, а расслоение её стенок распространяется до брюшной части. Патологический процесс имеет два варианта:
а) расслоение стенки заканчивается слепым мешком в дистальных отделах аорты;
б) имеется второй – дистальный разрыв аорты (дистальная фенестрация).
Тип II — разрыв внутренней оболочки локализуется в восходящей части аорты, расслоение заканчивается слепым мешком проксимальнее плечеголовного ствола.
Тип III — разрыв внутренней оболочки локализуется в начальном отделе нисходящей части грудной аорты дистальнее устья левой подключичной артерии. Процесс расслоения имеет 4 варианта:
а) заканчивается слепым мешком выше диафрагмы;
б) заканчивается слепым мешком в дистальных отделах брюшной части аорты;
в) направлено не только дистально, но и распространяется ретроградно на дугу и восходящую часть аорты, заканчиваясь слепыми мешками;
г) распространяется на брюшную часть аорты с развитием дистальной фенестрации.
Принято считать, что основной причиной расслоения стенки аорты является артериальная гипертензия, поскольку 84% больных имеют повышенные цифры артериального давления. Однако артериальная гипертензия и гемодинамические особенности различных сегментов аорты могут привести к подобным изменениям только при дегенеративных изменениях ее средней оболочки, мышечных и эластических ее структур. Последнее может быть вызвано различными этиологическими факторами: атеросклерозом, фиброзной дисплазией, идиопатическим медионекрозом, генетическим дефектом эластических структур (болезнь Марфана), гормональными изменениями в них, характерными для последнего триместра беременности. В последние годы в связи с развитием ангиографии и методов баллонной дилатации выделяют еще одну группу расслаивающих аневризм аорты и ее ветвей — ятрогенные аневризмы.

При разнообразных процессах в аорте этиологические факторы повышения артериального давления и дегенеративных изменений средней оболочки имеют различное значение. Так, например, расслаивающая аневризма при беременности, болезни Кушинга, феохромоцитоме в основном обусловлено «кризовыми» подъемами артериального давления. Расслоение при коарктации, так же как и при атеросклерозе, обусловлено обычно и высоким артериальным давлением, и дегенеративными изменениями стенки аорты. У больных моложе 40 лет расслоение аорты чаще всего обусловлено врожденными и генетическими изменениями в стенке аорты, нежели нарушениями гемодинамики. Ятрогенные причины повреждения сосудистой стенки (при ангиографии, баллонной дилатации, канюляции аорты при проведении ИК или введении кардиоплегического раствора) зависят только от технических погрешностей и не связаны ни с уровнем давления, ни с дегенеративными изменениями стенки кровеносного сосуда.
Выделяют три основных фактора:
- расслоение артериальной стенки;
- развитие обширной внутристеночной гематомы;
- сдавление или отрыв многочисленных ветвей аорты, снабжающих кровью жизненно важные органы (миокард, головной или спинной мозг, почки), с последующей их ишемией.
Возможны несколько вариантов течения расслоения артериальной стенки:
- ложный просвет полностью заполняется тромбом и при отсутствии симптомов компрессии соседних органов может наступить «самоизлечение»;
- расслоение стенки прекращается на том или ином уровне с неизмененной стенкой, однако всегда имеется опасность расширения ложного просвета с последующим разрывом наружных стенок аорты;
- при расслоении стенки аорты может произойти вторичный — дистальный — разрыв внутренней оболочки сосуда с образованием дистальной фенестрации. Вторая фенестрация снижает «напряженность» внутристеночной гематомы и прекращает процесс более дистального расслоения. Однако это важно только в период острой стадии развития процесса. В хронической стадии фактор сохранения кровотока по ложному просвету аорты всегда создает опасность увеличения его размеров и разрыва, даже в случае устранения проксимальной фенестрации оперативным путем;
- больной может умереть либо вследствие разрыва стенки аорты и внутреннего кровотечения, либо вследствие острой окклюзии магистральных артерий, снабжающих кровью миокард, мозг, почки, органы брюшной полости.
Симптомы расслоения сосудистой стенки разнообразны и могут имитировать практически все сердечно-сосудистые, а также неврологические, урологические заболевания. Клиническая картина обусловлена локализацией первичной фенестрации аорты и протяженностью процесса расслоения. Расслоение — процесс динамический и при более или менее продолжительном наблюдении за больным в финальной стадии болезни клиническая картина может значительно отличаться от первоначальной.
Процесс может иметь три формы течения:
- острую (до 2 суток);
- подострую (до 2-4 недели);
- хроническую (месяцы и даже годы).
В анамнезе обычно отмечается артериальная гипертензия. Наиболее частым симптомом расслоения аорты является боль настолько интенсивная, что нередко вызывает коллаптоидное состояние. Падение артериального давления приостанавливает процесс расслоения аорты, что несколько снижает интенсивность болей и стабилизирует общее состояние больных. Волнообразное течение болезни вновь приводит к повышению артериального давления и продолжению расслоения стенки аорты. При этом характер болевого синдрома по своей первичной локализации и иррадиации в значительной степени меняется.
При II типе расслоения боль обычно локализуется за грудиной и имитирует острый инфаркт миокарда. Эта ситуация особенно часто наблюдается в тех случаях, когда расслоение в действительности распространяется на корень аорты и способствует компрессии коронарных артерий. Болевой синдром действительно имеет коронарный генез. При дальнейшем расслоении аорты I типа боль «перемещается» в межлопаточную область, а затем постепенно «спускается» по позвоночнику в поясничную область.
При аневризмах III типа первоначально боль локализуется в межлопаточной области. Больные сравнивают ее с кинжальным ударом в спину. Боль иррадиирует в левую руку, левую половину грудной клетки, распространяется на поясницу. При распространении процесса расслоения на брюшную часть аорты при аневризмах I и III типа боль появляется в области эпигастрия, гипогастрия или же локализуется в поясничной области. При ретроградном расслоении аневризм III типа боль может носить загрудинный инфарктоподобный характер и иррадиировать в шею, что обусловлено расслоением дуги аорты. Значительно реже расслоение аорты протекает с малоинтенсивными болями. У ряда больных расслоение аорты протекает практически асимптомно и первыми признаками болезни являются симптомы ишемии головного или спинного мозга, аортальной недостаточности, ишемии почек, органов пищеварения и нижних конечностей. Нередко первым признаком расслоения бывает развитие пульсирующего образования в животе, трактующееся как аневризма брюшной части аорты.
Расслоение ветвей дуги и нисходящей грудной и брюшной отделов аорты может сопровождаться: 1) острой, а затем хронической ишемией головного или спинного мозга; 2) острой ишемией органов пищеварения; 3) стабильной вазоренальной гипертензией или инфарктом почки; 4) острой ишемией нижних конечностей. В связи с этим больным могут ставить самые различные диагнозы — инсульт, тромбоз мезентериальных сосудов, почечная колика, тромбоэмболия бифуркации аорты; и госпитализировать их в стационары различного профиля.
При остром развитии болезни и прорыве аневризмы в полость перикарда, плевральную полость или забрюшинное пространство первыми клиническими признаками могут быть боль и типичная картина внутреннего кровотечения.
Симптомы компрессии соседних органов, характерные для истинных аневризм грудной части аорты, могут развиваться и при расслаивающих аневризмах аорты. При аневризмах II типа нередко отмечаются симптомы венозной гипертензии головы, шеи, верхних конечностей, связанные со сдавлением верхней полой вены. При аневризмах I типа с расслоением дуги аорты могут появляться симптомы, связанные с компрессией трахеи, левого бронха (одышка, стридор, частые пневмонии) и возвратного нерва (осиплость голоса, сухой кашель).
В некоторых случаях клиническая картина при расслаивающей аневризме грудного отдела аорты имеет сходство с клинической картиной инфаркта миокарда, а при расслаивании брюшного отдела аорты — с картиной почечной колики. Начало боли при расслаивании аневризмы аорты обычно острое, внезапное, тогда как при острой коронарной недостаточности боль может нарастать постепенно. Большое значение имеет локализация боли: при расслаивающей аневризме аорты боль редко иррадиирует в руки, и локализация боли может меняться с постепенным движением боли по спине, вдоль позвоночника по ходу расслоения аорты; постепенно болевые ощущения могут распространяться в нижние отделы живота и малый таз.
При истинной почечной колике обычно характерны дизурические явления и другие симптомы. Доказательством наличия расслаивающей аневризмы аорты служит и появление вслед за болью симптомов, связанных с распространением расслоения аорты в области отхождения магистрального сосуда или нескольких сосудов (асимметрия пульса на верхних и нижних конечностях, гемипарез, параплегия или инсульт, боль в поясничной области, гематурия, отек мошонки). Известны и разнообразные «периферические сосудистые маски» заболевания (по типу синдрома Такаясу), а также «пневмонические», желудочно-кишечные (по типу острого живота).
Типичны острое начало болезни, указания в анамнезе на артериальную гипертензию, имеются внешние признаки болезни Марфана. При стандартном осмотре более чем у половины больных отмечается асимметрия пульсации и уровня артериального давления на верхних и нижних конечностях. В ряде случаев пульс не определяется; отмечаются признаки острой или хронической ишемии. Чаще снижение пульса и давления отмечается на левых конечностях. При перкуссии может определяться расширение средостения вправо или влево. Аускультативно над восходящей частью аорты при I-II типе расслоения аорты выслушивается систолический шум. Почти у половины таких больных отмечаются признаки аортальной недостаточности — диастолический шум и снижение уровня диастолического артериального давления. В ряде случаев над областью сердца выслушивается шум трения перикарда. При распространении расслоения на нисходящую часть аорты систолический шум может определяться сзади в межлопаточной области и паравертебрально слева в поясничной области. При этом шум выслушивается над брюшной частью аорты и в области эпигастрия. Выявление пульсации сонных артерий и систолического шума над ними позволяет определить вовлечение в процесс ветвей дуги аорты. Важным для постановки диагноза аневризм I и III типа с распространением расслоения на брюшную часть аорты является пальпаторное определение ее пульсации, которая может быть усилена. Аорта при пальпации расширена, мягкая на ощупь, податлива за счет увеличения в основном ложного просвета. Могут определяться и большие ложные аневризмы брюшной части, обычно неотделимые от реберной дуги.
Результаты электрокардиографии служат в основном двум целям: установить или исключить острый инфаркт миокарда (данный диагноз ставится практически у 90% больных с расслоением аорты). Если имеются признаки острого инфаркта миокарда, данные ЭКГ обязательно необходимо сопоставить с данными рентгенографии органов грудной клетки, поскольку расширение тени восходящей части аорты позволяет предположить у больного расслаивающую аневризму I-II типа с вовлечением в процесс устьев коронарных артерий. Кроме того, признаки острой коронарной недостаточности определяют как тактику подготовки больного к операции при наличии расслоения аорты, так и ее характер.
Фонокардиография подтверждает данные аускультации и позволяет зафиксировать у больного развитие аортальной недостаточности. Объемная сфигмография и ультразвуковая допплерография позволяют выявить «заинтересованность» магистральных артерий конечностей, уточнить распространенность процесса, особенности кровоснабжения головного мозга, а также вовлечение в процесс, расслоение сонных и позвоночных артерий.
Большое значение в диагностике расслаивающих аневризм грудной части аорты имеет рентгенологический метод. Практически у всех больных выявляется расширение тени верхнего средостения. Расширение восходящей части аорты лучше фиксируется в левой косой проекции. В той же проекции хорошо видна и тень нисходящей части аорты. Расширение ее тени наблюдается, у 50% больных с I типом расслоения и у 100% больных с III типом расслоения. При этом отмечаются неровность контуров нисходящей части аорты и деформация ее тени. Рентгенологически может выявляться жидкость в полости перикарда и в плевральной полости, причем даже в хронической стадии процесса. Для уточнения диагноза большую роль имеет динамическое рентгенологическое исследование.
Эхокардиография позволяет достаточно четко фиксировать двойной просвет восходящей аорты, а также состояние аортального клапана и наличие перикардиального выпота при угрожающем разрыве аорты.
Высокими информативными возможностями обладает в диагностике расслаивающих аневризм и компьютерная томография с одновременным введением рентгеноконтрастного вещества. Она позволяет дифференцировать тромбоз обычной аневризмы грудной части аорты от тромбоза ложного просвета при ее расслоении.
Заключительным методом диагностики является тотальная аортография. Ее особенности заключаются в том, что при трансфеморальном доступе катетер в ряде случаев не попадает в истинный просвет аорты, в связи с чем информативность метода значительно снижается. В подобных случаях лучше использовать трансаксиллярный доступ справа. Цель ангиографического исследования — определить точное место проксимальной фенестрации, протяженность расслоения, «заинтересованность» ветвей аорты и наличие или отсутствие дистальной фенестрации. Не все ангиографические признаки расслоения аорты могут быть получены в 100% случаев. Наиболее достоверный признак — расширение и деформация тени аорты. Этот признак позволяет диагностировать проксимальный уровень расслоения и его протяженность. Частым признаком (примерно у 75% больных) является одновременное контрастирование истинного и ложного просветов аорты. Чаще удается фиксировать ложный просвет в нисходящей части аорты. Истинный просвет аорты нередко значительно сужен. В 10-15% случаев ложный просвет может быть тромбирован, причем вероятность тромбоза возрастает в дистальном направлении. Однако наличие в этом сегменте стенозирования истинного просвета свидетельствует о тромбировании ложного просвета. Истинный просвет обычно носит спиралеобразный ход в нисходящей части аорты, что характерно для расслоения. У некоторых больных при аортографии фиксируется четкая разделительная полоса — отслоенная внутренняя оболочка — между истинным и ложным просветом. Уровень проксимальной фенестрации обычно определяется наличием сброса рентгеноконтрастного вещества в резко расширенный ложный просвет. В ряде случаев этот сброс не удается фиксировать, и по контуру истинного просвета аорты выявляется лишь небольшой дефект наполнения.
Одним из признаков расслоения является отрыв ветвей дуги и брюшной части аорты от истинного просвета. Если ветви аорты контрастируются одновременно с контрастированием истинного просвета, то это свидетельствует об их нормальном отхождении. Если контрастирование запаздывает или вообще отсутствует, следует думать об их отрыве. В подобных случаях необходимо дополнить исследование контрастированием ложного просвета аорты. Во-первых, это четче позволит определить размеры ложного просвета, степень его тромбоза и, во-вторых, выявить проходимость отходящих от ложного просвета ветвей аорты. При ангиографии корня аорты удается фиксировать регургитацию контрастного вещества из аорты в левый желудочек, что свидетельствует о той или иной степени аортальной недостаточности. Это осложнение обнаруживается примерно у 50% больных с расслоением восходящей части аорты. При II типе расслоения подобная недостаточность встречается в 2 раза чаще, чем при I типе.
При естественном течении расслаивающих аневризм грудной части треть больных погибает в течение первых суток, только 10% доживает до 3 месяцев с момента возникновения заболевания. 80% больных, переживших острую и подострую стадии болезни, остаются живы в течение 1-3 лет. Все больные с развитием проксимальной фенестрации в восходящей части аорты погибают в течение первого месяца болезни.
Хирургическое лечение более эффективно у больных с расслоением аорты I-II типа, консервативное при III типе.
При консервативном ведении: основной причиной смерти больных с I-II типом расслоения является тампонада сердца, менее частая причина — окклюзия магистральных ветвей аорты. У больных с III типом расслоения основной причиной смерти является кровотечение в левую плевральную полость и почечная недостаточность. Последняя развивается не только в результате окклюзии почечных артерий из-за расслоения брюшного отдела, но и воздействия проводимой гипотензивной терапии.
В настоящее время при остром расслоении грудной части аорты наиболее рациональным является дифференцированный подход к тактике лечения в зависимости от типа расслоения и развития осложнений. Лекарственная терапия показана больным с различными типами расслоения аорты как начальный этап лечения, до момента проведения аортографии и обеспечения оперативного лечения. Срочная операция необходима при угрожающем разрыве аневризмы, прогрессирующем расслоении, выраженной аортальной недостаточности, при образовании мешковидной аневризмы, а также при неэффективности проводимой терапии, не снимающей болевого синдрома, и при «неуправляемой» гипертензии. Показанием к операции является также наличие крови в перикарде или плевральной полости.
Лекарственная терапия в острой и подострой стадиях болезни рекомендуется больным с III типом расслоения, пациентам с предполагаемым I типом расслоения, но при стабильном течении процесса, больным с высокими факторами риска (обычно старше 50 лет), а также в тех случаях, когда место фенестрации не удается выявить на аортограмме и при отсутствии контрастирования ложного канала. Следует также придерживаться консервативного метода лечения при ее эффективности у больных, у которых с момента расслоения прошло более 14 дней. Основной целью лекарственной терапии являются предотвращение прогрессирования расслоения аорты и нормализация гемодинамики и гомеостаза. Для этого проводится управляемая гипотензия. Необходимы постоянный контроль за уровнем артериального давления, диуреза, мониторирование ЭКГ. Каждые 12 часов проводится рентгенологический контроль грудной клетки с целью выявления динамики размеров аневризмы и наличия жидкости в плевральных полостях и перикарде. Как показывает опыт, риск операций, производимых в хронической стадии процесса при стабилизации гемодинамики и гомеостаза, а также вследствие укрепления наружных слоев аорты в сегменте расслоения, значительно уменьшается, чем в острой и подострой стадиях.
- к основным целям лечения относят снижение АД и сократимости миокарда;
- желаемый уровень систолического АД – 100-120 мм рт. ст. или самый низкий уровень, не вызывающий ишемии сердца, головного мозга и почек у страдающих гипертонией;
- для быстрого снижения высокого АД прибегают к внутривенной инфузии нитропруссида натрия или нитроглицерина при обязательном одновременном применении β-блокатора;
- для быстрого снижения сократимости миокарда производят внутривенное введение β-блокаторов в возрастающей дозе до достижения ЧСС 50–60 в минуту;
- обеих целей можно добиться при помощи лабетолола (10 мг внутривенно в течение 2 минут, далее 20-80 мг каждые 10-15 мин до максимальной дозы 300 мг, в качестве поддерживающей меры – инфузии 2-20 мг в минуту);
- при противопоказаниях к β-блокаторам можно использовать антагонисты кальция, замедляющие ритм сердца (верапамил, дилтиазем);
- прием короткодействующих препаратов нифедипина внутрь или под язык может привести к быстрому снижению АД даже в рефрактерных случаях, однако сопряжено с риском возникновения рефлекторной тахикардии, по-видимому, эти средства не следует назначать без предварительного введения β-блокатора;
- при вовлечении в расслоение артерий почек для снижения АД наиболее эффективным может быть внутривенное введение ингибитора ангиотензин–превращающего фермента (эналаприл 0,625 — 5 мг каждые 4 – 6 ч);
- при клинически значимой гипотонии необходимо быстрое внутривенное введение жидкости; в рефрактерных случаях проводится инфузия прессорных агентов (предпочтительнее — норадреналина; допамин применяется только в низких дозах для стимуляции мочеотделения).
Тем не менее хирургическое лечение показано больным с I-II типом расслоения сразу же после стабилизации гомеостаза в связи с непредсказуемым развитием осложнений. Помимо указанных признаков угрожающих осложнений, важным симптомом для решения вопроса о срочной операции являются симптомы острой окклюзии ветвей аорты, снабжающих кровью жизненно важные органы (мозг, почки, висцеральные органы). При угрозе разрыва аорты операция показана по витальным показаниям. Для больных с III типом расслоения операцию чаще следует производить в хронической стадии процесса, преимущественно у больных не старше 50 лет, при аневризме только грудной части аорты либо мешковидных аневризмах брюшной части аорты, сочетающихся с болевым синдромом, при синдроме хронической ишемии органов пищеварения, вазоренальной гипертензии и ишемии нижних конечностей.
При тяжелых сопутствующих заболеваниях у больных пожилого возраста следует предпочесть лекарственную терапию, если она эффективна.
Техника операций при расслаивающих аневризмах I-II типа аналогична таковой при обычных аневризмах восходящей части аорты. При наличии расслоения аорты швы накладывают так, чтобы ликвидировать ложный просвет в ее стенке. Операции направлены на устранение проксимальной фенестрации в аорте. При развитии острой аортальной недостаточности восходящую часть аорты протезируют с помощью специального «кондуита», содержащего протез клапана. Для лучшей герметизации швов дистального анастомоза можно использовать специальный клей, заливаемый между расслоенными слоями сосудистой стенки.
При расслоении I типа, симптомах ишемии мозга вследствие окклюзии ветвей дуги аорты показано одновременное протезирование восходящей части и ее дуги с имплантацией брахиоцефальных сосудов в протез или их протезирование. При симптомах, характерных для расслоения брюшной части аорты и ее ветвей, не исчезающих и даже усугубляющихся после устранения проксимальной фенестрации расслоения, вторым этапом показана операция на брюшной части и ее ветвях. Второй этап операции направлен обычно на резекцию больших ложных аневризм брюшной части, а также на реваскуляризацию почек, органов брюшной полости и нижних конечностей.
При расслаивающих аневризмах III типа устранение только проксимальной фенестрации с протезированием грудного отдела следует считать радикальной при ограниченном участке поражения, не переходящем на брюшную часть аорты. Если расслоение распространяется на брюшную часть аорты, то устранение ложного просвета при протезировании грудной части аорты приводит часто к ишемии почек вследствие редукции кровотока по ложному просвету, от которого чаще отходит левая почечная артерия. Современная тактика при подобных операциях должна заключаться в одномоментной реконструкции всей нисходящей части и ее магистральных ветвей. Метод операции при этом по доступу к аорте и условиям ее проведения практически не отличается от такового при аневризме грудной и брюшной частей аорты, но требует некоторой детализации. В грудной части межреберные артерии обычно не вовлечены в процесс расслоения, так как ложный просвет расположен по переднелатеральной стенке аорты. В брюшной части ложный просвет в 85% случаев располагается слева. Именно поэтому левая почечная артерия значительно чаще отходит от ложного просвета аорты, чем правая. Устья висцеральных артерий могут быть вовлечены в процесс расслоения, но чаще отходят от истинного просвета. Они обычно расположены близко друг к другу и поэтому могут быть имплантированы в протез на одной площадке.
Сосуд пережимают и рассекают в продольном направлении. Внутреннюю оболочку между истинным и ложным просветом иссекают на всем протяжении. Площадку с межреберными артериями вшивают в окно протеза по задней его поверхности. По описанному методу на площадке имплантируют ветви брюшной части аорты. Отдельно вшивают на площадке устье левой почечной артерии. В случаях острого расслоения в связи со слабостью стенок аорты производится устранение проксимальной фенестрации аорты.
Учитывая, что кровоснабжение спинного мозга в основном осуществляется через артерию Адамкевича, которая чаще всего расположена на уровне Х-XI грудного позвонка, можно использовать несколько видоизмененный метод сохранения кровотока по спинномозговым ветвям. Четыре-пять пар верхних межреберных артерий можно перевязать. Из площадки нижнего сегмента грудного отдела с устьями межреберных артерий на уровне VIII-XII грудных позвонков создается слепой канал, открытый в просвет аорты. Именно в этом месте накладывается дистальный анастомоз протеза с аортой. В тех случаях, когда винтообразный ход расслоения грудной аорты выглядит таким образом, что нижние межреберные и верхние поясничные артерии, а также чревный ствол и верхняя брыжеечная артерия отходят от истинного просвета аорты, радикальную коррекцию аневризмы грудной и брюшной частей аорты производят одномоментно. При этом можно раздельно протезировать грудную часть аорты с целью ликвидации ложного просвета и проксимальной фенестрации, а затем произвести резекцию аневризмы брюшной части с протезированием и реваскуляризацией почек.
источник
А натомические дефекты сосудистых структур представляют колоссальную опасность для здоровья и жизни пациента. Включают в себя гетерогенную группу патологических процессов.
Проблема в том, что в большинстве своем указанные расстройства имеют латентное, вялое течение и не отличаются симптомами.
До определенного момента невозможно обнаружить проблему, если обращать внимание только на субъективные ощущения. Требуется качественная инструментальная диагностика.
Расслаивающая аневризма аорты — это нарушение целостности отдельных внутренних слоев сосуда, а затем тотальную деструкцию выстилки с развитием массивного кровотечения и гибелью больного в считанные секунды.
Частота или встречаемость процесса минимальна, в практике обнаруживается не более 1% пациентов с подобным страшным диагнозом.
Общая летальность близится к 40% даже при раннем выявлении патологии. Что связано с некоторыми трудностями оперативной коррекции (например, неудачная локализация дефекта или же множественное вовлечение участков).
Расслаивающаяся аневризма аорты имеет сложное происхождение. Речь не об одном факторе, а о целой группе нарушений органического плана.
Крайне редко это первичная патология. Много чаще говорят о вторичном типе, то есть таком, который обусловлен сторонними заболеваниями. Всего выделяют три механизма развития указанной проблемы.
Первый касается роста давления в системе. Изменение показателей АД вызывает стремительное изнашивание сосудов, снижается качество кровотока, начинаются дистрофические процессы.
Внутренняя выстилка и мышечный слой аорты истончаются, наружная оболочка не приспособлена для противодействия большим нагрузкам.
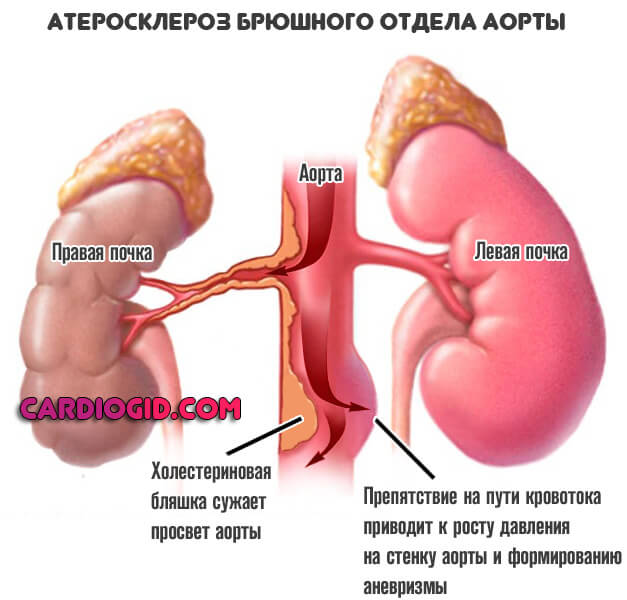
Второй весомый механизм — атеросклероз. Как правило, самостоятельного значения не имеет и идет в комплексе с ростом артериального давления, что объяснимо.
Закупорка просвета аорты холестериновой бляшкой или же стеноз (сужение) крупнейшей артерии приводит к невозможности нормального тока крови.
Организм отвечает на подобные препятствия усилением сердечной деятельности и ростом давления. Что и приводит уже по понятным причинам к дистрофии сосуда, деструкции стенок и повышает вероятность стеночного выпячивания.
Третий механизм имеет аутоиммунное происхождение. Возможны воспалительные процессы во внутреннем слое аорты, прямая деструкция стенок. Также встречается рубцевание просвета, образование фибриновых тяжей, препятствующих нормальному кровотоку.
Далее процесс идет по идентичной схеме. Рост давления в системе приводит к дистрофии (истончению стенки). Сосуд становится податливым, аномально пластичным.
Мышечный слой оказывается не способен поддерживать аорту в стабильном состоянии, противодействовать негативным факторам.
Потому происходит продавливание сосуда в одну из сторон или сразу по всему диаметру с развитием мешковидного или диффузного (веретенообразного) дефекта.
Уже на этом этапе возможен разрыв аневризмы и смерть от массивного кровотечения. Второй вариант — дальнейшая деструкция стенок.
Сначала жидкая соединительная ткань разрушает интиму (внутреннюю выстилку), затем просачивается в мышечный слой, потом в область наружной оболочки, пока не спровоцирует нарушения целостности и массивного кровотечения.
Полный «цикл» развития патологии, от старта до летального исхода составляет от 1 недели до 2 месяцев.
Известны случаи полугодового выживания, но это редкость и конец все равно идентичен. Без лечения спонтанного регресса не происходит, летального результата не избежать.
Как таковая типизация рассматриваемого дефекта не разработана, что связано с довольно малой распространенностью расслаивающей аневризмы аорты.
Основная классификация нарушения по локализации проводится по Де Бейки. Согласно ей выделяют три места расслоения:
- Первый тип. Порок расположен в восходящей части сосуда, может диффузно, экспансивно охватывать сразу группу участков (грудной и брюшной). Представляет собой наиболее встречаемый тип. При массивном поражении прогноз изначально хуже, потому как возрастает сложность предполагаемой операции.
- Второй тип. Отклонение локализуется строго изолированно, в восходящей части аорты. Также представляет трудности для хирурга, открытый доступ проблематичен, потому как мобилизовать сосуд непросто, слишком много тканей.
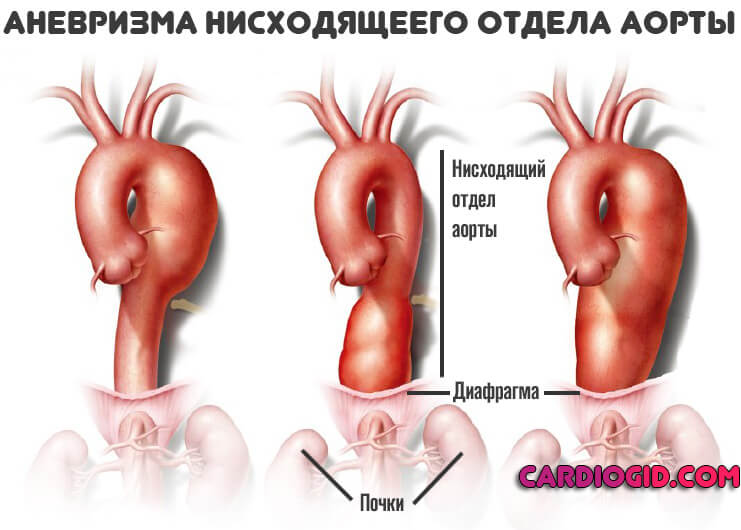
- Третий тип. Поражает нисходящий отдел аорты и брюшную часть включительно.
Существует упрощенная Стенфордская классификация. Согласно ей выделяют расслоение аневризмы, берущее начало в восходящем отделе аорты — тип (а) и в нисходящей части, тип (б).
Возможно подразделение расстройства также по симптомам (острое, хроническое), течению, размерам выпячивания (крайне запутанный критерий).
Универсальных методов подразделения нет. Врачей в первую очередь интересует диаметр патологического образования, скорость его прогрессирования и локализация.
Выяснение деталей позволяет снизить риски для пациента благодаря четкой, тщательной проработки оперативной стратегии.
Возможны два варианта течения расслаивающей аневризмы. Первый — острое. Представлено генерализовнанными признаками. Полная клиническая картина развивается в считанные секунды, отличается высокой тяжестью.
Продолжительность эпизода составляет несколько минут и менее, после чего наступает потеря сознания и гибель от массивного внутреннего кровотечения.
- Сильная, невыносимая боль. Располагается в области брюшины, спину, в грудной клетке. Зависит от локализации патологического процесса и его типа. Возникает внезапно, не купируется ничем. Вынуждает пациента принять положение лежа и не двигаться. Или же сесть.
- Потливость, бледность кожных покровов, выраженная одышка, слабость, тошнота, цианоз носогубного треугольника, спутанность сознания, предобморочное состояние. Так называемая коллаптоидная реакция. Объективно сопровождается падением уровня артериального давления.
- До становления описанного состояния возникает стремительный рост АД, на короткий промежуток времени.
Это типичные проявления. Прочие симптомы расслаивающей аневризмы аорты представлены ситуативными моментами, которые встречаются не у всех и не в каждом случае. Вероятность определяется в 1-15%.
- Боли в ногах, ощущение бегания мурашек, невозможность устоять, ходить.
- Почечная дисфункция. Сопровождается коликами в пояснице, задержкой мочи.
- Метеоризм, дискомфорт в животе. Причина кроется в нарушении соответствующего кровотока.
- Слабость мышц. Парезы, параличи. При снижении трофики нервных тканей спинного мозга.
- Боли в грудной клетке, отклонения ритма от нормального (по типу ускорения или урежения ЧСС), выраженная одышка.
- Потеря сознания. Сильная головная боль. При вовлечении в патологический процесс мозга, церебральных структур.
Расслаивающая аневризма грудного отдела аорты представлена наиболее полной клинической картиной.
Хроническая форма встречается примерно в 60% случаев. В то время как на долю острой приходится 20%. Остальные 20% определяются промежуточным типом.
- Боли в животе, запоры, диспепсические явления, артериальная гипертензия, которая не снимается препаратами и никак не реагирует на терапию. Встречается при поражении соответствующего одноименного отдела аорты.
- Дисфагия (невозможность глотать), нарушения голоса, процесса говорения, дыхания. По причине компрессии нервных тканей и самих систем, расположенных в грудной клетке. При значительных размерах аневризмы или же отклонения гемодинамики.
- Болевой синдром. Расположен в проекции сердца. Напоминает стенокардические или таковые при инфаркте. Однако это ложное впечатление.
- Отеки. В основном периферические. Страдают нижние и верхние конечности. Лицо.
- Посинение дермальных слоев. Возникает при компрессии вен, сопровождается ростом давления, одышкой.
- Нарушения зрения по типу потемнения, тумана в поле видимости.
- Наконец, обнаруживаются обмороки. Частые, пациента трудно вывести из подобного состояния.
Симптомы расслоения аневризмы, многообразны, но без должной подготовки и даже с таковой, но вне инструментальной диагностики определить, что стало причиной расстройства невозможно.
В некоторых клинических случаях, особенно сложных, патологический процесс маскируется столь хорошо, что даже по окончании обследования сказать что-либо конкретное не представляется возможным.
В основе развития расслаивающей аневризмы лежат врожденные и приобретенные патологии (соотношение — 30% против 70%).
Первые представлены соединительнотканными дефектами (синдром Морфана и прочие), анатомическими изменениями по типу стеноза аортального клапана, иных явлений. Они не обязательно провоцируют именно рассматриваемое расстройство. Вариантов множество.
Вторая группа отклонений многочисленна. Если ранжировать заболевания по встречаемости, обнаружится такая картина:
- Атеросклероз и гипертония. Также симптоматическое, стабильное повышение уровня давления в кровеносном русле. В сочетании они особенно опасны.
- Ятрогенный фактор. То есть врачебное вмешательство лечебного или диагностического плана. В основном — катетеризация аорты. Реже открытые или эндоваскулярные операции.
- Васкулиты вирусного, грибкового, бактериального, аутоиммунного (неинфекционного) рода. Сопровождаются воспалением сосудистых стенок, их деструкцией, рубцеванием.
- Перенесенные травмы грудной клетки. Особенно, если была вовлечена аорта.
Эндокринные факторы встречаются, но много реже. Обычно расслаивающая аневризма манифестирует в период беременности, на ранних сроках или в 3-й триместр. Настораживающим признаком оказывается тяжелый токсикоз.
В остальных случаях, если нет возможности определиться с фактором развития отклонения, говорят об идиопатической форме расстройства.
Выявить причину необходимо. Потому как даже после успешного хирургического вмешательства, полного восстановления, при самом благоприятном исходе ни один врач не даст гарантии отсутствии рецидива в будущем. Ведь патогенный фактор никуда не девается.
Среди редко встречающихся причин называют и сторонние инфекционные заболевания. Возможна транспортировка агентов в аорту, развитие воспаления и деструкции стенок.
Генетические врожденные синдромы генерализованного плана (например, Дауна) могут проявляться тем же неочевидным на первый взгляд образом.
Есть и предрасполагающие моменты, которые увеличивают риски развития расстройства: принадлежность к мужскому полу ( представители сильной половины человечества страдают рассматриваемым дефектом втрое чаще ), возраст от 55 лет и свыше (в связи с естественными процессами старения и воздействием накопленного груза заболеваний).
Выявление патологии ложится на плечи сосудистого хирурга. В основном. К кардиологу обратиться также можно, однако, это не профильный специалист. Обследование проводится в срочном порядке, времени на раздумья нет.
Примерный список мероприятий:
- Устный опрос больного. Направлен на выявление симптомов, выстраивание понятной клинической картины. Представляет собой основу.
- Сбор анамнеза. Перенесенные заболевания, образ жизни, семейная история (некоторые расстройства, особенно сопряженные с дефектами соединительной ткани передаются по наследству и повышают риски).
- Выслушивание сердечного звука. Аускультация. В 80% случаев обнаруживается синусовый шум над участочком локализации аневризмы.
- Рентгенография грудной клетке. Морально устаревшее исследование, дает минимум информации, но в рамках диагностики запущенных форм патологического процесса может оказаться полезным.
- Эхокардиография. УЗИ сердца и окружающих структур. Используется для визуализации грудного отдела аорты.
- Ультрасонография. Основная методика диагностики. Позволяет выявить дефект любой части крупнейшей артерии.
- МРТ-ангиография. Для визуализации тканей. Использовать контраст не имеет смысла, потому как кровь сама по себе хорошо усиливает рисунок. Компьютерная методика (КТ) применяется реже, она более предпочтительна в деле оценки состояния костных тканей.
После проведения тщательного обследования нужно начинать восстановление. Времени обычно не много.
Терапия строго хирургическая. Смысла в консервативных способах нет. Они не возымеют эффекта, зато время будет безвозвратно утрачено, а значит и шансы пациента на выживание и полное восстановление снизятся.
Открытым доступом. Суть заключается в иссечении аномальной, измененной области и ее ушивании. При необходимости проводится протезирование, либо эндоваскулярное вмешательство.
Хирургическое вмешательство представляет трудности, требует высокой квалификации врача. Порой дело осложняется «неудачной» локализацией дефекта.
Обязательное условие — лечение патологии, которая стала причиной расслаивающей аневризмы. Если речь о гипертонии — показаны специализированные средства (ингибиторы АПФ, бета-блокаторы, диуретики, лекарства центрального действия, антагонисты кальция).
При врожденных или приобретенных пороках проводится еще одна операция. Параллельно, как правило, несколько вмешательство не назначается, вопрос решается на усмотрение доктора.
Атеросклероз требует приема статинов, медикаментов, для растворения бляшек и выведения избытков холестерина.
Необходимо скорректировать образ жизни:
- Отказаться от курения, спиртного, психостимуляторов (наркотики), самовольного приема любых препаратов.
- Правильное питание (меньше животных жиров и соль до 7 граммов в сутки).
- Полноценный сон (не менее 7 часов за ночь).
- Адекватная, посильная физическая активность (оптимум — плавание или же прогулки неспешным шагом на свежем воздухе).
Соблюдение всех рекомендаций специалиста позволяет добиться максимального эффекта.
Лечение аневризмы проводится оперативными методами. Прочих вариантов не существует, потому терять время, надеяться на спонтанное самовосстановление не нужно.
Зависит от этапа, локализации дефекта, общего состояния здоровья пациента, первопричины аномалии и прочих факторов.
При раннем обнаружении и возможности «удобного» доступа к пороку — благоприятный. В остальных ситуациях — спорный.
Однозначно негативный только при разрыве образования. Шансы есть всегда. Опускать руки не стоит.
Общая летальность патологического процесса составляет порядка 40%, плюс-минус несколько процентов.
Без лечения смерть наступает в перспективе недели, максимум месяца. В исключительных ситуациях — полугода. Но это, скорее, казуистика, единичные случаи.
Основное и самое угрожающее последствие — разрыв аневризмы. С массивным кровотечением, гибелью человека. Тот же эффект наблюдается при прогрессирующем расслоении аорты в области мешотчатого или диффузного образования. Исход всегда один и тот же.
В процессе развития самого заболевания возможны грозные осложнения, спровоцированные сторонними явлениями.
Например, асфиксия вследствие компрессии дыхательных структур, инсульт, инфаркт на фоне недостаточного кровообращения в указанных тканях.
Расслаивающая аневризма аорты — смешанный патологический процесс. Сопровождается аномальным изменением крупнейшей артерии, деструкцией стенок.
Заканчивается смертью без лечения всегда . Единственный шанс на восстановление — своевременно провести операцию. Прогноз в такой ситуации благоприятный.
источник
Аневризма аорты – патологическое локальное расширение участка магистральной артерии, обусловленное слабостью ее стенок. В зависимости от локализации аневризма аорты может проявляться болью в грудной клетке или животе, наличием пульсирующего опухолевидного образования, симптомами компрессии соседних органов: одышкой, кашлем, дисфонией, дисфагией, отечностью и цианозом лица и шеи. Основу диагностики аневризмы аорты составляют рентгенологические (рентгенография грудной клетки и брюшной полости, аортография) и ультразвуковые методы (УЗДГ, УЗДС грудной/брюшной аорты). Хирургическое лечение аневризмы предполагает выполнение ее резекции с протезированием аорты либо закрытого эндолюминального протезирования аневризмы специальным эндопротезом.
Аневризма аорты характеризуется необратимым расширением просвета артериального ствола на ограниченном участке. Соотношение аневризм аорты различной локализации примерно следующее: аневризмы брюшной части аорты составляют 37% случаев, восходящего отдела аорты – 23%, дуги аорты – 19%, нисходящего отдела грудной аорты – 19,5%. Т. о., на долю аневризм грудной аорты в кардиологии приходится почти 2/3 всей патологии. Аневризмы грудного отдела аорты часто сочетаются с другими аортальными пороками — аортальной недостаточностью и коарктацией аорты.
По этиологии все аневризмы аорты могут быть разделены на врожденные и приобретенные. Формирование врожденных аневризм связано с наследственными заболеваниями стенки аорты:
Приобретенные аневризмы аорты могут иметь воспалительную и невоспалительную этиологию:
- Поствоспалительные аневризмы возникают вследствие специфического и неспецифического аортита при грибковых поражениях аорты, сифилисе, послеоперационных инфекциях.
- Невоспалительные дегенеративные аневризмы обусловлены атеросклерозом, дефектами шовного материала и протезов аорты .
- Гемодинамически-постстенотических и травматические аневризмы связаны с механическими повреждениями аорты
- Идиопатические аневризмы развиваются при медионекрозе аорты.
Факторами риска формирования аневризм аорты считаются пожилой возраст, мужской пол, артериальная гипертензия, табакокурение и злоупотребление алкоголем, наследственная отягощенность.
Кроме дефектности стенки аорты в формировании аневризмы принимают участие механические и гемодинамические факторы. Аневризмы чаще возникают в функционально напряженных зонах, испытывающих повышенную нагрузку вследствие высокой скорости кровотока, крутизны пульсовой волны и ее формы. Хроническая травматизация аорты, а также повышенная активность протеолитических ферментов вызывают деструкцию эластического каркаса и неспецифические дегенеративные изменения в стенке сосуда.
Сформировавшаяся аневризма аорты прогрессирующе увеличивается в размерах, поскольку напряжение на ее стенки возрастает пропорционально расширению диаметра. Кровоток в аневризматическом мешке замедляется и приобретает турбулентный характер. В дистальное артериальное русло поступает лишь около 45% крови от объема, находящегося в аневризме. Это связано с тем, что, попадая в аневризматическую полость, кровь устремляется вдоль стенок, а центральный поток сдерживается механизмом турбулентности и присутствием в аневризме тромботических масс. Наличие тромбов в полости аневризмы является фактором риска тромбоэмболий дистальных разветвлений аорты.
В сосудистой хирургии предложено несколько классификаций аневризм аорты с учетом их локализации по сегментам, формы, структуры стенок, этиологии. В соответствии с сегментарной классификацией выделяют
Оценка морфологического строения аневризм аорты позволяет подразделить их на истинные и ложные (псевдоаневризмы):
- Истинная аневризма характеризуется истончением и выпячиванием наружу всех слоев аорты. По этиологии истинные аневризмы аорты обычно атеросклеротические или сифилитические.
- Псевдоаневризма. Стенка ложной аневризмы представлена соединительной тканью, образовавшейся вследствие организации пульсирующей гематомы; собственные стенки аорты в формировании ложной аневризмы не задействованы. По происхождению чаще бывают травматическими и послеоперационными.
По форме встречаются мешотчатые и веретенообразные аневризмы аорты: первые характеризуются локальным выпячиванием стенки, вторые – диффузным расширением всего диаметра аорты. В норме у взрослых диаметр восходящей аорты составляет около 3 см, нисходящей грудной аорты — 2,5 см, брюшной аорты — 2 см. Об аневризме аорты говорят при увеличении диаметра сосуда на ограниченном участке в 2 и более раза.
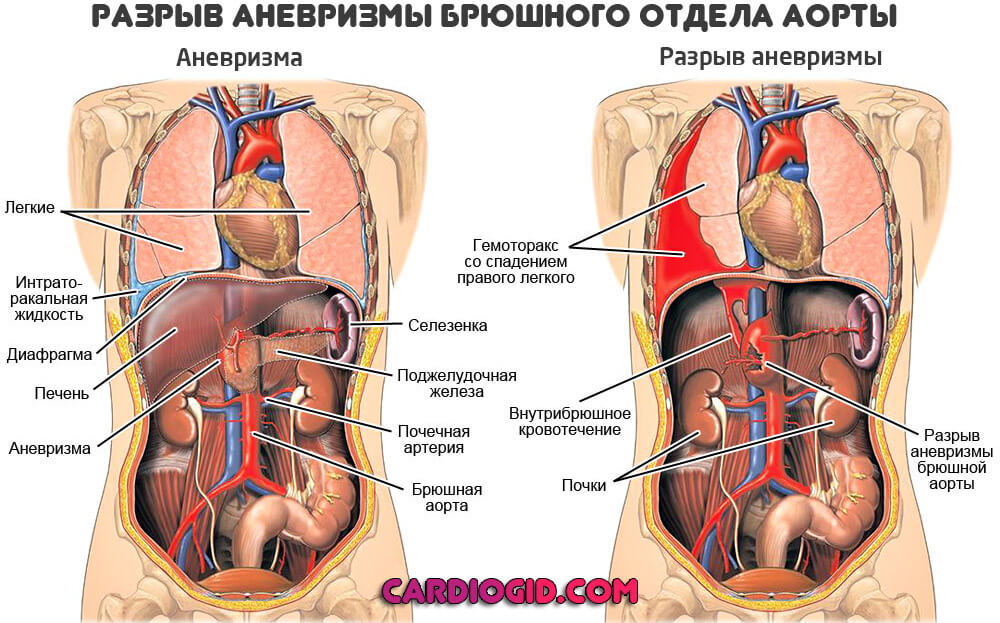
С учетом клинического течения различают неосложненные, осложненные, расслаивающиеся аневризмы аорты. К числу специфических осложнений аневризм аорты относятся разрывы аневризматического мешка, сопровождающиеся массивным внутренним кровотечением и образованием гематом; тромбозы аневризмы и тромбоэмболии артерий; флегмоны окружающих тканей вследствие инфицирования аневризмы.
Особый тип представляет собой расслаивающаяся аневризма аорты, когда через разрыв внутренней оболочки кровь проникает между слоями стенки артерии и распространяется под давлением по ходу сосуда, постепенно расслаивая его.
Клинические проявления аневризм аорты вариабельны и обусловлены локализацией, размерами аневризматического мешка, его протяженностью, этиологией заболевания. Аневризмы могут протекать бессимптомно или сопровождаться скудной симптоматикой и выявляться на профилактических осмотрах. Ведущим проявлением служит боль, обусловленная поражением стенки аорты, ее растяжением или компрессионным синдромом.
Клиника аневризмы брюшной аорты проявляется преходящими или постоянными разлитыми болями, дискомфортом в области живота, отрыжкой, тяжестью в эпигастрии, ощущением переполнения желудка, тошнотой, рвотой, дисфункцией кишечника, похуданием. Симптоматика может быть связана с компрессией кардиального отдела желудка, 12-перстной кишки, вовлечением висцеральных артерий. Часто больные самостоятельно определяют наличие усиленной пульсации в животе. При пальпации определяется напряженное, плотное, болезненное пульсирующее образование.
Для аневризмы восходящего отдела аорты типичны боли в области сердца или за грудиной, обусловленные сдавлением или стенозированием венечных артерий. Пациентов с аортальной недостаточностью беспокоит одышка, тахикардия, головокружение. Аневризмы больших размеров вызывают развитие синдрома верхней полой вены с головными болями, отечностью лица и верхней половины туловища.
Аневризма дуги аорты приводит к компрессии пищевода с явлениями дисфагии; в случае пережатия возвратного нерва возникает осиплость голоса (дисфония), сухой кашель; заинтересованность блуждающего нерва сопровождается брадикардией и слюнотечением. При компрессии трахеи и бронхов развиваются одышка и стридорозное дыхание; при сдавлении корня легкого — застойные явления и частые пневмонии.
При раздражении аневризмой нисходящей аорты периаортального симпатического сплетения возникают боли в левой руке и лопатке. В случае вовлечения межреберных артерий может развиваться ишемия спинного мозга, парапарезы и параплегии. Компрессия позвонков сопровождается их узурацией, дегенерацией и смещением с формированием кифоза. Сдавление сосудов и нервов клинически проявляется радикулярными и межреберными невралгиями.
Аневризмы аорты могут осложняться разрывом с развитием массивного кровотечения, коллапса, шока и острой сердечной недостаточности. Прорыв аневризмы может происходить в систему верхней полой вены, перикардиальную и плевральную полость, пищевод, брюшную полость. При этом развиваются тяжелые, подчас фатальные состояния – синдром верхней полой вены, гемоперикард, тампонада сердца, гемоторакс, легочное, желудочно-кишечное или внутрибрюшное кровотечение.
При отрыве тромботических масс из аневризматической полости развивается картина острой окклюзии сосудов конечностей: цианоз и болезненность пальцев стоп, ливедо на коже конечностей, перемежающаяся хромота. При тромбозе почечных артерий возникает реноваскулярная артериальная гипертензия и почечная недостаточность; при поражении мозговых артерий – инсульт.
Диагностический поиск при аневризме аорты включает оценку субъективных и объективных данных, проведение рентгенологических, ультразвуковых и томографических исследований. Аускультативным признаком аневризмы служит присутствие систолического шума в проекции расширения аорты. Аневризмы брюшной аорты обнаруживаются при пальпации живота в виде опухолевидного пульсирующего образования. Инструментальная диагностика:
- Рентгенография. В план рентгенологического обследования пациентов с аневризмой грудной или брюшной аорты включается рентгеноскопия и рентгенография грудной клетки, обзорная рентгенография брюшной полости, рентгенография пищевода и желудка.На заключительном этапе обследования выполняют аортографию, по данным которой уточняются локализация, размеры, протяженность аневризмы аорты и ее отношение к соседним анатомическим структурам.
- УЗИ. При распознавании аневризм восходящего отдела аорты используется эхокардиография; в остальных случаях проводится УЗДГ (УЗДС) грудной/брюшной аорты.
- Компьютерная томография. КТ (МСКТ) грудной/брюшной аорты позволяет точно и наглядно представить аневризматическое расширение, выявить наличие расслоения и тромботических масс, парааортальной гематомы, очагов кальциноза.
По результатам комплексного инструментального обследования принимается решение о показаниях к оперативному лечению. Аневризму грудной аорты следует дифференцировать от опухолей легких и средостения; аневризму брюшной аорты – от объемных образований брюшной полости, поражения лимфоузлов брыжейки, забрюшинных опухолей.
При бессимптомном непрогрессирующем течении аневризмы аорты ограничиваются динамическим наблюдением сосудистого хирурга и рентгенологическим контролем. Для снижения риска возможных осложнений проводится гипотензивная и антикоагулянтная терапия, снижение уровня холестерина.
Оперативное вмешательство показано при аневризмах брюшной аорты диаметром более 4 см; аневризмах грудной аорты диаметром 5,5-6,0 см или при увеличении аневризм меньшего размера более чем на 0,5 см за полгода. При разрыве аневризмы аорты показания к экстренному хирургическому вмешательству абсолютные.
Хирургическое лечение аневризмы аорты заключается в иссечении аневризматически измененного участка сосуда, ушивании дефекта либо его замещении сосудистым протезом. С учетом анатомической локализации выполняется резекция аневризмы брюшной аорты, грудной аорты, дуги аорты, торакоабдоминальной части аорты, подпочечного отдела аорты.
При гемодинамически значимой аортальной недостаточности резекцию восходящей грудной аорты сочетают с протезированием аортального клапана. Альтернативой открытому сосудистому вмешательству служит эндоваскулярное протезирование аневризмы аорты с установкой стента.
Прогноз аневризмы аорты, главным образом, определяется ее размерами и сопутствующим атеросклеротическим поражением сердечно-сосудистой системы. В целом естественное течение аневризмы неблагоприятное и связано с высоким риском смерти от разрыва аорты или тромбоэмболических осложнений. Вероятность разрыва аневризмы аорты диаметром 6 и более см составляет 50% в год, меньшего диаметра – 20% в год. Раннее выявление и плановое хирургическое лечение аневризм аорты оправдано низкой интраоперационной (5 %) летальностью и хорошими отдаленными результатами.
Профилактические рекомендации включают контроль АД, организацию правильного образа жизни, регулярное наблюдение у кардиолога и ангиохирурга, медикаментозную терапию сопутствующей патологии. Лицам из групп риска по развитию аневризмы аорты следует проходить скрининговое ультразвуковое обследование.
источник