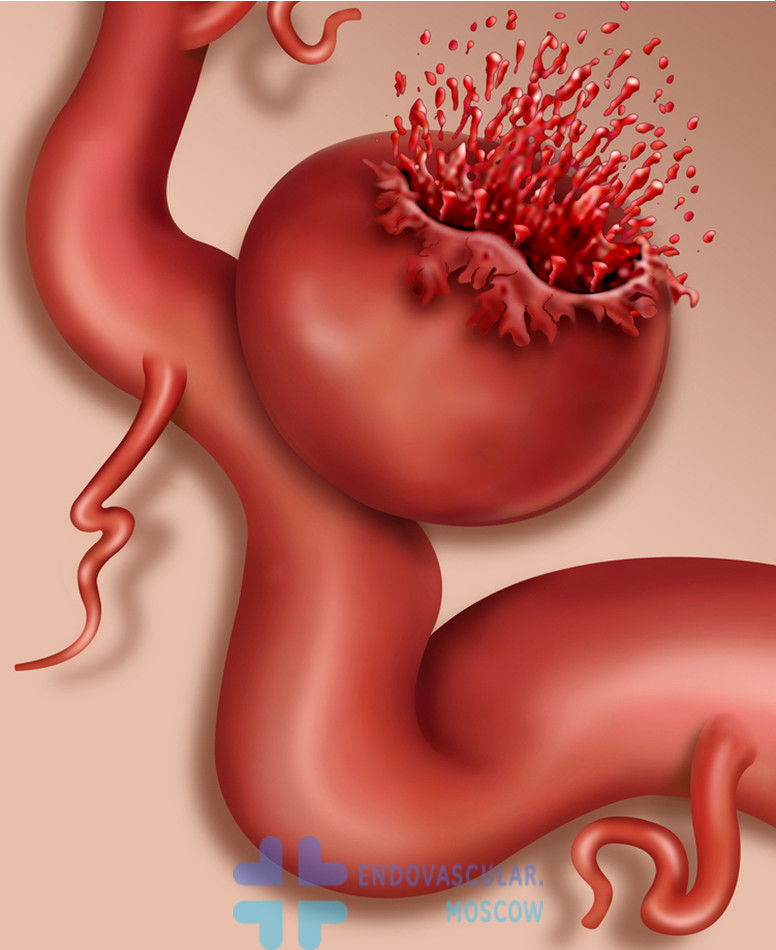
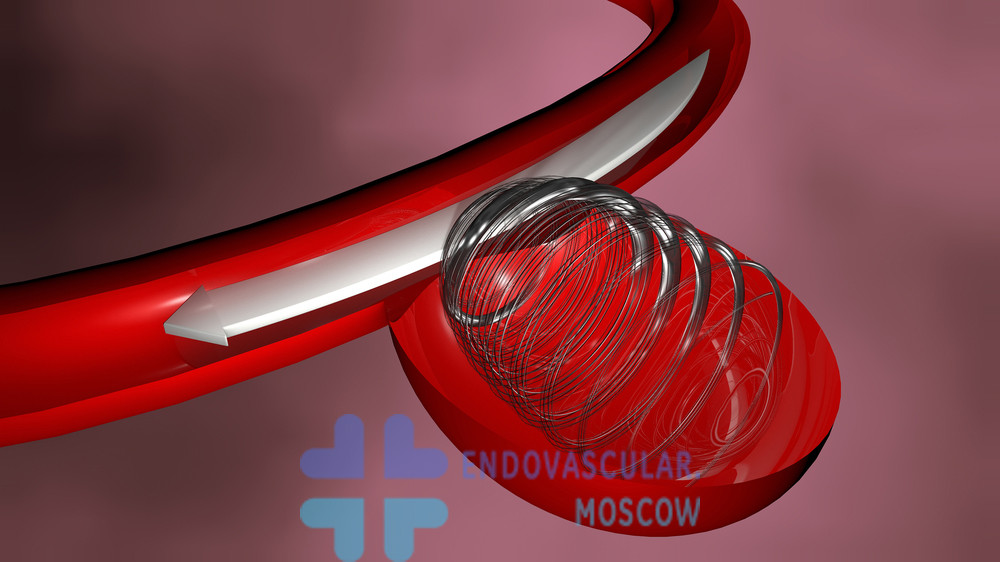
Заболевание считается довольно распространенным и очень опасным, поэтому нуждается в проведении адекватного лечения. Как правило, для устранения аневризм применяются оперативные методики. Консервативная терапия дает положительный результат только в редких случаях. Хирургическое лечение показано пациентам, у которых патологические новообразования увеличиваются в размерах, существует риск разрыва и кровоизлияния. Последствием таких осложнений станет летальный исход.
На сегодняшний день наиболее эффективной является эндоваскулярная эмболизация аневризмы головного мозга. Такая внутрисосудистая операция — это альтернатива открытому хирургическому вмешательству, позволяющая предотвратить кровотечения и разрывы патологического мешка.
При поражении кровеносных сосудов мозга важно применять наименее инвазивные оперативные методики.
В нейрохирургии большую распространенность получила эндоваскулярная эмболизация, зарекомендовавшая себя как действенный и безопасный способ лечения аневризм. Такая операция является щадящей, так как проводится без трепанации черепа и использования длительного наркоза. Еще одно преимущество методики — это относительно непродолжительный период реабилитации.
Эндоваскулярная эмболизация аневризмы головного мозга предусматривает устранение патологических новообразований при помощи инструментов, которые вводятся в бедренную артерию через предварительно сделанный небольшой прокол. Проводится операция под местной анестезией.
Перед выполнением хирургического вмешательства больного направляют на прохождение тщательного комплексного обследования.
Этапы оперативной коррекции аневризмы:
- К пациенту применяют местную анестезию и обрабатывают паховую зону антисептиками.
- Хирург выполняет разрез в области прохождения бедренной артерии.
- Далее врач вводит катетер, управляемый проводником при помощи ангиографа.
- После достижения места локализации патологического новообразования выполняется удаление проводника и вводится контрастное вещество для визуализации области поражения.
- После получения картины точного расположения внутричерепной аневризмы, в основной катетер направляют микрокатетер.
- Устанавливается системы катушки — платиновые спирали, которые частично или полностью блокируют кровоток в патологическом образовании.
- Удаляются катетеры, зашивается разрез и накладывается стерильная повязка.
Длительность процедуры — от 30 до 60 минут. После завершения операции пациенту следует оставаться в неподвижном состоянии на протяжении 8 часов.
Несмотря на то что эндоваскулярная эмболизация аневризмы головного мозга является безопасной малоинвазивной операцией, все же у некоторых пациентов могут возникнуть осложнения.
Около 20% оперированных больных выражают жалобы на такие симптомы, как слабость, покалывание и онемение в голове, расстройства зрения и речи, судороги, ухудшение памяти. Более серьезными последствиями хирургической коррекции аневризмы головного мозга считаются кровотечения, попадание инфекции, образование кровяных сгустков. Во время проведения операции может случиться разрыв патологического мешка.
В Южной Корее минимально-инвазивные методики оперирования успешно находят применение в самых разнообразных отраслях медицины, в том числе и в такой востребованной во все времена сфере, как нейрохирургия.
В частности за последние годы в этой стране получили широкое распространение эндоваскулярные вмешательства для лечения аневризм кровеносных сосудов головного мозга. Изначально такие операции предполагали осуществление эмболизации (закупорки) питающего сосуда особым баллоном. Затем на смену этой процедуре пришла прямая облитерация просвета аневризмы специальными микроспиралями.
Благодаря своей минимальной травматичности операции эндоваскулярной окклюзии аневризм головного мозга могут выполняться при наличии у пациента тяжелой сопутствующей соматической патологии, а также в тех случаях, когда идет речь о лицах пожилого возраста, которым противопоказано традиционное нейрохирургическое вмешательство. Кроме того, эндоваскулярная техника оперирования является методом выбора при труднодоступной локализации церебральной аневризмы и невозможности осуществления ее клипирования (к примеру, при веретенообразной форме).
Данная процедура довольно хорошо переносится пациентами и обеспечивает безопасное изолирование внутричерепной аневризмы и остановку дальнейшего поступления в нее тока крови, что уменьшает риск разрыва и повторного кровотечения.
Выполняется эндоваскулярная эмболизация аневризм головного мозга в клиниках Южной Кореи через периферическую артерию: в нее под местной анестезией в области паха вводят катетер, используя который по направляющей проволоке под контролем ангиографа (высокоскоростной контрастной рентгенографической съемки) проходят по кровеносному руслу именно в тот сосуд, где располагается аневризма. Затем проводник удаляют, а катетер используют для введения в кровоток контрастного вещества, чтобы визуализировать и аневризму, и нормальные кровеносные сосуды.
После того, как окончательно уточнено наличие, место локализации и размеры аневризматического расширения, внутрь основного катетера помещают специальный микро-катетер. Успешно войдя им в шейку аневризмы, доктор устанавливает систему катушки. Платиновые спиральки навсегда остаются в аневризме, уменьшая либо полностью блокируя поток крови в ней.
Если отверстие аневризмы слишком широкое, корейские доктора прибегают к так наз. стент-ассистирующим методикам, дающим возможность максимально уменьшить риск отдаленной реканализации. При этом внутри артерии вдоль шейки аневризмы размещают небольшой стент, потом через его ячейку проводят микрокатетер, через который в аневризму доставляются микроспирали. Таким образом, удается предотвратить смещение витков спиралей в сторону просвета несущего сосуда. Кстати, в последние годы устанавливается новая категория интракраниальных стентов – потоконаправляющие стенты, дающие возможность уменьшать кровоток в аневризме благодаря тому, что основной поток крови направляется по несущему сосуду. Тромбирование (закупорка) аневризмы после имплантации такого стента наступает в среднем в период от 4-х до 6-ти мес. после операции. Такая методика наиболее оправдана для лечения крупных и даже гигантских аневризм.
Выбор техники оперирования зависит, в первую очередь, от анатомических особенностей внутричерепной аневризмы. В каждой конкретной клинической ситуации врачи нейрохирургических центров Южной Кореи предлагают пациентам наиболее эффективные и современные методы лечения данной патологии. Ограничением для выполнения эндоваскулярных вмешательств служат выраженный атеросклероз и патологическая извитость брахиоцефальных артерий. При необходимости проведения операции со стент-ассистенцией обязательно принимается во внимание наличие в анамнезе каких-либо кровотечений, так как имплантация стента требует длительного приема антикоагулянтных средств в постоперационном периоде. Если в ходе эндоваскулярной окклюзии интракраниальной аневризмы достигнута лишь ее частичная закупорка, вторым этапом корейские доктора осуществляют микрохирургическую операцию. Также возможно эндоваскулярное вмешательство после прямой паллиативной операции.
Облитерация интракраниальных аневризм спиралями успешно практикуется сейчас в нейрохирургическом центре госпиталя Гиль при ун-те Гачон (Gachon Med. University Gil Hospital), а также в других не менее авторитетных клиниках Южной Кореи: в госпитале Северанс при ун-те Ёнсе в г. Сеул, в клинике ун-та Ханьянг в г. Сеуле, в госпитале Бунданг при Сеульском нац. Университете и др.
Ведущие специалисты Южной Кореи, практикующие в сфере эндоваскулярной нейрохирургии:
- проф. Чеон Чингхван (клиника ун-та Ханьянг в г. Сеуле);
- д-р О-Ки Куон (госпиталь Бунданг при Сеульском нац. университете) и др.
Лечение аневризмы головного мозга хирургическим методом
Зачастую аневризму сосудов головного мозга выявляют в двух случаях: во время поиска причин появления неврологических симптомов и при обследовании пациента уже при свершившемся кровоизлиянии в результате разрыва аневризмы. Сегодня медицина располагает несколькими методами лечения аневризмы. Один из них – хирургический. Далее мы разберемся, в каких случаях показана операция, какие виды оперативного вмешательства применяются и каковы возможные последствия такого лечения.
Каждый пациент с аневризмой требует индивидуального подхода, так как каждый случай заболевания – уникальный. Врач должен учитывать анамнез больного, данные диагностического обследования и ряд других факторов. Прежде всего, на выбор метода лечения влияет:
- тип аневризмы сосуда, ее локализация и размеры;
- общее состояние здоровья больного;
- вероятность разрыва аневризмы;
- возрастные характеристики пациента;
- наличие каких-либо других заболеваний;
- наследственные факторы;
- учет рисков, которые могут возникнуть в результате лечения и т.д.
Учитывая эти показатели, врач принимает важное решение о методе лечения. Оно может быть нескольких видов:
- Контроль над динамикой заболевания без вмешательства. Пациент находится под постоянным наблюдением врачей. Обычно к такому методу прибегают при мелких аневризмах с крепкой оболочкой, то есть вероятность разрыва и серьезных последствий кровоизлияния невысокая.
- Медикаментозная терапия. Назначаются препараты, помогающие убрать некоторые симптомы аневризмы мозговых сосудов – тошнота, головные боли, скачки артериального давления.
- Один из распространенных методов лечения аневризмы головного мозга – операция. Обычно применяют либо прямые операции на аневризме, либо метод эндоваскулярной эмболизации. Именно данную группу методов лечения мы рассмотрим более подробно.
Какие применяют виды оперативного вмешательства при аневризме головного мозга
В том случае, если аневризма располагается в жизненно важном участке головного мозга и риск кровоизлияния высок, оперативное вмешательство неизбежно. Также избежать операции не удастся, если размер аневризмы превышает 7 мм. Еще учитываются имеющиеся случаи кровоизлияний в головной мозг у кого-либо из близких родственников.
- Прямые операции:
- треппинг;
- клипирование;
- отключение несущей артерии;
- применение хирургической марли для упрочнения стенок поврежденного аневризмой сосуда.
- Эндоскопические операции.
Прямые операции предполагают хирургическое проникновение в определенную область головного мозга через отверстие в своде черепа.
Метод треппинга применяется в том случае, если аневризма мозгового сосуда расположена выгодно с точки зрения имеющегося альтернативного кровоснабжения, которое может на достаточном уровне обеспечить головной мозг необходимыми веществами. Такую операцию еще принято называть ловушкой для аневризмы. Суть заключается в том, что выполняется отключение сосуда в местах до аневризмы и после нее. Таким образом обесточивается конкретный участок сосуда, а не самой аневризмы.
Метод клипирования – самый распространенный. Во время операции выполняется наложение сдавливающей клипсы на тело или шейку аневризмы. Так отключается кровоток в ней, что препятствует разрыву и последующему кровоизлиянию.
Существует возможность полнейшего отключения артерии, несущей аневризму. Далее накладываются сообщения (анастомозы) между сосудами, что дает возможность наладить альтернативное кровоснабжение.
Использование хирургической марли для упрочнения стенок сосудов применяют тогда, когда клипирование невозможно в связи с повышенным риском возникновения серьезных осложнений. Принцип этого метода в том, что вследствие проникновения в организм человека инородного предмета (марли) начинают прогрессировать склеротические процессы вокруг аневризмы. Спустя некоторое время в области поврежденного сосуда начинает уплотняться соединительная ткань, что и препятствует разрыву аневризмы. Опасность такой операции в том, что вероятность кровотечения из самой аневризмы в первые несколько дней после вмешательства достаточно высокая.
Эндоскопические операции хоть и относят к хирургическому вмешательству, однако, такой метод более безопасный и менее травматичный для организма пациента.
Суть эндоваскулярного метода заключается в том, что никакие разрезы и вскрытия не производятся. Достаточно одного точного прокола артерии, чтобы ввести специальный катетер и по кровеносному сосуду под контролем рентгена добраться до аневризмы в головном мозгу. На пораженный участок устанавливают специальный баллон (более ранняя методика) или спираль (современная технология), что дает возможность остановить кровоток.
Преимущество установки спирали в том, что кровоток останавливается постепенно путем естественного образования тромба. Таким образом, нервная ткань имеет возможность адаптироваться к сокращению кровотока.
Того же нельзя сказать про установку баллона, когда кровоснабжение в определенном участке мозга прекращается резко, что, возможно, иногда и спасает жизнь пациенту, но иногда и влечет за собой негативные последствия.
Стоимость операции аневризмы головного мозга зависит от нескольких факторов. Таких, например, как конкретный вид хирургического лечения, состояние больного, возможности самой клиники и т.п.
Так как любое хирургическое вмешательство в области мозга – серьезный и ответственный процесс, возможны последствия операции аневризмы головного мозга:
- разрыв аневризмы во время операции;
- при установке спирали возможно повреждение стенки аневризмы;
- ухудшение кровоснабжения нервной ткани, развитие инсульта.
Большинство осложнений, возникнувших во время операций, устраняются незамедлительно.
Если операция была профилактической, а не вынужденной вследствие состоявшегося разрыва аневризмы, большинство пациентов возвращаются к привычному укладу жизни.
Так или иначе, риск развития инвалидизации или летального исхода при аневризме с оперативным вмешательством значительно уменьшается по сравнению с отсутствием своевременной операции. Длительность восстановления больного зависит от общего состояния организма, места расположения и размера аневризмы, конкретного вида операции и т.п.
источник
а) Методы эндоваскулярного лечения аневризмы сосуда головного мозга. Попытки окклюзии аневризмы при помощи отделяемого баллона в 1980-х годах сопровождались высокими рисками и не предотвращали повторное кровоизлияние. Введение Guglielmi отделяемых спиралей (GDC) в 1990 г. оказалось намного более безопасной и более эффективной альтернативой. Платиновые спирали вводятся через катетер в дно аневризмы и отделяются электролитически. «Плотная упаковка» аневризмы несколькими спиралями занимает менее одной трети фактического объема, но этого достаточно, чтобы предотвратить повторное кровотечение у большинства пациентов.
Примерно в одной трети случаев радиологи специально оставляют заполнение шейки аневризмы в связи с риском окклюзии спиралью проксимального сосуда, в этом случае риск повторного кровоизлияния выше.
Приблизительно в 5% случаев эмболизация аневризмы не удается. Аневризмы подходят для эмболизации если соотношение дно/ширина шейки больше чем 2:1. Радиологи могут выбирать спирали разного диаметра и ЗЭ-формы. Как правило, требуется от четырех до пяти спиралей, но возможное количество варьируется от одной спирали для 3 мм аневризмы до 20 спиралей для гигантских аневризм.
1. Коррекция с помощью баллона. Этот метод, разработанный Moret, позволяет эмболизировать аневризмы с широкой шейкой. Периодическое раздувание баллона на отдельном катетере в несущем сосуде предотвратцает выпадение спиралей в просвет сосуда. По окончании процедуры спирали сохраняют форму, приданную им баллоном. Некоторые центры используют эту технику в 30-40% случаев эндоваскулярной хирургии.
2. Биоабсорбирующие полимеры. Новые разработки включают в себя использование биоабсорбирующего полимерного покрытия вокруг спирали (Matrix) или в спирали (Cerecyte). Экспериментальные работы на животных показали, что эти полимеры стимулируют регенерацию клеток, способствуют организации тромба в аневризме и стимулируют образование новой интимы. Будут ли эти спирали улучшать общие результаты, остается неопределенным, эта информация будет получена в ходе исследований.
3. Гидрогелевые и волокнистые спирали. Гидрогелевые спирали покрыты гидрофильным полимером, расширяющимся при контакте с кровью, что помогает заполнить просвет аневризмы. Кроме того, спирали с волокнами дакрона или нейлона вызывают более тромбогенную реакцию, чем платина, однако все эти новые технологии ждут дальнейших исследований.
4. Интракраниальные стенты. Введение в практику стентов подходящего размера и достаточной гибкости для прохождения через внутричерепные сосуды предоставило другую альтернативу для аневризм, имеющих широкую шейку, гигантских или веретенообразных аневризм, особенно развивающихся из внутренней сонной артерии или развилки основной артерии. После установки стента микрокатетером можно пройти через стент в полость аневризмы, чтобы разместить в ней спираль без риска окклюзии просвета сосуда. Для предотвращения тромбоза стента назначается пожизненная антитромбоцитарная терапия.
5. Оникс. Оникс — жидкий полимер, который затвердевает при контакте с кровью, может быть введен в аневризму, если ее шейка защищена баллоном или стентом. Теоретически метод весьма привлекателен, но первые исследования показали высокий уровень сложности выполнения, что ограничивает его более широкое применение.
6. Отдаленные результаты эндоваскулярной хирургии. При любых вмешательствах необходимо проведение контрольной ангиографии, как правило, через шесть месяцев после лечения. Реканализация аневризмы за счет уплотнения или миграции спиралей требует повторного вмешательства примерно у 10% пациентов.
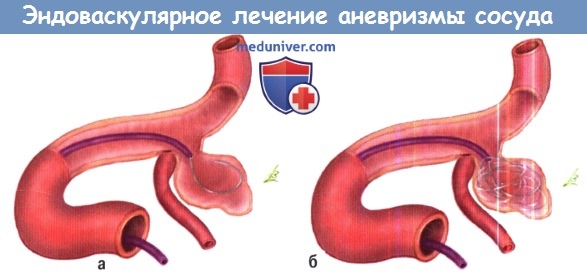
Б. Введение последующих спиралей.
б) Выбор эндоваскулярного метода лечения аневризмы сосуда головного мозга. Изначально, в 1990-х годах эндоваскулярное лечение предназначалось для неоперабельных аневризм. Данная методика лечения чаще используется для тех аневризм, которые трудно лечить открытым путем, в частности, аневризм заднего обращения, несмотря на все убедительные доказательства большей радикальности. Международное исследование аневризматического САК (ISAT)—клипирование против койлинга, началось в 1994 г. Комитет по мониторингу данных остановил сбор информации в 2001 г. после того, как центры изучили данные 2143 пациентов.
Исследование показало, что через один год после эндоваскулярной эмболизации абсолютный риск смерти снизился на 7% (относительный риск снижался на 23%) по сравнению с пациентами, перенесшими клипирование. Значительно больше повторных кровоизлияний и более высокая смертность от повторного кровоизлияния имели место в течение первого года в группе койлинга, однако исследователи по-прежнему выступают за данную методику. Несмотря на отсутствие долгосрочных результатов и то, что пациенты выбранной группы почти всегда имели хороший соматический и неврологический статус, а также небольшую аневризму переднего отдела вилизиева круга, в Великобритании резко сменилась тактика лечения в пользу эмболизации; доля операций внутрисосудистым методом увеличилась с 37 до 54%. Во многих центрах этот показатель в настоящее время превышает 80%.
Последующее семимилетнее наблюдение за пациентами ISAT показало, что выживаемость за это время выше, несмотря на повышенный риск позднего повторного кровоизлияния в эндоваскулярной группе.
Лечение аневризм проводится бригадой специалистов, состоящей из интервенционных радиологов и нейрохирургов. Даже если бы не было разницы в результатах между этими двумя методами лечения, большинство пациентов выбрали бы наименее инвазивный подход. Результаты ISAT подтверждают использование эмболизации в качестве метода первой линии. Тем не менее, не все аневризмы подходят для эндоваскулярного лечения. Следующие факторы делают эмболизацию более трудной или невозможной:
— Аневризма средней мозговой артерии
— Аневризмы с широкой шейкой и соотношением тело/ширина шейки менее чем 2:1
— Аневризмы 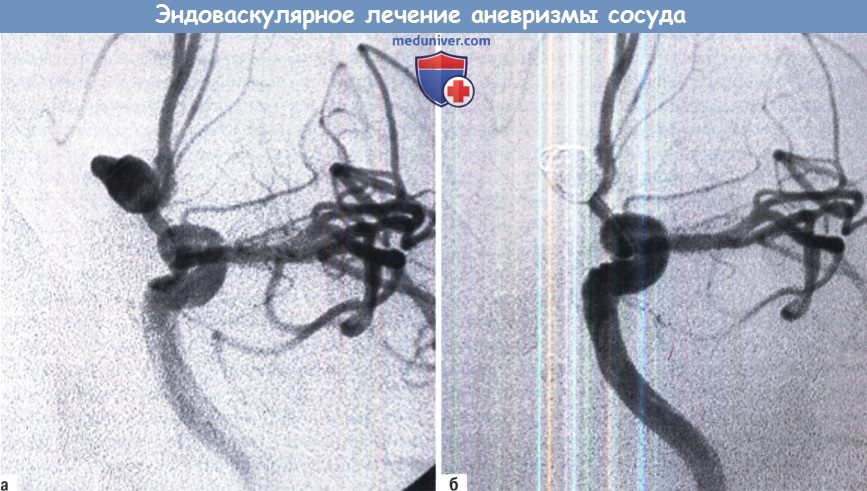
Б. Завершающая стадия эмболизации спиралями, показывающая дно, заполненное спиралями.
источник
В 1994 году Дейк и соавторы впервые сообщили об использовании «трансплантатов-стентов» для лечения нисходящих аневризм грудного отдела аорты у лиц, которые, подвергаются чрезмерному риску при проведении стандартной открытой хирургии. Они показали, что размещение трансплантатов-стентов грудной аорты, также называемое эндоваскулярным лечением аорты, может быть выполнено с технической точки зрения с относительно низкими возможными осложнениями; однако они отметили, что требуется долгосрочное наблюдение. Первоначальные стент-трансплантаты были фактически сконструированы самими имплантирующими клиническими врачами; позже устройства были ограничены теми, кто находился под исследованием.
Важно отметить, что у небольшого процента больных, перенесших эндоваскулярное лечение аневризм грудного отдела аорты, аневризмы не были полностью исключены из аортального кровообращения через 1 и 2 года наблюдения. Как и при исследовании 1994 года, проведенном Дейком и соавторами, авторы утверждали, что всем лицам, перенесшим установку стент-трансплантатов, требуется тщательное долгосрочное наблюдение врачей.
Эндоваскулярное лечение аневризм грудного отдела аорты технически возможно для лиц с расслоением нисходящего отдела грудной аорты. Однако, продолжающиеся исследования все еще пытаются определить, каким группам больных с расслоением грудной аорты может применяться указанная методика лечения. Больные со сложными диссекциями, в том числе с нарушением перфузии (когда кровоснабжение затруднено лоскутами аортальной ткани, вызванными диссекцией), вероятно, получают выгоду от применения эндоваскулярного лечения для герметизации места диссекции и повторного нанесения слоев стенки аорты.
Следует отметить, что исторически открытые хирургические подходы у больных с диссекцией, связанной с диссекцией, имели высокую смертность. Соответственно, в клиническом исследовании было изучено лечение для лиц со сложным расслоением. В этом многоцентровом клиническом исследовании участвовали пациенты, имеющие сложное расслоение аорты типа B, которым устанавливалась эндоваскулярная система, состоящая из проксимальных трансплантатов грудного стента TX2 и дистальных голометаллических стентов для расслоения. Показания к применению включали в себя следующее:
- Неправильная перфузия сосудов
- Возможный разрыв
- Диаметр аорты ≥40 мм
- Быстрое расширение аорты
- Постоянная боль или гипертония, несмотря на максимальную медикаментозную терапию
В данном клиническом исследовании 30-дневная смертность составила 5% (2/40); еще две смерти произошли через 30 дней, что привело к 1-летней выживаемости на уровне 90%. Исследователи отметили ремоделирование аорты с уменьшением диаметра ложного просвета и увеличением истинного диаметра просвета с полным тромбозом ложного просвета у 31% через 1 год.
Казалось бы логичным, что эндоваскулярное лечение аневризм грудного отдела аорты также может быть использовано для больных с неосложненным расслоением.
С 2005 года использование эндоваскулярных трансплантатов стента при заболеваниях грудной аорты резко возросло. Впоследствии хирурги разработали новые методы для облегчения использования эндоваскулярного лечения аневризм грудного отдела аорты у лиц с более высоким риском с более сложной анатомией. Ветвящиеся сосуды, которые были бы закрыты трансплантатами стента, часто можно обойти, и зону установки можно перемещать более проксимально, чтобы обеспечить адекватное уплотнение.
Помимо этого, в настоящее время проводятся испытания, которые направлены на устранение патологии грудной аорты, затрагивающей или затрагивающие сосуды дуговой ветви.
Со временем различные устройства стент-трансплантаты меньшего профиля были исследованы в ходе испытаний. В настоящее время устройства наименьшего профиля рассматриваются для больных с маленькими подвздошными артериями.
Эндоваскулярное лечение аневризм грудного отдела аорты существует уже два десятилетия, и его стали называть первой линией лечения большинства нисходящих патологий грудной аорты, аневризм, расслоений и проникающих язв аорты, что приводит к значительному снижению заболеваемости и смертности по сравнению с открытым хирургическим вмешательством. Улучшенные материалы, уменьшенные размеры оболочки для размещения, улучшенная совместимость, разработка конических трансплантатов и доступность более широкого диапазона размеров – все это улучшило применимость стент-трансплантатов и результаты процедуры в течение первого десятилетия широкого использования.
Официальное назначение для стент-трансплантатов, доступных в настоящее время, предназначено для лечения нисходящих аневризм грудного отдела аорты с диаметром по крайней мере, в два раза больше, чем у соседней аорты. Помимо этого, должно быть достаточное количество аорты (обычно 2 см) нормальных размеров с обеих сторон аневризмы (так называемые проксимальные и дистальные зоны посадки), чтобы позволить стент-графту прилипать (уплотнять) к стенкам аорты и добиваться исключения аневризма.
Стент-трансплантаты все чаще считаются оптимальным лечением сложных нисходящих расслоений грудной аорты, предпочитая открытую хирургию. Клинический опыт с течением времени, продолжающаяся эволюция эндоваскулярных устройств и несколько многоцентровых исследований привели к одобрению устройств для стент-трансплантации грудного отдела аорты для применения у пациентов с острой и хронической диссекцией.
Больные с очаговыми проникающими язвами в грудной аорте составляют другую группу, в которой эндоваскулярное лечение может оказаться полезным, потому что у этих лиц определены ограниченные участки грудной аорты, где потеря целостности эндотелия может привести к потенциально опасному для жизни разрыву. Покрытие язвы стент-графтом может быть выполнено с минимальной заболеваемостью. Тем не менее больные с проникающими язвами часто имеют обширное заболевание периферических сосудов, что может ограничивать их пригодность для лечения.
Эндоваскулярное лечение аневризм грудного отдела аорты может спасти жизнь больному и в настоящее время стало стандартом лечения лиц с травмой грудной аорты, приводящей к разрывам интимы аорты, псевдоаневризмам или открытым разрывам.
Пациенты, перенесшие стент-трансплантацию, должны иметь анатомию, подходящую для развертывания эндотрансплантатов.
Противопоказаниями для размещения данных устройств являются:
источник
Автор: Аверина Олеся Валерьевна, к.м.н., врач-патолог, преподаватель кафедры паталогической анатомии и патологической физиологии
Эндоваскулярная хирургия представляет собой относительно новое, но очень перспективное направление в современной медицине. Основное ее преимущество — малоинвазивность, когда для доступа к сложным анатомическим структурам или внутренним органам достаточно лишь небольшого кожного разреза и введения проводника через сосуд.
Особенно актуально эндоваскулярное лечение в сосудистой и нейрохирургии. Так, с помощью этой техники есть возможность избавлять пациентов от бляшек и тромбов в сосудах, проводить шунтирование при патологии печени, лечить аневризмы головного мозга и других органов, устанавливать специальные фильтры, улавливающие тромбы в венах, «выключать» из кровотока отдельные сосуды, вводить химиопрепараты и ограничивать кровообращение в опухолях.
В нейрохирургии эндоваскулярные вмешательства проводят все чаще из-за серьезного риска, который можно нанести мозгу не только в ходе открытой трепанации, но и при микрососудистых операциях. Интервенционные хирурги помогают справиться с тяжелейшей патологией в виде аневризматических образований и мальформаций в самых труднодоступных областях мозга.
Сегодня эндоваскулярные вмешательства становятся все более востребованными, ведь риск от них в разы меньше, чем при открытых операциях, а эффективность зачастую даже выше. Тем не менее, поставить такое лечение на поток пока невозможно ввиду дороговизны, технической сложности, отсутствия достаточного числа квалифицированных хирургов, владеющих техникой эндоваскулярных операций.
Сосудистый доступ изначально был направлен на поиск патологии и представлял собой сугубо диагностическую манипуляцию. Со временем стало понятно, что он вполне возможен и для лечения различных заболеваний. Совершенствование оборудования и методов визуализации позволили эндоваскулярной хирургии выйти в число приоритетных направлений медицинской науки и практики.
Основное отличие эндоваскулярных вмешательств от классических операций состоит в способе доступа к патологически измененным тканям или органам, который представляет собой небольшой разрез или прокол стенки сосуда. Сквозь полученное отверстие в сосуд вводится проводник, который направляется в нужную область тела.
Эндоваскулярная хирургия невозможна без качественной визуализации происходящего в сосуде ввиду риска тяжелых осложнений и невыполнимости тонких хирургических манипуляций вслепую, поэтому такие вмешательства проводятся в условиях обязательного ангиографического контроля. В специальной рентгеноперационной создаются все условия для слежения за ходом вмешательства и безопасности пациента.
Даже самое простое эндоваскулярное лечение может провести лишь специально обученный хирург, владеющий не только навыками работы со сложными инструментами и оборудованием, но и имеющий квалификацию рентгенолога.
В ходе эндоваскулярной операции, как правило, нет необходимости в применении общего наркоза. Достаточно местной анестезии в месте, где будет пунктирован или надрезан сосуд. Эта особенность дает возможность лечить пациентов с тяжелыми заболеваниями, при которых стандартные операции очень рискованны. После вмешательства не будет ран и заживающих рубцов, поэтому выписка из клиники происходит в максимально короткие сроки.
Таким образом, эндоваскулярная операция имеет неоспоримые преимущества, однако не лишена и недостатков. Весомыми плюсами метода считаются:
- Малоинвазивность и минимальная операционная травма в сочетании с высочайшей эффективностью;
- Более низкий операционный риск;
- Минимальный болевой синдром;
- Быстрое восстановление после лечения;
- Отсутствие необходимости наркоза;
- Возможность проведения при сопутствующем неблагоприятном фоне, когда стандартное хирургическое лечение противопоказано.
Недостатки эндоваскулярной хирургии связаны с высокой стоимостью оборудования, необходимостью наличия рентгеноперационной и проведения обучения хирургов, что доступно далеко не всем регионам и клиникам. Сегодня эндоваскулярное лечение проводится лишь в крупных специализированных медицинских центрах.
Эндоваскулярная хирургия уникальна по своей сути и позволяет проводить лечение самой сложной патологии жизненно важных органов, открытые манипуляции на которых могут представлять опасность для здоровья и даже жизни. Она используется:
-
В кардиологической практике для лечения острой и хронической ишемии миокарда на фоне атеросклероза артерий сердца;
- Нейрохирургами при обнаружении сосудистой патологии мозга (аневризма, мальформация, приобретенные атеросклеротические и тромботические изменения);
- В сосудистой хирургии для облегчения кровотока при облитерирующих заболеваниях артерий ног, при тромбоэмболических поражениях артерий легких, ишемии кишечника и др.
- При циррозе и злокачественных опухолях печени;
- При опухолевой патологии внутренних органов (миома матки, аденома простаты).
Эндоваскулярная хирургия может помочь как расширить сосуд в случае его закупорки, так и выключить из кровотока путем эмболизации. Второй вариант показан для малоинвазивного лечения некоторых доброкачественных новообразований, которые регрессируют сами, утратив источник питания.
К методам эндоваскулярной хирургии относятся:
Все эндоваскулярные операции проводят в специально оборудованной операционной, причем и пациенты, и хирурги применяют защиту от рентгеновского излучения, которое не раз понадобится в ходе вмешательства.
Подготовка перед лечением — стандартная, включающая анализы крови и мочи, инструментальные обследования, ЭКГ, консультации узких специалистов. На момент вмешательства пациент должен быть максимально обследован и стабилен, хроническая патология компенсируется медикаментозно. Противопоказано интервенционное радиохирургическое вмешательство при острой инфекционной патологии, аллергии на йод, декомпенсации работы внутренних органов, беременности, инфекционном поражении кожи в месте предполагаемой пункции.
Самой частой эндоваскулярной операцией считается ангиография, которая проводится с целью определения характера патологии, степени сужения сосуда, параметров аневризм или других сосудистых аномалий. Она нередко предваряет другие способы интервенционных операций, являясь первым, диагностическим, этапом лечения патологии.
В ходе ангиографии хирург пунктирует сосуд, затем вводит туда изогнутый полимерный катетер и рентгеноконтрастное йодсодержащее вещество. Контраст заполняет нужные сосуды и показывает их особенности на сериях рентгеновских снимков. Противопоказанием к процедуре может стать аллергия на йод. Ангиография обязательна при планировании стентирования, эмболизации и других интервенционных хирургических операций.
заключается во введении в просвет сосуда специального баллона, который раздувается воздухом и увеличивает диаметр артерии или вены, улучшая кровоток. Этот способ лечения применяется при локальном атеросклеротическом поражении со стенозом артериального просвета и признаками ишемии в тканях. Баллонная ангиопластика может сопровождаться имплантацией стента.
Суть операции состоит в проколе крупного сосуда, через который вводится проводник с баллоном. Баллон достигает зоны стеноза, там хирург его раздувает, благодаря чему происходит раздавливание и равномерное распределение по стенке артерии или вены тромботических масс или атеросклеротических наложений. В таком положении баллон удерживается примерно минуту, далее проводится рентгенологический контроль эффективности, и в случае благоприятного результата сдувается и выводится наружу.
Установка сосудистых фильтров тоже проводится методом интервенционной хирургии. Обычно объект — нижняя полая вена, в которую попадают тромботические массы из сосудов нижних конечностей. В ходе операции хирург пунктирует бедренную вену и вводит через нее специальный фильтр, который прикрепляется к стенке полой вены и не дает кровяным сгусткам проникнуть дальше — в сердце и сосуды легких. Операция показана при варикозной болезни, тромбофлебите, патологии гемостаза с тромбообразованием.
Стентирование — одно из самых частых рентгенэндоваскулярных вмешательств, которым активно пользуются кардио- и ангиохирурги всего мира. При операции в сосудистый просвет помещается специальная спираль или подобие пружины, которые, расправляясь, делают его шире, обеспечивая приемлемый уровень кровотока.
Не секрет, что патология сердца — одна из ведущих причин не только заболеваемости людей зрелого и пожилого возраста, но и смертности. Причина ишемических процессов в миокарде — атеросклероз, мешающий артериям осуществлять доставку кислорода. До того, как были внедрены эндоваскулярные способы лечения, кардиохирурги вынуждены были проводить шунтирование, а в части случаев — отказаться и от него из-за высокого операционного риска и наличия противопоказаний.
Стентирование позволяет многим пациентам избежать травматичной операции, оно проводится при атеросклерозе коронарных сосудов, когда имеющиеся бляшки сильно сужают артерию, нарушают кровоток и провоцируют ишемические изменения. Кроме того, метод особенно актуален для пожилых людей и лиц, страдающих тяжелыми сопутствующими заболеваниями, не позволяющими применять никакие другие операции, кроме малоинвазивных.
стенозирующий атеросклероз коронарных артерий
Стент представляет собой металлическую ячеистую трубку, которая, попав в просвет артерии, расправляется и плотно прижимается к ее стенкам, делая просвет более широким. Кровоток усиливается, а признаки ишемии устраняются.
Перед имплантацией стента пациенту проводят ангиографию, чтобы определить, где произошел стеноз и какова его степень. Во время исследования пунктируется бедренная артерия, в которую вводят рентгеноконтрастный препарат, достигающий артерий сердца и показывающий степень их изменений. Снимки производят в нескольких проекциях. Учитывая, что в состав контраста входит йод, аллергия на это вещество может стать препятствием к эндоваскулярному лечению.
стент в коронарной артерии сердца
Эндоваскулярное стентирование проводят в рентгеноперационной с постоянным ЭКГ-контролем. Анестезия — местная. Доступ проводится сквозь бедренную артерию или сосуды руки, в которые помещают катетер, а по нему — проводник для доставки стента. Проводник имеет баллон, который как бы раздует сосуд и поместит в нужное место сжатый стент. Стенты производят из биосовместимых материалов, которые не вызывают отторжения и аллергии и способны подстраивать свою ширину под диаметр артерии.
Когда стент будет установлен, хирург еще несколько раз раздует баллон, проверяя точность и надежность проведенной операции, а затем сдует его и выведет из сосуда. При тяжелом поражении артерий можно использовать несколько стентов сразу.
Стентирование дает стойкий положительный результат, при этом оно в разы безопаснее открытых вмешательств. Среди осложнений возможны кровоизлияния и кровотечения из мест прокола сосудов, для предупреждения которых пациент соблюдает постельный режим и находится под наблюдением специалистов отделения реанимации. Спустя несколько суток можно покинуть клинику.
Стентирование практически бескровно, длится около получаса, осложнения крайне редки. К слову, шунтирующие операции или открытая пластика сосудов требуют искусственного кровообращения, общей анестезии и могут занять 2-3 часа, после чего предстоит длительная реабилитация.
Одним из недостатков стентирования считают возможность возврата стеноза из-за прорастания импланта мышечными волокнами сосудистой стенки. Такое происходит у пятой части прооперированных после установки инертных стентов. Для профилактики рецидива разрабатываются стенты, имеющие лекарственную оболочку, препятствующую гиперплазии стенки сосуда.
Современные стенты очень разнообразны по составу, форме, наружному покрытию. Они могут саморасправляться, не требуя помощи баллона. При внедрении в артерию стента нового поколения рестеноз наблюдается лишь у 5 пациентов из ста.
Видео: стентирование сосудов нижних конечностей
Еще один эндоваскулярный метод, который активно практикуется хирургами, – это эмболизация сосудов. Такая операция состоит в выключении из кровотока сосуда путем введения эмболизирующих средств и проводится она рентгенохирургом. Эмболизация может устранить патологию либо предупредить постоперационные осложнения в случае применения перед радикальной операцией.
Показаниями к эндоваскулярной эмболизации считают:
- Кровотечения, в том числе — после родов, неудачных операций, травм;
- Сосудистую патологию — аневризма, мальформация, варикозное расширение вен пищевода и ног;
- Онкопатологию — новообразования печени, почек, миома матки.
Эмболизация — это малоинвазивная альтернатива открытой операции, которая проводится доступом через просвет сосуда и под местной анестезией либо и вовсе без обезболивания, однако вмешательства на сосудах головного мозга или воротной вене печени требуют общего наркоза.
Для уточнения особенностей анатомии и локализации нужного сосуда необходима предварительная ангиография, которая также помогает выбрать нужный катетер и проводник. После обработки кожи антисептиками хирург пунктирует сосуд и вводит в него эмболизирующее средство, коим может стать:
- Металлическая спираль из платины или стали либо другая частица — применяют для закупорки мелких сосудов, ликвидации аневризм и глубоких мальформаций;
- Желатиновая пена — вызывает временную закупорку сосуда, может сочетаться с установкой спиралей;
- Акрилово-желатиновые микросферы — считаются лучшими для постоянной эмболизации;
- Жидкие составы — липиодол, NBCA, этанол, сотрадекол;
- Съемные баллоны — имплантируются в аневризму или мальформацию, заполняются физраствором и прекращают кровоток.
После введения эмбола выполняется ангиография для контроля качества эмболизации.
Разновидностью эндоваскулярной окклюзии сосудов считают химиоэмболизацию, которая проводится в онкологии для введения химиопрепарата в опухолевые сосуды. После операции объем опухоли уменьшается, что облегчает последующее оперативное лечение.
Химиоэмболизация бывает масляной и с введением специальных микросфер. Под контролем ангиографии в сосуд вводят масляный раствор с противоопухолевым препаратом, который пропитывает опухоль локально. В качестве масляного препарата применяют липиодол. Этот эндоваскулярный метод не способствует продолжительной и постоянной эмболизации.
Введение микросфер проводится под контролем ангиографии с помощью специального катетера. Микросферы предварительно пропитывают цитостатиком, затем вводят в сосуд, который они закупоривают и начинают выделять химиопрепарат. Эмболизация микросферами дает постоянный эффект, ее проводят при первичных и метастатических опухолевых узлах.
Преимуществами эндоваскулярной эмболизации считаются:
- Малоинвазивность;
- Отсутствие разрезов и рубцов;
- Низкий риск осложнений;
- Возможность минимальной анестезии;
- Короткая реабилитация;
- Высокая эффективность при сохранности анатомических образований.
К недостаткам эмболизации относят необходимость наличия высококвалифицированного рентгенохирурга и соответствующего оборудования. Кроме того, эмболизация может дать рецидив патологии, применима не для каждого пациента, возможны серьезные осложнения в виде миграции эмболов и разрыва сосуда.
Таким образом, эндоваскулярная хирургия — это не только современное, но и очень эффективное лечение широкого круга заболеваний, которое все чаще заменяет традиционные хирургические операции благодаря массе преимуществ. Методики модифицируются, совершенствуются и становятся более безопасными.
источник
Сегодня мировая медицинская практика не содержит определенных правил при подборе тактики ведения пациентов с аневризматической болезнью головного мозга (АБГМ). Подбор оптимального метода лечения аневризм зависит от субъективных факторов: месторасположения, морфологических особенностей самой аневризмы (мешотчатая, фузиформная), ширины шейки аневризмы, наличия или отсутствия и локализации гематомы, тяжести общефизического состояния пациента, а также сроков его поступления в медучреждение. Лечебная стратегия обуславливается уровнем безопасности оперативного вмешательства и нацелена на снижение травматичности оперативных манипуляций.
Разрыв аневризмы мозговой артерии — самое опасное осложнение аневризматической болезни
Развитие, популяризация малоинвазивных техник эндоваскулярной хирургии АБГМ имеет следующие преимущества:
- Возможность проведения операции на тяжелых стадиях (III-V по классификационной шкале Hunt-Hess).
- Уменьшение продолжительности вмешательства, снижение наркозной интоксикации.
- Повышенная радикальность исключения аневризматического участка из общего кровотока.
- Возможность подбора методики локализации неразорвавшихся и разорвавшихся аневризм, в т.ч. для стадии кровоизлияния (холодной).
- Отсутствие необходимости в трепанации черепа, сокращение периода восстановления.
Эндоваскулярная окклюзия аневризмы представляет собой альтарнативный подход к лечению АБГМ, который помогает радикально, эффективно, минимально инвазивно купировать аневризмы разного типа, происхождения.
Около 60-70% мозговых аневризм протекают без выраженной симптоматики. При малейшем подозрении на наличие либо разрыв аневризматического мешка производится полное обследование сосудистого бассейна ГМ. Есть несколько способов верификации АБГМ.
Данная диагностическая методика признана наиболее информативной для своевременного обнаружения мозговых патологий: венозных соустий, артериальных аневризм, окклюзий, стеноза отдельных участков сосудистой системы. Данное исследование подразумевает введение контрастного йодсодержащего раствора с последующей фиксацией его распространения при помощи рентгеновской аппаратуры. Выделяются несколько видов ангиографии:
Виды ангиографии сосудов головного мозга: КТ, МР и прямая селективная
Доступ к целевым сосудам производится через правую бедренную артерию. Катетер специальной формы через интродъюсер (антитравмирующая трубка с клапаном) заводится в основные магистральные артерии, питающие мозг. Современные установки позволяют в режиме реального получать высококачественные трехмерные изображения сосудистого русла. При смене проекции (положения C-дуги) интегрированная объемная модель будет соответствующим образом отклоняться на демонстрационном мониторе, помогая визуально оценить реальное состояние сосудистого дерева, найти аневризматические поражения.
Ротационная ангиография с 3D реконструкцией – наиболее точный метод, помогающий выбрать ангуляцию с оптимальным отображением шейки аневризмы и расположенных рядом сосудов, выстроить верную тактику дальнейшего лечения интракраниальных аневризматических образований сложной формы, непростой локализации.
Оперативное малоинвазивное вмешательство производится с учетом имеющихся хронических патологий сердца и сосудов, возраста, общефизического состояния больного, типа, количества внутричерепных аневризм. Применение неинвазивных лечебных методик показано:
- пациентам старше 60 лет;
- людям, имеющим отягощенный соматический статус;
- при аневризмах с широкой шейкой, неблагоприятными размерными параметрами «шейка-дно»;
- анатомически неудачно расположенных аневризмах.
Все манипуляции на сосудах ГМ проводятся под многократным увеличением в специализированной операционной. Дополнительно осуществляется постоянный рентгенологический контроль. Эндоваскулярные вмешательства производятся через небольшой прокол, который делается около паховой связки. Посредством интрадюссера в бедренную артерию вводятся необходимые катетеры. Далее телескопический микрокатетер с внутренним просветом около 1 мм проводится в требуемый участок сосудов головного мозга.
Эмболизация аневризмы микроспиралями
Вмешательства подобного типа применяются при аневризмах с зауженным основанием (шейкой). Оно особенно показано в остром периоде кровоизлияния. Аневризматическая полость полностью заполняется изнутри тонкими платиновыми проволочками, имеющими мягкую структуру. За счет этого аневризма целиком выключается из процесса кровообращения. Тем самым исключает риск разрыва сосудистой стенки, уменьшает вероятность осложнений.
Эмболизация аневризмы микроспиралями со стент-ассистенцией
Эмболизация аневризмы микроспиралями axium со стент-ассистенцией стентом solitaire
Метод подразумевает использование микроспиралей совместно со специальным ячеистым стентом. Ячейки поддерживают витки спиралей в пришеечной области. Операции подобного типа назначаются исключительно в холодном периоде поскольку требуют обязательного назначения дезагрегантов. Используется как вспомогательное средство при лечении сложных аневризм (фузиформенных, генерелизованных). Предотвращает миграцию микроспиралей в просвет несущего сосуда. Обзор Shapiro et al. в 2015 г. показал: процент успешно окклюзированных аневризм мозга после стентирования – свыше 61%.
Суть методики заключается во временном раздувании в несущем сосуде (на уровне шейки аневризмы) неотделяемого баллона. Манипуляции проводятся одновременно с имплантацией платиновых спиралей. Существует несколько вариантов эмболизации: применение шарообразных, гиперрасширяющихся элементов, баллонов с двойным просветом. После достижения надежной фиксации спиралей в просвете аневризмы надувные элементы удаляются. Стойкость, эффективность баллон-ассистированной окклюзии согласно статистическим данным Cekirge S. et al. (способ проверки – контрольные ангиографии) – 82%.
Модифицированная стент-ассистенция применяется для купирования интракраниальных бифукационных аневризм с широкой шейкой. Стенирование производится с помощью специальных стентов. К одним из таких относится pCONYS – самораскрывающийся натилоновый матричный стент. Устройство предназначено для корректного ремоделирования сосудов при аневризмах биффуркационного типа.
Конструкция стента обеспечивает оптимальное позиционирование в аневризматической полости и предполагает возможность репозиционирования элемента с полным удалением в доставляющий микрокатетер. Согласно рданным, опубликованным в Journal of Vascular Surgery за 2013-2014 гг., положительный результат применения эндопротезов артерий ГМ достигается в 97,3% клинических случаев. Современные стент-ассистирующие методики не повышают процент инраоперационных осложнений, относительно безопасны, обеспечивают долговременный результат.
Поток перенаправляющий стент
Методика эффективна при лечении фузиформенных аневризм, аневризм с пришеечной реканализацией, когда есть трудность в проведении койлинга (GDC). Способ подразумевает установку самораскрывающихся стентов густого плетения, которые определенным образом перенаправляют поток крови в сосудистом просвете. Это приводит к стагнации крови в полости, провоцируя тромбоз аневризмы. Направляющий стент подбирается согласно диаметру артерии (+0,25 миллиметров). Его длина должна превышать размер артериального дефекта на 10-12 мм.
Эндоваскулярные операции являются на сегодняшний день методом выбора в лечении аневризм артерий головного мозга.
источник
Увеличение случаев заболеваний сосудов, сердца, атеросклероза аорты, требует постоянного поиска решения этой проблемы, поэтому ученые и медики активно ведут работу над изобретением новых методик диагностики и лечения. Помимо традиционного медикаментозного лечения и стандартных рекомендаций по контролю прогрессирования болезни, сейчас широко внедрили в повседневную медицинскую практику эндоваскулярные хирургические методы.
Эндоваскулярное лечение аневризм
Смысл их состоит в неинвазивной доставке лекарственного средства или специального приспособления с целью эмболизации сосуда, восстановления его просвета, удаления тромботических масс, а также в онкологии для прицельного воздействия на опухоль с помощью химио- и лучевой терапии.
Среди видов эндоваскулярных хирургических вмешательств на сосудах различают следующие методики.
- Установка специальных инструментов и устройств. Длинный катетер проводят к месту сосудистой проблемы через большую бедренную вену. На его свободном конце крепится баллон, стент или микроспираль.
- Баллоны устанавливают с целью открытия просвета сосудов во время ангиопластики.
- Стенты – сетчатые трубочки, которые помещают внутрь сосуда для стабилизации его стенки, особенно когда на ней есть атеросклеротические бляшки, и восстановления его проходимости.
- Спирали – специальные устройства, которые блокируют течение крови по сосудам. Наиболее часто используются для лечения аневризм сосудов мозга.
- Катетеры – ловушки для устранения тромбов и извлечения остатков тканей при нейрохирургических операциях.
Метод установки длинного катетера
- Доставка лекарственных средств с целью растворения тромботических масс, проведения прицельной химиотерапии злокачественных опухолей, а также препаратов, оказывающих спазмолитическое действие на мышечный слой артерий, что улучшает кровоток в них.
- Введение эмболизирующих веществ, останавливающих течение крови на протяжении определенного участка сосуда. Чаще всего применяют склерозанты на основе спирта, клеевидные материалы, к примеру, N-бутилцианакрилат, а также специальные гели, пены, выпускающиеся в виде микросфер.
Неинвазивные методики широко применяются в онкологии, например для прекращения или уменьшения кровоснабжения большой опухоли, если одномоментно ее удалить нельзя. Или наоборот, восстановления кровотока при инсульте или угрозе его возникновения. А также для ангиопластики при сосудистых мальформациях мозга, таких как операция по поводу аневризмы головного мозга. Изменения сосудов бывают следующие:
- Аневризмы – выпячивания стенок сосудов в самых слабых её местах.
Формы изменения сосудов
- Патологическое изменение формы сосуда – извитость и расширение, вследствие чего изменяется скорость кровотока, что приводит к повышенному тромобообразованию.
Изменение формы сосудов
- Сообщение между сосудами, например между венами и артериями через свищи, в результате чего происходит смешение высокооксигениованной артериальной крови с венозной, богатой углекислым газом.
Аневризма сосуда – это выпячивание стенки в месте её самого сильного ослабления и истончения. При повышении артериального давления, есть риск расслоения, разрыва и возникновения кровотечения в ткань мозга, в желудочки или под его оболочки.
Выделяют несколько причин образования аневризм. Во-первых, врожденное нарушение формирования мышечных волокон сосудистой стенки, а также структуры соединительной ткани. Из приобретенных состояний – атеросклероз, при котором возникает воспаление и над местом сужения в зоне бляшке формируется участок расширения сосуда.
Разновидности аневризм
Аневризмы бывают разных форм:
- боковая – как опухоль стенки сосуда;
- мешотчатая – выпячивание, в котором анатомически выделяют шейку, тело и купол аневризмы;
- веретенообразная – выпячивание на протяжении сосуда, делающее его широкими извитым.
- малые (до 3 мм);
- средние (от 4 до 15 мм);
- большие (от 16 до 25 мм);
- гигантские (более 25 мм).
Такой серьезной операции предшествует целый комплекс подготовительных мероприятий. К ним относится:
- беседа с лечащим врачом, в ходе которой он выясняет всю нужную информацию для точного установления окончательного диагноза,
- время появления и точную локализацию аневризмы.
Нужно сказать о перенесенных ранее оперативных вмешательствах, об их результатах и течении общего наркоза. О наличии различных устройств, имплантированных в тело: дефибрилляторы, водители ритма, нейростимуляторы, протезы внутреннего уха, глаза, центральных сосудистых катетеров.
В это же время доктор определяет препараты, применение которых необходимо отменить за двое-трое суток до проведения процедуры. К ним относятся препараты аспирина, обладающие кроворазжижающим эффектом, а также некоторые лекарства, которые применяются при гипертонической болезни и сердечной недостаточности. Так же нужно поставить в известность врача об имеющейся лекарственной аллергии на препараты, использующиеся для контрастирования, особенно йодсодержащие, антибиотики и нестероидные противовоспалительные средства.
Для качественной полноценной оценки состояния здоровья пациента назначают ряд анализов:
- клинический анализ крови,
- биохимический,
- анализ крови для определения уровня сахара,
- инфекционных заболеваний: вирусного гепатита В, сифилиса,
- а также общий анализ мочи,
- и анализ кала на обнаружение яиц глистов.
Инструментальное обследование перед операцией включает в себя:
- электрокардиограмму,
- эхокардиоскопию,
- флюорографию органов грудной клетки,
- УЗИ брюшной полости и забрюшинного пространства.
Женщинам детородного возраста нужно назначить тест на беременность, особенно если планируется рентгенологическое исследование, ведь оно обладает тератогенным и эмбриотоксическим действием.
После этого врач дает исчерпывающие инструкции по подготовке к операции, а также информацию о её ходе, этапах и послеоперационном периоде.
При наличии сужения участка сосуда, которое угрожает развитием инсульта, показано восстановление его проходимости с помощью медицинских инструментов. Для проведения этой процедуры пациента погружают в общую анестезию и внутривенно вводят контрастное вещество.
В это время он находится на операционном столе, место пункции бедренной вены специальным образом обрабатывается антисептическими средствами и накрывается стерильными простынями. В периферическую вену, чаще всего в области локтевого сгиба, ставят катетер для инфузий, чтобы была возможность введения растворов и средств для наркоза.
Жизненные показатели контролируют с помощью специальной аппаратуры, которую подключают и фиксируют частоту сердцебиения, артериальное давление, электрокардиограмму, степень насыщения крови кислородом.
В операционной должна быть рентгенографическая установка, с помощью которой осуществляют контроль за продвижением катетера по сосудам до установленного участка сосуда. Затем, через свободный конец катера в сосуд помещают специальное окклюзирующее устройство, либо оно должно быть закреплено заранее. Следят за тем, что оно установлено надежно, одним из критериев является полноценное восстановление кровотока.
Спираль в качестве метода лечения аневризм
Лечение аневризм мозга проводят при помощи спирали, действие которой противоположно. На ней оседают нити фибрина, клетки крови и, таким образом, постепенно формируется тромб, блокирующий течение крови и дальнейшее увеличение аневризмы.
Похожим действием обладает эндоваскулярная эмболизация аневризмы головного мозга, препараты для которой доставляют таким же образом, через катетер. После того, как удалось достигнуть места выпячивания или сосудистой мальформации вводят склезрозирующее вещество, например, на основе спирта.
Эндоваскулярная эмболизация
Происходит ожог внутренней поверхности сосуда и стенки склеиваются между собой. Прекращается кровоток по патологически изменённому сосуду, прогрессирование роста дефекта стенки приостанавливается, предотвращается вероятность разрыва и возникновения массивного внутримозгового кровотечения.
Другим, не менее эффективным, методом лечения аневризм сосудов является стереотаксическая радиохирургия. Процедура воздействия рентгенологическим излучением на патологически измененные сосуды абсолютно не требует каких-либо разрезов или проколов. Пучок гамма-излучения через ткани попадает точно к месту расположения аневризмы. Это возможно благодаря специальным расчетам, которые проводят врачи лучевой терапии, излучение фактически не рассеивается, минимизируя воздействие на окружающие здоровые ткани.
Использование стереотаксического оборудования
Голова пациента помещается в специальную фиксирующую рамку. Она крепится особыми винтами. Перед установкой, кожа головы обезбаливается на лбу и на затылке. Такая установка гарантирует надежное обездвиживание головы пациента и предупреждает от случайных непроизвольных подергиваний. Это также повышает точность направления гамма-лучей. В результате также возникает утолщение стенки сосуда, а полной окклюзии получается достигнуть через несколько лет, иногда требуется повторное проведение рентгенэндоваскулярной процедуры.
После того, как манипуляция окончена, делают серию снимков через определенное время для того, чтобы убедиться в надежности закупорки сосуда. Катетер аккуратно извлекают, а место пункции обрабатывают и заклеивают пластырем, либо накладывают давящую повязку. Длительность операции в зависимости от сложности составляет около 30-40 минут. После нее пациенту показан постельный режим на протяжении восьми часов.
Если существует необходимость в удалении аневризмы сосудов головного мозга, то лучше сделать выбор в пользу эндоваскулярных методик. Их самым важным и неоспоримым преимуществом является малоинвазивность. Для введения катетера не требуется больших доступов, достаточно небольшого разреза или даже прокола. По окончании операции не нужно накладывать швы, хватит небольшой повязки. Малотравматичность эндоваскулярных операций значительно сокращает время госпитализации пациентов. Выписку можно планировать уже на следующие сутки после вмешательства. Снижается риск возникновения таких неприятных последствий, как рубцы и серьезных осложнений в виде рецидива кровотечения, присоединения вторичной бактериальной инфекции.
Для экстренных операций, например при массивных кровотечениях, эмболизация аневризмы сосудов головного мозга более эффективна и требует меньших временных затрат.
Внедрение таких методов лечения позволило помогать людям, чье заболевание раньше считалось неизлечимым.
В некоторых случаях, такую операцию можно провести под местной анестезией с использованием седативных средств. Это особенно актуально для пациентов, чьи сопутствующие заболевания являются противопоказанием для общего наркоза.
- Возможность повторного кровотечения вследствие прокола сосудистой стенки, некачественной установки спиралей, обусловленных особенностями строения и размера аневризм. Есть большие выпячивания с широкими шейками, в которую установить спираль довольно затруднительно без дополнительного микроклипирования или эмболизации при помощи склерозантов.
- Риск инфицирования места пункции, развития флебита.
- Миграция стентов и спиралей, а также эмболизирующих материалов из места их введения. Но, развитие инсульта головного мозга вследствии этого маловероятно, устройства оснащены специальными сеточками, которые не препятствуют кровотоку. Очень редко, когда необходимо повторное оперативное вмешательство.
- Развитие аллергической реакции на контрастное вещество, которое опасно для жизни.
- Повторное образование тромбов и инсульта. Затруднение речи, нарушения зрения и памяти, проблемы с координацией и движениями, судорожные приступы.
- Осложнение, в виде отека головного мозга.
Реабилитация после операции аневризмы головного мозга не занимает длительного времени, больные фактически сразу полноценно возвращаются к повседневной жизни и работе. До конца восстановление занимает порядка двух месяцев. Пациенты могут предъявлять жалобы на такие симптомы:
- неинтенсивные головные боли,
- дискомфортные ощущения и отечность в месте пункции,
- а также на общую слабость.
В целом, последствия после удаления аневризмы головного мозга встречаются редко.
Таким людям лечащий врач дает рекомендации, касающиеся образа жизни, режима работы и отдыха, а также список лекарств, которые необходимо принимать в послеоперационном периоде. Нужно помнить о необходимости контроля результатов лечения через полгода и год после операции с помощью компьютерной томографии.
При выявлении бессимптомного течения болезни, есть смысл провести профилактическое эндоваскулярное лечение аневризм головного мозга для предотвращения тяжелых последствий.
источник
 В кардиологической практике для лечения острой и хронической ишемии миокарда на фоне атеросклероза артерий сердца;
В кардиологической практике для лечения острой и хронической ишемии миокарда на фоне атеросклероза артерий сердца;