Сущность данной анемии в нехватке железа в организме, вследствие чего нарушается синтез гемоглобина. Недостаток гемоглобина служит причиной гипоксии тканей; также дефицит железа способствует нарушения синтеза тканевых ферментов, что приводит к изменению тканевого метаболизма, поэтому быстро поражаются обновляющиеся эпителиальные ткани — слизистая ЖКТ, кожа.
- Недостаточний уровень железа в организме (нарушения маточно- плацентарного кровообращения, фетоматеринские и фетоплацентарные кровотечения, синдром фетальной трансфузии при многоплодной беременности, внутриутробная мелена, недоношенесть, многоплодие, глубокий и долговременный дефицит железа в организме беременной, преждевременная или поздняя перевязка пуповини, интранатальное кровотечение вследствие травматических акушерских вмешательств или аномалии развития плаценты и сосудов пуповины)
- Повышенная потребность в железе (недоношенные, дети с большой массой тела при рождении, с лимфатическим типом конституции, дети второго полугодия жизни).
- Недостаточное количество железа в еде (раннее искусственное вскармливание коровьим или козьим молоком, мучной, молочной или молочно-вегетарианской едой, несбалансированная диета, в которой нет достаточного содержания молочных продуктов)
- Повышенные потери железа вследствие кровотечений различной этиологии, нарушения кишечного всасывания (хронические заболевания кишечника, синдром мальабсорбции), а так же значительные и длительные геморрагические маточные кровотечения у девочек.
- Нарушения обмена железа в организме (пре и пубертатный гормональный дисбаланс)
- Нарушения транспорта и утилизации железа (гипо и атрансферинемия, энзимопатии, аутоиммунные процессы)
- Недостаточная резорбция железа в пищеварительном тракте (пострезекционные и агастральные состояния).
Клинические проявления ЖДА представляют совокупность двух синдромов: сидеропенического и анемического.
изменения кожи: сухость, появление маленьких пигментных пятен цвета «кофе с молоком»;
изменения слизистых оболочек: «заеды» в углу рта, глоссит, атрофический гастрит и эзофагит;
диспептические явления со стороны ЖКТ;
изменения волос – раздваивание кончика, ломкость и выпадение вплоть до гнездной алопеции; 3
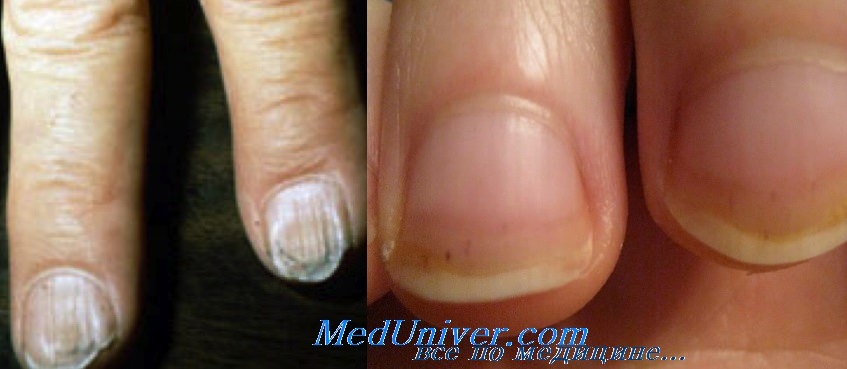
изменения ногтей – поперечная исчерченность ногтей больших пальцев рук (в тяжелых случаях и ног), ломкость, расслаивание на пластинки;
изменение обоняния – пристрастие больного к резким запахам лака, краски ацетона, выхлопных газов автомобиля, концентрированных духов;
изменения вкуса – пристрастие больного к глине, мелу, сырому мясу, тесту, пельменям и др.;
Считается, что наличие 4-х симптомов и более из перечисленных выше патогномонично для латентного дефицита железа (ЛДЖ) и ЖДА.
Для анемического синдрома характерны следующие симптомы:
мелькание мушек перед глазами;
плохая переносимость физических нагрузок;
слабость, вялость, головокружение, раздражительность;
снижение когнитивных функций;
бледность кожи и видимых слизистых оболочек;
изменение тонуса мышц в виде тенденции к гипотонии, гипотония мышц мочевого пузыря с развитием недержания мочи;
приглушенность сердечных тонов;
систолический шум на верхушке сердца.
Имеется 3 возможности лабораторной диагностики ЖДА:
ОАК, выполненный «ручным» методом — снижение концентрации Hb и эритроцитов, снижение ЦП (менее 0,85), увеличение СОЭ (более 10-12 мм/час), нормальное содержание ретикулоцитов (10-20‰).
Дополнительно врач-лаборант описывает анизоцитоз и пойкилоцитоз эритроцитов. ЖДА это микроцитарная, гипохромная, норморегенераторная анемия.
ОАК, выполненный на автоматическом анализаторе клеток крови — снижаются средний объем эритроцита – MCV (менее 80 фл), среднее содержание Hb в эритроците – MCН (менее 26 пг), средняя концентрация Hb в эритроците – МСНС (менее 320 г/л), повышается степень анизоцитоза эритроцитов – RDW (более 14%).
Биохимический анализ крови — снижение концентрации сывороточного железа (менее 12,5 мкмоль/л), повышение общей железосвязывающей способности сыворотки (более 69 мкмоль/л), снижение коэффициента насыщения 4 трансферрина железом (менее 17%), снижение сывороточного ферритина (менее 30 нг/мл). В последние годы появилась возможность определения растворимых трансферриновых рецепторов (рТФР), количество которых в условиях дефицита железа увеличивается (более 2,9 мкг/мл).
- Устранение этиологических факторов
- рациональное лечебное питание (для новорожденных – грудное естественное вскармливание, а при отсутствии молока у матери – адаптированные молочные смеси, обогащенные железом. Своевременное введение прикорма, мяса, особенно телятины, субпродуктов, гречневой и овсяной круп, фруктовых и овощных пюре, твёрдых сортов сыра; уменьшение приёма фитатов, фосфатов, танина, кальция, которые ухудшают всасывание железа.
- патогенетическое лечение препаратами железа преимущественно в виде капель, сиропов, таблеток.
Парентеральное введение препаратов железа показано только: при синдроме нарушенного кишечного всасывания и состояниях после обширной резекции тонкого кишечника, неспецифическом язвенном колите, тяжелом хроническом энтероколите и дисбактериозе, непереносимости пероральных препаратов желеаз, тяжелой степени анемии.
Профилактические мероприятия по предупреждению рецидива анемии
Коррекция дефицита железа при анемии легкой степени осуществляется преимущественно за счет рационального питания, достаточного пребывания ребенка на свежем воздухе. Назначение препаратов железа при уровне гемоглобина 100 г/л и выше – не показано.
Суточные терапевтические дозы пероральных препаратов железа при ЖДА средней и тяжелой степени:
до 3 лет – 3 -5 мг/кг/в сутки элементарного железа
от 3 до 7 лет – 50-70 мг/ в сутки элементарного железа
старше 7 лет – до 100 мг/ в сутки элементарного железа
- мальтофер
- ферроплекс
- актиферрин
- гемофер
- фумарат железа
- тотема
- ферронат
Контроль эффективности назначенной дозы осуществляется путем определения подъема уровня ретикулоцитов на 10-14 день лечения. Терапия железом осуществляется до нормализации уровня гемоглобина с дальнейшым уменьшением дозы на ? . Длительность лечения — 6 месяцев, а для детей недоношенных– в течение 2 лет для пополнения запасов железа в организме.
У детей старшего возраста поддерживающая доза курсом 3 – 6 месяцев, у девочек пубертатного возраста – в течение года прерывисто – каждую неделю после месячных.
Целесообразно назначать препараты трехвалентного железа благодаря их оптимальному всасыванию и отсутствию побочных эффектов.
Профилактика
Антенатальная: женщинам со 2-ой половины беременности назначают препараты железа или поливитамины, обогащенные железом.
При повторной или многоплодной беременности обязателен приём препаратов железа на протяжении 2-го и 3-го триместра.
Постнатальная профилактика для детей из группы высокого риска развития ЖДА.
Эту группу формируют:
- все недоношенные дети
- дети, рожденные от многоплодной беременности и при отягощенном протекании второй половины беременности (гестозы, фетоплацентарная недостаточность, осложнения хронических заболеваний)
- дети с дисбактериозами кишечника, пищевой аллергией
- дети, которые находятся на искусственном вскармливании
- дети, которые растут с опережением общепринятых стандартов физического развития.
Предусматривается регулярное проведение диагностики возможного развития ЖДА и, при её определении, назначаются профилактические дозы препаратов железа (0,5-1 мг/кг/сут) в течение 3-6 месяцев.
5. Диспансерное наблюдение
После нормализации показателей крови общий анализ крови проводится 1 раз в месяц во время первого года, затем – поквартально на протяжении следующих 3 лет.
источник
Железодефицитная анемия: определение, этиология, патогенез, классификация, клиника, диагностика, лечение, профилактика.
Это — группа анемических синдромов, основным патогенетическим фактором которых является недостаток железа в организме.
Этиология:Низкое содержание в пище. Нарушение всасывания при резекция желудка, синдром мальабсорбции. Хроническая кровопотеря при кровотечениях(язвенная болезнь, геморрой)Повышенный расход железа: при беременности и лактации, в период роста и полового созревания, при хронических инфекциях.
Патогенез:Три звена: 1)нарушение синтеза гемоглобина в результате уменьшения запасов железа2)генерализованные нарушения пролиферации клеток. 3)укорочение продолжительности жизни эритроцитов (при тяжёлом дефиците железа).
Классификация:Стадии:1 стадия — дефицит железа без клиники анемии (латентная анемия). 2 стадия —железодефицитная анемия с развернутой клинико-лабораторной картиной. Степень тяжести:Легкая (содержание Нb 90-120 г/л). Средняя (содержание Нb 70-90 г/л).Тяжелая (содержание Нb ниже 70 г/л)
Клиника: синдромы: Анемический (общая слабость, повышенная утомляемость, снижение работоспособности, головокружение, шум в ушах, мелькание мушек перед глазами, сердцебиения, одышку при физической нагрузке, появление обморочных состояний).Сидеропенический(извращение вкуса,извращение обоняния,мышечная слабость и утомляемость,ангулярный стоматит,симптом «синих склер»,снижение репаративных процессов)
Диагностика: Обследование ЖКТ, органов малого таза, полости рта. Лабораторно:В крови:Снижение уровня гемоглобина:гемоглобин-120,0 до 90 г/л (легкая анемия); 90-70 г/л (средней тяжести); менее 70 г/л (тяжелая).Эритроцитов менее 3,8 млн.Цветовой показатель менее 0,8 (гипохромная анемия). Пойкилоцитоз, анизоцитоз, микроцитоз.Снижение насыщения эритроцита гемоглобином — цитоморфологический критерий.Снижение железа сыворотки крови до уровня менее 12,5 мкмоль/л.Повышение общей железосвязывающей способности сыворотки (норма 45-62,5 ммоль/л), уменьшение насыщения трансферрина железом (норма 25-45%).В костном мозгу эритроидная гиперплазия.
Лечение: препараты железа (перорально или парентерально)-Тотема, актиферрин. Существует значительное количество препаратов солей железа (лак-тат, сульфат, карбонат, глюконат), позволяющих быстро ликвидировать его дефицит. Препараты железа следует назначать парентерально только в случае нарушения его всасывания в кишечнике, а также при обострениях язвенной болезни. Диета, содержащая мясные продукты.
Профилактика: правильное питание- мясо, печень, сыры, пшеничные отруби, крупы и др.Вторичная профилактика показана при завершении лечения желе-одефицитной анемии. При продолжающихся кровопотерях (меноррагии и др.) профилактический прием препаратов железа проводят в течение 6 мес и более после нормализации показателей крови.
62.В12-дефицитная анемия: определение, этиология, патогенез, клиника, диагностика, лечение.
Это-группа заболеваний, связанных с дефицитом цианокобаламина или нарушением его метаболизма. Витамин B12-дефицитную анемию в основном наблюдают в пожилом возрасте, несколько чаще у женщин.
Этиология: Наследственность. Алкоголизм. Операции на желудке (гастротомия, субтотальная резекция желудка, эзофагоеюноанастомоз). Заболевания кишечника (хронический энтерит, спру, дивертику-лез, кишечные свищи, опухоли). Атрофический гастрит, опухолевые поражения желудка (рак, по-липоз). Дивертикулез тонкой кишки. Глистная инвазия широким лентецом. Повышение потребности из-за беременности, гипертиреозе.
Патогенез: Дефицит нарушает синтез тимидина, нарушется синтез ДНК и клеточная пролиферация. В костном мозгу нарушается процесс созревания предшественников всех трех ростков кроветворения. Мегалобластный тип кроветворения. Эритропоэз ускорен, увеличивается количество незрелых клеток.гемическая гипоксия, нарушение внутриклеточного метаболизма. При недостатке-нарушение жирового обмена с накоплением токсичной для спинного мозга метилмалоновой кислоты, приводящая к дегенеративным процессам (фуникулярного миелоза)
Клиника:слабость, утомляемость, головокружение, шум в ушах, головные боли, мелькание «мушек» перед глазами. Одышка при ходьбе, сердцебиение при физической нагрузке, сонливость в течение дня и ночная бессонница.Отсутствие аппетита, поносы. Симптомы фуникулярного миелоза — чувство ползания мурашек, онемение дистальных отделов конечностей, ощущение холода, «ватных ног», мышечная слабость, нарушение поверхностной чувствительности, потеря вкусовых ощущений.
Бледность, субиктеричность, лицо одутловатое. Температурасубфебрильная. Язык- ярко-красные участки воспаления, лакированный язык,кариозное разрушение зубов. При поколачивании и пальпации плоских костей — болезненность. Гепато и спленомегалия. При аускультации систолический шум различной интенсивности. Снижение сухожильных рефлексов.
Диагностика:
ОАК: макроцитоз — основной признак мегалобластных анемий; в мазке крови находят тельца Жолли, кольца Кэбота, снижение содержания гемоглобина; нарастание ретикулоцитоза на 3-5 день лечения и достигающее максимума на 10-й день при лечении витамином B12. Исследование костного мозга: мегалобласты. Клетки миелоидного ряда увеличены; выявляют гигантские мегамиелоциты, эритроидную гиперплазию. Тест — реакция на введение витамина B12 с повторной стернальной пункцией через 8-12 ч: переход от мегалобластического к эритробластическому кроветворению.
Лечение: лечение основного заболевания и возмещение дефицита витамина B12 и фолиевой кислоты.
Папиллярные узоры пальцев рук — маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.
источник
В организме равновесие железа сохраняется отношением поглощения железа и его потери. Независимо от причины, нарушающей это равновесие, явление отражается на все разделы метаболизма железа — от запасов до его расхода.
На первой стадии недостаток железа скрытый, без анемии. Ее характеризует сокращение или отсутствие запасов железа, рост количества поглощаемого железа, а иногда и уровня свободного порфирина эритроцитов.
Когда фактор, нарушивший метаболическое равновесие железа продолжает действовать и после истощения запасов, недостаток железа превращается в железодефицитную анемию, в которой различаются умеренная и тяжелая фазы. На стадии умеренной железодефицитной анемии к аномалиям первого этапа присоединяется дефицит эритропоэза в результате сокращения количества железа в плазме.
На этой стадии анемия нормоцитная и нормохромная. Когда железодефицитная анемия становится тяжелой к ней присоединяются микроцитоз, гипохромия и эпителиальные изменения.
На стадии недостаточности железа без анемии, клиническая симптоматология отсутствует. Сложность клинических данных железодефицитной анемии создает сочетание признаков первичной болезни, анемии и недостатка железа в тканях. В нижеследующем описании опущены признаки нервичной болезни.
Болезнь чаще поражает женщин, чем мужчин, с подросткового возраста. У взрослых молодого возраста показатель частоты дефицита железа растет у лиц обоего пола, однако в значительно большей пропорции у женщин. После 50 лет риск недостатка железа уменьшается у женщин, но продолжает увеличиваться у мужчин, при этом на первом месте заболеваемости продолжают находиться женщины.
Начало железодефицитной анемии скрытое, преобладают симптомы анемии в том числе утомленность, головные боли, раздражительность, сердцебиения, головокружения. Поскольку недостаток железа развивается на протяжении длительного интервала, признаки заболевания проявляются относительно поздно. Наиболее часто встречающийся и озабочивающий больного признак это утомляемость. Еще не уточнено является ли это лишь результатом анемии или явление может быть отнесено также за счет недостатка железа в тканях.
Среди объективных признаков железодефицитной анемии, бледность это единственный симптом, относящийся за счет анемии. Для железодефицитной анемии характерна синеватая бледность бульбарных конъюнктивалных оболочек. В отдельных случаях бледность покровов сочетается с отеками на лице и голени.
Недостаток железа в тканях проявляется, в частности, в эпителиях. Однако онтенсивность явления не всегда пропорциональна тяжести анемии. Так, отмечены случаи недостатка железа в тканях без анемии или с наличием умеренной анемией. Еще не выявлены метаболические аномалии, составляющие основу тканевых нарушений в условиях недостатка железа.
При этом на первом месте поражаемости находится пищеварительный тракт. Ангулярный стоматит проявляется образованием изъязвлений или трещин е углах рта. Воспаление языка, развивающееся в результате сглаживания сосочков придает гладкий, блестящий аспект и красный оттенок передней половине этого органа. Вид языка похож на наблюдаемый при злокачественной анемии. Больные жалуются на внезапно появляющиеся боль и изжогу после приема пищи, в частности прибавок к ней.
Расстройство глотания развивающееся при недостатке желез а (синдром Plummer-Vinson) локализуется в зоне перстневидного хряша, причем является результатом перерождения эпителиальной ткани у слияния гортанной части глотки и пищевода, что ведет к сужению.
Атрофический гастрит в сочетании с ахлоргидрией также имеет общую характеристику с гастритом, вызываемым недостатком витамина В12.
В материалах одного из исследований, проведенного на значительном числе случаев заболевания недостатком железа, описана озена как результат атрофии слизистой оболочки носа.
Наблюдаемые изменения ногтей характерны, однако их проявление относится к далекозашедшей стадии недостаточности железа. В частности это касается роста ногтей с наличием трещин и поперечной и продольной полосатости. При очень тяжелой форме недостатка железа ногти уплощаются, а в конечном итоге изгибаются в обратном направлении, т.е. вогнутой стороной кверху, в виде ложки (ложкообразные ногти).
Кожа сухая, в отдельных случаях имеет трещины. Волосы усиленно выпадают и медленно растут.
Спленомегалия наблюдается в 5—10% случаев, при этом слабо выражена. Объемный рост селезенки при недостатке железа еще не получил патогенетического объяснения.
У некоторых лиц, страдающих недостатком железа проявляется наклонность кушать землю, известь, крахмал, муку, кирпич, лед (Crosby). На такое ненормальное поведение («pica») сделана ссылка и в качестве причины развития недостатка железа, в частности в тех географических зонах, в которых у детей вырабатывается привычка поедать подобные материалы.
Осложнения недостатка железа возникают на далеко зашедших стадиях болезни, при этом они связаны с анемией (недостатком кислорода) и тканевыми сдвигами (отсутствием тканевых ферментов). На вырождающихся слизистых оболочках пищеварительного тракта и половой системы могут развиться осложнения инфекционного характера (воспаление слизистой оболочки рта, пищевода, прямой кишки, влагалища).
Обильные менструальные кровотечения, составляющие исходную причину недостатка железа могут продолжаться и усугубляться изменениями трофики слизистой оболочки половых органов. В отдельных случаях железотерапия сокращает срок и уменьшает интенсивность менструального потока.
У лиц, страдающих железодефицитной анемией, наблюдается высокий показатель частоты желудочных новообразований. К тому же анемия этого вида может составить пусковую или усугубляющую причину сердечной недостаточности. Известна чувствительность страдающих железодефицитной анемией к инфекциям (Hines).
источник
Железодефицитная анемия – синдром, обусловленный недостаточностью железа и приводящий к нарушению гемоглобинопоэза и тканевой гипоксии. Клинические проявления представлены общей слабостью, сонливостью, пониженной умственной работоспособностью и физической выносливостью, шумом в ушах, головокружениями, обморочными состояниями, одышкой при нагрузке, сердцебиением, бледностью. Гипохромная анемия подтверждается лабораторными данными: исследованием клинического анализа крови, показателей сывороточного железа, ОЖСС и ферритина. Терапия включает лечебную диету, прием препаратов железа, в некоторых случаях – трансфузию эритроцитарной массы.
Железодефицитная (микроцитарная, гипохромная) анемия – анемия, обусловленная нехваткой железа, необходимого для нормального синтеза гемоглобина. Её распространенность в популяции зависит от половозрастных и климатогеографических факторов. По обобщенным сведениям, гипохромной анемией страдает около 50% детей раннего возраста, 15% женщин репродуктивного возраста и около 2% мужчин. Скрытый тканевой железодефицит выявляется практически у каждого третьего жителя планеты. На долю микроцитарной анемии в гематологии приходится 80–90% всех анемий. Поскольку железодефицит может развиваться при самых различных патологических состояниях, данная проблема актуальна для многих клинических дисциплин: педиатрии, гинекологии, гастроэнтерологии и др.
Ежесуточно с потом, калом, мочой, слущенными клетками кожи теряется около 1 мг железа и примерно столько же (2-2,5 мг) поступает в организм с пищей. Дисбаланс между потребностями организма в железе и его поступлением извне или потерями способствует развитию железодефицитной анемии. Железодефицит может возникать как при физиологических условиях, так и в результате ряда патологических состояний и быть обусловлен как эндогенными механизмами, так и внешними воздействиями:
Чаще всего анемия вызывается хронической потерей крови: обильными менструациями, дисфункциональными маточными кровотечениями; желудочно-кишечными кровотечениями из эрозий слизистой желудка и кишечника, гастродуоденальных язв, геморроидальных узлов, анальных трещин и др. Скрытая, но регулярная кровопотеря отмечается при гельминтозах, гемосидерозе легких, экссудативном диатезе у детей и др.
Особую группу составляют лица с болезнями крови — геморрагическими диатезами (гемофилией, болезнью Виллебранда), гемоглобинурией. Возможно развитие постгеморрагической анемии, вызванной одномоментным, но массивным кровотечением при травмах и операциях. Гипохромная анемия может возникать вследствие ятрогенных причин — у доноров, часто сдающих кровь; пациентов с ХПН, находящихся на гемодиализе.
К факторам алиментарного порядка относятся анорексия, вегетарианство и следование диетам с ограничением мясных продуктов, плохое питание; у детей — искусственное вскармливание, позднее введение прикорма. Снижение абсорбции железа характерно для кишечных инфекций, гипоацидного гастрита, хронического энтерита, синдрома мальабсорбции, состояния после резекции желудка или тонкой кишки, гастрэктомии. Значительно реже железодефицитная анемия развивается вследствие нарушения транспортировки железа из депо при недостаточной белково-синтетической функции печени – гипотрансферринемиях и гипопротеинемиях (гепатитах, циррозе печени).
Ежедневная потребность в микроэлементе зависит от пола и возраста. Наиболее высока необходимость в железе у недоношенных, детей раннего возраста и подростков (в связи с высокими темпами развития и роста), женщин репродуктивного периода (в связи с ежемесячными менструальными потерями), беременных (в связи с формированием и ростом плода), кормящих мам (в связи с расходом в составе молока). Именно эти категории являются наиболее уязвимыми в отношении развития железодефицитной анемии. Кроме того, повышение потребности и расхода железа в организме наблюдается при инфекционных и опухолевых заболеваниях.
По своей роли в обеспечении нормального функционирования всех биологических систем железо является важнейшим элементом. От уровня железа зависит поступление кислорода к клеткам, протекание окислительно-восстановительных процессов, антиоксидантная защита, функционирование иммунной и нервной систем и пр. В среднем содержание железа в организме находится на уровне 3-4 г. Более 60% железа (>2 г) входит в состав гемоглобина, 9% — в состав миоглобина, 1% — в состав ферментов (гемовых и негемовых). Остальное железо в виде ферритина и гемосидерина находится в тканевом депо – главным образом, в печени, мышцах, костном мозге, селезенке, почках, легких, сердце. Примерно 30 мг железа непрерывно циркулирует в плазме, будучи частично связанным основным железосвязывающим белком плазмы – трансферрином.
При развитии отрицательного баланса железа мобилизуются и расходуются запасы микроэлемента, содержащиеся в тканевых депо. На первых порах этого бывает достаточно для поддержания адекватного уровня Hb, Ht, сывороточного железа. По мере истощения тканевых резервов компенсаторно увеличивается эритроидная активность костного мозга. При полном истощении эндогенного тканевого железа его концентрация начинает снижаться в крови, нарушается морфология эритроцитов, уменьшается синтез гема в гемоглобине и железосодержащих ферментов. Страдает кислородтранспортная функция крови, что сопровождается тканевой гипоксией и дистрофическими процессами во внутренних органах (атрофический гастрит, миокардиодистрофия и др.).
Железодефицитная анемия возникает не сразу. Вначале развивается предлатентный железодефицит, характеризующийся истощением только запасов депонированного железа при сохранности транспортного и гемоглобинового пула. На этапе латентного дефицита отмечается уменьшение транспортного железа, содержащегося в плазме крови. Собственно гипохромная анемия развивается при уменьшении всех уровней метаболических запасов железа – депонированного, транспортного и эритроцитарного. В соответствии с этиологией различают анемии: постгеморрагические, алиментарные, связанные с повышенным расходом, исходным дефицитом, недостаточностью резорбции и нарушением транспорта железа. По степени выраженности железодефицитные анемии подразделяются на:
- Легкие (Нb 120-90 г/л). Протекают без клинических проявлений или с их минимальной выраженностью.
- Среднетяжелые (Нb 90-70 г/л). Сопровождаются циркуляторно-гипоксическим, сидеропеническим, гематологическим синдромами умеренной степени выраженности.
- Тяжелые (Нb
Циркуляторно-гипоксический синдром обусловлен нарушением синтеза гемоглобина, транспорта кислорода и развитием гипоксии в тканях. Это находит свое выражение в ощущении постоянной слабости, повышенной утомляемости, сонливости. Пациентов преследует шум в ушах, мелькание «мушек» перед глазами, головокружения, переходящие в обмороки. Характерны жалобы на сердцебиение, одышку, возникающую при физической нагрузке, повышенную чувствительность к низким температурам. Циркуляторно-гипоксические нарушения могут усугублять течение сопутствующей ИБС, хронической сердечной недостаточности.
Развитие сидеропенического синдрома связано с недостаточностью тканевых железосодержащих ферментов (каталазы, пероксидазы, цитохромов и др.). Этим объясняется возникновение трофических изменений кожных покровов и слизистых оболочек. Чаще всего они проявляются сухостью кожи; исчерченностью, ломкостью и деформацией ногтей; повышенным выпадением волос. Со стороны слизистых оболочек типичны атрофические изменения, что сопровождается явлениями глоссита, ангулярного стоматита, дисфагии, атрофического гастрита. Может возникать пристрастие к резким запахам (бензина, ацетона), искажение вкуса (желание есть глину, мел, зубной порошок и пр.). Признаками сидеропении также служат парестезии, мышечная слабость, диспепсические и дизурические расстройства. Астеновегетативные нарушения проявляются раздражительностью, эмоциональной неустойчивостью, снижением умственной работоспособности и памяти.
Поскольку в условиях железодефицита IgA теряет свою активность, больные становятся подвержены частой заболеваемости ОРВИ, кишечными инфекциями. Пациентов преследует хроническая усталость, упадок сил, снижение памяти и концентрации внимания. Длительное течение железодефицитной анемии может привести к развитию миокардиодистрофии, распознаваемой по инверсии зубцов Т на ЭКГ. При крайне тяжелом железодефиците развивается анемическая прекома (сонливость, одышка, резкая бледность кожи с цианотичным оттенком, тахикардия, галлюцинации), а затем – кома с потерей сознания и отсутствием рефлексов. При массивной стремительной кровопотере возникает гиповолемический шок.
На наличие железодефицитной анемии может указывать внешний вид больного: бледная, с алебастровым оттенком кожа, пастозность лица, голеней и стоп, отечные «мешки» под глазами. При аускультации сердца обнаруживается тахикардия, глухость тонов, негромкий систолический шум, иногда – аритмия. С целью подтверждения анемии и определения ее причин проводится лабораторное обследование.
- Лабораторные тесты. В пользу железодефицитного характера анемии свидетельствует снижение гемоглобина, гипохромия, микро- и пойкилоцитоз в общем анализе крови. При оценке биохимических показателей отмечается снижение уровня сывороточного железа и концентрации ферритина (60 мкмоль/л), уменьшение насыщения трансферрина железом (
- Инструментальные методики. Для установления причины хронической кровопотери должно быть проведено эндоскопическое обследование ЖКТ (ЭГДС, колоноскопия,), рентгенодиагностика (ирригоскопия, рентгенография желудка). Обследование органов репродуктивной системы у женщин включает УЗИ малого таза, осмотр на кресле, по показаниям — гистероскопию с РДВ.
- Исследование пунктата костного мозга. Микроскопия мазка (миелограмма) показывает значительное снижение количества сидеробластов, характерное для гипохромной анемии. Дифференциальная диагностика направлена на исключение других видов железодефицитных состояний — сидеробластной анемии, талассемии.
К основным принципам терапии железодефицитной анемии относятся устранение этиологических факторов, коррекция рациона питания, восполнение железодефицита в организме. Этиотропное лечение назначается и проводится специалистами гастроэнтерологами, гинекологами, проктологами и др.; патогенетическое – гематологами. При железодефицитных состояниях показано полноценное питание с обязательным включением в рацион продуктов, содержащих гемовое железо (телятины, говядины, баранины, мяса кролика, печени, языка). Следует помнить, что усилению ферросорбции в ЖКТ способствуют аскорбиновая, лимонная, янтарная кислота. Ингибируют всасывание железа оксалаты и полифенолы (кофе, чай, соевый протеин, молоко, шоколад), кальций, пищевые волокна и др. вещества.
Вместе с тем, даже сбалансированная диета не в состоянии устранить уже развившийся недостаток железа, поэтому больным с гипохромной анемией показана заместительная терапия ферропрепаратами. Препараты железа назначаются курсом не менее 1,5-2-х месяцев, а после нормализации уровня Hb проводится поддерживающая терапия в течение 4-6 недель половинной дозой препарата. Для фармакологической коррекции анемии используются препараты двухвалентного и трехвалентного железа. При наличии витальных показаний прибегают к гемотрансфузионной терапии.
В большинстве случаев гипохромная анемия подается успешной коррекции. Однако при неустраненной причине железодефицит может рецидивировать и прогрессировать. Железодефицитная анемия у детей раннего и младшего возраста может вызывать задержку психомоторного и интеллектуального развития (ЗПР). В целях профилактики железодефицита необходим ежегодный контроль параметров клинического анализа крови, полноценное питание с достаточным содержанием железа, своевременная ликвидация источников кровопотери в организме. Следует учитывать, что лучше всего усваивается железо, содержащееся в мясе и печени в форме гема; негемовое железо из растительной пищи практически не усваивается – в этом случае оно сначала должно восстановиться до гемового при участии аскорбиновой кислоты. Лицам групп риска может быть показан профилактический прием железосодержащих препаратов по назначению специалиста.
источник
Железодефицитная анемия (ЖДА) – гипохромная микроцитарная анемия, развивающаяся вследствие абсолютного уменьшения запасов железа в организме.
Эпидемиология: ЖДА страдают около 200 млн. людей во всем мире; самая частая форма анемий (80%).
1. Хронические периодические кровопотери (желудочно-кишечные кровотечения, маточные кровотечения, гематурия, кровоточащие опухоли, донорство и др.)
2. Повышенный расход железа (беременность, лактация, половое созревание, хронические инфекции)
3. Недостаточное поступление железа с пищей
4. Нарушение всасывания железа (синдром мальабсорбции, резекция желудка, высокая энтеропатия и др.)
5. Нарушение транспорта железа (наследственный недостаток трансферина, АТ к трансферрину)
6. Врожденный дефицит железа (нарушение реутилизации железа и т.д.)
В основе заболевания – дефицит железа, в котором выделяют 2 стадии:
а) латентный дефицит – уменьшаются запасы железа в печени, селезенке, костном мозге, при этом снижается уровень ферритина в крови, происходит компенсаторное усиление всасывания железа в кишечника и повышение уровня мукозного и плазменного трансферина; содержание сывороточного железа еще не снижено, анемии нет
б) собственно ЖДА – истощенные депо железа не способны обеспечить эритропоэтическую функцию костного мозга и, несмотря на сохраняющийся высокий уровень трансферина в крови, значительное содержается содержание сывороточного железа, синтез гемоглобина, развивается анемия и последующие тканевые нарушения.
При дефиците железа, помимо анемии, снижается активность железосодержащих и железозависимых ферментов в различных органах и тканях, уменьшается образование миоглобина ® дистрофические поражения эпителиальных тканей (кожи, слизистых ЖКТ, мочевыводящих путей и др.) и мышц (скелетный, миокарда).
Распределение железа в организме: 57-65% – гемоглобин; 27-30% – железо негемовых белков (ферритин, гемосидерин); 8-9% – миоглобин; до 0,5% – железо ферментов (цитохромов и пероксидаз); 0,1% – транспортное железо (с трансферрином).
а) хроническая постгеморрагическая ЖДА
б) ЖДА вследствие повышенного расхода железа
в) ЖДА вследстие недостаточного исходного уровня железа (у новорожденных и детей младшего возраста)
д) ЖДА вследствие недостаточного всасывания в кишечнике
е) ЖДА вследствие нарушения транспорта железа
2) по стадии развития: латентная анемия и ЖДА с развернутой клинико-лабораторной картиной заболевания
3) по степени тяжести: легкая (Hb 90-120 г/л), средняя (Hb 70-90 г/л), тяжелая (Hb ниже 70 г/л).
а) общеанемический синдром:
— общая слабость, повышенная утомляемость, снижение работоспособности, памяти, сонливость, головокружение, шум в ушах, мелькание мушек перед глазами, сердцебиение, одышка при физических нагрузках, склонность к ортостатическим обморокам
— бледность кожи и видимых слизистых оболочек (иногда с зеленоватым оттенком – «хлороз»)
— небольшая пастозность в области голеней, стоп, лица, утренние отеки – «мешки» над и под глазами
— синдром миокардиодистрофии (одышка, тахикардия, часто аритмия, умеренное расширение границ сердца влево, глухость тонов, систолический шум на верхушке)
б) сидеропеничекий синдром (синдром гипосидероза):
— извращение вкуса — непреодолимое желание употреблять в пищу что-либо необычное и малосъедобное (мел, зубной порошок, уголь, глину, сырое тесто, фарш, крупу); чаще встречается у детей и подростков
— пристрастие к острой, соленой, кислой, пряной пище
— извращение обоняния — пристрастие к запахам, которые большинством окружающих воспринимаются как неприятные (бензин, керосин, ацетон, запах лаков, красок, гуталина, нафталина и др.)
— выраженная мышечная слабость и утомляемость, атрофия мышц и снижение мышечной силы; императивные позывы на мочеиспускание, невозможность удержать мочу при смехе, кашле, чихании, возможно даже ночное недержание мочи (слабость сфиктера мочевого пузыря)
— дистрофические изменения кожи и ее придатков (сухость, шелушение, склонность к быстрому образованию на коже трещин; тусклость, ломкость, выпадение, раннее поседение волос; истончение, ломкость, поперечная исчерченность, тусклость ногтей; симптом койлонихии — ложкообразная вогнутость ногтей)
— дистрофические изменения слизистых: ангулярный стоматит — трещины, «заеды» в углах рта; глоссит — ощущение боли и распирания в области языка, покраснение его кончика, в дальнейшем атрофия сосочков («лакированный» язык); склонность к пародонтозу и кариесу; атрофические изменения ЖКТ (сухость слизистой пищевода и затруднения, а иногда боли при глотании пищи, особенно сухой — сидеропеническая дисфагия или симптом Пламмера-Винсона; атрофический гастрит и энтерит)
— снижение репаративных процессов в коже и слизистых
— симптом «синих склер» Ослера — синеватая окраска или выраженная голубизна склер (из-за нарушения гидроксилирования пролина и лизина при дефиците железа склера истончается и через нее просвечивается сосудистая оболочка глаза)
— «сидеропенический субфебрилитет» — длительное повышение температуры до субфебрильных величин
— выраженная предрасположенность к ОРВИ, хронизации инфекций (из-за нарушения фагоцитоза)
а) ОАК: снижение содержания гемоглобина и (в меньшей степени) эритроцитов; микроцитоз; ЦП 70,0 мкмоль/л; мужчины – норма 44,8-70,0 мкмоль/л, при дефиците железа > 70,0 мкмоль/л
3) процент насыщения трансферрина железом (%НТЖ): женщины – норма 25-40%, при дефиците железа
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Увлечёшься девушкой-вырастут хвосты, займёшься учебой-вырастут рога 9420 — 

193.124.117.139 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
38. Железодефицитные состояния: латентный дефицит и железодефицитная анемия. Эпидемиология, этиология, патогенез, клиника, диагностика, лечение и профилактика.
Латентный дефицит железа хар-ся уменьшением количества железа в его депо и снижением уровня транспортного железа крови при еще нормальных показателях гемоглобина и эритроцитов.
Железодефицитная анемия (ЖДА) — гипохромная микроцитарная анемия, обусловленная дефицитом железа в сыворотке крови и костном мозге, что сопровождается нарушением образования гемоглобина и эритроцитов, развитием трофических нарушений в органах и тканях. Наиболее распространенный вид анемии (80-95 % всех форм). Каждый 4-5-ый житель планеты страдает железодефицитом.
Этиология. 1. Хронические постгеморрагические анемии (желудочно-кишечные, маточные, рецидивирующие почечные, легочные, носовые кровотечения). 2. Нарушение всасывания железа (хронические энтериты, амилоидоз кишечника и др. заб-ния, приводящие к развитию синдрома мальабсорбции, обширные резекции тонкого кишечника). 3. Повышение потребности в железе (беременность, период лактации, резкий рост организма в юношеском возрасте). 4. Перераспределение железа (острые и хронические инфекционные заболевания, злокачественные новообразования). Женщины болеют значительно чаще, чем мужчины.
Обмен железа в организме. Железо участвует во всех биологических процессах организма. Общее количество его в организме составляет 4-4,5 г: 3 г содержится в эритроцитах, 1 г — в депо, 1 г расходуется на структуру тканей (350 мг) и ферментов (15-30 мг). Перечисленное количество составляет в основном клеточное железо, железо в депо (ферритин и гемосидерин) относится к железу запасов, а железо, находящееся в соединении с сывороточным белком или в плазме, относится к внеклеточному железу.
Суточная потребность организма в железе для синтеза гемоглобина составляет в среднем 10-20 мг (10-12 мг для мужчин и 18-20 мг для женщин). Для синтеза гемопорфирина, железофлавоноидов, железосодержащих белков, обеспечения гуморального и клеточного иммунитета, энергетического потенциала и др. целей расходуется до 40 мг железа в сутки. Из пищи в желудочно-кишечный тракт всасывается в среднем 1,5-2 мг железа. В то же время, ежесуточно потери железа составляют в среднем 1-2 мг: у мужчин — 1 мг (соответствует 2 мл крови), у менструирующих женщин — до 2 мг в сутки. Потери крови при нормальных менструациях (3-4 дня) составляют 20-30 мл крови, что эквивалентно потере 10-15 мг железа. Нормальные роды сопровождаются потерей около 300 мл крови (т. е. 150 мг железа, которое быстро извлекается из депо, но очень медленно восстанавливается). Следует иметь в виду и тот факт, что девочки, дочери матерей с железодефицитом, и сами имеют дефицит железа с рождения (жизнь женщин сопряжена с риском получения дефицита железа).
Клиника складывается из анемического, сидеропенического (тканевого дефицита железа) и метаболического синдромов (см. таблицу).
Симптомы железодефицитной анемии
Лабораторные данные. 1. В крови — гипохромная, гипорегенераторная микроцитарная анемия, анизоцитоз, пойкилоцитоз, преобладание микроцитов, возможно ускорение СОЭ. 2. Снижение содержания ферритина (N 15-150 мкг/л) и снижение уровня железа сыворотки крови (в норме 13-30 мкмоль/л). Для получения достоверных результатов в течение 5 дней перед исследованием не принимать препараты, содержащие железо. 3. Железосвязывающая способность сыворотки (общая и латентная) может быть повышена. В норме ОЖСС 30-85 мкмоль/л, латентная ЖСС выше 47 мкмоль/л.
Лечение. Существует 5 правил: 1. Не следует лечить только диетой (так как в суточном рационе пищи железа недостаточно для восстановления потери и всасываемость железа из пищевых продуктов ограничена). Без препаратов железа вылечить ЖДА невозможно, даже при употреблении пищи, богатой железом! Следует ограничить прием молочных продуктов за 2 часа до приема препаратов железа. 2. Не следует лечить переливанием эритромассы. Трансфузии делают только при уровне гемоглобина ниже 50 г/л (угроза гипоксической комы) либо перед экстренной операцией.
3. Не следует начинать лечение с парентерального введения железа. Парентеральная ферротерапия показана только при тяжелой непереносимости всех препаратов железа или появлении выраженной диспепсии после приема препаратов. В/в введение препаратов железа может сопровождаться тяжелыми аллергическими реакциями, саркомами мягких тканей, флебитов, абсцессов в местах в/м введения железосодержащих препаратов. 4. Основная патогенетическая терапия состоит в пероральном приеме железосодержащих препаратов. При выборе суточной дозировки следует ориентироваться на общее содержание в нем железа и на количество двухвалентного железа, содержащегося в выбранном препарате железа (какие, см. ниже). Суточная доза элементарного (двухвалентного) железа 100-300 мг.
Препарат железа (ПЖ) должен содержать оптимальное количество двухвалентного железа; хорошо переноситься больными, обладать минимальными побочными эффектами; быть удобным для приема; содержать дополнительные компоненты, улучшающие всасывание и биодоступность железа; при этом не содержать компоненты, затрудняющие всасывание железа или конкурирующие с ним.
5. Основной (насыщающий) курс ферротерапии обычно составляет 1,5-2 мес. Контроль эффективности лечения проводят по приросту гемоглобина на 21 день лечения. После нормализации уровня гемоглобина необходимо снизить суточную дозу препарата в 2 раза и продолжить поддерживающее лечение в течение 2-4 мес. Лечение начинают с приема препаратов железа в максимально переносимой дозе до полной нормализации содержания гемоглобина. Не следует принимать одновременно пищевые продукты и медикаменты, уменьшающие всасывание железа (крепкий чай и кофе, молочные продукты, фосфорная кислота, тетрациклины, альмагель, циметидин, соли кальция, магния, алюминия).
Для лечения железодефицитной анемии используют ПЖ: монокомпонентные, содержащие одно железо (Ферроградумет, Ферронат, Хеферол), сложные — с включением в состав аскорбиновой или янтарной к-т, фруктозы или др. компонентов, усиливающих всасывание железа (Сорбифер Дурулес, Ферроплекс), и комбинированные, содержащие также витамины В12, В6, В1, фолиевую кислоту, лизин, микроэлементы (Фенюльс, Фенотек, Актиферрин, Ранферон-12).
Основные препараты железа представлены в виде сульфата, глюконата, хлорида, фумарата железа. Любой препарат лучше рекомендовать за 0,5-1 час до еды или не ранее 2 часов после еды. Суточная доза железа определяется из расчета 2-3 мг/кг для взрослых. Для детей доза несколько выше: до 3-х лет — 5-8 мг/кг, 4-7 лет — 4-6 мг/кг, 8-16 лет — 3-5 мг/кг.
При создании препаратов железа для лучшей переносимости и профилактики перегрузки организма железом стояла задача: снизить дозу железа без ущерба для эффективности. С этой целью, например, комбинируют железо с аминокислотами (D-, L-серин). В препарат Тотема, помимо железа, входит также медь и марганец (все в виде органических соединений — глюконатов).
При назначении ПЖ в достаточной дозе в ходе лечения контролируется показатель ретикулоцитов. Их число на 7-10 день лечения повышается (ретикулоцитарный криз) и возрастает к 21 дню. Уровень Hb повышается на 3-4 неделе лечения, у некоторых больных на 6-8 неделе. После основного курса ферротерапии — поддерживающий курс в течение 1,5-3 мес, доза при этом уменьшается в 2 раза.
Профилактику железодефицитной анемии проводить у след. групп: доноры, беременные и кормящие грудью, девочки-подростки с обильными менструациями, женщины с обильными и длительными менструациями, с фибромиомой матки. Первичная профилактика заключается в рациональном питании. Всем лицам, имеющим факторы риска (после операций на ЖКТ, при полименорреи, во время беременности, лактации) проводится первичная профилактика препаратами железа. По рекомендациям ВОЗ все беременные на протяжении II—III триместров и в первые 6 мес лактации должны получать ПЖ. Вторичная профилактика железодефицитной анемии заключается в проведении поддерживающей ферротерапии после нормализации Hb еще 1-3 мес, противорецидивной терапии 1 раз в 3-6 мес, в профилактическом приеме при полименоррее препаратов железа женщинами после каждых менструаций в дозе 30-60 мг элементарного железа 7-10 дней. При рецидивирующих кровотечениях, например, геморроидальных, курс лечения железом в течение 6 мес и более.
источник

Железодефицитная анемия является самой распространенной патологией системы крови и самой часто встречаемой анемией. По данным ВОЗ (всемирной организации здравоохранения), более 2 миллиардов людей на планете имеют дефицит железа в организме. Несколько чаще данным недугом страдают женщины, что связано с беременностью, кормлением грудью, а также периодической кровопотерей во время менструаций.
Интересные факты
- Первое задокументированное упоминание о железодефицитной анемии датируется 1554 годом. В те времена данным недугом страдали преимущественно девушки 14 – 17 лет, в связи с чем заболевание называлось «de morbo virgineo», что в переводе означает «болезнь девственниц».
- Первые попытки лечения заболевания препаратами железа были предприняты в 1700 году.
- Латентный (скрытый) дефицит железа может отмечаться у детей в период интенсивного роста.
- Потребность в железе у беременной женщины в два раза больше, чем у двух здоровых взрослых мужчин.
- За время беременности и родов женщина теряет более 1 грамма железа. При обычном питании данные потери восстановятся лишь через 3 – 4 года.
Размер зрелого эритроцита колеблется в пределах от 7,5 до 8,3 микрометров (мкм). Он имеет форму двояковогнутого диска, которая поддерживается благодаря наличию в клеточной мембране эритроцита особого структурного белка – спектрина. Такая форма обеспечивает максимально эффективный процесс газообмена в организме, а наличие спектрина позволяет эритроцитам видоизменяться при прохождении через мельчайшие кровеносные сосуды (капилляры) и после этого восстанавливать свою первоначальную форму.
Более 95% внутриклеточного пространства эритроцита заполнено гемоглобином – веществом, состоящим из белка глобина и небелкового компонента – гема. Молекула гемоглобина состоит из четырех глобиновых цепей, в центре каждой из которых находится гем. Каждый эритроцит содержит более 300 миллионов молекул гемоглобина.
За транспортировку кислорода в организме отвечает небелковая часть гемоглобина, а именно атом железа, входящего в состав гема. Обогащение крови кислородом (оксигенация) происходит в легочных капиллярах, при прохождении через которые каждый атом железа присоединяет к себе 4 молекулы кислорода (формируется оксигемоглобин). Оксигенированная кровь разносится по артериям ко всем тканям организма, где происходит переход кислорода к клеткам органов. Взамен из клеток выделяется углекислый газ (побочный продукт клеточного дыхания), который присоединяется к гемоглобину (формируется карбгемоглобин) и по венам транспортируется к легким, где выделяется в окружающую среду вместе с выдыхаемым воздухом.
Помимо переноса дыхательных газов, дополнительными функциями эритроцитов являются:
- Антигенная функция. Эритроциты обладают собственными антигенами, которые определяют принадлежность к одной из четырех основных групп крови (по системе АВ0).
- Транспортная функция. К наружной поверхности мембраны эритроцитов могут прикрепляться антигены микроорганизмов, различные антитела и некоторые медикаменты, которые разносятся с током крови по всему организму.
- Буферная функция. Гемоглобин принимает участие в поддержании кислотно-щелочного равновесия в организме.
- Остановка кровотечений. Эритроциты включаются в состав тромба, формирующегося при повреждении сосудов.
В организме человека эритроциты формируются из так называемых стволовых клеток. Эти уникальные клетки образуются на стадии эмбрионального развития. Они содержат ядро, в котором находится генетический аппарат (ДНК – дезоксирибонуклеиновая кислота), а также множество других органелл, обеспечивающий процессы их жизнедеятельности и размножения. Стволовые клетки дают начало всем клеточным элементам крови.
Для нормального процесса эритропоэза необходимы:
- Железо. Данный микроэлемент входит в состав гема (небелковой части молекулы гемоглобина) и обладает способностью обратимо связывать кислород и углекислый газ, что и определяет транспортную функцию эритроцитов.
- Витамины (В2, В6, В9 и B12). Регулируют образование ДНК в кроветворных клетках красного костного мозга, а также процессы дифференцировки (созревания) эритроцитов.
- Эритропоэтин. Гормональное вещество, вырабатываемое почками, которое стимулирует процесс образования эритроцитов в красном костном мозге. При уменьшении концентрации красных кровяных телец в крови развивается гипоксия (недостаток кислорода), что является основным стимулятором выработки эритропоэтина.
Образование эритроцитов (эритропоэз) начинается в конце 3 недели эмбрионального развития. На ранних этапах внутриутробного развития красные клетки крови образуются, в основном, в печени и селезенке. Примерно на 4 месяце беременности происходит миграция стволовых клеток из печени в полости костей таза, черепа, позвонков, ребер и других, в результате чего в них формируется красный костный мозг, который также принимает активное участие в процессе кроветворения. После рождения ребенка кроветворная функция печени и селезенки угнетается, и костный мозг остается единственным органом, обеспечивающим поддержание клеточного состава крови.
В процессе превращения в эритроцит, стволовая клетка претерпевает целый ряд изменений. Она уменьшается в размерах, постепенно теряет ядро и практически все органеллы (в результате чего дальнейшее ее деление становится невозможным), а также накапливает гемоглобин. Конечным этапом эритропоэза в красном костном мозге является ретикулоцит (незрелый эритроцит). Он вымывается из костей в периферический кровоток, и в течение суток происходит его созревание до стадии нормального эритроцита, способного в полной мере выполнять свои функции.
Средняя продолжительность жизни красных клеток крови составляет 90 – 120 дней. По истечении этого периода их клеточная мембрана становится менее пластичной, в результате чего теряет способность обратимо деформироваться при прохождении через капилляры. «Старые» эритроциты захватываются и разрушаются особыми клетками иммунной системы – макрофагами. Данный процесс происходит, в основном, в селезенке, а также (в значительно меньшей степени) в печени и красном костном мозге. Незначительно малая доля эритроцитов разрушается непосредственно в сосудистом русле.
При разрушении эритроцита из него выделяется гемоглобин, который быстро распадается на белковую и небелковую части. Глобин подвергается ряду превращений, в результате чего формируется пигментный комплекс желтого цвета – билирубин (несвязанная форма). Он нерастворим в воде и весьма токсичен (способен проникать в клетки организма, нарушая процессы их жизнедеятельности). Билирубин быстро транспортируется в печень, где связывается с глюкуроновой кислотой и выводится вместе с желчью.
Небелковая часть гемоглобина (гем) также подвергается разрушению, в результате чего происходит выделение свободного железа. Оно токсично для организма, поэтому быстро связывается с трансферрином (транспортным белком крови). Большая часть железа, выделяющегося при разрушении эритроцитов, транспортируется в красный костный мозг, где повторно используется для синтеза эритроцитов.
В организме взрослого человека содержится около 4 грамм железа. Эта цифра варьирует в зависимости от пола и возраста.
Концентрация железа в организме составляет:
- у новорожденных – 75 мг на 1 килограмм массы тела (мг/кг);
- у мужчин – более 50 мг/кг;
- у женщин – 35 мг/кг (что связано с ежемесячной потерей крови).
Основными местами содержания железа в организме являются:
- гемоглобин эритроцитов – 57%;
- мышцы – 27%;
- печень – 7 – 8%.
Кроме того, железо входит в состав целого ряда других белковых ферментов (цитохромов, каталазы, редуктазы). Они участвуют в окислительно-восстановительных процессах в организме, в процессах клеточного деления и регуляции многих других реакций. Дефицит железа может привести к недостатку данных ферментов и появлению соответствующих нарушений в организме.
Всасывание железа в организме человека происходит преимущественно в двенадцатиперстной кишке, при этом все железо, поступающее в организм, принято разделять на гемовое (двухвалентное, Fe +2 ), содержащееся в мясе животных и птиц, в рыбе, и негемовое (трехвалентное, Fe +3 ), основным источником которого являются молочные продукты и овощи. Важным условием, необходимым для нормального всасывания железа, является достаточное количество соляной кислоты, входящей в состав желудочного сока. При уменьшении ее количества всасывание железа значительно замедляется.
Всосавшееся железо связывается с трансферрином и транспортируется в красный костный мозг, где используется для синтеза эритроцитов, а также к органам-депо. Запасы железа в организме представлены, в основном, ферритином – комплексом, состоящим из белка апоферритина и атомов железа. Каждая молекула ферритина содержит в среднем 3 – 4 тысячи атомов железа. При снижении концентрации данного микроэлемента в крови, происходит выделение его из ферритина и использование для нужд организма.
Скорость всасывания железа в кишечнике строго ограничена и не может превышать 2,5 мг в сутки. Этого количества достаточно лишь для того, чтобы восстанавливать ежедневные потери данного микроэлемента, которые в норме составляют около 1 мг у мужчин и 2 мг у женщин. Следовательно, при различных патологических состояниях, сопровождающихся нарушением всасывания железа либо повышенными его потерями, может развиться дефицит данного микроэлемента. При снижении концентрации железа в плазме уменьшается количество синтезируемого гемоглобина, в результате чего образующиеся эритроциты будут иметь меньшие размеры. Кроме того, нарушаются процессы роста эритроцитов, что приводит к уменьшению их количества.
Причиной дефицита железа в организме может быть:
- недостаточное поступление железа с пищей;
- повышение потребности организма в железе;
- врожденный недостаток железа в организме;
- нарушение всасывания железа;
- нарушение синтеза трансферрина;
- повышенная кровопотеря;
- алкоголизм;
- применение лекарственных препаратов.
Нарушение питания может привести к развитию железодефицитной анемии как у детей, так и у взрослых.
Основными причинами недостаточного поступления железа в организм являются:
- длительное голодание;
- вегетарианство;
- однообразная диета с малым содержанием животных продуктов.
У новорожденных и детей грудного возраста потребности в железе полностью покрываются при кормлении грудным молоком (при условии, что мать не страдает железодефицитным состоянием). Если же слишком рано переводить ребенка на искусственное вскармливание, у него также могут появиться симптомы дефицита железа в организме.
В нормальных, физиологических условиях может возникать повышенная потребность в железе. Это характерно для женщин во время беременности и в период кормления грудью.
Несмотря на то, что определенная часть железа в период беременности сохраняется (ввиду отсутствия менструальных кровотечений), потребность в нем увеличивается в несколько раз.
| Причина | Примерное количество расходуемого железа |
| Увеличение объема циркулирующей крови и количества эритроцитов | 500 мг |
| Железо, передаваемое плоду | 300 мг |
| Железо, входящее в состав плаценты | 200 мг |
| Кровопотеря во время родов и в послеродовом периоде | 50 – 150 мг |
| Железо, теряемое с грудным молоком за весь период кормления | 400 – 500 мг |
Организм ребенка получает от матери все необходимые питательные вещества, в том числе и железо. Однако при наличии определенных заболеваний у матери или плода, возможно рождение ребенка с дефицитом железа.
Причиной врожденного дефицита железа в организме может быть:
- тяжелая железодефицитная анемия у матери;
- многоплодная беременность;
- недоношенность.
В любом из вышеперечисленных случаев концентрация железа в крови новорожденного значительно ниже нормы, и симптомы железодефицитной анемии могут проявляться уже с первых недель жизни.
Всасывание железа в двенадцатиперстной кишке возможно лишь при нормальном функциональном состоянии слизистой оболочки данного отдела кишечника. Различные заболевания желудочно-кишечного тракта могу повреждать слизистую оболочку и значительно снижать скорость поступления железа в организм.
К уменьшению всасывания железа в двенадцатиперстной кишке может привести:
- Энтерит – воспаление слизистой оболочки тонкого кишечника.
- Целиакия – наследственное заболевание, характеризующееся непереносимостью белка глютена и связанным с этим нарушением всасывания в тонком кишечнике.
- Helicobacter Pylori – инфекционный агент, поражающий слизистую оболочку желудка, что, в конечном итоге, приводит к уменьшению секреции соляной кислоты и нарушению всасывания железа.
- Атрофический гастрит – заболевание, связанное с атрофией (уменьшением размеров и функции) слизистой оболочки желудка.
- Аутоиммунный гастрит – заболевание, вызванное нарушением работы иммунной системы и выработкой антител к собственным клеткам слизистой оболочки желудка с последующим их разрушением.
- Удаление желудка и/или тонкой кишки – при этом уменьшается как количество образуемой соляной кислоты, так и функциональная площадь двенадцатиперстной кишки, где происходит всасывание железа.
- Болезнь Крона – аутоиммунное заболевание, проявляющееся воспалительным поражением слизистой оболочки всех отделов кишечника и, возможно, желудка.
- Муковисцидоз – наследственное заболевание, проявляющееся нарушением секреции всех желез организма, в том числе слизистой оболочки желудка.
- Рак желудка или двенадцатиперстной кишки.
Нарушение образования данного транспортного белка может быть связано с различными наследственными заболеваниями. Симптомов дефицита железа у новорожденного не будет, так как он получал данный микроэлемент из организма матери. После рождения основным способом поступления железа в организм ребенка является всасывание в кишечнике, однако из-за недостатка трансферрина всосавшееся железо не может быть доставлено к органам-депо и к красному костному мозгу и не может использоваться в синтезе эритроцитов.
Так как трансферрин синтезируется только в клетках печени, различные ее поражения (цирроз, гепатиты и другие) также могут привести к уменьшению концентрации данного белка в плазме и развитию симптомов железодефицитной анемии.
Одноразовая потеря большого количества крови обычно не приводит к развитию железодефицитной анемии, так как запасов железа в организме достаточно, чтобы возместить потери. В то же время при хронических, длительных, часто незаметных внутренних кровотечениях организм человека может терять по несколько миллиграмм железа ежедневно, на протяжении нескольких недель или даже месяцев.
Причиной хронической кровопотери может быть:
- язва желудка или двенадцатиперстной кишки;
- геморрой;
- неспецифический язвенный колит (воспаление слизистой толстого кишечника);
- болезнь Крона;
- полипоз кишечника;
- распадающиеся опухоли желудочно-кишечного тракта (и другой локализации);
- грыжа пищеводного отверстия диафрагмы;
- эндометриоз (разрастание клеток внутреннего слоя стенки матки);
- системная красная волчанка;
- системный васкулит (воспаление кровеносных сосудов различной локализации);
- сдача крови донорами более 4 раз в год (300 мл донорской крови содержат около 150 мг железа).
Если причина кровопотери не будет своевременно выявлена и устранена, высока вероятность развития железодефицитной анемии у больного, так как всасывающееся в кишечнике железо способно лишь покрывать физиологические потребности в данном микроэлементе.
Прием некоторых лекарственных препаратов может нарушать процессы всасывания и утилизации железа в организме. Обычно это происходит при длительном приеме больших доз медикаментов.
Препаратами, которые могут вызвать дефицит железа в организме, являются:
- Нестероидные противовоспалительные средства (аспирин и другие). Механизм действия данных препаратов связан с улучшением текучести крови, что может привести к появлению хронических внутренних кровотечений. Кроме того, они способствуют развитию язвы желудка.
- Антациды (Ренни, Алмагель). Данная группа препаратов нейтрализует или уменьшает скорость выделения желудочного сока, содержащего соляную кислоту, необходимую для нормального всасывания железа.
- Железосвязывающие препараты (Десферал, Эксиджад). Данные препараты обладают способностью связывать и выводить из организма железо, причем как свободное, так и входящее в состав трансферрина и ферритина. В случае передозировки возможно развитие железодефицитного состояния.
Во избежание развития железодефицитной анемии принимать данные препараты следует только по назначению врача, строго соблюдая дозировку и длительность использования.
Проявлениями железодефицитной анемии являются:
- мышечная слабость;
- повышенная утомляемость;
- одышка;
- учащенное сердцебиение;
- изменения кожи и ее придатков (волос, ногтей);
- поражение слизистых оболочек;
- поражение языка;
- нарушение вкуса и обоняния;
- склонность к инфекционным заболеваниям;
- нарушения интеллектуального развития.
Как говорилось ранее, железо входит в состав множества ферментов, участвующих в процессах клеточного дыхания и деления. Дефицит данного микроэлемента приводит к повреждению кожи — она становится сухой, менее эластичной, шелушится и трескается. Кроме того, привычный красный или розоватый оттенок слизистым оболочками и коже придают эритроциты, которые находятся в капиллярах данных органов и содержат оксигенированный гемоглобин. При снижении его концентрации в крови, а также в результате уменьшения образования эритроцитов, может отмечаться бледность кожных покровов.
Волосы истончаются, теряют привычный блеск, становятся менее прочными, легко ломаются и выпадают. Рано появляется седина.
Поражение ногтей является весьма специфичным проявлением железодефицитной анемии. Они истончаются, приобретают матовый оттенок, расслаиваются и легко ломаются. Характерной является поперечная исчерченность ногтей. При выраженном дефиците железа может развиться койлонихия – края ногтей приподымаются и изгибаются в обратную сторону, приобретая ложкообразную форму.
Слизистые оболочки относятся к тканям, в которых процессы клеточного деления происходят максимально интенсивно. Вот почему их поражение является одним из первых проявлений дефицита железа в организме.
При железодефицитной анемии поражается:
- Слизистая оболочка полости рта. Она становится сухой, бледной, появляются участки атрофии. Затрудняется процесс пережевывания и проглатывания пищи. Также характерно наличие трещин на губах, образование заед в углах рта (хейлоз). В тяжелых случаях изменяется цвет и снижается прочность зубной эмали.
- Слизистая оболочка желудка и кишечника. В нормальных условиях слизистая оболочка данных органов играет важную роль в процессе всасывания пищи, а также содержит в себе множество желез, вырабатывающих желудочный сок, слизь и другие вещества. При ее атрофии (вызванной дефицитом железа) нарушается пищеварение, что может проявляться диареей или запорами, болями в животе, а также нарушением всасывания различных питательных веществ.
- Слизистая оболочка дыхательных путей. Поражение гортани и трахеи может проявляться першением, чувством наличия инородного тела в горле, что будет сопровождаться непродуктивным (сухим, без мокроты) кашлем. Кроме того, слизистая оболочка дыхательных путей в норме выполняет защитную функцию, предотвращая попадание чужеродных микроорганизмов и химических веществ в легкие. При ее атрофии повышается риск развития бронхита, пневмонии и других инфекционных заболеваний органов дыхания.
- Слизистая оболочка мочеполовой системы. Нарушение ее функции может проявляться болями при мочеиспускании и во время полового акта, недержанием мочи (чаще у детей), а также частыми инфекционными заболеваниями в пораженной области.
Как уже говорилось, слизистая оболочка языка богата вкусовыми рецепторами, расположенными преимущественно в сосочках. При их атрофии могут появляться различные вкусовые нарушения, начиная со снижения аппетита и непереносимости некоторых видов продуктов (обычно кислой и соленой пищи), и заканчивая извращением вкуса, пристрастием к поеданию земли, глины, сырого мяса и других несъедобных вещей.
Нарушения обоняния могут проявляться обонятельными галлюцинациями (ощущением запахов, которых на самом деле нет) либо пристрастием к непривычным запахам (лака, краски, бензина и другим).
Склонность к инфекционным заболеваниям
При дефиците железа нарушается образование не только эритроцитов, но и лейкоцитов – клеточных элементов крови, обеспечивающих защиту организма от чужеродных микроорганизмов. Недостаток данных клеток в периферической крови повышает риск развития различных бактериальных и вирусных инфекций, который еще больше возрастает при развитии анемии и нарушении микроциркуляции крови в коже и других органах.
Важно отметить, что лечение железодефицитной анемии будет неэффективным, если не выявить и не устранить причину ее возникновения.
В диагностике железодефицитной анемии применяется:
- опрос и осмотр пациента;
- общий анализ крови;
- биохимический анализ крови;
- пункция костного мозга.
Первое, что должен сделать врач при подозрении на железодефицитную анемию – это тщательно опросить и обследовать пациента.
Врач может задать следующий вопросы:
- Когда и в какой последовательности начали появляться симптомы заболевания?
- Как быстро они развивались?
- Имеются ли схожие симптомы у членов семьи или ближайших родственников?
- Как питается пациент?
- Страдает ли пациент какими-либо хроническими заболеваниями?
- Каково отношение к алкоголю?
- Принимал ли пациент какие-либо медикаменты в течение последних месяцев?
- Если больна беременная женщина – уточняется срок беременности, наличие и исход предыдущих беременностей, принимает ли она препараты железа.
- Если болен ребенок – уточняется его масса при рождении, родился ли он доношенным, принимала ли мать препараты железа во время беременности.
Во время обследования врач оценивает:
- Характер питания – по степени выраженности подкожно-жировой клетчатки.
- Цвет кожи и видимых слизистых оболочек – особое внимание уделяется слизистой полости рта и языку.
- Придатки кожи – волосы, ногти.
- Мышечную силу – врач просит пациента сжать свою руку или использует специальный прибор (динамометр).
- Артериальное давление – оно может быть снижено.
- Вкус и обоняние.
Это первый анализ, назначаемый всем пациентам при подозрении на анемию. Он позволяет подтвердить или опровергнуть наличие анемии, а также дает косвенную информацию о состоянии кроветворения в красном костном мозге.
Кровь для общего анализа может браться из пальца или из вены. Первый вариант более подходит в том случае, если общий анализ является единственным лабораторным исследованием, назначенным пациенту (когда достаточно небольшого количества крови). Перед взятием крови кожу пальца всегда обрабатывают ватой, смоченной в 70% спирте, чтобы избежать занесения инфекции. Прокол производится специальной одноразовой иглой (скарификатором) на глубину 2 – 3 мм. Кровотечение в данном случае несильное и полностью останавливается практически сразу после взятия крови.
В том случае, если планируется выполнять сразу несколько исследований (например, общий и биохимический анализ) – берут венозную кровь, так как ее легче получить в больших количествах. Перед забором крови на среднюю треть плеча накладывается резиновый жгут, что приводит к наполнению вен кровью и облегчает определение их местоположения под кожей. Место прокола также должно быть обработано спиртовым раствором, после чего медсестра одноразовым шприцем прокалывает вену и набирает кровь для анализа.
Полученную одним из описанных методов кровь направляют в лабораторию, где она исследуется в гематологическом анализаторе – современном высокоточном приборе, имеющемся в большинстве лабораторий мира. Часть полученной крови окрашивают специальными красителями и исследуют в световом микроскопе, что позволяет визуально оценить форму эритроцитов, их строение, а при отсутствии или неисправности гематологического анализатора – произвести подсчет всех клеточных элементов крови.
При железодефицитной анемии мазок периферической крови характеризуется:
- Пойкилоцитозом – наличием в мазке эритроцитов различных форм.
- Микроцитозом – преобладанием эритроцитов, размер которых меньше нормы (могут встречаться и нормальные эритроциты).
- Гипохромией – цвет эритроцитов изменяется с ярко-красного на бледно-розовый.
| Исследуемый показатель | Что обозначает? | Норма | Возможные изменения при железодефицитной анемии |
| Концентрация эритроцитов (RBC) | При истощении запасов железа в организме нарушается эритропоэз в красном костном мозге, ввиду чего общая концентрация эритроцитов в крови будет снижена. | Мужчины (М): 4,0 – 5,0 х 10 12 /л. | Менее 4,0 х 10 12 /л. |
| Женщины (Ж): 3,5 – 4,7 х 10 12 /л. | Менее 3,5 х 10 12 /л. | ||
| Средний объем эритроцита (MCV) | При дефиците железа нарушаются процессы образования гемоглобина, в результате чего уменьшается размер самих эритроцитов. Гематологический анализатор позволяет максимально точно определить данный показатель. | 75 – 100 кубических микрометров (мкм 3 ). | Менее 70 мкм 3 . |
| Концентрация тромбоцитов (PLT) | Тромбоциты – клеточные элементы крови, отвечающие за остановку кровотечений. Изменение их концентрации может наблюдаться в том случае, если дефицит железа вызван хронической кровопотерей, что приведет к компенсаторному увеличению их образования в костном мозге. | 180 – 320 х 10 9 /л. | В норме или увеличена. |
| Концентрация лейкоцитов (WBC) | При развитии инфекционных осложнений концентрация лейкоцитов может значительно повышаться. | 4,0 – 9,0 х 10 9 /л. | В норме или увеличена. |
| Концентрация ретикулоцитов (RET) | В нормальных условиях естественным ответом организма на анемию является увеличение скорости образования эритроцитов в красном костном мозге. Однако при дефиците железа развитие данной компенсаторной реакции невозможно, ввиду чего снижается количество ретикулоцитов в крови. | М: 0,24 – 1,7%. | Уменьшена либо находится на нижней границе нормы. |
| Ж: 0,12 – 2,05%. | |||
| Общий уровень гемоглобина (HGB) | Как уже говорилось, дефицит железа приводит к нарушению образования гемоглобина. Чем дольше длится заболевание, тем ниже будет данный показатель. | М: 130 – 170 г/л. | Менее 120 г/л. |
| Ж: 120 – 150 г/л. | Менее 110 г/л. | ||
| Среднее содержание гемоглобина в одном эритроците (MCH) | Данный показатель более точно характеризует нарушение образования гемоглобина. | 27 – 33 пикограмм (пг). | Менее 24 пг. |
| Гематокрит (Hct) | Данный показатель отображает количество клеточных элементов по отношению к объему плазмы. Так как основное большинство клеток крови представлено эритроцитами, уменьшение их количества приведет к снижению гематокрита. | М: 42 – 50%. | Менее 40%. |
| Ж: 38 – 47%. | Менее 35%. | ||
| Цветовой показатель (ЦП) | Цветовой показатель определяется путем пропускания через взвесь эритроцитов световой волны определенной длины, которая поглощается исключительно гемоглобином. Чем меньше будет концентрация данного комплекса в крови, тем ниже будет значение цветового показателя. | 0,85 – 1,05. | Менее 0,8. |
| Скорость оседания эритроцитов (СОЭ) | Все клетки крови, а также эндотелий (внутренняя поверхность) сосудов, имеют отрицательный заряд. Они отталкиваются друг от друга, что способствует поддержанию эритроцитов во взвешенном состоянии. При уменьшении концентрации эритроцитов расстояние между ними увеличивается, и сила отталкивания уменьшается, в результате чего они будут оседать на дно пробирки быстрее, чем в нормальных условиях. | М: 3 – 10 мм/час. | Более 15 мм/час. |
| Ж: 5 – 15 мм/час. | Более 20 мм/час. |
В ходе данного исследования удается установить концентрацию различных химических веществ, находящихся в крови. Это дает информацию о состоянии внутренних органов (печени, почек, костного мозга и других), а также позволяет выявить множество заболеваний.
Существует несколько десятков биохимических показателей, определяемых в крови. В данном разделе будут описаны только те из них, которые имеют значение в диагностике железодефицитной анемии.
| Исследуемый показатель | Что обозначает? | Норма | Возможные изменения при железодефицитной анемии |
| Концентрация сывороточного железа | Вначале данный показатель может быть в норме, так как дефицит железа будет компенсироваться выделением его из депо. Только при длительном течении заболевания концентрация железа в крови начнет снижаться. | М: 17,9 – 22,5 мкмоль/л. | В норме или снижена. |
| Ж: 14,3 – 17,9 мкмоль/л. | |||
| Уровень ферритина в крови | Как говорилось ранее, ферритин является одним из основных видов депонирования железа. При недостатке данного элемента начинается мобилизация его из органов-депо, ввиду чего уменьшение концентрации ферритина в плазме является одним из первых признаков железодефицитного состояния. | Дети: 7 – 140 нанограмм в 1 миллилитре крови (нг/мл). | Чем дольше длится дефицит железа, тем меньше уровень ферритина. |
| М: 15 – 200 нг/мл. | |||
| Ж: 12 – 150 нг/мл. | |||
| Общая железосвязывающая способность сыворотки | Данный анализ основан на способности трансферрина, находящегося в крови, связывать железо. В нормальных условиях, каждая молекула трансферрина только на 1/3 связана с железом. При дефиците данного микроэлемента печень начинает синтезировать больше трансферрина. Концентрация его в крови повышается, однако количество железа, приходящегося на каждую молекулу, снижается. Определив, какая доля молекул трансферрина находится в несвязанном с железом состоянии, можно сделать выводы о выраженности дефицита железа в организме. | 45 – 77 мкмоль/л. | Значительно выше нормы. |
| Концентрация эритропоэтина | Как было упомянуто ранее, эритропоэтин выделяется почками, если ткани организма испытывают недостаток в кислороде. В норме данный гормон стимулирует эритропоэз в костном мозге, однако при дефиците железа данная компенсаторная реакция малоэффективна. | 10 – 30 международных миллиединиц в 1 миллилитре (мМЕ/мл). | Значительно выше нормы. |
Данное исследование заключается в прокалывании одной из костей организма (обычно грудины) специальной полой иглой и заборе нескольких миллилитров вещества костного мозга, которое потом исследуется под микроскопом. Это позволяет напрямую оценить выраженность изменения структуры и функции органа.
В начале заболевания никаких изменений в пунктате костного мозга не будет. При развитии анемии может отмечаться разрастание эритроидного ростка кроветворения (увеличения количества клеток-предшественниц эритроцитов).
Для выявления причины железодефицитной анемии применяется:
- анализ кала на наличие скрытой крови;
- рентгенологическое исследование;
- компьютерная томография;
- эндоскопические исследования;
- консультация других специалистов.
Причиной появления крови в кале (мелены) может стать кровотечение из язвы, распад опухоли, болезнь Крона, неспецифический язвенный колит и другие заболевания. Обильные кровотечения легко определяются визуально по изменению цвета каловых масс на ярко-красный (при кровотечении из нижних отелов кишечника) или черный (при кровотечении из сосудов пищевода, желудка и верхнего отдела кишечника).
Массивные однократные кровотечения практически не приводит к развитию железодефицитной анемии, так как быстро диагностируются и устраняются. Опасность в этом плане представляют длительные, небольшие по объему кровопотери, возникающие при повреждении (или изъязвлении) мелких сосудов желудочно-кишечного трата. В таком случае выявить кровь в кале возможно только с помощью специального исследования, которое назначается во всех случаях анемии неясного генеза.
С целью выявления опухолей или язв желудка и кишечника, которые могли стать причиной хронического кровотечения, применяется рентген с контрастом. В роли контраста используется вещество, которое не поглощает рентгеновские лучи. Обычно это взвесь бария в воде, которую пациент должен выпить непосредственно перед началом исследования. Барий покрывает слизистые оболочки пищевода, желудка и кишечника, в результате чего на рентгеновском снимке становится четко различима их форма, контур и различные деформации.
Перед проведением исследования необходимо исключить прием пищи в течение последних 8 часов, а при исследовании нижних отделов кишечника назначаются очистительные клизмы.
В данную группу включен ряд исследований, суть которых заключается во введении в полости организма специального аппарата с видеокамерой на одном конце, подсоединенной к монитору. Этот метод позволяет визуально исследовать слизистые оболочки внутренних органов, оценить их строение и функцию, а также выявить опухоль или кровотечение.
С целью установления причины железодефицитной анемии используется:
- Фиброэзофагогастродуоденоскопия (ФЭГДС) – введение эндоскопа через рот и исследование слизистой оболочки пищевода, желудка и верхних отделов кишечника.
- Ректороманоскопия – исследование прямой и нижнего отдела сигмовидной кишки.
- Колоноскопия – исследование слизистой оболочки толстого кишечника.
- Лапароскопия – прокалывание кожи передней стенки живота и введение эндоскопа в брюшную полость.
- Кольпоскопия – исследование влагалищной части шейки матки.
При выявлении заболевания различных систем и органов гематолог может привлекать специалистов из других областей медицины с целью постановки более точного диагноза и назначения адекватного лечения.
Для выявления причины железодефицитной анемии может понадобиться консультация:
- Диетолога – при выявлении нарушения питания.
- Гастролога – при подозрении на наличие язвы или других заболеваний желудочно-кишечного тракта.
- Хирурга – при наличии кровотечения из желудочно-кишечного тракта или другой локализации.
- Онколога – при подозрении на опухоль желудка или кишечника.
- Акушера-гинеколога – при наличии признаков беременности.
| Название продукта | Содержание железа в 100 г продукта |
| Продукты животного происхождения | |
| Печень свиная | 20 мг |
| Печень куриная | 15 мг |
| Печень говяжья | 11 мг |
| Яичный желток | 7 мг |
| Мясо кролика | 4,5 – 5 мг |
| Баранина, говядина | 3 мг |
| Куриное мясо | 2,5 мг |
| Творог | 0,5 мг |
| Коровье молоко | 0,1 – 0,2 мг |
| Продукты растительного происхождения | |
| Плоды шиповника | 20 мг |
| Морская капуста | 16 мг |
| Чернослив | 13 мг |
| Гречка | 8 мг |
| Семена подсолнечника | 6 мг |
| Смородина черная | 5,2 мг |
| Миндаль | 4,5 мг |
| Персик | 4 мг |
| Яблоки | 2,5 мг |
Основным направлением в терапии данного заболевания является использование препаратов железа. Диетотерапия, хотя и является важным этапом лечения, не в состоянии самостоятельно восполнить дефицит железа в организме.
Методом выбора являются таблетированные формы препаратов. Парентеральное (внутривенное или внутримышечное) введение железа назначается в случае, если невозможно полноценное всасывание данного микроэлемента в кишечнике (например, после удаления части двенадцатиперстной кишки), необходимо быстро восполнить запасы железа (при массивной кровопотере) либо при развитии побочных реакций от применения пероральных форм препарата.
| Название препарата | Механизм лечебного действия | Способ применения и дозы | Контроль эффективности лечения |
| Гемофер пролонгатум | Препарат сульфата железа, восполняющий запасы данного микроэлемента в организме. | Принимать внутрь, за 60 минут до или через 2 часа после еды, запивая стаканом воды. |
Рекомендуемые дозы:
- детям – 3 миллиграмма на килограмм массы тела в сутки (мг/кг/сут);
- взрослым – 100 – 200 мг/сут.
Перерыв между двумя последующими приемами железа должен составлять не менее 6 часов, так как в этот период клетки кишечника невосприимчивы к новым дозам препарата.
Длительность лечения – 4 – 6 месяцев. После нормализации уровня гемоглобина переходят на поддерживающую дозу (30 – 50 мг/сутки) еще на 2 – 3 месяца.
- Повышение количества ретикулоцитов в анализе периферической крови на 5 – 10 день после начала приема препаратов железа.
- Повышение уровня гемоглобина (обычно отмечается через 3 – 4 недели лечения).
- Нормализация уровня гемоглобина и количества эритроцитов на 9 – 10 неделе лечения.
- Нормализация лабораторных показателей – уровня сывороточного железа, ферритина крови, общей железосвязывающей способности сыворотки.
- Постепенное исчезновение симптомов дефицита железа отмечается на протяжении нескольких недель или месяцев.
Данные критерии используются для контроля эффективности лечения всеми препаратами железа.
Рекомендуемые дозы:
- взрослым для лечения анемии – 2 таблетки 2 раза в день;
- женщинам при анемии во время беременности – 1 – 2 таблетки 1 раз в сутки.
После нормализации уровня гемоглобина переходят на поддерживающую терапию (20 – 50 мг 1 раз в сутки).
- сульфат железа;
- фолиевую кислоту;
- витамин В12.
Данный препарат назначается женщинам во время беременности (когда повышается риск развития дефицита железа, фолиевой кислоты и витаминов), а также при различных заболеваниях желудочно-кишечного тракта, когда нарушается всасывание не только железа, но и многих других веществ.
При внутривенном введении железа высок риск передозировки, поэтому данная процедура должна выполняться только в условиях стационара под контролем специалиста.
Важно помнить, что некоторые лекарственные средства (и другие вещества) могут в значительной степени ускорять либо замедлять скорость всасывания железа в кишечнике. Применять их совместно с препаратами железа стоит осторожно, так как это может привести к передозировке последних, или, наоборот, к отсутствию лечебного эффекта.
| Медикаменты, способствующие всасыванию железа | Вещества, препятствующие всасыванию железа |
|
|
При неосложненном течении и правильно проводимом лечении необходимости в данной процедуре нет.
Показаниями к переливанию эритроцитов являются:
- массивная кровопотеря;
- снижение концентрации гемоглобина менее 70 г/л;
- стойкое снижение систолического артериального давления (ниже 70 миллиметров ртутного столба);
- предстоящее хирургическое вмешательство;
- предстоящие роды.
Эритроциты следует переливать максимально короткий промежуток времени, пока не будет устранена угроза жизни пациента. Данная процедура может осложниться различными аллергическими реакциями, поэтому перед ее началом необходимо провести целый ряд тестов на определение совместимости крови донора и реципиента.

Причиной затруднений в лечении железодефицитной анемии может быть:
- неправильно выставленный диагноз;
- неустановленная причина дефицита железа;
- поздно начатое лечение;
- прием недостаточных доз препаратов железа;
- нарушение режима приема медикаментов или диеты.
При нарушениях в диагностике и лечении заболевания возможно развитие различных осложнений, некоторые из которых могут представлять опасность для здоровья и жизни человека.
Осложнениями железодефицитной анемии могут быть:
- Отставание в росте и развитии. Данное осложнение характерно для детей. Оно обусловлено ишемией и связанными с ней изменениями в различных органах, в том числе в ткани головного мозга. Отмечается как задержка физического развития, так и нарушение интеллектуальных способностей ребенка, которые при длительном течении заболевания могут оказаться необратимыми.
- Анемическая кома. Развитие комы обусловлено критическим снижением доставки кислорода к головному мозгу. Внешне это проявляется потерей сознания, отсутствием реакции на речь и болевые раздражители. Кома является опасным для жизни состоянием, требующим срочной медицинской помощи.
- Развитие недостаточности внутренних органов. При длительном дефиците железа и наличии анемии могут поражаться практически все органы человека. Наиболее характерным является развитие сердечной недостаточности, почечной недостаточности и печеночной недостаточности.
- Инфекционные осложнения. Часто рецидивирующие инфекции могут сопровождаться поражением внутренних органов и развитием сепсиса (попадания гноеродных бактерий в кровоток и ткани организма), что особенно опасно у детей и людей пожилого возраста.
источник