Анемия – это комплексный клинико-гематологический синдром, проявляющийся снижением количества эритроцитов и гемоглобина крови. Анемии — довольно распространенное заболевание и по разным данным заболеваемость составляет от 7 до 17% населения.
Анемии различаются по причинам, течению, симптомам и прогнозу. Среди всех первое место занимает железодефицитная анемия, которая составляет до 80% случаев. Согласно данным Всемирной Организации Здравоохранения железодефицитной анемией страдает каждая третья женщина и каждый шестой мужчина в мире, а также до 50% детей раннего возраста, а это порядка 2 миллиардов человек.
Железодефицитная анемия – это гипохромная (снижение содержания гемоглобина в эритроците) микроцитарная (уменьшение размеров эритроцитов) анемия, развивающаяся вследствие абсолютного дефицита железа в организме.
Первые запасы железа организм человека получает от матери через систему мать-плацента-плод, после рождения железо восполняется с приемом пищи или железосодержащих препаратов.
Выведение железа из организма осуществляется через мочевыделительную и пищеварительную системы, потовые железы и во время менструаций у женщин. В сутки выводится около 2 граммов железа, поэтому, чтобы не допустить истощения запасов, его нужно восполнять тем или иным образом.
1) Недостаточное поступление железа с пищей
— голодание,
— вегетарианство или обедненная железом и белком диета, соблюдаемая длительное время,
— у детей на грудном вскармливании причиной может быть железодефицитная анемия матери,
— ранний перевод на искусственное вскармливание,
— позднее введение прикорма.
2) Повышение потребности в железе
— период роста и полового созревания у подростков,
— становление менструальной функции у девочек,
— частые ОРВИ (потребление железа инфекционными агентами),
— опухолевый рост любой локализации,
— занятия спортом,
— беременность,
— грудное вскармливание.
Несмотря на то, что при беременности часть железа сберегается за счет отсутствия менструальных выделений, потребность в железе настолько возрастает, что необходимо его восполнение, чаще всего с лекарственными препаратами. Почти каждая беременность сопровождается железодефицитным состоянием, выраженным в той или иной степени. Потребность пропорционально возрастает при многоплодной беременности.
3) Врожденный недостаток железа в организме
— недоношенность,
— рождение от многоплодной беременности,
— тяжелая железодефицитная анемия у матери,
— патологические кровотечения во время беременности и родов,
— фетоплацентарная недостаточность.
4) Нарушение всасывания железа.
В этом случае имеет значение не столько процентное содержание железа в продуктах питания или препаратах, сколько эффективность его поступления в кровь. Нарушение всасывания железа обусловлено различными заболеваниями желудочно-кишечного тракта, всасывание происходит преимущественно в двенадцатиперстной тощей кишках и зависит от состояния слизистой оболочки этих отделов кишечника:
— энтерит (воспаление слизистой тонкой кишки, вызванное инфекцией или глистной инвазией),
— гастриты (атрофический, аутоиммунный) и язвенная болезнь желудка и двенадцатиперстной кишки (часто вызванными бактерией Helicobacter Pylori),
— наследственные заболевания: здесь первостепенное значение имеют муковисцидоз и целиакия. Помимо нарушения всасывания микроэлементов (включая железо) они проявляются тяжелым симптомокомплексом, и такие дети нуждаются в особенном питании. Поэтому анализ на эти заболевания производится на 3-4 сутки в роддоме;
— болезнь Крона (аутоиммунное поражение слизистой кишечника и возможно желудка),
— состояние после удаления желудка и/или двенадцатиперстной кишки,
— рак желудка и кишечника (здесь имеет место сложный механизм анемии, нарушается всасывание железа слизистой, высокий риск кровотечения и повышается потребление вследствие хронической болезни).
5) Повышенные потери железа:
— хронические кровопотери. Это самая масштабная причина в этой группе, анемия возникает в результате регулярных потерь малых объемов крови, сюда относятся потери по причине:
язвенной болезни желудка и двенадцатиперстной кишки, неспецифического язвенного колита, болезни Крона, геморроя и анальных трещин, полипоза кишечника, кровотечений из распадающихся опухолей любой локализации и варикознорасширенных вен пищевода;
легочных кровотечений (бронхоэктатическая болезнь, рак легких, туберкулез), гемосидероза легких (хроническое заболевание легких, проявляющееся повторными кровоизлияниями в легочные пузырьки — альвеолы);
микро- и макрогематурии (хронический пиелонефрит и гломерулонефрит, поликистоз и рак почек, полипоз и опухоли мочевого пузыря), потери при гемодиализе;
у женщин частыми причинами хронической железодефицитной анемии являются миома матки, эндометриоз, гиперполименорея, рак шейки матки и другой локализации;
у детей и подростков частой причиной служат носовые кровотечения (болезнь Рандю-Ослера и другие причины);
— аллергические заболевания (потери микроэлемента в составе слущивающегося эпителия).
6) Нарушение синтеза трансферрина. Трансферрин – это транспортный белок железа, который синтезируется в печени.
— врожденный дефект синтеза трансферрина (часто прослеживается наследственность)
— наличие антител (защитных белков, блокирующих его действие) к трансферрину
— хронические гепатиты различной природы и циррозы печени
7) Алкоголизм. Алкоголь повреждает слизистую желудка и кишечника, тем самым затрудняя всасывание железа, а так же угнетает кроветворную функцию красного костного мозга.
8) Применение лекарственных средств.
— нестероидные противовоспалительные средства (диклофенак, ибупрофен, аспирин) уменьшают вязкость крови и могут способствовать возникновению кровотечений, кроме того эти препараты могут провоцировать возникновение язв желудка и двенадцатиперстной кишки.
— антациды (альмагель, гастал, ренни) уменьшают продукцию соляной кислоты, которая необходима для эффективного всасывания железа
— железосвязывающие препараты (десферал), эти препараты связывают и выводят свободное железо и железо в составе ферритина и трансферрина, и при передозировке могут приводить к железодефицитным состояниям.
9) Донорство. 300 мл донорской крови содержат около 150 мг железа, при донациях чаще 4х раз в год развивается железодефицитное состояние.
1) Анемический синдром
2) Сидеропенический синдром
3) Негематологические проявления анемии
Анемический синдром формируется из-за снижения эритроцитов и гемоглобина крови, что вызывает снижение насыщения клеток и тканей кислородом. Признаки анемического синдрома неспецифичны, но помогают заподозрить наличие анемии и в комплексе с данными других обследований поставить диагноз.
Субъективные признаки вначале проявляются при нагрузке больше обычной, а далее (при прогрессировании заболевания) и в покое:
— общая слабость
— повышенная утомляемость и снижение работоспособности
— головокружение
— шум в ушах и мелькание «мушек» перед глазами
— эпизоды учащенного сердцебиения
— усиление одышки при физической нагрузке
— обморочные состояния
При объективном обследовании выявляются:
— бледность кожного покрова и видимых слизистых (например, внутренняя поверхность нижнего века)
— пастозность (небольшие отеки) голеней, стоп, лица (преимущественно области вокруг глаз)
— тахикардия, различные варианты аритмии
— умеренные шумы в сердце, приглушенность сердечных тонов
Сидеропенический синдром вызван дефицитом железа в тканях, что вызывает снижение активности многих ферментов (белковые субстанции, регулирующие многие жизненные функции).
Сидеропенический синдром проявляется многочисленными симптомами:
— изменение вкуса (непреодолимое желание употреблять в пищу необычные продукты: песок, мел, глину, зубной порошок, лед, а также сырой фарш, непропеченное тесто, сухие крупы), чаще выражен у женщин и подростков
— склонность к употреблению острой, соленой, пряной пище
— извращение обоняния (привлекают запахи, воспринимаемые большинством как неприятные: бензин, ацетон, запах лаков, красок, извести)
— снижение мышечной силы и атрофия мышц в связи с дефицитом миоглобина (кислородосвязывающий белок в скелетных мышцах) и ферментов тканевого дыхания
— дистрофические изменения кожи (сухость вплоть до образования трещин, шелушение), волос (ломкость, выпадение, тусклость, раннее поседение), ногтей (тусклость, поперечная исчерченность, койлонихии — ложкообразная вогнутость ногтей). Снижается восстановительная функция кожи (долго не заживают мелкие травмы, ссадины).
— ангулярный стоматит (сухость и трещины в углах рта) у 10-15% больных
— глоссит (воспаление языка), характеризуется чувством боли и распирания в области языка, покраснением и атрофией сосочков (так называемы «лакированный язык», поверхность языка в этом случае не бархатистая, как в норме, а гладкая и даже блестящая), частые пародонтозы и кариес
— атрофические изменения слизистой оболочки желудочно-кишечного тракта (сухость слизистой пищевода, что вызывает боли при глотании и затруднение при глотании твердой пищи – сидеропеническая дисфагия), развитие атрофического гастрита и энтерита
— дистрофические изменения в мышцах сфинктеров мочевого пузыря (неотложные позывы к мочеиспусканию, невозможность удержать мочу при кашле, смехе, чихании, эпизоды ночного недержания мочи)
— симптом «синих склер» характеризуется голубоватой окраской склер (из-за дефицита железа и недостаточной функции некоторых ферментов нарушается синтез коллагена белочной оболочке глаз, она истончается и через нее просвечивают мелкие сосуды)
— «сидеропенический субфебрилитет» — длительное повышение температуры тела до субфебрильных цифр (37.0-37.9°С) без видимых причин
— предрасположенность к инфекционно-воспалительным заболеваниям (частые ОРВИ и другие инфекции), склонность к хронизации инфекции
— снижение устойчивости при отравлении тяжелыми металлами
Негематологические последствия анемии:
— замедление роста плода у беременной с анемией,
— нарушение менструального цикла,
— импотенция,
— изменения поведения, снижение мотивации, интеллектуальных способностей, эти симптомы более выражены у детей и подростков и исчезают при восстановлении запасов железа.
I. Общий осмотр (цвет кожи и слизистых, тип телосложения), опрос пациента (хронические заболевания, отношение к алкоголю, наследственность, для женщина характер менструаций и дата последней менструации), пальпация (болезненность живота и поясницы, объемные образования живота и молочных желез, размер и подвижность лимфоузлов), перкуссия (выстукивание с целью определения границ сердца и печени, болезненности плоских и трубчатых костей), аускультация (выслушивание возможных хрипов в легких, шумов и ритма сердца).
II. ОАК (общий анализ крови) или КРАК (клинический развернутый анализ крови) – это главное исследование в первичной диагностике анемии.
Здесь мы приведем наиболее важные показатели, чтобы вы могли ориентироваться в результате анализа:
Hb (гемоглобин) — норма у женщин составляет 120-150 г/ л, у мужчин 130-170 г/л.
RBC (эритроциты) — норма 3,9-6,0*1012 у мужчин, 3,7-5,0*1012 /л у женщин, количество эритроцитов в новорожденных детей является максимальной и составляет 6,0-9,0 * 1012 / л, у пожилых людей концентрация эритроцитов также может быть увеличена до 6,0 * 1012 / л. В обоих случаях такие показатели считаются нормой.
RET (ретикулоциты) – норма от 0,8 — 1,3 до 0,2 — 2%.
Hct (гематокрит, то есть соотношение клеток крови и жидкой ее части) — у мужчин он достигает 40-48%, у женщин несколько ниже — 36-42%.
MCV (средний объем эритроцита) — норма 75-95мкм 3 .
MCH (среднее содержание гемоглобина в эритроцитах) – норма 24-33 пг.
MCHC (средняя концентрации гемоглобина в эритроцитах) — норма 30-38%.
WBC (лейкоциты) – 3.6-10.2 *10 9 /л.
PLT (тромбоциты) – 152-343 *10 9 /л.
III. ОАМ (общий анализ мочи) , первостепенное значение имеют потери белка с мочой и наличие в моче крови
IV. Общие биохимические исследования (общий белок, глюкоза, билирубин общий и прямой, АлАТ, АсАТ, ЩФ, креатинин, мочевина, ЛДГ, СРБ)
V. Специфические биохимические исследования
1. определение железа в сыворотке крови
Норма: дети до 1 года — 7,16-17,90 мкмоль/л;
дети с 1 года до 14 лет — 8,95-21,48 мкмоль/л;
женщины — 8,95-30,43 мкмоль/л;
мужчины — 11,64-30,43 мкмоль/л.
2. общая железосвязывающая способность сыворотки крови (норма у женщин: 38,0-64,0 мкм/л, у мужчин 45,0 — 75,0 мкм/л)
3. насыщение железом трансферрина (в норме около 30 %)
4. содержание трансферрина (норма 2.0-4.0 г/л)
5. содержание ферритина в сыворотке крови (мкг/л = нг/мл)
новорожденные 25 — 200
1 месяц 200 — 600
6 месяцев — 15 лет 30 — 140
мужчины 20 — 350
женщины 10 — 150
1-ый триместр 56 — 90
2-ой триместр 25 — 74
3-ий триместр 10 — 15
6. десфераловый тест (после внутривенного введения 500 мг десферала у здорового человека с мочой выделяется от 0,8 до 1,2 мг железа, у больных с железодефицитной анемией этот показатель ниже).
VI. Далее в плане дообследования вам могут назначить:
— анализ крови на ВИЧ и гепатиты В и С
— рентген легких, при необходимости бронхоскопия с биопсией (взятие кусочка ткани на анализ), компьютерная томография легких
— анализ кала на паразитов и скрытую кровь
— ФГДС и исследование кислотности желудочного сока
— УЗИ внутренних органов и почек
— исследование кишечника (ирригоскопия, ректороманоскопия, колоноскопия)
— консультация уролога, гинеколога, проктолога, гастроэнтеролога
— стернальная пункция (взятие образца красного костного мозга из грудины для исследования)
— УЗИ матки и придатков
— исследование мокроты на альвеолярные макрофаги, содержащие гемосидерин
— консультация эндокринолога, ревматолога
— анализ на онкомаркеры
1. Диета
2. Пероральные препараты железа
3. Инъекционные препараты железа
4. Гемотрансфузия
Диета в комплексном лечении железодефицитной анемии может быть эффективна при нормальном усвоении железа из пищи, отсутствии заболеваний желудочно-кишечного тракта.
Диета при железодефицитной анемии должна включат продукты, богатые железом (говяжий язык, мясо курицы, индейки, печень, морская рыба, сердце, гречневая крупа и пшено, яйца, зелень, горох, орехи, какао, абрикосы, яблоки, персики, хурма, айва, черника, тыквенные семечки), аскорбиновой кислотой, которая улучшает всасывание железа (болгарский перец, капуста, шиповник, смородина, цитрусовые, щавель).
Следует ограничить продукты, затрудняющие всасывание железа: черный чай, все молочные продукты.
Пероральные препараты железа (в таблетках, каплях, сиропе, растворе) являются стартовым лечением при анемии легкой и средней тяжести, при наличии беременности прием согласуется с акушером-гинекологом.
— сорбифер дурулес/ фенюльс 100 по 1-2 таблетки 1-2 раза в сутки до восстановления уровня гемоглобина (у беременных для профилактики 1 таблетка 1 раз в сутки, для лечения 1 таблетка 2 раза в сутки).
— ферретаб 1 капсула в сутки, максимально до 2-3 капсул в сутки в 2 приема, минимальный срок приема 4 недели, далее по показаниям.
— мальтофер бывает в трех лекарственных формах (капли, сироп, таблетки), прием при железодефицитной анемии по 40-120 капель/10-30 мл сиропа/1-3 таблетки в сутки в 1-2 приема. Детям до 1 года 10-20 капель, 2.5-5 мл сиропа в 1-2 приема, детям от 1 года до 12 лет 20-40 капель, 5-10 мл сиропа в 1-2 приема; прием в течение 3-5 месяцев под контролем уровня гемоглобина.
— тардиферрон/ ферроградумет по 1-2 таблетки в сутки до восстановления уровня гемоглобина, беременным женщинам по 1 таблетке в сутки II-III триместр.
— актиферрин по 1 капсуле 2-3 раза в день 8-12 недель, новорожденным и грудным детям препарат дается в форме капель 10-15 капель 2-3 раза в день, детям дошкольного возраста 25-35 капель 3 раза в день.
— тотема (комбинированный препарат железа, меди и марганца) по 2-4 ампулы в сутки, раствор разводят в 1 стакане воды, прием в течение 3-6 месяцев, детям 5-7 мг/кг веса в 3-4 приема.
Инъекционные препараты используются исключительно в стационаре (необходимо иметь возможность оказания противошоковой помощи), противопоказаны при беременности и лактации.
— венофер (раствор строго для в/в введения, расчет дозы и скорости введения производится индивидуально).
— космофер (раствор для в/в и в/м введения, расчет доза и способа введения производится индивидуально).
— ферринжект (раствор для введения в/в или в диализную систему).
Трансфузия (переливание компонентов крови) производится при тяжелой анемии, по строгим показаниям и в условиях стационара.
Анемия у детей проявляется общими симптомами (бледность кожи и слизистых, общая вялость, плаксивость, потливость, снижение аппетита, нарушения сна), у грудных детей наблюдаются частые срыгивания и рвота после кормления, у детей после года могут наблюдаться регресс моторных навыков, снижение зрения, дистрофические изменения кожи, волос и ногтей, разрушение зубов.
При прогрессировании заболевания можно наблюдать развитие функционального шума в сердце, тахикардии, головных болей, обмороков, возможно увеличение размеров печени и селезенки, появление необычных вкусовых влечений – желание есть мел, глину, землю.
Лечение анемии у детей включает 4 принципа: нормализация режима и питания, возможное устранение причины железодефицита, терапия препаратами железа, сопутствующая терапия.
— приоритет грудного вскармливания,
— длительные прогулки на воздухе, профилактика ОРВИ,
— введение мясного прикорма с 6 месяцев,
— исключить прикорм манной, рисовой, толокняной кашами, отдать предпочтение гречневой, ячменной, просяной,
— прием препаратов железа (мальтофера, актиферрина, тотемы) под контролем педиатра.
Об эффективности лечения можно судить уже через 7-10 дней (увеличение ретикулоцитов в 2 раза по сравнению с исходным, увеличение гемоглобина на 10г/л и более в неделю), лечение продолжается не менее 3 месяцев. Если назначенное лечение неэффективно, то следует рассмотреть другие препараты, возможно увеличение дозы до максимальной терапевтической, необходимо исключить источники хронической кровопотери, очаги хронических инфекций, наличие новообразований и глистных инвазий, сопутствующий дефицит витамина В12.
При соблюдении принципов комплексной терапии симптомы анемии быстро регрессируют.
Осложнения возникают при длительном течении анемии без лечения и снижают качество жизни.
— снижение иммунитета,
— учащение сердцебиения, которое ведет к большей нагрузке на сердце и в итоге к сердечной недостаточности,
— у беременных повышается риск преждевременных родов и задержки роста плода,
— у детей недостаток железа обуславливает задержку роста и развития,
— редким и тяжелым осложнением является гипоксическая кома,
— гипоксия из-за недостатка железа осложняет течение уже имеющихся сердечно-легочных заболеваний (ИБС, бронхиальная астма, бронхоэктатическая болезнь и другие).
В подавляющем числе случаев железодефицитная анемия успешно поддается коррекции, признаки и симптомы анемии отступают. Однако при отсутствии лечения развиваются осложнения и болезнь прогрессирует.
Если у вас выявлен пониженный уровень гемоглобина, то необходимо пройти полное клинико-лабораторное обследование и выявить причину анемии. Правильно поставленный диагноз – залог успешного лечения.
источник
В.Ю. Сельчук, С.С. Чистяков, Б.О. Толокнов, Л.В. Манзюк, мгмсу М.П. Никулин, Т.В. Юрьева, П.В. Кононец, Г.В. Титова
МГМСУ
Реферат: обсуждаются вопросы современного лечения железодефицитных анемий, включая препарат для внутривенного введения — карбоксимальтозат железа, который быстро восстанавливает дефицит железа, не вызывает реакции гиперчувствительности, характерные для препаратов, содержащих декстран, и обеспечивает медленное высвобождение железа, что снижает риск токсических эффектов.
Ключевые слова: железодефицитная анемия, лечение, карбоксимальтозат железа
Анемия — это клинико-гематологический синдром, характеризующийся уменьшением количества эритроцитов и гемоглобина в крови. Снижение содержания гемоглобина до уровня менее 120 г/л рассматривается как анемия [Aapro, 2008]. Самые разнообразные физиологические и патологические процессы могут служить основой развития анемических состояний, в связи с чем анемии в большинстве случаев рассматриваются как симптом, а не основное заболевание. Анемии наблюдаются при многих терапевтических, хирургических, онкологических и других заболеваниях. Различают железодефицитные, сидероахрестические (с избытком железа), В12— и фолиеводефицитные, гемолитические, анемии при костномозговой недостаточности, постгеморрагические, анемии, связанные с перераспределением железа, комбинированные анемии. Однако 80% всех анемий связано с дефицитом железа. Железо в организме человека участвует в регуляции обмена веществ, в процессах переноса кислорода, в тканевом дыхании и оказывает огромное влияние на состояние иммунологической резистентности.
Почти все железо в организме человека входит в состав различных белков и ферментов. Можно выделить две его основные формы: гемовое (входящее в состав гема — составной части гемоглобина и миоглобина) и негемовое. Железо гема мясных продуктов всасывается без участия соляной кислоты. Однако ахилия может в определенной мере способствовать развитию железодефицитной анемии (ЖДА) при наличии значительных потерь железа и высокой потребности в нем.
Всасывание железа осуществляется преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки. Степень всасывания железа зависит от потребности организма в нем. При выраженном дефиците железа всасывание его может происходить и в остальных отделах тонкого кишечника. При уменьшении потребности организма в железе происходит снижение скорости поступления его в плазму крови и увеличивается отложение в энтероцитах в виде ферритина, который элиминируется при физиологическом слущивании эпителиальных клеток кишечника. В крови железо циркулирует в комплексе с плазменным трансферрином. Этот белок синтезируется преимущественно в печени. Трансферрин захватывает железо из энтероцитов, а также из депо в печени и селезенке и переносит его к рецепторам на эритрокариоцитах костного мозга. В норме трансферрин насыщен железом приблизительно на 30%. Комплекс трансферрин-железо взаимодействует со специфическими рецепторами на мембране эритрокариоцитов и ретикулоцитов костного мозга, после чего путем эндоцитоза проникает в клетки, и железо переносится в их митохондрии, где включается в протопорфирин и таким образом участвует в образовании гема. Освободившийся от железа трансферрин неоднократно участвует в переносе железа. Количество железа, которое расходуется на эритропоэз, составляет 25 мг/сут., что значительно превышает возможности всасывания железа в кишечнике. В связи с этим для гемопоэза постоянно используется железо, освобождающееся при распаде эритроцитов в селезенке. Хранение (депонирование) железа осуществляется в депо в составе белков ферритина и гемосидерина.
Наиболее распространенная форма депонирования железа в организме — ферритин. Ферритин представляет собой водорастворимый гликопротеиновый комплекс, в центре которого расположено железо, покрытое белковой оболочкой из апоферритина. Каждая молекула ферритина содержит от 1000 до 3000 атомов железа. Ферритин определяется почти во всех органах и тканях, но наибольшее его количество обнаруживается в макрофагах печени, селезенки, костного мозга, эритроцитах, сыворотке крови, слизистой оболочке тонкой кишки. При нормальном балансе железа в организме устанавливается своеобразное равновесие между содержанием ферритина в плазме и депо (прежде всего в печени и селезенке). Уровень ферритина в крови отражает количество депонированного железа. Ферритин создает запасы железа в организме, которые могут быстро мобилизоваться при повышении потребности тканей в железе.
Другая форма депонирования железа — гемосидерин. Это малорастворимое производное ферритина с более высокой концентрацией железа, состоящее из агрегатов кристаллов железа, не имеющих апоферритиновой оболочки. Гемосидерин накапливается в макрофагах костного мозга, селезенки, купферовских клетках печени.
Общепринято выделять две формы железодефицитных состояний: латентный дефицит железа и ЖДА. Латентный дефицит железа характеризуется уменьшением количества железа в его депо и снижением уровня транспортного железа крови при нормальных показателях гемоглобина и эритроцитов. ЖДА — гипохромная микроцитарная анемия, развивающаяся вследствие дефицита железа в сыворотке крови, костном мозге и депо — печени и селезенке. ЖДА возникает как правило, при хронической потере крови и (или) недостаточном поступлении железа в организм.
По данным Всемирной организации здравоохранения (ВОЗ), дефицит железа в организме человека является одним из наиболее распространенных дефицитов питательных веществ в организме человека во всем мире [Benoist B. et al., 2008; WHO, 2001]. Анемия относится к числу глобальных проблем современного здравоохранения. В мире анемией страдают около 1,6 млрд человек, или 24,8% от общего населения. Частота встречаемости анемии оказалась высокой во всех группах и составила 25,4-47,4% у детей дошкольного и школьного возраста, 41,8% — у беременных женщин, 30,2% — у небеременных женщин репродуктивного возраста, 23,9% — у пожилых людей и 12,7% — у мужчин.
Хотя среди взрослого населения анемия чаще всего развивалась у женщин во время беременности, тем не менее в популяции основную долю пациентов с анемией составляли небеременные женщины репродуктивного возраста (468 млн человек). По крайней мере в половине случаев причиной анемии служит дефицит железа [WHO, 2001], который может быть следствием хронической кровопотери (менструации, оккультные кровотечения при опухолях желудочно-кишечного тракта (ЖКТ), неспецифические и специфические воспалительные заболевания тонкой и толстой кишки, другие причины), недостаточного поступления железа с пищей или нарушения его усвояемости (например, при хроническом алкоголизме), повышенной потребности (детский и подростковый возраст, беременность, послеродовый период), нарушения всасывания.
Дефицит железа бывает не только абсолютным, но и функциональным. Последний возникает, когда адекватное или даже повышенное общее содержание железа в организме оказывается недостаточным у больных при увеличении потребности в железе костного мозга на фоне стимуляции эритропоэза. Важную роль в регуляции обмена железа играет гепсидин — гормон, который образуется в печени, взаимодействует с ферропортином (белком, осуществляющим транспорт железа) и подавляет всасывание железа в кишечнике, а также его высвобождение из депо и макрофагов. Повышение уровня гепсидина, отмечающееся при воспалении, считают основной причиной анемии при хронических заболеваниях. Кроме того, уровень гепсидина повышается при хронической болезни почек, что способствует развитию нефрогенной анемии и резистентности к стимуляторам эритропоэза. При усилении эритропоэза под действием эритропоэтина скорость мобилизации железа из депо становится недостаточной для обеспечения возросших потребностей костного мозга. Пролиферирующим эритробластам необходимо все большее количество железа, что приводит к истощению лабильного пула железа и снижению сывороточного уровня ферритина. Для мобилизации и растворения железа из гемосидерина требуется определенное время. В результате количество поступающего в костный мозг железа уменьшается, что вызывает развитие его функционального и абсолютного дефицита.
В соответствии с Международной классификацией болезней 10-го пересмотра (МКБ-10) учитывают следующие формы анемий, связанных с абсолютным и относительным дефицитом железа:
Классификация, клиника и диагностика ЖДА
Общепризнанной классификации ЖДА не существует. Имеются клиническая классификация ЖДА и классификация по стадиям и тяжести протекания анемии.
Клиническая классификация ЖДА:
1. ЖДА постгеморрагические. Эту группу составляют анемии, развивающиеся на почве повторных небольших кровопотерь, — метроррагии, эпистаксис, гематурия и т.д.
2. ЖДА беременных. Причины возникновения анемий данной группы различны: дисбаланс питания беременных и связанное с этим ухудшение утилизации железа, передача организмом матери значительного его количества развивающемуся плоду, потери железа в период лактации и др.
3. ЖДА, связанные с патологией ЖКТ. К ним относятся анемии, возникающие после гастрэктомии, обширных резекций тонкой кишки, при различных энтеропатиях. По своей сути это ЖДА, обусловленные грубым, тяжелым нарушением функции всасывания железа -проксимальном отделе двенадцатиперстной кишки.
4. ЖДА вторичные, возникающие при инфекционных, воспалительных или опухолевых болезнях. Анемии в этих случаях развиваются вследствие больших потерь железа при гибели клеток опухолей, распаде тканей, микро- и даже макрогеморрагиях, повышении потребности в железе в очагах воспаления.
5. Эссенциальная (идиопатическая) ЖДА, при которой самый тщательный анамнестический и лабораторный поиск не выявляет общеизвестные причины возникновения дефицита железа. У большинства больных имеет место особая форма нарушения всасывания железа.
6. Ювенильная ЖДА — анемия, развивающаяся у молодых девушек (и чрезвычайно редко — у юношей). Данная форма железодефицитного малокровия связана с генетическими или фенотипическими дисгормональными явлениями.
7. ЖДА сложного генеза. В эту группу входят анемии алиментарные.
ЖДА также классифицируют по стадиям и тяжести протекания.
I стадия — потеря железа превышает его поступление, постепенное истощение запасов, всасывание в кишечнике компенсаторно увеличивается;
II стадия — истощение запасов железа (уровень сывороточного железа — ниже 50 мкг/л, насыщение трансферрина — ниже 16%) препятствует нормальному эритропоэзу, эритропоэз начинает падать;
III стадия — развитие анемии легкой степени (100-120 г/л гемоглобина, компенсированной), с незначительным снижением цветового показателя и других индексов насыщения эритроцитов гемоглобином;
IVстадия — выраженная (менее 100 г/л гемоглобина, субкомпенсированная) анемия с явным снижением насыщения эритроцитов гемоглобином;
Vстадия — тяжелая анемия (60-80 г/л гемоглобина) с циркуляторными нарушениями и тканевой гипоксией.
Клиническая картина ЖДА
Клиническими проявлениями ЖДА являются два важнейших синдрома — анемический и сидеропенический.
Анемический синдром обусловлен снижением содержания гемоглобина и уменьшением количества эритроцитов, недостаточным обеспечением тканей кислородом и представлен неспецифическими симптомами. Больные жалуются на общую слабость, повышенную утомляемость, снижение работоспособности, головокружение, шум в ушах, мелькание мушек перед глазами, сердцебиения, одышку при физической нагрузке, появление обморочных состояний. Может появляться снижение умственной работоспособности, ухудшение памяти, сонливость. Субъективные проявления анемического синдрома вначале беспокоят больных при физической нагрузке, а затем и в покое (по мере развития анемии).
При объективном исследовании обнаруживается бледность кожи и видимых слизистых оболочек, нередко — некоторая пастозность в области голеней, стоп, лица. Характерны утренние отеки — «мешки» вокруг глаз. Анемия обусловливает развитие синдрома миокардиодистрофии, который проявляется одышкой, тахикардией, часто аритмией, умеренным расширением границ сердца влево, глухостью тонов сердца, негромким систолическим шумом во всех аускультативных точках. При тяжелой и длительной анемии миокардиодистрофия может привести к выраженной недостаточности кровообращения. ЖДА развивается постепенно, поэтому организм больного адаптируется к низкому уровню гемоглобина, и субъективные проявления анемического синдрома не всегда бывают ярко выражены.
Сидеропенический синдром (синдром гипосидероза) обусловлен тканевым дефицитом железа, что приводит к снижению активности многих ферментов (цитохромоксидаза, пероксидаза, сукцинат-дегидрогеназа и др.). Сидеропенический синдром проявляется многочисленными симптомами, такими как:
Лабораторные данные
Диагностика латентного дефицита железа
Латентный дефицит железа диагностируется на основании следующих признаков:
Диагностика ЖДА
При снижении содержания гемоглобинового железа появляются характерные для ЖДА изменения общего анализа крови:
Наиболее часто используемыми в практике критериями ЖДА являются:
— низкий цветовой показатель;
— гипохромия эритроцитов, микроцитоз;
— снижение уровня сывороточного железа;
— повышение ОЖСС;
— снижение содержания ферритина в сыворотке.
При биохимическом исследовании крови, кроме снижения уровня сывороточного железа и ферритина, выявляются также изменения, обусловленные основным онкологическим или другим заболеванием.
Лечение
В настоящее время существует следующие этапы лечения ЖДА:
Не так давно гемотрансфузия являлась одним из самых распространенных способов коррекции анемии даже легкой степени у больных после операционной кровопотери и кровопотери при других клинических ситуациях (роды, маточные кровотечения, геморрой, опухоли ЖКТ и др.). Считалось, что надо остановить кровотечение и перелить донорскую кровь или эритроцитную массу. Необходимое для переливания количество эритроцитов определяли исходя из объема кровопотери и уровня гемоглобина. Однако ориентация на достижение нормального уровня гемоглобина иногда приводила к переливанию значительных количеств (до 5-6 л) донорской крови, что сопровождалось развитием синдрома массивной трансфузии, рецидивом кровотечения, появлением признаков полиорганной недостаточности с высокой смертностью.
В последнее время получила распространение новая трансфузионная тактика — компонентная гемотерапия, в связи с чем переливание эритроцитной массы заняло доминирующее место в лечении не только хронической, но и острой кровопотери. Однако отсутствие детально разработанных и сформулированных показаний к гемотерапии с учетом индивидуальных особенностей пациентов нередко приводит к необоснованным, неоправданным трансфузиям, которых, к сожалению, еще много. В современных условиях оправдана тенденция к ограничению переливания препаратов крови в связи с ростом числа таких осложнений, как перенос инфекций, формирование ложных групповых антител, подавление эндогенного эритропоэза.
Лечебная программа при ЖДА включает:
При выявлении причины развития ЖДА основное лечение должно быть направлено на ее устранение (оперативное лечение опухоли желудка, кишечника, лечение энтерита, коррекция алиментарной недостаточности и др.). В целом ряде случаев радикальное устранение причины ЖДА не представляется возможным, например, при продолжающихся меноррагиях, наследственных геморрагических диатезах, проявляющихся носовыми кровотечениями, у беременных и в некоторых других ситуациях. В таких случаях основное значение приобретает патогенетическая терапия железосодержащими лекарственными препаратами.
Путь введения препарата больному ЖДА определяется конкретной клинической ситуацией. При проведении купирующей терапии применяются пероральное и парентеральное введение препаратов железа (ПЖ) больному.
Первый путь — пероральный — является наиболее распространенным, хотя и дающим более отсроченные результаты.
Основными принципами лечения ПЖ для приема внутрь являются следующие:
— назначение ПЖ с достаточным содержанием трехвалентного железа;
— нецелесообразность одновременного назначения витаминов группы В (в том числе В12), фолиевой кислоты без специальных показаний;
— избегание назначения ПЖ внутрь при наличии признаков нарушения всасывания в кишечнике;
— достаточная продолжительность насыщающего курса терапии (не менее 3-5 мес.);
— необходимость проведения поддерживающей терапии ПЖ после нормализации показателей гемоглобина в соответствующих ситуациях.
Для адекватного прироста показателей гемоглобина у больных необходимо назначать от 100 до 300 мг трехвалентного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. Индивидуальные колебания в количестве необходимого железа обусловлены степенью его дефицита в организме, истощения запасов, скоростью эритропоэза, всасываемостью, переносимостью и некоторыми другими факторами. С учетом этого при выборе лекарственного ПЖ следует ориентироваться не только на содержание в нем общего количества, но и, главным образом, на количество трехвалентного железа, которое только и всасывается в кишечнике.
Причины неэффективности терапии ПЖ для приема внутрь:
— отсутствие дефицита железа (неправильная трактовка природы гипохромной анемии и ошибочное назначение ПЖ);
— недостаточная дозировка ПЖ (недоучет количества трехвалентного железа в препарате);
— недостаточная длительность лечения ПЖ;
— нарушение всасывания ПЖ, назначаемых внутрь больным с соответствующей патологией;
— одновременный прием препаратов, нарушающих всасывание железа;
— наличие хронических (оккультных) кровопотерь, чаще всего из органов ЖКТ;
— сочетание ЖДА с другими анемическими синдромами (В12-дефицитной, фолиеводефицитной).
Второй путь введения ПЖ — парентеральное введение, которое может быть внутримышечным и внутривенным. Показаниями для применения ПЖ парентерально могут быть следующие клинические ситуации:
— нарушение всасывания при патологии кишечника (энтериты, синдром недостаточности всасывания, резекция тонкого кишечника, резекция желудка по методу Бильрот II с выключением двенадцатиперстной кишки);
— обострение язвенной болезни желудка или двенадцатиперстной кишки;
— непереносимость ПЖ для приема внутрь, не позволяющая дальнейшее продолжение лечения;
— необходимость более быстрого насыщения организма железом, например, у больных ЖДА, которым предстоят оперативные вмешательства (миома матки, геморрой и др.).
В отличие от ПЖ для приема внутрь в инъекционных препаратах железо всегда находится в трехвалентной форме. Лечение больных с ЖДА имеет свои особенности в зависимости от конкретной клинической ситуации с учетом многих факторов, в том числе характера основного заболевания и сопутствующей патологии, возраста больных (дети, пожилые люди), выраженности анемического синдрома, дефицита железа, переносимости ПЖ и др. Общая ориентировочная доза ПЖ для внутримышечного введения, необходимая для коррекции дефицита железа и анемии, может быть рассчитана по формуле:
А = KxF (100 — 6 Х Hb) F = 0,0066,
где А — число ампул, К — масса больного в кг, НЬ — содержание гемоглобина в г %.
При парентеральном введении ПЖ возможны развитие флебитов, инфильтратов, потемнение кожи в местах инъекций, аллергических реакций, в том числе тяжелых (анафилактический шок). Внутримышечные инъекции болезненны, в некоторых случаях они ассоциировались с развитием саркомы ягодичной мышцы [Grasso P, 1973; Greenberg G., 1976]. По мнению некоторых авторов [Auerbach M. et al., 2007], от внутримышечного введения ПЖ следует отказаться.
В последнее время особенно большой интерес вызывают ПЖ для внутривенного введения с целью терапии постгеморрагических анемий. В нескольких работах показано, что внутривенное введение ПЖ более эффективно при сравнении с приемом железа внутрь при тех же показаниях. Помимо этого, внутривенная терапия позволяет избежать возникновения как побочных эффектов со стороны ЖКТ, наблюдающихся при приеме ПЖ внутрь, так и некоторых осложнений, вызываемых при внутримышечном введении ПЖ, однако требует определенного уровня реанимационной службы учреждения, в котором вводятся препараты.
ПЖ для внутривенного введения
Для внутривенного введения в России применяют карбоксимальтозат железа (Феринжект®), сахарат железа (Венофер), глюконат железа и декстран железа, которые представляют собой сферические железоуглеводные коллоиды. Углеводная оболочка придает комплексу стабильность, замедляет высвобождение железа и поддерживает образующиеся формы в коллоидной суспензии.
Внутривенное введение декстрана железа вызывает большое число анафилактических реакций, сопровождающихся летальностью в 13,5% случаев [Faich G. еt Strobos J., 1999], и в настоящее время применяется ограниченно. Применение натриевого комплекса глюконата железа в сукрозе вызывает значительно меньше осложнений и, как правило, не сопровождается смертельными исходами. Однако токсические эффекты, связанные с поступлением свободного железа в организм, существенно ограничивают применение препарата в ежедневной практике терапии ЖДА.
Сахарат железа (III) (Венофер®) является популярным препаратом для лечения синдрома ЖДА. Это связано с безопасностью и высокой переносимостью комплекса трехвалентного железа с сахаратом в отличие от декстрана железа и глюконата железа. Данный препарат одобрен для применения, в том числе и в период беременности. Венофер следует вводить только в учреждениях, располагающих оборудованием для сердечно-легочной реанимации, так как часто могут отмечаться сердечно-сосудистые осложнения в виде гипотонии. Максимальная разовая парентеральная доза сахарата железа (III) составляет 500 мг, предпочтительно развести препарат в 100 мл 0,9% раствора NaCl для введения в форме инфузии. Продолжительность инфузии составляет приблизительно 4,5 ч с использованием внутривенного доступа (следует помнить, что высокая скорость инфузии связана с риском развития гипотензивной реакции). В зависимости от исходных значений уровня гемоглобина внутривенное введение повторяют 1-3 раза/нед. до повышения уровня гемоглобина >105 г/л. Затем пациента можно перевести на прием пероральных ПЖ для поддерживающей терапии. Оснований ожидать возможной передозировки железом не имеется.
Комплекс железа с карбоксимальтозой (Феринжект®) — новый недекстрановый комплекс железа, преимуществом которого является возможность введения высоких доз (до 1000 мг за 1 введение) в короткий промежуток времени (на 1 инфузию требуется 15 мин.). Благодаря этому отсутствует необходимость в дорогостоящих повторных инфузиях небольших доз железа, при этом Феринжект® характеризуется хорошей переносимостью. Феринжект® также одобрен для применения, в том числе и в период беременности. На сегодняшний день (как и в случае сахарата железа) не проводилось масштабных рандомизированных исследований для оценки безопасности применения данного препарата для плода. По этой причине перед назначением любых ПЖ внутривенно необходимо тщательно оценить соотношение пользы и рисков.
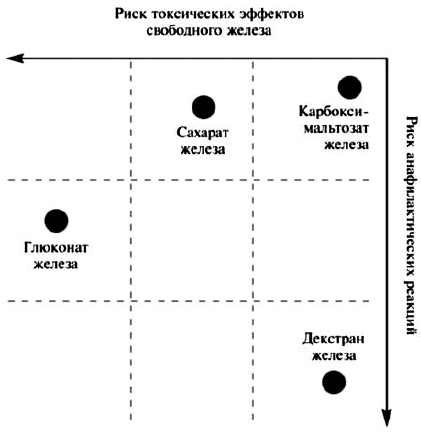
Эффективность и безопасность внутривенного введения ПЖ зависят от их молекулярной массы, стабильности и состава. Комплексы с низкой молекулярной массой, такие как глюконат железа, менее стабильны и быстрее высвобождают в плазму железо, которое в свободном виде может катализировать образование реактивных форм кислорода, вызывающих перекисное окисление липидов и повреждение тканей. Значительная часть дозы подобных препаратов выводится через почки в первые 4 ч после приема и не используется для эритропоэза. Хотя декстран железа обладает высокими молекулярной массой и стабильностью, его недостатком является повышенный риск развития аллергических реакций. Карбоксимальтозат железа сочетает в себе положительные свойства высокомолекулярных комплексов железа, но не вызывает реакции гиперчувствительности, наблюдающиеся при применении препаратов, содержащих декстран, и, в отличие от сахарата и глюконата железа, может вводиться в более высокой дозе [Geisser P., 2009]. Схема оценки риска токсических эффектов и анафилактических реакций препаратов свободного железа для внутривенного введения представлена на рисунке 1 [С.В. Моисеев, 2012].
Рис. 1. Риск токсических эффектов и анафилактических реакций при применении внутривенных препаратов железа
Из рисунка 1 видно, что глюконат железа может вызывать анафилактические реакции и одновременно обладает выраженным токсическим эффектом. Декстран железа, не являясь препаратом с выраженными токсическими эффектами, способен вызывать анафилаксию. Сахарат железа не приводит к развитию анафилактических реакций у больных с ЖДА, но обладает токсическими свойствами. Карбоксимальтозат железа — Феринжект® характеризуется сниженным риском возникновения как токсических эффектов свободного железа, так и анафилактических реакций.
Применение карбоксимальтозата железа позволяет вводить за 1 инфузию до 1000 мг железа (внутривенно капельно в течение 15 мин.), в то время как максимальная доза железа в виде сахарата составляет 500 мг и вводится в течение 4,5 ч, а длительность инфузии декстрана железа достигает 6 ч. Причем в двух последних случаях перед началом инфузии необходимо ввести тестовую дозу препарата. Введение большой дозы железа позволяет сократить необходимое число инфузий и затраты на лечение. Карбоксимальтозат железа отличается не только удобством применения, но и низкой токсичностью, а также отсутствием оксидативного стресса, которые определяются медленным и физиологичным высвобождением железа из стабильного комплекса с углеводом, по структуре сходного с ферритином.
Также, Феринжект® вводят внутривенно в виде болюса (максимальная доза — 4 мл, или 200 мг железа, не более 3 раз/нед.) или капельно (максимальная доза -20 мл, или 1000 мг железа, не чаще 1 раза/нед.). Перед началом лечения необходимо рассчитать оптимальную кумулятивную дозу препарата, которую не следует превышать. Кумулятивную дозу, необходимую для восстановления уровня гемоглобина в крови и восполнения запасов железа в организме, вычисляют по формуле Ганзони:
Кумулятивный дефицит железа (мг) = масса тела (кг) х (целевой НЬ — фактический НЬ) (г/дл) х 2,4 + содержание депонированного железа (мг), где целевой уровень гемоглобина (НЬ) у человека с массой тела или = 35 кг 15 г/дл (9,3 ммоль/л), соответственно, депо железа у человека с массой тела >35 кг и = 35 кг = 500 мг и ЛИТЕРАТУРА
1. Worldwide prevalence of anaemia 1993-2005. WHO global database of anaemia. Edited by de Benoist В. et al. World Health Organisation. 2008.
2. Iron deficiency anaemia: assessment, prevention, and control. A guide for programme managers. Geneva, WHO, 2001 (WH0/NHD/01.3).
3. Grasso P. Sarcoma after intramuscular iron injection // Br. Med. J. 1973. Vol. 2. Р. 667.
4. Greenberg G. Sarcoma after intramuscular iron injection // Br. Med. J. 1976. Vol. 1. Р. 1550-1550.
5. Auerbach M, Ballard H., Glaspy J. et al. Clinical update: intravenous iron for anaemia // Lancet. 2007. Vol. 369. Р. 1502-1504.
6. Geisser P. The pharmacology and safety profile of ferric carboxymaltose (Ferinjecf): structure/reactivity relationships of iron preparations // Port.. J. Nephrol. Hypert. 2009. Vol. 23 (1). Р. 11-16.
7. Моисеев С.В. Железа карбоксимальтозат (Феринжект) — новый внутривенный препарат для лечения железодефицитной анемии // Клиническая фармакология и терапия. 2012. № 21 (2). С. 2-7.
8. Faich G., Strobos J. //Am. J. Kidney Dis. 1999. Vol. 33. No. 3. P. 464-470.
9. Beshara S., Sorensen J., Lubberink M. et al. Pharmacokinetics and red cell utilization of 52Fe/59Fe-labelled iron polymaltose in anaemic patients using positron emission tomography// Br. J. Haematol. 2003. Vol. 120. Р. 853-859.
источник
Железодефицитная анемия – клинико-гематологический синдром, обусловленный недостатком железа в организме человека, что влечет нарушение нормального синтеза гемоглобина и гипоксию тканей.
Патология широко распространена. По статистическим данным, у 8-10% женщин детородного возраста диагностируется железодефицитная анемия, а у 30% женщин – латентный дефицит железа. В раннем детском возрасте признаки железодефицитной анемии выявляются у каждого второго ребенка. В структуре всех анемий на долю железодефицитной приходится 90%.
В основе развития железодефицитной анемии лежит отрицательный баланс обмена железа. К этому могут приводить разные факторы, но чаще всего причиной дефицита железа становится хроническая кровопотеря:
- кровотечения из геморроидальных узлов или анальных трещин;
- дисфункциональные маточные кровотечения;
- обильные менструации;
- желудочно-кишечные кровотечения (из эрозий и язв слизистой оболочки желудка или кишечника).
Другие причины кровопотери:
- гельминтозы;
- гемосидероз легких;
- геморрагические диатезы (болезнь Виллебранда, гемофилия);
- гемоглобинурия;
- обширные травмы и операции;
- частая сдача крови (донорство).
Нередко железодефицитная анемия развивается и у пациентов с хронической почечной недостаточностью, находящихся на программном гемодиализе.
При железодефицитных состояниях происходит снижение активности IgA; в результате у пациентов зачастую возникают кишечные и респираторные инфекции.
Недостаток железа в организме также может сформироваться в результате недостаточного поступления его из пищи по следующим причинам:
- низкий уровень жизни;
- вегетарианство;
- соблюдение диеты, ограничивающей употребление мясных продуктов;
- анорексия;
- искусственное вскармливание детей грудного возраста, особенно при позднем введении прикорма.
Ряд заболеваний и патологических состояний органов пищеварительной системы может приводить к нарушению всасывания железа и развитию железодефицитной анемии:
- гастерэктомия;
- состояние после резекции тонкой кишки;
- синдром мальабсорбции;
- хронический энтерит;
- гипоацидный гастрит;
- кишечные инфекции.
Железодефицитная анемия развивается и у пациентов, страдающих хроническими гепатитами или циррозом печени. В данном случае нарушается транспорт железа из депо.
Железодефицитная анемия может также появиться на фоне повышенной потребности в железе (в период полового созревания, беременности либо лактации) или при значительных потерях этого элемента (при онкологических, инфекционных заболеваниях).
В зависимости от причины железодефицитные анемии делятся следующим образом:
- алиментарные;
- постгеморрагические;
- связанные с нарушением транспорта железа, недостаточностью его резорбции или повышенным расходом;
- обусловленные врожденным (исходным) дефицитом железа.
По степени выраженности лабораторных и клинических признаков железодефицитные анемии бывают:
- легкими (гемоглобин выше 90 г/л);
- средней тяжести (гемоглобин от 70 до 90 г/л);
- тяжелыми (гемоглобин менее 70 г/л).
Железодефицитная анемия легкой степени в большинстве случаев протекает без-каких либо клинических проявлений или с минимальной их выраженностью. Тяжелая форма сопровождается развитием гематологического, сидеропенического и циркуляторно-гипоксического синдромов.
В течении железодефицитной анемии выделяют несколько стадий:
- Предлатентный железодефицит – истощается депонированное железо, гемоглобиновые и транспортные запасы сохранены.
- Латентный железодефицит – происходит снижение запасов содержащегося в плазме крови транспортного железа.
- Собственно железодефицитная анемия – истощение всех метаболических запасов железа (эритроцитарного, транспортного и депонированного).
В клинической картине железодефицитной анемии выделяют синдромы:
- циркуляторно-гипоксический;
- сидеропенический;
- астеновегетативный.
Возникающие на фоне железодефицитной анемии циркуляторно-гипоксические нарушения ухудшают течение сопутствующих заболеваний сердечно-сосудистой и дыхательных систем.
Развитие циркуляторно-гипоксического синдрома обусловлено нарушением синтеза гемоглобина, в результате чего страдает транспорт кислорода и развивается тканевая гипоксия. Клинически это проявляется:
- общей слабостью;
- сонливостью;
- головокружениями;
- шумом в ушах;
- преходящими обмороками;
- учащенным сердцебиением;
- повышенной чувствительностью к низкой температуре;
- одышкой, возникающей при физических нагрузках, а при тяжелой анемии – и в состоянии покоя.
Механизм развития сидеропенического синдрома связан с дефицитом железосодержащих тканевых ферментов (цитохромов, пероксидазы, каталазы). Недостаток названных ферментов становится причиной наблюдаемых на фоне железодефицитной анемии трофических расстройств со стороны слизистых оболочек и кожных покровов. Признаки сидеропенического синдрома:
- сухость кожи;
- деформация, повышенная ломкость и поперечная исчерченность ногтей;
- выпадение волос;
- атрофический гастрит;
- дисфагия;
- ангулярный стоматит;
- глоссит;
- искажения вкуса (желание употреблять в пищу несъедобные предметы, например глину или зубной порошок);
- дизурические расстройства;
- диспепсия;
- мышечная слабость.
Астеновегетативный синдром характеризуется эмоциональной лабильностью, повышенной раздражительностью, ухудшением памяти, снижением работоспособности.
Клиническая картина железодефицитной анемии у детей неспецифична, преобладает один из следующих синдромов:
- Астеновегетативный. Связан с кислородным голоданием тканей нервной системы. Проявляется снижением мышечного тонуса и задержкой психомоторного развития ребенка. При тяжелой степени железодефицитной анемии и отсутствии необходимой терапии возможна интеллектуальная недостаточность. К другим проявлениям астеновегетативного синдрома относят энурез, обморочные состояния, головокружение, раздражительность и плаксивость.
- Эпителиальный. Характеризуется изменениями со стороны кожи и ее придатков. Кожные покровы становятся сухими, в области коленей и локтей развивается гиперкератоз, волосы теряют блеск и активно выпадают. Часто развиваются хейлит, глоссит, ангулярный стоматит.
- Диспепсический. Снижается аппетит вплоть до полного отказа от еды, наблюдаются неустойчивость стула (поносы, чередующиеся с запорами), вздутие живота, дисфагия.
- Сердечно-сосудистый. Развивается на фоне тяжелой железодефицитной анемии и проявляется одышкой, снижением артериального давления, тахикардией, шумами в сердце и дистрофическими изменениями в миокарде.
- Синдром иммунодефицита. Характеризуется немотивированным повышением температуры до субфебрильных значений. Дети подвержены респираторным кишечным инфекциям с тяжелым и (или) затяжным течением.
- Гепатолиенальный. Наблюдается на фоне выраженной железодефицитной анемии, особенно сочетающейся с другими видами анемий или рахитом. Проявляется увеличением размеров печени и селезенки.
В раннем детском возрасте признаки железодефицитной анемии выявляются у каждого второго ребенка.
Диагностика состояния, а также определение степени его тяжести осуществляются по результатам лабораторных исследований. Для железодефицитной анемии характерны следующие изменения:
- снижение содержания гемоглобина в крови (норма для женщин – 120–140 г/л, для мужчин – 130–150 г/л);
- пойкилоцитоз (изменение формы эритроцитов);
- микроцитоз (наличие в крови аномально маленьких по своим размерам эритроцитов);
- гипохромия (цветовой показатель – менее 0,8);
- снижение концентрации сывороточного железа (норма для женщин – 8,95–30,43 мкмоль/л, для мужчин – 11,64–30,43 мкмоль/л);
- уменьшение концентрации ферритина (норма для женщин – 22–180 мкг/л, для мужчин – 30–310 мкг/л);
- уменьшение насыщения трансферрина железом (норма – 30%).
Для эффективного лечения железодефицитной анемии важно установить причину, ее вызвавшую. С целью обнаружения источника хронической кровопотери показано проведение:
- ФЭГДС;
- рентгенографии желудка с контрастированием;
- колоноскопии;
- ирригоскопии;
- ультразвукового исследования органов малого таза;
- исследования кала на скрытую кровь.
По статистическим данным, у 8-10% женщин детородного возраста диагностируется железодефицитная анемия, а у 30% женщин – латентный дефицит железа.
В сложных диагностических случаях выполняют пункцию красного костного мозга с последующим гистологическим и цитологическим исследованием полученного пунктата. Значительное снижение в нем сидеробластов свидетельствует о наличии железодефицитной анемии.
Дифференциальная диагностика проводится с другими видами гипохромных анемий (талассемией, сидеробластной анемией).
Принципы терапии железодефицитной анемии:
- устранение источника хронической кровопотери;
- коррекция рациона;
- восполнение недостатка железа.
Важную роль играет диетотерапия. В рацион включают язык, печень, мясо кролика, баранину, говядину, телятину – продукты, богатые гемовым железом. Для улучшения всасывания железа из желудочно-кишечного тракта необходимы аскорбиновая, янтарная и лимонная кислоты, которые в большом количестве содержатся в свежих фруктах и ягодах. Исключают шоколад, молоко, соевый протеин, чай, кофе, поскольку они ингибируют всасывание железа.
Но только лишь диетой восполнить уже образовавшийся дефицит железа невозможно. Пациенты с железодефицитной анемией проходят заместительную терапию ферропрепаратами длительным курсом (не менее 2-2,5 месяцев).
При тяжелой форме железодефицитной анемии и выраженном циркуляторно-гипоксическом синдроме возникают показания к проведению гемотрансфузии.
Возникающие на фоне железодефицитной анемии циркуляторно-гипоксические нарушения ухудшают течение сопутствующих заболеваний сердечно-сосудистой и дыхательных систем.
При железодефицитных состояниях происходит снижение активности IgA; в результате у пациентов зачастую возникают кишечные и респираторные инфекции.
На фоне длительного течения тяжелой формы железодефицитной анемии у больных может развиться миокардиодистрофия.
Прогноз благоприятный при условии своевременной коррекции дефицита железа и устранения причины развития анемии.
Профилактика железодефицитной анемии включает:
- полноценное рациональное питание;
- ежегодный контроль содержания гемоглобина в крови;
- своевременное устранение источников хронической кровопотери;
- профилактический прием препаратов железа лицами из группы риска.
Видео с YouTube по теме статьи:
Образование: окончила Ташкентский государственный медицинский институт по специальности лечебное дело в 1991 году. Неоднократно проходила курсы повышения квалификации.
Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
источник