Анализу крови отводят основную роль в постановке диагноза малокровия. Лабораторные исследования помогают определить тип и характер анемии, её тяжесть. Даже при отсутствии других симптомов, присущих анемии, результат обследования крови покажет отклонение от нормы.
Лабораторные обследования проводят, чтобы выдать точное заключение, выявить тип малокровия, провести адекватную терапию. Назначают анализы:
- общий (клинический) анализ крови;
- биохимический анализ.
Результаты лабораторных обследований дают ясное представление об этих основных значениях.
Общий анализ крови для диагностики анемии берут из пальца. Процедуру желательно проводить утром, натощак.
Исследуя данные ОАК, устанавливают следующее:
- общее количество эритроцитов в крови;
- соотношение объёма и диаметра эритроцитов, их соответствие норме;
- число ретикулоцитов (клеток-предшественников);
- уровень гемоглобина в эритроците (цветовой показатель);
- соотношение видов лейкоцитов, тромбоцитов;
- определение гематокритного числа.
Значения этих показателей помогают установить причину понижения гемоглобина в крови.
Биохимическое исследование проводят, если на гемограмме выявлено пониженное значение гемоглобина. С его помощью устанавливают:
- количественное значение железа в сыворотке;
- уровень трансферрина;
- связывающую способность сыворотки;
- количество ферритина.
Эти данные дают наиболее полную картину характера анемии и особенности её протекания.
Кровь для биохимического исследования берут из вены.
На начальном этапе для определения наличия какой-либо анемии сравнивают основные показатели анализа крови с референсными значениями. Основные значения исследуемых величин представлены в таблице:
| Пациенты | Гемоглобин, г/л (HB) | Эритроциты, млн/мкл (RBC) | Цветовой показатель | Ретикулоциты, % (RTC) |
| Мужчины | 130 – 160 | 3,8 – 5,6 | 0,83 – 1,05 | 5,1 – 18,0 |
| Женщины | 120 – 140 | 3,7 – 5,3 | 5,0 – 17,0 | |
| Подростки (14-18 лет) | 125 – 145 | 3,7 – 5,2 | 0,9 – 1,0 | 4,8 – 18,0 |
| Дети (10-14) | 120 – 140 | 3,8 – 5,0 | 4,8 – 18,0 | |
| Дети (5-10) | 110 – 135 | 3,9 – 5,1 | 4,8 – 18,0 |
Это основное красящее вещество, входящее в состав эритроцитов, которое отвечает за перенос кислорода. Пониженная составляющая гемоглобина указывает на наличие малокровия различной этиологии.
На основании показателей количественного отклонения гемоглобина от референсных значений выявляют характер протекания анемии по степени интенсивности:
- лёгкая – содержание гемоглобина от 110-90 г/л;
- средняя – от 90-70 г/л;
- тяжёлая – менее 70 г/л.
Определить характер и возможные причины, вызывающие анемию, помогают и другие показатели.
Красные безъядерные кровяные клетки, которые имеют форму диска. Благодаря двояковыпуклой форме эритроциты могут деформироваться, приспосабливаясь к узким капиллярам. Эритроциты доставляют кислород из лёгких ко всем тканям и забирают углекислоту. Низкий уровень этих клеток характеризует любой тип анемии.
Эти клетки представляют собой недозрелую форму эритроцитов. Выявляются в костном мозге, в некотором количестве содержатся в периферической крови. Увеличение доли ретикулоцитов говорит о разрушении эритроцитов, что указывает на прогрессирование анемии. Расчёт ведётся в % отношении от всех эритроцитов. Значение ретикулоцитов помогает оценить степень тяжести заболевания.
Этот показатель нужен для определения степени насыщения гемоглобином кровяных клеток (эритроцитов). Если он ниже нормы, это может указывать на наличие анемии. По значению ЦП различают:
- гипохромную анемию (менее 0,8);
- нормохромную анемию (0,8-1,05);
- геперхромную анемию (свыше 1,05).
Эти данные помогают выявить тип заболевания. Высокий цветовой показатель указывает на фолиеводефицитную и В12 анемию. Нормальное значение ЦП бывает при острой постгеморрагической анемии. Сниженный показатель свидетельствует о дефиците железа.
Для более точной диагностики видов анемии определяют другие неспецифические показатели анализов крови.
МCV – средний объём эритроцита. Выявленные значения свидетельствуют о наличии таких анемий:
| Тип | Значение MCV | Вид анемии |
| Нормоцитарная | от 80-100 фл | Гемолитические |
| Микроцитарная | менее 80 фл | Железодефицитные |
| Макроцитарная | более 100 фл | Фолиево и В12 дефицитные |
MCH – уровень гемоглобина в одном эритроците, в среднем. Это значение отражает синтез гемоглобина в кровяных клетках. Он схож с цветовым показателем. Диапазоны нормы таковы:
- женщины – от 27-34 нг;
- мужчины – 27-35 нг;
- дети (10-18 лет) – 26-34 нг.
Показатели в пределах нормы определяют нормохромный тип, который может встречаться при апластической и гемолитической анемии. Такие значения наблюдаются при большой кровопотере.
Уменьшение объёма (микроцитоз) обусловлено гипохромным типом, встречающимся у железодефицитной анемии. Превышение среднего показателя уровня гемоглобина в эритроците свидетельствует о наличии мегобластной и гипопластической анемии.
MCHC – средняя степень насыщения гемоглобина в одной клетке эритроцита (концентрация). Значение этого показателя может указывать:
- на дефицит железа, если уровень ниже нормы (меньше 29 г/дл);
- на микросфероцитарную анемию, если значение повышено (больше 37 г/дл).
Для выявления степени тяжести анемии используют и такой показатель, как гематокрит. Это значение указывает на соотношение объёма плазмы и эритроцитов. Это значение меняется в процентном соотношении. Снижение до 20-15% указывает на тяжёлую степень анемии.
Для более точной диагностики анемии, особенно при подозрении на дефицит железа, часто проводят биохимический анализ крови, который определяет важные характеристики:
Главная роль этого белкового комплекса – хранение и высвобождение железа для клеток. Определяя уровень этого белка, можно косвенно измерить количество железа, которое хранится в организме. Норма содержания ферритина составляет 20 – 250 мкг/л (мужчины), 10 – 120 мкг/л (женщины). Низкие показатели указывают на железодефицитную анемию.
Назначение этого белка – перенос железа в нужное место. Нарушение уровня трансферрина приводит к нехватке элемента. Количество поступающего железа может быть при этом достаточным. Этот показатель выявляет активность сыворотки к связыванию железа. Нормальный уровень белка – 2,0-4,0 г/л. Повышение количества может указывать на железодефицитное малокровие. Сниженный уровень характерен при апластической и гипопластической анемии.
Для исследования на трансферрин необходимо специальное оборудование и определённые тесты, которые не всегда доступны.
В определённых случаях выявляют железосвязывающую способность сыворотки, которая показывает способность крови связывать железо. При диагностике анемии определяют латентное значение железосвязывающего показателя. Норма – 20-63 мкмоль/л.
После проведения общего анализа и выявления скорости обмена железа могут назначать другие обследования:
- анализы на маркеры воспаления, если выявлены симптомы аутоиммунных или ревматических заболеваний;
- установление уровня содержания фолитов и витамина В12.
Проводимые виды исследования помогают выявить этиологию наиболее распространённых типов малокровия.
В ряде случаев могут назначаться дополнительные обследования и анализы крови для более точной диагностики анемии:
- микроскопия мазка крови;
- УЗИ внутренних органов;
- костномозговая пункция (миелограмма);
- обследование кишечника и желудка (эндоскопия);
- анализ мочи;
- электрокардиограмма.
Эти методы диагностики применяют, когда трудно установить точное происхождение анемии.
Для установления конкретного вида заболевания предполагается выявление характерных показателей:
- количество фолиевой кислоты, которая находится в эритроцитах: проводят, если есть показания, биопсию костного мозга (подозрение на фолиеводефицитную анемию);
- количественное значение витамина В12: если не определяется уровень витамина, назначают аспирационную биопсию (подозрение на В12-дефицитную анемию);
- показатель уровня наличия билирубина в моче и сыворотке: выявляют стойкость эритроцитов, проводят пробу Кумбса (наличие гемолитической анемии).
Если есть подозрение на гипопластическое малокровие, которое характерно сбоем кроветворения костного мозга, определяют процесс и степень разрушения эритроцитов. Проводят исследование на наличие билирубина в кале и моче. Также назначают УЗИ печени и селезёнки для определения их размера.
При определении анемии, вызванной заболеваниями хронического характера, наряду с определением стандартных лабораторных показателей, проводят определение содержания ферритина вместе с выявлением уровня С-реактивного белка. Этот элемент указывает на стадию воспаления.
Проходить лабораторное обследование при подозрении на анемию необходимо. Данные анализов крови помогут установить точный диагноз, определить тип и стадию заболевания. Это даст возможность подобрать необходимое лечение, которое будет эффективным.
источник
Сравнение и обобщение данных по проведению общего анализа крови при диагностике анемий, на примере клинико-диагностических лабораторий г. Пензы. Выявление отклонений от нормальных значений общего анализа крови при диагностике различных видов анемий.
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Тема: Мониторинг данных общего анализа крови при диагностике анемий
1. Общие сведения об анемиях
1.2 Классификация видов анемий
2. Мониторинг данных общего анализа крови при различных видах анемий
2.1 Лабораторная диагностика при анемиях
2.2 Значение общего анализа крови при анемиях различной этиологии
В настоящее время анемия стала насущной проблемой для большого числа людей по всему миру. Группой риска развития анемии являются дети до 1-го года (70-80%), девочки в период полового созревания (14%), беременные женщины (30-80%). В России до 30% населения имеют признаки анемий. Однако с этим аномальным состоянием можно и нужно бороться. Правильная диагностика, включающая выполнение различных лабораторных исследований, позволяет своевременно выявить эту болезнь и выбрать подходящий метод лечения.
Таким образом, анемия считается самым распространенным патологическим состоянием и диагностируется при исследовании крови Основным признаком анемий является уменьшение концентрации гемоглобина и в подавляющем большинстве случаев числа эритроцитов в единице объема крови.
Проблема: Как изменяются значения общего клинического анализа крови при диагностике различных видов анемий?
Объект исследования: Общий анализ крови — как основное исследование для постановки диагноза анемия.
Предмет исследования: Выявление отклонений, от нормальных значений общего анализа крови при диагностике различных видов анемий.
Цель работы: Сравнение и обобщение данных по проведению общего анализа крови при диагностике анемий, на примере клинико-диагностических лабораторий г. Пензы.
· Изучить специальную литературу о причинах возникновения и клинической картине при анемиях.
· Подобрать и проанализировать научную литературу по выполнению общего анализа крови ручными методами и с помощью гематологических анализаторов.
· Обработать и проанализировать статистические данные по количеству проведенных анализов крови и диагностике анемий.
· Методы исследования: анализ, описание, сравнение.
· База исследования: Клинико — диагностические лаборатории г. Пензы.
анализ кровь анемия диагностика
1. Общие сведения об анемиях
Анемия или малокровие — уменьшение в крови общего количества гемоглобина, которое, за исключением острых кровопотерь, характеризуется снижением уровня гемоглобина в единице объема крови (См.: приложение 1). Анемия возникает во все периоды жизни человека не только при различных заболеваниях, но и при некоторых физиологических состояниях, например, в период усиленного роста, при беременности, лактации. Большое значение имеет проблема анемий у детей раннего возраста, так как анемия в этом возрасте может привести к нарушениям физического развития и обмена железа. Развитие анемии может быть связано с пубертатным и климактерическим периодом, заболеваниями пищеварительного тракта, печени, почек, гормональными нарушениями, характером питания, аутоиммунными состояниями, нарушением всасывания, оперативным вмешательством и другими факторами влияющие на организм. Нередко анемия является симптомом многих внутренних заболеваний, онкологических болезней и инфекционных.
Общими симптомами для всех форм анемий, возникновение которых связано с гипоксией, являются одышка, сердцебиение, а также жалобы на головокружение, головные боли шум в ушах, бледность кожных покровов и слизистых оболочек, неприятные ощущения в области сердца, резкую общую слабость и быструю утомляемость. В легких случаях анемии общие симптомы могут отсутствовать, так как компенсаторные механизмы обеспечивают физиологическую потребность тканей в кислороде. При тяжелых формах анемии в крови появляются патологические формы эритроцитов. Иногда анемия является симптомом труднодиагностируемого заболевания, которое длительное время не обнаруживается. В ряде случаев анемия усугубляет течение главного заболевания. При длительной анемии возможны нарушения функций различных паренхиматозных органов, развивающиеся в результате дистрофических процессов, обусловленных хронической гипоксией. Однако чаще всего изменения функций различных органов и систем представляют собой признаки основного заболевания, симптомом которого является малокровие.
Большое значение при обнаружении анемии имеет лабораторное исследование крови — определение концентрации гемоглобина, количества эритроцитов, величины и насыщенности их гемоглобином. Во всех случаях анемии необходимо полное морфологическое исследование крови с определением количества ретикулоцитов, тромбоцитов, лейкоцитов и лейкограммы. В случаях, когда на основании результатов клинических и лабораторных исследований нельзя установить диагноз, необходимо провести морфологическое исследование пунктата костного мозга, которое позволяет судить о функциональном состоянии кроветворной системы и установить диагноз. Для уточнения характера анемии необходимы исследования мочи и крови, определение СОЭ, содержания свободного гемоглобина в сыворотке крови, количества билирубина в крови, концентрации уробилиногена и желчных пигментов в моче, серологические исследования для определения содержания антиэритроцитарных факторов (антител), сывороточного железа, железосвязывающей способности плазмы и другие исследования.
Точное определение типа и причины анемии является главным основанием для выбора правильного лечения. Сравнительная легкость диагностики анемии часто приводит к необоснованному применению «антианемических» средств (препаратов железа, пиридоксина, цианокобаламина, переливания крови) без выяснения причины и патогенеза анемии.
Такое лечение, как правило, малоэффективно, а в большем случае приносит вред больному. Несвоевременная диагностика анемии или стирание ее клинических проявлений вследствие лечения без установления причины анемии могут привести к позднему распознаванию ряда заболеваний, в начальном периоде которых анемия является единственным диагностируемым симптомом (некоторые коллагенозы, злокачественные опухоли, хронические воспалительные процессы и другие заболевания); поэтому, в случае выявления анемического состояния необходимо придерживаться следующего правила: вначале нужно установить характер и причину анемии и только после этого назначить соответствующее лечение.
Таким образом, учитывая сказанное выше не трудно предположить, что анемия является одним из более распространенных синдромов на сегодняшний день.
В основу классификаций анемий положен патогенетический принцип.
По патогенезу различают следующие виды анемий:
Анемии вследствие кровопотери (постгеморрагические)
1) Острая постгеморрагическая анемия (гемолитическая гипоксия);
2) Хроническая постгеморрагическая анемия;
Анемии вследствие нарушения кровообразования
1) Железодефицитная анемия (ЖДА);
2) В12 — и фолиеводефицитные анемии;
3) Гипопролиферативные анемии;
4) Апластическая анемия (АА);
5) Парциальная красноклеточная аплазия (ПКА);
6) Анемия у онкологических больных;
Анемии вследствие усиленного кроверазрушения (гемолитические)
Анемии вследствие кровопотери (постгеморрагические)
Острая постгеморрагическая анемия (гемолитическая гипоксия).
Острая постгеморрагическая анемия — состояние, которое развивается в результате быстрой потери значительного объема крови (См.: приложение 2). Независимо от патогенеза заболевания при анемии в организме нарушаются окислительные процессы и возникает гипоксия. Степень анемии зависит от быстроты и количества кровопотери, степени адаптации организма к новым условиям существования.
Причиной острой кровопотери могут быть нарушение целостности стенок сосуда вследствие его ранения, поражения патологическим процессом при различных заболеваниях (язва желудка и кишечника, опухоль, туберкулез, инфаркт легкого, варикозное расширение вен голеней, патологические роды), изменение проницаемости капилляров (геморрагические диатезы) или нарушение в системе гемостаза (гемофилия). Последствия этих изменений независимо от причин, вызвавших его, однотипны.
Ведущие симптомы обширного кровотечения — остро возникающий дефицит объема циркулирующей крови (ОЦК) и нарушение гомеостаза. В ответ на развитие дефицита ОЦК включаются адаптационные механизмы, направленные на его компенсацию.
В первый момент после кровопотери наблюдаются признаки коллапса: резкая слабость, падение кровяного давления, бледность, головокружение, обморочное состояние, тахикардия, холодный пот, рвота, цианоз, судороги. В случае благоприятного исхода появляются собственно анемические симптомы, вызванные снижением дыхательной функции крови и развитием кислородного голодания.
Нормальная реакция организма на кровопотерю характеризуется активацией гемопоэза. В ответ на гипоксию увеличивается синтез и секреция почками ЭПО, что приводит к усилению эритропоэза и повышению эритропоэтической функции костного мозга. Резко увеличивается количество эритробластов. При больших кровопотерях желтый костный мозг трубчатых костей может временно замещаться активным — красным, появляются очаги внекостно-мозгового кроветворения.
2) Хроническая постгеморрагическая анемия.
Хроническая постгеморрагическая анемия развивается в результате обильных однократных, но длительно повторяющихся кровотечений. Является частым вариантом железодефицитной анемии. Связанно с нарастающим дефицитом железа в организме вследствие длительных кровотечений, причиной которых являются кровотечение из желудочно-кишечного тракта (язва, рак, геморрой), почечных, маточных. Даже оккультные кровопотери при язвенных или неопластических процессах в желудочно-кишечном тракте или ничтожные геморроидальные кровотечения, повторяющиеся изо дня в день, способны привести к тяжелому малокровию.
Зачастую источник кровотечения настолько незначителен, что он остается нераспознанным. Чтобы представить себе, каким образом малые кровопотери могут способствовать развитию значительной анемии, достаточно привести следующие данные: суточное количество алиментарного железа, необходимое для поддержания баланса гемоглобина в организме, составляет для взрослого человека около 5 мг. Это количество железа содержится в 10 мл крови.
Следовательно, ежедневная потеря при дефекации 2—3 чайных ложек крови не только лишает организм его суточной потребности в железе, но с течением времени приводит к значительному истощению «железного фонда» организма, в результате чего развивается тяжелая железодефицитная анемия. Жалобы больных сводятся в основном к резкой слабости, частым головокружениям и соответствуют обычно степени анемии. Иногда, однако, поражает несоответствие между субъективным состоянием больного и его внешним видом.
У больных отмечается слабость, быстрая утомляемость, бледность кожи и видимых слизистых, зон или шум в ушах, головокружение, отдышка, сердцебиение даже при незначительной физической нагрузке, отмечаются анемические сердечные шумы, чаще всего выслушивается систолический шум на верхушке, проводящийся на легочную артерию; на яремных венах отмечается «шум волчка». Как правило, больные анемией не истощены, если только истощение не вызвано основным заболеванием (рак желудка или кишечника).
Лечение включает наиболее ранее выявление и устранение причины кровопотери, а также восполнение дефицита железа и содержания железа в сыворотке крови. В тяжелых случаях показано под контролем сатурации гемоглобина переливание эритроцитной массы.
Анемии вследствие нарушения кровообразования
1) Железодефицитная анемия (ЖДА)
Железодефицитные анемии (ЖДА) — широко распространенные заболевания, при которых снижается содержание железа в сыворотке крови, костном мозге и других депо. В результате этого нарушается образование гемоглобина, а в дальнейшем и эритроцитов, возникают гипохромная анемия и трофические расстройства в тканях (См.: приложение 3).
По данным Всемирной организации здравоохранения (ВОЗ), железодефицитные анемии встречаются у 1,7 млрд населения земного шара, а людей со скрытым дефицитом железа, когда уровень гемоглобина остается еще нормальным, а запасы железа снижены — в 2 раза больше.
Группами риска развития анемии являются женщины детородного возраста, беременные и кормящие грудью, дети в период быстрого роста, доноры. Даже в развитых странах Европы от 7 до 14 % женщин репродуктивного возраста страдают железодефицитным малокровием, В странах с более низким уровнем жизни частота анемии достигает 50-60 %. В России до 30 % населения имеет признаки железодефицитной анемии.
Таким образом, дефицит железа — это одно из наиболее распространенных патологических состояний, которое встречается у 25-30% населения планеты, в связи, с чем проблема профилактики и лечения этого состояния имеет большое социальное значение и выходит за рамки одной только медицинской компетенции.
Основными причинами дефицита железа в организме являются:
a) кровопотери (кровотечения из желудочно-кишечного тракта и носовые, длительное донорство, массивные операционные кровопотери)
b) нарушение всасывания железа, связанное с заболеваниями желудочно-кишечного тракта;
c) повышенная потребность в железе (в период роста организма, беременности, родов, лактации);
d) недостаточное поступление железа в организм (вегетарианство, голодание).
1) снижение работоспособности и ухудшение качества жизни;
2) развитие дистрофических изменений внутренних органов;
3) развитие осложнений во время беременности и в родах;
4) задержку развития и роста детей;
5) снижение интеллекта и нарушение поведенческих реакций.
Клинические проявления дефицита железа в организме очень многообразны и зависят от ряда факторов. При недостатке железа в организме анемия проявляется не сразу. Ей предшествует длительный период латентного (скрытого) дефицита железа с явными признаками снижения запасов железа в организме без выраженных симптомов анемии.
В случае выраженного снижения количества гемоглобина на первый план в клинике выступают симптомы, связанные с недостаточным обеспечением тканей кислородом: головокружение, головная боль, слабость, чувство сердцебиения, затруднение дыхания (одышка), обмороки. Частота этих симптомов неодинакова. В большинстве случаев больные жалуются на головную боль, возникающую, как правило, в душном помещении. Однако эти симптомы присущи не только железодефицитной, они бывают и при других формах анемий.
Дефициту железа присущи так называемые сидеропенические признаки: выраженные изменения кожи, ногтей, волос, которые не встречаются при других видах малокровия, мышечная слабость, не соответствующая глубине анемии, извращения вкуса. У больных часто отмечаются сухость и трещины кожи на руках и ногах. Трещины в углах рта при дефиците железа бывают у 10-15% взрослых людей. При тяжелых формах железодефицитной анемии выпуклые ногти становятся уплощенными и даже вогнутыми, резко истончаются, ломаются. Часто описывают койлонихию (ложкообразные ногти) как симптом дефицита железа у взрослых и детей. Глоссит, выражающийся в появлении боли и покраснении языка, атрофии его сосочков, также нередко встречается при железодефицитной анемии. Бывает дисфагия (нарушение глотания), которую ошибочно расценивают как опухоль пищевода. Характерный признак дефицита железа — мышечная слабость.
С мышечной слабостью связан еще один симптом, часто наблюдаемый при железодефицитной анемии. Больные жалуются на императивные позывы на мочеиспускание. Нередко у девочек с дефицитом железа наблюдается ночное недержание мочи. Часто больные не способны удержать мочу при смехе, кашле, не могут остановить начавшееся мочеиспускание. Моча быстро накапливается в мочевом пузыре после травмы, взятия крови из вены, болезненного укола.
Дефицит железа приводит к повреждению пищеварительного тракта — нарушается желудочная секреция. Почти у половины больных обнаруживается атрофический гастрит. Лечение препаратами железа может приводить к повышению кислотности желудочного содержимого.
У детей при дефиците железа обнаруживаются признаки нарушения кишечного всасывания жиров, ксилозы, железа.
При дефиците железа, как у взрослых людей, так и у подростков бывает извращение вкуса. Больные часто едят мел, зубной порошок, уголь, глину, песок, особенно обращает на себя внимание употребление льда (погофагия), а также сырой крупы, теста, сырого мясного фарша. Бывает пристрастие к запаху керосина, мазута, бензина, ацетона, гуталина, выхлопных газов машин, резины и даже мочи.
Причина этих извращений полностью не ясна. Можно только говорить о четкой зависимости этих необычных склонностей от дефицита железа, так как они полностью проходят после назначения препаратов железа и редко обостряются в дальнейшем.
2) В12 — и фолиеводефицитные анемии
Клинеко — гематологичский симптомокомплекс, объединяющий группу заболеваний, с макроцитарной анемией и мегалобластическим типом кровотворения, т.е. возрастом к фетальному кровотворению, которые поэтому называются мегалобластными анемиями (См.: приложение 4).
Мегалобластный эритропоэз с нарушенным созреванием эритроцитов, обычно обусловлен эндо- или экзогенным дефицитом витамина В12 и фолиевой кислоты. Развивается по разным причинам, среди которых:
— неполноценное питание (например у детей или вегетарианцев);
— хронические болезни желудочно — кишечного тракта и печени;
— аутоиммунное разрушение париетальных клеток (пернициозная анемия);
— вскармливание козьим молоком (у маленьких детей);
— целиакия (нарушение всасывание из кишечника);
— глистная инвазия (широкий лентец) и др.
В12-дефицитная анемия развивается относительно медленно и может быть малосимптомной. Клинические признаки анемии неспецифичны: слабость, быстрая утомляемость, одышка, головокружение, сердцебиение. Больные бледны, субиктеричны.
У большей части больных развивается глоссит — сопровождается жжением и болями в языке. Сосочки языка атрофируются, язык становится гладким, блестящим («лакированный язык»). Иногда поражаются слизистые оболочки щек и пищевода. Желудочная секреция резко снижения. При фиброгастроскопии выявляется атрофия слизистой оболочки желудка, которая подтверждается и гистологически. Возможно развитие диареи, вероятно, связанной с ахлоргидрией. Может быть увеличение селезенки и печени.
Наблюдаются и симптомы поражения нервной системы — белого вещества задних и боковых столбов спинного мозга (фуникулярный миелоз), церебральные нарушения и дегенерация периферических нервов. В основе неврологических проявлений лежит демиелинизация нервных волокон. Больные жалуются на покалывание в кончиках пальцев и нарушения чувствительности к холоду. При прогрессировании анемии появляется атаксия, нарушается походка, нарастает общая слабость, развивается гиперрефлексия.
3) Гипопролиферативные анемии.
Неспособность эритроцитарной массы адекватно увеличиваться в ответ на запрос тканей и клеток, сопрежена с относительным или абсолютным дефицитом эритропоэтина проявляется нормохромно — нормоцитарной анемией. Снижение продукции эритропоэтинав приводит к недостаточной стимуляции костного мозга при развитии гипоксии. В результате возникает ретикулоцитопения и соразмерно с выраженностью анемии снижается реактивность мозга.
4) Апластическая анемия (АА)
Апластическая анемия — состояние, характеризующееся снижением гематопоэтической активности (депрессией) костного мозга с развитием наряду с анемией также лейко- и тромбоцитопении (См.: приложение 5). Впервые АА была описана Эрлихом в 1888 году у 21 летней женщины.
Заболевание встречается в любом возрасте, чаще после 50 лет (65 % случаев). Пол существенно не влияет на частоту апластических анемий. В середине XX столетия заболевания системы крови стали причиной смерти у 1,54 % больных, в т.ч. вследствие апластических анемий — у 0,13%. Летальность при апластических анемиях достигает 60 % и более.
Этиология апластических анемий в 49,2-78,5 % случаев остается неизвестной. В остальных случаях ее причиной служат различные экзогенные и эндогенные факторы. К химическим экзогенным факторам относятся многие лекарственные препараты: сульфаниламиды, антибиотики (левомицетин, стрептомицин и др.), противовоспалительные средства (анальгин), цитостатики, противотуберкулезные средства (ПАСК, изониазид).
Кроме того, угнетают кроветворение бензольные соединения, пары ртути, продукты нефти, а из физических факторов — радиационное воздействие. К эндогенным факторам, способным вызвать апластическую анемию, относится ряд эндокринных и иммунных нарушений. У женщин с апластической анемией часто находят кистозное перерождение яичников, гипофункцию щитовидной железы; эритробластофтиз наблюдается иногда при нарушении функции тимуса. В части случаев апластические анемии развивается после различных инфекций: гриппа, ангины, инфекционного мононуклеоза, что дает основание предположить участие инфекционного фактора в этиологии апластических анемий. Однако перечисленные факторы риска влияют, как правило, на многих людей, заболевают же из них немногие, поэтому, вероятнее всего, решающая роль принадлежит все-таки индивидуальной реакции организма на действие перечисленных экзогенных и эндогенных факторов. Реакция организма в свою очередь может быть обусловлена генетически. Так, у больных апластической анемией часто встречается антиген гистосовместимости системы HLA DR2 лейкоцитов. При апластической анемии, как правило, поражена стволовая клетка, в связи с чем колониеобразующая способность костного мозга понижена. Этот процесс обусловлен повышенной активностью костномозговых Т-супрессоров, а также действием антител, направленных против костномозговых элементов, которые ингибируют активность колониестимулирующих факторов. В результате их действия нарушается эритро-, грануло- и тромбоцитопоэз. У больных апластической анемией понижена активность в эритроцитах ферментов глутатионредуктазы, Г-6-ФД; нарушена антиоксидантная защита; увеличен синтез HbF; в стволовых и коммитированных клетках наблюдается дефицит нуклеиновых кислот. Продолжительность жизни эритроцитов при апластической анемии укорочена, наблюдается внутрикостномозговое разрушение эритроидных клеток на всех уровнях созревания; нарушена утилизация железа, которое откладывается в виде гемосидерина в эритрокариоцитах, в печени и селезенке. В то же время содержание эритропоэтина чаще всего повышено вследствие уменьшения его использования бездействующим костным мозгом. Одновременно снижается количество гранулоцитов, нарушается их функция; уменьшается количество мегакариоцитов в костном мозге и содержание тромбоцитов в периферической крови. Полагают, что в патогенезе апластических анемий участвует механизм апоптоза (запрограммированного клеточного суицида), который может быть как врожденным, так и приобретенным, и обусловлен активацией проапоптотических генов.
В патогенезе апластических анемий принимает участие кроветворное микроокружение, в частности снижена колониеобразующая функция фибробластов костного мозга, а в клетках микроокружения увеличено содержание рибосом, митохондрий; стромальные клетки снижают выработку гемопоэтических ростовых факторов. Дефекты в микроокружении, как и в самих кроветворных клетках, могут быть индуцированы вирусами гепатита С, Эпштейна-Барр, цитомегаловирусом. Следовательно, в развитии апластических анемий участвуют различные патогенетические механизмы, ведущие к снижению количества и депрессии функций стволовых и коммутированных клеток гемопоэза, что выражается в их неспособности продуцировать необходимое количество зрелых клеток кроветворения.
При исследовании костного мозга резко уменьшена его клеточность, наблюдается замещение костного мозга жировой тканью; количество стромальных и лимфоидных клеток увеличено. Иногда костный мозг «пустой» — панмиелофтиз. Нарушения кроветворения отражаются на состоянии всех других органов и систем. Так, атрофические изменения развиваются в органах эндокринной системы — надпочечниках, яичниках, гипофизе, — обусловленные, вероятнее всего, выраженной гипоксией.
5) Парциальная красноклеточная аплазия (ПКА)
У взрослых больных ПКА- приобретенная характеризуется резким угнетением эритройдного отростка кроветворения. Глубокая анемия нормохромного типа в следствии почти полного подавления эритропоэза, сопровождается тяжёлым гипоксемическим симптомокомплексом. Можно обнаружить антитела к эритрокариоцитам. Поэтому предпочтение отделяется иммунодепрессивной терапии (цикоспорин А) в сочетание отдается иммунодепрессивной под контролем обмена железа, чтобы избежать вторичного гемосидероза и дополнительного угнетения эритропоэза. При повышении уровня ферритина более 400мкг/л — десфералотерапия.
6) Анемия у онкологических больных
Онкологические заболевания практически всегда сопровождаются анемией. Последние годы отмечены очень серьезным вниманием к качеству жизни пациентов с опухолевыми заболеваниями. На сегодняшний день одной из основных жалоб таких пациентов является слабость. Этот симптом встречается у 75% онкологических больных. Более того, в условиях доступности полноценного обезболивания слабость описывается больными как самый частый симптом рака. Согласно проведенным опросам 41% больных предпочли бы в первую очередь лечить ощущение постоянной усталости, и только 34% в первую очередь предпочли бы лечить боль. У пациентов с опухолевыми заболеваниями наблюдается множество причин для возникновения слабости: это и нарушения питания, и аффективные расстройства, и депрессия, но в большей степени возникновение слабости у онкологических больных конкурирует с показателем уровня гемоглобина. У первичных онкологических пациентов анемия имеет место в трети случаев, однако если пациент получает цитостатическую терапию, частота таких осложнений многократно возрастает. Так, среди пациентов, получающих химиотерапию, анемия наблюдается у 60%. Стремление улучшить качество жизни пациентов и поиск возможных резервов повышения эффективности лечения определили необходимость изучения анемии в онкологической практике. Снижение уровня гемоглобина ниже физиологической нормы влияет на качество жизни пациента, прогноз жизни и течение заболевания и на эффективность специфического лечения. Между тем состояние пациентов можно улучшить, поскольку анемия поддается лечению. Традиционно врачи выписывают железосодержащие препараты или применяют переливание крови. Назначаются и инъекции эритропоэтина — гормона, вырабатываемого почками.
Анемии вследствие усиленного кроверазрушения (гемолитические)
Анемия, при которой процесс разрушения эритроцитов преобладает над процессом регенерации, называется гемолитической (См.: приложение 6).
Естественная гибель эритроцита (эритродиерез) происходит спустя 90-120 дней после его рождения в сосудистых пространствах ретикулогистиоцитарной системы, главным образом в синусоидах селезенки и значительно реже непосредственно в кровеносном русле. При гемолитической анемии наблюдается преждевременное разрушение (гемолиз) эритроцитов. Устойчивость эритроцита к различным воздействиям внутренней среды обусловлена как структурными белками клеточной мембраны (спектрин, анкирин, белок 4,1 и др.), так и ее ферментным составом, кроме того, нормальным гемоглобином и физиологическими свойствами крови и других сред, в которых циркулирует эритроцит. При нарушении свойств эритроцита или изменении среды его пребывания, он преждевременно разрушается в кровеносном русле либо в ретикулогистиоцитарной системе различных органов, прежде всего селезенки.
Иммунные гемолитические анемии включают 4 варианта: изоиммунные, трансиммунные, гетероиммунные и аутоиммунные.
Изоимунный вариант наблюдается в тех случаях, когда реципиенту перелиты эритроциты и клетки донора, несовместимые по системе АВО. При этом клетки крови донора разрушаются антителами, имеющимися у реципиента и направленными против антигена донора, т.е. гемолизу подвергаются эритроциты донора в крови реципиента (больного). Кроме того, подобная ситуация возможна при антигенной несовместимости клеток крови матери и плода.
Трансиммунная гемолитическая анемия развивается у плода, имеющего одинаковые антигены с материнскими, если мать страдает аутоиммунной гемолитической анемией; при этом антитела матери через плаценту проникают в организм плода и оказывают разрушительное действие на его эритроциты.
Гетероиммунная гемолитическая анемия отличается от предыдущей тем, что антитела направлены не против эритроцитов, а против антигена, фиксированного на эритроцитах; в ходе реакции антиген-антитело разрушаются и эритроциты. Антитела, к примеру, могут быть направлены против лекарственного препарата, фиксированного на эритроцитах. Гетероиммунной считается также гемолитическая анемия при наличии эритроцитов с измененной антигенной структурой; в этих случаях эритроцит становится «чужим» для организма и иммунная система целенаправленно организует специфическую защиту (синтезируются антитела против измененной антигенной структуры эритроцита).
Об аутоиммунном характере гемолитической анемии свидетельствуют лишь те случаи, когда образующиеся антитела направлены против собственных неизмененных антигенов, конкретно — против нормальной антигенной структуры клеток эритропоэза: эритрокариоцитов или эритроцитов периферической крови. Антитела могут быть представлены неполными тепловыми агглютининами, тепловыми гемолизинами, полными холодовыми агглютининами и двухфазными гемолизинами.
Анемии вследствие кровопотери (постгеморрагические)
Острая постгеморрагическая анемия (гемолитическая гипоксия).
Причинами острой постгеморрагической анемии являются различные внешние травмы (ранения), кровотечения из внутренних органов (легочные, желудочно-кишечные, маточные).
Клиническая картина складывается из симптомов, свойственных анемии, и симптомов коллапса или шока. Характерны бледность кожных покровов и слизистых оболочек, слабость, головокружение, шум в ушах, обморочное состояние, частый нитевидный пульс, падение температуры тела, падение кровяного давления, холодный пот, иногда рвота, цианоз, судороги.
Вывод: При написании первой главы мной была собрана специальная литература, включая в себя учебники, описаны теоретические аспекты и раскрыты ключевые понятия анемий.
2. Мониторинг данных общего анализа крови при различных видах анемий
2.1 Лабораторная диагностика анемий
В настоящее время анемии являются самыми распространенными патологическими состояниями и стоят на первом месте среди наиболее распространенных заболеваний человека.
В лабораторной диагностике используют множество способов определения малокровия, но для того чтобы выявить пациент должен пройти консультацию с врачом. По общим симптомам пациента врач направит на ОАК, так как он является самым распространенным анализом для предварительного выявления заболевания. Отталкиваясь от данного анализа, врач сможет распознать характер заболевания и назначить лечение или следующие анализы для определения точного диагноза.
Подготовка к сдачи крови на общий анализ
Для диагностики анемии в общем анализе крови обязательным является определение следующих показателей крови;
Количества эритроцитов, количества ретикулоцитов, гемоглобина, гематокрита, среднего объема эритроцитов, ширины распределения эритроцитов по объему, среднего содержания гемоглобина в эритроците, средней концентрации гемоглобина в эритроците, количества лейкоцитов, количество тромбоцитов.
Исследование производится утром натощак — между последним приемом пищи и взятием крови должно пройти не менее 8 — 12 часов. Вечером предшествующего дня рекомендуется необильный ужин. Желательно за 1 — 2 дня до обследования исключить из рациона жирное, жареное и алкоголь. Если накануне состоялось застолье или было посещение бани или сауны — необходимо перенести лабораторное исследование на 1 — 2 дня.
За 1 час до взятия крови необходимо воздержаться от курения.
Не следует сдавать кровь после рентгенологических исследований, физиотерапевтических процедур.
Необходимо исключить факторы, влияющие на результаты исследований: физическое напряжение (бег, подъем по лестнице), эмоциональное возбуждение. Перед процедурой следует отдохнуть 10 — 15 минут и успокоиться.
Необходимо помнить, что результат исследования может быть искажен действием принимаемых лекарственных препаратов или продуктами их метаболизма. Назначение и отмена любого лекарственного препарата сопровождается изменением лабораторных показателей. Поэтому перед сдачей анализа следует проконсультироваться у врача о возможности ограничения приема лекарственных препаратов для подготовки к исследованию. Рекомендуется отказаться от приема лекарственных препаратов перед сдачей крови на исследование, то есть забор крови производится до приема лекарственных препаратов.
Учитывая суточные ритмы изменения показателей крови повторные исследования целесообразно проводить в одно и то же время.
В разных лабораториях могут применяться разные методы исследования и единицы измерения. Чтобы оценка результатов обследования была корректной и была приемлемость результатов, желательно проводить исследования в одной и той же лаборатории, в одно и тоже время.
Прием воды на показатели крови влияние не оказывает, поэтому воду пить можно.
Кровь — ткань внутренней среды защитно-трофической функции, состоящая из жидкого межклеточного вещества (плазмы), постклеточных структур (эритроцитов и тромбоцитов) и клеток как периферической крови и лимфы, так и клеток на всех стадиях своего развития в кроветворных органах. Клеточные и постклеточные структуры периферической крови называются форменными элементами. Объем крови в организме человека равен 5-5,5 л (или около 7% массы тела), при этом форменные элементы составляют 40-45%, а плазма — 55-60%.
Кровь выполняет следующие функции:
1) трофическую — перенос питательных веществ ко всем клеткам и тканям;
2) дыхательную — газообменную, или транспорт кислорода к тканям и удаление из организма углекислоты;
3) защитную — (фагоцитоз, выработка антител);
4) регуляторную — транспорт гормонов и других гуморальных факторов регуляции;
5) гомеостатическую — поддержание физико-химического постоянства состава внутренней среды организма.
Показатели общего анализа крови для диагностики анемии:
· Средний объем эритроцитов (MCV)
· Ширины распределений эритроцитов по объему (RDW)
· Среднее содержание гемоглобина в эритроците (MCH)
· Средней концентрации гемоглобина в эритроците (MCHC)
Общий анализ крови проводят в гематологической лаборатории ручными методами. В настоящее время появилось новая техника, которая способна заменить руки лаборанта и сделать за него почти всю работу, эти машины называются гематологическими анализаторами.
Нормальные показатели крови (См.: Таблицу 1):
источник
Анемия. Виды анемий: железодефицитная, гемолитическая, В12 дефицитная, апластическая. Причины, диагностика, степени анемии.
Анемия или пониженное количество гемоглобина в крови, а в просторечии – «малокровие». Практически каждый человек хотя бы один раз сталкивался с такой формулировкой, особенно женщины. Что же означает этот пугающий термин? Почему возникает данное состояние организма? Чем опасна анемия? Как вовремя распознать её на начальных этапах?
Анемия – это патологическое состояние организма, при котором наблюдается снижение количества гемоглобина и эритроцитов ниже нижних границ нормы. Причем уменьшение содержания гемоглобина является обязательным признаком анемии, в отличие от снижения количества эритроцитов. То есть снижение концентрации гемоглобина при анемии есть всегда, а снижение количества эритроцитов может и не быть. Однако в некоторых случаях при анемии выявляются патологические формы эритроцитов (не двояко – вогнутые).
Анемия – это не самостоятельное заболевание, а следствие основной патологии, потому, выявление сниженного уровня эритроцитов и гемоглобина, требует проведения тщательной диагностики для выявления причины!
Гидремия – разжижение крови.
Такое состояние возможно при поступлении в кровоток тканевой жидкости при схождении отека, обильном питье. Гидремия – это псевдоанемия.
Сгущение крови
Сгущение крови может происходить вследствие потери жидкой части крови, что происходит при сильном обезвоживании. Обезвоживание наблюдается в результате сильной рвоты, поноса, обильного потения. Однако в этом случае за счет сгущения крови количество гемоглобина и эритроцитов может быть в пределах нормальных значений. В таких ситуациях говорят о наличии скрытой анемии.
Специфические и неспецифические признаки анемии – что относится к ним?
В первую очередь рассмотрим, как же проявляется анемия. Существуют неспецифические проявления и специфические. Неспецифические проявления называются так, потому что эти признаки общие для всех видов анемий. Специфические же проявления строго индивидуальны и характерны только для каждого конкретного вида анемии.Сейчас мы рассмотрим только неспецифические проявления, а специфические укажем при рассмотрении видов анемий.
Итак, к неспецифическим признакам анемий, относят следующие симптомы:
- бледность кожи и слизистых оболочек
- слабость
- головокружение
- шум в ушах
- головные боли
- быстрая утомляемость
- сонливость
- одышка
- анорексия (патологическая потеря аппетита или отвращение к пище)
- нарушение сна
- нарушения менструального цикла вплоть до полного прекращения менструаций (аменореи)
- импотенция
- тахикардия (увеличение частоты сердечных сокращений)
- шумы в сердце (усиление сердечного толчка, систолический шум на верхушке сердца)
- сердечная недостаточность
- при снижении количества гемоглобина менее 50 г/л возможно развитие ацидоза (закисление крови)
- снижение содержания гемоглобина ниже нормальных показателей
- снижение содержания эритроцитов ниже нормы
- изменение цветного показателя
- изменение содержания лейкоцитов и тромбоцитов
Виды анемий – постгеморрагическая, гемолитическая, дефицитная и гипопластическая
Анемии могут вызываться совершенно разными причинами, поэтому принято все анемии делить по различным признакам, в том числе по причинам, их вызывающим. Согласно причинам (патогенезу) выделяют три вида анемии: постгеморрагические, гемолитические и связанные с нарушением кровообразования (дефицитные и гипопластические). Что это значит? Разберем подробнее.
Постгеморрагические анемии связаны с острой или хронической кровопотерей (кровотечение, ранение).
Гемолитические – развиваются в связи с усиленным разрушением эритроцитов.
Дефицитные анемии вызваны недостатком витаминов, железа или других микроэлементов, которые необходимы для кроветворения.
Гипопластические анемии – это самый тяжелый вид анемий и связан он с нарушением кроветворения в костном мозгу.
- По степени тяжести. Существует три степени тяжести анемии – легкая, средняя и тяжелая в зависимости от содержания гемоглобина и эритроцитов в крови:
| Степень тяжести | Гемоглобин, г/л | Эритроциты, Т/л | ||||||||||||||||||||||
| Легкая | > 100 г/л | > 3 Т/л | ||||||||||||||||||||||
| Средняя | 100 – 66 г/л | 3 – 2 Т/л | ||||||||||||||||||||||
| Тяжелая | 1,05) и гипохромные (ЦП 8,0 микрон) и мегалобластные (СДЭ > 9,5 микрон). Нормоцитарные анемии характеризуются нормальным диаметром эритроцитов, микроцитарные – уменьшенным диаметром эритроцитов, а макроцитарные и мегалобластные связаны с увеличением диаметра эритроцитов. К нормоцитарным анемиям относят – острую постгеморрагическую и большинство гемолитических анемий; к микроцитарным – железодефицитную анемию, микросфероцитоз и хроническую постгеморрагическую анемию. Макроцитарные анемии – это гемолитическая болезнь новорожденных, фолиево дефицитная анемии. Мегалоцитарная – В12 дефицитнаяанемия.
Мы рассмотрели, на какие типы, и по каким признакам классифицируют анемии. Перейдем к рассмотрению, как проявляются отдельные виды анемий, какие изменения при этом наблюдаются в крови и в организме человека в целом.
Симптомы острой постгеморрагической анемии, картина крови Симптомами острой постгеморрагической анемии являются такие признаки: бледность, резкое головокружение, обмороки, частый пульс, холодный пот, снижение температуры тела, иногда рвота. Потеря крови более 30% от исходного уровня является критической и опасна для жизни. Диагностика постгеморрагической острой анемии В крови увеличивается количество ретикулоцитов более 11%, также появляются «незрелые» эритроциты и эритроциты с измененной формой клетки. Со стороны лейкоцитов наблюдается увеличение их общего количества выше 12 Г/л, а в лейкоцитарной формуле идет сдвиг влево. В последующие два месяца после острой кровопотери происходит восстановление показателей эритроцитов и гемоглобина. Однако восстановление количества эритроцитов и содержания гемоглобина связано с расходованием фонда железа в организме и может повлечь за собой развитие железодефицита. Поэтому в период восстановления после кровопотери необходимо соответствующее питание, то есть в рационе должны быть продукты с высоким содержанием железа (например, гранаты, гречка, печень и т.д.). Принципы лечения острой постгеморрагической анемии Лечение острой постгеморрагической анемии должно проводиться в условиях стационара и быть направлено на восстановление количества циркулирующей крови, количества форменных элементов крови и поддержание этих показателей. В первую очередь необходимо остановить кровотечение. Затем в зависимости от количества кровопотери применяют переливание крови, эритроцитарной массы и кровезаменителей. Симптомы хронической постгеморрагической анемии Симптомы хронической постгеморрагической анемии такие же, как при железодефицитной анемии. Какие же это симптомы? Итак, признаками хронической постгеморрагической анемии являются: кожа «алебастрового» оттенка (очень белая, бледная), извращение обоняния (непереносимость запахов или, наоборот, тяга к каким-либо запахам), изменение вкуса, одутловатость лица, пастозность голеней, ломкость волос и ногтей, сухость, шершавость кожи. Также возможно образование койлонехий – истонченных и уплощенных ногтей. Помимо этих внешних признаков возможно появление одышки, тошноты, головокружения, учащения пульса, слабости, утомляемости, субфебрильной температуры (до 37° С) и прочее. Из-за дефицита железа могут проявляться нарушения со стороны желудочно-кишечного тракта – кариес, глоссит, сниженная кислотность желудочного сока, а также непроизвольное мочеиспускание при смехе, потливость. Диагностика хронической постгеморрагической анемии В крови при хронической постгеморрагической анемии появляются слабо окрашенные эритроциты маленького размера, овальные эритроциты, снижено общее количество лейкоцитов, а в лейкоцитарной формуле наблюдается незначительный лимфоцитоз. В сыворотке крови концентрация железа ниже нормы – 9,0 мкмоль/л, также ниже нормального содержание меди, кальция, витаминов А, В, С, но, однако, повышена концентрация цинка, марганца и никеля в крови. Причины хронической постгеморрагической анемии Почему же возникает такое состояние – хроническая постгеморрагическая анемия? Причины этого явления следующие:
Лечение хронической постгеморрагической анемии Именно в силу причин, приводящих к развитию хронической постгеморрагической анемии, при лечении этого состояния, прежде всего, необходимо устранить причину хронической кровопотери.Затем необходимо сбалансированное питание, содержащее продукты с высоким содержанием железа, фолиевой кислоты и витаминов. В случае тяжелой анемии необходимо принимать препараты железа (сорбифер, феррум-лек) в виде таблеток или инъекций, препараты фолиевой кислоты, витамин В12 в виде таблеток или в виде инъекций. Наиболее эффективными препаратами для восстановления уровня железа в организме являются таблетированные препараты, которые выпускаются различными фирмами. В силу этого в аптеках представлен широкий выбор препаратов железа. При выборе препарата необходимо обращать внимание на содержание железа в одной таблетке и биологическую доступность данного препарата. Препараты железа необходимо принимать совместно с аскорбиновой кислотой и фолиевой кислотой, поскольку в такой комбинации происходит наилучшее усвоение железа. Однако при выборе препарата и дозы необходимо обязательно проконсультироваться с врачом. Гемолитические анемии – это группа анемий, при которых процессы разрушения эритроцитов преобладают над процессами их производства. Иными словами разрушение эритроцитов происходит быстрее, чем образуются новые клетки, взамен разрушенных. Гемолитические анемии могут быть наследственными и приобретенными. Наследственные гемолитические анемии это:
Симптомы гемолитических анемий Общим признаком всех гемолитических анемий является желтуха. Желтуха появляется вследствие того, что при разрушении эритроцитов выделяется в кровь большое количество билирубина, который и приводит к данному симптому. Помимо желтухи имеются следующие признаки, общие для всех гемолитических анемий – увеличение печени и селезенки, увеличение концентрации билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев». В связи с тем, что наиболее широкое распространение среди наследственных гемолитических анемий имеют серповидно – клеточная анемия и талассемия, более подробно рассмотрим именно их.
Серповидно – клеточная анемия вызвана тем, что синтезируется молекула гемоглобина с дефектом. Такие дефектные молекулы гемоглобина собираются в веретенообразные кристаллы (тактоиды), которые растягивают эритроцит, придавая ему серповидную форму. Такие серповидные эритроциты мало пластичны, повышают вязкость крови и закупоривают мелкие кровеносные сосуды. Кроме этого своими острыми концами такие эритроциты протыкают друг друга и разрушаются. Симптомы серповидно–клеточной анемии Серповидно – клеточная анемия внешне проявляется следующими признаками:
Диагностика серповидно–клеточной анемии В анализе крови сниженное количество гемоглобина (50 – 80 г/л) и эритроцитов (1 – 2 Т/л), увеличение ретикулоцитов до 30% и более. В мазке крови видны серповидные эритроциты и эритроциты с тельцами Жолли и кольцами Кабо. Лечение серповидно-клеточной анемии Основной принцип лечения данного вида анемии –это недопущение гемолитических кризов. Данный эффект достигается тем, что человек избегает гипоксических состояний – присутствия в разреженном воздухе, в местах с низким содержанием кислорода и прочее. Используют переливание эритроцитарной массы или кровезаменителей.
Талассемия возникает вследствие нарушения скорости образования гемоглобина. Такой незрелый гемоглобин не стабилен, в результате чего он выпадает в эритроцитах в виде включений – телец, а весь эритроцит приобретает внешний вид мишеневидной клетки. Талассемия – это тяжелое наследственное заболевание, которое невозможно вылечить, а можно лишь облегчить ее проявления. Симптомы талассемии
Диагностика талассемии В крови обнаруживаются мишеневидные эритроциты, увеличенное количество ретикулоцитов, снижение концентрации гемоглобина до 20 г/л, а эритроцитов до 1 Т/л. Также наблюдаются уменьшение количества лейкоцитов и тромбоцитов. Итак, мы рассмотрели основные виды наследственных гемолитических анемий, которые передаются от родителей к детям. Перейдем к рассмотрению приобретенных гемолитических анемий, которые возникают вследствие наличия провоцирующего фактора. Приобретенные гемолитические анемии, иммунные и не иммунные анемии Прежде всего, необходимо отметить, что приобретенные гемолитические анемии могут развиваться при участии иммунной системы (иммунные) или без ее участия (не иммунные). К анемиям, развивающимся при участии иммунной системы, относятся вирусная, сифилитическая анемия и гемолитическая болезнь новорожденных. Не иммунные гемолитические анемии – это болезнь Маркиафавы – Микелли, а также анемии, возникшие вследствие длительной маршевой ходьбы, отравления алкоголем, кислотами, солями тяжелых металлов, ядами змей, насекомых и грибов. При ожогах, составляющих более 20% поверхности тела, недостатке витамина Е и малярии, также развивается не иммунная гемолитическая анемия.
Лечение этих видов анемии, как правило, не требуется. Гемолитическая болезнь новорожденного, причины развития, симптомы заболевания, степени тяжести.
В настоящее время проводится профилактика гемолитической болезни новорожденных путем отслеживания наличия антител у матери. Если у матери выявляются антитела, то лечение проводят в стационаре. При этом производят вливание антирезусных иммуноглобулинов. Признаки не иммунных гемолитических анемий, лабораторные симптомы Не иммунные гемолитические анемии имеют следующие признаки – желтуха,увеличенные печень и селезенка,повышенная концентрация билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев».В картине крови отмечается наличие эритроцитов различной формы и размеров, ретикулоцитоз до 30% и выше, сниженное количество лейкоцитов и тромбоцитов. Такие анемии сами по себе не требуют отдельного и особенного лечения, так как в первую очередь необходимо убрать фактор, вызывающий эту анемию (яды змей, соли тяжелых металлов и т.д.). Анемии, вызванные нарушением кровообразования, делятся на две большие группы – дефицитные анемии и гипопластические. Дефицитные анемии связаны с дефицитом необходимых для кроветворения элементов. К дефицитным анемиям относят – железодефицитную анемию, железорефрактерную анемию, В12 – дефицитную и фолиево дефицитную. Гипопластические анемии вызваны гибелью клеток – предшественниц в костном мозгу. Гипопластические анемии могут быть наследственными (анемия Фанкони, анемия Эстрена – Дамешика, анемия Блекфэрна — Даймонда) и приобретенными. Приобретенные гипопластические анемии развиваются либо сами по себе вследствие неизвестной причины, либо на фоне имеющегося заболевания — лучевой болезни, инфекций, повреждений иммунитета. Для большинства людей больший интерес представляют дефицитные анемии, которые могут возникнуть практически у каждого человека. Поэтому наиболее подробно остановимся именно на этом виде анемий.
Причины железодефицитной анемии Железодефицитная анемия возникает в следующих случаях:
Симптомы железодефицитной анемии Клинически железодефицитная анемия проявляется тремя основными синдромами – гипоксическим, сидеропеническим и анемическим. Что это за синдромы? Чем характеризуется каждый из них?Синдром – это устойчивая совокупность симптомов. Итак, гипоксический синдром характеризуется одышкой, головными болями, шумом в ушах, быстрой утомляемостью, сонливостью и тахикардией; анемический синдром выражается в уменьшении содержания количества эритроцитов и гемоглобина. Сидеропенический синдром напрямую связан с уменьшением количества железа в организме и проявляется так: нарушение питания кожи, ногтей, волос – кожа «алебастрового» оттенка, сухость и шершавость кожи, ломкие волосы и ногти. Затем присоединяетсяизвращение вкуса и обоняния (желание есть мел, вдыхать запах мытых бетонных полов и т.д.). Возможно появление осложнений со стороны желудочно-кишечного тракта – кариеса, дисфагии, снижения кислотности желудочного сока, непроизвольного мочеиспускания (в тяжелых случаях), потливости. Диагностика железодефицитной анемии В крови наблюдается снижение содержания гемоглобина до 60 – 70 г/л, эритроцитов до 1,5 – 2 Т/л, также снижено количество или вовсе отсутствуют ретикулоциты. Появляются эритроциты различных форм и размеров. Концентрация сывороточного железа ниже нормы. Лечение железодефицитной анемии В основе лечения железодефицитной анемии лежат принципы устранения причины ее возникновения – лечение заболеваний желудочно – кишечного тракта, а также введение сбалансированного пищевого рациона. В диете должны присутствовать продукты с высоким содержанием железа (печень, мясо, молоко, сыр, яйца, злаки и т.д.). Однако главным средством восстановления количества железа в организме на начальном этапе являются лекарственные препараты железа. В большинстве случаев такие лекарства назначают в виде таблеток. В тяжелых случаях прибегают к внутримышечным или внутривенным инъекциям. В лечении данной анемии используют, например, такие препараты: сорбифер, феррум-лек, тардиферон, тотема и другие. Выбор различных лекарственных средств, в том числе комбинированных, очень широк. При выборе необходимо консультироваться с врачом. Обычно, суточная доза для профилактики и лечения анемии легкой степени составляет 50-60 мг железа, для лечения анемии средней тяжести – 100-120 мг железа в сутки. Лечение анемии тяжелой степени проводят в стационаре и применяют препараты железа в виде инъекций. Затем переходят на таблетированные формы. Препараты железа вызывают потемнение стула, однако в данной ситуации это нормально.Если препарат железа вызывает неприятные ощущения в желудке, то его необходимо заменить.
Железорефрактерную анемию также называют сидеробластной или сидероахристической. Железорефрактерная анемия развивается на фоне нормального содержания железа в сыворотке крови и недостатка ферментов, которые участвуют в синтезе гемоглобина. То есть основная причина железорефрактерной анемии – нарушение процессов «усвоения» железа. Симптомы железорефрактерной анемии, что такое гемосидероз? Проявляется железорефрактерная анемия одышкой, головными болями, головокружением, шумом в ушах, быстрой утомляемостью, сонливостью, нарушениями сна и тахикардией. Из-за высокого содержания железа в крови тканях наблюдается гемосидероз.Гемосидероз – это отложение железа в органах и тканях вследствие его избытка. При гемосидерозе развивается недостаточность сердечно – сосудистой системы вследствие отложения железа в сердечной мышце, сахарный диабет, поражение легких и увеличиваются размеры печени и селезенки. Кожа приобретает землянистый оттенок. Диагностика железорефрактерной анемии, что такое сидеробласты? Цветной показатель крови снижен до 0,6 – 0,4, присутствуют эритроциты различных форм и размеров, количество гемоглобина и эритроцитов ниже нормы. Имеются изменения и в костном мозгу – появляются клетки – сидеробласты. Сидеробласты – это клетки, имеющие вокруг ядра венчик из железа. В норме таких клеток в костном мозгу 2,0 – 4,6%, а при железорефрактерной анемии их количество может доходить до 70%. Лечение железорефрактерной анемии Лечения, которое смогло бы устранить ее совсем, на сегодняшний день нет. Возможно применение заместительной терапии – вливание эритроцитарной массы и кровезаменителей.
Во-первых, что такое В12? В12 – это витамин, который имеет также название цианкобаламин. Цианкобаламин содержится в основном в продуктах животного происхождения – мясо, печень, почки, молоко, яйца, сыр. Уровень витамина В12 необходимо постоянно поддерживать употреблением соответствующих продуктов, поскольку происходят его естественные физиологические потери с калом и желчью. Причины В12 дефицитной анемии Итак, В12 – дефицитная анемия – это анемия, возникающая вследствие недостаточности витамина В12. Недостаток витамина В12 может быть вызван недостаточным его поступлением с пищей или нарушением его усвоения в желудочно-кишечном тракте. Недостаточное поступление цианкобаламина с пищей возможно у строгих вегетарианцев. Также недостаток В12 может проявиться при повышении потребности в нем у беременных женщин, кормящих матерей, раковых больных. Неусвоение витамина В12, поступающего с пищей в достаточном количестве, происходит при заболеваниях желудка, тонкого кишечника (дивертикулы, глисты) и лечении противосудорожными средствами или оральными контрацептивами. Симптомы В12 дефицитной анемии Симптомы проявления В12 – дефицитной анемии характеризуются нарушениями в центральной нервной системе и желудочно-кишечном тракте. Итак, рассмотрим эти две большие группы симптомов:
Диагностика В12 дефицитной анемии В системе крови происходит переход на мегалобластический тип кроветворения. Это означает, что в крови появляются гигантские эритроциты с укороченным сроком жизни, ярко окрашенные эритроциты без просветления в центре, грушевидные и овальные эритроциты с тельцами Жолли и кольцами Кабо. Также появляются гигантские нейтрофилы, уменьшается количество эозинофилов (вплоть до полного отсутствия), базофилов и общего количества лейкоцитов. В крови повышена концентрация билирубина, в связи с чем, может наблюдаться легкая желтушность кожи и склер глаз. Лечение В12 дефицитной анемии В первую очередь необходимо вылечить заболевания желудочно-кишечного тракта и наладить сбалансированное питание, с достаточным содержанием витамина В12. Применение курса инъекций витамина В12 быстро нормализует кроветворение в костном мозгу, а далее необходимо постоянное, регулярное поступление с пищей достаточного количества витамина В12.
Симптомы фолиеводефицитной анемии При фолиево дефицитной анемии страдает желудочно-кишечный тракт, поэтому и проявления данной анемии связаны с нарушениями работы желудочно-кишечного тракта. Наблюдается появление повышенной чувствительности к кислой пище, глоссита, трудностей глотания, атрофии слизистой желудка, увеличения размеров печени и селезенки. Лечение фолиеводефицитной анемии Для лечения данного вида анемии применяют таблетки фолиевой кислоты и нормализуют рацион питания, в котором должны быть продукты, содержащие достаточное количество фолиевой кислоты.
Симптомы гипопластических анемий Гипопластические анемии могут быть наследственными или приобретенными, однако все подвиды данного типа анемий характеризуются одинаковыми проявлениями. Рассмотрим эти симптомы:
Причины, вызывающие развитие гипопластической анемии Какие же причины способны вызывать подобное поражение костного мозга? Наследственные анемии, соответственно, передаются по наследству, а вот приобретенные? Все факторы, способные приводить к развитию гипопластической анемии, делятся на экзогенные (внешние) и эндогенные (внутренние). В таблице приведены основные экзогенные и эндогенные причины, способные вызвать развитие гипопластической анемии.
Принципы лечения гипопластических анемий Лечение гипопластических анемий находится строго в компетенции врача – гематолога. Могут применяться различные методы стимулирования кроветворения, или пересадка костного мозга. Итак, мы рассмотрели все основные виды анемий. Конечно, их гораздо больше, однако мы не можем объять необъятное. При появлении каких-либо признаков анемии необходимо своевременно обратиться к врачу. И регулярно сдавать анализ крови на содержание гемоглобина. источник |

 Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.
Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.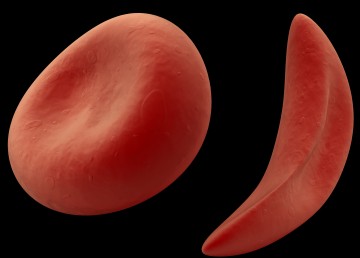 Причины серповидно–клеточной анемии
Причины серповидно–клеточной анемии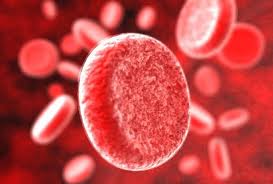 Талассемия – причины заболевания
Талассемия – причины заболевания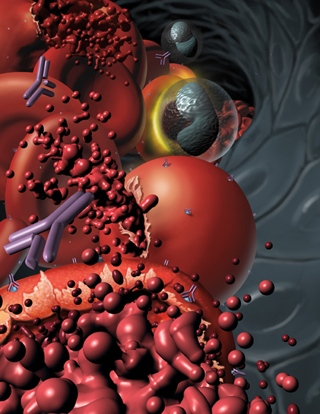 Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы.
Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы. Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.
Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.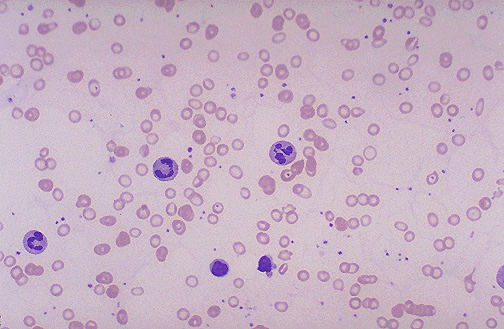 Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты.
Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты. Причина железорефрактерной анемии
Причина железорефрактерной анемии Что такое В12? Где содержится этот витамин?
Что такое В12? Где содержится этот витамин? Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12.
Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12. Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.
Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.