Паспортная часть
Ф.И.О: Мусокова Роза Абдуллаевна
Адрес: Черекский район с.Жемтала
Дата поступления: 26.10.17г
Диагноз при поступлении: Шизофрения параноидная форма
Диагноз клинический: Шизофрения параноидная форма, непрерывное течение. Депрессивно-паранидный синдром.Эмоционально-волевой дефект личности
Жалобы: на бессонницу, тревогу, страх, слабость, плаксивость
Наследственность психопатологически не отягощена.
Больная – родилась от 1 беременности, беременность протекала нормально, роды срочные. Травм при родах не было. Росла и развивалась соответственно возрасту. Детский сад не посещала. Окончила 10 классов СОШ с неплохой успеваемостью. Дальше нигде не училась, в 19 лет вышла замуж. Менструация с 14 лет по 4 дня через 21 день, беременностей 4, роды 4. В настоящее время вдова, проживает с сыновьями. Не работает. Инвалид ll группы. Жилищно-бытовые условия удовлетворительные. Перенесенные заболевания: ОРВИ, ОРЗ.
Неврологическое состояние
Со стороны ЧМН патологии не выявлено. Двигательные функции конечностей и туловища: атрофии мышц, фибриллярных, фасцикулярных подергиваний нет. Объем активных и пассивных движений в суставах рук и ног, головы сохранен. Мышечный тонус в норме. Каталепсии, акинеза, амимии, скованности, гиперкинезов нет. Припадки, судорожные подергивания отсутствуют. Координация движений: устойчива в позе Ромберга, пальце-носовую пробу выполняет свободно. Тактильная, болевая, температурная чувствительность не нарушена. Нормальные рефлексы:
сухожильные сохранены, одинаково выражены с обеих сторон. Реакция зрачков на свет живая, одинаковая с обеих сторон, анизокарии нет. Патологических рефлексов и менингиальных знаков не выявлено. Исследование высших корковых функций: моторной, сенсорной, амнестической афазии не выявлено. Алексии, аграфии, апроксии, агнозии не наблюдаются
Психический статус
Внешне депрессивный вид, страдальческое выражение лица. Медлительна, гиподинамична. В контакт вступает охотно, сразу начинает плакать « не знаю, что со мной постоянно плачу» Больная опрятна. Видимых физических недостатков и уродств не отмечается.
Больная в сознании, ориентирована в месте, где находится, а также во времени и собственной личности.
Обманы восприятия отрицает «раньше были голоса, сейчас не слышу»
Память сохранена. Объем запоминания хорошего качества.
Уровень интеллекта соответствует возрасту и полученному образованию
Мышление паралогичное, непоследовательное. Сообщает, что «мысли путаются, наплывают друг на друга, плохие мысли приходят в голову, что что-то плохое случится». Высказывает бредовые идеи самоуничтожения, самообвинения « дети у меня хорошие, а я сама очень плохая, все время только плохое думаю»
8.Эмоционально волевая сфера
Больная предъявляет жалобы на снижение настроения, тревожность, страх, плаксивость
10.Оценка своего состоянии, критическое отношение к своей болезни
Критики к состоянию нет, но на лечение в отделении соглашается, просит о помощи.
Анамнез заболевания
Психические расстройства отмечаются с 1993года. В клинике галлюцинаторно- параноидная симптоматика, колебания настроения, заболевание протекает непрерывно. За годы болезни сформировался эмоционально – волевой дефект личности. Многократно лечилась стационарно в ПНД. Последняя госпитализация с 13.02.14.г по 5.02.14.г выписывалась с улучшением. Регулярно принимала трофтазин, циклодол. Последние три месяца прием препаратов прекратила самостоятельно, состояние ухудшилось. Сообщает, что «мысли путаются, наплывают друг на друга, плохие мысли приходят в голову, что что-то плохое случится». Высказывает бредовые идеи самоуничтожения, самообвинения « дети у меня хорошие, а я сама очень плохая, все время только плохое думаю» Отмечает плаксивость « не знаю, что со мной постоянно плачу». Госпитализирована для обследования и лечения.
Соматический статус
Общее состояние: средней тяжести
Кожа и видимые слизистые: кожа бледно-розового цвета , высыпаний нет, влажность кожи умеренная, эластичность сохранена . Видимые слизистые розовые, блестящие, чистые, влажные.
Подкожная жировая клетчатка: развита умеренно, распределена равномерно
Лимфатические узлы.затылочные, заушные , околоушные, поднижнечелюстные, подбородочные, задне- и переднешейные,, над- и подключичные, подмышечные, локтевые, паховые, подколенные не пальпируются
Мышечная система. Тонус мышц сохранен
Кости и суставы: патологических изменений при осмотре в костях черепа, позвоночника , грудной клетки , таза , длинных трубчатых костях не обнаружено.
Органы дыхания: по данным осмотра, пальпации, перкуссии и аускультации органов дыхательной системы патологии не найдено. Чисто дыханий 16 в минуту.
Сердечно-сосудистая система: границы относительной тупости сердца соответствуют норме. При аускультации тоны сердца ритмичные, приглушены, . Пульс слабого наполнения, удовлетворительного напряжения. АД -120/70 мм. рт.ст. ЧСС 74 уд. мин.
Органы пищеварения: язык слегка обложен белым налетом. Живот мягкий, безболезненный. Печень не выходит за края правой реберной дуги, пальпация ее безболезненна, край ровный, эластичный . Поджелудочная железа и селезенка не пальпируются
Мочеполовая система: симптом поколачивания отрицательный с обеих сторон, мочеиспускание свободное, безболезненное.
Область шей визуально не изменена.Щитовидная железа не пальпируется.
Обоснование клинического диагноза:
Шизофрения параноидная форма, непрерывное течение. Депрессивно-паранидный синдром.Эмоционально-волевой дефект личности
Жалоб: на бессонницу, тревогу, страх, слабость, плаксивость
Психические расстройства отмечаются с 1993года. В клинике галлюцинаторно- параноидная симптоматика, колебания настроения, заболевание протекает непрерывно. За годы болезни сформировался эмоционально – волевой дефект личности.
Психический статус Внешне депрессивный вид, страдальческое выражение лица. Медлительна, гиподинамична. В контакт вступает охотно, сразу начинает плакать « не знаю, что со мной постоянно плачу Обманы восприятия отрицает «раньше были голоса, сейчас не слышу» Мышление паралогичное, непоследовательное. Сообщает, что «мысли путаются, наплывают друг на друга, плохие мысли приходят в голову, что что-то плохое случится». Высказывает бредовые идеи самоуничтожения, самообвинения « дети у меня хорошие, а я сама очень плохая, все время только плохое думаю» Речь тихая, медленная Больная отмечает снижение настроения, тревожность, страх, плаксивость
Трифтазин. С целью антипсихотического действия.
Rp: Tab. Triftazini 0,005
D.t.d: №100 in tab.
S: По 1 таблетке 2 раза в день.
Циклодол С целью предупреждения экстрапирамидных побочных эффектов от приема трифтазина.
Rp: Tab. Cyclodoli 0,001
D.t.d: №10 in tab.
S: Внутрь по 1 таблетке 3 раза в день.
Элениум 10 мг на ночь в связи с бессонницей
Rр.: Tab. Chlordiazepoxiddi 0,5
№20
D.S. по 2 таблетки перед сном
Р-р физ 200мл +Амитриптилин 2мл. С целью антидепрессивного действия
Rp.: Sol. Amitriptylini 1% — 2 ml D.t.d. № 10 in amp. S. в/в развести в физ. р-ре 200мл
Предъявляет жалобы на слабость, отсутствие желания что-либо делать. Временами плачет без видимых причин. Остается тревожной, напряженной
Ночью спала хорошо, ест хорошо. Меньше плачет, много времени проводит в постели.. Отмечает слабость, уменьшение тревоги
Неблагоприятный (учитывая возраст начала заболевания, длительность, а так же признаки шизофренического дефекта).
Лечебно-профилактические рекомендации при выписке
-Наблюдение психиатра.
-Соблюдение режима дня и исключение чрезмерных психических и физических нагрузок, психотравмирующих ситуаций.
-Аутотренинг.
-Трудотерапия.
-Ежедневный прием лекарств
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Увлечёшься девушкой-вырастут хвосты, займёшься учебой-вырастут рога 9420 — 

193.124.117.139 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
При недостатке железа в организме в меньшем количестве образуется гемоглобин, необходимый для переноса кислорода. В результате этого человек входит в состояние кислородного голодания, наступают патологические изменения во всех органах и тканях, ведь кислород является основой для всех обменных процессов. Возникают жалобы в виде слабости, снижения работоспособности, головокружения, головной боли или учащения пульса.
Именно благодаря молекуле железа гемоглобин способен присоединить и перенести кислород. Нехватку железа можно восполнить приемом лекарственных средств, а также с пищей. Продукты, содержащие железо, уберегут от анемии. Но нужно помнить, что железо из пищи усваивается только на 20%, к тому же существуют несколько условий для эффективного его усваивания. Питание при анемии должно быть дробным, не менее 5 раз в день. Также должен быть налажен питьевой режим (в расчете около 50 мл/кг веса пациента в сутки). Недостаток воды в организме также замедляет процессы кроветворения.
- В рационе должно быть достаточное количество животного белка (до 150 грамм в сутки). Он необходим для построения гема – белковой части гемоглобина. Предпочтение отдается говядине, телятине, так как кроме белков она содержит готовый гем животных. Такие продукты как печень не содержат гема, поэтому железо из них поступает не в чистом виде, а в составе сложных веществ (ферритина, гемосидерина).
- Животные жиры, наоборот, должны быть ограничены (не более 80 грамм в сутки). Липиды затрудняют кроветворение (процесс образования клеток крови) и нарушают работу печени – одного из главных органов кроветворной системы. Кроме этого, жиры засоряют сосуды и препятствуют поступлению кислорода из крови в ткани.
- Углеводы в виде каш, фруктов и меда не ограничиваются.
- Витамины и растительная клетчатка, содержащаяся в овощах и фруктах, должны употребляться ежедневно в неограниченных количествах. Клетчатка поможет нормальному функционированию кишечника и очищению его от шлаков. Это, в свою очередь, улучшит всасывание полезных веществ из пищи в кишечнике.
Продукты, содержащие повышенное количество железа:
- мясо и мясные продукты (говяжий язык, телятина, кролик индюшатина);
- белые грибы содержат больше железа, чем мясо;
- крупы (гречневая и овсяная);
- овощи (бобовые, зеленая фасоль, морковь, свекла, зелень). Особенно полезны свежевыжатые соки;
- фрукты и ягоды (яблоки, земляника, черника, чернослив, абрикосы);
- какао, шоколад, мед.
Как уже было сказано, для усваивания железа необходимо несколько условий. В первую очередь, это некоторые микроэлементы и витамины:
- кобальт (содержится в бобовых, печени и почках животных, молоке и молочных продуктах, черной смородине, малине, крыжовнике, вишне, груше и свекле);
- медь (ее источником являются крупы, арбузы, грибы и хрен);
- цинком богаты дрожжи, легкие животных, твердые сыры, яйца;
- марганцем насытит организм любая зелень (петрушка, укроп, щавель, шпинат), а также овощи (тыква, свекла) и ягоды (малина, черная смородина);
- витамин С (аскорбиновая кислота) содержится в черной смородине, капусте, лимоне.
Конечно, есть медикаментозные препараты, содержащие комплекс витаминов и микроэлементов, но к ним лучше прибегать, когда нет возможности употребления натуральных продуктов, например, в зимнее время.
Этот продукт пчеловодства обладает уникальным составом, в который входят необходимые для всасывания железа микроэлементы и фруктоза (фруктовый сахар). Врачи рекомендуют именно темный мед. Он в большем количестве содержит железо, марганец и медь, чем светлый мед. При употреблении меда нужно учитывать кислотность желудочного сока пациента. При повышенной кислотности мед нужно принимать не позже чем за 2 часа до приема пищи, при пониженной кислотности – за полчаса до еды.
Недостаток витамина С можно возместить и травяными отварами из веточек или листьев черной смородины, плодов шиповника или бузины. Хорошим лечебным эффектом обладает сбор из веточек черной смородины, плодов земляники, листа череды и крапивы. Продукты, замедляющие процесс всасывания железа:
- молоко и молочные продукты содержат большое количество кальция, который затрудняет усваивание железа;
- сало и жирные сорта мяса (баранина, гусь, утка, свинина) содержат большое количество жиров, мешающих образованию клеток крови;
- алкоголь и крепкий кофе;
- хлебобулочные изделия содержат вещества, уменьшающие всасывание железа.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Железодефицитная анемия (ЖДА) представляет собой клинико–гематологический синдром, возникающий при развитии дефицита железа вследствие различных патологических (физиологических) процессов и характеризующийся снижением уровня гемоглобина (в меньшей степени эритроцитов) наряду с клиническими признаками анемии и сидеропении.
Клинические рекомендации ведения больных ЖДА включают: – выявление причины ЖДА и при необходимости – ее коррекция; – обучение больных ЖДА; – принятие решения о назначении лекарственных препаратов железа (ПЖ); – выбор лекарственного ПЖ; – путь введения ПЖ (внутрь или парентерально); – длительность лечения и необходимость поддерживающей терапии; – контроль переносимости ПЖ и коррекция при плохой переносимости; – оценку эффективности и выявление причин отсутствия или недостаточного эффекта; – коррекцию выявленных причин неэффективности.
Выявление причины ЖДА и возможности ее коррекции
После верификации железодефицитного характера анемии, т.е. синдрома ЖДА, необходимо выявление причины, лежащей в основе данного варианта анемического синдрома (нозологическая диагностика). Для клинициста этот этап является не менее важным и вместе с тем наиболее трудным и ответственным, поскольку в основе имеющейся ЖДА могут лежать потенциально курабельные заболевания. Наличие в МКБ–10 рубрики «Железодефицитная анемия неуточненная» оставляет для врача «лазейку» в случаях отсутствия явной причины анемии, «освобождая» его от тщательности и углубления диагностического поиска на этапе нозологической диагностики. Следует особо подчеркнуть роль врача–интерниста на этапах синдромной и нозологической диагностики, поскольку подавляющее большинство больных ЖДА (независимо от конкретной причины) обращаются прежде всего, как и многие другие пациенты, к терапевту, а не к гематологу или другому специалисту. При выявлении причины ЖДА лечение должно быть направлено на устранение этой причины (по возможности) или коррекцию имеющихся нарушений – лечение эрозивно–язвенных процессов в желудке, оперативные лечения при опухолях ЖКТ, миоме матки, лечение энтеритов, коррекция алиментарной недостаточностии т.д.
Существенным компонентом ведения больных ЖДА является повышение их образовательного уровня в отношении данной патологии, создание мотивации к лечению, вовлечение пациентов в контроль за своим состоянием и лабораторными показателями. Необходимо разъяснение сущности ЖДА, причин ее возникновения, реальных возможностей коррекции дефицита железа и нормализации уровня гемоглобина. Особое значение имеют обучающие программы у беременных женщин с наличием ЖДА и пациенток, страдающих меноррагиями. У беременных должна создаваться мотивация необходимости коррекции дефицита железа с целью предотвращения недостатка железа у плода. Больные должны быть осведомлены о возможных побочных эффектах при лечении лекарственными препаратами железа, необходимости соблюдения врачебных назначений, в том числе и регулярности приема ПЖ. Следует обязательно указать на недопустимость попыток коррекции дефицита железа с помощью различных пищевых продуктов, а также на строгие показания к назначению инъекционных форм ПЖ.
Принятие решения о назначении лекарственных препаратов железа
Всем больным ЖДА показана патогенетическая терапия препаратами железа. Следует подчеркнуть ошибочность мнения о возможности коррекции дефицита железа с помощью пищевых продуктов с высоким содержанием железа, что является одним из мифов в представлениях о ведении больных ЖДА. Об этом должны быть осведомлены больные, что следует считать важным образовательным компонентом ведения данной категории пациентов. Разумеется, пища должна быть богата продуктами, содержащими железо. Однако следует иметь в виду неодинаковую степень всасываемости железа из различных продуктов. Так например, железо, содержащееся в мясе в виде гема, всасывается на 40–50%, в то время как из растительных продуктов, овощей, фруктов всасывается всего 3–5% содержащегося в них железа. Поэтому средством выбора для коррекции дефицита железа и уровня гемоглобина у больных ЖДА являются лекарственные препараты железа. На фармацевтическом рынке России в настоящее время имеется большой арсенал ПЖ в различных лекарственных формах, с неодинаковым содержанием в них железа, наличием дополнительных компонентов, влияющих на биодоступность железа, различной стоимостью (рис. 1). Из ПСЖ железо всасывается в двухвалентной форме, в последующем превращается в трехвалетное, которое связывается с трансферрином и используется для построения молекулы гемоглобина. В ПЖК железо находится в трехвалентной форме и всасывается как бы в готовом виде. В ПЖК, в частности, в гидрооксиполимальтозном комплексе, связано как в физиологическом состоянии в молекуле ферритина. Существуют различия в механизмах всасывания железа из ПСЖ и ПЖК. Всасывание железа из ПСЖ происходит главным образом в виде пассивной диффузии согласно градиенту концентрации и в меньшей степени активно, в то время как абсорбция железа из ПЖК является активным процессом в виде конкурентного обмена. Это ведет к различному уровню железа в сыворотке, объему распределения, константам элиминации после абсорбции. Всасывание железа из ПЖК и нарастание его концентрации в сыворотке происходит медленно, но оно быстро поступает в запасы. При применении ПСЖ могут возникать нарушения окислительных процессов (оксидативные повреждения) вследствие превращения ионов двухвалентного железа в трехвалентное, которое соединяется с трансферрином и включается в молекулу гемоглобина. При окислении образуются свободные радикалы, которые вызывают клеточные повреждения, такие как перекисное окисление липидов, нарушение структуры мембранных и клеточных белков, повреждение клеточной ДНК и РНК. ПЖК в отличие от ПСЖ не вызывают «оксидативного стресса», поскольку ионы железа не меняют свою валентность в процессе всасывания (табл. 1). Для лучшей абсорбции ПСЖ рекомендуется принимать за час до еды т.е. на пустой желудок, что может вызывать нарушения со стороны желудка, кишечника и другие побочные эффекты. Современные технологии производства препаратов железа позволяют производить ПСЖ с замедленным высвобождением железа в тонком кишечнике, что уменьшает токсическое воздействие ионов железа на слизистую желудка. Частота побочных эффектов при лечении ПЖК меньше по сравнении с ПСЖ, что обеспечивает лучший комплайенс больных ЖДА. ПСЖ взаимодействуют с некоторыми пищевыми продуктами (танин, фитаты, соли кальция) и медикаментами (пленкообразующие препараты, тетрациклины, препараты кальция), снижающими биодоступность железа. В связи с этим ПСЖ не следует принимать одновременно с указанными пищевыми продуктами и лекарственными препаратами. В то же время пища и медикаменты не оказывают влияния на всасывание железа из ПЖК. Темпы прироста показателей гемоглобина при применении ПСЖ и ПЖК примерно одинаковые.
Путь введения препаратов железа
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний ПЖ следует назначать внутрь. Путь введения ПЖ у больных ЖДА определяется конкретной клинической ситуацией, в частности, состоянием кишечного всасывания и переносимостью пероральных ПЖ.
Основными показаниями для парентерального введения ПЖ являются: – патологии кишечника с нарушением всасывания (различные энтериты, синдром недостаточности всасывания); – резекция тонкой кишки; – резекция желудка по Бильрот II с формированием «слепой петли»; – эрозивно–язвенные процессы в желудке (обострение язвенной болезни и др.); – непереносимость ПЖ для приема внутрь. Многие врачи обосновывают назначение парентеральных ПЖ выраженностью анемического синдрома в расчете на якобы больший их эффект, что также не имеет достаточных оснований и не подтверждается клинической практикой. Темпы прироста уровня гемоглобина при назначении ПЖ внутрь и парентерально оказались приблизительно одинаковыми, в связи с чем предпочтение ПЖ в инъекционных формах при необходимости более быстрой нормализации содержания гемоглобина (например, при подготовке к оперативному вмешательству) следует считать неоправданным. ПЖ для парентерального введения могут назначаться при плохой переносимости пероральных ПЖ, однако большинство современных ПСЖ и ПЖК переносятся сравнительно удовлетворительно. В связи с этим принятие решения о назначении парентерального ПЖ должно осуществляться только после ряда «врачебных маневров» (снижение дозы ПЖ, прием вместе с пищей, смена ПЖ для приема внутрь и т.д.).
Выбор лекарственного препарата железа
Выбор ПЖ и оптимального режима его дозирования должен определяться количеством и биодоступностью содержащегося в нем железа, переносимостью, стоимостью. При этом необходимо иметь в виду, что адекватный прирост показателей гемоглобина у больных ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг элементарного железа . Учитывая, что при развитии ЖДА всасывание железа увеличивается по сравнению с нормой и составляет 25–30% (при нормальных запасах железа – всего 3–7%), необходимо назначать от 100 до 300 мг элементарного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. С учетом этого при выборе ПЖ следует ориентироваться не на содержание в нем общего количества соединения железа, а на количество элементарного железа. Например, при назначении препаратов сульфата железа с низким содержанием элементарного железа (менее 100 мг) количество принимаемых таблеток должно быть от 3 и выше (в зависимости от содержания железа в каждой таблетке), в то время как препараты сульфата, фумарата или гидроксиполимальтозного комплекса железа с содержанием 100 мг элементарного железа можно принимать в количестве 1–2 таблеток в сутки. Основные ПСЖ представлены сульфатом железа, глюконатом, хлоридом, фумаратом, глицин сульфатом. Наибольшей степенью абсорбции обладают препараты сульфата железа, а наименьшей – глицин сульфата. Многие из ПСЖ содержат вещества, например, аскорбиновую кислоту, усиливающие всасывание железа и улучшающие биодоступность препарата, а также витамины (фолиевую кислоту, цианкобаламин). Среди ПЖК на отечественно рынке имеются гидроксиполимальтозный комплекс, железо–сорбитоловый комплекс, протеин сукцинилат железа, железо–сахарозный комплекс. К новым высокоэффективным и безопасным препаратам железа относятся препараты, представляющие собой неионные соединения железа на основе гидроксиполимальтозного комплекса (ГПК) трехвалентного железа. Структура комплекса состоит из многоядерных центров гидроксида Fe (III), окруженных нековалентно связанными молекулами полимальтозы. Комплекс имеет большой молекулярный вес, что затрудняет его диффузию через мембрану слизистой кишечника. Химическая структура комплекса максимально приближена к структуре естественных соединений железа с ферритином. Абсорбция железа в виде ГПК имеет принципиально иную схему по сравнению с его ионными соединениями и обеспечивается поступлением Fe (III) из кишечника в кровь путем активного всасывания. Неионная структура комплекса обеспечивает его стабильность и перенос железа с помощью транспортного белка, что предотвращает в организме свободную диффузию ионов железа, т.е. прооксидантные реакции. Данные по безопасности, полученные во время клинических исследований препарата железа на основе гидроксида Fe (III) с полимальтозой, свидетельствуют о более низкой частоте побочных эффектов по сравнению с солевыми препаратами железа. Для лучшей переносимости ПСЖ следует принимать во время еды, хотя следует иметь в виду, что всасывание железа лучше при приеме лекарственных препаратов перед едой. Всасываниежелеза может уменьшаться под влиянием содержащихся в некоторых пищевых продуктах веществ – фитинов (рис, соя), фосфатов (рыба, морепродукты), танина (чай, кофе). Многие больные склонны запивать лекарства чаем, что в случаях приема ПЖ в виде солей недопустимо, поскольку образуются плохо растворимые комплексы с низкой их абсорбцией в кишечнике. Кроме того, всасывание железа из ПЖ в виде солей ухудшается при одновременном приеме ряда медикаментов (тетрациклины, антациды, соли магния). С учетом этого следует рекомендовать прием препаратов солей железа в различное время с другими вышеуказанными медикаментами. Препараты ПЖК, в частности, гидроксиполимальтозный комплекс лишены подобных недостатков, поскольку пищевые продукты и медикаменты не оказывают влияние на всасываемость железа (в виде трехвалентной формы) из железосодержащих комплексов. В таблице 2 представлены основные зарегистрированные в России лекарственные ПСЖ и ПЖК для приема внутрь.
Оценка эффективности лечения
В случаях назначения ПЖ в достаточной дозе на 7–10–й день от начала лечения наблюдается повышение количества ретикулоцитов. Достоверное повышение уровня гемоглобина отмечается через 3–4 нед. от начала лечения. Нормализация показателей гемоглобина обычно происходит в сроки 4–9 нед. Иногда наблюдается резкое скачкообразное повышение гемоглобина. Эти индивидуальные колебания могут быть обусловлены, с одной стороны, выраженностью ЖДА, степенью истощения запасов железа, а с другой – эффективностью назначенного ПЖ (количество содержащегося железа, биодоступность и др.). Имеет также значение некомплаентность больных (нерегулярность приема ПЖ, побочные эффекты).
Длительность лечения и поддерживающая терапия
Оптимальная тактика ведения больных ЖДА предполагает насыщающую и поддерживающую терапию ПЖ. Длительность насыщающей терапии зависит от темпов прироста и сроков нормализации показателей гемоглобина, составляя в среднем 4–6 недель. Поддерживающая терапия показана в тех ситуациях, когда причина дефицита железа сохраняется (меноррагии, беременность) или в силу различных ситуаций является трудноустранимой (патология кишечника, носовые и другие кровотечения при геморрагических диатезах). Женщинам, страдающим ЖДА на фоне меноррагий, после нормализации показателей гемоглобина рекомендуется поддерживающая терапия ПЖ в течение 5–7 дней после очередной менструации. Больным надо разъяснять необходимость поддерживающего лечения в связи с продолжающимися избыточными потерями железа. Беременные с ЖДА должны получать ПЖ до конца беременности в целях обеспечения адекватной потребности плода в железе.
Переносимость препаратов железа
Среди побочных эффектов на фоне применения ПЖ внутрь наиболее часто возникают тошнота, анорексия, металлический вкус во рту, запоры, реже – поносы. Развитие запоров обусловлено, по всей вероятности, связыванием в кишечнике сероводорода, являющегося одним из стимулов кишечной перистальтики. В большинстве случаев современные ПЖ вызывают незначительные побочные явления, не требующие их отмены и перехода на парентеральный путь введения. Диспептические расстройства могут уменьшаться при приеме препаратов после еды или уменьшения суточной дозы препарата. Чаще побочные эффекты регистрируютсяпри приеме ПСЖ, в то время как препараты ПЖК (гидроксиполимальтозный комплекс) переносятся лучше и имеют в связи с этим определенные преимущества. В случаях сохраняющейся плохой переносимости пероральных ПЖ показано назначение ПЖ парентерально (внутримышечно или внутривенно). На фоне лечения парентеральными ПЖ, особенно для внутривенного введения, могут возникать аллергические реакции в виде крапивницы, лихорадка, флебиты, анафилактический шок. Кроме того, при внутримышечном введении ПЖ возможно потемнение кожи в местах инъекций, инфильтраты, абсцессы. Если ПЖ для парентерального введения назначают больным гипохромной анемией, не связанной с дефицитом железа, имеется повышенный риск возникновения тяжелых нарушений из–за «перегрузки» железом различных органов и тканей (печень, поджелудочная железа и др.) с развитием гемосидероза.
Причины неэффективности лечения препаратами железа
В случае отсутствия или недостаточного эффекта от лечения ПЖ следует выяснить причину с целью возможности ее коррекции. Возможные причины неэффективности лечения ПЖ и способы их коррекции представлены в таблице 3. Необходима убежденность в правильной трактовке всех клинико–лабораторных признаков и в достоверности синдрома ЖДА. Причиной отсутствия или недостаточной эффективности ПЖ может быть недостаточная суточная доза железа, что обычно связано с назначением ПЖ с низким содержанием в нем железа и малым количеством принимаемых таблеток. Так, например, при лечении препаратом, в котором содержится всего лишь 10 мг двухвалентного железа, число принимаемых таблеток должно быть не менее 10 в сутки. Такой режим дозирования неудобен для больных, чем и объясняется, вероятнее всего, невыполнение ими врачебного назначения. С учетом вышесказанного для обеспечения комплаентности следует назначать ПЖ с высоким содержанием железа (не менее 100 мг). Препараты с низким содержанием железа целесообразно использовать в педиатрической практике. Одной из причин неэффективности ПЖ при назначении внутрь может быть нарушение всасывания железа, в частности, у больных с невыявленной или недооцененной кишечной патологией. В этих случаях показано назначение парентеральных ПЖ. В ряде случаев вследствие улучшения самочувствия больные начинают нерегулярно принимать ПЖ или вообще прекращают лечение. В результате показатели гемоглобина не достигают нормальных значений и ЖДА при этом остается фактически недолеченной. С учетом этого длительность насыщающей терапии ПЖ должна определяться сроками достижения нормального уровня гемоглобина, что требует постоянного лабораторного мониторинга. Ряд больных не всегда выполняют назначение врача (регулярность приема ПЖ, достаточная продолжительность и т.д.). В некоторых случаях это может быть обусловлено развитиемпобочных эффектов от ПЖ и самостоятельным прекращением лечения. Поэтому необходим контроль за лечением, эффективностью, переносимостью ПЖ со стороны врача, среднего медперсонала, родственников больных. Отсутствие эффекта от ПЖ может быть связано с неустраненными причинами ЖДА, среди которых клинически наиболее значимыми являются скрытые кровопотери из желудочно–кишечного тракта, чаще из кишечника (невыявленная опухоль!). С учетом этого в подобных ситуациях при исключении других возможных причин неэффективности ПЖ необходимо тщательное эндоскопическое исследование кишечника (в ряде случаев – повторное). Таким образом, у больных ЖДА наряду с устранением причины обязательна патогенетическая терапия ПЖ (ПСЖ и ПЖК), которые должны назначаться преимущественно внутрь. Тактика лечения ПЖ предусматривает выбор пути введения ПЖ с учетом клинической ситуации, оптимального ПЖ с достаточным содержанием в нем железа, оценку эффективности и переносимости препарата, длительность насыщающей и обоснованность поддерживающей терапии. Своевременная верификация синдрома ЖДА и выявление ее причины, адекватная патогенетическая терапия с назначением ПЖ с оптимальными фармакокинетическими свойствами, клинической эффективностью, переносимостью позволяет корригировать анемический синдром и обеспечивать достаточный уровень качества жизни у данной категории пациентов.
источник
Правильное питание при анемии для пациентов направлено на восстановление процесса кроветворения и нормализацию состава крови. Помимо употребления продуктов, богатых железом, при анемии важно больше времени проводить на свежем воздухе, полноценно отдыхать и соблюдать остальные правила, предусмотренные вашим лечащим врачом.
Если у вас была диагностирована лёгкая стадия малокровия, тогда лечение будет заключаться только в соблюдении диеты. При средней и тяжёлой формах используются дополнительно медикаменты, витамины и другие полезные вещества в виде лекарственных препаратов. Но соблюдать правила диеты всё равно нужно и дальше.
В диетотерапии, направленной против малокровия, есть свои правила, особенности, ограничения и рекомендации. Даже полезные продукты могут оказать негативное воздействие на ваш организм. Потому старайтесь употреблять только то, что одобрят ваш лечащий врач и диетолог.
Чтобы не называть целый перечень продуктов, которые нельзя есть во время диеты против анемии или следует ограничить, рассмотрим наиболее вредные вещества.
Больным нужно избегать употребления:
Эти вещества способствуют тому, что нарушается всасываемость железа. Потому если у вас обнаружена железодефицитная форма малокровия, как самая распространённая в мире (95% всех случаев анемии), то ограничивайте в рационе продукты, содержание эти компоненты.
Кальций необходим каждому, особенно детям в период их роста и развития. Но, кроме пользы, кальций нарушает процессы всасывания. Наибольшая его концентрация в молочной продукции, потому не стройте диету, основываясь на ней.
Оксалаты являются ещё одним компонентом, который мешает нормальному всасыванию железа. Они содержатся в орехах (грецких), бобовых культурах, цельном зерне, шпинате, шоколаде и прочих продуктах. Хотя тут есть выход из ситуации. Если вы любите бобовые, просто замочите их в воде, выдержав 12 часов. Это заметно снизит негативное воздействие на организм, позволив насладиться блюдами из этих продуктов.
Полифенолы считаются главными ингибиторами всасывания. Наибольшая концентрация в чёрных сортах чая и кофе. Какао и некоторые травяные чаи тоже придётся ограничить. Никакого кофе, ведь он на 60% способен блокировать всасываемость организмом железа.
Чтобы правильно питаться при анемии, вам необходимо отказаться от наиболее вредной и опасной пищи. Старайтесь не употреблять в пищу большое количество жиров. Они способствуют угнетению процессов образования крови. Суточная норма жиров составляет до 80 грамм.
Это ограничение относится к чистому животному жиру, жирным сортам рыбы. Если вы будете питаться диетическим мясом и птицей, то принесёте только пользу своему организму. А опасный жир стоит заменить растительными маслами.
Из названия понятно, что причиной развития железодефицитной анемии выступает нехватка в организме такого вещества, как железо. Чтобы справиться с проблемой, нужно обеспечить кровь этим элементом через продукты, которые его содержат.
К причинам развития патологии относят:
- плохое питание;
- чрезмерную физическая активность и усталость;
- длительное голодание;
- соблюдение строгих диет;
- внутренние кровотечения;
- злокачественные новообразования.
В последних двух случаях простой корректировкой рациона проблему не решить. Здесь придётся обращаться за помощью и заниматься сложным длительным лечением.
Если же причины не связаны с опасными патологиями, тогда восстановить образование крови и вернуть человека к нормальному самочувствию поможет правильно построенная диета.
Здесь есть несколько основных правил питания, которых нужно придерживаться.
- Употребление продуктов, богатых железом, при анемии способствует восстановлению количества этого вещества в крови. Поднимается гемоглобин и восстанавливается хорошее самочувствие;
- Железосодержащие продукты при анемии употребляют в виде белковой пищи (не больше 120 грамм в сутки), фруктов и различных овощей. Количество жиров снижается до 40 грамм. Обязательно делается упор на ягоды, зелень и свежие соки.
- При диетической терапии соблюдайте правило, которое предусматривает одновременное употребление железосодержащих блюд и витамина С. Последний помогает нормализовать всасываемость и усвоение вещества в организме человека.
- Поскольку молочные продукты кушать нужно из-за наличия в них кальция, сделайте их отдельным приёмом пищи. Иначе кальций не позволит железу усваиваться.
Только квалифицированные специалисты могут точно сказать своим пациентам, что есть при анемиях. Это объясняется необходимостью сначала сдать анализы, провести некоторые исследования и определить причины развития малокровия.
Строить диеты самостоятельно не рекомендуется. Путём анализов следует определить, чего в организме не хватает, в каких веществах ощущается нехватка, и на какие продукты есть аллергия.
Хотя заболевание встречается реже по сравнению с детьми, но при анемии у взрослых патология протекает сложнее, и на лечение уходит больше времени. В основном к такому состоянию приводят тяжёлые физические нагрузки, сильная утомляемость на работе вместе с отсутствием нормального, разнообразного и сбалансированного питания.
Для них питание при анемии основано на повышении количества потребляемого белка, необходимых микроэлементов и витаминов. Что нужно есть и в каком количестве, скажет лечащий врач. Для взрослых рекомендуется соблюдение такой суточной схемы:
- не более 120 граммов белка в течение дня;
- максимум 40 грамм жира в сутки;
- до 450 грамм углеводов, потребляемых за день;
- средний показатель калорийности составляет от 2,5 до 3 тысяч ккал.
Для получения всего необходимого еда взрослого человека с малокровием должна включать фрукты и овощи. Упор делается на:
Этот список условный. В него включены продукты, богатые на железо и его соединения. Но у каждого взрослого могут иметься свои индивидуальные противопоказания, аллергия и непереносимость.
Питание при анемии у женщин, которые находятся в положении, будет отличаться. Среди беременных малокровие считается довольно распространённым нарушением, которое способно негативно влиять на рост и развитие плода. Это потенциально высокая угроза для ребёнка.
Диета при анемии является частью комплексной терапии, рекомендованной для беременных при выявлении этого заболевания. Кроме правильно подобранных продуктов, в состав терапии входит приём лекарственных препаратов и витаминов.
Развитие малокровия объясняется несколькими причинами:
- растёт потребность организма в питательных веществах из-за развития плода;
- организм мамы является единственным источником питания для малыша;
- объём циркулирующей крови увеличивается, из-за чего растёт и количество клеток крови.
Не зря существует фраза, что беременные питаются за двоих. Это так, потому прежнего количества пищи уже недостаточно для нормального функционирования женского организма и растущего внутри него плода.
Диета беременной основывается на:
Будьте осторожными с каждым из продуктов, поскольку многие из них выступают потенциальными аллергенами. Прежде чем есть цитрусовые, некоторые овощи, ягоды и рыбу, проконсультируйтесь со своим врачом. Он даст рекомендации по подбору наиболее полезной и безопасной для малыша пищи.
Если малокровие обусловлено дефицитом витаминов группы В, тогда придётся отказаться от молока, яиц и всего мясного.
При анемии у пожилых людей есть свои особенности составления рациона. Малокровие считается распространённой патологией людей преклонного и старческого возраста. Это объясняется началом малоподвижного образа жизни, целым букетом хронических заболеваний и сокращением функций и дееспособности иммунной системы.
Здесь врачи дают важные рекомендации касательно того, как питаться. Важно не допускать приступов голода, но и не переедать. То есть кушать следует регулярно, но небольшими порциями.
Такое правило связано с тем, что органы и системы начинают стареть. Физиологически пищеварительная система не способна работать так же, как у молодых людей. Потому переедания перегружают систему, а голодание отрицательно сказывается на дальнейшей усвояемости еды.
Нет конкретных запретов на употребление пищи. Но упор лучше сделать на:
- качественное нежирное мясо;
- молочные продукты;
- фрукты;
- зелень;
- свежие сезонные ягоды и овощи.
Важно получать все необходимые витамины при анемии в достаточном количестве. Потому ошибкой считается переход на вегетарианское меню. Пожилой организм не может быстро и эффективно перестроиться под новый вариант питания, потому это негативно отразится на его состоянии.
Постарайтесь есть по 2 – 4 яйца за неделю, употреблять больше гречки, свёклы и капусты. А вот от бобовых стоит отказаться, ведь они плохо усваиваются организмом в этом возрасте.
Хорошим решением станет измельчение полезных растительных продуктов с помощью блендера или мясорубки. Это позволит есть такую пищу людям, у которых проблемы с пищеварением или слабые зубы. Перетёртая и измельчённая еда быстрее переваривается, на неё затрачивается меньше сил и энергии.
С едой для детей проблем намного меньше. Им можно давать больше разнообразных продуктов. Важно организовать разнообразное и аппетитное меню, чтобы у ребёнка возникало желание съесть что-нибудь полезное и вкусненькое.
Удостоверьтесь, что за сутки ваш ребёнок съедает:
Если малокровие находится в средней стадии, тогда от большого количества жиров лучше отказаться. Вместо них включите продукты, богатые на железо, витамины А, В и С. Отлично подойдут печень, язык, бобовые, крупы, пюре из овощей и рагу. Если вы правильно и оригинально приготовите эти продукты, дети будут кушать их с огромным удовольствием.
Для компенсации недостающего витамина А добавьте в повседневный рацион морскую рыбу. А витамин В получают из говядины, чернослива и бобовых.
Если дети отказываются кушать печень, тогда придётся идти на небольшие хитрости. Для этого её измельчают, добавляя в пюре, кашу и прочие блюда. Взрослым детям рекомендуется делать домашние печёночные паштеты и готовить из печени запеканки. Жарить её не рекомендуется.
Проблема малокровия характерна для той категории детей, которые придерживаются слишком однообразного питания. Нет ничего плохого в том, что ребёнок любит вкусные мясные сосиски с макаронами из твёрдых сортов, йогурты или другие полезные блюда. Некоторые могут есть такое по несколько раз в день. Родителям проще, поскольку ничего выдумывать не приходится. Но в однообразном рационе наблюдается нехватка ряда витаминов, минералов и микроэлементов, которые можно получить только из других продуктов, которые дети не едят.
Ещё одной распространённой ошибкой родителей при коррекции меню для детей при малокровии является попытка заставить кушать то или иное блюдо. Когда малыша заставляют что-то съесть, это ещё больше отталкивает его от пищи. Лучше попробуйте приготовить что-то вместе, позвольте ему принять участие в готовке. Разносящиеся ароматы будут стимулировать питание, а участие в процессе заставить сильно захотеть попробовать то, что он приготовил своими руками.
Суть правильного питания при возникновении малокровия или анемии у людей разного возраста состоит в разнообразии меню. Используйте разную вкусную и аппетитную еду. Список продуктов обширный, что позволяет выбирать оптимальный перечень блюд для своей диеты.
Правильное питание не является панацеей против анемии. Чтобы справиться с этим заболеванием, нужно определить первопричину его развития. Избавившись от неё, вы сможете вернуться к нормальной жизни, устранить неприятные симптомы и восстановить все функции своего организма. Полезная пища способна поддерживать состояние здоровья и частично компенсировать нехватку ряда витаминов, минералов и микроэлементов. Хотя иногда без помощи лекарственных препаратов не обойтись.
Правильная и здоровая пища полезна всегда и для всех. Придерживаясь правил питания, можно предотвратить целый ряд опасных патологий и заболеваний, включая малокровие. Но заметив первые же признаки анемии, сразу обращайтесь за помощью к квалифицированному врачу. Только он поставит точный диагноз и даст конкретные рекомендации по лечению и питанию для борьбы с недугом.
Спасибо всем вам за внимание! Обязательно подписывайтесь, не забывайтесь оставлять комментарии, задавать интересующие вас вопросы и приглашать к обсуждению своих друзей!
источник
Н.И. Стуклов, Е.Н. Семенова
ФГБОУ ВПО Российский университет дружбы народов, Москва
Рассмотрен современный взгляд на проблему железодефицитной анемии (ЖДА) с точки зрения эпидемиологии, этиологии, патогенеза. Описаны известные в настоящее время механизмы регуляции обмена железа, приведены наиболее важные данные литературы и результаты собственных исследований. Основываясь на рекомендациях по лечению больных ЖДА, авторы представляют описанный в литературе и собственный клинический опыт использования железосодержащих препаратов и рассматривают полученные результаты. В рамках статьи авторы объясняют механизмы низкой эффективности лечения при ЖДА и предлагают способы решения проблемы с учетом опубликованных в литературе последних научных исследований.
Ключевые слова: анемия; обмен железа; сидеропенический синдром; лечение железодефицитной анемии.
N.I. Stuklov, E.N. Semenova
Russian University of People’s Friendship, Moscow, Russia
Modern views of epidemiology, etiology and pathogenesis of iron deficiency anemia are considered. Mechanisms of iron metabolism regulation are described based on the most important literature data and the results of the authors ’ research. The authors present their own and literature clinical experience of using iron-containing drugs with reference to the existing recommendations on the treatment of iron deficiency anemia. Causes of low treatment efficiency are discussed and the ways to address this problem are proposed based on the published results of clinical research.
Key words: anemia; iron metabolism; sideropenic syndrome; treatment of iron deficiency anemia.
Анемии (греч. αναιμια — бескровие) определяются как ряд клинических состояний, связанных со снижением уровня гемоглобина менее 120 г/л у женщин и менее 130 г/л у мужчин; (ВОЗ, 2001) и (или) гематокрита ( менее 36,4% соответственно), что обусловлено уменьшением количества эритроцитов или содержания гемоглобина в них [1]. В настоящее время железодефицитная анемия (ЖДА) является самым распространенным состоянием, связанным со снижением уровня гемоглобина, поэтому ее признают государственной проблемой более чем в 100 странах мира, где разрабатываются программы, направленные на профилактику и снижение заболеваемости. ЖДА чаще выявляется у представителей наиболее социально значимых и незащищенных слоев населения — у женщин детородного возраста и детей. Количество больных анемией в указанных группах, по данным ВОЗ (2001), превышает 1 млрд [2]. В итоге ЖДА является причиной роста материнской и детской смертности [3].
Регуляция обмена железа.
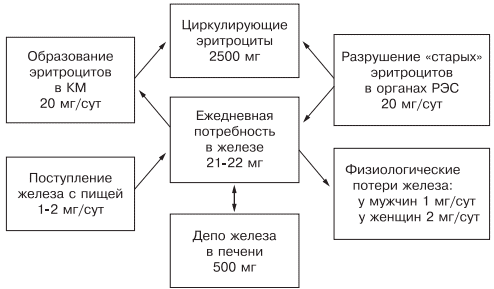
Ежедневно организму для нормальной жизнедеятельности требуется 20—25 мг железа, причем экзогенного железа необходимо только 1— 2 мг: женщинам — 2 мг (из-за физиологической кровопотери), а мужчинам — 1—1,5 мг. Около 20 мг железа поступает из «старых» разрушенных эритроцитов, столько же расходуется на синтез нового гемоглобина.
Железо накапливается в органах ретикулоэндотелиальной системы (до 500 мг), остальные запасы железа на 70% сосредоточены в гемоглобине, что и обусловливает развитие ЖДА при хронической кровопотере (рис. 1).
Рис. 1. Схема обмена железа.
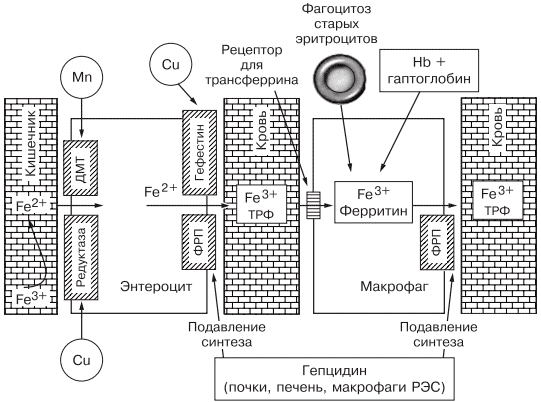
Всасывание железа происходит в верхних отделах тонкой кишки, причем этот процесс требует участия множества белков. В основном до 70—80% железа усваивается в двухвалентном состоянии (гемовое железо, содержащееся в основном в мясе, меньше — в печени и рыбе). При поступлении в кишечник растительного трехвалентного железа с помощью медьзависимой ферроредуктазы на апикальной мембране энтероцитов или под действием витамина С оно восстанавливается до двухвалентного. Двухвалентное железо через марганецзависимые белки — транспортеры двухвалентных металлов (ДМТ — двухвалентный металлотранспортер) поступает в энтероцит, а затем через белок ферропортин на базальной мембране — в кровь, где с помощью медьзависимых феррооксидаз (гефестина, расположенного на базальной мембране и связанного с ферропортином, и церулоплазмина, находящегося в плазме) окисляется до трехвалентного состояния, чтобы связаться с транспортным белком — трансферрином (рис. 2). Только очень незначительная часть железа, образуя комплекс с муцином, может поступить в энтероциты путем пиноцитоза [4, 5].
Рис. 2. Схема регуляции обмена железа.
Универсальным регулятором метаболизма железа является гепцидин [6—9], который блокирует транспорт железа, причем этот механизм реализуется с помощью регуляции активности белка ферропортина, т.е. путем воздействия на высвобождение железа из клеток кишечника и макрофагов ретикулоэндотелиальной системы [10—13]. Увеличение количества железа в организме ведет к стимуляции синтеза гепцидина, что уменьшает абсорбцию железа в кишечнике и его транспорт в циркуляцию. В свою очередь уменьшение абсорбции железа в кишечнике ведет к угнетению синтеза гепцидина в печени и по обратной связи — к восстановлению захвата железа из пищи и кишечника (см. рис. 2) [14—18]. Помимо железорегуляторной функции, гепцидин оказывает выраженное бактерицидное действие, является белком воспаления, его уровень повышается при инфекционных, воспалительных, опухолевых заболеваниях, блокируя выход железа в кровь [6]. Такой эффект гепцидина отрицательно влияет на рост бактерий, опухолей, блокирует избыточный воспалительный процесс. В работе, проведенной в 2011 г. [19], доказана роль гепцидина как основного фактора развития ЖДА у женщин с гинекологическими заболеваниями без патологической кровопотери. Показатели гепцидина в указанной группе составили 108,75 ± 40,08 нг/л (референсные значения 60— 85 нг/л), что обусловило резкое уменьшение содержания ферропортина — 0,43 ± 0,21 нг/л (референсные значения 3,1 ± 0,2 нг/л) и привело к нарушению поступления железа из кишечника в кровь [19].
Железо, которое остается внутри клеток, депонируется в виде ферритина, количество которого в крови прямо пропорционально содержанию железа в депо [20].
Клиническая картина и диагностические критерии.
Дефицит железа приводит к нарушению синтеза гемоглобина в эритрокариоцитах костного мозга, уменьшению содержания миоглобина в мышцах, активности цитохромов и каталаз в митохондриях клеток, миелопероксидазы в нейтрофилах [21—23].
В настоящее время выделяют несколько этапов развития дефицита железа [5, 24].
1. Предрасположенность к развитию дефицита железа (вегетарианство, подростковый возраст в сочетании с нарушением менструального цикла у девочек, частые роды, наличие хронических болезней желудочно-кишечного тракта — ЖКТ, заболеваний женской репродуктивной системы, связанных с кровопотерей).
2. Предлатентный дефицит железа. На этой стадии нет никаких лабораторных критериев дефицита железа, однако можно определить повышение абсорбции трехвалентного железа в ЖКТ, которое может превышать 50% (в норме 10—15%).
3. Латентный дефицит железа характеризуется развитием сидеропенического синдрома и уменьшением запасов железа в организме (по данным лабораторных исследований).
4. ЖДА. Диагноз устанавливается при уровне гомоглобина менее 120 г/л у женщин и 130 г/л у мужчин. Выделяют следующие стадии ЖДА:
В основе патологии эритропоэза при дефиците железа лежит нарушение синтеза гема, в результате которого уменьшается количество гемоглобина в эритрокариоцитах костного мозга, что проявляется на первом этапе гипохромией эритроцитов, а в дальнейшем — развитием гипохромной микроцитарной анемии.
Клинические проявления ЖДА связаны с развитием как сидеропенического синдрома, для которого характерны выраженная мышечная слабость, нарушение целостности слизистых оболочек, кожи, ее придатков (ломкость и расслаивание ногтей, выпадение волос), снижение иммунитета, так и непосредственно симптомов анемии (головокружение, мелькание «мушек» перед глазами, сонливость, снижение работоспособности).
Наиболее характерным лабораторным признаком ЖДА являются гипохромия, микроцитоз эритроцитов, анизоцитоз. О гипохромии эритроцитов свидетельствуют цветовой показатель менее 0,8, среднее содержание гемоглобина в эритроците менее 28 пг, средняя концентрация гемоглобина в эритроците менее 290 г/л. О микроцитозе говорят, когда средний диаметр эритроцита менее 7 мкм, а средний объем эритроцита — менее 80 фл [21, 22, 24].
Параметры обмена железа широко используются в клинической практике, но в связи с отсутствием четко определенных значений, доказывающих наличие ЖДА, высокой стоимостью исследования и большим количеством больных их применение не всегда оправдано. Так, показатель ферритина сыворотки (ФС) как единственный маркер, отражающий запасы железа в организме и используемый для верификации и дифференциальной диагностики ЖДА, по мнению разных исследователей [5, 20], варьирует от 15 до 100 мкг/л. Известно, что показатель ФС является положительным маркером воспаления, а количество его определяется белково-синтетической функцией печени. В настоящее время для установления диагноза ЖДА принято считать достоверным показатель ФС менее 30 мкг/л [25]. Уровень такого транспортного белка, как трансферрин, как правило, повышен при недостатке железа, однако при наличии инфекции его содержание уменьшается и не может использоваться в диагностике ЖДА [26]. Тем более изменчивы такие параметры обмена железа, как железосвязывающая способность (общая и латентная) и коэффициент насыщения трансферрина железом, так как они рассчитываются исходя из содержания трансферрина и сывороточного железа, а последний показатель вообще не имеет связи с содержанием железа в организме и зависит от времени, в которое проведено исследование, и приема пищи [21]. Значения коэффициента насыщения трансферрина железом у больных ЖДА, по опубликованным данным, могут составлять от 15 до 20%. Наиболее точным методом диагностики ЖДА в настоящее время считается подсчет растворимых рецепторов для трансферрина, однако этот метод не используется в качестве рутинного из-за отсутствия единого способа детекции, высокой стоимости исследования, невозможности интерпретировать результат при наличии любых пролиферативных процессов [26].
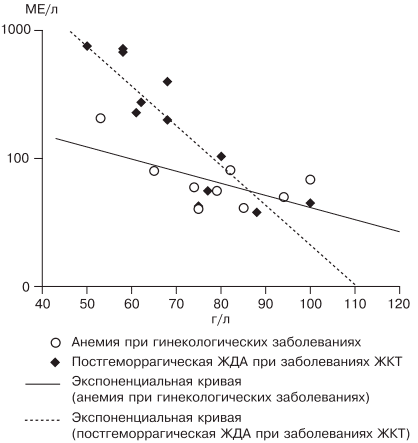
Наиболее частыми причинами ЖДА являются как физиологические, так и патологические состояния. В группу риска развития ЖДА входят недоношенные дети, так как у них не успевает сформироваться депо железа, и подростки, которым требуется больше железа в связи с быстрым ростом организма [27]. Наиболее часто ЖДА развивается при беременности. В период беременности, родов и лактации в среднем расходуется до 1000 мг железа, что в 2 раза больше его запасов в депо [28]. Репродуктивный возраст у женщин связан с повышенной потерей железа при менструациях; этот недостаток компенсируется увеличением всасывания железа в ЖКТ, что в настоящее время объясняется изменением влияния гепцидина. При наличии гиперполименореи, однако, такой баланс нарушается в связи с увеличением кровопотери [29, 30], при сопутствующих заболеваниях ЖКТ нарушается всасывание железа и развивается ЖДА [6, 19]. Часто у женщин меноррагии имеют органические причины: полипы, эндометрит, миома матки, аденомиоз, открывающийся в полость матки; мало того, такие заболевания, как миома матки и дисплазия шейки матки, оказывают влияние на развитие анемии и без патологической кровопотери [5, 19, 30]. Указанный механизм связан с увеличением содержания гепцидина в крови и снижением активности эритропоэза, доказанным синдромом неадекватной выработки эритропоэтина. В настоящее время продукцию эритропоэтина принято считать неадекватной при отношении определяемого эритропоэтина к предполагаемому (О/П log эритропоэтина менее 0,9) [28, 31]. Так, В.А. Бурлевым и Е.Н. Коноводовой [32] при обследовании женщин с миомой матки выявлено отношение О/П log эритропоэтина менее 0,8, а при обследовании гинекологических больных с анемией без нарушения менструальной функции в 2011 г. отношение О/П log эритропоэтина составило 0,89 (рис. 3). Для всех женщин с диагностированной ЖДА необходимо обязательное обследование у гинеколога. В случае обнаружении ЖДА у мужчин, наоборот, показано исключение заболеваний ЖКТ.
Рис. 3. Зависимость между уровнем гемоглобина и сывороточного эритропоэтина (логарифмическая шкала и экспоненциальные кривые) у больных с постгеморрагической ЖДА при заболеваниях ЖКТ (предполагаемый эритропоэтин) и анемии при гинекологических заболеваниях (определяемый эритропоэтин) [5].
Помимо повышенной потребности в железе и хронической кровопотери, патологическими состояниями, способными вызывать развитие ЖДА, являются различные нарушения всасывания железа и поступления его с пищей (в том числе и обусловленные вегетарианством), нарушения транспорта железа (гипотрансферринемии при заболеваниях печени и наследственные атрансферринемии) [21].
Таким образом, гипохромная микроцитарная анемия, особенно при наличии характерной для сидеропенического синдрома клинической картины, даже без исследования обмена железа может определяться как ЖДА при условии полноценного клинического и инструментального обследования больного и установления причины ее развития [5].
Лечение.
Современная тактика лечения при ЖДА в настоящее время направлена на устранение этиологического фактора и восполнение запасов железа в организме [4, 5]. Наиболее оправдано более физиологическое пероральное применение препаратов железа; парентерально препараты можно использовать только при доказанном дефиците железа. Перорально следует назначать препараты железа в высоких дозах (от 200 до 300 мг/сут), что, однако, может приводить к возникновению диспепсических явлений, поэтому (особенно в детской и акушерской практике) рекомендуется постепенное повышение дозы до терапевтической, а при достижении нормальных значений уровня гемоглобина — ее снижение [20].
Степень абсорбции двухвалентных солей железа в несколько раз выше, чем трехвалентных, так как они пассивно диффундируют через каналы ДМТ-белков [33], поэтому препараты, содержащие двухвалентное железо, дают быстрый эффект и нормализуют уровень гемоглобина в среднем через 1—2 мес, а нормализация депо железа происходит уже через 3—4 мес от начала лечения в зависимости от степени тяжести анемии и дозы препарата. Препараты, содержащие железо в трехвалентном состоянии, требуют более длительного применения, а в случае дефицита меди в организме будут неэффективны. Нормализация уровня гемоглобина при лечении препаратом трехвалентного железа наступит только через 2—4 мес, а нормализация показателей депо железа — через 5—7 мес от начала терапии [5, 19, 33]. Степень абсорбции отражается и на частоте развития побочных эффектов. Уменьшить нежелательное влияние таблетированных препаратов железа на ЖКТ можно, принимая их во время еды, но при этом уменьшается всасывание железа. Лучше (но также с потерей эффективности) использовать формы с замедленным высвобождением, так как часть препарата будет высвобождаться в нижних отделах ЖКТ, где железо практически не всасывается [34]. Несмотря на рекомендации ВОЗ по применению для лечения ЖДА препаратов двухвалентного железа как более эффективных, препараты с низкой биодоступностью на основе трехвалентного железа активно применяются благодаря их лучшей переносимости.
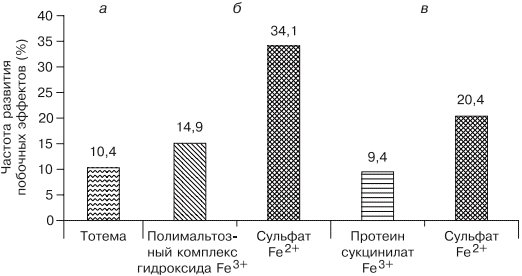
В современной клинической практике используются различные варианты сочетаний двухвалентного железа с витаминами С, В9, В12, что позволяет минимизировать побочные эффекты и одновременно повысить эффективность терапии, однако переносимость такого лечения до настоящего времени была основным лимитирующим фактором [20, 33]. Анализ переносимости различных препаратов железа более чем у тысячи пациентов показал, что современная жидкая форма двухвалентного железа (препарат тотема, лаборатория Иннотек Интернасиональ, Франция) по количеству побочных эффектов не превышает таковые у трехвалентного (рис. 4) [4]. Такой эффект достигается равномерным распределением препарата по слизистой оболочке желудка и его высокой биодоступностью. Двухвалентное железо равномерно и максимально эффективно проникает в энтероциты и, не накапливаясь в них, поступает в кровь. Это обусловлено наличием в составе препарата меди и марганца, которые входят в состав ДМТ-белков и гефестина, окисляющего железо, что способствует наилучшему его метаболизму (см. рис. 2) [33]. Помимо этого, указанные металлы участвуют в работе системы антиоксидантов, наиболее важными составляющими которой являются Cu, Zn-супероксиддисмутаза, Mn-супероксиддисмутаза (в митохондриях), каталаза, глутатионпероксидаза и глутатион. При уменьшении антиоксидантной защиты происходит сдвиг в сторону избыточного накопления свободных радикалов, что обусловливает их повреждающее действие на клетки. Следует понимать, что процесс активации перекисного окисления липидов запускается ионами двухвалентного железа, что проявляется частым развитием побочных эффектов при лечении препаратами железа. Наличие меди и марганца в составе тотемы уменьшает образование свободных радикалов, что улучшает переносимость препаратов железа [37].
Пациентам с заболеваниями ЖКТ назначать препараты железа перорально следует с осторожностью, причем острые заболевания, такие как язва желудка и двенадцатиперстной кишки, эрозивный гастрит, являются противопоказаниями; также не следует использовать указанный метод лечения у больных с заболеваниями тонкой кишки (болезнь Крона, целиакия, мальабсорбция) или отсутствием ее части.
Рис. 4. Сравнение результатов исследований безопасности применения различных железосодержащих препаратов.
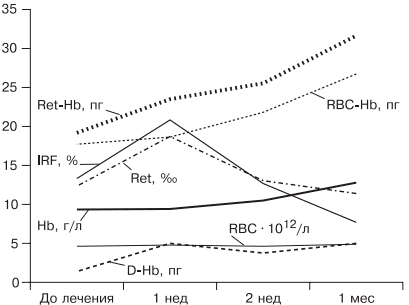
При лечении больных ЖДА остро стоит вопрос оценки эффективности терапии, так как часто ЖДА диагностируется у соматически тяжелых больных с крайне низким уровнем гемоглобина. Попытки ранней диагностики, как правило, связаны с исследованием количества ретикулоцитов [38], однако в настоящее время такой подход не является доказательным, так как часто ретикулоцитоз возникает компенсаторно при наличии кровотечения. В работе [5, 9] показано, что наиболее достоверными показателями, указывающими на хороший эффект препаратов железа, служат появление молодых форм ретикулоцитов и увеличение дельты гемоглобина (разницы между средним содержанием гемоглобина в ретикулоците и эритроците) уже через 1 нед после начала лечения (рис. 5).
Рис. 5. Динамика гемоглобина эритроцитов (RBC), количества ретикулоцитов (Ret), фракции незрелых ретикулоцитов (IRF-) среднего содержания гемоглобина в эритроците (RBC-Hb), среднего содержания гемоглобина в ретикулоците (Ret-Hb), дельты гемоглобина (D-Hb) при лечении ЖДА в течение 1 мес.
Основным критерием положительного ответа на терапию ЖДА является прирост уровня гемоглобина через 1 мес после начала применения препаратов железа, однако рекомендации разных организаций по этому вопросу не согласуются друг с другом. Минимальным приростом уровня гемоглобина в периферической крови для признания терапии эффективной является его увеличение более чем на 10 г/л за 1 мес (Центр по контролю и профилактике заболеваний в США) [39]. В нашем исследовании, проведенном при лечении 61 пациентки с гинекологической патологией и заболеваниями ЖКТ, у которых лечение привело к полному восстановлению показателей гемоглобина и обмена железа, прирост уровня гемоглобина в течение первого месяца составил от 10 до 50 г/л с медианой прироста 30 г/л [19]. Поэтому с учетом большого количества сопутствующих заболеваний у больных ЖДА и доказанной роли гепцидина в нарушении метаболизма железа за оптимальный критерий оценки эффективности терапии лучше принять прирост уровня гемоглобина более 10 г/л за 1 мес [5].
При отсутствии прироста уровня гемоглобина, согласно указанным критериям, необходимо обязательно исследовать обмен железа, провести диагностический поиск, исключить другой механизм развития анемии. При подтверждении абсолютного дефицита железа и отсутствии злокачественной опухоли следует перейти на парентеральное применение препаратов железа со строго рассчитанной терапевтической дозой. При назначении препаратов парентерально предпочтение следует отдавать внутривенному пути введения. Наиболее часто в настоящее время используются венофер (100 мг в 5 мл), космофер, феринъект (50 мг в 1 мл). За один раз, как правило, вводят 100—200 мг, но, используя феринъект, это количество можно увеличить до 1000 мг. Эти препараты должны применяться только при наличии показаний, доказанном абсолютном дефиците железа и невозможности перорального применения. Существенным недостатком парентерального применения является то, что необходимо использовать строго рассчитанное количество препарата, врач может назначать препараты только в условиях стационара, применение препаратов ограничено из-за наличия большого количества тяжелых побочных реакций (анафилактический шок, аллергические реакции, передозировка железа, системный гемосидероз, локальный гемосидероз тканей). Кроме того, как правило, есть ограничения парентерального применения препаратов при беременности, особенно в ранние сроки.
В случае отсутствия гипоферритинемии есть основания проводить лечение анемии с использованием препаратов рекомбинантного человеческого эритропоэтина, эффективность которого доказана при терапии ЖДА в поздние сроки беременности [28] и у больных с миомой матки [40, 41]. Такую тактику необходимо выбирать у больных с доказанными хроническими воспалительными или инфекционными заболеваниями, доброкачественными опухолями при наличии синдрома неадекватной степени тяжести анемии выработки эритропоэтина [5, 19, 28].
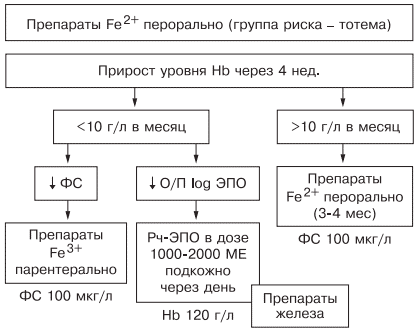
Таким образом, оптимальным у больных с наличием гипохромной микроцитарной анемии является выявление причины развития дефицита железа, после чего следует начинать лечение. Если есть сомнения в железодефицитном характере анемии, лучше проверить обмен железа, подтвердив диагноз ЖДА низкими показателями ФС и насыщения трансферрина железом. Далее следует устранить хроническое заболевание, остановить кровотечение, убрать погрешности в диете и начать пероральный прием препаратов железа (с обязательным учетом противопоказаний). Лечение следует начинать с двухвалентных препаратов железа. При наличии хронических воспалительных, пролиферативных, инфекционных заболеваний лучше использовать жидкую лекарственную форму (препарат тотема), содержащую в своем составе глюконат двухвалентного железа, медь и марганец. Через 1 мес следует определить прирост уровня гемоглобина и если он выше 10 г/л в месяц — продолжить лечение, если нет — пересмотреть диагноз (рис. 6).
Рис. 6. Схема лечения ЖДА.
При использовании препаратов железа необходимо ориентироваться на показатель ФС, целевое значение которого должно составлять около 100 мкг/л, после чего можно остановить лечение (поздние критерии эффективности терапии [39]). При пероральном приеме препаратов достаточно подтвердить нормализацию содержания ФС через 3 мес терапии, при назначении препаратов железа внутривенно этот показатель необходимо проверять каждую неделю. Лечение препаратами рекомбинантного человеческого эритропоэтина опасно из-за возможности развития эритроцитоза и тромботических осложнений, поэтому ориентироваться прежде всего необходимо на уровень гемоглобина, целевая концентрация которого не должна превышать 120 г/л [42].
Таким образом, ЖДА представляет собой важную социально значимую проблему, а ее диагностика и лечение до сих пор являются трудной задачей. Только выполнение современных рекомендаций позволит существенно повысить качество и эффективность оказания медицинской помощи больным ЖДА.
Сведения об авторах:
Российский университет дружбы народов, Москва
Кафедра госпитальной терапии с курсом клинической лабораторной диагностики Стуклов Николай Игоревич — д-р мед. наук, проф. кафедры; руководитель курса гематологии;
Семенова Елена Николаевна — учебный мастер кафедры.
источник