Опубликовано в журнале:
Поликлиника 5/2012,c. 1-5
Научный центр акушерства, гинекологии и перинатологии РАМН, Москва
Рассматриваются причины железодефицитных состояний (ЖДС), включая железодефицитную анемию (ЖДА). Подчеркивается, что в патогенезе ЖДС важную роль могут играть нарушения обмена других эссенциальных микроэлементов, в частности меди и марганца. Таким образом, для успешной терапии ЖДС необходимо учитывать особенности взаимодействия микроэлементов в живом организме и помнить, что железо является не единственным микроэлементом, необходимым для синтеза гемоглобина. В этой связи особое место среди ферропрепаратов занимает препарат Тотема, в состав которого помимо железа входят медь и марганец. Подчеркивается, что Тотема оптимально соответствует физиологии обмена железа и выпускается в чрезвычайно удобной для применения жидкой лекарственной форме. Рассматриваются результаты клинических исследований Тотемы, свидетельствующие о высокой эффективности этого препарата в лечении и профилактике ЖДС и ЖДА у различных категорий больных и его хорошей переносимости.
Железодефицитное состояние (ЖДС) – клинико-гематологический синдром, наблюдаемый в любом возрасте (от периода новорожденности до глубокой старости) из-за развивающегося дефицита железа. ЖДС – самая распространенная патология среди населения различных стран. По некоторым данным, в мире дефицит железа имеется более чем у 1,5 млрд человек, при этом железодефицитная анемия (ЖДА) – примерно у 500 млн [10].
Наиболее частыми причинами развития ЖДС являются:
- маточные (меноррагии различной этиологии, миома, эндометриоз, внутриматочные контрацептивы);
- носовые (наследственная геморрагическая телеангиэктазия и другие геморрагические диатезы);
- почечные (IgA-нефропатия, геморрагический нефрит, опухоли почек, перманентный внутрисосудистый гемолиз);
- легочные (идиопатический легочный гемосидероз);
- o ятрогенные и искусственные кровопотери (частые кровопускания и заборы крови для исследований, лечение гемодиализом, донорство и др.);
- энтериты различного генеза;
- синдром недостаточности всасывания;
- резекция тонкой кишки;
- резекция желудка с выключением двенадцатиперстной кишки;
- беременность, лактация;
- интенсивный рост и пубертатный период;
- В12-дефицитная анемия, леченная витамином В12;
- нарушение транспорта железа (гипопротеинемии различного генеза);
- алиментарная недостаточность [2]. Дефицит железа характерен для всех групп населения, однако наиболее уязвимыми в отношении риска развития ЖДА являются дети, особенно раннего возраста, беременные и кормящие женщины. В связи с этим именно в эти периоды жизни необходимо тщательно контролировать обеспеченность их организма железом.
Так, по данным официальной статистики Минздрава России, из числа женщин, закончивших беременность, в 1995 г. имели анемию 34,4%, а в 2000г.-уже 43,9% [8, 9].
У детей ЖДА наиболее часто встречается в возрасте до 2 лет. Так, концентрация гемоглобина менее 110 г/л обнаружена в Москве у 16–20% детей в возрасте 6–24 месяца, в Екатеринбурге у 31–35%, в Московской области у 30–41%, в Свердловской области у 47 % [11].
Клиническое значение дефицита железа
Биологическая роль железа в организме велика: оно участвует в окислительно-восстановительных процессах, росте и старении тканей, механизмах иммунитета, кроветворении, снабжении органов и тканей кислородом, функционировании ряда ферментов [1, 3].
По данным литературы, ЖДС являются причиной снижения работоспособности у взрослых, увеличения восприимчивости к острым респираторным вирусным инфекциям, вызывают задержку роста и развития детей. Дефицит железа у беременных не только в манифестных, но и в латентных проявлениях неблагоприятно отражается на течении беременности и родов, послеродового периода, состоянии плода и новорожденного. Дефицит железа и крайняя его степень – ЖДА могут вызывать повышение частоты гестоза у беременных, пиелонефрита, преждевременных родов, плацентарной недостаточности, отставания роста и развития, внутриутробной гибели плода; рост числа инфекционных осложнений и гипогалактии у родильниц; повышение частоты и увеличение объема патологической кровопотери в родах и послеродовом периоде; слабость родовой деятельности. Кроме того, недостаточное депонирование железа в антенатальном периоде является одной из причин развития ЖДС и анемии у грудных детей. Имеются данные, указывающие на связь анемии у детей со снижением их интеллектуального развития, работоспособности и нарушениями поведения [3, 11].
Выделяют три формы ЖДС: дефицит железа без анемии (предлатентный и латентный) и ЖДА. Первые две характеризуются снижением уровней депонированного и транспортного железа при сохраненном эритроцитарном пуле железа, вторая – уменьшением уровня всех метаболических пулов железа.
Предлатентный дефицит железа – состояние, предшествующее дефициту железа, сопровождается увеличением его абсорбции в желудочно-кишечном тракте. Клинические симптомы отсутствуют. Лабораторные показатели (картина периферической крови, сывороточное железо, трансферрин, ферритин) обычно остаются в пределах нормы. Реально определить истощение депонированного железа позволяет только тест абсорбции 39Fe3+. Примерно в 60 % случаев выявляется повышение абсорбции более 50 % при норме 10-15 %.
Латентный дефицит железа сопровождается так называемыми сидеропеническими симптомами, обусловленными дефицитом железа в тканях. Лабораторные показатели метаболизма железа характеризуются снижением концентрации ферритина (5-15 мкг/л), сывороточного железа в плазме, увеличением содержания трансферрина. При истощении запасов железа развивается недостаток транспортного железа, хотя синтез гемоглобина (Нb) на этой стадии не нарушен и, следовательно, показатели красной крови – Нb, гематокрит (Ht), эритроциты (RBC), MCV, МСН, МСНС -сохраняются в пределах нормы. Однако при дополнительных стрессах или потерях железа латентный дефицит железа может перейти в ЖДА [3].
Заключительным этапом ЖДС является железодефицитная анемия, возникающая при снижении гемоглобинового фонда железа и проявляющаяся симптомами анемии и гипосидероза.
Анемический синдром проявляется неспецифическими симптомами. Основные жалобы больных сводятся к слабости, повышенной утомляемости, головокружениям, шуму в ушах, мельканию мушек перед глазами, сердцебиениям, одышке при физической нагрузке [2].
Клинические проявления гипосидероза обусловлены тканевым дефицитом железа. В результате снижения активности некоторых железосодержащих тканевых энзимов, в частности цитохромов, развиваются изменения в эпителиальных тканях (коже и ее придатках, слизистых оболочках). Отмечаются бледность и сухость кожи, ломкость и слоистость ногтей, извращение вкуса, затрудненное глотание сухой и твердой пищи (сидеропеническая дисфагия). К симптомам, связанным с дефицитом железа, относится мышечная слабость (из-за дефицита железосодержащих ферментов) [2].
Для диагностики ЖДА используются следующие гематологические показатели:
- HGB (Нb) – содержание гемоглобина;
- RBC – количество эритроцитов;
- Ht (НСТ) – гематокрит – отражает долю эритроцитов в общем объеме крови;
- ЦП – цветной показатель – отражает относительное содержание Нb в эритроците (при ЖДА ЦП
источник
ОЖСС расшифровывается как общая железосвязывающая способность сыворотки. Анализ ОЖСС является лабораторным тестом, отражающим способность трансферина, то есть специфического кровяного белка, связывать свободное железо. Выполняется анализ во время диагностирования и дифференциального диагностирования анемий.
Если ОЖСС повышается, можно сделать выводы о низком содержании в крови железа, что является характерным признаком железодефицитной анемии. Сыворотка связывает железа больше, чем требуется в норме. Если же показатели ОЖСС низкие, то это является итогом увеличения сывороточного железа, которое сопровождает гиперхромную анемию (то есть накопление железа в избытке), инфекции или злокачественные образования в организме.
Давайте подробнее узнаем о том, что это такое – ОЖСС?
Трансферрин производят клетки печени. Если функции её изменяются (например, из-за недостаточности, при гепатите или циррозе), то концентрация белка-переносчика значительно уменьшается, а значит, меняются и показания теста ОЖСС.
Концентрация железа и ОЖСС в сыворотке являются основаниями для расчёта коэффициента насыщения трансферрина.
Нужно сказать, что снижать ОЖСС может употребление таких групп препаратов, как кортикотропин, аспарагиназа, тестостерон, хлорамфеникол, кортизон. Повышению же результатов способствуют контрацептивы перорального типа и эстрогены. Снижается ОЖСС также вследствие приёма железосодержащих препаратов, именно поэтому примерно за неделю (минимум – за пять дней) до взятия крови нужно их приём прекратить.
Итак, в данной статье разберемся, что это такое — ОЖСС.
К основным методам, при помощи которых устанавливается ОЖСС кровяной сыворотки, относятся колориметрический анализ и абсорбционная спектроскопия. Сейчас наибольшее употребление получает первый метод, который заключается в том, что в анализируемую сыворотку вводят железо в избыточном количестве. Какая-то его часть связывается с белком-переносчиком, а железо, которое не вступило в связи, удаляется. По определённому его количеству можно делать вывод о величине ОЖСС. Повышен, как и понижен, он бывает часто.
Поскольку описанный метод (несмотря на высокую степень достоверности) довольно длительный и требует больших затрат труда, в некоторых лабораториях применяется альтернативный метод анализа, который отдельно определяет, каково содержание железа в НЖСС (ненасыщенная способность железа к связыванию) и в кровяной сыворотке. Данные показатели суммируются, в результате получаются показатели ОЖСС. В связи с этим довольно часто происходит одновременное определение ОЖСС, сывороточного железа и НЖЖС во многих лабораториях.
Если ОЖСС повышен, что это значит? Этот вопрос интересует многих.
Гипотиреоз – это состояние, детерминированное долговременным и устойчивым дефицитом гормонов щитовидной железы. Его противоположность – тиреотоксикоз. Крайнее проявление симптоматики у взрослых людей – микседема, а у детей – кретинизм.
Любая разновидность анемии сама по себе заболеванием не является, однако может быть сопутствующим симптомом при перечне болезней, а они, в свою очередь, могут быть как взаимосвязаны с первичным поражением кровяной системы, так и протекать независимо от него. Именно поэтому строго классифицировать анемии не представляется возможным. Основанием для их структурирования выступает принцип практической целесообразности. Чтобы сделать это с максимальным удобством, анемии делят по цветовому показателю как единому признаку классификации. Сывороточное железо ОЖСС – важный показатель.
Состояние дефицита железа наверняка известно многим людям, но мало кто догадывается, что нарушение функционирования щитовидной железы может стать его причиной. Известно это стало не так давно, более того, не каждый российский врач знает о подобном осложнении, поэтому не обращает внимания на содержание гемоглобина и эритроцитов у пациента.
Кроме того, учёные определили, что изначальный дефицит железа является причиной развития гипотиреоза. Для этого и определяют ОЖСС в крови. Что это, мы уже пояснили.
Нарушение функционирования железа имеет два направления:
— к гипотиреозу — понижению функции;
— к гипертиреозу — увеличение функционирования органа.
Абсолютно доказанным фактом в настоящее время является тот, что гипотиреоз способен вызвать плохую усвояемость железа из-за его недостатка. Относительно гипертиреоза ведутся споры, подобное сочетание встречается гораздо реже, чем соединение анемии и гипотиреоза (50 % случаев, даже если анемия выражена слабо). Что это такое – ОЖСС? Это частый вопрос пациентов.
Чтобы разобраться в механизме влияния гормонов щитовидной железы на усвоение железа, нужно понять суть данного процесса. Организм может синтезировать железо, но поскольку его запасы в организме небольшие, оно должно поступать в организм из употребляемой человеком пищи во избежание нехватки.
Железо находится в еде в трёхвалентном окисленном состоянии, является частью состава белков и солей органических кислот. Подобная его форма организмом не усваивается. Чтобы осуществились освобождение из содержания солей и белков и переход железа в двухвалентную усвояемую форму, необходимы кислый сок желудка и витамин С.
Всасывается оно в тонком кишечнике и в двенадцатиперстной кишке. При отсутствии превращения железа в усвояемую форму, оно просто выводится из организма человека посредством кала. А происходит превращение при активном влиянии аскорбиновой кислоты.
Недостаток содержания гормонов щитовидной железы обусловливает и уменьшение кислотности желудка через снижение числа париетальных клеток, которые выводят соляную кислоту, железо из-за этого не превращается в нужную форму и организмом не всасывается. В итоге возникает железодефицитная анемия. Когда ОЖСС повышен, что это значит? Что к этому ведет?
Недостаток железа в организме может проявиться не только из-за того, что нарушается его всасывание. Он возникает в следующих случаях:
— при малом поступлении железа с едой (например, при вегетарианском меню);
— у женщин при обильном характере менструаций;
— при синдроме мальабсорбции;
— при кровотечениях пищеварительного тракта, имеющих скрытый характер (например, при геморрое либо кровоточащей язве);
— при частых кровотечениях из носа;
— при частых безмерных донорских кроводачах;
— при серьёзных потерях крови;
— при попытке суицида посредством вскрытия вен, которая не была завершена;
— при психическом отклонении, заключающемся в постоянном кровопускании.
Данные состояния не относятся к нормальным, поэтому необходимо налюдение у врача. Если не выявить причину анемии, то и откорректировать самочувствие не получится.
Хроническая нехватка железа провоцирует сбои в функционировании щитовидной железы. Из-за пониженного содержания фермент дейодиназа блокируется, превращая Т4 в более активный Т3. В итоге биологическое воздействие гормонов сокращается, проявляются признаки гипотиреоза. Параллельно снижается деятельность ещё одного значимого фермента: речь идёт о тиреопероксидазе, принимающей непосредственное участие в синтезе гормонов щитовидной железы. Данный фермент также характеризуется железозависимостью.
Научно доказаны характер протекания анемии (ОЖСС понижен) при гипотиреозе и причины развития заболевания. Кроме того, есть информация о том, что во время гипотиреоза показатели совокупной массы эритроцитов могут уменьшаться, однако подобный процесс не может замаскироваться вместе с параллельно происходящим понижением плазмы крови.
Железодефицитная разновидность анемии, сопутствующая гипотиреозу, протекает довольно мягко. Иногда можно проследить повышение MCV, а при расшифровке анализов крови в некоторых случаях могут присутствовать сморщенные эритроциты, имеющие неправильную форму. У костного мозга при этом обнаруживаются характеристики эритроидной гипоплазии. Тщательное изучение кинетики железа позволяет выяснить, что его показатели и данные клиренса из плазмы уменьшаются. Такой же процесс наблюдается и во время созревания эритроцитов с утилизацией. У пациентов, имеющих гипотиреоз, очень часто находят такую болезнь, как гастрит атрофического типа, следствием которого выступает недостаток железа либо витамина В12. На основании этих данных в клинической картине могут появиться изменения.
При наличии гипотиреоза об этих данных не стоит забывать. Порой рутинно назначенный общий анализ крови даёт врачу повод задуматься о наличии у пациента гипотиреоза. Поскольку гормоны щитовидной железы непосредственно участвуют в регулирования кроветворения, то нехватка их отражается в том, что параметры крови изменяются. Вылечить анемию при этом можно только в том случае, если будет успешно вылечена главная провоцирующая ее патология.
Мы рассмотрели показатель ОЖСС. Что это такое — теперь понятно.
источник
Пониженные уровни железа могут привести к анемии, спровоцировать уменьшение выработки эритроцитов, микроцитоз (уменьшенный размер эритроцитов) и гипохромию, при которой эритроциты становятся бледного цвета из-за недостатка гемоглобина. Одним из тестов, что помогает оценить состояние железа в организме, является «общая железосвязывающая способность сыворотки». Он измеряет количество всех протеинов в крови, которые могут связать частицы железа, включая трансферрин, главный белок-переносчик железа в плазме.
Железо (сокр. Fe) – это вещество, необходимое для поддержания жизни. Благодаря ему, организм формирует нормальные эритроциты, поскольку этот элемент является главной частью гемоглобина, что входит в состав этих клеток крови. Он связывает и присоединяет к себе молекулы кислорода в легких и отдает их другим частям тела, забирая от тканей отработанный газ – углекислоту, выводя её наружу.
Чтобы обеспечить клетки тела железом, печень из аминокислот вырабатывает белок трансферрин, который транспортирует Fe по организму. Когда запасы Fe в организме понижены, уровень трансферрина увеличивается.
И наоборот, при увеличении запасов железа, выработка этого протеина уменьшается. У здоровых людей одна третья всего количества трансферрина используется для переноса железа.
Остатки Fe, которые не используются для строительства клеток, запасаются в тканях в форме двух веществ, ферритина и гемосидерина. Этот запас применяют для производства других разновидностей белков, таких как миоглобин и некоторые энзимы.
Анализы, показывающие железосодержащий статус организма, могут проводиться для установления количества железа, циркулирующего в кровеносной системе, способности крови к переносу этого вещества, а также количество Fe, запасенного в тканях для будущих потребностей организма. Тестирование также может помочь провести различие разных причин анемии.
Для оценки уровня железа в крови врач назначает сдавать несколько анализов. Эти тесты обычно проводятся одновременно, чтобы провести сравнительную интерпретацию результатов, необходимых для диагностики и/или мониторинга недостатка или избытка Fe в организме. Диагностируют недостаток или избыток железа в организме следующие анализы:
- Анализ на ОЖСС (общую железосвязывающую способность сыворотки крови) – поскольку трансферрин является первичным железосвязывающим протеином, ОЖСС норма считается надежным показателем.
- Анализ на уровень Fe в крови.
- НЖСС (ненасыщенная железосвязывающая способность) – измеряет количество трансферрина, который несвязан с молекулами железа. НЖСС также отражает общий уровень трансферрина. Этот тест также известен как «латентная железосвязывающая способность сыворотки».
- Расчет насыщения трансферрина производится в соответствии с насыщением его молекулами железа. Это позволяет узнать долю трансферрина, насыщенную Fe.
- Показатели сывороточного ферритина отражают запасы железа в организме, которые сохраняются в основном в этом белке.
- Тестирование рецепторов к растворимому трансферрину. Этот тест можно использовать для выявления железодефицитной анемии и отличить ее от вторичной анемии, причина которой хроническое заболевание или воспаление.
Еще один тест – анализ на протопорфирин, связанный с цинком. Так называется прекурсор части гемоглобина (гемма), что содержит в своем составе Fe. Если железа в гемме недостаточно, протопорфирин связывается с цинком, что показывает анализ крови. Поэтому этот тест может использоваться в качестве скрининга, особенно у детей. Тем не менее, измерение протопорфирина, связанного с цинком, не является специфическим тестом для определения проблем с Fe. Поэтому повышенные значения этого вещества должны подтверждаться другими анализами.
Для исследования железа могут назначаться генетические теста гена HFE. Гемохроматоз – это генетическое заболевание, при котором организм усваивает больше Fe, чем это необходимо. Причиной этому является аномальное строение специфического гена, который называется HFE. Этот ген управляет количеством всасывания железа из пищи в кишечнике.
У пациентов, которые имеют две копии аномального гена, в организме собирается избыток железа, который откладывается в различных органах. Из-за этого они начинают разрушаться и функционировать неправильно. Тест на исследование гена HFE выявляет различные мутации, которые могут привести к заболеваниям. Наиболее распространенной мутацией гена HFE является мутация под названием C282Y.
Вместе с вышеперечисленными анализами врач изучает данные общего анализа крови. К таким исследованиям относятся тесты на гемоглобин и гематокрит. Пониженные значения одного или обоих анализов говорит о наличии у пациента анемии.
Подсчеты среднего числа эритроцитов (среднего объема клеток) и среднего числа гемоглобина в эритроцитах (среднего клеточный гемоглобин) также входят в общий анализ крови. Дефицит Fe и сопутствующее ему недостаточное производство гемоглобина создают условия, при которых эритроциты уменьшаются в размерах (микроцитоз) и становятся более бледными (гипохромия). При этом как средний объем клеток, так и средний клеточный гемоглобин ниже нормы.
Позволяет определить проблемы с железом подсчет молодых эритроцитов, ретикулоцитов, абсолютное число которых уменьшено при железодефицитной анемии. Но это число увеличивается до нормального уровня после того, как пациент проходит терапию железосодержащими препаратами.
Один или больше анализов может назначаться, когда результаты общего анализа крови выходят за рамки нормальных значений. Часто это бывает при пониженных значениях гематокрита или гемоглобина. Также врач может направить пациента на анализы на Fe при наличии следующих симптомов:
- Хроническая усталость и утомляемость.
- Головокружение.
- Слабость.
- Головные боли.
- Бледная кожа.
Определение содержания железа, ОЖСС и ферритина может назначаться, если у пациента присутствуют симптомы избытка или отравления Fe. Это может проявляться болью в суставах, недостатком энергии, болью в животе, проблемами с сердцем. Если ребенок подозревается в том, что он съел слишком много железосодержащих таблеток, эти тесты помогают определить степень отравления.
Анализ на железо врач может назначить, если предполагает у пациента хронический избыток железа в организме (гемохроматоз). В этом случае назначаются дополнительные исследования HFE гена, чтобы подтвердить диагноз этого наследственного заболевания. В пользу такого подозрения могут говорить случаи заболевания гемохроматозом у родственников пациента.
Дефицит Fe у женщин и мужчин может проявляться при недостаточном поступлении этого вещества вместе с пищей, недостаточном усвоении питательных веществ. Также приводят к недостатку железа возросшие потребности организма во время некоторых состояний, среди которых – беременность, острая или хроническая потеря крови.
Острый избыток железа может появиться в результате употребления большого количества железосодержащих пищевых добавок. Особенно часто это бывает у детей. Хронический избыток Fe также может быть следствием избыточного употребления этого вещества вместе с пищей, а также появиться в результате наследственных заболеваний (гемохроматоз), частых переливаний крови и по некоторым другим причинам.
Значения результатов на железосодержащий статус организма указаны в следующей таблице:
| Заболевание | Fe | ОЖСС/трансферрин | НЖСС | % насыщения трансферрина | Ферритин |
| Недостаточность железа | Понижено | Выше нормы | Повышено | Ниже нормы | Понижено |
| Гемохроматоз | Повышено | Понижено | Понижено | Повышено | Повышено |
| Хронические заболевания | Понижено | Понижено | Понижено/в норме | Ниже нормы | В норме/повышено |
| Гемолитическая анемия | Выше нормы | В норме/понижено | Понижено/в норме | Повышено | Повышено |
| Сидеробластическая анемия | В норме/повышено | В норме/ понижено | Понижено/в норме | Повышено | Повышено |
| Отравление железом | Повышено | В норме | Ниже нормы | Повышено | В норме |
В легкой стадии дефицита железа расход запасов этого вещества происходит медленно. Это значит, что находящийся в организме Fe функционирует нормально, но его запасы не пополняются. Железа в сыворотке на этой стадии может быть нормальным, но уровень ферритина обычно понижен.
Поскольку расход железа при этом продолжается, его дефицит нарастает, а потому запас Fe постепенно приходит к концу. Для компенсации этого недостатка в организме повышается выработка трансферрина, чтобы увеличить перенос Fe. Таким образом, уровень железа в плазме продолжает падать, а трансферрина и ОЖСС – расти. По мере прогрессирования этого состояния эритроцитов вырабатывается все меньше, а их размер также уменьшается. В результате развивается железодефицитная анемия. Эту проблему легко решить, обеспечив поступление в организм продуктов, содержащих достаточное количество необходимого организму железа и повышающие его недостаток.
источник
Железодефицитная анемия – синдром, обусловленный недостаточностью железа и приводящий к нарушению гемоглобинопоэза и тканевой гипоксии. Клинические проявления представлены общей слабостью, сонливостью, пониженной умственной работоспособностью и физической выносливостью, шумом в ушах, головокружениями, обморочными состояниями, одышкой при нагрузке, сердцебиением, бледностью. Гипохромная анемия подтверждается лабораторными данными: исследованием клинического анализа крови, показателей сывороточного железа, ОЖСС и ферритина. Терапия включает лечебную диету, прием препаратов железа, в некоторых случаях – трансфузию эритроцитарной массы.
Железодефицитная (микроцитарная, гипохромная) анемия – анемия, обусловленная нехваткой железа, необходимого для нормального синтеза гемоглобина. Её распространенность в популяции зависит от половозрастных и климатогеографических факторов. По обобщенным сведениям, гипохромной анемией страдает около 50% детей раннего возраста, 15% женщин репродуктивного возраста и около 2% мужчин. Скрытый тканевой железодефицит выявляется практически у каждого третьего жителя планеты. На долю микроцитарной анемии в гематологии приходится 80–90% всех анемий. Поскольку железодефицит может развиваться при самых различных патологических состояниях, данная проблема актуальна для многих клинических дисциплин: педиатрии, гинекологии, гастроэнтерологии и др.
Ежесуточно с потом, калом, мочой, слущенными клетками кожи теряется около 1 мг железа и примерно столько же (2-2,5 мг) поступает в организм с пищей. Дисбаланс между потребностями организма в железе и его поступлением извне или потерями способствует развитию железодефицитной анемии. Железодефицит может возникать как при физиологических условиях, так и в результате ряда патологических состояний и быть обусловлен как эндогенными механизмами, так и внешними воздействиями:
Чаще всего анемия вызывается хронической потерей крови: обильными менструациями, дисфункциональными маточными кровотечениями; желудочно-кишечными кровотечениями из эрозий слизистой желудка и кишечника, гастродуоденальных язв, геморроидальных узлов, анальных трещин и др. Скрытая, но регулярная кровопотеря отмечается при гельминтозах, гемосидерозе легких, экссудативном диатезе у детей и др.
Особую группу составляют лица с болезнями крови — геморрагическими диатезами (гемофилией, болезнью Виллебранда), гемоглобинурией. Возможно развитие постгеморрагической анемии, вызванной одномоментным, но массивным кровотечением при травмах и операциях. Гипохромная анемия может возникать вследствие ятрогенных причин — у доноров, часто сдающих кровь; пациентов с ХПН, находящихся на гемодиализе.
К факторам алиментарного порядка относятся анорексия, вегетарианство и следование диетам с ограничением мясных продуктов, плохое питание; у детей — искусственное вскармливание, позднее введение прикорма. Снижение абсорбции железа характерно для кишечных инфекций, гипоацидного гастрита, хронического энтерита, синдрома мальабсорбции, состояния после резекции желудка или тонкой кишки, гастрэктомии. Значительно реже железодефицитная анемия развивается вследствие нарушения транспортировки железа из депо при недостаточной белково-синтетической функции печени – гипотрансферринемиях и гипопротеинемиях (гепатитах, циррозе печени).
Ежедневная потребность в микроэлементе зависит от пола и возраста. Наиболее высока необходимость в железе у недоношенных, детей раннего возраста и подростков (в связи с высокими темпами развития и роста), женщин репродуктивного периода (в связи с ежемесячными менструальными потерями), беременных (в связи с формированием и ростом плода), кормящих мам (в связи с расходом в составе молока). Именно эти категории являются наиболее уязвимыми в отношении развития железодефицитной анемии. Кроме того, повышение потребности и расхода железа в организме наблюдается при инфекционных и опухолевых заболеваниях.
По своей роли в обеспечении нормального функционирования всех биологических систем железо является важнейшим элементом. От уровня железа зависит поступление кислорода к клеткам, протекание окислительно-восстановительных процессов, антиоксидантная защита, функционирование иммунной и нервной систем и пр. В среднем содержание железа в организме находится на уровне 3-4 г. Более 60% железа (>2 г) входит в состав гемоглобина, 9% — в состав миоглобина, 1% — в состав ферментов (гемовых и негемовых). Остальное железо в виде ферритина и гемосидерина находится в тканевом депо – главным образом, в печени, мышцах, костном мозге, селезенке, почках, легких, сердце. Примерно 30 мг железа непрерывно циркулирует в плазме, будучи частично связанным основным железосвязывающим белком плазмы – трансферрином.
При развитии отрицательного баланса железа мобилизуются и расходуются запасы микроэлемента, содержащиеся в тканевых депо. На первых порах этого бывает достаточно для поддержания адекватного уровня Hb, Ht, сывороточного железа. По мере истощения тканевых резервов компенсаторно увеличивается эритроидная активность костного мозга. При полном истощении эндогенного тканевого железа его концентрация начинает снижаться в крови, нарушается морфология эритроцитов, уменьшается синтез гема в гемоглобине и железосодержащих ферментов. Страдает кислородтранспортная функция крови, что сопровождается тканевой гипоксией и дистрофическими процессами во внутренних органах (атрофический гастрит, миокардиодистрофия и др.).
Железодефицитная анемия возникает не сразу. Вначале развивается предлатентный железодефицит, характеризующийся истощением только запасов депонированного железа при сохранности транспортного и гемоглобинового пула. На этапе латентного дефицита отмечается уменьшение транспортного железа, содержащегося в плазме крови. Собственно гипохромная анемия развивается при уменьшении всех уровней метаболических запасов железа – депонированного, транспортного и эритроцитарного. В соответствии с этиологией различают анемии: постгеморрагические, алиментарные, связанные с повышенным расходом, исходным дефицитом, недостаточностью резорбции и нарушением транспорта железа. По степени выраженности железодефицитные анемии подразделяются на:
- Легкие (Нb 120-90 г/л). Протекают без клинических проявлений или с их минимальной выраженностью.
- Среднетяжелые (Нb 90-70 г/л). Сопровождаются циркуляторно-гипоксическим, сидеропеническим, гематологическим синдромами умеренной степени выраженности.
- Тяжелые (Нb
Циркуляторно-гипоксический синдром обусловлен нарушением синтеза гемоглобина, транспорта кислорода и развитием гипоксии в тканях. Это находит свое выражение в ощущении постоянной слабости, повышенной утомляемости, сонливости. Пациентов преследует шум в ушах, мелькание «мушек» перед глазами, головокружения, переходящие в обмороки. Характерны жалобы на сердцебиение, одышку, возникающую при физической нагрузке, повышенную чувствительность к низким температурам. Циркуляторно-гипоксические нарушения могут усугублять течение сопутствующей ИБС, хронической сердечной недостаточности.
Развитие сидеропенического синдрома связано с недостаточностью тканевых железосодержащих ферментов (каталазы, пероксидазы, цитохромов и др.). Этим объясняется возникновение трофических изменений кожных покровов и слизистых оболочек. Чаще всего они проявляются сухостью кожи; исчерченностью, ломкостью и деформацией ногтей; повышенным выпадением волос. Со стороны слизистых оболочек типичны атрофические изменения, что сопровождается явлениями глоссита, ангулярного стоматита, дисфагии, атрофического гастрита. Может возникать пристрастие к резким запахам (бензина, ацетона), искажение вкуса (желание есть глину, мел, зубной порошок и пр.). Признаками сидеропении также служат парестезии, мышечная слабость, диспепсические и дизурические расстройства. Астеновегетативные нарушения проявляются раздражительностью, эмоциональной неустойчивостью, снижением умственной работоспособности и памяти.
Поскольку в условиях железодефицита IgA теряет свою активность, больные становятся подвержены частой заболеваемости ОРВИ, кишечными инфекциями. Пациентов преследует хроническая усталость, упадок сил, снижение памяти и концентрации внимания. Длительное течение железодефицитной анемии может привести к развитию миокардиодистрофии, распознаваемой по инверсии зубцов Т на ЭКГ. При крайне тяжелом железодефиците развивается анемическая прекома (сонливость, одышка, резкая бледность кожи с цианотичным оттенком, тахикардия, галлюцинации), а затем – кома с потерей сознания и отсутствием рефлексов. При массивной стремительной кровопотере возникает гиповолемический шок.
На наличие железодефицитной анемии может указывать внешний вид больного: бледная, с алебастровым оттенком кожа, пастозность лица, голеней и стоп, отечные «мешки» под глазами. При аускультации сердца обнаруживается тахикардия, глухость тонов, негромкий систолический шум, иногда – аритмия. С целью подтверждения анемии и определения ее причин проводится лабораторное обследование.
- Лабораторные тесты. В пользу железодефицитного характера анемии свидетельствует снижение гемоглобина, гипохромия, микро- и пойкилоцитоз в общем анализе крови. При оценке биохимических показателей отмечается снижение уровня сывороточного железа и концентрации ферритина (60 мкмоль/л), уменьшение насыщения трансферрина железом (
- Инструментальные методики. Для установления причины хронической кровопотери должно быть проведено эндоскопическое обследование ЖКТ (ЭГДС, колоноскопия,), рентгенодиагностика (ирригоскопия, рентгенография желудка). Обследование органов репродуктивной системы у женщин включает УЗИ малого таза, осмотр на кресле, по показаниям — гистероскопию с РДВ.
- Исследование пунктата костного мозга. Микроскопия мазка (миелограмма) показывает значительное снижение количества сидеробластов, характерное для гипохромной анемии. Дифференциальная диагностика направлена на исключение других видов железодефицитных состояний — сидеробластной анемии, талассемии.
К основным принципам терапии железодефицитной анемии относятся устранение этиологических факторов, коррекция рациона питания, восполнение железодефицита в организме. Этиотропное лечение назначается и проводится специалистами гастроэнтерологами, гинекологами, проктологами и др.; патогенетическое – гематологами. При железодефицитных состояниях показано полноценное питание с обязательным включением в рацион продуктов, содержащих гемовое железо (телятины, говядины, баранины, мяса кролика, печени, языка). Следует помнить, что усилению ферросорбции в ЖКТ способствуют аскорбиновая, лимонная, янтарная кислота. Ингибируют всасывание железа оксалаты и полифенолы (кофе, чай, соевый протеин, молоко, шоколад), кальций, пищевые волокна и др. вещества.
Вместе с тем, даже сбалансированная диета не в состоянии устранить уже развившийся недостаток железа, поэтому больным с гипохромной анемией показана заместительная терапия ферропрепаратами. Препараты железа назначаются курсом не менее 1,5-2-х месяцев, а после нормализации уровня Hb проводится поддерживающая терапия в течение 4-6 недель половинной дозой препарата. Для фармакологической коррекции анемии используются препараты двухвалентного и трехвалентного железа. При наличии витальных показаний прибегают к гемотрансфузионной терапии.
В большинстве случаев гипохромная анемия подается успешной коррекции. Однако при неустраненной причине железодефицит может рецидивировать и прогрессировать. Железодефицитная анемия у детей раннего и младшего возраста может вызывать задержку психомоторного и интеллектуального развития (ЗПР). В целях профилактики железодефицита необходим ежегодный контроль параметров клинического анализа крови, полноценное питание с достаточным содержанием железа, своевременная ликвидация источников кровопотери в организме. Следует учитывать, что лучше всего усваивается железо, содержащееся в мясе и печени в форме гема; негемовое железо из растительной пищи практически не усваивается – в этом случае оно сначала должно восстановиться до гемового при участии аскорбиновой кислоты. Лицам групп риска может быть показан профилактический прием железосодержащих препаратов по назначению специалиста.
источник
Всасывание железа, транспорт, фонды железа в организме человека.
Роль железа в организме.
1. Роль железа в организме.
Железо в норме 12,5- 30,4 мкмоль/л. Оно необходимо для нормального кроветворения и тканевого дыхания.
Железо входит в состав дыхательных пигментов (преимущественно — гемоглобина, и частично — миоглобина), цитохромов, железосодержащих ферментов (каталазы, миелопероксидазы). Это так называемое, гемовое железо, которое обратимо связывает кислород и участвует в транспорте кислорода, ряде окислительно-восстановительных реакций, играет важную роль в процессах кроветворения.
Железо принимает участие в:
Средние показатели железа у женщин ниже, чем у мужчин, но и у тех и у других с возрастом показатель железа падает. Недостаток сна и стрессы, выраженная физическая нагрузка также вызывают снижение этого показателя. При беременности содержание железа в организме уменьшается, особенно во второй половине беременности (повышение потребности в железе в этот период связано с формированием депо железа у плода).
2. Всасывание железа, транспорт, фонды железа в организме человека.
В организм железо поступает с пищей. В пищевых продуктах железо присутствует или в виде составной части гема (мясо, рыба) или как негемовое железо (овощи, фрукты). Из пищи усваивается около 10 — 15 % железа, всасывание происходит в 12-типерстной кишке. Из животной пищи железо усваивается лучше, чем из растительной. Всасыванию железа способствуют лимонная и аскорбиновая кислоты и фруктоза, которые содержатся во фруктах, ягодах, их соках. Так, при питье фруктового сока увеличивается усвоение железа из яиц и хлеба. В зерновых и бобовых продуктах и некоторых овощах содержатся фосфаты, фитины и щавелевая кислота, препятствующие всасыванию железа. При добавлении мяса или рыбы к этим продуктам усвоение железа улучшается. Подавляет усвоение железа крепкий чай и кофе. Около 70% железа входит в состав гемоглобина, 5% — миоглобина, 20% находится в депо (печени, селезенке, костном мозге) в виде растворимого ферритина и нерастворимого гемосидерина. Всасывание железа регулируется клетками кишечника: оно возрастает при дефиците железа и неэффективном эритропоэзе и блокируется при избытке железа в организме. Транспорт железа от кишечной стенки до предшественников эритроцитов и клеток-депо (макрофагов) осуществляется плазменным белком — трансферрином. В организме железо не встречается в виде свободных катионов, только в связи с белками.
Железо выделяется из организма в основном путем слущивания слизистой оболочки кишечника и с желчью. Оно теряется также с волосами, ногтями, мочой и потом. Несмотря на нестабильность уровня Fe в сыворотке, исследование этого параметра важно для скрининга, дифференциальной диагностики железодефицитных и других анемий, а также оценки эффективности лечения больных железодефицитными анемиями. Выраженный дефицит железа сопровождается снижением уровня гемоглобина и цветного показателя. Выраженное снижение концентрации железа в сыворотке крови может быть отмечено при дефиците железа в организме, но для диагностики латентной анемии недостаточно определения содержания железа в сыворотке крови. Для более точной оценки баланса железа в организме необходимо провести дополнительные исследования (ферритин, трансферрин, ЛЖСС).
При дефиците железа в организме прежде всего ухудшается клеточное дыхание что ведет к дистрофии тканей и органов и нарушению состояния организма еще до развития анемии. Скрытый дефицит железа проявляется: больные отмечают общую слабость, недомогание, снижение работоспособности. Уже в этот период могут наблюдаться извращение вкуса, сухость и пощипывание языка, нарушение глотания с ощущением инородного тела в горле (синдром Пламмера — Винсона), сердцебиение, одышка.
Хронические заболевания печени (гепатит, цирроз);
Прием аллопуринола, андрогенов, аспирина, холестирамина, глюкокортикоидов. У большинства больных при продолжающемся дефиците железа после исчерпания его тканевых резервов развивается железодефицитная анемия, являющаяся признаком тяжелой недостаточности железа в организме. Изменения функции различных органов и систем при железодефицитной анемии являются не столько следствием малокровия, сколько тканевого дефицита железа. Доказательством этого служит несоответствие тяжести клинических проявлений болезни и степени анемии и появление их уже в стадии скрытого дефицита железа.
Больные железодефицитной анемией отмечают общую слабость, быструю утомляемость, затруднение в сосредоточении внимания, иногда сонливость. Появляются головная боль после переутомления, головокружение. При тяжелой анемии возможны обмороки. Эти жалобы, как правило, зависят не от степени малокровия, а от продолжительности заболевания и возраста больных.
Железодефицитная анемия характеризуется изменениями кожи, ногтей и волос. Кожа обычно бледная, иногда с легким зеленоватым оттенком (хлороз) и с легко возникающим румянцем щек, она становится сухой, дряблой, шелушится, легко образуются трещины. Волосы теряют блеск, сереют, истончаются, легко ломаются, редеют и рано седеют. Специфичны изменения ногтей: они становятся тонкими, матовыми, уплощаются, легко расслаиваются и ломаются, появляется исчерченность. При выраженных изменениях ногти приобретают вогнутую, ложкообразную форму (койлонихия). В общем анализе крови при ЖДА будут регистрироваться снижение уровня гемоглобина и эритроцитов. Умеренная эритроцитопения может проявляться при НЬ
| | | следующая лекция ==> | |
| Практическая работа № 3 | | | Предмет и задачи культуры речи |
Дата добавления: 2015-05-10 ; Просмотров: 1758 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
В соответствии с рекомендациями ВОЗ, стандартизованы следующие критерии диагностики железодефицитных анемий у детей:
- снижение уровня СЖ менее 12 мкмоль/л;
- повышение ОЖСС более 69 мкмоль/л;
- насыщение трансферрина железом менее 17%;
- содержание гемоглобина ниже 110 г/л в возрасте до 6 лет и ниже 120 г/л — в возрасте старше 6 лет.
Таким образом, ВОЗ рекомендует достаточно точные критерии для диагностики железодефицитной анемии, однако методы диагностики требуют забора крови из вены и проведения достаточно дорогих биохимических исследований, что не всегда возможно в украинских лечебных учреждениях. Имеются попытки минимизации критериев диагностики железо-дефицитной анемии.
Федеральная служба по заболеваемости, эпидемиологии и образованию (United States Federal Government Centers for Disease Control — CDC) со штаб-квартирой в Атланте (Джорджия, США) рекомендует использовать для диагностики железо-дефицитной анемии 2 доступных критерия: снижение концентрации гемоглобина и гематокрита (Ht) при отсутствии у больного других заболеваний. Устанавливают предположительный диагноз железодефицитной анемии и назначают лечение препаратами железа на 4 нед из расчёта 3 мг элементарного железа на 1 кг массы тела больного в сутки. Достоинство данных рекомендаций — регистрация ответа на терапию препаратами железа по строго фиксированным критериям. К концу 4-й нед лечения концентрация гемоглобина должна повыситься на 10 г/л по отношению к исходной, a Ht — на 3%. Такой ответ подтверждает диагноз «железодефицитная анемия», и лечение продолжают в течение нескольких месяцев. Если ответ не получен, рекомендуют остановить лечение препаратами железа и пересмотреть данный случай с точки зрения диагностики процесса. Перегрузка железом организма за 4 нед при приёме препаратов железа внутрь маловероятна.

Лабораторную диагностику железодефицитной анемии осуществляют с помощью:
- общего анализа крови, выполненного «ручным» методом;
- анализа крови, выполненного на автоматическом анализаторе крови;
- биохимических исследований.
При диагностике любой анемии обязательно выполнение общего анализа крови с определением количества ретикулоцитов. Врач ориентируется на гипохромный и микроцитарный характер анемии. В общем анализе крови, выполненном «ручным» методом, выявляют:
- снижение концентрации гемоглобина ( 12 /л) количество эритроцитов;
- снижение цветового показателя ( 12-16 мм/ч);
- анизоцитоз (характерны микроциты) и пойкилоцитоз эритроцитов.
Ошибка определения параметров может достигать 5% и более. Стоимость одного общего анализа крови составляет около 5 долларов США.
Точным и удобным методом диагностики и дифференциальной диагностики служит метод определения эритроцитарных показателей на автоматических анализаторах крови. Исследование проводят как в венозной, так и в капиллярной крови. Ошибка в определении параметров значительно ниже, чем при «ручном» методе, и составляет менее 1%. При развитии дефицита железараньше всего повышается показатель выраженности анизоцитоза эритроцитов — RDW (норма
Портал iLive не предоставляет медицинские консультации, диагностику или лечение.
Информация, опубликованная на портале, предназначена только для ознакомления и не должна использоваться без консультации со специалистом.
Внимательно ознакомьтесь с правилами и политикой сайта. Вы также можете связаться с нами!
Copyright © 2011 — 2019 iLive. Все права защищены.
источник
Однако, для точной диагностики причины развития анемии необходимо провести ряд уточняющих анализов. Подтвердить возможную причину развития анемии позволяют пять лабораторных анализов крови:
- Сывороточное железо
- Общая железосвязывающая способность сыворотки
- Сывороточный ферритин
- Витамин B12 (Цианокобаламин)
- Витамин B9 (Фолиевая кислота)
Дефицит железа – самая распространенная причина развития анемии. По данным ВОЗ (Всемирной организации здравоохранения) анемией страдает примерно 25% населения во всем мире, при этом около 50% случаев анемии вызвано именно дефицитом железа. В развитых странах железодефицитная анемия обнаруживается у 2-5% взрослого населения. Среди беременных анемия встречается чаще.
Анализ крови на содержание железа, общей железосвязывающей способности сыворотки и ферритина дает возможность установить диагноз железодефицитной анемии. Определение уровня фолиевой кислоты (фолата) и цианокобаламина в крови, а также уровень фолата в эритроцитах позволяет установить диагноз «мегабластная анемия», которая возникает при дефиците витаминов B9 и B12. Причиной отклонения от нормы упомянутых выше показателей является не только анемия, но и другие состояния (рассмотрены ниже).
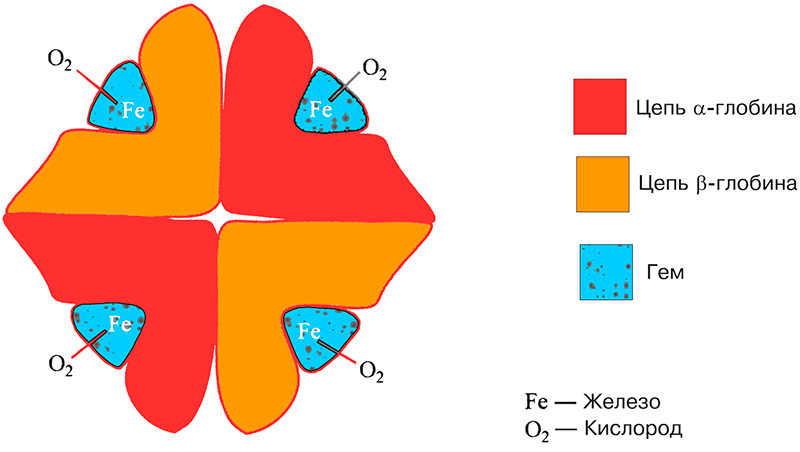
Способность гемоглобина, содержащегося в эритроцитах, транспортировать кислород зависит от содержания железа в молекуле гема (см рисунок 1), где кислород вступает в слабую взаимосвязь с атомом железа. Для образования и функционирования гемоглобина необходимо железо. Отметим, что железо также содержится в миоглобине (мышечном белке) и некоторых ферментах.
Рисунок 1. Молекула гемоглобина
В организме взрослого человека содержится около 5 г железа, из которого примерно 70% находится в эритроцитах циркулирующей крови (см рисунок 2). Большая часть остального количества содержащегося в организме железа депонируется в тканях (в основном в костном мозге, печени и селезенке). В этих «депо» железо входит в состав белка ферритина и гемосидерина.
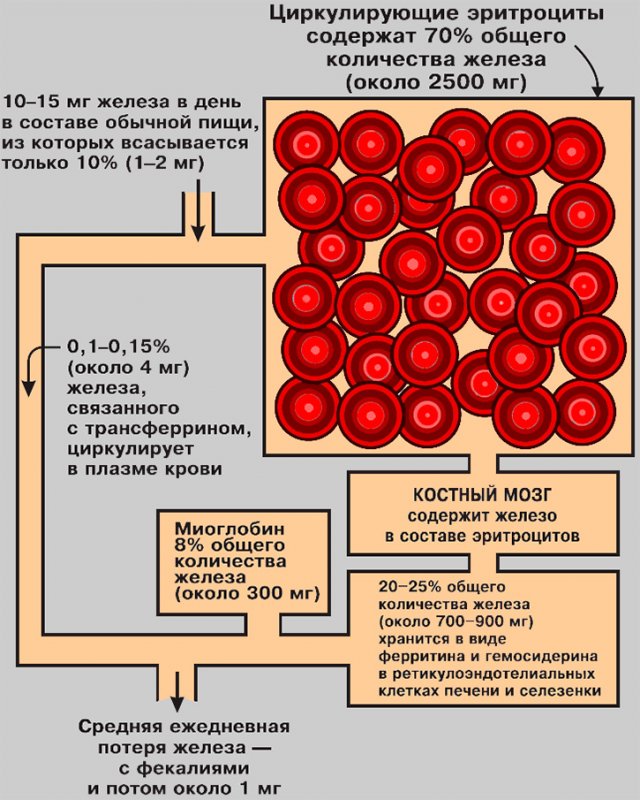
Рисунок 2. Распределение железа в организме: суточное поступление и потери
Определенная часть ферритина находится в крови. Именно концентрация ферритина в крови является точным индикатором состояния запасов железа в организме. Содержание железа в циркулирующей крови составляет примерно 3-4 мг (0,1% от общего содержания железа в организме); это железо связано с трансферрином (транспортным белком). Анализ на содержание железа в крови основан на определении именно трансферриносвязанной фракции.
Организм человека хорошо сохраняет железо. Эритроциты жизнеспособны примерно 100-120 дней, после их гибели (эритропоэза) высвобождается железо, которое возвращается в резерв костного мозга, чтобы участвовать в образовании новых эритроцитов. Железо имеет связь с белком – это не позволяет ему проникать через почечный фильтр, поэтому выделение его с мочой очень ограничено. Единственная значительная потеря железа происходит с эпителиальными клетками, которые постоянно слущиваются с поверхности кожи (таким образом организм теряет до 1 мг железа в сутки). В эритроцитах содержится основная часть железа, поэтому кровотечение представляет потенциальную опасность истощения его запасов. Так, при нормальном менструальном кровотечении организм ежемесячно теряет примерно 15 мг железа, поэтому здоровая женщина в период месячных теряет в среднем 1,5-2 мг железа в сутки.
Для компенсации потерь и для поддержания необходимых запасов железа в организме, дети, мужчины и женщины (в межменструальный период) должны получать минимум 1 мг железа с пищей, а женщины в период менструации – не менее 2 мг железа в сутки. Сбалансированное питание позволяет обеспечить поступление в среднем 10-15 мг железа в день. Среди продуктов питания основными источниками железа являются мясо, рыба, свежие фрукты и овощи, зелень, крупы. Усвоению железа способствует витамин C. В норме организм усваивает из пищи примерно 10% железа – это количество компенсирует суточные потери. Усвоение железа происходит в верхней части тонкой кишки. Важно отметить, что избыток железа опасен для организма не меньше, чем его дефицит. Поскольку в организме отсутствуют механизмы, регулирующие потери железа, контроль за его запасами зависит в основном от механизмов его усвоения. Так, усвоение железа с пищей регулируется потребностями организма в конкретный промежуток времени. Неусвоенное в кишечнике железо выводится с фекалиями.
К витаминам относится группа жизненно важных органических компонентов, имеющих разное химическое строение, которые необходимы организму в очень малых количествах. Организм человека не способен самостоятельно синтезировать витамины, поэтому единственным их источником является пища. Основная часть витаминов группы B, в том числе витамин B9 (фолиевая кислота, или фолат) и B12 (цианокобаламин) выполняют функцию коферментов в ферментативных реакциях клеточного метаболизма.
Фолиевая кислота и цианокобаламин обеспечивают функцию ключевых ферментов в процессе синтеза ДНК (ДНК необходимо для деления клеток). Особенно зависят от полноценного синтеза ДНК и, следовательно, от витаминов B9 и B12 ткани, в которых происходит постоянное деление клеток и быстрое клеточное обновление. Одна из этих тканей – костный мозг. В костном мозге непрерывно на протяжение всей жизни организма происходит продукция клеток, и для обеспечения этой функции требуется адекватное поступление витаминов B9 и B12. Фолиевая кислота и цианокобаламин участвуют в разных ферментативных реакциях, но для нормального процесса кроветворения они необходимы в первую очередь, что определяет их клиническое значение.
Витамины B9 и B12 синтезируются бактериями, а в организм человека они попадают с животной и растительной пищей, содержащей эти бактерии. Основной источник цианокобаламина – мясные продукты (особенно много витамина B12 содержится в печени животных), рыба и молочные продукты. Растительная пища (овощи, фрукты, зелень), как правило, не содержит этот витамин. Основным источником фолиевой кислоты является печень животных, зелень. Многие крупы содержат фолиевую кислоту и цианокобаламин. Минимальная суточная потребность взрослого человека в фолиевой кислоте составляет 150 мкг, в цианокобаламине – 1-2 мг. При условии соблюдения рекомендаций по здоровому питанию, дневной рацион позволяет покрыть необходимую суточную потребность организма в этих витаминах.
Для успешного высвобождения витамина B12 из поступающей пищи и дальнейшего его усвоения в кишечнике огромное значение имеет кислая среда желудка. То есть, чтобы цианокобаламин успешно усвоился в тонкой кишке, он должен вступить в связь с белком, синтезируемом в эпителиальных клетках желудка – внутренним фактором (см рисунок 3). После усвоения в кишечнике транскобаламин (транспортный белок) переносит с кровотоком витамин B12 в разные ткани (в том числе и костный мозг).
Рисунок 3. Усвоение витамина B12
Витамин B12 способен накапливаться в достаточных количествах в печени, что позволяет организму компенсировать его дефицит при отсутствии цианокобаламина в пище на протяжение длительного периода времени (в течение нескольких лет).
Процесс усвоения фолиевой кислоты в организме человека проходит гораздо проще, по сравнению с цианокобаламином. Фолат усваивается в верхних отделах тонкой кишки и с током крови транспортируется в свободной форме или в связи с альбумином к тканям организма (включая костный мозг).
Как и цианокобаламин, фолиевая кислота способна накапливаться в организме (в основном в печени). Но запасов витамина B9 организму хватает всего лишь на несколько месяцев (в случае отсутствия этого компонента в пище).
Итак, рассмотрев кратко физиологию процесса кроветворения, можно сделать вывод, что образование клеток крови зависит от следующих факторов:
- Адекватного поступления в организм с пищей витаминов B9 и B12
- Нормального синтеза желудком соляной кислоты и внутреннего фактора, необходимых для полноценного усвоения витамина B12 в кишечнике
- Функционирования желудочно-кишечного тракта, то есть от нормального усвоения в подвздошной кишке
- Продукции транскобаламина (транспортного белка)
Рассматриваемые анализы, за редким исключением, назначают пациентам, у которых была обнаружена анемия на общем анализе крови (см статью «Анализ крови: Эритроциты, Гемоглобин, Индексы эритроцитов» ). Основываясь на показателе среднего объема эритроцитов можно определить, какой из нижеперечисленных анализов лучше всего назначать. То есть, сниженный объем эритроцитов указывает на вероятность того, что у пациента железодефицитная анемия – в этом случае необходимо исследовать уровень железа и ферритина в крови; если средний объем эритроцитов увеличен, необходимо назначить анализ крови на уровень витаминов B9 и B12.
Уровень железа в плазме (сыворотке) крови – определение концентрации железа в плазме (не включает определение содержания железа в эритроцитах и ферритине).
Общая железосвязывающая способность – определение уровня трансферрина в крови (трансферрин – белок, который связывает железо в плазме крови).
Сывороточный ферритин – определение уровня ферритина в крови (ферритин – белок, в составе которого железо находится в тканях организма). Уровень ферритина в крови является индикатором запаса железа в организме.
Витамин B12 и фолиевая кислота в крови – определение уровня цианокобаламина и фолиевой кислоты в крови. Низкий показатель указывает на дефицит этих витаминов.
Фолат эритроцитов – определение концентрации фолиевой кислоты в эритроцитах. Низкий показатель указывает на дефицит витамина B9.
Для проведения этих анализов пациент не нуждается в какой-либо специальной подготовке.
Забор крови для проведения анализа можно проводить в любое время. Рекомендуется брать кровь в удобное для транспортировки в лабораторию время.
Для проведения анализа на содержание железа в крови, железосвязывающей способности и определения уровня ферритина необходимо 5 мл венозной крови. Для исследования как правило используют сыворотку (при этом кровь собирают в обыкновенную пробирку без антикоагулянта).
Для проведения анализа на содержание фолата в эритроцитах кровь собирают в пробирку с антикоагулянтом (ЭДТА).
Для проведения анализа на содержание фолиевой кислоты и цианокобаламина необходимо 5 мл венозной крови, которую собирают в обычную пробирку (без каких-либо добавок).
Железо: 10-30 мкмоль/л
Общая железосвязывающая способность: 40-75 мкмоль/л
Ферритин: 10-300 мкмоль/л
Витамин B12: 150-1000 нг/л
Фолиевая кислота: 150-700 мкмоль/л
Лаборатории используют разные методики исследования, поэтому референсные значения могут быть другими (их предоставляет лаборатория, проводившая анализ). Также при интерпретации результатов анализа необходимо учитывать половые различия пациентов.
Отклонения от нормы уровня железа в крови, общей железосвязывающей способности и ферритина связаны со следующими состояниями:
- Железодефицитная анемия
- Инфекционные заболевания (АХЗ – анемия при хронических заболеваниях) и хронические воспаления (болезнь Крона и др)
- Избыток железа
Железодефицитная анемия часто носит многофакторный характер, то есть, у пациента может быть сразу несколько причин развития этого состояния. Наиболее вероятными причинами развития железодефицитной анемии являются:
- Недостаток железа в пище
- Повышенные потери железа организмом
- Нарушения процесса усвоения железа в кишечнике
- Повышенная потребность организма в железе
Недостаток железа в пище среди населения, проживающего в экономически развитых странах – редкая причина развития анемии (конечно, бывают случаи, когда дефицит железа оказывает влияние). Тем не менее, в депрессивных регионах плохое питание – основная причина дефицита железа в организме. Патологии желудочно-кишечного тракта (например, дизентерия, тропическое спру и др) нарушают процесс усвоения железа, однако это довольно редкие причины дефицита этого элемента.
Самая распространенная причина развития железодефицитной анемии у взрослого населения развитых стран – хроническая кровопотеря. Так как основной пул железа (примерно 70%) содержится в эритроцитах, кровопотери способны вызвать дефицит железа. Отметим, что организм накапливает железо в тканях, поэтому единичные случаи кровотечения (даже тяжелой кровопотери) не вызовет дефицит железа. Но хроническая кровопотеря (регулярная и/или продолижительная потеря небольших объемов крови) в течение долгого периода времени, постепенно истощает запасы железа. Частая причина развития дефицита железа среди женщин детородного возраста – меноррагия (очень обильные менструации).
Хронические кровопотери часто связаны с распространенными, но тяжелыми патологиями желудочно-кишечного тракта (язва желудка или двенадцатиперстной кишки, язвенный колит, рак и др). В этом случае кровотечения могут оставаться незамеченными на протяжение многих месяцев и даже лет, поскольку кровь незаметно выводится с фекальными массами. Причиной возникновения кровотечения может быть прием некоторых лекарственных препаратов, вызывающих раздражение слизистой оболочки желудка (например, аспирин и другие нестероидные противовоспалительные средства). Поэтому риск развития железодефицитной анемии повышается при длительной терапии аспирином. Исследования показали, что самой частой причиной развития железодефицитной анемии в взрослых мужчин и женщин в период постменопаузы являются кровотечения в желудочно-кишечном тракте.
При некоторых патологиях пищеварительной системы происходят нарушения процесса усвоения железа в кишечнике, что также способствует развитию железодефицитной анемии. Прежде всего – это целиакия (мультифакториальная патология, характеризующаяся нарушением процесса пищеварения, при котором нарушается чувствительность к некоторым белкам). Исследования показывают, что распространенность целиакии среди населения гораздо выше, чем предполагалось ранее (сегодня целиакия считается относительно распространенной причиной дефицита железа). Хронические воспалительные заболевания кишечника (язвенный колит, болезнь Крона) также характеризуются нарушением усвоения железа и последующим развитием его дефицита. Такие же последствия возникают после гастрэктомии (хирургического удаления желудка).
У здоровых людей желудок колонизирован бактериями Helicobacter pylori. При определенных факторах эти микробы могут стать причиной развития гастрита, язвы или железодефицитной анемии. Механизм развития этой патологии полностью не изучен, но ученые предполагают, что он связан с нарушением усвоения железа. В этом случае терапия антибактериальными препаратами, целью которой является эрадикация Helicobacter pylori, эффективная и в отношении железодефицитной анемии.
Беременность сопровождается рядом физиологических изменений, в том числе повышенной продукцией эритроцитов. При адаптации к таким изменениям потребность организма в железе увеличивается в 2-3 раза. Если запасы железа при этом не восполняются, возникает дефицит этого элемента. Развитие железодефицитной анемии наблюдается у многих женщин на поздних сроках беременности. У детей в период интенсивного роста повышается потребность в железе, что также может быть причиной развития железодефицитной анемии, особенно при плохом питании.
Любые случаи железодефицитной анемии требуют обязательного поиска причины ее возникновения. Это состояние может быть симптомом серьезных патологий пищеварительной системы или гинекологических заболеваний. Многие последние рекомендации для пациентов с железодефицитной анемией неясного генеза в независимости от степени тяжести указывают на необходимость проведения диагностики на предмет обнаружения целиакии (для этого назначают анализ крови на антитела к тканевой трансглутаминазе (IgA-tTG). Также необходимо провести анализ мочи на предмет обнаружения гематурии (одного из симптомов рака мочевого пузыря). Кроме этого, все взрослые мужчины и женщины старше 50 лет (период постменопаузы) должны пройти обследование желудочно-кишечного тракта (эндоскопия, ренгенография с барием и др).
Помимо основных признаков анемии, описанных в статье «Анализ крови: Эритроциты, Гемоглобин, Индексы эритроцитов» , у больных железодефицитной анемией могут возникать некоторые специфические симптомы:
- Глоссит (воспаление языка)
- Ангулярный стоматит (заеды)
- Изменения ногтей (изменение формы: вогнутые или гребневидные; ломкость и т.д.)
Уровень ферритина в крови – точный показатель состояния запасов железа в организме. Снижение концентрации ферритина происходит в период прогрессивного истощения запасов железа, до момента возникновения первых симптомов анемии. Когда запасы железа в организме полностью истощаются, возникают признаки его дефицита (при этом уровень ферритина в крови очень низкий или он вообще не определяется). Уровень железа в крови часто снижен, однако может оставаться на нижней границе нормы. Железосвязывающая способность крови всегда высокая.
При железодефицитной анемии типичным результатом анализа крови является:
- Уровень железа: 5-10 мкмоль/л (может быть на нижней границе нормы)
- Железосвязывающая способность сыворотки: выше 75 мкмоль/л (всегда повышена)
- Ферритин:«Анализ крови: Эритроциты, Гемоглобин, Индексы эритроцитов»
- Желтуха (незначительная)
- Заеды (ангулярный стоматит)
- Воспаление зыка (глоссит)
При значительном дефиците фолиевой кислоты и цианокобаламина у пациентов может возникать нейропатия. При этом развиваются следующие неврологические симптомы:
- Повышенная раздражительность
- Неспособность сосредоточиться
- Нарушения памяти
- Парестезии (аномальная чувствительность, например, покалывание, жжения или «мурашки» в руках и ногах)
- Расстройства моторики, например, атаксия (проявляется затруднениями при ходьбе)
- Нарушения психики (редко)
Отметим, что при дефиците цианокобаламина неврологические симптомы могут возникать даже при отсутствии других признаков анемии.
При пернициозной анемии, как и в других случаях мегалобластной анемии, а также при нейропатии (вызванной дефицитом витамина B12) уровень цианокобаламина в крови как правило низкий. Бывают случаи, когда уровень витамина B12 в крови находится на нижней границе нормы, что приводит к трудностям в постановке диагноза. Уровень фолиевой кислоты в крови при этом в основном остается в пределах нормы (может быть незначительно повышен). Отметим, что при дефиците цианокобаламина концентрация фолиевой кислоты в эритроцитах остается в пределах нормы или понижается.
Если мегалобластная анемия вызвана дефицитом фолиевой кислоты, уровень цианокобаламина в крови остается в пределах нормы (при этом концентрация фолиевой кислоты в эритроцитах и крови снижена). Отметим, что содержание фолиевой кислоты в эритроцитах является более надежным маркером, поскольку при некоторых патологиях (например, тяжелые заболевания почек или печени) уровень фолиевой кислоты в крови может быть низким несмотря на достаточное количество этого витамина в организме.
источник