РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК — 2017
| МКБ-10 | |
| Код | Название |
| D50 | Железодефицитная анемия |
| D50.0 | Постгеморрагическая (хроническая) анемия |
| D50.8 | Другие железодефицитные анемии |
| D50.9 | Железодефицитная анемия неуточненная |
Дата разработки/пересмотра протокола: 2013 год (пересмотрен в 2017 г.)
Сокращения, используемые в протоколе:
(англ. Iron-refractory iron-deficiency anemia) железорефрактерная железодефицитная анемия
(англ. Mean corpuscular hemoglobin) – среднее содержание гемоглобина в эритроците в пг
(англ. Mean corpuscular volume) средний объем эритроцита в фл
сатурация трансферрина (англ. Transferrin Saturation) или коэффициент насыщение трансферрина железом
общая железосвязывающая способность сыворотки
растворимые рецепторы трансферрина
Пользователи протокола: врач общей практики, терапевт, гематолог, гинеколог, хирург, ревматолог, нефролог, пульмонолог, гастроэнтеролог, эндокринолог.
Категория пациентов: взрослые.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |
Классификация[1,3]:
Общепризнанной классификации ЖДА не существует.
Латентный дефицит железа, функциональный дефицит железа, анемия хронических заболеваний являются самостоятельными нозологическими формами в классификацию ЖДА не включены.
Наиболее часто используется классификация по степени тяжести и этиологическая классификация [1].
Классификация ЖДА по степени тяжести [3]:
Этиологическая классификация ЖДА (по Camaschella C., 2015 в модификации)[1]:
| Причина | Примеры |
| Повышенное потребление железа | Быстрый рост в подростковом периоде, менструальные кровопотери, беременность во втором и третьем триместрах, донорство крови |
| Недостаточное алиментарное поступление железа | Недостаточное алиментарное поступление железа вследствие недоедания, обусловленного социальными причинами, вегетарианства и др. |
| Нарушение абсорбции железа | Гастроэктомия, дуоденальный шунт, бариатрическая хирургия, целиакия, воспалительные заболевания кишечника, атрофический гастрит, глистная инвазия |
| Хронические кровопотери | Из желудочно-кишечного тракта: эзофагит, гастрит, язва желудка, язва двенадцатиперстной кишки, дивертикулез, опухоли желудочно-кишечного тракта, воспалительные заболевания кишечника, ангиодисплазия, геморрой, паразитоз, оккультные кровотечения Из половых и мочевыводящих путей: обильные и/или продолжительные менструации, внутрисосудистый гемолиз (в т.ч. при пароксизмальной ночной гемоглобинурии, аутоиммунной гемолитической анемии с холодовыми антителами, маршевая гемоглобинурия, микроангиопатический гемолиз, повреждение эритроцитов протезом клапанов) Системные кровотечения, включая геморрагическую телеангиоэктазию, хронический шистосомоз, синдром Мюнхгаузена |
| Связанные с лекарственными препаратами | Глюкокортикостероиды, салицилаты, нестероидные противовоспалительные, ингибиторы протонной помпы [4, 5] |
| Наследственные | IRIDA (мутация в гене TMPRSS6) и более редкие причины |
| Эритропоэз, ограниченный железом | Лечение с использованием эритропоэтинов анемии хронических заболеваний, хронической болезни почек |
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ [1-3]
Диагностические критерии
Жалобы и физикальное обследование:
Общеанемический синдром: слабость, повышенная утомляемость, головокружение, головные боли (чаще в вечернее время), одышка при физической нагрузке, ощущение сердцебиения, синкопальные состояния, мелькание «мушек» перед глазами при невысоком уровне артериального давления, часто наблюдается умеренное повышение температуры, нередко сонливость днем и плохое засыпание ночью, раздражительность, нервность, конфликтность, плаксивость, снижение памяти и внимания, ухудшение аппетита. Выраженность жалоб зависит от адаптации к анемии. Лучшей адаптации способствует медленный темп анемизации.
Сидеропенический синдром:
· изменение кожи и ее придатков (сухость, шелушение, легкое образование трещин, бледность). Волосы тусклые, ломкие, «секутся», рано седеют, усиленно выпадают, изменения ногтей: истончение, ломкость, поперечная исчерченность, иногда ложкообразная вогнутость (койлонихии).
· изменения слизистых оболочек (глоссит с атрофией сосочков, трещины в углах рта, ангулярный стоматит).
· изменения со стороны желудочно-кишечного тракта (атрофический гастрит, атрофия слизистой пищевода, дисфагия). Затруднение глотания сухой и твердой пищи.
· мышечная система. Миастения (вследствие ослабления сфинктеров появляются императивные позывы на мочеиспускание, невозможность удерживать мочу при смехе, кашле, иногда ночное недержание мочи у девочек). Следствием миастении могут быть и невынашивание беременности, осложнения в процессе беременности и родов (снижение сократительной способности миометрия).
· пристрастие к необычным запахам.
· извращение вкуса. Выражается в стремлении есть что-либо малосъедобное.
· склонность к тахикардии, гипотонии.
Лабораторные исследования:
Лабораторные исследования при подозрении на ЖДА могут включать помимо ОАК с ретикулоцитами и показателей обмена железа также исследование уровня витамина В12, фолиевой кислоты, биохимические показатели (общий белок, креатинин, мочевина, глюкоза крови, общий билирубин, прямой билирубин, трансаминазы) и другие исследования в зависимости от особенностей клинической картины и широты дифференциально-диагностического поиска. План исследований также может расширяться для уточнения причин железодефицита и исключения скрытых кровопотерь и проведения онкопоиска.
| № п/п | Лабораторный показатель | Референсный интервал (может меняться в зависимости от лаборатории) | Изменения при ЖДА |
| 1 | Морфологические изменения эритроцитов | нормоциты – 68% микроциты – 15,2% макроциты – 16,8% | Микроцитоз сочетается с анизоцитозом, пойкилоцитозом, в наличии анулоциты, плантоциты |
| 2 | Цветовой показатель | 0,86 -1,05 | Гипохромия показатель менее 0,86 |
| 3 | Содержание гемоглобина | Женщины – не менее 120 г/л Мужчины – не менее 130 г/л | Уменьшено |
| 4 | МСН | 27-31 пг | Менее 27 пг |
| 5 | МСНС | 33-37% | Менее 33 % |
| 6 | МСV | 80-100 фл | Снижен |
| 9 | Количество ретикулоцитов | 2-10:1000 | Не изменено |
| 11 | Железо сыворотки | Женщины – 12-25 мкмль/л Мужчины –13-30 мкмоль/л | Снижено |
| 12 | Общая железосвязывающая способность сыворотки крови | 30-85 мкмоль/л | Повышена |
| 13 | Латентная железосвязывающая способность сыворотки | Менее 47 мкмоль/л | Выше 47 мкмоль/л |
| 14 | Коэффициент насыщения трансферрина железом (TSat) | ≥16% | Уменьшено |
| 15 | Уровень ферритина * | 15-150 мкг/л | Уменьшение |
* — показатель информативен только при отсутствии признаков системного воспалительного ответа (например — при нормальном уровне СРБ)
Инструментальные исследования:
С целью выявления источников кровопотери, патологии других органов и систем, в том числе солидных опухолей:
· фиброгастродуоденоскопия по показаниям;
· рентгенологическое исследование органов ЖКТ по показаниям;
· рентгенологическое исследование органов грудной клетки по показаниям;
· фиброколоноскопия по показаниям;
· ректороманоскопия по показаниям;
· УЗИ органов малого таза по показаниям;
· УЗИ органов брюшной полости по показаниям;
Показания для консультации специалистов:
· консультация хирурга – для исключения кровотечения из желудочно-кишечного тракта;
· консультация гастроэнтеролога – при подозрении на мальабсорбцию или хронические кровопотери при патологии органов желудочно-кишечного тракта;
· консультация стоматолога – стоматологические проблемы, приводящие к анемии;
· консультация оториноларинголога – носовые кровотечения;
· консультация онколога – злокачественное поражение, которое является причиной кровотечения;
· консультация нефролога – исключение заболеваний почек при дифференциальной диагностике с анемией хронических заболеваний;
· консультация фтизиатра – кровотечение или вторичная анемия на фоне туберкулеза;
· консультация пульмонолога – кровопотери или вторичная анемия на фоне заболеваний бронхолегочной системы;
· консультация гинеколога – кровотечение из половых путей (ювенильные кровотечения, дисменореи и т.д.);
· консультация эндокринолога – снижение функции щитовидной железы, наличие диабетической нефропатии;
· консультация гематолога – для исключения заболеваний системы крови и при неэффективности ферротерапии у пациентов с верифицированным дефицитом железа;
· консультация проктолога – ректальные кровотечения;
· консультация инфекциониста – при наличии признаков гельминтоза или другого паразитоза, приводящего к анемии.
Диагностический алгоритм: см. Приложение 1
Дифференциальный диагноз и обоснование дополнительных исследований:
Железодефицитная анемия до получения результатов исследования обмена железа на основании ОАК требует проведения дифференциальной диагностики с другими гипохромными анемиями, вызванными нарушением синтеза гемоглобина. К ним относятся анемии, связанные с нарушением синтеза порфиринов (анемия при свинцовом отравлении, при врожденных нарушениях синтеза порфиринов), а также талассемии. Гипохромные анемии в отличие от железодефицитных анемий протекают с высоким содержанием железа в крови и депо, которое не используется для образования гема (сидероахрезия), при этих заболеваниях отсутствуют признаки тканевого дефицита железа. Дифференциальным признаком анемии, обусловленной нарушением синтеза порфиринов, является гипохромная анемия с базофильной пунктацией эритроцитов, ретикулоцитов, усиленным эритропоэзом в костном мозге с большим количеством сидеробластов. Для талассемии характерны мишеневидная форма и базофильная пунктация эритроцитов, ретикулоцитоз и наличие признаков повышенного гемолиза.
Верификация дефицита железа и ЖДА проводится только на основании лабораторных данных – снижения уровня гемоглобина, ферритина, сывороточного железа, TSat и др. в связи с чем дифференциальная диагностика с нозологиями, при которых не характерен дефицит железа (миелодиспластический синдром, апластическая анемия, витамин В12 дефицитная анемия, фолиеводефицитная анемия, гемолитические анемии) не вызывает затруднений.
В случаях, когда у пациента с анемией и лабораторно подтвержденным дефицитом железа со стороны системы крови выявляются симптомы или лабораторные изменения, которые не характерны для ЖДА, требуется дообследование у гематолога.
Дифференциальная диагностика при лабораторно подтвержденной ЖДА требуется с другими заболеваниями и состояниями при которых возможно развитие сидеропении [1].
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Основные критерии диагноза |
| Латентный дефицит железа | Характерно снижение уровня сывороточного железа | Сывороточное железо, мкмоль/л | ê |
| TSat, % | ≥16% | ||
| Ферритин, мкг/л | |||
| Гемоглобин, г/л | Норма | ||
| MCV [2] | ê или в норме | ||
| MCH [3] | ê или в норме | ||
| Дополнительно: | |||
| sTFR, мг/л | é | ||
| Содержание гемоглобина в ретикулоцитах, пг | |||
| Функциональный дефицит железа | Возможно снижение уровня сывороточного железа | Сывороточное железо, мкмоль/л | ê или в норме |
| TSat, % | ê или в норме | ||
| Ферритин, мкг/л | Норма | ||
| Гемоглобин, г/л | Норма | ||
| MCV | Норма | ||
| MCH | Норма | ||
| Дополнительно: | |||
| sTFR, мг/л | é | ||
| Содержание гемоглобина в ретикулоцитах, пг | |||
| Функциональный дефицит железа | Возможно снижение уровня сывороточного железа | Сывороточное железо, мкмоль/л | ê или в норме |
| TSat, % | ê или в норме | ||
| Ферритин, мкг/л | Норма | ||
| Гемоглобин, г/л | Норма | ||
| MCV | Норма | ||
| MCH | Норма | ||
| Дополнительно: | |||
| sTFR, мг/л | é | ||
| Содержание гемоглобина в ретикулоцитах, пг | |||
| IRIDA (ведущий признак – неэффективность ферротерапии) | Характерно снижение уровня сывороточного железа и TSat | Сывороточное железо, мкмоль/л | ê |
| TSat, % | |||
| Ферритин, мкг/л | вариабельно | ||
| Гемоглобин, г/л | ê | ||
| MCV | êê | ||
| MCH | êê | ||
| Дополнительно: | |||
| sTFR, мг/л | é | ||
| Содержание гемоглобина в ретикулоцитах, пг | ê | ||
| Анемия хронических заболеваний | Характерно снижение сывороточного железа | Сывороточное железо, мкмоль/л | ê |
| TSat, % | ê или в норме | ||
| Ферритин, мкг/л | >100 | ||
| Гемоглобин, г/л | ê | ||
| MCV | ê или в норме | ||
| MCH | ê или в норме | ||
| Дополнительно: | |||
| sTFR, мг/л | ê или в норме | ||
| Содержание гемоглобина в ретикулоцитах, пг | ê | ||
| ЖДА и анемия хронических заблеваний | Характерно снижение сывороточного железа | Сывороточное железо, мкмоль/л | ê |
| TSat, % | ê или в норме | ||
| Ферритин, мкг/л | |||
| Гемоглобин, г/л | ê | ||
| MCV | êê | ||
| MCH | êê | ||
| Дополнительно: | |||
| sTFR, мг/л | вариабельно | ||
| Содержание гемоглобина в ретикулоцитах, пг | ê | ||
| ЖДА | Характерно снижение сывороточного железа, TSat и ферритина | Сывороточное железо, мкмоль/л | ê |
| TSat, % | |||
| Ферритин, мкг/л | |||
| Гемоглобин, г/л | ê | ||
| MCV | ê | ||
| MCH | ê | ||
| Дополнительно: | |||
| sTFR, мг/л | é | ||
| Содержание гемоглобина в ретикулоцитах, пг | ê |
Получить консультацию по медтуризму
Получить консультацию по медтуризму
| Аскорбиновая кислота (Ascorbic acid) |
| Железа (III) гидроксид декстран (Ferric (III) hydroxide destrane) |
| Железа (III) гидроксид полимальтозат (Ferric (III) hydroxide polymaltosate) |
| Железа (III) гидроксид сахарозный комплекс (Ferric (III) hydroxide sacharose complex) |
| Железа глюконат (Ferrous gluconate) |
| Железа карбоксимальтозат (Ferric carboxymaltosate) |
| Железа сульфат (Ferric sulfate) |
| Железа фумарат (Ferrous fumarate) |
| Фолиевая кислота (Folic acid) |
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ [6-16]
ЖДА является хроническим заболеванием, развитие которого требует времени, за которое успевают включиться механизмы адаптации и в большинстве случаев достигается компенсация. Пациенты сохраняют неплохое самочувствие и клинические проявления ЖДА минимальны. Поэтому лечение ЖДА должно проводиться амбулаторно. При использовании парентеральных препаратов железа возможна госпитализация в дневной стационар.
Лечебная программа при ЖДА включает:
· устранение этиологических факторов (лечение основного заболевания);
· лечебное питание (диета № 11);
· лечение железосодержащими препаратами;
· восполнение запасов железа (терапию насыщения).
· противорецидивную терапию.
Немедикаментозное лечение:
· Диета. При железодефицитной анемии больному показана диета, богатая железом. Железо из продуктов животного происхождения всасывается в кишечнике в значительно больших количествах, чем из растительных продуктов.
Медикаментозное лечение:
ЖДА не может быть успешно излечена в случае, если не устранена её причина. Основой патогенетической терапии ЖДА являются препараты железа. Трансфузии не заменяют ферротерапию. Ферротерапия может проводиться препаратами железа для приема внутрь и парентеральными препаратами.
Из парентеральных препаратов предпочтительнее использование внутривенных, т.к. введение внутримышечных болезненно, имеет вариабельную абсорбцию и может приводить к формированию инфильтратов.
Конечный результат терапии препаратами железа вне зависимости от пути введения одинаков – рост уровня гемоглобина. Отличия между различными препаратами с различными путями введения заключаются в переносимости лечения и темпах прироста уровня гемоглобина.
Препараты железа для приема внутрь
Основными принципами лечения ПЖ для приема внутрь являются следующие:
· назначение ПЖ с достаточным содержанием элементарного железа;
· нецелесообразность одновременного назначения витаминов группы В (в том числе В12), фолиевой кислоты без специальных показаний в связи с отсутствием доказательств преимуществ в эффективности и безопасности перед монокомпонентными препаратами, невозможностью отследить фармакокинетику препарата при наличии 3 и более компонентов в 1 таблетке;
· избегание назначения препаратов железа внутрь при наличии признаков нарушения всасывания в кишечнике;
· достаточная продолжительность насыщающего курса терапии (не менее 3 мес., может увеличиваться до 5-6 месяцев);
· необходимость проведения поддерживающей терапии ПЖ после нормализации показателей гемоглобина в соответствующих ситуациях.
Рекомендуемая суточная доза элементарного железа у большинства взрослых составляет 150-200 мг. [9] Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. Например, таблетка железа сульфата массой 325 мг содержит 65 элементарного железа, три таблетки – 195 мг железа из которых может быть адсорбированно и утилизированно только 25 мг. [10]
Терапия препаратами железа для приема внутрь должна проводиться в течение 3х месяцев для восполнения запасов в депо. [9]
При пероральной ферротерапии наиболее распространены гастроинтестинальные побочные эффекты. Они включают металлический вкус, тошноту, диарею, запор, потемнение стула.
Для уменьшения выраженности побочных эффектов возможно уменьшение дозы (перевод на однократный прием, например) или увеличение интервала приёма, переход на прием другого препарата железа с меньшим содержанием элементарного железа, переход с таблеток на жидкие лекарственные формы, которые позволяют более просто подбирать переносимую дозу, отмена пероральных препаратов и назначение внутривенных.
Причины неэффективности терапии ПЖ для приема внутрь:
· отсутствие дефицита железа (неправильная трактовка природы гипохромной анемии и ошибочное назначение ПЖ);
· недостаточная дозировка ПЖ (недоучет количества трехвалентного железа в препарате);
· недостаточная длительность лечения ПЖ;
· нарушение всасывания ПЖ, назначаемых внутрь больным с соответствующей патологией;
· одновременный прием препаратов, нарушающих всасывание железа;
· наличие хронических (оккультных) кровопотерь, чаще всего из органов ЖКТ;
· сочетание ЖДА с другими анемическими синдромами (В12-дефицитной, фолиеводефицитной).
Парентеральные препараты железа.
Показания для назначения парентеральных препаратов железа [1, 11]:
· нарушение всасывания при патологии кишечника (энтериты, синдром недостаточности всасывания, резекция тонкого кишечника, резекция желудка по методу Бильрот II с выключением двенадцатиперстной кишки);
· выраженные гастроинтестинальные побочные эффекты пероральной терапии, не устранимые другими способами;
· постоянные потери крови, при которых потребность в железе превышает физиологические возможности для всасывания железа (например, тяжелое маточное кровотечение, наследственная геморрагическая телеангиоэктазия с поражением слизистых оболочек);
· пожелание пациента о быстром (за 1-2 визита) восполнении дефицита железа и отказ от продолжительной многомесячной ферротерапии;
Кумулятивную дозу, необходимую для восстановления уровня гемоглобина в крови и восполнения запасов железа в организме, при внутривенном введении ПЖ вычисляют по формуле Ганзони:
*депо железа у человека с массой тела >35 кг и = 35 кг = 500 мг и
| Лекарственная группа (МНН) | Лекарственные средства | Способ применения | Уровень доказательности | |
| Монокомпонентные препараты железа B03A (код АТХ) | ||||
| Глюконат железа** | Глюконат железа* 300 мг | Пероральный прием по 2 таб. х 2-3 раза в день | III C | |
| Сульфат железа** B03AA07 | Сульфат железа табл. 256.3 мг (80 мг железа), Сульфат железа 325 мг (105 мг иона (II) железа (Fe 2+ )) | Пероральный прием по 1таб. х 2 раза в день | III C | |
| Фумарат железа** B03AA02 | Фумарат железа* (суспензия 3 гр) для детей, Железа фумарат 200 – таб. 200 мг (65 мг железа), Железа фумарат капс.300 мг (100 мг эл. Железа) | Пероральный прием: железа фумарат по 1таб. х 3 раза в день, по 1 капс. х 2-4 раза в день | III C | |
| Комбинированные препараты В03АА | ||||
| В03АА Железа (II) сульфат сухой + Аскорбиновая кислота 60 мг | Сульфат железа таб.320 мг+аскорбиновая кислота 60 мг | Пероральный прием, по 1 таб. х 1-2 раза в сутки | III C | |
| Фумарат железа, фолиевая кислота B03AD02 | Железа фумарат 163,56 мг (50 мг железа) и фолиевая кислота 540 мкг | Перорально по 1 капс. х 2 раза в сутки | III C | |
| Препараты железа (III) валентные | ||||
| Железа (III) гидроксид полимальтозат** | Железа (III) гидроксид полимальтозат 400 мг (100 мг эл.железа) Таб. 375 мг (100 мг эл.железа) | Пероральный прием по 1 жеват. таб. х 2-3 р в день | IIB | |
| Препараты железа для парентерального введения. | ||||
| Лекарственная группа (МНН) | Лекарственные средства | Способ применения | Уровень доказательности | |
| B03AC02 Железа оксида сахарат | Железо III гидроксид сахарозный комплекс 540 мг (железа 20 мг); | |||
Железа (III) гидроксида сахарозного комплекса 333,0 мг (эквивалентно элементарному железу) 20,0 мг
В/в медленно (0,2 мл/мин) в дозе 100–200 мг железа (2–4 мл), предпочтительно разведенного в 10–20 мл 0,9% раствора натрия хлорида или 5% раствора глюкозы. Начальная доза препарата составляет 25 мг железа или 0,5 мл раствора, которая вводится в/в медленно в течение 1–2 мин
в/в (внутривенно) капельно (инфузионно) 1000 мг железа 1 раз в неделю.
*применение препарата после регистрации на территории РК
**нет в КНФ
Хирургическое вмешательство:
Проводятся при продолжающихся кровотечениях на стационарном уровне.
Дальнейшее ведение:
· Для пациентов, получающих пероральную ферротерапию контрольные исследования ОАК следует проводить через 1-2 недели от начала лечения.
· При терапии парентеральными препаратами, особенно с однократным введением, контрольные исследования ОАК могут проводится через 4-8 недель от введения препарата.
· Пациенты с продолжающимися кровотечениями (например, с наследственной геморрагической телеангиоэктазией) нуждаются в более частом контроле.
NB! Причинами рецидива ЖДА могут быть недостаточная длительность приема пероральных препаратов, продолжающиеся потери крови, некорректный диагноз ЖДА, наличие дополнительных причин для развития анемии.
Индикаторы эффективности лечения: см. стационарный уровень.
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ [7-9]
Тактика лечения аналогична амбулаторному уровню. При гемодинамической нестабильности может проводиться трансфузия эритроцитсодержащих компонентов крови.
Эритроцитсодержащие компоненты крови при ЖДА следует переливать только в случаях гемодинамической нестабильности (УД – С; см. ниже) и подобная практика не должна быть рутинной [7].
Критерии гемодинамической нестабильности (должны присутствовать все признаки) [8]:
· Систолическое артериальное давление менее 100 мм.рт.ст.;
· Изменения сознания;
· Одышка/тахипное;
Количество трансфузий нужно максимально ограничивать. Уровень гемоглобина не является определяющим для оценки показаний к трансфузиям и выбору тактики лечения, т.к. пациенты могут иметь разную степень адаптации к анемии и клинические проявления являются более значимыми.
· Перечень основных лекарственных средств (имеющих 100% вероятность применения) – см. Амбулаторный уровень;
· Перечень дополнительных лекарственных средств (менее 100% вероятности применения) – см. Амбулаторный уровень.
Хирургическое вмешательство:
Показаниями к хирургическому лечению является продолжающееся кровотечение, нарастание анемии, вследствие причин, которые не могут быть устранены путем медикаментозной терапии.
Дальнейшее ведение: см. Амбулаторный уровень.
Индикаторы эффективности лечения [9]:
· разрешение симптомов;
· ретикулоцитарный криз на 7-10 дни от начала терапии препаратами железа, может быть не выражен при анемии легкой степени;
· повышение уровня гемоглобина происходит как правило медленно, начиная с 1-2 недель лечения с последующим приростом примерно 20 г/л в течение последующих трех недель с нормализацией к 6-8 неделям от начала лечения;
· контролировать показатели обмена железа рекомендуется не ранее, чем 4 недели после завершения терапии. Терапия препаратами железа завершается, если показатели обмена железа (TSat и ферритин) нормализуются. В случае дискордантности между TSat и ферритином рекомендуется ориентироваться на первый показатель.
Госпитализация в круглосуточный стационар может проводиться только в исключительных случаях при наличии признаков гемодинамической нестабильности, обусловленной только подтверждённой ЖДА при исключении всех других причин гемодинамической нестабильности.
Показания для плановой госпитализации: нет.
Показания для экстренной госпитализации:
Экстренная госпитализация пациента с ЖДА показана только при наличии признаков гемодинамической нестабильности при исключении других причин гемодинамической нестабильности:
· при выявленном источнике кровотечения в зависимости от источника кровопотери в отделение хирургического профиля (хирургию, гинекологию, проктологию и т.д.);
· при отсутствии установленного кровотечения – госпитализация в терапевтическое отделение.
- Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2017
- 1) Camaschella C. Iron-Deficiency Anemia /N Engl J Med 2015; 372:1832-1843. 2) Peyrin-Biroulet L.,Williet N., Cacoub P. Guidelines on the diagnosis and treatment of iron deficiency across indications: a systematic review /Am J Clin Nutr doi: 10.3945/ajcn.114.103366. 3) Сельчук В.Ю. Чистяков С.С. Толокнов Б.О. и соавт. Железодефицитная анемия: современное состояние проблемы /РМЖ, 2012. №1:1. 4) Sarzynski E. I., Puttarajappa C., Xie Y., Grover M., Laird-Fick H. Association between proton pump inhibitor use and anemia: a retrospective cohort study // Dig Dis Sci. 2011, Aug; 56 (8): 2349–2353. 5) Dado DN, Loesch EB, Jaganathan SP A Case of Severe Iron Deficiency Anemia Associated with Long-Term Proton Pump Inhibitor Use Curr Ther Res Clin Exp. 2017 Jan 21;84:1-3. 6) Auerbach M, Ballard H, Glaspy J. Clinical update: intravenous iron for anaemia. Lancet 2007; 369:1502. 7) Red Blood Cell Transfusion: 2016 Clinical Practice Guidelines from the AABB (Journal of the American Medical Association; October 12, 2016. 8) San Luis Obispo County EMS Agency ALS Treatment Protocols 2007 [Rev. 11/1/10] 9) Schrier S., Auerbach M. Treatment of iron deficiency anemia in adults / www.uptodate.com, aug, 2017. 10) Schrier SL. So you know how to treat iron deficiency anemia. Blood 2015; 126:1971. 11) Auerbach M, Deloughery T. Single-dose intravenous iron for iron deficiency: a new paradigm. Hematology Am Soc Hematol Educ Program. 2016 Dec;2016(1):57-66. 12) Rodgers GM, Auerbach M, Cella D, Chertow GM, Coyne DW, Glaspy JA, Henry DH High-molecular weight iron dextran: a wolf in sheep’s clothing? J Am Soc Nephrol. 2008;19(5):833 13) Administration of intravenous iron sucrose as a 2-minute push to CKD patients: a prospective evaluation of 2,297 injections.Macdougall IC, Roche A/Am J Kidney Dis. 2005;46(2):283. 14) Safety and efficacy of rapidly administered (one hour) one gram of low molecular weight iron dextran (INFeD) for the treatment of iron deficient anemia. Auerbach M, Pappadakis JA, Bahrain H, Auerbach SA, Ballard H, Dahl NV/Am J Hematol. 2011 Oct;86(10):860-2. Epub 2011 Aug 29. 15) Intravenous iron treatment in pregnancy: comparison of high-dose ferric carboxymaltose vs. iron sucrose. Christoph P, Schuller C, Studer H, Irion O, De Tejada BM, Surbek D/J Perinat Med. 2012;40(5):469. Epub 2012 May 13. 16) Intravenous ferric carboxymaltose compared with oral iron in the treatment of postpartum anemia: a randomized controlled trial. Van Wyck DB, Martens MG, Seid MH, Baker JB, Mangione A/Obstet Gynecol. 2007;110(2 Pt 1):267.
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Пивоварова Ирина Алексеевна – председатель РОО «Казахстанское Общество врачей-гематологов» Республики Казахстан, Председатель Правления ТОО «Центр гематологии».
2) Загурская Елена Юрьевна – заместитель Председателя Правления ТОО «Центр гематологии».
3) Клодзинский Антон Анатольевич – кандидат медицинских наук, гематолог ТОО «Центр гематологии», медицинский советник, заместитель председателя РОО «Казахстанское Общество врачей – гематологов» Республики Казахстан.
4) Хан Олег Ромуальдович – ассистент кафедры внутренних болезней, гематолог РГП на ПХВ «Научно- исследовательский институт кардиологии и внутренних болезней».
5) Юхневич Екатерина Александровна – и.о. доцента кафедры клинической фармакологии и доказательной медицины РГП на ПХВ «Карагандинский государственный медицинский университет», клинический фармаколог
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
Тургунова Людмила Геннадиевна – доктор медицинских наук, профессор, заведующая кафедрой терапевтических дисциплин факультета непрерывного профессионального развития, врач-гематолог РГП на ПХВ «Карагандинский государственный медицинский университет».
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение 1
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
На основании данных современной литературы и анализа собственных клинических наблюдений освещены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий у детей. Представлены основные принципы верификации причин анемического синдрома, обусловленного недостаточностью в организме ребенка железа, фолиевой кислоты и витамина В12. Изложены ключевые положения, лежащие в основе дифференциального диагноза между железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемиями. Представлены принципы лечения указанных дефицитных анемий у детей. Выявление анемии у ребенка определяет необходимость обязательного уточнения причин указанного патологического состояния. При этом своевременная верификация этиологии анемии позволяет без промедления начать адекватную терапию, что определяет ее эффективность и улучшает качество жизни ребенка в целом. Поздняя диагностика и отсутствие адекватной терапии при этом приводят к прогрессированию патологических процессов. Это негативно сказывается на росте и развитии детского организма, ухудшает качество жизни ребенка. Принимая во внимание актуальность данной проблемы, авторы пришли к выводу о необходимости представить для практикующих врачей-педиатров ключевые положения по дифференциальной диагностике и лечению анемий, обусловленных дефицитом железа, фолиевой кислоты и витамина В12 у детей.
Ключевые слова: анемия, витамин В12-дефицитная анемия, дети, железодефицитная анемия, фолиеводефицитная анемия.
Для цитирования: Заплатников А.Л., Османов И.М., Ефимов М.С., Дементьев А.А., Чабаидзе Ж.Л., Майкова И.Д., О.А. Кузнецова, А.С. Воробьева, Е.Р. Радченко, Гончарова Л.В., Гавеля Н.В. Диагностика и принципы лечения дефицитных анемий у детей (в таблицах и схемах) // РМЖ. Медицинское обозрение. 2019. №3. С. 2-5
Diagnosis and treatment principles of deficiency anemia in children (in tables and diagrams)
A.L. Zaplatnikov 1,2 , I.M. Osmanov 2 , M.S. Efimov 1 , A.A. Dementiev1, Zh.L. Chabaidze 1 , I.D. Maikova 2 , O.A. Kuznetsova 2 , A.S. Vorobieva 2 , E.R. Radchenko 2 , L.V. Goncharova 2 , N.V. Gavelia 2
1 Russian Medical Academy of Continuous Professional Education, Moscow
2 Z.A. Bashlyaeva Children’s City Clinical Hospital, Moscow
The article highlights the clinical, anamnestic and laboratory properties of iron-deficiency, folic acid-deficiency, and vitamin B12-deficiency anemia in children, based on the data of modern literature and in-house clinical observation analysis. The basic verification principles of the anemic syndrome causes associated with iron, folic acid and vitamin B12 deficiency in children are presented. The fundamental provisions underlying the differential diagnosis between iron-deficiency, folic acid-deficiency, and vitamin B12-deficiency anemia are also reviewed. In addition, the article describes the treatment principles in children with nutritional deficiency anemia. Anemia manifestation in a child determines the need for mandatory cause clarification of this pathological condition. At the same time, timely verification of the anemia etiology allows starting adequate therapy without delay, which determines its effectiveness and improves the child’s life quality as a whole. Late diagnosis and lack of adequate therapy, however, lead to the pathological processes progression. This has a negative impact on the child’s body growth and development and worsens his life quality in general. The authors came to the conclusion that it is necessary to present fundamental provisions for practicing pediatricians on anemia differential diagnosis and treatment associated with iron, folic acid and vitamin B12 deficiency in children, taking into account this problem urgency.
Keywords: anemia, vitamin B12-deficiency anemia, children, iron-deficiency anemia, folic acid- deficiency anemia.
For citation: Zaplatnikov A.L., Osmanov I.M., Efimov M.S. et al. Diagnosis and treatment principles of deficiency anemia in children (in tables and diagrams). RMJ. Medical Review. 2019;3:6–9.
В статье освещены клинико-анамнестические и лабораторные особенности железодефицитной, фолиеводефицитной и витамин В12-дефицитной анемий у детей. Представлены основные принципы дифференциальной диагностики и лечения указанных дефицитных анемий у детей.
Критерием анемии, независимо от этиологии, является снижение уровня гемоглобина (Hb) ниже возрастной нормы. Так, синдром анемии констатируют, если концентрация Hb в капиллярной крови ниже: 110 г/л — у детей в возрасте от 1 мес. до 5 лет, 115 г/л — у детей 6–12 лет, 120 г/л — у детей старше 12 лет и подростков. Кроме этого, зная уровень Hb, можно определить тяжесть анемического синдрома. Так, для детей, достигших месячного возраста и старше, снижение Нb до 90 г/л является признаком анемии легкой степени, уровень Нb в пределах 70–90 г/л характерен для анемии средней тяжести, а падение Нb ниже 70 г/л определяет тяжелую степень анемии [1–4].
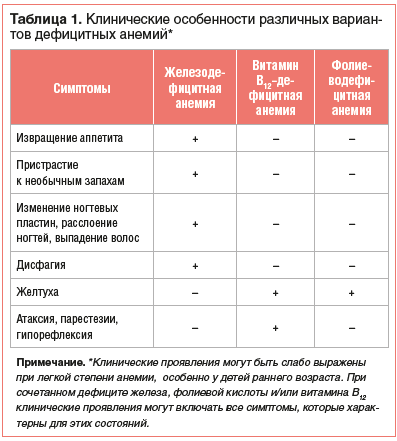
Нозологическая верификация характера анемии проводится на основе анализа клинико-анамнестических данных, результатов лабораторного и, если необходимо, инструментального обследования пациента. Общими клиническими проявлениями анемии, независимо от этиологии, являются повышенная утомляемость, снижение работоспособности, склонность к инфекциям. Среди дополнительных симптомов, которые могут отмечаться при ЖДА, — извращение аппетита и пристрастие к необычным запахам, изменение ногтевых пластин, расслоение ногтей, выпадение волос, атрофия сосочков языка, дисфагия. В свою очередь, при витамин В12-дефицитной анемии имеют место неврологические нарушения (атаксия, парестезии, гипорефлексия и другие проявления фуникулярного миелоза), «лакированный» язык и желтуха. Непрямая гипербилирубинемия может также отмечаться и при фолиеводефицитной анемии (табл. 1).
Наличие желтухи и анемии при этом нередко становится причиной ошибочного заключения о гемолитическом характере анемии, если врач не обращает внимания на отсутствие ретикулоцитоза. Следует отметить, что иктеричность при анемиях, обусловленных дефицитом витамина В12 или фолиевой кислоты, связана с неэффективным эритропоэзом и повышенным разрушением предшественников эритроцитов в костном мозге [1–3, 5–7].
Несмотря на описанные выше симптомы, типичные для конкретных ДА, их клинические проявления могут быть слабо выражены при легкой степени анемии, особенно у детей раннего возраста. В связи с этим этиологическая верификация генеза анемического синдрома проводится на основании не только клинических проявлений и анамнестических данных. Обязательным условием установления диагноза является корректная трактовка результатов лабораторного обследования. При этом минимально достаточным уровнем лабораторного обследования является проведение клинического и биохимического анализов крови.
Хорошо известно, что показаниями к исследованию клинического анализа крови для исключения анемии у детей являются анамнестические (недоношенность, задержка внутриутробного развития, исключительно грудное вскармливание ребенка, если мать имеет хронические заболевания кишечника или является вегетарианкой и др.) и/или клинические факторы риска (геморрагический синдром, синдром мальабсорбции, инфекционно-воспалительные заболевания, желтуха, лимфаденопатия, гепато- или спленомегалия и другие патологические состояния). При оценке результатов клинического анализа крови нельзя ограничиваться только поиском лабораторных признаков анемии. Обязательно должны быть проанализированы все параметры гемограммы (эритроциты и их индексы, ретикулоциты, тромбоциты и их индексы, общее количество лейкоцитов, лейкоцитарная формула, а также абсолютное количество нейтрофилов, лимфоцитов, моноцитов и эозинофилов, СОЭ). Это позволяет уже при первичном обращении пациента очертить круг основных причин выявленной анемии и наметить основные диагностические мероприятия для расшифровки генеза заболевания [1–4].
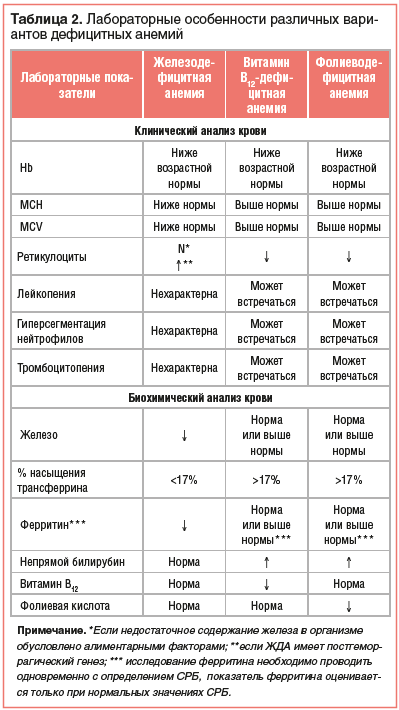
Так, для ЖДА типичными признаками являются: гипохромия и микроцитоз эритроцитов при нормальном уровне ретикулоцитов, если недостаточное содержание железа в организме обусловлено алиментарными факторами или синдромом мальабсорбции. В тех же случаях, когда ЖДА имеет постгеморрагический генез, гипохромия и микроцитоз эритроцитов будут сопровождаться ретикулоцитозом [1–4]. В свою очередь для анемий, обусловленных недостатком в организме как фолиевой кислоты, так и витамина В12, характерны гиперхромия и макроцитоз эритроцитов, а также ретикулоцитопения (табл. 2).
Кроме этого, при фолиево- и витамин В12-дефицитной анемиях могут встречаться лейко- и тромбоцитопения, гиперсегментация нейтрофилов. С учетом того, что в ряде случаев ДА имеет комбинированный генез, при котором дефицит железа сочетается с дефицитом фолиевой кислоты или витамина В12, типичные гематологические признаки могут не выявляться или быть разнонаправленными. Это определяет необходимость обязательного проведения биохимического анализа крови с определением, кроме общепринятых показателей, таких параметров, как железо, железосвязывающая способность, процент насыщения трансферрина, ферритин, фолиевая кислота и витамин В12 [6, 7]. Особо следует подчеркнуть, что ферритин должен определяться вместе с С-реактивным белком (СРБ). При этом оценивать уровень ферритина можно только в тех случаях, когда значения СРБ находятся в пределах нормативных. Это объясняется тем, что ферритин относится к протеинам воспаления и его уровень повышается при воспалительных процессах в организме. В связи с этим нормальный или высокий уровень ферритина при повышенных значениях СРБ может стать причиной ошибочного заключения об отсутствии железодефицитного состояния [2–4]. Особенности биохимического анализа крови при различных вариантах ДА представлены в таблице 2.
Только для зарегистрированных пользователей
источник
Анемия – состояние, при котором снижается общее количество гемоглобина в организме. Снижение концентрации гемоглобина в крови является ключевым показателем, поскольку может быть измерено напрямую.
В этиологии фолиеводефицитной анемии играют роль следующие факторы:
Недостаточное поступление с питанием (вскармливание козьим молоком);
Нарушение всасывания в кишечнике (энтерит);
Повышенная потребность (недоношеность; малый вес при рождении; гемолитическая анемия, гипертиреоз, инфекционно-воспалительные заболевания);
Использование медикаментов – антагонистов фолиевой кислоты (препараты для лечения эпилепсии, метотрексат);
Повышенное выведение (гемодиализ).
Изолированный дефицит фолиевой кислоты встречается редко, как правило, он сочетается с дефицитом железа, белка, других витаминов.
Фолиевая кислота содержится в зеленых листьях растений, фруктах, печени, почках. Запасы фолатов в организме взрослого человека составляют 5-10 мг, минимальная потребность — 50 мкг в день. Мегалобластная анемия может развиться через 4 месяца полного отсутствия поступления фолатов с пищей.
После попадания в организм фолиевая кислота превращается в активный метаболит тетрагидрофолиевую кислоту, которая играет важнейшую роль в метаболизме нуклеиновых кислот и протеинов. Дефицит фолиевой кислоты приводит к нарушению клеточного деления и накоплению токсичных метаболитов, таких как гомоцистеин [1,2].
Данных о распространенности дефицита фолиевой кислоты и фолиеводефицитной анемии у детей в России нет.
Фолиеводефицитная анемия (D52):
D52.0 — Фолиеводефицитная анемия, связанная с питанием
D52.1 — Фолиеводефицитная анемия медикаментозная
D52.8 — Другие фолиеводефицитные анемии
D52.9 — Фолиеводефицитная анемия неуточненная
Клиническая картина складывается из симптомов, характерных для анемии: слабости, головокружения, одышки сердцебиения при физической нагрузке, повышенной утомляемости, нарушения успеваемости в школе. Общие признаки, являющиеся следствием гипоксии тканей: бледность, тахикардия, одышка, плохой аппетит, вялость или повышенная возбудимость. Кроме того могут наблюдаться ангулярный стоматит, глоссит. Пациенты могут жаловаться на анорексию, тошноту, рвоту, боли в животе и диарею.
Фолиеводефицитная анемия крайне редко наблюдается в чистом виде. Как правило, дефицит фолиевой кислоты сочетается с дефицитом железа, так как эти состояния развиваются вследствие действия единых этиопатогенетических факторов. При этом и клинические проявления и лабораторные характеристики анемии зависят от соотношения выраженности дефицита железа и фолата. Учитывая, что при ЖДА и при фолиеводефицитной анемии наблюдаются разнонаправленные сдвиги в показателях обмена железа и эритроцитарных индексах, лабораторные тесты при смешанной форме анемии становятся малоинформативными. В данной ситуации решающее значение имеет анамнез и клиника анемии.
Дифференциальный диагноз проводят с витамин В12 дефицитной анемией, другими формами анемии с мегалобластоидным типом кроветворения: врожденной оротатацидурией, синдром Леша-Найена (Lesch-Nyhan), тиамин-зависимой мегалобластной анемией, врожденной дизэритропоэтической анемией, эритролейкемией. Кроме того, необходимо исключить формы анемии, протекающие с макроцитозом, но без признаков мегалобластоидности – апластическую анемию, аутоиммунную гемолитическую анемию, заболевания печени, гипотиреоз, сидеробластные анемии.
Необходимо оценить размеры лимфатических узлов, печени, селезенки, исключить наличие образований в брюшной полости, забрюшинном пространстве, другие признаки злокачественных заболеваний. [1,2]
Необходимо отметить, что при сочетанном дефиците назначение фолиевой кислоты без препаратов железа приведет к неполному восстановлению гемоглобина и к проявлению клинических и лабораторных признаков дефицита железа. И наоборот, если начать лечение с препаратов железа, проявятся признаки дефицита фолиевой кислоты.
Общий осмотр подразумевает оценку общего физического состояния, роста и массы тела. Выявляется бледность кожных покровов, слизистых, при тяжелой анемии присутствует учащенное сердцебиение, одышка.
Поскольку при фолиеводефицитной анемии в костном мозге происходит неэффективный эритропоэз и за счет этого повышенное разрушение гемоглобинсодержащих клеток, в крови повышается уровень непрямого билирубина и появляется легкая желтушнось склер и кожи. При тяжелых формах может наблюдаться небольшое увеличение селезенки (реактивная гиперплазия). Таким образом, имеется некоторое сходство симптоматики фолиеводефицитной анемии и гемолитической анемии. Лабораторное обследование позволяет провести надежную дифференциальную диагностику этих форм анемии.
По лабораторным признакам фолиеводефицитная анемия почти совпадает с В12-дефицитной анемией. Различия заключаются в разном уровне витамина В12 и фолиевой кислоты в крови. Кроме того, для фолиеводефицитной анемии в отличие от В12-дефицитной анемии, не характерны признаки поражения нервной системы. Следует помнить, что изолированный дефицит витамина В12 в детском возрасте встречается редко и является обычно осложнением глистной инвазии широким лентецом или наследственных нарушений обмена, а также результатом воздействия некоторых медикаментов [1,2, 3].
- Рекомендовано проведение общего клинического анализа крови и биохимического анализа крови.
Уровень убедительности рекомендаций А (уровень достоверности доказательств 1)
Комментарии:
Для фолиеводефицитной анемии характерны:
низкий уровень ретикулоцитов;
высокий уровень сывороточного железа;
высокий уровень ферритина;
умеренное повышение непрямого билирубина;
низкий уровень фолата в сыворотке крови (норма более 3 нг/мл);
низкий уровень фолата в эритроцитах;
нормальный уровень витамина В12 в крови;
картина мегалобластического кроветворения в костном мозге.
При сочетании дефицита железа и фолиевой кислоты могут наблюдаться сочетания лабораторных признаков, что приводит к неопределенной картине и затруднению диагностики; в этом случае надо ориентироваться на клинические симптомы и анамнез.
Высокий ретикулоцитоз может являться признаком продолжающегося кровотечения, гемолиза, а также наблюдается при фолиеводефицитной анемии через неделю после назначения фолиевой кислоты.
Наряду с анемией, как правило, отмечается умеренное снижение уровня тромбоцитов и лейкоцитов.
Необходимо исследование мочи для исключения протеинурии, характерной для синдрома Иммерслунд-Грэссбек [4]. Для исключения врожденного отсутствия внутреннего фактора проводится тест Шиллинга с радиоактивным меченным витамином В12. Учитывая недоступность меченного витамина В12 в общей лабораторной практике можно использовать модифицированный тест Шиллинга: после приема внутрь витамина В12 определяется уровень витамина в крови. При отсутствии повышения уровня витамина В12 диагностируется нарушение всасывания витамина в кишечнике.
При наличии двух- или трехростковой цитопении необходимо рассмотреть необходимость исследования костного мозга для исключения лейкемии, миелодиспластического синдрома, апластической анемии.
Характерные признаки мегалобластического кроветворения в костном мозге исчезают через несколько часов после приема фолиевой кислоты.
Уровень убедительности рекомендаций А (уровень достоверности доказательств 1)
Комментарии: Детям первого года жизни фолиевая кислота назначается в дозе 0,25-0,5 мг/кг в сутки в течение месяца. В более старшем возрасте суточная доза составляет 1 мг/сутки. Пероральный прием эффективен даже в случае мальабсорбции, однако в этом случае дозу следует увеличить до 5-15 мг/сутки.
- Рекомендовано в процессе лечения проводить контроль показателей крови:
Общий анализ крови с подсчетом ретикулоцитов, тромбоцитов, гематокрита — на 7 — 10 день от начала лечения. Наличие ретикулоцитарной реакции является важным признаком правильности лечения.
Контроль показателей крови 1 раз в неделю. Нормализация уровня Hb происходит через 4 — 6 недель от начала лечения и является решающим подтверждением правильности диагноза и лечения [1,2,5].
Уровень убедительности рекомендаций С (уровень достоверности доказательств 2с)
Специфических реабилитационных мероприятий в отношении пациентов с фолиеводефицитной анемией нет. Диспансерное наблюдение проводится с учетом устранения причин дефицита фолиевой кислоты (основного заболевания, неправильного питания).
Правильное вскармливание грудных детей, назначение фолиевой кислоты недоношенным детям. Рациональное питание детей старшего возраста. Необходимо учитывать возможность развития дефицита фолиевой кислоты при различных заболеваниях. Фолиевая кислота в дозе 0,25 — 1 мг/сутки назначается недоношенным детям, детям с низкой массой тела при рождении, детям, страдающим хроническими воспалительными заболеваниями, заболеваниями кишечника с синдромом мальабсорбции.
Критерии качества
Уровень достоверности доказательств
Уровень убедительности рекомендаций
Выполнен общий клинический анализ крови с подсчетом ретикулоцитов и тромбоцитов
источник
Анемия клинические рекомендации педиатрия. Федеральные клинические рекомендации по диагностике и лечению железодефицитной анемии у детей
Catad_tema Железодефицитная анемия — статьи
Год утверждения (частота пересмотра): 2016 (пересмотр каждые 5 лет)
Научным советом Министерства Здравоохранения Российской Федерации__ __________201_ г.
Анемия – состояние, при котором снижается общее количество гемоглобина в организме. Снижение концентрации гемоглобина в крови является ключевым показателем, поскольку может быть измерено напрямую.
В этиологии фолиеводефицитной анемии играют роль следующие факторы:
Недостаточное поступление с питанием (вскармливание козьим молоком);
Нарушение всасывания в кишечнике (энтерит);
Повышенная потребность (недоношеность; малый вес при рождении; гемолитическая анемия, гипертиреоз, инфекционно-воспалительные заболевания);
Использование медикаментов – антагонистов фолиевой кислоты (препараты для лечения эпилепсии, метотрексат);
Повышенное выведение (гемодиализ).
Изолированный дефицит фолиевой кислоты встречается редко, как правило, он сочетается с дефицитом железа, белка, других витаминов.
Фолиевая кислота содержится в зеленых листьях растений, фруктах, печени, почках. Запасы фолатов в организме взрослого человека составляют 5-10 мг, минимальная потребность — 50 мкг в день. Мегалобластная анемия может развиться через 4 месяца полного отсутствия поступления фолатов с пищей.
После попадания в организм фолиевая кислота превращается в активный метаболит тетрагидрофолиевую кислоту, которая играет важнейшую роль в метаболизме нуклеиновых кислот и протеинов. Дефицит фолиевой кислоты приводит к нарушению клеточного деления и накоплению токсичных метаболитов, таких как гомоцистеин .
Данных о распространенности дефицита фолиевой кислоты и фолиеводефицитной анемии у детей в России нет.
Фолиеводефицитная анемия (D52):
D52.0 — Фолиеводефицитная анемия, связанная с питанием
D52.1 — Фолиеводефицитная анемия медикаментозная
D52.8 — Другие фолиеводефицитные анемии
D52.9 — Фолиеводефицитная анемия неуточненная
Клиническая картина складывается из симптомов, характерных для анемии: слабости, головокружения, одышки сердцебиения при физической нагрузке, повышенной утомляемости, нарушения успеваемости в школе. Общие признаки, являющиеся следствием гипоксии тканей: бледность, тахикардия, одышка, плохой аппетит, вялость или повышенная возбудимость. Кроме того могут наблюдаться ангулярный стоматит, глоссит. Пациенты могут жаловаться на анорексию, тошноту, рвоту, боли в животе и диарею.
Фолиеводефицитная анемия крайне редко наблюдается в чистом виде. Как правило, дефицит фолиевой кислоты сочетается с дефицитом железа, так как эти состояния развиваются вследствие действия единых этиопатогенетических факторов. При этом и клинические проявления и лабораторные характеристики анемии зависят от соотношения выраженности дефицита железа и фолата. Учитывая, что при ЖДА и при фолиеводефицитной анемии наблюдаются разнонаправленные сдвиги в показателях обмена железа и эритроцитарных индексах, лабораторные тесты при смешанной форме анемии становятся малоинформативными. В данной ситуации решающее значение имеет анамнез и клиника анемии.
Дифференциальный диагноз проводят с витамин В12 дефицитной анемией, другими формами анемии с мегалобластоидным типом кроветворения: врожденной оротатацидурией, синдром Леша-Найена (Lesch-Nyhan), тиамин-зависимой мегалобластной анемией, врожденной дизэритропоэтической анемией, эритролейкемией. Кроме того, необходимо исключить формы анемии, протекающие с макроцитозом, но без признаков мегалобластоидности – апластическую анемию, аутоиммунную гемолитическую анемию, заболевания печени, гипотиреоз, сидеробластные анемии.
Необходимо оценить размеры лимфатических узлов, печени, селезенки, исключить наличие образований в брюшной полости, забрюшинном пространстве, другие признаки злокачественных заболеваний.
Необходимо отметить, что при сочетанном дефиците назначение фолиевой кислоты без препаратов железа приведет к неполному восстановлению гемоглобина и к проявлению клинических и лабораторных признаков дефицита железа. И наоборот, если начать лечение с препаратов железа, проявятся признаки дефицита фолиевой кислоты.
Общий осмотр подразумевает оценку общего физического состояния, роста и массы тела. Выявляется бледность кожных покровов, слизистых, при тяжелой анемии присутствует учащенное сердцебиение, одышка.
Поскольку при фолиеводефицитной анемии в костном мозге происходит неэффективный эритропоэз и за счет этого повышенное разрушение гемоглобинсодержащих клеток, в крови повышается уровень непрямого билирубина и появляется легкая желтушнось склер и кожи. При тяжелых формах может наблюдаться небольшое увеличение селезенки (реактивная гиперплазия). Таким образом, имеется некоторое сходство симптоматики фолиеводефицитной анемии и гемолитической анемии. Лабораторное обследование позволяет провести надежную дифференциальную диагностику этих форм анемии.
По лабораторным признакам фолиеводефицитная анемия почти совпадает с В12-дефицитной анемией. Различия заключаются в разном уровне витамина В12 и фолиевой кислоты в крови. Кроме того, для фолиеводефицитной анемии в отличие от В12-дефицитной анемии, не характерны признаки поражения нервной системы. Следует помнить, что изолированный дефицит витамина В12 в детском возрасте встречается редко и является обычно осложнением глистной инвазии широким лентецом или наследственных нарушений обмена, а также результатом воздействия некоторых медикаментов .
- Рекомендовано проведение общего клинического анализа крови и биохимического анализа крови.
Для фолиеводефицитной анемии характерны:
низкий уровень ретикулоцитов;
высокий уровень сывороточного железа;
высокий уровень ферритина;
умеренное повышение непрямого билирубина;
низкий уровень фолата в сыворотке крови (норма более 3 нг/мл);
низкий уровень фолата в эритроцитах;
нормальный уровень витамина В12 в крови;
картина мегалобластического кроветворения в костном мозге.
При сочетании дефицита железа и фолиевой кислоты могут наблюдаться сочетания лабораторных признаков, что приводит к неопределенной картине и затруднению диагностики; в этом случае надо ориентироваться на клинические симптомы и анамнез.
Высокий ретикулоцитоз может являться признаком продолжающегося кровотечения, гемолиза, а также наблюдается при фолиеводефицитной анемии через неделю после назначения фолиевой кислоты.
Наряду с анемией, как правило, отмечается умеренное снижение уровня тромбоцитов и лейкоцитов.
Необходимо исследование мочи для исключения протеинурии, характерной для синдрома Иммерслунд-Грэссбек . Для исключения врожденного отсутствия внутреннего фактора проводится тест Шиллинга с радиоактивным меченным витамином В12. Учитывая недоступность меченного витамина В12 в общей лабораторной практике можно использовать модифицированный тест Шиллинга: после приема внутрь витамина В12 определяется уровень витамина в крови. При отсутствии повышения уровня витамина В12 диагностируется нарушение всасывания витамина в кишечнике.
При наличии двух- или трехростковой цитопении необходимо рассмотреть необходимость исследования костного мозга для исключения лейкемии, миелодиспластического синдрома, апластической анемии.
Характерные признаки мегалобластического кроветворения в костном мозге исчезают через несколько часов после приема фолиевой кислоты.
Комментарии: Детям первого года жизни фолиевая кислота назначается в дозе 0,25-0,5 мг/кг в сутки в течение месяца. В более старшем возрасте суточная доза составляет 1 мг/сутки. Пероральный прием эффективен даже в случае мальабсорбции, однако в этом случае дозу следует увеличить до 5-15 мг/сутки.
- Рекомендовано в процессе лечения проводить контроль показателей крови:
Общий анализ крови с подсчетом ретикулоцитов, тромбоцитов, гематокрита — на 7 — 10 день от начала лечения. Наличие ретикулоцитарной реакции является важным признаком правильности лечения.
Контроль показателей крови 1 раз в неделю. Нормализация уровня Hb происходит через 4 — 6 недель от начала лечения и является решающим подтверждением правильности диагноза и лечения .
Специфических реабилитационных мероприятий в отношении пациентов с фолиеводефицитной анемией нет. Диспансерное наблюдение проводится с учетом устранения причин дефицита фолиевой кислоты (основного заболевания, неправильного питания).
Правильное вскармливание грудных детей, назначение фолиевой кислоты недоношенным детям. Рациональное питание детей старшего возраста. Необходимо учитывать возможность развития дефицита фолиевой кислоты при различных заболеваниях. Фолиевая кислота в дозе 0,25 — 1 мг/сутки назначается недоношенным детям, детям с низкой массой тела при рождении, детям, страдающим хроническими воспалительными заболеваниями, заболеваниями кишечника с синдромом мальабсорбции.
Детская гематология/ Под ред: А.Г. Румянцева, А.А. Масчана, Е.В. Жуковской. Москва. Издательская группа « ГЭОТАР Медиа» 2015 г. С. 656
Whitehead VM. Acquired and inherited disorders of cobalamin and folate in children. Br J Haematol . 2006 Jul. 134(2):125-36.
Duma A, Cartmill C, Blood J, Sharma A, Kharasch ED, Nagele P. The hematological effects of nitrous oxide anesthesia in pediatric patients. Anesth Analg . 2015 Jun. 120 (6):1325-30.
Dugu? B, Ismail E, Sequeira F, Thakkar J, Gr?sbeck R. Urinary excretion of intrinsic factor and the receptor for its cobalamin complex in Gr?sbeck-Imerslund patients: the disease may have subsets. J Pediatr Gastroenterol Nutr . 1999 Aug. 29(2):227-30
Trakadis YJ, Alfares A, Bodamer OA, et al. Update on transcobalamin deficiency: clinical presentation, treatment and outcome. J Inherit Metab Dis . 2014 May. 37 (3):461-73
Румянцев А.Г. доктор медицинских наук, профессор, главный детский гематолог Министерства здравоохранения Российской Федерации , директор Федерального научно-клинического центра детской гематологии, онкологии и иммунологии им. Дмитрия Рогачёва , член правления Союза педиатров России, академик РАН.
Масчан А.А. д.м.н., зам. генерального директора ФГБУ ФНКЦ ДГОИ им. Дмитрия Рогачева, профессор кафедры гематологии, онкологии и лучевой терапии педиатрического факультета РНИМУ им. Н.И.Пирогова, президент Национального общества детских гематологов и онкологов, член Европейского общества гематологов.
Демихов Валерий Григорьевич — д.м.н., профессор, директор Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО, член Европейской гематологической ассоциации (EHA).
Скобин В.Б., к.м.н., врач-гематолог Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО.
Журина О.Н ., к.м.н., зав. лабораторией Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО.
Конфликт интересов отсутствует.
Таблица П1 – Уровни достоверности доказательств
Проспективные рандомизированные контролируемые исследования
Достаточное количество исследований с достаточной мощностью, с участием большого количества пациентов и получением большого количества данных
Как минимум одно хорошо организованное рандомизированное контролируемое исследование
Репрезентативная выборка пациентов
Проспективные с рандомизацией или без исследования с ограниченным количеством данных
Несколько исследований с небольшим количеством пациентов
Хорошо организованное проспективное исследование когорты
Мета-анализы ограничены, но проведены на хорошем уровне
Результаты не презентативны в отношении целевой популяции
Хорошо организованные исследования «случай-контроль»
Нерандомизированные контролируемые исследования
Исследования с недостаточным контролем
Рандомизированные клинические исследования с как минимум 1 значительной или как минимум 3 незначительными методологическими ошибками
Ретроспективные или наблюдательные исследования
Серия клинических наблюдений
Противоречивые данные, не позволяющие сформировать окончательную рекомендацию
Мнение эксперта/данные из отчета экспертной комиссии, экспериментально подтвержденные и теоретически обоснованные
Таблица П2 – Уровни убедительности рекомендаций
Метод/терапия первой линии; либо в сочетании со стандартной методикой/терапией
Метод/терапия второй линии; либо при отказе, противопоказании, или неэффективности стандартной методики/терапии. Рекомендуется мониторирование побочных явлений
нет убедительных данных ни о пользе, ни о риске)
Нет возражений против данного метода/терапии или нет возражений против продолжения данного метода/терапии
Отсутствие убедительных публикаций I, II или III уровня доказательности, показывающих значительное превосходство пользы над риском, либо убедительные публикации I, II или III уровня доказательности, показывающие значительное превосходство риска над пользой
Нехватка фолиевой кислоты может наблюдаться у недоношенных детей, детей, родившихся с низким весом, а также при хронических воспалительных заболеваниях, особенно заболеваниях кишечника, сопровождающихся нарушением всасывания питательных веществ. Дефицит фолиевой кислоты приводит к нарушению образования эритроцитов и снижению уровня гемоглобина в крови. Для профилактики дефицита фолиевой кислоты и развития анемии необходимо обеспечить ребенку правильное вскармливание на первом году жизни. Оптимальным для ребенка является грудное вскармливание. При отсутствии грудного молока следует использовать смеси для детского питания, которые содержат все необходимые ребенку витамины в том числе фолиевую кислоту. Вскармливание козьим и коровьим молоком является одной из причин анемии. Детям из группы риска (недоношенные, родившиеся с малым весом, страдающие хроническими воспалительными заболеваниями, синдромом нарушения всасывания питательных веществ в кишечнике) следует давать фолиевую кислоту в медикаментозной форме. Самостоятельное использование препарата недопустимо. Назначить фолиевую кислоты с учетом всех показаний и противопоказаний должен ваш врач.
Для цитирования: Дворецкий Л.И. Клинические рекомендации по лечению больных железодефицитной анемией // РМЖ. 2004. №14. С. 893
Железодефицитная анемия (ЖДА) представляет собой клинико-гематологический синдром, возникающий при развитии дефицита железа вследствие различных патологических (физиологических) процессов и характеризующийся снижением уровня гемоглобина (в меньшей степени эритроцитов) наряду с клиническими признаками анемии и сидеропении.
Клинические рекомендации ведения больных ЖДА включают: — выявление причины ЖДА и при необходимости — ее коррекция; — обучение больных ЖДА; — принятие решения о назначении лекарственных препаратов железа (ПЖ); — выбор лекарственного ПЖ; — путь введения ПЖ (внутрь или парентерально); — длительность лечения и необходимость поддерживающей терапии; — контроль переносимости ПЖ и коррекция при плохой переносимости; — оценку эффективности и выявление причин отсутствия или недостаточного эффекта; — коррекцию выявленных причин неэффективности.
Выявление причины ЖДА и возможности ее коррекции
После верификации железодефицитного характера анемии, т.е. синдрома ЖДА, необходимо выявление причины, лежащей в основе данного варианта анемического синдрома (нозологическая диагностика). Для клинициста этот этап является не менее важным и вместе с тем наиболее трудным и ответственным, поскольку в основе имеющейся ЖДА могут лежать потенциально курабельные заболевания. Наличие в МКБ-10 рубрики «Железодефицитная анемия неуточненная» оставляет для врача «лазейку» в случаях отсутствия явной причины анемии, «освобождая» его от тщательности и углубления диагностического поиска на этапе нозологической диагностики. Следует особо подчеркнуть роль врача-интерниста на этапах синдромной и нозологической диагностики, поскольку подавляющее большинство больных ЖДА (независимо от конкретной причины) обращаются прежде всего, как и многие другие пациенты, к терапевту, а не к гематологу или другому специалисту. При выявлении причины ЖДА лечение должно быть направлено на устранение этой причины (по возможности) или коррекцию имеющихся нарушений — лечение эрозивно-язвенных процессов в желудке, оперативные лечения при опухолях ЖКТ, миоме матки, лечение энтеритов, коррекция алиментарной недостаточностии т.д.
Существенным компонентом ведения больных ЖДА является повышение их образовательного уровня в отношении данной патологии, создание мотивации к лечению, вовлечение пациентов в контроль за своим состоянием и лабораторными показателями. Необходимо разъяснение сущности ЖДА, причин ее возникновения, реальных возможностей коррекции дефицита железа и нормализации уровня гемоглобина. Особое значение имеют обучающие программы у беременных женщин с наличием ЖДА и пациенток, страдающих меноррагиями. У беременных должна создаваться мотивация необходимости коррекции дефицита железа с целью предотвращения недостатка железа у плода. Больные должны быть осведомлены о возможных побочных эффектах при лечении лекарственными препаратами железа, необходимости соблюдения врачебных назначений, в том числе и регулярности приема ПЖ. Следует обязательно указать на недопустимость попыток коррекции дефицита железа с помощью различных пищевых продуктов, а также на строгие показания к назначению инъекционных форм ПЖ.
Принятие решения о назначении лекарственных препаратов железа
Всем больным ЖДА показана патогенетическая терапия препаратами железа. Следует подчеркнуть ошибочность мнения о возможности коррекции дефицита железа с помощью пищевых продуктов с высоким содержанием железа, что является одним из мифов в представлениях о ведении больных ЖДА. Об этом должны быть осведомлены больные, что следует считать важным образовательным компонентом ведения данной категории пациентов. Разумеется, пища должна быть богата продуктами, содержащими железо. Однако следует иметь в виду неодинаковую степень всасываемости железа из различных продуктов. Так например, железо, содержащееся в мясе в виде гема, всасывается на 40-50%, в то время как из растительных продуктов, овощей, фруктов всасывается всего 3-5% содержащегося в них железа. Поэтому средством выбора для коррекции дефицита железа и уровня гемоглобина у больных ЖДА являются лекарственные препараты железа. На фармацевтическом рынке России в настоящее время имеется большой арсенал ПЖ в различных лекарственных формах, с неодинаковым содержанием в них железа, наличием дополнительных компонентов, влияющих на биодоступность железа, различной стоимостью (рис. 1). Из ПСЖ железо всасывается в двухвалентной форме, в последующем превращается в трехвалетное, которое связывается с трансферрином и используется для построения молекулы гемоглобина. В ПЖК железо находится в трехвалентной форме и всасывается как бы в готовом виде. В ПЖК, в частности, в гидрооксиполимальтозном комплексе, связано как в физиологическом состоянии в молекуле ферритина. Существуют различия в механизмах всасывания железа из ПСЖ и ПЖК. Всасывание железа из ПСЖ происходит главным образом в виде пассивной диффузии согласно градиенту концентрации и в меньшей степени активно, в то время как абсорбция железа из ПЖК является активным процессом в виде конкурентного обмена. Это ведет к различному уровню железа в сыворотке, объему распределения, константам элиминации после абсорбции. Всасывание железа из ПЖК и нарастание его концентрации в сыворотке происходит медленно, но оно быстро поступает в запасы. При применении ПСЖ могут возникать нарушения окислительных процессов (оксидативные повреждения) вследствие превращения ионов двухвалентного железа в трехвалентное, которое соединяется с трансферрином и включается в молекулу гемоглобина. При окислении образуются свободные радикалы, которые вызывают клеточные повреждения, такие как перекисное окисление липидов, нарушение структуры мембранных и клеточных белков, повреждение клеточной ДНК и РНК. ПЖК в отличие от ПСЖ не вызывают «оксидативного стресса», поскольку ионы железа не меняют свою валентность в процессе всасывания (табл. 1). Для лучшей абсорбции ПСЖ рекомендуется принимать за час до еды т.е. на пустой желудок, что может вызывать нарушения со стороны желудка, кишечника и другие побочные эффекты. Современные технологии производства препаратов железа позволяют производить ПСЖ с замедленным высвобождением железа в тонком кишечнике, что уменьшает токсическое воздействие ионов железа на слизистую желудка. Частота побочных эффектов при лечении ПЖК меньше по сравнении с ПСЖ, что обеспечивает лучший комплайенс больных ЖДА. ПСЖ взаимодействуют с некоторыми пищевыми продуктами (танин, фитаты, соли кальция) и медикаментами (пленкообразующие препараты, тетрациклины, препараты кальция), снижающими биодоступность железа. В связи с этим ПСЖ не следует принимать одновременно с указанными пищевыми продуктами и лекарственными препаратами. В то же время пища и медикаменты не оказывают влияния на всасывание железа из ПЖК. Темпы прироста показателей гемоглобина при применении ПСЖ и ПЖК примерно одинаковые.
Путь введения препаратов железа
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний ПЖ следует назначать внутрь. Путь введения ПЖ у больных ЖДА определяется конкретной клинической ситуацией, в частности, состоянием кишечного всасывания и переносимостью пероральных ПЖ.
Основными показаниями для парентерального введения ПЖ являются: — патологии кишечника с нарушением всасывания (различные энтериты, синдром недостаточности всасывания); — резекция тонкой кишки; — резекция желудка по Бильрот II с формированием «слепой петли»; — эрозивно-язвенные процессы в желудке (обострение язвенной болезни и др.); — непереносимость ПЖ для приема внутрь. Многие врачи обосновывают назначение парентеральных ПЖ выраженностью анемического синдрома в расчете на якобы больший их эффект, что также не имеет достаточных оснований и не подтверждается клинической практикой. Темпы прироста уровня гемоглобина при назначении ПЖ внутрь и парентерально оказались приблизительно одинаковыми, в связи с чем предпочтение ПЖ в инъекционных формах при необходимости более быстрой нормализации содержания гемоглобина (например, при подготовке к оперативному вмешательству) следует считать неоправданным. ПЖ для парентерального введения могут назначаться при плохой переносимости пероральных ПЖ, однако большинство современных ПСЖ и ПЖК переносятся сравнительно удовлетворительно. В связи с этим принятие решения о назначении парентерального ПЖ должно осуществляться только после ряда «врачебных маневров» (снижение дозы ПЖ, прием вместе с пищей, смена ПЖ для приема внутрь и т.д.).
Выбор лекарственного препарата железа
Выбор ПЖ и оптимального режима его дозирования должен определяться количеством и биодоступностью содержащегося в нем железа, переносимостью, стоимостью. При этом необходимо иметь в виду, что адекватный прирост показателей гемоглобина у больных ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг элементарного железа . Учитывая, что при развитии ЖДА всасывание железа увеличивается по сравнению с нормой и составляет 25-30% (при нормальных запасах железа — всего 3-7%), необходимо назначать от 100 до 300 мг элементарного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. С учетом этого при выборе ПЖ следует ориентироваться не на содержание в нем общего количества соединения железа, а на количество элементарного железа. Например, при назначении препаратов сульфата железа с низким содержанием элементарного железа (менее 100 мг) количество принимаемых таблеток должно быть от 3 и выше (в зависимости от содержания железа в каждой таблетке), в то время как препараты сульфата, фумарата или гидроксиполимальтозного комплекса железа с содержанием 100 мг элементарного железа можно принимать в количестве 1-2 таблеток в сутки. Основные ПСЖ представлены сульфатом железа, глюконатом, хлоридом, фумаратом, глицин сульфатом. Наибольшей степенью абсорбции обладают препараты сульфата железа, а наименьшей — глицин сульфата. Многие из ПСЖ содержат вещества, например, аскорбиновую кислоту, усиливающие всасывание железа и улучшающие биодоступность препарата, а также витамины (фолиевую кислоту, цианкобаламин). Среди ПЖК на отечественно рынке имеются гидроксиполимальтозный комплекс, железо-сорбитоловый комплекс, протеин сукцинилат железа, железо-сахарозный комплекс. К новым высокоэффективным и безопасным препаратам железа относятся препараты, представляющие собой неионные соединения железа на основе гидроксиполимальтозного комплекса (ГПК) трехвалентного железа. Структура комплекса состоит из многоядерных центров гидроксида Fe (III), окруженных нековалентно связанными молекулами полимальтозы. Комплекс имеет большой молекулярный вес, что затрудняет его диффузию через мембрану слизистой кишечника. Химическая структура комплекса максимально приближена к структуре естественных соединений железа с ферритином. Абсорбция железа в виде ГПК имеет принципиально иную схему по сравнению с его ионными соединениями и обеспечивается поступлением Fe (III) из кишечника в кровь путем активного всасывания. Неионная структура комплекса обеспечивает его стабильность и перенос железа с помощью транспортного белка, что предотвращает в организме свободную диффузию ионов железа, т.е. прооксидантные реакции. Данные по безопасности, полученные во время клинических исследований препарата железа на основе гидроксида Fe (III) с полимальтозой, свидетельствуют о более низкой частоте побочных эффектов по сравнению с солевыми препаратами железа. Для лучшей переносимости ПСЖ следует принимать во время еды, хотя следует иметь в виду, что всасывание железа лучше при приеме лекарственных препаратов перед едой. Всасываниежелеза может уменьшаться под влиянием содержащихся в некоторых пищевых продуктах веществ — фитинов (рис, соя), фосфатов (рыба, морепродукты), танина (чай, кофе). Многие больные склонны запивать лекарства чаем, что в случаях приема ПЖ в виде солей недопустимо, поскольку образуются плохо растворимые комплексы с низкой их абсорбцией в кишечнике. Кроме того, всасывание железа из ПЖ в виде солей ухудшается при одновременном приеме ряда медикаментов (тетрациклины, антациды, соли магния). С учетом этого следует рекомендовать прием препаратов солей железа в различное время с другими вышеуказанными медикаментами. Препараты ПЖК, в частности, гидроксиполимальтозный комплекс лишены подобных недостатков, поскольку пищевые продукты и медикаменты не оказывают влияние на всасываемость железа (в виде трехвалентной формы) из железосодержащих комплексов. В таблице 2 представлены основные зарегистрированные в России лекарственные ПСЖ и ПЖК для приема внутрь.
Оценка эффективности лечения
В случаях назначения ПЖ в достаточной дозе на 7-10-й день от начала лечения наблюдается повышение количества ретикулоцитов. Достоверное повышение уровня гемоглобина отмечается через 3-4 нед. от начала лечения. Нормализация показателей гемоглобина обычно происходит в сроки 4-9 нед. Иногда наблюдается резкое скачкообразное повышение гемоглобина. Эти индивидуальные колебания могут быть обусловлены, с одной стороны, выраженностью ЖДА, степенью истощения запасов железа, а с другой — эффективностью назначенного ПЖ (количество содержащегося железа, биодоступность и др.). Имеет также значение некомплаентность больных (нерегулярность приема ПЖ, побочные эффекты).
Длительность лечения и поддерживающая терапия
Оптимальная тактика ведения больных ЖДА предполагает насыщающую и поддерживающую терапию ПЖ. Длительность насыщающей терапии зависит от темпов прироста и сроков нормализации показателей гемоглобина, составляя в среднем 4-6 недель. Поддерживающая терапия показана в тех ситуациях, когда причина дефицита железа сохраняется (меноррагии, беременность) или в силу различных ситуаций является трудноустранимой (патология кишечника, носовые и другие кровотечения при геморрагических диатезах). Женщинам, страдающим ЖДА на фоне меноррагий, после нормализации показателей гемоглобина рекомендуется поддерживающая терапия ПЖ в течение 5-7 дней после очередной менструации. Больным надо разъяснять необходимость поддерживающего лечения в связи с продолжающимися избыточными потерями железа. Беременные с ЖДА должны получать ПЖ до конца беременности в целях обеспечения адекватной потребности плода в железе.
Переносимость препаратов железа
Среди побочных эффектов на фоне применения ПЖ внутрь наиболее часто возникают тошнота, анорексия, металлический вкус во рту, запоры, реже — поносы. Развитие запоров обусловлено, по всей вероятности, связыванием в кишечнике сероводорода, являющегося одним из стимулов кишечной перистальтики. В большинстве случаев современные ПЖ вызывают незначительные побочные явления, не требующие их отмены и перехода на парентеральный путь введения. Диспептические расстройства могут уменьшаться при приеме препаратов после еды или уменьшения суточной дозы препарата. Чаще побочные эффекты регистрируютсяпри приеме ПСЖ, в то время как препараты ПЖК (гидроксиполимальтозный комплекс) переносятся лучше и имеют в связи с этим определенные преимущества. В случаях сохраняющейся плохой переносимости пероральных ПЖ показано назначение ПЖ парентерально (внутримышечно или внутривенно). На фоне лечения парентеральными ПЖ, особенно для внутривенного введения, могут возникать аллергические реакции в виде крапивницы, лихорадка, флебиты, анафилактический шок. Кроме того, при внутримышечном введении ПЖ возможно потемнение кожи в местах инъекций, инфильтраты, абсцессы. Если ПЖ для парентерального введения назначают больным гипохромной анемией, не связанной с дефицитом железа, имеется повышенный риск возникновения тяжелых нарушений из-за «перегрузки» железом различных органов и тканей (печень, поджелудочная железа и др.) с развитием гемосидероза.
Причины неэффективности лечения препаратами железа
В случае отсутствия или недостаточного эффекта от лечения ПЖ следует выяснить причину с целью возможности ее коррекции. Возможные причины неэффективности лечения ПЖ и способы их коррекции представлены в таблице 3. Необходима убежденность в правильной трактовке всех клинико-лабораторных признаков и в достоверности синдрома ЖДА. Причиной отсутствия или недостаточной эффективности ПЖ может быть недостаточная суточная доза железа, что обычно связано с назначением ПЖ с низким содержанием в нем железа и малым количеством принимаемых таблеток. Так, например, при лечении препаратом, в котором содержится всего лишь 10 мг двухвалентного железа, число принимаемых таблеток должно быть не менее 10 в сутки. Такой режим дозирования неудобен для больных, чем и объясняется, вероятнее всего, невыполнение ими врачебного назначения. С учетом вышесказанного для обеспечения комплаентности следует назначать ПЖ с высоким содержанием железа (не менее 100 мг). Препараты с низким содержанием железа целесообразно использовать в педиатрической практике. Одной из причин неэффективности ПЖ при назначении внутрь может быть нарушение всасывания железа, в частности, у больных с невыявленной или недооцененной кишечной патологией. В этих случаях показано назначение парентеральных ПЖ. В ряде случаев вследствие улучшения самочувствия больные начинают нерегулярно принимать ПЖ или вообще прекращают лечение. В результате показатели гемоглобина не достигают нормальных значений и ЖДА при этом остается фактически недолеченной. С учетом этого длительность насыщающей терапии ПЖ должна определяться сроками достижения нормального уровня гемоглобина, что требует постоянного лабораторного мониторинга. Ряд больных не всегда выполняют назначение врача (регулярность приема ПЖ, достаточная продолжительность и т.д.). В некоторых случаях это может быть обусловлено развитиемпобочных эффектов от ПЖ и самостоятельным прекращением лечения. Поэтому необходим контроль за лечением, эффективностью, переносимостью ПЖ со стороны врача, среднего медперсонала, родственников больных. Отсутствие эффекта от ПЖ может быть связано с неустраненными причинами ЖДА, среди которых клинически наиболее значимыми являются скрытые кровопотери из желудочно-кишечного тракта, чаще из кишечника (невыявленная опухоль!). С учетом этого в подобных ситуациях при исключении других возможных причин неэффективности ПЖ необходимо тщательное эндоскопическое исследование кишечника (в ряде случаев — повторное). Таким образом, у больных ЖДА наряду с устранением причины обязательна патогенетическая терапия ПЖ (ПСЖ и ПЖК), которые должны назначаться преимущественно внутрь. Тактика лечения ПЖ предусматривает выбор пути введения ПЖ с учетом клинической ситуации, оптимального ПЖ с достаточным содержанием в нем железа, оценку эффективности и переносимости препарата, длительность насыщающей и обоснованность поддерживающей терапии. Своевременная верификация синдрома ЖДА и выявление ее причины, адекватная патогенетическая терапия с назначением ПЖ с оптимальными фармакокинетическими свойствами, клинической эффективностью, переносимостью позволяет корригировать анемический синдром и обеспечивать достаточный уровень качества жизни у данной категории пациентов.
Е.С.Сахарова, Е.С.Кешишян, CONSILIUM Medicum 2002 г., Приложение: Педиатрия
Анемия является одной из наиболее частых патологий у детей раннего возраста. Около 20% доношенных детей страдают данным заболеванием, а среди недоношенных на первом году жизни анемия развивается практически у всех. При этом тяжесть анемии тем выше, чем меньше гестационный возраст ре6енка. В первые месяцы жизни у недоношенных детей с очень низкой массой тела при рождении (менее 1500 г) и гестационным возрастом менее 30 нед. тяжелая анемия, требующая переливание эритроцитарной массы, составляет до 90% .
В патогенезе ранней анемии недоношенных играет роль не только формирование железодефицита, характерное для всех детей раннего возраста, но и факторы незавершенного онтогенеза.
Кроветворение во внутриутробном периоде начинается очень рано. Уже в первые 2 нед. развития эмбриона определяются островки кроветворения — эритроциты продуцируются желточным мешком. Начиная с 12-16 нед., основным местом кроветворения становится печень и в меньшей степени селезенка. Примерно в 20 нед. внутриутробного развития плода начинается эритропоэз в костном мозге, а в печени и селезенке постепенно угасает. Таким образом, к моменту рождения у доношенных детей кроветворение в печени почти полностью прекращается, тогда как у глубоконедоношенных очаги кроветворения сохраняются практически до 40-й недели гестации (т.е. от 3 нед. до 3 мес. их фактического возраста). На ранних стадиях внутриутробного развития отмечается небольшое количество эритроцитов. До начала костномозгового кроветворения концентрация эритроцитов в крови плода растет медленно, а к моменту рождения резко возрастает и составляет уже 5-6 млн в 1 мм 3 .
Для недоношенных детей характерны морфологические изменения эритроцитов. Так, эритроциты аномальной формы составляют 27%, тогда как у доношенных новорожденных всего — 14%. Это способствует тому, что период жизни эритроцита у доношенных почти в 2 раза дольше, чем у недоношенных детей, и составляет 60-70 и 35-50 дней соответственно.
Укорочению жизни эритроцитов могут способствовать особенности строения их мембран. При изучении состава общих липидов мембран эритроцитов у детей с ранней анемией недоношенных выявлено, что со 2-й недели у них наблюдается снижение содержания фосфолипидов и повышается содержание холестерина. Эти изменения прогрессируют к 6-й неделе жизни и в разгар анемии достигают максимума, что коррелирует с клиническими и лабораторными симптомами.
В нарушении проницаемости мембран эритроцитов у недоношенных детей также играет роль низкий уровень витамина Е, который локализуется в мембранах и активно участвует в перекисном фосфорилировании. Дефицит витамина Е наблюдается у 86% недоношенных детей .
Зародышевые эритроциты на ранних этапах онтогенеза продуцируют зародышевую (эмбриональную) форму гемоглобина.
Между 7-12-й неделей внутриутробной жизни эмбриональный гемоглобин заменяется фетальным. Уровень гемоглобина также зависит от срока гестации, составляя на 10-й неделе в среднем 90 г/л, а к 38-й неделе 170±20 г/л.
Фетальный гемоглобин обладает более высоким сродством к кислороду и более медленной отдачей кислорода тканям по сравнению с гемоглобином взрослых. Переключение синтеза фетального гемоглобина на гемоглобин взрослых находится под контролем генов, находящихся в 11 и 16-й хромосомах и начинается на 30-32-й неделе внутриутробного развития. Содержание фетального гемоглобина у недоношенных детей при рождении составляет в среднем 70-80%, у доношенных новорожденных — 60-70%. Более половины объема фетального гемоглобина заменяется на гемоглобин взрослых в первые дни жизни ребенка, в дальнейшем этот процесс несколько замедляется, но к 4-5-му месяцу постнатальной жизни у большинства детей остается около 1% фетального гемоглобина. У недоношенных детей этот процесс замедлен, основной объем смены гемоглобина приходится на 40-ю неделю гестации, а полная смена растягивается практически на весь первый год жизни. Кроме того, задержка переключения синтеза с фетального гемоглобина на гемоглобин взрослых усиливается при тяжелой гипоксии и стрессе у плода.
Уровень гематокрита определяется концентрацией гемоглобина и эритроцитов в крови. В норме гематокрит у новорожденных выше, чем у взрослых, и составляет 50-55%.
Отражением состояния эритропоэза является уровень ретикулоцитов. Среднее количество ретикулоцитов у новорожденного составляет 4,2-7,2%. В конце 1-й недели постнатального возраста этот показатель снижается до уровня взрослых и составляет 1%.
При рождении доношенного ребенка определяется высокое содержание гемоглобина, что в условиях повышенного по сравнению с внутриутробным потреблением кислорода является избыточным. Это в свою очередь ведет к усилению выработки эритропоэтина и снижению эритропоэза. При угнетении функции костного мозга и усиленном разрушении эритроцитов происходит постепенное снижение и смена гемоглобина, который к 8-12-й неделе у доношенных детей достигает 110-120 г/л. Если гемоглобин снижается до этого порога — для доношенных 100-110 г/л, нарушается отдача кислорода тканям, что стимулирует продукцию эритропоэтина. В результате начинается процесс увеличения продукции эритроцитов .
У недоношенных детей процесс разрушения эритроцитов идет быстрее в связи с более коротким периодом жизни этих клеток. Уровень гемоглобина, при котором начинает увеличиваться продукция эритропоэтина у недоношенных детей, значительно ниже, чем у доношенных, и составляет 90-70 г/л (таким образом, такой уровень гемоглобина — критический для доношенных детей, является допустимым для недоношенных!).
У взрослых и детей старшего возраста в ответ даже на легкую гипоксию наблюдается быстрое увеличение продукции эритропоэтина, в то время как недоношенные не способны продуцировать адекватные количества эритропоэтина даже при критических значениях циркулирующих эритроцитов, что обусловлено, по-видимому, более низкой потребностью в кислороде.
Таким образом, анемия недоношенных характеризуется прогрессивным снижением уровня гемоглобина (до 90-70 г/л и ниже), относительно низким уровнем ретикулоцитов и угнетением костномозгового кроветворения.
Выделяют раннюю и позднюю анемию недоношенных.
Ранняя анемия развивается на 4-10-й неделе постнатальной жизни и характеризуется снижением уровня ретикулоцитов менее 1%, уровня гемоглобина до 80-70 г/л и ниже, а гематокрита до 20-30% .
Клиническая картина ранней анемии недоношенных проявляется симптомами, свойственными истинной анемии, такими как бледность кожных покровов, тахикардия или брадикардия, тахипное, апноэ.
Среди причин ранней анемии недоношенных, кроме указанных, определенное значение придается высокой скорости увеличения массы тела и объема циркулирующей крови, несоизмеримых с уровнем эритропоэза .
Кроме того, в генезе ранней анемии недоношенных играет роль дефицит фолиевой кислоты, витамина В6, микроэлементов: цинка, меди, селена, молибдена. Запасы фолиевой кислоты истощаются в течение первых недель жизни, что приводит к нарушению синтеза фолатов микрофлорой кишечника.
Известно, что ранняя анемия недоношенных может быть одним из проявлений инфекции и потенцироваться ее постнатальным развитием.
Существуют исследования, доказывающие зависимость между концентрацией гемоглобина и уровнем тиреоидных гормонов (Т3 и Т4). В условиях относительного дефицита Т3 и Т4, характерного для недоношенных детей, происходит нарушение тех этапов эритропоэза, которые требуют интенсивного синтеза специфических белков — ферментов, участвующих в образовании гемоглобина .
Кроме «условно физиологических» причин анемии, связанных с незавершенным онтогенезом, к сожалению, в потенцировании тяжести анемии определенную роль играют так называемые ятрогенные причины, такие как частые, хоть и небольшие по объему кровопотери в результате заборов крови для лабораторных исследований без восполнения ОЦК. По данным литературы, за первую неделю жизни у новорожденного недоношенного ребенка для исследований забирается около 38,9 мл крови. Относительно общего объема крови (80 мл/кг массы) это — очень большая цифра .
Суммируя все сказанное, в патогенезе анемии недоношенных играют роль сочетание нескольких факторов:
а) укороченная продолжительность жизни эритроцитов;
б) пролонгированная циркуляция и поздняя смена фетального гемоглобина;
в) особенность обмена белков, витаминов, микроэлементов;
г) инфекционные агенты, в частности грамотрицательная флора, для жизнедеятельности которой необходимо активное потребление железа;
д) ятрогенные причины.
Одним из основных методов лечения ранней анемии недоношенных до настоящего времени остаются гемотрансфузии. Наиболее часто для гемотрансфузий используется донорская эритроцитарная масса. Показаниями для переливаний эритроцитарной массы при анемии недоношенных являются: снижение гемоглобина ниже 130 г/л и гемотокрита ниже 0,4 в период ранней адаптации (первые 7 дней жизни) в сочетании с тяжелыми нарушениями дыхания и сердечной деятельности. Широкое использование гемотрансфузий у недоношенных детей сопряжено хотя и с невысоким, но существенным риском. Это прежде всего возможность передачи с трансфузиями вирусных инфекций (ВИЧ, ЦМВ), возможны также перегрузки сосудистого русла жидкостью, развития состояния «трансплантант против хозяина», электролитного дисбаланса. В настоящее время ведется поиск альтернативных путей решения этой проблемы. Одной из них является применение рекомбинантного человеческого эритропоэтина, эффективность которого сейчас интенсивно изучается .
Поздняя анемия недоношенных развивается на 3-4-м месяце жизни. Она имеет большее сходство с железодефицитной анемией детей раннего возраста. Клиническая картина поздней анемии недоношенных характеризуется снижением аппетита, уплощением весовой кривой, бледностью кожи и слизистых оболочек, сухостью кожи, увеличением печени и селезенки. Отмечается снижение сывороточного железа — гипохромия, с тенденцией к микроцитозу и гиперрегенераторной реакцией костного мозга.
Кроме всех особенностей, присущих ранней анемии недоношенных, в период развития поздней анемии начинают проявляться симптомы дефицита железа. Наиболее активное поступление железа от матери к плоду осуществляется в последние 2 мес. беременности, поэтому недоношенность в 4-8 нед. может привести к сокращению запасов железа в 1,5-3 раза по сравнению с доношенными .
У доношенных детей ретикулоэндотелиальная система имеет запас железа на 15-20 дней. Как только достигается нижний уровень гемоглобина — 100-110 г/л у доношенных и 70-90 г/л у недоношенных, начинается стимуляция эритропоэза. Если запасов железа недостаточно, происходит дальнейшее снижение гемоглобина и анемия становится железодефицитной. У недоношенного ребенка потребность в железе выше, чем у доношенного, а запасов разительно меньше. Учитывая, что железо находится в организме не только в виде гема, но также идет на построение миоглобина и ферментов — каталазы, пероксидазы, цитохромов и цитохромоксидазы, постнатальный расход его крайне велик.
После рождения источниками железа для развивающегося организма являются поступление экзогенного железа в составе пищевых продуктов и его утилизация из эндогенных запасов.
Попытки обогащения рациона питания введением адаптированных смесей, в том числе и обогащенных железом, не приводят к желаемому результату, поскольку последнее плохо всасывается. Для недоношенных детей, особенно первых месяцев жизни, единственным физиологическим продуктом питания, который обеспечивает равновесие обмена железа в организме, является материнское молоко, сбалансированное по всем ингредиентам в соответствии с физиологическим потребностям растущего организма. Хотя в женском молоке содержание железа невелико (0,2-1,5 мг/л), существуют специальные механизмы для более эффективного его усвоения (до 50%) . Вместе с тем большой проблемой является поддержание лактации у женщин, находящихся в состоянии стресса в результате досрочно прерванной беременности и больного ребенка. Просветительская работа, психологическая поддержка матери являются единственным способом обеспечения грудным вскармливанием недоношенного ребенка.
Для диетической коррекции железодефицита требуется своевременное (но не ранее 4-5-го месяца жизни) введение продуктов прикорма (фруктов, овощей, в дальнейшем, после 8 мес. — мяса). В то же время исследованиями доказано, что для лечения анемии (но не для ее профилактики) недостаточно только повышения уровня пищевого железа, а требуется медикаментозная дотация.
Чем же так опасна железодефицитная анемия?
Железодефицитная анемия способствует развитию хронической гипоксии, которая в свою очередь может приводить к замедлению умственного и психомоторного развития ребенка .
В связи с этим лечение анемии у недоношенных детей и профилактика дефицита железа у всех детей является важной и обязательной составной частью в общей схеме наблюдения за детьми на 1-м году жизни . Кроме немаловажных диетических подходов, актуально раннее назначение профилактических доз препаратов железа всем недоношенным детям. Препаратами выбора в этом случае являются современные представители гидроксид полимальтозного комплекса трехвалентного железа: Мальтофер и Феррум Лек. Гидроксид полимальтозный комплекс стабилен в физиологических условиях, что исключает образование свободных ионов железа. В отличие от распространенных ранее солевых (ионных) препаратов железа — двухвалентные соединения солей железа (например, сульфат железа), полимальтозные комплексы (Мальтофер и Феррум Лек) не оказывают раздражающего действия на слизистую оболочку кишечника, что часто проявляется в виде запора, диареи, тошноты, срыгиваний. Всасывание железа из полимальтозных комплексов приближена к абсорбции гемового железа и обеспечивается активным транспортным механизмом, наиболее физиологичным для организма. В данном случае железо непосредственно переносится через трансферриновые рецепторы в места кроветворения или доставляется в места хранения железа, где депонируется в ретикулоэндотелиальной системе (печени и селезенке) в виде ферритина.
Клинические исследования препарата “Мальтофер” показали его одинаковую эффективность по сравнению с солевыми препаратами. При этом количество побочных эффектов со стороны желудочно-кишечного тракта в 3 раза меньше при применении полимальтозного комплекса железа, а число пациентов, отказавшихся от продолжения курса лечения, более чем в 2 раза больше в группе солевых препаратов .
Химическая структура комплекса не выделяет железо в свободном виде. Совместно с активным транспортным механизмом всасывания железа это предохраняет организм от интоксикации свободными ионами железа , а также их оксидативного воздействия, присущее солевым препаратам железа .
Эти же механизмы поддерживают систему саморегуляции по принципу «обратной связи»: всасывание железа из комплекса прекращается, как только восстанавливается его необходимый уровень в организме, что исключает возможность отравления данными препаратами при их передозировке .
Недоношенным детям с первых недель жизни до 1-го года рекомендуется профилактический прием указанных препаратов железа из расчета 2 мг/кг/сут элементарного железа. Лечебная доза составляет 5 мг/кг/сут элементарного железа и не меняется до нормализации уровня гемоглобина. Контроль показателей красной крови (уровень гемоглобина, ЦП, эритроциты) недоношенным детям после выписки из отделений выхаживания необходимо проводить в обязательном порядке в 3, 6 и 12 мес, затем 2 раза в год, а при выявлении анемии — каждые 14 дней до стабилизации показателей гемограммы.
Учитывая особенности патогенеза анемии недоношенных детей, тенденцию к развитию гипорегенераторной реакции костного мозга, мегалобластозу, макроцитозу, повышенному гемолизу эритроцитов, детям с низкой массой тела при рождении необходимо раннее, с 7 дней жизни, введение фолиевой кислоты по 1 мг в сутки, витамина Е по 20 мг/кг в сутки, витаминов группы В.
Согласно Приказу Минздрава РФ № 375 от 18.12.97 г. о проведении профилактических прививок железодефицитная анемия не является противопоказанием к вакцинации. Напротив, недоношенные дети представляют особую группу риска по развитию осложненного инфекционного процесса. Поэтому даже в случае тяжелых проявлений анемии профилактические прививки могут быть проведены сразу после купирования острых проявлений. Умеренное снижение гемоглобина, проведение противоанемического лечения не является основанием для отсрочки вакцинации .
- Бисярина В.П., Казакова Л.М. Железодефицитная анемия у детей раннего возраста. М., 1979; 176.
- Nex E., Cristensen N.S., Olesen S. Volume of blood removed for analytical purposes during hospitalization of low birth weight infants. Clinical chemistry, 1981; 27: 759-61.
- Алдышева Т.В. Соединение веществ в плазме крови и активность антиокислительных ферментов эритроцитов при наличии анемии недоношенных детей. Вопросы адаптации недоношенных и детей грудного возраста. М., 1985; 127-30
- Дегтярев Д.Н., Курмашева Н.А., Володин Н.Н. Современные представления о патогенезе и лечении анемии у недоношенных детей. Лекции кафедры неонатологии ФУВ РГМУ, 1994.
- Dallmann P.R. Nutritional anemia in infancy in Tsang R.C., Nicols B.L. Nutrition during infancy, Philadelphia, 1988.
- Красницкая Л.Н. Содержание тиреоидных гормонов, тестостерона и кортизола в сыворотки крови у недоношенных детей при ранней анемии. Автореф. дисс. канд.мед.наук, Л., 1988; 22.
- Пригожина Т.А. Эффективность рекомбинантного эритропоэтина в комплексной профилактике и лечении ранней анемии недоношенных. Дисс. канд.мед.наук, М., 1988.
- Акре Д. Кормление детей первого года жизни: функциональные основы. Бюллетень ВОЗ, 1989; приложение к тому 67: 30-35.
- Walter T. Infancy: mental and motor development. American Jornal of Clinical Nutrition, 1989; 50: 655-66
- Jacobs P. et. al. Better tolerance of iron polymaltose complex compared with ferrous sulfate in the treatment of anemia. Hematology, 2000; 5: 77-83
- Geisser P. et. al. Structure / histotoxicity relationship of peroral iron preparations. Drug Research, 1992; 42: 1439-52.
- Tuomainen, T-P, et.al. Oral supplementation with ferrous sulfate but not with non-ionic iron polymaltose complex increases the susceptibility of plasma lipoproteins to oxidation, Nutrition Research, 1999; 19: 1121-32
- Geisser P., Hohl H. and Mueller A. Klinische Wirksamkeit dreier verschiedener Eisenpraeparate an Schwangeren. Schweiz. Apotheker-Zeitung, 1987; 14: 393-8
- Федоров А.М. О новом календаре профилактических прививок. Детский доктор, 1999; 1: 27-9.
Снижение гемоглобина довольно часто встречается у детей раннего возраста. Почти каждый второй ребенок, имеющий анемию, страдает железодефицитом.
Патологическое состояние, при котором снижается количество эритроцитов и гемоглобина, называется анемией. Если причиной анемического состояния стало снижение поступления железа, то такая анемия называется железодефицитной.
Регулярное пополнение запасов этого вещества происходит во время грудных вскармливаний. Материнское молоко содержит все необходимые питательные компоненты, а также микро- и макроэлементы. При полноценном вскармливании и своевременном введении прикормов количества железа в организме вполне хватает для осуществления всех жизненно необходимых функций.
Феррум входит в состав гемоглобина. Достаточное наполнение железом красных кровяных телец приводит к выполнению транспортной функции. Гемоглобин позволяет переносить кислород к каждой клеточке организма. Для компенсации железа грудным малышам достаточно 1-2 граммов.
Всасывание микроэлемента происходит в тонком кишечнике. После этого большая часть железа остается в эритроцитах. Там находится порядка 80% всего феррума. Около 20% железа остается в макрофагах и клетках печени. Такой запас называется резервным, он нужен только в экстренных ситуациях. Обычно они возникают при сильных травмах и повреждениях, сопровождающихся сильной кровопотерей.
К развитию дефицита железа могут приводить:
- Недостаточное поступление с пищей. Растительное вегетарианское питание с отсутствием животных белков часто приводит к развитию анемических состояний. В мясных продуктах и птице содержится гемовое железо. Оно легче всасывается и хорошо усваивается детским организмом.
- Хронические болезни органов пищеварения. Патологии желудка и кишечника способствуют нарушению всасывания железа.
- Многоплодная беременность . Двойняшки или близнецы – это более высокий риск развития железодефицита. Если будущая мама, которая вынашивает в период беременности сразу несколько малышей, употребляет недостаточное количество богатых железом продуктов, то у малышей после рождения часто развивается анемическое состояние.
- Недоношенность. Приводит к недоразвитию органов кроветворения, которые не могут осуществлять свои функции по образованию эритроцитов в достаточном для организма количестве.
- Патологии, возникшие во время беременности. Гипоксия плода, плацентарная недостаточность и нарушения строения плаценты могут приводить к развитию анемического состояния у будущего ребенка.
- Неполноценное питание мамы во время беременности. Если будущая мама ест мало продуктов, которые содержат достаточное количество железа, то у нее может развиться железодефицитное состояние. Это приводит к развитию анемии у ребенка.
- Несвоевременное введение прикормов. Отсутствие в детском рационе пюре, приготовленного из говядины или птицы, может способствовать развитию анемического состояния.
- Выраженный рост в период пубертата. В результате гормонального дисбаланса у подростков часто наблюдается анемический синдром. Это расстройство носит транзиторный характер и исчезает после окончания пубертатного периода.
- Чрезмерно сильные менструации у девочек в подростковом возрасте. Длительные и слишком обильные выделения в критические дни приводят к сильной кровопотере.
- Функциональные нарушения кишечника. Стойкий синдром раздраженной кишки и дисбактериоз способствуют нарушению всасывания железа из поступающей пищи.
Все железодефицитные состояния по степени тяжести делятся на:
- Легкие. Диагностируются при уровне гемоглобина от 90 до 110 г/литр. Характеризуются появлением небольших клинических симптомов или могут долго оставаться неопознанными.
- Среднетяжелые. Уровень гемоглобина составляет от 70 до 90 г/литр.
- Тяжелые. Возникают при снижении гемоглобина ниже 70 г/литр. Требуют безотлагательного назначения лечения.
- Крайне тяжелые. Встречаются при снижении гемоглобина ниже 50 г/литр. Для лечения может потребоваться переливание крови или эритроцитарной массы.
Для недоношенных малышей применяется классификация железодефицитных состояний по сроку появления анемических проявлений.
Все дефициты железа могут быть:
- Ранними. Возникают у малышей сразу после рождения. Отказ от грудных кормлений или использование неправильно подобранных адаптированных смесей, недоразвитие органов кроветворения приводят к появлению анемических симптомов.
- Поздними. Встречаются у малышей в 3-4 месяца после рождения. Связаны с истощением резервного запаса железа и чрезмерным разрушением гемоглобина.
Во многих случаях определить признаки железодефицитной анемии достаточно трудно. Если дефицит железа выражен незначительно, то симптомы болезни проявляются не очень ярко. Только у ослабленных малышей или при длительном развитии анемического состояния можно заподозрить наличие железодефицитной анемии.
При анемии встречаются следующие симптомы:
- Бледность кожи. На фоне бледных кожных покровов губы приобретают синий оттенок. Кожа становится истонченной, хорошо видны вены.
- Быстрая утомляемость и выраженная слабость. Симптом хорошо проявляется у школьников и подростков. Дети хуже учатся в школе, плохо запоминают учебный материал, не могут хорошо концентрироваться на предмете.
- Повышенная сухость кожных покровов. Применение специальных увлажняющих средств не приводит к улучшению состояния. Кожа становится очень сухой и легко травмируется.
- Появление мелких морщинок около губ.
- Снижение артериального давления на фоне повышения пульса.
- Изменение поведения. Малыши становятся более капризными, быстро утомляются. Груднички могут отказываться от кормлений грудью.
- Нарушения стула. Наиболее часто возникают запоры. Поносы встречаются гораздо реже, обычно при развитии дисбактериоза кишечника.
- Частый кариес зубов. В некоторых случаях — кровоточивость десен.
- Повышенная ломкость ногтей и чрезмерное выпадение волос.
- Нарушение вкусовых предпочтений. Пристрастие к чрезмерно острой пище может свидетельствовать о снижении железа в организме.
- Отставание в физическом развитии. Недостаточный набор веса или отклонения от нормальных показателей роста могут свидетельствовать о наличии анемического синдрома.
- Подверженность частым простудным и инфекционным заболеваниям. Длительное кислородное голодание приводит к снижению иммунитета.
Установить железодефицит можно уже на ранних стадиях. Обычный анализ крови позволяет выявить снижение количества эритроцитов и гемоглобина. Железодефицитные анемии сопровождаются также пониженным цветовым показателем. Такие состояния называются гипохромными.
При прелатентном периоде болезни, когда еще отсутствуют изменения в общем анализе крови, можно выявить дефицит железа только в тканях. При следующих стадиях заболевания наблюдается уже снижение концентрации железа в сыворотке крови. При конечной стадии болезни регистрируется низкий уровень гемоглобина и эритроцитов.
В некоторых случаях требуются дополнительные консультации у гастроэнтеролога, гематолога, нефролога. Девочку-подростка следует обязательно показать гинекологу. Для установления потерь железа требуется первичный диагноз, который привел к развитию анемического состояния.
Для определения болезней и анатомических дефектов врачи иногда назначают ультразвуковое обследование печени и селезенки. Такое обследование позволяет выявить различные патологии органов на самых ранних стадиях.
Длительное кислородное голодание, которое возникает при дефиците железа в организме, приводит к развитию неблагоприятных последствий. Наиболее опасны такие состояния для головного мозга и сердца.
При длительном течении заболевания может развиться миокардит. Это состояние опасно развитием нарушений сердечного ритма, а также сильным снижением артериального давления. Аритмии и сильная тахикардия доставляют малышам выраженный дискомфорт.
Для лечения анемического состояния, вызванного дефицитом железа, применяют:
- Лечебное питание. Такое детское меню включает большое количество продуктов с высоким содержанием железа. Ежедневное включение в рацион питания мяса, птицы и субпродуктов будет способствовать нормализации уровня гемоглобина. Такая диета должна соблюдаться в течение длительного времени.
- Назначение препаратов железа. Такие лекарства выписываются на курсовой прием. Нормализация гемоглобина и эритроцитов происходит только через несколько месяцев. Наиболее часто малышам назначаются таблетки и сиропы. При наличии хронических заболеваний желудка и кишечника железосодержащие препараты выписываются в виде уколов.
Для восстановления нормального уровня железа в организме требуется обязательный контроль за достаточным поступлением продуктов с богатым содержанием этого микроэлемента. Своевременное лечение и профилактика обострений заболеваний желудочно-кишечного тракта помогают предотвратить развитие железодефицитного состояния в дальнейшем.
Все малыши, родившиеся раньше положенного срока или имеющие малый вес при рождении, должны получать достаточное количество железа. Для этого мамочке следует осуществлять грудные вскармливания как можно дольше. Если по каким-то причинам лактация прекращается, нужно будет подобрать правильные адаптированные смеси с повышенным содержанием железа и витаминов.
О том, как определить уровень гемоглобина, и что делать, если он стал низким, смотрите в следующем видео.
Национальное общество детских гематологов и онкологов
Составители: Чернов В.М., Тарасова И.С.
3. Критерии лабораторной диагностики ЖДА …. 5
4. Дифференциальная диагностика ЖДА ……………………………….….………. 6
5.1. Расчет дозы препарата железа …………………….………………………. 8
5.2. Терапевтический план лечения ЖДА у детей. ……………………….… 10
5.3. Препараты для лечения ЖДА ……………………………………………. 12
5.4. Контроль эффективности лечения ЖДА препаратами железа ………….. 18
5.5. Причины неэффективности лечения ЖДА препаратами железа …. 19
5.6. Отношение к переливанию эритроцитной массы ………………………… 21
6. Меры общественной и индивидуальной профилактики ЖДА..…………………… 22
7. Диспансерное наблюдение больных с ЖДА ………………………………………. 27
Железодефицитная анемия (ЖДА) – полиэтиологичное заболевание, возникновение которого связано с дефицитом железа в организме из-за нарушения его поступления, усвоения или повышенных потерь, характеризующееся микроцитозом и гипохромной анемией.
Возникновению ЖДА, как правило, предшествует развитие латентного дефицита железа (ЛДЖ), который рассматривается как приобретенное функциональное состояние и характеризуется латентным (скрытым) дефицитом железа, снижением запасов железа в организме и недостаточным его содержанием в тканях (сидеропения, гипосидероз), отсутствием анемии.
ЖДА характеризуется сочетанием сидеропенического и анемического синдромов.
Рубрики, присвоенные различным железодефицитным состояниям в Международной статистической классификации болезней и проблем, связанных со здоровьем десятого пересмотра (МКБ-10), представлены в табл. 1.
Таблица 1. Рубрики в МКБ-10, присвоенные железодефицитным состояниям (цит. по )
- Международная статистическая классификация болезней и проблем, связанных со здоровьем (МКБ-10). Десятый пересмотр. – Том 1, часть 1. – Всемирная организация здравоохранения, Женева, 1995: С. 216–222.
2. Причины развития ЖДА
Основная причина развития ЖДА, по мнению экспертов ВОЗ, это неправильное (несбалансированное) питание. Гораздо реже ЖДА развивается вследствие кровотечений различных локализаций, что приводит к хронической постгеморрагической анемии (ХПА), или глистных инвазий в странах с низкой санитарной культурой.
Основными причинами развития ЖДА в детской практике являются:
- дефицит железа при рождении ребенка;
- алиментарный дефицит железа вследствие несбалансированного питания;
- повышенные потребности организма в железе вследствие бурного роста ребенка;
- потери железа из организма, превышающие физиологические.
Алиментарно-зависимыми факторами в развитии дефицита железа у детей являются:
- недостаточное поступление железа с пищей;
- сниженное всасывание железа;
- увеличенные потери железа из-за микрокровотечений из кишечника, обусловленных ранним введением кефира и коровьего молока.
Причинами развития ХПА у лиц мужского пола являются различные заболевания желудочно-кишечного тракта (ЖКТ): язвенные кровотечения, полипы толстой кишки, неспецифический язвенный колит, ангиоматоз кишечника, дивертикул Меккеля, кровотечения из геморроидальных образований, опухоли желудка и кишечника. Среди причин ХПА у девушек и женщин на первом месте находятся маточные кровотечения, а заболевания ЖКТ занимают второе место. Гендерные различия необходимо учитывать в выявлении причин развития ЖДА.
3. Критерии лабораторной диагностики ЖДА
В общем анализе крови, выполненном «ручным» методом, ориентируются на снижение концентрации гемоглобина – Hb (менее 110 г/л), небольшое снижение количества эритроцитов (менее 3,8 10 12 /л), снижение цветового показателя (менее 0,85), увеличение СОЭ (более 10–12 мм/час), сниженное или нормальное количество ретикулоцитов (10–20‰). Дополнительно врач-лаборант описывает морфологические изменения эритроцитов – анизоцитоз и пойкилоцитоз. ЖДА – это микроцитарная, гипохромная, нормо- или реже гипорегенераторная анемия.
В общем анализе крови, выполненном на автоматическом гематологическом анализаторе, изменяются указанные выше показатели и ряд эритроцитарных индексов. Снижаются средний объем эритроцита – MCV (менее 80 фл), среднее содержание Hb в эритроците – MCH (менее 26 пг), средняя концентрация Hb в эритроците – MCHC (менее 320 г/л), повышается степень анизоцитоза эритроцитов – RDW (более 14%).
В биохимическом анализе крови ориентируются на снижение концентрации сывороточного железа – СЖ (менее 12,5 мкмоль/л), повышение общей железосвязывающей способности сыворотки – ОЖСС (более 69 мкмоль/л), снижение коэффициента насыщения трансферрина железом – НТЖ (менее 17%), снижение концентрации сывороточного ферритина – СФ (менее 30 нг/мл или мкг/л). В последние годы появилась возможность определения растворимых трансферриновых рецепторов (рТФР), концентрация которых в условиях дефицита железа увеличивается (более 2,9 мкг/мл).
4. Дифференциальная диагностика ЖДА
Дифференциальный диагноз ЖДА следует проводить с:
- другими анемиями из группы дефицитных анемий: В 12 -дефицитной анемией (D51) и фолиево-дефицитной анемией (D52), т.е. мегалобластными анемиями;
- с анемией хронических заболеваний – АХБ (D63.8).
Для мегалобластных анемий характерны следующие лабораторные признаки:
- макроцитарная анемия (MCV более 100 фл);
- вовлечение в процесс 2–3-х ростков кроветворения и как следствие наличие, кроме анемии, лейкопении, нейтропении и тромбоцитопении;
- гиперсегментация ядер нейтрофилов (пяти- и шестидольчатые, многолопастные ядра);
- мегалобластный тип кроветворения, наличие в костном мозге крупных эритроидных клеток;
- снижение концентрации в сыворотке крови витамина В 12 (норма 100–250 пг/мл) при В 12 -дефицитной анемии;
- снижение концентрации в сыворотке фолиевой кислоты (норма 125–600 нг/мл) при фолиево-дефицитной анемии.
АХБ имеет определенные причины развития и довольно сложный патогенез. Для дифференциальной диагностики ЖДА и АХБ, кроме наличия основного заболевания, необходимо проведение обследования. Наиболее информативными лабораторными показателями являются НТЖ, СФ и рТФР (табл. 2).
Таблица 2. Дифференциальная диагностика ЖДА и АХБ
N – нормальное значение показателя; ↓ – снижение показателя; – повышение показателя.
Основными причинами развития АХБ являются:
- инфекции, протекающие хронически (туберкулез, сепсис, остеомиелит, абсцесс легких, бактериальные эндокардиты и др.);
- системные заболевания соединительной ткани (системная красная волчанка, ревматоидный артрит);
- хронические заболевания печени (гепатит, цирроз);
- хронические воспалительные заболевания кишечника (неспецифический язвенный колит, болезнь Крона);
- злокачественные новообразования (солидные опухоли, множественная миелома, лимфомы).
В патогенезе развития АХБ имеется несколько механизмов: нарушения метаболизма железа (реутилизации железа из макрофагов), супрессия эритропоэза (ингибиторы эритропоэза, цитокины, подавляющие действие эритропоэтина – ЭПО), неадекватная продукция ЭПО (выработка ЭПО повышена, но не соответствуют степени тяжести анемии), гемолиз эритроцитов (из-за повреждения мембраны микротромбами или продуктами перекисного окисления липидов).
5. Лечение ЖДА
Целью лечения ЖДА являются устранение причины, лежащей в основе развития заболевания (коррекция питания, выявление и устранение источника кровопотери), и возмещение дефицита железа в организме.
В связи с этим основными принципами лечения ЖДА являются:
- назначение лекарственных железосодержащих препаратов, поскольку возместить дефицит железа в организме иными способами невозможно;
- использование преимущественно препаратов железа для перорального приема;
- назначение препаратов железа в адекватных дозах, которые рассчитываются для каждого конкретного больного с учетом массы его тела и терапевтического плана лечения;
- достаточная длительность курса лечения препаратами железа, составляющая при анемии легкой степени 3 мес., при анемии средней степени 4,5 мес., и при тяжелой анемии 6 мес.;
- преодоление тканевой сидеропении и пополнение запасов железа в депо, что определяется по нормализации концентрации СФ;
- необходимость контроля эффективности терапии препаратами железа.
5.1. Расчет дозы препарата железа
В России лечение ЖДА определяется протоколом, утвержденным Минздравсоцразвития России 22 октября 2004 г., – «Протокол ведения больных. Железодефицитная анемия» . Создание этого протокола группой ведущих специалистов нашей страны явилось значительным движением вперед, поскольку «вооружило» врачей единым пониманием проблемы дефицита железа, критериями его диагностики, принципами лечения и наблюдения больных ЖДА, оценки качества их жизни.
С точки зрения врача-педиатра лечение ЖДА у детей имеет некоторые особенности, которые следует учитывать в лечебном протоколе. Прежде всего, применение у детей в возрасте до 3 лет солевых препаратов двухвалентного железа в дозе 5–8 мг/кг массы тела в сутки, как это рекомендовано в «Протоколе», вызывает проявления токсичности у многих больных и не оправдано с терапевтической точки зрения.
При расчете доз солевых препаратов железа следует использовать рекомендации ВОЗ (табл. 3). Аналогичная доза солевых препаратов железа (3 мг/кг массы тела в сутки) для детей в возрасте до 3 лет указана и в пособии для врачей, утвержденном Департаментом здравоохранения Москвы в 2004 г. .
Таблица 3. Возрастные дозы пероральных солевых препаратов железа для лечения ЖДА (рекомендации ВОЗ, 1998; цит. по )
Различный возраст детей (от периода новорожденности до старшего подросткового возраста) и, соответственно, различная масса тела (3,2–70 кг и более), делают необходимым индивидуальный расчет дозы препарата железа для каждого ребенка.
В «Протоколе» дозу препарата на основе гидроксид полимальтозного комплекса (ГПК) трехвалентного железа рекомендуют рассчитывать, ориентируясь на возраст детей, а не на массу их тела. Мы считаем, что в детской практике доза препаратов железа (III) на основе ГПК должна составлять 5 мг/кг массы тела в сутки независимо от возраста, именно эта доза рекомендована в упомянутом выше пособии для врачей .
- Протокол ведения больных. Железодефицитная анемия. – М.: Ньюдиамед, 2005. – 76 с.
- WHO, UNICEF, UNU. IDA: prevention, assessment and control: report of joint WHO/UNICEF/UNU consultation. Geneva, WHO; 1998.
- UNICEF, United Nations University, WHO. Iron deficiency anemia: assessment, prevention and control. A guide for programme managers. – Geneva: World Health Organization, 2001 (WHO/NHD/01.3). – 114 p. – Режим доступа: http://www.who.int/nutrition/publications/micronutrients/anaemia_iron_deficiency/WHO_NHD_01.3/en .
- Румянцев А.Г., Коровина Н.А., Чернов В.М. и др. Диагностика и лечение железодефицитной анемии у детей: Метод. пособие для врачей. – М., 2004. – 45 c.
5.2. Терапевтический план лечения ЖДА у детей
В российской педиатрической практике многие годы был принят так называемый «трапециевидный» терапевтический план лечения ЖДА у детей. В соответствии с этим планом в первые 3–5 дней дозу солевых препаратов железа постепенно повышали, чтобы не вызвать у больного раздражения слизистой оболочки ЖКТ. Полную (100%) дозу солевого препарата железа применяли в течение 1,5–3 мес. в зависимости от степени тяжести анемии с последующим ее снижением до 50% к окончанию лечения. Этот план, как и большинство других, был разработан эмпирическим путем, и его эффективность никогда не была подтверждена рандомизированными исследованиями.
Появление препаратов железа (III) на основе ГПК заставило пересмотреть план лечения ЖДА.
Под руководством сотрудников Федерального научно-клинического центра детской гематологии, онкологии и иммунологии (ФНКЦ ДГОИ) Минздрава России было проведено рандомизированное исследование по сравнению эффективности двух планов лечения ЖДА различной степени тяжести у детей и подростков: традиционного «трапециевидного» и нового, предусматривающего прием 100% дозы препарата железа (III) на основе ГПК в течение всего периода лечения. Во время исследования оценивали переносимость препарата на основе ГПК и эффективность терапии в ранние (ретикулоцитарная реакция, прирост концентрации Hb) и поздние сроки (нормализация концентрации Hb, СЖ и СФ). Была доказана эффективность терапии у детей и подростков с ЖДА препаратом железа (III) на основе ГПК. После завершения курса лечения нормализация концентрации Hb была достигнута у 96,9% пациентов, СЖ – у 73,4%, СФ – у 60,9% пациентов. Незначительное количество (6,3%) нежелательных явлений (запор в течение 1-го месяца лечения) и 100% приверженность пациентов к лечению позволили заключить, что препарат железа (III) на основе ГПК является оптимальным препаратом для терапии ЖДА у детей и подростков .
Также было доказано преимущество использования 100% дозы препарата железа (III) на основе ГПК в течение всего курса лечения: нормализация концентрации СЖ была зафиксирована у 90,6%, СФ – у 75% детей и подростков. При использовании традиционного «трапециевидного» плана лечения аналогичные показатели составили 56,3 и 46,9% соответственно .
- Ожегов Е.А., Тарасова И.С., Ожегов А.М. и др. Сравнительная эффективность двух терапевтических планов лечения железодефицитной анемии у детей и подростков. Вопросы гематологии/онкологии и иммунопатологии в педиатрии 2005; 4(1): 14–9.
- Ожегов Е.А. Оптимизация лечения железодефицитной анемии у детей и подростков. Автореф. дис. … канд. мед. наук. – М., 2005. – 23 с.
- Тарасова И.С., Чернов В.М. Факторы, определяющие эффективность лечения детей с железодефицитной анемией. Вопросы практической педиатрии 2011; 3(6): 49–52.
источник