Патологическая анатомия
Конспект лекций. Минск: Международный государственный экологический университет имени А. Д. Сахарова, 2009.
Амилоидоз (от лат. amylum — крахмал) — это стромально-сосудистый диспротеиноз, который сопровождается глубоким нарушением белкового обмена и появлением аномального фибриллярного ультраструктурно, но гомогенного светооптически белка с отложением его в межуточной ткани и стенках сосудов.
Этот диспротеиноз был впервые описан венским патологом К.Рокитанским в 1844 под названием “сальная болезнь”, поскольку своеобразные изменения паренхиматозных органов при этой патологии, помимо резкого уплотнения, сопровождались приобретением восковидного, сального вида. Спустя несколько лет, выдающийся немецкий патолог Р.Вирхов обратил внимание на то, что вещество, которое откладывается в органах, подобно крахмалу, под действием йода и серной кислоты окрашивается в синий цвет. Это вещество он назвал амилоидом, а “сальную болезнь” — амилоидозом. Белковая природа амилоида была установлена Кюне в 1865 году.
Амилоид в гистологических препаратах очень похож на гиалин и выглядит в световом микроскопе как бесструктурный, гомогенный, плотный, стекловидный, розового цвета белок.
Термином “амилоид” обозначают разнообразные фибриллярные белки, которые могут депонироваться в соединительной ткани при определенных патологических состояниях. Все типы амилоида имеют следующие физико-химические характеристики:
1) при нанесении йодидов на свежую ткань, содержащую амилоид, она окрашивается в коричневый цвет.
2) в гистологических препаратах амилоид может выглядеть следующим образом:
a) при окраске гематоксилином и эозином имеет гомогенно розовый цвет;
b) в поляризованном свете амилоид, окрашенный конго красным, обладает светло-зеленым двойным лучепреломлением;
с) при окраске метилвиолетом, йод грюн, конго рот амилоид демонстрирует метахромазию, окрашиваясь в кирпично-красный цвет (примечание: когда вещество окрашивается в цвет, который отличается от цвета красителя, то это называется метахромазией);
d) амилоид выявляется иммуногистохимически при помощи антител, специфичных для различных подтипов фибрилл;
3) при электронной микроскопии амилоид выявляется в виде неветвящихся фибрилл толщиной 7.5-10 нм;
4) при рентгендифракционном исследовании установлено, что амилоид представляет собой гофрированную бета-слоистую структуру. Это делает белок очень устойчивым к ферментативному расщеплению и способствует накоплению его в тканях.
Химическая структура белка амилоида весьма разнообразна (таблица 2). Однако, для практики их можно разделить на две группы:
A. Амилоид из иммуноглобулинов: В AL амилоиде белок составлен из фрагментов легких цепей молекул иммуноглобулинов. AL синтезируются неопластическими плазматическими клетками (миелома) и В-лимфоцитами (B-клеточные лимфомы). Легкие цепи амилоида похожи на свободные легкие цепи (белки Бенс-Джонса) или на фрагменты легких цепей, которые синтезируются неопластическими плазматическими клетками или B-лимфоцитами.
B. Амилоид другого происхождения: фибрилы которого составлены из:
1) сывороточного амилоид-ассоциированого белка (MМ — 18,000), который является белком острой фазы во время любого воспалительного процесса и производится печенью;
2) преальбумина
3) других пептидных фрагментов (АА-, АF-, AS-, AD- и др.)
Кроме того, все амилоиды содержат небольшие количества P-белка амилоида и, обычно, гепарансульфат.
Тип белка амилоида
Основной источник
Связанные заболевания
Локализация
Легкие цепи иммуноглобулинов
Первичный амилоидоз
Плазмоклеточная миелома
В-клеточная злокачественная лимфома
Язык, сердце, ЖКТ, печень, селезенка, почки
Сывороточный А протеин (a1-глобулин)
Сывороточный А протеин (a1-глобулин)
Хронические инфекции (туберкулез, лепра, бронхоэктатическая болезнь, хронический остеомиелит)
Болезнь Ходжкина
Воспалительные заболевания мочевого пузыря
Сывороточный А протеин (a1-глобулин)
Семейная средиземноморская лихорадка
Семейный амилоидоз (португальский, шведский и др.)
Периферические нервы, почки
Сердечный амилоидоз
Сенильный амилоидоз
Церебральная амилоидная ангиопатия
Сердце
Сердце, селезенка, поджелудочная железа
Сосуды мозга
Предшественники пептидных гормонов (например, кальцитонина)
Медуллярный рак щитовидной железы
Аденомы из клеток островкового аппарата поджелудочной железы
А4 пептид* или белок-предшественник бета амилоида
Нейрофибриллярные сплетения, бляшки и сосуды мозга (ангиопатия)
* А4 пептид- пептид, определяемый при болезни Альцгеймера (МВ 4000), возникающий из предшественника с МВ 40000, который определяется в крови и цереброспинальной жидкости (кодируется в 21 хромосоме)
Клиническая классификация амилоидоза основана на типе белка и типе ткани, в которой он накапливается, распространенности и возможной причине его возникновения.
1. Первичный системный амилоидоз с преимущественным накоплением амилоида в сердце, желудочно-кишечном тракте, языке, коже и нервах. Эта локализация отмечается при первичном амилоидозе и при новообразованиях из B-лимфоцитов (плазмоклеточная миелома и B-клеточные злокачественные лимфомы). Более чем у 90% пациентов с первичным амилоидозом (в этих случаях накапливается амилоид AL) в качестве основного заболевания обнаруживается плазмоклеточный неопластический процесс с продукцией моноклональных иммуноглобулинов. В вышеперечисленных органах амилоид накапливается и при ревматоидном артрите, однако он имеет не иммуноглобулиновое происхождение (АА амилоид).
2. Вторичный амилоидоз с преимущественным накоплением амилоида в печени, селезенке, почках, кишечнике, надпочечниках. Он возникает при хронических воспалительных заболеваниях, таких как туберкулез, сифилис, лепра, хронические нагноительные процессы (остеомиелит, бронхоэктатическая болезнь, хронический пиелонефрит). Белок амилоида (АА) возникает из a1-глобулина плазмы крови.
B. Ограниченный (местный) амилоидоз: ограниченный амилоидоз может иметь узловую, опухолеподобную форму. Он встречается редко и наблюдается в языке, мочевом пузыре, легких и коже. Накопление амилоида обычно связано с небольшими новообразованиями из плазматических клеток. При болезни Альцгеймера, скопления амилоида особого типа определяются во внеклеточном веществе мозга (в виде бляшек).
C. Амилоид в новообразованиях: амилоид накапливается в строме большого количества эндокринных новообразований, например, медуллярного рака щитовидной железы. При этом тип белка амилоида — AE, который обычно образуется из молекул предшественников определенных пептидных гормонов (например, кальцитонина).
D. Семейный врожденный амилоидоз: семейный амилоидоз был описан в небольшом количестве семей. Тип амилоида — AF или АА. Семейный амилоидоз классифицируется на нейропатический, нефропатический и сердечный, в зависимости от преобладания поражения той или иной системы.
E. Сенильный амилоидоз: небольшие количества амилоида (АS) часто обнаруживаются в сердце, поджелудочной железе и селезенке у пожилых людей. В последних стадиях сахарного диабета амилоидоз возникает в пораженных панкреатических островках. Предполагается, что это особый тип амилоида, составленного из полипептидов, синтезируемых островковыми клетками, которые имеют гормональную активность, воздействуя на утилизацию глюкозы в мышцах.
Амилоид продуцируется специальными клетками, называемыми амилоидобластами.
При различных формах амилоидоза роль амилоидобластов выполняют разные клетки. Предполагают, что мутации и появление клонов амилоидобластов связаны с длительной антигенной стимуляцией. При генерализованных формах амилоидоза — это главным образом макрофаги, плазматические и миеломные клетки (возможно, фибробласты, ретикулярные клетки и эндотелиоциты). При локализованных формах амилоидоза в этой роли выступают кератиноциты и клетки APUD-системы.
—в интиме или адвентиции мелких кровеносных сосудов;
—в интерстициальной ткани по ходу ретикулярных и коллагеновых волокон;
—в базальной мембране эпителиальных структур.
Макро- и микроскопическая характеристика амилоидоза. Внешний вид органов при амилоидозе зависит от степени развития процесса. Если отложения амилоида небольшие, внешний вид органа изменяется мало и амилоидоз диагностируется лишь при микроскопическом исследовании. При выраженном амилоидозе органы увеличиваются в объеме, бледные, с сальным блеском (гепатоспленомегалия, кардиомегалия, утолщение периферических нервов, макроглоссия). Поврежденные ткани имеют более плотную консистенцию и сниженную эластичность по сравнению с нормальными тканями. Поэтому кровеносные сосуды, пораженные амилоидозом, не могут достаточно сокращаться и имеют тенденцию кровоточить при повреждении; вследствие этого диагностическая биопсия может сопровождаться кровотечением и/или кровоизлиянием. Признаками наиболее выраженного поражения ткани являются бледно-серый оттенок и своеобразный восковидный, или сальный, вид ее на разрезе.
В селезенке амилоид может откладываться как изолированно в лимфатических фолликулах, так и равномерно по всей пульпе. В первом случае амилоидно-измененные фолликулы увеличенной и плотной селезенки на разрезе имеют вид полупрозрачных зерен, напоминающих зерна саго (саговая селезенка). Во втором случае селезенка увеличена, плотная, коричнево-красная, гладкая, имеет сальный блеск на разрезе (сальная селезенка). Саговая и сальная селезенка представляют последовательные стадии процесса.
В почках амилоид откладывается в стенках приносящих и выносящих артериол, в капиллярных петлях и мезангии клубочков, в базальных мембранах канальцев и в строме. Почки становятся плотными, большими и «сальными». По мере нарастания процесса клубочки полностью замещаются амилоидом, разрастается соединительная ткань и развивается амилоидное сморщивание почек.
В печени отложение амилоида наблюдается между звездчатыми ретикулоэндотелиоцитами синусоидов, по ходу ретикулярной стромы долек, в стенках сосудов, протоков и в соединительной ткани портальных трактов. По мере накопления амилоида печеночные клетки атрофируются и погибают. При этом печень увеличена, плотная, выглядит «сальной».
В кишечнике амилоид выпадает в строме ворсин слизистой оболочки, а также в стенках сосудов как слизистой оболочки, так и подслизистого слоя. При резко выраженном амилоидозе железистый аппарат кишечника атрофируется.
Амилоидоз надпочечников, как правило, двусторонний, отложение амилоида встречается в корковом веществе по ходу сосудов и капилляров.
В сердце амилоид обнаруживается под эндокардом, в волокнах и сосудах стромы, а также в эпикарде по ходу вен. Отложение амилоида в сердце ведет к резкому его увеличению (амилоидная кардиомегалия). Оно становится очень плотным, миокард приобретает сальный вид.
В скелетных мышцах, как и в миокарде, амилоид выпадает по ходу межмышечной соединительной ткани, в стенках сосудов и в нервах. Периваскулярно и периневрально нередко образуются массивные отложения амилоидного вещества. Мышцы становятся плотными, полупрозрачными.
В легких отложения амилоида появляются сначала в стенках разветвлений легочных артерии и вены, а также в перибронхиальной соединительной ткани. Позже амилоид появляется в межальвеолярных перегородках.
В головном мозге при старческом амилоидозе амилоид находят в сенильных бляшках коры, сосудах и оболочках.
Амилоидоз кожи характеризуется диффузным отложением амилоида в сосочках кожи и ее ретикулярном слое, в стенках сосудов и базальных мембранах сальных и потовых желез, что сопровождается деструкцией эластических волокон, резкой атрофией эпидермиса и придатков кожи.
Амилоидоз поджелудочной железы имеет некоторое своеобразие. Помимо поражения артерий железы, встречается и амилоидоз островков, что наблюдается в глубокой старости.
Исход. Неблагоприятный, практически необратимый.
Функциональное значение определяется степенью развития амилоидоза. Выраженный амилоидоз ведет к дистрофии и атрофии паренхимы и склерозу стромы органов, к их функциональной недостаточности. При выраженном амилоидозе чаще всего наблюдается хроническая почечная, реже — печеночная, сердечная, легочная, надпочечниковая, кишечная (синдром нарушенного всасывания) недостаточность.
источник
Не существует постоянных или отличительных форм распределения отложений амилоида в органах и тканях для какой-либо из описанных категорий. Классическая локализация — почки, печень, селезенка, лимфоузлы, надпочечники, щитовидная железа и многие другие ткани.
Макроскопически пораженные органы часто увеличены, восковидные, имеют плотную консистенцию. Если отложения достаточно велики, то нанесение йода на поверхность среза дает желтое окрашивание, переходящее в сине-фиолетовое после аппликации серной кислоты.
Как указано ранее, гистологическая диагностика амилоидоза основана на особенностях окрашивания амилоида. Чаще всего используют метод окрашивания конго красным, после чего отложения амилоида приобретают розовый или красный цвет при обычном освещении. В поляризованном свете окрашенный конго красным амилоид дает ярко-зеленое двойное лучепреломление.
Такая реакция является общей для всех форм амилоида и обусловлена перекрестной p-складчатой конфигурацией его фибрилл. Подтверждение можно получить с помощью электронной микроскопии. Амилоиды АА, AL и транстиретин различают, используя специфические иммуногистохимические методы. Поскольку типы распределения амилоида в органах при различных клинических формах амилоидоза варьируют, рассмотрим каждый из наиболее часто поражаемых органов отдельно.
а) Почки. Амилоидоз почек является наиболее частой и потенциально наиболее опасной формой заболевания. Почки могут иметь нормальные размеры и цвет или быть увеличенными, а в запущенных случаях иметь сальный вид и сморщиваться вследствие ишемии, вызванной сужением сосудов за счет отложения амилоида в стенках артерий и артериол.
Гистологические исследования выявили, что в основном амилоид откладывается в базальных мембранах клубочков, однако также поражаются интерстициальная перитубулярная ткань, артерии и артериолы. Гломерулярные отложения вначале выглядят как незначительные утолщения мезангиального матрикса, обычно сопровождающиеся неровным расширением базальной мембраны гломерулярных капилляров.
Со временем мезангиальные отложения и отложения вдоль базальной мембраны вызывают сужение капилляров, а также искривление сосудистого пучка клубочка. С развитием гломерулярного амилоидоза просвет капилляров облитерируется и исчезающий клубочек заполняется слившейся массой или широкими переплетенными лентами амилоида.
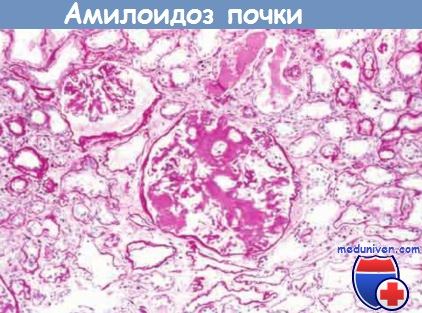
Клубочек почти целиком облитерирован в результате массивного накопления амилоида.
б) Селезенка. Амилоидоз селезенки может не отразиться на ее величине, а может вызвать спленомегалию — от умеренной до выраженной (до 800 г). Существует две формы отложений амилоида в селезенке, причины которых неизвестны. В первом случае отложения в основном ограничиваются фолликулами селезенки с образованием подобных тапиоке гранул, видимых при макроскопическом исследовании. Это так называемая саговая селезенка.
При другой форме амилоид откладывается в стенках синусов селезенки и захватывает соединительнотканную сеть красной пульпы. Слияние ранних отложений приводит к образованию больших, похожих на карту областей амилоидоза. Это так называемая сальная (напоминающая свиное сало) селезенка.
в) Печень. Отложения могут быть незаметными либо приводить к умеренной или выраженной гепатомегалии. Вначале амилоид появляется в пространстве Диссе, а затем неуклонно оттесняет соседние клетки печеночной паренхимы и синусоиды. Со временем происходят деформация и атрофия (в результате сдавливания), гепатоциты исчезают и обширные области печеночной паренхимы замещаются амилоидом. Часто вовлекаются сосуды и амилоид откладывается в перисинусоидальном пространстве. Функция печени обычно сохранена, несмотря на порой обширное вовлечение органа.
г) Сердце. Амилоидоз сердца может иметь любую форму системного амилоидоза. Сердце — главный орган, поражаемый при сенильном системном амилоидозе. Сердце может быть увеличенным и плотным, однако чаще при макроскопическом исследовании отклонения не обнаруживаются. Гистологическими изменениями могут быть локальные скопления амилоида под эндокардом и в миокарде между мышечными волокнами. Распространение этих отложений в миокарде со временем вызывает компрессионную атрофию волокон миокарда.
Если отложения амилоида располагаются субэндокардиально, могут произойти повреждения проводящей системы, отражающиеся у некоторых пациентов на электрокардиограмме.
д) Другие органы. Амилоидоз других органов встречается, как правило, в случае системных заболеваний. Обычными местами его локализации являются надпочечники, щитовидная железа и гипофиз. Может вовлекаться ЖКТ на любом уровне — от полости рта (десны, язык) до ануса. На ранних стадиях отложения амилоида появляются в кровеносных сосудах, однако могут распространяться на прилежащие области подслизистой и субсерозной ткани и мышц.
Узелковые отложения в языке могут вызвать макроглоссию, откуда возник термин опухолеобразующий амилоид языка. Дыхательные пути могут быть вовлечены локально или диффузно, начиная с гортани и заканчивая мельчайшими бронхиолами. Образуются амилоидные бляшки, поражаются также кровеносные сосуды. Амилоидоз периферических и вегетативных нервов служит признаком некоторых амилоидных нейропатий.
Отложения амилоида у пациентов на длительном гемодиализе наиболее выражены в связках запястья, что приводит к сдавливанию срединного нерва (туннельному синдрому запястья). У таких пациентов также могут быть обширные отложения амилоида в суставах.
— Рекомендуем ознакомиться со следующей статьей «Клиника амилоидоза и его проявления»
источник
Почки поражаются в 80-90% случаев вторичного амилоидоза и в приблизительно 30% при первичном амилоидозе. У таких больных обнаруживается выраженная протеинурия или нефротический синдром. Почечные проявления у 50% больных являются первым проявлением заболевания.
В почках амилоид откладывается в стенках сосудов, в капиллярных петлях, что сопровождается утолщением базальной мембраны, в мезангиуме клубочков, в базальных мембранах канальцев и в строме. При электронной микроскопии выявляется специфический фибриллярный белок амилоида (АА-амилоид). Почки становятся плотными, большими и “сальными”. По мере нарастания процесса клубочки и пирамиды полностью замещаются амилоидом, разрастается соединительная ткань и развивается амилоидное сморщивание почек.
Патологическая анатомия. В течении амилоидоза почек различают следующие стадии:
В разные стадии изменения почек различны и отражают динамику процесса.
В латентной стадии внешне почки изменены мало, хотя в пирамидах (сосочках) обнаруживаются склероз и отложение амилоида по ходу прямых сосудов и собирательных трубок. Изменения клубочков состоят в утолщении и двухконтурности мембран их капилляров, просветы которых аневризматически расширены. В интермедиарной зоне и пирамидах строма пропитана белками плазмы.
В протеинурической стадии амилоид появляется не только в пирамидах, но и в клубочках в виде небольших отложений в мезангиуме и отдельных капиллярных петлях, а также в артериолах. Склероз и амилоидоз пирамид и пограничного слоя резко выражены и ведут к атрофии многих глубоко расположенных нефронов, редукции путей юкстамедуллярного кровотока и лимфотока в мозговом веществе почек. Эпителий канальцев главных отделов в состоянии гиалиново-капельной или гидропической дистрофии; в просвете канальцев обнаруживаются цилиндры. Почки увеличены, плотны, поверхность их бледно-серая или желто-серая. На разрезе корковый слой широкий, матовый, мозговое вещество серо-розовое, “сального” вида, нередко цианотичное (большая сальная почка).
В нефротической стадии количество амилоида в почках увеличивается. Он обнаруживается во многих капиллярных петлях большинства клубочков, в артериолах и артериях, по ходу собственной мембраны канальцев, однако выраженный склероз коркового вещества отсутствует. Канальцы расширены, заполнены цилиндрами. В эпителии канальцев в строме много липидов (холестерина). Почки имеют вид, типичный для так называемого амилоидно-липоидного нефроза. Они становятся большими, плотными, восковидными – большая белая амилоидная почка.
В азотемической (уремической) стадии в связи с нарастающим амилоидозом и склерозом наблюдаются гибель большинства нефронов, их атрофия, замещение соединительной тканью. Почки обычных размеров или несколько уменьшены. Они очень плотные, со множеством рубцовых западений на поверхности (амилоидно-сморщенные почки) В этой стадии нередко развивается гипертрофия сердца, особенно левого желудочка, что связано с развитием нефрогенной артериальной гипертензии.
Клинически, отложение амилоида проявляется повышением сосудистой проницаемости гломерулярных капилляров, что приводит к развитию нефротического синдрома.
Амилоидоз довольно быстро прогрессирует. Хроническая почечная недостаточность является основной причиной смерти больных амилоидозом.
Тубулопатии представляют собой заболевания почек с первичным ведущим поражением канальцев, которое сопровождается нарушением их концентрационной, реабсорбционной и секреторной функции. Различают приобретенные и наследственные тубулопатии (обусловленные различными формами ферментопатий). К приобретенным тубулопатиям относят: острая почечная недостаточность (ОПН) и хронические тубулопатии (миеломная и подагрическая почка).
Морфологическим субстратом ОПН является острый некротический нефроз (ОНН); у больных при этом развивается резкая олигурия (менее 100 мл мочи в сутки). Основными причинами ОПН являются ишемия и токсическое поражение.
Ишемический ОНН может развиться при различных состояниях, например, травмах, ожогах, инфекциях, при которых развивается шоковое состояние и коллапс. Выраженная гипотензия является причиной критического понижения кровотока в почках, особенно в кортикальных клубочках в связи с особенностями их кровоснабжения. Почки выглядят бледными и отечными. При гистологическом исследовании определяется повреждение эпителиальных клеток канальцев практически по всей их длине, часто развивается вакуольная дистрофия, разрыв канальцевой базальной мембраны (тубулорексис). Интерстициум становиться отечным. Часто образуются цилиндры в дистальных канальцах и собирательных трубочках; цилиндры состоят из клеточного детрита и белков. При краш-синдроме в цилиндрах обнаруживается миоглобин, а при нарушении правил переливания крови – гемоглобин.
Различают две стадии развития заболевания. После стадии анурии, которая развивается из-за перекрытия просвета канальцев набухшими и некротизированными клетками, наступает полиурическая стадия, связанная с нарушением концентрационной способности почек. В олигурическую стадию большой риск для жизни больного представляет развивающаяся гиперкалиемия, которая может привести к аритмии сердца. Однако в начале полиурической стадии может развиться, наоборот, гипокалиемия.
Исход. Если состояние будет вовремя диагностировано и будет проведена адекватная инфузионная терапия и гемодиализ больной может полностью выздороветь. Эпителий канальцев регенерирует, если сохранена базальная мембрана. При неблагоприятном развитии процесса больные умирают от острой почечной недостаточности.
Обструктивная уропатия (гидронефроз)является частой причиной интерстициального нефрита. Причинами обструкции мочевыводящих путей могут быть:
· врожденные аномалии (мочеточниково-лоханочный стеноз, пузырно-мочеточниковый рефлюкс);
· опухоли (рак мочевого пузыря и предстательной железы);
· гиперпластические состояния (доброкачественная гиперплазия предстательной железы);
Клинические симптомы и прогноз зависят от уровня обструкции. Так, например, камень или фрагмент оторвавшегося сосочка может стать причиной почечной колики, а рак мочевого пузыря или доброкачественная гиперплазия предстательной железы проявиться пузырными симптомами. Острая обструкция нижних отделов мочевого тракта приведут к анурии и болям.
Частичная или односторонняя обструкция может протекать скрытно, иногда бессимптомно в течении нескольких лет. Проявляется она полиурией и никтурией. На ранних стадиях определяется снижение концентрационной функции почек, канальцевый ацидоз и отложение большого количества солей. Часто развивается гипертензия.
Патогенез. Лоханка и чашечки становятся расширенными в результате повышения давления; при острой обструкции расширение выражено не сильно. Перистальтическая активность мочеточников повышается, что приводит к повышению внутрилоханочного давления, которое передается на паренхиму. Первоначально образующийся ультрафильтрат реадсорбируется через лимфатические и кровеносные сосуды. При продолжающемся быстром повышении давления происходит снижение кровотока в клубочках и мозговом слое, что приводит к нарушению фильтрации. В результате длительной обструкции развивается сильное расширение лоханки с истончением паренхимы (гидронефроз).
Пиелонефрит – это инфекционное заболевание, при котором инфекция может попадать в почки гематогенным (нисходящим) или уриногенным (восходящим) путем. В результате обильного кровоснабжения почек они часто поражаются при различных состояниях, сопровождаемых септицемией. Наиболее часто возбудителями являются бактерии. Инфекции мочевых путей встречаются достаточно часто, занимая второе место после инфекций дыхательных путей. Однако не при всех инфекциях мочевыводящих путей может развиться пиелонефрит, для его развития необходим пузырно-мочеточниковый рефлюкс.
Распространенность пиелонефрита коррелирует с частотой различных обструкций мочевых путей. В детстве чаще болеют мальчики, т.к. у них чаще встречаются различные аномалии строения мочевыводящих путей. С пубертатного периода до средних лет чаще болеют женщины, что связано с более частыми травмами мочеиспускательного канала и беременностью. После 40 лет чаще болеют мужчины из-за развития различных заболеваний предстательной железы. Также предрасполагающими факторами являются инструментальные обследования и манипуляции (например, катетеризация и цистоскопия) и сахарный диабет.
Острый пиелонефрит развивается при инфицировании пиогенными микроорганизмами. Начинается заболевание с высокой лихорадки, озноба и боли в пояснице. Дизурические проявления говорят о наличии также инфекции нижних отделов мочевыводящей системы. В моче определяется легкая протеинурия (до 1 г/л), лейкоцитоз, лейкоцитарные (белые) цилиндры и бактерии. Диагноз подтверждают бактериологическим исследованием. Наличие более 100000 микроорганизмов в 1 мл мочи является диагностическим. Острый пиелонефрит встречается во всех возрастах, однако, наиболее часто после начала половой жизни и во время беременности.
Этиология и патогенез. Инфицирование почек может происходить гематогенным (нисходящим) или уриногенным (восходящим) путем. Гематогенный занос инфекции встречается довольно редко. Гематогенный занос может происходить при инфекционном эндокардите или бактериемии из других источников; спектр микроорганизмов широкий, включающий бактерии, грибы и вирусы.
Чаще пиелонефрит развивается в результате восходящего распространения инфекции. Основными способствующими факторами являются:
· рефлюкс с нижних отделов мочевыводящей системы;
· стаз мочи любой этиологии;
· пузырно-мочеточниковый рефлюкс. У 50% детей и подростков с пиелонефритом обнаруживается это состояние, которое является наследственным в результате нарушения вхождения мочеточника в мочевой пузырь.
· катетеризация мочевого пузыря.
Наиболее частые возбудители – Escherichia coli, Proteus и Enterobacter. При возникновении заболевания после катетеризации спектр микроорганизмов может быть достаточно широким: Klebsiella, Proteus, Enterococcus faecalis, Pseudomonas aeruginosa и др.
Высокая заболеваемость мочевыми инфекциями при беременности связана с повышенным содержанием в крови прогестерона, который понижает сократительную активность гладкой мускулатуры, что приводит к стазу мочи.
Морфология. Острый пиелонефрит может быть как двух-, так и односторонним. Почки увеличены в размерах, в коре обнаруживаются зоны нагноения (абсцессы) с желтыми радиальными полосами, пресекающими мозговое вещество. При гематогенном пиелонефрите небольшие абсцессы располагаются хаотично, преимущественно в верхнем, а при уриногенном заносе инфекции – в нижнем полюсе почки. Также может наблюдаться воспаление чашечек и лоханок, что сопровождается накоплением гноя в просвете лоханок.
При гистологическом исследовании обнаруживаются полиморфноядерные лейкоциты в просвете канальцев, отек и воспаление интерстиция. При заживлении развивается фиброз интерстициума и в воспалительном инфильтрате начинают преобладать лимфоциты и плазмоциты.
Осложнения. При остром пиелонефрите могут развиться следующие осложнения:
Некроз сосочков почки. В результате воспаления может нарушаться кровоснабжение мозгового слоя, что приводит к инфаркту сосочков. Некротизированные сосочки отторгаются в просвет лоханки. Данное осложнение наиболее часто встречается у диабетиков.
Пионефроз.Он развивается при высокой обструкции мочеточников (на границе с почкой). При этом жидкость в лоханке и чашечках нагнаивается. Почки становятся увеличенными, заполненными гноем.
Околопочечный абсцесс.При проникновении инфекции через капсулу почки происходит нагноение околопочечной клетчатки.
Хронический пиелонефрит является причиной хронической почечной недостаточность у 15% пациентов.
Различают хронический обструктивный пиелонефрит и хронический пиелонефрит, связанный с пузырно-мочеточниковым рефлюксом.
Хронический обструктивный пиелонефрит встречается довольно часто и наблюдается во всех возрастных группах. Обструкция может быть механической (например, камнями, при гиперплазии предстательной железы, опухолях, врожденных аномалиях, забрюшинном фиброзе) или обусловлена парезом стенки мочевого пузыря (нейропатический мочевой пузырь). У 50% больных в анамнезе имел место острый пиелонефрит.
Морфология.Поражение почек обычно асимметричное, определяется различной степени выраженности сморщивание почек в основном на полюсах. Часто наблюдается деформация чашечно-лоханочной системы. Хронический пиелонефрит отличается от хронического гломерулонефрита асимметричностью поражения и наличием глубоких рубцов в коре. В области сморщивания наблюдается деформация и расширение чашечек.
Микроскопически определяется интерстициальный фиброз с атрофией и расширение трубочек, в которых обнаруживаются эозинофильные цилиндры, что приводит к появлению своеобразной гистологической картины, напоминающей строение щитовидной железы, поэтому такие изменения называются “тиреоидизацией” почек.
При микроскопии обнаруживаются очаги воспаления и фиброза в интерстиции. Воспалительный экссудат в основном состоит из лимфоцитов и плазмоцитов с небольшой примесью нейтрофилов. Перигломерулярный склероз прогрессирует с развитием глобального склероза нефрона. Может наблюдаться гипертрофия и дилатация выживших канальцев (этот процесс называется тиреодизацией, т.к. на первый взгляд многочисленные плотно расположенные расширенные канальцы напоминают фолликулы щитовидной железы. При иммунофлюоресценции и электронной микроскопии не обнаруживаются иммунные комплексы в клубочках.
При преобладании в экссудате макрофагов, имеющих пенистую цитоплазму, говорят о ксантогранулематозном пиелонефрите. Ксантогранулематозный пиелонефрит – это редкое состояние, которое развивается у больных с хроническим пиелонефритом, вызванном Proteus и E. coli. При ксантогранулематозном воспалении происходит увеличение почек и образование в лоханке больших коралловидных камней. Клиническое значение данного состояния состоит в том, что его можно спутать с раком почки. Часто воспалительный процесс распространяется на окружающие органы (например, кишечник, кожу спины, диафрагму и плевру). Иногда могут формироваться фистулы между лоханкой почки и этими органами.
ХРОНИЧЕСКАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ
Хроническая почечная недостаточность, характеризуемая повышением концентрации в крови азотистых шлаков (азотемическая уремия) и другими признаками, такими как анемия, тошнота, рвота, желудочно-кишечные кровотечения и кожный зуд; часто наблюдаются полиурия и никтурия. Пациентов с ХПН делят на две группы: у одних установлено почечное заболевания, которое привело к деструкции паренхимы, у других ХПН развивается de novo на фоне заболевания, острая фаза которого не проявлялась клинически.
Клинические проявления ХПН развиваются в результате нарушения нормальной функции почек. Накопление азотистых шлаков происходит в результате снижение фильтрации крови в почках. Анемия развивается в результате снижения продукции почками эритропоэтинов под воздействием уремических токсинов, истощения костного мозга, а также из-за гематурии и гемолиза. С помощью генной инженерии удалось воссоздать структуру эритропоэтинов и синтезировать их вне организма, что позволило корригировать данное проявление ХПН. У больных часто развивается остеодистрофия, очень напоминающая поражение костей при рахите, которая развивается в результате нарушения метаболизма витамина D в пораженных почках, что приводит к снижению всасывания кальция в кишечнике и является причиной стимуляции паращитовидных желез. Процесс осложняется также задержкой фосфатов в организме. Это проявление можно лечить активным метаболитом витамина D1-альфа-гидроксихолекальциферолом. По мере фиброзирования почки продукция ренина повышается, что приводит к развитию гипертензии.
При вскрытии трупа умершего от уремии ощущается запах мочи. Кожа серо-землистой окраски в результате накопления урохрома. Иногда, особенно на лице, она бывает как бы припудрена беловатым порошком (хлориды, кристаллы мочевины и мочевой кислоты). Иногда обнаруживаются очаговые кровоизлияния и петехиальная сыпь как выражение геморрагического диатеза. Часто обнаруживается уремический ларингит, трахеит, пневмония, которые имеют чаще фибринозно-некротический или фибринозно-геморрагический характер. Также можно встретить полисерозит, фарингит, гастрит, энтероколит катарального, фибринозного или фибринозно-геморрагического характера. Причиной их развития служит заместительное выделение серозными оболочками и слизистыми этих органов мочевины, которая, превращаясь в аммиак, оказывает раздражающее действие и вызывает воспалительную реакцию. В печени возникает жировая дистрофия. Селезенка увеличена, напоминает септическую.
Очень часто обнаруживаются серозный, серозно-фибринозный или фибринозный перикардит, уремический миокардит, реже – бородавчатый эндокардит. Возможно развитие уремического плеврита и перитонита.
Головной мозг при уремии бледный и отечный, иногда появляются очаги размягчения и кровоизлияния.
Не нашли то, что искали? Воспользуйтесь поиском:
источник
Амилоидоз почек одно из проявлений общего амилоидоза) -, в основе лежат изменения, приводящие к внеклеточному выпадению в ткани амилоида, вызывающего в конечном итоге нарушение функций органа.
Причины: нефропатический амилоидоз находят при вторичном амилоидозе как осложнение туберкулеза, бронхоэктазов, хронического гнойного осткомиелита. Амилоидоз почек — это чаще всего «вторая болезнь».
Патогенез: обычно наблюдается длительная компенсированная клиническая латентная стадия- в этот период отсутствие протеинурии достигается напряженной работой систем резорбции почки. Начавшись в пирамидах амилоидоз постепенно охватывает и корковое вещ, клубочки, сосуды. По мере прогрессирования амилоидоза клубочков появляются гипопротеинемия, гиперхолестеринимия и отеки- возникает нефротическая стадия. Резко снижается клубочковая фильтрация.В финале развивается амилоидное сморщивание почек.
-латентная— в пирамидах обнаруживаются склероз и амилоидоз, клубочки утолщаются, цитоплазма эпителия канальцев и просветы канальцев забиты белковыми гранулами, в пирамидах зона пропитана белками плазмы.
-протеинурическая— амилоид появляется и в пирамиде и в клубочках в виде отложений в мезангии, и артериолах. Склероз и амилоидоз ведут к выключению и атрофии глубоко расположенных нефронов. Эпителий канальцев главных отделов в состоянии гиалиново-капельной дистрофии. Почки увеличены, плотны, поверхность их бледно-серая или желто-серая.
— нефротическая — количество амилоида в почках увеличивается. . В пирамидах склероз и амилоидоз имеют диффузный характер. Канальцы расширены, забиты цилиндрами. В эпителии канальцев в строме много липидов . Почки становятся « большая белая амилоидная почка».
-азотемическая (уремическая) — наблюдается гибель нефронов. Почки уменьшены, плотные, рубцовые западения на поверхности. В этой стадии нередко развивается гипертрофия сердца.
Осложнением амилоидоза почек обычно является какая-либо инфекция (пневмония, рожа, паротит), Возможны осложнения в связи с развивающееся артериальной гипертензией (инфаркты, кровоизлияния, сердечная недостаточность).
Смерть в следствие хронической почечной недостаточности, уремия в финальной стадии заболевания.
97) Пиелонефрит и инфекции мочевыводящих путей. Определение, классификация, этиология, предрасполагающие факторы, пути распространения, патогенез, исходы, осложнения.
Пиелонефрит — инфекционное заболевание, при котором в процесс вовлекается лоханка, чашечки, вещество почки с преимущественным поражением интерстиция.
Возбудители различные микробы –кишечная палочка, энтерококк, стафилококк, стркптококк . Инфекия попадает в почки либо гематогенным путем либо восходящим — из уретры, мочевого пузыря, мочеточников.
Распространению инфекта при восходящем пути способствует везикоуретеральный рефлюкс. Возможен и лимфогенный занос инфекции в почки- источником инфекции являются толстая кишка и половые органы.
Предрасполагают факторы к развитию : обструкция мочевых путей (камни, стриктуры, сдавление опухолью и т.д.); операции на почках и мочевыводящих путях; катетеризация мочевых путей; заболевания половых органов.
Острый пиелонефрит.- наблюдается полнокровие, лейкоцитарная инфильтрация лоханки и чашечек, очаги некроза слиз обол, межуточная ткань всех слоев почки отечна, канальцы в состоянии дистрофии, просветы забиты цилиндрами, почки увеличены, нкань набухшая, полости лоханок и чашечек расширены заполнены мутной мочой или гноем.
Хронический- характерна пестрота изменений, склероз лоханок и чашечек, полироз слиз обол, лейкоцитарная инфильтрация, в ткани почки выражено хроническое межуточное воспаление с разрастанием соед. ткани, инкапсуляцией абсцессов, канальцы растянуты, просветы заполнены густым коллоидоподобным содержимым, в финале развивается пиелонефротическая сморщенная почка- рубцовое сморщивание, склероз лоханок, плотные спайки между тканью почки и капсулой.
Осложнения: при остром пиелонефрите – образование карбункула почки, пиелонефроз, перинефрит, пипиллонекроз. При хроническом- развитие нефрогенной гипертонии и артериолосклероза во второй почке, и хроническая почечная недостаточность.
Исход- острого пиелонефрита – выздоровление но врезультате осложнений может возникнуть смерть. Хронический- заканчивается уремией
источник
АМИЛОИДОЗ ПОЧЕК — одно из проявлений амилоидоза внутренних органов – системного заболевания, характеризующегося отложением в различных органах патологического белковоподобного вещества – амилоида.
1. Идиопатический (первичный) амилоидоз
2. Наследственный (генетический) амилоидоз
3. Приобретенный (вторичный) амилоидоз
а) как осложнение хронических инфекций, коллагенозов, опухолей
б) параамилоидоз (при парапротеинемических гемобластозах)
5. Локальный опухолевый амилоидоз
Патогенез: В настоящее время существует три теории 1 – мутационная теория – амилоид является продуктом особого клона клеток – амилоидобластов макрофагальной системы; 2 – иммунологическая теория – амилоидоз есть результат реакции антиген – антитело, где антиген – продукт распада тканей или чужеродный белок, а амилоидоз – белковый преципитат, откладывающийся в местах фиксации антител; 3 – теория диспротеиноза рассматривает амилоид как продукт извращенного белкового обмена.
Амилоидные массы откладываются в стенках кровеносных и лимфатических сосудов, в результате чего нарушается метаболизм в расположенных вблизи клетках.
Морфология: Почки при амилоидозе увеличены, плотны, серого цвета. При гистологическом исследовании под аргирофильной мембраной артерий и капилляров клубочков видны глыбки амилоида. В эпителии канальцев обнаруживаются значительные дистрофические изменения.
Клиника: Больные предъявляют жалобы на общую слабость, отсутствие аппетита, отеки, часто впервые возникающие на нижних конечностях. Могут быть жалобы на боли в пояснице. Гипертензивный синдром чаще возникает в конечной стадии болезни, как проявление диффузного поражения почек, но может быть и в начале ее. Длительное существование артериальной гипертонии приводит к поражению левого сердца с развитием сердечной недостаточности.
Диагностика: Важным диагностическим признаком является стойкая и выраженная протеинурия. За сутки выделяется от 2 до 20 г белка, преимущественно альбумины. Также в моче обнаруживаются гиалиновые, реже зернистые, цилиндры, микрогематурия. Потеря белка приводит к гипопротеинемии и диспротеинемии. Обычно имеет место увеличение содержания альфа-2 и гамма глобулинов сыворотки. Одновременно с диспротеинемией отмечается ускорение СОЭ и измененные осадочные пробы (тимоловая). Частым признаком амилоидоза является гиперлипидемия. Диагностическое значение имеет проба с метиленовым синим (1 мл 1% р-ра подкожно). После введения раствора каждый час берут порцию мочи в течение 5 – 6 часов. В норме все порции окрашены в зеленый цвет. При амилоидозе изменение цвета мочи не происходит. Наиболее достоверным методом диагностики является пункционная биопсия почек.
Лечение. 1. Лечение основного заболевания; 2. Диета с повышенным содержанием белка, ограничением поваренной соли; 3. Витаминотерапия; 4. Симптоматическая терапия (мочегонные, гипотензивные, коррекция ацидоза).
В основе почечно-каменной болезни лежит образование конкрементов разного химического состава в почечных лоханках.
Этиология: — инфекции мочевых путей
— нарушение минерального обмена ( гиперпаратиреоз )
Патогенез: 1. Кристаллизационная теория – камни в почках образуются вследствие кристаллизации мочи; 2. Теория матриц – камни образуются в результате осаждения солей на белковую основу
По химическому составу камни бывают неорганическими (ураты, фосфаты, оксалаты, карбонаты, цистеиновые и др.) и органические (бактериальные, фибриновые, амилоидные).
Клиника: В межприступном периоде больные жалоб не предъявляют. Симптом Пастернацкого, как правило, положительный. Приступ почечной колики начинается внезапно: интенсивные боли локализуются в поясничной области, иррадиируют вниз, по ходу мочеточников. Приступ сопровождается частым болезненным мочеиспусканием и различными рефлекторными синдромами (тошнота, рвота, метеоризм), повышением температуры. При объективном исследовании определяются болезненность при пальпации почек и по ходу мочеточников, положительный симптом Пастернацкого.
Дополнительные методы исследования: В межприступный период при исследовании мочи изредка выявляется непостоянная гематурия, часто обнаруживаются кристаллы солей, лейкоцитурия. Во время приступа в моче определяются неизмененные эритроциты, белок.
Ультразвуковое исследование позволяет выявлять конкременты любого химического состава размером более 3-4 мм. Также можно определить размеры почек, деформации почечных чашек и лоханок.
Рентгенологическое исследование: По экскреторным урограммам можно судить о локализации, величине, форме и количестве камней. В 10% случаев камни почек рентгенонегативные.
Осложнения: — пиелит, пиелонефрит
Лечение: во время приступа — тепло
— спазмолитики (но-шпа, папаверин, баралгин)
— новокаиновая блокада поясничной области
План самостоятельной работы:
На курацию представить больных с хроническим гломерулонефритом, мочекаменной болезнью; продемонстрировать больного с амилоидозом. Провести опрос больного, уточнив жалобы при поступлении (головные боли, их локализация, время их появления, повышение артериального давления, наличие одышки). Обратить внимание на наличие диспептических расстройств,кожного зуда, изменение диуреза (полиурия, никтурия). Собрать анамнез болезни, обратив внимание на наличие в прошлом симптомов заболевания почек, время появления признаков почечной недостаточности. Провести объективное обследование больного ,обратив особое вниманиена выявление отеков, признаков поражения сердечно – сосудистой системы, повышение артериального давления, пальпацию почек, симптом Пастернацкого. Обобщить полученные данные. Ознакомиться с данными дополнительных методов исследований больного. Сформулировать окончательный диагноз, в котором отразить функциональное состояние почек.
Пример: Хронический гломерулонефрит, гипертонический (нефротический, смешанный и др.) вариант, стадия обострения (ремиссии), хроническая почечная недостаточность I стадии.
Контрольные задания:
Набор тестов и клинических задач по теме занятия
Оснащение, средства наглядности:
Набор анализов мочи, набор ренгенограмм при патологии почек, коллекция камней при МКБ.
1. Гребенев А.Л. Пропедевтика внутренних болезней. Москва., Медицина, 2002.
2. Яворский О.Г., Ющик Л.В. Пропедевтика внутренних болезней в вопросах и ответах. Киев, Здоровье, 2003.
Дополнительная:
1. Основы нефрологии. Под ред. Е.М.Тареева, т.I, Москва, Медицина, 1972, с. 350-417.
Тема: Итоговое занятие по заболеваниям органов
Учебное время: 2 часа.
Цель занятия: проверить уровень усвоения студентами основных заболеваний органов пищеварения и почек.
Вопросы для теоретической подготовки:
Содержание занятия.
Провести тестовый контроль (письменный и/или компьютерный). Решить ситуационные задачи по теме итогового занятия. Провести обследование больного по схеме истории болезни. Обосновать предположительный диагноз по данным анамнеза и объективного обследования. Согласно предполагаемого диагноза получить у преподавателя данные дополнительных исследований, обосновать клинический диагноз. Наметить план лечения. Результаты курации больного оформить в виде фрагмента истории болезни и сдать преподавателю.
План самостоятельной работы.
Студенты работают в компьютерном классе, а также в учебной комнате и палате. Для курации студенты распределяются по 2 человека к одному больному с изучаемой патологией, собирают анамнез, проводят объективное обследование. Результаты курации сообщают преподавателю, высказывают предположительный диагноз, обсуждают лабораторные и инструментальные данные, формулируют клинический диагноз, определяют план лечения.
Контрольные задания.
См. план самостоятельной работы.
Оснащения, средства наглядности:
Тесты, Rhg граммы при патологии желудка, почек, скенограммы печени, коллекция камней при желчекаменной и мочекаменной болезни.
Тема: Анемии
Учебное время: — 2 часа.
Цель занятия: знать: этиологию, патогенез, клиническую картину, диагностику и лечение анемий; уметь: собрать анамнез, провести внешний осмотр, аускультацию сердца и легких, пальпацию живота.
Вопросы для теоретической подготовки:
Определение анемий. Классификация. Понятие о синдром анемии. Клиника и картина крови при железодефицитной, В12-фолиеводефицитной, гемолитической (врожденной и приобретенной) и гипопластической анемии.
Анемия (малокровие) – патологическое состояние, характеризующееся параллельным уменьшением против физиологической нормы количества гемоглобина и эритроцитов, либо уменьшение в превалирующей степени количества одного из них в определенном объеме крови.
Классификация анемий (по происхождению):
1. Постгеморрагические (острые и хронические).
2. Гемолитические (врожденные и приобретенные)
3. Вследствие нарушения кровообразования:
Синдром анемии определяется гипоксией мозга и компенсаторными механизмами со стороны сердечно-сосудистой и дыхательной систем.
Постгеморрагическая анемия может быть острая и хроническая.
При острой кровопотери наблюдается бледность, падение артериального давления, обморок. Компенсаторные механизмы следующие: 1) сужение сосудистого русла; 2) выброс крови из депо; 3) приток тканевой жидкости; 4) увеличение скорости кровотока и минутного объема, что клинически проявляется тахикардией, падением артериального давления, сухостью языка.
Лабораторные данные: анемия нормоцитарная, нормохромная, гиперрегенераторная. Тромбопения в первые часы острой кровопотери сменяется к концу суток тромбоцитозом (до 1 млн. тромбоцитов в 1 мм 3 ). Повышается свертываемость крови. Отмечается лейкоцитоз до 20 тыс. в 1 мм 3 .
Хроническая постгеморрагическая анемия является железодефицитной. Клиника определяется анемией (слабость, головокружение, шум в ушах, потемнение в глазах при быстром переходе из горизонтального положения в вертикальное, тахикардия, одышка при физической нагрузке) и симптомами дефицита железа (ломкость ногтей, волос).
В анализе крови: анемия гипохромная, нормоцитарная, есть анизоцитоз и пойкилоцитоз. Умеренный ретикулоцитоз и тромбоцитоз. Лейкопения за счет гранулоцитопении, относительный лимфоцитоз.
Врожденная ГА носит семейнонаследственный характер. Характеризуется внутриклеточным гемолизом в органах ретикулоэндотелиальной системы (печени, селезенке, костном мозге, лимфоузлах) и увеличением некоторых из них (селезенки, печени).
Клиника. Первые симптомы заболевания появляются в детском возрасте. О таких детях говорят, что они больше желтушны, чем больны. Жалобы могут быть обусловлены анемией, а также давлением увеличенных печени и селезенки. Течение заболевания волнообразное, ремиссии сменяются гемолитическими кризами с ознобом, повышением температуры, болями в костях, увеличением желтухи, селезенки.
Анализ крови: анемия нормохромная, гиперрегенераторная, микросфероцитарная (или серповидноклеточная, или другие аномальные формы эритроцитов). Осмотическая резистентность эритроцитов снижена (норма – 0,34-0,48). Повышен свободный билирубин.
Приобретенная ГА характеризуется внутрисосудистым гемолизом. По течению чаще острая. Причина ее – инфекции, интоксикации, медикаменты, переливание несовместимой крови. Клиника подобна гемолитическому кризу при врожденной ГА. Но увеличение печени и селезенки не характерно.
Анализ крови: анемия нормохромная, гиперрегенераторная. Лейкоцитоз. Повышен непрямой билирубин. Есть гемоглобинурия, возможная острая почечная недостаточность.
Анемия в связи с нарушением кровообразования.
Железодефицитные анемии различают врожденные и приобретенные. Врожденные или ахрестические обусловлены нарушением синтеза гемоглобина, носят семейнонаследственный характер, характеризуются анемией гипохромной, резистентной к заместительной терапии препаратами железа. Количество эритроцитов обычно нормальное, а количество гемоглобина низкое, низкий цветной показатель (0,5-0,6). Как и врожденная гемолитическая анемия может наследоваться.
Приобретенная железодефицитная анемия развивается при нарушении всасывания железа в желудочно-кишечном тракте, недостаточном поступлении железа с пищей, повышенной потребности организма в железе (в пубертатном периоде, во время беременности, лактации). Железодефицитная анемия со своеобразным окрашиванием кожи в зеленоватый цвет получила название хлороз. Различают ранний хлороз (в пубертатном периоде) и поздний (в климактерическом периоде). В основе хлороза лежит несоответствие между поступлением железа и потребностью в нем. Клиника определяется симптомами анемии и дефицита железа.
Анализ крови: анемия гипохромная, гипорегенераторная, есть анизоцитоз пойкилоцитоз. Количество лейкоцитов и тромбоцитов обычно не изменено, в тяжелых случаях – лейкопения и тромбоцитопения.
В12-фолиеводефицитная анемия характеризуется мегалобластическим (эмбриональным) кроветворением.
1. Отсутствие фактора Кастля (при атрофическом гастрите, субтотальной резекции желудка);
2. Нарушение внешнесекреторной функции поджелудочной железы;
3. Конкурентное поглощение В12 в кишечнике (инвазия широким лентецом, синдром “слепой” кишки при резекции кишечника);
4. Отсутствие рецепторов для присоединения фактора Кастля (хронические энтериты, глутеновая энтеропатия и др.);
6. Снижение транскобаламина II, что ведет к нарушению транспорта В12 в костный мозг.
Дефицит фолиевой кислоты может развиваться при: 1) назначении противосудорожных препаратов; 2) хроническом алкоголизме (особенно у женщин); 3) строгом вегетарианстве; 4) применении цитостатиков; 5) в период беременности при отсутствии овощей и фруктов.
Анализ крови при В12-фолиеводефицитной анемии: гиперхромная, мегалоцитарная, гипорегенераторная. Отмечается также гиперсегментация нейтрофилов, относительная лимфопения, моноцитопения. Анэозинофилия. Содержание билирубина обычно повышено, как и выделение стеркобилина и уробилина.
Болезнь Аддисона-Бирмена или “пернициозная анемия“ характеризуется 1) мегалобластическим кроветворением, а также 2) атрофическим гастритом и гунтеровским глосситом 3) фуникулярным миелозом.
Апластическая (гипопластическая анемия). Полиэтиологический синдром. Характеризуется снижением эритромиелопоэза: при норме миелокариоцитов 40-150 тыс. в 1 мм 3 , из которых эритропоэз составляет 25%, в патологии снижается как количество миелокариоцитов, так и % эритропэза. Это анемия нормохромная, гипорегенераторная (арегенераторная!), обычно снижено количество лекоцитов за счет нейтрофилов, отмечается тромбопения.
План обследования при хронических анемиях.
Обследование проводится до лечения!
1. Общий анализ крови с ретикулоцитами и тромбоцитами.
2. Определение сывороточного железа (общего, свободного и связанного), ферритина.
4. Исследование мочи (белок Бенс-Джонса!).
5. Исследование миелограммы.
6. Трепанобиопсия по показаниям.
Этиологическое, патогенетическое. Должно выполняться под контролем врача-гематолога. В лечении анемий роль трансфузий эритромассы практически сведена к нулю и показана может быть только при гипопластической (апластической) анемии.
При лечении железодефицитной анемии восстановление красной крови наблюдается к концу второго месяца, при В12-фолиеводефицитной анемии – ретикулоцитарный криз через 4-7 дней, нормализация крови через 4-6 недель.
План самостоятельной работы:
Собрать жалобы с подробной их детализацией у курируемых больных, анамнез болезни и жизни. Провести объективное исследование. Проанализировать данные дополнительных методов исследования. Сформулировать диагноз и наметить план лечения.
Контрольные задания:
Написать анализ крови при анемиях: острой постгеморрагической, хронической постгеморрагической, железодефицитной, В12-фолиеводефицитной, гемолитической врожденной и приобретенной.
Оснащение, средства наглядности:
Микроскопы. Мазки крови при анемиях. Тесты и ситуационные задачи для выявления конечного уровня знаний.
1. Пропедевтика внутренних болезней (под ред. А.Л. Гребенева): Учебник — 5-е изд. — М. Медицина, 2002.
Дополнительная
1. П.А. Воробьев. Анемический синдром. М.: Медицина, 2001. – 165 с.
Тема: Геморрагические синдромы.
Учебное время: 2 часа.
Цель занятия: студент должен знать: этиологию, классификацию и основные клинические проявления геморрагических синдромов, принципы диагностики; уметь: самостоятельно оценивать данные лабораторных и инструментальных методов исследования больных с геморрагическими синдромами; быть ознакомленным: с осложнениями и принципами лечения геморрагических синдромов.
Вопросы для теоретической подготовки: Понятие о геморрагических диатезах. Классификация. Клиника и лабораторная диагностика болезни Верльгофа, гемофилии, геморрагического васкулита. Основы терапевтической тактики при геморрагических диатезах.
Под кровоточивостью (геморрагическим диатезом) в широком смысле слова следует понимать склонность к повторным кровоизлияниям или кровотечениям, наступающим самопроизвольно или под влиянием условий, которые при физиологическом состоянии организма кровоизлияний и кровотечений не вызывают.
По патогенетическому принципу они чрезвычайно разнообразны, потому условно могут быть представлены следующими группами:
1. Геморрагические синдромы (ГС), в основе которых лежит изменение количества и качества тромбоцитов: болезнь Верльгофа, симптоматическая тромбопения (лейкозы, панмиелофтиз), тромбастения Гланцмана.
2. ГС, в основе которых лежат нарушения в системе гуморальных факторов свертывания крови: гемофилии, геморрагические гипопротромбинемии (авитаминоз К, при применении антикоагулянтов).
3. Микротромбоваскулиты – тромботическая тромбоцитопеническая пурпура (болезнь Мошковица), гемолитико-уремический синдром, геморрагический васкулит – болезнь Шенляйн – Геноха.
4. Синдром диссеминированного внутрисосудистого свёртывания (ДВС- синдром, тромбогеморрагический синдром).
5. Нарушение гемостаза сосудистого и смешанного генеза – наследственная геморрагическая телеангиэктазия (болезнь Рандю-Ослера), гемангиомы (микроангиоматозы с тромбопенией), формы с наследственной неполноценностью соединительной ткани, часто сочетающиеся с дисфункцией тромбоцитов, дефицитом фактора Виллебранда и др. нарушениями гемостаза.
Болезнь Верльгофа (тромбопеническая пурпура, эссенциальная, аутоиммунная, «пятнистая» болезнь). Верльгоф описал впервые в 1740 г. заболевание, характеризующееся кровоточивостью и кровоизлияниями без видимых причин, и назвал его morbus maculosus hemorrhaqicus. Клиника характеризуется кровоизлияниями различной величины, от петехий до крупных, величиной с ладонь, разной давности. Локализация кровоизлияний на конечностях, туловище, реже – на лице, ладонях, стопах. Болеют мужчины и женщины. Заболевание начинается иногда внезапно кровотечением из слизистых оболочек, реже – кровоизлиянием в мозг, сетчатую оболочку глаза и др. локализаций.
Течение заболевания обычно хроническое с периодами обострения и ремиссии. Клиника определяется локализацией кровоизлияний. В диагностике основным является исследование крови и костного мозга (миелограммы). Характерным является тромбопения, увеличение длительности кровотечения при нормальном времени свертывания крови. В миелограмме отмечается увеличение количества мегакариоцитов, но почти все они не функционируют. Повышена проницаемость сосудистой стенки.
Механизм кровоточивости: тромбопения и повышение проницаемости сосудистой стенки.
Гемофилии. Особенность ГС заключается в том, что проявление его всегда связано с травмой и даже самые легкие повреждения могут привести к тяжелым кровотечениям или обширным кровоизлияниям. Склонность к ГС выявляется иногда уже в первые моменты жизни ребёнка: при перерезе пуповины, при прорезывании зубов. При гемофилии кровоизлияния не являются множественными, чаще они имеют характер более или менее обширных кровоподтёков или гематом. Особенно характерны кровоизлияния в полость суставов (гемартрозы), чаще коленных и локтевых. Пораженный сустав увеличивается, резко болезнен, часто повышается температура за счет резорбции крови. Повторные кровоизлияния в один и тот же сустав ведут к анкилозам, контрактуре и атрофии мышц. Течение заболевания хроническое, с периодами обострения и ремиссий. В диагностике важен анамнез (гемофилия А передаётся через женщин, болеют только мужчины). Лабораторные показатели: свертываемость крови резко замедлена (до нескольких часов вместо 5-7 мин. в норме), длительность кровотечения, проницаемость сосудистой стенки и количество тромбоцитов не изменены. Отсутствует антигемофилический глобулин (фактор VIII).
При гемофилии В отсутствует IX фактор. Она не является наследственной.
При гемофилии С отсутствует X фактор, болеют мужчины и женщины.
Геморрагический васкулит (ГВ) – иммунный микротромбоваскулит или болезнь Шенляйн-Геноха – одно из самых распространенных и хорошо известных врачам геморрагических заболеваний, в основе которого лежит асептическое воспаление и дезорганизация стенок микрососудов, множественное микротромбообразование, поражающее как сосуды кожи, так и сосуды внутренних органов. Чаще встречается у детей в возрасте до 14 лет. Этиология неизвестна. Возможна связь со стрептококковой и вирусной инфекцией. Провоцирующими факторами наряду с инфекцией, могут быть прививки, пищевая и лекарственная аллергия, охлаждение и пр.
Доказана принадлежность ГВ к иммуннокомплексным заболеваниям, при которых микрососуды подвергаются асептическому воспалению с более или менее глубокой деструкцией стенок, тромбированием и образованием экстравазатов вследствие повреждающего действия циркулирующих низкомолекулярных иммунных комплексов и активированных компонентов системы комплемента.
Клиника ГВ. Принято различать основные синдромы: кожный, суставной, абдоминальный с коликой и кишечными кровотечениями, почечный, протекающий как острый гломерулонефрит, иногда с нефротическим синдромом, злокачественный ГВ с молниеносным течением (чаще у детей). Кожно-суставную форму ГВ часто называют простой. При ГВ в процесс могут быть вовлечены сосуды любой области, в т.ч. легких, мозга и его оболочек. Кожный синдром характеризуется симметричным появлением на конечностях, ягодицах и, реже на туловище, папулёзно – геморрагической сыпи, иногда с уртикарными элементами. Высыпания мономорфны, имеют воспалительную основу, часто пальпируемую. Суставной синдром подобен ревматическому полиартриту: поражаются крупные суставы, характерна летучесть поражения. Абдоминальный синдром – чаще у детей, нередко предшествует кожному синдрому. Клиника подобна острому животу и обусловлена субсерозными и в брыжейку кровоизлияниями, что может проявляться кровавой рвотой, меленой, коллапсом, анемией.
Варианты течения ГВ: молниеносное, острое, затяжное, рецидивирующее, хроническое.
Осложнения ГВ: 1) кишечная непроходимость, перфорация, перитонит, панкреатит; 2) ДВС – синдром; 3) постгеморрагическая анемия; 4) тромбозы и инфаркты в органах, в т.ч. церебральные расстройства, невриты.
Диагностика: клинические данные — характер и локализация геморрагического синдрома; повышение температуры до 38 – 39 0 С, лабораторные показатели: лейкоцитоз, ускоренная СОЭ, повышенные фибриноген, α1-, α2— и γ — глобулины, фактор Виллебранда и криоглобулины. Не изменены: количество тромбоцитов, длительность кровотечения и время свертывания, проницаемость сосудистой стенки.
Лечение геморрагических синдромов определяется их этиологией, патогенезом. Строго ограничены показания к назначению кортикостероидов. В лечении гемофилий перспективной является заместительная терапия факторами свертывания, полученных методом генной инженерии.
План самостоятельной работы: Студенты собирают жалобы и анамнез у больных с геморрагическими синдромами, производят их объективное исследование. Совместно с преподавателем дают интерпретацию основных клинических синдромов, данных лабораторных методов исследования, формулируют клинический диагноз.
Контрольные задания:
1. Для какого из геморрагических диатезов характерна тромбопения? Особенность геморрагического синдрома при нем.
2. Признаком какого геморрагического диатеза являются гемартрозы.
3. При каком геморрагическом диатезе различают кожный, суставной, абдоминальный, почечный синдромы.
Клинические задачи по теме занятия.
Оснащение, средства наглядности:
Слайды, клинические и биохимические анализы больных с геморрагическими синдромами, рентгенограммы крупных суставов с признаками гемартрозов.
1. Пропедевтика внутренних болезней (под. ред. Гребенева А.Л.), Москва.: Медицина, 2002 г.
2. Яворский О.Г., Ющик Л.В. Пропедевтика внутренних болезней в вопросах и ответах, К.: Здоровье, 2003.- 300с.
Дополнительная:
1. Баркаган З.С. Геморрагические заболевания и синдромы. М., 1988
2. Яновский Д.Н. Клиническая гематология. Киев, 1962.
источник