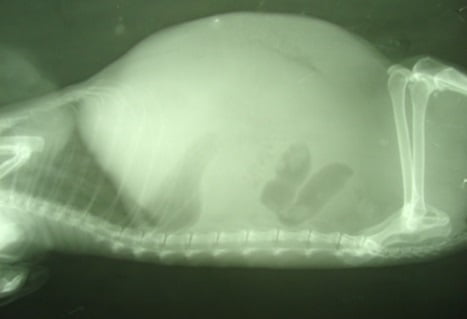
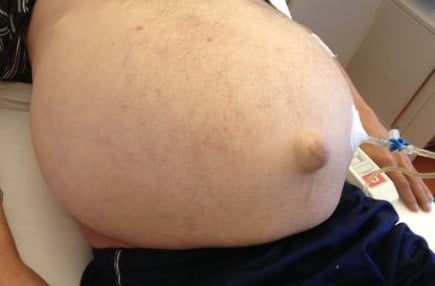
Карциноматозный асцит — это патологическое накопление жидкости в брюшной полости, развивающееся вследствие опухолевого поражения брюшины. Асцит вызывает значительный дискомфорт и приводит к различным функциональным нарушениям у пациентов в запущенных стадиях онкологического заболевания и является сложной клинической проблемой. Однако наличие асцита далеко не всегда свидетельствует об онкологическом заболевании.
Так скопление жидкости в полости брюшины может возникать как следствие цирроза печени и сердечной недостаточности. Малигнизированный асцит составляет, примерно, 10% среди всех случаев асцита и наиболее часто развивается при раке молочной железы, яичников, желудка, поджелудочной железы и толстой кишки.
В основе скопления в брюшной полости жидкости при злокачественном асците лежит несколько основных причин. Это закупорка опухолевыми клетками лимфатических сосудов брюшины, что нарушает нормальный отток перитонеальной жидкости, увеличение количества сосудов в стенке брюшины и повышение их проницаемости, связанные с продукцией опухолевыми клетками ряда специфических веществ, нарушение в организме больного белкового обмена вследствие потери белка с асцитической жидкостью и повышенного его распада.
Повышение внутрибрюшного давления при асците, сопровождающееся болями, потерей аппетита, одышкой, снижением физической активности, тошнотой и рвотой, значительно истощает силы больных. Эвакуация асцитической жидкости улучшает качество жизни больных с асцитом и может увеличивать сроки выживаемости.
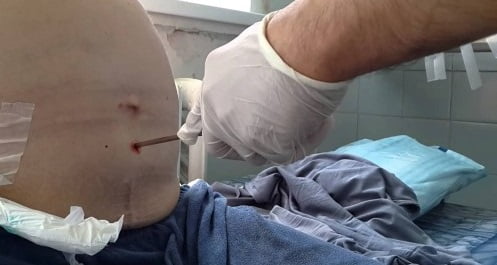
На сегодняшний день арсенал методов лечения злокачественного асцита достаточно разнообразен. При напряженном асците наиболее часто производят лапароцентез. Процедура заключается в выполнении прокола передней брюшной стенки и введении в брюшную полость дренажа, через который эвакуируется содержащаяся в брюшной полости асцитическая жидкость. Несмотря на широкое распространение метода, его выполнение часто болезненно для пациента, сопряжено с риском повреждения внутренних органов, увеличивающимся с каждой последующей процедурой.
Альтернативой лапароцентезу является установка постоянных катетеров и подкожных портов, позволяющих, с одной стороны, эвакуировать асцитическую жидкость по мере ее накопления, а с другой – предотвратить необходимость повторных проколов.
Однако и эти методы не лишены недостатков, так как являются более дорогостоящими, требуют постоянного ухода за катетером и могут сопровождаться такими соложениями, как воспаление брюшины (перитонит) и закупоркой катетера.
Важное место в терапии злокачественного асцита занимает внутрибрюшинная химиотерапия. Введение противоопухолевых препаратов в брюшную полость подавляет активность злокачественных клеток, что уменьшает скорость накопления асцитической жидкости и, таким образом, увеличивает срок между эвакуациями.
Дополнительное значение при лечении злокачественного асцита имеют диуретики. Данные об их эффективности противоречивы. В целом положительный эффект от назначения мочегонных препаратов наблюдается в 45% случаев. Однако необходимо подчеркнуть, что применение диуретиков имеет второстепенное значение и может проводиться только как дополнение к хирургическим методам и внутрибрюшинной химиотерапии.
Таким образом, несмотря на то, что проблема лечения злокачественного асцита остается не решенной, существующие методы терапии во многом позволяют облегчить страдания больных и существенно повысить их качество жизни.
Эвакуация асцитической жидкости, несомненно, приводит к улучшению самочувствия больных с напряженным асцитом, однако эта процедура представляет собой достаточно большую нагрузку на организм. Снижение давление в брюшной полости приводит к изменению работы сердца, почек, других органов и может сопровождаться в первые двое-трое суток после операции значительными нарушениями функционирования сердечно-сосудистой системы. Кроме того, при эвакуации асцита больной неизбежно теряет до 10, а иногда и более, литров жидкости, богатой белками и электролитами. Поэтому крайне важно своевременно и эффективно предотвратить возникающие расстройства правильно подобранной медикаментозной терапией.
— применение полностью имплантируемых порт-систем и постоянных катетеров.
Карциноматозный асцит является рецидивирующим заболеванием.
Эвакуация асцита не предотвращает повторное накопление асцитической жидкости в брюшной полости, что часто требует проведение повторных лапароцентезов и пункций брюшной полости. Одной из методик, позволяющих предотвратить необходимость повторных проколов, является установка постоянного катетера. После лапароцентеза в брюшную полость устанавливается постоянный катетер, изготавливаемый из специального материала, не вызывающего аллергических реакций, что позволяет оставлять катетер в брюшной полости на длительный период времени.
По мере накопления асцита жидкость откачивается через катетер, что облегчает состояние пациента. Важно отметить, что такой катетер требует тщательного систематического ухода за ним со стороны больного для предотвращения возможных инфекционных осложнений.
Перитонеальный порт представляет собой титановую камеру с силиконовой мембраной, к которой присоединяется катетер. Установка порта представляет собой хирургическую операцию, в ходе которой свободный конец катетера вводится в брюшную полость, а титановый порт, устанавливается подкожно в области реберной дуги. При необходимости эвакуировать скопившуюся в брюшной полости жидкость врач специальной иглой прокалывает кожу и силиконовую мембрану камеры, попадая, таким образом, иглой в полость камеры. Через иглу откачивается асцитическая жидкость и при необходимости вводятся противоопухолевые препараты. Таким образом, установка подкожного порта позволяет, с одной стороны, предотвратить необходимость повторных проколов брюшной стенки (всегда опасных с точки зрения возможного повреждения внутренних органов), а с другой стороны, уменьшить число инфекционных осложнений, так как сама камера не контактирует с внешней средой.
— экстракорпоральная ультрафильтрация и реинфузия асцитической жидкости у онкологических больных.
Асцитическая жидкость при карциноматозном асците представляет собой биологическую жидкость по своему составу близкую к плазме крови.
При эвакуации асцита больной неизбежно теряет до 10, а иногда и более, литров жидкости, богатой белками и электролитами, что в последующем часто требует введения больших доз белковых и других плазмозамещающих растворов. Метод реинфузии асцитической жидкости заключается в фильтрации и концентрации асцитической жидкости больного, что позволяет очистить асцитическую жидкость и обогатить ее белком, и дальнейшем ее внутривенном введении. Таким образом, с одной стороны, отпадает необходимость в приобретении дорогостоящих препаратов, а с другой –больному возвращаются его собственные белки, необходимые организму.
-внутрибрюшинная и внутриплевральная химиотерапия.
источник
при Санкт-Петербургском НИИ СП им. И.И. Джанелидзе
8 (812) 384-46-87 круглосуточно
Руководитель отделения — доктор медицинских наук
Суров Дмитрий Александрович
Заведующий отделением — кандидат медицинских наук
прУофилактика рака в ваших руках — его лечение в наших силах
Путем нажатия кнопки «Оправить» Вы даете согласие на обработку своих персональных в порядке, установленном Федеральным законом Российской Федерации от 27.07.2006 № 152-ФЗ «О персональных данных»
Карциноматозный асцит — это патологическое накопление жидкости в брюшной полости, развивающееся вследствие опухолевого поражения брюшины. Асцит вызывает значительный дискомфорт и приводит к различным функциональным нарушениям у пациентов в запущенных стадиях онкологического заболевания и является сложной клинической проблемой. Однако наличие асцита далеко не всегда свидетельствует об онкологическом заболевании.
Так скопление жидкости в полости брюшины может возникать как следствие цирроза печени и сердечной недостаточности. Малигнизированный асцит составляет, примерно, 10% среди всех случаев асцита и наиболее часто развивается при раке молочной железы, яичников, желудка, поджелудочной железы и толстой кишки.
В основе скопления в брюшной полости жидкости при злокачественном асците лежит несколько основных причин. Это закупорка опухолевыми клетками лимфатических сосудов брюшины, что нарушает нормальный отток перитонеальной жидкости, увеличение количества сосудов в стенке брюшины и повышение их проницаемости, связанные с продукцией опухолевыми клетками ряда специфических веществ, нарушение в организме больного белкового обмена вследствие потери белка с асцитической жидкостью и повышенного его распада.
Повышение внутрибрюшного давления при асците, сопровождающееся болями, потерей аппетита, одышкой, снижением физической активности, тошнотой и рвотой, значительно истощает силы больных. Эвакуация асцитической жидкости улучшает качество жизни больных с асцитом и может увеличивать сроки выживаемости.
На сегодняшний день арсенал методов лечения злокачественного асцита достаточно разнообразен. При напряженном асците наиболее часто производят лапароцентез. Процедура заключается в выполнении прокола передней брюшной стенки и введении в брюшную полость дренажа, через который эвакуируется содержащаяся в брюшной полости асцитическая жидкость. Несмотря на широкое распространение метода, его выполнение часто болезненно для пациента, сопряжено с риском повреждения внутренних органов, увеличивающимся с каждой последующей процедурой.
Альтернативой лапароцентезу является установка постоянных катетеров и подкожных портов, позволяющих, с одной стороны, эвакуировать асцитическую жидкость по мере ее накопления, а с другой – предотвратить необходимость повторных проколов.
Однако и эти методы не лишены недостатков, так как являются более дорогостоящими, требуют постоянного ухода за катетером и могут сопровождаться такими соложениями, как воспаление брюшины (перитонит) и закупоркой катетера.
Важное место в терапии злокачественного асцита занимает внутрибрюшинная химиотерапия. Введение противоопухолевых препаратов в брюшную полость подавляет активность злокачественных клеток, что уменьшает скорость накопления асцитической жидкости и, таким образом, увеличивает срок между эвакуациями.
Дополнительное значение при лечении злокачественного асцита имеют диуретики. Данные об их эффективности противоречивы. В целом положительный эффект от назначения мочегонных препаратов наблюдается в 45% случаев. Однако необходимо подчеркнуть, что применение диуретиков имеет второстепенное значение и может проводиться только как дополнение к хирургическим методам и внутрибрюшинной химиотерапии.
Таким образом, несмотря на то, что проблема лечения злокачественного асцита остается не решенной, существующие методы терапии во многом позволяют облегчить страдания больных и существенно повысить их качество жизни.
Эвакуация асцитической жидкости, несомненно, приводит к улучшению самочувствия больных с напряженным асцитом, однако эта процедура представляет собой достаточно большую нагрузку на организм. Снижение давление в брюшной полости приводит к изменению работы сердца, почек, других органов и может сопровождаться в первые двое-трое суток после операции значительными нарушениями функционирования сердечно-сосудистой системы. Кроме того, при эвакуации асцита больной неизбежно теряет до 10, а иногда и более, литров жидкости, богатой белками и электролитами. Поэтому крайне важно своевременно и эффективно предотвратить возникающие расстройства правильно подобранной медикаментозной терапией.
— применение полностью имплантируемых порт-систем и постоянных катетеров.
Перитонеальный порт представляет собой титановую камеру с силиконовой мембраной, к которой присоединяется катетер. Установка порта представляет собой хирургическую операцию, в ходе которой свободный конец катетера вводится в брюшную полость, а титановый порт, устанавливается подкожно в области реберной дуги. При необходимости эвакуировать скопившуюся в брюшной полости жидкость врач специальной иглой прокалывает кожу и силиконовую мембрану камеры, попадая, таким образом, иглой в полость камеры. Через иглу откачивается асцитическая жидкость и при необходимости вводятся противоопухолевые препараты. Таким образом, установка подкожного порта позволяет, с одной стороны, предотвратить необходимость повторных проколов брюшной стенки (всегда опасных с точки зрения возможного повреждения внутренних органов), а с другой стороны, уменьшить число инфекционных осложнений, так как сама камера не контактирует с внешней средой.
— экстракорпоральная ультрафильтрация и реинфузия асцитической жидкости у онкологических больных.
Асцитическая жидкость при карциноматозном асците представляет собой биологическую жидкость по своему составу близкую к плазме крови.
При эвакуации асцита больной неизбежно теряет до 10, а иногда и более, литров жидкости, богатой белками и электролитами, что в последующем часто требует введения больших доз белковых и других плазмозамещающих растворов. Метод реинфузии асцитической жидкости заключается в фильтрации и концентрации асцитической жидкости больного, что позволяет очистить асцитическую жидкость и обогатить ее белком, и дальнейшем ее внутривенном введении. Таким образом, с одной стороны, отпадает необходимость в приобретении дорогостоящих препаратов, а с другой –больному возвращаются его собственные белки, необходимые организму.
-в нутрибрюшинная и внутриплевральная химиотерапия.
источник
Специалисты клиники лечат асцит разного происхождения. Существенную часть пациентов клиники с асцитом составляют онкологические больные. В Клинике есть уникальное интервенционное отделение, где размещают качественные порт — системы от лучших изготовителей медицинского оборудования.
Каждый год специалисты клиники выполняет множество процедур, позволяющие имплантировать специальные порты для лечения боли. Некоторым людям они устанавливаются на долгие годы, другим — всего лишь несколько месяцев. Период, на который имплантируется порт, определяется от способа лечения, а заодно от доктора, назначающего лечение. Причина, в связи с которой лечащий доктор решил имплантировать порт, состоит в желании избежать множественных инфузий проводимых непосредственно в одну из периферических вен.
Вероятно, пациенту уже было выполнено большое число инъекций, и лечащий доктор или медсестра считают, что теперь весьма непросто нащупывать вену для выполнения новых пункций. Вероятно, подобные инфузии являются чересчур болезненными для пациента. Какова бы ни была причина установки, размещение порта позволяет осуществлять инъекции без боли в любое время и по мере того, когда это необходимо.
Установка качественного порта никак не сказывается обычном образе жизни человека и не заставляет его отказываться от многого из того, сем он занимался ранее. После заживления шва от имплантированного порта, человек вновь сможет заниматься плаванием, купанием, бегом. Если пациент достаточно ведет достаточно подвижный образ жизни, рыбачит или охотится, занимается приусадебным хозяйством, то ему нужно рассказать об этом лечащему доктору до установки порта. В этом случае он заблаговременно установит место его имплантации так, чтобы порт не препятствовал заниматься обычным делом. Порт практически не заметен и выглядит лишь как малая припухлость, находящаяся под кожей.
Размещение эпидурального порта эффективно обезболивает тяжелых онкобольных. Причем доза местного анестетика уменьшается почти в сто раз!
Порт, который имплантируется, позволяет выполнять инъекции медпрепаратов в целях обезболивания непосредственно в эпидуральную область в позвоночнике в течение продолжительного времени.
Благодаря размещению порта пациент или его родные могут самостоятельно выполнять каждодневные инъекции обезболивающих средств для обезболивания. Это позволяет сэкономить время и усилия, которые затрачиваются на помещения медучреждения, и способствует значительному улучшению качества жизни человека.
Пациент пребывает в клинике приблизительно четыре-пять часов. Сюда входит:
- регистрация пациента;
- подготовка к установке порта;
- выполнение процедуры имплантации порта
- последующее мониторинг со стороны лечащих врачей перед тем, как пациент будет выписан из клиники.
В операционной пациента попросят прилечь на бок. Потом в кисть или предплечье ему будет размещен внутривенный катетер. При этом врачи станут отслеживать параметры работы сердца, дыхания и давления, используя специальный монитор. Человека попросят прилечь на стол, где проводятся операции. Для того, чтобы повысить безопасность лечебной процедуры, создания большего удобства и уменьшения дозы облучения доктор применит ультразвуковой медаппарат диагностики – это позволит локализовать место, куда будет введен катетер. Затем врач подберет самую подходящую траекторию вкалывания иглы благодаря УЗ навигации. Пациенту выполнят введение малой дозы успокаивающего медпрепарата в целях расслабления и минимизации дискомфортных ощущений, а заодно сделают инъекцию анестетика непосредственно в место, куда будет установлен порт.
Установка эпидурального катетера выполняется сквозь малый надрез в спине. После этого его проводят под кожей (туннелируют) и выводят на кожную поверхность впереди на грудной клетке. Под кожей формируется карман для размещения камеры медикаментов. Ее присоединяют к катетеру, после чего два надреза закрывают швами. В последующем заполнение помпы осуществляется благодаря игле Губера.
На то, чтобы восстановиться после процедуры размещения порта, пациенту понадобится совсем немного времени. Могут наблюдаться боли непосредственно в стенке живота в том месте, где выходит порт, а заодно раздражение спины там, где имплантирован катетер. Как правило, такие ощущения являются минимальными и не приносят дискомфорта.
источник
Асцит также называют водянкой, поскольку он характеризуется скоплением жидкости в брюшной полости. Заболевание прогрессирует и создает угрозу для здоровья и даже жизни. Для диагностики пациентам проводится лапароцентез при асците, который позволяет откачать содержимое и отправить его на исследование. Результаты анализа важны для назначения правильного лечения.

Лапароцентез проводят для уточнения диагноза при неясной клинической картине асцита. Он бывает и лечебным – к нему прибегают специально для откачивания лишней жидкости при асците либо врач удаляет аномальное содержимое живота при его обнаружении. Можно проводить процедуру амбулаторно. В условиях стационара ее применяют при травмах неясного генеза и для введения углекислоты перед лапароскопией брюшной полости.
Врач всегда оценивает показания и противопоказания к лапароцентезу перед его проведением. Прибегают к процедуре при:
- накоплении в животе жидкости (асците);
- тупых травмах живота, когда пациент в коме, сильном опьянении и не способен четко описать симптомы;
- подозрении на кровоизлияния в брюшной полости, перитонит;
- подозрении на кисты, прободение язвы желудка или 12-перстной кишки при нечеткой симптоматике;
- множественных травмах, если больной потерял сознание или у него посттравматический шок, но есть подозрение на разрыв внутренних органов;
- риске перфорации кишечника в случае закрытой травмы;
- смазанных симптомах острого живота, если перед госпитализацией пациенту ввели наркотические анальгетики, которые затрудняют постановку точного диагноза;
- проникающих ранениях грудной клетки, если имеется риск повреждения диафрагмы, но отсутствуют показания для срочного проведения операции.
Нередко рентген, УЗИ и другие способы не позволяют исключить повреждения органов с вытеканием содержимого в брюшную полость. В таких случаях лапароцентез становится единственным методом диагностики.
Асцитическую жидкость, гной, кровь передают на анализы. Экссудат неясного состава исследуют на наличие содержимого ЖКТ, желчи, мочи, сока поджелудочной.
Противопоказания к лапароцентезу брюшной полости при асците следующие:
- проблемы со свертываемостью крови (в связи с риском кровотечения);
- сильное вздутие живота;
- тяжелая спаечная болезнь брюшной полости;
- вентральная послеоперационная грыжа;
- риск травмирования кишечника;
- наличие больших опухолей;
- беременность.
Спаечная болезнь создает повышенный риск повредить сосуды и органы брюшной полости, но все же это относительное противопоказание. Врач выносит решение о назначении процедуры в зависимости от конкретного случая.
Лапароцентез не рекомендуется проводить вблизи мочевого пузыря и при увеличении его объемов, при пальпируемой опухоли.
Перед тем, как выполнить прокол брюшной стенки, пациенту назначают стандартные обследования:
- анализы мочи и крови;
- коагулограмму;
- УЗИ органов брюшной полости;
- рентгенографию.
При травмах и острых хирургических патологиях проводят только анализ крови на свертываемость, ее группу и резус-фактор. По возможности делают УЗИ или рентген.
Прямо перед процедурой больной асцитом опорожняет мочевой пузырь и желудок. Если больной без сознания, мочевой пузырь ему опустошают с помощью катетера, для выведения содержимого желудка применяют назогастральный зонд.
Если пациент получил тяжелые травмы, находится без сознания или в шоковом состоянии перед лапароцентезом проводят противошоковую терапию, чтобы поддержать гемодинамику. При наличии показаний делают искусственную вентиляцию легких. Для проведения лапароцентеза больного асцитом перевозят в операционную, где можно оперативно перейти к лапароскопии.
Когда выполняют прокол брюшной стенки при асците, пациент сидит. Техника выполнения лапароцентеза следующая:
- Место будущего прокола смазывается антисептиком, выполняется разрез на животе на расстоянии 1-2 см ниже пупка.
- Выполняется послойная инфильтрация тканей вблизи прокола лидокаином 2% и новокаином 1%.
- Проводится обезболивание, затем скальпелем рассекается кожа, подкожная клетчатка и брюшные мышцы. При этом разрез-прокол должен затронуть лишь верхние кожные слои. Для предотвращения травмирования кишечника катетером используют УЗИ или специальные насадки для создания безопасного канала, свободного от кишечных петель.
- При помощи троакара вращательными движениями делается окончательный прокол. Внутри инструмента есть пространство, в которое вставляется трубка из полихлорвинила для выполнения пункции.
- Когда вытекает струя жидкости, трубку проталкивают еще на 2-3 см. Это предотвратит ее смещение в сторону мягких тканей при длительной откачке содержимого.
- Используя трубку, выполняют пункцию, а потом удаляют выпот. За раз в ходе лапароцентеза удаляют до 10 литров асцитической жидкости.
- Чтобы предотвратить падение внутрибрюшного давления, живот больного постоянно утягивают полотенцем.
После завершения лапароцентеза рана закрывается тугой повязкой. Пациента кладут на правый бок, он должен провести в таком положении какое-то время. Живот затягивают повязкой, чтобы поддержать нормальное внутрибрюшное давление.
После проведения лапароцентеза исследуют содержимое живота, чтобы определить меры по будущему лечению. Если обнаруживаются примеси крови и мочи, каловые массы либо жидкость желтая или серо-зеленая, проводится экстренная операция. Такое содержимое указывает на внутрибрюшное кровотечение, перитонит или перфорацию стенок пищеварительных органов.
На точность диагностики при асците влияет количество выделенной жидкости. Минимально необходимый объем – 300-500 мл. Если лапароцентез дает неубедительные результаты, а у больного острая хирургическая патология, проводят диагностическую лапароскопию или лапаротомию.
Пункция брюшной полости при асците – малотравматичная процедура, которая не требует общего наркоза, поэтому длительная реабилитация не требуется. Швы снимают спустя 7-10 дней, хотя постельный режим и некоторые другие ограничения соблюдают до исчезновения симптомов асцита.
Чтобы предотвратить повторное накопление выпота после лапароцентеза, пациента переводят на бессолевую диету с ограничением потребления жидкости до 1 л в день. В рационе должны быть животные белки, включая белое мясо, яйца, и кисломолочную продукцию. От жирного, острого, маринадов и сладостей нужно отказаться.
Физические нагрузки после лапароцентеза, особенно вызывающие напряжение передней брюшной стенки, запрещаются.
Если катетер ставится надолго, каждые 2 часа пациент изменяет положение, чтобы улучшался отток содержимого.
Осложнения после лапароцентеза появляются в 8-10% случаев. Обычно они обуславливаются пренебрежением нормами асептики и проникновением инфекции в место прокола.
При проведении процедуры из-за резкого перераспределения крови в сосудах может развиться обморок, а после удаления троакара есть риск кровотечения.
Также лапароцентез может привести к:

- развитию калового перитонита вследствие повреждения кишечных петель;
- флегмоне передней брюшной стенки;
- травмированию сосудов с появлением гематом или обширного кровоизлияния в брюшную полость;
- длительному вытеканию жидкости через прокол (при напряженном асците);
- проникновению воздуха сквозь прокол и развитию подкожной эмфиземы;
- активизации онкологического процесса и метастазированию (при пункции злокачественных опухолей).
Риски осложнений минимальны, поэтому лапароцентез признается эффективной и безопасной процедурой. Однако они повышаются при неудовлетворительном питании, неопорожненном мочевом пузыре, беременности. Пациент с жидкостью теряет альбумины, что провоцирует дефицит белков. Поэтому нужно учитывать природу выпота и самочувствие больного асцитом.
Часто лапароцентез оказывается единственно возможным способом облегчения состояния при асците, устранения тяжелых нарушений дыхания и работы сердца, а иногда – и продления жизни. При своевременном начале лечения водянки есть шансы купировать симптомы и восстановить функциональность пораженного органа.
источник
Асцит (водянка живота) – состояние, характеризующееся скоплением свободной жидкости в брюшной полости (больше 25 мл), которая может быть как воспалительного (экссудат), так и не воспалительного (транссудат) характера. Заболевание проявляется увеличением окружности живота, нарушением дыхания, болью в брюшине, чувством тяжести и распирания.
Наиболее часто (в 80% случаев) асцит возникает на фоне цирроза печени, достигшего финальной стадии декомпенсации. Эта стадия характеризуется истощением ресурсов печени, серьезными нарушениями печеночного и брюшного кровообращения, то есть появлением благоприятных условий для накопления жидкости.
Асцит – это скопление в брюшной полости жидкости, которое сопровождается прогрессирующим увеличением живота и нарастанием веса больного. Жидкость эта обычно имеет невоспалительный характер, то есть является транссудатом. Ее количество может значительно варьировать – от нескольких сотен миллилитров до 15-20 литров.
Причины асцитической болезни имеют неожиданный характер, самые распространенные среди них представлены ниже. Это:
- злокачественные новообразования и метастазы;
- цирроз печени и увеличение давления крови в портальной системе;
- тромбоз (сужение печеночных, нижней полой и воротной вен);
- острые и хронические воспалительные заболевания почек;
- нефротический сидром (с мочой начинает выводится белок);
- хроническая почечная недостаточность;
- воспалительное поражение серозной оболочки сердца;
- острая и хроническая сердечная недостаточность;
- некоторые инфекционные и воспалительные заболевания кишечника, при которых наблюдается диарея и потеря белка;
- воспаление поджелудочной железы;
- туберкулез;
- псевдомиксома (накопление слизи);
- анасрка.
Указанное заболевание является осложнением цирроза печени и не только. В организме прогрессирует постепенно, первое время никак себя не проявляет. Асцит брюшной полости сложно поддается успешному лечению. Однако исцеление наступает, если устранить основной патогенный фактор.
Формирование асцита брюшной полости у большинства пациентов при онкологических заболеваниях происходит постепенно, в течение нескольких недель или даже месяцев. Поэтому первые признаки этого грозного осложнения остаются без внимания.
Клинически асцит начинает проявляться уже после того, как в брюшной полости скопится достаточно большое количество жидкости, проявляется это осложнение:
- Чувством распирания в животе.
- Разными по характеру и длительности абдоминальными болями.
- Отрыжкой и изжогой.
- Тошнотой.
Визуально обратить внимание можно на постепенно увеличивающийся живот, в вертикальном положении он свисает вниз, а в горизонтальном расплывается по бокам. Растягивание кожи брюшной стенки позволяет увидеть сеть кровеносных сосудов и выпячивающийся пупок.
Давление на грудную клетку вызывает одышку и перебои в работе сердца. При асците человеку трудно наклониться, застегнуть обувь, надеть брюки.
На фото ниже показано, как проявляется заболевание у человека.
В зависимости от количества скопившегося экссудата выделяют три стадии асцита:
| Транзиторный | жидкости в брюшной полости не более 400 мл. На этой стадии может быть лишь вздутие живота. |
| Умеренный | выставляется, когда экссудата в брюшной полости не более 5 литров. На этой стадии осложнение проявляется клиническими симптомами в виде нарушения работы органов пищеварения, одышки. В случае отсутствия лечения асцита возможно развитие перитонита, дыхательной и сердечной недостаточности. |
| Напряженный | характеризуется скоплением до 20 литров жидкости. Состояние пациента тяжелое, значительно нарушается работа жизненно важных органов. |
Водянка живота может быть диагностирована врачом даже без применения специального оборудования – достаточно прощупать брюшную полость больного. Если при прощупывании врач обнаружит тупость в животе сбоку, при этом посередине обнаружится тимпанит, пациент болен асцитом.
Для проведения более глубокой диагностики требуется провести УЗИ в полости брюшины, исследовать печень, а также сделать пункцию брюшины (парацентез). Взятие жидкости на анализ позволяет выявить стадию заболевания и определить его лечение. Парацентез проводится для выяснения причин болезни. Также парацентез может быть сделан в случае возникновения трудностей с дыханием и возникновения болей.
Кроме вышеперечисленных методов диагностики, пациент должен сдать анализы мочи, крови, а также пройти исследования иммунологического типа. От того, сколько информации врачу дадут полученные анализы, зависит возможность назначения дополнительных анализов и тестов.
Асцит брюшной полости, развивающийся как осложнение онкологического заболевания, следует лечить совместно с основной болезнью.
- Важно также начать устранение избытка лишней жидкости в первые две недели ее образования, так как затягивание терапии приводит к развитию массы осложнений. Излишняя жидкость может быть удалена при помощи прокола и ее откачивания – лапароцентезе, путем приема мочегонных средств.
- Соблюдение специальной диеты поможет снизить внутрибрюшное давление, уменьшит вероятность дальнейшего продуцирования чрезмерного экссудата.
Химиотерапия эффективна только в том случае, если асцит спровоцирован раком кишечника. При раке желудка, яичников и матки использование химиопрепаратов не дает выраженного положительного результата.
Основными препаратами, помогающими выводить лишнюю жидкость из организма, являются диуретики. Благодаря их приему удается добиться перехода лишней жидкости из брюшной полости в кровяное русло, что способствует уменьшению симптомов асцита.
- Для начала пациентам назначают самую маленькую дозу диуретиков, чтобы минимизировать риск развития побочных эффектов. Важный принцип лечения мочегонными препаратами – это медленное нарастание диуреза, который не будет приводить к значительным потерям калия и иных важнейших метаболитов. Чаще всего рекомендуют прием препаратов Альдактон, Верошпирон, Триамтерен, Амилорид. Параллельно назначают препараты калия. Одновременно в схему лечения вводят гепатопротекторы.
- При этом врачи осуществляют ежесуточный контроль диуреза больного и при неэффективности лечения дозу препаратов увеличивают, либо заменяют их на более сильные средства, например, на Триампур или на Дихлотиазид.
Кроме мочегонных препаратов пациентам назначают средства, направленные на укрепление стенок сосудов (витамин С, витамин Р, Диосмин), препараты, препятствующие выходу жидкости за пределы сосудистого русла (Реополиглюкин). Улучшает обмен печеночных клеток введение белковых препаратов. Чаще всего для этой цели применяют концентрированную плазму, либо раствор Альбумина в 20%-ой концентрации.
Антибактериальные препараты назначают в том случае, если асцит имеет бактериальную природу.
При асците лапароцентез брюшной полости является хирургической манипуляцией, при которой жидкость из брюшной полости удаляют пункционно. За один раз не следует откачивать более 4 литров экссудата, так как это грозит развитием коллапса.
Чем чаще осуществляют пункцию при асците, тем выше риск развития воспаления брюшины. Кроме того, повышается вероятность формирования спаек и осложнений от проводимой процедуры. Поэтому при массивных асцитах предпочтительнее установка катетера.
Показаниями к проведению лапароцентеза является напряженный и рефрактерный асцит. Жидкость может быть откачана с помощью катетера, либо она просто свободно вытекает в заранее подготовленную посуду, после установки в брюшную полость троакара.
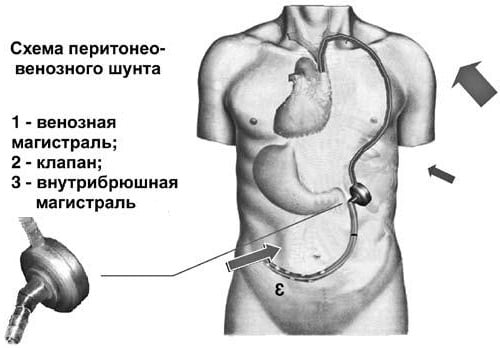
Порой применяется для лечения рефрактерного асцита т.е. того, который не поддается медикаментозной терапии и быстро возвращается после пункции. Операция заключается в увеличении объема циркулирующей крови путем постоянного поступления жидкости из брюшной полости в общую систему кровотока.
Шунт Левина – это длинная пластиковая трубка, устанавливающаяся в абдоминальную полость, достигая тазового дна. Далее шунт соединяют с клапаном и силиконовой трубкой, которая подкожно проходит к области шеи для последующего подключения с внутренней яремной и верхней полой веной. Клапан открывается с помощью образующейся силы смещения диафрагмы и увеличения внутрибрюшного давления. Таким образом, происходит беспрепятственное поступление жидкости в верхнюю полую вену.
Предусматривает уменьшение употребления жидкости, а также соли по причине того, что она задерживает в организме жидкость. Врачи советуют диету по Авиценне. Такая диета при асците предусматривает практически полный отказ от жирной пищи, употребление орехов в большом количестве, отказ от свежих фруктов в пользу сухих.
Также жидкую пищу (борщ, суп) следует заменить бульоном с добавками в виде сельдерея, петрушки, фенхеля. Диета при асците не регламентирует, сколько мяса должен употреблять больной, однако все мясо должно быть нежирного типа (курица, индейка, кролик).
Срок жизни людей с диагностированным асцитом варьирует в широких пределах, что зависит от целого ряда факторов. Продолжительность жизни пациента с асцитом обусловлена:
- Временем начала лечения. Если асцит выявлен на ранних стадиях развития, когда функции жизненно-важных органов не нарушены (или нарушены незначительно), устранение основного заболевания может привести к полному излечению пациента. В то же время, при длительно прогрессирующем асците может произойти поражение многих органов и систем (дыхательной, сердечно-сосудистой, выделительной), что приведет к смерти пациента.
- Выраженностью асцита. Транзиторный (слабовыраженный) асцит не представляет непосредственной угрозы для жизни пациента, в то время как напряженный асцит, сопровождающийся скапливанием в брюшной полости десятков литров жидкости, может привести к развитию острой сердечной или дыхательной недостаточности и смерти пациента в течение часов или дней.
- Основным заболеванием. Это, пожалуй, основной фактор, определяющий выживаемость пациентов с асцитом. Дело в том, что даже при проведении самого современного лечения благоприятный исход маловероятен, если у пациента имеется недостаточность сразу нескольких органов. Так, например, при декомпенсированном циррозе печени (когда функция органа практически полностью нарушена) шансы пациента на выживание в течение 5 лет после установки диагноза составляют менее 20%, а при декомпенсированной сердечной недостаточности – менее 10%. Более благоприятен прогноз при хронической почечной недостаточности, так как пациенты, находящиеся на гемодиализе и соблюдающие все предписания врача, могут прожить десятки лет и более.
Наличие асцита существенно утяжеляет течение основного заболевания и ухудшает его прогноз. Осложнениями самого асцита могут стать спонтанный бактериальный перитонит, печеночная энцефалопатия, гепаторенальный синдром, кровотечения.
источник
Владельцы патента RU 2527843:
Изобретение относится к медицине, а именно к хирургии. Осуществляют лапароцентез. Прокол троакаром с трубкой 25 см производят в точке McBurney. Трубку располагают под углом 23-30 о . Продвигают трубку параллельно Пупартовой связке по боковому каналу брюшной полости к полости малого таза. Муфту троакара фиксируют к коже брюшной стенки. На проксимальный конец трубки троакара одевают и фиксируют дренажную трубку 100-175 см. Регулируют аспирацию зажимом 1-2 дня. Способ позволяет устранять асцит путем наружного фракционного регулируемого аспирационного дренирования при асците. Обеспечивает полноту удаления жидкости и предупреждает осложнения. 2 ил., 1 пр.
Изобретение относится к медицине, а именно к хирургии и терапии, и предназначено для устранения асцита различного происхождения путем операции лапароцентеза и проведения продленного, фракционного наружного, регулируемого аспирационного дренирования брюшной полости, обеспечивающего полноту удаления асцитической жидкости и предупреждение осложнений.
Известен способ устранения асцита путем чрескожной пункции брюшной стенки специальной иглой с мандреном [БМЭ т.12, издание третье. М.: «Советская энциклопедия» — 1982, с.323-324]. Пункция брюшной полости проводится в точке по средней линии живота на 3-5 см ниже пупка. После проникновения иглы в брюшную полость, конец иглы размещается сразу под брюшиной во избежание травмы внутренних органов. После удаления мандрена из просвета пункционной иглы вытекание асцитической жидкости осуществляется путем ее наружного свободного оттока через просвет иглы.
Недостатком данного способа является малая эффективность, обусловленная тем, что небольшой диаметр просвета иглы не позволяет быстро эвакуировать достаточное для декомпрессии количество жидкости.
Манипуляция занимает продолжительное время с участием и под контролем врача. При этом фракционность оттока достигается ручным перекрытием наружного отверстия просвета иглы пальцем врача, проводящего пункцию. Фракционность удаления жидкости из брюшной полости необходима для предупреждения осложнений, связанных с быстрым ее удалением особенно в случаях напряженного асцита и выраженным компрессионным синдромом, вызывающим дыхательную недостаточность.
В данном способе пункция брюшной полости проводится по средней линии живота на 3-5 см ниже пупка при помощи троакара после предварительного небольшого разреза кожи и апоневроза. При этом больной находится в положении сидя, с целью обеспечения лучшей дыхательной экскурсии легких и диафрагмы.
При этом после удаления определенного количества асцитической жидкости ее уровень в брюшной полости снижается, а также за счет декомпрессии снижается внутрибрюшное давление. Уровень жидкости перестает достигать уровня расположения иглы в брюшной полости и свободный отток экссудата прекращается, что не обеспечивает в дальнейшем полноты эвакуации накопленной асцитической жидкости. Баланс достижения полноты эвакуации асцита и скорости эвакуации нельзя осуществить одновременно за сеанс пункции, и ее приходится неоднократно повторять.
Известен способ устранения асцита, включающий проведение лапароцентеза с помощью троакара с трубкой, который вводят через брюшную стенку в полость малого таза, с последующей аспирацией находящегося в ней патологического содержимого (Пат. РФ №2460552, кл. А61М 27/00, 2012).
В данном способе просвет трубки троакара, через который происходит наружный свободный отток асцитической жидкости, имеет больший на порядок внутренний диаметр по сравнению с диаметром просвета пункционной иглы, что обеспечивает быстрый отток жидкости.
Однако после извлечения стилета из просвета трубки троакара может наступить быстрая декомпрессия органов живота и питающих их сосудов, особенно венозных.
Такое дренирование не всегда желательно и может давать осложнение. Быстрая декомпрессия вызывает несоответствие объема сосудистого русла и объема циркулирующей крови, что в свою очередь ведет к резкому падению артериального давления вплоть до угнетения и остановки кровообращения с летальным исходом.
В данном способе пункция брюшной полости проводится по средней линии живота на 1-2 см ниже пупка при помощи троакара после предварительного небольшого разреза кожи и апоневроза.
Однако заведения трубки троакара данным образом бывает затруднено из-за анатомических особенностей данной области. В отличии от известного решения предложено заводить трубку троакара через прокол брюшной стенки в точке Mc-Burney, которая проецируется на боковой канал брюшной полости. Это обеспечивает более безопасное введение трубки, т.к. ее продвижение происходит по ходу анатомического бокового канала живота, который продолжается в подвздошной области и опускается в малый таз, что делает продвижение трубки более безопасным, беспрепятственным, а саму процедуру менее травматичной.
В соответствии с этим поставлена задача, направленная на снижение травматичности, повышение безопасности и эффективности удаления асцитической жидкости из брюшной полости за счет создания контролируемого и регулируемого полуавтоматического режима. Это позволяет избежать появление осложнений связанных с быстрым отведением асцитической жидкости из полости малого таза.
Эта задача достигается тем, что в способе устранения асцита, включающем проведение лапароцентеза с помощью троакара с трубкой, которую вводят через брюшную стенку в полость малого таза, с последующей аспирацией находящегося в ней патологического содержимого, предложено трубку троакара вводить через прокол в точке Mc-Burney перпендикулярно по отношению к плоскости брюшной стенки в подвздошной области справа или слева, затем трубку устанавливать параллельно Пупартовой связке и осуществлять поступательное перемещение ее по боковому каналу брюшной полости, вдоль связки в сторону малого таза до размещения дистального конца трубки в полости малого таза, а для аспирации жидкости образовывать дренажный канал, для чего на проксимальный конец троакара соосно с трубкой надевать дополнительную дренажную трубку с зажимом, длина которой должна составлять 3-5 L, где L — длина троакара с трубкой и через нее осуществлять непрерывную, регулируемую аспирацию патологического содержимого в течение 1-2 дней.
На фиг.1 и 2 показаны схемы проведения операций.
Способ осуществляют следующим образом.
Операция проводится в условиях перевязочной или малой операционной под местным обезболиванием. Общее обезболивание требуется в случае непереносимости местных анестетиков. В отличие от известного решения прокол троакаром брюшной стенки проводится в точке Mc-Burney 1 перпендикулярно по отношению к плоскости брюшной стенки 2 в подвздошной области (справа или слева) в зависимости от наличия или отсутствия препятствий и противопоказаний. После этого извлекают стилет 3 из трубки 4 троакара 5, наружный просвет трубки 4 перекрывают пальцем оператора для препятствия оттока экссудата.
Трубку троакара разворачивают под углом 25-30° по отношению к брюшной стенке 2, дистальный конец 6 направляют параллельно Пупартовой связке с одновременным медленным осторожным продвижением в сторону малого таза. Такое продвижение способствует прилеганию трубки троакара к боковому каналу брюшной полости, вдоль связки в сторону малого таза. После этого образуют дренажный канал. Для чего на проксимальный конец троакара надевают дополнительную дренажную трубку 7 с зажимом 8, опускают ее свободный конец 9 ниже уровня расположения больного. Для этого длина дополнительной дренажной трубки составляет 5-7 L (100-175 см), где L — длина троакара с трубкой (20-25 см.) Благодаря этому создается дренажная система для оттока асцитической жидкости из брюшной полости. Зажим 8 регулирует подачу жидкости при инфузии, а также используется в качестве регулятора оттока асцитической жидкости. После продвижения трубки 4 троакара 5 до ограничительной муфты 10, которая препятствует проваливанию трубки в брюшную полость, трубка 4 в данном положении фиксируется к коже брюшной стенки подшиванием лигатурой 11, 12. Это не позволяет ей в дальнейшем смещаться относительно тканей брюшной стенки. Одновременно этой же лигатурой фиксируется конец системы соединенной с трубкой троакара с натяжением лигатуры между ограничительной муфтой 10 трубки и системой. Такая фиксация предупреждает самопроизвольное разъединение системы и трубки троакара при полуавтоматическом режиме работы дренажной системы. Трубка при таком расположении и соединенная с системой инфузии выполняет функцию аспирации брюшной полости. Для предупреждения отклонения трубки троакара при сокращении мышц брюшной стенки при движении больного наружный конец трубки троакара дополнительно прижимается к брюшной стенке наложением повязки, которая фиксируется к брюшной стенке пластырем.
Работа дренажной системы происходит следующим образом. После того как система сформирована, производится продленное фракционное выведение асцитической жидкости из брюшной полости путем открытия зажима 8 на дополнительной трубке 7, с контролем состояния и самочувствия пациента и забором экссудата для клинико-лабораторного исследования. В дальнейшем данные сеансы фракционного отведения асцитической жидкости повторяются в течение 1-2 суток до полного устранения асцита. Регулирование объема фракций проводится вручную самим пациентом или персоналом. Аспирация экссудата происходит в автоматическом режиме. Введенная в брюшную полость трубка 4 троакара направляет и аспирирует асцитическую жидкость, поступающую из полости таза, куда она стекает из верхних отделов, в положении больного — лежа с приподнятой головой. Таким продленным в течение нескольких суток полуавтоматическом режиме достигается постепенность, контролируемость и регулируемость дренажного механизма по устранению асцита. Это позволяет избежать осложнений связанных с быстрым отведением асцитической жидкости из брюшной полости. После ликвидации асцита трубка троакара извлекается из брюшной полости, канал после дренирования закрывается за счет смыкания стенок вследствие сокращения мыщц и фасций брюшной стенки, дренирование прекращается.
Данным способом успешно пролечено 34 взрослых пациента, ни у одного больного не было осложений, связанных с быстрой эвакуацией асцитической жидкости из брюшной полости. Во всех случаях улучшалось состояние больного, и достигалась полнота устранения асцита на более длительный период по сравнению с традиционной операцией.
Конкретный пример выполнения способа
Больной А., диагноз алкогольный цирроз печени, с объемом асцитической жидкости более 30 литров. Проведена операция лапароцентеза, при этом троакар с трубкой ввели через прокол в точке Mc-Burney перпендикулярно по отношению к плоскости брюшной стенке в подвздошной области справа, затем установили его под углом 25-30° по отношению к брюшной стенке параллельно Пупартовой связке, продвинули по боковому каналу брюшной полости вдоль связки в сторону малого таза, разместили дистальный конец трубки в полости малого таза. Для аспирации жидкости образовали дренажный канал. При этом на проксимальный конец троакара надели дренажную трубку с зажимом и опустили ее свободный конец ниже уровня расположения больного, длина дренажной трубки составляет 7L — 175 см, где L — длина троакара с трубкой 25 см. Непрерывную регулируемую аспирацию патологического содержимого осуществляли в течение 2 дней. После ликвидации асцита трубка троакара извлечена, дренирование прекращено.
Использование постепенного устранения асцита в течение 1-2 суток за счет полуавтоматического режима контроля и регулирования дренажного механизма позволяет избежать осложнения, связанные с быстрым отведением асцитической жидкости из брюшной полости.
Способ устранения асцита путем проведения лапароцентеза, включающий прокол брюшной стенки с помощью троакара со стилетом, извлечение стилета и образование дренажного канала для аспирации патологического содержимого, при этом прокол производят в точке McBurney перпендикулярно брюшной стенке в подвздошной области и используют дренажную трубку 100-175 см для непрерывной аспирации, регулируют аспирацию зажимом, при этом аспирацию проводят в течение 1-2 дней, отличающийся тем, что для образования дренажного канала используют трубку троакара, которую вводят под углом 25-30° через прокол в брюшной стенке, устанавливают параллельно Пупартовой связке и перемещают по боковому каналу брюшной полости вдоль связки до размещения дистального конца трубки троакара в полости малого таза и ограничительной муфты, препятствующей проваливанию трубки, у брюшной стенки, затем фиксируют муфту троакара к коже брюшной стенки с помощью лигатур, на проксимальный конец трубки троакара надевают и фиксируют дренажную трубку с зажимом и осуществляют непрерывную регулируемую аспирацию патологического содержимого.
источник
а) Показания для перитонеовенозного шунта:
— Плановые: цирротический асцит, устойчивый к лечению мочегонными средствами, у больных, которые не являются кандидатами на трансплантацию печени. Злокачественный асцит после использования всех других мер и при ожидаемой продолжительности жизни > 1 месяца.
— Противопоказания: бактериально загрязненный асцит.
— Альтернативные операции: повторный лечебный парацентез, хирургическая или рентгенологическая установка чрезъяремного внутрипеченочного портосистемного шунта (TIPS), пересадка печени.
б) Предоперационная подготовка:
— Предоперационные исследования: тщательное обследование по поводу основного заболевания печени; анализ асцитической жидкости (бактериология, цитология, продукты распада фибрина); исследование свертывания крови.
— Подготовка пациента: периоперационная антибиотикопрофилактика, возможно замещение жидкости и электролитов.
в) Специфические риски, информированное согласие пациента:
— Обструкция и инфицирование катетерной системы (20-40% случаев)
— Системные нарушения свертывания (менее 10% серьезных случаев)
— Перитонит (менее 5% случаев)
— Кровотечение (менее 5% случаев)
— Смещение системы катетер-порт (менее 5% случаев).
— Эмболия опухолевыми клетками при наличии злокачественного асцита (редко)
г) Обезболивание. Общее обезболивание (интубация), возможно местное обезболивание.
д) Положение пациента. Лежа на спине, с немного приподнятой правой стороной тела.
е) Оперативный доступ при перитонеовенозном шунте. Через грудино-ключично-сосцевидную мышцу и в правом или в левом верхнем отделе брюшной полости.
ж) Этапы операции:
— Расположение шунта и кожные разрезы
— Установка брюшного катетера
— Введение катетера
— Проведение катетера на груди
— Венозный доступ на шее
з) Анатомические особенности, серьезные риски, оперативные приемы:
— Место ушивания брюшины вокруг брюшного конца катетера должно быть водонепроницаемым.
— Наиболее часто применяются шунт Денвера (со сжимаемой камерой) и шунт Ле Вина (без функции насоса).
— Рекомендуется интраоперационная замена асцитической жидкости физиологическим изотоническим солевым раствором или раствором Рингера (реже человеческим альбумином).
— На объем шунтируемой жидкости могут влиять простые действия: он увеличивается под влиянием внутрибрюш-ного давления и форсированного вдоха в горизонтальном положении верхней части тела.
и) Меры при специфических осложнениях:
— Развитие инфекции требует удаления всей шунтирующей системы.
— Исследования, выполняемые при окклюзии шунта и увеличенном сопротивлении насоса, включают дуплексную ультрасонографию, а также рентгенологическое обследование в виде «шунтограммы» после прямой пункции; заблокированная система обычно нуждается в замене.
к) Послеоперационный уход:
— Медицинский уход: тщательный послеоперационный контроль кровообращения, баланса жидкости и свертывания крови (отделение интенсивной терапии); удаление назогастрального зонда на 1-й день.
— Возобновление питания: питье с 1-го дня и увеличение его объема при тщательном контроле баланса жидкости.
— Активизация: сразу же.
— Период нетрудоспособности: зависит от общей ситуации.
л) Этапы и техника наложения перитонеовенозного шунта:
1. Расположение шунта и кожные разрезы.
2. Установка брюшного катетера.
3. Введение катетера.
4. Проведение катетера на груди.
5. Венозный доступ на шее.
1. Расположение шунта и кожные разрезы. Перитонеовенозный шунт (Денвера) создает связь между брюшной полостью и яремной веной. Обычно он устанавливается с правой стороны. Необходимо выполнить три разреза кожи: ниже правого реберного края, над правой яремной веной и, в случае необходимости, дополнительный латеральный разрез у соска.
2. Установка брюшного катетера. Брюшная полость должна быть открыта экономно с сохранением мышц, чтобы избежать истечения асцитической жидкости. На три поперечных пальца ниже края правой реберной дуги выполняется поперечный разрез (а) с последующим поперечным рассечением фасции (б) и продольным разведением мышц тупым путем ножницами (в).
3. Введение катетера. Брюшина захватывается одним или, предпочтительно, двумя концентрическими кисетными швами (а). Катетер для шунта может быть заранее введен подкожно. Важно, чтобы над реберным краем с помощью тупой диссекции было выделено достаточное пространство для шунтирущей трубки.
Затем, после аспирации асцитической жидкости, брюшной конец катетера вводится в брюшную полость под контролем зрения и фиксируется водонепроницаемым образом кисетными швами, чтобы избежать истечения асцита (б).
4. Проведение катетера на груди. Шунт проводится над правым реберным краем, чтобы обеспечить поддержку насоса. Тупая подкожная диссекция позволяет провести венозный конец шунта до шеи через цервикальный разрез.
5. Венозный доступ на шее. Яремная вена, которая идет позади грудино-ключичнососцевидной мышцы, достигается через цервикальный разрез (а). Доступ обеспечивается тупой диссекцией после обнаружения легко пальпируемой сонной артерии. Вена обнажается, обводится двумя сосудистыми петлями, после чего накладывается кисетный шов (полипропилен 5-0).
Вена перекрывается путем натяжения сосудистых петель, затем в центре кисетного шва выполняется разрез, и венозный конец катетера проводится до верхней полой вены (б, в). Положение катетера на уровне правого предсердия подтверждается рентгенологически. Операцию завершает подкожный шов, швы кожи и повязка.
источник
Асцит, или брюшная водянка, нередко является следствием другого, более опасного и сложного в лечении заболевания. Тем не менее и сам по себе асцит способен осложнить жизнь больному и привести к печальным последствиям. Современной медициной разработаны достаточно эффективные методы лечения асцита на разных его стадиях. Что нужно знать о первых признаках асцита, ходе его развития и к какому врачу обратиться за помощью?
Под асцитом в медицине понимают вторичное патологическое состояние, для которого характерно скопление жидкости в брюшной полости. Чаще всего асцит вызывается нарушением регуляции обмена жидкости в организме в результате серьезных патологических состояний.
В здоровом организме в брюшной полости всегда находится немного жидкости, при этом она не скапливается, а всасывается лимфатическими капиллярами. При различных заболеваниях внутренних органов и систем увеличивается скорость образования жидкости и снижается скорость ее всасывания. При развитии асцита жидкости становится все больше, она начинает сдавливать жизненно важные органы. Это способствует усугублению развития основного заболевания и прогрессированию асцита. Кроме этого, поскольку основная часть жидкости скапливается в брюшной полости, происходит значительное уменьшение объема циркулирующей крови. Это приводит к запуску компенсаторных механизмов, задерживающих в организме воду. У больного существенно замедляется скорость образования мочи и ее выделения, при этом количество асцитической жидкости увеличивается.
Накопление жидкости в полости живота обычно сопровождается повышением внутрибрюшного давления, нарушением кровообращения и сердечной деятельности. В некоторых случаях возникают потеря белка и электролитные нарушения, вызывающие сердечную и дыхательную недостаточность, что значительно ухудшает прогноз основного заболевания.
В медицине выделяют три основных стадии развития асцита.
- Транзиторный асцит. На этой стадии в брюшной полости скапливается не более 400 мл жидкости. Выявить заболевание можно только при помощи специальных исследований. Функции органов не нарушены. Снятие симптомов асцита возможно с помощью терапии основного заболевания.
- Умеренный асцит. В брюшной полости на этой стадии скапливается до 4 л жидкости. Наблюдается увеличение живота у пациента. В положении стоя можно заметить выпирание нижней части брюшной стенки. В положении лежа больной нередко жалуется на одышку. Наличие жидкости определяется с помощью перкуссии (простукивания) или симптома флюктуации (колебания противоположной стенки живота при простукивании).
- Напряженный асцит. Количество жидкости на этой стадии может достигать, а в некоторых случаях даже превышать, 10–15 л. Давление в брюшной полости повышается и нарушает нормальную работу жизненно важных органов. Состояние пациента при этом тяжелое, его необходимо срочно госпитализировать.
Отдельно рассматривают рефрактерный асцит, практически не поддающийся лечению. Его диагностируют в том случае, если все виды проводимой терапии не дают результата и количество жидкости не только не уменьшается, но и постоянно увеличивается. Прогноз при таком виде асцита неблагоприятный.
По статистике основными причинами возникновения асцита брюшной полости являются:
- болезни печени (70%);
- онкологические заболевания (10%);
- сердечная недостаточность (5%).
Кроме того, асцитом могут сопровождаться следующие заболевания:
- болезни почек;
- туберкулезное поражение брюшины;
- гинекологические заболевания;
- эндокринные нарушения;
- ревматизм, ревматоидный артрит;
- красная волчанка;
- сахарный диабет второго типа;
- уремия;
- болезни пищеварительной системы;
- перитониты неинфекционной этиологии;
- нарушение оттока лимфы из брюшной полости.
Возникновению асцита, кроме указанных заболеваний, могут способствовать следующие факторы:
- злоупотребление спиртным, ведущее к циррозу печени;
- инъекции наркотических препаратов;
- переливание крови;
- ожирение;
- высокий уровень холестерина;
- татуаж;
- проживание в регионе, для которого характерны случаи возникновения вирусных гепатитов.
Во всех случаях в основе возникновения асцита лежит сложное сочетание нарушений жизненно важных функций организма, ведущее к скоплению жидкости в брюшной полости.
Одним из главных внешних признаков асцита брюшной полости является увеличение размера живота. В положении стоя у пациента он может свисать в форме фартука, а в положении лежа образовывать так называемый лягушачий живот. Возможно выпячивание пупка и появление растяжек на коже. При портальной гипертензии, вызванной повышением давления в воротной вене печени, на передней брюшной стенке появляется венозный рисунок. Этот рисунок принято называть «головой Медузы» из-за отдаленного сходства с мифологической Медузой Горгоной, на голове которой вместо волос находились извивающиеся змеи.
В животе появляются боли и чувство распирания изнутри. Человек испытывает трудности при наклонах туловища. К внешним проявлениям также относятся отеки ног, рук, лица, цианоз кожных покровов. У больного развивается дыхательная недостаточность, тахикардия. Возможно появление запоров, тошнота, отрыжка и потеря аппетита.
При лабораторных и инструментальных исследованиях врач подтверждает диагноз и устанавливает причину, вызвавшую асцит. Для этого проводятся УЗИ, МРТ, диагностический лапароцентез и лабораторные исследования. С помощью УЗИ выявляют наличие свободной жидкости в брюшной полости и ее объем, увеличение печени и селезенки, расширение полой и воротной вены, нарушение структуры почек, наличие опухолей и метастазов.
МРТ позволяет послойно изучить ту или иную ткань, выявить даже незначительное количество асцитической жидкости и диагностировать основное заболевание, вызвавшее асцит.
Кроме этого, врач проводит исследование при помощи пальпации и перкуссии. Пальпация помогает выявить признаки, указывающие на поражение определенного органа (печени или селезенки). Перкуссия используется непосредственно для выявления асцита. Суть ее заключается в простукивании брюшной полости пациента и анализе перкуторных звуков. При выраженном асците, например, тупой перкуторный звук определяется над всей поверхностью живота.
Лабораторные исследования крови показывают снижение концентрации эритроцитов, увеличение количества лейкоцитов и СОЭ, возможно повышение концентрации билирубина (при циррозе печени), белков острой фазы воспаления. Анализ мочи при асците на начальной стадии может показывать большее количество мочи меньшей плотности, поскольку асцит вызывает отклонения в работе мочевыделительной системы. При терминальной стадии плотность мочи может быть нормальной, но ее общее количество значительно снижается.
Общие принципы лечения асцита предполагают прежде всего терапию основного заболевания. Лечение самого асцита направлено на выведение жидкости из брюшной полости и предотвращение рецидивов.
Пациенты с первой степенью асцита не нуждаются в медикаментозном лечении и соблюдении бессолевой диеты.
Пациентам со второй степенью асцита назначается диета с пониженным содержанием натрия и диуретическая терапия. Она должна проводиться при постоянном мониторинге состояния больного, включая содержания электролитов в сыворотке крови.
Пациенты с третьей степенью заболевания проводят удаление жидкости из брюшной полости, а в дальнейшем диуретическую терапию в сочетании с бессолевой диетой.
Асцит обычно указывает на серьезные нарушения в работе пораженных органов, но тем не менее смертельным осложнением сам он не является. При своевременной диагностике и правильном лечении возможна полная ликвидация асцитической жидкости из брюшной полости и восстановление функций пораженного органа. В ряде случаев, например при раке, асцит способен быстро прогрессировать, вызывая осложнения и даже гибель пациента. Это объясняется тем, что на течение асцита большое влияние оказывает основное заболевание, способное вызывать серьезные поражения печени, почек, сердца и других органов.
На прогноз влияют и другие факторы:
- Степень асцита. Транзиторный асцит (первой степени) не является непосредственной угрозой жизни пациента. В этом случае все внимание следует уделить терапии основной болезни.
- Время начала лечения. При выявлении асцита на той стадии, когда жизненно важные органы еще на разрушены или их функции поражены незначительно, устранение основного заболевания также может привести к полному выздоровлению пациента.
На статистику выживаемости при асците также влияет вид и тяжесть основного заболевания. При компенсированном циррозе печени 50% больных способны прожить от 7 до 10 лет, а при декомпенсированном — пятилетняя выживаемость не превышает 20%.
При онкологических заболеваниях асцит, как правило, появляется на поздних стадиях, и пятилетняя выживаемость составляет не более 50% при своевременном лечении. Средний показатель жизни у таких больных составляет 1–2 года.
При неправильном лечении асцит может вызвать серьезные осложнения, ухудшающие прогноз:
- кровотечение;
- перитонит;
- отек мозга;
- дисфункцию сердечной деятельности;
- тяжелую дыхательную недостаточность.
Рецидивы асцита также могут возникать как побочные эффекты при неправильном лечении. Рецидивирование очень опасно, поскольку в большинстве случаев не поддающиеся излечению асциты приводят к летальному исходу.
Консервативное или симптоматическое лечение асцита применятся в тех случаях, когда асцит брюшной полости находится на ранней стадии развития или в качестве паллиативной терапии при онкологии и нецелесообразности применения других методов.
Во всех случаях основной задачей лечения является выведение асцитической жидкости и поддержание состояние пациента на определенном уровне. Для этого необходимо уменьшить количество поступающего в организм натрия и усилить его выведение с мочой.
Достичь положительных результатов можно только при комплексном подходе, соблюдая диету, контролируя изменения веса и принимая диуретические препараты.
Главные принципы диеты при асците следующие:
- Минимум соли. Ее избыточное потребление приводит к развитию отеков, а следовательно, асцита. Пациентам рекомендуется максимально ограничить прием соленой пищи.
- Минимум жидкости. При умеренном или напряженном асците нормой должно быть не более 500–1000 мл жидкости в чистом виде в сутки.
- Минимум жиров. Потребление пищи с большим количеством жиров приводит к развитию панкреатита.
- Достаточное количество белков в рационе. Именно белковая недостаточность может привести к возникновению отеков.
Рекомендуется употреблять в пищу нежирные сорта мяса и рыбы, обезжиренный творог и кефир, фрукты, овощи, зелень, пшеничную крупу, компоты, кисели. Готовить лучше на пару или запекая в духовке.
Запрещены жирное мясо и рыба, жареные блюда, копчености, соль, алкоголь, чай, кофе, специи.
При лечении асцита необходимо контролировать динамику веса. При начале бессолевой диеты в течение недели производится ежедневное взвешивание. Если пациент потерял более 2 кг, то диуретические препараты ему не назначаются. При потере веса менее 2 кг в течение следующей недели начинают медикаментозную терапию.
Мочегонные препараты помогают вывести лишнюю жидкость из организма и способствуют переходу части жидкости из брюшной полости в кровеносное русло. Клинические проявления асцита при этом существенно снижаются. Основными препаратами, используемыми в терапии, являются фуросемид, маннитол и спиронолактон. В амбулаторных условиях фуросемид назначается внутривенно не более 20 мг 1 раз в два дня. Он выводит жидкость из сосудистого русла через почки. Основной недостаток фуросемида — чрезмерное выведение калия из организма.
Маннитол применяется совместно с фуросемидом, поскольку их действие комбинируется. Маннитол выводит жидкость из межклеточного пространства в сосудистое русло. Назначается по 200 мг внутривенно. Однако в амбулаторных условиях его применять не рекомендуется.
Спиронолактон также является мочегонным средством, однако он способен предотвращать чрезмерное выведение калия.
Дополнительно назначаются препараты, укрепляющие сосудистые стенки (витамины, диосмин), средства, влияющие на систему крови («Желатиноль», «Реополиглюкин»), альбумин, антибиотики.
Оперативное вмешательство при асците показано в тех случаях, когда скопление жидкости не может быть устранено при помощи консервативного лечения.
Лечебный лапароцентез при асците (прокол передней брюшной стенки) способен вывести большие объемы жидкости — от 6 до 10 литров за один раз. Проводят процедуру под местным обезболиванием с предварительным опустошением мочевого пузыря. Пациент принимает полусидячее или лежачее положение. Прокол производится по средней линии живота между пупком и лобковой костью. Скальпелем выполняется разрез кожи, через который в брюшную полость вводится специальный инструмент — троакар. Через него выводится жидкость в нужном объеме. После процедуры рану ушивают. Лапароцентез при асците можно выполнять только в условиях стационара, поскольку необходимо соблюдение норм антисептики и владение методикой проведения операции. Чтобы упростить процедуру для тех больных, которым лапароцентез требуется периодически, его проводят через постоянный перитонеальный порт.
Еще одной эффективной хирургической манипуляцией является оментогепатофренопексия. Она заключается в подшивании сальника к предварительно обработанным участкам поверхности диафрагмы и печени. Благодаря возникновению контакта между печенью и сальником появляется возможность всасывания асцитической жидкости соседними тканями. Дополнительно снижается давление в венозной системе и выход жидкости в брюшную полость через стенки сосудов.
ТИПС — трансъюгулярное интрапеченочное портосистемное шунтирование — позволяет провести декомпрессию портальной системы и устранить асцитический синдром. В основном ТИПС проводится при рефрактерном асците, не поддающемся медикаментозной терапии. При процедуре ТИПС в яремную вену вводится проводник до попадания в печеночную вену. Затем по проводнику специальный катетер проводится в саму печень. При помощи длинной изогнутой иглы в воротной вене устанавливается стент, создающий канал между воротной и печеночной венами. Кровь направляется в печеночную вену со сниженным давлением, что приводит к устранению портальной гипертензии. После выполнения ТИПС у пациентов с рефрактерным асцитом наблюдается уменьшение объема жидкости в 58% случаев.
Несмотря на то, что асцит и вызывающие его болезни являются достаточно серьезными и сложно поддающимися лечению, своевременная комплексная терапия может значительно повысить шансы на выздоровление или улучшить качество жизни неизлечимых больных. Лечить асцит нужно только под наблюдением врача, поскольку сложность основного заболевания редко позволяет обойтись домашними или народными методами. Особенно это касается асцитов, вызванных онкологией.
источник