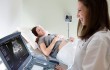
Асцит-перитонит — это острое или хроническое воспаление брюшины с последующим инфицированием асцитической жидкости, сопровождающееся местными и общими симптомами и нарушением функций органов и систем.
По этиологии асцит-перитонит подразделяют на первичный и вторичный. Первичным асцитом-перитонитом называют воспаление брюшины у больного с асцитом в отсутствии явного источника инфекции в виде нарушения целостности внутренних органов. Напротив, вторичный асцит-перитонит развивается в результате инфицирования брюшины при остром аппендиците, панкреатите, перфорациях, абсцессах, локализующихся в брюшной полости в результате всех тех причин, которые вызывают перитонит у больных без асцита. Первичный асцит-перитонит встречается достаточно редко и по статистике составляет около 1% от общего числа перитонитов.
Патогенетические механизмы развития асцита-перитонита до настоящего времени изучены недостаточно. К возможным путям инфицирования брюшной полости микрофлорой относят:
гематогенный путь из отдаленных очагов инфекции (одентогенный, бронхолегочный, урогенитальный, как проявление системного инфекционного заболевания (туберкулез, сальмонеллез);
лимфогенный путь, когда нарушение защитных механизмов брюшины происходит на этапе эвакуации микроорганизмов из брюшной полости за счет лимфатического механизма;
непосредственное поступление микроорганизмов в брюшную полость через маточные трубы при сальпингоофоритах.
Отдельную группу составляют больные спонтанным бактериальным перитонитом (СБП), который является вполне устоявшимся термином, означающим воспаление брюшины с последующей контаминацией асцитической жидкости, развивающееся без нарушения целостности внутренних органов.
Термин “спонтанный бактериальный перитонит” впервые предложил известный американский гепатолог Гарольд О`Конн в 1964 г., опубликовав в журнале “Анналы внутренней медицины” 5 случаев его описания. Свою работу он назвал “Спонтанный перитонит и бактериемия при Лаэннековском циррозе, вызванный кишечными микроорганизмами. Относительно частый, но редко диагностируемый синдром”. В своих воспоминаниях автор пишет, что к 1964 г. это тяжелое, часто смертельное заболевание было диагностировано всего лишь в 40 случаях на протяжении последних 200 лет. В период с 1964 по 1974 г. в этой же клинике уже наблюдались 50 больных СБП. В дальнейшем появившееся “вдруг” новое заболевание стало общепризнанным.
Развитие спонтанного бактериального перитонита в настоящее время объясняется транслокацией микроорганизмов из кишки в лимфатические узлы с последующим поступлением в кровь и в брюшную полость.
Факторами риска для развития асцита-перитонита, с одной стороны, являются:
наличие цирроза печени, класса В и С по Child-liugh, с нарушением функции печени, сопровождающимся снижением белково-синтетической функции, функции ретикулоэндотелиальной системы;
сниженный трофологический статус больного;
гастроинтестинальное кровотечение;
наличие бактериальных очагов, бактериемия, виремия;
артериовенозное шунтирование;
нарушение микроциркуляции в стенке кишки, облегчающее транслокацию микроорганизмов, снижение бактериальной и опсонизирующей способности.
Частота СБП у стационарных больных циррозом печени, по данным различных авторов, варьирует от 10 до 30%. Диагностируемые во время госпитализации эпизоды СБП составляют примерно половину общего количества случаев СБП, преимущественно у пациентов с циррозом печени класса В и С по Child-Pugh.
Летальность при СБП — 30—50%, однако в последние годы эти показатели имеют выраженную тенденцию к снижению. Так, например, по данным Центрального научно-исследовательского института гастроэнтерологии, летальность при СБП за последние 3 года составила 21%; основные причины смерти — гастроинтестинальные кровотечения, печеночная недостаточность, гепаторенальный синдром.
Клинические проявления асцита-перитонита, как правило, носят стертый характер. Выделяют:
Системные проявления инфекции (лихорадка, лейкоцитоз, септический шок).
Энцефалопатия и быстро нарастающая печеночная недостаточность без видимых причин.
Местные признаки перитонита (боль в животе).
Нарушение моторики ЖКТ (рвота, диарея).
Обязательным в диагностике асцита-перитонита является исследование асцитической жидкости с проведением подсчета числа полиморфно-ядерных лейкоцитов, определение содержания белка, концентрации альбумина, вычисление сывороточно-асцитического альбуминового градиента.
Получение содержания полиморфно-ядерных лейкоцитов более 250 клеток на мм3 служит показанием для дополнительных исследований на других образцах асцитической жидкости — произведение посева нового образца асцитической жидкости на культуру для посева крови. При СБП высевают как грамотрицательные микроорганизмы, так и грамположительные, реже — анаэробные (см. табл.).
СБП наиболее часто протекает в виде моноинфекции, основными возбудителями его являются грамотрицательные аэробные энтеробактерии и неэнтерококковые стрептококки.
В настоящее время выделяют три варианта СБП в зависимости от количества полиморфно-ядерных лейкоцитов и идентификации микроорганизмов в асцитической жидкости:
классический, полный вариант СБП. Асцитическая жидкость содержит более 250 полиморфно-ядерных лейкоцитов на мм3, дает рост культуры при высевании. Такое сочетание признается наиболее часто встречающимся.
культуронегативный нейтрофильный асцит, когда асцитическая жидкость содержит более 500 полиморфно-ядерных лейкоцитов на мм3, не дает роста культуры при высевании. Выявляется в 4—5% случаев у больных, страдающих циррозом печени, и в 35% случаев больных с подозрением на СБП.
культуропозитивный с низким содержанием нейтрофилов, когда асцитическая жидкость содержит менее 250 полиморфно-ядерных лейкоцитов на мм3, дает рост культуры при высевании. Как правило, при культивировании выявляются грамм-позитивные микроорганизмы в виде монокультуры. Асимптоматично протекает, имеет более благоприятное прогностическое течение.
При обследовании больного циррозом печени с асцитом наиболее часто проводится дифференциальная диагностика с вторичным бактериальным перитонитом, разрывом внутреннего полого органа, локальным абсцессом. Во всех случаях необходима оценка клинической картины заболевания. Наиболее характерно повышение уровня лактатдегидрогеназы >225 mU/L, глюкозы — 50 мг/дл, общего белка — >1 г/дл, как правило, при вторичном асците-перитоните отмечается значительный нейтрофилез, при ультразвуковом исследовании значительно чаще выявляются нити фибрина.
При панкреатогенном асците, который достаточно часто встречается у больных алкогольным циррозом в асцитической жидкости, отмечается повышение уровня амилазы, липазы. Доказана высокая информативность прокальцитонина (предшественника кальцитонина).
При канцероматозе брюшины — в асцитической жидкости проводят выявление атипичных клеток.
Хронический туберкулезный перитонит чаще всего развивается в результате распространения инфекции с мезентериальных или забрюшинных лимфатических узлов или придатков матки. Возможно гематогенное инфицирование. Характерны явления хронической туберкулезной интоксикации с субфебрильной температурой. Выделяют два варианта течения туберкулезного перитонита: асцитическая форма и псевдоопухолевая. В последнем случае продуктивное воспаление приводит к образованию спаечного процесса, спаянию петель кишечника и развитию механической кишечной непроходимости. При ультразвуковом исследовании на фоне асцита часто выявляются нити фибрина, а также фибрин визуализируется в виде взвеси. Диагноз ставят на основании жалоб, явлений туберкулезной интоксикации, исследования асцитической жидкости с последующим посевом на специальные среды. Иногда в диагностике помогает лапароскопия с биопсией.
В соответствии с рекомендациями Международного клуба асцита алгоритм лечения больного со спонтанным бактериальным перитонитом при циррозе печени может быть представлен следующим образом.
Алгоритм обследования больного с впервые выявленным асцитом при циррозе печени:
Всесторонняя оценка клинической картины.
Ультразвуковое исследование с оценкой наличия нитей фибрина, взвеси.
Диагностический парацентез:
подсчет числа полиморфно-ядерных лейкоцитов;
биохимическое исследование асцитической жидкости — общего белка, альбумина, глюкозы, лактатдегидрогеназы, амилазы, липазы;
выявление атипичных клеток в асцитической жидкости.
Посев асцитической жидкости на специальные гемолитические среды.
Должны быть исключены все патологические состояния, которые могут привести к перитониту — панкронекроз, аппендицит, канцероматоз, туберкулез, сальмонеллез, сальпингоофорит.
Рекомендуется до получения результатов посева асцитической жидкости всем больным при превышении числа полиморфно-ядерных лейкоцитов более 250 в мм3 проводить эмпирическую антибактериальную терапию цефалоспоринами III поколения (цефотаксим, цефтриксозим, цефтизидим, цефоницид). Наиболее хорошо изученный и часто применяемый препарат из этой группы цефотаксим назначается каждые 12 ч в течение 5 дней внутривенно, минимальная разовая доза — 2 г.
Амоксициллин/клавулановая кислота по эффективности сравнимы с цефотаксимом, применяются внутривенно в стандартных дозах, рекомендуемых для лечения тяжелых инфекций в течение 5—7 дней.
Больным неосложненным СБП (при отсутствии шока, илеуса, гастроинтестинального кровотечения, выраженной печеночной энцефалопатии или повышения сывороточного креатинина более 3 мг/дл), не получавших ранее профилактически фторхинолоны, может быть рекомендован офлоксацин внутрь в дозе не менее 400 мг каждые 12 ч.
Аминогликозиды согласно международным рекомендациям применять при спонтанном бактериальном перитоните нецелесообразно в связи с более низкой эффективностью и высокой нефротоксичностью.
Эффективность проведения адекватной антибактериальной терапии достигает 90%, характеризуется снижением содержания полиморфно-ядерных лейкоцитов менее 250 клеток на мм3 в асцитической жидкости, исчезновением местных и системных проявлений инфекции. Оптимальным критерием эффективности считается снижение числа полиморфно-ядерных лейкоцитов в асцитической жидкости через два дня от начала антибактериальной терапии по сравнению с исходными показателями. В связи с чем в ходе терапии рекомендуется проводить хотя бы один повторный парацентез через 48 ч от начала терапии.
Критериями неэффективности считают ухудшение состояния в течение первых часов антибактериальной терапии, а также снижение числа полиморфно-ядерных лейкоцитов в асцитической жидкости менее чем на 25%. При отсутствии эффекта от антибактериальной терапии рекомендуется смена антибиотика с учетом чувствительности микрофлоры или эмпирически при отрицательных результатах посева проводить дифференциальный диагноз с вторичным перитонитом.
В лечении спонтанного бактериального перитонита необходимо наряду с этиотропной терапией проведение мероприятий, направленных на предупреждение и лечение осложнений цирроза печени, являющихся факторами риска.
Печеночная энцефалопатия — L-орнитил-L-аспартат, внутривенно по 20 г на 500 мл физиологического раствора, в течение 7—10 дней, в дальнейшем — внутрь по 5 г (гранулят) 3 раза в день 6—8 нед и более, лактулоза — 60—120 г внутрь до послабления стула, длительно.
Гастроинтестинальное кровотечение — ингибиторы протонной помпы.
Гепаторенальный синдром — альбумин, отмена диуретиков, больших объемов парацентезов, нефротоксических препаратов.
Рекомендуется также проведение дезинтоксикационной терапии, применение пребиотиков и пробиотиков для нормализации флоры, снижения эндотоксикоза, уменьшения внутрибрюшного давления.
Профилактику СБП рекомендуется проводить всем больным циррозом печени, осложнившимся желудочно-кишечным кровотечением в связи с высоким риском развития тяжелых бактериальных инфекций с применением фторхинолонов (норфлоксацин, ципрофлоксацин, офлоксацин) 400 мг внутрь каждые 12 ч не менее 7 дней. В качестве альтернативных схем предлагаются комбинации фторхинолонов (ципрофлоксацин или офлоксацин) в сочетании с амоксициллин/клавулановой кислотой внутривенно, а после прекращения кровотечения — ципрофлоксацин внутрь.
Спонтанный бактериальный перитонит является грозным осложнением цирроза печени у больных с асцитом, в связи с чем прогноз для пациентов, перенесших это осложнение, остается серьезным. Вопрос о проведении трансплантации печени необходимо своевременно рассматривать для всех выживших больных.
К группе риска развития СБП также относятся больные циррозом печени класса С по Child-Pugh, перенесшие его в анамнезе.
В настоящее время большие рандомизированные исследования показали высокую эффективность непрерывной антибиотикопрофилактики у больных циррозом печени, перенесших СБП. В соответствии с международными рекомендациями профилактика возвратного бактериального перитонита проводится непрерывно норфлоксацином по 400 мг/сут. Появление резистентной микрофлоры в этом случае остается потенциальной проблемой. В связи с низкой выживаемостью после первого эпизода спонтанного перитонита, которая в течение первого года составляет 30—50%, а в течение второго — всего 25—30%, рекомендуется рассматривать таких пациентов в качестве кандидатов на трансплантацию печени.
источник
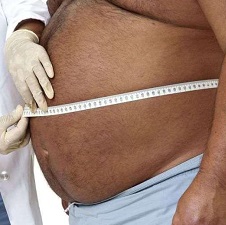
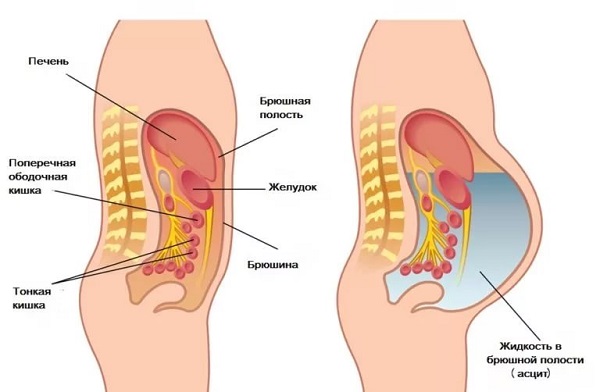
Полость живота вмещает в себя часть кишечника, желудок, печень, желчный пузырь, селезенку. Она ограничивается брюшиной – оболочкой, которая состоит из внутреннего (прилегающего к органам) и внешнего (прикрепленного к стенкам) слоя. Задача полупрозрачной серозной оболочки – фиксировать внутренние органы и участвовать в метаболизме. Брюшина обильно снабжена сосудами, которые обеспечивают обмен веществ через лимфу и кровь.
Между двумя слоями брюшины у здорового человека присутствует определенный объем жидкости, которая постепенно всасывается в лимфатические узлы, чтобы освободить пространство для поступления новой. Если по каким-либо причинам повышается скорость образования воды или замедляется его всасывание в лимфу, то транссудат начинает в брюшине накапливаться.
Асцит – патологическое скопление жидкости в брюшной полости. Он может развиваться стремительно (в течение нескольких дней) либо на протяжении длительного периода (недель или месяцев). Клинически наличие свободной жидкости в брюшной полости проявляется при достижении довольно большого объема – от 1,5 л.
Количество жидкости в брюшной полости иногда достигает значительных цифр – 20 л и более. По происхождению асцитическая жидкость может быть воспалительного характера (экссудат) и невоспалительного, являясь следствием нарушения гидростатического либо коллоидно-осмотического давления при патологиях кровеносной или лимфатической системы (транссудат).
В зависимости от количества жидкости в брюшной полости говорят о нескольких степенях патологического процесса:
- Небольшой асцит (не более 3 л).
- Умеренный (3–10 л).
- Значительный (массивный) (10–20 л, в редких случаях – 30 л и более).
По инфицированности асцитического содержимого выделяют:
- стерильный (неинфицированный) асцит;
- инфицированный асцит;
- спонтанный бактериальный перитонит.
По ответу на проводимую терапию асцит бывает:
- транзиторным. Исчезает на фоне проводимого консервативного лечения параллельно с улучшением состояния пациента навсегда либо до периода очередного обострения патологического процесса;
- стационарным. Появление жидкости в брюшной полости не является случайным эпизодом, в незначительном объеме сохраняется даже несмотря на адекватную терапию;
- резистентным (торпидным, или рефрактерным). Большой асцит, который не удается не только купировать, но и даже уменьшить большими дозами диуретиков.
Если скопление жидкости продолжает неуклонно увеличиваться и достигает огромных размеров, вопреки проводимому лечению, такой асцит называют напряженным.
Причины асцита брюшной полости разнообразны и всегда связаны с каким-то серьезным нарушением в организме человека. Брюшная полость является замкнутым пространством, в котором не должно образовываться лишней жидкости. Это место предназначено для внутренних органов – там находится желудок, печень, желчный пузырь, часть кишечника, селезенка, поджелудочная железа.
Брюшина выстлана двумя слоями: наружным, который крепится к стенке живота, и внутренним, который прилегает к органам и окружает их. В норме между этими листами всегда есть незначительное количество жидкости, которая является результатом работы кровеносных и лимфатических сосудов, находящихся в полости брюшины. Но эта жидкость не накапливается, так как практически сразу после выделения она всасывается лимфатическими капиллярами. Остающаяся незначительная часть необходима для того, чтобы петли кишечника и внутренние органы могли свободно передвигаться в брюшной полости и не склеивались друг с другом.
Когда происходит нарушение барьерной, выделительной и резорбтивной функции, экссудат перестает нормально всасываться и скапливается в животе, в результате чего и развивается асцит.
ТОП 10 причин возникновения асцита брюшной полости:
- Болезни сердца. Асцит может развиваться из-за сердечной недостаточности, либо по причине констриктивного перикардита. Сердечная недостаточность может явиться следствием практически всех кардиологических заболеваний. Механизм развития асцита в данном случае будет связан с тем, что гипертрофированная сердечная мышца не в состоянии перекачивать необходимые объемы крови, которая начинает скапливаться в кровеносных сосудах, в том числе и в системе нижней полой вены. В результате высокого давления жидкость будет выходить из сосудистого русла, формируя асцит. Механизм развития асцита при перикардите примерно такой же, но в данном случае воспаляется наружная оболочка сердца, что приводит к невозможности его нормального наполнения кровью. В дальнейшем это сказывается на работе венозной системы;
- Болезни печени. В первую очередь, это цирроз, а также рак органа и синдром Бадда-Киари. Цирроз может развиваться на фоне гепатита, стеатоза, приема токсичных лекарственных средств, алкоголизма и иных факторов, но всегда сопровождается гибелью гепатоцитов. В итоге нормальные клетки печени замещаются рубцовой тканью, орган увеличивается в размерах, пережимает воротную вену и поэтому развивается асцит. Также способствует выходу лишней жидкости снижение онкотического давления, потому что сама печень уже не в состоянии синтезировать белки плазмы и альбумины. Усугубляет патологический процесс целый ряд рефлекторных реакций, запускаемых организмом в ответ на печеночную недостаточность;
- Болезни почек. Обуславливается асцит хронической почечной недостаточностью, которая возникает в результате самых разнообразных болезней (пиелонефрит, гломерулонефрит, мочекаменная болезнь и т. д.). Болезни почек приводят к тому, что повышается артериальное давление, натрий вместе с жидкостью задерживается в организме, в итоге формируется асцит. Снижение онкотического давления плазмы, приводящее к асциту, также может происходить на фоне нефротического синдрома;
- Болезни органов пищеварения способны спровоцировать избыточное скопление жидкости в брюшной полости. Это может быть панкреатит, хроническая диарея, болезнь Крона. Сюда же можно отнести любые процессы, происходящие в брюшине и препятствующие лимфатическому оттоку;
- Различные поражения брюшины способны спровоцировать асцит, среди них разлитой, туберкулезный и грибковый перитонит, перитонеальный карциноз, рак толстого кишечника, желудка, молочной железы, яичников, эндометрия. Сюда же относится псевдомиксома и мезотелиома брюшины;
- Асцит может развиваться при повреждении лимфатических сосудов. Это случается из-за травмы, из-за наличия в организме опухоли, дающей метастазы, из-за заражения филяриями (глистами, откладывающими яйца в крупных лимфатических сосудах);
- Полисерозит является заболеванием, при котором асцит выступает в комплексе с иными симптомами, среди которых плеврит и перикардит;
- Системные заболевания способны приводить к накоплению жидкости в брюшине. Это ревматизм, ревматоидный артрит, красная волчанка и пр.;
- Белковая недостаточность – один из факторов, предрасполагающих к формированию асцита;
- Привести к асциту способна микседема. Это заболевание сопровождается отечностью мягких тканей и слизистых оболочек, манифестирует при нарушении синтеза тироксина и трийодтиронина (гормонов щитовидной железы).
Итак, в основе асцита могут находиться самые различные воспалительные, гидростатические, метаболические, гемодинамические и иные нарушения. Они влекут за собой ряд патологических реакций организма, в результате которых интерстициальная жидкость пропотевает сквозь вены и скапливается в брюшине.
Как уже было сказано, онкологические (опухолевые) заболевания характеризуются бесконтрольным размножением опухолевых клеток. Грубо говоря, любая опухоль может стать причиной развития асцита, если произойдет метастазирование опухолевых клеток в печень с последующим сдавливанием печеночных синусоидов и повышением давления в системе воротной вены. Однако существуют некоторые опухолевые заболевания, которые осложняются асцитом чаще других.
Причиной асцита может быть:
- Канцероматоз брюшины. Данным термином обозначается поражение брюшины опухолевыми клетками, которые метастазируют в нее из опухолей других органов и тканей. Механизм развития асцита при этом такой же, как при мезотелиоме.
- Мезотелиома. Данное злокачественное новообразование встречается крайне редко и происходит непосредственно из клеток брюшины. Развитие опухоли приводит к активации иммунной системы с целью уничтожения опухолевых клеток, что проявляется развитием воспалительного процесса, расширением кровеносных и лимфатических сосудов и пропотеванием жидкости в брюшную полость.
- Рак яичников. Хотя яичники и не относятся к органам брюшной полости, листки брюшины участвуют в фиксации данных органов в малом тазу. Этим объясняется тот факт, что при раке яичников патологический процесс легко может распространиться на брюшину, что будет сопровождаться повышением проницаемости ее сосудов и образованием выпота в брюшной полости. На поздних стадиях заболевания может отмечаться метастазирование рака в листки брюшины, что усилит выход жидкости из сосудистого русла и приведет к прогрессированию асцита.
- Рак поджелудочной железы. Поджелудочная железа является местом образования пищеварительных ферментов, которые выделяются из нее по протоку поджелудочной железы. После выхода из железы данный проток сливается с общим желчным протоком (по которому отходит желчь из печени), после чего они вместе впадают в тонкий кишечник. Рост и развитие опухоли вблизи места слияния данных протоков может привести к нарушению оттока желчи из печени, что может проявляться гепатомегалией (увеличением размеров печени), желтухой, кожным зудом и асцитом (асцит развивается на поздних стадиях заболевания).
- Синдром Мейгса. Данным термином обозначается патологическое состояние, характеризующееся скапливанием жидкости в брюшной и в других полостях организма (например, в плевральной полости легких). Причиной заболевания считаются опухоли органов малого таза (яичников, матки).
Симптомы, которыми проявляется асцит (см. фото), конечно, сильно зависят от тяжести состояния. Если асцит легкой степени заболевания, то не проявляется никаких симптомов, его трудно выявить даже с помощью инструментальных обследований, помогает только УЗИ или КТ брюшной полости.
Если асцит является серьезным, сопровождается следующими симптомами:
- Вздутие и тяжесть живота.
- Вздутие, разбухание и увеличение объема живота.
- Проблемы с дыханием из-за давления содержимого брюшного полости на диафрагму. Сдавливание приводит к диспноэ (одышка, короткое и быстрое дыхание).
- Боли в животе.
- Плоский пупок.
- Отсутствие аппетита и мгновенное ощущение сытости.
- Опухшие лодыжки (отёк) из-за избытка жидкости.
- Другие типичные симптомы заболевания, такие как портальная гипертензия (сопротивление прохождению потока крови) при отсутствии цирроза печени.
Диагноз асцита можно выявить уже при первом осмотре:
- увеличенный живот (схож с таковым при беременности), выпячивающийся пупок, в лежачем положении распластывается по бокам из-за стекания жидкости («лягушачий живот»), подкожные вены на передней стенке расширены;
- при перкуссии (простукивании) живота звук становится тупым (как по дереву);
- при аускультации (выслушивании фонендоскопом) живота кишечные шумы будут отсутствовать вследствие значительного накопления жидкости.
Показательным является признак флюктуации — одну ладонь кладут на бок пациента, другой рукой производят колебательные движения с другого бока, в результате будет ощущаться движение жидкости в брюшной полости.
Для дополнительной диагностики применимы следующие виды лабораторных анализов и инструментальных исследований:
- ультразвуковое исследование органов брюшной полости и почек (УЗИ). Метод обследования позволяет выявить наличие жидкости в брюшной полости, объёмные образования, даст представление о размерах почек и надпочечников, наличие или отсутствие в них опухолей, об эхоструктуре поджелудочной железы, желчного пузыря и др.;
- УЗИ сердца и щитовидной железы — можно определить фракцию выброса (её снижение является одним из признаков сердечной недостаточности), размеры сердца и его камер, наличие фибриновых отложений (признак констриктивного перикардита), размеры и структуру щитовидной железы;
- компьютерная и магнитно-резонансная томография — позволяет визуализировать даже малейшее скопление жидкости, оценить структуру органов брюшной полости, выявить аномалии их развития, наличие новообразований и др.;
- обзорная рентгенограмма органов грудной клетки — позволяет судить о наличии туберкулёза или опухолей лёгких, размерах сердца;
- диагностическая лапароскопия — на передней брюшной стенке делают незначительный прокол, вводят в него эндоскоп (аппарат со встроенной камерой). Метод позволяет определить жидкость в брюшной полости, взять её часть на дальнейшее исследование, чтобы выяснить природу возникновения асцита, также возможно удастся обнаружить повреждённый орган, вызвавший скопление жидкости;
- ангиография — метод, позволяющий определить состояние сосудов;
- общий анализ крови — возможно снижение числа тромбоцитов из-за нарушенной функции печени, увеличение скорости оседания эритроцитов при аутоиммунных и воспалительных заболеваниях и др.;
- общий анализ мочи — позволяет судить о наличии заболеваний почек;
- биохимический анализ крови, гормоны щитовидной железы. Определяются: уровень белка, трансаминазы (АЛАТ, АСАТ), холестерин, фибриноген для определения функционального состояния печени, ревмопробы (С-реактивный белок, ревматоидный фактор, антистрептолизин) для диагностики ревматоидного артрита, красной волчанки или других аутоиммунных заболеваний, мочевина и креатинин для определения функции почек, натрий, калий и др.;
- определение онкомаркёров, например, альфа-фетопротеина при раке печени;
- микроскопическое исследование асцитической жидкости позволяет определить природу асцита.
При наличии в брюшной полости большого количества жидкости может развиваться дыхательная недостаточность и перегрузка правых отделов сердца из-за сдавления поднятой вверх диафрагмой лёгких и крупных сосудов. В случае присоединения инфекции возможно развитие перитонита (воспаления брюшины), который является крайне тяжёлым заболеванием, требующим неотложного хирургического вмешательства.
Лечение асцита должно начинаться как можно раньше и проводиться только опытным врачом, так как в противном случае возможно прогрессирование заболевания и развитие грозных осложнений. В первую очередь необходимо определить стадию асцита и оценить общее состояние пациента. Если на фоне напряженного асцита у больного развиваются признаки дыхательной недостаточности или сердечной недостаточности, первостепенной задачей будет уменьшение количества асцитической жидкости и снижение давления в брюшной полости. Если же асцит транзиторный или умеренный, а имеющиеся осложнения не представляют непосредственной угрозы для жизни пациента, на первый план выходит лечение основного заболевания, однако при этом регулярно контролируется уровень жидкости в брюшной полости.
Свободную жидкость несложно удалить из брюшной полости – но причины возникновения асцита останутся. Поэтому полноценным лечением асцита является лечение заболеваний, спровоцировавших его возникновение.
Независимо от того, что спровоцировало асцит, общие назначения следующие:
- постельный или полупостельный (с подниманием с кровати только в случае физиологической необходимости) режим;
- ограничение, а в запущенных случаях – полное исключение натрия из пищи. Достигается ограничением (или исключением) употребления поваренной соли.
Если асцит возник из-за цирроза печени, то при снижении в крови количества натрия ограничивают и прием жидкости в разном виде (чай, соки, супы) – до 1 литра.
Медикаментозная терапия зависит из болезни, спровоцировавшей асцит. Общим назначением, независимо от причины асцита, являются мочегонные препараты.
Это может быть или их комбинация с препаратами калия, или калий-сберегающие мочегонные. Также назначают:
- при циррозе печени – гепатопротекторы (препараты, защищающие клетки печени);
- при низком количестве белка в крови – белковые препараты, которые вводят внутривенно капельно. Как пример – альбумин, свежезамороженная плазма (ее вводят, если при асците наблюдаются нарушения со стороны свертывающей системы крови);
- при сердечно-сосудистой недостаточности – препараты, поддерживающие работу сердца (их подбирают в зависимости от того, какова причина сбоя)
Хирургические методы лечения асцита применяют при:
- значительном скоплении свободной жидкости в брюшной полости;
- если консервативные методы показывают низкую результативность или не показывают ее вообще.
Основные хирургические методы, которые применяют при асците, это:
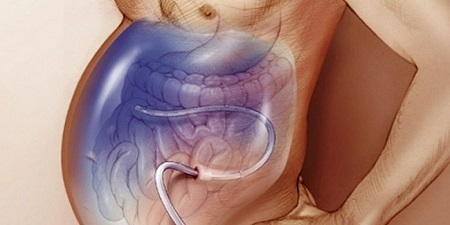
- Лапароцентез. Происходит удаление экссудата через прокол полости живота под контролем УЗИ. После операции устанавливается дренаж. За одну процедуру удаляется не более 10 л воды. Параллельно пациенту вводят капельно солевые растворы и альбумин. Осложнения очень редки. Иногда в месте прокола происходят инфекционные процессы. Не проводится процедура при нарушениях свертываемости крови, сильном вздутии живота, травмах кишечника, ветральной грыже и беременности.
- Трансъюгулярное внутрипеченочное шунтирование. Во время операции искусственным путем сообщаются печеночная и воротная вены. У пациента могут возникнуть осложнения в виде внутрибрюшного кровотечения, сепсиса, артериовенозного шунтирования, инфаркта печени. Не назначают операцию, если у больного присутствуют внутрипеченочные опухоли или кисты, окклюзия сосудов, обтурация желчных протоков, сердечно-легочные патологии.
- Трансплантация печени. Если асцит развился на фоне цирроза печени, то может быть назначена пересадка органа. Шанс на такую операцию выпадает немногим пациентам, поскольку донора найти сложно. Абсолютными противопоказаниями к трансплантации являются хронические инфекционные патологии, тяжелые нарушения работы других органов, онкологические заболевания. Среди самых тяжелых осложнений – отторжение трансплантата.
Причиной образования асцитической жидкости при опухоли может быть сдавливание кровеносных и лимфатических сосудов брюшной полости, а также поражение брюшины опухолевыми клетками. В любом случае для эффективного лечения заболевания необходимо полностью удалить злокачественное новообразование из организма.
В лечении онкологических заболеваний может применяться:
- Химиотерапия. Химиотерапия является основным методом лечения канцероматоза брюшины, при котором опухолевые клетки поражают оба листка серозной оболочки брюшной полости. Назначаются химические препараты (метотрексат, азатиоприн, цисплатин), которые нарушают процессы деления опухолевых клеток, тем самым приводя к уничтожению опухоли. Основной проблемой при этом является тот факт, что данные средства нарушают также деление нормальных клеток во всем организме. В результате этого в период лечения у пациента могут выпадать волосы, могут появляться язвы желудка и кишечника, может развиться апластическая анемия (недостаток красных клеток крови вследствие нарушения процесса их образования в красном костном мозге).
- Лучевая терапия. Суть данного метода заключается в высокоточном воздействии радиацией на опухолевую ткань, что приводит к гибели опухолевых клеток и уменьшению размеров новообразования.
- Хирургическое лечение. Заключается в удалении опухоли посредством хирургической операции. Данный метод особенно эффективен при доброкачественных опухолях либо в том случае, когда причиной асцита является сдавливание кровеносных или лимфатических сосудов растущей опухолью (ее удаление может привести к полному выздоровлению пациента).
Лечения хронических болезней почек, которые могут стать причиной асцита, практически всегда сложный и длительный процесс. В зависимости от конкретного вида заболевания, решается вопрос о необходимости назначения гормонов-глюкокортикостероидов, проведения операции по коррекции пороков, постоянного гемодиализа или другого лечебного мероприятия. Однако общие принципы терапии данных патологий едины. К ним относятся следующие рекомендации:
- Ограничение соли. Так как при нарушении почечных функций нарушается выведение электролитов, прием даже небольшого количества соли может привести к задержке жидкости и повышению артериального давления. Максимально допустимая доза при данных заболеваниях – не более 1 г/сут. Такого количества можно достичь, употребляя пресную пищу и неподсоленные напитки.
- Регулярный контроль токсических веществ в крови. Это мероприятие помогает предотвратить развитие тяжелых осложнений, таких как повреждение мозга (энцефалопатия).
- Поддержание достаточного диуреза. При хроническом повреждении органа, у человека в крови начинают накапливаться токсичные вещества. Именно они приводят к нарушениям сна, постоянной слабости, снижению работоспособности и плохому самочувствию. Поэтому важно регулярно использовать мочегонные средства, для улучшения выведения «шлаков».
- Уменьшение воспалительного процесса. При аутоиммунных заболеваниях, таких как гломерулонефрит, красная волчанка, ревматоидный артрит, необходимо снижать иммунные функции организма. За счет этого, почечные ткани будут повреждаться значительно меньше. Как правило, для этой цели используют гормоны-глюкокортикостероиды (Преднизолон, Дексаметазон) или препараты иммуносупрессанты (Сульфасалазин, Метотрексат).
- Прием нефропротекторных препаратов. Ингибиторы АПФ и БРА помимо защитного действия на сердце, обладают аналогичным действием на почки. Улучшая состояние их микрососудов, они профилактируют их дальнейшее повреждение и отдаляют от пациента гемодиализ.
Одним из основных этапов лечения асцита при циррозе печения является приостановление прогрессирования патологического процесса в ней и стимуляция восстановления нормальной печеночной ткани. Без соблюдения данных условий симптоматическое лечение асцита (применение мочегонных препаратов и повторные лечебные пункции) будет давать временный эффект, однако в конечном итоге все закончится смертью пациента.
Лечение цирроза печени включает:
- Гепатопротекторы (аллохол, урсодезоксихолевую кислоту) – препараты, улучшающие обмен веществ в клетках печени и защищающие их от повреждения различными токсинами.
- Эссенциальные фосфолипиды (фосфоглив, эссенциале) – восстанавливают поврежденные клетки и повышают их устойчивость при воздействии токсических факторов.
- Флавоноиды (гепабене, карсил) – нейтрализуют свободные радикалы кислорода и другие токсические вещества, образующиеся в печени при прогрессировании цирроза.
- Препараты аминокислот (гептрал, гепасол А) – покрывают потребность печени и всего организма в аминокислотах, необходимых для нормального роста и обновления всех тканей и органов.
- Противовирусные средства (пегасис, рибавирин) – назначаются при вирусном гепатите В или С.
- Витамины (А, В12, Д, К) – данные витамины образуются или депонируются (хранятся) в печени, а при развитии цирроза их концентрация в крови может значительно снижаться, что приведет к развитию ряда осложнений.
- Диетотерапию – рекомендуется исключить из рациона продукты, которые увеличивают нагрузку на печень (в частности жирную и жареную пищу, любые виды алкогольных напитков, чай, кофе).
- Пересадку печени – единственный метод, позволяющий радикально решить проблему цирроза. Однако стоит помнить, что даже после успешной пересадки следует выявить и устранить причину возникновения заболевания, так как в противном случае цирроз может поразить и новую (пересаженную) печень.
Прогноз при асците во многом определяется основным заболеванием. Он считается серьёзным, если, вопреки проводимому лечению, объём жидкости в брюшной полости продолжается быстрыми темпами увеличиваться. Прогностическое значение самого асцита состоит в том, что его нарастание усугубляет тяжесть основного заболевания.
источник
Асцит — это состояние, при котором в брюшной полости появляется свободная жидкость в больших количествах.
Асцит является следствием цирроза печени в 75%; злокачественных новообразований — в 10%; сердечной недостаточности в 5% случаев.
В клинической картине у пациентов отмечается вздутие живота и прогрессирующее нарастание веса.
Диагноз основывается на результатах физикального и визуализирующих (рентгенологических, ультразвуковых) методов исследования.
Лечение заключается в назначении бессолевой диеты, диуретиков. Больным может производиться терапевтический лапароцентез, выполняются хирургические вмешательства. Пациенты с асцитом — кандидаты на трансплантацию печени.
Наиболее частым осложнением асцита является спонтанный бактериальный перитонит . Он возникает при инфицировании асцитической жидкости, которое в 90% случаев происходит спонтанно. У больных появляются боли в животе, повышается температура тела.
Для диагностики этого осложнения производится исследование асцитической жидкости. Для лечения спонтанного бактериального перитонита назначаются антибактериальные препараты.
- Классификация асцита
Асцит классифицируется в зависимости от количества жидкости, наличия инфицирования асцитической жидкости и варианту ответа на медикаментозную терапию.
- По количеству жидкости в брюшной полости:
- Небольшое количество жидкости.
- Умеренное количество жидкости.
- Значительное количество жидкости (напряженный, массивный асцит).
- По инфицированности содержимого:
- Стерильное содержимое.
- Инфицированное содержимое.
- Спонтанный бактериальный перитонит.
- По варианту ответа на медикаментозную терапию:
- Асцит поддающийся медикаментозной терапии.
- Рефрактерный асцит.
Асцит, который не может быть устранен, или ранний рецидив которого не может быть адекватно предотвращен лечением.
- Асцит, резистентный к диуретикам: асцит, рефрактерный к диете с ограничением натрия и интенсивной терапии диуретиками ( спиронолактон 400 мг/день, фуросемид 160 мг/день в течение не менее 1 недели; диета с ограничением поваренной соли менее 5,2 г/день).
- Асцит, не контролированный диуретиками: асцит, рефрактерный к терапии из-за развития вызванных диуретиками осложнений, которые препятствуют применению эффективных дозировок диуретиков.
- Эпидемиология асцита
Асцит является следствием цирроза печени в 75%; злокачественных новообразований — в 10%; сердечной недостаточности — в 5% случаев.
Примерно у половины пациентов с циррозом печени асцит развивается в течение 10 лет от начала заболевания. Он обусловлен нарушениями почечной функции, портального и висцерального кровообращения.
Примерно 50% пациентов с цирротическим асцитом умирают в течение 2 лет от начала заболевания. Показатели однолетней выживаемости у больных с асцитом, резистентным к терапии, составляют 50%.
У здоровых мужчин внутриперитонеальная жидкость обнаруживается в меньших количествах, чем у женщин, у которых ее объем составляет примерно 20 мл (в зависимости от фазы менструального цикла). При асците этот объем значительно увеличивается.
Частота возникновения спонтанного бактериального перитонита составляет 15-20%.
- Этиология и факторы риска развития асцита
- Факторы риска при отсутствии патологических процессов в брюшине.
- Портальная гипертензия (градиент концентрации альбумина сыворотка-асцит ≥11 г/л).
- Цирроз печени .
- Алкогольный гепатит.
- Фулминантная печеночная недостаточность.
- Метастазы в печень .
- Хроническая сердечная недостаточность .
- Констриктивный перикардит .
- Синдром Бадда-Киари .
- Обструкция нижней полой вены.
- Гипоальбуминемия (градиент концентрации альбумина сыворотка-асцит
Размер пор внутренних капилляров в 50-100 раз меньше, чем печеночных синусоидов, поэтому градиент транссинусоидального онкотического давления в печени почти нулевой, в то время как в печеночной циркуляции он равняется 0,8-0,9. Высокий градиент онкотического давления минимизирует влияние любых изменений концентрации альбумина плазмы на трансмикроваскулярный обмен жидкостью.
У пациентов с алкогольным циррозом на поверхности эндотелия синусоидов происходит отложение иммуноглобулина А, что приводит к еще большему снижению его проницаемости.
На поздних стадиях цирроза печени поры в эндотелии синусоидов исчезают, его проницаемость снижается. Возникает градиент давления между интерстициальными пространствами гепатоцитов и просветом синусоидов.
Кроме того, при портальной гипертензии происходит увеличение уровня оксида азота (NO) в организме, который также способствует вазодилатации висцеральных и периферических сосудов. Доказательством этому служит тот факт, что у пациентов с асцитом в печеночной артерии обнаруживается повышение активности NO синтазы.
Недостаточности лимфатической системы.
Ведущая роль в формировании асцита у больных циррозом печени принадлежит недостаточности лимфатической системы.
В печени формируется до 70% всей лимфы организма, которая через систему грудного лимфатического протока транспортируется в венозную систему большого круга кровообращения. Из-за декомпенсации венозной системы печени при циррозе, становится невозможной перфузия необходимого количества портальной крови через больную печень. При этом резко возрастает нагрузка на систему лимфооттока, которая вынужденно возмещает недостаточность венозного оттока и отводит максимально возможное количество жидкости от органа в виде «печёночной» лимфы. Отток лимфы от печени достигает 15-20 л/сут и более при норме 8-9 л.
Усиленное функционирование лимфатической системы способствует разгрузке венозной сети, но в дальнейшем развивается динамическая недостаточность лимфообращения. На определенном этапе болезни лимфатическая система перестаёт справляться с запредельной нагрузкой. Лимфатические капилляры, мелкие сосуды и магистральные стволы расширяются, возникает дезорганизация нормальной микролимфоциркуляции на уровне лимфангионов, нарастает застой лимфы, развивается лимфатическая гипертензия. Эти процессы приводят к пропотеванию жидкости с поверхности печени в брюшную полость и к появлению асцита.
Некоторое время эта жидкость может адекватно всасываться париетальной брюшиной, но и эти компенсаторные возможности не могут быть беспредельными, так как за перемещение жидкости из брюшной полости и возврат её в сосудистое русло отвечает всё та же система лимфооттока, которая к моменту развития асцита находится в состоянии суб (а чаще де-) компенсации, и дополнительная нагрузка в виде увеличения количества жидкости, которую необходимо переместить из брюшной полости, приводит к полной её несостоятельности.
Патологические изменения в системы ренин-ангиотензин-альдостерона.
Патологические процессы в печени при развитии цирроза проходят с участием системы ренин-ангиотензин-альдостерона.
Накопление асцитической жидкости приводит к снижению эффективного объема плазмы, что стимулирует секрецию ренина в юкстагломерулярном аппарате почек. Ренин усиливает синтез ангиотензина I, который превращается в ангиотензин II. Ангиотензин II приводит к снижению гломерулярной фильтрации и почечного кровотока, повышает секрецию антидиуретического гормона гипофиза и альдостерона надпочечников.
Под влиянием альдостерона у больных циррозом печени усиливается реабсорбция натрия и экскреция калия в дистальных отделах почечных канальцев и возрастает реабсорбция натрия и воды в проксимальных отделах.
Повышенная потеря калия и водорода на фоне гиперальдостеронизма способствует снижению содержания калия, магния в сыворотке крови и метаболическому алкалозу. При этом у большинства больных развивается гипонатриемия, так как большая часть натрия переходит в интерстициальную и асцитическую жидкость.
Таким образом, вследствие гемодинамических нарушений (недостаточного наполнения центрального венозного и артериального русла) происходит активация ренин-ангиотензин-альдостероновой системы. Все это приводит к реабсорбции натрия в канальцах почек и задержке воды в организме.
Накопление асцитической жидкости в брюшной полости отражает состояние водно-электролитного обмена в организме. Одним из ключевых звеньев патогенеза почечной дисфункции и задержки натрия при циррозе являются расстройства системного висцерального кровообращения (вазодилатация), возникающими вследствие портальной гипертензии .
Параллельно происходит развитие почечной вазоконстрикции у пациентов с циррозом печени, которое связано с повышением симпатической активности почек и ренин-ангиотензиновой системы для поддержания артериального давления при системной вазодилатации. Сниженный почечный кровоток снижает скорость клубочковой фильтрации и секрецию натрия.
Цирроз печени сопровождается повышенной реабсорбцией натрия в проксимальных и дистальных канальцах, на что также влияет увеличение концентрации циркулирующего альдостерона.
При компенсированном циррозе задержка натрия может возникать в отсутствие вазодилатации и гиповолемии. Синусоидальная портальная гипертензия может снижать почечный кровоток, не сопровождаясь гемодинамическими изменениями системной циркуляции, вследствие, так называемого, гепаторенального рефлекса.
Гемодинамические сдвиги изменяются с положением тела. Установлены выраженные постуральные колебания секреции натрийуретического пептида и системной гемодинамики: в положении лежа увеличиваются сердечный выброс и вазодилатация.
Несомненно, существуют и другие механизмы развития асцитического синдрома, о которых мы пока не знаем или не можем оценить степень их значимости. Например, доказано, что при циррозах печени отмечается повышение тонуса симпатической нервной системы, повышены уровни эпинефрина и норэпинефрина, нарушен синтез и метаболизм кининов, простагландинов, предсердного натрийуретического фактора.
источник
Скопление жидкости в животе называют водянкой или асцитом. Патология не является самостоятельной болезнью, а лишь следствием других заболеваний. Чаще – это осложнение рака (цирроза) печени. Прогрессирование асцита повышает объем жидкости в полости живота, и она начинает давить на органы, что усугубляет протекание заболевания. По статистике, каждая третья водянка заканчивается летальным исходом.
Симптоматическое явление, при котором в брюшине собирается транссудат или экссудат, называют асцитом. Полость живота вмещает в себя часть кишечника, желудок, печень, желчный пузырь, селезенку. Она ограничивается брюшиной – оболочкой, которая состоит из внутреннего (прилегающего к органам) и внешнего (прикрепленного к стенкам) слоя. Задача полупрозрачной серозной оболочки – фиксировать внутренние органы и участвовать в метаболизме. Брюшина обильно снабжена сосудами, которые обеспечивают обмен веществ через лимфу и кровь.
Между двумя слоями брюшины у здорового человека присутствует определенный объем жидкости, которая постепенно всасывается в лимфатические узлы, чтобы освободить пространство для поступления новой. Если по каким-либо причинам повышается скорость образования воды или замедляется его всасывание в лимфу, то транссудат начинает в брюшине накапливаться. Такой процесс может происходить по причине множественных патологий, о которых речь пойдет ниже.
Часто возникает асцит брюшной полости при онкологии и многих других заболеваниях, когда нарушается барьерная и секреторная функция листков брюшины. Это приводит к заполнению жидкостью всего свободного пространства живота. Постоянно увеличивающийся экссудат может доходить до 25 литров. Как уже упоминалось, основная причина поражения брюшной полости – это ее тесный контакт с органами, в которых образуется злокачественная опухоль. Плотное прилегание складок брюшины друг к другу обеспечивает быстрый захват близлежащих тканей раковыми клетками.
Основные причины асцита брюшной полости:
- перитонит;
- мезотелиома брюшины;
- перитонеальный карциноз;
- рак внутренних органов;
- полисерозит;
- портальная гипертензия;
- цирроз печени;
- саркоидоз;
- гепатоз;
- тромбоз печеночных вен;
- венозный застой при правожелудочковой недостаточности;
- сердечная недостаточность;
- микседема;
- болезни ЖКТ;
- занос атипичных клеток в брюшину.
Жидкость внутри брюшной полости у женского населения не всегда является патологическим процессом. Она может собираться во время эякуляции, которая происходит ежемесячно у женщин репродуктивного возраста. Такая жидкость рассасывается самостоятельно, не представляя опасности для здоровья. Помимо этого причиной возникновения воды нередко становятся чисто женские заболевания, требующие незамедлительного лечения – воспаление репродуктивной системы или внематочная беременность.
Провоцируют развитие асцита внутрибрюшные опухоли или внутренние кровотечения, например, после перенесенной операции, из-за травмы или кесарева сечения. Когда эндометрий, выстилающий полость матки, бесконтрольно разрастается, из-за чего выходит за пределы женского органа, то в брюшине тоже собирается вода. Эндометриоз часто развивается после перенесенных вирусных или грибковых инфекций половой системы.
Во всех случаях возникновения водянки у представителей сильного пола лежит в основе сочетание нарушений важных функций организма, которые приводят к накоплению экссудата. Мужчины нередко злоупотребляют спиртными напитками, что приводит к циррозу печени, а это заболевание провоцирует асцит. Также возникновению заболевания способствуют такие факторы, как переливание крови, инъекции наркотических препаратов, высокий уровень холестерина вследствие ожирения, множественный татуаж на теле. Помимо этого, причиной водянки у мужчин становятся следующие патологии:
- туберкулезной поражение брюшины;
- эндокринные нарушения;
- ревматоидный артрит, ревматизм;
- красная волчанка;
- уремия.
Жидкость в животе собирается не только у взрослых, но и у детей. Чаще асцит у новорожденных возникает из инфекционных процессов, происходящих в организме матери. Как правило, болезнь развивается еще в утробе. У плода могут наблюдаться дефекты печени и/или желчевыводящих путей. Из-за этого застаивается желчь, что приводит к водянке. После рождения у грудного ребенка асцит может развиваться на фоне:
- сердечно-сосудистых нарушений;
- нефротического синдрома;
- хромосомных отклонений (болезнь Дауна, синдром Патау, Эдвардса или Тернера);
- вирусных инфекций;
- гематологических неполадок;
- врожденных опухолей;
- серьезного нарушения метаболизма.
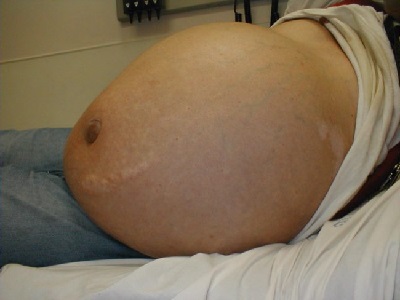
Признаки асцита брюшной полости зависят от того, насколько быстро собирается асцитическая жидкость. Симптомы могут проявиться в один день или на протяжении нескольких месяцев. Самый явный признак водянки – увеличение брюшной полости. Это вызывает увеличение массы тела и необходимость в одежде большего размера. У больного при вертикальном положении живот свисает вниз по типу фартука, а при горизонтальном – распластан по двум сторонам. При большом объеме экссудата выпячивается пупок.
Если причиной водянки стала портальная гипертензия, то на передней брюшине образуется венозный рисунок. Он возникает вследствие варикозного расширения околопупочных вен и варикоза пищевода. При большом скоплении воды в животе повышается внутреннее давление, вследствие чего диафрагма перемещается в брюшную полость, а это провоцирует дыхательную недостаточность. У больного ярко выражена одышка, тахикардия, цианоз кожных покровов. Существуют и общие симптомы асцита:
- боль или чувство распирания внизу живота;
- диспепсия;
- флюктуация;
- периферические отеки на лице и конечностях;
- запоры;
- тошнота;
- изжога;
- потеря аппетита;
- замедленные движения.
В клинической практике выделяют 3 стадии водянки живота, каждая из которых имеет свои признаки и особенности. Степени развития асцита:
- Транзиторный. Начальное развитие болезни, симптомы которой самостоятельно заметить невозможно. Объем жидкости не превышает 400 мл. Лишняя вода выявляется лишь во время инструментальных исследований (ультразвукового обследования брюшной полости или МРТ). При таких объемах экссудата работа внутренних органов не нарушается, поэтому больной не замечает у себя никаких патологических симптомов. На начальной стадии водянка успешно поддается лечению, если пациент соблюдает водно-солевой режим и придерживается специально назначенного питания.
- Умеренный. На этой стадии живот становится большего размера, а объемы жидкости достигают 4 литров. Больной уже замечает тревожные симптомы: вес увеличивается, становится трудно дышать, особенно в лежачем положении. Врач легко определяет водянку при осмотре и пальпации брюшной полости. Патология и на этой стадии хорошо поддается лечению. Иногда возникает необходимость удаления жидкости из полости живота (пункция). Если вовремя не проведена эффективная терапия, то возникает нарушение работы почек, развивается самая тяжелая стадия болезни.
- Напряженный. Объемы жидкости превышают 10 литров. В брюшной полости сильно повышается давление, возникают проблемы с функционированием всех органов желудочно-кишечного тракта. Состояние больного ухудшается, ему требуется незамедлительная медицинская помощь. Проводимая ранее терапия уже не дает нужного результата. На этой стадии обязательно проводится лапароцентез (прокол брюшной стенки) в составе комплексной терапии. Если процедура не дает эффекта, развивается рефрактерный асцит, который уже не поддается лечению.
Заболевание само по себе является стадией декомпенсации (осложнением) других патологий. К последствиям водянки относят образование паховых или пупочных грыж, выпадение прямой кишки или геморроидальных узлов. Этим состояниям способствует повышение внутрибрюшного давления. Когда диафрагма давит на легкие, то это ведет к дыхательной недостаточности. Присоединение вторичной инфекции приводит к перитониту. К другим осложнениям асцита относят:
- массивные кровотечения;
- печеночную энцефалопатию;
- тромбоз селезеночной или воротной вены;
- гепаторенальный синдром;
- кишечную непроходимость;
- диафрагмальную грыжу;
- гидроторакс;
- воспаление брюшины (перитонит);
- смертельный исход.
Перед постановкой диагноза врач должен убедиться, что увеличение живота не является следствием других состояний, к примеру, беременности, ожирения, кисты брыжейки или яичника. Исключить другие причины поможет пальпация и перкуссия (пальцем по пальцу) брюшины. Осмотр больного и собранный анамнез сочетается с ультразвуковым исследованием, сканированием селезенки и печени. При УЗИ исключается жидкость в желудке, опухолевые процессы в органах брюшины, характеризуется состояние паренхимы, диаметр портальной системы, размеры селезенки и печени.
Сцинтиграфия печени и селезенки – это метод лучевой диагностики, используемый для оценки работы тканей. Инициализация позволяет определить положение и размеры органов, диффузные и очаговые изменения. Все больные с выявленным асцитом направляются на проведение диагностического парацентеза с исследованием асцитической жидкости. Во время изучения плеврального выпота подсчитывается число клеток, количество осадка, альбумина, белка, проводится посев и окраска по Граму. Проба Ривальта, дающая химическую реакцию на белок, помогает отличить экссудат от транссудата.
Двухмерная допплероскопия (УЗДГ) венозных и лимфатических сосудов помогает оценить в сосудах портальной системы кровоток. При сложно дифференцируемых случаях асцита дополнительно проводится диагностическая лапароскопия, при которой в полость живота вводится эндоскоп для точного определения количества жидкости, разрастания соединительной ткани, состояния кишечных петель. Определить объем воды поможет и обзорная рентгенография. Эзофагогастродуоденоскопия (ЭГДС) дает хорошую возможность увидеть наличие варикоза в желудке и пищеводе.
Независимо от причины, спровоцировавшей асцит, патология должна лечиться вместе с основным заболеванием. Различают три основных терапевтических метода:
- Консервативное лечение. На начальной стадии асцита назначается медикаментозная терапия, направленная на нормализацию работы печени. Если у пациента диагностирована паренхима органа воспалительного характера, то дополнительно прописываются лекарственные средства, которые снимают воспаление и другие виды медикаментов, в зависимости от симптоматики и заболевания, спровоцировавшего скопление жидкости.
- Симптоматическое. Если консервативное лечение не дает результатов или врачам не удается надолго продлить ремиссию, то больному назначается пункция. Лапароцентез брюшной полости при асците проводят нечасто, поскольку существует опасность повреждения стенок кишечника у пациента. Если жидкость слишком быстро заполняет живот, то больному устанавливают перитонеальный катетер, чтобы предотвратить развитие спаечного процесса.
- Хирургическое. Если две предыдущих схемы лечения не помогают, то пациенту назначается специальная диета и переливание крови. Метод состоит в соединении воротниковой и нижней полой вены, при котором создается коллатеральное кровообращение. Если больному нужна трансплантация печени, то ему проводится операция после курса диуретиков.
Основной метод лечения асцита – медикаментозная терапия. Она включает длительный прием мочегонных препаратов с введением солей калия. Доза и продолжительность лечения индивидуальна и зависит от темпа потери жидкости, что определяется по ежедневному снижению массы тела и визуально. Правильная дозировка – важный нюанс, поскольку неправильное назначение может привести больного к сердечной недостаточности, отравлению, смерти. Часто назначаемые препараты:
- Диакарб. Системный ингибитор карбоангидразы, имеющий слабую диуретическую активность. В результате применения увеличивается выделение воды. Препарат вызывает выведение из организма магния, фосфатов, кальция, что может привести к метаболитическим нарушениям. Дозировка индивидуальна, применяется строго по назначению врача. Нежелательные эффекты наблюдаются со стороны кроветворения, иммунной и нервной системы, обмена веществ. Противопоказанием для приема лекарственного средства является острая почечная и печеночная недостаточность, уремия, гипокалиемия.
- Фуросемид. Петлевой диуретик, вызывающий сильный, но кратковременный диурез. Оказывает выраженное натрийуретическое, мочегонное, хлоруретическое действие. Режим и длительность приема назначает врач, в зависимости от показаний. Среди побочных эффектов: выраженное снижение артериального давления, головная боль, вялость, сонливость, снижение потенции. Не назначают Фуросемид при острой почечной/печеночной недостаточности, гиперурикемии, беременности, лактации, детском возрасте до 3 лет.
- Верошпирон. Калийсберегающий диуретик пролонгированного действия. Подавляет калийвыводящий эффект, препятствует задержке воды и натрия, снижает кислотность мочи. Диуретический эффект появляется на 2-5 день лечения. При отеках на фоне цирроза суточная дозировка составляет 100 мг. Длительность лечения выбирается индивидуально. Нежелательные реакции: заторможенность, атаксия, гастрит, запор, тромбоцитопения, нарушения менструального цикла. Противопоказания: болезнь Аддисона, анурия, непереносимость лактозы, гиперкалиемия, гипонатриемия.
- Панангин. Лекарство, влияющее на метаболические процессы, являющееся источником ионов магния и калия. Применяется в составе комплексной терапии при асците, чтобы восполнить дефицит магния и калия, выводимых во время приема диуретиков. Назначают по 1-2 таблетки/сутки на протяжения всего курса мочегонных препаратов. Побочные действия возможны со стороны водно-электролитного баланса, пищеварительной системы. Не назначают Панангин при наличии болезни Аддисона, гиперкалиемии, гипермагниемии, тяжелой миастении.
- Аспаркам. Источник ионов магния и калия. Снижает проводимость и возбудимость миокарда, устраняет дисбаланс электролитов. Во время приема мочегонных препаратов назначают по 1-2 таблетки 3 раза/сутки в течение 3-4 недель. Возможно развитие рвоты, диареи, покраснения кожи лица, угнетения дыхания, судорог. Не назначают Аспаркам при нарушении обмена аминокислот, недостаточности коры надпочечников, гиперкалиемии, гипермагниемии.
При брюшной водянке нужен ограниченный рацион. Диета предусматривает небольшое потребление жидкости (750-1000 литров/сутки), полный отказ от потребления соли, включение в рацион натуральных пищевых продуктов с мочегонным действием и достаточного количества белка. Исключаются полностью соления, маринады, копчености, консервы, соленая рыба, колбасные изделия.
В меню пациента с асцитом должны присутствовать:
- постное мясо птицы, кролика;
- бобовые, орехи, соевое молоко;
- морепродукты, нежирная рыба;
- коричневый рис, овсяные хлопья;
- растительные масла, семечки;
- кисломолочные продукты, творог;
- петрушка, тмин, майоран, шалфей;
- перец, лук, чеснок, горчица;
- лавровый лист, лимонный сок, гвоздика.
Когда асцит прогрессирует и не помогает лечение, то в особо запущенных случаях назначается хирургическое лечение. К сожалению, далеко не всегда даже с помощью операции удается сохранить пациенту жизнь, но других методов на сегодняшний день не существует. Самое распространенное хирургическое лечение:
- Лапароцентез. Происходит удаление экссудата через прокол полости живота под контролем УЗИ. После операции устанавливается дренаж. За одну процедуру удаляется не более 10 л воды. Параллельно пациенту вводят капельно солевые растворы и альбумин. Осложнения очень редки. Иногда в месте прокола происходят инфекционные процессы. Не проводится процедура при нарушениях свертываемости крови, сильном вздутии живота, травмах кишечника, ветральной грыже и беременности.
- Трансъюгулярное внутрипеченочное шунтирование. Во время операции искусственным путем сообщаются печеночная и воротная вены. У пациента могут возникнуть осложнения в виде внутрибрюшного кровотечения, сепсиса, артериовенозного шунтирования, инфаркта печени. Не назначают операцию, если у больного присутствуют внутрипеченочные опухоли или кисты, окклюзия сосудов, обтурация желчных протоков, сердечно-легочные патологии.
- Трансплантация печени. Если асцит развился на фоне цирроза печени, то может быть назначена пересадка органа. Шанс на такую операцию выпадает немногим пациентам, поскольку донора найти сложно. Абсолютными противопоказаниями к трансплантации являются хронические инфекционные патологии, тяжелые нарушения работы других органов, онкологические заболевания. Среди самых тяжелых осложнений – отторжение трансплантата.
Присоединение к основной болезни асцита значительно утяжеляет ее течение и ухудшает прогноз выздоровления. Особенно неблагоприятна патология для пациентов старшего возраста (после 60 лет), у которых в анамнезе почечная недостаточность, гипотония, сахарный диабет гептоцеллюлярная карцинома, печеноклеточная недостаточность или цирроз печени. Двухлетняя выживаемость таких больных составляет не более 50%.
источник
- Портальная гипертензия (градиент концентрации альбумина сыворотка-асцит ≥11 г/л).
Этиология асцита в 90% случаев связана с хроническими заболеваниями печени: портальной гипертензией (развившейся вследствие цирроза печени ), алкогольным гепатитом, обструкцией печеночной вены (синдром Бадда-Киари).
Непеченочными причинами асцита могут быть: заболевания сердца ( сердечная недостаточность , констриктивный перикардит), злокачественные новообразования (карциноматоз, псевдомиксома брюшины), заболевания брюшины (инфекционный перитонит), выраженная гипоальбуминемия (нефротический синдром), другие болезни (опухоли и кисты яичников, панкреатит , саркоидоз , системная красная волчанка, микседема).
Факторы риска возникновения асцита: