Заболевания печени часто приводят к тяжелым осложнениям. Среди них можно выделить наиболее опасное для жизни — цирроз. При этом состоянии патология печени сочетается с недостаточностью других органов и систем. Усугубляет цирроз развитие асцита, который возникает у половины пациентов в течение 10 лет от постановки диагноза. Ухудшение качества жизни, увеличение смертности от этой сочетанной патологии заставляет глубже разобраться в проблеме.
Асцит — это патология, характеризующаяся скоплением жидкости в брюшной полости. В народе эту болезнь называют водянкой, у больного увеличивается объем живота, появляются неприятные симптомы и боли.
Современная классификация разделяет асциты по 3 характерным признакам: объему экссудата (жидкого содержания), наличию микроорганизмов в жидкости, возможностям медикаментозной терапии.
По количеству внутрибрюшной жидкости:
- небольшое (определяется на УЗИ);
- умеренное (растяжение живота при осмотре специалистом);
- значительное (выраженное, отчетливо видное, симметричное увеличение объема брюшной полости).
По инфицированности экссудата:
- стерильный;
- инфицированный;
- спонтанный перитонит бактериальной природы.
По ответу на применяемую терапию:
- поддающийся лечению
- устойчивый асцит, который не устраняется диуретиками.
Образование и прогрессирование асцита при циррозе печени происходит под действием разнообразных факторов.
Патогенез этого патологического процесса до конца не изучен, основными механизмами принято считать выход жидкости из кровяного русла и портальную гипертензию.
Осложненные поражения печени характеризуются значительным снижением функционирующих гепатоцитов. Орган перестает выполнять свои функции.
В клетках печени уменьшается синтез альбуминов. Эти белки удерживают жидкость в сосудистом русле. При снижении их концентрации происходит уменьшение объема циркулирующей крови за счет появления избыточного инфильтрата в полостях. Чтобы восстановить артериальный кровоток происходит усиленная компенсаторная выработка альдостерона, что приводит к задержке жидкости в организме и способствует усугублению отеков.
Второй компонент в патогенезе развития асцита – портальная гипертензия. Увеличение давления в системе воротной вены при системной гипотензии способствует проникновению жидкости из кровяного русла в свободное пространство полостей.
Важным звеном патогенеза можно считать усиленную лимфопродукцию в печени. Это создает нагрузку на систему лимфатических сосудов. При её несостоятельности избыточное давление выталкивает лишнюю жидкость в брюшную полость.
У пациента определяются признаки выраженного поражения печени. Ухудшается общее состояние, нарастает утомляемость.
Возможны спонтанные кровотечения: пищеводные, носовые, желудочные, кишечные. Появляются печеночные знаки: сосудистые телеангиоэктазии (звездочки) на верхней части тела, эритема (покраснение) ладоней. Из-за снижения иммунитета повышается вероятность инфекционных заболеваний.
Пациенты с асцитом при циррозе печени на начальной стадии могут не предъявлять специфических жалоб. С нарастанием отека становится видимым увеличение живота, кожа натягивается, на ней появляется венозная сетка. Прогрессирование асцита влечет за собой нарушение дыхания, мочеиспускания, расстройство пищеварения. Большой объем жидкости является причиной развития сердечной недостаточности.
Характерный симптомокомплекс позволяет заподозрить начало развития асцита при циррозе печени. Инструментальные методы обследования помогут подтвердить этот диагноз. Даже небольшое количество жидкости выявляется с помощью УЗИ. Помимо этого, можно оценить степень поражения органов брюшной полости, диаметр портальных сосудов.
Увеличение размеров селезенки чаще всего свидетельствует о возможности портальной гипертензии.
Для углубленного изучения характера кровотока по венозной системе используют допплерографию. Можно оценить проходимость сосудов, скорость движения крови и давление в них. При асците эти показатели значительно отличаются от нормы.
Наиболее информативным методом при асците является парацентез – пункция брюшной полости с забором инфильтрата. Помимо количественных показателей объема жидкости можно определить качественные характеристики: наличие эритроцитов, лейкоцитов, белка, бактериальных клеток, ферментов.
Лечение асцита при циррозе печени можно проводить 3 путями: народными средствами, лекарственными препаратами, хирургическими методами. Важно внимательно следить за течением патологического процесса. При малейших признаках прогрессирования заболевания нужно пересмотреть проводимую терапию с целью коррекции. Возможно, потребуются изменения в дозировках, действующих веществах или схемах лечения. Иногда требуется переход от консервативной медицины к оперативной.
Какой бы ни была терапия, начинать нужно с общих для всех пациентов рекомендаций. Строгий постельный режим показан только больным с тяжелым асцитом. Для остальных рекомендовано ограничение физической активности. Минимальное употребление поваренной соли (до 5 грамм в сутки) помогает создать отрицательный баланс натрия в организме и улучшить возврат жидкости из брюшной полости в сосудистое русло. Ограничение потребления воды может отрицательно сказаться на уровне артериального давления, усугубляя центральную гипотензию.
Лечение «брюшной водянки» народными средствами проводили целители с давних времен. Они назначали растительные вещества для приема внутрь или наружно. Их можно считать достаточно безопасными.
Однако, никаких исследований эффективности не проводилось. Поэтому народные средства применяются на свой страх и риск.
Сильным мочегонным эффектом обладает отвар из сухих стручков фасоли. Для приготовления достаточно томить их на водяной бане в течение 20 минут. Потом жидкость процеживают, остужают и пьют равными порциями 3 раза в день.
К известным народным средствам относятся плоды абрикоса. Ими можно не только лечить асцит, но и восполнять потерю микроэлементов в организме, в частности, калия. Используют концентрированный отвар из свежих плодов или из кураги. В сутки можно пить до 500 мл полученной жидкости.
Для удаления асцетического содержимого из брюшной полости можно использовать петрушку. Народный рецепт заключается в следующем: листья растения отваривают 15–20 минут и пьют полученный охлажденный напиток на протяжении дня
Большим потенциалом для лечения застойных явлений обладают березовые листья. Их можно использовать в виде ванн, обертываний, отвара.
Ванны разделяются на сухие и традиционные. При первой методике молодые листья на несколько часов оставляют на солнце для того, чтобы они выпустили сок. Потом их складывают в ванну, туда усаживают больного с асцитом и оставляют на час. Традиционные процедуры проводят с березовым отваром, который добавляют в теплую воду. Длительность составляет 30 минут.
Проведение обертываний заключается в следующем: хлопчатобумажную ткань пропитывают отваром листьев березы. После этого больного заворачивают в нее. Процедуру делают каждый день по одному часу.
Еще одно народное средство – отвар листьев березы. Его готовят на водяной бане, потом оставляют на 6 часов для настаивания. Продолжительность курса лечения составляет 14 дней.
Для усиления эффекта в березовый отвар можно добавить хвощ. Эти компоненты увеличивают мочегонные свойства друг друга. Принимать такую жидкость лучше с утра.
Для увеличения выведения жидкости через поры кожи используют горячие потогонные чаи. В народных рецептах применяют цветы липы и мать-и-мачехи. За счет свойств растений и высокой температуры отвара достигается усиленное потоотделение. Таким образом уменьшается количество экссудата в брюшной полости.
Традиционными препаратами для лечения асцита остаются диуретики. Наиболее эффективными из них являются: спиронолактон, фуросемид и буметанид.
Спиронолактон – препарат, уменьшающий действие альдостерона. Эффективен при начальной терапии асцитов. Минимальная доза 100 мг в сутки может быть увеличена в 4 раза для обеспечения адекватного диуреза. Эффект развивается в течение 3–5 дней после начала лечения. Во время применения спиронолактона важно контролировать электролитный состав крови.
Фуросемид – петлевой диуретик, обеспечивающий форсированный диурез. Средство применяется в комплексной терапии со спиронолактоном. Суточная дозировка фуросемида не должна быть больше 160 мг в сутки. Превышение данной дозы приводит к выраженным электролитным расстройствам.
При необходимости замены спиронолактона обычно используют буметанид.
У пациентов с асцитом применяют ступенчатую терапию. Ограничение потребления соли сочетают с минимальными дозами спиронолактона. При отсутствии эффекта дозировку препарата увеличивают, добавляют фуросемид. При назначении диуретиков обязателен контроль электролитов крови.
Для лечения устойчивого к лекарственным препаратам асцита используют прямые и косвенные методики. К прямым относятся: лапароцентез и перитонеовенозный шунт.
Лапароцентез осуществляется по средней линии живота с использованием специальной полой трубки – троакара. Его вводят в брюшную полость и через подсоединенный катетер удаляется избыток жидкости. При выполнении этой манипуляции толстой иглой есть риск повреждения кишечника (перфорации).
Перитонеовенозный шунт представляет собой клапан, односторонне открывающийся в венозное русло. Таким образом, при повышении давления в брюшной полости жидкость беспрепятственно вытекает в сосуды. При высоком венозном давлении клапан находится в закрытом состоянии. Эта оперативная манипуляция может осложняться инфекциями, тромбозом, воздушной эмболией. Поэтому хирургические методы используют при неэффективности консервативной терапии.
К косвенным оперативным методикам относятся: удаление селезенки, трансплантация печени, различные виды шунтирования, перевязка селезеночной артерии, лимфовенозное соустье.
Развитие асцита при циррозе печени и его прогрессирование являются крайне неблагоприятными признаками. Выживаемость у пациентов с такой патологией составляет 50% в течение 2 лет. Если асцит не поддается медикаментозной терапии, то продолжительность жизни — в среднем 6 месяцев. Консервативная терапия и народные средства могут улучшить самочувствие пациента, однако, в долгосрочной перспективе наиболее эффективным методом оказалась трансплантация печени.
источник
Патогенез цирроза печени тесно связан с его этиологией, что накладывает особый отпечаток и на характер морфологических изменений в печени. Этиологические факторы (алкоголь, вирусная инфекция, дефекты метаболизма и др.) вызывают некроз гепатоцитов. Определенное значение при этом имеют аутоиммунные реакции к печеночному липопротеиду. При массивных, субмассивных некрозах, а также при распространении некроза от центра дольки до портального тракта (мостовидный порто-центральный некроз) под действием внутрипеченочного давления наступает коллапс дольки — потеря пространства, которое ранее занимала паренхима. Восстановление печеночной ткани при этом становится невозможным. В результате сближаются портальные тракты и центральные вены, начинается разрастание соединительной ткани. Уцелевшие гепатоциты или фрагменты печеночных долек регенерируют и формируют узлы-регенераты, которые вместе с остатками сохранившейся паренхимы образуют псевдодольки. Псевдодольки представляют собой участки паренхимы, лишенные обычной радиальной ориентации трабекул к центральной вене. В центре псевдодолек в отличие от нормальных долек не обнаруживают центральных вен, а по периферии не выявляют портальных трактов.
Очаги регенерировавшей паренхимы и разросшиеся соединительнотканные тяжи сдавливают кровеносные сосуды, особенно тонкостенные печеночные вены, нарушается микроциркуляция, возникает облитерация венозных сосудов. Повышается внутри- печеночное давление (в 2—5 раз выше нормы), замедляется скорость портального кровотока, на 30—70 % снижается объемный кровоток в печени. Одновременно с этим соединительнотканные тяжи, постепенно врастая в глубь паренхимы, соединяют портальные тракты с центральной зоной дольки. В итоге печеночная долька фрагментируется, портальные сосуды соединяются с ветвями печеночной вены, образуя артериовенозные анастомозы (шунты). По этим анастомозам кровь из воротной вены направляется непосредственно в систему печеночной вены, минуя паренхиму печени, что резко нарушает оксигенацию и питание печеночных клеток и неизбежно ведет к появлению новых некрозов. Таким образом, прогрессирование цирроза печени идет по типу цепной реакции: некроз—регенерация — перестройка сосудистого русла—ишемия паренхимы — некроз.
В настоящее время нет единой клинической классификации цирроза печени. Классификация, предложенная V Панамериканским конгрессом гастроэнтерологов в Гаване (1956 г.), согласно которой различали постнекротический, портальный и билиарный цирроз печени, оказалась несовершенной. В связи с этим на Международной конференции по стандартизации номенклатуры и классификации болезней печени в Акапулько (1974) было решено классифицировать цирроз печени по этиологическому принципу, а также на основании морфологических изменений. При этом цирроз печени подразделяли на микронодулярный (с диаметром узлов до 3 мм), макронодулярный (с диаметров узлов свыше 3 мм) и смешанный. В связи с тем что в клнической практике при постановке диагноза и назначении лечения необходимо учитывать не только этиологию, патогенез, морфологические особенности, но также стадию, активность процесса и наличие осложнений, классификация должна отражать все эти показатели: 1. По этиологии: — вирусный, — алкогольный, — токсический, — связанный с врожденными нарушениями метаболизма, — связанный с поражениями желчевыводящих путей (первич ный и вторичный билиарный цирроз), — криптогенный цирроз. 2. По степени активности процесса: — подострый (гепатит-цирроз), — быстро прогрессирующий (активный), — медленно прогрессирующий (активный), — вялотекущий, — латентный. 3. Стадия заболевания по степени функциональных нарушений (по критериям Чайльда-Пью—Child-Pugh — гипоальбуминемия, снижение протромбинового индекса, гипербилирубинемия, печеночная энцефалопатия, асцит): А — компенсированная, В — субкомпенсированная, С — декомпенсированная. 4. По морфологической картине: — микронодулярный, — макронодулярный, — смешанный. 5. Осложнения: — пищеводно-желудочные кровотечения, —печеночная недостаточность (энцефалопатия О, I, II, III стадии, кома), — спонтанный бактериальный асцит-перитонит, — тромбоз воротной вены, — гепаторенальный синдром, — гепатоцеллюлярная карцинома.
К морфологическим признакам активности цирроза печени принято относить выраженность дистрофических и регенераторных изменений в паренхиме, распространенность клеточных инфильтратов в строме, нечеткость границ между узловыми регенератами и межузловой соединительной тканью. Для компенсированной (начальной) стадии цирроза печени характерна начинающаяся перестройка архитектоники печени с очаговыми псевдолобулярными структурами и единичными узлами-регенератами, для субкомпенсированной — глубокая перестройка архитектоники печени с наличием множественных узлов-регенератов, окруженных зрелой соединительной тканью. Для декомпенсированной стадии цирроза печени типично значительное уменьшение объема паренхимы при утрате дольковой структуры и выраженном преобладании фиброза. Клиника всех форм цирроза печени имеет ряд общих черт. В большинстве случаев заболевание начинается постепенно. Больные обычно жалуются на слабость, повышенную утомляемость, снижение или потерю трудоспособности, частые диспепсические проявления: снижение или отсутствие аппетита, тошноту, реже рвоту, чувство распирания, тяжести или переполнения, особенно после еды, в эпигастрии и правом подреберье, могут наблюдаться нерезкая боль, вздутие живота, плохая переносимость жирной пищи и алкоголя, диарея. Нарушения сна, раздражительность особенно свойственны алкогольному циррозу. Больных беспокоят зуд кожи, боль в суставах, повышение температуры тела. Отмечаются носовые кровотечения, реже геморроидальные, снижение зрения в вечернее время («куриная слепота» — гемералопия). Из других характерных симптомов цирроза можно отметить появление гормональных расстройств: импотенцию, гинекомастию у мужчин, нарушение менструального цикла, снижение либидо у женщин, а также потерю массы тела вплоть до кахексии в терминальных стадиях. Кожа больных — серовато-грязного цвета, может наблюдаться субиктеричность или выраженная желтуха, особенно при вирусном или билиарном циррозе печени. На коже могут быть следы от расчесов, в тяжелых случаях — геморрагии. Иногда на коже появляются телеангиэктазии (паукообразные расширения артериальных сосудов — «сосудистые звездочки», впервые описанные С.П.Боткиным). Нередко наблюдают и гиперемию ладоней, иногда с желтушным оттенком («печеночная ладонь»), а в более редких случаях — изменение ногтей в виде часовых стекол, нерезко выраженное утолщение дистальных фаланг пальцев («барабанные палочки»). Одним из наиболее частых объективных симптомов является гепатомегалия. В большинстве случаев печень имеет уплотненную консистенцию, заостренный край, мало- или безболезненна. У части больных удается пропальпировать узловатую поверхность (особенно при макронодулярном поражении печени). В терминальной стадии болезни можно отметить уменьшение размеров печени. Селезенка увеличена более чем у половины больных. В далекозашедших стадиях цирроз печени может проявляться асцитом и периферическими отеками. Появлению асцита обычно предшествует вздутие живота, связанное с метеоризмом, развившимся в результате ухудшения всасывания газов в кишках при нарушении портального кровообращения. В процессе прогрессирования всех этиологических типов цирроза печени наблюдается следующая динамика перечисленных симптомов. Компенсированная стадия цирроза печени (группа А по Чайльду-Пью) клинически характеризуется появлением астеновегетативных и диспепсических расстройств, жалоб на боль в правом подреберье. Печень увеличена, имеет неровную поверхность, болезненна при пальпации. Возможно повышение активности аминотрансфераз, изменение показателей белково-осадочных проб и белковых фракций крови. При сканировании выявляют гепатомегалию и умеренно повышенное накопление радионуклида в селезенке. Однако наиболее достоверным диагностическим критерием считают пункционную биопсию печени или лапароскопию с прицельной биопсией и последующим гистологическим исследованием биоптата.
Стадия субкомпенсации (группа В по Чайльду-Пью) сопровождается быстрым, клинически выраженным прогрессированием заболевания. На первый план выступают проявления функциональных нарушений печени: желтуха, умеренно выраженные геморрагические проявления, гинекомастия, преходящий асцит. У большинства больных увеличивается не только печень, но и селезенка, достигающая значительных размеров. При биохимическом исследовании крови отмечают значительное уменьшение уровня альбуминов и резкое увеличение содержания глобулиновых фракций, высоких цифр достигает тимоловая проба, снижен уровень протромбина, холестерина. У части больных имеются проявления гиперспленизма (анемия, лейкопения, тромбоцитопения). Анемия чаще носит гипохромный, микроцитарный характер, связанный с усиленным гемолизом эритроцитов в селезенке, дефицитом железа. В связи с нарушением обмена фолиевой кислоты и витамина В12, а также угнетением эритропоэтической активности костного мозга возможно развитие микроцитарной гиперхромной анемии. Усиленный гемолиз эритроцитов объясняет высокую частоту (30 %) формирования пигментных желчных камней при циррозе печени. Появление тромбоцитопении у этих больных связывают с повышенным депонированием тромбоцитов в селезенке.
Декомпенсированная стадия цирроза (группа С по Чайльду- Пью) характеризуется наличием выраженной паренхиматозной и (или) сосудистой декомпенсации. Паренхиматозная декомпенсация клинически проявляется в виде геморрагического синдрома с пурпурой и экхимозами, развитием желтухи, печеночной энцефалопатии и комы. При лабораторном исследовании выявляют снижение в сыворотке крови уровней альбумина, факторов свертывающей системы крови, синтезируемых в печени, холестерина и холинэстеразы. Проявлением сосудистой декомпенсации являются тяжелые осложнения портальной гипертензии: резко выраженная спленомегалия с развернутой картиной гиперспленизма (лейкопения, тромбоцитопения, анемия), с повышенной кровоточивостью, кровотечения из варикозно расширенных вен пищевода и желудка, появление стабильного асцита и периферических отеков в сочетании с расширением подкожных венозных колпатералей передней брюшной стенки, пупочной грыжей.
На основании анализа большого клинического материала А.И.Хазанов (1995) дает следующую характеристику активности патологического процесса при циррозе печени:
Подострый цирроз (гепатит-цирроз) представляет собой начальную стадию развития цирроза печени на фоне острого гепатита.
Быстро прогрессирующий (активный) цирроз. Имеются четкие клинические, биохимические и морфологические признаки высокой активности патологического процесса в печени. Быстро развиваются портальная гипертензия и нарушение функционального состояния печени.
Медленно прогрессирующий (активный) цирроз. Клинические признаки активности выражены нечетко. Важное значение имеет отчетливое уплотнение и фестончатость нижнего края печени, увеличение селезенки. У всех больных отмечают изменение биохимических показателей функционального состояния печени и регистрируют морфологические признаки активности. Портальная гипертензия, функциональная недостаточность печени развиваются медленно, сравнительно часто при многолетнем наблюдении регистрируется развитие гепатоцеллюлярной карциномы.
Вялотекущий (индолентный) цирроз. Клинические признаки активности у большинства больных отсутствуют, биохимические наблюдаются только в периоды обострения патологического процесса. Морфологические признаки активности выражены умеренно. Портальная гипертензия развивается очень медленно, функциональная недостаточность печени при отсутствии повторных повреждений, как правило, не возникает. Из осложнений цирроза может наблюдаться первичный рак печени.
Латентный цирроз печени. У больных отсутствуют клинические, биохимические и морфологические признаки активности. Портальная гипертензия и печеночная недостаточность, как правило, не развиваются. Диагноз ставится на основе гистологического исследования биоптатов печени.
Дифференциация различных этиологических вариантов цирроза печени основывается на комплексе клинико-эпидемиологических данных и результатов лабораторных и инструментальных исследований, отражающих проявления цитолитического, мезенхимально-воспалительного, холестатического синдромов, а также синдромов печеночно-клеточной недостаточности и портальной гипертензии.
источник
Асцит — скопление свободной жидкости в брюшной полости, приводящее к увеличению объема живота. Асцит может возникать внезапно или развиваться постепенно, в течение нескольких месяцев, сопровождаясь ощущением распирающей тяжести и боли в животе, метеоризмом. При большом объеме асцита появляются затруднения при наклоне туловища, одышка при ходьбе, отеки ног.
Определить значительное количество свободной жидкости в брюшной полости (более 1,5 л) нетрудно обычными клиническими методами. При перкуссии живота у больных с асцитом обнаруживается тупость над боковыми его областями живота, а посередине — кишечный тимпанит. Перемещение больного на левый бок вызывает смещение тупого звука книзу, и он определяется над левой половиной живота, а в области правого фланга — тимпанический звук. При наличии осумкованной жидкости, обусловленной слипчивым перитонитом туберкулезной этиологии или кисты яичника, тимпанит не смещается при перемене положения больного.
Для выявления небольшого количества жидкости применяется перкуссия в положении больного стоя: при асците появляется тупой или притуплённый звук в нижних отделах живота, исчезающий при переходе больного в горизонтальное положение. С этой же целью используется такой пальпаторный прием, как флюктуация жидкости: врач правой рукой наносит отрывочные толчки по поверхности живота, а ладонь его левой руки ощущает волну, передающуюся на противоположную стенку живота.
Небольшое количество жидкости в брюшной полости (субклинический асцит) определяется с помощью УЗ И и компьютерной томографии (КТ). Для более точного определения количества асцитической жидкости внутриперитонеально вводят 5 мл 5% раствора бромсульфалеина. В извлеченной через 2 ч асцитической жидкости определяют концентрацию бромсульфалеина и рассчитывают весь объем асцитической жидкости. Однако эта методика клинического распространения не получила.
При большом количестве асцитической жидкости появляются такие дополнительные симптомы, как пупочная и паховая грыжа, варикозное расширение вен голени, геморроидальных вен, смещение диафрагмы вверх, смещение сердца и повышение давления в яремной вене. Механическими факторами объясняются также часто встречающиеся у больных асцитом диафрагмальная грыжа и пищеводный рефлюкс, которые способствуют эрозии и кровотечению из вен пищевода. На растянутой брюшной стенке обычно обнаруживают венозные коллатерали. Вследствие сдавления нижней полой вены асцитической жидкостью, а также в связи с гипоальбуминемией возможен отек нижележащих частей тела.
Плевральный выпот, обычно на правой стороне, имеется приблизительно у 10% больных асцитом, обусловленным циррозом. Одним из основных механизмов образования плеврального выпота является движение перитонеальной жидкости наверх через диафрагмальные лимфатические сосуды; известную роль могут играть приобретенные дефекты диафрагмы и повышенное портальное давление. Из этого следует нецелесообразность плевральной пункции у больных циррозом при отсутствии дыхательной недостаточности. Ликвидация или уменьшение асцита приводит к исчезновению плеврального выпота.
Асцитическая жидкость представляет собой как бы ультрафильтрат плазмы, ее компоненты находятся в динамическом равновесии с составляющими плазмы. В течение часа с плазмой обменивается 40-80 % асцитической жидкости, а меченый альбумин попадает в асцитическую жидкость через 30 мин после внутривенного введения. Альбумин, введенный в брюшную полость, обнаруживают в плазме еще быстрее.
Патогенез асцита при циррозе печени сложен и зависит от взаимодействия нескольких факторов: портальной гипертензии, гормонального и нервно-гуморального, обусловленных гемодинамическими сдвигами и нарушением водно-электролитного равновесия.
Портальная гипертензия и связанный с ней застой в воротной вене считаются серьезными факторами, предрасполагающими к развитию асцита. Повышение синусоидального гидростатического давления при внутрипеченочной портальной гипертензии вызывает повышенную транссудацию богатого белком фильтрата через стенки синусоидов в пространства Диссе.
Внутрипеченочный блок оттока приводит у больных циррозом печени к повышенному лимфообразованию. По данным патологоанатомических и клинических наблюдений, при циррозе печени значительно увеличивается число под капсульных, внутрипеченочных и отводящих лимфатических сосудов, их стенка истончена, просвет переполнен лимфой. Скорость истечения лимфы из грудного протока увеличивается в несколько раз. Отток лимфы от печени достигает 15-20 л/сут и более при норме 8-9 л. Усиленное функционирование лимфатической системы способствует разгрузке венозной сети, но в дальнейшем развивается динамическая недостаточность лимфообращения, приводящая к пропотеванию жидкости с поверхности печени в брюшную полость.
Гипоальбуминемия, возникающая в результате снижения синтеза белков, нарушения их усвоения, а также потери белков при удалении асцитической жидкости, наряду с повышенным лимфообразованием и увеличением объема интерстициальной жидкости способствует снижению онкотического давления. Следствием этих гидростатических и гипоонкотических нарушений являются пропотевание интерстициальной жидкости в полость брюшины и формирование асцита.
Накопление асцитической жидкости приводит к снижению эффективного, т.е. участвующего в циркуляции, объема плазмы, так как значительная ее часть депонирована в сосудах брюшной полости. Уменьшение эффективного объема плазмы стимулирует повышенную секрецию ренина в юкстагломерулярном аппарате почек. Ренин в свою очередь усиливает образование ангиотензина I из синтезируемого печенью ангиотензиногена. Ангиотензин I превращается в ангиотензин II. Ангиотензин II приводит не только к снижению гломерулярной фильтрации и почечного кровотока, но и повышает секрецию антидиуретического гормона гипофиза и альдостерона надпочечников.
Развитию вторичного гиперальдостеронизма способствует уменьшение инактивации гормона в гепатоцитах вследствие снижения почечного кровотока и уменьшения метаболического клиренса альдостерона. Под влиянием альдостерона у больных циррозом печени увеличиваются реабсорбция натрия и экскреция калия в дистальных отделах почечных канальцев и возрастает реабсорбция натрия и воды в проксимальных отделах почечных канальцев со снижением толерантности к водной нагрузке.
Повышенная потеря калия и водорода на фоне гиперальдостеронизма приводит к снижению содержания калия, магния в сыворотке крови и метаболическому алкалозу. Несмотря на снижение экскреции натрия с мочой, у большинства больных развивается гипонатриемия, так как большая часть натрия переходит в интерстициальную и асцитическую жидкость.
Таким образом, вследствие гемодинамических нарушений — недостаточного наполнения центрального венозного и артериального русла — возникает активация ренин-ангиотензин-альдостероновой системы. Вторичная задержка почками ионов натрия приводит к накоплению в организме воды. В последние годы появились данные, свидетельствующие о том, что у большинства больных циррозом печени, не получавших гипонатриевой диеты и мочегонных средств, активирующих продукцию альдостерона, не обнаруживается стимуляция ренин-ангиотензин-альдостероновой системы. Эти данные привели к предположению, что в начальной стадии имеются задержка натрия почками и увеличение объема плазмы, так называемая теория сверхпритока. Избыток жидкости в связи с портальной гипертензией и увеличением коллоидно-осмотического давления плазмы выделяется в брюшную полость и приводит к снижению эффективного объема плазмы с вторичной реакцией печеночных канальцев.
Обе изложенные теории не в состоянии полно и точно объяснить механизм задержки воды и натрия почками при циррозе. Ввиду этого предложена третья гипотеза, согласно которой инициатором задержки воды и натрия почками является вазодилатация периферических артерий, сужение почечных сосудов и уменьшение центрально регулируемого объема крови.
Развитие асцита при злокачественных опухолях и инфекциях с поражением брюшины происходит вследствие гематогенного или контактного метастазирования с карциноматозом брюшины и вторичной воспалительной экссудацией. Существенную роль может играть сдавление или прорастание опухолью лимфатических путей оттока, поражение крупных сосудов, а также метастатическое поражение печени.
Заболевания, способные проявляться исключительно или преимущественно асцитом, можно разделить на 5 групп.
Болезни печени и ее сосудов: цирроз печени, рак печени, болезнь Бадда-Киари, веноокклюзионная болезнь.
Злокачественные заболевания: вторичный карциноматоз, лимфома и лейкоз, первичная мезотелиома.
Болезни брюшины: туберкулезный перитонит, перитонит другой этиологии (в т.ч. панкреатический, грибковый, паразитарный).
Болезни сердца: констриктивный перикардит, застойная сердечная недостаточность.
Другие болезни: опухоли и кисты яичников (синдром Мейгса), киста поджелудочной железы, болезнь Уиппла, саркоидоз, системная красная волчанка, микседема.
Самыми частыми причинами асцита являются цирроз печени, метастазы злокачественных опухолей в брюшину и печень, реже — туберкулез брюшины. Редкая причина асцита — тромбоз печеночных вен — иногда сочетается со стенозом или даже окклюзией нижней полой вены. В этих случаях развиваются также кавакавальные анастомозы.
Прежде всего следует убедиться, что увеличение живота обусловлено асцитом. За асцит можно принять увеличение живота при ожирении, кистах яичника и брыжейки, беременности. Отличить эти состояния от асцита помогают перкуссия живота в горизонтальном и вертикальном положении больного, определение флюктуации жидкости, УЗИ и КТ.
Подробно собранный анамнез и осмотр больного во всех случаях должны сочетаться с ультразвуковым исследованием органов брюшной полости, а также сканированием печени и селезенки с 99m Тс. При ультразвуковом исследованиихарактеризуют состояние паренхимы и размеры печени и селезенки, диаметр сосудов портальной системы. Кроме того, исключают опухолевый процесс в других органах и заболевания брюшины. С помощью допплерографии оценивают кровоток по портальной, печеночной и селезеночной венам. Все больные с впервые выявленным асцитом нуждаются в госпитализации, так как в этих случаях желательно проведение диагностического парацентеза с обязательнымисследованием асцитической жидкости: подсчетом числа клеток, определением белка, альбумина, окраской по Граму и посевом. В последние годы существенное значение придается оценке градиента сывороточно-асцитического альбумина, получаемой при вычитании концентрации альбумина асцитической жидкости из концентрации альбумина сыворотки крови.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Брюшная полость представляет собой замкнутое пространство, ограниченное брюшиной (тонкой полупроницаемой оболочкой) и содержащее различные органы (желудок, селезенку, печень, желчный пузырь и некоторые отделы кишечника). Брюшина состоит из двух листков – париетального (наружного, который прикрепляется к стенкам живота изнутри) и висцерального (внутреннего), который прилегает к стенкам внутрибрюшных органов, окружая их. Основными функциями брюшины являются фиксация расположенных в ней органов и регуляция обмена веществ в организме.
В брюшине имеется огромное количество мелких кровеносных и лимфатических сосудов, которые обеспечивают обмен веществ. В нормальных условиях в брюшной полости и между листками брюшины постоянно находится небольшое количество жидкости, которая образуется в результате пропотевания жидкой части крови и определенного количества белков через кровеносные сосуды. Однако данная жидкость не скапливается в брюшной полости, так как практически сразу же происходит ее обратное всасывание в лимфатические капилляры (в сутки брюшина может всасывать более 50 литров жидкости). Образующаяся при этом лимфа по лимфатическим сосудам поступает в венозную систему организма, возвращая в системный кровоток жидкость, белки и другие, растворенные в ней, микроэлементы.
Исходя из вышесказанного следует, что скапливание жидкости в брюшной полости может произойти в двух случаях — при увеличении скорости ее образования либо при уменьшении скорость ее всасывания. На практике эти два механизма присутствуют одновременно, то есть при различных заболеваниях внутренних органов (печени, поджелудочной железы, при опухолях, при воспалении брюшины и так далее) возникает увеличение продукции жидкости, что непременно влечет за собой нарушение ее реабсорбции (всасывания) в результате сдавливания и закупорки мелких лимфатических и кровеносных сосудов продуктами распада клеток, патогенными микроорганизмами или опухолевыми клетками. По мере развития заболевания жидкости в брюшной полости становится все больше, и она начинает сдавливать расположенные там органы, что, в свою очередь, может усугубить течение основного заболевания и способствовать прогрессированию асцита.
Также стоит отметить, что помимо жидкости в брюшной полости задерживаются и белки (а также и другие микроэлементы). В нормальных условиях белки плазмы крови (преимущественно альбумины) участвуют в создании так называемого онкотического давления, то есть они удерживают жидкость в сосудах. При асците большая доля белков находится в асцитической жидкости, в связи с чем онкотическое давление крови снижается, что также может способствовать выходу жидкости из сосудистого русла и прогрессированию заболевания.
При прогрессировании заболевания происходит уменьшение объема циркулирующей крови, так как большая часть жидкости скапливается в брюшной полости. Это приводит к активации компенсаторных механизмов, направленных на задержку воды в организме (в частности уменьшается скорость образования и выделения мочи), что еще больше повышает гидростатическое давление в кровеносных сосудах и также способствует образованию асцитической жидкости.
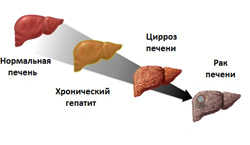
Цирроз печени – это хроническое заболевание, при котором нарушаются строение и практически все функции данного органа, что приводит к возникновению и прогрессированию различных осложнений.
В нормальных условиях в печень по воротной (портальной) вене стекается кровь от многих внутренних органов (от желудка, селезенки, поджелудочной железы, тонкого и толстого кишечника). В печени она проходит через тонкие канальцы (печеночные синусоиды), где фильтруется, очищается и обогащается различными веществами (например, белками), после чего поступает в нижнюю полую вену и возвращается в системный кровоток. При циррозе под действием различных причинных факторов (например, вирусов гепатита В или С) происходит повреждение и разрушение большого количества гепатоцитов (клеток печени). Погибшие клетки замещаются фиброзной тканью, что значительно снижает функцию печени. Это, в свою очередь, приводит к активации компенсаторных механизмов, заключающихся в усиленном делении оставшихся (неповрежденных) клеток. Однако структура новообразовавшейся ткани нарушается (в частности отсутствуют характерные для нормальной печени синусоиды), в результате чего снижается фильтрационная способность органа (то есть уменьшается количество крови, которое может проходить через печень за единицу времени).
Нарушение функции печени, а также изменение ее структуры приводит к тому, что кровь не может профильтровываться в полном объеме, в результате чего она начинает скапливаться в воротной вене. По мере прогрессирования заболевания гидростатическое давление (то есть давление, оказываемое кровью на стенку сосуда) в воротной вене повышается (развивается портальная гипертензия), что нарушает процесс оттока крови от внутренних органов (желудка, кишечника и других). В результате застоя крови в них происходит расширение кровеносных сосудов и повышение проницаемости сосудистых стенок, что и приводит к пропотеванию части жидкости в брюшную полость.
Также стоит отметить, что печень является основным местом образования белков в организме. На поздних стадиях заболевания (когда большая часть гепатоцитов замещается фиброзной тканью) белково-образующая функция печени снижается, в результате чего развивается гипопротеинемия (недостаток белков в крови). Это, в свою очередь, приводит к снижению онкотического давления крови, что также способствует выходу части жидкости из сосудистого русла.
Рак печени – это опухолевое заболевание, которое приводит к повреждению структуры печени и нарушению всех ее функций. Способствовать развитию рака могут различные факторы внешней среды (радиация, токсины, вирусы и так далее), под действием которых происходит образование мутантных опухолевых клеток. Обычно такие клетки сразу выявляются иммунной системой организма и уничтожаются, однако при определенных условиях (например, при ослаблении иммунитета или при облучении большой дозой радиации) одна опухолевая клетка может выжить и начать постоянно (бесконечно) делиться.
Со временем опухоль увеличивается в размерах и может сдавливать крупные внутрипеченочные сосуды. Также раковые клетки могут отрываться от основной опухоли и перемещаться (метастазировать) в другие отделы органа, закупоривая печеночные синусоиды, кровеносные и лимфатические сосуды и желчные протоки. Это будет приводить к нарушению всех функций печени, повышению давления в воротной вене и развитию асцита.
Помимо цирроза и рака есть еще несколько патологий, которые могут нарушить кровообращение в печени и воротной вене и стать причиной выхода жидкости в брюшную полость.
Асцит может быть обусловлен:
- Синдромом (болезнью) Бадда-Киари. Кровь из печени собирается в крупные печеночные вены, которые впадают в нижнюю полую вену. При синдроме (болезни) Бадда-Киари происходит воспаление стенок данных вен с последующим образованием в них тромбов (кровяных сгустков). Это приводит к нарушению оттока крови из печени и повышению давления в системе воротной вены, что и является причиной развития асцита.
- Сдавливанием ветвей воротной вены. После входа в ткань печени воротная вена делится на две крупные ветви (правую и левую), которые направляются в соответствующие доли органа. Сдавливание этих ветвей растущей опухолью или эхинококковой кистой (эхинококкоз – глистное заболевание, при котором в печени и других органах образуются объемные полости – кисты, заполненные развивающимися паразитами) также может стать причиной портальной гипертензии и выхода жидкости из сосудистого русла в брюшную полость.
Причиной асцита может быть:
- Мезотелиома. Данное злокачественное новообразование встречается крайне редко и происходит непосредственно из клеток брюшины. Развитие опухоли приводит к активации иммунной системы с целью уничтожения опухолевых клеток, что проявляется развитием воспалительного процесса, расширением кровеносных и лимфатических сосудов и пропотеванием жидкости в брюшную полость.
- Канцероматоз брюшины. Данным термином обозначается поражение брюшины опухолевыми клетками, которые метастазируют в нее из опухолей других органов и тканей. Механизм развития асцита при этом такой же, как при мезотелиоме.
- Рак поджелудочной железы.Поджелудочная железа является местом образования пищеварительных ферментов, которые выделяются из нее по протоку поджелудочной железы. После выхода из железы данный проток сливается с общим желчным протоком (по которому отходит желчь из печени), после чего они вместе впадают в тонкий кишечник. Рост и развитие опухоли вблизи места слияния данных протоков может привести к нарушению оттока желчи из печени, что может проявляться гепатомегалией (увеличением размеров печени), желтухой, кожным зудом и асцитом (асцит развивается на поздних стадиях заболевания).
- Рак яичников. Хотя яичники и не относятся к органам брюшной полости, листки брюшины участвуют в фиксации данных органов в малом тазу. Этим объясняется тот факт, что при раке яичников патологический процесс легко может распространиться на брюшину, что будет сопровождаться повышением проницаемости ее сосудов и образованием выпота в брюшной полости. На поздних стадиях заболевания может отмечаться метастазирование рака в листки брюшины, что усилит выход жидкости из сосудистого русла и приведет к прогрессированию асцита.
- Синдром Мейгса. Данным термином обозначается патологическое состояние, характеризующееся скапливанием жидкости в брюшной и в других полостях организма (например, в плевральной полости легких). Причиной заболевания считаются опухоли органов малого таза (яичников, матки).
Сердечная недостаточность – заболевание сердца, при котором оно оказывается не в состоянии обеспечить адекватную циркуляцию крови в организме. В нормальных условиях при каждом сердечном сокращении в аорту (самую крупную артерию организма) выбрасывается определенное количество крови. По мере удаления от сердца происходит деление аорты на более мелкие артерии, пока не образуются капилляры – самые тонкие сосуды, в которых происходит обмен кислорода между тканями и клетками организма. После прохождения через капилляры кровь собирается в вены и доставляется обратно к сердцу. Часть жидкости (около 10%) при этом поступает в лимфатические сосуды и превращается в лимфу.
Важной особенностью сосудистой системы является то, что стенка артерий плотная и упругая, в то время как венозная стенка относительно тонкая и легко растягивается при повышении внутрисосудистого давления. При развитии сердечной недостаточности (причиной которой может быть инфаркт, инфекция, длительное повышение артериального давления и так далее) снижается насосная функция сердечной мышцы, в результате чего развивается застой в системе нижней полой вены, которая собирает кровь от всей нижней части тела. Вследствие расширения стенок переполненных венозных сосудов, а также из-за повышения гидростатического давления определенная доля жидкой части крови выходит из сосудистого русла и скапливается в брюшной полости.
Почки являются органами выделительной системы, которые регулируют состав и объем жидкости в организме. Однако при некоторых заболеваниях их функция может нарушаться, что, в свою очередь, может привести к развитию различных осложнений.
Асцитом может осложниться:
- почечная недостаточность;
- нефротический синдром.
Почечная недостаточность
Патологическое состояние, при котором поражается более 75% функциональной ткани (так называемых нефронов) почек. В результате этого орган больше не может в полной мере выполнять свою выделительную функцию, поэтому часть побочных продуктов жизнедеятельности (таких как мочевина, мочевая кислота и другие) задерживаются в организме. Данные вещества являются осмотически активными (то есть притягивают к себе жидкость) и при проникновении в межклеточное пространство тканей приводят к развитию отеков.
Также при почечной недостаточности нарушается кровоснабжение почечной ткани, вследствие чего активируются компенсаторные механизмы, направленные на повышение системного артериального давления и увеличение количества доставляемой к почкам крови. Наряду с этим в почках уменьшается скорость выделения натрия и воды, что еще больше увеличивает объем циркулирующей крови, повышает давление в венозной системе и способствует прогрессированию асцита.
Нефротический синдром
Данное заболевание характеризуется повреждением почечного фильтра (который в норме непроницаем для белков и других крупномолекулярных веществ), в результате чего организм теряет с мочой большое количество белков плазмы (более 3 грамм в сутки). Уже через несколько дней это приводит к значительному снижению онкотического давления крови, в результате чего жидкая ее часть больше не может удерживаться в сосудистом русле и пропотевает в брюшную полость, приводя к развитию асцита.
Панкреатит – это заболевание поджелудочной железы, характеризующееся разрушением ее ткани и распространением патологического процесса на соседние органы. Причиной развития данного заболевания является патологическая активация образующихся в железе пищеварительных ферментов. В норме они выделяются в кишечник в неактивной форме и активируются только после смешивания с кишечным содержимым. При различных патологических состояниях (при злоупотреблении алкоголем, после приема большого количества жареной пищи, после травмы живота или в результате вирусных инфекций) данные ферменты могут активироваться прямо внутри железы, что приведет к ее самоперевариванию.
Во время описанного процесса происходит повреждение сосудов поджелудочной железы, что обуславливает проникновение пищеварительных ферментов в кровь. Если вовремя не начать лечение, патологический процесс может разрушить стенку железы и перейти на брюшину, что станет причиной развития перитонита (воспаления брюшины) и может привести к образованию асцитической жидкости в брюшной полости.
Перитонит – это воспаление брюшины, характеризующееся выраженными болями в животе и прогрессирующими симптомами общей интоксикации организма (повышением температуры тела более 40 градусов, учащенным дыханием и сердцебиением, нарушением сознания и так далее). Развивается данное состояние при проникновении патогенных бактерий в брюшную полость извне.
Причиной перитонита может быть:
- разрыв полого органа (желудка, кишечника, мочевого или желчного пузыря);
- проникающее ранение брюшной полости;
- прободение язвы желудка или кишечника;
- распад опухоли кишечника с повреждением его стенки;
- миграция бактерий из других очагов инфекции;
- распространение воспалительного процесса из соседних органов.
Как говорилось ранее, брюшина содержит большое количество кровеносных и лимфатических сосудов. При развитии инфекционного или другого воспалительного процесса отмечается миграция к очагу воспаления большого количества лейкоцитов, что обуславливает расширение сосудов и выход жидкости в брюшную полость.
Также стоит отметить, что распространение инфекции по брюшине происходит довольно быстро, ввиду чего локальный (местный) перитонит в короткие сроки может перейти в диффузную (распространенную) форму, поражающую всю брюшину, что без своевременного и адекватного лечения может привести к смерти пациента в течение нескольких часов.
Анасарка – это крайняя степень отека, при которой жидкость скапливается в подкожно-жировой клетчатке туловища, рук и ног, а также в полостях организма (в брюшной и в плевральной полости, в полости перикарда). Данное состояние требует срочной медицинской помощи, так как может привести к смерти пациента в считанные часы или дни.
Причиной анасарки могут быть:
- Сердечная недостаточность. В данном случае отеки и асцит развиваются из-за выраженного повышения гидростатического давления в венозной и лимфатической системах, что обусловлено неспособностью сердечной мышцы перекачивать кровь.
- Почечная недостаточность. При данной патологии причиной задержки воды в организме является нарушение выделительной функции почек.
- Заболевания печени. При выраженном циррозе и печеночной недостаточности снижается концентрация белков в крови, что может стать причиной развития генерализованных отеков.
- Микседема. Характеризуется снижением концентрации в крови гормонов щитовидной железы (тироксина и трийодтиронина), что проявляется уменьшением количества образующихся в организме белков и приводит к выходу жидкости из сосудистого русла.
- Гиперальдостеронизм. Данное заболевание характеризуется избыточным образованием в надпочечниках (эндокринных железах) гормонаальдостерона. В нормальных условиях данный гормон отвечает за поддержание объема циркулирующей крови на постоянном уровне, однако при его избыточной секреции происходит выраженная задержка натрия и воды в организме, что способствует развитию отеков и асцита.
Также причиной выхода лимфы в брюшную полость могут быть:
- ранения крупных лимфатических сосудов;
- аномалии развития органов брюшной полости;
- перенесенные ранее операции на брюшной полости;
- опухолевые заболевания (системный лимфангиоз);
- хронические воспалительные заболевания кишечника.
Скапливание жидкости в брюшной полости плода может быть обусловлено различными патологиями матери или ребенка.
Причиной асцита у плода могут быть:
- Гемолитическая болезнь новорожденных. Данное заболевание развивается в том случае, если мать с отрицательным резус-фактором (резус-фактор – это особый антиген, который присутствует на красных клетках крови у определенных людей) будет вынашивать плода с положительным резус-фактором. Во время первой беременности никаких отклонений от нормы не будет, однако во время родов произойдет контакт крови матери и плода, что приведет к сенсибилизации материнского организма (в нем начнут выделяться антитела против резус-фактора). При повторной беременности резус-положительным плодом данные антитела начнут поражать клетки крови плода, нарушая функции всех его органов и тканей и приводя к развитию генерализованных отеков и асцита. Без своевременного лечения данное заболевание приводит к гибели плода.
- Генетические заболевания. Генетический аппарат человека состоит из 46 хромосом, образующихся в результате слияния 23 материнских и 23 отцовских хромосом. Повреждение одной или нескольких из них может проявляться различными заболеваниями, которые могут передаваться потомству. Асцит во внутриутробном периоде может быть проявлением синдрома Дауна (при котором появляется лишняя хромосома в 21 паре), синдрома Тернера (для которого характерен дефект половой Х-хромосомы) и других наследственных заболеваний.
- Внутриутробные аномалии развития. Причиной внутриутробных аномалий развития может быть инфекция, радиация или травма. Асцит при этом может возникать вследствие нарушения нормального развития печени, сердечно-сосудистой или лимфатической системы, при недоразвитии желчевыделительной системы и при других пороках развития.
- Повреждение плаценты.Плацента – это орган, который появляется в организме беременной женщины и обеспечивает жизнедеятельность (доставку кислорода и питательных веществ) плода в течение всего внутриутробного периода развития. Нарушение оттока крови от плаценты или пупочного канатика может повысить давление в кровеносной системе плода, тем самым создав предпосылки для развития отеков и асцита.
Все перечисленные выше причины асцита у взрослых могут также встречаться и в детском возрасте. Однако у новорожденных и детей раннего возраста асцит может быть обусловлен и другими заболеваниями.
Причиной асцита у детей могут быть:
- Пороки развития сердца. В данном случае подразумеваются аномалии развития сердечной мышцы, которые приводят к нарушению насосной функции сердца (дефекты клапанов, дефекты межжелудочковых и межпредсердных перегородок). Во внутриутробном периоде данные аномалии могут никак себя не проявлять, однако после рождения (когда нагрузка на сердце возрастает) могут развиться отеки, асцит и другие признаки сердечной недостаточности.
- Пороки развития почек. Во внутриутробном периоде выделительную функцию осуществляет плацента, поэтому даже при тяжелых аномалиях развития почечной системы признаки почечной недостаточности у плода могут отсутствовать. После рождения ребенка токсические вещества и продукты обмена скапливаются в крови и в тканях малыша, что может привести к развитию отеков и асцита.
- Инфекционные заболевания. Инфицирование плода различными вирусами (вирусом краснухи, герпеса, цитомегаловирусом, энтеровирусом) или бактериями (например, при сифилисе) может привести к поражению внутренних органов и развитию полиорганной недостаточности. Это может проявляться асцитом, который появится во внутриутробном периоде либо сразу после рождения ребенка.
- Опухоли. Новообразования у новорожденных встречаются крайне редко, так как для развития опухолевого процесса и роста опухоли необходимо время. Тем не менее, появление опухоли (злокачественной или доброкачественной) во внутриутробном периоде или в раннем детском возрасте возможно. Растущая опухоль может сдавливать кровеносные или лимфатические сосуды ребенка, повреждать различные органы и ткани (печень, селезенку), что может привести к развитию асцита с первых дней жизни.
- Врожденные анемии.Анемия – общее название состояний, характеризующихся снижением концентрации эритроцитов (красных клеток крови) и гемоглобина (находящегося в эритроцитах дыхательного пигмента) в крови. Некоторые виды анемий (серповидноклеточная анемия, гемоглобинопатии, анемия при дефиците ферментов и так далее) характеризуются деформацией и разрушением эритроцитов. Разрушаются они преимущественно в печени и селезенке, что может со временем приводить к поражению данных органов и развитию отеков и асцита.
Асцит у беременных может развиться в результате различных заболеваний печени, сердца, почек и других органов и систем. Также скапливанию жидкости в брюшной полости способствует рост и увеличение размеров плода, который может сдавливать нижнюю полую вену (крупный сосуд, собирающий венозную кровь от всей нижней части тела).
Рост и развитие плода само по себе требует от всех органов и систем женского организма более интенсивной работы. Скапливание жидкости в брюшной полости и повышение внутрибрюшного давления еще больше увеличивает нагрузку на органы, что может привести к декомпенсации хронических заболеваний и развитию полиорганной недостаточности, угрожающей здоровью или даже жизни матери и плода.
Наиболее грозными проявлениями асцита у беременных могут быть:
- Дыхательная недостаточность. Увеличение матки на поздних сроках беременности приводит к смещению диафрагмы (основной дыхательной мышцы, отделяющей брюшную полость от грудной клетки) вверх, что приводит к уменьшению дыхательного объема легких. Появление большого количества жидкости в брюшной полости еще больше усугубляет данный процесс, что приводит к недостатку кислорода в крови матери и плода.
- Сердечная недостаточность. Как уже было сказано, рост и развитие плода приводит к повышению давления в брюшной полости. В результате этого повышается кровяное давление в располагающихся там кровеносных сосудах. Чтобы преодолеть это давление, сердце вынуждено работать в усиленном режиме. Появление асцита на поздних сроках беременности еще больше увеличивает нагрузку на сердце, что может стать причиной нарушения его функции. Это, в свою очередь, может привести к недостаточному поступлению крови к плаценте и стать причиной внутриутробной гибели плода.
- Сдавливание растущего плода. При асците количество скапливающейся в брюшной полости жидкости может достигать нескольких десятков литров. Это приведет к выраженному повышению внутрибрюшного давления и сдавливанию всех внутренних органов, в том числе и матки с развивающимся плодом. Как правило, такое состояние делает невозможным дальнейшее развитие беременности.
При геморрагическом асците в асцитической жидкости присутствуют красные клетки крови (эритроциты) в том или ином количестве. Как правило, такое состояние развивается на фоне уже имеющихся хронических заболеваний, ставших причиной образования асцита (цирроза печени, рака, туберкулеза).
Причиной геморрагического асцита может быть:
- травма печени;
- травма селезенки;
- кровотечение при распаде опухоли;
- тромбоз (закупорка кровяным сгустком) печеночных вен;
- перфорация (прободение) стенки кишечника (например, при язве).
Появление крови в асцитической жидкости является неблагоприятным прогностическим признаком и требует срочных диагностических и лечебных мероприятий.
Туберкулез – это инфекционное заболевание, которое поражает легкие, кишечник и другие органы. Вызывается заболевание микобактериями туберкулеза, которые попадают в организм преимущественно воздушно-капельным путем (при вдыхании воздуха, загрязненного возбудителем) или с пищей. Первичный очаг туберкулеза обычно локализуется в легочной ткани, реже – в кишечнике. По мере прогрессирования заболевания и при снижении защитных сил организма микобактерии могут распространяться из первичного очага в другие ткани, в том числе и в брюшину.
Поражение брюшины туберкулезом приводит к развитию специфического воспалительного процесса (перитонита), что проявляется расширением кровеносных сосудов и пропотеванием большого количества жидкости, лимфы и белков в брюшную полость.
Эндометриоз – заболевание, при котором происходит разрастание эндометрия (слизистой оболочки матки) в нетипичных для него местах (то есть в других органах и тканях). Причиной заболевания может быть нарушение гормонального фона женщины, а также наследственная предрасположенность.
Вначале клетки эндометрия выходят за пределы слизистой оболочки матки и проникают в ее мышечный слой, начиная там делиться. Во время менструального цикла они (как и обычный эндометрий) подвергаются определенным изменениям, что может привести к развитию кровотечения. На поздних стадиях заболевания клетки эндометрия выходят за пределы матки и могут поражать любые органы и ткани, в том числе и брюшину. Помимо прочих симптомов (болей в животе, нарушения мочеиспускания и так далее) это может проявляться скапливанием жидкости в брюшной полости.
Легочной плеврой называется тонкая соединительнотканная оболочка, которая состоит из двух листков — наружного и внутреннего. Наружный листок прилегает к внутренней поверхности грудной клетки, а внутренний окутывает легочную ткань. Между данными листками имеется щелевидное пространство (плевральная полость), где содержится небольшое количество жидкости, необходимой для обеспечения скольжения листков друг относительно друга во время дыхания.
Плевритом называется воспаление листков легочной плевры, что обычно сопровождается пропотеванием жидкости в плевральную полость. Асцит и плеврит одновременно могут наблюдаться при системных воспалительных заболеваниях аутоиммунного характера (когда иммунная система атакует клетки и ткани собственного организма) – при ревматической лихорадке, системной красной волчанке, ревматоидном артрите и так далее. Стоит отметить, что при перечисленных заболеваниях также может отмечаться скапливание жидкости в полости перикарда (сердечной сумки).
Однако, независимо от причины возникновения, скапливание жидкости в брюшной полости всегда будет проявляться определенными симптомами, выявление которых позволит заподозрить диагноз на ранних стадиях заболевания.
Асцит может сопровождаться:
- отеками;
- повышением температуры тела;
- болями в животе;
- увеличением размеров живота;
- увеличением печени;
- увеличением селезенки;
- тошнотой;
- рвотой;
- «головой медузы»;
- желтухой;
- одышкой;
- обезвоживанием.
Отеки при асците развиваются в результате выхода жидкости из сосудистого русла и перехода ее в межклеточное пространство различных тканей. Механизм образования и характер отеков зависит от основного заболевания, ставшего причиной асцита.
Отеки при асците могут быть следствием:
- почечной недостаточности (почечные отеки);
- сердечной недостаточности (сердечные отеки);
- печеночной недостаточности (безбелковые отеки).
Почечные отеки
Почечные отеки возникают из-за задержки воды и осмотически активных веществ в организме. Они (отеки) симметричны (наблюдаются в обеих частях тела), присутствуют постоянно, однако могут усиливаться в утренние часы, так как в течение ночного сна в организме скапливается большое количество жидкости и токсических веществ. Вначале отеки локализуются преимущественно в области лица, шеи, верхних конечностей, затем спускаются в область бедер и голеней. Кожа в области отека имеет нормальную или слегка повышенную температуру, может отмечаться бледность кожи. При продолжительном (в течение 20 – 30 секунд) надавливании на отечные ткани образуется углубление, которое исчезает сразу после прекращения давления.
Сердечные отеки
Сердечные отеки развиваются из-за того, что сердце не может перекачивать кровь из вен в артерии. Возникают они преимущественно к вечеру, вначале локализуются в области стоп и голеней, а затем поднимаются в область бедер и туловища. Объясняется это тем, что днем человек в течение длительного времени находится в вертикальном положении, в результате чего значительно повышается гидростатическое давление в венах нижних конечностей и развивается застой крови в них. Это и приводит к выходу жидкости из сосудов в межклеточное пространство.
Кожа в области сердечных отеков синюшного цвета, холодная на ощупь. При продолжительном надавливании образующееся углубление исчезает медленно.
Безбелковые отеки
При дефиците белков жидкая часть крови выходит в межклеточное пространство, что проявляется крайне выраженными, генерализованными (наблюдающимися во всех участках тела) отеками. Кожа в области отечных конечностей растянута, напряжена, бледная и сухая, температура ее снижена. При надавливании на отечную ткань вмятина исчезает в течение нескольких секунд.
Непосредственно асцит к повышению температуры тела не приводит. Причиной нарушения терморегуляции являются основные заболевания, ставшие причиной скапливания жидкости в брюшной полости.
При асците повышение температуры тела может быть проявлением:
- Перитонита. Поражение брюшины чужеродными микроорганизмами приводит к активации иммунной системы и повышению температуры тела. Наиболее высокие цифры (до 40 и более градусов) отмечаются при бактериальном перитоните, когда патогенные бактерии и выделяемые ими токсины всасываются в кровь и разносятся по всему организму. При перитоните туберкулезной этиологии температура обычно держится в пределах 37 – 39 градусов.
- Панкреатита. При панкреатите происходит развитие неинфекционного воспалительного процесса в поджелудочной железе, что сопровождается повышением температуры до 38 градусов. Переход воспаления на брюшину и развитие перитонита может сопровождаться более выраженной температурной реакцией (до 39 – 40 градусов).
- Цирроза печени. На ранних стадиях развития цирроза у всех пациентов отмечается субфебрилитет (повышение температуры тела до 37 – 37,5 градусов). Если цирроз является следствием поражения вирусами гепатита В или С, повышение температуры до 37 – 39 градусов будет являться естественной защитной реакцией организма, возникающей в ответ на внедрение чужеродных агентов. Повышение температуры тела выше 39 градусов обычно является следствием развития бактериальных осложнений и требует срочного медицинского вмешательства.
- Опухоли. При всех злокачественных опухолевых заболеваниях у пациента отмечается субфебрилитет в течение нескольких недель или месяцев, что обычно сопровождается чувством слабости и снижением массы тела. При метастазировании рака в брюшину может отмечаться повышение температуры тела до 39 – 40 градусов, что объясняется развитием воспалительной реакции в ответ на внедрение «чужих» (опухолевых) клеток.
Также стоит отметить, что для асцита при микседеме характерно снижение температуры до 35 градусов. Объясняется это недостатком гормонов щитовидной железы, которые в норме регулируют (повышают) скорость обменных процессов в организме и температуру тела.
Возникновение, характер и локализация болей зависят преимущественно от причины асцита, однако в некоторых случаях скапливание большого количества жидкости в брюшной полости может непосредственно приводить к усилению болей, сдавливая органы брюшной полости.
Болевой синдром при асците может быть обусловлен:
- Циррозом печени. Цирроз печени развивается постепенно и ему обычно предшествуют воспалительные заболевания печени (гепатиты). Сама печень не содержит болевых рецепторов, однако окружающая орган капсула богата ими. Увеличение размеров печени при различных заболеваниях приводит к перерастяжению капсулы, что проявляется болями различной интенсивности. В начальных стадиях цирроза пациенты могут жаловаться на дискомфорт или легкие боли в области правого подреберья, которые с течением времени могут усиливаться. Также пациенты могут жаловаться на тяжесть или боль в других отделах живота. Это объясняется нарушением пищеварения, имеющим место на поздних стадиях цирроза.
- Синдромом (болезнь) Бадда-Киари. При данной патологии происходит закупорка вен, по которым кровь оттекает от печени. Вследствие этого происходит переполнение внутрипеченочных кровеносных сосудов, увеличение органа в размерах и растяжение печеночной капсулы, что сопровождается острыми, колющими болями в правом подреберье, отдающими в правые отделы спины.
- Воспалением брюшины. В листках брюшины содержится большое количество болевых рецепторов, поэтому ее воспаление сопровождается выраженными режущими или колющими болями в животе, которые усиливаются при надавливании на переднюю брюшную стенку.
- Панкреатитом. Развитие воспалительного процесса в поджелудочной железе проявляется острыми болями опоясывающего характера, которые максимально выражены в области верхней части живота. Боли могут отдавать в область правого или левого подреберья, в спину, в сердце.
- Опухолью. Боли при опухоли редко бывают сильно выраженными, что значительно затрудняет раннюю диагностику злокачественных новообразований. Пациенты могут в течение нескольких недель или месяцев ощущать тупые, тянущие или ноющие боли в животе. Интенсивность болей при этом может самопроизвольно увеличиваться или уменьшаться.
- Эндометриозом. Боли при данной патологии локализуются преимущественно внизу живота, однако при метастазировании клеток эндометрия в другие органы могут иметь любую локализацию. Обычно женщины жалуются на усиление болей во время полового акта, во время менструации, болей при мочеиспускании или дефекации. Боль при этом острая, режущая, не купируется приемом обычных обезболивающих препаратов.
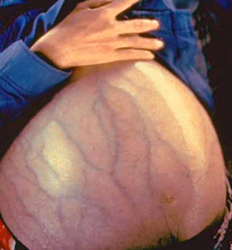
Данный симптом становится заметен невооруженным глазом при скапливании в брюшной полости более 1 литра жидкости. Вначале это может проявляться лишь в положении стоя, когда жидкость скапливается в нижних отделах брюшной полости, обуславливая выпячивание передней стенки живота. В положении лежа живот может быть нормальных размеров, однако пациент при этом может начинать жаловаться на одышку (чувство нехватки воздуха), так как жидкость будет перемещаться в верхние отделы брюшной полости, ограничивая движения диафрагмы и легких.
При дальнейшем прогрессировании заболевания количество асцитической жидкости увеличивается, вследствие чего выпирание передней брюшной стенки становится заметным и в положении лежа. При выраженном асците (когда в брюшной полости скапливается более 10 – 12 литров жидкости) кожа живота становится натянутой, напряженной, блестящей.
Увеличение печени (гепатомегалия) и селезенки (спленомегалия) может быть важным диагностическим признаком, указывающим на ту или иную причину асцита.
Причиной гепатомегалии и спленомегалии может быть:
- Цирроз печени. При циррозе печени происходит нарушение структуры печеночной ткани и частичное ее замещение фиброзной (рубцовой) тканью. Это создает препятствие на пути тока крови, в результате чего она скапливается в венах печени и в воротной вене, приводя к увеличению органа в размерах. Чтобы понизить давление в системе воротной вены часть крови сбрасывается в венозные сосуды селезенки, что также приводит к переполнению ее кровью и увеличению в размерах.
- Опухоль. Причиной увеличения печени может быть увеличение размеров внутрипеченочной опухоли или разрастание метастазов из опухолей другой локализации. При метастазировании злокачественной опухоли в ткань печени также произойдет закупорка печеночных капилляров опухолевыми клетками, что приведет к нарушению кровотока в органе и может стать причиной увеличения его в размерах.
- Болезнь Бадда-Киари. При тромбозе печеночных вен происходит переполнение печеночной ткани кровью и увеличение размеров печени. Селезенка при этом увеличивается лишь в тяжелых случаях заболевания (при развитии и прогрессировании портальной гипертензии).
- Сердечная недостаточность. При сердечной недостаточности кровь застаивается в системе нижней полой вены, повышая давление в ней. Так как печеночные вены (выносящие венозную кровь из печени) также впадают в нижнюю полую вену, выраженная сердечная недостаточность может нарушить отток крови от печени, что приведет к увеличению ее размеров.
На начальных стадиях развития асцита возникновение тошноты и рвоты может быть обусловлено основным заболеванием (циррозом печени, панкреатитом, перитонитом и так далее). По мере прогрессирования патологического процесса количество жидкости в брюшной полости увеличивается, что приводит к сдавливанию и нарушению функции многих органов (в частности желудка и кишечника).
Сдавливание желудка может значительно снизить его объем и нарушить моторику, в результате чего человек может испытывать тошноту даже после приема небольшого количества пищи. В случае появления рвоты рвотные массы будут содержать только что съеденную, непереваренную пищу. После рвоты желудок опустошается, что обычно приносит облегчение пациенту.
Сдавливание кишечника также может нарушить его моторику. При выраженном асците кишечные петли могут сдавливаться с такой силой, что продвижение перерабатываемой пищи (химуса) по ним станет невозможным. В результате этого химус начнет скапливаться выше места сдавливания, обуславливая усиление перистальтики в данном отделе кишечника. Пациент при этом будет жаловаться на приступообразные боли в животе, тошноту. Возникающая в данном случае рвота будет содержать частично переваренные продукты или каловые массы, а также будет иметь характерный неприятный запах.
Желтуха (окраска кожных покровов и видимых слизистых оболочек в желтый цвет) возникает при различных заболеваниях печени, сопровождающихся нарушением ее функции. Скапливание жидкости в брюшной полости на фоне желтухи позволяет с большой долей вероятности предположить, что причиной асцита является патология печени (цирроз или рак).
Механизм возникновения желтухи заключается в следующем — при разрушении красных клеток крови (эритроцитов) в кровоток выделяется пигмент желтого цвета – билирубин. Он является довольно токсичным продуктом, поэтому в нормальных условиях сразу же захватывается клетками печени, нейтрализуется и выводится из организма в составе желчи. При нарушении функций печении данный процесс замедляется или вовсе прекращается, вследствие чего концентрация билирубина в крови начинает расти. Со временем он проникает в различные ткани и органы и оседает в них, что и является непосредственной причиной появления желтушной окраски кожи и слизистых оболочек.
Одышка (чувство нехватки воздуха) при асците является следствием повышения давления в брюшной полости и ограничения подвижности легких. В нормальных условиях во время вдоха происходит сокращение диафрагмы (основной дыхательной мышцы), в результате чего она смещается вниз (в сторону брюшной полости), обеспечивая расширение легких и поступление в них порции свежего воздуха. Скапливание большого количества жидкости в брюшной полости и повышение внутрибрюшного давления делает невозможным полноценное смещение диафрагмы вниз, в результате чего при каждом вдохе пациент получает меньшее количество воздуха.
В начальном периоде развития асцита одышка возникает только в положении лежа, когда жидкость смещается вверх и давит на диафрагму. В положении стоя жидкость отекает в нижние отделы живота и человек дышит свободно. На поздних стадиях заболевания (когда объем асцитической жидкости достигает 10 литров и более) одышка наблюдается в положении стоя и усиливается в положении лежа, ввиду чего пациенты обычно отдыхают и спят полусидя.
Обезвоживание – это патологическое состояние, характеризующееся уменьшением количества жидкости в клетках и уменьшением объема циркулирующей крови (ОЦК). Хотя при асците жидкость из организма не теряется, она выходит из сосудистого русла в брюшную полость (то есть «выключается» из системы кровообращения) в результате чего ОЦК снижается и появляются характерные признаки обезвоживания.
Обезвоживание организма проявляется:
- жаждой;
- сухостью во рту;
- сухостью кожных покровов;
- снижением эластичности кожи;
- появлением морщин в области лица;
- повышением температуры тела;
- западением глазных яблок;
- уменьшением суточного диуреза (количества выделяемой мочи);
- запорами;
- снижением артериального давления;
- нарушением сознания (вплоть до возникновения галлюцинаций).
В отсутствии своевременного и адекватного лечения пациент с выраженным обезвоживанием может впасть в кому или даже умереть из-за нарушения функций жизненно-важных органов (головного мозга, сердца).
источник