Асцит представляет собой тяжелое осложнение разных заболеваний, при котором в полости живота накапливается большой объем жидкости. Обнаруженный асцит при онкологии серьезно осложняет течение и лечение основного заболевания, ухудшает прогноз. У пациентов с онкологическими заболеваниями органов, имеющих контакт с листками брюшины, средняя вероятность выпота жидкости в брюшную полость составляет 10%.
Процесс скопления лишней жидкости в полости живота сопровождает около половины всех случаев рака яичников у женщин. Он также осложняет течение новообразований:
- толстой кишки;
- молочных желез;
- желудка;
- поджелудочной железы;
- прямой кишки;
- печени.
Тяжесть состояния пациента не зависит от того первичная опухоль стала причиной патологии или ее метастазирование. К проявлениям рака добавляются признаки повышенного внутрибрюшного давления, подъема диафрагмы, сокращения дыхательных движений легочной ткани. В результате ухудшаются условия для работы сердца и легких, нарастает сердечная и дыхательная недостаточность, что приближает летальный исход болезни.
Брюшную полость образуют 2 листка. Один из них (париетальный) выстилает внутреннюю поверхность, а другой (висцеральный) окружает ближайшие органы. Оба листка продуцируют небольшое количество жидкого секрета своими железистыми клетками. С его помощью ликвидируется небольшое локальное воспаление, защищаются от трения органы, кишечник.
Жидкость постоянно обновляется, поскольку излишки всасываются эпителием. Накопление возможно при условии нарушения баланса этого состояния. В 75% случаев у пациентов с асцитом имеется цирроз печени. Это заболевание имеет максимальное число этиологических факторов, приводящих к патологии.
К ним относятся рост гидростатического давления в сосудах под влиянием застоя в венозной и лимфатической системах из-за нарушения сердечной деятельности и падение онкотического давления в крови за счет поражения функции печени и снижения содержания альбуминовой белковой фракции.
Асцит брюшной полости при онкологии не исключает эти механизмы в качестве дополнения к основному поражающему фактору — гиперфункции эпителия брюшной полости при опухолевом поражении листков брюшины. Рост злокачественных клеток вызывает раздражение и неспецифическое воспаление.
Наиболее значима роль обсеменения злокачественными клетками при раке яичников, матки у женщин. Осложнение в этих случаях настолько утяжеляет общее состояние пациенток, что они погибают при нарастании асцита брюшной полости.
Немалое значение имеет непосредственное сдавливание опухолью печеночной ткани и создание условий портальной гипертензии. При росте венозного давления водная часть крови сбрасывается в брюшную полость.
Раковая интоксикация сопровождается недостатком кислорода в клетках (тканевая гипоксия). Почечная ткань очень остро чувствует любые изменения и реагирует снижением фильтрации. Это приводит в действие механизм влияния антидиуретического гормона гипофиза, который задерживает натрий и воду.
Некоторые авторы в патогенезе асцита выделяют печеночный и внепеченочный механизмы. На примере злокачественного роста мы видим, как эти причины дополняют друг друга. Нарушается всасывающая функция брюшины и лимфатических сосудов.
Примером местных изменений может быть лимфома брюшной полости. Эта опухоль сопровождается нарушенной проходимостью внутрибрюшных лимфатических протоков. Из них жидкость переходит прямо в брюшную полость.
Провоцирующими причинами асцита при онкологических заболеваниях может быть такая анатомическая особенность, как близкое расположение складок брюшины (прилегание), обилие кровеносных и лимфатических сосудов, что вызывает быстрое распространение злокачественного роста на соседние ткани.
Стимулировать пропотевание жидкости может занос атипических клеток в полость брюшины при оперативном вмешательстве, внутреннее прорастание стенок брюшины злокачественной опухолью, а также проведение курса химиотерапии.
У онкологических больных асцит развивается постепенно за несколько недель или месяцев. Пациенты ощущают признаки при скоплении значительного количества жидкости. Основные симптомы:
- распирающая тяжесть в животе;
- отрыжка после еды;
- изжога или тошнота;
- тупые боли в животе;
- одышка в покое, особенно в положении лежа.
Эти признаки связаны с подъемом купола диафрагмы, нарушением перистальтики пищевода, кишечника, рефлюксным забросом кислого содержимого желудка в пищевод. Некоторые пациенты жалуются на приступы сердечной аритмии. При наблюдении лечащий врач выявляет увеличенный живот. В положении стоя он опускается вниз, пупок выпячивается.
Для больных с «печеночным» асцитом характерна картина «головы медузы» за счет образования плотных расширенных вен вокруг пупка. Накопление жидкости создает трудности при наклонах, обувании.
К сожалению, еще нередки случаи выявления молодых женщин с опухолью яичников в запущенном состоянии, которые длительно были уверены в своей беременности, этому способствовало прекращение менструаций.
Скопившаяся жидкость сама давит на опухоль, вызывает распад. Метастазирование по венозной системе и сердечная недостаточность проявляется затрудненным оттоком крови к сердцу. Это приводит к отечности стоп, голеней, наружных половых органов.
Все описанные симптомы развиваются не изолированно. На первом месте остаются признаки злокачественной опухоли. Асцит требует дополнительного лечения, поскольку жить с его проявлениями становится более опасно из-за возможностей других осложнений.
Независимо от причин в течении асцита выделяют 3 стадии. Они характерны и для пациентов с онкологическими заболеваниями:
- транзиторная — больной чувствует только вздутие живота, объем накопившейся жидкости не более 400 мл;
- умеренная — количество экссудата в брюшине доходит до 5 л, проявляются все описанные симптомы, возможны разные осложнения;
- напряженная — асцит скапливает 20 л и более, считается устойчивым (резистентным), лечить мочегонными средствами невозможно, сопровождается тяжелым состоянием, нарушает работу сердца и дыхание.
Тяжесть основного заболевания в случае появления асцита снижает шансы больного на выздоровление. Еще более увеличивается риск опасных осложнений. К ним относятся:
- бактериальный перитонит — присоединение инфекции вызывает острое воспаление брюшины;
- кишечная непроходимость;
- появление грыж в области белой линии живота, пупка, в паху с возможным защемлением;
- сердечная декомпенсация;
- накопление жидкости между плевральными листками — гидроторакс с острой дыхательной недостаточностью;
- развитие гепаторенального синдрома;
- геморроидальные кровотечения, выпадение нижнего отдела прямой кишки.
Такое осложнение, как асцит заранее предполагается в течение онкологического заболевания. При контроле за пациентом врач обязан проводить взвешивание. Рост массы на фоне выраженного похудения рук, ног, тела вызывает подозрение на скрытые отеки.
Если сделать толчковое движение рукой с одной стороны живота, то при наличии жидкости вторая рука ощутит волну в противоположном боку. Объективным подтверждением служат дополнительные исследования:
- УЗИ — позволяет выявить 200 мл жидкости в брюшной полости, одновременно служит контролем за изменениями во внутренних органах;
- обзорная рентгенография и томография — потребуют хорошей подготовки пациента перед исследованием, выявляет жидкость при изменении положения тела;
- лапароцентез — прокол передней брюшной стенки с целью откачивания жидкости и ее лабораторного анализа, процедура является одновременно лечебной и диагностической, позволяет выявить степень обсеменения брюшины, состав экссудата, наличие микрофлоры.
Терапия асцита теоретически должна в первую очередь заключаться в подавлении роста злокачественных клеток в брюшине. Тогда можно ожидать удаления раздражающего механизма и восстановления функции всасывания жидкости.
Но на практике методы химиотерапии помогают уменьшить асцит только при новообразованиях в кишечнике, а при локализации в печени, желудке, матке, яичниках остаются безрезультатными.
Остается контролировать поступление и выведение жидкости с продуктами питания, рассчитывать на оптимальные условия действия мочегонных средств (диуретиков). Убрать излишки воды можно с помощью ограничительной диеты. Пациенту назначается бессолевое питание, все блюда готовятся без соли, по согласованию с врачом возможно присаливание в тарелку.
Исключаются острые приправы, тяжелая жирная пища, все приготовленное в жареном виде. Объем употребляемой жидкости рассчитывается по диурезу (количеству выделенной мочи за сутки). При этом в меню должны быть продукты, обеспечивающие организм белком и калием. Поэтому рекомендуется:
- отварное нежирное мясо и рыба;
- творог, кефир при хорошей переносимости;
- запеченный картофель;
- компот из кураги, изюма;
- морковь, шпинат;
- овсяная каша.
В назначении диуретиков нельзя переусердствовать. Известна рекомендация врачей пить больше жидкости при любой интоксикации. Это касается и рака. Выведение большого объема воды из организма повышает общую интоксикацию продуктами распада злокачественных клеток, поэтому допустимым считается снижение веса на фоне приема диуретиков на 500 г за сутки.
Выбор диуретиков и дозировки всегда остается за врачом. Нельзя самостоятельно менять препараты, нарушать схему приема. Наиболее действенной оказывается комбинация из Фуросемида, Верошпирона и Диакарба.
Фуросемид (Лазикс) относится к группе петлевых диуретиков. Действие основано на блокировании обратного всасывания натрия и хлора в канальцах и петле Генле, выводящего аппарата почек. Одновременно выводит калий. Чтобы не нарушить баланс электролитов и не вызвать приступы аритмии назначаются препараты калия (Панангин, Аспаркам).
Верошпирон в отличии от Фуросемида является калийсберегающим препаратом. В его состав входит спиронолактон (гормон надпочечников). Именно с помощью гормонального механизма удается вывести лишнюю жидкость без калия. Таблетки начинают действовать спустя 2–5 дней после начала приема. Остаточный эффект продолжается 3 дня после отмены препарата.
Диакарб — препарат, имеющий целевое назначение. Особенно показан для предупреждения отека мозга, менее эффективен в процессе вывода мочи. Его действие начинается спустя 2 часа после приема. Связано с блокированием фермента карбоангидразы в тканях почек и мозга.
Наиболее часто для вывода накопившейся жидкости в полости брюшины при резистентной стадии асцита применяют процедуру лапароцентеза. Метод считается хирургическим, хотя им владеют терапевты в специализированных отделениях.
Суть методики: пациент сидит на стуле, живот вокруг пупка обрабатывается йодом. В точку примерно на 2 см ниже пупочного кольца вводится раствор Новокаина для обеспечения местной анестезии. После чего делается прокол брюшной стенки специальным инструментом (троакаром). Появление жидкости указывает на попадание в полость брюшины. Присоединяется трубка, по которой откачивается жидкость самотеком.
Однократно удаляется до 10 литров жидкости. На фоне постепенного уменьшения живота проводят стягивание простыней для предотвращения коллапса больного. В некоторых случаях при невозможности сразу вывести большой объем жидкости в полость брюшины вставляют дренажную трубку и перекрывают ее до следующего раза. Таким образом, повтор процедуры проводят 2–3 дня подряд.
При лапароцентезе необходимо следить за стерильностью, поскольку возрастает риск заражения брюшины и перитонита
Лапароцентез не проводится:
- при спаечной болезни брюшной полости;
- на фоне выраженного метеоризма;
- в периоде восстановления после грыжесечения.
Перитонеовенозное шунтирование — заключается в соединении специальной трубкой брюшной полости с верхней полой веной, по ней при дыхании пациента жидкость отходит в венозное русло. Деперитонизация — иссечение участков брюшины для обеспечения дополнительными путями вывода жидкости.
Оментогепатофренопексия — иссечение сращенного с передней брюшной стенкой сальника и подшивание его к диафрагме или печени, необходимо, если сальник мешает проведению лапароцентеза.
В народных лечебниках описываются растительные настойки, которые помогают уменьшить асцит при онкозаболеваниях. Врачи относятся к ним крайне негативно, поскольку нередко пациенты, уверовав в сказочные результаты, бросают основное лечение.
Однако при отсутствии реальной помощи от проводимой терапии больного раком можно понять. Поэтому мы приводим перечень растений, которые, по мнению травников, способны помочь:
- астрагал перепончатый;
- корень болотного аира;
- молочай;
- корень травы копытня;
- трава княжика сибирского;
- болотный сабельник.
Гораздо увереннее врачи рекомендуют мочегонные сборы в дополнение к лекарственным препаратам. Они включают растущие в средней полосе России:
- расторопшу,
- березовые почки и сок,
- чабрец,
- цветы липы, календулы,
- мелиссу,
- шалфей,
- зверобой,
- душицу,
- мяту,
- пустырник.
Общий показатель выживаемости пациентов с асцитом при онкологических заболеваниях дает неутешительные цифры — два года проживет только половина больных.Окончательный исход бывает как лучше, так и хуже предполагаемого срока.
Он зависит от реакции пациента на лечение, возраста, наличия хронических заболеваний почек, печени, сердца, характера опухолевого роста. Асцит в начальной стадии при опухолях лечится значительно эффективнее. Поэтому в терапии злокачественных новообразований следует предусматривать раннюю диагностику осложнений.
источник
Лапароцентез при асците: понятие, определение, классификация, характеристика и методы проведения процедуры, показания и противопоказания
Одним из способов диагностики при водянке брюшной полости является лапароцентез. При асците эта процедура является наиболее информативной. Сама процедура представляет собой несложную хирургическую манипуляцию по проколу живота и забору содержимого с целью лабораторного исследования.
При асците этот вид диагностического хирургического вмешательства необходим для уточнения характера содержимого в брюшине. Первые попытки осуществить процедуру были предприняты в позапрошлом веке. Тогда лекари пытались проколоть живот при патологическом увеличении его объема. Лапароцентез при асците помог установить разрыв желчного пузыря после травмирования брюшной полости. В середине прошлого века методика активно осваивалась хирургами в разных странах. Сегодня манипуляция является не только одной из самых информативных и эффективных, но и безопасных для человека.
В наши дни такая хирургическая операция проводится не только при асците. К лапароцентезу брюшной полости часто прибегают при необходимости точного обследования пациентов после травм, при подозрении на кровотечение, прободение стенок кишечника. Благодаря малой инвазивности и минимальной травматичности, после лапароцентеза не развиваются осложнения. Главное – это соблюдение правил асептики и точной техники выполнения манипуляции врачом-хирургом.
Пункция брюшной полости назначается исключительно в целях диагностики и постановки точного достоверного диагноза при смазанной клинической картине. Отдельные техники лапароцентеза при асците позволяют использовать данную процедуру для лечения патологии путем эвакуации жидкости. Исследовательскую пункцию можно назвать лечебной в том случае, если, помимо обнаружения аномального образования, хирург сразу же удалит его.
Лапароцентез проводится амбулаторно, в стационарном отделении к нему прибегают в случае травматических повреждений и невыясненного диагноза. Процедуру проводят не только при асците. Показаниями для лапароцентеза могут служить и другие патологические состояния:
- подозрение на внутреннее кровотечение в животе;
- перитонит;
- перфорация кишечных стенок в результате закрытых травм;
- прободение язвы желудка или 12-перстной кишки;
- разрыв кисты;
- тупые травмы брюшной полости у пациента, находящегося в коме, тяжелом алкогольном или наркотическом опьянении и не способного указать конкретные симптомы;
- многочисленные травмы у человека без сознания в случае, если имели место серьезные повреждения и разрыв внутренних органов;
- раны с проникновением в область грудины из-за риска повреждения диафрагмы.
Жидкий материал, полученный через прокол брюшной полости, направляется на лабораторное исследование. Асцитический экссудат должен быть детально изучен на предмет примесей крови, гноя, фекалий, мочи, желчи и желудочного сока.
В некоторых случаях хирургическое вмешательство в брюшную полость является недопустимым из большой вероятности неблагоприятных последствий при асците. Лапароцентез зачастую служит единственным вариантом исследования, особенно тогда, когда другие способы диагностики оказываются недостаточно информативными по поводу содержимого брюшной полости.
Прокол живота противопоказан при:
- заболеваниях свертываемости крови из-за высоких рисков развития кровотечения;
- осложненной спаечной болезни;
- сильном вздутии живота;
- рецидивирующей пупочной или эпигастральной грыже;
- кишечная непроходимость;
- вероятности травматизации кишечника или опухоли;
- беременности.
Лапароцентез нужно крайне осторожно проводить на участке, близко расположенном к мочевому пузырю, а также органах, увеличенных в размере. Стоит отметить, что наличие спаек — это не абсолютное противопоказание для осуществления манипуляции. Все дело в том, что сама по себе патология обуславливает высокую вероятность повреждения кровеносных сосудов и соседних органов. Показания к лапароцентезу при асците должны оцениваться врачом в индивидуальном порядке.
В ходе подготовки к запланированному вмешательству в брюшную полость при асците, техника лапароцентеза подбирается индивидуально. Пациенту назначают предварительные стандартные обследования. Больной должен сдать общие анализы мочи и крови, коагулограмму, пройти УЗИ внутренних органов и, если врач посчитает нужным и необходимым, рентгенографию с контрастным веществом.
Лапароцентез брюшной полости при асците на дому не выполняется. Степень подготовки к проведению лапароцентеза приближена к такой, какая требуется перед любым другим хирургическим вмешательством. К тому же, хирург, выполняющий манипуляцию, всегда должен быть готов к переходу от диагностического лапароцентеза к лечебной лапаротомии.
За сутки до хирургического вмешательства больной должен отказаться от еды, а непосредственно перед манипуляцией опорожнить мочевой пузырь, кишечник и желудок. При серьезных повреждениях и тупых травмах живота, сопровождающихся шоком или коматозным состоянием, осуществляется искусственная вентиляция легких. Лапароцентез при асците проводят в операционной, где всегда имеется возможность экстренно перейти открытому хирургическому вмешательству.
Прокол живота осуществляется при местной анестезии, а в общем наркозе, как считают врачи, нет никакой необходимости. Перед лапароцентезом при асците, по отзывам некоторых пациентов, проводят премедикацию, которая показана людям с психическими отклонениями, а также особо впечатлительным и нервным лицам. Суть премедикации заключается в предварительном введении подкожной инъекции «Атропина сульфата», «Промедола», «Лидокаина» или «Новокаина».
Перед пункцией больному следует пройти тест на чувствительность к анестетикам, так как большинство обезболивающих препаратов вызывает аллергические реакции. Чтобы убедиться в безопасности выбранного средства, на коже предплечья пациенту делают легкую царапину стерильной иглой и наносят пару капель лекарства. Если спустя 20-30 минут никакой реакции не последовало, в том числе остался прежним цвет кожных покровов, отсутствует зуд и отечность, пробу считают удачной. При положительной реакции, сопровождающейся покраснением кожи, анестетик меняют.
Для осуществления данной процедуру потребуются специальные медицинские инструменты. Прокол брюшной стенки проводится с помощью специального троакара, трубки для отвода жидкости, шприцев и зажимов. Асцитическую жидкость, извлеченную из живота, собирают в стерильную емкость, которую впоследствии отправят на бактериологическое исследование. Хирург в обязательном порядке должен использовать стерильные перчатки.
Техника лапароцентеза при асците подразумевает сидячее положение пациента, но в некоторых случаях допускается проведение операции лежа на спине. Под его ягодицы кладут клеенчатый материал, одноразовую пеленку. Для хирурга такая манипуляция не представляет особой сложности. Перед проколом место предполагаемого доступа обрабатывают антисептическим раствором.
Пункцию делают посередине живота, отступив 2-3 см вниз от пупка, иногда немного левее. Намного реже иглу запускают в срединную точку между пупком и лобковой областью. Перед тем как проникнуть троакаром внутрь брюшной полости, врач делает незначительный надрез скальпелем, чтобы рассечь кожу, слой подкожно-жировой клетчатки и мышц. Хирург должен действовать максимально осторожно, чтобы случайно соскользнувший скальпель не повредил внутренности. Сегодня хирурги все чаще начинают операцию с раздвижения тканей тупым методом, без использования ножа.
По мере продвижения троакара вглубь полости задачей хирурга является своевременная остановка кровотечения из сосудов кожи и клетчатки. В противном случае не исключаются погрешности в результатах исследования асцитической жидкости. Троакар направляют в отверстие брюшины под острым углом в 45° по отношению к мечевидному отростку грудины. Врач должен обеспечить пространство для проникновения иглы, захватив пупочное кольцо и слегка приподняв брюшную стенку. Правильная техника выполнения лапароцентеза при асците позволит совершить пункцию безопасно для пациента. Часто в процессе хирурги используют специальную нить, которую вводят в область прокола живота через апоневроз прямой мышцы брюшного пресса. Прикрепив хирургическую нить к этому мускулу, появляется возможность приподнять мягкие ткани живота.
Техника выполнения лапароцентеза при асците брюшной полости не мешает проводить манипуляцию в амбулаторных условиях. Введение иглы осуществляется по описанному ранее принципу. Как только их полости троакара появится жидкость, инструмент наклоняют к емкости, приготовленной заранее. Во процессе оттока жидкости важно удерживать пальцами дистальный конец, чтобы он не соскочил.
При асците нельзя извлекать брюшную жидкость слишком быстро. Стремительная потеря асцитической воды может привести к резкому снижению артериального давления, в тяжелых случаях вплоть до коллапса. Это происходит из-за резкого перенаправления крови по сосудам брюшной полости, которые до этого были сдавлены жидкостью. Чтобы не допустить подобного осложнения, жидкость извлекают медленно – каждый час по 400 мл. При этом пациента не оставляют без внимания. Рядом с ним должен постоянно находиться персонал медучреждения. Ассистент хирурга в ходе процедуры, по мере уменьшения объемов живота, стягивает брюшную полость полотенцем с целью предотвращения гемодинамических расстройств.
После окончательного удаления асцитической жидкости, иглу осторожно извлекают, а разрез зашивают и накладывают стерильную повязку. Сжимающее полотенце нежелательно снимать, так как в первое время оно поможет создать правильное внутрибрюшное давление и помочь больному привыкнуть к новым условиям кровоснабжения. В случае оставления трубки для поэтапной эвакуации жидкости, больному следует периодически менять положение тела для улучшения оттока жидкости.
Если решение о проведении данной манипуляции принималось с целью полного обследования пациента, процедура будет проходить немного иначе. Для того чтобы обнаружить патологическое содержимое в брюшной полости, хирург использует так называемый шарящий катетер. Он соединяется со шприцем, который отсасывает асцитический экссудат. Если шприц остается пустым, то в живот вводится физраствор (приблизительно 300 мл), затем его извлекают и отправляют на исследование.
Если в ходе осуществления манипуляции потребуется осмотреть внутренние органы, то в трубку троакара помещают лапароскоп. Врач, обнаруживая тяжелые повреждения, может принять решение об оперативном лечении прямо в процессе лапароцентеза. В этом случае диагностическая процедура принимает масштабы серьезного полостного вмешательства.
По завершении лапароцентеза полученное содержимое отправляют на исследование в лабораторию. Там оценивается не только внешний вид жидкой массы, но и составляется заключение о ее биохимических показателях. Если в биоматериале обнаруживается кровь, присутствуют элементы фекалий или примеси мочи, пациента необходимо срочно оперировать. Вызывать серьезные опасения может и характерный для перитонита гнойный серо-зеленый или желтоватый цвет. Такой внешний вид брюшной жидкости, полученной в ходе лапароцентеза, может свидетельствовать о внутрибрюшном кровотечении, прободении стенки кишечника или желудка, гнойно-воспалительном или некротическом процессе, что означает лишь одно: нельзя терять ни минуты.
Распознать кровотечение при исследовании жидкой массы из живота пациента можно по примеси эритроцитов и лейкоцитов. Кстати, с помощью лапароцентеза могут проводиться пробы для уточнения, удалось ли остановить кровотечение или нет. При этом присутствие кровяных частиц в незначительном объеме может являться ложноположительным признаком активного кровотечения.
Если в асцитическом экссудате обнаружилась моча, скорее всего, имеет место разрыв стенки мочевого пузыря. Присутствие фекалий – прямое подтверждение прободения кишечной стенки. Мутный вид жидкости и большой процент фибрина (белка) в ней указывает на перитонит, который является показанием к экстренному хирургическому лечению.
Прокол живота чаще всего делают при асците. Лапароцентез может быть показан даже при стабильном состоянии больного и отсутствии патологического содержимого в животе, если факт тупой травмы живота не исключает вероятность повреждения органа или кровотечения. Так, например, при разрыве селезенки или гематоме печени возможно их увеличение в размере и излитие крови в полость. В подобных случаях хирург устанавливает силиконовый дренаж после лапароцентеза на двое суток, обеспечивая нормальный отток жидкости.
Негативные последствия манипуляции развиваются в исключительных случаях. С наибольшей вероятностью может развиться инфекционный процесс в месте пункции при игнорировании правил асептики. У больных с тяжелыми заболеваниями печени и желудочно-кишечного имеется риск появления флегмоны брюшной стенки. Если врач повредит крупные сосуды, не исключено внутреннее кровотечение. Причиной повреждения внутренних органов после лапароцентеза также может стать неосторожность хирурга.
Неблагоприятным последствием лапароцентеза брюшной полости при асците может стать коллапс и кровотечение на фоне длительного истечения асцитической жидкости после пункции. При этом послеоперационный период всегда протекает без осложнений, так как данное вмешательство не требует применения общего наркоза и значительного повреждения тканей. Швы после лапароцентеза снимают спустя неделю после операции. После прокола живота больному рекомендуют воздерживаться от физических нагрузок, придерживаться ограничений в питании и соблюдать постельный режим.
источник
Лапароцентез – хирургическая процедура, которое представляет собой прокол брюшной стенки для извлечения патологического содержимого (например, при асците).
Причиной возникновения асцита является нарушение оттока венозной крови через печень и повышение давления в сосудистых коллекторах живота, в результате чего перитонеальная жидкость просачивается в брюшную полость.
В зависимости от количества жидкости в полости врач принимает решение о назначении лапароцентеза. В тех случаях, когда количество жидкости не очень большое, пациенту назначаются мочегонные средства, с помощью которых за некоторое время можно избавиться от лишней воды естественным путем. Вместе с тем, встречаются случаи, когда количество жидкости в брюшной полости достигает 15-20 л, и без лапароцентеза не обойтись.
В Юсуповской больнице врачи могут назначать лапароцентез не только при асците, но и для обнаружения, исключения или удаления патологического содержимого в брюшной полости. Показаниями к проведению этой процедуры являются:
- наличие закрытой травмы живота, если установить повреждения не удалось с помощью рентгеновских, клинических и лабораторных исследований;
- наличие повреждений нескольких органов;
- травма, осложненная шоком или коматозным состоянием;
- закрытая травма живота у пациентов в тяжелом алкогольном или наркотическом опьянении;
- стремительное угасание жизненных функций при травмах головы, груди и конечностей;
- проникающие раны в грудную клетку с возможным повреждением диафрагмы;
- подозрение на внутрибрюшное кровотечение, разрыв кисты;
- скопление свободной жидкости в брюшной полости – асцит (наиболее частая причина применения лапароцентеза).
В каждой клинической ситуации к решению вопроса о проведении лапароцентеза доктор подходит индивидуально. Если есть резерв времени, то лапароцентезу предшествует тщательное исследование (лабораторная диагностика, ультразвуковое исследование) и сбор анамнеза. В критических ситуациях, когда речь идет о жизни пациента, лапароцентез позволяет быстро обнаружить причину патологии и принять своевременные меры.
Среди противопоказаний к лапароцентезу отмечают спаечную болезнь, выраженный метеоризм, высокий процент повреждения стенок кишечника, наличие опухолей больших размеров в брюшной полости, присутствие воспалительных и гнойных процессов, наличие послеоперационной вентральной грыжи.
Перед лапароцентезом доктор назначает ряд необходимых анализов и диагностических процедур, среди которых:
- физический осмотр;
- анализ на свертываемость крови;
- рентгеновское обследование;
- УЗИ;
Все диагностические процедуры можно пройти на месте, ведь оснащение Юсуповской больницы находится на высоте. Здесь есть все необходимое оборудование новейших образцов, которое позволяет быстро и точно установить диагноз с минимальным негативным воздействием на организм пациента.
Также пациент должен сообщить врачу об аллергии на препараты, беременности или если он уже принимает медикаменты. Непосредственно перед процедурой нужно опорожнить мочевой пузырь и кишечник, а за 12 часов до операции не есть и не пить.
Такое мини-вмешательство, как лапароцентез, осуществляется под местной анестезией, при этом пациент чаще находится в положении сидя, иногда его кладут на спину. Область, где будет производиться прокол, очищается и стерилизуется. После введения анестетика специальной иглой производится прокол внизу живота (примерно посредине между пупком и лобком), куда вводят небольшую трубку. С ее помощью будет удаляться жидкость. Количество выведенной жидкости за одну процедуру в среднем колеблется от 3 до 5 л, но в более тяжелых случаях доктор может принять решение и об извлечении 10 л.
Обычно лапароцентез занимает около получаса, но может длиться больше. Время будет зависеть от объема удаляемой жидкости и состояния пациента.
После завершения процедуры место прокола туго перевязывают. У пациента всегда измеряют температуру, пульс, давление. Перед лапароцентезом и после него измеряют вес.
После лапароцентеза образцы полученной жидкости исследуют для определения ее происхождения (цитологическое исследование). Пациенту не придется искать учреждение, где смогут исследовать полученную жидкость, ведь на базе Юсуповской больницы есть собственная лаборатория.
Если жидкость имеет отечную природу, то это может «говорить» о сердечной недостаточности, циррозе печени или нефротическом синдроме. При получении жидкости воспалительной природы следует говорить о наличии опухолей или метастазов в органах брюшной полости.
Процент возникновения осложнений при проведении лапароцентеза в Юсуповской больнице очень низкий (меньше 1%), но никакая операция не может гарантировать их отсутствие. Среди осложнений у пациента может возникнуть:
- кровотечение;
- случайный прокол органов, расположенных в брюшной полости;
- инфекция.
Увеличивается риск осложнений при беременности, проведении операции с полным мочевым пузырем, кровотечении и плохом питании. Поэтому, по возможности, стоит исключить эти факторы.
В домашних условиях нужно соблюдать рекомендации врача и по возможности взять несколько отгулов.
Немедленно стоит обратиться в больницу, если наблюдаются симптомы:
- лихорадка, озноб и другие признаки инфекции;
- выбухание брюшной стенки;
- покраснение, сильная боль, опухоль в месте прокола;
- болезненные ощущения, которые не проходят даже после приема обезболивающих средств;
- слабость и боль в груди, одышка, кашель.
Цена лапароцентеза зависит от сложности операции, анестезии и клиники, в которой проводилась процедура. Более подробно узнать о стоимости процедуры можно по телефону.
В Юсуповской больнице лапароцентез проводят достаточно часто. В клинике работают врачи высшей категории и кандидаты медицинских наук, у которых большой практический опыт.
источник
Автор: Аверина Олеся Валерьевна, к.м.н., врач-патолог, преподаватель кафедры паталогической анатомии и патологической физиологии
Лапароцентез представляет собой диагностическую хирургическую операцию, при которой врач производит прокол передней брюшной стенки для уточнения характера содержимого брюшной полости.
Первые попытки провести прокол живота были осуществлены еще в конце XIX века, когда вполне успешно с помощью этой методики установили разрыв желчного пузыря после тупой травмы живота. В середине прошлого столетия метод был активно освоен хирургами разных стран и доказал не только высокую эффективность, но и безопасность для пациента.
Сейчас лапароцентез широко применяется для диагностики различных последствий травм и при других патологических состояниях — асцит, перфоративная язва, кровотечения и т. д. Операция малоинвазивна, малотравматична и практически не дает осложнений при соблюдении правил асептики, антисептики и точной техники ее проведения.
Обычно к пункции брюшной полости прибегают в диагностических целях, когда клиническая картина не позволяет поставить достоверный диагноз. В других случаях ее проводят для лечения — эвакуация жидкости, например. Кроме того, диагностическая пункция может стать лечебной, если в ее ходе врач не только обнаружит аномальное содержимое в животе, но и его удалит.
Лапароцентез может быть проведен амбулаторно при асците, в стационаре его используют при травматических повреждениях в случае неясного диагноза, а также перед лапароскопическими вмешательствами на органах живота для введения углекислоты.
Показаниями в лапароцентезу считаются:
Подозрение на кровотечение в брюшную полость, перитонит;
Проведение лапароцентеза — часто единственно возможный способ диагностики, когда другие методы (рентгенография, ультразвук и т. д.) не дают шанса исключить повреждения внутренних органов с выходом содержимого в брюшную полость.
Полученная в ходе операции жидкость — асцитическая, гной, кровь — направляются на лабораторное исследование. Экссудат неопределенного состава должен быть исследован на примеси содержимого желудочно-кишечного тракта, желчи, мочи, сока поджелудочной железы.
Лапароцентез противопоказан при:
- Нарушениях свертываемости крови ввиду риска кровотечения;
- Тяжелой спаечной болезни брюшной полости;
- Сильном вздутии живота;
- Вентральной грыже после предыдущих оперативных вмешательств;
- Риске травмы кишечника, крупной опухоли;
- Беременности.
Не рекомендуется проводить лапароцентез близко к области мочевого пузыря, увеличенных в объеме органов, пальпируемого опухолевидного образования. Наличие спаек — относительное противопоказание, но сама по себе спаечная болезнь предполагает высокий риск повреждения сосудов и органов брюшной полости, поэтому показания к лапароцентезу в этом случае оцениваются индивидуально.
В процессе подготовки к плановому лапароцентезу (обычно по поводу асцита), больному показаны стандартные обследования. Он сдает анализы крови и мочи, коагулограмму, проходит ультразвуковое исследование органов живота, рентгенографию и т. д., в зависимости от показаний к манипуляции.
Учитывая возможность перехода к лапаротомии или лапароскопии, подготовка максимально приближена к таковой перед любой другой операцией, но в случаях травм или экстренной хирургической патологии исследования занимают минимум времени и включают общеклинические анализы, определение свертываемости крови, ее группы и резус-принадлежности. По возможности — УЗИ или рентген органов брюшной или грудной полости.
Непосредственно перед проколом брюшной стенки необходимо опорожнить мочевой пузырь и желудок. Мочевой пузырь опустошается самостоятельно либо при помощи катетера, если пациент без сознания. Желудочное содержимое удаляется посредством зонда.
При серьезных травмах, шоковом состоянии, коме проводится противошоковая терапия для поддержания гемодинамики, по показаниям налаживается искусственная вентиляция легких. Лапароцентез таким пациентам проводят в операционной, где есть возможность быстрого перехода к открытой операции или лапароскопии.
Прокол брюшной стенки проводится под местной анестезией, требуемые инструменты для лапароцентеза — специальный троакар, трубка для отвода содержимого, шприцы, зажимы. Жидкость, извлеченная из брюшной полости, собирается в емкость, а при направлении на бактериологическое исследование — в стерильные пробирки. Врач обязательно использует стерильные перчатки, а при асците больного укрывают клеенчатым фартуком или пленкой.

Прокол производится по средней линии, отступя 2 см книзу от пупка или немного левее, в некоторых случаях — в середине расстояния между пупком и лобком. Перед проникновением троакара хирург делает небольшой надрез скальпелем, рассекая кожу, клетчатку и мышцы, действуя максимально аккуратно, так как острый скальпель может соскользнуть глубже и повредить внутренние органы. Многие хирурги раздвигают ткани тупым способом, без скальпеля, что более безопасно для пациента. По мере продвижения вглубь важно обеспечить остановку кровотечения из сосудов кожи и клетчатки, чтобы избежать недостоверных результатов.
В полученное отверстие брюшной стенки направляют троакар, вводят его в брюшную полость вращательными движениями под углом 45 градусов относительно мечевидного отростка грудины.
Чтобы создать пространство для движения троакара захватывается пупочное кольцо, и брюшная стенка несколько приподнимается. Облегчить и обезопасить пункцию помогает также хирургическая нить, введенная в области пункции через апоневроз прямой мышцы, за которую можно приподнять мягкие ткани живота.

При быстром извлечении асцитической жидкости возможны колебания артериального давления вплоть до коллапса, так как кровь мгновенно перенаправится в сосуды брюшной полости, сдавленные ранее жидкостью. Чтобы избежать резкой гипотонии, жидкость удаляют медленно (не более литра в течение пяти минут), тщательно наблюдая за состоянием пациента. Помощник хирурга в процессе манипуляции постепенно стягивает живот больного полотенцем, чтобы избежать гемодинамических расстройств.
Когда асцитическая жидкость полностью удалена, троакар извлекают, а на разрез накладывают шов и стерильную повязку. Целесообразно не снимать сжимающее полотенце, которое поможет создать привычное для больного внутрибрюшное давление и постепенно адаптироваться к новым условиям кровоснабжения органов брюшной полости.
Если в процессе лапароцентеза возникает необходимость в осмотре внутренних органов, то в трубку троакара можно поместить лапароскоп. При диагностике тяжелых повреждений, требующих хирургического вмешательства, операция расширяется до лапароскопии или лапаротомии.
После того, как хирург получил содержимое брюшной полости, важно оценить его внешний вид и принять соответствующие меры по дальнейшему лечению. Если в полученном материале обнаружена кровь , каловые массы, примеси мочи, содержимого кишечника и желудка либо жидкость имеет серо-зеленый, желтый цвет, больному необходима срочная операция. Такой вид содержимого может говорить о внутрибрюшном кровотечении, перфорации стенки органов пищеварения, перитоните, а это значит, что медлить нельзя для спасения жизни пациента.
Диагностическая ценность лапароцентеза зависит от объема жидкости, полученной в процессе выполнения манипуляции. Чем ее больше, тем точнее диагноз, а минимальным считается 300-500 мл, но и этот объем позволяет уточнить патологию не более, чем в 80% случаев.
При неубедительных результатах лапароцентеза, но имеющейся клинике острой хирургической патологии хирурги переходят к лапаротомии, чтобы не упустить драгоценное для больного время и не пропустить тяжелой и смертельно опасной патологии.
В случае, когда не удается получить никакого патологического отделяемого, а клиническая картина либо факт травмы дают четкие указания на его наличие, возможно проведение перитонеального лаважа физиологическим раствором. Для этого вводится до литра стерильного раствора, который затем удаляется для исследования.
Примесь эритроцитов, лейкоцитов в извлеченной жидкости, определенных с помощью цитологического исследования, дает возможность диагностировать кровотечение. Кроме того, хирурги проводят пробы для уточнения, остановилось кровотечение или нет. Даже при большом объеме кровянистых масс есть вероятность, что кровотечение все же остановилось, а если оно продолжается, то незамедлительно начинаются противошоковые мероприятия, позволяющие снизить риски при последующей срочной лапаротомии.
Наличие в содержимом брюшинной полости мочи, которая определяется по характерному запаху, говорит о разрыве стенки мочевого пузыря, а каловые массы — о перфорации стенки кишки. Если экссудат имеет мутный вид, зеленоватый или желтый цвет, определяются хлопья белка фибрина, то высока вероятность перитонита вследствие повреждения полых внутренних органов, а эта ситуация требует срочной открытой операции.
Бывает, что патологического содержимого в брюшной полости нет, состояние пациента стабильное, но факт травмы не позволяет исключить вероятность разрыва органа или кровотечения в ближайшем будущем. К примеру, гематомы селезенки или печени, располагающиеся под капсулой органа, по мере увеличения в размерах могут привести к разрыву и излитию крови в живот. В таких случаях хирург после лапароцентеза может оставить силиконовый дренаж для контроля на 24-48 часов, установив его таким образом, чтобы обратный ток жидкости был адекватным, иначе возможно не обнаружить вовремя патологию.
Лапароцентез — относительно безопасная, простая и, в то же время, информативная манипуляция, но в числе его недостатков — не только возможные осложнения, но и недостоверные результаты, как ложноположительные, так и ложноотрицательные, поэтому первоочередная задача специалиста — правильно оценить характер полученного материала, что зачастую бывает затруднительно.
Ложноотрицательные результаты наиболее часто связаны с тем, что гибкие силиконовые катетеры плохо управляемы и могут не достичь мест скопления жидкости. Участки живота, отграниченные спайками, и вовсе недоступны для «шарящих» катетеров, но там может скопиться жидкость при повреждении полых органов. Ложноотрицательный результат бывает вызван закупоркой катетера тромбом.
Ложноположительные результаты в отношении кровотечения часто связаны с неправильной техникой процедуры лапароцентеза, попаданием из места прокола внутрь небольшого количества крови, которая может быть принята за содержимое брюшной полости.
Чтобы избежать диагностических ошибок, которые могут быть чрезвычайно опасны, при получении нечетких данных о кровотечении, малого объема кровянистого отделяемого либо отсутствии содержимого при явной клинике «острого» живота, хирурги проводят диагностическую лапароскопию, которая более достоверна в неотложной хирургии.

«Домашний» лапароцентез очень актуален для больных, которые в силу имеющихся заболеваний не могут перемещаться на большие расстояния, вынуждены соблюдать постельный режим, страдают застойной сердечной недостаточностью, а также для лиц пожилого и старческого возраста.
На дому лапароцентез проводят после предварительного осмотра, под контролем ультразвука. Такую услугу предлагают многие платные клиники, оснащенные необходимым переносным оборудованием и имеющие в штате высококвалифицированных специалистов. Риск осложнений лапароцентеза, проведенного на дому, может быть выше, поэтому очень важно соблюдать и технику манипуляции, и профилактику инфекционных осложнений.
Осложнения после лапароцентеза довольно редки. Наиболее вероятны инфекционные процессы в месте прокола при несоблюдении правил асептики и антисептики. У тяжелых больных возможно развитие флегмоны брюшной стенки и перитонита. Повреждение крупных сосудов чревато кровотечением, а неосторожные действия хирурга могут привести к травмам внутренних органов скальпелем или острым троакаром.
Лапароцентез используется для наложения пневмоперитонеума при лапароскопических вмешательствах. Неправильное введение газа в брюшную полость может повлечь его попадание в мягкие ткани с развитием подкожной эмфиземы, а избыток нарушает экскурсию легких вследствие слишком высокого поднятия диафрагмы.
Последствиями извлечения асцитической жидкости может стать кровотечение, длительное истечение жидкости после пункции брюшной стенки, а во время самой процедуры — коллапс из-за перераспределения крови.
Послеоперационный период протекает благоприятно, так как вмешательство не предполагает ни наркоза, ни большого разреза тканей. Кожные швы снимаются на 7 день, а ограничения в режиме связаны с основным заболеванием (например, диета при циррозе или сердечной недостаточности, постельный режим после удаления гематом и остановки кровотечений).
После лапароцентеза не рекомендуются физические нагрузки, а в случае оставления трубки для медленной эвакуации жидкости пациенту рекомендуется менять положение тела, переворачиваясь периодически на другую сторону, для улучшения оттока жидкости.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
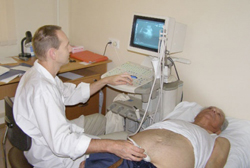
Подтвердить диагноз и установить причину асцита можно с помощью:
- перкуссии живота;
- пальпации живота;
- лабораторных анализов;
- ультразвукового исследования (УЗИ);
- магнитно-резонансной томографии (МРТ);
- диагностического лапароцентеза (прокола).
Пальпация (прощупывание) живота может дать важную информацию о состоянии внутренних органов и помочь врачу заподозрить ту или иную патологию. Определить наличие небольшого количества жидкости (менее 1 литра) методом пальпации довольно сложно. Однако на данном этапе развития заболевания можно выявить ряд других признаков, указывающих на поражение определенных органов.
С помощью пальпации можно обнаружить:
- Увеличение печени. Может быть признаком цирроза или рака печени. Печень при этом плотная, поверхность ее бугристая, неровная.
- Увеличение селезенки. У здоровых людей селезенка не пальпируется. Ее увеличение может быть признаком прогрессирующей портальной гипертензии (при циррозе или раке), метастазирования опухоли или гемолитических анемий (при которых клетки крови разрушаются в селезенке).
- Признаки воспаления брюшины (перитонита). Основным симптомом, указывающим на наличие воспалительного процесса в брюшной полости, является симптом Щеткина-Блюмберга. Для его выявления пациент ложится на спину и сгибает ноги в коленях, а врач медленно надавливает пальцами на переднюю брюшную стенку, после чего резко убирает руку. Появляющиеся при этом сильнейшие острые боли свидетельствуют в пользу перитонита.
При выраженном асците передняя брюшная стенка будет напряженной, твердой, болезненной, поэтому выявить выше перечисленные симптомы будет невозможно.
Симптом флюктуации (колебания) является важным признаком наличия жидкости в брюшной полости. Для его выявления пациент ложится на спину, врач левую руку прижимает к брюшной стенке пациента с одной стороны, а правой рукой слегка поколачивает по противоположной стенке живота. Если в брюшной полости имеется достаточное количество свободной жидкости, при постукивании будут образовываться характерные волнообразные толчки, которые будут ощущаться на противоположной стороне.
Симптом флюктуации может быть выявлен, если в брюшной полости имеется более 1 литра жидкости. В то же время, при выраженном асците он может быть малоинформативен, так как чрезмерно высокое давление в брюшной полости не позволит правильно провести исследование и оценить его результаты.
Лабораторные анализы назначаются после тщательного клинического обследования пациента, когда врач подозревает патологию того или иного органа. Целью лабораторных исследований является подтверждение диагноза, а также исключений других возможных заболеваний и патологических состояний.
При асците врач может назначить:
- общий анализ крови;
- биохимический анализ крови;
- общий анализ мочи;
- бактериологическое исследование;
- биопсию печени.
Общий анализ крови (ОАК)
Назначается с целью оценки общего состояния пациента и выявления различных отклонений, встречающихся при тех или иных заболеваниях. Так, например, у больных с циррозом печени и спленомегалией (увеличением селезенки) может отмечаться снижение концентрации эритроцитов (красных клеток крови), гемоглобина (дыхательного пигмента, транспортирующего кислород в организме), лейкоцитов (клеток иммунной системы) и тромбоцитов (кровяных пластинок, обеспечивающих остановку кровотечений). Объясняется это тем, что клетки крови задерживаются и разрушаются в увеличенной селезенке.
При инфекционно-воспалительных заболеваниях органов брюшной полости (в частности при перитоните и панкреатите) может отмечаться выраженное увеличение концентрации лейкоцитов (как ответ иммунной системы в ответ на внедрение чужеродной инфекции) и увеличение скорости оседания эритроцитов (СОЭ), что также указывает на наличие воспалительного процесса в организме.
Биохимический анализ крови (БАК)
При данном исследовании оценивается количество различных веществ в крови, что позволяет судить о функциональной активности определенных органов.
При циррозе печени будет отмечаться повышение концентрации билирубина (вследствие снижения обезвреживающей функции органа). Также для цирроза характерно уменьшение концентрации белков в крови, так как все они образуются в печени.
При воспалении брюшины или при панкреатите БАК позволяет выявить увеличение концентрации белков острой фазы воспаления (С-реактивного белка, фибриногена, церулоплазмина и других), причем их концентрация в крови напрямую зависит от выраженности и активности воспалительного процесса. Это позволяет вовремя распознать перитонит, а также контролировать состояние пациента в динамике в процессе лечения и вовремя выявить возможные осложнения.
При почечном асците (развивающемся в результате почечной недостаточности) в крови будет повышаться концентрации веществ, которые обычно выводятся почками. Особое значение имеют такие вещества как мочевина (норма 2,5 – 8,3 ммоль/литр), мочевая кислота (норма 120 – 350 мкмоль/литр) и креатинин (норма 44 – 100 мкмоль/литр).
БАК также важен при диагностике панкреатита (воспаления поджелудочной железы). Дело в том, что при прогрессировании заболевания происходит разрушение ткани железы, вследствие чего пищеварительные ферменты (панкреатическая амилаза) поступают в кровь. Повышение концентрации панкреатической амилазы более 50 Единиц действия/литр (Ед/л) позволяет подтвердить диагноз.
Общий анализ мочи (ОАМ)
Исследование мочи позволяет выявить отклонения в работе мочевыделительной системы. В нормальных условиях через почки ежедневно профильтровывается более 180 литров жидкости, однако около 99% из данного объема всасывается обратно в кровоток. На начальной стадии почечной недостаточности концентрационная и всасывающая функция почек может нарушаться, в результате чего будет выделяться большее количество менее плотной мочи (в норме удельный вес мочи колеблется в пределах от 1010 до 1022). При терминальной стадии заболевания удельный вес мочи может быть в норме или даже слегка повышенным, однако общее количество выделяемой в сутки мочи значительно снижается.
При нефротическом синдроме будет отмечаться выделение мочи повышенной плотности, в которой будет определяться увеличенная концентрация белков (более 3,5 грамм в сутки). Также ОАМ ценен при диагностике панкреатита, так как при данном заболевании концентрация амилазы повышается не только в крови, но и в моче (более 1000 Ед/л).
Бактериологическое исследование
Особую ценность данное исследование имеет при бактериальном и туберкулезном перитоните. Суть его заключается в заборе различного биологического материала (крови, асцитической жидкости, слюны) и выделении из него патогенных микроорганизмов, которые могли бы стать причиной развития инфекционно-воспалительного процесса. Это позволяет не только подтвердить диагноз, но и определить те антибиотики, которые лучше всего подойдут для лечения инфекции у данного пациента (чувствительность различных бактерий к антибактериальным препаратам различная, что можно определить в лабораторных условиях).
Биопсия печени
При биопсии производится прижизненное удаление небольшого фрагмента печеночной ткани пациента с целью его исследования в лаборатории под микроскопом. Это исследование позволяет подтвердить диагноз цирроза более чем в 90% случаев. При раке печени биопсия может оказаться неинформативной, так как никто не может гарантировать, что раковые клетки окажутся именно в том участке печеночной ткани, который будет исследован.
Принцип УЗИ основан на способности звуковых волн отражаться от объектов различной плотности (они легко проходят через воздух, однако преломляются и отражаются на границе воздуха и жидкости или плотной ткани органа). Отраженные волны регистрируются специальными приемниками и после компьютерной обработки представляются на мониторе в виде изображения исследуемой области.
Данное исследование абсолютно безвредно и безопасно, может выполняться множество раз в течение всего периода лечения для контроля состояния пациента и своевременного выявления возможных осложнений.
С помощью УЗИ можно выявить:
- Свободную жидкость в брюшной полости – определяется даже небольшое ее количество (несколько сотен миллилитров).
- Жидкость в плевральной полости и в полости перикарда – при системных воспалительных заболеваниях и опухолях.
- Увеличение печени – при циррозе, раке, тромбозе печеночных вен.
- Увеличение селезенки – при повышении давления в системе воротной вены (портальной гипертензии) и при гемолитических анемиях (сопровождающихся разрушением клеток крови).
- Расширение воротной вены – при портальной гипертензии.
- Расширение нижней полой вены – при сердечной недостаточности и застое крови в венах нижней части тела.
- Нарушение структуры почек – при почечной недостаточности.
- Нарушение структуры поджелудочной железы – при панкреатите.
- Аномалии развития плода.
- Опухоль и ее метастазы.
Данное исследование позволяет выявить даже небольшие количества асцитической жидкости, находящейся в труднодоступных местах брюшной полости, которые нельзя исследовать с помощью других методов. Также МРТ полезна при диагностике цирроза печени, доброкачественных и злокачественных опухолей любой локализации, при перитоните, панкреатите и других заболеваниях, которые могли бы стать причиной асцита.
Помимо УЗИ и МРТ врач может назначить целый ряд дополнительных инструментальных исследований, необходимых для установки диагноза и оценки состояния различных органов и систем.
Для выявления причины асцита врач может назначить:
- Электрокардиографию (ЭКГ). Данное исследование позволяет оценить электрическую активность сердца, выявить признаки увеличения сердечной мышцы, нарушение ритма сердечных сокращений и другие патологии.
- Эхокардиографию (ЭхоКГ). При данном исследовании оценивается характер сердечных сокращений при каждой систоле и диастоле, а также производится оценка структурных нарушений сердечной мышцы.
- Рентгенологическое исследование.Рентген грудной клетки назначается всем пациентам при подозрении на асцит. Это простое исследование позволяет исключить инфекционные заболевания легких, плеврит. Рентгенография брюшной полости позволяет выявить увеличение печени, наличие кишечной непроходимости или перфорацию (прободение) кишечника и выход части газов в брюшную полость.
- Допплерографию. Это исследование основано на принципе УЗИ с применением эффекта Доплера. Суть его заключается в том, что при ультразвуковом исследовании приближающиеся и отделяющиеся объекты (в частности кровь в кровеносных сосудах) будут отражать звуковые волны по-разному. По результатам данного исследования можно оценить характер кровотока по воротной вене и другим кровеносным сосудам, можно выявить наличие тромбов в печеночных венах и определить другие возможные нарушения.
Диагностическая пункция (то есть прокол передней брюшной стенки и откачивание небольшого количества асцитической жидкости) назначается пациентам, которым не удалось выставить диагноз на основании других методов исследования. Этот метод позволяет исследовать состав жидкости и ее свойства, что в некоторых случаях полезно для постановки диагноза.
Диагностический лапароцентез противопоказан:
- При нарушении свертывающей системы крови, так как при этом повышается риск кровотечения во время проведения исследования.
- При инфицировании кожи в области переднебоковой стенки живота, так как во время прокола возможно занесение инфекции в брюшную полость.
- При кишечной непроходимости (высок риск прободения иглой раздутых петель кишечника, что приведет к выходу каловых масс в брюшную полость и развитию калового перитонита).
- При подозрении на наличие опухоли вблизи места прокола (повреждение опухоли иглой может спровоцировать метастазирование и распространение опухолевых клеток по всему организму).
Также стоит отметить, что в третьем триместре беременности лапароцентез проводиться только по строгим показаниям и под контролем ультразвукового аппарата, помогающего контролировать глубину введения иглы и ее расположение по отношению к другим органам и к плоду.
Подготовка больного
Подготовка к процедуре заключается в опустошении мочевого пузыря (при необходимости в него может быть установлен специальный катетер), желудка (вплоть до промывания через зонд) и кишечника. Сама процедура выполняется под местным обезболиванием (то есть пациент при этом находится в сознании), поэтому особо чувствительным и эмоциональным пациентам можно назначить легкие успокоительные препараты.
Лидокаин и новокаин (местные анестетики, вводимые в мягкие ткани и угнетающие боль и другие виды чувствительности на некоторое время) довольно часто вызывают аллергические реакции (вплоть до анафилактического шока и смерти пациента). Вот почему перед началом обезболивания в обязательном порядке проводится тест на аллергию. На коже предплечья пациента стерильной иглой делается 2 царапины, на одну из которых наносится анестетик, а на другую – обычный физиологический раствор. Если через 5 – 10 минут цвет кожных покровов над ними одинаков, реакция считается отрицательной (аллергии нет). Если же над царапиной с анестетиком отмечается покраснение, отечность и припухлость кожи, это говорит о том, что у данного пациента имеется аллергия на данный анестетик, поэтому его применение категорически противопоказано.
Техника выполнения процедуры
Пациент принимает полусидячее или лежачее (на спине) положение. Непосредственно перед началом пункции его укрывают стерильными простынями таким образом, чтобы свободным осталась только область передней брюшной стенки, через которую будет осуществляться прокол. Это позволяет снизить риск развития инфекционных осложнений в послеоперационном периоде.
Прокол обычно производится по средней линии живота, между пупком и лобковой костью (в данной области находится меньше всего кровеносных сосудов, поэтому риск их травматизации минимален). Вначале врач обрабатывает место предполагаемой пункции раствором антисептика (йодным раствором, перекисью водорода), после чего обкалывает кожу, подкожную клетчатку и мышцы передней брюшной стенки раствором анестетика. После этого скальпелем выполняется небольшой разрез кожи, через который вводится троакар (специальный инструмент, представляющий собой трубку, внутри которой находится стилет). Троакар медленно, с помощью вращательных движений продвигают вглубь, пока врач не решит, что он находится в брюшной полости. После этого стилет извлекается. Вытекание асцитической жидкости через троакар говорит о правильно проведенной пункции. Производят забор необходимого количества жидкости, после чего троакар извлекают, и рану ушивают. Пробирка с полученной жидкостью отправляется в лабораторию для дальнейшего исследования.
Интерпретация результатов исследования
В зависимости от характера и состава различают два вида асцитической жидкости — транссудат и экссудат. Это крайне важно для дальнейшей диагностики, так как механизмы образования этих жидкостей различны.
Транссудат представляет собой ультрафильтрат плазмы, образующийся при пропотевании жидкости через кровеносные или лимфатические сосуды. Причиной скапливания транссудата в брюшной полости может быть сердечная недостаточность, нефротический синдром и другие патологии, сопровождающиеся повышением гидростатического и уменьшением онкотического давления крови. При лабораторном исследовании транссудат определяется как прозрачная жидкость пониженной плотности (удельный вес колеблется в пределах от 1,006 до 1,012). Концентрация белка в транссудате не превышает 25 г/л, что подтверждается специальными пробами.
Экссудат, в отличие от транссудата, представляет собой мутную, блестящую жидкость, богатую белками (более 25 г/л) и другими микромолекулярными веществами. Плотность экссудата обычно колеблется в пределах от 1,018 до 1,020, а концентрация лейкоцитов может превышать 1000 в одном микролитре исследуемой жидкости. Также в экссудате могут обнаруживаться примеси других биологических жидкостей (крови, лимфы, желчи, гноя), что будет свидетельствовать о поражении того или иного органа.
В клинической практике выделяют три стадии развития асцита, которые определяются в зависимости от количества свободной жидкости в брюшной полости.
Асцит может быть:
- Транзиторным. В данном случае в брюшной полости скапливается не более 400 мл жидкости, которая может быть выявлена только с помощью специальных исследований (УЗИ, МРТ). Транзиторный асцит не нарушает функцию органов брюшной полости или легких, поэтому все имеющиеся симптомы обусловлены основным заболеванием, адекватная терапия которого может привести к рассасыванию жидкости.
- Умеренным. При умеренном асците в брюшной полости может скапливаться до 4 литров асцитической жидкости. Живот у таких пациентов будет слегка увеличенным, в положении стоя будет отмечаться выпирание нижней части брюшной стенки, а в положении лежа может появляться одышка (чувство нехватки воздуха). Наличие асцитической жидкости может быть определено с помощью перкуссии или симптома флюктуации.
- Напряженным. В данном случае количество асцитической жидкости может превышать 10 – 15 литров. Давление в брюшной полости при этом повышается на столько, что может нарушать функции жизненно-важных органов (легких, сердца, кишечника). Состояние таких пациентов оценивается как крайне тяжелое, поэтому они должны быть немедленно госпитализированы в отделение реанимации для диагностики и лечения.
Также в клинической практике принято выделять рефрактерный (не поддающийся лечению) асцит. Данный диагноз выставляется в том случае, если на фоне проводимого лечения количество жидкости в брюшной полости продолжает увеличиваться. Прогноз в данном случае крайне неблагоприятный.
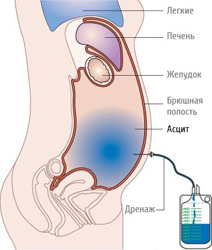
В лечении асцита применяются:
- мочегонные средства;
- диетотерапия;
- физические упражнения;
- лечебный лапароцентез;
- народные методы лечения.
Мочегонные препараты обладают способностью выводить жидкость из организма посредством различных механизмов. Уменьшение объема циркулирующей крови может способствовать переходу части жидкости из брюшной полости в кровеносное русло, что уменьшит выраженность клинических проявлений асцита.
Мочегонные средства при асците
Важно помнить, что скорость выведения асцитической жидкости не должна превышать 400 мл в сутки (именно столько может всасывать брюшина в сосудистое русло). При более интенсивном выведении жидкости (что может наблюдаться при неправильном и неконтролируемом приеме мочегонных средств) может развиться обезвоживание организма.
Помимо мочегонных препаратов может применяться целый ряд других медикаментов, влияющих на развитие асцита.
Медикаментозное лечение асцита может включать:
- Средства, укрепляющие сосудистую стенку (диосмин, витамины С, Р). Расширение сосудов и повышение проницаемости сосудистой стенки являются одними из основных элементов в развитии асцита. Применение препаратов, которые могут снизить проницаемость сосудов и повысить их устойчивость перед лицом различных патогенных факторов (повышенного внутрисосудистого давления, медиаторов воспаления и так далее) может значительно замедлить прогрессирование асцита.
- Средства, влияющие на систему крови (>полиглюкин, реополиглюкин, желатиноль). Введение данных препаратов в системный кровоток способствует удерживанию жидкости в сосудистом русле, препятствуя ее переходу в межклеточное пространство и в брюшную полость.
- Альбумин (белок).Альбумин является основным белком, обеспечивающим онкотическое давление крови (которое удерживает жидкость в сосудистом русле и не дает ей переходить в межклеточное пространство). При циррозе или раке печени, а также при нефротическом синдроме количество белка в крови может значительно снижаться, что нужно компенсировать внутривенным введением альбуминов.
- Антибиотики. Назначаются при бактериальном или туберкулезном перитоните.
Питание при асците должно быть высококалорийным, полноценным и сбалансированным, чтобы обеспечить организм всеми необходимыми питательными веществами, витаминами и микроэлементами. Также пациентам следует ограничить потребление ряда продуктов, которые могли бы усугубить течение заболевания.
Главными принципами диеты при асците являются:
- Ограничение потребления соли. Избыточное потребление соли способствует переходу жидкости из сосудистого русла в межклеточное пространство, то есть приводит к развитию отеков и асцита. Вот почему таким пациентам рекомендуется исключить из рациона соль в чистом виде, а соленую пищу принимать в ограниченном количестве.
- Ограничение потребления жидкости. Больным с умеренным или напряженным асцитом не рекомендуется принимать более 500 – 1000 мл жидкости (в чистом виде) в сутки, так как это может способствовать прогрессированию заболевания и ухудшению общего самочувствия.
- Достаточное потребление белков. Как уже говорилось, белковая недостаточность может стать причиной развития отеков. Вот почему в ежедневный рацион пациента с асцитом должны входить белки животного происхождения (содержащиеся в мясе, яйцах). Однако стоит помнить, что при циррозе печени избыточное потребление белковой пищи может стать причиной интоксикации организма (так как нарушается обезвреживающая функция печени), поэтому в данном случае лучше согласовать диету с лечащим врачом.
- Ограничение потребления жиров. Это правило особенно важно при асците, вызванном панкреатитом. Дело в том, что потребление жирной пищи стимулирует образование пищеварительных ферментов в поджелудочной железе, что может привести к обострению панкреатита.
Диета при асците
|
|
Планируя физическую активность при асците важно помнить, что данное состояние само по себе свидетельствует о выраженном нарушении функции одного или сразу нескольких внутренних органов, поэтому подбирать нагрузку рекомендуется совместно с лечащим врачом. В целом же вид и характер допустимых физических упражнений зависит от общего состояния пациента и причины асцита.
Основным «ограничителем» физической активности при асците является состояние сердечной и дыхательной систем. Так, например, при выраженной сердечной недостаточности (когда одышка возникает в покое) любая физическая активность противопоказана. В то же время, при более легком течении заболевания и транзиторном или умеренном асците пациенту рекомендуется ежедневно прогуливаться на свежем воздухе (легким, небыстрым шагом), заниматься утренней гимнастикой и другими легкими видами спорта. Особое внимание следует уделить плаванию, так как во время пребывания в воде улучшается циркуляция крови и, в то же время, снижается нагрузка на сердце, что замедляет прогрессирование асцита.
Также ограничить физическую активность пациента может напряженный асцит, при котором наблюдается сдавливание легких и органов брюшной полости. Выполнение обычных физических упражнений в данном случае невозможно, так как любая нагрузка может привести к декомпенсации состояния пациента и развитию острой дыхательной недостаточности.
Как говорилось ранее, пункция (прокол) передней брюшной стенки и удаление части асцитической жидкости из брюшной полости важно в диагностике асцита. В то же время, данная процедура может выполняться и в лечебных целях. Это показано при напряженном и/или рефрактерном асците, когда давление жидкости в брюшной полости настолько велико, что приводит к нарушению работы жизненно-важных органов (в первую очередь, сердца и легких). В данном случае единственным эффективным методом лечения является пункция брюшной полости, во время которой удаляют часть асцитической жидкости.
Техника и правила подготовки больного такие же, как при диагностическом лапароцентезе. После прокола передней брюшной стенки в брюшную полость устанавливается специальная дренажная трубка, по которой будет оттекать асцитическая жидкость. К другому концу трубки обязательно присоединяется емкость с градацией объема (чтобы контролировать количество удаленной жидкости).
Важно помнить, что в асцитической жидкости может содержаться большое количество белков (альбуминов). Одномоментное удаление большого объема жидкости (более 5 литров) может не только привести к падению артериального давления (вследствие расширения ранее сдавленных кровеносных сосудов), но и к выраженной белковой недостаточности. Вот почему количество удаляемой жидкости должно определяться в зависимости от характера асцитической жидкости (транссудат или экссудат) и общего состояния пациента.
Народные методы лечения широко применяются для лечения асцита при различных заболеваниях. Основной задачей лекарственных трав и растений является удаление асцитической жидкости из организма, поэтому все они обладают мочегонным действием.
В лечении асцита можно применять:
- Настой петрушки. 40 грамм измельченной зеленой травы и корней петрушки нужно залить 1 литром кипятка и настаивать при комнатной температуре в течение 12 часов. Принимать внутрь по 1 столовой ложке 3 – 4 раза в день (перед едой).
- Отвар из стручков фасоли. 2 столовых ложки измельченных стручков фасоли нужно залить литром воды, довести до кипения и кипятить на водяной бане в течение 20 – 30 минут. После этого охладить и принимать внутрь по 2 столовых ложки 4 – 5 раз в день перед едой.
- Отвар из листьев мать-и-мачехи. 1 столовую ложку измельченных листьев мать-и-мачехи залить 1 стаканом (200 мл) воды, довести до кипения и кипятить в течение 10 минут. Охладить, процедить и принимать внутрь по 1 столовой ложке 3 раза в сутки.
- Настойку пустырника. 1 столовую ложку измельченных листьев пустырника нужно поместить в стеклянную банку и залить 100 мл 70% спирта, после чего настаивать в темном месте при комнатной температуре в течение 3 – 5 дней. Принимать настойку следует трижды в день перед едой по 30 капель, разбавляемых в небольшом количестве кипяченой воды.
- Абрикосовый компот. Обладает не только мочегонным, но и калийсберегающим действием, что крайне важно при длительном применении мочегонных трав и препаратов. Компот лучше готовить из сушеных абрикосов, 300 – 400 грамм которых заливают 2 – 3 литрами воды и кипятят в течение 15 – 20 минут. Важно помнить, что при напряженном асците количество потребляемой жидкости должно быть ограниченным, поэтому не рекомендуется принимать более 200 – 300 мл компота в сутки.
Операция при асците показана в том случае, если причина его возникновения может быть устранена хирургически путем. В то же время, возможность хирургического лечения ограничивается количеством асцитической жидкости и общим состоянием пациента, которое может быть крайне тяжелым.
Хирургическое лечение может применяться:
- При раке печени. Удаление пораженной опухолью части печени может приостановить прогрессирование патологического процесса (при отсутствии метастазов в отдаленных органах).
- При пороках сердца. Коррекция клапанного порока сердца (замена поврежденного клапана искусственным) может привести к полному выздоровлению пациента, нормализации функции сердца и рассасыванию асцитической жидкости.
- При онкологии брюшной полости. Своевременное удаление опухоли, сдавливающей кровеносные сосуды системы воротной вены, может привести к полному излечению пациента.
- При перитоните. Бактериальный перитонит является показанием к хирургическому лечению. Брюшная полость вскрывается, очищается от гнойных масс и промывается растворами антисептиков.
- При хилезном асците. Если проникновение лимфы в брюшную полость обусловлено повреждением крупного лимфатического сосуда данной области, его ушивание во время хирургической операции может привести к полному выздоровлению пациента.
Хирургическое лечение асцита не выполняется при декомпенсированной сердечной и дыхательной недостаточности. В данном случае пациент просто не переживет наркоз и само оперативное вмешательство, поэтому перед операцией обычно назначается курс мочегонных препаратов, а при необходимости – лечебная пункция и удаление части асцитической жидкости. Также определенные трудности могут возникнуть при оперировании пациента с напряженным асцитом, так как одномоментное удаление большого объема жидкости может привести к развитию осложнений и смерти.
Сегодня широко применяется метод возвращения асцитической жидкости (точнее содержащихся в ней белков и других микроэлементов) в системный кровоток посредством внутривенных вливаний, что позволяет снизить риск смертельного исхода у таких больных.
Одним из основных этапов лечения асцита при циррозе печения является приостановление прогрессирования патологического процесса в ней и стимуляция восстановления нормальной печеночной ткани. Без соблюдения данных условий симптоматическое лечение асцита (применение мочегонных препаратов и повторные лечебные пункции) будет давать временный эффект, однако в конечном итоге все закончится смертью пациента.
Лечение цирроза печени включает:
- Гепатопротекторы (аллохол, урсодезоксихолевую кислоту) – препараты, улучшающие обмен веществ в клетках печени и защищающие их от повреждения различными токсинами.
- Эссенциальные фосфолипиды (фосфоглив, эссенциале) – восстанавливают поврежденные клетки и повышают их устойчивость при воздействии токсических факторов.
- Флавоноиды (гепабене, карсил) – нейтрализуют свободные радикалы кислорода и другие токсические вещества, образующиеся в печени при прогрессировании цирроза.
- Препараты аминокислот (гептрал, гепасол А) – покрывают потребность печени и всего организма в аминокислотах, необходимых для нормального роста и обновления всех тканей и органов.
- Противовирусные средства (пегасис, рибавирин) – назначаются при вирусном гепатите В или С.
- Витамины (А, В12, Д, К) – данные витамины образуются или депонируются (хранятся) в печени, а при развитии цирроза их концентрация в крови может значительно снижаться, что приведет к развитию ряда осложнений.
- Диетотерапию – рекомендуется исключить из рациона продукты, которые увеличивают нагрузку на печень (в частности жирную и жареную пищу, любые виды алкогольных напитков, чай, кофе).
- Пересадку печени – единственный метод, позволяющий радикально решить проблему цирроза. Однако стоит помнить, что даже после успешной пересадки следует выявить и устранить причину возникновения заболевания, так как в противном случае цирроз может поразить и новую (пересаженную) печень.
Причиной образования асцитической жидкости при опухоли может быть сдавливание кровеносных и лимфатических сосудов брюшной полости, а также поражение брюшины опухолевыми клетками. В любом случае для эффективного лечения заболевания необходимо полностью удалить злокачественное новообразование из организма.
В лечении онкологических заболеваний может применяться:
- Химиотерапия.Химиотерапия является основным методом лечения канцероматоза брюшины, при котором опухолевые клетки поражают оба листка серозной оболочки брюшной полости. Назначаются химические препараты (метотрексат, азатиоприн, цисплатин), которые нарушают процессы деления опухолевых клеток, тем самым приводя к уничтожению опухоли. Основной проблемой при этом является тот факт, что данные средства нарушают также деление нормальных клеток во всем организме. В результате этого в период лечения у пациента могут выпадать волосы, могут появляться язвы желудка и кишечника, может развиться апластическая анемия (недостаток красных клеток крови вследствие нарушения процесса их образования в красном костном мозге).
- Лучевая терапия. Суть данного метода заключается в высокоточном воздействии радиацией на опухолевую ткань, что приводит к гибели опухолевых клеток и уменьшению размеров новообразования.
- Хирургическое лечение. Заключается в удалении опухоли посредством хирургической операции. Данный метод особенно эффективен при доброкачественных опухолях либо в том случае, когда причиной асцита является сдавливание кровеносных или лимфатических сосудов растущей опухолью (ее удаление может привести к полному выздоровлению пациента).
Сердечная недостаточность характеризуется неспособностью сердечной мышцы перекачивать кровь в организме. Лечение данного заболевания заключается в уменьшении давления в кровеносной системе, устранении застоя крови в венах и улучшении работы сердечной мышцы.
Лечение сердечной недостаточности включает:
- Мочегонные препараты. Уменьшают объем циркулирующей крови, снижая нагрузку на сердце и давление в венах нижней части тела, тем самым предотвращая дальнейшее развитие асцита. Назначать их следует осторожно, под контролем артериального давления, чтобы не спровоцировать обезвоживание организма.
- Препараты, понижающие артериальное давление (рамиприл, лозартан). При повышенном артериальном давлении (АД) сердечной мышце нужно выполнять большую работу, выбрасывая кровь в аорту во время сокращения. Нормализация давления уменьшает нагрузку на сердце, тем самым способствуя устранению венозного застоя и отеков.
- Сердечные гликозиды (дигоксин, дигитоксин). Данные препараты увеличивают силу сердечных сокращений, что способствует устранению застоя в венах нижней части туловища. Принимать их следует осторожно, так как в случае передозировки может наступить смерть.
- Бессолевую диету. Потребление большого количества соли приводит к задержке жидкости в организме, что еще больше увеличивает нагрузку на сердце. Вот почему пациентам с сердечной недостаточностью не рекомендуется принимать более 3 – 5 грамм соли в сутки (включая соль, используемую при приготовлении различных блюд).
- Ограничение приема жидкости (не более 1 – 1,5 литров в сутки).
- Соблюдение режима дня. Если позволяет состояние сердечно-сосудистой системы, пациентам рекомендуется умеренная физическая активность (ходьба, утренняя гимнастика, плавание, занятия йогой).
При почечной недостаточности нарушается выделительная функция почек, в результате чего жидкость и побочные продукты обмена веществ (мочевина, мочевая кислота) задерживаются в организме в больших количествах. Лечение почечной недостаточности заключается в нормализации функций почек и удалении токсических веществ из организма.
Лечение почечной недостаточности включает:
- Мочегонные препараты. На начальных стадиях заболевания могут оказывать положительное действие, однако при терминальной стадии почечной недостаточности малоэффективны. Объясняется это тем, что механизм действия мочегонных препаратов заключается в регуляции (то есть в усилении) выделительной функции почечной ткани. При последней стадии заболевания количество функциональной почечной ткани крайне мало, что и обуславливает отсутствие эффекта при назначении мочегонных средств.
- Препараты, снижающие артериальное давление. При почечной недостаточности происходит нарушение кровоснабжения оставшейся функциональной почечной ткани, вследствие чего активируется ряд компенсаторных механизмов, направленных на поддержание почечного кровотока на адекватном уровне. Одним из таких механизмов является увеличение артериального давления. Однако повышение АД не улучшает состояния почек, а наоборот, способствует прогрессированию патологического процесса, развитию отеков и асцита. Вот почему нормализация показателей АД является важным этапом лечения, позволяющим замедлить скорость образования асцитической жидкости.
- Гемодиализ. Во время данной процедуры кровь пациента пропускается через специальный аппарат, в котором происходит ее очищение от побочных продуктов обмена веществ и других токсинов, после чего она возвращается обратно в кровеносное русло. Гемодиализ и другие методы очищения крови (плазмаферез, перитонеальный диализ, гемосорбция) являются последним эффективным способом продления жизни пациентов с хронической почечной недостаточностью.
- Пересадку почки. Радикальный метод лечения, при котором пациенту пересаживают донорскую почку. Если операция пройдет успешно и трансплантат приживется в организме хозяина, новая почка может в полном объеме выполнять выделительную функцию, обеспечивая нормальное качество и продолжительность жизни пациента.
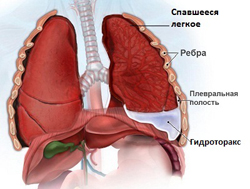
Асцит может осложниться:
- воспалением брюшины (асцитом-перитонитом);
- сердечной недостаточностью;
- гидротораксом;
- дыхательной недостаточностью;
- диафрагмальной грыжей;
- пупочной грыжей;
- кишечной непроходимостью.
Асцит-перитонит
Данное состояние возникает в результате проникновения чужеродных бактерий в брюшную полость, что приводит к воспалению брюшины. Развитию данного осложнения способствует застой асцитической жидкости, нарушение моторики сдавленных кишечных петель, а также расширение и повышение проницаемости сосудов в системе воротной вены. Также важную роль в развитии инфекционных осложнений играет снижение общих защитных сил организма в результате прогрессирования основной патологии, ставшей причиной асцита (почечной, сердечной или печеночной недостаточности, опухоли и так далее).
Важным является тот факт, что какого-либо видимого дефекта брюшины или внутренних органов, который мог бы стать источником инфекции при этом не наблюдается. Предполагают, что бактерии просачиваются в брюшную полость через расширенные и перерастянутые стенки кишечных петель.
Независимо от механизма развития наличие перитонита требует госпитализации пациента и срочного хирургического лечения.
Сердечная недостаточность
Скапливание большого количества жидкости в брюшной полости приводит к сдавливанию расположенных там органов и кровеносных сосудов (артерий и вен), нарушая ток крови по ним. В результате этого сердцу требуется выполнять большую работу, чтобы перекачивать кровь по сосудам.
Если асцит развивается медленно, в сердце активируются компенсаторные механизмы, заключающиеся в разрастании мышечных волокон и увеличении размеров сердечной мышцы. Это позволяет до определенного момента компенсировать увеличение нагрузки. При дальнейшем прогрессировании асцита резервы сердечной мышцы могут истощаться, что и станет причиной развития сердечной недостаточности.
Если же асцит развивается быстро (в течение нескольких дней), сердце не успевает приспособиться к возрастающей нагрузке, вследствие чего может развиться острая сердечная недостаточность, требующая экстренной медицинской помощи.
Гидроторакс
Данным термином обозначается скапливание жидкости в грудной клетке. Развитию гидроторакса при асците способствует повышение давления асцитической жидкости, в результате чего жидкость из кровеносных и лимфатических сосудов брюшной полости может переходить в сосуды диафрагмы и грудной клетки. При прогрессировании заболевания количество свободной жидкости в грудной клетке будет увеличиваться, что приведет к сдавливанию легкого на стороне поражения (или обоих легких при двустороннем гидротораксе) и нарушению дыхания.
Дыхательная недостаточность
Развитию данного состояния может способствовать подъем и ограничение экскурсии диафрагмы в результате повышения давления в брюшной полости, а также прогрессирование гидроторакса. В отсутствии своевременного лечения дыхательная недостаточность приведет к выраженному снижению концентрации кислорода в крови, что может проявляться одышкой, синюшностью кожных покровов и нарушением сознания, вплоть до его утраты.
Диафрагмальная грыжа
Диафрагмальной грыжей называется выпячивание органа или ткани через дефект в диафрагме либо через ее пищеводное отверстие. Причиной этого является выраженное повышение внутрибрюшного давления.
Через грыжевое отверстие могут выпячиваться желудок, петли кишечника или серозная оболочка, наполненная асцитической жидкостью. Проявляется данное состояние болями в грудной клетке и в области сердца, в верхних отделах живота. Если в грыжевое отверстие выходит достаточно большой по объему участок органа, он может сдавливать легкие и сердце, приводя к нарушению дыхания и сердцебиения.
Лечение заболевания в основном хирургическое, заключающееся во вправлении грыжевого мешка и ушивание дефекта в диафрагме.
Пупочная грыжа
Причиной образования пупочной грыжи также является повышенное давление в брюшной полости. Передняя брюшная стенка почти на всем своем протяжении покрыта мышцами. Исключение составляет пупочная область и срединная линия живота, где данные мышцы сходятся вместе и формируют так называемый апоневроз передней брюшной стенки. Состоит данный апоневроз из сухожильной ткани, которая является «слабым местом» брюшной стенки (именно здесь чаще всего отмечается выпячивание грыжевого мешка). Лечения заболевания также хирургическое (производится вправление грыжи и ушивание грыжевых ворот).
Кишечная непроходимость
Развивается в результате сдавливания петель кишечника асцитической жидкостью, что обычно встречается при напряженном, рефрактерном асците. Нарушение проходимости кишечника приводит к скапливанию каловых масс выше места сдавливания и усиленной перистальтике (моторной активности) кишечника в данной области, что сопровождается выраженными приступообразными болями в животе. Если в течение нескольких часов кишечная непроходимость не разрешается, наступает паралич кишечника, расширение и повышение проницаемости кишечной стенки. В результате этого многочисленные бактерии (являющиеся постоянными обитателями толстого кишечника) проникают в кровь, вызывая развитие грозных, опасных для жизни пациента осложнений.
Лечение заключается во вскрытии брюшной полости и устранении кишечной непроходимости. Если поврежденные петли кишечника оказываются нежизнеспособны, их удаляют, а образовавшиеся концы пищеварительного канала соединяют между собой.

Исходя из вышесказанного следует, что прогноз при асците определяется не только количеством жидкости в брюшной полости и качеством проводимого лечения, но также и основным заболеванием, ставшим причиной скапливания жидкости в брюшной полости.
Срок жизни людей с диагностированным асцитом варьирует в широких пределах, что зависит от целого ряда факторов.
Продолжительность жизни пациента с асцитом обусловлена:
- Выраженностью асцита. Транзиторный (слабовыраженный) асцит не представляет непосредственной угрозы для жизни пациента, в то время как напряженный асцит, сопровождающийся скапливанием в брюшной полости десятков литров жидкости, может привести к развитию острой сердечной или дыхательной недостаточности и смерти пациента в течение часов или дней.
- Временем начала лечения. Если асцит выявлен на ранних стадиях развития, когда функции жизненно-важных органов не нарушены (или нарушены незначительно), устранение основного заболевания может привести к полному излечению пациента. В то же время, при длительно прогрессирующем асците может произойти поражение многих органов и систем (дыхательной, сердечно-сосудистой, выделительной), что приведет к смерти пациента.
- Основным заболеванием. Это, пожалуй, основной фактор, определяющий выживаемость пациентов с асцитом. Дело в том, что даже при проведении самого современного лечения благоприятный исход маловероятен, если у пациента имеется недостаточность сразу нескольких органов. Так, например, при декомпенсированном циррозе печени (когда функция органа практически полностью нарушена) шансы пациента на выживание в течение 5 лет после установки диагноза составляют менее 20%, а при декомпенсированной сердечной недостаточности – менее 10%. Более благоприятен прогноз при хронической почечной недостаточности, так как пациенты, находящиеся на гемодиализе и соблюдающие все предписания врача, могут прожить десятки лет и более.

Профилактика асцита включает:
- Своевременное лечение заболеваний печени. Развитию цирроза печени всегда предшествует длительное воспаление печеночной ткани (гепатит). Крайне важно вовремя установить причину данного заболевания и устранить ее (провести противовирусное лечение, отказаться от употребления алкоголя, начать принимать здоровую пищу и так далее). Это позволит приостановить прогрессирование патологического процесса и сохранить жизнеспособной большую часть печеночной ткани, что обеспечит пациенту полноценную жизнь в течение долгих лет.
- Своевременное лечение врожденных пороков сердца. На современном этапе развития операцию по замене поврежденного сердечного клапана или закрытию дефекта в стенках сердечной мышцы можно провести в раннем детском возрасте, что позволит ребенку нормально расти и развиваться и избавит его от сердечной недостаточности в будущем.
- Своевременное лечение заболеваний почек. Хотя гемодиализ может компенсировать выделительную функцию почки, он не в состоянии обеспечить целый ряд других функций данного органа. Вот почему гораздо легче вовремя и полноценно лечить различные инфекционные заболевания мочевыделительной системы, такие как цистит (воспаление мочевого пузыря), гломерулонефрит (воспаление почечной ткани), пиелонефрит (воспаление почечных лоханок), чем потом проводить на гемодиализе по 2 – 3 часа дважды в неделю на протяжении всей оставшейся жизни.
- Соблюдение диеты при панкреатите. При хроническом панкреатите спровоцировать обострение заболевания и разрушение ткани поджелудочной железы может прием большого количества алкоголя, сладостей, острой, копченой или жареной пищи. Однако следует понять, что такие пациенты не должны полностью исключать из рациона вышеперечисленные продукты. 1 конфета или 1 съеденный кусочек копченой колбасы в день не спровоцирует обострение панкреатита, поэтому больным крайне важно умеренно питаться и не переедать (особенно перед сном).
- Выполнение плановых УЗИ во время беременности. Беременным женщинам рекомендуется выполнять минимум три УЗИ в период вынашивания плода. Первое из них проводится в период от 10 до 14 недели беременности. К этому времени происходит закладка всех органов и тканей плода, что позволяет выявить грубые аномалии развития. Второе УЗИ выполняется на 18 – 22 неделе беременности. Оно также позволяет выявить различные аномалии развития и при необходимости поднять вопрос о прерывании беременности. Третье исследование выполняется на 30 – 34 неделе с целью выявления аномалий развития или положения плода. Прерывание беременности на таком сроке невозможно, однако врачи могут выявить ту или иную патологию и начать ее лечение сразу после рождения ребенка, что значительно повысит его шансы на выживание.
источник