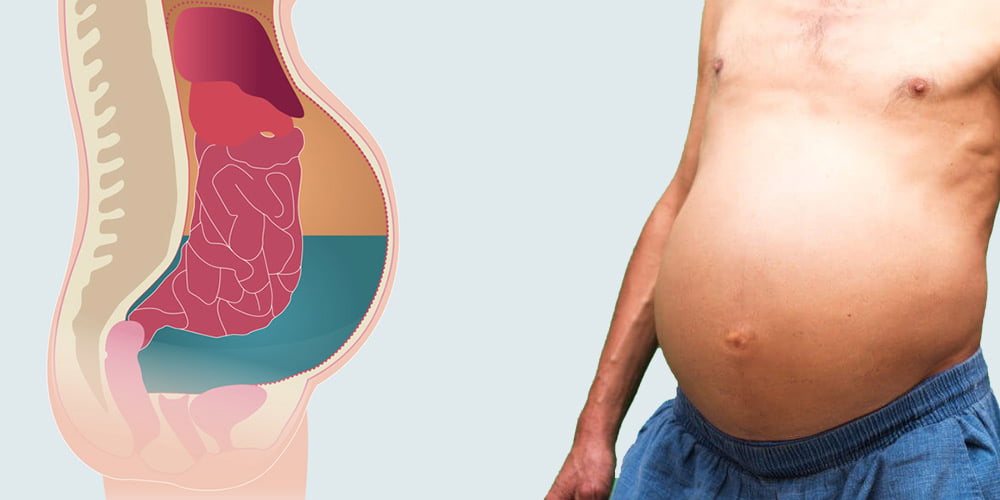
Асцит, или брюшная водянка, нередко является следствием другого, более опасного и сложного в лечении заболевания. Тем не менее и сам по себе асцит способен осложнить жизнь больному и привести к печальным последствиям. Современной медициной разработаны достаточно эффективные методы лечения асцита на разных его стадиях. Что нужно знать о первых признаках асцита, ходе его развития и к какому врачу обратиться за помощью?
Под асцитом в медицине понимают вторичное патологическое состояние, для которого характерно скопление жидкости в брюшной полости. Чаще всего асцит вызывается нарушением регуляции обмена жидкости в организме в результате серьезных патологических состояний.
В здоровом организме в брюшной полости всегда находится немного жидкости, при этом она не скапливается, а всасывается лимфатическими капиллярами. При различных заболеваниях внутренних органов и систем увеличивается скорость образования жидкости и снижается скорость ее всасывания. При развитии асцита жидкости становится все больше, она начинает сдавливать жизненно важные органы. Это способствует усугублению развития основного заболевания и прогрессированию асцита. Кроме этого, поскольку основная часть жидкости скапливается в брюшной полости, происходит значительное уменьшение объема циркулирующей крови. Это приводит к запуску компенсаторных механизмов, задерживающих в организме воду. У больного существенно замедляется скорость образования мочи и ее выделения, при этом количество асцитической жидкости увеличивается.
Накопление жидкости в полости живота обычно сопровождается повышением внутрибрюшного давления, нарушением кровообращения и сердечной деятельности. В некоторых случаях возникают потеря белка и электролитные нарушения, вызывающие сердечную и дыхательную недостаточность, что значительно ухудшает прогноз основного заболевания.
В медицине выделяют три основных стадии развития асцита.
- Транзиторный асцит. На этой стадии в брюшной полости скапливается не более 400 мл жидкости. Выявить заболевание можно только при помощи специальных исследований. Функции органов не нарушены. Снятие симптомов асцита возможно с помощью терапии основного заболевания.
- Умеренный асцит. В брюшной полости на этой стадии скапливается до 4 л жидкости. Наблюдается увеличение живота у пациента. В положении стоя можно заметить выпирание нижней части брюшной стенки. В положении лежа больной нередко жалуется на одышку. Наличие жидкости определяется с помощью перкуссии (простукивания) или симптома флюктуации (колебания противоположной стенки живота при простукивании).
- Напряженный асцит. Количество жидкости на этой стадии может достигать, а в некоторых случаях даже превышать, 10–15 л. Давление в брюшной полости повышается и нарушает нормальную работу жизненно важных органов. Состояние пациента при этом тяжелое, его необходимо срочно госпитализировать.
Отдельно рассматривают рефрактерный асцит, практически не поддающийся лечению. Его диагностируют в том случае, если все виды проводимой терапии не дают результата и количество жидкости не только не уменьшается, но и постоянно увеличивается. Прогноз при таком виде асцита неблагоприятный.
По статистике основными причинами возникновения асцита брюшной полости являются:
- болезни печени (70%);
- онкологические заболевания (10%);
- сердечная недостаточность (5%).
Кроме того, асцитом могут сопровождаться следующие заболевания:
- болезни почек;
- туберкулезное поражение брюшины;
- гинекологические заболевания;
- эндокринные нарушения;
- ревматизм, ревматоидный артрит;
- красная волчанка;
- сахарный диабет второго типа;
- уремия;
- болезни пищеварительной системы;
- перитониты неинфекционной этиологии;
- нарушение оттока лимфы из брюшной полости.
Возникновению асцита, кроме указанных заболеваний, могут способствовать следующие факторы:
- злоупотребление спиртным, ведущее к циррозу печени;
- инъекции наркотических препаратов;
- переливание крови;
- ожирение;
- высокий уровень холестерина;
- татуаж;
- проживание в регионе, для которого характерны случаи возникновения вирусных гепатитов.
Во всех случаях в основе возникновения асцита лежит сложное сочетание нарушений жизненно важных функций организма, ведущее к скоплению жидкости в брюшной полости.
Одним из главных внешних признаков асцита брюшной полости является увеличение размера живота. В положении стоя у пациента он может свисать в форме фартука, а в положении лежа образовывать так называемый лягушачий живот. Возможно выпячивание пупка и появление растяжек на коже. При портальной гипертензии, вызванной повышением давления в воротной вене печени, на передней брюшной стенке появляется венозный рисунок. Этот рисунок принято называть «головой Медузы» из-за отдаленного сходства с мифологической Медузой Горгоной, на голове которой вместо волос находились извивающиеся змеи.
В животе появляются боли и чувство распирания изнутри. Человек испытывает трудности при наклонах туловища. К внешним проявлениям также относятся отеки ног, рук, лица, цианоз кожных покровов. У больного развивается дыхательная недостаточность, тахикардия. Возможно появление запоров, тошнота, отрыжка и потеря аппетита.
При лабораторных и инструментальных исследованиях врач подтверждает диагноз и устанавливает причину, вызвавшую асцит. Для этого проводятся УЗИ, МРТ, диагностический лапароцентез и лабораторные исследования. С помощью УЗИ выявляют наличие свободной жидкости в брюшной полости и ее объем, увеличение печени и селезенки, расширение полой и воротной вены, нарушение структуры почек, наличие опухолей и метастазов.
МРТ позволяет послойно изучить ту или иную ткань, выявить даже незначительное количество асцитической жидкости и диагностировать основное заболевание, вызвавшее асцит.
Кроме этого, врач проводит исследование при помощи пальпации и перкуссии. Пальпация помогает выявить признаки, указывающие на поражение определенного органа (печени или селезенки). Перкуссия используется непосредственно для выявления асцита. Суть ее заключается в простукивании брюшной полости пациента и анализе перкуторных звуков. При выраженном асците, например, тупой перкуторный звук определяется над всей поверхностью живота.
Лабораторные исследования крови показывают снижение концентрации эритроцитов, увеличение количества лейкоцитов и СОЭ, возможно повышение концентрации билирубина (при циррозе печени), белков острой фазы воспаления. Анализ мочи при асците на начальной стадии может показывать большее количество мочи меньшей плотности, поскольку асцит вызывает отклонения в работе мочевыделительной системы. При терминальной стадии плотность мочи может быть нормальной, но ее общее количество значительно снижается.
Общие принципы лечения асцита предполагают прежде всего терапию основного заболевания. Лечение самого асцита направлено на выведение жидкости из брюшной полости и предотвращение рецидивов.
Пациенты с первой степенью асцита не нуждаются в медикаментозном лечении и соблюдении бессолевой диеты.
Пациентам со второй степенью асцита назначается диета с пониженным содержанием натрия и диуретическая терапия. Она должна проводиться при постоянном мониторинге состояния больного, включая содержания электролитов в сыворотке крови.
Пациенты с третьей степенью заболевания проводят удаление жидкости из брюшной полости, а в дальнейшем диуретическую терапию в сочетании с бессолевой диетой.
Асцит обычно указывает на серьезные нарушения в работе пораженных органов, но тем не менее смертельным осложнением сам он не является. При своевременной диагностике и правильном лечении возможна полная ликвидация асцитической жидкости из брюшной полости и восстановление функций пораженного органа. В ряде случаев, например при раке, асцит способен быстро прогрессировать, вызывая осложнения и даже гибель пациента. Это объясняется тем, что на течение асцита большое влияние оказывает основное заболевание, способное вызывать серьезные поражения печени, почек, сердца и других органов.
На прогноз влияют и другие факторы:
- Степень асцита. Транзиторный асцит (первой степени) не является непосредственной угрозой жизни пациента. В этом случае все внимание следует уделить терапии основной болезни.
- Время начала лечения. При выявлении асцита на той стадии, когда жизненно важные органы еще на разрушены или их функции поражены незначительно, устранение основного заболевания также может привести к полному выздоровлению пациента.
На статистику выживаемости при асците также влияет вид и тяжесть основного заболевания. При компенсированном циррозе печени 50% больных способны прожить от 7 до 10 лет, а при декомпенсированном — пятилетняя выживаемость не превышает 20%.
При онкологических заболеваниях асцит, как правило, появляется на поздних стадиях, и пятилетняя выживаемость составляет не более 50% при своевременном лечении. Средний показатель жизни у таких больных составляет 1–2 года.
При неправильном лечении асцит может вызвать серьезные осложнения, ухудшающие прогноз:
- кровотечение;
- перитонит;
- отек мозга;
- дисфункцию сердечной деятельности;
- тяжелую дыхательную недостаточность.
Рецидивы асцита также могут возникать как побочные эффекты при неправильном лечении. Рецидивирование очень опасно, поскольку в большинстве случаев не поддающиеся излечению асциты приводят к летальному исходу.
Консервативное или симптоматическое лечение асцита применятся в тех случаях, когда асцит брюшной полости находится на ранней стадии развития или в качестве паллиативной терапии при онкологии и нецелесообразности применения других методов.
Во всех случаях основной задачей лечения является выведение асцитической жидкости и поддержание состояние пациента на определенном уровне. Для этого необходимо уменьшить количество поступающего в организм натрия и усилить его выведение с мочой.
Достичь положительных результатов можно только при комплексном подходе, соблюдая диету, контролируя изменения веса и принимая диуретические препараты.
Главные принципы диеты при асците следующие:
- Минимум соли. Ее избыточное потребление приводит к развитию отеков, а следовательно, асцита. Пациентам рекомендуется максимально ограничить прием соленой пищи.
- Минимум жидкости. При умеренном или напряженном асците нормой должно быть не более 500–1000 мл жидкости в чистом виде в сутки.
- Минимум жиров. Потребление пищи с большим количеством жиров приводит к развитию панкреатита.
- Достаточное количество белков в рационе. Именно белковая недостаточность может привести к возникновению отеков.
Рекомендуется употреблять в пищу нежирные сорта мяса и рыбы, обезжиренный творог и кефир, фрукты, овощи, зелень, пшеничную крупу, компоты, кисели. Готовить лучше на пару или запекая в духовке.
Запрещены жирное мясо и рыба, жареные блюда, копчености, соль, алкоголь, чай, кофе, специи.
При лечении асцита необходимо контролировать динамику веса. При начале бессолевой диеты в течение недели производится ежедневное взвешивание. Если пациент потерял более 2 кг, то диуретические препараты ему не назначаются. При потере веса менее 2 кг в течение следующей недели начинают медикаментозную терапию.
Мочегонные препараты помогают вывести лишнюю жидкость из организма и способствуют переходу части жидкости из брюшной полости в кровеносное русло. Клинические проявления асцита при этом существенно снижаются. Основными препаратами, используемыми в терапии, являются фуросемид, маннитол и спиронолактон. В амбулаторных условиях фуросемид назначается внутривенно не более 20 мг 1 раз в два дня. Он выводит жидкость из сосудистого русла через почки. Основной недостаток фуросемида — чрезмерное выведение калия из организма.
Маннитол применяется совместно с фуросемидом, поскольку их действие комбинируется. Маннитол выводит жидкость из межклеточного пространства в сосудистое русло. Назначается по 200 мг внутривенно. Однако в амбулаторных условиях его применять не рекомендуется.
Спиронолактон также является мочегонным средством, однако он способен предотвращать чрезмерное выведение калия.
Дополнительно назначаются препараты, укрепляющие сосудистые стенки (витамины, диосмин), средства, влияющие на систему крови («Желатиноль», «Реополиглюкин»), альбумин, антибиотики.
Оперативное вмешательство при асците показано в тех случаях, когда скопление жидкости не может быть устранено при помощи консервативного лечения.
Лечебный лапароцентез при асците (прокол передней брюшной стенки) способен вывести большие объемы жидкости — от 6 до 10 литров за один раз. Проводят процедуру под местным обезболиванием с предварительным опустошением мочевого пузыря. Пациент принимает полусидячее или лежачее положение. Прокол производится по средней линии живота между пупком и лобковой костью. Скальпелем выполняется разрез кожи, через который в брюшную полость вводится специальный инструмент — троакар. Через него выводится жидкость в нужном объеме. После процедуры рану ушивают. Лапароцентез при асците можно выполнять только в условиях стационара, поскольку необходимо соблюдение норм антисептики и владение методикой проведения операции. Чтобы упростить процедуру для тех больных, которым лапароцентез требуется периодически, его проводят через постоянный перитонеальный порт.
Еще одной эффективной хирургической манипуляцией является оментогепатофренопексия. Она заключается в подшивании сальника к предварительно обработанным участкам поверхности диафрагмы и печени. Благодаря возникновению контакта между печенью и сальником появляется возможность всасывания асцитической жидкости соседними тканями. Дополнительно снижается давление в венозной системе и выход жидкости в брюшную полость через стенки сосудов.
ТИПС — трансъюгулярное интрапеченочное портосистемное шунтирование — позволяет провести декомпрессию портальной системы и устранить асцитический синдром. В основном ТИПС проводится при рефрактерном асците, не поддающемся медикаментозной терапии. При процедуре ТИПС в яремную вену вводится проводник до попадания в печеночную вену. Затем по проводнику специальный катетер проводится в саму печень. При помощи длинной изогнутой иглы в воротной вене устанавливается стент, создающий канал между воротной и печеночной венами. Кровь направляется в печеночную вену со сниженным давлением, что приводит к устранению портальной гипертензии. После выполнения ТИПС у пациентов с рефрактерным асцитом наблюдается уменьшение объема жидкости в 58% случаев.
Несмотря на то, что асцит и вызывающие его болезни являются достаточно серьезными и сложно поддающимися лечению, своевременная комплексная терапия может значительно повысить шансы на выздоровление или улучшить качество жизни неизлечимых больных. Лечить асцит нужно только под наблюдением врача, поскольку сложность основного заболевания редко позволяет обойтись домашними или народными методами. Особенно это касается асцитов, вызванных онкологией.
источник
Характерными симптомами болезни являются увеличенный живот, проблемы с дыханием, боли в брюшной полости, ощущение распирания либо тяжести. В более чем 80 процентов случаев асцит провоцируется циррозом печени последней стадии.
Это связано с дегенерацией органа и неправильным кровообращением, способствующим скоплению воды. Жидкость при асците бывает двух типов: экссудат (воспалительного характера) и транссудат (не воспалительного характера).
Асцит – это накопление воды или жидкости в брюшной полости, которое приводит к визуальному увеличению объема живота и повышению массы тела пациента. В большинстве случаев жидкость (от 100 мг до 20 л) является транссудатом, то есть носит не воспалительный характер.
Асцит брюшной полости в начале себя никак не проявляет, для него характерно постепенное прогрессирование. Как правило, асцит является следствием другого, уже имеющегося заболевания, поэтому его лечение достаточно затруднено.
К болезням, провоцирующим асцит, относят:
- цирроз печени, повышение давления в портальной системе;
- тромбоз в нижней полой и воротной венах печени;
- почечную недостаточность;
- иные острые либо хронические болезни почек;
- нефроз;
- инфекционные и воспалительные заболевания кишечника;
- заболевания поджелудочной железы;
- сердечную недостаточность;
- воспаление серозной оболочки сердца;
- онкологию;
- туберкулез;
- водянку клетчатой ткани (анасарка);
- скопление слизи в полостях (псевдомиксома).
Проявление клинического асцита возможно только тогда, когда в брюшине скопилось большое количество воды.
Характерными симптомами асцита брюшной полости являются:
- ощущение распирания в брюшине;
- длительные боли в области живота;
- изжога;
- отрыжка;
- тошнота;
- увеличенный живот (свисает в положении стоя, сидя – расплывается в стороны);
- видимая сетка кровеносных сосудов в месте растяжения;
- выпуклый пупок;
- одышка;
- нарушение работы сердечной мышцы.
При наличии онкологических заболеваний асцит развивается медленно (от нескольких недель до нескольких месяцев). В связи с этим его обнаружение крайне затруднено.
Развитие водянки живота проходит 3 стадии:
- транзиторную (около 400 мл жидкости в брюшине; небольшое вздутие живота);
- умеренную (около 5 л жидкости в брюшной полости; сбои в работе органов пищеварения, наличие одышки; перитонит, а также сердечная и дыхательная недостаточность при отсутствии лечения асцита);
- напряженную (до 20 л воды в брюшной полости; тяжелое состояние больного, характеризующееся нестабильной работой жизненно важных органов).
Диагноз «асцит брюшной полости» устанавливается путем проведения обычной пальпации, если в процессе врач ощущает тугость в животе либо если при легком ударении раздается тимпанический перкуторный звук.
Для дальнейшей диагностики пациенту понадобится сдать анализы крови и мочи, а также пройти ряд обследований. Обычно назначают ультразвуковое исследование органов брюшной полости и парацентез (забор жидкости из живота). Иногда может быть показано проведение иммунологических исследований.
Данные методы позволяют выявить стадию заболевания, а также помогают определиться с общим курсом лечения.
Лечение асцита брюшной полости при наличии онкологии следует проводить комплексно. Первостепенным является удаление лишней воды, так как затягивание с данной процедурой лишь приведет к развитию различных осложнений.
Излишек жидкости выводится через прокол и ее последующее откачивание (лапароцентез). Данную процедуру лучше проводить через 14 дней после начала течения асцита. Процессу выведения также способствует прием мочегонных препаратов, а соблюдение диеты понизит внутрибрюшное давление.
Выкачку избытка воды из организма проводят посредством приема диуретиков. Препараты данной группы способствуют переходу жидкости в кровоток, что автоматически снижает ее уровень в брюшине.
В начале больному прописывают небольшую дозу в целях снижения вероятности возникновения осложнений. Обычно назначают Амилорид, Альдактон, Верошпирон или Триамтерен.
Основным принципом применения мочегонных средств является постепенное повышение дозировки. Это позволяет избежать вымывания значительного количества калия из организма. Параллельно в курс лечения входит его прием через витамины. Также показано применение гепатопротекторов для защиты печени.
Прием мочегонных препаратов постоянно контролируется врачом. При необходимости корректируется дозировка, а неэффективные диуретики заменяются на более сильные (Дихлотиазид, Триампур).
Одновременно с мочегонными средствами используются препараты, укрепляющие сосуды (Диосмин, витамины С и Р), и препараты, препятствующие потере жидкости сосудов (Реополиглюкин). Для улучшения метаболизма в печени прописывают белковые средства (концентрат плазмы, Альбумин). Бактериальный асцит требует назначения иных препаратов (таких, которые борются с советующим типом микроорганизмов).
Пациент с асцитом брюшной полости должен выработать в себе ряд пищевых привычек:
- снизить потребление жидкости;
- отказаться от соли (она способствует задержке воды в организме человека);
- исключить жирную еду;
- снизить количество орехов в рационе;
- заменить свежие фрукты на сухие;
- вместо супов и борщей пить бульон с травами (петрушка, укроп, фенхель, сельдерей способствуют удалению излишка жидкости из организма);
- разрешено употреблять мясо кролика, курицы, индейки.
Лапароцентез представляет собой пункционный метод удаления жидкости от брюшины. За один сеанс выводят около 4 л, так как избавление от большего количества экссудата способно привести к коллапсу. Среди последствий прокола брюшной полости отмечают различные воспаления, образование спаек и другие осложнения.
Поэтому лапароцентез показан пациентам с напряженным или рефрактерным асцитом. При этом, если жидкость скопилась в большом количестве, устанавливают катетер либо троакар. Во втором случае экссудат свободно вытекает в подставленную емкость.
Шунт Левина представляет собой трубку из пластика, которая вставляется в живот и доходит до дна таза. Шунт скреплен клапаном с трубкой из силикона, которая ведет к яремной и верхней полой венам шеи.
Посредством регулировки клапана абдоминальная жидкость поступает прямиком в шейные вены. Это позволяет увеличить объем крови непосредственно в системе кровотока за счет излишка воды в брюшине. Шунт Левина используется для лечения рефрактерного асцита, который отличает стойкость к медикаментам и быстрый рецидив после операции.
Следует помнить, что народные средства способствуют не исцелению от асцита, а лишь облегчению симптомов и более быстрому выводу ненужной жидкости из организма.
Методы народной медицины однозначно эффективны, однако перед их применением необходимо посоветоваться со своим лечащим врачом. Общее количество потребляемой жидкости в сутки при асците брюшной полости не должно превышать один литр.
12 засушенных стручков фасоли залить 1 л воды. Кипятить на небольшом огне около 10 минут. Снять с плиты, дать настояться в течение 20 минут. Процедить. Пить по 200 мл до приема пищи.
Залить хвощ и листья березы 1 стаканом воды. Кипятить в течение 15 минут, далее дать остыть. Пить по ½ стакана на голодный желудок.
300 г свежей петрушки залить 1 л крутого кипятка. Варить 30 минут. Остудить. Принимать по ½ стакана ежечасно утром и в обеденное время.
1 стакан свежих или засушенных абрикосов залить 1 л воды. Варить около 40 минут. Остудить. Пить по 400 мл в сутки.
Грыжник и толокнянку в виде листьев (в одинаковом соотношении) залить 1 стаканом воды. Кипятить четверть часа. Полученный чай пить натощак каждый день с утра.
Листву малины, брусники и смородины, плоды шиповника (в равных долях) залить 1 стаканом крутого кипятка. Далее варить на небольшом огне около 10 минут. После снять с плиты и дать постоять четверть часа. Процедить. Пить дважды в сутки вместо обычного чая.
Продолжительность жизни при асците брюшной полости зависит от ряда факторов:
- Начало терапии. Диагностирование асцита на начальной стадии с последующей откачкой экссудата означает благоприятный прогноз. Это связано с тем, что функционал внутренних органов еще не нарушен или нарушен незначительно. Лечение же основной болезни, спровоцировавшей асцит, гарантирует полное исцеление. Длящийся асцит или асцит с прогрессивным течением вызывает нарушение нормального функционирования целых систем внутренних органов, что приводит к летальному исходу.
- Степень выраженности заболевания. Слабовыраженный асцит не способен вызвать смерть пациента. В отличие от него, напряженный асцит, сопряженный со скапливанием 10-20 л жидкости в брюшине, несет серьезную угрозу жизни и здоровью больного (смерть может наступить в интервале от нескольких часов до нескольких дней).
- Заболевание, спровоцировавшее асцит брюшной полости. Прогноз не может быть положительным, если пациент страдает от полинедостаточности внутренних органов или если у него наблюдается полная дегенерация хотя бы одного органа. Например, при декомпенсированном циррозе печени шанс на жизнь составляет лишь 1/5. Исход более благоприятен, если болезнь имеет хроническое течение, а пациент подвергается регулярному гемодиализу. В таком случае человек может прожить несколько десятилетий.
- Осложнения при асците. Асцит брюшной полости может стать причиной банального кровотечения, а может вызвать и более тяжелые заболевания. Например, бактериальный перитонит, печеночную энцефалопатию, гепаторенальный синдром и др., которые, в свою очередь, негативно влияют на и без того ослабленные внутренние органы и мешают восстановлению их функционала. В этом случае прогноз зависит от степени дегенерации органа.
© 2018 – 2019, Буната Дмитрий. Все права защищены.
источник
Асцит не является самостоятельным заболеванием, он всегда скрывается под «маской» других патологий. Различают более ста причин формирования данного состояния. Но как же узнать, что именно привело к скоплению жидкости в брюшной полости?
- Болезни печени. Среди патологий печени к асциту могут приводить:
- цирроз печени. Заболевание, при котором клетки печени замещаются соединительнотканными структурами с образованием плотных узлов. Соответственно, происходит разрушение гепатоцитов (клеток печени) с формированием функциональной недостаточности печени (снижение выработки белков — альбуминов и глобулинов), что ведёт к снижению онкотического давления. Кроме этого, образованные узлы нарушают архитектонику печени, нарушают процессы кровообращения, развивается портальная гипертензия (повышение давления в воротной вене), которая приводит к повышению проницаемости сосудистой стенки и формированию асцита. Всё это ведёт к снижению объёма циркулирующей крови, рефлекторным реакциям (высвобождаются гормоны, повышающие давления — ренин, альдостерон, вазопрессин и др.) и к повышению нагрузки на сердечно-сосудистую систему, ведущей к формированию сердечной недостаточности, что приведёт к ещё большему объёму асцитической жидкости;
- рак печени. Постоянно увеличивающаяся в объёме опухоль приводит к сдавлению сосудов печени, лимфатических ходов. Кроме того, она может оторваться от первичного очага и попасть в брюшину, тем самым нарушится функция печени, брюшины, внутрипечёночных сосудов, что и приведёт к асциту;
- синдром Бадда-Киари — это перекрытие просвета печёночных вен сгустком крови (тромбом). Это приводит к нарушению циркуляции крови, увеличению давления и, в конечном итоге, к водянке живота.
- Болезни сердца:
- сердечная недостаточность. На своих последних стадиях данное заболевание приводит к несостоятельности сердца перекачивать большие объёмы крови, в результате чего она застаивается в венах организма (например, при левожелудочковой недостаточности кровь задерживается в системе нижней полой вены), что ведёт к повышению гидростатического давления (переполнению сосудов кровью), жидкая часть крови выходит из сосудистого русла и формируется асцит или в тяжёлых случаях анасарка (генерализованный отёк всех мягких тканей и подкожной клетчатки);
- констриктивный перикардит. Это воспаление перикарда (наружной оболочки сердца), при котором образуется множество спаек, окружающих сердце плотным нерастяжимым каркасом. В результате сердце не может нормально сокращаться и формируются застои в нижней полой вене, что ведёт к отёкам и асциту.
- Заболевания почек. При таких болезнях, как хроническая почечная недостаточность, последние стадии гломерулонефрита (воспаление почечных клубочков) или пиелонефрита (воспаление почечных канальцев), развивается нефротический синдром, который ведёт к расширению пор в мембранах почечных нефронов (функциональная единица почки), и выходу через них большого количества белков плазмы (3 и более грамм в сутки), что приводит к снижению онкотического давления и выходу жидкой части крови в брюшную полость с формированием водянки живота. Также при заболеваниях почек нарушается их кровоснабжение, что ведёт к выработке вазоактивных (действующих на сосуды) гормонов — ренина и ангиотензина. Нарушается вывод из организма осмотически активных веществ — креатинина и мочевины (задерживают воду).
- Заболевания лимфатических сосудов:
- филяриатоз. Патология, при которой глисты откладывают яйца в лимфатических сосудах крупного калибра (кишечные либо поясничные) и тем самым перекрывают отток лимфы от органов брюшной полости;
- опухоли лимфатических сосудов или грудного лимфатического протока. В результате роста опухолей сдавливаются лимфатические сосуды, лимфа пропотевает через стенку и выходит в брюшную полость. Большое скопление жидкости в полости сдавливает сосуды, например, нижнюю полую вену, в ней повышается давление и ещё более усугубляется течение заболевания с формированием отёков и асцита.
- Онкологические заболевания:
- мезотелиома. Редкое злокачественное новообразование, происходящее из клеток брюшины. Механизм формирования асцита: иммунная система активируется, чтобы победить раковые клетки, в результате образуется воспалительный процесс, расширяются кровеносные и лимфатические сосуды, пропотевает жидкость, нарастает водянка живота;
- канцероматоз брюшины. Метастазирование раковых клеток из других очагов (лёгких, почек, яичников, печени и др.). Механизм схож с таковым при мезотелиоме;
- рак поджелудочной железы. Железа имеет связь с желчевыводящей системой печени. В результате роста опухоли происходит сдавление желчевыводящих протоков с увеличением печени в размерах, желтухой и другими проявлениями. На последних стадиях заболевания формируется асцит;
- синдром Демона — Мейгса — сочетание рака яичников или матки с асцитом или гидротораксом (скопление жидкости в лёгких).
- Заболевания поджелудочной железы. При остром панкреатите (воспаление поджелудочной железы) происходит выброс ферментов (трипсина, химотрипсина) в брюшную полость в результате самопереваривания поджелудочной железы с образованием перитонита (воспалением брюшины) и образованием водянки. Образуется незначительный асцит (100 — 200 мл жидкости), в конечном итоге формируются псевдокисты. В повреждённой поджелудочной железе формируются мелкие дефекты, через которые начинают выходить пищеварительные ферменты, поддерживается длительный воспалительный процесс в брюшной полости с накоплением значительного количества экссудата (2 — 3 литра и более).
- Туберкулёз. Микобактерии туберкулёза проникают в брюшину и вызывают в ней специфический воспалительный процесс, который нарушает её функции и приводит к асциту с большим количеством экссудата (более 5 — 10 литров).
- Заболевания щитовидной железы. При недостаточной её функции (гипотиреозе) развивается болезнь — микседема, характеризующаяся отёками различных локализаций, в частности и в брюшной полости.
- Ревматические заболевания. Такие заболевания, как системная красная волчанка, ревматоидный артрит и др. могут вызывать аутоиммунное поражение сосудистой стенки (васкулит) и печени. Таким образом снижается проницаемость сосудистой стенки, белковосинтетическая функция печени, развивается асцит.
- Длительное голодание. Приводит к недостаточному поступлению белков в организм, снижению онкотического давления и отёкам.
Ответ на данный вопрос, к сожалению, положительный. У детей, новорождённых и плода асцит может возникать по следующим причинам:
- гемолитическая болезнь новорождённых. Заболевание, при котором плод с резус-положительной группой крови вынашивается матерью с резус-отрицательной. Развивается во время вынашивания второго ребёнка, после того как у матери уже сформированы антитела против данной группы крови при первой беременности;
- аномалии развития (внутриутробные) — ввиду того, что внутренние органы сформированы некорректно (в частности, печень, селезёнка, сердечно-сосудистая система и др.), нарушена их функциональная активность, которая может сопровождаться асцитом;
- генетические заболевания — синдром Дауна (дефект 21 хромосомы) или синдром Тёрнера (поломка в Х-хромосоме) могут приводить к развитию отёков и асцита;
- повреждение плаценты (орган, который обеспечивает жизнедеятельность плода). Если нарушен отток крови от неё, то повышается гидростатическое давление, которое может привести в итоге к асциту;
У детей асцит могут вызывать:
- врождённые пороки развития сердца (митральная недостаточность, аортальный стеноз, коарктация аорты и др.);
- пороки развития почек. После рождения множество токсических веществ и продуктов обмена скапливаются в тканях и крови малыша, приводя к отёкам и асциту;
- опухоли. У детей новообразования встречаются намного реже, но не являются исключением;
- врождённые гемолитические анемии. При таких заболеваниях (серповидно-клеточная анемия, бета-талассемия, микросфероцитоз и др.) происходит повышенное разрушение клеток крови печенью и селезёнкой. Это может привести к повреждению данных органов и появлению асцита;
- квашионкор — заболевание, поражающее детей беднейших стран (чаще африканских), вследствие длительного голодания и характеризуется водянкой живота и другими проявлениями.
Заболевание может проявиться молниеносно или развиваться в течение многих месяцев. Симптомы асцита зависят от заболевания, вызвавшего его. Характерны следующие проявления:
- увеличение живота в объёме;
- «голова медузы» — расширение вен передней брюшной стенки;
- телеангиэктазии — сосудистые звёздочки различной локализации;
- желтушность кожного покрова и склер. Первые признаки желтухи лучше всего определять под языком;
- боли в животе;
- метеоризм — вздутие живота;
- диспепсические явления — тошнота, рвота, изжога, отрыжка и др.;
- одышка — чувство нехватки воздуха (особенно после физических нагрузок), отёки голеней стоп и лица, нарушения сердечного ритма — при заболеваниях сердца;
- гепато- и спленомегалия — увеличение печени и селезёнки в размерах;
- нарушения мочеиспускания, боли в области почек, повышение артериального давления, сухость и снижение эластичности кожи — при заболеваниях почек;
- головная боль, слабость, повышенная утомляемость;
- снижение массы тела, длительный кашель, одышка, необъяснимая усталость свидетельствует о туберкулёзной природе асцита;
- бронзовый оттенок кожи, отёки лодыжек и стоп (претибиальные отёки), выпадение волос, истончение ногтей, снижение температуры тела — говорит о снижении функции щитовидной железы и развитии ассоциированного с этим асцита.
Диагноз асцита можно выявить уже при первом осмотре:
- увеличенный живот (схож с таковым при беременности), выпячивающийся пупок, в лежачем положении распластывается по бокам из-за стекания жидкости («лягушачий живот»), подкожные вены на передней стенке расширены;
- при перкуссии (простукивании) живота звук становится тупым (как по дереву);
- при аускультации (выслушивании фонендоскопом) живота кишечные шумы будут отсутствовать вследствие значительного накопления жидкости.
Для дополнительной диагностики применимы следующие виды лабораторных анализов и инструментальных исследований:
- ультразвуковое исследование органов брюшной полости и почек (УЗИ). Метод обследования позволяет выявить наличие жидкости в брюшной полости, объёмные образования, даст представление о размерах почек и надпочечников, наличие или отсутствие в них опухолей, об эхоструктуре поджелудочной железы, желчного пузыря и др.;
- УЗИ сердца и щитовидной железы — можно определить фракцию выброса (её снижение является одним из признаков сердечной недостаточности), размеры сердца и его камер, наличие фибриновых отложений (признак констриктивного перикардита), размеры и структуру щитовидной железы;
- компьютерная и магнитно-резонансная томография — позволяет визуализировать даже малейшее скопление жидкости, оценить структуру органов брюшной полости, выявить аномалии их развития, наличие новообразований и др.;
- обзорная рентгенограмма органов грудной клетки — позволяет судить о наличии туберкулёза или опухолей лёгких, размерах сердца;
- диагностическая лапароскопия — на передней брюшной стенке делают незначительный прокол, вводят в него эндоскоп (аппарат со встроенной камерой). Метод позволяет определить жидкость в брюшной полости, взять её часть на дальнейшее исследование, чтобы выяснить природу возникновения асцита, также возможно удастся обнаружить повреждённый орган, вызвавший скопление жидкости;
- ангиография — метод, позволяющий определить состояние сосудов;
- общий анализ крови — возможно снижение числа тромбоцитов из-за нарушенной функции печени, увеличение скорости оседания эритроцитов при аутоиммунных и воспалительных заболеваниях и др.;
- общий анализ мочи — позволяет судить о наличии заболеваний почек;
- биохимический анализ крови, гормоны щитовидной железы. Определяются: уровень белка, трансаминазы (АЛАТ, АСАТ), холестерин, фибриноген для определения функционального состояния печени, ревмопробы (С-реактивный белок, ревматоидный фактор, антистрептолизин) для диагностики ревматоидного артрита, красной волчанки или других аутоиммунных заболеваний, мочевина и креатинин для определения функции почек, натрий, калий и др.;
- определение онкомаркёров, например, альфа-фетопротеина при раке печени;
- микроскопическое исследование асцитической жидкости позволяет определить природу асцита.
Для успешного избавления от асцита важно лечение заболевания, приведшего к нему. В каждом конкретном случае оно индивидуально. Рассмотрим лечение основных заболеваний, приводящих к водянке живота.
При сердечной недостаточности используются 4 основные группы препаратов:
- ингибиторы ангиотензинпревращающего фермента (Диротон, Амприл, Энап и др.). Способствуют снижению давления и ремоделированию сердечной мышцы;
- мочегонные (Гидрохлортиазид, Торасемид и др.). Способствуют уменьшению нагрузки на сердце, выводу натрия и лишней жидкости, тем самым снижая проявления асцита;
- бета-блокаторы (Конкор, Небилет, Карведилол и др.). Действуют 24 часа, являются единственными препаратами, достоверно продлевающими жизнь;
- антагонисты альдостерона (Верошпирон, Спиронолактон). Блокируют работу ренин-ангиотензин-альдостероновой системы, которая играет важную роль в развитии сердечной недостаточности.
Также не менее важно соблюдение диеты №10, ограничение употребления жидкости до полутора литров и поваренной соли до пяти граммов в сутки.
Лечение констриктивного перикардита — хирургическое (иссечение поражённого перикарда). Медикаментозно назначают антибактериальную терапию (Цефтриаксон и др.), при выраженном воспалительном процессе гормональные препараты (Преднизолон или др.).
Печень является органом с самой высокой регенеративной функцией (способна к самовосстановлению). Чем раньше начато лечение, тем больше ткани такого особо важного органа удастся сохранить. В зависимости от причины заболеваний печени возможно назначение:
- противовирусные препараты (блокируют размножение вируса). Назначаются при гепатитах вирусного происхождения; при гепатите С (в нынешнее время излечим) — Харвони и его аналоги; при В, D типе — ингибиторы обратной транскриптазы вирусов (Адефовир, Ламивудин) и препараты интерферона;
- гормональные средства (Преднизолон, Метипред и др.) — при аутоиммунных поражениях печени;
- гепатопротекторы (Фосфоглив, Эссенциале, Гептрал, Легалон и др.). Способствуют укреплению мембран гепатоцитов (печёночных клеток), улучшают процессы восстановления печени, обладают незначительным противовирусным действием;
- с дезинтоксикационной целью назначается Гепа-мерц и его аналоги — снижает повышенный уровень аммиака при циррозе печени, улучшает белковый обмен и функции печени;
- мочегонные препараты — Фуросемид, Верошпирон;
- белковые препараты (Альбумин) — нормализуют количества белка в крови, улучшая тем самым онкотическое давление.
Для питания пациентов с заболеваниями печени используется диета № 5 (по Певзнеру).
При отсутствии эффекта или в случае развития рефрактерного асцита (не поддающегося лечению) проводят лапароцентез (ниже пупка выполняется разрез, в рану вводят полую трубку (троакар), через которую вводят катетер и выкачивают скопившуюся жидкость).
Лечение синдрома Бадда-Киари в первые часы заболевания заключается в назначении препаратов, разрушающих тромбы — фибринолитиков (Урокиназа, Альтеплаза и др.) и антикоагулянтов (препятствуют образованию сгустков крови) — Гепарин, Клексан, Фрагмин. В более поздние сроки показано только хирургическое вмешательство:
- трансплантация печени — при множественном тромбозе печёночных вен;
- чрескожная дилатация — в повреждённый сосуд устанавливают специальный баллон, раздувают его, тем самым, расширяя просвет сосуда и улучшая кровообращение;
- портосистемный анастомоз — кровь будет оттекать в обход тромба, между системой воротной и нижней полой вен.
При опухолях печени, вызывающих асцит, показана операция по устранению преграды.
При явлениях хронической почечной недостаточности используют:
- препараты, снижающие артериальное давление — Периндоприл, Валсартан, Ирбесартан;
- мочегонные — Трифас, Диувер, Фуросемид используются при начальных стадиях почечной недостаточности;
- при наличии анемии (снижении гемоглобина) — Ферсинол, Фенюльс (при железодефиците), витамин В12 и фолиевую кислоту при их недостаточности;
- антиагреганты (улучшают кровообращение в почках) — Трентал, Курантил, Тивортин; при крайних степенях почечной недостаточности может использоваться допамин («почечные» дозы) для улучшения кровообращения.
При неэффективности вышеперечисленной терапии переходят к гемодиализу («искусственная почка»). Кровь очищается, проходя через специальный аппарат, который способствует нормализации водного и электролитного баланса и удалению побочных продуктов обмена (азот, креатинин, мочевина). Проводится только в специализированных стационарах в присутствии специально обученного персонала.
В лечении заболеваний, приведших к нефротическому синдрому, могут использоваться стероидные препараты (Метипред, Дексаметазон) и цитостатики (Циклофосфамид и др.) При заболеваниях почек показано использование диеты №7.
Лечение острого панкреатита осуществляется в условиях стационара хирургического отделения. Консервативное лечение включает в себя:
- антисекреторные препараты (Октреотид) — блокируют выработку ферментов поджелудочной железы;
- препараты, угнетающие действие ферментов в тканях и крови организма — Гордокс, Контрикал;
- нестероидные противовоспалительные средства — Ксефокам, Вольтарен. Обладают обезболивающим, противовоспалительным и жаропонижающим эффектами. При их неэффективности наркотические анальгетики — Трамадол;
- спазмолитики — Но-шпа, Дюспаталин, Мебеверин. Устраняют спазм протоков и сфинктеров поджелудочной железы;
При развитии перитонита или асцита, при панкреонекрозе (омертвение участка поджелудочной железы) показано хирургическое лечение, заключающееся в иссечении поражённого участка, дренировании брюшной полости (отток жидкости из брюшной полости через установленные в неё специальные трубки).
Назначается массивная антибактериальная терапия, включающая в себя 5 основных антибиотиков — Рифампицин, Этамбутол, Пиразинамид, Спирамицин, Изониазид. При неэффективности используют запасные группы антибиотиков. Для лечения асцита используют мочегонные препараты — Фуросемид (Лазикс), Торасемид (Торвента) и др. При отсутствии эффекта или развитии кишечной непроходимости (из-за образования спаек) показано хирургическое вмешательство.
Консервативная терапия может использоваться только при филяриатозе — глистной инвазии. Эффективен препарат диэтилкарбамазин, он препятствует обменным процессам филярий, вызывает их гибель. Требуется проведение 5 курсов по 10 дней.
При опухолях, препятствующих оттоку лимфы, производят их удаление. В случае неоперабельной опухоли возможно наложение анастомоза с ближайшей крупной веной. В дальнейшем пациенту потребуется лечебный лапароцентез для удаления лишней жидкости. При удалении асцитической жидкости, содержащей лимфу, необходимо сочетать её забор с введением альбуминов внутривенно.
Не рекомендуются тяжёлые физические нагрузки, так как они повышают давление, что способствует выходу жидкости из сосудистого русла.
Хирургическое лечение при канцероматозе показано при незначительном поражении брюшины. В этом случае поражённый участок иссекают до здоровых тканей, и в дальнейшем лечение будет направлено на устранение первичного очага. При неоперабельных опухолях назначается химиотерапия, направленная на предотвращение роста опухолевых клеток. Назначают препараты, угнетающие синтез ДНК (Блеомицин, Фторурацил, Цисплатин и др.). Для симптоматической терапии могут использоваться противорвотные препараты (Метоклопрамид, Церукал), обезболивающие наркотические (Морфин), мочегонные (Фуросемид).
При микседеме назначают гормоны щитовидной железы:
- L-тироксин (Эутирокс) — аналог гормона тироксина;
- Лиотиронин — аналог трийодтиронина;
- Йодомарин, калия йодид — если снижение функции щитовидной железы обусловлено дефицитом йода в организме.
Препараты улучшают обменные процессы в организме. Также рекомендовано снизить употребление жидкости до 2 литров и соли до 10 г в сутки. Употреблять продукты, богатые йодом (лосось, креветки, печень трески, морской окунь и др.).
При напряжённом асците (более 10 литров жидкости в брюшной полости, нарушается работа внутренних органов) и рефрактерном (отсутствие эффекта от мочегонной терапии) показано проведение лапароцентеза (техника описана выше). За 1 раз рекомендуют удалять не более четырёх литров жидкости, которые компенсируют плазмозаменителями (реополиглюкин, желатиноль и др.) или альбумином (т.к. асцитическая жидкость богата белками, её удаление влияет на онкотическое давление). Выкачивание большего количества жидкости чревато коллапсом (резким падением артериального давления).
Асцит — это грозное осложнение, которое может привести к:
- спонтанному бактериальному перитониту. Длительный застой жидкости создаёт предпосылки для развития в ней патогенной микрофлоры и воспаления листков брюшины, которое сопровождается общим тяжёлым состоянием и чревато гибелью пациента;
- гидротораксу — скопление жидкости в лёгких с последующей дыхательной недостаточностью;
- кишечной непроходимости. Скопившаяся жидкость сдавливает петли кишечника и препятствует прохождению каловых масс;
- гепаторенальному синдрому — вторичное поражение почек при циррозе печени с развитием тяжелейшей почечной недостаточности;
- пупочной грыже. При высоком внутрибрюшном давлении сильно растягивается околопупочное кольцо, через которое могут выпячиваться внутренние органы (кишечник и др.).
Сам по себе асцит не является причиной смерти. Летальность зависит от состояния, вызвавшего его. При скоплении жидкости, появившейся вследствие голодания, прогноз благоприятный. Достаточно добавить в рацион питания белковую пищу и проявления асцита сойдут на «нет». Выживаемость зависит от функционального состояния печени, почек, сердца, от адекватности проводимого лечения. Например, при терминальных стадиях пятилетняя выживаемость составляет не более 15 — 20 %. (т.е. из ста человек только пятнадцать-двадцать проживут 5 лет). При часто рецидивирующем асците, плохо поддающемуся консервативной терапии, выживаемость составляет не более 2 лет.
Субстратом образования метеоризма являются скопившиеся в кишечнике газы, для асцита — жидкость. Поэтому отличить их не составляет труда. При метеоризме, если простукивать по передней брюшной стенке, звук будет очень звонкий (как по барабану). Увеличение живота при метеоризме равномерное, отёки других локализаций также отсутствуют. Для разрешения метеоризма достаточно включить в свой рацион продукты богатые клетчаткой (отруби и тд.), принять средства, уменьшающие вздутие живота — эспумизан, метеоспазмил и др. Также не стоит путать асцит и «лягушачий живот» при рахите у детей. У малышей такой живот появляется из-за слабости мышц передней и боковой стенок живота, в связи с чем он принимает выпуклое и висячее положение (в вертикальном положении).
Стоить помнить, асцит — это состояние, которое не проходит самостоятельно. При первых симптомах стоит немедленно обратиться к врачу. Своевременно проведённая диагностика и лечение заболевания, приведшего к скоплению жидкости, многократно увеличивает шансы на улучшение вашей жизни.
источник
Асцит или водянка живота – заболевание, связанное со скоплением чрезмерного количества жидкости в брюшной полости, и возникающее в качестве осложнения какой-либо имеющейся в организме патологии. Причин развития данного заболевания может быть огромное количество. У взрослого человека асцит обычно сопровождает нефротический синдром, порок сердца, цирроз печени.
Возникновение асцита у ребенка чаще всего свидетельствует о наличии злокачественной опухоли или нефротического синдрома. В брюшной полости здорового человека происходит постоянное выделение небольшого количества жидкости, необходимой для нормального функционирования расположенных в данной области организма внутренних органов. Такая жидкость носит название экссудата и всасывается обратно самой брюшиной.
Мнение эксперта: Существует два вида жидкости: экссудат и транссудат, которые отличаются друг от друга содержанием белка. При асците может быть и тот и другой вид.
Нарушение функции выделения и всасывания жидкости, возникшее в результате какого-либо заболевания, приводит к развитию асцита.
Возникновению данной патологии подвержены люди всех возрастных категорий, даже новорожденные дети. Асцит у новорожденных обычно сопровождает гемолитическую болезнь – заболевание, при котором иммунные клетки организма матери начинают угнетать кровяные клетки организма ребенка, в результате чего у последнего развивается патологическое состояние в виде желтухи, отечности отдельных частей тела и т.п.
Еще одной распространенной причиной асцита у новорожденных детей является врожденный нефротический синдром – комплекс симптомов, развивающийся в результате поражения почек и сопровождающийся нарушением обмена белка, его чрезмерным выведением из организма, возникновением отеков разных частей тела.
Практически все заболевания, поражающие брюшную полость (перитонит, глистная инвазия, псевдомиксома, злокачественные новообразования толстого кишечника, желудка, яичников, эндометрия, молочной железы), также сопровождаются развитием асцита. Нередко встречается сочетание плеврита. водянки живота и перикардита при уремии, ревматизме, системной красной волчанке.
Асцит развивается при саркоидозе, непроходимости печеночных вен, гипернефроме, хроническом гломерулонефрите, панкреатите, лимфостазе, хронической диарее. В основе развития асцита лежит комплекс гидростатических, воспалительных, метаболических, гемодинамических нарушений, приводящих к скоплению экссудата в брюшной полости.
Основным симптомом асцита является резкое увеличение живота в объеме, возникновение в нем дискомфорта и болей. Общие признаки заболевания таковы:
Люди, больные асцитом, обычно очень быстро наедаются, иногда возможен полный отказ от приема пищи. При этом независимо от ежедневного рациона питания живот продолжает увеличиваться в размерах. У мужчин часто наблюдается отек половых органов и нижних конечностей.
В зависимости от того, какое заболевание повлекло за собой накопление жидкости в брюшной полости, асцит может развиваться очень медленно или, наоборот, стремительно. Иногда при медленном развитии заболевания человек ошибочно принимает увеличение живота за признак ожирения и начинает бороться с излишним весом. Однако все методы этой борьбы оказываются напрасными.
По мере увеличения живота у больного выпячивается пупок (как на поздних сроках беременности), развивается паховая или пупочная грыжа. В случае сочетания туберкулеза и асцита наблюдается медленное похудение человека, при этом быстро увеличивающийся в размерах живот становится еще более заметным. При сочетании асцита с почечной недостаточностью наблюдается стойкий отек кожных покровов.
Количество жидкости, которая может скопиться в животе больного при развитии асцита, может быть различным: от 3 до 10 литров. Редко встречаются случаи, когда количество экссудата в брюшной полости больного достигает 20 литров. Обычно такая жидкость имеет бело-молочный цвет, при проведении лабораторного анализа в ней обнаруживается большое количество липоидов и жиров.
Асцит необходимо диагностировать от опухолей внутренних органов брюшной полости, беременности, кисты яичника, ожирения. Основными методами диагностики данного заболевания является ультразвуковое исследование брюшной полости, мультиспиральная компьютерная томография органов брюшной полости, лапароскопия с последующим забором жидкости, лабораторное исследование экссудата, анализ мочи.
Лечение асцита начинается с устранения основного заболевания. Если основная патология требует длительной терапии (например, злокачественная опухоль), параллельно назначается прием мочегонных препаратов (амилорид, спиронолактон), действие которых направлено на коррекцию водно-соляного обмена в организме. Лечится заболевание обычно в домашних условиях с обязательным поседением специалиста. Всем больным прописан постельный режим и специальная диета, подразумевающая отказ от употребления соли.
Мнение эксперта: В большинстве случаев остро возникший асцит лечится в стационаре. Асцит хронический может вестись и амбулаторно. Мочегонные же средства назначаются для улучшения и увеличения выведения избытка жидкости из организма.
В тех случаях, когда медикаментозное лечение не оказывает положительного результата либо скопление жидкости слишком велико, проводится хирургическое вмешательство – пункция брюшной полости. Перед началом процедуры больному следует полностью опорожнить мочевой пузырь. В момент проведения операции пациент находится в сидячем положении (либо лежит на боку). Пункция или прокол при помощи специального инструмента – троакара проводится по средней линии живота (между лобком и пупком) после введения больному анестезирующего средства. Жидкость из брюшной полости выводится, как правило, медленно и не более 5 литров за один раз. Частое повторение операции может привести к таким нежелательным последствиям, как воспаление брюшной полости и сращение кишок.
Прогноз лечения полностью зависит от течения основного заболевания. Чем больше пункций требуется провести, тем более он неблагоприятен.
Гломерулонефрит – это двустороннее поражение почек. как правило, аутоиммунной природы. Название патологии происходит от термина «гломерула» (синоним — клубочек ), который обозначает функциональную единицу почки. Это означает, что при гломерулонефрите поражаются основные функциональные структуры почек, вследствие чего быстро развивается почечная недостаточность .
Среди мужского населения это заболевание выявляется в 2 – 3 раза чаще. У детей, среди всех приобретенных почечных болезней, гломерулонефрит занимает 2 место. По данным статистики, эта патология выступает в роли самой частой причины инвалидности. которая развивается из-за хронической почечной недостаточности. Примерно у 60 процентов больных острым гломерулонефритом развивается гипертония. У детей в 80 процентах случаев острая форма этой болезни провоцирует различные сердечно-сосудистые нарушения.
Изначально в организм попадает инфекция, которая может являться причиной ангины. бронхита, пневмонии или других заболеваний дыхательных путей. Патогенный микроорганизм, в данном случае бета-гемолитический стрептококк. воспринимается организмом как чужеродное тело (по-научному — как антиген ). Следствием этого является выработка собственным организмом антител (специфических белков ) против данных антигенов. Чем дольше инфекция находится в организме, тем больше антител вырабатывает организм. Впоследствии антитела соединяются с антигенами, формируя иммунные комплексы. Изначально данные комплексы циркулируют в кровеносном русле, но затем постепенно оседают на почках. Мишенью для иммунных комплексов является мембрана нефрона.
Оседая на мембранах, иммунные комплексы активируют систему комплимента и запускают каскад иммунологических реакций. В результате этих реакций на мембране нефрона оседают различные иммунокомпетентные клетки, которые повреждают ее. Таким образом, нарушаются основные функции почки — фильтрация, всасывание и секреция.
Патогенез (механизмы образования ) условно можно выразить в следующей схеме — инфекция – выработка организмом антител – активация системы комплемента – выход иммунокомпетентных клеток и оседание их на базальной мембране – образование
Причинами развития гломерулонефрита являются:
Ангины и другие стрептококковые инфекции
Данная причина гломерулонефрита является самой частой, поэтому чаще всего используется термин постстрептококковый гломерулонефрит. Причинами постстрептококкового гломерулонефрита являются патогенные штаммы стрептококков группы А. Среди них особенное внимание заслуживает бета-гемолитический стрептококк. Это грамположительный, неподвижный микроорганизм, который встречается повсеместно. В определенной концентрации он находится на слизистых оболочках человека. Главным путем передачи является аэрогенный (воздушно-капельный ) и пищевой путь. Данный микроорганизм продуцирует множество токсинов, а именно дезоксирибонуклеазу, гемолизин, стрептокиназу А и В, стрептолизин, гиалуронидазу. Также он обладает обширным антигенным комплексом. Именно благодаря своей антигенной структуре и продукции токсинов по медицинской значимости стрептококки занимают второе место после стафилококка .
Самым частым заболеванием, которое вызывается стрептококк, является ангина или тонзиллофарингит. Это острое инфекционное заболевание с поражением слизистой оболочки и лимфатической ткани (миндалин ) глотки. Начинается оно внезапно с резкого повышения температуры тела до 38 – 39 градусов. Основными симптомами являются боль в горле. общие симптомы интоксикации. покрытие миндалин гнойным налетом желтовато-белого цвета. В крови отмечается лейкоцитоз. повышение СОЭ (скорость оседания эритроцитов ). появление С-реактивного белка. В период болезни регистрируются положительные бактериологические тесты. Сама по себе ангина редко представляет опасность, больше всего она опасна своими осложнениями. Основными осложнениями стрептококковой ангины являются постстрептококковый гломерулонефрит, токсический шок, ревматическая лихорадка.
Однако, для постстрептококкового гломерулонефрита недостаточно одного эпизода ангины. Как правило, необходимы множественные эпизоды заболевания или так называемая рецидивирующая стрептококковая ангина. В этом случае постепенно происходит сенсибилизация (повышенная чувствительность ) организма антигенами стрептококка и выработка антител. После каждого эпизода болезни происходит повышение титров (концентрации ) противострептококковых антител. В то же время, у детей крайне редко возможно развитие гломерулонефрита после единичного эпизода ангины.
Дифтерией называется острое инфекционное заболевание, которое протекает с преимущественным поражением слизистой оболочки носоглотки. Возбудителем дифтерии является дифтерийная палочка или палочка Леффлера. Данный микроорганизм обладает мощными патогенными свойствами, а также продуцирует экзотоксин. Высвобождаясь в кровеносное русло, экзотоксин разносится с током крови по всему организму. Он способен поражать сердце. нервную систему, мышцы. При дифтерии также поражаются почки. Однако чаще всего поражаются не клубочки, а канальцы почек. Таким образом, наблюдается картина нефроза, а не гломерулонефрита. Острый гломерулонефрит наблюдается при гипертоксической (молниеносной ) форме дифтерии. Клинически он проявляется отеками, гематурией (кровью в моче ). резким снижением суточного диуреза (общего количества выделяемой мочи ).
Симптомами гломерулонефрита являются:
Боль при гломерулонефрите локализуется с обеих сторон, носит тупой и постоянный характер, может усиливаться при ходьбе.
Дизурические проявления – это различные расстройства мочеиспускания, которые выражаются в затрудненном и частом мочеиспускании. Дизурия является симптомом гломерулонефрита только на ранних этапах. Очень быстро она переходит в олигурию – снижение суточного диуреза менее 500 миллилитров в сутки. Снижение объема выделяемой мочи развивается вследствие нарушенной внутрипочечной гемодинамики. Из-за отложения иммунных комплексов на базальной мембране почек нарушаются процессы фильтрации, всасывания и секреции. Это приводит к формированию меньшего объема мочи, а самое главное — к задержке жидкости в организме.
Самым тяжелым и опасным дизурическим проявлением гломерулонефрита является анурия – полное прекращение выделения мочи. Анурией осложняются самые тяжелые формы гломерулонефрита. Вместе с мочой в организме задерживаются токсические продукты обмена, такие как креатинин. мочевина. аммиак. Задержка этих веществ ведет к интоксикации организма, развитию уремии и энцефалопатии .
Механизмами развития артериальной гипертензии являются:
Асцит – это скопление жидкости в брюшной полости, которое может быть вызвано различными патологическими состояниями, чаще всего циррозом печени. Таким образом, асцит – это симптом, а не самостоятельное заболевание. Живот увеличивается в размерах, повышается внутрибрюшное давление, количество жидкости в брюшной полости может достигать 20 литров. Скопление жидкости нарушает работу многих внутренних органов, в том числе дыхание, так как купол диафрагмы оттесняется вверх.
Самой частой причиной асцита является цирроз печени. он регистрируется примерно в ? случаев асцита. Цирроз, как и другие заболевания печени (саркоидоз. рак печени), вызывает портальную гипертензию (увеличение давления в воротной вене и ее притоках), что способствует застою крови и увеличению количества выпота в брюшную полость. Портальная гипертензия развивается не только при заболеваниях печени, препятствия оттоку крови могут возникать из-за сосудистых нарушений (тромбоз. стеноз сосудов системы воротной вены). В норме брюшина выделяет небольшое количество жидкости, которое потом сама же всасывает, это нужно для свободного передвижения петель кишечника. При портальной гипертензии количество жидкости значительно возрастает.
Вторая по частоте причина асцита – опухоли брюшной полости. Асцит при онкологии связан с нарушением нормальной циркуляции жидкости. При сердечной недостаточности тоже возникает застой в малом круге кровообращения, что приводит к увеличению количества выпота.
Асцит развивается при полисерозите (воспалении серозных оболочек сразу нескольких органов, в том числе брюшины), который часто встречается при системных заболеваниях соединительной ткани (ревматизм. ревматоидный артрит, системная красная волчанка).
Частой причиной асцита являются состояния, связанные с уменьшением содержания белков в крови. Это могут быть обменные нарушения, нефротический синдром (при гломерулонефрите), заболевания желудочно-кишечного тракта с нарушением всасывания белков.
Множество других состояний, сопровождающихся портальной гипертензией или патологическими изменениями в брюшине, вызывают развитие асцита, поэтому при его признаках необходима тщательная диагностика для выявления причины, что важно для выбора тактики лечения.
Признаки асцита могут появляться и нарастать резко или постепенно, все зависит от вызывающих его причин. Пациент обращает внимание на увеличение объема живота, чувство тяжести в нем, тянущие боли, иногда выпячивается пупок. По мере нарастания симптомов становится трудно передвигаться, наклоняться, появляется одышка из-за смещения диафрагмы выше физиологичного уровня, появляется отечность ног. Живот имеет характерную форму «пузыря с водой». В вертикальном положении он свисает, в горизонтальном – распластывается. Увеличение внутрибрюшного давления приводит к появлению грыжевых выпячиваний (пупочные, паховые грыжи), может спровоцировать геморрой или выпадение прямой кишки.
В зависимости от причины, вызывающей асцит, могут отмечаться симптомы, характерные для основного заболевания. Асцит при раке (яичников, печени, других органов брюшной полости) сопровождается увеличением лимфатических узлов. Асцит при сердечной недостаточности сопровождается отеком ног, акроцианозом, увеличением печени. Помимо асцита, обычно отмечается гидроторакс (скопление жидкости в грудной полости). При портальной гипертензии, связанной с заболеваниями печени, асцит сопровождается появлением на передней брюшной стенке венозной сети.
Если Вы обнаружили у себя схожие симптомы, незамедлительно обратитесь к врачу .
Легче предупредить болезнь, чем бороться с последствиями.
Увеличение живота может быть связано с разными причинами (ожирение. беременность, новообразования и пр.), поэтому при подозрении на асцит проводится очень подробное обследование.
Самыми простыми способами выявить асцит являются пальпация и перкуссия живота, которые проводит терапевт во время осмотра. При пальпации определяется увеличение объема, напряжение живота, пропальпировать внутренние органы часто бывает невозможно. При перкуссии живота характерно притупление звука и смещение границ тупости при изменении положения тела. Важным диагностическим признаком является симптом флюктуации. Он определяется следующим образом: к одной стороне живота прикладывается ладонь, а с другой стороны выполняются постукивания пальцами. При асците ладонью ощущаются колебания, передаваемые за счет жидкости.
Инструментальная диагностика проводится для уточнения диагноза иопределения объема жидкости в брюшной полости, ее характера. Существуют следующие способы визуализации асцита:
- Рентгенография брюшной полости (выявляет объем жидкости не менее 0,5 л).
- Снимок грудной клетки позволяет выявить подъем купола диафрагмы из-за давления асцитической жидкости.
- УЗИ определяет не только жидкость в брюшной полости, но и возможные причины асцита, поэтому исследуются все органы брюшной полости, особое внимание уделяется печени.
- Гепатосцинтиграфия – метод, позволяющий визуализировать структуру печени и оценить ее функцию.
- Доплерография проводится для определения состояния кровотока в системе портальной вены.
- Ангиография – оценка состояния кровотока в печени с использованием рентгеноконтрастного вещества.
- Лабораторное обследование проводится для оценки функционального состояния печени. Выполняются биохимические пробы (АЛТ, АСТ, билирубин), коагулограмма, иммунограмма.
- Анализ экссудата, полученного при помощи пункции, позволяет предположить характер патологического процесса. Например, при онкологии в брюшной полости асцитическая жидкость содержит атипичные клетки.
Лечение асцита должно проводиться с учетом вызвавшей его причины, иначе жидкость будет образовываться вновь. При циррозе печени лечение асцита обязательно включает назначение гепатопротекторов, при онкологии – химиотерапию или оперативное лечение, при сердечной недостаточности – назначение препаратов, улучшающих деятельность сердца.
Патогенетическая терапия асцита заключается в ограничении употребления жидкости и соли, которая удерживает воду в организме, назначении мочегонных средств. Одновременно повышается содержание белков в крови путем внутривенного введения альбумина или препаратов плазмы. Белок удерживает жидкость в кровеносном русле, препятствуя ее выходу в брюшную полость. Диета при асците назначается бессолевая, с ограниченным количеством жидкости и повышенным содержанием белка.
Если консервативное лечение асцита неэффективно, жидкость удаляется при помощи лечебной пункции, эта манипуляция называется «лапароцентез брюшной полости». Повторные пункции могут стать причиной образования спаек, инфицирования, поэтому при необходимости частого удаления жидкости устанавливается шунт.
Лечение асцита народными средствами может быть рекомендовано только в качестве вспомогательной терапии или при небольшом объеме жидкости в брюшной полости. Оно заключается в использовании трав с мочегонным эффектом. Хороший эффект оказывают березовые листья и почки (настои, обертывания, ванны).
Асцит является осложнением многих заболеваний, утяжеляя их течение. Асцит при циррозе печени свидетельствует о значительных нарушениях в структуре ткани и развитии портальной гипертензии, при онкологии – о распространении процесса с вовлечением брюшины. Сколько живут пациенты с асцитом при циррозе, онкологии и других заболеваниях, зависит от своевременности и эффективности проводимого лечения.
Гломерулонефрит – инфекционно-аллергическое заболевание, относящееся к группе приобретенных заболеваний почек. Различные формы гломерулонефрита различаются по этиологии, проявлениям, течению болезни и ее исходу. Чаще всего характеризуется иммунным воспалением почечных клубочков, а также дальнейшим, вторичным воспалением канальцев почек и интерстицией .
Различают острый гломерулонефрит. быстротекущую форму болезни. и хронический гломерулонефрит. Острая форма заболевания наиболее часто может быть вызвана перенесенной ранее стрептококковой инфекцией – постстрептококковый гломерулонефрит. По этиологии различают первичные гломерулонефриты и вторичные. которые возникают при системных заболеваниях – системной красной волчанке. ревматизме . узелковом периартериите и других.
Причинами заболевания являются перенесенные ранее инфекции – стрептококковая. стафилококковая и иные бактериальные инфекции. В некоторых случаях этиологическим фактором в развитии заболевания могут выступать гепатиты В и С . и возможно цитомегаловирусная инфекция . Гломерулонефрит может развиваться на фоне заболеваний паразитарной природы, под токсическим воздействием некоторых лекарств, при употреблении алкоголя и наркотиков, особенно сильное влияние эти привычки имеют в подростковом возрасте. Нарушение в календарном планировании плановых профилактических прививок также может способствовать возникновению болезни. Поэтому профилактика гломерулонефрита должна содержать точное соблюдение плановых прививок и медосмотров.
Развитие гломерулонефрита происходит на фоне реакций клеточного и гуморального иммунитета. Как правило, перенесенное ранее инфекционное заболевание, вызывает в организме иммунную реакцию, образуются иммунные комплексы. Выработанные для этого антитела разносятся током крови по всем системам, поражая чувствительные к ним органы. Это могут быть сердечная мышца, возникает ревматическая болезнь сердца, суставы – ревматизм, или как в данном случае клубочки почек — острый гломерулонефрит.
У детей заболевание приводит к почечной недостаточности и как следствие инвалидности. Постстрептококковый гломерулонефрит в отличие от других форм заболевания чаще встречается у детей в возрасте 5-12 лет, так же наблюдается развитие болезни у подростков и молодых людей. Острая форма болезни может развиться в любом возрасте, реже заболевание встречается после 40 лет.
Заболевание развивается не позднее чем через три недели после перенесенной стрептококковой инфекции, к примеру, ангины . тонзиллита . пиодермии. поражая обе почки. Для начала течения болезни характерны общие симптомы это слабость, головная боль . озноб, тошнота, боль в пояснице, высокая температура. Острый гломерулонефрит вызывает отечность век, бледность, уменьшение выделяемой мочи.
Клиническая картина заболевания неоднозначна. Течение болезни может проходить в циклической форме с бурным развитием и многими симптомами, а может быть и в латентной, то есть стертой скрытой форме. Часто диагностика гломерулонефрита при латентной форме течения болезни происходит несвоевременно, что дает возможность болезни перейти в хроническую.
Характерные клинические симптомы гломерулонефрита это наличие крови при мочеиспускании и отеки на лице. Гематурия может быть незначительной и обнаружить этот симптом можно только с помощью анализа мочи. Но чаще моча имеет красно-бурый цвет. Отечность также не всегда заметна это либо мешки под глазами и заметное сужение глаз, либо резкое повышение массы тела на 3-4 килограмма.
Снижение количества мочи, так называемая олигурия может продолжаться до 5 дней, потом выделение мочи нормализуется, но наблюдается сниженная плотность мочи. Также для острого гломерулонефрита характерно повышение артериального давления, которое может продолжаться в течение нескольких недель.
При положительном прогнозе основные симптомы гломерулонефрита исчезают в течение первого месяца, а выздоровление происходит за 2-2,5. В случаях поздней диагностики, или если болезнь не поддается лечению в течение года, заболевание переходит в тяжелую хроническую форму.
Гломерулонефрит у детей зачастую развивается в острой форме. Более подвержены заболеванию дети старшего дошкольного и младшего школьного возраста. Груднички практически не болеют гломерулонефритом. Течение болезни крайне бурное с критическими повышениями температуры тела.
Хронический гломерулонефрит различают на четыре клинические формы. При любом течении характерны периоды ремиссии. которые сменяются обострениями схожими с острой формой болезни. Обострения могут быть сезонными, а также возникающие при повторном заражении инфекционными заболеваниями стрептококковой природы.
Некротическая форма гломерулонефрита характеризуется генерализоваными отеками, возможно, их развитие до асцита и анасарки. При лабораторных исследованиях обнаруживается повышение белка в моче и его снижение в крови. При этом повышается уровень липидов и глобулинов. снижается уровень альбуминов .
Гипертоническая форма болезни не включает такие ярко выраженные симптомы гломерулонефрита как некротическая. для этой формы характерна гипертензия. Возможна и смешанная форма течения хронического гломерулонефрита. В этом случае симптомы обеих форм присутствуют одновременно.
Также как и острый гломерулонефрит хронический может протекать практически бессимптомно. Латентная форма характеризуется лишь слабым нарушением выделения мочи.
Подозрение на острый гломерулонефрит вызывает триада симптомов: отеки. гематурия. артериальная гипертензия. При латентной форме течения болезни показаниями к дальнейшей диагностике является данные анамнеза предыдущего заболевания и определение антистрептококковых антител и их концентрации в сыворотке крови .
Назначается рентгенконтрасное исследование и ряд лабораторных анализов, что бы исключить наличие других почечных заболеваний. Так дифференциальная диагностика гломерулонефрита должна исключить обострения нефритов, в том числе наследственной формы, туберкулёза почек. нефролитиаза. Диагностика гломерулонефрита включает также данные ранее перенесенных заболеваний, длительное наблюдение за состоянием пациента, консультации окулиста. При гломерулонефрите происходят изменения глазного дна. При крайне бурном течении болезни проводят исследование тканей – биотапта почки .
При лабораторных исследованиях мочи наличие гематурии или цилиндрурии является подтверждением диагноза. В первые дни течения болезни в анализе мочи обнаруживаются лимфоциты . Они являются отражением иммунного процесса в клубочках почек.
Анализ крови выявляет нейрофильный лейкоцитоз. анемию. увеличение СОЭ. Данные показывают сниженную клубочковую фильтрацию, увеличение азотистых шлаков в крови. Обнаруживаются нарушения системы свертываемости крови. Это чаще всего представлено продуктами деградации фибрина. а также фибриногена в сыворотке крови и моче.
При подтверждении диагноза больного следует госпитализировать. Лечение гломерулонефрита в стационаре требует постельного режима, пациенту требуется покой и тепло, что способствует нормализации кровообращения в почках и снижению артериального давления. Назначается диета с дозированным приемом жидкости для купирования отеков. В первые дни режим питания строго контролируется, исключается наличие соли в пище, ее употребление постепенно возобновляется после исчезновения отеков. Также исключают блюда с богатым содержанием калия, экстрактивных веществ, аллергенов.
Медикаментозное лечение гломерулонефрита включает антибактериальную терапию, чаще всего назначаются антибиотики пенициллинового ряда курсом 1.5-2 месяца. Рекомендовано назначение гепарина подкожно курсом 2-4 недели. Препарат предотвращает внутрисосудистое свёртывание крови. Если симптомы гломерулонефрита включают артериальную гипертензию назначаются ингибиторы АПФ, внутривенные вливания аминофиллина в растворе глюкозы и последующую инфузию фуросемида . Допустимо применение клофелина . метилдопа .
Прогноз лечения гломерулонефрита чаще всего благоприятный. 85-90% пациентов выздоравливают полностью, у остальных больных сохраняются изменения мочи, что не дает возможности говорить о полном выздоровлении. При длительном лечении заболевания возможен переход в хроническую форму с признаками некротического синдрома. Летальный исход регистрируют редко, чаще всего при несвоевременном обнаружении латентной формы течения болезни.
На первом этапе развития болезни возможно возникновение тяжелых осложнений, опасных для жизни пациента. Тяжелое течение болезни может вызывать почечную эклампсию. острую почечную и сердечную недостаточность.
Почечная эклампсия одно из самых частых осложнений острого гломерулонефрита. Эклампсия или ангиопастическая энцефалопатия является спазмом сосудов головного мозга, отеками мозга. Признаками осложнения являются тонико-клонические судороги, перед ними следуют головная боль, тошнота, рвота, нарушение зрения. Приступ эклампсии напоминает эпилептический. сопровождается скачком артериального давления и может длиться несколько минут. Также наблюдается серия приступов. Без своевременного купирования приступа происходит кровоизлияние в мозг.
При гиперергическом течении острой формы болезни развивается острая почечная недостаточность. Осложнения гломерулонефрита вызываются бурным течением болезни. Острая почечная недостаточность сопровождается резким прекращением мочевыделения. В результате задержки воды в организме шлаки и калий накапливаются, тем самым вызывая гипергидрацию и ацидоз . При дальнейшем развитии почечной недостаточности возникают симптомы интоксикации – анорея. тошнота, многократные рвоты, диарея . Присоединяются геморрагический синдром. поражение сердечнососудистой системы и ЦНС. Пациент может впасть в уремическую кому. чаще всего кому вызывает осложненный гломерулонефрит у детей.
Реже, особенно у детей, возникают осложнения гломерулонефрита со стороны работы сердца. Острая сердечно-сосудистая недостаточность характеризуется такими признаками как увеличение печени, нарастание периферической отечности и отеком легких. Именно отек легких чаще всего и становится причиной летального исхода без своевременной помощи.
Правильное лечение стрептококковых заболеваний, соблюдение календаря профилактических прививок и санация очагов инфекции в организме составляют главные меры профилактики. Дети, перенесшие постстрептококковый гломерулонефрит, должны находиться под диспансерным наблюдением на протяжении 5 лет после лечения.
Профилактические медицинские осмотры и лабораторные исследования позволяют рано обнаружить болезнь и избежать осложнений. Самолечение, пренебрежение общими симптомами чаще всего приводит к тяжелым формам заболевания.
Гломерулонефрит. Причины и симптомы. Синдромы при гломерулонефрите. Острый и хронический гломерулонефрит
На сегодняшний день гломерулонефритом страдает от 10 до 15 взрослых пациентов на 10 000 человек. По частоте выявления среди всех патологий почек это заболевание занимает 3 место. Гломерулонефрит может быть диагностирован среди пациентов любой возрастной группы, но наиболее часто болезнь встречается у людей, не достигших 40 лет.
В последнее время частота диагностирования гломерулонефрита среди жителей разных стран увеличивается. Это объясняется ухудшением экологической обстановки, а также общим снижением иммунитета среди населения, которое является следствием несоблюдения рекомендаций по здоровому образу жизни.
На сегодняшний день гломерулонефрит принято считать аутоиммунным заболеванием. В основе его развития лежит иммунокомплексное поражение почек, которое развивается после перенесенной бактериальной или вирусной инфекции. Поэтому гломерулонефрит также называется простудным нефритом или постинфекционной болезнью почек. Эти названия отражают патогенез заболевания — почки поражаются, после того как человек перенес какое-либо инфекционное заболевание. Однако, также провоцировать развитие гломерулонефрита могут лекарственные препараты, токсины.
инфильтрата из нейтрофилов и других клеток – поражение базальной мембраны нефрона – нарушение функции почек.
Вирусная инфекция также играет важную роль в развитии гломерулонефрита. Ранее перенесенное вирусное заболевание является второй по частоте (после стрептококковой инфекции ) причиной гломерулонефрита. Чаще всего развитие гломерулонефрита провоцируют такие вирусы как аденовирусы, ECHO, вирус Коксаки. В качестве антигенов выступает сложная структура вирусов. Также гломерулонефрит у детей может быть следствием ветряной оспы (ветрянки ) или эпидемического паротита (свинки ) .
В настоящее время все чаще встречается лекарственное поражение почек. Так, некоторые лекарства обладают нефротоксичным действием, что означает их избирательность к почкам. Среди таких лекарств особое внимание привлекают сульфаниламиды и препараты пенициллинового ряда. К первой категории препаратов относятся сульфатиазол, сульгин, сульфацил-натрий, а ко второй – D-пеницилламин и его производные. Сульфаниламидные препараты могут поражать различные структуры почек с дальнейшим развитием обструктивной уропатии (заболевания, при котором нарушен ток мочи ) или гемолитической почки.
То, что лечение пенициллинами может провоцировать поражение почек, было известно еще с 50-х годов прошлого столетия. Однако лишь недавно была описана детальная морфологическая картина почек при пенициллиновом гломерулонефрите. Так, D-пеницилламин обладает особой тропностью (избирательностью ) к клубочкам, то есть к гломерулам. Поражая функциональные единицы почек, препараты из этой группы приводят к развитию мембранозного гломерулонефрита. При этом вдоль мембран клубочков происходит отложение иммунных комплексов. Также пенициллины могут вызывать и другие виды гломерулонефритов, такие как пролиферативный и экссудативный.
Токсическое поражение почек встречается при отравлении ртутью, свинцом, мышьяком. Эти и многие другие вещества обладают нефротоксическими свойствами, поражая при этом клубочки, канальцы и другие структуры почек.
В клинике гломерулонефрита выделяют мочевые и общие (не мочевые ) симптомы. К первым относятся такие как снижение суточного диуреза, кровь и белок в моче, ко вторым – повышенное артериальное давление. отеки. Объясняется это тем, что почки осуществляют важные функции в организме, а также участвуют в регуляции артериального давления и водно-солевого обмена.
Боль – является одним из самых ранних симптомов гломерулонефрита. Поскольку при данной патологии поражаются одновременно обе почки (патологический процесс при гломерулонефрите двусторонний ), то боль локализуется с обеих сторон. Жалобы на боль в пояснице слева или справа не характерны для гломерулонефрита.
В основе развития болевой симптоматики при гломерулонефрите лежат два момента. Первый – это увеличение размеров почек на первых этапах. Сами почки не содержат в себе нервных окончаний. Однако они покрыты фиброзной капсулой, которая обильно снабжена нервными окончаниями. Когда почки увеличиваются в размерах, растягивается и капсула, которая их покрывает. Именно растяжение фиброзной капсулы провоцирует болевые ощущения. Второй механизм развития боли – это сдавливание нервно-сосудистых окончаний, увеличенной в объеме тканью почки.
Эти симптомы являются следствием синдрома общей интоксикации. Гломерулонефрит – это аутоиммунное заболевание, которое кроме почек вовлекает и другие органы и системы организма. Вовлечение в патологический процесс отдельных систем приводит к слабости и недомоганию. Также причиной этих симптомов может являться повышенная температура, которая всегда сопровождает острые процессы в почках.
Тяжелым и трудно поддающимся лечению симптомом гломерулонефрита является артериальная гипертензия (повышенное артериальное давление ). При этом систолическое давление повышается более 120 миллиметров ртутного столба, а диастолическое — более 80. Патогенез (механизм развития ) артериальной гипертензии при гломерулонефрите является очень сложным и включает в себя несколько механизмов.
Задержка в организме натрия и воды являются первыми механизмами, которые включаются при плохой работе почек. В норме почки выводят излишки натрия из плазмы крови путем его секреции с мочой. Однако при гломерулонефрите, когда нарушены функции фильтрации и секреции, этого не происходит. Следствием этого является задержка натрия в организме. В то же время, натрий задерживается не один, а затягивает с собой и воду.
Другой механизм развития артериальной гипертензии заключается в активации ренин-ангиотензиновой системы. Активация этой системы происходит вследствие гипоперфузии (снижения кровоснабжения ) почек. Из-за недостаточного кровоснабжения активируется каскад реакций, в результате которых происходит высвобождение ренина. Это гормонально активное вещество, которое, в свою очередь, приводит к превращению ангиотензина I в ангиотензин II. Последний приводит к секреции гормона альдостерона, который увеличивает обратное всасывание натрия (реабсорбцию ). Таким образом, формируется замкнутый круг — активация различных механизмов, так или иначе, приводит к задержке натрия и воды. С другой стороны на повышенное артериальное давление оказывает влияние снижение синтеза простагландинов. В норме эти вещества регулируют сосудистый тонус, препятствуя сужению просвета сосудов. Когда же простагландинов секретируется недостаточно, сосуды сужаются, что создает дополнительную нагрузку к повышенному артериальному давлению. Суженные сосуды и повышенный объем циркулирующей крови являются основной причиной повышенного артериального давления.
В основе развития одышки, как и в основе развития артериальной гипертензии, лежит задержка натрия и воды. Вода задерживается в тканях, создавая, тем самым, отеки. До определенного времени жидкость задерживается только в тканях. Однако вскоре она начинается переходить в полости и заполнять их. Так, лишняя жидкость организма накапливается в плевральной полости, в полости перикарда, в брюшной полости и так далее. Это, в свою очередь, провоцирует другие симптомы. Например, накапливаясь в полости перикарда, жидкость сжимает сердце, становясь причиной одышки и брадикардии (медленного сердцебиения ). Одышку также провоцирует скопление жидкости в легких. что является причиной венозного застоя в малом кругу кровообращения. Так, развиваются элементы нефрогенного (почечного ) отека легких. Выпот жидкости в брюшную полость приводит к развитию асцита. в народе – водянки .
Однако, первым по значимости механизмом появления отеков является протеинурия. Потеря белков организмом ведет к выходу жидкости из кровеносного русла и пропитыванию тканей этой жидкостью (то есть к формированию отеков ). В норме альбумины (белки с высокой молекулярной массой ) крови удерживают в сосудах жидкость. Но при гломерулонефрите происходит массивная потеря этих белков с мочой, вследствие чего их концентрация в сыворотке крови падает. Чем меньше альбуминов остается в крови, тем больше жидкости переходит из кровеносного русла в ткани, и тем массивнее отеки.
Гломерулонефрит проявляется не только внешними признаками, но и отклонениями со стороны анализа крови и анализа мочи. И если изменения со стороны крови пациент не может определить, то некоторые отклонения в анализе мочи видны невооруженным глазом.
Лабораторные признаки гломерулонефрита
источник