Гломерулонефрит – инфекционно-аллергическое заболевание, относящееся к группе приобретенных заболеваний почек. Различные формы гломерулонефрита различаются по этиологии, проявлениям, течению болезни и ее исходу. Чаще всего характеризуется иммунным воспалением почечных клубочков, а также дальнейшим, вторичным воспалением канальцев почек и интерстицией.
Различают острый гломерулонефрит, быстротекущую форму болезни, и хронический гломерулонефрит. Острая форма заболевания наиболее часто может быть вызвана перенесенной ранее стрептококковой инфекцией – постстрептококковый гломерулонефрит. По этиологии различают первичные гломерулонефриты и вторичные, которые возникают при системных заболеваниях – системной красной волчанке, ревматизме, узелковом периартериите и других.
Причинами заболевания являются перенесенные ранее инфекции – стрептококковая, стафилококковая и иные бактериальные инфекции. В некоторых случаях этиологическим фактором в развитии заболевания могут выступать гепатиты В и С, и возможно цитомегаловирусная инфекция. Гломерулонефрит может развиваться на фоне заболеваний паразитарной природы, под токсическим воздействием некоторых лекарств, при употреблении алкоголя и наркотиков, особенно сильное влияние эти привычки имеют в подростковом возрасте. Нарушение в календарном планировании плановых профилактических прививок также может способствовать возникновению болезни. Поэтому профилактика гломерулонефрита должна содержать точное соблюдение плановых прививок и медосмотров.
Развитие гломерулонефрита происходит на фоне реакций клеточного и гуморального иммунитета. Как правило, перенесенное ранее инфекционное заболевание, вызывает в организме иммунную реакцию, образуются иммунные комплексы. Выработанные для этого антитела разносятся током крови по всем системам, поражая чувствительные к ним органы. Это могут быть сердечная мышца, возникает ревматическая болезнь сердца, суставы – ревматизм, или как в данном случае клубочки почек — острый гломерулонефрит.
У детей заболевание приводит к почечной недостаточности и как следствие инвалидности. Постстрептококковый гломерулонефрит в отличие от других форм заболевания чаще встречается у детей в возрасте 5-12 лет, так же наблюдается развитие болезни у подростков и молодых людей. Острая форма болезни может развиться в любом возрасте, реже заболевание встречается после 40 лет.

Клиническая картина заболевания неоднозначна. Течение болезни может проходить в циклической форме с бурным развитием и многими симптомами, а может быть и в латентной, то есть стертой скрытой форме. Часто диагностика гломерулонефрита при латентной форме течения болезни происходит несвоевременно, что дает возможность болезни перейти в хроническую.
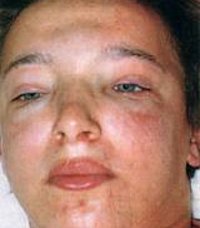
Характерные клинические симптомы гломерулонефрита это наличие крови при мочеиспускании и отеки на лице. Гематурия может быть незначительной и обнаружить этот симптом можно только с помощью анализа мочи. Но чаще моча имеет красно-бурый цвет. Отечность также не всегда заметна это либо мешки под глазами и заметное сужение глаз, либо резкое повышение массы тела на 3-4 килограмма.
Снижение количества мочи, так называемая олигурия может продолжаться до 5 дней, потом выделение мочи нормализуется, но наблюдается сниженная плотность мочи. Также для острого гломерулонефрита характерно повышение артериального давления, которое может продолжаться в течение нескольких недель.
При положительном прогнозе основные симптомы гломерулонефрита исчезают в течение первого месяца, а выздоровление происходит за 2-2,5. В случаях поздней диагностики, или если болезнь не поддается лечению в течение года, заболевание переходит в тяжелую хроническую форму.
Гломерулонефрит у детей зачастую развивается в острой форме. Более подвержены заболеванию дети старшего дошкольного и младшего школьного возраста. Груднички практически не болеют гломерулонефритом. Течение болезни крайне бурное с критическими повышениями температуры тела.
Хронический гломерулонефрит различают на четыре клинические формы. При любом течении характерны периоды ремиссии, которые сменяются обострениями схожими с острой формой болезни. Обострения могут быть сезонными, а также возникающие при повторном заражении инфекционными заболеваниями стрептококковой природы.
Некротическая форма гломерулонефрита характеризуется генерализоваными отеками, возможно, их развитие до асцита и анасарки. При лабораторных исследованиях обнаруживается повышение белка в моче и его снижение в крови. При этом повышается уровень липидов и глобулинов, снижается уровень альбуминов.
Гипертоническая форма болезни не включает такие ярко выраженные симптомы гломерулонефрита как некротическая, для этой формы характерна гипертензия. Возможна и смешанная форма течения хронического гломерулонефрита. В этом случае симптомы обеих форм присутствуют одновременно.
Также как и острый гломерулонефрит хронический может протекать практически бессимптомно. Латентная форма характеризуется лишь слабым нарушением выделения мочи.
Назначается рентгенконтрасное исследование и ряд лабораторных анализов, что бы исключить наличие других почечных заболеваний. Так дифференциальная диагностика гломерулонефрита должна исключить обострения нефритов, в том числе наследственной формы, туберкулёза почек, нефролитиаза. Диагностика гломерулонефрита включает также данные ранее перенесенных заболеваний, длительное наблюдение за состоянием пациента, консультации окулиста. При гломерулонефрите происходят изменения глазного дна. При крайне бурном течении болезни проводят исследование тканей – биотапта почки.
При лабораторных исследованиях мочи наличие гематурии или цилиндрурии является подтверждением диагноза. В первые дни течения болезни в анализе мочи обнаруживаются лимфоциты. Они являются отражением иммунного процесса в клубочках почек.
Анализ крови выявляет нейрофильный лейкоцитоз, анемию, увеличение СОЭ. Данные показывают сниженную клубочковую фильтрацию, увеличение азотистых шлаков в крови. Обнаруживаются нарушения системы свертываемости крови. Это чаще всего представлено продуктами деградации фибрина, а также фибриногена в сыворотке крови и моче.
При подтверждении диагноза больного следует госпитализировать. Лечение гломерулонефрита в стационаре требует постельного режима, пациенту требуется покой и тепло, что способствует нормализации кровообращения в почках и снижению артериального давления. Назначается диета с дозированным приемом жидкости для купирования отеков. В первые дни режим питания строго контролируется, исключается наличие соли в пище, ее употребление постепенно возобновляется после исчезновения отеков. Также исключают блюда с богатым содержанием калия, экстрактивных веществ, аллергенов.
Медикаментозное лечение гломерулонефрита включает антибактериальную терапию, чаще всего назначаются антибиотики пенициллинового ряда курсом 1.5-2 месяца. Рекомендовано назначение гепарина подкожно курсом 2-4 недели. Препарат предотвращает внутрисосудистое свёртывание крови. Если симптомы гломерулонефрита включают артериальную гипертензию назначаются ингибиторы АПФ, внутривенные вливания аминофиллина в растворе глюкозы и последующую инфузию фуросемида. Допустимо применение клофелина, метилдопа.
Прогноз лечения гломерулонефрита чаще всего благоприятный. 85-90% пациентов выздоравливают полностью, у остальных больных сохраняются изменения мочи, что не дает возможности говорить о полном выздоровлении. При длительном лечении заболевания возможен переход в хроническую форму с признаками некротического синдрома. Летальный исход регистрируют редко, чаще всего при несвоевременном обнаружении латентной формы течения болезни.
источник
Острый гломерулонефрит – это заболевание иммуновоспалительного характера, характеризующееся вовлечением структурных единиц почек – нефронов и преимущественным поражением клубочкового аппарата. Патология протекает с развитием экстраренальных синдромов (отечного и гипертонического) и ренальных проявлений (мочевого синдрома). В диагностике применяется исследование мочи (общий анализ, проба Реберга, Зимницкого, Нечипоренко), УЗИ почек, биохимическое и иммунологическое исследование крови, биопсия почечной ткани. Лечение требует соблюдения постельного режима и диеты, назначения стероидных гормонов, гипотензивных, диуретических средств.
Острый гломерулонефрит развивается преимущественно у детей в возрасте 2-12 лет и взрослых до 40 лет. Мужчины заболевают в 15,2 раза чаще, чем женщины. Пик заболеваемости приходится на влажное и холодное время года. При болезни происходит преимущественное поражение клубочков (почечных телец), кроме этого в патологический процесс вовлекаются канальца и межуточная ткань обеих почек. Поражение почек связано со специфической иммунной реакцией, обусловленной инфекционным или аллергическим процессом.
В большинстве случаев развитие острого гломерулонефрита сопряжено с перенесенной стрептококковой инфекцией – фарингитом, ангиной, обострением тонзиллита, скарлатиной, рожистым воспалением кожи. Этиологическим агентом в этих случаях, как правило, выступает b-гемолитический стрептококк группы А. О стрептококковой этиологии острого гломерулонефрита свидетельствует определение повышенного титра антител к стрептококковой гиалуронидазе и стрептолизину-О, увеличение ЦИК, содержащих антигены к стрептококку.
Иногда развитию болезни предшествует вирусная инфекция – грипп, эпидемический паротит, ветряная оспа, краснуха, инфекционный мононуклеоз, герпес, гепатит. Реже патология возникает после дифтерии, стафилококковых и пневмококковых пневмоний, малярии, бруцеллеза, инфекционного эндокардита, брюшного и сыпного тифа и других инфекций.
Кроме инфекционно-иммунных острых гломерулонефритов встречаются неинфекционно-иммунные формы заболевания, вызванные введением сывороток и вакцин, индивидуальной непереносимостью пыльцы растений, приемом нефротоксичных лекарственных препаратов, укусом насекомых или змей, алкогольной интоксикацией и др. причинами. Предрасполагающими факторами служат переохлаждение, анатомо-физиологическая незавершенность строения нефронов у детей.
Специалисты в сфере современной урологии придерживаются мнения, что острый гломерулонефрит — это иммунокомплексная патология. После инфекционного или аллергического воздействия происходит изменение реактивности организма, что проявляется образованием антител к чужеродным антигенам. Взаимодействуя с комплементом, иммунные комплексы откладываются на поверхностях базальных мембран капилляров клубочков. Изменяется структура капиллярных стенок, увеличивается проницаемость сосудов, создаются условия для тромбообразования.
Расстройство трофики почечной ткани ведет к тому, что в ишемической почке активизируется функция ренин-ангиотензин-альдостероновой системы, что приводит к спазму периферических сосудов и, как следствие, повышению АД. На этом фоне нарушаются процессы фильтрации и реабсорбции, происходит задержка Na и воды, в моче появляются патологические элементы.
По вызывающим поражение причинам различают первичный, идиопатический и вторичный гломерулонефрит. Первичный гломерулонефрит связан с инфекционным, аллергическим или токсическим воздействием на почечную ткань; вторичный – служит проявлением системной патологии (геморрагического васкулита, СКВ и др.); идиопатический гломерулонефрит развивается по неопределенным причинам. В зависимости от этиофакторов гломерулонефриты могут быть инфекционно-иммунными и неинфекционно–иммунными.
В зависимости от объема поражения клубочкового аппарата различают очаговую (поражено
источник
Опросите больного с острым гломерулонефритом и выявите жалобы на:
§ отеки, особенно на лице по утрам;
§ уменьшение количества отделяемой мочи за сутки (олигурию), кровавую мочу (цвета «мясных помоев», кроваво-бурую);
§ головные боли, головокружение, нарушение зрения, одышку смешанного характера, сердцебиение, обусловленные артериальной гипертонией;
§ боли в поясничной области, которые бывают в 1/3 случаев, двусторонние, неинтенсивные, без иррадиации, обусловлены растяжением почечной капсулы увеличивающимися почками.
Соберите анамнез у больного острым гломерулонефритом.
Для острого гломерулонефрита характерно острое начало после острых инфекционных заболеваний. Чаще это ангина, обострение хронического тонзиллита, несколько реже ОРЗ, отиты, синуситы, скарлатина, гнойничковые поражения кожи. Ведущая роль в возникновении острого гломерулонефрита принадлежит стрептококку, особенно β-гемолитичес-кому стрептококку группы А, 4 и 12 типов. Кроме стрептококковой инфекции развитию острого гломерулонефрита может предшествовать стафилококковая, пневмококковая инфекция, а в некоторых случаях и вирусная инфекция (пневмония, паротит, краснуха, ветряная оспа, инфекционный мононуклеоз).
Между вспышкой инфекции и появлениями первых симптомов острого гломерулонефрита проходит 10-20 дней, в течение которых в результате аутоиммунных процессов образуются комплексы антиген-антитело, фиксирующиеся на базальных мембранах эндотелия капилляров клубочков, вызывая их повреждение.
Продолжительность острого гломерулонефрита 1-4 месяца. В 70% случаев наступает выздоровление, если же симптомы гломерулонефрита не исчезают в течение 12 месяцев и более, то это является критерием перехода в хроническую форму.
Кроме классического течения с бурным началом, наличием отеков, артериальной гипертензией, изменениями в моче возможна латентная форма – с постепенным началом без выраженных клинических проявлений, которая выявляется только по изменениям мочи.
Проведите общий осмотр больного.
Состояние больного — может быть тяжелым, средней тяжести и даже удовлетворительным.
Сознание – обычно сохранено даже при тяжелом течении, исключение составляют случаи, протекающие с отеком мозга.
Отеки – являются одним из наиболее ранних и частых признаков острого гломерулонефрита. Они обычно больше выражены по утрам, локализуются на лице (facies nefritica), особенно на веках, под глазами, нередки отеки нижних конечностей, крестца. При большой задержке жидкости возможен отек наружных половых органов и появляется жидкость в полостях (асцит, гидроторакс). К вечеру отеки мене выражены. Эти отеки бледные.
Основной причиной отеков при остром гломерулонефрите является поражение почечных клубочков, ведущее к уменьшению фильтрации воды и задержке ее в организме, то есть развивается гиперволемия, повышается гидростатическое давление в сосудистом русле. Наряду с этим имеет значение повышение реабсорбции натрия в почечных канальцах, обусловленное гиперальдостеронизмом, повышение проницаемости капилляров вследствие увеличения содержания гиалуронидазы.
Выявите симптомы острого гломерулонефрита при обследовании сердечно-сосудистой системы.
Одним из ведущих синдромов гломерулонефрита является артериальная гипертония, что обусловливает все изменения со стороны сердечно-сосудистой системы.
Степень повышения артериального давления соответствует тяжести острого гломерулонефрита. Обычно систолическое артериальное давление (САД) повышается до 140-160 мм рт.ст., диастолическое (ДАД)– до 90-110 мм рт.ст., но возможен и более высокий уровень: САД до 200 мм рт.ст, ДАД до 130 мм рт.ст.
Ведущее значение в возникновении артериальной гипертонии имеет увеличение объема циркулирующей крови вследствие гиперволемии, что связано со снижением фильтрационной способности почек, задержкой воды и натрия. Увеличение объема циркулирующей крови приводит к увеличению ударного объема сердца и подъему САД.
Если вступает в действие механизм ренин-ангиотензин, ренин-альдостерон вследствие гиперемии юкстагломерулярного аппарата, то повышается ОПС и ДАД, причем повышение будет стойким.
При исследовании сердца определяется его расширение влево за счет дилатации левого желудочка, обусловленной остро возникшим увеличением массы крови.
При пальпации — верхушечный толчок смещен влево, разлитой, несильный, нерезистентный.
При перкуссии – смещение левой границы относительной тупости сердца влево.
При аускультации – тоны сердца приглушены, если есть гидроперикард – ослаблен 1 тон на верхушке вследствие отека, миокардиодистрофии, акцент 2 тона на аорте (артериальная гипертония), возможен систолический шум на верхушке при возникновении относительной недостаточности митрального клапана, при выраженных поражениях миокарда выслушивается диастолический ритм галопа, экстрасистолия. Определяется брадикардия – раздражение барорецепторов каротидного синуса вследствие повышенного артериального давления. Появление тахикардии у больных острым гломерулонефритом говорит о сердечной недостаточности.
У больного с острым гломерулонефритом может развиться острая левожелудочковая недостаточность в виде сердечной астмы, застойного кашля, влажных хрипов в легких, в тяжелых случаях – отека легких. Это возникает вследствие быстро развивающейся артериальной гипертонии, нарушения питания сердца из-за сужения коронарных артерий.
Проведите пальпацию почек:
При остром гломерулонефрите почки не пальпируются, болезненность не типична.
При физическом исследовании определяется олигурия до 500 мл в сутки из-за уменьшения фильтрации, высокая относительная плотность мочи (более 1020) – гиперстенурия, цвет «мясных помоев» или красно-бурый вследствие макрогематурии (происходит проникновение эритроцитов в мочу через пораженную стенку капилляров клубочков).
При биохимическом исследовании определяется протеинурия, которая наряду с гематурией относится к обязательным классическим изменениям мочи при остром гломерулонефрите. Величина протеинурии обычно 1-10 г/л, но в первые дни заболевания может достигать 40-90 г/л. Высокое содержание белка в моче отмечается первые 7-10 дней, в дальнейшем протеинурия невысокая, около 1 г/л, но держится долго, порой до 12 месяцев. Механизм протеинурии тот же, что и гематурии.
При микроскопическом исследовании осадка мочи отмечается:
§ гематурия – обязательный, постоянный признак, в 13-15% случаях бывает макрогематурия, в остальных случаях микрогематурия от 4-5 до 50-60 эритроцитов в поле зрения, эритроциты преимущественно выщелоченные;
§ лейкоцитурия может быть, но не более 10-15 в поле зрения (асептическая);
§ цилиндрурия – необязательный симптом острого гломерулонефрита. В 75% случаев находят единичные гиалиновые и зернистые цилиндры до 10-20 в поле зрения.
2. Анализ мочи по Нечипоренко – определяется значительное повышение количества измененных эритроцитов, количество лейкоцитов и цилиндров остается нормальным или незначительно повышается.
3. Бактериологическое исследование мочи (посев) – бактериурия отсутствует.
Оцените функциональные пробы почек.
1. Проба по Зимницкому: выявляется олигурия, повышение плотности мочи во всех порциях.
2. Проба Реберга: определяется снижение фильтрации ниже 65 мл/мин, реабсорбция остается нормальной.
Оцените клинический и биохимический анализы крови.
1. Клинический анализ крови: часто выявляется умеренная нормохромная анемия, обусловленная снижением гемопоэтической функции почек, умеренный нейтрофильный лейкоцитоз с незначительным сдвигом влево, преходящая эозинофилия, ускорение СОЭ.
2. Биохимический анализ крови: уровень креатинина, мочевины, мочевой кислоты обычно остается неизмененным.
Увеличивается содержание в сыворотке крови a2— и g-глобулинов на фоне умеренной гипопротеинемии.
§ при артериальной гипертонии будут отмечаться признаки гипертрофии левого желудочка;
§ при развитии гидроперикарда – снижение вольтажа всех зубцов;
§ при гидротораксе – нагрузка на правые отделы сердца.
Оцените рентгенограммы грудной клетки.
§ при исследовании сердца может выявляться увеличение левого желудочка за счет его гипертрофии и дилатации, при развитии гидроперикарда – увеличение размеров сердечной талии;
§ при исследовании легких может выявляться застой в корнях легких при выраженном отечном синдроме или сердечной недостаточности, при наличии гидроторакса – жидкость в плевральных полостях.
Оцените данные изотопного и ультразвукового методов исследования.
§ при изотопном исследовании почек на ренограммах выявляется симметричное снижение секреции, при сцинтиграфии – диффузное уменьшение функционально активной ткани;
§ при ультразвуковом исследовании почек выявляется двухстороннее диффузное изменение структуры почечной ткани, размеры почек нормальные или несколько увеличены.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Увлечёшься девушкой-вырастут хвосты, займёшься учебой-вырастут рога 9517 — 

193.124.117.139 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
Острый гломерулонефрит — это воспалительное заболевание потек с иммунным компонентом, характеризующееся вовлечением в патологический процесс преимущественно клубочкового аппарата, а затем и других структур почек.
Чаще страдают лица до 40 лет.
Развивается после перенесенной стрептококковой инфекции (ангины, тонзиллита, инфекции верхних дыхательных путей, скарлатины, гнойного отита и др.), а также пневмонии, дифтерии, бруцеллеза, малярии, вирусных инфекций, после введения вакцин и сывороток. Основную этиологическую роль играет бета-гемолитический стрептококк группы А. Провоцирующим фактором может являться переохлаждение организма, особенно во влажной среде.
Возможно развитие заболевания вследствие индивидуальной непереносимости некоторых лекарственных веществ, химикатов, пыльцы растений, змеиного яда и др. Определенную роль играет наследственная предрасположенность.
В основе патогенеза острого гломерулонефрита лежит отложение в капиллярах почечных клубочков иммунных комплексов, образованных в результате взаимодействия антигена, циркулирующего в крови, со специфическим антителом. Наиболее часто иммунные комплексы откладываются под эпителием на базальной мембране капилляров клубочков и в мезангиальной зоне, вызывая иммунное воспаление — васкулит. Симптомы заболевания обычно появляются через 1-3 недели после перенесенной инфекции.
Характерны боли в поясничной области, чаще с обеих сторон, повышение температуры тела, уменьшение количества мочи (олигурия) до 400-700 мл в сутки, слабость, головная боль, тошнота, рвота. В некоторых случаях моча приобретает красноватый цвет или вид мясных помоев. В тяжелых случаях в течение нескольких дней возможна анурия с развитием острой почечной недостаточности.
Появляется отечный синдром с характерным внешним видом больного — «лицо нефритика» (бледные отеки преимущественно в области век, лица, появляются утром, уменьшаются к вечеру). В тяжелых случаях возможно появление массивных отеков (вплоть до асцита, гидроперикарда, гидроторакса). У некоторых больных, несмотря на отсутствие отеков, отмечается ежедневная прибавка массы тела, что свидетельствует о задержке жидкости в организме. Отеки обычно исчезают через 2-3 недели.
Одним из частых проявлений острого гломерулонефрита является повышение АД. Обычно АД не достигает высоких цифр, поднимается до 180/120 мм рт.ст. Артериальная гипертензия может осложняться острой левожелудочковой недостаточностью с развитием сердечной астмы и отека легкого, позднее — гипертрофией левого желудочка, а также эклампсией с возникновением припадков. Эклампсия развивается в результате отека головного мозга, проявляется судорогами мышц конечностей с потерей сознания, цианозом лица, шумным дыханием, ригидностью мышц.
Основные формы острого гломерулонефрита:
1) острая циклическая форма — характерно бурное начало, быстрое развитие выраженной симптоматики; обычно заболевание заканчивается выздоровлением;
2) затяжная форма — характерно постепенное нарастание симптомов; длительность заболевания обычно от 6 месяцев до 1 года.
Острый гломерулонефрит может сопровождаться нефротическим синдромом (массивная протеинурия, гипопротеинемия, диспротеинемия, гиперлипидемия в сочетании с отеками). Возможен переход острой формы гломерулонефрита в хроническую, а также в подострую быстропрогрессирующую.
Острая сердечная недостаточность, острая почечная недостаточность, эклампсия, кровоизлияние в головной мозг, острые нарушения зрения.
ОАМ — повышение удельного веса, высокая протеинурия (от 1 до 10 г/л, но нередко достигающая 20 г/л и более), обычно выявляемая в первые 7-10 дней от начала заболевания, затем уменьшающаяся до 1 г/л и менее; макро- или микрогематурия, иногда — цилиндрурия, лейкоцитурия.
При пробе Реберга выявляется снижение клубочковой фильтрации.
ОАК — уменьшение содержания гемоглобина и эритроцитов, лейкоцитоз, ускорение СОЭ, в БАК — азотемия (повышение уровня креатинина, мочевины), повышение уровня фибриногена, при нефротическом синдроме — гипопротеинемия, гипоальбуминемия, гиперлипидемия.
Иммунологический анализ крови показывает повышение содержания иммуноглобулинов, появление ЦИК, высокий титр антител к антигенам стрептококка.
УЗИ почек позволяет оценить состояние паренхимы органа.
При сердечно-сосудистых осложнениях на ЭКГ определяются диффузные изменения миокарда, изменение зубцов Т в стандартных отведениях, глубокий зубец Q, снижение вольтажа комплекса QRS.
На глазном дне — сужение артериол, иногда — отек зрительного нерва, точечные кровоизлияния.
Биопсия почки позволяет морфологически верифицировать диагноз.
Строгий постельный режим, избегание переохлаждений.
В первые дни в питании резко ограничивается поваренная соль или рекомендуется бессолевая диета, резко ограничиваются белки, полностью исключаются пряности и раздражающие продукты. В дальнейшем после свертывания клинической картины диету можно постепенно расширять за счет увеличения белкового компонента, поваренной соли (около 2,5г в сутки). Количество употребляемой жидкости рассчитывают с учетом диуреза (к количеству выделенной жидкости прибавляют 400 мл).
оксациллин внутримышечно по 0,5г 4 раза в сутки;
эритромицин по 0,25г 4 раза в сутки и др.
Применение антибиотиков целесообразно при очевидной связи развития заболевания с перенесенной стрептококковой инфекцией.
В качестве иммунодепрессивной терапии при отсутствии артериальной гипертензии, затянувшемся течении заболевания, а также развитии острой почечной недостаточности назначают глюкокортикостероиды: преднизолон в дозе 1мг на 1кг массы тела в течение 1,5-2 месяцев с постепенным снижением дозы. При чрезвычайно высокой активности процесса проводится пульс-терапия метилпреднизолоном.
При неэффективности глюкокортикостероидов применяют цитостатики:
азатиоприн по 2-3 мг на 1кг массы тела;
циклофосфамид по 1,5-2 мг на 1кг массы тела.
Цитостатики принимают в течение 6-8 недель (иногда более длительно), а затем дозу уменьшают до поддерживающей.
В некоторых случаях показана комбинированная терапия преднизолоном и цитостатиками.
Для улучшения микроциркуляции в капиллярах клубочков показаны антиагреганты и антикоагулянты:
1) гепарин по 5000-10000 ЕД подкожно каждые 4-6 часов в течение 6-8 недель;
2) курантил 225-400 мг в сутки в течение 6-8 недель, а затем в поддерживающей дозе 50-75 мг в сутки длительно;
3) трентал 0,2-0,3 г в сутки в 3 приема.
Симптоматическое лечение подразумевает лечение артериальной гипертензии. Назначаются:
ингибиторы АПФ (капотен 25-100 мг в сутки);
антагонисты кальциевых рецепторов (верапамил 80-360 мг в сутки).
Для лечения отечного синдрома рекомендуется ограничение потребления жидкости, назначение мочегонных средств:
гипотиазид 50-100 мг в сутки;
фуросемид 40-80мг в сутки (при необходимости можно увеличить дозировку);
верошпирон 75-200 мг в сутки.
Возможно сочетание нескольких препаратов.
При выраженной упорной гематурии, не поддающейся коррекции с помощью основной терапии, показаны:
1) аминокапроновая кислота внутрь по 3г каждые 6 ч или внутривенно капельно 150 мг 5%-ного раствора; курс — 4-7 дней;
2) дицинон внутримышечно по 2 мл 12,5%-ного раствора 2 раза в день.
Лечение острой сердечной недостаточности — см. лекция 12 раздела L
При эклампсии необходимы экстренные реанимационные мероприятия.
Больным показано санаторное лечение не ранее чем через 6 месяцев от начала заболевания. Рекомендуется климатолечение: сухой жаркий воздух, минеральные воды.
Профилактические мероприятия предусматривают санацию хронических очагов инфекции в организме, устранение переохлаждений, отказ от вакцинаций у лиц с отягощенным аллергическим фоном.
источник
Острый гломерулонефрит — внезапно начавшееся заболевание почек, характеризующееся повреждением маленьких кровеносных сосудов клубочкового аппарата. В результате воспаления происходит недостаточная фильтрация отходов и избыток жидкости в организме, что приводит к появлению крови и белка в моче, отекам лица и лодыжек, повышению артериального давления. При несвоевременном обращении за медицинской помощью заболевание может развиться в хроническою почечную недостаточность.
Острый гломерулонефрит обычно встречается у мужчин до 40 лет, пожилых людей и детей в возрасте от 5 до 12 лет. Наиболее распространенными причинами заболевания являются бактериальные инфекции, возникающие в результате заражения организма стрептококками бета-гемолитической группы A: фарингит, отит, синусит, пиодермии, скарлатина, пневмония. В некоторых случаях острый гломерулонефрит возникает после перенесенной вирусной инфекции.
Согласно данным государственной статистики, уровень распространенности гломерулонефрита на территории России начиная с 2000 года постепенно растет и на 2010 год составляет примерно 10 заболевших человек на 10 000 населения. По данным обращаемости при гломерулонефрите преобладают мужчины, средний возраст пациентов составляет 40 лет. В таблице приведены данные о распространенности заболеваний органов мочеполовой системы в России за 2006-2010 гг. (на 10 тыс. населения):
| Заболевания почек | Распространенность, % |
| Гломерулонефриты | 12,7 |
| Тубулоинтерстициальные нефриты | 94 |
| Острая почечная недостаточность | 0,14 |
| Хроническая почечная недостаточность | 9,9 |
| Мочекаменная болезнь | 54,1 |
| Диабетическая нефропатия | 10 |
| Амилоидоз почек | 0,4 |
| Волчаночный нефрит | 0,34 |
| Гипертоническая нефропатия | 1,7 |
Наиболее частыми встречающимися причинами развития острого гломерулонефрита являются бактериальные и вирусные инфекции. Причем в первом случае заболевание возникает в результате заражения организма стрептококками бета-гемолитический группы A: фарингит, отит, синусит, пиодермии, скарлатина, пневмония. Во втором случае причиной может стать ветряная оспа. Воспалительные заболевания печени, сахарный диабет, СПИД и аутоиммунные заболевания, такие как волчанка, повышают риск развития гломерулонефрита.
Длительное применение некоторых лекарственных средств в числе которых находятся нестероидные противовоспалительные препараты (ибупрофен или аспирин) также увеличивает риск развития заболевания.
Почечные клубочки — шарообразные структуры, являющиеся частью нефрона. Нефрон в свою очередь состоит из одного такого клубочка и системы канальцев, в которых осуществляется обратное всасывание и выделение веществ. Именно здесь образуется первичная и вторичная моча, которая после полной фильтрации поступает в мочевой пузырь и через мочеточник выводится из организма через мочеиспускательный канал.
При заражении организма стрептококками бета-гемолитической группы A происходит формирование иммунных комплексов, которые застревают в почечном клубочке, вызывая воспалительную реакцию. В результате нарушается фильтрация крови, происходит задержка воды, в моче появляется кровь и белок. Организм сталкивается с заболеванием острый гломерулонефрит.
Одной из распространенных причин возникновения гломерулонефрита считается рубцевание клубочков, которое происходит при наличии сахарного диабета или волчанки у пациента. Поражение клубочка приводит к образованию белка в моче и в конечном итоге к почечной недостаточности.
Диабетическая нефропатия или диабетическая болезнь почек является основной причиной почечной недостаточности во многих странах мира. У любого человека с сахарным диабетом может развиться данное заболевание. Высокие уровни глюкозы увеличивают приток крови к почкам, повышая процесс фильтрации и артериальное давление. В результате капиллярам и клубочкам наносится существенный урон.
Уменьшить риск повреждения почек можно с помощью контроля питания и потребления глюкозы. Кровяное давление необходимо поддерживать на уровне 140/90 мм рт. ст.
Почки выполняют ряд жизненно важных функций в организме человека:
- производят фильтрацию отходов из крови посредством производства мочи, предотвращая накопление опасных вредных веществ в организме;
- регулируют концентрацию электролитов и минералов (натрия, кальция и калия), а также количество жидкости в организме;
- вырабатывают гормоны, которые контролируют другие функции организма: регуляцию артериального давления, поддержание костной массы и производство красных кровяных телец.
Учитывая важную роль почек в поддержании общего состояния здоровья, гломерулонефрит и почечная недостаточность вызывают довольно разнообразные симптомы, особенно при острой форме заболевания:
- отечность лица и лодыжек при пробуждении;
- красно-коричневая моча с содержанием крови;
- уменьшение суточного выделения мочи;
- высокое кровяное давление.
Несвоевременное обращение к врачу может усугубить ситуацию и спровоцировать возникновение хронической почечной недостаточности, при которой происходит неспособность почек удалять токсины и лишнюю жидкость из организма. При наличии хронической почечной недостаточности на поздней стадии могут возникнуть следующие симптомы:
- потеря способности к ясному мышлению;
- подергивание мышц или судороги;
- кожный зуд;
- одышка, усталость и головные боли;
- тошнота и рвота;
- желтовато-коричневый цвет кожи;
- потеря аппетита и веса;
- высокое кровяное давление;
- кровотечение из носа;
- опухшие руки, ноги и глаза.
Симптомы могут усилиться при отсутствии лечения, в результате может наступить кома.
Повреждение почек при гломерулонефрите происходит постепенно, первые симптомы проявляются через 3-4 недели после ангины и других бактериальных инфекций. В редких случаях заболевание обнаруживают случайно, в ходе анализа крови или мочи. Если при осмотре у врача возникает подозрение на гломерулонефрит, назначаются дополнительные обследования и лабораторные тесты:
- анализ крови;
- анализ мочи на уринолизис;
- УЗИ почек или брюшной полости;
- КТ почек или брюшной полости;
- рентгенография почек, мочеточников и мочевого пузыря;
- рентген грудной клетки (при подозрении на сердечную недостаточность);
- биопсия почек.
Анализ крови позволяют обнаружить скопление вредных веществ в крови (мочевины). Анализ мочи позволяет определить наличие белка или красных кровяных телец, которые при обычной ситуации должны там отсутствовать. Ультразвук и КТ показывают размер почек, которые могут увеличиться в объеме при гломерулонефрите и любых других нарушений, таких как опухоли или закупорки.
Биопсия почки может быть выполнена в случае окончательного подтверждения диагноза. При помощи ультразвука в почку вводится тонкая игла для взятия небольшого образца ткани, которую исследуют под микроскопом для выявления патологии или заболевания.
При острой форме гломерулонефрита задача доктора заключается в снижении вероятности возникновения симптомов заболевания и предотвращения дальнейшего повреждения почек. Если у пациента развивается гипертензия врач назначит прием антигипертензивных препаратов для снижения артериального давления. При наличии бактериальной инфекции назначается антибиотикотерапия, причем принимать лекарственные средства необходимо так, как это предписано специалистом, даже если симптомы инфекции исчезают через несколько дней лечения.
Кортикостероиды и иммунодепрессанты используются для подавления очагов воспаления, мочегонные средства помогают снизить гипертонию и нормализовать кровяное давление. Обычно рекомендуется принимать мочегонные утром или в обед, чтобы избежать необходимости вставать ночью для похода в туалет.
На основе результатов анализа крови врач может назначить прием витаминов или минералов для поддержания электролитного баланса. При остром гломерулонефрите придется сократить потребление жидкости и исключить из рациона напитки или пищевые продукты, содержащие алкоголь, высокие уровни белка, соли и калия. Диетические ограничения не требуются если повреждения почек незначительны.
В тяжелых случаях гломерулонефрита может потребоваться диализ — удаление из организма продуктов обмена веществ и лишней жидкости. Процедура полностью не вылечивает заболевание, поэтому после ее проведения пациент должен следовать специальной диете, ограничить потребление жидкости и принимать лекарства в соответствии с предписанием.
При необходимости врач может назначить пересадку почки. В настоящее время такие операции стали довольно распространенным явлением и в большинстве случаев заканчиваются успешно. После удачной пересадки пациент может вести нормальный, здоровый образ жизни.
Гломерулонефрит может привести к гипертонии, сердечно-сосудистой недостаточности, отекам легких и повреждению других органов. Без должного лечения у пациента может возникнуть терминальная стадия заболевания, при которой необходим регулярный диализ или пересадка почки, чтобы остаться в живых.
Большинство форм гломерулонефрита нельзя предотвратить, но существует несколько способов снижения риска:
- Посещение врача в случае возникновения ангины или импетиго.
- Контроль содержания сахара в крови и артериального давления.
- Практика безопасного секса, отказ от алкогольных напитков и наркотических средств.
Риск возникновения гломерулонефрита может быть снижен при соблюдении здорового образа жизни, выполнении регулярных спортивных упражнений, качественном сне и здоровом питании. Данные рекомендации также позволяют снизить риск инфекций и гипертонии.
источник
Асцит или водянка живота – заболевание, связанное со скоплением чрезмерного количества жидкости в брюшной полости, и возникающее в качестве осложнения какой-либо имеющейся в организме патологии. Причин развития данного заболевания может быть огромное количество. У взрослого человека асцит обычно сопровождает нефротический синдром, порок сердца, цирроз печени.
Возникновение асцита у ребенка чаще всего свидетельствует о наличии злокачественной опухоли или нефротического синдрома. В брюшной полости здорового человека происходит постоянное выделение небольшого количества жидкости, необходимой для нормального функционирования расположенных в данной области организма внутренних органов. Такая жидкость носит название экссудата и всасывается обратно самой брюшиной.
Мнение эксперта: Существует два вида жидкости: экссудат и транссудат, которые отличаются друг от друга содержанием белка. При асците может быть и тот и другой вид.
Нарушение функции выделения и всасывания жидкости, возникшее в результате какого-либо заболевания, приводит к развитию асцита.
Возникновению данной патологии подвержены люди всех возрастных категорий, даже новорожденные дети. Асцит у новорожденных обычно сопровождает гемолитическую болезнь – заболевание, при котором иммунные клетки организма матери начинают угнетать кровяные клетки организма ребенка, в результате чего у последнего развивается патологическое состояние в виде желтухи, отечности отдельных частей тела и т.п.
Еще одной распространенной причиной асцита у новорожденных детей является врожденный нефротический синдром – комплекс симптомов, развивающийся в результате поражения почек и сопровождающийся нарушением обмена белка, его чрезмерным выведением из организма, возникновением отеков разных частей тела.
Практически все заболевания, поражающие брюшную полость (перитонит, глистная инвазия, псевдомиксома, злокачественные новообразования толстого кишечника, желудка, яичников, эндометрия, молочной железы), также сопровождаются развитием асцита. Нередко встречается сочетание плеврита. водянки живота и перикардита при уремии, ревматизме, системной красной волчанке.
Асцит развивается при саркоидозе, непроходимости печеночных вен, гипернефроме, хроническом гломерулонефрите, панкреатите, лимфостазе, хронической диарее. В основе развития асцита лежит комплекс гидростатических, воспалительных, метаболических, гемодинамических нарушений, приводящих к скоплению экссудата в брюшной полости.
Основным симптомом асцита является резкое увеличение живота в объеме, возникновение в нем дискомфорта и болей. Общие признаки заболевания таковы:
Люди, больные асцитом, обычно очень быстро наедаются, иногда возможен полный отказ от приема пищи. При этом независимо от ежедневного рациона питания живот продолжает увеличиваться в размерах. У мужчин часто наблюдается отек половых органов и нижних конечностей.
В зависимости от того, какое заболевание повлекло за собой накопление жидкости в брюшной полости, асцит может развиваться очень медленно или, наоборот, стремительно. Иногда при медленном развитии заболевания человек ошибочно принимает увеличение живота за признак ожирения и начинает бороться с излишним весом. Однако все методы этой борьбы оказываются напрасными.
По мере увеличения живота у больного выпячивается пупок (как на поздних сроках беременности), развивается паховая или пупочная грыжа. В случае сочетания туберкулеза и асцита наблюдается медленное похудение человека, при этом быстро увеличивающийся в размерах живот становится еще более заметным. При сочетании асцита с почечной недостаточностью наблюдается стойкий отек кожных покровов.
Количество жидкости, которая может скопиться в животе больного при развитии асцита, может быть различным: от 3 до 10 литров. Редко встречаются случаи, когда количество экссудата в брюшной полости больного достигает 20 литров. Обычно такая жидкость имеет бело-молочный цвет, при проведении лабораторного анализа в ней обнаруживается большое количество липоидов и жиров.
Асцит необходимо диагностировать от опухолей внутренних органов брюшной полости, беременности, кисты яичника, ожирения. Основными методами диагностики данного заболевания является ультразвуковое исследование брюшной полости, мультиспиральная компьютерная томография органов брюшной полости, лапароскопия с последующим забором жидкости, лабораторное исследование экссудата, анализ мочи.
Лечение асцита начинается с устранения основного заболевания. Если основная патология требует длительной терапии (например, злокачественная опухоль), параллельно назначается прием мочегонных препаратов (амилорид, спиронолактон), действие которых направлено на коррекцию водно-соляного обмена в организме. Лечится заболевание обычно в домашних условиях с обязательным поседением специалиста. Всем больным прописан постельный режим и специальная диета, подразумевающая отказ от употребления соли.
Мнение эксперта: В большинстве случаев остро возникший асцит лечится в стационаре. Асцит хронический может вестись и амбулаторно. Мочегонные же средства назначаются для улучшения и увеличения выведения избытка жидкости из организма.
В тех случаях, когда медикаментозное лечение не оказывает положительного результата либо скопление жидкости слишком велико, проводится хирургическое вмешательство – пункция брюшной полости. Перед началом процедуры больному следует полностью опорожнить мочевой пузырь. В момент проведения операции пациент находится в сидячем положении (либо лежит на боку). Пункция или прокол при помощи специального инструмента – троакара проводится по средней линии живота (между лобком и пупком) после введения больному анестезирующего средства. Жидкость из брюшной полости выводится, как правило, медленно и не более 5 литров за один раз. Частое повторение операции может привести к таким нежелательным последствиям, как воспаление брюшной полости и сращение кишок.
Прогноз лечения полностью зависит от течения основного заболевания. Чем больше пункций требуется провести, тем более он неблагоприятен.
Гломерулонефрит – это двустороннее поражение почек. как правило, аутоиммунной природы. Название патологии происходит от термина «гломерула» (синоним — клубочек ), который обозначает функциональную единицу почки. Это означает, что при гломерулонефрите поражаются основные функциональные структуры почек, вследствие чего быстро развивается почечная недостаточность .
Среди мужского населения это заболевание выявляется в 2 – 3 раза чаще. У детей, среди всех приобретенных почечных болезней, гломерулонефрит занимает 2 место. По данным статистики, эта патология выступает в роли самой частой причины инвалидности. которая развивается из-за хронической почечной недостаточности. Примерно у 60 процентов больных острым гломерулонефритом развивается гипертония. У детей в 80 процентах случаев острая форма этой болезни провоцирует различные сердечно-сосудистые нарушения.
Изначально в организм попадает инфекция, которая может являться причиной ангины. бронхита, пневмонии или других заболеваний дыхательных путей. Патогенный микроорганизм, в данном случае бета-гемолитический стрептококк. воспринимается организмом как чужеродное тело (по-научному — как антиген ). Следствием этого является выработка собственным организмом антител (специфических белков ) против данных антигенов. Чем дольше инфекция находится в организме, тем больше антител вырабатывает организм. Впоследствии антитела соединяются с антигенами, формируя иммунные комплексы. Изначально данные комплексы циркулируют в кровеносном русле, но затем постепенно оседают на почках. Мишенью для иммунных комплексов является мембрана нефрона.
Оседая на мембранах, иммунные комплексы активируют систему комплимента и запускают каскад иммунологических реакций. В результате этих реакций на мембране нефрона оседают различные иммунокомпетентные клетки, которые повреждают ее. Таким образом, нарушаются основные функции почки — фильтрация, всасывание и секреция.
Патогенез (механизмы образования ) условно можно выразить в следующей схеме — инфекция – выработка организмом антител – активация системы комплемента – выход иммунокомпетентных клеток и оседание их на базальной мембране – образование
Причинами развития гломерулонефрита являются:
Ангины и другие стрептококковые инфекции
Данная причина гломерулонефрита является самой частой, поэтому чаще всего используется термин постстрептококковый гломерулонефрит. Причинами постстрептококкового гломерулонефрита являются патогенные штаммы стрептококков группы А. Среди них особенное внимание заслуживает бета-гемолитический стрептококк. Это грамположительный, неподвижный микроорганизм, который встречается повсеместно. В определенной концентрации он находится на слизистых оболочках человека. Главным путем передачи является аэрогенный (воздушно-капельный ) и пищевой путь. Данный микроорганизм продуцирует множество токсинов, а именно дезоксирибонуклеазу, гемолизин, стрептокиназу А и В, стрептолизин, гиалуронидазу. Также он обладает обширным антигенным комплексом. Именно благодаря своей антигенной структуре и продукции токсинов по медицинской значимости стрептококки занимают второе место после стафилококка .
Самым частым заболеванием, которое вызывается стрептококк, является ангина или тонзиллофарингит. Это острое инфекционное заболевание с поражением слизистой оболочки и лимфатической ткани (миндалин ) глотки. Начинается оно внезапно с резкого повышения температуры тела до 38 – 39 градусов. Основными симптомами являются боль в горле. общие симптомы интоксикации. покрытие миндалин гнойным налетом желтовато-белого цвета. В крови отмечается лейкоцитоз. повышение СОЭ (скорость оседания эритроцитов ). появление С-реактивного белка. В период болезни регистрируются положительные бактериологические тесты. Сама по себе ангина редко представляет опасность, больше всего она опасна своими осложнениями. Основными осложнениями стрептококковой ангины являются постстрептококковый гломерулонефрит, токсический шок, ревматическая лихорадка.
Однако, для постстрептококкового гломерулонефрита недостаточно одного эпизода ангины. Как правило, необходимы множественные эпизоды заболевания или так называемая рецидивирующая стрептококковая ангина. В этом случае постепенно происходит сенсибилизация (повышенная чувствительность ) организма антигенами стрептококка и выработка антител. После каждого эпизода болезни происходит повышение титров (концентрации ) противострептококковых антител. В то же время, у детей крайне редко возможно развитие гломерулонефрита после единичного эпизода ангины.
Дифтерией называется острое инфекционное заболевание, которое протекает с преимущественным поражением слизистой оболочки носоглотки. Возбудителем дифтерии является дифтерийная палочка или палочка Леффлера. Данный микроорганизм обладает мощными патогенными свойствами, а также продуцирует экзотоксин. Высвобождаясь в кровеносное русло, экзотоксин разносится с током крови по всему организму. Он способен поражать сердце. нервную систему, мышцы. При дифтерии также поражаются почки. Однако чаще всего поражаются не клубочки, а канальцы почек. Таким образом, наблюдается картина нефроза, а не гломерулонефрита. Острый гломерулонефрит наблюдается при гипертоксической (молниеносной ) форме дифтерии. Клинически он проявляется отеками, гематурией (кровью в моче ). резким снижением суточного диуреза (общего количества выделяемой мочи ).
Симптомами гломерулонефрита являются:
Боль при гломерулонефрите локализуется с обеих сторон, носит тупой и постоянный характер, может усиливаться при ходьбе.
Дизурические проявления – это различные расстройства мочеиспускания, которые выражаются в затрудненном и частом мочеиспускании. Дизурия является симптомом гломерулонефрита только на ранних этапах. Очень быстро она переходит в олигурию – снижение суточного диуреза менее 500 миллилитров в сутки. Снижение объема выделяемой мочи развивается вследствие нарушенной внутрипочечной гемодинамики. Из-за отложения иммунных комплексов на базальной мембране почек нарушаются процессы фильтрации, всасывания и секреции. Это приводит к формированию меньшего объема мочи, а самое главное — к задержке жидкости в организме.
Самым тяжелым и опасным дизурическим проявлением гломерулонефрита является анурия – полное прекращение выделения мочи. Анурией осложняются самые тяжелые формы гломерулонефрита. Вместе с мочой в организме задерживаются токсические продукты обмена, такие как креатинин. мочевина. аммиак. Задержка этих веществ ведет к интоксикации организма, развитию уремии и энцефалопатии .
Механизмами развития артериальной гипертензии являются:
Асцит – это скопление жидкости в брюшной полости, которое может быть вызвано различными патологическими состояниями, чаще всего циррозом печени. Таким образом, асцит – это симптом, а не самостоятельное заболевание. Живот увеличивается в размерах, повышается внутрибрюшное давление, количество жидкости в брюшной полости может достигать 20 литров. Скопление жидкости нарушает работу многих внутренних органов, в том числе дыхание, так как купол диафрагмы оттесняется вверх.
Самой частой причиной асцита является цирроз печени. он регистрируется примерно в ? случаев асцита. Цирроз, как и другие заболевания печени (саркоидоз. рак печени), вызывает портальную гипертензию (увеличение давления в воротной вене и ее притоках), что способствует застою крови и увеличению количества выпота в брюшную полость. Портальная гипертензия развивается не только при заболеваниях печени, препятствия оттоку крови могут возникать из-за сосудистых нарушений (тромбоз. стеноз сосудов системы воротной вены). В норме брюшина выделяет небольшое количество жидкости, которое потом сама же всасывает, это нужно для свободного передвижения петель кишечника. При портальной гипертензии количество жидкости значительно возрастает.
Вторая по частоте причина асцита – опухоли брюшной полости. Асцит при онкологии связан с нарушением нормальной циркуляции жидкости. При сердечной недостаточности тоже возникает застой в малом круге кровообращения, что приводит к увеличению количества выпота.
Асцит развивается при полисерозите (воспалении серозных оболочек сразу нескольких органов, в том числе брюшины), который часто встречается при системных заболеваниях соединительной ткани (ревматизм. ревматоидный артрит, системная красная волчанка).
Частой причиной асцита являются состояния, связанные с уменьшением содержания белков в крови. Это могут быть обменные нарушения, нефротический синдром (при гломерулонефрите), заболевания желудочно-кишечного тракта с нарушением всасывания белков.
Множество других состояний, сопровождающихся портальной гипертензией или патологическими изменениями в брюшине, вызывают развитие асцита, поэтому при его признаках необходима тщательная диагностика для выявления причины, что важно для выбора тактики лечения.
Признаки асцита могут появляться и нарастать резко или постепенно, все зависит от вызывающих его причин. Пациент обращает внимание на увеличение объема живота, чувство тяжести в нем, тянущие боли, иногда выпячивается пупок. По мере нарастания симптомов становится трудно передвигаться, наклоняться, появляется одышка из-за смещения диафрагмы выше физиологичного уровня, появляется отечность ног. Живот имеет характерную форму «пузыря с водой». В вертикальном положении он свисает, в горизонтальном – распластывается. Увеличение внутрибрюшного давления приводит к появлению грыжевых выпячиваний (пупочные, паховые грыжи), может спровоцировать геморрой или выпадение прямой кишки.
В зависимости от причины, вызывающей асцит, могут отмечаться симптомы, характерные для основного заболевания. Асцит при раке (яичников, печени, других органов брюшной полости) сопровождается увеличением лимфатических узлов. Асцит при сердечной недостаточности сопровождается отеком ног, акроцианозом, увеличением печени. Помимо асцита, обычно отмечается гидроторакс (скопление жидкости в грудной полости). При портальной гипертензии, связанной с заболеваниями печени, асцит сопровождается появлением на передней брюшной стенке венозной сети.
Если Вы обнаружили у себя схожие симптомы, незамедлительно обратитесь к врачу .
Легче предупредить болезнь, чем бороться с последствиями.
Увеличение живота может быть связано с разными причинами (ожирение. беременность, новообразования и пр.), поэтому при подозрении на асцит проводится очень подробное обследование.
Самыми простыми способами выявить асцит являются пальпация и перкуссия живота, которые проводит терапевт во время осмотра. При пальпации определяется увеличение объема, напряжение живота, пропальпировать внутренние органы часто бывает невозможно. При перкуссии живота характерно притупление звука и смещение границ тупости при изменении положения тела. Важным диагностическим признаком является симптом флюктуации. Он определяется следующим образом: к одной стороне живота прикладывается ладонь, а с другой стороны выполняются постукивания пальцами. При асците ладонью ощущаются колебания, передаваемые за счет жидкости.
Инструментальная диагностика проводится для уточнения диагноза иопределения объема жидкости в брюшной полости, ее характера. Существуют следующие способы визуализации асцита:
- Рентгенография брюшной полости (выявляет объем жидкости не менее 0,5 л).
- Снимок грудной клетки позволяет выявить подъем купола диафрагмы из-за давления асцитической жидкости.
- УЗИ определяет не только жидкость в брюшной полости, но и возможные причины асцита, поэтому исследуются все органы брюшной полости, особое внимание уделяется печени.
- Гепатосцинтиграфия – метод, позволяющий визуализировать структуру печени и оценить ее функцию.
- Доплерография проводится для определения состояния кровотока в системе портальной вены.
- Ангиография – оценка состояния кровотока в печени с использованием рентгеноконтрастного вещества.
- Лабораторное обследование проводится для оценки функционального состояния печени. Выполняются биохимические пробы (АЛТ, АСТ, билирубин), коагулограмма, иммунограмма.
- Анализ экссудата, полученного при помощи пункции, позволяет предположить характер патологического процесса. Например, при онкологии в брюшной полости асцитическая жидкость содержит атипичные клетки.
Лечение асцита должно проводиться с учетом вызвавшей его причины, иначе жидкость будет образовываться вновь. При циррозе печени лечение асцита обязательно включает назначение гепатопротекторов, при онкологии – химиотерапию или оперативное лечение, при сердечной недостаточности – назначение препаратов, улучшающих деятельность сердца.
Патогенетическая терапия асцита заключается в ограничении употребления жидкости и соли, которая удерживает воду в организме, назначении мочегонных средств. Одновременно повышается содержание белков в крови путем внутривенного введения альбумина или препаратов плазмы. Белок удерживает жидкость в кровеносном русле, препятствуя ее выходу в брюшную полость. Диета при асците назначается бессолевая, с ограниченным количеством жидкости и повышенным содержанием белка.
Если консервативное лечение асцита неэффективно, жидкость удаляется при помощи лечебной пункции, эта манипуляция называется «лапароцентез брюшной полости». Повторные пункции могут стать причиной образования спаек, инфицирования, поэтому при необходимости частого удаления жидкости устанавливается шунт.
Лечение асцита народными средствами может быть рекомендовано только в качестве вспомогательной терапии или при небольшом объеме жидкости в брюшной полости. Оно заключается в использовании трав с мочегонным эффектом. Хороший эффект оказывают березовые листья и почки (настои, обертывания, ванны).
Асцит является осложнением многих заболеваний, утяжеляя их течение. Асцит при циррозе печени свидетельствует о значительных нарушениях в структуре ткани и развитии портальной гипертензии, при онкологии – о распространении процесса с вовлечением брюшины. Сколько живут пациенты с асцитом при циррозе, онкологии и других заболеваниях, зависит от своевременности и эффективности проводимого лечения.
Гломерулонефрит – инфекционно-аллергическое заболевание, относящееся к группе приобретенных заболеваний почек. Различные формы гломерулонефрита различаются по этиологии, проявлениям, течению болезни и ее исходу. Чаще всего характеризуется иммунным воспалением почечных клубочков, а также дальнейшим, вторичным воспалением канальцев почек и интерстицией .
Различают острый гломерулонефрит. быстротекущую форму болезни. и хронический гломерулонефрит. Острая форма заболевания наиболее часто может быть вызвана перенесенной ранее стрептококковой инфекцией – постстрептококковый гломерулонефрит. По этиологии различают первичные гломерулонефриты и вторичные. которые возникают при системных заболеваниях – системной красной волчанке. ревматизме . узелковом периартериите и других.
Причинами заболевания являются перенесенные ранее инфекции – стрептококковая. стафилококковая и иные бактериальные инфекции. В некоторых случаях этиологическим фактором в развитии заболевания могут выступать гепатиты В и С . и возможно цитомегаловирусная инфекция . Гломерулонефрит может развиваться на фоне заболеваний паразитарной природы, под токсическим воздействием некоторых лекарств, при употреблении алкоголя и наркотиков, особенно сильное влияние эти привычки имеют в подростковом возрасте. Нарушение в календарном планировании плановых профилактических прививок также может способствовать возникновению болезни. Поэтому профилактика гломерулонефрита должна содержать точное соблюдение плановых прививок и медосмотров.
Развитие гломерулонефрита происходит на фоне реакций клеточного и гуморального иммунитета. Как правило, перенесенное ранее инфекционное заболевание, вызывает в организме иммунную реакцию, образуются иммунные комплексы. Выработанные для этого антитела разносятся током крови по всем системам, поражая чувствительные к ним органы. Это могут быть сердечная мышца, возникает ревматическая болезнь сердца, суставы – ревматизм, или как в данном случае клубочки почек — острый гломерулонефрит.
У детей заболевание приводит к почечной недостаточности и как следствие инвалидности. Постстрептококковый гломерулонефрит в отличие от других форм заболевания чаще встречается у детей в возрасте 5-12 лет, так же наблюдается развитие болезни у подростков и молодых людей. Острая форма болезни может развиться в любом возрасте, реже заболевание встречается после 40 лет.
Заболевание развивается не позднее чем через три недели после перенесенной стрептококковой инфекции, к примеру, ангины . тонзиллита . пиодермии. поражая обе почки. Для начала течения болезни характерны общие симптомы это слабость, головная боль . озноб, тошнота, боль в пояснице, высокая температура. Острый гломерулонефрит вызывает отечность век, бледность, уменьшение выделяемой мочи.
Клиническая картина заболевания неоднозначна. Течение болезни может проходить в циклической форме с бурным развитием и многими симптомами, а может быть и в латентной, то есть стертой скрытой форме. Часто диагностика гломерулонефрита при латентной форме течения болезни происходит несвоевременно, что дает возможность болезни перейти в хроническую.
Характерные клинические симптомы гломерулонефрита это наличие крови при мочеиспускании и отеки на лице. Гематурия может быть незначительной и обнаружить этот симптом можно только с помощью анализа мочи. Но чаще моча имеет красно-бурый цвет. Отечность также не всегда заметна это либо мешки под глазами и заметное сужение глаз, либо резкое повышение массы тела на 3-4 килограмма.
Снижение количества мочи, так называемая олигурия может продолжаться до 5 дней, потом выделение мочи нормализуется, но наблюдается сниженная плотность мочи. Также для острого гломерулонефрита характерно повышение артериального давления, которое может продолжаться в течение нескольких недель.
При положительном прогнозе основные симптомы гломерулонефрита исчезают в течение первого месяца, а выздоровление происходит за 2-2,5. В случаях поздней диагностики, или если болезнь не поддается лечению в течение года, заболевание переходит в тяжелую хроническую форму.
Гломерулонефрит у детей зачастую развивается в острой форме. Более подвержены заболеванию дети старшего дошкольного и младшего школьного возраста. Груднички практически не болеют гломерулонефритом. Течение болезни крайне бурное с критическими повышениями температуры тела.
Хронический гломерулонефрит различают на четыре клинические формы. При любом течении характерны периоды ремиссии. которые сменяются обострениями схожими с острой формой болезни. Обострения могут быть сезонными, а также возникающие при повторном заражении инфекционными заболеваниями стрептококковой природы.
Некротическая форма гломерулонефрита характеризуется генерализоваными отеками, возможно, их развитие до асцита и анасарки. При лабораторных исследованиях обнаруживается повышение белка в моче и его снижение в крови. При этом повышается уровень липидов и глобулинов. снижается уровень альбуминов .
Гипертоническая форма болезни не включает такие ярко выраженные симптомы гломерулонефрита как некротическая. для этой формы характерна гипертензия. Возможна и смешанная форма течения хронического гломерулонефрита. В этом случае симптомы обеих форм присутствуют одновременно.
Также как и острый гломерулонефрит хронический может протекать практически бессимптомно. Латентная форма характеризуется лишь слабым нарушением выделения мочи.
Подозрение на острый гломерулонефрит вызывает триада симптомов: отеки. гематурия. артериальная гипертензия. При латентной форме течения болезни показаниями к дальнейшей диагностике является данные анамнеза предыдущего заболевания и определение антистрептококковых антител и их концентрации в сыворотке крови .
Назначается рентгенконтрасное исследование и ряд лабораторных анализов, что бы исключить наличие других почечных заболеваний. Так дифференциальная диагностика гломерулонефрита должна исключить обострения нефритов, в том числе наследственной формы, туберкулёза почек. нефролитиаза. Диагностика гломерулонефрита включает также данные ранее перенесенных заболеваний, длительное наблюдение за состоянием пациента, консультации окулиста. При гломерулонефрите происходят изменения глазного дна. При крайне бурном течении болезни проводят исследование тканей – биотапта почки .
При лабораторных исследованиях мочи наличие гематурии или цилиндрурии является подтверждением диагноза. В первые дни течения болезни в анализе мочи обнаруживаются лимфоциты . Они являются отражением иммунного процесса в клубочках почек.
Анализ крови выявляет нейрофильный лейкоцитоз. анемию. увеличение СОЭ. Данные показывают сниженную клубочковую фильтрацию, увеличение азотистых шлаков в крови. Обнаруживаются нарушения системы свертываемости крови. Это чаще всего представлено продуктами деградации фибрина. а также фибриногена в сыворотке крови и моче.
При подтверждении диагноза больного следует госпитализировать. Лечение гломерулонефрита в стационаре требует постельного режима, пациенту требуется покой и тепло, что способствует нормализации кровообращения в почках и снижению артериального давления. Назначается диета с дозированным приемом жидкости для купирования отеков. В первые дни режим питания строго контролируется, исключается наличие соли в пище, ее употребление постепенно возобновляется после исчезновения отеков. Также исключают блюда с богатым содержанием калия, экстрактивных веществ, аллергенов.
Медикаментозное лечение гломерулонефрита включает антибактериальную терапию, чаще всего назначаются антибиотики пенициллинового ряда курсом 1.5-2 месяца. Рекомендовано назначение гепарина подкожно курсом 2-4 недели. Препарат предотвращает внутрисосудистое свёртывание крови. Если симптомы гломерулонефрита включают артериальную гипертензию назначаются ингибиторы АПФ, внутривенные вливания аминофиллина в растворе глюкозы и последующую инфузию фуросемида . Допустимо применение клофелина . метилдопа .
Прогноз лечения гломерулонефрита чаще всего благоприятный. 85-90% пациентов выздоравливают полностью, у остальных больных сохраняются изменения мочи, что не дает возможности говорить о полном выздоровлении. При длительном лечении заболевания возможен переход в хроническую форму с признаками некротического синдрома. Летальный исход регистрируют редко, чаще всего при несвоевременном обнаружении латентной формы течения болезни.
На первом этапе развития болезни возможно возникновение тяжелых осложнений, опасных для жизни пациента. Тяжелое течение болезни может вызывать почечную эклампсию. острую почечную и сердечную недостаточность.
Почечная эклампсия одно из самых частых осложнений острого гломерулонефрита. Эклампсия или ангиопастическая энцефалопатия является спазмом сосудов головного мозга, отеками мозга. Признаками осложнения являются тонико-клонические судороги, перед ними следуют головная боль, тошнота, рвота, нарушение зрения. Приступ эклампсии напоминает эпилептический. сопровождается скачком артериального давления и может длиться несколько минут. Также наблюдается серия приступов. Без своевременного купирования приступа происходит кровоизлияние в мозг.
При гиперергическом течении острой формы болезни развивается острая почечная недостаточность. Осложнения гломерулонефрита вызываются бурным течением болезни. Острая почечная недостаточность сопровождается резким прекращением мочевыделения. В результате задержки воды в организме шлаки и калий накапливаются, тем самым вызывая гипергидрацию и ацидоз . При дальнейшем развитии почечной недостаточности возникают симптомы интоксикации – анорея. тошнота, многократные рвоты, диарея . Присоединяются геморрагический синдром. поражение сердечнососудистой системы и ЦНС. Пациент может впасть в уремическую кому. чаще всего кому вызывает осложненный гломерулонефрит у детей.
Реже, особенно у детей, возникают осложнения гломерулонефрита со стороны работы сердца. Острая сердечно-сосудистая недостаточность характеризуется такими признаками как увеличение печени, нарастание периферической отечности и отеком легких. Именно отек легких чаще всего и становится причиной летального исхода без своевременной помощи.
Правильное лечение стрептококковых заболеваний, соблюдение календаря профилактических прививок и санация очагов инфекции в организме составляют главные меры профилактики. Дети, перенесшие постстрептококковый гломерулонефрит, должны находиться под диспансерным наблюдением на протяжении 5 лет после лечения.
Профилактические медицинские осмотры и лабораторные исследования позволяют рано обнаружить болезнь и избежать осложнений. Самолечение, пренебрежение общими симптомами чаще всего приводит к тяжелым формам заболевания.
Гломерулонефрит. Причины и симптомы. Синдромы при гломерулонефрите. Острый и хронический гломерулонефрит
На сегодняшний день гломерулонефритом страдает от 10 до 15 взрослых пациентов на 10 000 человек. По частоте выявления среди всех патологий почек это заболевание занимает 3 место. Гломерулонефрит может быть диагностирован среди пациентов любой возрастной группы, но наиболее часто болезнь встречается у людей, не достигших 40 лет.
В последнее время частота диагностирования гломерулонефрита среди жителей разных стран увеличивается. Это объясняется ухудшением экологической обстановки, а также общим снижением иммунитета среди населения, которое является следствием несоблюдения рекомендаций по здоровому образу жизни.
На сегодняшний день гломерулонефрит принято считать аутоиммунным заболеванием. В основе его развития лежит иммунокомплексное поражение почек, которое развивается после перенесенной бактериальной или вирусной инфекции. Поэтому гломерулонефрит также называется простудным нефритом или постинфекционной болезнью почек. Эти названия отражают патогенез заболевания — почки поражаются, после того как человек перенес какое-либо инфекционное заболевание. Однако, также провоцировать развитие гломерулонефрита могут лекарственные препараты, токсины.
инфильтрата из нейтрофилов и других клеток – поражение базальной мембраны нефрона – нарушение функции почек.
Вирусная инфекция также играет важную роль в развитии гломерулонефрита. Ранее перенесенное вирусное заболевание является второй по частоте (после стрептококковой инфекции ) причиной гломерулонефрита. Чаще всего развитие гломерулонефрита провоцируют такие вирусы как аденовирусы, ECHO, вирус Коксаки. В качестве антигенов выступает сложная структура вирусов. Также гломерулонефрит у детей может быть следствием ветряной оспы (ветрянки ) или эпидемического паротита (свинки ) .
В настоящее время все чаще встречается лекарственное поражение почек. Так, некоторые лекарства обладают нефротоксичным действием, что означает их избирательность к почкам. Среди таких лекарств особое внимание привлекают сульфаниламиды и препараты пенициллинового ряда. К первой категории препаратов относятся сульфатиазол, сульгин, сульфацил-натрий, а ко второй – D-пеницилламин и его производные. Сульфаниламидные препараты могут поражать различные структуры почек с дальнейшим развитием обструктивной уропатии (заболевания, при котором нарушен ток мочи ) или гемолитической почки.
То, что лечение пенициллинами может провоцировать поражение почек, было известно еще с 50-х годов прошлого столетия. Однако лишь недавно была описана детальная морфологическая картина почек при пенициллиновом гломерулонефрите. Так, D-пеницилламин обладает особой тропностью (избирательностью ) к клубочкам, то есть к гломерулам. Поражая функциональные единицы почек, препараты из этой группы приводят к развитию мембранозного гломерулонефрита. При этом вдоль мембран клубочков происходит отложение иммунных комплексов. Также пенициллины могут вызывать и другие виды гломерулонефритов, такие как пролиферативный и экссудативный.
Токсическое поражение почек встречается при отравлении ртутью, свинцом, мышьяком. Эти и многие другие вещества обладают нефротоксическими свойствами, поражая при этом клубочки, канальцы и другие структуры почек.
В клинике гломерулонефрита выделяют мочевые и общие (не мочевые ) симптомы. К первым относятся такие как снижение суточного диуреза, кровь и белок в моче, ко вторым – повышенное артериальное давление. отеки. Объясняется это тем, что почки осуществляют важные функции в организме, а также участвуют в регуляции артериального давления и водно-солевого обмена.
Боль – является одним из самых ранних симптомов гломерулонефрита. Поскольку при данной патологии поражаются одновременно обе почки (патологический процесс при гломерулонефрите двусторонний ), то боль локализуется с обеих сторон. Жалобы на боль в пояснице слева или справа не характерны для гломерулонефрита.
В основе развития болевой симптоматики при гломерулонефрите лежат два момента. Первый – это увеличение размеров почек на первых этапах. Сами почки не содержат в себе нервных окончаний. Однако они покрыты фиброзной капсулой, которая обильно снабжена нервными окончаниями. Когда почки увеличиваются в размерах, растягивается и капсула, которая их покрывает. Именно растяжение фиброзной капсулы провоцирует болевые ощущения. Второй механизм развития боли – это сдавливание нервно-сосудистых окончаний, увеличенной в объеме тканью почки.
Эти симптомы являются следствием синдрома общей интоксикации. Гломерулонефрит – это аутоиммунное заболевание, которое кроме почек вовлекает и другие органы и системы организма. Вовлечение в патологический процесс отдельных систем приводит к слабости и недомоганию. Также причиной этих симптомов может являться повышенная температура, которая всегда сопровождает острые процессы в почках.
Тяжелым и трудно поддающимся лечению симптомом гломерулонефрита является артериальная гипертензия (повышенное артериальное давление ). При этом систолическое давление повышается более 120 миллиметров ртутного столба, а диастолическое — более 80. Патогенез (механизм развития ) артериальной гипертензии при гломерулонефрите является очень сложным и включает в себя несколько механизмов.
Задержка в организме натрия и воды являются первыми механизмами, которые включаются при плохой работе почек. В норме почки выводят излишки натрия из плазмы крови путем его секреции с мочой. Однако при гломерулонефрите, когда нарушены функции фильтрации и секреции, этого не происходит. Следствием этого является задержка натрия в организме. В то же время, натрий задерживается не один, а затягивает с собой и воду.
Другой механизм развития артериальной гипертензии заключается в активации ренин-ангиотензиновой системы. Активация этой системы происходит вследствие гипоперфузии (снижения кровоснабжения ) почек. Из-за недостаточного кровоснабжения активируется каскад реакций, в результате которых происходит высвобождение ренина. Это гормонально активное вещество, которое, в свою очередь, приводит к превращению ангиотензина I в ангиотензин II. Последний приводит к секреции гормона альдостерона, который увеличивает обратное всасывание натрия (реабсорбцию ). Таким образом, формируется замкнутый круг — активация различных механизмов, так или иначе, приводит к задержке натрия и воды. С другой стороны на повышенное артериальное давление оказывает влияние снижение синтеза простагландинов. В норме эти вещества регулируют сосудистый тонус, препятствуя сужению просвета сосудов. Когда же простагландинов секретируется недостаточно, сосуды сужаются, что создает дополнительную нагрузку к повышенному артериальному давлению. Суженные сосуды и повышенный объем циркулирующей крови являются основной причиной повышенного артериального давления.
В основе развития одышки, как и в основе развития артериальной гипертензии, лежит задержка натрия и воды. Вода задерживается в тканях, создавая, тем самым, отеки. До определенного времени жидкость задерживается только в тканях. Однако вскоре она начинается переходить в полости и заполнять их. Так, лишняя жидкость организма накапливается в плевральной полости, в полости перикарда, в брюшной полости и так далее. Это, в свою очередь, провоцирует другие симптомы. Например, накапливаясь в полости перикарда, жидкость сжимает сердце, становясь причиной одышки и брадикардии (медленного сердцебиения ). Одышку также провоцирует скопление жидкости в легких. что является причиной венозного застоя в малом кругу кровообращения. Так, развиваются элементы нефрогенного (почечного ) отека легких. Выпот жидкости в брюшную полость приводит к развитию асцита. в народе – водянки .
Однако, первым по значимости механизмом появления отеков является протеинурия. Потеря белков организмом ведет к выходу жидкости из кровеносного русла и пропитыванию тканей этой жидкостью (то есть к формированию отеков ). В норме альбумины (белки с высокой молекулярной массой ) крови удерживают в сосудах жидкость. Но при гломерулонефрите происходит массивная потеря этих белков с мочой, вследствие чего их концентрация в сыворотке крови падает. Чем меньше альбуминов остается в крови, тем больше жидкости переходит из кровеносного русла в ткани, и тем массивнее отеки.
Гломерулонефрит проявляется не только внешними признаками, но и отклонениями со стороны анализа крови и анализа мочи. И если изменения со стороны крови пациент не может определить, то некоторые отклонения в анализе мочи видны невооруженным глазом.
Лабораторные признаки гломерулонефрита
источник