Асцит-перитонит — это острое или хроническое воспаление брюшины с последующим инфицированием асцитической жидкости, сопровождающееся местными и общими симптомами и нарушением функций органов и систем.
По этиологии асцит-перитонит подразделяют на первичный и вторичный. Первичным асцитом-перитонитом называют воспаление брюшины у больного с асцитом в отсутствии явного источника инфекции в виде нарушения целостности внутренних органов. Напротив, вторичный асцит-перитонит развивается в результате инфицирования брюшины при остром аппендиците, панкреатите, перфорациях, абсцессах, локализующихся в брюшной полости в результате всех тех причин, которые вызывают перитонит у больных без асцита. Первичный асцит-перитонит встречается достаточно редко и по статистике составляет около 1% от общего числа перитонитов.
Патогенетические механизмы развития асцита-перитонита до настоящего времени изучены недостаточно. К возможным путям инфицирования брюшной полости микрофлорой относят:
гематогенный путь из отдаленных очагов инфекции (одентогенный, бронхолегочный, урогенитальный, как проявление системного инфекционного заболевания (туберкулез, сальмонеллез);
лимфогенный путь, когда нарушение защитных механизмов брюшины происходит на этапе эвакуации микроорганизмов из брюшной полости за счет лимфатического механизма;
непосредственное поступление микроорганизмов в брюшную полость через маточные трубы при сальпингоофоритах.
Отдельную группу составляют больные спонтанным бактериальным перитонитом (СБП), который является вполне устоявшимся термином, означающим воспаление брюшины с последующей контаминацией асцитической жидкости, развивающееся без нарушения целостности внутренних органов.
Термин “спонтанный бактериальный перитонит” впервые предложил известный американский гепатолог Гарольд О`Конн в 1964 г., опубликовав в журнале “Анналы внутренней медицины” 5 случаев его описания. Свою работу он назвал “Спонтанный перитонит и бактериемия при Лаэннековском циррозе, вызванный кишечными микроорганизмами. Относительно частый, но редко диагностируемый синдром”. В своих воспоминаниях автор пишет, что к 1964 г. это тяжелое, часто смертельное заболевание было диагностировано всего лишь в 40 случаях на протяжении последних 200 лет. В период с 1964 по 1974 г. в этой же клинике уже наблюдались 50 больных СБП. В дальнейшем появившееся “вдруг” новое заболевание стало общепризнанным.
Развитие спонтанного бактериального перитонита в настоящее время объясняется транслокацией микроорганизмов из кишки в лимфатические узлы с последующим поступлением в кровь и в брюшную полость.
Факторами риска для развития асцита-перитонита, с одной стороны, являются:
наличие цирроза печени, класса В и С по Child-liugh, с нарушением функции печени, сопровождающимся снижением белково-синтетической функции, функции ретикулоэндотелиальной системы;
сниженный трофологический статус больного;
гастроинтестинальное кровотечение;
наличие бактериальных очагов, бактериемия, виремия;
артериовенозное шунтирование;
нарушение микроциркуляции в стенке кишки, облегчающее транслокацию микроорганизмов, снижение бактериальной и опсонизирующей способности.
Частота СБП у стационарных больных циррозом печени, по данным различных авторов, варьирует от 10 до 30%. Диагностируемые во время госпитализации эпизоды СБП составляют примерно половину общего количества случаев СБП, преимущественно у пациентов с циррозом печени класса В и С по Child-Pugh.
Летальность при СБП — 30—50%, однако в последние годы эти показатели имеют выраженную тенденцию к снижению. Так, например, по данным Центрального научно-исследовательского института гастроэнтерологии, летальность при СБП за последние 3 года составила 21%; основные причины смерти — гастроинтестинальные кровотечения, печеночная недостаточность, гепаторенальный синдром.
Клинические проявления асцита-перитонита, как правило, носят стертый характер. Выделяют:
Системные проявления инфекции (лихорадка, лейкоцитоз, септический шок).
Энцефалопатия и быстро нарастающая печеночная недостаточность без видимых причин.
Местные признаки перитонита (боль в животе).
Нарушение моторики ЖКТ (рвота, диарея).
Обязательным в диагностике асцита-перитонита является исследование асцитической жидкости с проведением подсчета числа полиморфно-ядерных лейкоцитов, определение содержания белка, концентрации альбумина, вычисление сывороточно-асцитического альбуминового градиента.
Получение содержания полиморфно-ядерных лейкоцитов более 250 клеток на мм3 служит показанием для дополнительных исследований на других образцах асцитической жидкости — произведение посева нового образца асцитической жидкости на культуру для посева крови. При СБП высевают как грамотрицательные микроорганизмы, так и грамположительные, реже — анаэробные (см. табл.).
СБП наиболее часто протекает в виде моноинфекции, основными возбудителями его являются грамотрицательные аэробные энтеробактерии и неэнтерококковые стрептококки.
В настоящее время выделяют три варианта СБП в зависимости от количества полиморфно-ядерных лейкоцитов и идентификации микроорганизмов в асцитической жидкости:
классический, полный вариант СБП. Асцитическая жидкость содержит более 250 полиморфно-ядерных лейкоцитов на мм3, дает рост культуры при высевании. Такое сочетание признается наиболее часто встречающимся.
культуронегативный нейтрофильный асцит, когда асцитическая жидкость содержит более 500 полиморфно-ядерных лейкоцитов на мм3, не дает роста культуры при высевании. Выявляется в 4—5% случаев у больных, страдающих циррозом печени, и в 35% случаев больных с подозрением на СБП.
культуропозитивный с низким содержанием нейтрофилов, когда асцитическая жидкость содержит менее 250 полиморфно-ядерных лейкоцитов на мм3, дает рост культуры при высевании. Как правило, при культивировании выявляются грамм-позитивные микроорганизмы в виде монокультуры. Асимптоматично протекает, имеет более благоприятное прогностическое течение.
При обследовании больного циррозом печени с асцитом наиболее часто проводится дифференциальная диагностика с вторичным бактериальным перитонитом, разрывом внутреннего полого органа, локальным абсцессом. Во всех случаях необходима оценка клинической картины заболевания. Наиболее характерно повышение уровня лактатдегидрогеназы >225 mU/L, глюкозы — 50 мг/дл, общего белка — >1 г/дл, как правило, при вторичном асците-перитоните отмечается значительный нейтрофилез, при ультразвуковом исследовании значительно чаще выявляются нити фибрина.
При панкреатогенном асците, который достаточно часто встречается у больных алкогольным циррозом в асцитической жидкости, отмечается повышение уровня амилазы, липазы. Доказана высокая информативность прокальцитонина (предшественника кальцитонина).
При канцероматозе брюшины — в асцитической жидкости проводят выявление атипичных клеток.
Хронический туберкулезный перитонит чаще всего развивается в результате распространения инфекции с мезентериальных или забрюшинных лимфатических узлов или придатков матки. Возможно гематогенное инфицирование. Характерны явления хронической туберкулезной интоксикации с субфебрильной температурой. Выделяют два варианта течения туберкулезного перитонита: асцитическая форма и псевдоопухолевая. В последнем случае продуктивное воспаление приводит к образованию спаечного процесса, спаянию петель кишечника и развитию механической кишечной непроходимости. При ультразвуковом исследовании на фоне асцита часто выявляются нити фибрина, а также фибрин визуализируется в виде взвеси. Диагноз ставят на основании жалоб, явлений туберкулезной интоксикации, исследования асцитической жидкости с последующим посевом на специальные среды. Иногда в диагностике помогает лапароскопия с биопсией.
В соответствии с рекомендациями Международного клуба асцита алгоритм лечения больного со спонтанным бактериальным перитонитом при циррозе печени может быть представлен следующим образом.
Алгоритм обследования больного с впервые выявленным асцитом при циррозе печени:
Всесторонняя оценка клинической картины.
Ультразвуковое исследование с оценкой наличия нитей фибрина, взвеси.
Диагностический парацентез:
подсчет числа полиморфно-ядерных лейкоцитов;
биохимическое исследование асцитической жидкости — общего белка, альбумина, глюкозы, лактатдегидрогеназы, амилазы, липазы;
выявление атипичных клеток в асцитической жидкости.
Посев асцитической жидкости на специальные гемолитические среды.
Должны быть исключены все патологические состояния, которые могут привести к перитониту — панкронекроз, аппендицит, канцероматоз, туберкулез, сальмонеллез, сальпингоофорит.
Рекомендуется до получения результатов посева асцитической жидкости всем больным при превышении числа полиморфно-ядерных лейкоцитов более 250 в мм3 проводить эмпирическую антибактериальную терапию цефалоспоринами III поколения (цефотаксим, цефтриксозим, цефтизидим, цефоницид). Наиболее хорошо изученный и часто применяемый препарат из этой группы цефотаксим назначается каждые 12 ч в течение 5 дней внутривенно, минимальная разовая доза — 2 г.
Амоксициллин/клавулановая кислота по эффективности сравнимы с цефотаксимом, применяются внутривенно в стандартных дозах, рекомендуемых для лечения тяжелых инфекций в течение 5—7 дней.
Больным неосложненным СБП (при отсутствии шока, илеуса, гастроинтестинального кровотечения, выраженной печеночной энцефалопатии или повышения сывороточного креатинина более 3 мг/дл), не получавших ранее профилактически фторхинолоны, может быть рекомендован офлоксацин внутрь в дозе не менее 400 мг каждые 12 ч.
Аминогликозиды согласно международным рекомендациям применять при спонтанном бактериальном перитоните нецелесообразно в связи с более низкой эффективностью и высокой нефротоксичностью.
Эффективность проведения адекватной антибактериальной терапии достигает 90%, характеризуется снижением содержания полиморфно-ядерных лейкоцитов менее 250 клеток на мм3 в асцитической жидкости, исчезновением местных и системных проявлений инфекции. Оптимальным критерием эффективности считается снижение числа полиморфно-ядерных лейкоцитов в асцитической жидкости через два дня от начала антибактериальной терапии по сравнению с исходными показателями. В связи с чем в ходе терапии рекомендуется проводить хотя бы один повторный парацентез через 48 ч от начала терапии.
Критериями неэффективности считают ухудшение состояния в течение первых часов антибактериальной терапии, а также снижение числа полиморфно-ядерных лейкоцитов в асцитической жидкости менее чем на 25%. При отсутствии эффекта от антибактериальной терапии рекомендуется смена антибиотика с учетом чувствительности микрофлоры или эмпирически при отрицательных результатах посева проводить дифференциальный диагноз с вторичным перитонитом.
В лечении спонтанного бактериального перитонита необходимо наряду с этиотропной терапией проведение мероприятий, направленных на предупреждение и лечение осложнений цирроза печени, являющихся факторами риска.
Печеночная энцефалопатия — L-орнитил-L-аспартат, внутривенно по 20 г на 500 мл физиологического раствора, в течение 7—10 дней, в дальнейшем — внутрь по 5 г (гранулят) 3 раза в день 6—8 нед и более, лактулоза — 60—120 г внутрь до послабления стула, длительно.
Гастроинтестинальное кровотечение — ингибиторы протонной помпы.
Гепаторенальный синдром — альбумин, отмена диуретиков, больших объемов парацентезов, нефротоксических препаратов.
Рекомендуется также проведение дезинтоксикационной терапии, применение пребиотиков и пробиотиков для нормализации флоры, снижения эндотоксикоза, уменьшения внутрибрюшного давления.
Профилактику СБП рекомендуется проводить всем больным циррозом печени, осложнившимся желудочно-кишечным кровотечением в связи с высоким риском развития тяжелых бактериальных инфекций с применением фторхинолонов (норфлоксацин, ципрофлоксацин, офлоксацин) 400 мг внутрь каждые 12 ч не менее 7 дней. В качестве альтернативных схем предлагаются комбинации фторхинолонов (ципрофлоксацин или офлоксацин) в сочетании с амоксициллин/клавулановой кислотой внутривенно, а после прекращения кровотечения — ципрофлоксацин внутрь.
Спонтанный бактериальный перитонит является грозным осложнением цирроза печени у больных с асцитом, в связи с чем прогноз для пациентов, перенесших это осложнение, остается серьезным. Вопрос о проведении трансплантации печени необходимо своевременно рассматривать для всех выживших больных.
К группе риска развития СБП также относятся больные циррозом печени класса С по Child-Pugh, перенесшие его в анамнезе.
В настоящее время большие рандомизированные исследования показали высокую эффективность непрерывной антибиотикопрофилактики у больных циррозом печени, перенесших СБП. В соответствии с международными рекомендациями профилактика возвратного бактериального перитонита проводится непрерывно норфлоксацином по 400 мг/сут. Появление резистентной микрофлоры в этом случае остается потенциальной проблемой. В связи с низкой выживаемостью после первого эпизода спонтанного перитонита, которая в течение первого года составляет 30—50%, а в течение второго — всего 25—30%, рекомендуется рассматривать таких пациентов в качестве кандидатов на трансплантацию печени.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Брюшная полость представляет собой замкнутое пространство, ограниченное брюшиной (тонкой полупроницаемой оболочкой) и содержащее различные органы (желудок, селезенку, печень, желчный пузырь и некоторые отделы кишечника). Брюшина состоит из двух листков – париетального (наружного, который прикрепляется к стенкам живота изнутри) и висцерального (внутреннего), который прилегает к стенкам внутрибрюшных органов, окружая их. Основными функциями брюшины являются фиксация расположенных в ней органов и регуляция обмена веществ в организме.
В брюшине имеется огромное количество мелких кровеносных и лимфатических сосудов, которые обеспечивают обмен веществ. В нормальных условиях в брюшной полости и между листками брюшины постоянно находится небольшое количество жидкости, которая образуется в результате пропотевания жидкой части крови и определенного количества белков через кровеносные сосуды. Однако данная жидкость не скапливается в брюшной полости, так как практически сразу же происходит ее обратное всасывание в лимфатические капилляры (в сутки брюшина может всасывать более 50 литров жидкости). Образующаяся при этом лимфа по лимфатическим сосудам поступает в венозную систему организма, возвращая в системный кровоток жидкость, белки и другие, растворенные в ней, микроэлементы.
Исходя из вышесказанного следует, что скапливание жидкости в брюшной полости может произойти в двух случаях — при увеличении скорости ее образования либо при уменьшении скорость ее всасывания. На практике эти два механизма присутствуют одновременно, то есть при различных заболеваниях внутренних органов (печени, поджелудочной железы, при опухолях, при воспалении брюшины и так далее) возникает увеличение продукции жидкости, что непременно влечет за собой нарушение ее реабсорбции (всасывания) в результате сдавливания и закупорки мелких лимфатических и кровеносных сосудов продуктами распада клеток, патогенными микроорганизмами или опухолевыми клетками. По мере развития заболевания жидкости в брюшной полости становится все больше, и она начинает сдавливать расположенные там органы, что, в свою очередь, может усугубить течение основного заболевания и способствовать прогрессированию асцита.
Также стоит отметить, что помимо жидкости в брюшной полости задерживаются и белки (а также и другие микроэлементы). В нормальных условиях белки плазмы крови (преимущественно альбумины) участвуют в создании так называемого онкотического давления, то есть они удерживают жидкость в сосудах. При асците большая доля белков находится в асцитической жидкости, в связи с чем онкотическое давление крови снижается, что также может способствовать выходу жидкости из сосудистого русла и прогрессированию заболевания.
При прогрессировании заболевания происходит уменьшение объема циркулирующей крови, так как большая часть жидкости скапливается в брюшной полости. Это приводит к активации компенсаторных механизмов, направленных на задержку воды в организме (в частности уменьшается скорость образования и выделения мочи), что еще больше повышает гидростатическое давление в кровеносных сосудах и также способствует образованию асцитической жидкости.
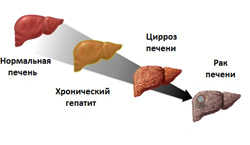
Цирроз печени – это хроническое заболевание, при котором нарушаются строение и практически все функции данного органа, что приводит к возникновению и прогрессированию различных осложнений.
В нормальных условиях в печень по воротной (портальной) вене стекается кровь от многих внутренних органов (от желудка, селезенки, поджелудочной железы, тонкого и толстого кишечника). В печени она проходит через тонкие канальцы (печеночные синусоиды), где фильтруется, очищается и обогащается различными веществами (например, белками), после чего поступает в нижнюю полую вену и возвращается в системный кровоток. При циррозе под действием различных причинных факторов (например, вирусов гепатита В или С) происходит повреждение и разрушение большого количества гепатоцитов (клеток печени). Погибшие клетки замещаются фиброзной тканью, что значительно снижает функцию печени. Это, в свою очередь, приводит к активации компенсаторных механизмов, заключающихся в усиленном делении оставшихся (неповрежденных) клеток. Однако структура новообразовавшейся ткани нарушается (в частности отсутствуют характерные для нормальной печени синусоиды), в результате чего снижается фильтрационная способность органа (то есть уменьшается количество крови, которое может проходить через печень за единицу времени).
Нарушение функции печени, а также изменение ее структуры приводит к тому, что кровь не может профильтровываться в полном объеме, в результате чего она начинает скапливаться в воротной вене. По мере прогрессирования заболевания гидростатическое давление (то есть давление, оказываемое кровью на стенку сосуда) в воротной вене повышается (развивается портальная гипертензия), что нарушает процесс оттока крови от внутренних органов (желудка, кишечника и других). В результате застоя крови в них происходит расширение кровеносных сосудов и повышение проницаемости сосудистых стенок, что и приводит к пропотеванию части жидкости в брюшную полость.
Также стоит отметить, что печень является основным местом образования белков в организме. На поздних стадиях заболевания (когда большая часть гепатоцитов замещается фиброзной тканью) белково-образующая функция печени снижается, в результате чего развивается гипопротеинемия (недостаток белков в крови). Это, в свою очередь, приводит к снижению онкотического давления крови, что также способствует выходу части жидкости из сосудистого русла.
Рак печени – это опухолевое заболевание, которое приводит к повреждению структуры печени и нарушению всех ее функций. Способствовать развитию рака могут различные факторы внешней среды (радиация, токсины, вирусы и так далее), под действием которых происходит образование мутантных опухолевых клеток. Обычно такие клетки сразу выявляются иммунной системой организма и уничтожаются, однако при определенных условиях (например, при ослаблении иммунитета или при облучении большой дозой радиации) одна опухолевая клетка может выжить и начать постоянно (бесконечно) делиться.
Со временем опухоль увеличивается в размерах и может сдавливать крупные внутрипеченочные сосуды. Также раковые клетки могут отрываться от основной опухоли и перемещаться (метастазировать) в другие отделы органа, закупоривая печеночные синусоиды, кровеносные и лимфатические сосуды и желчные протоки. Это будет приводить к нарушению всех функций печени, повышению давления в воротной вене и развитию асцита.
Помимо цирроза и рака есть еще несколько патологий, которые могут нарушить кровообращение в печени и воротной вене и стать причиной выхода жидкости в брюшную полость.
Асцит может быть обусловлен:
- Синдромом (болезнью) Бадда-Киари. Кровь из печени собирается в крупные печеночные вены, которые впадают в нижнюю полую вену. При синдроме (болезни) Бадда-Киари происходит воспаление стенок данных вен с последующим образованием в них тромбов (кровяных сгустков). Это приводит к нарушению оттока крови из печени и повышению давления в системе воротной вены, что и является причиной развития асцита.
- Сдавливанием ветвей воротной вены. После входа в ткань печени воротная вена делится на две крупные ветви (правую и левую), которые направляются в соответствующие доли органа. Сдавливание этих ветвей растущей опухолью или эхинококковой кистой (эхинококкоз – глистное заболевание, при котором в печени и других органах образуются объемные полости – кисты, заполненные развивающимися паразитами) также может стать причиной портальной гипертензии и выхода жидкости из сосудистого русла в брюшную полость.
Причиной асцита может быть:
- Мезотелиома. Данное злокачественное новообразование встречается крайне редко и происходит непосредственно из клеток брюшины. Развитие опухоли приводит к активации иммунной системы с целью уничтожения опухолевых клеток, что проявляется развитием воспалительного процесса, расширением кровеносных и лимфатических сосудов и пропотеванием жидкости в брюшную полость.
- Канцероматоз брюшины. Данным термином обозначается поражение брюшины опухолевыми клетками, которые метастазируют в нее из опухолей других органов и тканей. Механизм развития асцита при этом такой же, как при мезотелиоме.
- Рак поджелудочной железы.Поджелудочная железа является местом образования пищеварительных ферментов, которые выделяются из нее по протоку поджелудочной железы. После выхода из железы данный проток сливается с общим желчным протоком (по которому отходит желчь из печени), после чего они вместе впадают в тонкий кишечник. Рост и развитие опухоли вблизи места слияния данных протоков может привести к нарушению оттока желчи из печени, что может проявляться гепатомегалией (увеличением размеров печени), желтухой, кожным зудом и асцитом (асцит развивается на поздних стадиях заболевания).
- Рак яичников. Хотя яичники и не относятся к органам брюшной полости, листки брюшины участвуют в фиксации данных органов в малом тазу. Этим объясняется тот факт, что при раке яичников патологический процесс легко может распространиться на брюшину, что будет сопровождаться повышением проницаемости ее сосудов и образованием выпота в брюшной полости. На поздних стадиях заболевания может отмечаться метастазирование рака в листки брюшины, что усилит выход жидкости из сосудистого русла и приведет к прогрессированию асцита.
- Синдром Мейгса. Данным термином обозначается патологическое состояние, характеризующееся скапливанием жидкости в брюшной и в других полостях организма (например, в плевральной полости легких). Причиной заболевания считаются опухоли органов малого таза (яичников, матки).
Сердечная недостаточность – заболевание сердца, при котором оно оказывается не в состоянии обеспечить адекватную циркуляцию крови в организме. В нормальных условиях при каждом сердечном сокращении в аорту (самую крупную артерию организма) выбрасывается определенное количество крови. По мере удаления от сердца происходит деление аорты на более мелкие артерии, пока не образуются капилляры – самые тонкие сосуды, в которых происходит обмен кислорода между тканями и клетками организма. После прохождения через капилляры кровь собирается в вены и доставляется обратно к сердцу. Часть жидкости (около 10%) при этом поступает в лимфатические сосуды и превращается в лимфу.
Важной особенностью сосудистой системы является то, что стенка артерий плотная и упругая, в то время как венозная стенка относительно тонкая и легко растягивается при повышении внутрисосудистого давления. При развитии сердечной недостаточности (причиной которой может быть инфаркт, инфекция, длительное повышение артериального давления и так далее) снижается насосная функция сердечной мышцы, в результате чего развивается застой в системе нижней полой вены, которая собирает кровь от всей нижней части тела. Вследствие расширения стенок переполненных венозных сосудов, а также из-за повышения гидростатического давления определенная доля жидкой части крови выходит из сосудистого русла и скапливается в брюшной полости.
Почки являются органами выделительной системы, которые регулируют состав и объем жидкости в организме. Однако при некоторых заболеваниях их функция может нарушаться, что, в свою очередь, может привести к развитию различных осложнений.
Асцитом может осложниться:
- почечная недостаточность;
- нефротический синдром.
Почечная недостаточность
Патологическое состояние, при котором поражается более 75% функциональной ткани (так называемых нефронов) почек. В результате этого орган больше не может в полной мере выполнять свою выделительную функцию, поэтому часть побочных продуктов жизнедеятельности (таких как мочевина, мочевая кислота и другие) задерживаются в организме. Данные вещества являются осмотически активными (то есть притягивают к себе жидкость) и при проникновении в межклеточное пространство тканей приводят к развитию отеков.
Также при почечной недостаточности нарушается кровоснабжение почечной ткани, вследствие чего активируются компенсаторные механизмы, направленные на повышение системного артериального давления и увеличение количества доставляемой к почкам крови. Наряду с этим в почках уменьшается скорость выделения натрия и воды, что еще больше увеличивает объем циркулирующей крови, повышает давление в венозной системе и способствует прогрессированию асцита.
Нефротический синдром
Данное заболевание характеризуется повреждением почечного фильтра (который в норме непроницаем для белков и других крупномолекулярных веществ), в результате чего организм теряет с мочой большое количество белков плазмы (более 3 грамм в сутки). Уже через несколько дней это приводит к значительному снижению онкотического давления крови, в результате чего жидкая ее часть больше не может удерживаться в сосудистом русле и пропотевает в брюшную полость, приводя к развитию асцита.
Панкреатит – это заболевание поджелудочной железы, характеризующееся разрушением ее ткани и распространением патологического процесса на соседние органы. Причиной развития данного заболевания является патологическая активация образующихся в железе пищеварительных ферментов. В норме они выделяются в кишечник в неактивной форме и активируются только после смешивания с кишечным содержимым. При различных патологических состояниях (при злоупотреблении алкоголем, после приема большого количества жареной пищи, после травмы живота или в результате вирусных инфекций) данные ферменты могут активироваться прямо внутри железы, что приведет к ее самоперевариванию.
Во время описанного процесса происходит повреждение сосудов поджелудочной железы, что обуславливает проникновение пищеварительных ферментов в кровь. Если вовремя не начать лечение, патологический процесс может разрушить стенку железы и перейти на брюшину, что станет причиной развития перитонита (воспаления брюшины) и может привести к образованию асцитической жидкости в брюшной полости.
Перитонит – это воспаление брюшины, характеризующееся выраженными болями в животе и прогрессирующими симптомами общей интоксикации организма (повышением температуры тела более 40 градусов, учащенным дыханием и сердцебиением, нарушением сознания и так далее). Развивается данное состояние при проникновении патогенных бактерий в брюшную полость извне.
Причиной перитонита может быть:
- разрыв полого органа (желудка, кишечника, мочевого или желчного пузыря);
- проникающее ранение брюшной полости;
- прободение язвы желудка или кишечника;
- распад опухоли кишечника с повреждением его стенки;
- миграция бактерий из других очагов инфекции;
- распространение воспалительного процесса из соседних органов.
Как говорилось ранее, брюшина содержит большое количество кровеносных и лимфатических сосудов. При развитии инфекционного или другого воспалительного процесса отмечается миграция к очагу воспаления большого количества лейкоцитов, что обуславливает расширение сосудов и выход жидкости в брюшную полость.
Также стоит отметить, что распространение инфекции по брюшине происходит довольно быстро, ввиду чего локальный (местный) перитонит в короткие сроки может перейти в диффузную (распространенную) форму, поражающую всю брюшину, что без своевременного и адекватного лечения может привести к смерти пациента в течение нескольких часов.
Анасарка – это крайняя степень отека, при которой жидкость скапливается в подкожно-жировой клетчатке туловища, рук и ног, а также в полостях организма (в брюшной и в плевральной полости, в полости перикарда). Данное состояние требует срочной медицинской помощи, так как может привести к смерти пациента в считанные часы или дни.
Причиной анасарки могут быть:
- Сердечная недостаточность. В данном случае отеки и асцит развиваются из-за выраженного повышения гидростатического давления в венозной и лимфатической системах, что обусловлено неспособностью сердечной мышцы перекачивать кровь.
- Почечная недостаточность. При данной патологии причиной задержки воды в организме является нарушение выделительной функции почек.
- Заболевания печени. При выраженном циррозе и печеночной недостаточности снижается концентрация белков в крови, что может стать причиной развития генерализованных отеков.
- Микседема. Характеризуется снижением концентрации в крови гормонов щитовидной железы (тироксина и трийодтиронина), что проявляется уменьшением количества образующихся в организме белков и приводит к выходу жидкости из сосудистого русла.
- Гиперальдостеронизм. Данное заболевание характеризуется избыточным образованием в надпочечниках (эндокринных железах) гормонаальдостерона. В нормальных условиях данный гормон отвечает за поддержание объема циркулирующей крови на постоянном уровне, однако при его избыточной секреции происходит выраженная задержка натрия и воды в организме, что способствует развитию отеков и асцита.
Также причиной выхода лимфы в брюшную полость могут быть:
- ранения крупных лимфатических сосудов;
- аномалии развития органов брюшной полости;
- перенесенные ранее операции на брюшной полости;
- опухолевые заболевания (системный лимфангиоз);
- хронические воспалительные заболевания кишечника.
Скапливание жидкости в брюшной полости плода может быть обусловлено различными патологиями матери или ребенка.
Причиной асцита у плода могут быть:
- Гемолитическая болезнь новорожденных. Данное заболевание развивается в том случае, если мать с отрицательным резус-фактором (резус-фактор – это особый антиген, который присутствует на красных клетках крови у определенных людей) будет вынашивать плода с положительным резус-фактором. Во время первой беременности никаких отклонений от нормы не будет, однако во время родов произойдет контакт крови матери и плода, что приведет к сенсибилизации материнского организма (в нем начнут выделяться антитела против резус-фактора). При повторной беременности резус-положительным плодом данные антитела начнут поражать клетки крови плода, нарушая функции всех его органов и тканей и приводя к развитию генерализованных отеков и асцита. Без своевременного лечения данное заболевание приводит к гибели плода.
- Генетические заболевания. Генетический аппарат человека состоит из 46 хромосом, образующихся в результате слияния 23 материнских и 23 отцовских хромосом. Повреждение одной или нескольких из них может проявляться различными заболеваниями, которые могут передаваться потомству. Асцит во внутриутробном периоде может быть проявлением синдрома Дауна (при котором появляется лишняя хромосома в 21 паре), синдрома Тернера (для которого характерен дефект половой Х-хромосомы) и других наследственных заболеваний.
- Внутриутробные аномалии развития. Причиной внутриутробных аномалий развития может быть инфекция, радиация или травма. Асцит при этом может возникать вследствие нарушения нормального развития печени, сердечно-сосудистой или лимфатической системы, при недоразвитии желчевыделительной системы и при других пороках развития.
- Повреждение плаценты.Плацента – это орган, который появляется в организме беременной женщины и обеспечивает жизнедеятельность (доставку кислорода и питательных веществ) плода в течение всего внутриутробного периода развития. Нарушение оттока крови от плаценты или пупочного канатика может повысить давление в кровеносной системе плода, тем самым создав предпосылки для развития отеков и асцита.
Все перечисленные выше причины асцита у взрослых могут также встречаться и в детском возрасте. Однако у новорожденных и детей раннего возраста асцит может быть обусловлен и другими заболеваниями.
Причиной асцита у детей могут быть:
- Пороки развития сердца. В данном случае подразумеваются аномалии развития сердечной мышцы, которые приводят к нарушению насосной функции сердца (дефекты клапанов, дефекты межжелудочковых и межпредсердных перегородок). Во внутриутробном периоде данные аномалии могут никак себя не проявлять, однако после рождения (когда нагрузка на сердце возрастает) могут развиться отеки, асцит и другие признаки сердечной недостаточности.
- Пороки развития почек. Во внутриутробном периоде выделительную функцию осуществляет плацента, поэтому даже при тяжелых аномалиях развития почечной системы признаки почечной недостаточности у плода могут отсутствовать. После рождения ребенка токсические вещества и продукты обмена скапливаются в крови и в тканях малыша, что может привести к развитию отеков и асцита.
- Инфекционные заболевания. Инфицирование плода различными вирусами (вирусом краснухи, герпеса, цитомегаловирусом, энтеровирусом) или бактериями (например, при сифилисе) может привести к поражению внутренних органов и развитию полиорганной недостаточности. Это может проявляться асцитом, который появится во внутриутробном периоде либо сразу после рождения ребенка.
- Опухоли. Новообразования у новорожденных встречаются крайне редко, так как для развития опухолевого процесса и роста опухоли необходимо время. Тем не менее, появление опухоли (злокачественной или доброкачественной) во внутриутробном периоде или в раннем детском возрасте возможно. Растущая опухоль может сдавливать кровеносные или лимфатические сосуды ребенка, повреждать различные органы и ткани (печень, селезенку), что может привести к развитию асцита с первых дней жизни.
- Врожденные анемии.Анемия – общее название состояний, характеризующихся снижением концентрации эритроцитов (красных клеток крови) и гемоглобина (находящегося в эритроцитах дыхательного пигмента) в крови. Некоторые виды анемий (серповидноклеточная анемия, гемоглобинопатии, анемия при дефиците ферментов и так далее) характеризуются деформацией и разрушением эритроцитов. Разрушаются они преимущественно в печени и селезенке, что может со временем приводить к поражению данных органов и развитию отеков и асцита.
Асцит у беременных может развиться в результате различных заболеваний печени, сердца, почек и других органов и систем. Также скапливанию жидкости в брюшной полости способствует рост и увеличение размеров плода, который может сдавливать нижнюю полую вену (крупный сосуд, собирающий венозную кровь от всей нижней части тела).
Рост и развитие плода само по себе требует от всех органов и систем женского организма более интенсивной работы. Скапливание жидкости в брюшной полости и повышение внутрибрюшного давления еще больше увеличивает нагрузку на органы, что может привести к декомпенсации хронических заболеваний и развитию полиорганной недостаточности, угрожающей здоровью или даже жизни матери и плода.
Наиболее грозными проявлениями асцита у беременных могут быть:
- Дыхательная недостаточность. Увеличение матки на поздних сроках беременности приводит к смещению диафрагмы (основной дыхательной мышцы, отделяющей брюшную полость от грудной клетки) вверх, что приводит к уменьшению дыхательного объема легких. Появление большого количества жидкости в брюшной полости еще больше усугубляет данный процесс, что приводит к недостатку кислорода в крови матери и плода.
- Сердечная недостаточность. Как уже было сказано, рост и развитие плода приводит к повышению давления в брюшной полости. В результате этого повышается кровяное давление в располагающихся там кровеносных сосудах. Чтобы преодолеть это давление, сердце вынуждено работать в усиленном режиме. Появление асцита на поздних сроках беременности еще больше увеличивает нагрузку на сердце, что может стать причиной нарушения его функции. Это, в свою очередь, может привести к недостаточному поступлению крови к плаценте и стать причиной внутриутробной гибели плода.
- Сдавливание растущего плода. При асците количество скапливающейся в брюшной полости жидкости может достигать нескольких десятков литров. Это приведет к выраженному повышению внутрибрюшного давления и сдавливанию всех внутренних органов, в том числе и матки с развивающимся плодом. Как правило, такое состояние делает невозможным дальнейшее развитие беременности.
При геморрагическом асците в асцитической жидкости присутствуют красные клетки крови (эритроциты) в том или ином количестве. Как правило, такое состояние развивается на фоне уже имеющихся хронических заболеваний, ставших причиной образования асцита (цирроза печени, рака, туберкулеза).
Причиной геморрагического асцита может быть:
- травма печени;
- травма селезенки;
- кровотечение при распаде опухоли;
- тромбоз (закупорка кровяным сгустком) печеночных вен;
- перфорация (прободение) стенки кишечника (например, при язве).
Появление крови в асцитической жидкости является неблагоприятным прогностическим признаком и требует срочных диагностических и лечебных мероприятий.
Туберкулез – это инфекционное заболевание, которое поражает легкие, кишечник и другие органы. Вызывается заболевание микобактериями туберкулеза, которые попадают в организм преимущественно воздушно-капельным путем (при вдыхании воздуха, загрязненного возбудителем) или с пищей. Первичный очаг туберкулеза обычно локализуется в легочной ткани, реже – в кишечнике. По мере прогрессирования заболевания и при снижении защитных сил организма микобактерии могут распространяться из первичного очага в другие ткани, в том числе и в брюшину.
Поражение брюшины туберкулезом приводит к развитию специфического воспалительного процесса (перитонита), что проявляется расширением кровеносных сосудов и пропотеванием большого количества жидкости, лимфы и белков в брюшную полость.
Эндометриоз – заболевание, при котором происходит разрастание эндометрия (слизистой оболочки матки) в нетипичных для него местах (то есть в других органах и тканях). Причиной заболевания может быть нарушение гормонального фона женщины, а также наследственная предрасположенность.
Вначале клетки эндометрия выходят за пределы слизистой оболочки матки и проникают в ее мышечный слой, начиная там делиться. Во время менструального цикла они (как и обычный эндометрий) подвергаются определенным изменениям, что может привести к развитию кровотечения. На поздних стадиях заболевания клетки эндометрия выходят за пределы матки и могут поражать любые органы и ткани, в том числе и брюшину. Помимо прочих симптомов (болей в животе, нарушения мочеиспускания и так далее) это может проявляться скапливанием жидкости в брюшной полости.
Легочной плеврой называется тонкая соединительнотканная оболочка, которая состоит из двух листков — наружного и внутреннего. Наружный листок прилегает к внутренней поверхности грудной клетки, а внутренний окутывает легочную ткань. Между данными листками имеется щелевидное пространство (плевральная полость), где содержится небольшое количество жидкости, необходимой для обеспечения скольжения листков друг относительно друга во время дыхания.
Плевритом называется воспаление листков легочной плевры, что обычно сопровождается пропотеванием жидкости в плевральную полость. Асцит и плеврит одновременно могут наблюдаться при системных воспалительных заболеваниях аутоиммунного характера (когда иммунная система атакует клетки и ткани собственного организма) – при ревматической лихорадке, системной красной волчанке, ревматоидном артрите и так далее. Стоит отметить, что при перечисленных заболеваниях также может отмечаться скапливание жидкости в полости перикарда (сердечной сумки).
Однако, независимо от причины возникновения, скапливание жидкости в брюшной полости всегда будет проявляться определенными симптомами, выявление которых позволит заподозрить диагноз на ранних стадиях заболевания.
Асцит может сопровождаться:
- отеками;
- повышением температуры тела;
- болями в животе;
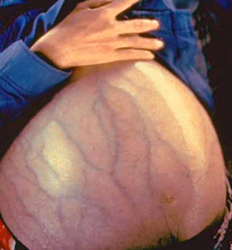
- увеличением размеров живота;
- увеличением печени;
- увеличением селезенки;
- тошнотой;
- рвотой;
- «головой медузы»;
- желтухой;
- одышкой;
- обезвоживанием.
Отеки при асците развиваются в результате выхода жидкости из сосудистого русла и перехода ее в межклеточное пространство различных тканей. Механизм образования и характер отеков зависит от основного заболевания, ставшего причиной асцита.
Отеки при асците могут быть следствием:
- почечной недостаточности (почечные отеки);
- сердечной недостаточности (сердечные отеки);
- печеночной недостаточности (безбелковые отеки).
Почечные отеки
Почечные отеки возникают из-за задержки воды и осмотически активных веществ в организме. Они (отеки) симметричны (наблюдаются в обеих частях тела), присутствуют постоянно, однако могут усиливаться в утренние часы, так как в течение ночного сна в организме скапливается большое количество жидкости и токсических веществ. Вначале отеки локализуются преимущественно в области лица, шеи, верхних конечностей, затем спускаются в область бедер и голеней. Кожа в области отека имеет нормальную или слегка повышенную температуру, может отмечаться бледность кожи. При продолжительном (в течение 20 – 30 секунд) надавливании на отечные ткани образуется углубление, которое исчезает сразу после прекращения давления.
Сердечные отеки
Сердечные отеки развиваются из-за того, что сердце не может перекачивать кровь из вен в артерии. Возникают они преимущественно к вечеру, вначале локализуются в области стоп и голеней, а затем поднимаются в область бедер и туловища. Объясняется это тем, что днем человек в течение длительного времени находится в вертикальном положении, в результате чего значительно повышается гидростатическое давление в венах нижних конечностей и развивается застой крови в них. Это и приводит к выходу жидкости из сосудов в межклеточное пространство.
Кожа в области сердечных отеков синюшного цвета, холодная на ощупь. При продолжительном надавливании образующееся углубление исчезает медленно.
Безбелковые отеки
При дефиците белков жидкая часть крови выходит в межклеточное пространство, что проявляется крайне выраженными, генерализованными (наблюдающимися во всех участках тела) отеками. Кожа в области отечных конечностей растянута, напряжена, бледная и сухая, температура ее снижена. При надавливании на отечную ткань вмятина исчезает в течение нескольких секунд.
Непосредственно асцит к повышению температуры тела не приводит. Причиной нарушения терморегуляции являются основные заболевания, ставшие причиной скапливания жидкости в брюшной полости.
При асците повышение температуры тела может быть проявлением:
- Перитонита. Поражение брюшины чужеродными микроорганизмами приводит к активации иммунной системы и повышению температуры тела. Наиболее высокие цифры (до 40 и более градусов) отмечаются при бактериальном перитоните, когда патогенные бактерии и выделяемые ими токсины всасываются в кровь и разносятся по всему организму. При перитоните туберкулезной этиологии температура обычно держится в пределах 37 – 39 градусов.
- Панкреатита. При панкреатите происходит развитие неинфекционного воспалительного процесса в поджелудочной железе, что сопровождается повышением температуры до 38 градусов. Переход воспаления на брюшину и развитие перитонита может сопровождаться более выраженной температурной реакцией (до 39 – 40 градусов).
- Цирроза печени. На ранних стадиях развития цирроза у всех пациентов отмечается субфебрилитет (повышение температуры тела до 37 – 37,5 градусов). Если цирроз является следствием поражения вирусами гепатита В или С, повышение температуры до 37 – 39 градусов будет являться естественной защитной реакцией организма, возникающей в ответ на внедрение чужеродных агентов. Повышение температуры тела выше 39 градусов обычно является следствием развития бактериальных осложнений и требует срочного медицинского вмешательства.
- Опухоли. При всех злокачественных опухолевых заболеваниях у пациента отмечается субфебрилитет в течение нескольких недель или месяцев, что обычно сопровождается чувством слабости и снижением массы тела. При метастазировании рака в брюшину может отмечаться повышение температуры тела до 39 – 40 градусов, что объясняется развитием воспалительной реакции в ответ на внедрение «чужих» (опухолевых) клеток.
Также стоит отметить, что для асцита при микседеме характерно снижение температуры до 35 градусов. Объясняется это недостатком гормонов щитовидной железы, которые в норме регулируют (повышают) скорость обменных процессов в организме и температуру тела.
Возникновение, характер и локализация болей зависят преимущественно от причины асцита, однако в некоторых случаях скапливание большого количества жидкости в брюшной полости может непосредственно приводить к усилению болей, сдавливая органы брюшной полости.
Болевой синдром при асците может быть обусловлен:
- Циррозом печени. Цирроз печени развивается постепенно и ему обычно предшествуют воспалительные заболевания печени (гепатиты). Сама печень не содержит болевых рецепторов, однако окружающая орган капсула богата ими. Увеличение размеров печени при различных заболеваниях приводит к перерастяжению капсулы, что проявляется болями различной интенсивности. В начальных стадиях цирроза пациенты могут жаловаться на дискомфорт или легкие боли в области правого подреберья, которые с течением времени могут усиливаться. Также пациенты могут жаловаться на тяжесть или боль в других отделах живота. Это объясняется нарушением пищеварения, имеющим место на поздних стадиях цирроза.
- Синдромом (болезнь) Бадда-Киари. При данной патологии происходит закупорка вен, по которым кровь оттекает от печени. Вследствие этого происходит переполнение внутрипеченочных кровеносных сосудов, увеличение органа в размерах и растяжение печеночной капсулы, что сопровождается острыми, колющими болями в правом подреберье, отдающими в правые отделы спины.
- Воспалением брюшины. В листках брюшины содержится большое количество болевых рецепторов, поэтому ее воспаление сопровождается выраженными режущими или колющими болями в животе, которые усиливаются при надавливании на переднюю брюшную стенку.
- Панкреатитом. Развитие воспалительного процесса в поджелудочной железе проявляется острыми болями опоясывающего характера, которые максимально выражены в области верхней части живота. Боли могут отдавать в область правого или левого подреберья, в спину, в сердце.
- Опухолью. Боли при опухоли редко бывают сильно выраженными, что значительно затрудняет раннюю диагностику злокачественных новообразований. Пациенты могут в течение нескольких недель или месяцев ощущать тупые, тянущие или ноющие боли в животе. Интенсивность болей при этом может самопроизвольно увеличиваться или уменьшаться.
- Эндометриозом. Боли при данной патологии локализуются преимущественно внизу живота, однако при метастазировании клеток эндометрия в другие органы могут иметь любую локализацию. Обычно женщины жалуются на усиление болей во время полового акта, во время менструации, болей при мочеиспускании или дефекации. Боль при этом острая, режущая, не купируется приемом обычных обезболивающих препаратов.
Данный симптом становится заметен невооруженным глазом при скапливании в брюшной полости более 1 литра жидкости. Вначале это может проявляться лишь в положении стоя, когда жидкость скапливается в нижних отделах брюшной полости, обуславливая выпячивание передней стенки живота. В положении лежа живот может быть нормальных размеров, однако пациент при этом может начинать жаловаться на одышку (чувство нехватки воздуха), так как жидкость будет перемещаться в верхние отделы брюшной полости, ограничивая движения диафрагмы и легких.
При дальнейшем прогрессировании заболевания количество асцитической жидкости увеличивается, вследствие чего выпирание передней брюшной стенки становится заметным и в положении лежа. При выраженном асците (когда в брюшной полости скапливается более 10 – 12 литров жидкости) кожа живота становится натянутой, напряженной, блестящей.
Увеличение печени (гепатомегалия) и селезенки (спленомегалия) может быть важным диагностическим признаком, указывающим на ту или иную причину асцита.
Причиной гепатомегалии и спленомегалии может быть:
- Цирроз печени. При циррозе печени происходит нарушение структуры печеночной ткани и частичное ее замещение фиброзной (рубцовой) тканью. Это создает препятствие на пути тока крови, в результате чего она скапливается в венах печени и в воротной вене, приводя к увеличению органа в размерах. Чтобы понизить давление в системе воротной вены часть крови сбрасывается в венозные сосуды селезенки, что также приводит к переполнению ее кровью и увеличению в размерах.
- Опухоль. Причиной увеличения печени может быть увеличение размеров внутрипеченочной опухоли или разрастание метастазов из опухолей другой локализации. При метастазировании злокачественной опухоли в ткань печени также произойдет закупорка печеночных капилляров опухолевыми клетками, что приведет к нарушению кровотока в органе и может стать причиной увеличения его в размерах.
- Болезнь Бадда-Киари. При тромбозе печеночных вен происходит переполнение печеночной ткани кровью и увеличение размеров печени. Селезенка при этом увеличивается лишь в тяжелых случаях заболевания (при развитии и прогрессировании портальной гипертензии).
- Сердечная недостаточность. При сердечной недостаточности кровь застаивается в системе нижней полой вены, повышая давление в ней. Так как печеночные вены (выносящие венозную кровь из печени) также впадают в нижнюю полую вену, выраженная сердечная недостаточность может нарушить отток крови от печени, что приведет к увеличению ее размеров.
На начальных стадиях развития асцита возникновение тошноты и рвоты может быть обусловлено основным заболеванием (циррозом печени, панкреатитом, перитонитом и так далее). По мере прогрессирования патологического процесса количество жидкости в брюшной полости увеличивается, что приводит к сдавливанию и нарушению функции многих органов (в частности желудка и кишечника).
Сдавливание желудка может значительно снизить его объем и нарушить моторику, в результате чего человек может испытывать тошноту даже после приема небольшого количества пищи. В случае появления рвоты рвотные массы будут содержать только что съеденную, непереваренную пищу. После рвоты желудок опустошается, что обычно приносит облегчение пациенту.
Сдавливание кишечника также может нарушить его моторику. При выраженном асците кишечные петли могут сдавливаться с такой силой, что продвижение перерабатываемой пищи (химуса) по ним станет невозможным. В результате этого химус начнет скапливаться выше места сдавливания, обуславливая усиление перистальтики в данном отделе кишечника. Пациент при этом будет жаловаться на приступообразные боли в животе, тошноту. Возникающая в данном случае рвота будет содержать частично переваренные продукты или каловые массы, а также будет иметь характерный неприятный запах.
Желтуха (окраска кожных покровов и видимых слизистых оболочек в желтый цвет) возникает при различных заболеваниях печени, сопровождающихся нарушением ее функции. Скапливание жидкости в брюшной полости на фоне желтухи позволяет с большой долей вероятности предположить, что причиной асцита является патология печени (цирроз или рак).
Механизм возникновения желтухи заключается в следующем — при разрушении красных клеток крови (эритроцитов) в кровоток выделяется пигмент желтого цвета – билирубин. Он является довольно токсичным продуктом, поэтому в нормальных условиях сразу же захватывается клетками печени, нейтрализуется и выводится из организма в составе желчи. При нарушении функций печении данный процесс замедляется или вовсе прекращается, вследствие чего концентрация билирубина в крови начинает расти. Со временем он проникает в различные ткани и органы и оседает в них, что и является непосредственной причиной появления желтушной окраски кожи и слизистых оболочек.
Одышка (чувство нехватки воздуха) при асците является следствием повышения давления в брюшной полости и ограничения подвижности легких. В нормальных условиях во время вдоха происходит сокращение диафрагмы (основной дыхательной мышцы), в результате чего она смещается вниз (в сторону брюшной полости), обеспечивая расширение легких и поступление в них порции свежего воздуха. Скапливание большого количества жидкости в брюшной полости и повышение внутрибрюшного давления делает невозможным полноценное смещение диафрагмы вниз, в результате чего при каждом вдохе пациент получает меньшее количество воздуха.
В начальном периоде развития асцита одышка возникает только в положении лежа, когда жидкость смещается вверх и давит на диафрагму. В положении стоя жидкость отекает в нижние отделы живота и человек дышит свободно. На поздних стадиях заболевания (когда объем асцитической жидкости достигает 10 литров и более) одышка наблюдается в положении стоя и усиливается в положении лежа, ввиду чего пациенты обычно отдыхают и спят полусидя.
Обезвоживание – это патологическое состояние, характеризующееся уменьшением количества жидкости в клетках и уменьшением объема циркулирующей крови (ОЦК). Хотя при асците жидкость из организма не теряется, она выходит из сосудистого русла в брюшную полость (то есть «выключается» из системы кровообращения) в результате чего ОЦК снижается и появляются характерные признаки обезвоживания.
Обезвоживание организма проявляется:
- жаждой;
- сухостью во рту;
- сухостью кожных покровов;
- снижением эластичности кожи;
- появлением морщин в области лица;
- повышением температуры тела;
- западением глазных яблок;
- уменьшением суточного диуреза (количества выделяемой мочи);
- запорами;
- снижением артериального давления;
- нарушением сознания (вплоть до возникновения галлюцинаций).
В отсутствии своевременного и адекватного лечения пациент с выраженным обезвоживанием может впасть в кому или даже умереть из-за нарушения функций жизненно-важных органов (головного мозга, сердца).
источник
Асцит — это состояние, при котором в брюшной полости появляется свободная жидкость в больших количествах.
Асцит является следствием цирроза печени в 75%; злокачественных новообразований — в 10%; сердечной недостаточности в 5% случаев.
В клинической картине у пациентов отмечается вздутие живота и прогрессирующее нарастание веса.
Диагноз основывается на результатах физикального и визуализирующих (рентгенологических, ультразвуковых) методов исследования.
Лечение заключается в назначении бессолевой диеты, диуретиков. Больным может производиться терапевтический лапароцентез, выполняются хирургические вмешательства. Пациенты с асцитом — кандидаты на трансплантацию печени.
Наиболее частым осложнением асцита является спонтанный бактериальный перитонит . Он возникает при инфицировании асцитической жидкости, которое в 90% случаев происходит спонтанно. У больных появляются боли в животе, повышается температура тела.
Для диагностики этого осложнения производится исследование асцитической жидкости. Для лечения спонтанного бактериального перитонита назначаются антибактериальные препараты.
- Классификация асцита
Асцит классифицируется в зависимости от количества жидкости, наличия инфицирования асцитической жидкости и варианту ответа на медикаментозную терапию.
- По количеству жидкости в брюшной полости:
- Небольшое количество жидкости.
- Умеренное количество жидкости.
- Значительное количество жидкости (напряженный, массивный асцит).
- По инфицированности содержимого:
- Стерильное содержимое.
- Инфицированное содержимое.
- Спонтанный бактериальный перитонит.
- По варианту ответа на медикаментозную терапию:
- Асцит поддающийся медикаментозной терапии.
- Рефрактерный асцит.
Асцит, который не может быть устранен, или ранний рецидив которого не может быть адекватно предотвращен лечением.
- Асцит, резистентный к диуретикам: асцит, рефрактерный к диете с ограничением натрия и интенсивной терапии диуретиками ( спиронолактон 400 мг/день, фуросемид 160 мг/день в течение не менее 1 недели; диета с ограничением поваренной соли менее 5,2 г/день).
- Асцит, не контролированный диуретиками: асцит, рефрактерный к терапии из-за развития вызванных диуретиками осложнений, которые препятствуют применению эффективных дозировок диуретиков.
- Эпидемиология асцита
Асцит является следствием цирроза печени в 75%; злокачественных новообразований — в 10%; сердечной недостаточности — в 5% случаев.
Примерно у половины пациентов с циррозом печени асцит развивается в течение 10 лет от начала заболевания. Он обусловлен нарушениями почечной функции, портального и висцерального кровообращения.
Примерно 50% пациентов с цирротическим асцитом умирают в течение 2 лет от начала заболевания. Показатели однолетней выживаемости у больных с асцитом, резистентным к терапии, составляют 50%.
У здоровых мужчин внутриперитонеальная жидкость обнаруживается в меньших количествах, чем у женщин, у которых ее объем составляет примерно 20 мл (в зависимости от фазы менструального цикла). При асците этот объем значительно увеличивается.
Частота возникновения спонтанного бактериального перитонита составляет 15-20%.
- Этиология и факторы риска развития асцита
- Факторы риска при отсутствии патологических процессов в брюшине.
- Портальная гипертензия (градиент концентрации альбумина сыворотка-асцит ≥11 г/л).
- Цирроз печени .
- Алкогольный гепатит.
- Фулминантная печеночная недостаточность.
- Метастазы в печень .
- Хроническая сердечная недостаточность .
- Констриктивный перикардит .
- Синдром Бадда-Киари .
- Обструкция нижней полой вены.
- Гипоальбуминемия (градиент концентрации альбумина сыворотка-асцит
Размер пор внутренних капилляров в 50-100 раз меньше, чем печеночных синусоидов, поэтому градиент транссинусоидального онкотического давления в печени почти нулевой, в то время как в печеночной циркуляции он равняется 0,8-0,9. Высокий градиент онкотического давления минимизирует влияние любых изменений концентрации альбумина плазмы на трансмикроваскулярный обмен жидкостью.
У пациентов с алкогольным циррозом на поверхности эндотелия синусоидов происходит отложение иммуноглобулина А, что приводит к еще большему снижению его проницаемости.
На поздних стадиях цирроза печени поры в эндотелии синусоидов исчезают, его проницаемость снижается. Возникает градиент давления между интерстициальными пространствами гепатоцитов и просветом синусоидов.
Кроме того, при портальной гипертензии происходит увеличение уровня оксида азота (NO) в организме, который также способствует вазодилатации висцеральных и периферических сосудов. Доказательством этому служит тот факт, что у пациентов с асцитом в печеночной артерии обнаруживается повышение активности NO синтазы.
Недостаточности лимфатической системы.
Ведущая роль в формировании асцита у больных циррозом печени принадлежит недостаточности лимфатической системы.
В печени формируется до 70% всей лимфы организма, которая через систему грудного лимфатического протока транспортируется в венозную систему большого круга кровообращения. Из-за декомпенсации венозной системы печени при циррозе, становится невозможной перфузия необходимого количества портальной крови через больную печень. При этом резко возрастает нагрузка на систему лимфооттока, которая вынужденно возмещает недостаточность венозного оттока и отводит максимально возможное количество жидкости от органа в виде «печёночной» лимфы. Отток лимфы от печени достигает 15-20 л/сут и более при норме 8-9 л.
Усиленное функционирование лимфатической системы способствует разгрузке венозной сети, но в дальнейшем развивается динамическая недостаточность лимфообращения. На определенном этапе болезни лимфатическая система перестаёт справляться с запредельной нагрузкой. Лимфатические капилляры, мелкие сосуды и магистральные стволы расширяются, возникает дезорганизация нормальной микролимфоциркуляции на уровне лимфангионов, нарастает застой лимфы, развивается лимфатическая гипертензия. Эти процессы приводят к пропотеванию жидкости с поверхности печени в брюшную полость и к появлению асцита.
Некоторое время эта жидкость может адекватно всасываться париетальной брюшиной, но и эти компенсаторные возможности не могут быть беспредельными, так как за перемещение жидкости из брюшной полости и возврат её в сосудистое русло отвечает всё та же система лимфооттока, которая к моменту развития асцита находится в состоянии суб (а чаще де-) компенсации, и дополнительная нагрузка в виде увеличения количества жидкости, которую необходимо переместить из брюшной полости, приводит к полной её несостоятельности.
Патологические изменения в системы ренин-ангиотензин-альдостерона.
Патологические процессы в печени при развитии цирроза проходят с участием системы ренин-ангиотензин-альдостерона.
Накопление асцитической жидкости приводит к снижению эффективного объема плазмы, что стимулирует секрецию ренина в юкстагломерулярном аппарате почек. Ренин усиливает синтез ангиотензина I, который превращается в ангиотензин II. Ангиотензин II приводит к снижению гломерулярной фильтрации и почечного кровотока, повышает секрецию антидиуретического гормона гипофиза и альдостерона надпочечников.
Под влиянием альдостерона у больных циррозом печени усиливается реабсорбция натрия и экскреция калия в дистальных отделах почечных канальцев и возрастает реабсорбция натрия и воды в проксимальных отделах.
Повышенная потеря калия и водорода на фоне гиперальдостеронизма способствует снижению содержания калия, магния в сыворотке крови и метаболическому алкалозу. При этом у большинства больных развивается гипонатриемия, так как большая часть натрия переходит в интерстициальную и асцитическую жидкость.
Таким образом, вследствие гемодинамических нарушений (недостаточного наполнения центрального венозного и артериального русла) происходит активация ренин-ангиотензин-альдостероновой системы. Все это приводит к реабсорбции натрия в канальцах почек и задержке воды в организме.
Накопление асцитической жидкости в брюшной полости отражает состояние водно-электролитного обмена в организме. Одним из ключевых звеньев патогенеза почечной дисфункции и задержки натрия при циррозе являются расстройства системного висцерального кровообращения (вазодилатация), возникающими вследствие портальной гипертензии .
Параллельно происходит развитие почечной вазоконстрикции у пациентов с циррозом печени, которое связано с повышением симпатической активности почек и ренин-ангиотензиновой системы для поддержания артериального давления при системной вазодилатации. Сниженный почечный кровоток снижает скорость клубочковой фильтрации и секрецию натрия.
Цирроз печени сопровождается повышенной реабсорбцией натрия в проксимальных и дистальных канальцах, на что также влияет увеличение концентрации циркулирующего альдостерона.
При компенсированном циррозе задержка натрия может возникать в отсутствие вазодилатации и гиповолемии. Синусоидальная портальная гипертензия может снижать почечный кровоток, не сопровождаясь гемодинамическими изменениями системной циркуляции, вследствие, так называемого, гепаторенального рефлекса.
Гемодинамические сдвиги изменяются с положением тела. Установлены выраженные постуральные колебания секреции натрийуретического пептида и системной гемодинамики: в положении лежа увеличиваются сердечный выброс и вазодилатация.
Несомненно, существуют и другие механизмы развития асцитического синдрома, о которых мы пока не знаем или не можем оценить степень их значимости. Например, доказано, что при циррозах печени отмечается повышение тонуса симпатической нервной системы, повышены уровни эпинефрина и норэпинефрина, нарушен синтез и метаболизм кининов, простагландинов, предсердного натрийуретического фактора.
источник
- Портальная гипертензия (градиент концентрации альбумина сыворотка-асцит ≥11 г/л).
Этиология асцита в 90% случаев связана с хроническими заболеваниями печени: портальной гипертензией (развившейся вследствие цирроза печени ), алкогольным гепатитом, обструкцией печеночной вены (синдром Бадда-Киари).
Непеченочными причинами асцита могут быть: заболевания сердца ( сердечная недостаточность , констриктивный перикардит), злокачественные новообразования (карциноматоз, псевдомиксома брюшины), заболевания брюшины (инфекционный перитонит), выраженная гипоальбуминемия (нефротический синдром), другие болезни (опухоли и кисты яичников, панкреатит , саркоидоз , системная красная волчанка, микседема).
Факторы риска возникновения асцита: