В мировой литературе к хроническим воспалительным заболеваниям кишечника относят только болезнь Крона и язвенный колит. Термины «хронический энтерит» и «хронический энтероколит» считают необоснованными, т.к. они отражают лишь морфологию, исключая поиск конкретных нозологических форм.
Идиопатические воспалительные заболевания кишечника: болезнь Крона и язвенный колит.
●Болезнь Крона — воспалительное заболевание всех слоёв стенки кишечника с прерывистым (сегментарным) характером поражения различных отделов желудочно-кишечного тракта. Следствие трансмурального воспаления — образование свищей и абсцессов. Заболевание имеет многообразную клиническую картину с кишечными и внекишечными проявлениями и осложнениями. Полное излечение невозможно.
●Язвенный колит (в отечественной литературе — неспецифический язвенный колит) — поражение слизистой оболочки толстой кишки, преимущественно дистальных отделов. Изменения первоначально возникают в прямой кишке, затем распространяются проксимально и примерно в 10% случаев захватывают всю толстую кишку. Излечения возможно после тотальной колонэктомии.
Болезнь Крона и неспецифический язвенный колит (НЯК) клинически имеют между собой больше сходства, чем различия.
Эпидемиология. Заболеваемость воспалительных заболеваний кишечника в разных странах различна и составляет 0,05–13,2 случаев на 100 тыс. населения.
Распространённость НЯК и болезнь Крона имеет общие закономерности: в северных странах, таких как Англия, Швеция, Норвегия, США заболеваемость наибольшая, в странах южной Европы, Азии, Ближнего Востока, Африке, Австралии — низкая. Есть основание полагать, что на возникновение этих заболеваний влияют факторы внешней среды. Результаты эпидемиологических исследований свидетельствуют о повсеместном увеличении частоты воспалительных заболеваний кишечника: за последние тридцать лет заболеваемость увеличилась в пять раз. Однако об истинной заболеваемости судить трудно, т.к. больные к врачу обращаются поздно, и правильный диагноз устанавливают через два года и более от начала заболевания.
Воспалительными заболеваниями кишечника болеют люди всех возрастов: от маленьких детей до стариков, но наиболее часто молодые люди от 15 до 30 лет. Для болезни Крона возрастной пик — 20–29 лет, для НЯК — 20–40 лет. Второй пик заболеваемости — возраст 60–80 лет. Бимодальное распределение заболеваемости связывают с разными этиологическими факторами: генетическими у молодых лиц, внешними факторами среды у пожилых. Не исключено, что у пожилых лиц воспалительные заболевания кишечника скрыты за ишемическим колитом. Молодой возраст, тяжёлое течение с частой пожизненной инвалидизацией, повсеместное нарастание заболеваемости делают проблему воспалительных заболеваний кишечника чрезвычайно актуальной.
Этиологиявоспалительных заболеваний кишечника до настоящего времени неизвестна. Существуют многочисленные теории: инфекционная, влияние факторов внешней среды (приёма оральных контрацептивов, антибиотиков, курения, диеты), генетическая, иммунологическая.
●Инфекционная теория вызывала наибольший интерес, т.к. подразумевалось, что хроническое воспаление должен поддерживать какой-то возбудитель. Современная концепция предполагает следующие механизмы участия инфекционного агента: персистирующая инфекция, иммунная реакция на кишечную микрофлору с изменёнными свойствами, повышенная проницаемость слизистой оболочки для бактериальных метаболитов (нарушение барьерной функции слизистой оболочки), изменённый иммунный ответ на нормальную кишечную микрофлору.
Персистирующими агентами, прежде всего, считали микобактерию туберкулёза, вирус кори, клебсиеллу и др. Однако возможно, что инфекция — один из неспецифических триггерных факторов в развитии воспалительных заболеваний кишечника. У пациентов с воспалительными заболеваниями кишечника выявлена кишечная микрофлора с изменённой вирулентностью (повышены адгезия, гидрофобность, усилена продукция эпителиальных токсинов, иммуномодулирующих пептидов, муцин-деградирующих энзимов, гиалуронидазы, белков теплового шока, суперантигенов).
Однако нормальная кишечная флора и её метаболиты (эндотоксины, хемотаксические пептиды) при определённых условиях также поддерживают в кишке хроническое воспаление, что приводит к нарушению барьерной функции слизистой оболочки. Возможен изменённый иммунный ответ на нормальную кишечную микрофлору: в участках скоплений анаэробной флоры обнаруживают антиэпителиальные антитела, перекрёстно реагирующие с бактериальными эпитопами. Это приводит к развитию хронического воспаления и повреждения слизистой оболочки кишки. Воспалительный процесс, в свою очередь, сопровождается активацией местной иммунной системы: при обострении воспалительных заболеваний кишечника интраэпителиальные лимфоциты продуцируют значительное количество IgG, направленных против цитоплазматических протеинов кишечной микрофлоры. Следовательно, обострение, а иногда и дебют воспалительных заболеваний кишечника связан со срывом толерантности к нормальной кишечной микрофлоре.
●Факторы внешней среды вызывают значительный рост числа воспалительных заболеваний кишечника. Наиболее изучены влияние курения, приёма оральных контрацептивов, антибиотиков, питания.
◊ Курение в два раза увеличивает заболеваемость, причём выявлен и дозозависимый эффект: чем больше интенсивность курения, тем выше риск возникновения болезни Крона. У детей курящих родителей в два раза чаще развивается НЯК и в пять раз чаще — болезнь Крона. Предполагаемый патофизиологический механизм включает нарушение образования слизи в кишечнике, ослабление ректального кровотока, иммунологические эффекты (обнаружено нарушение соотношения T-хелперов, T-супрессоров и продукции цитокинов).
◊ Оральные контрацептивы. Влияние на развитие воспалительных заболеваний кишечника до конца не изучено, но предполагают, что эстрогены способствуют возникновению микротромбов, прежде всего, при болезни Крона.
◊ Питание. Связь с возникновением воспалительных заболеваний кишечника пока не достоверна. Полагают, что употребление жиров, в частности длинноцепочечных триглицеридов, коррелирует с частотой этих заболеваний. Возможно, имеют значение ω3-жирные кислоты, в их метаболизме участвуют иммунорегуляторные лейкотриены и простагландины. Соблюдение диеты больными воспалительными заболеваниями кишечника приводило к длительной ремиссии.
◊ Антибиотики. Их использование и заболеваемость воспалительными заболеванями кишечника возрастают параллельно. Данные популяционных исследований подтверждают повышенный риск заболевания у лиц, получавших антибиотики. Антибиотики изменяют биологические свойства кишечной флоры, у лиц с генетической предрасположенностью к воспалительным заболеваниям кишечника возможна их манифестация на фоне приёма антибиотиков.
●Генетические факторыразвития болезни Крона и НЯК доказаны. Обнаружена восприимчивость к воспалительным заболеваниям кишечника лиц с генами, кодирующими хромосомы 6 и 7. У больных изучали маркёры генов, участвующих в регуляции иммунного ответа, генов I и II классов системы гистосовместимости HLA. Доказана связь болезни Крона с аллелем DRB1 у европейцев. Напротив, аллель HLA DPB1 крайне редко обнаруживают у пациентов с болезнью Крона, возможна её протективная роль в отношении этого заболевания. Для НЯК характерна ассоциация с HLA DR2 (85%) и HLA DO1wl (96%).
Принимая во внимание центральную роль цитокинов в модулировании иммунного ответа, пытались выявить мутации или полиморфизм в генах, кодирующих цитокины. Доказана связь болезни Крона с определённым гаплотипом микросателлитов ФНО. В перицентромерном регионе хромосомы 16 были открыты локусы, предрасполагающие к развитию этого заболевания. Именно в этих локусах располагаются гены, определяющие структуру молекулы адгезии — сиалофорина, рецепторов к ИЛ-4 и С3-компоненту комплемента. Наличие семейных случаев воспалительных заболеваний кишечника, высокий риск их развития у родственников первой степени родства пациентов с болезнью Крона (3,9%, что в 13 раз выше, чем в популяции) подтверждают генетическую предрасположенность к этим заболеваниям. Кроме того, отмечена высокая частота заболевания воспалительных заболеваний кишечника у моно- и дизиготных близнецов.
●Нарушение клеточного и гуморального иммунитета у больных подтверждено многочисленными данными. Помимо гипергаммаглобулинемии и гиперпродукции IgG, у всех больных НЯК и болезнью Крона обнаруживают антитела к цитоплазматическим антигенам нейтрофилов и моноцитов ANCA (антинейтрофильные цитоплазматические антитела). При болезни Крона их обнаруживают у 27% больных, при НЯК — у 70%. Наличие их при воспалительных заболеваниях кишечника не отвечает на вопрос, идёт ли речь о патологическом процессе, непосредственно ассоциированном с иммунным феноменом или иммунный ответ вторичен по отношению к поражению кишечника.
Патологический процесс при НЯК всегда начинается в прямой кишке и в редких случаях ограничивается только этим отделом (проктит). Воспаление постепенно распространяется в проксимальном направлении, захватывая прилежащие отделы сигмовидной (проктосигмоидит), нисходящей ободочной кишки (левосторонний колит) и из относительно изолированного превращается в тотальный колит. Иногда в процесс бывает вовлечён дистальный отдел подвздошной кишки (ретроградныйили back—wash илеит).
Клинические признаки: жидкий стул с примесью крови от 5–10 раз в сутки до бессчётного количества раз, боли в левой половине живота, тенезмы.
Характер течения заболевания определяет морфологические изменения, может быть острым (в том числе, молниеносным) и хроническим(рецидивирующим или непрерывно текущим).
●Острая форма.Складки слизистой оболочки утолщены или, наоборот, сглажены, резко отёчны, полнокровны, покрыты тонким слоем фибрина. Видны многочисленные эрозии и язвы. Язвы разных размеров, чаще крупные, неправильной формы, с подрытыми нависающими краями, обычно неглубокие, локализуются в слизистой оболочке. Островки слизистой оболочки между язвами приобретают вид полипов, образуя выбухания размером от нескольких миллиметров до нескольких сантиметров. Они часто напоминают истинные железистые полипы, однако тело и ножка в них не различимы. Иногда язвы глубоко проникают в стенку кишки, образуя карманы между подслизистым слоем и мышечной оболочкой. Слизистая оболочка отторгается, вся внутренняя поверхность толстой кишки представляет собой сплошную язву. При глубоких язвах и разрушениях мышечной оболочки возникает токсическая дилатация: стенка кишки истончена, просвет её резко расширен. Это осложнение НЯК нередко приводит к перфорации.
Гистологически в начальной стадии заболевания в кишке преобладают воспалительные изменения. Инфильтрат из лимфоцитов, полинуклеарных лейкоцитов, эозинофилов и плазматических клеток располагается в собственной пластинке слизистой оболочки, не проникая в подслизистую основу. Затем в инфильтрате накапливаются полиморфноядерные лейкоциты, они по периваскулярным пространствам проникают в толщу стенки кишки, через покровный эпителий путем лейкопедеза — в просвет кишки, а через эпителий крипт — в просвет последних. Развивается криптит, при этом облитерированы дистальные отделы либеркюновых желёз, количество слущенного эпителия и нейтрофилов резко увеличено, формируется крипт-абсцесс. В области дна крипт-абсцессы вскрываются. Содержимое прорывается в подслизистую основу с формированием язвы. Деструктивные процессы при острой форме НЯК преобладают.
●Хроническая форма.Преобладают репаративно-склеротические изменения с рубцеванием язв. Кишка грубо деформирована, нередко значительно укорочена. Стенка её утолщена за счёт гипертрофии мышечной оболочки, просвет неравномерно сужен. Однако укорочение и сужение кишки потенциально обратимы. Слизистая оболочка резко сглажена, с множеством воспалительных полипов. Полипы состоят из соединительной ткани с лимфоидной инфильтрацией, покрыты слизистой оболочкой с деформированными или неизменёнными криптами. Обилие воспалительных полипов иногда имитирует картину диффузного полипоза. Часть язв рубцуется с образованием грубых обширных рубцовых полей. Полной эпителизации язв не наступает.
Гистологически характерна картина хронического продуктивного воспаления. Лимфоплазмоцитарная инфильтрация с примесью эозинофилов сохраняется всегда, даже в период многолетней ремиссии. Регенерация при НЯК несовершенна, о чём свидетельствует характер новообразованной слизистой оболочки в участках эпителизации язв: эпителий «тёмный» (бокаловидных клеток практически нет), выраженная дезорганизация крипт, полноценные крипты отсутствуют. Нередко видна дисплазия разной степени выраженности.
Помимо кишечника, бывают поражены многие органы и системы, чаще всего печень, кожа, суставы и глаза.
Осложнения НЯК делят на следующие группы:
кишечные, наиболее грозные — токсическая дилатация и перфорация стенки кишки с развитием перитонита или парапроктита;
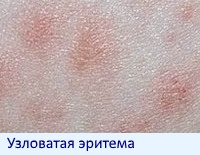
внекишечные — поражения кожи (узловатая эритема, гангренозная пиодермия), глаз (эписклерит, увеит, иридоциклит), печени (первичный склерозирующий холангит, билиарный цирроз), суставов (артриты).
Колоректальный рак может возникнуть при длительном течении НЯК, это зависит от распространённости процесса, возраста больных, наличия поражения печени. Чаще рак возникает при тотальных формах НЯК: через 10 лет от начала заболевания — у 3% больных, через 30 лет — у 9,5–16,5%. Средняя продолжительность НЯК до развития рака — 18,1 года. Если неспецифический язвенный колит возникает до 18 лет, нередко в дальнейшем развивается не одна, а несколько карцином. При НЯК, ассоциированном с первичным склерозирующим холангитом, рак возникает значительно чаще.
В 1932 г. В.В. Crohn дал полное описание клиники и морфологии заболевания с изолированным поражением терминального отдела подвздошной кишки — терминального илеита, с этого времени он носит название болезни Крона. Установлено, что при этом заболевании бывают поражены все отделы желудочно-кишечного тракта, начиная с полости рта и заканчивая перианальной областью.
Клинически заболевание в период обострения проявляется диареей, однако не такой тяжёлой, как при НЯК, не более пяти раз в сутки. В фекалиях иногда видна кровь. У всех больных со временем развивается выраженная анемия и похудание. Клиническое течение волнообразное, после обострения следует длительная ремиссия, иногда до двадцати лет.
По локализации основных изменений при болезни Крона выделяют три формы: энтерит, энтероколит и колит.
Толстая кишка бывает поражена преимущественно в восходящей части. Анальная и перианальная область страдают всегда, нередко поражение именно этой области (трещины, свищи, парапроктит) предшествует клинической манифестации болезни. Макроскопические измененияпри любой локализации заболевания, в основном, сходны и зависят от стадии заболевания:
Воспалительный процесс начинается в подслизистом слое кишки (из глубины) и распространяется на все слои стенки. В месте поражения стенка кишки утолщена, плотна на ощупь; по внешнему виду её в зависимости от протяжённости процесса сравнивают со «шлангом» или «чемоданной ручкой». Такие участки размерами от 8–15 см до 1,5–2 м особенно часто обнаруживают в тощей и подвздошной кишке.
Процесс многоочаговый и распространяется подобно «прыжкам кенгуру»: очаги поражения чередуются с участками совершенно сохранной слизистой оболочки кишки. Внешний вид язв характерен: они длинные, узкие, с ровными краями. Язвы параллельными рядами (линейные язвы) тянутся в продольном направлении (рентгенологически — «следы грабель»). Одновременно с продольными образуются поперечные язвы,они щелевидные, глубокие, как ножевые раны. Язвы часто проникают в подслизистый слой и мышечную оболочку, где, соединяясь между собой, образуют большой интрамуральный канал или интрамуральные абсцессы. В связи с этим регулярно возникает воспаление серозной оболочки и брыжейки. Макроскопически утолщённая отёчная брыжейка выглядит, как пальцевидные выпячивания, распространяющиеся по всей серозной оболочке («ползучий жир»).
Островки слизистой оболочки, заключённые между пересекающимися язвами-трещинами, по образному выражению Крона, напоминают «булыжную мостовую». Язвы, проникая через все слои стенки кишки, часто способствуют образованию спаек и свищей между петлями кишок и соседними органами. В отдельных случаях возникают наружные свищи.
Микроскопические измененияразнообразны. Наиболее характерный микроскопический признак — неспецифический гранулематоз. Во всех слоях стенки кишки развивается продуктивное воспаление с формированием гранулём, состоящих преимущественно из эпителиоидных клеток, иногда с примесью гигантских клеток типа инородных тел и/или Лангханса. Гранулёмы не содержат очагов казеозного некроза, в них никогда не выявляют туберкулёзных микобактерий. Больше всего они напоминают гранулёмы при саркоидозе, но, в отличие от последних, они меньше по размерам, без чётких границ, гигантские клетки содержат меньшее количество ядер. Это саркоидоподобные гранулёмы (рис. 13-5а).
Рис. 13-5. Подвздошная кишка при болезни Крона: а — саркоидоподобная гранулёма (окраска гематоксилином и эозином, x250); б — щелевидная язва, проникающая до серозной оболочки (окраска гематоксилином и эозином, x90).
Возможно образование макрофагальных гранулём. Помимо кишки, гранулёмы находят в лимфатических узлах, краях колостом, биоптатах из язв анальной области. Однако гранулёмы выявляют не всегда: не более чем в 50% случаев, в биоптатах в 14–19%. Воспалительная инфильтрация возникает в подслизистой основе, по соединительнотканным прослойкам распространяется на мышечную оболочку и субсерозный слой, затем по периваскулярным пространствам переходит на клетчатку брыжейки. Слизистая оболочка при болезни Крона вовлечена в процесс в меньшей степени, чем при НЯК. Характерная особенность — наличие многочисленных лимфоидноклеточных узелков и типичных лимфоидных фолликулов со светлыми центрами.
Описанные выше язвы-трещины при гистологическом исследовании обычно узкие, глубокие, проникают в мышечную оболочку, субсерозный слой, иногда в подлежащую клетчатку (рис. 13-5б).
Осложнения при болезни Крона, как и при НЯК делят на кишечные и внекишечные.
●Кишечные осложнения. В период обострения возможна перфорация язв, требующая экстренного оперативного вмешательства. Внутренние свищи и перфорации могут стать причиной образования абсцессов (межкишечных, ретроперитонеальных, абсцессов печени). В 2–6,4% случаев при фульминантном течении возникает токсический мегаколон. Большинство кишечных осложнений протекает длительно. В первую очередь, это свищи: внутренние (кишечно-кишечные, кишечно-пузырные), наружные (кишечно-кожные) и перианальные (ректовагинальные, свищи заднего прохода). У 30–50% пациентов с БК обнаруживают стриктуры и стенозы кишечника, у 20–60% — перианальные осложнения (в основном, трещины). У одной трети больных они — первое клиническое проявление болезни. В 0,4–0,8% случаев при БК возникает колоректальный рак.
●Внекишечные осложнения: поражение суставов (полиартрит, сакроилеит, анкилозирующий спондилит, «барабанные палочки»), кожи (узловатая эритема), полости рта (афты, язвы, трещины) и глаз (склерит, эписклерит, иридоциклит). Наиболее часто поражение гепатобилиарной системы (первичный склерозирующий холангит в 13,4% случаев, со временем возможна трансформация в билиарный цирроз печени). Первичный билиарный цирроз печени у больных с БК возникает в двенадцать раз чаще, чем в общей популяции.
Псевдомембранозный колит — острое воспалительное заболевание кишечника, связанное с антибиотикотерапией, вызвано Clostridium difficile. Симптомы различны, от кратковременной диареи до тяжёлого колита с фибринозными бляшками на слизистой оболочке толстой кишки. Колит, вызванный С. difficile, признан наиболее частой причиной диареи у больных в стационаре (его частота — 7 случаев на 1000).
C. difficile — грамположительный спорообразующий анаэробный микроорганизм. Патогенные штаммы C. difficile продуцируют токсин А (энтеротоксин, вызывающий патологические изменения толстой кишки) и токсин В (цитотоксин). Для реализации патогенных свойств микроорганизма необходимы условия для его избыточного роста, возникающие при применении антибиотиков. Характерно возникновение колита через несколько дней или недель после приёма антибиотиков широкого спектра действия. У большинства пациентов заболевание протекает относительно легко с водянистой диареей и схваткообразными болями в животе. При тяжёлых вариантах течения возможно повышение температуры тела до 40 °C, частота стула до двадцати раз в сутки, обезвоживание, гипотензия.
Токсин C. diffcile повреждает кишечный эпителий и кровеносные сосуды слизистой оболочки. При этом происходит выделение богатого фибриногеном экссудата и превращение фибриногена в фибрин. Слизистая оболочка замещена псевдомембраной — плёнкой из погибших клеток слизистой оболочки, фибрина, лейкоцитов, слизи, способной отторгаться от подлежащих тканей. Псевдомембраны, таким образом, отличаются от «истинных мембран», выстилающих внутренние органы, т.е. слизистых оболочек. Новообразованные псевдомембраны бледно-серые, затем бывают окрашены каловыми массами в зелёный или коричневый цвет. После их удаления видна обнажённая, кровоточащая эрозированная слизистая оболочка кишки.
Осложнения (токсический мегаколон, перфорация толстой кишки) редки.
Коллагеновый колит—редкоезаболевание толстой кишки (1,0–2,3 случаев на 100 тыс. населения), протекающее с хронической водной диареей, без характерных эндоскопических и рентгенологических признаков; диагноз устанавливают исключительно морфологически. Среди больных 90% составляют женщины 55–65 лет.
Этиология заболевания неизвестна. Патогенезпредполагает участие иммунологических механизмов, т.к. собственная пластинка слизистой оболочки инфильтрирована CD4 + T-лимфоцитами, обнаружены интраэпителиальные лимфоциты, экспрессирующие CD8 иT-клеточный рецептор α илиβ. Антиген, стимулирующий T-лимфоциты, неизвестен. Возможно, антигенное раздражение исходит из просвета кишечника, т.к. при устранении пассажа кала явления воспаления стихают. В качестве пусковых факторов предлагают токсин C. difficile, Campylobacter jejuni, нестероидные противовоспалительные препараты, жёлчные кислоты. Предполагают, что курение увеличивает риск развития коллагенового колита.
Морфологический признак — утолщение коллагеновой базальной мембраны поверхностного эпителия (в области крипт базальная мембрана не утолщена). В норме толщина этой пластинки — 3–7 мкм, а при коллагеновом колите она достигает 10–60, иногда 90 мкм. Утолщение коллагеновой пластинки связывают с нарушением функции фибробластов под влиянием инфекционных и других факторов. В собственной пластинке слизистой оболочки видна лимфоплазмоцитарная инфильтрация. Отличительный признак — увеличение числа интраэпителиальных лимфоцитов.
Лимфоцитарный колитклинически протекает так же, как коллагеновый. Болеют, как правило, люди среднего возраста, одинаково часто мужчины и женщины. Длительность заболевания около трёх лет.
Этиология и патогенез неизвестны. Связь с инфекциями и питанием не установлена. При эндоскопическом и рентгенологическом исследовании слизистая оболочка не изменена. Микроскопическое исследование биоптатов выявляет лимфоцитарную инфильтрацию собственной пластинки слизистой оболочки, деструкцию покровного эпителия, увеличение числа интраэпителиальных лимфоцитов. Иногда лимфоцитарный колит переходит в коллагеновый.
Микроскопический колит. Этот термин ввели Рид и соавт. (1980 г.) на основании исследования больных с хронической диареей неясного генеза и признаками хронического воспаления в биоптате при неизменённой слизистой оболочке. Этот колит не имеет специфических клинических и морфологических проявлений, обнаруживаемые изменения могут носить вторичный характер. У части больных при повторном изучении биоптатов был обнаружен коллагеновый колит. На этом основании в клинической практике коллагеновый и микроскопический колит рассматривают как единое заболевание.
Радиационый колит.Широкое распространение лучевой терапии для лечения опухолей малого таза или брюшной полости иногда требует интенсивного облучения рядом расположенных органов, в частности, толстой кишки. После облучения возникает воспаление слизистой оболочки кишки, кровотечение, язвы.
Макроскопически в очагах поражения слизистая оболочка кишки зернистого вида, с кровоизлияниями и лучевыми язвами, покрытыми желтовато-белым налётом.
Микроскопически обнаруживают картину острого или хронического воспаления, крипт-абсцессы, очаги деструкции покровного эпителия, полнокровие сосудов. Характерные признаки радиационного колита:
скопление фибробластов среди клеток воспалительного инфильтрата;
появление очагов гиалиноза в собственной пластинке слизистой (предвестник развития в последующем стриктуры кишки);
наличие эндартериита в мелких артериях и артериолах.
Повреждение сосудов и склероз — признаки, объединяющие радиационный и ишемический колиты.
Дивертикулёз — заболевание с характерными выпячиваниями стенки толстой кишки.Большинство дивертикулов ложные, т.е. возникают за счёт дистопии слизистой оболочки и подслизистой основы между мышечными пучками. Генез дивертикулов пульсионный и, предположительно, связан с повышением внутрибрюшного давления при натуживании. Характерна множественность дивертикулов, обычно возникающих в месте прохождения артерий через мышечную оболочку.
Более широкая распространённость в развитых странах связана, вероятно, с особенностями пищевого рациона (бедная клетчаткой пища предрасполагает к запорам). Дивертикулёзом чаще болеют пожилые люди, в развитых странах 30% населения в возрасте 50 лет и 60% населения в возрасте 80 лет. Преобладает поражение сигмовидной кишки (85% случаев).
При дивертикулёзе возможно развитие дивертикулита.
Дивертикулит— воспаление стенки дивертикула, связанное с проникновением бактерий через слизистую оболочку, повреждённую каловыми камнями или страдающую от недостаточного кровоснабжения.
Основные симптомы: боль в животе, изменение частоты дефекации (запор или понос), кишечные кровотечения, общие признаки воспаления (лихорадка, лейкоцитоз).
межкишечные абсцессы, возникающие при переходе воспаления на околокишечную жировую клетчатку;
спаечная болезнь, сопровождающая воспаление окружающих кишку тканей;
перитонит (при разрыве стенки дивертикула);
сужение или полное закрытие просвета кишки вследствие кольцевого фиброза кишечной стенки.
Аппендицит — воспаление червеобразного отростка слепой кишки.Осложнения острой формы аппендицита лидируют в хирургической практике при состояниях, объединённых понятием острый живот. По течению различают острый и хронический аппендицит.
Причина заболевания окончательно не установлена. Чаще всего её связывают с непроходимостью, обусловленной обтурацией отростка каловыми массами и конкрементами (фекалитом), реже глистами, опухолью или жёлчным камнем.
Патогенез. Секреция слизи в закупоренном отростке приводит к нарастанию давления содержимого на стенки аппендикса. Это вызывает сдавление вен, дренирующих отросток, последующую ишемию и некроз. В этих условиях происходит размножение местной микробной флоры, ещё более способствующей нарастанию отёка и расстройствам кровообращения. Однако в ряде случаев обтурацию отростка не выявляют.
Морфологические формы острого аппендицита: простой, поверхностный, флегмонозный и гангренозный.
●Простой аппендицит обычно диагностируют только гистологически: выраженное полнокровие сосудов, стаз в капиллярах и венулах, отёк и диапедезные кровоизлияния, краевое стояние лейкоцитов в сосудах, местами лейкопедез эпителия.
●Поверхностный аппендицит—результат прогрессирования простого аппендицита. Дисциркуляторные изменения нарастают, отросток макроскопически выглядит набухшим, а серозная оболочка его — тусклой, гиперемированной, зернистого вида. В слизистой оболочке дистального отдела видны фокусы гнойного воспаления конусовидной формы, иногда с поверхностными очагами некроза.
●Флегмонозный аппендицит.Макроскопически отросток увеличен, серозная оболочка тусклая, покрыта фибринозным налетом, под ней точечные кровоизлияния. На разрезе просвет заполнен гноевидным содержимым, стенка утолщена, диффузно пропитана гноем. Иногда в толще стенки видны мелкие абсцессы (апостематозный, т.е. гнойничковый аппендицит). Слизистая оболочка нередко изъязвлена (флегмонозно-язвенный аппендицит). При гистологическом исследовании заметна диффузная нейтрофильная инфильтрация всех слоёв стенки отростка, полнокровие сосудов всех калибров, кровоизлияния.
●Гангренозный аппендицит— дальнейшее развитие флегмонозного аппендицита в случае присоединения гнилостной флоры. Воспаление переходит на брыжейку отростка (мезентериолит) и её сосуды, прежде всего, артерии. Возникает тромбоз аппендикулярной артерии. Макроскопически аппендикс ещё более увеличен в размерах, серозная оболочка его тусклая, с багровыми и синюшными пятнами, покрыта зеленовато-серыми наложениями. Просвет заполнен гноем или распадающимися грязно-серыми массами. Под микроскопом видна диффузная инфильтрация стенки лейкоцитами, обширные кровоизлияния, почти тотальный некроз слизистой оболочки, в некротическом детрите — колонии микроорганизмов.
Осложнения чаще возникают при деструктивных вариантах: флегмонозном, флегмонозно-язвенном и гангренозном аппендиците. Наиболее частое осложнение — перфорация стенки отростка с развитием разлитого или ограниченного перитонита. Гнойное расплавление стенки отростка может привести к его самоампутации или скоплению большого количества гнойного экссудата в просвете отростка (эмпиема). При мезентериолите в артериях и венах развивается воспаление и тромбоз. При этом воспаление с аппендикулярной вены переходит на воротную (пилефлебит). Иногда возможна тромбобактериальная эмболия, что приводит к пилефлебитическим абсцессам печени.
Повторные приступы вяло текущего острого аппендицита могут приводить к разрастанию в стенке отростка грануляционной и фиброзной ткани, атрофическим изменениям эпителия и мышечных волокон, сужению или облитерации просвета отростка. Истинный хронический аппендицит диагностируют крайне редко. Иногда при рубцовой облитерации просвета отростка в его проксимальной части скапливается серозная жидкость (водянка отростка) или секрет эпителия желёз (мукоцеле).
Дата добавления: 2015-06-04 ; Просмотров: 1813 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
Аппендикс — пальцеобразный мешочек, который присоединен к толстой кишке — может инфицироваться и воспалиться, и такое состояние часто называют просто «аппендицит».
Хронический аппендицит представляет собой воспаление аппендикса, которое длится в течение недель, месяцев или даже лет.
Симптомы хронического аппендицита, которые возникают – особенно боль в нижней правой части живота, где аппендикс находится — могут стихать сами по себе, но только чтобы вернуться позже.
На хронический аппендицит приходится, по статистике, 1,5 процента всех случаев аппендицита.
Когда говорят про аппендицит, обычно имеют в виду острый аппендицит, который начинается с боли в животе вокруг пупка, которая затем мигрирует в правую нижнюю часть живота и усиливается.
Могут присутствовать и другие симптомы, в том числе:
- Тошнота;
- Невыраженная лихорадка;
- Рвота;
- Запор;
- Понос;
- Потеря аппетита;
- Неспособность выпустить газы.
Острый аппендицит, как правило, вызван брюшной инфекцией, которая распространилась на аппендикс, или сдавливанием — например, твердые каловые массы при запоре, посторонний предмет, или язва — которые заблокировали просвет червеобразного отростка (внутренняя полость аппендикса).
Если аппендикс не удаляется своевременно, давление внутри органа будет увеличиваться до тех пор, пока аппендикс не прорвется, высвобождая свое содержимое в брюшную полость, что может привести к другим серьезным инфекциям.
- Твердые каловые конкременты, называемые еще копролит;
- Увеличенные лимфатические ткани на стене аппендикса;
- Опухоли;
- Посторонние предметы, такие как булавки, камни, пули.
Со временем воспаление аппендикса будет ухудшаться и его внутреннее давление нарастать.
Но вместо разрыва, содержимое аппендикса под давлением будет выбрасываться в кишечник.
После «выброса», симптомы хронического аппендицита частично или полностью стихают — до тех пор, пока заблокированное содержимое не начнет воспаляться вновь.
Как и острый аппендицит, хронический аппендицит чаще всего характеризуется болью в нижнем правом боку живота.
Боль может быть резкой и сильной, как при остром аппендиците, но чаще пациент жалуется на тупую боль.
Иногда боль в животе — единственный признак хронического аппендицита.
В некоторых случаях могут наблюдаться и другие типичные симптомы острого аппендицита, в том числе тошнота, лихорадка и понос.
В начале 1900-х годов, диагноз хронический аппендицит был очень распространен.
Но ведь боль в животе может быть вызвана большим списком заболеваний, в том числе кистой яичников, расстройством пищеварения и пищевой аллергией, и т.д.. Врачи часто неправильно диагностировали боль как хронический аппендицит, что и приводило к большому числу неоправданных аппендэктомий (хирургическая операция, при которой аппендикс удаляется).
Хронический аппендицит стал спорным диагнозом, и некоторые эксперты начали сомневаться в том, что такое заболевание вообще существует.
Сегодня хронический аппендицит хорошо документирован в медицинской литературе, но до сих пор врачи иногда ставят своим пациентам другой диагноз, когда они, по сути, имеют хронический аппендицит.
Чаще всего хронический аппендицит путают с другими заболеваниями, которые могут вызвать периодические боли в животе или хроническое воспалении, в том числе:
- Болезнь крона.
- Язвенный колит.
- Синдром раздраженного кишечника.
- Воспалительные заболевания тазовых органов, например инфекция женских половых органов.
Использование методов визуализации, в том числе ультразвука, магнитно-резонансной томографии (МРТ) и, в частности, компьютерной томографии (КТ) — в целом может помочь отличать эти заболевания и хронические воспаления, но они не являются надежными.
Медицинская статистика и отчеты рассказывают о случаях, когда, к примеру, женщину с хроническим аппендицитом направляли на обследование и лечение с предполагаемым диагнозом «воспалительные заболевания органов малого таза» или с пациента с болезнью Крона.
И наоборот — из-за того, что симптомы аппендицита похожи на симптомы многих других заболеваний, иногда ставится неправильный диагноз, в результате чего проводятся ненужные аппендэктомии.
По статистике около 12% операций аппендэктомии, были проведены у пациентов, не имеющих аппендицит, но страдающих другими заболеваниями со схожими симптомами.
Если симптомы хронического аппендицита протекают относительно вяло, врач постарается вылечить заболевание консервативными методами и физиотерапевтическими процедурами.
Больному могут быть назначены спазмолитики, антибиотики, пребиотики и пробиотики а также средства, улучшающие циркуляцию крови. Физиотерапевтические процедуры подбираются с направленным противовоспалительным и улучшающим трофику действием. Народные и домашние средства не избавят пациента от проблемы, но будут хорошими помощниками в комплексном лечении хронического аппендицита консервативным методом.
Категорически запрещены грелки и согревающие компрессы на область живота, так как они могут привести к перитониту.
Если же консервативное лечение не помогает и боль не стихает, будет проведена операция апендэктомия – удаление аппендикса. Операция возможна как открытым способом, так и лапараскопически.
источник
Осложнения НЯК подразделяются на местные и общие (системные). К местным относятся перфорация, токсическая дилатация (токсический мегаколон), кишечные кровотечения, стриктуры прямой или толстой кишки, парапроктиты, свищи, трещины, перианальное раздражение кожи и рак толстой кишки.
Системные осложнения связаны с внекишечными проявлениями язвенного колита.
О причинах, диагностике и видах язвенного колита можно прочитать в статье Язвенный колит .
О методах лечения НЯК читайте здесь.
Перфорация стенки кишки возникает при ее расширении, истончении. Отверстие обычно располагается в сигмовидной кишке или в области селезеночного изгиба.
Чаще перфорации множественные и проникают в брюшную полость, реже они одиночные и прикрытые. При впервые возникшем язвенном колите частота перфорации не превышает 4 %. Тяжелый, длительно протекающий НЯК осложняется перфорацией примерно в 10 % случаев.
Диагностика этого осложнения довольно затруднительна, так как оно вызывает тяжелое состояние больного, и не всегда удается получить от него информацию о беспокоящих его симптомах. Недостаточно информативны и результаты физикального исследования (для перфорации характерны симптомы раздражения брюшины).
Установить диагноз перфорации кишечника помогает рентгенологическое исследование, при котором в брюшной области обнаруживается свободный газ.
Это тяжелое осложнение НЯК, которое развивается в 5-10 % случаев.
К развитию токсической дилатации приводят
- поражение нервно-кишечного аппарата кишечника,
- воспалительное повреждение гладких мышц кишечной стенки,
- гипокалиемия с нарушением мышечного тонуса,
- инфекция (сальмонеллез, шигеллез, иерсиниоз и др.),
- изъязвление,
- токсемия,
- диагностические манипуляции (рентгенологическое исследование, колоноскопия),
- нерациональная лекарственная терапия (назначение опиоидных препаратов, антихолинергических средств).
Некоторые исследователи отмечают влияние стероидной терапии, холинергических средств на развитие данного синдрома.
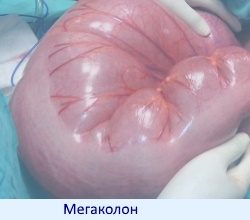
Точно так же как и применение слабительных средств при наличии запоров у больных НЯК, особенно на фоне гипокалиемии, может быть причиной появления признаков токсического мегаколона.
Токсический мегаколон толстой кишки проявляется
- резким ухудшением состояния больного,
- нарастанием интоксикации,
- заторможенностью реакций,
- повышением температуры тела более 38,8⁰С,
- снижением частоты стула,
- увеличением живота,
- ослаблением перистальтических кишечных шумов,
- метеоризмом,
- незначительном напряжением мышц передней брюшной стенки,
- тахикардией более 120 уд/мин.,
- лейкоцитозом свыше 10,6х10⁹/л,
- анемией.
Наиболее важный метод в диагностике этого осложнения — обзорное рентгенологическое исследование брюшной стенки. Оно проводится в положении больного лежа на спине. Характерный рентгенологический признак этого осложнения — значительно расширение ободочной кишки от 5 до 16 см, в среднем на 9 см.
Как правило, наибольшему расширению подвержена поперечная ободочная кишка. И в приблизительно 50 % случаев оно устраняется оперативным вмешательством. Прямая кишка расширению не подвергается.
Прогноз при этом осложнении очень серьезный, особенно при одновременном возникновении токсической дилатации и перфорации толстой кишки.
Консервативная терапия токсического мегаколона проводится обычно в течение 24 часов.
Отменяют все лекарственные препараты, вводившиеся перорально (через рот).
Задача консервативной терапии — коррекция водно-электролитного баланса, дефицита белка и анемии. Обязательно назначают антибиотики, глюкокортикоиды в ударных дозах. Необходимо проводить постоянный контроль состояния больного. Обязателен контроль диуреза. Важным является проведение УЗИ и рентгенологического контроля состояния дилатированной ободочной кишки.
Если у больного с тяжелым течением язвенного колита не удается достичь положительной динамики в течение 2-3 дней, то ему показана срочная хирургическая операция.
Кровотечения как осложнение при НЯК необходимо отличать от выделения алой крови с калом при обычном течении язвенного колита.
При этом осложнении кровь из ануса выделяется сгустками. Массивное кровотечение при язвенном колите развивается не более чем у 1 % больных. Причинами, вызывающими кишечное кровотечение, могут быть разрастания грануляционной ткани на дне язвы, васкулиты дна и краев язв.
Эти изменения сопровождаются некрозом стенки сосудов, флебитами, ведут к резкому сужению вен слизистой, подслизистой и мышечной оболочек кишки, расширению их просвета с образование сосудов, напоминающих широкие лакуны или сосуды кавернозного типа, которые подвергаются разрыву и дают массивные кровотечения.
Хирургическое лечение необходимо больному с кишечным кровотечение в том случае, если для стабилизации состояния больного требуется введение крови в объеме, превышающем 3000 мл в течение 24 часов.
Обнаруживаются приблизительно у 10 % больных с язвенным колитом. У трети пациентов препятствие локализуется в прямой кишке. При наличии стриктур толстой кишки всегда возникает потребность проведения дифференциального диагноза с раком толстой кишки или болезнью Крона.
Полипы диагностируются при эндоскопическом и рентгенологическом исследовании. Характерным признаком этого осложнения, выявляемого при ирригоскопии, служит наличие множественных дефектов наполнения по ходу кишечной стенки. Диагноз псевдополипоза подтверждается гистологически.
Системными называются осложнения, которые поражают различные системы и органы человека. Они встречаются у значительной части больных с тяжелой формой НЯК. Большинство осложнений имеет аутоиммунную природу и является показателем активности патологического процесса. Эти осложнения язвенного колита делят на две группы: связанные с колитом и не зависящие от него.
При язвенном колите могут проявляться как кишечные, так и внекишечные заболевания. Необходимо знать о возможных симптомах, которые на первый взгляд не связаны с кишечником. Это позволит насторожиться, пройти обследование и диагностировать серьезное воспаление кишечника как можно раньше.
Такие проявления болезни возникают у 30 % пациентов, страдающих от НЯК. Наблюдается определенная зависимость между внекишечными проявлениями, протяженностью поражения толстой кишки и тяжестью заболевания.
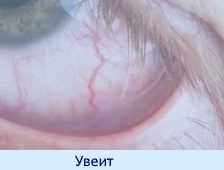
- эписклерит;
- увеит;
- ретробульбарный неврит;
- иридоциклит;
- кератит;
- облитерирующий артериит сетчатки.
Из этих заболеваний чаще всего встречается увеит. Причем нередко глазные симптомы определяются за много лет до проявления кишечных симптомов неспецифического язвенного колита.
Обострение глазных болезней развивается на фоне тяжелых обострений язвенного колита и может привести даже к слепоте. Причем патология глаз может сохраняться и в периоды ремиссии основного заболевания.
- длительное покраснение глаза;
- деформация зрачка;
- появление “мушек” перед глазами,
- ухудшение остроты зрения,
- появление вспышек и мерцания перед глазами,
- форма предметов искажается,
- зрение затуманивается,
- трудности при чтении,
- ухудшение сумеречного зрения, нарушение цветоощущения.
Эти осложнения встречаются у 15 % людей с болезнью язвенный колит и их течение связано непосредственно с обострениями этого заболевания.
Этот вид осложнений проявляется следующими заболеваниями:
- узловатая эритема;
- некротическая пиодермия;
- афтозный стоматит;
- гингивит;
- изъязвления нижних конечностей (многоформная эритема);
- псориаз.
Поражение слизистой оболочки полости рта чаще проявляется у больных
- с анемией,
- с дефицитом массы тела,
- с авитаминозом.
Это заболевание относительно часто встречается при НЯК. Прогрессирование болезни может привести к развитию гангренозного стоматита.
Это осложнение часто сочетается с артритом (хроническое воспаление суставов) и довольно часто является первым проявлением язвенного колита.
Проявляется узловатая эритема такими симптомами, как:
- появление плотных узлов разного диаметра от 5 мм до 5 см,
- над узлами кожа красная и гладкая,
- узлы немного возвышаются над общим кожным покровом, но четких границ не наблюдается,
- ткани вокруг узлов отекают,
- узлы вырастают очень быстро, но, увеличившись до определенного размера, они прекращают расти,
- боль при пальпации,
- через 3-5 дней узлы меняют цвет, кожа становится буроватой, потом синеет и постепенно желтеет,
- узлы чаще появляются на передней поверхности голеней,
- чаще всего заболевание начинается остро, с лихорадкой.
Кожа поражается на фоне тяжелого течения болезни, чаще всего на голенях и в области грудины. Появление этого осложнения позволяет сделать выводы о развитии сепсиса (заражения крови).
В последнее время описываются такие осложнения НЯК, как
- очаговый дерматит,
- фурункулы,
- поверхностные кожные абсцессы,
- изъязвления кожи,
- кожные высыпания (макулярные, папулезные, пустулезные, уртикарные).
Эти осложнения возникают у 20-60 % больных язвенным колитом. Они проявляются чаще при хронической форме заболевания.
Диагнозы, которые могут быть следствием язвенного колита:
- остеопатия;
- перифирические артриты;
- анкилозирующий спондилит;
- артралгия;
- сакроилеит.
Артриты (болезнь суставов) встречаются одинаково часто как у взрослых, так и у детей, как у мужчин, так и у женщин. При язвенном колите чаще поражаются суставы верхних конечностей и мелкие суставы, при болезни Крона — коленные и голеностопные суставы.
Это осложнение возникает, как правило, при значительном поражении ободочной кишки. Обострения заболевания в 60-70 % случаев связаны с обострениями НЯК.
Основными симптомами являются:
- опухание суставов;
- болезненность;
- покраснение кожи над суставами;
- выпот в синовиальную полость.
При каждом обострении, как правило, поражается не более трех суставов. Причем от приступа к приступу могут страдать разные суставы.
Анкилозирующий спондилит нередко сочетается с периферическим артритом, увеитом и псориазом.
Основными симптомами спондилита являются:
- боль в спине;
- малоподвижность позвоночника;
- улучшение состояния при движении и выполнении упражнений.
Заболевание может прогрессировать и при ремиссии язвенного колита и нередко приводит к инвалидности.
Часто язвенный колит сопровождают такие заболевания, как:
- жировой гепатоз печени;
- абсцесс печени;
- камни желчного пузыря;
- склерозирующий холангит.
По частоте жировой гепатоз печени занимает первое место. Процесс не прогрессирует и нет тенденции трансформации его в цирроз печени. Строгое соблюдение режима питания, нормализация массы тела, нормальное содержание белка, витаминов и микроэлементов крови значительно улучшает состояние больного и положительно влияет на течение заболевания.
При этом осложнении следует особенно внимательно относиться к введению и длительности парентерального питания, так как вводимые при этом растворимые аминокислоты могут оказывать токсическое действие на печень.
Одно из самых грозных осложнений НЯК. В его развитии имеют большое значение наследственные и иммунологические факторы.
Для него характерны воспалительный фиброз, стриктуры внепеченочных и внутри- печеночных желчных протоков, может сопровождаться панкреатитом. Данная патология встречается чаще у молодых мужчин и проявляется следующими симптомами:
- кожный зуд;
- лихорадка;
- боли в правом подреберье.
Желчнокаменная болезнь развивается при язвенном колите, как следствие нарушения всасывания желчных кислот в тощей кишке из-за хронической диареи.
Тяжесть заболевания напрямую связана с протяженностью поражения тощей кишки. При диарее происходит связывание желчных кислот и кальция , а пищевые оксалаты остаются в просвете кишки и интенсивно всасываются при повышенной проницаемости слизистой оболочки кишечника.
Как правило, при язвенном колите развивается железо-дефицитная анемия, В₁₂-дефицитная анемия, аутоиммунная гемолитическая анемия.
При НЯК увеличивается риск развития флеботромбозов. Причиной этого является высокий уровень фибриногена в острую фазу заболевания и низкая концентрация антитромбина.
К внешним факторам, провоцирующим это осложнение, относятся гидратация, постельный режим, парентеральное питание.
Может отмечаться тромбоз печеночных вен, эмболия легочной артерии, которые могут быть причиной смерти при воспалительных заболеваниях кишечника.
В медицинской практике отмечены относительно редкие случаи заболеваний, развитие которых также непосредственно связано с язвенным колитом:
- бронхолегочные заболевания (легочный фиброз, бронхит, бронхоэктазы),
- заболевания сердца (миокардит, перикардит, септический эндокардит).
При развитии этих заболеваний и неэффективности их лечения следует провести обследование желудочно-кишечного тракта, так как если они являются осложнениями его воспаления, то без комплексной терапии невозможно достичь хорошего результата.
источник
Колл-центр: +7 (812) 235-71-65
будни с 08:30 час. до 19:00 час.
Автор — Элина Александровна Кондрашина
Гастроэнтеролог-консультатнт городского центра диагностики и лечения воспалительных заболеваний кишечника на базе СПБ ГБУЗ «Городская клиническая больница № 31»,
доцент кафедры гастроэнтерологии и диетологии СПб ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И.И.Мечникова»
Какие чувства обычно возникают у человека, когда он впервые узнает о своем заболевании – язвенном колите? Одного охватывает растерянность, страх и отчаяние. Другой, поняв, что беспокоящие его симптомы не являются онкологической патологией, наоборот, излишне легкомысленно относится к своему заболеванию и не придает ему должного значения. Причина такого отношения пациентов к своему недугу кроется в неизвестности и недостатке нужной им информации.
Зачастую у врачей не хватает времени и необходимых знаний, чтобы подробно рассказать больному о его болезни, дать исчерпывающие ответы на закономерно возникающие вопросы пациента и его родных. А дефицит знаний о сути язвенного колита, его проявлениях, последствиях, необходимости полноценного обследования, современных терапевтических и хирургических возможностях отрицательным образом сказывается на результатах лечения.
Язвенный колит является серьезным хроническим заболеванием. При неблагоприятном развитии он может представлять угрозу для жизни больного, приводит к тяжелым осложнениям и инвалидизации. Заболевание требует длительного грамотного лечения с индивидуальным подбором лекарственных препаратов и врачебного наблюдения не только в стационаре, но и в условиях поликлиники или амбулаторного специализированного центра. В то же время данный недуг не представляет собой «смертный приговор». Мощные современные лекарственные средства и своевременное оперативное лечение приводят к длительной ремиссии. У многих больных язвенным колитом в период ремиссии качество жизни мало отличается от состояния здоровых людей. Они полностью справляются с домашними обязанностями, добиваются успехов на профессиональном поприще, рожают и воспитывают детей, посещают спортивные клубы, путешествуют.
Цель этой брошюры заключается в предоставлении пациентам необходимых для них сведений: о язвенном колите, о процедурах, без которых невозможно установить диагноз и выяснить тяжесть, а также протяженность воспалительного процесса в кишечнике, о существующих в арсенале российских врачей лекарствах, возможностях медикаментозной терапии и хирургического лечения, о профилактике обострений и осложнений этого заболевания.
Язвенный колит (ЯК) – это хроническое воспалительное заболевание кишечника, поражающее, слизистую оболочку толстой кишки, имеющее прогрессирующее течение нередко с развитием опасных для жизни осложнений. В России данное заболевание также нередко называют неспецифическим язвенным колитом.
Воспаление всегда начинается с прямой кишки, непрерывно распространяясь выше вплоть до поражения слизистой оболочки всех отделов толстой кишки. Выраженность воспалительных изменений может быть различной, варьируя от умеренного покраснения до образования обширных язвенных дефектов.
Хотя ЯК впервые был описан в 1842 году в докладе видного ученого К. Рокитанского «О катаральном воспалении кишечника», причины его возникновения до настоящего времени остаются неизвестными, что не может не сказаться на эффективности его лечения.
Заболеваемость ЯК в развитых странах мира (США, страны Северной Европы) составляет 2 – 15 больных на 100 000 населения. В Российской Федерации она достигает 4 – 10 случаев на 100 000 населения, в настоящее время в нашей стране этот статистический показатель уточняется. Частота возникновения ЯК обычно оказывается более высокой в крупных городах северных регионов. Заболевание встречается с одинаковой частотой и у мужчин, и у женщин.
Нередко при тщательном расспросе больного ЯК выясняется, что схожие жалобы имеются и у некоторых членов его семьи. Заболеваемость ЯК при наличии близких родственников с данной патологией увеличивается на 10 – 15 %. Если же болезнь поражает обоих родителей, то риск возникновения ЯК у ребенка к 20-летнему возрасту достигает 52 %.
ЯК может поражать людей любого возраста, однако наибольшая частота дебюта заболевания встречается в 2 возрастных группах (у лиц — 20 — 40 лет и 60 — 80 лет). Наивысшие показатели смертности отмечаются в течение 1-го года (при крайне тяжелом молниеносном течении ЯК) и через 10 – 15 лет после начала заболевания в результате развития грозного осложнения — рака толстой кишки, который чаще появляется при полном тотальном поражении слизистой оболочки толстой кишки. При адекватном лечении и врачебном наблюдении продолжительность жизни больных ЯК не отличается от средней продолжительности жизни человека в целом.
Как и в случае любого другого хронического заболевания, течение ЯК характеризуется периодами обострений (рецидивов) и ремиссий. Во время обострения состояние больного ухудшается, появляются характерные клинические проявления заболевания (например, кровь в стуле). Выраженность клинических признаков ЯК отличается у разных людей. При наступлении ремиссии самочувствие пациента значительно улучшается. У большинства больных исчезают все жалобы, пациенты возвращаются к привычному для них до заболевания образу жизни. Продолжительность периодов обострений и ремиссии также является индивидуальной. При благоприятном течении заболевания ремиссия может длиться десятилетиями.
К сожалению, происхождение заболевания до сих пор окончательно не установлено. Вероятно ученые, которые найдут убедительную причину ЯК, заслужат присуждения Нобелевской премии.
На роль факторов, провоцирующих развитие ЯК претендуют воздействия внешней среды (питание рафинированными продуктами, увлечение фаст-фудом, стрессы, детские и кишечные инфекции, прием таких негормональных противовоспалительных и обезболивающих лекарственных средств, как аспирин, индометацин и др), поломки в генетическом аппарате больных, микробы, постоянно обитающие или попадающие извне в кишечник здорового человека. С каждым годом появляется все больше серьезных научных исследований, посвященных поиску причин ЯК, но пока их результаты противоречивы и недостаточно убедительны.
В современной медицине считается установленным, что в результате действия этой неизвестной причины возникают нарушения в иммунной системе больного ЯК. Иммунная система вместо своей прямой обязанности, заключающейся в уничтожении чужеродных клеток (микробных, вирусных, клеток грибов и паразитов, раковых), начинает разрушать собственную кишечную слизистую оболочку. Вследствие развития сложных иммунных механизмов с участием специальных белков – цитокинов возникает воспалительный процесс, появляются участки поврежденной слизистой оболочки в виде эрозий и язв. Инфицирование язв приводит к образованию гноя. В результате разъедания кровеносных сосудов возникает кровотечение.
Кроме этого, существуют факторы внешней среды, защищающие от развития ЯК. К ним относятся курение и хирургическое удаление червеобразного отростка – аппендикса (аппендэктомия). Так, вероятность возникновения заболевания у некурящих в 4 раза выше, чем у курящих лиц. Следует заметить, что при прекращении табакокурения людьми, которые ранее длительно и много курили, относительный риск развития ЯК в 4,4 раза превышает аналогичный показатель у некурящих. Аппендэктомия снижает риск развития заболевания при условии, что операция была выполнена в связи с острым аппендицитом в молодом возрасте.
У большинства больных (у 75%) заболевание начинается постепенно. Иногда пациенты на протяжении долгого времени не обращаются за квалифицированной помощью врача-специалиста, расценивая наличие крови в стуле, как проявление хронического геморроя. Между появлением первых симптомов ЯК и моментом установления диагноза может пройти от 10 месяцев до 5 лет. Гораздо реже ЯК дебютирует остро.
Выраженность клинических проявлений ЯК зависит от протяженности воспалительного поражения и тяжести заболевания.Характерные ЯК для симптомы можно разделить на три группы:
Наиболее частыми кишечными симптомами являются нарушения стула в виде поноса (у 60–65 % больных ЯК частота стула составляет от 3–5 до 10 и более раз в сутки небольшими порциями) или запора (в 16–20 % случаев, в основном при поражении нижних отделов толстой кишки). Более чем у 90% пациентов в кале обнаруживается примесь крови. Ее количество различно (от прожилок до стакана и более). При воспалении нижних отделов толстой кишки кровь обычно имеет алый цвет и располагается поверх кала. Если же заболевание затронуло большую часть толстой кишки, то кровь появляется в виде сгустков темно-вишневого цвета, перемешанных с каловыми массами. Нередко в стуле пациенты замечают также патологические примеси гноя и слизи. Характерными клиническими признаками ЯК являются недержание кала, безотлагательные позывы на опорожнение кишечника, ложные позывы с выделением из заднего прохода крови, слизи и гноя, практически без каловых масс («ректальный плевок»). В отличие от пациентов с функциональными кишечными расстройствами (синдром раздраженного кишечника) стул у больных ЯК бывает также и в ночное время. Кроме этого, около 50% больных предъявляют жалобы на боли в животе, как правило, умеренной интенсивности. Чаще боли возникают в левой половине живота, после отхождения стула они ослабевают, реже усиливаются.
Общие или системные симптомы ЯК отражают влияние заболевания не только на толстую кишку, но и на весь организм больного в целом. Их появление свидетельствует о тяжелом и распространенном воспалительном процессе в кишечнике. Вследствие интоксикации и потери вместе с жидким стулом и кровью полезных веществ у больного развиваются повышение температуры тела, потеря аппетита, тошнота и рвота, учащение сердцебиения, снижение массы тела, обезвоживание, малокровие (анемия), гиповитаминозы и др. Нередко у пациентов возникают различные нарушения со стороны психо-эмоциональной сферы.
Внекишечные проявления ЯК, встречающиеся у 30% больных, являются результатом иммунных нарушений. Выраженность большинства из них сопряжена с активностью ЯК. Следует заметить, что пациенты часто не связывают эти симптомы с патологией кишечника и ищут помощи у различных врачей-специалистов (ревматологов, невропатологов, окулистов, дерматологов, гематологов и др.). Иногда их появление предшествует кишечной симптоматике. В болезнетворный процесс могут вовлекаться самые различные органы.
При поражении опорно-двигательного аппарата больные предъявляют жалобы на боли, припухлость, снижение подвижности различных суставов (коленных, голеностопных, тазобедренных, локтевых, лучезапястных, межфаланговых и др.). Как правило, боли мигрируют от одного сустава к другому, не оставляя значимых деформаций. Поражение крупных суставов обычно связано с выраженностью воспалительного процесса в кишечнике, а артропатия мелких суставов протекает независимо от активности ЯК. Длительность описанного суставного синдрома иногда достигает до нескольких лет. Также могут появляться воспалительные изменения позвоночника с ограничением его подвижности (спондилит) и крестцово-подвздошных сочленений (сакроилеит).
Поражения кожи и слизистой оболочки ротовой полости у больных ЯК проявляются в виде различных высыпаний. Типичными являются болезненные красные или фиолетовые подкожные узелки на руках или голенях (узловатая эритема), пузырьки на участках с небольшой толщиной подкожной клетчатки – голенях, в области грудины, самостоятельно вскрывающиеся с образованием язв (гангренозная пиодермия), язвочки на слизистой оболочке щек, десен, мягкого и твердого неба.
При вовлечении глазу больных ЯК развиваются боль, зуд, жжение в глазах, покраснение глаз, светобоязнь, ощущение «песка в глазах», ухудшение зрения, головные боли. Такие жалобы сопровождают появление воспаления слизистой оболочки глаза (конъюнктивита), радужной оболочки (ирита), белой оболочки глаза (эписклерита), среднего слоя глаза (увеита), роговицы (кератита) и зрительного нерва. Для правильной диагностики пациентам необходима консультация окулиста и проведение исследования с применением щелевой лампы.
Нередко к внекишечным симптомам ЯК относятся признаки поражения других органов пищеварения (печени и желчных путей (в т.ч. плохо поддающийся медикаментозному лечению первичный склерозирующий холангит), поджелудочной железы), нарушения в системе крови (флебиты, тромбозы, аутоиммунная гемолитическая анемия).
Европейским консенсусом по диагностике и лечению ЯК, принятым Европейской организацией Крона и колита в 2006 г., по распространенности ЯК выделяют три формы заболевания:
- проктит (воспалительное поражение ограничено только прямой кишкой), проксимальной границей воспаления является ректосигмоидный угол),
- левосторонний колит (воспалительный процесс, начинаясь от прямой кишки, достигает селезеночного изгиба ободочной кишки)
- распространенный колит (воспаление распространяется выше селезеночного изгиба ободочной кишки).
Отечественные доктора также часто используют термины: ректосигмоидит или дистальный колит (вовлечение в воспалительный процесс прямой и сигмовидной кишки), субтотальный колит (воспаление достигает печеночного изгиба ободочной кишки), тотальный колит или панколит (заболевание затронуло всю толстую кишку).
В зависимости от тяжести заболевания, которая оценивается лечащим врачом по совокупности клинических, эндоскопических и лабораторных показателей выделяют три степени тяжести: легкую, средней степени и тяжелую.
Являясь серьезным заболеванием, в случае неблагоприятного течения при отсутствии надлежащей терапии ЯК имеет грозные для жизни пациентов осложнения. Нередко в таких случаях необходима хирургическая операция .
- Токсическая дилатация толстой кишки (токсический мегаколон). Данное осложнение заключается в чрезмерном расширении просвета толстой кишки (до 6 см в диаметре и более), сопровождающимся резким ухудшением самочувствия больного, лихорадкой, вздутием живота, уменьшением частоты стула.
- Кишечные массивные кровотечения. Такие кровотечения развиваются при поражении крупных сосудов, кровоснабжающих кишечную стенку. Объем кровопотери превышает 300 – 500 мл в сутки.
- Перфорация стенки толстой кишки.Возникает при перерастяжении и истончении кишечной стенки. При этом все содержимое просвета толстой кишки попадает в брюшную полость и вызывает в ней грозный воспалительный процесс — перитонит.
- Стриктура толстой кишки.Сужение просвета толстой кишки встречается в 5 – 10 % случаев ЯК. При этом у некоторых больных нарушается прохождение каловых масс по толстой кишке и возникает кишечная непроходимость. Каждый случай обнаружения стриктуры при ЯК требует тщательного обследования пациента для исключения болезни Крона и рака толстой кишки.
- Рак толстой кишки (колоректальный рак). Онкологический процесс развивается, как правило, при длительном течении ЯК, чаще при тотальном поражении толстой кишки. Так, в первые 10 лет течения ЯК развитие колоректального рака отмечается у 2% больных, в первые 20 лет – у 8%, при длительности более 30 лет – у 18%.
Перед обсуждением методов обследования, позволяющих правильно установить диагноз, хочется обратить внимание,что воспалительные и язвенные поражения слизистой оболочки толстой кишки далеко не всегда являются проявлением ЯК. Список заболеваний, протекающих со схожей клинической и эндоскопической картиной велик:
- инфекционные колиты (бактериальные, вирусные, паразитарные),
- болезнь Крона,
- ишемический колит (связан с недостаточным кровоснабжением кишечной стенки),
- дивертикулит,
- ассоциированный с приемом лекарственных препаратов колит,
- радиационный колит,
- рак ободочной кишки,
- солитарная язва прямой кишки
- эндометриоз и др.
Лечение же перечисленных заболеваний различается. Поэтому при появлении рассмотренных выше симптомов пациенту обязательно нужно обратиться за квалифицированной врачебной помощью, а не заниматься самолечением.
Для полного видения врачом картины заболевания и выбора оптимальной лечебной тактики должно быть проведено комплексное обследование больного. Необходимые диагностические процедуры включают лабораторные и инструментальные методы.
Анализы крови необходимы для оценки активности воспаления, степени кровопотери, выявления нарушений обмена веществ (белкового, водно-солевого), вовлечения в патологический процесс печени, других органов (почек, поджелудочной железы и др.), определения эффективности проводимого лечения, отслеживания побочных реакций от принимаемых лекарств.
Однако, к сожалению, пока не существует анализов крови «на язвенный колит», достаточных для постановки диагноза. Современные иммунологические исследования на специфические показатели (перинуклеарные цитоплазматические антинейтрофильные антитела (рANCA), антитела к сахаромицетам (ASCA) и др.) служат лишь дополнительным подспорьем при трактовке результатов всех проведенных обследований и дифференциальной диагностике ЯК и болезни Крона.
Анализы кала, которые возможно выполнить в любой поликлинике и стационаре (копрограмма, реакция Грегерсена – исследование на скрытую кровь) позволяют выявить невидимые невооруженному глазу патологические примесикрови, гноя, слизи. Бактериологические (посевы) и молекулярно-генетические (ПЦР) исследования стула обязательны для исключения инфекционной патологии и подбора антибиотиков. Сравнительно новым перспективным исследованием считается определение в кале показателей кишечного воспаления (фекального кальпротектина, лактоферрина и др.), позволяющее исключить функциональные расстройства (синдром раздраженного кишечника).
Эндоскопические процедуры занимают ведущее место в диагностике воспалительных заболеваний кишечника. Они могут проводиться как в амбулаторных, так и в стационарных условиях. Перед обследованием кишечника очень важно получить рекомендации врача по правильной подготовке к процедуре. В зависимости объема эндоскопического исследования для полноценной очистки кишечника обычно используют специальные слабительные препараты, очистительные клизмы или их комбинацию. В день исследования разрешается прием только жидкостей. Суть процедуры заключается во введении через задний проход в кишечник эндоскопического аппарата – трубки с источником света и присоединенной видеокамерой на конце. Это позволяет доктору не только оценить состояние слизистой оболочки кишечника, выявить характерные признаки ЯК, но и произвести безболезненный забор нескольких биоптатов (маленьких кусочков кишечной ткани) с помощью специальных щипцов. Биоптаты в дальнейшем используются для осуществления гистологического исследования, необходимого для правильной постановки диагноза.
В зависимости от объема обследования кишечника проводят:
- ректороманоскопию (осмотр жестким ректороманоскопом прямой и части сигмовидной кишки),
- фибросигмоидоскопию (исследование гибким эндоскопом прямой и сигмовидной кишки),
- фиброколоноскопию (исследование гибким эндоскопом толстой кишки),
- фиброилеоколоноскопию (обследование гибким эндоскопом всей толстой и участка тонкой (подвздошной) кишки).
Предпочтительным диагностическим исследованием является фиброилеоколоноскопия, позволяющая отличить ЯК от болезни Крона. Для уменьшения неприятных ощущений пациента во время процедуры часто используется поверхностный наркоз. Длительность этого исследования составляет от 20 минут до 1,5 часов.
Рентгенологические исследования толстой кишки проводятся при невозможности проведения полноценного эндоскопического осмотра.
Ирригоскопия(клизма с барием) также может быть осуществлена в условиях больницы или амбулаторно. Накануне исследования пациент принимает слабительное средство, ему делают очистительные клизмы. Во время исследования в кишку больному с помощью клизмы вводят контрастное вещество — бариевую взвесь, затем выполняют рентгенологические снимки толстой кишки. После опорожнения в кишку вводят воздух, который раздувает ее, и снова делают рентгенологические снимки. Полученные изображения могут выявить участки воспаленной и изъязвленной слизистой толстой кишки, а также ее сужения и расширения.
Обзорная рентгенография брюшной полости у больных ЯК позволяет исключить развитие осложнений: токсической дилатации кишки и ее перфорации. Специальной подготовки больного не требует.
Ультразвуковое исследование (УЗИ) органов брюшной полости, гидроколоно-УЗИ, лейкоцитарная сцинтиграфия, выявляющие воспалительный процесс в толстой кишке, имеют низкую специфичность в дифференцировке ЯК от колитов другого происхождения. Диагностическая значимость МРТ- и КТ-колонографии (виртуальной колоноскопии) продолжает уточняться.
Иногда чрезвычайно сложно отличить ЯК от болезни Крона, для этого требуются дополнительные обследования: иммунологические, рентгенологические (энтерография, гидроМРТ) и эндоскопические (фибродуоденоскопия, энтероскопия, исследование с помощью эндоскопической видеокапсулы) обследования тонкой кишки. Правильная постановка диагноза важна, так как, несмотря на то, что в развитии обоих заболеваний задействованы иммунные механизмы, в некоторых ситуациях лечебные подходы могут принципиально различаться. Но даже в развитых странах при полноценном обследовании не менее чем в 10-15% случаев не удается отличить друг от друга эти две патологии. Тогда устанавливается диагноз недифференцированного (неклассифицированного) колита, имеющего анамнестические, эндоскопические, рентгенологические и гистологические признаки, как ЯК, так и болезни Крона.
Задачами лечения больного ЯК являются:
- достижение и поддержание ремиссии (клинической, эндоскопической, гистологической),
- минимизация показаний к хирургическому лечению,
- уменьшение частоты осложнений и побочных эффектов лекарственной терапии,
- сокращение сроков госпитализации и стоимости лечения,
- улучшение качества жизни пациента.
Результаты лечения во многом зависят не только от усилий и квалификации доктора, но и от силы воли пациента, четко выполняющего врачебные рекомендации. Имеющиеся в арсенале врача современные лекарственные препараты позволяют многим пациентам вернуться к нормальной жизни.
Комплекс лечебных мероприятий включает:
- соблюдение диеты (диетотерапия)
- прием лекарственных препаратов (медикаментозная терапия)
- хирургическое вмешательство (оперативное лечение)
- изменение образа жизни.
Диетотерапия. Обычно больным ЯК в период обострения рекомендуется вариант бесшлаковой (с резким ограничением клетчатки) диеты, цель которой заключается в механическом, термическом и химическом щажении воспаленной слизистой оболочки кишечника. Клетчатку ограничивают путем исключения из рациона свежих овощей и фруктов, бобовых, грибов, жесткого, жилистого мяса, орехов, семечек, кунжута, мака. При хорошей переносимости допустимы соки без мякоти, консервированные (лучше в домашних условиях) овощи и фрукты без семян, спелые бананы. Разрешаются хлебобулочные изделия и выпечка только из рафинированной муки. При поносах блюда подают в теплом виде, протертыми, ограничивают продукты с большим содержанием сахара. Употребление алкоголя, острых, соленых, продуктов, блюд с добавлением специй крайне нежелательно. В случае непереносимости цельного молока и молочнокислых продуктов они также исключаются из питания больного.
При тяжелом течении заболевания с потерей массы тела, снижением уровня белка в крови увеличивают в рационе питания суточное количество белка, рекомендуя нежирное мясо животных и птиц (говядина, телятина, курица, индейка, кролик), нежирную рыбу (судак, щука, минтай), гречневую и овсяную каши, белок куриного яйца. С целью восполнения потерь белка также назначают искусственное питание: через вену вводят специальные питательные растворы (чаще в условиях стационара) или через рот или зонд специальные питательные смеси, в которых основные пищевые ингредиенты были подвергнуты специальной обработке для их лучшей усвояемости (организму не надо тратить свои силы на переработку этих веществ). Такие растворы или смеси могут служить дополнением к естественному питанию или полностью его заменять. В настоящее время уже созданы специальные питательные смеси для больных с воспалительными заболеваниями кишечника, содержащие также противовоспалительные вещества.
Несоблюдение принципов лечебного питания в период обострения может повлечь усугубление клинической симптоматики (поносов, боли в животе, наличия патологических примесей в стуле) и даже спровоцировать развитие осложнений. Кроме того, следует помнить, что реакция на различные продукты у разных больных индивидуальна. Если обращает внимание ухудшение самочувствия после употребления в пищу какого-либо продукта, то после консультации с лечащим врачом он также должен быть устранен из питания (хотя бы в период обострения).
Медикаментозная терапия определяется:
- распространенностью поражения толстой кишки;
- тяжестью ЯК, наличием осложнений заболевания;
- эффективностью предыдущего курса лечения;
- индивидуальной переносимостью пациентом лекарственных препаратов.
Лечение при легких и среднетяжелых формах заболевания может проводиться в амбулаторных условиях. Пациентам с тяжелым ЯК необходима госпитализация. Выбор лечащим врачом необходимых лекарственных средств осуществляется пошагово.
При легком и среднетяжелом течении заболевания обычно лечение начинают с назначения 5-аминосалицилатов (5-АСК). К ним относятся сульфасалазин и месалазин. В зависимости от протяженности воспалительного процесса при ЯК эти лекарственные средства рекомендуют в виде свечей, клизм, пен, которые вводят через задний проход, таблеток или сочетания местных и таблетированных форм. Препараты уменьшают воспаление в толстой кишке в период обострения, используются для поддержания ремиссии, а также являются доказанным средством профилактики развития рака толстой кишки при условии их длительного приема. Побочные эффекты чаще возникают на фоне приема сульфасалазина в виде тошноты, головной боли, усиления поноса и боли в животе, нарушения функции почек.
Если улучшения не наступает или заболевание имеет более тяжелое течение, то больному ЯК назначают гормональные препараты — системные глюкокортикоиды (преднизолон, метилпреднизолон, дексаметазон). Эти препараты быстрее и результативнее справляются с воспалительным процессом в кишечнике. При тяжелом течении ЯК глюкокортикоиды вводят внутривенно. Из-за серьезных побочных эффектов (отеки, повышение артериального давления, остеопороз, увеличение уровня глюкозы крови и др.) они должны приниматься по определенной схеме (с постепенным снижением суточной дозы препарата до минимальной или вплоть до полной отмены) под строгим руководством и контролем лечащего врача. У некоторых пациентов отмечаются явления стероидорефрактерности (отсутствие ответа на лечение глюкокортикоидами) или стероидозависимости (возобновление клинических симптомов обострения ЯК при попытке снижения дозы или вскоре после отмены гормонов). Следует заметить, что в период ремиссии гормональные препараты не являются средством профилактики новых обострений ЯК, поэтому одной из целей должно быть удержание ремиссии без глюкокортикоидов.
При развитии стероидозависимости или стероидорефрактерности, тяжелом или часто рецидивирующем течении заболевания показано назначение иммуносупрессантов (циклоспорин, такролимус, метотрексат, азатиоприн, 6-меркаптопурин). Препараты данной группы подавляют активность иммунной системы, тем самым блокируя воспаление. Наряду с этим, влияя на иммунитет, снижают сопротивляемость организма человека к различным инфекциям, оказывают токсичное воздействие на костный мозг.
Циклоспорин, такролимус являются быстродействующими препаратами (результат очевиден через 1-2 недели). Их своевременное применение у 40-50 % больных с тяжелым ЯК позволяет избежать хирургического лечения (удаления толстой кишки). Препараты вводятся внутривенно или назначаются в виде таблеток. Однако их использование ограничивают высокая стоимость и значимые побочные эффекты (судороги, повреждение почек и печени, повышение артериального давления, желудочно-кишечные расстройства, головная боль др.).
Метотрексат является лекарственным средством для внутримышечного или подкожного введения. Его действие разворачивается через 8 – 10 недель. При применении метотрексата также приходится считаться с его высокой токсичностью. Препарат запрещен к применению у беременных женщин, так как вызывает пороки развития и гибель плода. Эффективность применения у больных ЯК уточняется.
Азатиоприн, 6-меркаптопурин являются препаратами с медленным действием. Эффект от их приема развивается не ранее, чем через 2-3 месяца. Препараты способны не только вызывать, но и удерживать ремиссию при длительном применении. Кроме этого, назначение азатиоприна или 6-меркаптопурина позволяет постепенно отказаться от приема гормональных препаратов. Они обладают меньшим по сравнению с другими иммуносупрессантами количеством побочных эффектов, хорошо сочетаются с препаратами 5-АСК и глюкокортикоидами. Однако, в связи с тем, что у некоторых пациентов тиопурины оказывают токсическое воздействие на костный мозг, больным обязательно следует периодически выполнять клинический анализ крови для мониторинга этого побочного эффекта и проведения своевременных лечебных мероприятий.
В конце XX века революцией в лечении больных воспалительными заболеваниями кишечника (болезнь Крона, ЯК) оказалось применение принципиально новых лекарственных средств — биологических (антицитокиновых) препаратов. Биологические препараты – это белки, которые избирательно блокируют работу определенных цитокинов – ключевых участников воспалительного процесса. Такое селективное действие способствует более быстрому наступлению положительного эффекта и вызывает меньшее по сравнению с другими противовоспалительными препаратами число побочных эффектов. В настоящее время во всем мире идет активная работа по созданию и усовершенствованию новых и уже существующих биологических препаратов (адалимумаб, цертолизумаб и др.), проводятся их широкомасштабные клинические испытания.
В России для лечения больных воспалительными заболеваниями кишечника (ЯК и болезни Крона) пока зарегистрирован единственный препарат этой группы – инфликсимаб (торговое название – Ремикейд). Механизм его действия заключается в блокировке множественных эффектов центрального провоспалительного (поддерживающего воспаление) цитокина – фактора некроза опухоли α. Сначала в 1998 году препарат был лицензирован в США и Европе, как резервное лекарственное средство терапии рефрактерной и свищевой форм болезни Крона. В октябре 2005 года на основании накопившегося опыта высокой клинической эффективности и безопасности применения инфликсимаба в лечении больных ЯК круглый стол, посвященный разработке новых стандартов лечения ЯК и БК в странах ЕС и США, постановил включить в перечень показаний к лечению инфликсимабом и ЯК. С апреля 2006 года инфликсимаб (ремикейд) рекомендован для лечения больных тяжелым язвенным колитом и в России.
Инфликсимаб стал настоящим прорывом в современной медицине и считается «золотым стандартом», с которым в настоящее время сравнивается большинство новых препаратов (адалимумаб, цертолизумаб и др.), находящихся на стадии клинических исследований.
При ЯК инфликсимаб (Ремикейд) назначается:
- пациентам, у которых неэффективна традиционная терапия (гормоны, иммуносупрессанты)
- пациентам, зависимым от гормональных препаратов (отмена преднизолона невозможна без возобновления обострения ЯК)
- пациентам с умеренным и тяжелым течением заболевания, которое сопровождается поражением других органов (внекишечные проявления ЯК)
- пациентам, которые в противном случае нуждались бы в хирургическом лечении
- пациентам, у которых успешное лечение инфликсимабом вызвало ремиссию (для ее поддержания).
Инфликсимаб вводят в виде внутривенной инфузии в процедурном кабинете или в центре антицитокиновой терапии. Побочные эффекты наблюдаются редко и включают повышение температуры тела, боль в суставах или мышцах, тошноту.
Инфликсимаб по скорости купирования симптомов опережает преднизолон. Так, у некоторых пациентов уже в течение первых 24 часов после введения препарата наступает улучшение самочувствия. Уменьшаются боль в животе, понос, кровотечение из заднего прохода. Происходит восстановление физической активности, повышается аппетит. Для некоторых пациентов впервые становится возможной отмена гормонов, у других – спасение толстой кишки от хирургического удаления. Благодаря положительному влиянию инфликсимаба на течение тяжелых форм ЯК, уменьшается риск развития осложнений и летальных случаев.
Данный лекарственный препарат показан не только для достижения ремиссии ЯК, но и может вводиться в виде внутривенных инфузий в течение длительного промежутка времени в качестве поддерживающей терапии.
Инфликсимаб (Ремикейд) в настоящее время является одним из наиболее изученных лекарственных препаратов с оптимальным профилем соотношения польза/риск. Инфликсимаб (Ремикейд) даже разрешен к применению у детей от 6 лет.
Тем не менее, биологические препараты не лишены побочных эффектов. Подавляя активность иммунной системы, также как и другие иммуносупрессанты, они могут приводить к усилению инфекционных процессов, в частности туберкулеза. Поэтому пациентам перед назначением инфликсимаба необходимо выполнить рентгенографию органов грудной клетки и другие исследования для своевременной диагностики туберкулеза (например, квантифероновый тест – «золотой стандарт» выявления латентного туберкулеза за рубежом).
Пациент, получающий терапию инфликсимабом, как и любым другим новым средством, должен постоянно наблюдаться своим лечащим врачом или специалистом в области антицитокиновой терапии.
Перед проведением первой инфузии инфликсимаба (Ремикейда) пациентам проводятся следующие исследования:
- рентгенография грудной клетки
- кожная проба Манту
- анализ крови.
Рентгенография грудной клетки и кожная проба Манту делаются для исключения скрытого туберкулеза. Анализ крови необходим для оценки общего состояния пациента и исключения заболевания печени. Если есть подозрение на активную тяжелую инфекцию (например, сепсис) могут потребоваться другие исследования.
Инфликсимаб (Ремикейд) вводят непосредственно в вену, капельно, в виде внутривенной инфузии, медленно. Процедура занимает приблизительно 2 часа и требует постоянного контроля со стороны медицинского персонала.
Стандартная рекомендованная доза однократного применения инфликсимаба у больных ЯК составляет 5 мг на 1 кг массы тела.
Пример расчета однократной дозы инфликсимаба, необходимой для проведения одной инфузии. При весе пациента 60 кг однократная доза инфликсимаба составляет: 5 мг х 60 кг = 300 мг (3 флакона Ремикейда по 100 мг).
Инфликсимаб (Ремикейд) помимо терапевтической эффективности предоставляет пациентам щадящий режим терапии. В первые 1,5 месяца на начальном, так называемом индукционном этапе терапии, препарат вводят внутривенно всего 3 раза с постепенно увеличивающимся интервалом между последующими инъекциями, проводимыми под наблюдением врача. По окончании индукционного периода врач оценивает эффективность лечения у данного пациента и, в случае наличия положительного эффекта, рекомендует продолжить терапию инфликсимабом (Ремикейдом) обычно по схеме 1 раз в 2 месяца (или каждые 8 недель). Возможна коррекция дозы и режима введения препарата в зависимости от индивидуального течения заболевания у определенного пациента. Инфликсимаб рекомендуют использовать на протяжении года, а при необходимости и более длительно.
Будущее в лечении воспалительных заболеваний кишечника (ЯК и болезни Крона) представляется весьма обнадеживающим. То, что инфликсимаб (Ремикейд) включен в схему государственной помощи пациентам с ЯК и болезнью Крона, означает, что большее число пациентов может получить доступ к самому современному лечению.
При неэффективности консервативной (медикаментозной) терапии решается вопрос о необходимости хирургического вмешательства.
К сожалению, не во всех случаях ЯК удается справиться с активностью заболевания с помощью лекарственной терапии. Не менее 20 – 25 % больных нуждается в хирургической операции. Абсолютными (обязательными для сохранения жизни больного) показаниями к хирургическому лечению являются:
- неэффективность мощной консервативной терапии (глюкокортикоиды, иммуносупрессанты, инфликсимаб) тяжелого ЯК
- острые осложнения ЯК,
- рак толстой кишки.
Кроме того, вопрос о целесообразности плановой операции встает при формировании гормонозависимости и невозможности лечения другими препаратами (непереносимость других лекарств, экономические причины), задержке роста у детей и больных юношеского возраста, наличии выраженных внекишечных проявлений, развитии предраковых изменений (дисплазии) кишечной слизистой оболочки. В тех случаях, когда заболевание принимает тяжелую или непрерывно рецидивирующую форму, операция приносит избавление от многочисленных страданий.
Эффективность хирургического лечения и качество жизни больного ЯК после операции во многом зависит от ее типа.
Полное удаление всей толстой кишки (проктоколэктомия) считается радикальным методом лечения ЯК. Протяженность воспалительного поражения кишки не влияет на объем операции. Так, даже при поражении только прямой кишки (проктите) для положительного результата необходимо удаление всей толстой кишки. После колэктомии больные обычно чувствуют себя значительно лучше, у них исчезают симптомы ЯК, восстанавливается вес. Но часто в плановом порядке пациенты на такую операцию соглашаются неохотно, так как для выведения каловых масс из оставшейся части здоровой тонкой кишки в передней брюшной стенке делается отверстие (постоянная илеостома). К илеостоме прикрепляется специальная емкость для сбора кала, которую пациент сам освобождает по мере ее заполнения. Сначала пациенты трудоспособного возраста испытывают значительные психологические и социальные проблемы. Однако со временем большинство из них адаптируется к илеостоме, возвращаясь к нормальной жизни.
Более щадящей толстую кишку операцией является — субтотальная колэктомия. В ходе ее выполнения удаляется вся толстая кишка кроме прямой. Конец сохраненной прямой кишки соединяется со здоровой тонкой кишки (илеоректальный анастомоз). Это позволяет отказаться от формирования илеостомы. Но, к сожалению, через некоторое время неизбежно возникает рецидив ЯК, повышается риск развития рака в сохраненном участке толстой кишки. В настоящее время субтотальная колэктомия рассматривается многими хирургами как разумный первый шаг в хирургическом лечении ЯК, особенно при остром тяжелом течении заболевания, так как является относительно безопасной процедурой даже для критически больных. Субтотальная колэктомия позволяет уточнить патологию, исключить болезнь Крона, улучшить общее состояние пациента, нормализовать его питание и дает пациенту время тщательно обдумать выбор дальнейшего хирургического лечения (проктоколэктомия с созданием илеоанального резервуара или колэктомия с постоянной илеостомой).
Проктоколэктомия с созданием илеоанального резервуара заключается в удаление всей толстой кишки с соединением конца тонкой кишки с задним проходом. Преимуществом этого типа операции, выполняемой хирургами высокой квалификации, является удаление всей пораженной воспалением слизистой оболочки толстой кишки с сохранением традиционного способа опорожнения кишечника без необходимости илеостомы. Но в ряде случаев (у 20-30% больных) после операции развивается воспаление в области сформированного илеоанального кармана («паучит»), которое может быть рецидивирующим или постоянным. Причины появления «паучита» неизвестны. Кроме этого, возможны септические осложнения, нарушения функции сформированного резервуара и снижение фертильности у женщин из-за спаечного процесса .
Меры первичной профилактики (предотвращение развития ЯК), еще не разработаны. Видимо они появятся, как только будет точно установлена причина заболевания.
Профилактика обострений ЯК во многом зависит не только от мастерства лечащего врача, но и от самого больного. Для того чтобы симптомы заболевания не возвращались, обычно больному ЯК рекомендуется на протяжении длительного времени принимать лекарственные средства, способные поддержать ремиссию. К таким препаратам относятся препараты 5-АСК, иммуносупрессанты, инфликсимаб. Дозы лекарств, путь введения препаратов, режим и длительность их приема определяется индивидуально для каждого пациента лечащим врачом.
В период ремиссии следует с осторожностью принимать нестероидные противовоспалительные препараты (аспирин, индометацин, напроксен и др.), увеличивающие риск обострения ЯК. При невозможности их отмены (например, в связи с сопутствующей неврологической патологией) необходимо обсудить со своим доктором выбор препарата с наименьшим негативным влиянием на органы пищеварения или целесообразность замены на лекарственное средство другой группы.
Связь возникновения ЯК с психологическими факторами не установлена. Однако доказано, что хронические стрессы и депрессивный настрой больного не только провоцирует обострения ЯК, но и увеличивают его активность, а также ухудшают качество жизни. Нередко, вспоминая историю течения болезни, больные определяют связь ее ухудшения с негативными событиями в жизни (смерть близкого человека, развод, проблемы на работе и др.). Симптомы возникающего обострения, в свою очередь, усугубляют негативный психоэмоциональный настрой больного. Наличие психологических нарушений способствует низкому качеству жизни и увеличивает число посещений врача, независимо от тяжести состояния. Поэтому как в период рецидива заболевания, так и в период ремиссии пациенту обязательно должна оказываться психологическая поддержка, как со стороны медицинского персонала, так и со стороны домочадцев. Иногда требуется помощь специалистов (психологов, психотерапевтов), прием специальных психотропных лекарственных препаратов.
В период ремиссии большинству больных ЯК не требуется придерживаться жестких ограничений в диете. Подход к выбору продуктов и блюд должен быть индивидуальным. Пациенту следует ограничить или исключить употребление тех продуктов, которые именно у него вызывают неприятные ощущения. Показано включение в повседневный рацион рыбьего жира (он содержит омега-3-жирные кислоты, обладающие противовоспалительным эффектом) и натуральных продуктов, обогащенных полезной микрофлорой (некоторые виды бактерий участвуют в защите от обострения болезни). При стойкой ремиссии ЯК возможен прием качественного алкоголя в количестве не более 50 – 60 г.
При хорошем самочувствии пациентам с ЯК разрешены умеренные физические нагрузки, оказывающие благотворное общеукрепляющее действие. Выбор видов упражнений и интенсивность нагрузки лучше обсудить не только с тренером спортивного клуба, но и согласовать с лечащим врачом.
Даже если симптомы заболевания полностью пропадают пациенту необходимо находиться под медицинским наблюдением, так как ЯК может иметь отдаленные осложнения. Самым грозным последствием является рак толстой кишки. Чтобы не пропустить его на ранних стадиях развития, когда можно спасти здоровье и жизнь больного, пациенту необходимо проходить регулярное эндоскопическое обследование. Особенно это касается групп повышенного риска, к которым относятся пациенты, у которых ЯК дебютировал в детском и юношеском возрасте (до 20 лет), больные с длительно существующим тотальным ЯК, пациенты с первичным склерозирующим холангитом, больные, имеющие родственников с онкологическими заболеваниями. Британское общество гастроэнтерологов и Американское общество онкологов рекомендуют проводить контрольное эндоскопическое исследование с множественной биопсией (даже при отсутствии признаков обострения ЯК) через 8 – 10 лет после появления первых симптомов тотального ЯК, через 15 – 20 лет при левостороннем колите, далее фиброколоноскопию выполняют с частотой не реже 1 раза в 1-3 года.
источник