Аневризма грудной аорты представляет собой необратимый и сложный патологический процесс, при котором происходит аномальное расширение части сосуда.
Патология опасна для жизни, нуждается в своевременном диагностировании и лечении.
Аорта представляет собой самый крупный сосуд в человеческом теле. Она берет свое начало с левого сердечного желудочка, направляется вверх и плавно дугой спускается вниз. Участок данного сосуда, который пересекает грудную полость, называется грудной аортой. Участок сосуда, переходящий в брюшное пространство, именуется брюшной аортой.
Последняя продолжается двумя ветвями, которые называются подвздошными артериями. Они обеспечивают нормальное кровоснабжение внутренних органов, ног, половой системы.
Когда происходит расслоение сосудистых стен, их расширение из-за сильного истончения, диагностируется грудная аневризма. Худшее развитие дальнейших событий – разрыв аорты. Стандартно опасные патологии появляются в месте сильного ослабления сосуда, которое растягивается под действием высокого АД.
При несвоевременном обнаружении и при отсутствии лечения аневризмы происходит ее разрывание, провоцирующее очень сильное кровотечение. Выживаемость при развитии описываемого заболевания не превышает 30%, вот почему так важно своевременно обнаружить тревожные симптомы и обратиться за квалифицированной помощью.
Описываемые аневризмы могут образовываться в любом месте на тела. Около ¼ из них приходится именно на грудной сегмент. По форме такие новообразования принято разделять на мешотчатые и веретенообразные. Также патологические изменения восходящего отдела грудины классифицируются в зависимости от этиологии и места расположения, видов.
По месту расположения бывают:
- Аневризма синусов Вальсальвы/синусов Вальсальвы параллельно с восходящей дугой.
- Аневризма восходящей аорты/восходящей аорты параллельно с ее дугой.
- Патологическое изменение в дугах аорты/в дугах и в нисходящей аорте одновременно.
- Новообразование в нисходящей аорте.
- Торракоабдоминальная аневризма.
- Патология одновременно нисходящей части, восходящей аорты и дуги.
В зависимости от этиологии принято выделять следующие формы патологии:
- Аневризмы воспалительного типа образуются на фоне неспецифического аортоартерита, бывают сифилитическими, микотическими, ревматическими и пр.
- Аневризмы невоспалительной формы представлены травматическими, атеросклеротическими, послеоперационными осложнениями.
- Врожденные аневризмы появляются в результате кистозного медионекроза, при прогрессировании синдрома Марфана, врожденного изменения извивистой дуги грудной аорты, коарктации.
Описываемая болезнь представлена несколькими видами. Аневризмы грудного сегмента бывают ложными, истинными, расслаивающимися. Остаются неопределенными конкретные причины развития аневризм, поражающих грудную зону. Изучены сопутствующие факторы в виде болезней, которые способствуют повреждению стенок кровяных сосудов.
Прежде всего, это гипертензия, при которой устойчиво высокими показателями проявляется артериальное давление (начиная с отметки 140/90 и более). Заболевание провоцирует появление аневризм в грудном отделе.
Еще одной первопричиной структурного изменения аорты выступает атеросклероз. Данная болезнь характеризуется появлением в организме человека липидных образований.
Такие бляшки создаются на внутренних стенках сосудов, которые с течением времени уплотняются, под действием таких изменений становятся более хрупкими.
Данный механизм преобразования ведет к сужению просвета вены, в результате чего может произойти расслоение сосудистой стенки, появление аневризмы и ее разрыв.
Аневрозматический мешок появляется из-за ослабленного тонуса аорты на фоне ее воспаления, вызванного инфекционными поражениями, различными травмами. Воспалительный процесс стен аорты принято называть аортитом, который является одной из первопричин аневризмы аорты.
Среди врожденных патологий выделяется синдром Марфана. Данная болезнь относится к группе наследственных коллагенопатий, представлена поражением соединительной ткани во всем организме.
Около 20% аневризм возникает на фоне генетической предрасположенности. Сильное действие на аорту оказывают болезни инфекционного характера, поражающие ее внутреннюю структуру (пример — сифилис, туберкулез).
Увеличение аорты в области груди также происходит в результате патологического изменения клапанного аппарата на сердце.
Причиной может послужить и травмирование самой аорты, яркий пример – автомобильные аварии. На практике зафиксировано появление аневризмы из-за сильного ожирения и изменения обменных процессов в организме (незначительный процент пациентов).
Фактор риска патологии в грудной клетке:
- Курение негативно сказывается на легочной ткани, органах дыхательной системы, в том числе и на аорте.
- Возрастные изменения – изменения внутри аорты появляются у людей после 60 лет.
- Исследования показывают, что грудная аорта повреждается чаще у людей, относящихся к белой расе.
Принадлежность по половому признаку. Патологические изменения аорты грудного сегмента чаще беспокоят мужчин. У женщин же они появляются изредка, но у них патологические участки сосудов в большинстве случаев подвергаются разрыванию.
Наиболее опасное развитие событий при прогрессирующей сосудистой болезни – разрывание аорты. Данное состояние является реальной опасностью для жизни. Риск вскрытия сосуда повышается с увеличением патологического участка в размерах.
Не менее опасное осложнение, которое может привести к необратимым последствиям, заключается в появлении тромба внутри сосуда из-за сниженной скорости тока крови. Более того, уплотнения, имеющиеся на стенках аорты, отрываются и вместе с кровяными массами транспортируются по организму. Попадая в любой внутренний орган, перемещаясь в конечности, тромб вызывает развитие новых болезней.
Вся опасность аневризмы в том, что она длительное время абсолютно никак о себе не заявляет, развивается и прогрессирует без малейших признаков. Проявление симптоматики зависит от ряда факторов, в частности это место локализации, наличие расслоения сосудистой стенки, размеры новообразования. Клиническая картина аневризмы на аорте обусловлена давлением увеличившейся вены на грудную полость.
Проявляются такие признаки:
- Появление кашля и одышки при оказываемом давлении на дыхательные пути, трахею.
- Хрипота в голосе, вызванная передавливанием нервных окончаний, иннервирующих область гортани.
- Ухудшение глотательного рефлекса, явно ощущается дискомфорт из-да давления проблемного места на пищевод.
- Неестественная пульсация в грудной полости.
- Проявление синдрома Горнера, который развивается из-за давления на вегетативные нервные отростки, проходящие через грудную зону. Данный синдром выражен интенсивной потливостью, сужеными зрачками, при этом веки частично опущены.
При разрывании грудной аорты симптоматика выражается сразу и очень резко. Появляется острая, пронизывающая боль, которая из грудной клетки перетекает в шейную зону, на позвоночник, конечности, спускается в брюшину. Болевой синдром указывает на неполноценное кровоснабжение сердечной мышцы, в результате чего происходит сбой работы аортального клапана. Печально, но статистика показывает, что разрыв аневризмы, образовавшейся на грудной аорте, сопровождается шоковым состоянием, ведущим к летальному исходу.
Предварительное определение описываемой патологии предполагает изучение доктором всех данных, касающихся появления и развития болезни, анализ всех жалоб, поступающих от человека, и сопутствующих факторов.
Важен первичный осмотр пациента, по окончании которого назначаются соответствующие манипуляции:
- ЭКГ представляет собой процедуру УЗИ сердца. Это доступный и абсолютно недорогой диагностический метод, в ходе которого обнаруживается аневризма аорты. Процедура предполагает выполнение чреспищеводной эхокардиографии, для чего задействуется зонд, оснащенный специальным датчиком УЗИ.
- Рентгенологическое обследование осуществляется стандартно в прямой и боковой проекции. Для выявления дуговых аневризм аорты выполняется косая левая проекция. Главный признак патологического изменения аорты в грудном сегменте представлен локальным расширением ее тени.
- Компьютерная томография – методика, при которой доктор имеет возможность получить снимки послойного строения организма человека. Происходит максимально точное ионизирующее излучение, после чего полученные изображения подвергаются компьютерной обработке.
- Во время магнитно-резонансной ангиографии также изучается послойное строение интересующих сосудов и прилегающих к ним частей тканей при помощи электромагнитного поля.
Люди, относящиеся к группе риска, должны регулярно обследоваться на предмет появления и развития аневризмы. Диагностировать ее стоит с изначальной консультации и осмотра специалистом, проведения при необходимости УЗИ. По показаниям доктора проводятся дополнительные виды обследований. Что касается прогноза при аневризме восходящего отдела аорты, в большинстве случаев и с большой долей вероятности он неблагоприятен, может привести к смерти.
Лечение описываемой патологии представлено двумя основными способами. На начальном этапе развития болезни задействуется медикаментозная терапия, целью которой выступает купирование признаков, предотвращение или частичное снижение интенсивности развития аневризмы. Терапия основывается на приеме анальгетиков, устраняющих болевой синдром, использовании медикаментов, действие которых направлено на стабилизацию тонуса в сосудах, восстановление показателей АД. Часто аневризма в нисходящей грудной аорте провоцирует расстройство работы ЖКТ. В таком случае назначаются препараты, улучшающие работу кишечника.
Хирургическое вмешательство строго показано всем пациентам без исключения, если случился разрыв аневризмы. Операции проводятся даже при острой сердечной недостаточности, в период беременности, в детском возрасте. Речь идет о спасении жизни человека, который при внутреннем кровоизлиянии аорты может с большой вероятностью умереть.
Принято выделять несколько видов хирургического вмешательства, направленного на улучшение состояния пациента:
- Стентирование – процедура, практически не влекущая за собой осложнений. Выполняется через проделанный разрез небольших размеров. В поврежденную аорту помещается стент из металла, который необходим для укрепления стенок сосуда и предотвращения их последующего разрыва. Положительный результат стентирования ощущается пациентом практически сразу же после операции. Происходит планомерное выздоровление человека, восстанавливаются нарушенные функции организма с незначительными ограничениями.
- Эндоваскулярное лечение еще называется бесполосной операцией. Стандартная практика протезирования вен, артерий предполагает совершение брюшного разреза, в результате чего все манипуляции совершаются открытым способом. Что касается эндоваскулярного вмешательства, оно построено на введении в аорту стента-графта, который плотно прилегает к поврежденным стенкам. Таким образом полностью из кровотока исключается раздел аневризмы. Восстановление после подобного вмешательства составляет 3-5 дней, возвращение к нормальной жизнедеятельности наступает по истечению 1-2 месяцев.
С аневризмой грудной аорты шутить нельзя. Данное патологическое состояние может привести к летальному исходу. Вот почему так важно своевременно обнаружить изменения в сосудистой системе, пройти своевременное лечение, при необходимости устранить причину хирургическим путем.
источник
Боль в груди — одна из самых частых причин обращения за врачебной помощью. Причина боли в груди может быть ясной, но часто бывает атипичной. Случаи, когда пациенты жалуются на боль в груди, представляют наибольшие трудности для диагностики.
Дифференциально-диагностический ряд в таких случаях чрезвычайно широк и включает, в том числе, заболевания, представляющие непосредственную угрозу жизни, такие как инфаркт миокарда с подъемом и без подъема сегмента ST, нестабильную стенокардию, тромбоэмболию легочной артерии и расслаивающую аневризму аорты.
Расслаивающая аневризма аорты (РАА) представляет достаточно сложную проблему в плане первичной диагностики. Причиной этого является как низкая частота данной патологии, так и большая вариабельность клинических проявлений.
Без применения кардиохирургических методов в ранние сроки заболевания прогноз крайне неблагоприятен, а двухнедельная выживаемость не превышает 20 % , поэтому своевременная диагностика РАА является важнейшей задачей.
Под термином «расслаивающая аневризма аорты» подразумевают внезапное образование вследствие различных причин дефекта интимы аорты с последующим проникновением крови через этот дефект в дегенеративно измененную срединную оболочку, образованием гематомы и продольным расслоением стенки аорты.
Расслоение (диссекция) происходит преимущественно в дистальном, реже в проксимальном отделе. Гематома может развиваться по ходу аорты и закупоривать одну из ее ветвей, начиная от ветвей дуги аорты и заканчивая кишечными артериями.
Ретроградная диссекция может поражать коронарные артерии. Чаще вовлекается правая коронарная артерия. Ретроградное расслоение может привести к нарушению прочности одной или нескольких створок аортального клапана и его недостаточности.
Ложный канал располагается в наружной половине средней оболочки аорты. Наружная его стенка составляет всего четверть первоначальной толщины стенки аорты. Это является причиной частых разрывов аорты у больных с расслаивающей аневризмой.
Разрыв аневризмы дуги аорты происходит чаще всего в полость средостения, разрыв нисходящей аорты — в левую плевральную полость, брюшной аорты — в забрюшинную клетчатку. Так как париетальный перикард прикрепляется к восходящей части аорты, непосредственно проксимальнее места отхождения плечеголовного ствола, разрыв любого отдела восходящей части аорты может привести к тампонаде перикарда.
Классификации расслаивающих аневризм аорты обычно основаны на локализации проксимального разрыва внутренней оболочки аорты и протяженности расслоения стенки аорты. Поскольку разрыв внутренней оболочки аорты может теоретически произойти в любом сегменте и быть множественным, варианты расслоения аорты весьма разнообразны.
Однако на практике разрыв внутренней оболочки чаще всего происходит в передней стенке восходящей части аорты на границе проксимальной и средней трети, а также в начальном сегменте нисходящей части аорты дистальнее русла левой подключичной артерии.
Именно на этом принципе основана простая и широко распространенная Стэндфордская классификация, согласно которой выделяют несколько типов расслоения:
- тип А — разрыв интимы находится в восходящей аорте с поражением дуги или нисходящей аорты, или без них;
- тип В — надрыв находится в нисходящей аорте, при этом расслоение распространяется проксимально и дистально.
Для определения прогноза болезни и выработки консервативной и оперативной тактики в клинике применяется модификация классификации М. DeBakey:
- тип I — разрыв внутренней оболочки локализуется в восходящей части аорты, а расслоение ее стенок распространяется до брюшной части аорты;
- тип II — разрыв внутренней оболочки локализуется в восходящей части аорты, расслоение заканчивается слепым мешком проксимальнее плечеголовного ствола;
- тип III — разрыв внутренней оболочки аорты локализуется в начальном отделе нисходящей части грудной аорты дистальнее устья левой подключичной артерии.
Классификация расслаивающей аневризмы аорты
Согласно другой классификации, выделяют пять классов диссекции аорты.
- К 1-му классу относят классическое расслоение аорты с формированием ложного и истинного ходов без образования сообщения между ними,
- к 2-му— интрамуральную гематому или кровоизлияние,
- к 3-му — пенетрирующее изъявление атеросклеротической бляшки стенки аорты вследствие надрыва ее капсулы,
- к 4-му — небольшие ограниченные или частичные диссекции аорты с образованием выпячивания ее стенки
- к 5-му — ятрогенные или посттравматические диссекции аорты (например, расслоение аорты проведенным в нее для катетеризации сердца катетером).
Классификация диссекций аорты по L. G. Svensson и соавт.
Разрыв интимы, являющийся началом расслаивающей аневризмы, обнаруживается в восходящей части аорты примерно в 70 % случаев. В 10 % случаев его находят в дуге, в 20 % — в нисходящей части грудной аорты. В редких случаях наблюдается надрыв интимы брюшной аорты.
Диссекция (расслоение) аорты может быть острой (до 2 недель) и хронической (более 2 недель).
Распространенность РАА оценивается в среднем как 1 на 10 000 госпитализированных (однако значительная часть больных погибает на догоспитальном этапе). Данная патология является причиной 1,1 % случаев внезапной смерти и 3-4 % случаев всех внезапных смертей от сердечно-сосудистых заболеваний; выявляется в 1 случае на 400 аутопсий.
К предрасполагающим факторам расслоений аорты относятся заболевания и состояния, сопровождающиеся кистозной дегенерацией медии:
- длительно существующая артериальная гипертензия,
- врожденные дефекты соединительной ткани (синдромы Марфана, Элерса — Данлоса, Тернера),
- поликистозная болезнь почек,
- пожилой возраст (60-70 лет);
- врожденные пороки сердца (коарктация аорты, бикуспидальный или одностворчатый клапан);
- атеросклероз аорты;
- беременность;
- травма грудной клетки,
- сильное физическое и эмоциональное напряжение;
- системные васкулиты (особенно часто гранулематозный, гигантоклеточный артериит);
- химические и токсические воздействия (наркотики, например, кокаин);
- ятрогенные причины.
Наиболее частыми симптомами при РАА являются внезапное начало боли с молниеносным достижением максимальной интенсивности, локализация боли в грудной клетке, боль в спине. Боль описывается пациентами как очень интенсивная или нестерпимая, самая сильная боль, которую они когда-либо испытывали, боль острая или рвущая.
У значительной части пациентов могут наблюдаться те или иные изменения сегмента ST или зубца Т.
При проксимальном типе расслоения может выслушиваться шум аортальной регургитации.
Как при проксимальном, так и при дистальном типе расслоения может определяться асимметрия пульса (снижение его наполнения или отсутствие) и артериального давления на верхних или нижних конечностях.
У части пациентов могут выявляться те или иные неврологические нарушения.
Относительно редко встречается вторичный (чаще всего задненижний) инфаркт миокарда, связанный с распространением расслоения на устье коронарной артерии.
К заболеваниям, имеющим сходную с РАА клиническую картину, относятся:
- острый коронарный синдром;
- аортальная недостаточность без диссекции (расслоения);
- аневризма аорты без диссекции (расслоения);
- костно-мышечные;
- перикардит;
- опухоль средостения;
- плеврит;
- тромбоэмболия легочной артерии;
- холецистит.
Наличие РАА можно подозревать, если у пациента имеется боль; боль в сочетании с обмороком (синкопе); боль в сочетании с симптомами сердечной недостаточности; боль в сочетании с симптомами поражения ЦНС (инсульт); сердечная недостаточность без болевого синдрома; симптомы поражения ЦНС (инсульт) без болевого синдрома; изменения на рентгенограмме органов грудной клетки без болевого синдрома; отсутствие пульса без болевого синдрома.
Согласно рекомендациям рабочей группы Европейского общества кардиологов, для подтверждения диагноза, уточнения типа расслоения (локализация, протяженность), диагностики и уточнения тяжести аортальной недостаточности и диагностики экстравазации (периаортальная или медиастинальная гематома, плевральный или перикардиальный выпот) предпочтение следует отдавать трансторакальной ЭхоКГ с последующей трансэзофагеальной ЭхоКГ и внутрисосудистым УЗИ, мультиспиральной компьютерной томографии или магнитно-резонансной томографии.
Ангиография может проводиться для определения анатомического субстрата при планируемом чрескожном вмешательстве у гемодинамически стабильных и нестабильных пациентов, но не рутинно. Рентгенография грудной клетки не дает дополнительной информации.
Ниже представлены начальные лечебно-диагностические мероприятия, которые следует проводить при подозрении на РАА в соответствии с рекомендациями группы экспертов Европейского общества кардиологов.
- Сбор детального анамнеза и полный осмотр (при возможности).
- Обеспечение венозного доступа, анализы крови (ОАК, КФК, тропонин I (Т), Д-димер, гематокрит, липиды).
- Мониторирование артериального давления и ЭКГ.
- Снижение систолического артериального давления, предпочтительно β-адреноблокаторы (пропранолол, метопролол, эсмолол), при противопоказаниях — антагонисты кальция.
- При тяжелой артериальной гипертензии дополнительно вазодилататоры.
- Трансторакальная (трансэзофагеальная) ЭхоКГ.
Всем пациентам с расслаивающей аневризмой аорты показано хирургическое лечение.
Представляем клинический пример прижизненной диагностики РАА на основании особенностей течения заболевания и клинической картины.
Пациентка А., 59 лет. Жалоб в момент поступления нет. Ранее сердечно-сосудистых заболеваний не переносила.
Впервые за 3 дня до обращения в стационар возникла колющая, пронизывающая боль умеренной интенсивности в области сердца и между лопатками без связи с физической нагрузкой и движением, усиливавшаяся при пальпации, сохранялась несколько часов после самостоятельного приема анальгетиков. Повторный подобный приступ развился накануне поступления в стационар.
Консультирована неврологом, высказано предположение о вертеброгенной торакалгии. Проведена ЭКГ, выявлены изменения (отрицательные зубцы Т в отведениях III и aVF), по поводу которых пациентка направлена в стационар с диагнозом: «ИБС. Заднедиафрагмальный инфаркт миокарда».
При объективном обследовании обращал на себя внимание умеренно интенсивный диастолический шум, выслушивавшийся над аортой и по правому краю грудины.
С учетом острого характера и длительности боли в грудной клетке в сочетании с выявленными признаками аортальной недостаточности, предположительно остро развившейся (не было сведений о существовавшем ранее пороке сердца, границы сердца в пределах нормы, отсутствовали признаки хронической сердечной недостаточности) было высказано предположение о наличии РАА восходящего отдела аорты.
Пациентка была госпитализирована в ОРИТ, где планировалось начать инфузию эсмолола, провести трансторакальную и, при необходимости, трансэзофагеальную ЭхоКГ.
Через 10 мин после поступления больная внезапно потеряла сознание, диагностировано прекращение кровообращения (электромеханическая диссоциация). Реанимационные мероприятия безуспешны.
Диагноз: «Расслаивающая аневризма восходящей аорты. Гемоперикард. Тампонада сердца».
При патологоанатомическом исследовании было обнаружено непротяженное расслоение восходящей аорты с надклапанным разрывом и кровоизлиянием в полость перикарда.
П. В. Долотовская, И. В. Грайфер, С. В. Ефремов, Н. В. Фурман
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Клиническое подозрение на расслаивающую аневризму аорты
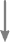
• компьютерная томография с введением контрастного вещества
• магнитный резонанс
• аортография
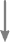
Подтверждение наличия расслаивающей аневризмы аорты


• метод выбора при остром проксимальном расслоении
• острое расслоение в дистальном отделе при наличии осложнений
• метод выбора при неосложненном дистальном расслоении
• стабильное изолированное расслоение дуги аорты
• стабильное хроническое расслоение (неосложненное расслоение давностью 2 нед и более)
П р и м е ч а н и е: Клиническое подозрение на расслаивающую аневризму аорты возникает на основании данных анамнеза, физикального обследования, рентгенографии грудной клетки и ЭКГ. К острой относят расслаивающую аневризму давностью менее 2 нед, к хронической – существующую более длительное время. Среди осложнений этого состояния – прогрессирование поражения с вовлечением жизненно важных органов или конечностей, разрыв или угроза разрыва (например, формирование мешотчатой аневризмы), регургитация в аортальном клапане (встречается очень редко), ретроградное распространение расслоения на восходящую аорту, невозможность контролировать боль и АД медикаментозно, синдром Марфана. К проксимальной относят расслаивающую аневризму с вовлечением восходящего отдела и дуги аорты, к дистальной – локализующуюся ниже отхождения левой подключичной артерии.
• во многом зависят от локализации поражения;
• характерно внезапное начало с появления сильной “разрывающей” боли;
• боль чаще всего локализуется за грудиной, в межлопаточной области, в пояснице (характерно изменение ее локализации по мере прогрессирования расслоения);
• возможна потеря сознания;
• выявляются как гипертония, так и гипотония (следует предварительно убедиться, что АД не определяется на сосуде, вовлеченном в процесс расслоения);
• при надклапанной локализации поражения возможно появление регургитации в аортальном клапане (в тяжелых случаях приводящей к сердечной недостаточности), тампонады сердца;
• дефицит пульса, снижение амплитуды пульсации на сосудах, вовлеченных в разрыв;
• возможно появление симптомов ишемии миокарда, головного и спинного мозга, конечностей, органов брюшной полости.
Рентгенография грудной клетки:
• находки неспецифичны, часто не помогают диагностике;
• возможно расширение тени аорты (иногда с наличием характерного выпячивания в месте расслоения), реже средостения, появление жидкости в плевральной полости (чаще слева);
• нормальная рентгенограмма диагноза не исключает.
• при отсутствии характерных изменений можно исключить ишемию миокарда как причину боли в грудной клетке;
• наличие изменений, характерных для инфаркта миокарда (чаще нижней локализации), расслаивающую аневризму аорты не исключает.
Методы визуализации аорты:
• выбор метода во многом зависит от возможностей и опыта;
• чреспищеводная эхокардиография особенно показана при нестабильном состоянии больного (может быть быстро выполнена у постели больного, а также в операционной непосредственно перед оперативным вмешательством, не требует прекращения мониторного наблюдения и проводимых терапевтических мероприятий);
• компьютерную томографию с введением контрастного вещества можно использовать в случае, если чреспищеводная эхокардиография недоступна;
• магнитный резонанс чаще применяют у больных, чье состояние стабильно, при хронической форме заболевания;
• аортографию используют в случаях, когда определенный диагноз не был установлен с помощью указанных выше исследований.
Методы медикаментозного лечения:
• к основным целям лечения относят снижение АД и сократимости миокарда;
• желаемый уровень систолического АД – 100 – 120 мм рт. ст. или самый низкий уровень, не вызывающий ишемии сердца, головного мозга и почек у страдающих гипертонией;
• для быстрого снижения высокого АД прибегают к внутривенной инфузии нитропруссида натрия или нитроглицерина при обязательном одновременном применении b -блокатора;
• для быстрого снижения сократимости миокарда производят внутривенное введение b -блокаторов в возрастающей дозе до достижения ЧСС 50 – 60 в 1 мин (пропранолол – по 1 мг через 3 – 5 мин до достижения эффекта или до общей дозы 0,15 мг/кг с повторением через 4 – 6 ч по 2-6 мг; эсмолол – болюс 30 мг, далее инфузия 3-12 мг/мин);
• обеих целей можно добиться при помощи лабетолола (10 мг внутривенно в течение 2 мин, далее 20 – 80 мг каждые 10 – 15 мин до максимальной дозы 300 мг, в качестве поддерживающей меры – инфузии 2 – 20 мг/мин);
• при противопоказаниях к b -блокаторам можно использовать антагонисты кальция, замедляющие ритм сердца (верапамил, дилтиазем);
• прием короткодействующих препаратов нифедипина внутрь или под язык может привести к быстрому снижению АД даже в рефрактерных случаях, однако сопряжено с риском возникновения рефлекторной тахикардии, по-видимому, эти средства не следует назначать без предварительного введения b -блокатора;
• при вовлечении в расслоение артерий почек для снижения АД наиболее эффективным может быть внутривенное введение ингибитора ангиотензин-конвертирующего фермента (эналаприл 0,625 – 5 мг каждые 4 – 6 ч);
• при клинически значимой гипотонии необходимо быстрое внутривенное введение жидкости; в рефрактерных случаях проводится инфузия прессорных агентов (предпочтительнее норадреналина; допамин применяется только в низких дозах для стимуляции мочеотделения).
• при подозрении на разрыв аорты, а также на тампонаду сердца необходимо как можно быстрее доставить больного в операционную;
• срочность и целесообразность оперативного вмешательства зависят от локализации поражения, давности возникновения расслоения и наличия осложнений (см. схему) .
источник
Расслаивающая аневризма аорты представляет собой отдельную нозологическую единицу, патологоанатомическая сущность которой состоит в том, что на интиме и приблизительно на половине средней оболочки образуется трещина, через которую кровь из просвета аорты нагнетается в толщу артериальной стенки, где возникает ин-трамуральная гематома, разделяющая до того единую аортальную стенку на внутренний и наружный слои.
Интрамуральная гематома, постепенно расслаивая стенку аорты по окружности, образует внутреннюю «трубку», состоящую из интимы и внутренней половины средней оболочки, и наружную «трубку», образованную наружной половиной средней оболочки и адвентицией. Если расслоение произошло по всей окружности аорты, то последняя представляет собой как бы две трубки, насаженные одна на другую. Интрамуральная гематома производит расслоение стенки аорты не только по окружности, но и распространяется в проксимальном и дистальном направлениях от места повреждения аорты.
Наружная трубка в дистальном направлении может иметь слепое окончание. Случается, однако, что дистальный конец наружной трубки также прорывается в просвет аорты. В первом случае при аортографии в кровь, заполняющую наружную трубку, попадает лишь незначительное количество контрастного вещества, в то время как во втором случае в обеих трубках (внутренней и внешней) появляется значительное количество контрастного вещества, так как и в той, и в другой трубке имеетсяпостоянный кровоток.
Поперечный разрыв интимы и половины средней оболочкиобычно встречается в двух местах. Одно из таких типичных мест находится на несколько сантиметров выше аортального клапана на выпуклой стороне аорты. Другим таким местом является начало нисходящей части аорты ниже устья подключичной артерии, также на выпуклой стороне аорты.
При расслаивающей аневризме может произойти разрывнаружной оболочки,когда интрамуральная гематома прорывается через наружную часть средней оболочки и адвентицию. При этом, в зависимости от локализации разрыва, происходит кровоизлияние в полость перикарда с внезапным развитием тампонады сердца и гибелью больного. Кровоизлияние в средостение сопровождается симптомами сдавливания расположенных в нем крупных артериальных и венозных сосудов. Кровоизлияние возможно также в свободную плевральную полость, а при распространении гематомы на брюшной отдел аорты —и в брюшную полость.
Чаще всего расслаивающая аневризма аорты встречается в относительно молодом возрасте, у больных от 20до 40лет и, в виде исключения, у пожилых. Наиболее частойпричинойвозникновения расслаивающей аневризмы аорты является синдром Marfan,характерными признаками которого признано считать высокий рост, астеническое телосложение и арахнодактилию. Причиной образования расслаивающей аневризмы при этом синдроме является дегенерация средней оболочки аорты, т. н. кистозный некроз средней оболочки (Erdheim).В возникновении расслаивающей аневризмы у пожилых больных приблизительно в 50%всех случаев важную роль играет гипертензия. Этиологическим фактором может быть коарктация аорты и поддерживаемая ею гипертензия верхней половины тела, а также беременность. Атеросклероз и сифилис, по всей вероятности, не являются причиной возникновения расслаивающей аневризмы аорты, даже у больных пожилого возраста.
Различаюттри вида расслаивающих аневризм аорты(рис. 3-204):
а) расслоение распространяется на восходящую часть аорты и начальный отдел дуги аорты (чаще всего при синдроме Marfan);
б) расслоение начинается около аортального кольца и распространяется до или даже ниже диафрагмы;
Рис. 3-204. Три вида расслаивающих аневризм аорты (а в)
в) расслоение начинается ниже устья левой подключичной артерии и распространяется ниже диафрагмы; этот вид аневризм встречается чаще всего.
Клиническиразличают острую, подострую и хроническую формы. Чаще всего встречаются острые формы: 80%всех больных с расслаивающей аневризмой аорты погибает в первую неделю заболевания. Лишь приблизительно в 10 -15% случаев заболевания аневризма становится хронической, ав исключительных случаяхпосле тром-бирования интрамуральной гематомы больной может спонтанно выздороветь.
Хирургическое лечениерасслаивающей аневризмы аорты представляет собой весьма сложную задачу. Оперативное вмешательство по поводу вышеупомянутого вида расслаивающих аневризм типа а) следует производить, как и при простой, не расслаивающей веретенообразной аневризме восходящей части аорты и ее дуги. Больного подключают к аппарату искусственного кровообращения, затем производят резекцию аневризмы и замещение дефекта аорты соответствующим по величине аллотрансплантатом. При наличии сопутствующей недостаточности аортального клапана производят вшивание в аорту искусственного клапана(рис. 3-205).
При аневризмах типа б) (см. выше) может возникнуть необходимостьэкстренной операции. Доступ к восходящей части аорты обеспечивается срединной стернотомией, после чего больного подключают к аппарату искусственного кровообращения. В начальном отделе восходящей части аорты поперечным разрезом пересекают аорту
и как в проксимальной, так идистальной ее частях подшивают внутреннюю стенку к наружной, создавая единую стенку аорты. Вслед за этим наложением швов соединяют обе культи аорты.
После операции интрамуральная гематома, расположенная в закрытой полости, постепенно тром-бируется, а затем следует организация тромба и излечение.
Рис. 3-205. Метода» хирургического лечения расслаивающей аневризмы аорты типа «а», а) Иссечение аневризмати-ческого участка аорты; б) замещение дефекта аорты сосудистым протезом из синтетического материала и вшивание искусственного клапана типа Starr — Edwards
источник
1 За підтримки фармакотерапія 5 (141) / 2010 P Расслаивающая аневризма аорты Е.Г. ПОЧЕПЦОВА, к. мед. н.; В.И. ЦЕЛУЙКО, д. мед. н., профессор /Харьковская медицинская академия последипломного образования/ Расслаивающая аневризма аорты это патологический дополнительный внутрисосудистый канал (ложный просвет), образующийся в толще стенки аорты как следствие расслаивания ее кровью, поступающей из просвета аорты через дефект (разрыв) во внутренней оболочке стенки аорты в дегенеративно измененный средний слой. В результате образуется внутристеночная гематома. Таким образом, расслаивание происходит внутри средней оболочки. Чаще всего расслоение возникает в дистальном (антеградном) направлении, реже в проксимальном (ретроградном). В случае существенного расширения ложного просвета формируется аневризма аорты. Очень часто аневризма (расширение аорты) бывает небольшой или отсутствует, в связи с чем в последнее время общепринятым стал термин «расслоение аорты» (РА), заменив термин «расслаивающая аневризма» (введенный в клиническую практику Лаэннеком в 1819 г.). Расслоение аорты достаточно редкое, но потенциально опасное заболевание. Встречается РА у 1 из 10 тыс пациентов, но большая часть больных умирает на догоспитальном этапе. РА является причиной 3 4% внезапных смертей от сердечнососудистых заболеваний. Ранняя смертность от РА при отсутствии лечения составляет 1% в час (один человек из ста умирает каждый час) в первый день, 75% в течение двух недель и свыше 90% в течение первого года. При наличии современной техники, новых диагностических возможностей и при условии своевременного лечения выживаемость больных может быть значительно увеличена. Этиология Этиология РА разнообразна. Основными факторами являются артериальная гипертензия (встречается у 85% пациентов с РА) и возраст (атеросклероз). Эти факторы способствуют дегенерации меди с последующей дезорганизацией коллагена, гладкомышечных элементов и эластических волокон. Мужчины страдают в 2 3 раза чаще, чем женщины. У больных в возрасте от 40 до 70 лет, длительно страдающих высокой артериальной гипертензией и атеросклерозом, имеется угроза РА. Вначале на внутренней оболочке аорты возникают небольшие дефекты, содержащие мукоидное вещество, т.е. происходит идиопатический кистозный некроз средней оболочки аорты, вследствие чего разрывается внутренняя и средняя оболочки аорты, преимущественно в начальной части восходящей аорты и реже в конечной части дуги аорты у начала левой подключичной артерии. В место надрыва аортальной стенки под большим давлением устремляется кровь, что обусловливает расслаивание внутренних бессосудистых слоев. Продвигаясь вперед, кровь может сдавить отходящие от аорты артерии и вызвать нарушение кровоснабжения питаемых ими областей. РА может происходить на всем протяжении, вплоть до бифуркации, а также может распространиться на подвздошные артерии. Если происходит второй надрыв внутренних слоев аортальной стенки по ходу расслаивания, при выходе крови в просвет сосуда образуется «двуствольная аорта». Наиболее неблагоприятным является проксимальный разрыв чем проксимальнее, тем больше вероятность возникновения смертельного кровотечения на протяжении нескольких часов или дней после начала расслаивания. Разрыв восходящей аорты приводит к массивному кровотечению в перикард с быстрым летальным исходом. Возможно также кровоизлияние в свободную плевральную полость как в левую, так и в правую. Редкие причины развития расслоения аорты 1. Заболевания и состояния, сопровождающиеся кистозной дегенерацией медии: длительно существующая артериальная гипертензия (АГ); врожденные дефекты соединительной ткани (синдромы Марфана, Эллерса Данло, Тернера, поликистозная болезнь почек); пожилой возраст (60 70 лет). 2. Врожденные пороки сердца: коарктация аорты; двустворчатый (в 7 14% случаев) и одностворчатый клапан. 3. Атеросклероз аорты. 4. Беременность. 5. Травма грудной клетки, сильное физическое и эмоциональное напряжение. 6. Системные васкулиты. 7. Химические и токсические воздействия (наркотики). 8. Ятрогенные причины. Синдром Марфана (наследственный дефект соединительной ткани, обусловливающий патологию скелетной мышечной ткани) встречается в небольшом числе случаев (6 9% РА), чаще в молодом возрасте, с локализацией расслоения в проксимальном отделе. Для больного с синдромом Марфана характерны астеническое телосложение, арахнодактилия, деформация грудной клетки, кифосколиоз, высокое арковидное небо, слабость связок глаз, подвывих хрусталика, отслоение сетчатки, близорукость высокой степени, а также сердечнососудистые осложнения (дилатация корня аорты, аортальная регургитация, расслоение и аневризма аорты, пролапс митрального клапана). При отсутствии своевременного лечения большая часть больных умирает от осложнений до 40-летнего возраста. 8
3 фармакотерапія 5 (141) / 2010 P В 50% случаев РА может развиться при беременности. РА наблюдается у беременных старше 40 лет и чаще в третьем тримест ре беременности, редко в ранний послеродовой период. Этиология не ясна. Вероятно, имеет значение повышение артериального давления (АД). РА развивается у 18% пациентов после операции протезирования клапанов, обычно через несколько месяцев или лет. Группа пациентов после протезирования аортального клапана имеет наибольший риск развития РА. Ятрогенные расслоения обусловлены проведением ангиографии и баллонной дилатации, канюляции аорты при проведении искусственного кровообращения. Расслоение в этих случаях связано только с техническими погрешностями. РА также встречается в местах резекции аорты или наложения швов. Патогенез Обычно расслоение аорты начинается с надрыва внутренней оболочки аорты и/или спонтанного образования интрамуральной гематомы из-за разрыва vasa vasorum, что может привести к образованию гематомы без дефекта интимы или с последующим разрывом интимы при клинической картине классического расслоения. Интрамуральная гематома является атипичным проявлением расслоения аорты. В ряде случаев расслоению аорты может способствовать пенетрирующая атеросклеротическая язва, часто приводящая к формированию псевдоаневризмы с разрывом аорты. К развитию РА могут привести различные состояния, которые способствуют ослаблению и дегенерации компонентов медии аорты, эластических волокон, гладких мышц. Классификация Классификация по анатомической локализации и степени вовлеченности различных отделов аорты (по М. Дебейки): тип I местом возникновения разрыва является восходящая аорта, а расслоение распространяется на дугу и часто дистальнее на грудной и брюшной отделы аорты; тип II разрыв локализуется в восходящей части, расслоение ограничено только восходящей аортой; тип III разрыв интимы локализуется в нисходящей грудной аорте, распространяется чаще антеградно дистально, по нисходящей аорте на различном протяжении с вовлечением только всего грудного отдела и/или и грудного, и брюшного отделов, редко ретроградно на дугу и восходящую аорту. Анатомическая классификация: тип А проксимальный или восходящий (что включает в себя типы I и II по Дебейки); тип Б дистальный или нисходящий (соответствует типу III по Дебейки). По данным аутопсий тип А встречается в 2 4 раза чаще. Этот тип характеризуется достаточно высокой частотой ранних осложнений (разрыв с тампонадой, острая недостаточность мозгового кровообращения, аортальная регургитация), имеет высокую догоспитальную летальность и требует неотложного хирургичес кого лечения. Наиболее часто расслоение происходит в двух наиболее гемодинамически уязвимых участках: восходящая аорта в пределах нескольких см от аортального клапана (65%); нисходящая аорта чуть дистальнее места отхождения левой подключичной артерии (20%). Имеет место также изолированное расслоение дуги (10%), брюшной аорты (5%) и отдельных артерий, отходящих от аорты, особенно каротидной и коронарной. При РА, затрагивающем восходящий отдел, показано хирургическое лечение, а без его вовлечения рекомендуется консервативное лечение. Классификация в зависимости от времени возникновения расслоения аорты: острые (менее 2 недель) более 2/3 случаев; хронические (свыше 2 недель). Клиника Ведущим (90 95% случаев) симптомом расслаивающей аневризмы аорты является острая интенсивная «раздирающая» боль за грудиной, возникающая внезапно (начало расслоения), также боль в спине, в подчревье; пациент тревожен, беспокоит одышка. Обезболивающие препараты не эффективны. Может развиться внезапная тампонада сердца (кровоизлияние в полость перикарда) или гемоторакс (кровоизлияние в полость плевры). Часто развивается острый коллапс с потерей сознания. Если больной остается в живых, у него наблюдаются последующее повышение температуры тела, лейкоцитоз, увеличение скорости оседания эритроцитов. Описанная клиническая картина обусловлена следующими факторами, лежащими в основе расслоения: расслоением стенки аорты (вызывает сильную боль); развитием обширной внутристеночной гематомы; сдавлением или отрывом ветвей аорты, снабжающих жизненно важные органы (сердце, головной и спинной мозг, почки), с последующей их ишемией. Внутристеночная гематома в области восходящей аорты приводит к сдавлению коронарных артерий, сужению выходного отдела левого желудочка, острой недостаточности кровообращения, проксимальной коарктации. Клинические симптомы РА могут быть разнообразными, потому что расслоение процесс динамичный, и изначальная картина заболевания может отличаться от заключительной. РА может имитировать многие сердечно-сосудистые, неврологические, хирургические и урологические заболевания. Боль при РА может мигрировать от места возникновения по направлению расслоения, может вначале сопровождаться вагусными проявлениями, тошнотой, рвотой, повышением АД. Локализация боли при РА определяется местом начала расслоения. Боль за грудиной, спереди грудной клетки, имитирующая инфаркт миокарда, характерна для проксимального расслоения (более 90% случаев), особенно если оно распространяется на корень и вызывает сдавление коронарных артерий. При дальнейшем расслоении боль перемещается в межлопаточное пространство, затем смещается вдоль позвоночника. Мигрирующая боль по пути распространения расслаивающей гематомы отмечается у 17 70% больных. Локализация боли в шее, глотке, челюсти, лице, зубах указывает на вовлечение восходящей аорты и дуги. Боль в грудной клетке сзади, спине, нижних конечностях характерна для дистального расслоения, при этом она изначально локализуется в межлопаточном пространстве. Отсутствие боли в межлопаточном пространстве достаточное свидетельство против дистального расслоения. При распространении РА типов I и II на брюшную 10
4 P Післядипломне навчання аорту боль локализуется в надчревной области, подчревной области, пояснице, имитируя острые заболевания пищевого канала, урологические заболевания. Асимптомное (безболевое) течение (кроме больных с нарушением сознания) может быть у больных с хроническим расслоением. Обычно у пожилых людей надрыв аорты с образованием расслаивающей аневризмы протекает без болевого синдрома, но с внезапно появившейся резкой одышкой. Иногда развивается параплегия как временная, так и постоянная. Тромбоз какой-либо из основных ветвей аорты (сонной, почечной, верхней брыжеечной, подвздошных артерий) может быть ведущим клиническим проявлением, определяющим остроту течения заболевания. Расслаивание стенки аорты гематомой может привести к закупорке венечных артерий с развитием клинической картины инфаркта миокарда. При прогрессирующем проксимальном расслаивании стенки аорты возникает острая недостаточность аортальных клапанов. При прогрессировании дистального расслаивания стенки аорты гематомой наблюдается определенная последовательность вовлечения в процесс нижележащих органов, которая сопровождается соответствующим клиническим течением РА. После появления сильной боли соответственно месту надрыва стенки аорты при продвижении струи крови к месту отхождения желудочной и брыжеечной артерий появляются рвота кровью и кровавый стул. При расслоении аорты в области почечных артерий, бифуркации аорты может наблюдаться боль в пояснице в сочетании с гематурией, боль в ногах. Диагноз В связи с тем, что клиническая картина может очень быстро нарастать и наступает летальный исход, диагностика РА может вызывать некоторые затруднения. Дифференциальный диагноз РА надо проводить с острым инфарктом миокарда (электрокардиографическое исследование, эхокардиоскопия ЭХОКС, определение уровней креатинфосфокиназы КФК, тропонина), если, конечно, не произошло сдавление расслаивающей кровью венечных артерий сердца, т.е. не развился инфаркт миокарда вследствие расслаивающей аневризмы аорты. При прогрессировании дистального расслаивания и появлении абдоминальных симптомов необходимо исключить острый живот (отсутствие напряжения брюшного пресса и др.). Методы диагностики Если имеется хоть малейшее подозрение на расслоение аорты, важно быстро и точно верифицировать диагноз. Рентгенография органов грудной клетки позволяет выявить признаки, указывающие на расслоение аорты. Результаты рентгенологического обследования не являются специфичными, однако могут быть основанием для применения других методов исследования. Основные рентгенологические признаки РА: расширение тени аорты, лучше выявляемое в левой косой проекции (иногда локальное выпячивание в области расслоения); сепарация (отделение) кальцинированной интимы в области выпячивания от адвентиция более чем на 1 см (в норме до 0,5 см) вероятный, но не диагностический признак; изменение тени контуров аорты или средостения при сравнении с данными предыдущего исследования; отклонение трахеи или плевральный выпот (чаще левосторонний); резкое снижение или отсутствие пульсации ненормально широкой аорты. Большинство больных с РА имеет один или более рентгенологических признаков. Однако у 12% пациентов отклонения на рентгенограмме отсутствуют, поэтому отсутствие изменений при рентгенографии не позволяет исключить диагноз РА. Электрокардиография (ЭКГ) в 12 стандартных отведениях остается нормальной у 1/3 пациентов. Чаще всего выявляются неспецифические для РА признаки гипертрофии миокарда левого желудочка и связанные с ней изменения (депрессия сегмента ST, отрицательный зубец Т). Однако проведение ЭКГ, тем не менее, важно, потому что отсутствие изменений на ЭКГ (либо наличие очаговых изменений) у больного с выраженным болевым синдромом является важным дифференциально-диагностическим критерием РА с инфарктом миокарда. Лабораторные признаки не являются специфичными для диагностики РА: анемия (при значительной секвестрации крови в ложном канале или разрыве в полости); умеренный нейтрофильный лейкоцитоз; повышение уровней лактатдегидрогеназы и билирубина (из-за гемолиза крови в ложном канале); нормальные уровни КФК и трансаминаз; изредка возможно развитие тромбогеморрагического синдрома (ДВС-синдрома). Основными методами диагностики РА в настоящее время считают методы, позволяющие визуализировать аорту: аортография; контрастно-усиливающая компьютерная томография; ядерно-магнитный резонанс (ЯМР); трансторакальная эхокардиография. Каждая методика имеет свои преимущества и недостатки. Выбор метода зависит от возможности и опыта. Аортография раньше считалась единственно точным и достоверным методом диагностики РА. Прямыми признаками РА при аортографии являются: визуализация двух просветов (истинного и ложного), интимального лоскута; непрямыми деформация просвета аорты, расширение и деформация ее стенки. Аортография позволяет: определить протяженность расслоения; выявить вовлеченность ветвей аорты; определить место начального разрыва; оценить степень состоятельности аортального клапана и коронарных артерий. Недостатком аортографии является возможность получения ложноотрицательных результатов, что случается при слабой контрастированности ложного просвета из-за его возможного тромбоза. К сложностям применения аортографии следует отнести риск инвазивной процедуры и введения контрастного вещества (возможная его непереносимость), невозможность выполнения аортографии у нестабильных больных. Эхокардиография (ЭхоКГ) является доступным неинвазивным методом диагностики РА. По данным многих авторов, трансторакальная ЭхоКГ позволяет выявить 80% РА. В настоящее время особую роль в диагностике РА отводят чреспищеводной ЭхоКГ (чувст- 11
5 фармакотерапія 5 (141) / 2010 P вительность метода составляет 95%, специфичность 75%), являющейся методикой выбора при нестабильном состоянии больного. ЭХОКС позволяет визуализировать расширение луковицы аорты, увеличение толщины стенок аорты, функцию аортального клапана, определить подвижный лоскут в просвете аорты, а также дает дополнительную информацию о сердечных структурах и функции. При проведении компьютерной томографии (КТ) с введением контраста РА определяется по наличию двух различных просветов, видимо разделенных интимальным лоскутом, либо по различной степени контрастного затемнения. Чувствительность метода 83 94%, специфичность %. Существенными преимуществами КТ являются: неинвазивность, хотя и требуется внутривенное введение контраста, доступность, возможность установить диагноз РА в случае тромбоза ложного просвета, возможность определить наличие перикардиального выпота. Недостатки КТ: относительно невысокая чувствительность в отношении диагностики РА, невозможность в 1/3 случаев выявить интимальный лоскут, редкость установления места начального разрыва, невозможность выявить наличие аортальной регургитации и вовлечение сосудистых ветвей. Ядерно-магнитный резонанс является неинвазивной методикой, не требует внутривенного введения контраста, при этом предоставляет высококачественное изображение в нескольких плоскостях. ЯМР облегчает распознавание РА, позволяет выявить вовлеченность ветвей, а также диагностировать РА у пациентов с предшествующими заболеваниями аорты. Чувствительность и специфичность метода около 98%, при этом чувствительность составляет 88% для установки места интимального разрыва и аортальной регургитации, 98% для диагностики наличия тромбоза и 100% для выявления перикардиального выпота. Благодаря высокой точности ЯМР признан современным «золотым стандартом» в диагностике РА. Однако у этого метода все же имеются недостатки: проведение ЯМР противопоказано больным с пейсмейкером, пациентам при наличии определенного типа сосудистых скрепок. ЯМР не является широкодоступным методом. Некоторые авторы считают относительным противопоказанием к проведению ЯМР нестабильное состояние больного, требующее внутривенного назначения гипотензивных препаратов и мониторинга АД. Лечение Без своевременного и соответствующего лечения РА имеет высокий уровень летальности. Основной причиной смерти при проксимальном расслаивании является тампонада сердца или окклюзия магистральных ветвей аорты. При дистальном расслаивании кровотечение в левую плевральную полость и почечная недостаточность. Лечение при РА направлено на остановку прогрессирования расслаивающей гематомы. Летальный исход обычно обусловлен не самим интимальным разрывом, а возможными сосудистыми осложнениями или разрывом аорты. Летальность при проксимальном типе среди пациентов, лечившихся консервативно, примерно в 4 раза выше, чем у оперированных. Все больные с РА должны быть госпитализированы в отделение интенсивной терапии для стабилизации гемодинамики, мониторинга АД, сердечного ритма и диуреза, контроля центрального венозного давления, независимо от дальнейшей тактики лечения. Интенсивная терапия при остром расслоении направлена на купирование болевого синдрома (введением морфина) и снижение АД. Блокаторы β-адренорецепторов применяют в постепенно возрастающих дозах (для уменьшения сердечного выброса) до снижения частоты сокращений сердца 60 в минуту. Метопролол назначают в дозе 5 мг внутривенно каждые 5 минут (до трех раз). Лабеталол как блокатор β-адренорецепторов в 2 7 раз менее активен, чем фентоламин. Блокирует альфа- и бетаадренорецепторы в соотношении 1:3. Артериальное давление снижается, в основном, за счет уменьшения периферического сопротивления при практически не изменяющемся сердечном выбросе. Внутривенное введение осуществляется либо болюсно мг, либо медленно капельно мг в сутки в 200 мл физиологического раствора или глюкозы. Препарат противопоказан при нарушениях атриовентрикулярной (АВ) проводимости, склонности к бронхоспазму. При наличии противопоказаний к применению блокаторов β-адренорецепторов (брадикардия, АВ-блокада, бронхоспазм) применяют антагонисты кальциевых каналов. Нифедипин сублингвально может быть применим неотложно. Недостатком нифедипина является слабое отрицательное инотропное и хронотропное дейст вия, в связи с чем могут быть применены дилтиазем и верапамил. При неэффективности блокаторов β-адренорецепторов возможно применение нитропруссида натрия в дозе 0,5 10 мг/кг в минуту внутривенно капельно. При стойкой артериальной гипертензии в результате вовлечения почечных артерий наиболее эффективно применение ингибиторов ангиотензинпревращающего фермента (эналаприл 0,625 мг внутривенно каждые 4 6 часов с постепенным увеличением дозы). При нормальном АД применяются только блокаторы β-адренорецепторов (а при невозможности их применения дилтиазем или верапамил) для уменьшения скорости изгнания левого желудочка. При гипотензии нельзя исключить развитие тампонады сердца, что требует быстрого восстановления объема циркулирующей крови. При рефракторной гипотензии предпочтительно использовать норадреналин, мезатон. Допамин используется для улучшения функции почек и только в малых дозах. Последующая тактика определяется типом расслоения. Хирургическое лечение Все больные с подозрением на РА должны быть проконсультированы сосудистым хирургом. Хирургическое вмешательство является методом выбора при острых проксимальных расслоениях аорты. Хирургическое лечение также показано при хроническом восходящем расслоении с тяжелой аортальной регургитацией, локализованной аневризме. При хроническом дистальном расслоении операция показана при аневризме более 6 см в диаметре. При дистальном расслоении консервативная терапия оправдана в связи с более низким риском ранней смерти, более пожилым возрастом пациентов, наличием выраженного атеросклероза или легочно-сердечных заболеваний, повышающих риск хирурги- 12
6 P Післядипломне навчання ческого вмешательства. При этом типе расслоения хирургическое лечение показано при формировании мешотчатой аневризмы, при вовлечении жизненно важных органов, ишемии конечностей, продолжающемся, несмотря на консервативную терапию, расслоении, ретроградном распространении на восходящую аорту. Хирургическое лечение показано всем больным с синдромом Марфана. Консервативное лечение является методом выбора при не осложненном дистальном расслоении, стабильном изолированном расслоении дуги аорты и стабильном неосложненном хроническом расслоении (давностью более двух недель). Риск оперативного вмешательства увеличивается при наличии сопутствующих заболеваний, особенно эмфиземы легких, при нарушении целостности аневризмы, тампонаде сердца, шоке, вовлечении жизненно важных органов. Послеоперационная летальность при быстром хирургическом лечении значительно ниже (3%), чем при длительной предоперационной подготовке (20%). Цели хирургического лечения: резекция наиболее поврежденного сегмента аорты, содержащего интимальный разрыв; удаление интимального лоскута; облитерация входа в ложный канал; протезирование иссеченного участка аорты; восстановление состоятельности аортального клапана (вальвулопластика). Возможные осложнения хирургического вмешательства при РА: ранние кровотечения, инфекции, легочная и почечная недостаточность, иногда ишемия спинного мозга с параплегией; прогрессирование аортальной регургитации; формирование локальной аневризмы; повторное расслоение. С внедрением новых хирургических методов послеоперационная выживаемость составляет при проксимальном расслоении 80%, при дистальном 90%. Такими методами, позволившими снизить летальность у оперированных пациентов с РА, являются: тромбоэксклюзия в типичных случаях расслоения нисходящей аорты, применение эндоваскулярных методов (баллонная дилатация почечных артерий), применение специального клея для заполнения ложного просвета. Последующее длительное лечение всех больных после выписки из стационара включает поддержание систолического АД на уровне не выше мм рт. ст., назначение гипотензивных средств с отрицательным инотропным действием (блокаторы β-адренорецепторов, антагонисты кальция), проведение контрольной рентгенографии, компьютерной томографии, магнитнорезонансной томографии каждые три месяца в течение первого года, затем каждые 6 месяцев. Возможно развитие поздних осложнений формирование аневризм после хирургического лечения на месте восстановления. Часть поздних смертей может быть обусловлена разрывом ложного просвета после успешного хирургического вмешательства. Таким образом, при расслаивающей аневризме аорты показано хирургическое лечение. Кратковременное консервативное лечение направлено на подготовку больного к предстоящей операции. Прогноз неблагоприятный. Как правило, больные с данной патологией быстро умирают. Случаи длительного выживания больных и самоизлечения наблюдаются крайне редко. Профилактика связана с профилактикой и лечением заболеваний, обусловливающих расслаивающую аневризму аорты (атеросклероз, гипертоническая болезнь и др.). Литература 1. Атьков О.Ю., Атауллаханова Д.А., Синицын В.Е. Применение визуализирующих методов в диагностике расслаивающей аневризмы аорты // Визуализация в клинике С Бураковский В.И., Бокерия Л.А. Расслаивающие аневризмы аорты // Сердечнососудистая хирургия. 2003, 29 марта. 3. Громнацкий Н.И. Руководство по внутренним болезням. М.: Мед. информ. агентство, с. 4. Follath F., Hjalmarson A., Tubaro M. Всемирный конгресс клинических исследователей в области сердечно-сосудистых заболеваний // Здоров я України С Атыков О.Ю., Атаулханов Д.М., Синицын В.Е. Применение визуализирующих методов в диагностике расслаивающей аневризмы аорты // Визуализация в клинике
источник







