Ложная аневризма (псевдоаневризма, пульсирующая гематома, ПА) представляет собой сообщение между просветом артерии и расположенной рядом соединительной тканью, что приводит к образованию полости, заполненной кровью. Полость гематомы не содержит структур нормальной стенки артерии (медии и адвентиции), что и отличает ее от истинной аневризмы. Механизм образования ПА заключается в рассасывании тромба, закрывающего место пункции. В результате пульсирующий кровоток из бедренной артерии во время систолы растягивает окружающие ткани, образуя сообщающуюся с просветом артерии полость, а во время диастолы происходит ее декомпрессия.

Факторами риска развития ложной аневризмы являются использование интродьюсера большего диаметра, комбинации ангитромботичсских препаратов, большая длительность процедуры, сложности при проведении пункции бедренной артерии, анатомические особенности пациента. Частота развития ее составляет от 0,1-0,2 % при диагностической коронарографии и до 0,5-6,3 % (в среднем 1 %) в случае ЧКВ.

Клинически ложная аневризма проявляется болью в паховой областью, хотя она может протекать и бессимптомно. Физикально ложную аневризму можно отличить от обычной гематомы по наличию пульсирующей массы в паху, аскультативно — по наличию локального шума. Однако при физикальном осмотре не диагностируется до 60 % ПА. Поэтому при подозрении на ложную аневризму больному проводят цветное дуплексное сканирование места пункции. К У3-признакам ПА относят выявление сообщения (так называемой шейки) между просветом ложной аневризмы.
Клиническое значение ложной аневризмы зависит от ее размера. Если диаметр ПА менее 2 см, то через 2 нед. она закрывается самостоятельно в 50 % случаев, а через 2 мес. — в 90 % случаев. Таким образом, при отсутствии клинической симптоматики в случае небольших ложных аневризм возможна консервативная тактика и лишь при сохранении ПА по данным контрольного УЗИ через 2 мес. наблюдения рекомендуется применение инвазивной тактики.
С другой стороны, большие ложные аневризмы могут постепенно увеличиваться и в конечном итоге разрываться с развитием брюшинного кровотечения или забросом крови в межмышечные пространства бедра. Кроме того, ложная аневризма может сдавливать окружающие нейроваскулярные структуры, что может привести к тромбозу бедренной вены (при сдавлении бедренной вены) или нейропатии (при сдавлении бедренного нерва). В этом случае больному требуется экстренное хирургическое лечение.
В настоящее время большинство ложных аневризм лечат малоинвазивными методиками. Наиболее часто используется метод мануальной компрессии. Сущность его состоит в пальцевом прижатии шейки ПА под контролем УЗ-датчика, как правило, в течение 15-30 мин, что приводит к закрытию сообщения между просветом артерии и полости ложной аневризмы. В конце процедуры выполняют контрольное УЗИ. Частота закрытия ложной аневризмы при данной методике после первой попытки составляет 86 %. В 5 % случаев в конечном итоге требуется хирургическое лечение. Недостатками данного метода являются ее длительность (до 2 ч в некоторых случаях), болезненность процедуры, отсутствие полного закрытия в случае больших ложных аневризм. Также возможны ранние рецидивы, особенно в случае ПА более 4 см в диаметре или на фоне интенсивной антитромботической терапии. Рецидивы преимущественно устраняются повторным проведением процедуры.
Другим способом лечения ложной аневризмы является инъекция тромбина в полость ПА под УЗ-контролем. Успех процедуры составляет около 98 %, в отличие от мануальной компрессии ПА закрывается сразу после инъекции. Этот метод может применяться при различном размере ПА (от 1,5 до 7,5 см), а также в случае многокамерных ложных аневризм. Рецидивы возникают в 5 % случаев, они успешно устраняются повторной инъекцией тромбина. В целом метод безопасен, однако в случае попадании препарата в основную артерию возможны тромбоз бедренной артерии или дистальная эмболия, что может привести к острой ишемии нижней конечности. Очень редко развивается тромбоэмболия легочной артерии. Противопоказаниями к проведению инъекции тромбина является наличие у ложной аневризмы широкой или короткой шейки, а также артериовенозная фистула.
Основной мерой профилактики ПА является точная пункция общей бедренной артерии (при пункции не общей бедренной артерии, а поверхностной или глубокой бедренной артерии риск развития ложной аневризмы выше), а также тщательное соблюдение времени и методики проведения гемостаза после удаления интродьюсера.
источник
Последнее обновление статьи: Апрель , 2019
Псевдоаневризма или ложная аневризма — это патологическое образование, возникающее в результате нарушения целостности стенки крупной артерии и продолжающегося кровотечения. Излившаяся кровь скапливается в тканях вокруг артерии образуя опухолевидное образование.
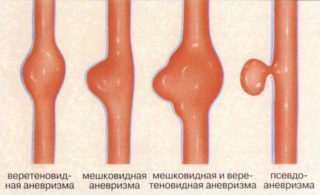
Возникновение настоящей (истинной) аневризмы вообще не связано с кровотечением и представляет собой «мешковидное» расширение артерии.
Приставка «псевдо» объясняется тем, что без дополнительного обследования отличить настоящую аневризму от псевдоаневризмы на первый взгляд не так просто, особенно не зная истории болезни.
На представленной иллюстрации аневризма отмечена цифрой (1), а псевдоаневризма (2)
Основная причина — это нарушение целостности артерии, возникающее при различных проникающих травмах. Но в кардиологической практике псевдоаневризма встречается как осложнение коронарографии, проводимой через бедренную артерию, как следствие не адекватного гемостаза (остановки крови).
Далее мы будем говорить только о псевдоаневризме бедренной артерии .
Это осложнение встречается относительно часто, около 5% и хотя оно во многом зависит от опыта врача, но предупредить его полностью не в состоянии даже самый лучший специалист. Кроме того, часть вины за возникновение псевдоаневризмы возлагается на пациента, который не выполняет указаний врача, встает с постели раньше времени, сгибает ногу, через которую была выполнена процедура, и делает прочие вещи, которые делать не стоит.
После того как врач заканчивает коронарографию, из артерии извлекается проводник оставляющий достаточно широкое отверстие. Чтобы избежать кровотечения из места прокола, сразу выполняется давление на артерию: сначала вручную, а затем при помощи давящей повязки. Иногда используют специальное закрывающее устройство, работающее по типу пробки. Но если отверстие не было закрыто полностью, то кровь под давлением начинает распространяться и раздвигать мышечную ткань, образуя пульсирующее опухолевидное образование.
Основной симптом псевдоаневризмы это боль. Однако давящая повязка, да и сама рана в области прокола артерии создают неприятные и иногда болезненные ощущения, больные даже при нормальном течении послеоперационного процесса могут похрамывать еще день из-за боли в паху. Поэтому боль как основной симптом псевдоаневризмы обычно малополезен хотя и позволяет заподозрить что речь идет об аневризме.
Другой симптом в виде внезапного похолодания конечности и исчезновения пульсации артерий бедра, голени или ступни является признаком того, что случилась катастрофа — псевдоаневризма достигла значительных размеров и сдавила артерию. В этих случаях необходимо срочное хирургическое вмешательство для спасения не только ноги, но и жизни больного.
Обычно хирурги вскрывают псевдоаневризму и затем при помощи швов останавливают дальнейшее кровотечение. Обычно эта процедура не сложная и случаи, когда после коронарографии псевдоаневризмой причиняется существенный вред здоровью, крайне редки и даже казуистичны.
Наиболее доступным и точным метод диагностики является УЗИ исследование. Реже возникает необходимость провести томографию, если есть подозрение что имеется более обширное кровотечение. Хотя во многих случаях опытный врач, только применив свои тактильные ощущения и стетоскоп, способен установить диагноз.
Если речь идет о неосложненной псевдоаневризме, то лечение заключается в прекращении кровотока между артерией и полостью псевдоаневризмы. Это сообщение осуществляется через так называемую «шейку» которую можно просто пережать давлением пальцами в течение 10-15 минут. После этого проводят контрольное УЗИ, и если прижатие не помогло, то есть две опции.
Первая – под контролем УЗИ можно сделать несколько инъекций стерильного физиологического раствора в область шейки, тем самым пережав ее.
Второй вариант — ввести в полость тромбин — вещество, которое вызывает тромбоз псевдоаневризмы, таким образом ее распространение становится невозможным.
Четкое выполнение требований врача и медперсонала после вмешательства является критичным моментом в профилактике осложнений. Необходимо лежать 4 часа, не шевелить ногой и ни в коем случае не сгибать ее. В 99% случаев эти меры позволяют избавить пациента от большинства проблем и позволят ему вернуться к обычному образу жизни уже на другой деть после процедуры.
источник
Чем опасна ложная аневризма бедренной артерии и способы ее лечения: операционный, компрессионный, эндоваскулярный и народная медицина
Бедренная артерия — крупный периферический сосуд, транспортирующий кровь и полезные вещества через паховые узлы, наружные половые органы, нижние конечности. Служит продолжением предвздошной артерии. Его анатомическое строение у всех людей одинаковое, не считая незначительных индивидуальных особенностей. С возрастом сосуд истончается, теряет эластичность и способность сопротивляться кровяному потоку. Это приводит к появлению различных заболеваний. Одно из них — аневризма бедренной артерии.
Аневризма бедренной артерии — патологическая проблема, которая характеризуется изменением состояния стенок сосуда. Они начинают отделяться друг друга и истощаются.
Внешний признак заболевания — припухлость вены в области паха или под коленом.
- резкое повышение уровня холестерина;
- хирургическое вмешательство;
- травма;
- инфекция (сифилис, туберкулез);
- генетическая предрасположенность.
Негативно сказываются на здоровье сосудов атеросклеротические бляшки, воспалительные процессы, повышенное артериальное давление.
Аневризмы бедренной артерии могут быть одиночными и множественными.
Большинство страдающих аневризмой не замечают первых симптомов заболевания или вовсе не имеют их. Чтобы распознать опасность, необходимо очень чутко относится к своему организму и реагировать на изменения. Характерные признаки патологии бедренной артерии:
- боль в животе, спине;
- острая боль под коленом, в паху;
- онемение конечности;
- похолодание ног;
- нарушение чувствительности;
- бледный кожный покров;
- пульсация в месте выпячивания сосуда.
Ухудшение состояния отмечается после длительных физических нагрузок. В результате прогрессирования болезни появляются судороги. Нарушение чувствительности приобретает стойкий характер, вплоть до парализации конечностей.
Острая форма закупорки сосудов развивается за 1-10 дней. Симптомы при этом имеют ярко выраженный характер. Кожа в области бедренной артерии меняет цвет на бледный или, наоборот, багровый. Боль и жжение проявляются по нарастающей.
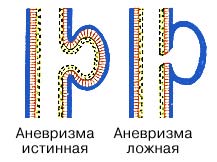
Проблема может возникнуть на месте истинной, если истонченные мышечные или эластичные волокна будут заменены соединительной тканью.
Псевдоаневризма бедренной артерии формируется от 15 до 17 дней после поражения сосуда. Чаще всего это происходит глубокого в тканях. Из-за этого своевременно диагностировать патологию крайне проблематично. Главные симптомы — усиление шумов при пульсации, припухлость, боль, изменение цвета кожи.
Самый опасный вид протекания заболевания — бессимптомный. Больной продолжает вести привычный образ жизни и рискует в любой момент получить разрыв аневризмы. Формирование и разрастание этого образования может длиться более 3 лет и любая перенагрузка способна вызвать рецидив.
Разрыв аневризмы часто приводит к летальному исходу при родах, на поздних сроках беременности или во время приступа гипертонии.
Другие виды осложнений, которые появляются на фоне аневризмы:
- закупорка сосудов тромбами;
- гангрена нижних конечностей;
- нагноение гематомы с флегмоной окружающих тканей (ложная аневризма);
- дерматологические проблемы из-за недостатка притока крови.
Чтобы не допустить перечисленных проблем, следует регулярно проходить медицинское обследование и следить за здоровьем сосудов.
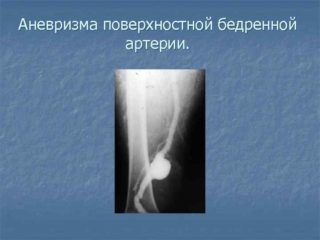
- ангиография;
- УЗИ сосудов нижних конечностей.
По полученным данным можно определить истинные размеры аневризмы, её форму, наличие обходных путей и состояние кровообращения выше и ниже патологии.
Для лечения заболевания бедренной артерии консервативный метод не используется. Медикаменты помогают лишь отсрочить разрыв аневризмы, но не избавляют от него. Оптимальный вариант — операционное вмешательство. Народные средства, компрессы и прочие методики эффективны в комплексе с хирургией.
Выделяют три основных типа операции при аневризме:
- Протезирование. Пораженный отрезок сосуда иссекается, а на его место устанавливается синтетический протез.
- Шунтирование. Больной фрагмент сосуда удаляется. Для дальнейшего питания тканей к ним прокладывают обходной путь от артерии. Чаще всего используют периферический сосуд или близлежащую вену.
- Стентирование. Наименее травматичная методика, которая заключается во введении металлического каркаса в сосуд. За счет процедуры укрепляется стенка бедренной артерии, что предотвращает разрыв и тромбоз.
Если риски операционного вмешательства слишком большие, врач предлагает занять выжидательную позицию. В этом случае следует придерживаться здорового образа жизни, избегать физических нагрузок и стрессов. В качестве временной терапии назначаются препараты для разжижения крови и нормализации давления.
Эффективность компрессионного метода лечения аневризмы — от 50% до 90%. Конечный результат зависит от индивидуальных особенностей, глубины и расположения патологии. Осложнения, которые могут возникнуть при данной терапии:
- разрыв аневризмы;
- тромбоз глубоких вен.
Прежде, чем соглашаться на использование компресса, взвесьте все за и против и проконсультируйтесь с несколькими специалистами.
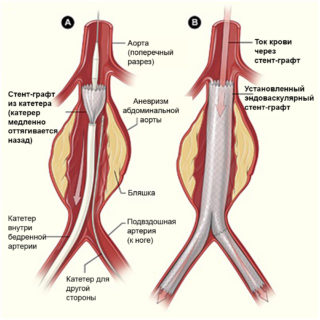
- выполняется амбулаторно, редко требует госпитализации;
- не требует общего наркоза;
- высокий уровень безопасности;
- низкий болевой порог;
- минимальный риск осложнений.
Недостатками эндоваскулярного лечения являются его высокая стоимость и короткий срок службы стент-графта.
В народной медицине для профилактики и улучшения состояния сосудов применяют травяные отвары. Лучше всех себя зарекомендовали:
- сибирская бузина;
- укроп;
- ягоды боярышника.
Их следует заварить кипятком, настоять и принимать внутрь в небольших количествах перед каждым приемом. Однако обязательно стоит учитывать противопоказания и склонность к аллергии. Предварительно проконсультируйтесь с лечащим врачом.
Обращение в клинику на начальной стадии заболевания гарантирует успешное лечение. В некоторых случаях это возможно без хирургического вмешательства, например, с помощью препаратов или компрессионного метода. Запущенные патологии сложнее поддаются терапии, но в условиях современной медицины осложнения и риск летального исхода минимален.
Высшее образование:
- 1985 — Военно-медицинская академия имени С. М. Кирова (лечебно-профилактическое дело)
- 1986 — Военно-медицинская академия имени С. М. Кирова (интернатура северного флота по специальности: «хирургия», г. мурманск.)
- 1991 — Военно-медицинская академия имени С. М. Кирова (клиническая ординатура на кафедре военно-морской и госпитальной хирургии)
Повышение квалификации:
- 1992 — Тренинг по ангиографии и сосудистой хирургии в Гамбурге, Германия
- 1992 — Хирургия сосудов
- 2003 — Сердечно-сосудистая хирургия
- 2004 — Стажировка в университетской клинике Нюрнберга ( клиника сосудистой хирургии) профессор D.Raithel; Германия
- 2006 — Лимфедема и венозный отек: Европейский опыт лечения
- 2006 — Стажировка в университетской клинике Нюрнберга ( клиника сосудистой хирургии) профессор D.Raithel; Германия
- 2008 — Сердечно-сосудистая хирургия
- 2008 — Лазерная система Dornier Medilas D MultiBeam
- 2009 — «Ультразвуковые методы исследования в диагностике хирургической патологии сосудов нижних конечностей»
- 2009 — Сердечно-сосудистая хирургия
- 2009 — Тренинг во флебологической клинике; Висбаден, Германия.
- 2012 — «Рентгенэндоваскулярная диагностика и лечение»
- 2013 — «Сердечно-сосудистая хирургия»
- 2016 — «Ультразвуковая диагностика»
Опыт работы:
- 1985-1989 Большая атомная подводная лодка Северного флота
- 1989-1991 Военно-Медицинская Академия им.С.М.Кирова
- 1991-1994 Центральный военно-морской клинический госпиталь
- 1994-1998 Центральный военно-морской клинический госпиталь
- 1998-2015 Центальный военно-морской клинический госпиталь
- 2016-н. в. Многопрофильная клиника ЦЭЛТ (Центр эндохирургии и литотрипсии)
источник
Патологическое выпячивание стенки бедренной артерии называют аневризмой. Она возникает при истончении средней оболочки сосуда. Вначале протекает бессимптомно, по мере развития осложняется закупоркой просвета артерии тромбом или разрывом с массивным кровотечением. Для лечения нужна операция – удаление аневризматического мешка или установка шунта, стента.
Не всегда возможно определить этиологию формирования аневризмы. На основании научных исследований это заболевание признано мультифакторным. Основными причинами изменений артериальной стенки бывают:
- генетическая предрасположенность;
- атеросклеротические изменения сосудов;
- врожденные дефекты соединительной ткани (синдромы Марфана, Элерса-Данлоса, фиброзномышечная дисплазия, недостаток эластина);
- воспаление артерии (артериит);
- узелковый периартериит;
- закупорка эмболом при бактериальной или грибковой инфекции;
- злокачественные или доброкачественные новообразования;
- лучевая терапия;
- огнестрельные, колотые ранения, удары тупыми предметами;
- операции и диагностические исследования.
К факторам риска относятся наличие у пациента определенных патологий: артериальной гипертензии, поликистоза почек, ожирения, никотиновой или алкогольной, наркотической зависимостей.
А здесь подробнее об атеросклерозе брюшного отдела аорты и подвздошных артерий .
Начальных проявлений заболевания пациенты обычно не ощущают. Но аневризмам свойственно постепенно увеличиваться в размерах под воздействием давления крови. Большое образование нарушает кровоток и прохождение нервных импульсов. Возникает следующая симптоматика:
- боль в паховой или бедренной области, возрастающая при физическом напряжении;
- ощущение пульсации;
- онемение нижележащих тканей;
- судорожные подергивания мышц;
- бледность и цианотичный оттенок стоп.
На месте аневризмы появляется припухлость кожи, которая имеет плотную консистенцию, круглую или овальную форму, пульсирует в такт сокращениям сердца. В образованном мешке кровь течет не по прямой, а вдоль стенок, направление с линейного меняется на турбулентное. Это приводит к ускоренному тромбообразованию и прекращению питания тканей.
Если бедренная артерия повреждается извне при пункции, операции на сосудах, огнестрельном ранении, нанесении удара колющим или тупым предметом, то возникает такое заболевание, как ложная аневризма. Место нарушения целостности сосуда оказывается прикрытым кожей или мягкой тканью, а вытекшая кровь сохраняется в мягких тканях.
Формируется пульсирующая гематома, которая не является в прямом понимании аневризмой. В полости этого образования появляются сгустки крови, они постепенно уплотняются и покрываются капсулой, она срастается со стенкой артерии и выглядит как аневризматическое выпячивание.
Многие пациенты, не подозревая о наличии аневризмы, продолжают вести обычный образ жизни. Формирование и разрастание этого образования может длиться более 3 лет, сопровождаясь незначительными симптомами. Под действием физических перегрузок, в период беременности или родов, при резком повышении давления может произойти разрыв стенки бедренной артерии. Если своевременно пациенту не провести операцию, то интенсивное кровотечение несет угрозу для жизни.
Помимо разрыва, наличие аневризмы повышает риск таких осложнений:
- закупорка артерии тромбом;
- передвижение частей кровяного сгустка с эмболией ветвей и гангреной нижних конечностей;
- нагноение гематомы (ложной аневризмы) с флегмоной окружающих тканей;
- трофические нарушения (дерматит, язвы) из-за недостатка притока крови.
Внешними признаками заболевания является наличие плотного пульсирующего образования. При аускультации над ним можно услышать систолический шум, исчезающий при сдавлении вышележащего участка. Ниже локализации аневризмы отмечается пониженная пульсация артерий. Для подтверждения диагноза показано проведение ангиографии и УЗИ сосудов нижних конечностей с дуплексным сканированием. Эти методики помогают установить:
- истинные размеры;
- форму образования;
- состояние кровообращения выше и ниже аневризмы;
- наличие обходных путей.
Такие данные важны для планирования оперативного вмешательства.
Консервативное лечение при наличии аневризмы не проводится. При помощи медикаментов можно только отсрочить разрыв стенки артерии, применив гипотензивные препараты. Оптимальным вариантом терапии является операция. Основные виды хирургических вмешательств представлены в таблице.
| Виды операции | Краткое описание |
| Протезирование | Отрезок сосуда с аневризматическим мешком иссекается, а на его место устанавливается протез из синтетического материала или вены пациента. |
| Шунтирование | После удаления фрагмента артерии с аневризмой прокладывается обходной путь для питания тканей, для шунта используют собственный сосуд больного (чаще периферическую вену). |
| Стентирование | Считается менее травматичной методикой, так как не требует открытого доступа, в сосуд вводится металлический каркас, который укрепляет стенки бедренной артерии, предотвращая ее разрыв и тромбоз. |
При небольшом размере и высоком риске операции может быть выбрана выжидательная тактика. В этом случае пациенту противопоказано физическое перенапряжение, назначаются препараты для поддержания нормального давления крови и препятствующие тромбообразованию. Такие больные должны регулярно проходить обследование, наблюдаться сосудистым хирургом.
А здесь подробнее об аневризме сонной артерии.
Аневризма бедренной артерии возникает при истончении оболочек сосуда (истинная) или внешнем повреждении (ложная). Начальные проявления обычно отсутствуют. По мере роста нарушается кровоснабжение и иннервация тканей нижних конечностей, что проявляется болью, судорожным синдромом, онемением и образованием пульсирующей припухлости на коже.
Для подтверждения диагноза показана ангиография и УЗИ сосудов. Лечение аневризмы хирургическое – иссечение расширенного фрагмента, протезирование, шунтирование или стентирование.
Смотрите на видео о стентировании сосудов нижних конечностей:
Проводится операция на бедренной артерии при угрозе жизни из-за тромба, эмбола, бляшки. Процедура профундопластика может быть проведена разными способами. После вмешательства человек остается в стационаре.
Возникнуть аневризма подколенной артерии может даже из-за травмы. Симптомы — шишка, выпячивание. Лечение преимущественно хирургическое, народные средства могут оказаться бессильны.
Выполняется резекция аневризмы при сосудистых патологиях, угрожающих жизни. Резекция брюшной аорты с протезированием позволяет избежать обильного кровотечения и смерти пациента.
После 65 лет нестенозирующий атеросклероз брюшного отдела аорты и подвздошных вен встречается у 1 из 20 человек. Какое лечение допустимо в этом случае?
Если выявлена аневризма сердца, операция может стать единственным шансом на спасение, только с ней прогноз улучшается. Жить без операции в целом можно, но только в том случае, если аневризма, например, левого желудочка очень маленькая.
Выпячивание или аневризма сонной артерии может быть врожденным состоянием. Также она бывает левой и правой, внутренней и внешней, мешотчатой или веретенообразной. Симптомы проявляются не только в виде шишки, но и нарушении самочувствия. Лечение — только операция.
Если воспалилась аневризма аорты, операция может спасти жизнь. Пациенту стоит знать, какие проводят операции, важные показатели к хирургическому вмешательству, реабилитация и прогноз после, последствия вмешательства. А также об образе жизни и питании после. Какие есть виды замены аорты, протезирование аневризмы и осложнения после. Сколько идет эндоваскулярное протезирование.
Если выявлена аневризма аорты, жизнь пациента в опасности. Важно знать причины и симптомы ее проявления, чтобы как можно раньше начать лечение. В основном это операция. Может диагностироваться разрыв аорты брюшного, грудного и восходящего отдела.
Если образовалась аневризма сердца, симптомы могут быть схожи с обычной сердечной недостаточностью. Причины — инфаркт, истощение стенок, изменения сосудов. Опасное последствие — разрыв. Чем раньше проведена диагностика, тем больше шансов.
источник
Артерии в организме человека – это самые крупные кровеносные сосуды. Бедренная артерия относится к их числу, она снабжает кровью нижние конечности, органы малого таза и паховые узлы. Величина сосудов не защищает их от различных заболеваний. Одной из патологий является ложная аневризма, которая встречается достаточно часто.
При развитии этой болезни происходит выпячивание стенок сосудов в результате их истончения. Вполне возможно методом прощупывания обнаружить у себя такую патологию. Она проявляется как припухлость по ходу пролегания сосуда. Чтобы не допустить развития этого заболевания необходимо разобраться с причинами, симптомами и тактикой лечения. Это мы постараемся сделать в этой статье.
Любое заболевание не возникает на пустом месте, для этого нужен некий толчок, который спровоцирует развитие болезни. Если говорить про аневризму бедренной артерии, то для начала ее развития пусковым механизмом могут быть следующие факторы:
- Вредное воздействие никотина и смолистых веществ, содержащихся в сигаретах.
- Гипертония.
- Увлечение продуктами с высоким содержанием холестерина.
- Если масса тела превышает норму.
- Играет роль в какой-то степени и наследственный фактор.
Совет! Если у родственников встречается такая патология, как недостаточно развитая соединительная ткань, то риск заполучить аневризму повышается в несколько раз.
Если первые шесть пунктов больше относятся к развитию истинной аневризмы, то последние характерны для ложной. В этом случае припухлость сосудов может отсутствовать, а имеется гематома, окруженная соединительной тканью.
Несмотря на то, что травмы и оперативные вмешательства часто провоцируют развитие ложной аневризмы бедренной артерии, но это происходит далеко не всегда. Это можно объяснить тем, что для ее появления необходимо, чтобы были выполнены следующие условия:
- Область разрушения мягких тканей в районе сосуда была небольшая.
- Рана должна иметь неровный и длинный ход.
- Входное и выходное отверстие должны закрыться мягкими тканями.
Эти условия не дают вытекать крови наружу, она скапливается внутри, что и приводит к развитию гематомы, а это и есть начало формирования аневризмы бедренной артерии.
Гематома может иметь разные размеры, поэтому при наличии небольшого образования на первых стадиях заболевания человек может ничего не ощущать. Если говорить о симптомах, то они будут зависеть не только от того, какие размеры имеет ложная аневризма, но и от ее локализации. 
- Прощупывание пульсирующего образования.
- Появление болевых ощущений, которые усиливаются во время физических нагрузок.
- Частые судороги в ноге.
- В области пальцев ног могут появляться язвочки и ранки.
- При развитии аневризмы может происходить сдавливание нервных окончаний, что приводит к онемению конечности.
- Некроз тканей в случае закупорки просвета артерий.
Если хоть несколько перечисленных признаков наблюдаются, то не стоит чего-то дожидаться, необходимо отправляться на консультацию к доктору.
Поставить диагноз псевдоаневризма бедренной артерии без тщательного обследования невозможно. Обычно после обращения к врачу назначают следующие анализы и исследования:
- УЗИ.
- МРТ.
- Спиральная компьютерная томография.
- Ангиография.
- Анализ крови и мочи.
- ЭКГ.
Кроме этого, обязательно посещение сосудистого хирурга, который адекватно может провести диагностику состояния артерий.
Терапия аневризмы бедренной артерии зависит от многих факторов:
- Размеров гематомы.
- Локализации.
- Скорости увеличения размеров.
Выбирая тактику лечения, врач всегда взвешивает все за и против, только тогда выбирается способ терапии. В современной медицине существует несколько методов лечения:
- Оперативное вмешательство.
- Компрессионный способ.
- Эндоваскулярные способы лечения ложной аневризмы бедренной артерии.
Если гематома уже приличных размеров, то чаще всего показано оперативное удаление. Этот метод имеет высокую эффективность, но после операции почти в 50% случаев развиваются осложнения.
Компрессионный метод лечения имеет эффективность от 50 до 90%, которая зависит от свертываемости крови пациента, размеров и глубины расположения аневризмы. Этот способ также может осложняться, например, разрывом гематомы, тромбозом глубоких вен. Эндоваскулярное лечение заключается в установке стент-графта, эмболизации спиралями полости сосуда. Этот метод лечения имеет свои недостатки:
- Высокая стоимость.
- Маленький срок службы стент-графта.
- Необходимо проводить дополнительную пункцию артерии.

При наличии ложной аневризмы необходимо внимательно относиться к своим ощущениям и состоянию. Несмотря на то, что разрыв гематомы бывает редко, но все-таки это может случиться.
При увеличении в размерах аневризма может сдавливать соседние нервы, сосуды, что может приводить к боли, отекам и онемению. Если не заниматься лечением, то возможны следующие осложнения:
- Эмболия.
- Тромбоз артерий.
- Гангрена конечности.
Стоит согласиться, что это уже достаточно серьезно, поэтому не надо пускать на самотек течение болезни. Учитывая, что вызвать развитие аневризмы бедренных артерий могут многие факторы, поэтому стоит по возможности исключить их.
От состояния артерий зависит функционирование всего организма, а сосуды в нижних конечностях самые крупные, снабжают питательными веществами и кислородом органы малого таза, ноги. Необходимо тщательнее следить за их состоянием и не допускать травм, вести здоровый образ жизни, контролировать свой вес и тогда сосуды будут всегда здоровы.
источник
Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день.
Псевдоаневризма или ложная аневризма — это патологическое образование, возникающее в результате нарушения целостности стенки крупной артерии и продолжающегося кровотечения. Излившаяся кровь скапливается в тканях вокруг артерии образуя опухолевидное образование.
Возникновение настоящей (истинной) аневризмы вообще не связано с кровотечением и представляет собой «мешковидное» расширение артерии.
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Приставка «псевдо» объясняется тем, что без дополнительного обследования отличить настоящую аневризму от псевдоаневризмы на первый взгляд не так просто, особенно не зная истории болезни.
На представленной иллюстрации аневризма отмечена цифрой (1), а псевдоаневризма (2)
Основная причина — это нарушение целостности артерии, возникающее при различных проникающих травмах. Но в кардиологической практике псевдоаневризма встречается как осложнение коронарографии, проводимой через бедренную артерию, как следствие не адекватного гемостаза (остановки крови).
Далее мы будем говорить только о псевдоаневризме бедренной артерии.
Это осложнение встречается относительно часто, около 5% и хотя оно во многом зависит от опыта врача, но предупредить его полностью не в состоянии даже самый лучший специалист. Кроме того, часть вины за возникновение псевдоаневризмы возлагается на пациента, который не выполняет указаний врача, встает с постели раньше времени, сгибает ногу, через которую была выполнена процедура, и делает прочие вещи, которые делать не стоит.
После того как врач заканчивает коронарографию, из артерии извлекается проводник оставляющий достаточно широкое отверстие. Чтобы избежать кровотечения из места прокола, сразу выполняется давление на артерию: сначала вручную, а затем при помощи давящей повязки. Иногда используют специальное закрывающее устройство, работающее по типу пробки. Но если отверстие не было закрыто полностью, то кровь под давлением начинает распространяться и раздвигать мышечную ткань, образуя пульсирующее опухолевидное образование.
Основной симптом псевдоаневризмы это боль. Однако давящая повязка, да и сама рана в области прокола артерии создают неприятные и иногда болезненные ощущения, больные даже при нормальном течении послеоперационного процесса могут похрамывать еще день из-за боли в паху. Поэтому боль как основной симптом псевдоаневризмы обычно малополезен хотя и позволяет заподозрить что речь идет об аневризме.
Другой симптом в виде внезапного похолодания конечности и исчезновения пульсации артерий бедра, голени или ступни является признаком того, что случилась катастрофа — псевдоаневризма достигла значительных размеров и сдавила артерию. В этих случаях необходимо срочное хирургическое вмешательство для спасения не только ноги, но и жизни больного.
Обычно хирурги вскрывают псевдоаневризму и затем при помощи швов останавливают дальнейшее кровотечение. Обычно эта процедура не сложная и случаи, когда после коронарографии псевдоаневризмой причиняется существенный вред здоровью, крайне редки и даже казуистичны.
Наиболее доступным и точным метод диагностики является УЗИ исследование. Реже возникает необходимость провести томографию, если есть подозрение что имеется более обширное кровотечение. Хотя во многих случаях опытный врач, только применив свои тактильные ощущения и стетоскоп, способен установить диагноз.
Если речь идет о неосложненной псевдоаневризме, то лечение заключается в прекращении кровотока между артерией и полостью псевдоаневризмы. Это сообщение осуществляется через так называемую «шейку» которую можно просто пережать давлением пальцами в течение 10-15 минут. После этого проводят контрольное УЗИ, и если прижатие не помогло, то есть две опции.
Первая – под контролем УЗИ можно сделать несколько инъекций стерильного физиологического раствора в область шейки, тем самым пережав ее.
Второй вариант — ввести в полость тромбин — вещество, которое вызывает тромбоз псевдоаневризмы, таким образом ее распространение становится невозможным.
Четкое выполнение требований врача и медперсонала после вмешательства является критичным моментом в профилактике осложнений. Необходимо лежать 4 часа, не шевелить ногой и ни в коем случае не сгибать ее. В 99% случаев эти меры позволяют избавить пациента от большинства проблем и позволят ему вернуться к обычному образу жизни уже на другой деть после процедуры.
Аневризма сосудов головного мозга – опасное для жизни заболевание, которое протекает настолько скрыто, что чаще всего диагностируется уже при развитии осложнения – разрыве стенки, тем самым не давая шансов на раннее лечение.
Существует миф о том, что аневризмы присущи творческим людям и выдающимся ученым. От них погибли Андрей Миронов, Энштейн, Шарль де Голь. На самом же деле, принадлежность к интеллигенции роли не играет, все дело в провоцирующих заболевание факторах, которыми так богата жизнь публичных людей.
Аневризма головного мозга – это патология сосудов, в основе которой лежит истончение и растяжение стенки артерии, питающей нервную ткань. Под действием давления крови измененный сосуд начинает расширяться, формируя образование, напоминающее раздувшийся баллон.
По своему строению большинство аневризм бывают: мешотчатые и веретенообразные. Мешотчатыми называются такие образования, которые включают только одну стенку сосуда и напоминают по форме ягоду на ножке или надувной шарик.
Веретенообразные аневризмы распространяются сразу на обе сосудистые стенки и похожи на бусины на нитке.
На фото аневризма головного мозга может быть различной формы и размера.
Пока размер аневризмы небольшой, она остается незамеченной, не влияя на самочувствие. Но как только она начинает сдавливать близрасположенные нервные пути или мозговые оболочки, появляются клинические симптомы заболевания. Опасная непредсказуемость аневризмы сосудов головного мозга состоит в том, что из-за особенностей расположения, она редко дает характерные проявления, впервые заявляя о себе клиникой кровоизлияния в ткань мозга при разрыве ее стенки.
Ранняя диагностика и лечение этого заболевания составляют большую медицинскую проблему, так как около 45% больных погибают, не прожив и 1 месяца с момента разрыва аневризмы, а около трети выживших становятся инвалидами.
В зависимости от причины аневризма головного мозга может быть подразделена на врожденную и приобретенную.
При неправильном формировании сосудов головного мозга у эмбриона возникает врожденные аневризмы. Часто им сопутствуют другие наследственные патологии: поликистозная болезнь почек, фибромышечная дисплазия. Врачами наблюдались случаи, когда множественные расширения сосудов головного мозга передавались от родителей к их детям.
В основе приобретенных внутричерепных аневризм лежит изменение строения сосудистой стенки – постепенное истончение и исчезновение мышечного слоя.
Основными причинами этого являются:
- длительная гипертония;
- атеросклероз;
- отрицательное влияние никотина (курение);
- употребление алкоголя.
Разрыв аневризмы головного мозга, в свою очередь, развивается при травме (падении или ударе тупым предметом по голове), скачке артериального давления при стрессе, сильных эмоциях.
Проявления внутричерепной аневризмы можно разделить на 2 группы:
- связанные с давлением расширенного сосуда на окружающие ткани;
- признаки кровоизлияния в мозг.
Симптомы, обусловленные непосредственным сдавливанием нейронов и проводящих путей, зависят от того, в каком отделе головного мозга проходит кровеносный сосуд.
Так, признаками аневризм, расположенных в разных частях внутренней сонной артерии, будут нарушения со стороны органа зрения:
- боль за глазным яблоком;
- двоение в глазах;
- косоглазие;
- опущение верхнего века (птоз);
- выпадение полей зрения.
Если поражаются артерии основания мозга, это может приводить к снижению слуха, неприятному шуму в ушах, нарушению движений мимической мускулатуры.
Симптомы аневризмы головного мозга, расположенной передних мозговых артериях, проявляются нарушениями произвольных движений в конечностях – парезами. Кроме того, при такой локализации на первое место могут выходить нарушения психики – ослабление памяти, акритичность поведения.
Особые проявления имеет разрыв аневризмы мозга. Для него характерно острое начало: на фоне полного здоровья развивается резкая головная боль в месте локализации поврежденного сосуда. Она может быть такой силы, что больной впадает в болевой шок и теряет сознание. Развивается типичная картина кровоизлияния в мозг с развитием рвоты, тонуса мышц затылка, судорогами, утратой произвольных движений в конечностях. Чаще всего разрыв аневризмы происходит при интенсивной физической нагрузке, сильных эмоциях, скачке артериального давления.
Поставить правильный диагноз при аневризме помогают следующие методы, позволяющие определить состояние системы кровообращения головного мозга: ангиография с катетеризацией; КТ ангиография; МРТ ангиография.
Все они основаны на создании снимков (рентгеновских или магнитно-резонансных) сосудов головного мозга с введением в них контраста. Каждый из них применяется исходя из возможностей лечебного учреждения и конкретного случая.
Ангиография с катетеризацией представляет собой рентгенографический метод исследования, при котором в сосуды головного мозга вводится контрастное вещество через катетер, расположенный в бедренной артерии, а затем делается серия снимков с обработкой на компьютере. Он позволяет точно выявить признаки аневризмы сосудов головного мозга даже очень мелких размеров. Однако является инвазивной, болезненной процедурой, не рекомендованной к применению у больных, страдающих тяжелыми заболеваниями почек.
Ангиография с компьютерной томографией позволяет получать трехмерные снимки сосудов головного мозга, сконструированные на основе тонких срезов. С ее помощью можно определить местоположение аневризмы и ее соотношение с соседними анатомическими образованиями. Этот метод проводится в течение нескольких минут и является самым предпочтительным при диагностике в неотложных состояниях. Однако высокая доза контраста делает ограниченным его применение у пациентов с заболеваниями почек. Кроме того, он не позволяет определять аневризмы меньше 3 мм.
Ангиография с поддержкой МРТ отличается от КТ методом производства снимков и требует до 30—60 минут, что не позволяет использовать ее при острых состояниях.
Лечение аневризмы сосудов головного мозга может происходить по 3 направлениям: выжидательная тактика (ежегодное наблюдение); открытая операция с наложением клипсы; эндоскопическая эмболизация полости аневризмы.
При мелких расширениях сосудов, которые были обнаружены случайно при обследовании и не сопровождающихся неврологическими симптомами, специальное лечение аневризмы головного мозга не проводится. В этом случае вполне достаточным является проведение ежегодной ангиографии (любого ее вида) с консультацией невролога.
Показаниями к проведению хирургического лечения являются средние и крупные расширения сосудов головного мозга и аневризмы любых размеров, которые сопровождаются неврологическими проявлениями. Основными методами являются: клипирование и эндоваскулярная эмболизация.
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Клипирование аневризмы головного мозга – сложная операция, производимая со вскрытием полости черепа и наложением на обнаруженную аневризму специальной металлической клипсы. Это прекращает доступ крови и дальнейшее растяжение стенки сосуда. Со временем пережатая аневризма замещается на соединительную ткань с образованием небольшого рубца.
Другая операция при аневризме сосудов головного мозга носит название внутрисосудистой эмболизации и представляет собой введение в аневризматическое расширение специальных спиралей через микрокатетер. Это предохраняет сосудистую стенку от дальнейшего перерастяжения в этом месте. В отличие от клипирования эндоваскулярная эмболизация относится к малоинвазивным методикам, которые не требуют доступа через кости черепа.
Аневризма сосудов головного мозга – серьезное заболевание, к которому нельзя относиться легкомысленно. Помочь избежать опасных для жизни осложнений может только ранняя диагностика и вовремя проведенное лечение.
Видео передачи «Жить здорово» на тему «Аневризма сосудов головного мозга»:
источник
Не стоит допускать легкомысленность в отношении данного заболевания. Ведь отсутствие своевременной диагностики и лечения могут привести к плачевным последствиям.
Аневризмой артерии называется патологическое расширение просвета сосуда на ограниченном участке, которое имеет форму «мешочка» или веретена. Истончённый в этом месте участок теряет, в отличие от остальной части сосуда, способность оказывать сопротивление постоянному току крови.
Это происходит по причине того, что снижаются эластичность и упругость сосудистой стенки. Что же может стать причиной возникновения аневризмы? Выделяют ряд факторов, наиболее часто приводящих к развитию аневризмы: наличие жировых (атеросклеротических) бляшек в сосуде, воспаление в артерии (васкулит), артериальная гипертензия, курение, травмы бедренной артерии, и пр.
В зависимости от расположения поражаются бедренная, подколенная, подвздошная, почечная, лёгочная артерии и др.
Артерии питают не только нижние конечности. Бедренная обеспечивает кровью переднюю стенку живота и половые органы. Закупорка просвета сосуда может привести к постепенному развитию паралича, гангрене конечности или в редких случаях может произойти разрыв аневризмы.
Симптомы заболевания. Первое время аневризма бедренной артерии и подкаленной может никак себя не проявлять, и человек совершенно не догадывается о том, что у него что-то не в порядке. По мере увеличения выпячивания происходит сдавление рядом расположенных сосудов и нервов.
Кроме того, сам изменённый сосуд может являться местом образования тромбов, которые могут перекрывать его просвет и приводить к острому нарушению кровоснабжения. Первым признаком заболевания является острая боль в этом участке, которая со временем стихает. На первый план впоследствии начинают выступать чувство онемения конечности, её похолодание, нарушение чувствительности.
Внешне кожные покровы бледнеют, а в месте выпячивания можно заметить или нащупать пульсацию. При этом ухудшение состояния наблюдается при длительной ходьбе. По мере прогрессирования могут появиться судороги, нарушения чувствительности приобретают стойкий характер и, в отсутствии лечения конечность может парализовать.
В случае остро возникшей закупорки сосуда симптомы развиваются в короткий период от 1 до 10 суток и имеют выраженный характер. Резкая боль и жжение в конечности, которые могут возникнуть на фоне общего благополучия, продолжают постепенно нарастать.
Аневризма почечной артерии
Эти сосуды по-другому ещё называют висцеральными (внутренними) сосудами, так как они отвечают за кровоток во внутренних органах. Аневризмы, образующиеся в этих сосудах, имеют все те же признаки.
Первые симптомы появляются в том случае, когда аневризма достигает больших размеров и начинает сдавливать соседние органы, сосуды и нервы, или осложняется разрывом.
Аневризма почечной артерии при значительных размерах сдавливает мочевыводящие пути и преграждает путь оттоку мочи из почки. Это приводит к тому, что токсины, не выводясь с мочой, застаиваются в почке и поступая в кровь, начинают отравлять организм. Развивается опасное состояние — уремия. Появляются слабость и головные боли, неприятный привкус на языке, а изо рта пахнет ацетоном.
Необходимо как можно раньше обратиться за медицинской помощью. Иначе может развиться уремический шок и наступить смерть.
При разрыве аневризмы возникает выраженный болевой синдром в пояснице, который через время стихает. На первый план начинают выступать признаки потери крови — одышка, слабость, сонливость, тахикардия, бледность кожных покровов, головные боли и головокружение. Это состояние также требует безотлагательной медицинской помощи.
Схема расположения артерии
Аневризма подвздошной артерии также начинает себя проявлять, когда сдавливаются соседние структуры или нарушается кровоток в этом сосуде. При закупорке артерии появляются боли в животе и в пояснице неопределенной локализации. Присоединяются расстройства мочеиспускания.
Расширенная аневризма сдавливает рядом расположенные нервные пучки, идущие к конечностям. Это проявляется прогрессирующим нарушением чувствительности и развитием паралича конечности. Разрыв аневризмы очень опасен, так как сосуд достаточно крупный, и за короткое время теряется большое количество крови.
Резкий болевой синдром может быстро сменится слабостью и головокружением, а также может случиться обморок. Кожные покровы становятся бледными, а частота сердечных сокращений резко увеличивается. Падает артериальное давление. И при отсутствии оказания неотложной помощи смертельный исход неизбежен.
Аневризма лёгочной артерии представляет собой врождённое или приобретённое выпячивание самой артерии или её ветвей. Длительное время может себя никак не проявлять.
Обычно какие-то проявления связаны с основным заболеванием сердца, которое привело к образованию аневризмы. Течение данного заболевания неблагоприятное, так как имеется высокий риск разрыва сосуда.
Наступает быстрое ухудшение состояния с потерей сознания. Давление крови в лёгочной артерии достаточно высокое. Поэтому разрыв аневризмы неизбежно приводит к смертельному исходу.
Дуплексное ультразвуковое сканирование сосудов
Диагностика основана на выявлении симптомов заболевания и проведении различных инструментальных исследований. Обнаружение пульсирующего образования возможно в паховой области или подколенной ямке.
Применяются аппаратные методы диагностики. Дуплексное ультразвуковое исследование — наиболее доступное исследование, позволяющее оценить форму и размеры аневризмы.
Также применяются контрастное исследование сосудов и магниторезонансная томография. В диагностике висцеральных артерий наиболее используется контрастное исследование сосудов, компьютерная и магниторезонансная томография.
Применение лекарственных препаратов и народных методов не приводит к излечению. Если аневризма маленьких размеров, её необходимо постоянно наблюдать.
Показаниями к хирургическому лечению являются:
- большие размеры аневризмы,
- выраженная симптоматика с нарушением двигательной чувствительности,
- присоединение инфекции,
- закупорка сосуда,
- разрыв аневризмы.
В ходе операции удаляется расширенный участок сосуда и устраняется дефект стенки путём её ушивания либо постановки протеза сосуда.
источник
Автореферат и диссертация по медицине (14.01.17) на тему: комплексное лечение постпункционных ложных аневризм бедренных артерий
Автореферат диссертации по медицине на тему комплексное лечение постпункционных ложных аневризм бедренных артерий
Панфилов Дмитрий Сергеевич
КОМПЛЕКСНОЕ ЛЕЧЕНИЕ ПОСТПУНКЦИОННЫХ ЛОЖНЫХ АНЕВРИЗМ БЕДРЕННЫХ АРТЕРИЙ
АВТОРЕФЕРАТ на соискание ученой степени кандидата медицинских наук
Работа выполнена в Федеральном бюджетном государственном учреждении «Научно-исследовательский институт кардиологии» Сибирского отделения Российской академии медицинских наук
доктор медицинских наук, профессор, заведующий кафедрой хирургии ФПК и ППС Государственного бюджетного образовательного учреждения высшего профессионального образования «Сибирский государственный медицинский университет» Министерства здравоохранения и социального развития Российской Федерации Кошель Андрей Петрович
доктор медицинских наук, профессор, хирург-эксперт клинико-экспертного отдела Областного государственного автономного учреждения здравоохранения «Томская областная клиническая больница» Поярков Виталий Дмитриевич
Государственное бюджетное образовательное учреждение высшей профессиональной подготовки «Новосибирский государственный медицинский университет» Министерства здравоохранения и социального развития Российской Федерации.
Защита состоится «_» _ 2012 г. в _ часов на
заседании диссертационного совета Д 208.096.01 при ГБОУ ВПО СибГМУ Минздравсоцразвития РФ (634050, г. Томск, Московский тракт, 2).
С диссертацией можно ознакомиться в научно-медицинской библиотеке Сибирского государственного медицинского университета
Автореферат разослан «_»_2012 года.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы исследования
За последнее десятилетие во всем мире количество выполняемых эндоваскулярных процедур выросло более чем в 2 раза (Reeder S.B. et al., 2001; Webber G.W. et al., 2007). Соответственно увеличилось число местных осложнений после пункции сосуда и составляет 2,2-9% случаев (Righini M. et al., 2004; Seidel A. et al., 2006, Sânchez-Enciso M.A., 2012). Наиболее часто встречаются ложные аневризмы бедренных артерий (Kang S. et al.,2000).
Ложные аневризмы опасны разрывом с развитием жизнеугрожающего кровотечения (Гришин И.Н., 1981), а также возникновением тромбозов и тромбоэмболий артерий. Эти риски обусловливают парадигму неотложного лечения псевдоаневризм, а выжидательная тактика наблюдения в надежде на «самостоятельное излечение» признается необоснованной.
На сегодняшний день существует несколько видов лечения ЛАБА.
Оперативное лечение ЛАБА применяется до настоящего времени в 25%-50% случаев и является абсолютным и неотложным методом выбора (Bergentz S.E. et al., 1966; Filis К. et al., 2007). Несмотря на радикальность и высокую эффективность оперативного лечения, местные послеоперационные осложнения встречаются в 21-50% случаях (La Perna L. et al., 2000; Гавриленко A.B. и соавт, 2005). Возможно развитие ИМ в 2,9-20% случаев, что приводит к смерти у 1,1-3,8% больных (Perkins J. Et al., 1996; Yavuz S. et al., 2001).
В 1991 году был предложен компрессионный подход к лечению ЛАБА (Fellmeth B.D. et al., 1991). Различные клиники представили эффективность компрессионного лечения в 50% — 88% случаях (Chatteijee T. et al., 1996; Hood D.B. et al., 1996). По мере накопления клинического опыта, ряд исследователей отметили, что результат компрессионного лечения может зависеть от антикоагуляционного статуса пациента, а также параметров ЛАБА — размеры, глубина расположения в тканях и количество камер ложной аневризмы (Morgan R. et al., 2003). Компрессионное лечение осложняется в 2,4% — 4,3% случаях острым увеличением пульсирующей гематомы, разрывом псевдоаневризмы, вазовагальными реакциями, эмболиями артериального русла, тромбозом глубоких вен (Filis К. et al., 2007).
Существуют и эндоваскулярные способы лечения ложных аневризм: эмболизация спиралями полости и установка стент-графта в проекцию сосудистого дефекта (Onal В. et al., 2005; Shetty R., 2012). Недостатками установки стент-графта являются: дополнительная пункция артерии; дороговизна методики; препятствие повторному использованию этой артерии для будущих катетеризаций; недолговечность стент-графта из-за возможных деформаций (Thalhammer С. et al., 2000).
В последние годы появились единичные сообщения о перспективном направлении — пункционных методах лечения ЛАБА путем инъекции
тромбирующих агентов (тромбина и др.) в полость ложной аневризмы под ультразвуковым и рентгеновским контролем (Ярощук А.С. и соавт., 2001; Vázquez V. et al., 2005; Kim K.-S., 2010).
Эффективность пункционного лечения по опубликованному опыту различных клиник составляет 90-100% (Kang S. et al, 2000; Krueger К. et al., 2005; Gelwix С., 2010; Vlachou P.A., 2011). Были отмечены и осложнения процедуры инъекции тромбина, достигавшие 13% случаев (Dasyam А.К. et al., 2006). Наиболее частое осложнение — эмболия артерии (0,5-2%), возникающая при миграции тромбина из полости ЛАБА в сосудистое русло (Sheiman R. et al., 2003). Гораздо реже описаны такие осложнения, как массивная ТЭЛА с летальным исходом в результате внутривенного введения тромбина (Kurz D. et al., 2003).
Таким образом, в настоящее время в клиническом арсенале имеется несколько способов лечения постпункционных ЛАБА. Однако до сих пор не определены тактические подходы в отношении ведения таких пациентов, нет клинически аргументированных показаний и противопоказаний для отдельных методов лечения ложных аневризм, не разработаны научно обоснованные критерии для применения конкретной методики лечения. Разноречивые литературные данные об эффективности и безопасности каждого из изучаемых методов требуют дополнительного анализа. В доступной отечественной литературе недостаточно данных о наличии подобного клинического опыта.
Обосновать тактику комплексного лечения ложных аневризм бедренных артерий на основании оценки эффективности компрессионного, пункционного и оперативного методов.
1. Разработать и внедрить оригинальную пункционную методику лечения ложных аневризм бедренных артерий.
2. Оценить эффективность компрессионного, оперативного и пункционного методов лечения ложных аневризм бедренных артерий в ближайшем и отдаленном 12-месячном периоде.
3. Провести анализ осложнений после компрессионного, оперативного и пункционного методов лечения ложных аневризм бедренных артерий.
4. Оценить влияние антитромботической терапии на эффективность компрессионного, оперативного и пункционного методов лечения ложных аневризм бедренных артерий.
5. Подготовить и предложить для клинической практики научно обоснованные рекомендации по выбору оптимальной тактики лечения пациентов с постпункционными ложными аневризмами бедренных артерий.
Впервые проанализированы клинические, лабораторные и ультразвуковые факторы риска формирования ложных аневризм бедренных
артерий и предложено научное обоснование прогнозирования эффективности компрессионного, пункционного и оперативного методов лечения.
На основании полученных данных научно обоснован выбор тактики лечения у больных с постпункционными ложными аневризмами бедренных артерий.
Разработана оригинальная пункционная методика для лечения ложных аневризм бедренных артерий, заключающаяся в инъекции тромбина под контролем прямого измерения АД в полости ложной аневризмы, которая является эффективной и безопасной.
Разработаны показания для каждого из исследуемых способов лечения ложных аневризм бедренных артерий (оперативное, компрессионное, пункционное лечение).
На основании полученных данных предложена оптимальная тактика ведения ложных аневризм бедренных артерий, которая заключается в выборе необходимого метода лечения (компрессионного, оперативного, пункционного), в зависимости от клинических и ультразвуковых критериев.
Внедрение результатов исследования в практику
Результаты внедрены в ФГБУ НИИ кардиологии СО РАМН г. Томска, ФЦ ССХ г. Хабаровска, МБЛПУ «ГКБ №29» г. Новокузнецка, ФГБУ ННПЦ МСЭ и реабилитации инвалидов ФМБА России г. Новокузнецка.
Объем и структура диссертации
Диссертация состоит из введения, обзора литературы, четырех глав собственных исследований, заключения, выводов, практических рекомендаций, списка использованной литературы. Диссертация изложена на 181 страницах машинописного текста, содержит 27 таблиц и 73 рисунка. Список литературы включает 16 работ отечественных и 137 зарубежных авторов.
По материалам диссертации опубликовано 2 статьи в журналах, рецензируемых ВАК, 19 тезисов докладов, в том числе 8 в журналах из перечня ВАК, получены патент на полезную модель и патент на изобретение.
Основные положения диссертации изложены:
■ на Всероссийской научно-практической конференции «Стандартизация медицинских технологий, реабилитация в ангиологии и сосудистой хирургии» (Новокузнецк, 2006 г.)
■ на II Съезде кардиологов Сибирского федерального округа (Томск, 2007 г.)
■ на XXIII Международной конференции Российского общества ангиологов и сосудистых хирургов (Новосибирск, 2007 г.)
■ на XIV ежегодной научно-практической конференции с международным участием «Актуальные вопросы кардиологии», с III
международным симпозиумом по эхокардиографии и сосудистому ультразвуку (Тюмень, 2007 г.)
■ на XIII Всероссийского съезда сердечно-сосудистых хирургов (Москва, 2007 г.)
■ на Третьем международном хирургическом конгрессе (Москва, 2008 г.)
■ на Научно-практической конференции, посвященной 50-летнему юбилею ГКБ № 29 г. Новокузнецка (Новокузнецк, 2008 г.)
■ на 19-й международной конференции российского общества ангиологов и сосудистых хирургов (Краснодар, 2008 г.)
■ на XIV Всероссийском съезде сердечно-сосудистых хирургов (Москва, 2008 г.)
■ на XV Всероссийском съезде сердечно-сосудистых хирургов (Москва, 2009 г.)
■ на Международной конференции «Современная кардиология: эра инноваций» (Томск, 2010 г.)
» на XVI Всероссийском съезде сердечно-сосудистых хирургов (Москва, 2010 г.)
■ IV съезде кардиологов Сибирского федерального округа (Кемерово,
■ на XVII Всероссийском съезде сердечно-сосудистых хирургов (Москва, 2011 г.)
Положения, выносимые на защиту
1. Эффективность компрессионного и пункционного методов лечения зависит от ультразвуковых параметров ложных аневризм бедренных артерий: длины, диаметра шейки ложной аневризмы и локализации места пункции.
2. При наличии следующих ультразвуковых признаков: локализация сосудистого дефекта в общей бедренной артерии диаметром до 2 мм и объеме ложной аневризмы бедренной артерии до 30 см3 эффективность компрессионного лечения максимальна. В других случаях данное лечение не показано.
3. Показаниями для пункционного лечения является наличие ультразвуковых критериев: локализация сосудистого дефекта в общей, поверхностной, глубокой бедренных артериях диаметром более 2 мм, объеме ложной аневризмы бедренной артерии более 30 см3.
4. Оперативное лечение показано в тех случаях, когда неэффективны компрессионный и пункционный методы, а также при острых клинических состояниях: пульсирующая гематома с явлениями продолжающегося кровотечения, отсутствие других источников кровотечения, гиповолемия со снижением артериального давления, клиника сдавления сосудов и нервов.
5. Эффективность компрессионного лечения составляет 40,7%, пункционного лечения — 93,7%, оперативного лечения — 100% при количестве осложнений 7,7%, 6,3% и 22,6% соответственно.
В основу работы положены исследования 91 пациента с постпункционными ЛАБА. Все пациенты находились на стационарном лечении в клинических отделениях ФГБУ НИИ кардиологии СО РАМН г.Томска в период с 2006 по 2011 гг. Возраст обсуждаемых пациентов составил 59±10,3 лет.
Большинство обсуждаемых в работе пациентов находились в стационаре с коронарной 62(68,1%) и клапанной 17(18,7%) патологией в качестве основной. В структуре основных заболеваний были отмечены следующие нозологии. Гипертоническая болезнь встречалась у 5(5,5%) человек. Сложные нарушения ритма сердца (WPW-синдром, желудочковая экстрасистолия) были зафиксированы в 3(3,3%) случаях. В единичных случаях фигурировал диагноз: миксома левого предсердия — 1(1,1%), дилатационная кардиомиопатия — 1(1,1%), хроническое расслоение аорты III типа (классификация De Bakey) — 1(1,1%), миокардит — 1(1,1%).
Всем пациентам, включенным в исследование, согласно протоколу ведения больных после эндоваскулярных манипуляций, принятому в ФГБУ НИИ кардиологии СО РАМН, выполняли лечебно-профилактические мероприятия с целью остановки кровотечения из места пункции и профилактики ЛАБА с УЗИ контролем. Всем 91 больным с выявленными постпункционными ЛАБА специальное лечение начинали с компрессионного метода (I этап лечения). В зависимости от результатов компрессионной терапии определяли дальнейшую тактику лечения. Наличие тромбоза ложной аневризмы у пациентов после компрессионного лечения считали положительным результатом. Отсутствие тромбоза ЛАБА расценивали как отрицательный результат.
Рис. 1. План лечения пациентов с ложными аневризмами бедренных артерий
Пациенты с отрицательным результатом были разделены на 2 группы (II этап лечения). Первая группа пациентов (п=22) была подвергнута плановому оперативному лечению. Второй группе пациентов (п=32) было проведено пункционное лечение ЛАБА. Результаты пункционного лечения оценивали с позиции функционирования полости ложной аневризмы. Отсутствие кровотока в полости аневризмы соответствовало положительному результату. Сохранение функционирующей полости считали показанием для планового оперативного лечения. План лечения представлен в виде схемы (рис. 1).
Данное исследование было одобрено этическим комитетом ФГБУ НИИ кардиологии СО РАМН (протокол заседания этического комитета № 44 от 24 мая 2009 г.). Все пациенты, включенные в исследование, обязательном порядке подписали информированное согласие.
Диагностика ЛАБА, прежде всего, основывалась на клинико-анамнестических данных. Верификация клинического диагноза осуществлялась с помощью УЗИ в B-режиме с применением допплеровского сканирования и цветового картирования. Все исследования были выполнены по разработанному в клинике протоколу на ультразвуковых аппаратах «Esaote MyLab 30» (Италия), «Acusón Sequoia 512» (Германия) с использованием линейных датчиков с рабочей частотой 5-8 MHz.
Компрессионное лечение. Для компрессии постпункционных ЛАБА в клинике применяли систему бедренного сжатия «FemoStop» (Radi Medical Systems, Швеция). Компрессионное лечение выполняли по методике, согласно рекомендациям производителя по использованию системы «FemoStop».
Виды оперативного лечения: резекция ЛАБА с ушиванием дефекта БА, резекция ЛАБА с пластикой сосудистого дефекта синтетической заплатой, резекция ЛАБА с протезированием БА.
Пункционное лечение с использованием раствора тромбина выполняли лиофилизатом человеческого тромбина в концентрации 500 ME в 1 мл, восстановленным 2 мл кальция хлорида в концентрации 40 ммоль/л на водяной бане при температуре 37 по Цельсию. Под контролем ультразвука в реальном времени пунктировали полость ЛАБА. Затем вводили раствор тромбина со скоростью 0,3 мл/сек до полного прекращения кровотока в полости.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ОБСУЖДЕНИЕ
Компрессионное лечение постпункционных ЛАБА. Данную группу составил 91 пациент, которым проводилось компрессионное лечение. Мужчин было 38 (41,8%), женщин — 53 (58,2%). Средний возраст пациентов составил 59±10,3 лет.
Характеристика клинических признаков у пациентов с ЛАБА до и после компрессионного лечения (п=91)
Клинический признак Количество пациентов
До компрессии После компрессии
Пульсирующее образование в месте пункции Да 48(52,7%) 37(40,7%)
Болезненность в месте пункции Да Слабая 39(42,9%) 48(52,7%)
Потребность в анальгетиках Да Ненаркотические 15(16,5%) 3(3,3%)**
Наличие подкожной гематомы Да До 50 см2 28(30,8%) 21(23,1%)
* — статистически достоверные отличия в частоте встречаемости (р Панфилов, Дмитрий Сергеевич :: 2012 :: Томск
СПИСОК ПРИНЯТЫХ В ДИССЕРТАЦИИ СОКРАЩЕНИЙ.
Глава I. МЕТОДЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ЛОЖНЫХ АНЕВРИЗМ. СОВРЕМЕННОЕ СОСТОЯНИЕ ПРОБЛЕМЫ (ОБЗОР ЛИТЕРАТУРЫ).
1.1. Проблема ложных аневризм.
1.2. Диагностика ложных аневризм.
1.3. Методы лечения ложных аневризм.
Глава И. МАТЕРИАЛЫ И МЕТОДЫ.
2.1. Общая характеристика клинического материала.
2.2. План лечения пациентов с ЛАБА.
2.3. Методы обследования пациентов.
2.3.1. Клиническое обследование пациентов с ЛАБА.
2.3.2. Лабораторное обследование пациентов с ЛАБА.
2.3.3. Инструментальное обследование пациентов с ЛАБА.
2.3.4. Морфогистологическое исследование капсулы ЛАБА.
2.4. Методы лечения постпункционных ЛАБА.
2.4.1. Компрессионное лечение.
2.4.2.1. Резекция ложной аневризмы с ушиванием дефекта бедренной артерии.
2.4.2.2. Резекция ложной аневризмы с пластикой сосудистого дефекта синтетической заплатой.
2.4.2.3. Резекция ложной аневризмы с протезированием артерии.
2.4.3. Пункционное лечение с использованием раствора тромбина.
2.5. Методы статистической обработки результатов.
ГЛАВА III. КОМПРЕССИОННОЕ ЛЕЧЕНИЕ ПОСТПУНКЦИОННЫХ ЛОЖНЫХ АНЕВРИЗМ БЕДРЕННЫХ АРТЕРИЙ.
3.1. Клиническая характеристика пациентов с компрессионным лечением ЛАБА.
3.2. Ультразвуковая характеристика ЛАБА у пациентов с компрессионным лечением.
3.3. Анализ клинических данных у пациентов с ЛАБА в группе компрессионного лечения.
3.4. Анализ ультразвуковых параметров ЛАБА у пациентов в группе компрессионного лечения.
3.5. Результаты компрессионного лечения ЛАБА.
3.6. Анализ осложнений компрессионного лечения ЛАБА.
ГЛАВА IV. ОПЕРАТИВНОЕ ЛЕЧЕНИЕ ПОСТПУНКЦИОННЫХ ЛОЖНЫХ АНЕВРИЗМ БЕДРЕННЫХ АРТЕРИЙ (I группа).
4.1. Клиническая характеристика пациентов с оперативным лечением ЛАБА.
4.2. Лабораторная характеристика пациентов с оперативным лечением ЛАБА.
4.3. Ультразвуковая характеристика ЛАБА у пациентов в группе оперативного лечения.
4.4. Виды оперативных вмешательств.
4.4.1. Морфологическая характеристика капсулы ЛАБА.
4.5. Результаты оперативного лечения ЛАБА.
4.6. Анализ интраоперационных осложнений.
4.6.1. интраоперационная кровопотеря у пациентов с ЛАБА.
4.7. Анализ послеоперационных осложнений.
ГЛАВА V. ПУНКЦИОННОЕ ТРОМБ ИРОВАНИЕ ПОСТПУНКЦИОННЫХ ЛОЖНЫХ АНЕВРИЗМ БЕДРЕННЫХ АРТЕРИЙ (II группа).
5.1. Клиническая и ультразвуковая характеристика пациентов.в группе пункционного лечения ЛАБА.
5.2. Анализ лабораторных данных у пациентов в группе пункционного лечения ЛАБА.
5.3. Анализ ультразвуковых параметров ЛАБА у пациентов в группе пункционного лечения.
5.4. Результаты пункционного лечения ЛАБА.
5.5. Анализ осложнений пункционного лечения ЛАБА.
Актуальность темы. В последнее десятилетие во всем мире количество выполняемых эндоваскулярных процедур выросло более чем в 2 раза. Так, в США ежегодно выполняется более 1 миллиона эндоваскулярных исследований сердечно-сосудистой системы [28, 68, 103].
Соответственно увеличилось абсолютное число осложнений после пункции сосуда, которые встречаются, в среднем, в 0,2% — 0,61% случаев [3, 37, 43]. По данным V. Erentug et al. и Е. Sueyoshi et al., в структуре всех ятрогенных осложнений эндоваскулярных процедур, ложные аневризмы занимают 60% — 80% [123, 150]. По данным ряда авторов псевдоаневризмы осложняют диагностические и лечебные эндоваскулярные манипуляции в 0,05%-9% случаев [24, 50, 59, 66, 68, 86, 105, 110]. Наиболее частая локализация постпункционных ложных аневризм бедренных артерий объясняется тем, что данный сосуд является традиционно доступным портом для катетеризации артериального русла [40,46].
Ложные аневризмы опасны разрывом с развитием жизнеугрожающего кровотечения [3, 4, 22, 143], а также возникновением тромбозов и тромбоэмболий артерий. Длительно существующие гематомы склонны к инфицированию [88]. Эти риски обусловливают парадигму неотложного лечения псевдоаневризм, а выжидательная тактика наблюдения в надежде на «самостоятельное излечение» признается необоснованной.
Кроме того, как осложнение, ложные аневризмы требуют дополнительных экономических затрат на лечение, увеличивают сроки пребывания пациента в стационаре и ухудшают прогноз основного заболевания [68,141].
На сегодняшний день существует несколько видов лечения ложных аневризм бедренных артерий.
Оперативное лечение ложных аневризм применяется до настоящего времени в 25%-50% случаев и является абсолютным и неотложным методом выбора [23, 31, 71, 129]. Операция необходима в случаях продолжающегося кровотечения — прогрессивного увеличения объемов пульсирующей гематомы, разрыве псевдоаневризмы, наличие ишемических явлений в конечности. Показаниями к хирургическому вмешательству являются безуспешность консервативных методов лечения, а также наличие инфицированных ложных аневризм, некротические изменения кожи и подкожной клетчатки вследствие компрессионного лечения [3, 20, 53, 68, 75, 105].
Восстановление целостности стенки сосуда возможно как путем наложения простого сосудистого шва, так и используя различные методы пластики и протезирования сосуда [3, 20, 26, 54, 71, 122].
Несмотря на радикальность и высокую эффективность оперативного лечения, местные послеоперационные осложнения встречаются в 21-50% случаях [3, 28, 71, 143]. К ним относят длительное заживление мягких тканей (3,9-19%) [91], кровотечение, инфицирование и абсцедирование гематом (20,3%) [53, 79]. Кроме того, в послеоперационном периоде возможно развитие невралгии и гиперестезии (32%) и лимфореи (40%) [28, 91, 143].
Оперативное лечение ЛАБА сопровождается риском таких состояний, как наркоз-индуцированные осложнения (3%) [82, 99], тромбоэмболия легочной артерии (0,99%) [46, 63], периоперационный ИМ (2,9-20%) [28, 99], а также смертностью (1,1-3,8%) [28, 37, 53, 99, 100, 143].
В 1991 году B.D. Fellmeth et al. предложили новый подход к лечению ятрогенных ложных аневризм. Он заключается в компрессии полости ложной аневризмы ультразвуковым датчиком [88]. В последствие, было предложено заменить датчик на механические приспособления [20, 31, 98, 119, 136]. Различные клиники представили эффективность компрессионного лечения в 50% — 88% случаях [8, 37, 46, 50, 73, 80, 98, 103].
По мере накопления клинического опыта, ряд исследователей отметили, что результат компрессионного лечения может зависеть от антикоагуляционного статуса больного [75, 91, 99]. Кроме этого, на положительный результат оказывает влияние телосложение пациента, а также параметры ложной аневризмы — размеры, глубина расположения в тканях и количество камер ложной аневризмы [28]. Успешный результат компрессионного лечения прямо пропорционален малой длине и небольшому диаметру шейки ложной аневризмы, раннему «возрасту» псевдоаневризмы, меньшему количеству камер [75, 99].
Компрессионное лечение осложняется в 2,4% — 4,3% случаях острым увеличением пульсирующей гематомы, разрывом псевдоаневризмы, вазовагальными реакциями, эмболиями артериального русла, тромбозом глубоких вен [71, 75, 116].
Существуют и эндоваскулярные способы лечения псевдоаневризм: эмболизация полости ЛАБА спиралями и установка стент-графта в проекцию сосудистого дефекта [30, 42, 43]. Для эндоваскулярного лечения требуется дополнительная пункция артерии с рисками формирования новой псевдоаневризмы и сложностями катетерных манипуляций в зоне имеющейся ложной аневризмы. Эмболизация спиралями полости не исключает их миграции в сосудистое русло с последующими тромботическими осложнениями. Недостатками установки стент-графта являются: дороговизна методики; препятствие повторному использованию этой артерии для будущих катетеризаций; недолговечность стент-графта из-за возможных деформаций [68, 75, 89].
В последние годы в литературе появились единичные сообщения о пункционных методах лечения ятрогенных ложных аневризм. К ним относят инъекцию тромбирующих агентов (бычьего и человеческого тромбина и др.) в полость ложной аневризмы под ультразвуковым и рентгеновским контролем [16, 39, 59, 68, 73, 82, 111,].
Являясь инородной для человека субстанцией, бычий тромбин способен индуцировать выработку антител в и ^М) с развитием аллергических реакций [24, 80, 142]. При применении бычьего тромбина могут развиваться кровотечения как результат перекрестной реакции бычьего и человеческого факторов свертываемости V [50, 59, 74, 80, 86, 103, 113].
Препараты человеческого тромбина получают из крови доноров или данного пациента, что исключает наличие нежелательных реакций, связанных с использованием бычьего тромбина [59].
Существует несколько методик инъекции тромбина в полость ложной аневризмы: трансартериальное введение при помощи катетера, чрескожное введение с временной окклюзией «питающей» артерии баллоном и чрескожное введение без временной окклюзии сосуда [47, 50, 75].
Эффективность пункционного лечения по опубликованному опыту различных клиник составляет 90-100% [8, 46, 59, 79, 80, 91, 145] и не зависит от антикоагуляционного статуса пациента [55, 113]. Были отмечены и осложнения процедуры инъекции тромбина, достигавшие 13% случаев [28, 32, 66, 75, 80, 99, 107, 117, 129, 135]. Наиболее частое осложнение — эмболия артерии (0,5-2%), возникающая при миграции тромбина из полости ложной аневризмы в сосудистое русло [59, 66, 91, 96, 141]. Гораздо реже описаны такие осложнения, как массивная ТЭЛА с летальным исходом в результате внутривенного введения тромбина [59, 66]. Имеются единичные данные о развитии ДВС [74].
Важно отметить, что, несмотря на незначительный зарубежный опыт пункционного лечения ложных аневризм, представленный отдельными клиниками (от 15 до 240 случаев), метод считается самым перспективным способом лечения ложных аневризм [75, 28]. В отечественной литературе было найдено одно сообщение, в котором описывается лечение ЛАБА с помощью чрескожного введения тромбина [16].
Таким образом, в настоящее время в клиническом арсенале имеется три основных способа лечения постпункционных ЛАБА. Однако до сих пор не определены тактические подходы в отношении ведения таких пациентов, нет клинически аргументированных показаний для отдельных методов лечения псевдоаневризм, не разработаны научно обоснованные критерии для применения оперативной, компрессионной, пункционной методик лечения. Разноречивые литературные данные об эффективности и безопасности каждого из изучаемых методов требуют дополнительного анализа.
Значительный рост эндоваскулярных процедур и, как следствие, увеличение абсолютного количества ятрогенных осложнений делают актуальной любую проблему, решение которой позволило бы оптимизировать лечение этих осложнений и улучшить ближайшие и отдаленные результаты.
В доступной отечественной литературе недостаточно данных о наличии подобного клинического опыта.
Обосновать тактику комплексного лечения ложных аневризм бедренных артерий на основании оценки эффективности компрессионного, пункционного и оперативного методов.
1. Разработать и внедрить оригинальную пункционную методику лечения ложных аневризм бедренных артерий.
2. Оценить эффективность компрессионного, оперативного и пункционного методов лечения ложных аневризм бедренных артерий в ближайшем и отдаленном 12-месячном периоде.
3. Провести анализ осложнений после компрессионного, оперативного и пункционного методов лечения ложных аневризм бедренных артерий.
4. Оценить влияние антитромботической терапии на эффективность компрессионного, оперативного и пункционного методов лечения ложных аневризм бедренных артерий.
5. Подготовить и предложить для клинической практики научно обоснованные рекомендации по выбору оптимальной тактики лечения пациентов с постпункционными ложными аневризмами бедренных артерий.
Впервые проанализированы клинические, лабораторные и ультразвуковые факторы риска формирования ложных аневризм бедренных артерий и предложено научное обоснование прогнозирования эффективности компрессионного, пункционного и оперативного методов лечения.
На основании полученных данных научно обоснован выбор тактики лечения у больных с постпункционными ложными аневризмами бедренных артерий.
Разработана оригинальная пункционная методика для лечения ложных аневризм бедренных артерий, заключающаяся в инъекции тромбина под контролем прямого измерения артериального давления в полости ложной аневризмы.
Разработаны показания для каждого из исследуемых способов лечения ложных аневризм бедренных артерий (оперативное, компрессионное, пункционное лечение).
На основании полученных данных предложена оптимальная тактика ведения ложных аневризм бедренных артерий, которая заключается в выборе необходимого метода лечения (компрессионного, оперативного, пункционного), в зависимости от клинических и ультразвуковых критериев.
Внедрение результатов исследования в практику
Результаты внедрены в ФГБУ НИИ кардиологии СО РАМН г. Томска, ФЦ ССХ г. Хабаровска, МБЛПУ «ГКБ №29» г. Новокузнецка, ФГБУ ННГТЦ МСЭ и реабилитации инвалидов ФМБА России г. Новокузнецка.
Объем и структура диссертации
Диссертация состоит из введения, обзора литературы, материалов и методов, трех глав собственных исследований, заключения, выводов, практических рекомендаций, списка литературы. Диссертация изложена на 181 странице машинописного текста, содержит 27 таблиц и 73 рисунка.
Заключение диссертационного исследования на тему «комплексное лечение постпункционных ложных аневризм бедренных артерий»
1. Разработанная оригинальная методика пункционного лечения, заключающаяся в инъекции тромбина под контролем прямого измерения артериального давления в полости ложной аневризмы бедренной артерии, является эффективной и безопасной.
2. Эффективность компрессионного лечения у пациентов с ложными аневризмами бедренных артерий достоверно ниже (40,7%), чем эффективность пункционного (93,7%) и оперативного способа методов (100%) (р по медицине, диссертация 2012 года, Панфилов, Дмитрий Сергеевич
1. Боровиков В.П. Statistica. Статистический анализ и обработка данных в среде Windows / В.П. Боровиков, И.П. Боровиков М. : Филин, 1997. -608 с.
2. Бураковский В.И. Сердечно-сосудистая хирургия : рук. /
3. B.И. Бураковский, Л.А. Бокерия. М. : Медицина, 1989. — С. 688-689.
4. Гавриленко A.B. Лечение ложных ятрогенных артериальных аневризм / A.B. Гавриленко, Г.В. Синявин // Ангиология и сосудистая хирургия.-2005.-Т. 11, № 3. С. 135-138.
5. Гришин И.Н. Клиническая ангиология и ангиохирургия. Ч. 2 / И.Н.Гришин, А.Н. Савченко. Минск : Вышэйшая школа, 1981.1. C. 164-170.
6. Дрюк A.A. Хирургия аорты и магистральных артерий / A.A. Дрюк, Н.Ф. Шалимов. Киев : Здоров’я, 1979. — С. 359-378.
7. Лучевое лечение лимфореи в паховой области после артериальной реконструкции / A.A. Фокин и др. // Ангиология и сосудистая хирургия. -2001.-Т. 7, № 1. С. 91-94.
8. Национальные рекомендации по ведению взрослых пациентов с аневризмами брюшной аорты. -М., 2010.
9. Панфилова Н.О. Ультразвуковая диагностика постинъекционных сосудистых осложнений у наркозависимых больных : дис. . канд. мед. наук / Н.О. Панфилова. Томск, 2005. — С. 8-23.
10. Покровский A.B. Клиническая ангиология / A.B. Покровский. М. : Медицина, 1979.-С. 194-209.
11. Случай хирургического лечения посттравматической ложной артериовенозной аневризмы сосудов правой почки / A.M. Чернявский и др. // Ангиология и сосудистая хирургия. 2004. — Т. 10, № 3. — С. 118-122.
12. Султаналиев Т.А. Этиология и патогенез повреждения кровеносных сосудов у наркоманов / Т.А. Султаналиев, С.Е. Турсынбаев, В.М. Ивакин // Ангиология и сосудистая хирургия. 2007. — Т. 13.2. — С. 25-33.
13. Физиология человека. Т. I / под ред. В.М. Покровского, Г.Ф. Коротько. -М. : Медицина, 1997. С. 313-325.
14. Хирургическая тактика при травматических повреждениях артерий голени / Д.Д. Султанов и др. // Ангиология и сосудистая хирургия. 2003. -Т. 9, №2.-С. 111-117.
15. Экстренная хирургия сердца и сосудов / под ред. М.Е. Де Бейки, Б.В. Петровского. М. : Медицина, 1980. — С. 75-120.
16. Abu-Yosef М.М. The «To-and-fro» sign: duplex Doppler evidence of femoral artery pseudoaneurysm / M.M. Abu-Yosef, J.A. Wiese, A.R. Shamma // AJR. 1988. -№ 150. — P. 632-634.
17. Altin R.S. Pseudoaneurysm and arteriovenous fistula after femoral artery catheterization: association with low femoral punctures / R.S. Altin, S. Flicker, H.J. Naidech // AJR. 1988. — № 152. — P. 629-631.
18. An aneurysm at the cannulation site discovered 40 years after cardiac surgery: report of a case / T. Nakayama et al. // Ann. Thorac. Cardiovasc. Surg. -2008. Vol. 14. — P. 267-269.
19. A review of alternative approaches in the management of iatrogenic femoral pseudoaneurysms / G. O’Sullivan et al. // Ann. R. Coll. Surg. Engl.1999.-Vol. 81.-P. 226-234.
20. Arterial False Aneurysms and their Modern Management / G. Szendro et al. // IMAJ. 2001. — Vol. 3. — P. 5-8.
21. Balloon catheterization for hemostasis during the operation of ruptured femoral artery pseudoaneurysm / S. De-bing et al. // Chinese Medical Journal. -2007.-Vol. 120, №21. -P. 1943-1944.
22. Bergentz S.E. Surgical management of complications to arterial puntrure / S.E. Bergentz, L.O. Hansson, B. Norback // Annals of surgery. 1966. -Vol. 164, № 6. — P. 1021-1026.
23. Brophy D. Iatogenic femoral pseudoaneurysms: thrombin injection after failed US-guided compression Radilogy / D. Brophy, R. Sheiman, P. Amatulle.2000. Vol. 214. — P. 278-282.
24. Carotid artery pseudoaneurysm in Behcet’s disease / A. Ozyazicioglu et al. // European Journal of Cardiothoracic Surgery. 2001. — Vol. 19. -P. 938-939.
25. Chiu K.-M. Huge Femoral Artery Pseudoaneurysm / K.-M. Chiu, T.-Y. Lin, S.-H. Chu // Circulation. 2008. — Vol. 117. — P. 1100.
26. Color Doppler Sonography of Groin Complications Following Femoral Artery Catheterization / E.K. Paulson et al. // AJR. 1995. — Vol. 165. -P. 439—444.
27. Contemporary Management of Postcatheterization Pseudoaneurysms / G.W. Webber et al. // Circulation. 2007. — Vol. 115. — P. 2666-2674.
28. Cope C. Coagulations of aneurysms by direct percutaneous thrombin injection / C. Cope, R. Zeit // AJR. 1986. — Vol. 143. — P. 383-387.
29. Current guidelines produce competent endovascular surgeons / F.A. Weaver et al. // J. Vase. Surg. 2006. — Vol. 43, № 5. — P. 992-998.
30. Currie P. Pseudoaneurysm of the femoral artery after cardiac catheterisation: diagnosis and treatment by manual compression guided by Doppler colour flow imaging / P. Currie, C. Turnbull // Br. Heart Jf. 1994. — Vol. 72. -P. 80-84.
31. Dasyam A.K. Development of Nonobstructive Intraarterial Thrombi After Injection of Thrombin into Pseudoaneurysms / A.K. Dasyam, W.D. Middleton, S.A. Teefey // A JR. 2006. — Vol. 186. — P. 401^105.
32. Delayed Posttraumatic Pseudoaneurysm of the Anterior Tibia! Artery Mimicking a Malignant Tumor / A. Ladermann et al. // Orthopedics. 2008. -Vol. 31.-P. 500.
33. Demey K. False aneurysm of the superficial femoral artery following minimally invasive plate osteosynthesis of a femoral shaft fracture / K. Demey, L. Haeck, W. Sioen // Acta Orthop. Belg. 2008. — Vol. 74, № 5. — P. 700-703.
34. Digman K.E. Ultrasound Case of the Day / K.E. Digman, M.A. Pozniak // RadioGraphics. 1993. — Vol. 13. — P. 962-964.
35. Dorfrnan G.S. Poscatheterization femoral artery injuries: is there a role for nonsurgical treatment? / G.S. Dorfman, J.J. Cronana // Radiology. 1991. -№ 178.-P. 629-630.
36. Duplex-guided compression of femoral artery false aneurysms reduces the need for surgery / J. Perkins et al. // Ann. R. Coll. Surg. Engl. 1996. -Vol. 78.-P. 473-475.
37. Efficacy and Safety of Percutaneous Treatment of Iatrogenic Femoral Artery Pseudoaneurysm by Biodegradable Collagen Injection / K. Hamraoui et al. // JACC. 2002. — Vol. 39, № 8. — P. 1297-1304.
38. Elford J. Ultrasound guided percutaneous thrombin injection for the treatment of iatrogenic pseudoaneurysms / J. Elford, C. Burrell, C. Roobottom // Heart. 1999. — Vol. 82. — P. 526-527.
39. Endovascular coil embolization for acute management of traumatic pulmonary artery pseudoaneurysm / M. Block et al. // J. Thorac. Cardiovasc. Surg. 2004. — Vol. 128. — P. 784-785.
40. Endovascular Treatment of Carotid and Vertebral Pseudoaneurysms with Covered Stents / A.C. Yi et al. // Am J. Neuroradiol. 2008. — Vol. 29. — P. 983-987.
41. Endovascular treatment of peripheral vascular lesions with stent-grafts / B. Onal et al. // Diagn. Intervent. Radiol. 2005. — Vol. 11. — P. 170-174.
42. Ernst J.M. Percutaneous closure of a false aneurysm of the superficial femoral artery under fluoroscopic guidance / J.M. Ernst, B.J. Rensing // Heart. -2003.-Vol. 89.-P. 326.
43. Etemad-Rezai R. Ultrasound-guided thrombin injection of femoral artery pseudoaneurysms / R. Etemad-Rezai, D.J. Peck // Can. Assoc. Radiol. J. 2003. -Vol. 54, №2.-P. 118-120.
44. Expanded indications for ultrasound-guided thrombin injection of pseudoaneurysms / S. Kang et al. // J. Vase. Surg. 2000. — Vol. 31. — P. 289-98.
45. Farrell M.A. Sonographically Guided Percutaneous Thrombin Injection for Treatment of a Vein Graft Pseudoaneurysm / M.A. Farrell, B.R. Douglas, T.C. Bower//AJR.-2001.-Vol. 176.-P. 1032-1034.
46. Fatal complication after thrombin injection for postcatheterization femoralpseudoaneurysm / R. Gabrielli et al. // Thorac. Cardiovasc. Surg. 2011. -Vol. 59, №6. -P. 372-375.
47. Femoral artery pseudoaneurysms: value of color Doppler sonography in predicting which ones will thrombose without treatment / E.K. Paulson et al. // AJR. 1992.-№ 159.-P. 1077-1081.
48. Femoral Pseudoaneurysms: Management with Percutaneous Thrombin Injections Success Rates and Effects on Systemic Coagulation / K. Kruger et al. // Radiology. — 2003. — Vol. 226. — P. 452-458.
49. Femoral psodoanevrizma tedavisinde US kilavuzlugunda perkutan glue enjeksiyonu / C. Aytekin et al. // Tansal ve Girifiimsel Radyoloji. 2003. -Vol. 9. — P. 257-259.
50. Frush D.P. Successful Sonographically Guided Thrombin Injection in an Infant with a Femoral Artery Pseudoaneurysm / D.P. Frush, E.K. Paulson, M.P. O’Laughlin//AJR. -2000. Vol. 175.-P. 485-487.
51. García E. Femoral pseudoaneurysms postcardiac catheterization surgically treated: evolution and prognosis / E. García, J.-A. González-Fajardo, V. Gutiérrez // Interact. Cardiovasc. Thorac. Surg. 2009. — Vol. 8. — P. 353-357.
52. Giant Right Femoral Pseudoaneurysm Diagnosed 7 Years after Cardiac Catheterization / A. Gurbuz et al. // Texas Heart. Institute Journal. 2008. -Vol. 35, №2.-P. 222-223.
53. Gorge G. Management of complex, two chamber false aneurysm by thrombin injections / G. Gorge, T. Kunz // Heart. 2003. — Vol. 89. — P. 564.
54. Harris M. Medical statistics. Made easy / M. Harris, G. Taylor. -London : Taylor&Francis, 2004. P. 114.
55. Hemoperitoneum secondary to rupture of cystic artery pseudoaneurysm / A. Ghoz et al. // Hepatobiliary Pancreat. Dis. Int. 2007. — Vol. 6. — P. 321-323.
56. Human Thrombin for Treatment of Pseudoaneurysms: Comparison of Bovine and Human Thrombin Sonogram-Guided Injection / V. Vázquez et al. // AJR.-2005.-Vol. 184.-P. 1665-1671.
57. Iatrogenic femoral artery pseudoaneurysms a review of current methods of diagnosis and treatment / F. Ahmad et al. // Clin. Radiol. — 2008. -Vol. 63, № 12.-P. 1310-1316.
58. Iatrogenic femoral pseudoaneurysms a simple solution of inconvenient problem?/A. Lisowska et al. //Adv. Med. Sei.-2011.-Vol. 56, №2. -P. 215221.
59. Iatrogenic Pseudoaneurysms of the Extrahepatic Arterial Vasculature: Management and Outcome / T. Christensen et al. // HPB. 2006. — Vol. 8. -P. 458-464.
60. Iatrogenic pseudoaneurysms of the peripheral arteries / R. Borioni et al. // Chir. Ital. 2008. — Vol. 60, № 1. — P. 103-111.
61. Keeling A.N. Interventional radiology in the diagnosis, management, and follow-up of pseudoaneurysms / A.N. Keeling, F.P. McGrath, M.J. Lee // Cardiovasc. Intervent. Radiol. 2009. — Vol. 32, № 1. — P. 2-18.
62. Kozelj M. Infected femoral pseudoaneurysms from intravenous drug abuse in young adults / M. Kozelj, N. Kobilica, V. Flis // Wien Klin. Wochenschr. -2006.-Vol. 118, №2.-P. 71-75.
63. Kurz D. Delayed Femoral Vein Thrombosis after Ultrasound-guided Thrombin Injection of a Postcatheterization Pseudoaneurysm / D. Kurz, K.-P. Jungius, T. Lescher // J. Vase. Interv. Radiol. 2003. — Vol. 14. -P. 1067-1070.
64. Large Iatrogenic Pseudoaneurysm of the Posterior Tibial Artery Treated with Sonographically Guided Thrombin Injection / R. Corso et al. // A JR. 2003. -Vol. 180.-P. 1479-1480.
65. Lenartova M. Iatrogenic Pseudoaneurysm of Femoral Artery: Case Report and Literature Review / M. Lenartova, T. Tak // Clinical Medicine & Research. 2003. — Vol. 1, № 3. — P. 243-247.
66. Lewandowski P. Femoral pseudoaneurysms ultrasound-guided thrombin injection as a method of treatment / P. Lewandowski, W. Wasek, A. Budaj // Kardiol. Pol. — 2008. — Vol. 66. — P. 775-780.
67. Loose H.W. The management of peripheral arterial aneurysms using percutaneous injection of fibrin adhesive / H.W. Loose, PJ. Haslam // The British Journal of Radiology. 1998.-Vol. 71.-P. 1255-1259.
68. Management of Early and Late Detected Vascular Complications Following Femoral Arterial Puncture for Cardiac Catheterization / K. Filis et al. // Hellenic. J. Cardiol. 2007. — Vol. 48. — P. 134-142.
69. Manifestations of temporary symptoms during endoscopic variceal sclerotherapy using thrombin as a sclerosant / N. Yuki et al. // Jpn. J. Med. -1991.-Vol. 30.-P. 193-201.
70. Matson M. Percutaneous treatment of pseudoaneurysms using fibrin adhesive / M. Matson, R. Morgan, A.-M. Belli // The British Journal of Radiology. 2001. — Vol. 74. — P. 690-694.
71. McNeil N.L. Sonographically Guided Percutaneous Thrombin Injection Versus Sonographically Guided Compression for Femoral Artery Pseudoaneurysms / N.L. McNeil, T.W.I. Clark // A JR. 2001. — Vol. 176. -P. 459-462.
72. Morgan R. Current Treatment Methods for Postcatheterization Pseudoaneurysms / R. Morgan, A.-M. Belli // J. Vase. Interv. Radiol. 2003. -Vol. 14.-P. 697-710.
73. Mycotic Aneurysm of the Popliteal Artery Secondary to Tuberculosis / V.A. Jebara et al. //Tex. Heart. Inst. J. 1998. — Vol. 25. — P. 136-139.
74. Non-invasive ultrasound guided compression repair of post puncture femoralpseudoaneurysm / A. Latic et al. // Med. Arh. 2011. — Vol. 65, №2.-P. 113-114.
75. Non-surgical management of iatrogenic arterial pseudoaneurysms-ultrasound-guided manual compression, an Indian experience / V. Kumar et al. // Indian Heart. J. 2008. — Vol. 60, № 6. — P. 574-577.
76. Obliteration of Femoral Artery Pseudoaneurysm by Thrombin Injection / J.R. Edgerton et al. // Ann. Thorac. Surg. 2002. — Vol. 74. — P. 1413-1415.
77. Occlusion of postcatheterization femoral pseudoaneurysms with percutaneous thrombin injection under ultrasound guidance / R. Corso et al. // Radilogica Medica. -2004. Vol. 108. — P. 385-393.
78. Occlusion of pseudoaneurysms using human or bovine thrombin using contrast-enhanced ultrasound guidance / P.H. Grewe et al. // Am. J. Cardiol. -2004. Vol. 93, № 12. — P. 1540-1542.
79. Percutaneous Thrombin Injection for Closure of Femoral Pseudoaneurysms: Preliminary Experience / M.S. Fernández et al. // Rev. Esp. Cardiol. 2002. — Vol. 55, № 7. — P. 771-774.
80. Percutaneous ultrasound-guided thrombin injection for the treatment of iatrogenic femoral artery pseudoaneurysms / P.A. Vlachou et al. // Eur. J. Radiol.-2011.-Vol. 77, № l.-P. 172-174.
81. Peroneal artery pseudoaneurysm a case report and literature review / U. Sadat et al. // BMC Surgery. — 2007. — Vol. 7, №4.- URL: http://www.biomedcentral.eom/1471-2482/7/4.
82. Personal experiences in direct ultrasound-guided injection of thrombin into the lumen of pseudoaneurysm as a method of treatment in case of iatrogenic femoral artery damage / J. Sloninal et al. // Pol. J. Radiol. 2010. — Vol. 75, №2.-P. 33-37.
83. Pezzullo J. Percutaneous Injection of Thrombin for the Treatment of Pseudoaneurysms After Catheterization: An Alternative to Sonographically Guided Compression / J. Pezzullo, D. Dupuy, J. Cronan // AJR. 2000. — Vol. 175. — P. 1035-1040.
84. Pezzullo J.A. Successful Percutaneous Thrombin Injection of a Brachial Artery Pseudoaneurysm in a Neonate / J.A. Pezzullo, M.T. Wallach // AJR. -2002. Vol. 178. — P. 244-245.
85. Postangiographic femoral artery injuries: nonsurgical repair with US-guided compression / B.D. Fellmeth et al. // Radiology. 1991. — № 178. -P. 671-675.
86. Postcatheterization Pseudoaneuiysms and AV fistulas: repair with Percutaneous implantation or endovascular covered stents / C. Thalhammer et al. // Radiology. 2000. — Vol. 214. — P. 127-131.
87. Postcatheterization pseudoaneurysm in a one-year-old child treated by ultrasound-guided human thrombin injection / Q. Hussain et al. // JBR-BTR. -2009. Vol. 92, № 2. — P. 76-77.
88. Postcatheterization Pseudoaneurysm: Results of US-guided Percutaneous Thrombin Injection in 240 Patients / K. Krueger et al. // Radiology. 2005. -Vol. 236.-P. 1104-1110.
89. Postlaparoscopic iatrogenic pseudoaneuiysms of the arteries of the peritoneal and retroperitoneal space: case report and review of the literature / D.G. Parthenis et al. // Surg. Laparosc. Endosc. Percutan. Tech. 2009. -Vol. 19, №2.-P. 90-97.
90. Prediction of Iatrogenic Pseudoaneurysm after Percutaneous Endovascular Procedures / W. Mlekusch et al. // Radiology. 2006. — Vol. 240. -P. 597-602.
91. Presentation, diagnosis, and management of arterial mycotic pseudoaneuiysms in injection drug users / J.W. Tsao et al. // Ann. Vase. Surg. -2002. Vol. 16, № 5. — P. 652-662.
92. Profunda femoris artery pseudoaneurysm after surgery and trauma / K. Unay et al. // Strat. Traum. Limb. Recon. 2008. — Vol. 3. — P. 127-129.
93. Prolonged Generalized Urticarial Reaction after Percutaneous Thrombin Injection for Treatment of a Femoral Artery Pseudoaneurysm / P.J. Sheldon et al. // JVIR. 2000. — Vol. 11. — P. 759-761.
94. Pseudoaneurysm of anterior tibial artery following tibial nailing: A case report / D. Inamdar et al. // Journal of Orthopaedic Surgery. 2005. — Vol. 13, №2.-P. 186-189.
95. Pseudoaneurysm of femoral arteiy after catheterisation: treatment by a mechanical compression device guided by colour Doppler ultrasound / T. Chatterjee // Heart. 1998. — Vol. 79. — P. 502-504.
96. Pseudoaneurysms and the Role of Minimally Invasive Techniques in Their Management / N. Saad et al. // Radiographics. 2005. — Vol. 25. -P. 173-189.
97. Pseudoaneurysms of the profunda femoris artery / S. Yavuz et al. // Asian cardiovascular & thoracic annals. 2001. — Vol. 9, № 1. — P. 73-75.
98. Rabbani A. Obturator Bypass as an Alternative Technique for Revascularization in Patients with Infected Femoral Pseudoaneurysms / A. Rabbani, M. Moini, M.-R. Rasouli // Arch. Iranian. Med. 2008. — Vol. 11, № l.-P. 50-53.
99. Reddy D.J. Infected aneurysms / D.J. Reddy, C.B. Ernst // Vascular Surgery / R.B. Rutherford (ed.). 5th ed. — Philadelphia : W.B. Saunders, 2000. -P. 1383-97.
100. Reeder S.B. Low-Dose Thrombin Injection to Treat Iatrogenic Femoral Artery Pseudoaneurysms / S.B. Reeder, D.M. Widlus, M. Lazinger // AJR.-2001.-Vol. 177. P. 595-598.
101. Regarding «percutaneous ultrasound guided thrombin injection: a new method for treating postcatheterization femoral pseudoaneurysms» (letter) / A. Lennox et al. // J. Vase. Surg. 1998. — Vol. 28. — P. 1120-1121.
102. Righini M. Treatment of postcatheterization femoral false aneurysms / M. Righini, I. Quere, J.P. Laroche // J. Mai. Vase. 2004. — Vol. 29, № 2. -P. 63-72.
103. Robbs J.V. Nerve Compression Injuries Due to Traumatic False Aneurysm / J.V. Robbs, K.S. Naidoo // Ann. Surg. 1984. — Vol. 200, № 1. -P. 80-82.
104. Sadiq S. Thromboembolism Complicating Thrombin Injection of Femoral Artery Pseudoaneurysm: Management with Intraarterial Thrombolysis / S. Sadiq, W. Ibrahim //J. Vase. Interv. Radiol. -2001. Vol. 12. — P. 633-636.
105. Safety and feasibility of transradial approach for primary percutaneous coronary intervention in elderly patients with acute myocardial infarction / Zhen-xian Yan et al. // Chin. Med. J. 2008. — Vol. 121, № 9. — P. 782-786.
106. Sealing pseudoaneurysms of the femoral artery with saline injection: a new technique / D. Periard et al. // Eurointervention. 2012. — Vol. 7, № 10. -P. 1206-1209.-DOI: 10.4244/EIJV7I10A192.
107. Seidel A. Iatrogenic Pseudoaneurysm of Axillary Artery / A. Seidel,
108. F. Miranda, L. Fregadolli // Arquivos Brasileiros de Cardiologia. 2006. -Vol. 86, № 4. — P. 302-304.
109. Shabani A.G.S. Inferior epigastric artery pseudoaneurysm: ultrasound diagnosis and treatment with percutaneous thrombin / A.G.S. Shabani,
110. G.M. Baxter // The British Journal of Radiology. 2002. — Vol. 75. — P. 689-691.
111. Sheiman R. Iatrogenic Femoral Pseudoaneurysms That Are Unresponsive to Percutaneous Thrombin Injection: Potential Causes / R. Sheiman, M. Mastromatteo// AJR. -2003. -Vol. 181.-P. 1301-1304.
112. Sheiman R.G. Treatment of Iatrogenic Femoral Pseudoaneurysms with Percutaneous Thrombin Injection: Experience in 54 Patients / R.G. Sheiman, D.P. Brophy // Radiology. 2001. — Vol. 219. — P. 123-127.
113. Shetty R. Treatment of an iatrogenic femoral artery pseudoaneurysm with concomitant arteriovenous fistula with percutaneous implantation of anamplatzer vascular plug / R. Shetty, K. Lotun // Catheter Cardiovasc. Interv. -2012. -DOI: 10.1002/ccd.24372.
114. Skibo L. Compression Repair of a Postcatheterization Pseudoaneurysm of the Brachial Artery Under Sonographic Guidance / L. Skibo, J.F. Polak // AJR. 1993. — Vol. 60. — P. 383-384.
115. Sonographically Guided Compression Repair of Pseudoaneurysms: Further Experience from a Single Institution / L. Eisenberg et al. // AJR. 1999. -Vol. 173.-P. 1567-1573.
116. Sonographically Guided Thrombin Injection of Iatrogenic Femoral Pseudoaneurysms: Further Experience of a Single Institution / E. Paulson et al. // AJR.-2001.-Vol. 177.-P. 309-316.
117. Spontaneous Rupture of the Dorsalis Pedis Artery: Report of a Case / S. Hiromatsu et al. // Ann. Thorac. Cardiovasc. Surg. 2007. — Vol. 13, № 4. -P. 290-292.
118. Sridhar K. Peripheral Vascular Complications after Intracoronary Stent Placement: Prevention by Use of a Pneumatic Vascular Compression Device / K. Sridhar // Catheterization and Cardiovascular Diagnosis. 1996. — Vol. 39. -P. 224-229.
119. Successful direct thrombin injection of a femoral artery pseudoaneurysm in an anticoagulated patient with a mechanical mitral valve / C. Gelwix et al. // Int. J. Angiol. 2010. — Vol. 19, № 4. — P. el35-el36.
120. Successful Treatment of an Iatrogenic Giant Femoral Artery Pseudoaneurysm With Percutaneous Thrombin Injection / K.-S. Kim et al. // Korean. Cire. J. 2010. — Vol. 40. — P. 292-294.
121. Surgical approach to giant femoral artery pseudoaneurysm due to gunshot injury / O. Tetik et al. // Anadolu Kardiyol. Derg. 2008. — Vol. 8. -P. 15-21.
122. Surgical Treatment of Peripheral Vascular Injuries After Cardiac Catheterization / V. Erentug et al. // Anadolu Kardiyol. Derg. 2003. — Vol. 3. -P. 216-220.
123. Tase II. Inter-Society Consensus for the Management of Peri feral Arterial Desease / // Euf. J. Vase. Endovasc. Surg. 2007. — Vol. 33 (suppl 1). — P. 61.
124. The management of mycotic femoral pseudoaneurysms in intravenous drug abusers / C. Peirce et al. // Ann. Vase. Surg. 2009. — Vol. 23, № 3. -P. 345-349.
125. The recurrence of iatrogenic femoral artery pseudoaneurysm after occlusion by ultrasound guided percutaneous thrombin injection / J. Madaric et al. // Eurointervention. 2009. — Vol. 5, № 4. — P. 443-447.
126. Thrombin Injection for the repair of brachial artery pseudoaneurysms / R.G. Sheiman et al.//AJR. 1999. — Vol. 173.-P. 1029-1030.
127. Ting A.C.W. Femoral Pseudoaneurysms in Drug Addicts / A.C.W. Ting, S.W.K. Cheng // World J. Surg. 1997. — Vol. 21. — P. 783-787.
128. Tisi P. Surgery versus non-surgical treatment for femoral pseudoaneurysms / P. Tisi, M. Callam // Cochrane Database of Systematic Reviews. 2006. — Issue l.-DOI: 10.1002/14651858.CD004981.pub2.
129. Transcatheter thrombin embolization of a giant visceral artery aneurysm / M. Carmo et al. // J. Cardiovasc. Surg. (Torino). 2008. — Vol. 49, № 6. — P. 777-782.
130. Traumatic Giant Pseudoaneurysm of Innominate Arteiy / R.S. Dhaliwal et al. // Asian Cardiovasc. Thorac. Ann. 2005. — Vol. 13. -P. 369-371.
131. Treatment of an Iatrogenic Femoral Artery Pseudoaneurysm With Percutaneous Duplex-Guided Injection of Thrombin / A. Lennox et al. // Circulation. 1999. — Vol. 100. — P. 39-41.
132. Treatment of arterial pseudoaneurysms with percutaneous ultrasound-guided thrombin injection / M.A. Sanchez-Enciso et al. // Cir. 2012. — Vol. 80, №2.-P. 134-139.
133. Treatment of false aneurysm by using a detachable balloon / R.P. Sharma etal.//AJR. 1987.-№ 149.-P. 1279-1280.
134. Treatment of Iatrogenic Femoral Arterial Pseudoaneurysms: Comparison of US-guided Thrombin Injection with Compression Repair / E.K. Paulson et al. // Radiology. 2000. — Vol. 215. — P. 403^108.
135. Treatment of radial and ulnar artery pseudoaneurysms using percutaneous thrombin injection / E. Komorowska-Timek et al. // Hand Surg. -2004. Vol. 29, № 5. — P. 936-942.
136. Treatment options for postcatheterisation femoral pseudoaneurysm closure / A. Kabiak-Ziembicka et al. // Kardiol. Pol. 2005. — Vol. 62, № 3. -P. 229-239.
137. Tsetis D. Endovascular treatment of complications of femoral arterial access / D. Tsetis // Cardiovasc. Intervent. Radiol. 2010. — Vol. 33, № 3. -P. 457-468.
138. Tsutsumi K. Traumatic pseudoaneurysm of the subclavian artery following anterior dislocation of the shoulder: a report of a surgical case / K. Tsutsumi, H. Saito, M. Ohkura // Ann. Thorac. Cardiovasc. Surg. 2006. -Vol. 12, № l.-P. 74-76.
139. Ultrasound Guided Percutaneous Thrombin Injection for the Treatment of Postcatheterisation Femoral Pseudoaneurysm / D. Tsetis et al. // Hellenic. J. Cardiol. 2006. — Vol. 47. — P. 112-113.
140. Ultrasound guided percutaneous thrombin injection of iatrogenic femoral artery pseudoaneurysms after coronary angiography and intervention / J.Ferguson et al. // Heart. 2001. — Vol. 85. — URL: http://www.heartjnl.eom/cgi/content/full/85/4/e5.
141. Ultrasound-Guided Thrombin Injection for the Treatment of Iatrogenic Pseudoaneurysm of the Femoral Artery / A. Bloom et al. // IMAJ. -2001.-Vol. 3.-P. 649-652.
142. Ultrasound-Guided Thrombin Injection for the Treatment of Postcatheterization Pseudoaneurysms / L. La Perna et al. // Circulation. 2000. -Vol. 102.-P. 2391-2395.
143. Ultrasound-guided thrombin injection for the treatment of femoral artery pseudoaneurysms report of three cases / A. Sustic et al. // Lijec. Vjesn. — 2009. — Vol. 131, № 9-10. — P. 251-253.
144. Undseth R.M. Treatment of pseudoaneurysms after vascular interventions / R.M. Undseth, N.E. Klow, P. Hoffmann // Tidsskr. Nor. Laegeforen. 2004. — Vol. 124, № 10. — P. 1384-1386.
145. Unusual cause of haemorrhage from surgical wound in a child / R. Singh et al. // Strat. Traum. Limb. Recon. 2009. — Vol. 4. — P. 45-48.
146. Usefulness of sonographically guided thrombin injection of iatrogenic femoral pseudoaneurysms / V. Vázquez et al. // Med. Clin. 2003. — Vol. 121, №2.-P. 53-57.
147. Use of a pneumatic compression system (FemoStop®) as a treatment option for femoral artery pseudoaneurysms after percutaneous cardiac procedures / G. Dangas et al. // Catheterization and Cardiovascular Diagnosis. 1996. -Vol. 39.-P. 138-142.
148. US-guided percutaneous thrombin injection of postcatheterization pseudoaneurysms / K. Gürel et al. // Diagn. Interv. Radiol. 2012. — Vol. 18. -P. 319-325.
149. Visceral and Peripheral Arterial Pseudoaneurysms / E. Sueyoshi et al. //AJR.-2005.-Vol. 185.-P. 741-749.
150. Walker T.G. Transcatheter occlusion of a profunda femoral artery pseudoaneurysm using thrombin / T.G. Walker, S.C. Geller, D.C. Brewster // ARJ. 1987. -№ 149.-P. 185-186.
151. Weinmann E.E. Postcatheterization False Aneurysms / E.E. Weinmann, A. Bass // IMAJ. 2001. — Vol. 3. — P. 39-40.
152. Wojtarowicz A. Ultrasonographic contrast injection enhances safety of thrombin induced obliteration of femoral artery pseudoaneurysm / A. Wojtarowicz, M. Lewandowski, E. Piocska // Kardiol. Pol. — 2005. — Vol. 63. -P. 649-650.
источник





