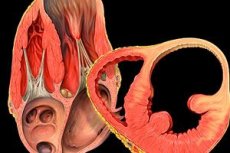
Аневризмой называется остро возникшее или постепенно формирующееся мешкообразное выпячивание сердечной стенки, возникшее в силу патологических изменений нормальной мышечной ткани. Аневризма может быть локализована в стенке и предсердий, и правого желудочка, но в связи с анатомо-функциональными особенностями сердца, чаще всего формирование аневризмы происходит в стенке левого желудочка. По статистике, аневризма левого желудочка развивается у 5-20% пациентов, перенесших острый инфаркт миокарда, и чаще диагностируется у лиц мужского пола старше 50 лет.
Аневризма левого желудочка представляет собой рубцовую ткань, которая формируется в том участке миокарда, в котором локализованы некротические или воспалительные процессы. Механизм развития аневризмы заключается в следующем. Нормальная мышечная ткань представлена гладко-мышечными волокнами, которые выполняют сократительную функцию. Для того, чтобы сокращаться в полную силу, волокнам необходима бесперебойная доставка кислорода с кровью, притекаемой по коронарным артериям. В случае закупорки артерии возникает острая нехватка кислорода в сердечной мышце (гипоксия) и развивается некроз, или отмирание сердечных клеток. Сердечная мышца в данном участке некроза превращается в “мягкую” ткань (процесс называется миомаляцией), и стенка сердца не способна выдержать высокое давление крови, нагнетаемой в желудочек из предсердной полости. Кроме этого, этот участок миокарда не способен нормально сокращаться в систолу и расслабляться в диастолу, и определенный кровяной объем так и остается в сформированном аневризматическом мешке. Такой механизм формирования аневризмы обусловлен острым инфарктом миокарда.
Формирование постинфактной аневризмы ЛЖ
Кроме острого инфаркта, аневризма левого желудочка может быть сформирована при развитии постинфарктного кардиосклероза. Кардиосклероз – это процесс развития соединительнотканных (рубцовых) волокон на месте погибших кардиомиоцитов. Другими словами, в сердце формируется рубец, которого в норме быть не должно. В том случае, если инфаркт миокарда был обширным, трансмуральным или циркулярным, рубцовой ткани в сердце становится слишком много, но она не может вынести тех нагрузок, которые испытывает мощная сердечная мышца. Под воздействием кровяного давления образуется постинфарктная аневризма. Таким образом, аневризма после инфаркта чаще развивается у тех пациентов, которые переносили обширный инфаркт, особенно повторно.
Не только некроз кардиомиоцитов может привести к образованию рубцовой ткани в сердце. Острые или хронические воспалительные процессы в сердечной мышце также приводят к истончению сердечной стенки за счет соединительной ткани. Такие процессы называются миокардитами, и вызваны они могут быть чем угодно. Чаще всего миокардит вызывается вирусами (грипп, ветрянка, брюшной тиф и др), бактериями (сифилис, стрептококки, стафилококки, пневмококки и др), грибками или обусловлен аутоиммунным воспалением в сердечной мышце, как, например, это бывает при системной красной волчанке или ревматизме.
Из провоцирующих факторов, способствующих развитию выпячивания в стенке сердца, следует отметить высокие цифры артериального давления и отсутствие строго постельного режима в первые недели после острого инфаркта или миокардита. Вот почему так важно лечить причинные заболевания в условиях стационара, контролировать гипертонию и строго следовать рекомендациям врача.
Клиническая картина аневризмы сердца не является строго специфичной. Другими словами, симптомов, по которым можно четко определить аневризму, не существует. Однако, быстрое прогрессирование сердечной недостаточности после обширного инфаркта миокарда, частая ее декомпенсация могут свидетельствовать о формировании выпячивания в стенке сердца.
Итак, симптомами, которые должны насторожить пациента и врача, являются следующие:
- Быстрое развитие (в течение нескольких недель и месяцев) левожелудочковой недостаточности, которая проявляется нарастанием одышки при физической активности и в покое, усиливающейся в положении лежа. У пациента снижается переносимость обычных бытовых нагрузок – пациент после инфаркта не может завязать шнурки, приготовить пищу, спокойно пройти в другую комнату без одышки.
- При инфаркте миокарда с аневризмой у пациента в остром периоде отмечаются частые приступы острой левожелудочковой недостаточности, проявляющиеся эпизодами сердечной астмы (сухой навязчивый кашель и учащение дыхания) и/или отека легких (влажный кашель с пенящейся мокротой, посинение кожи и другие признаки).
- Быстрое присоединение правожелудочковой недостаточности, которая проявляется отечностью нижних конечностей. У пациента буквально за несколько дней может увеличиться живот, что обусловлено застоем крови в печени и выпотом жидкости в брюшную полость (асцит). Отеки могут распространиться по всему телу (анасарка).
При появлении подобных признаков пациенту необходимо незамедлительно обратиться в поликлинику или в скорую помощь с целью дообследования и лечения.
Немаловажным в установке диагноза аневризмы является полноценный осмотр пациента. Так, в подавляющем числе случаев врач может увидеть патологическую прекардиальную пульсацию, которая определяется как периодическое выпячивание передней грудной стенки в 3-4 межреберьях слева от грудины, совпадающее с частотой сердечных сокращений. Этот феномен назван симптомом “перекатывающейся волны” или симптомом “коромысла”.
Кроме осмотра, при аускультации сердца можно выслушать систоло-диастолический шум, называемый “шумом писка”, но он выслушивается у незначительной части пациентов. Кроме этого, при выслушивании легких можно определить единичные или множественные, сухие или влажные хрипы в нижних отделах легких при сердечной недостаточности.
Также помимо истинной аневризмы левого желудочка, принято выделять ложную, обусловленную выпячиванием участка сердечной сумки – перикарда. Отличия – на рисунке ниже:
Если у врача возникло подозрение на формирование аневризмы сердца, он направляет пациента на обследование. Из методов диагностики информативными являются следующие:
- Электрокардиограмма. На ЭКГ аневризма, достигшая значительных размеров, характеризуется признаками острого повреждения миокарда и его некроза. В таком случае говорят о том, что ЭКГ имеет “застывший вид” острого инфаркта миокарда. Однако, отсутствие признаков инфаркта на ЭКГ еще не говорит о том, что у пациента нет аневризмы сердца.
- Рентгенография. Рентгенограмма органов грудной полости у пациентов с аневризмой, достигшей больших размеров, характеризуется увеличением тени сердца в поперечнике, а также выпячиванием сердечного контура. В том случае, когда аневризма имеет небольшие размеры, рентгено-диагностические методы оказываются малоинформативными.
- Эхокардиоскопия (эхо-кардиография, УЗИ сердца). Является информативным методом диагностики, так как позволяет не только уточнить форму, локализацию и размеры аневризмы, но еще и выявить наличие пристеночных тромбов, которые могут представлять значительную опасность для пациента.
- Компьютерная, магнитно-резонансная и мульти-спиральная компьютерная томография сердца (КТ, МРТ и МСКТ) являются самыми информативными методами выявления аневризмы и используются в качестве дополнения для УЗИ сердца в диагностически неясных случаях.
Консервативная терапия аневризмы неэффективна, поэтому медикаментозные препараты назначаются для лечения воспаления в остром периоде миокардита, для восстановления кровотока в миокарде при остром инфаркте, а также для профилактики или для лечения уже развивающейся хронической сердечной недостаточности.
Тактика лечения аневризмы может быть выжидательной или хирургической. В первом случае за пациентом осуществляется динамическое наблюдение – раз в полгода или раз в год ему необходимо посещать кардиолога с проведением ЭКГ, рентгенографии органов грудной клетки и УЗИ сердца. При увеличивающихся размерах аневризмы, или при появлении выраженных симптомов, значительно нарушающих качество жизни, пациенту может потребоваться кардиохирургическое вмешательство.
Средние (несколько сантиметров) и гигантские размеры аневризмы, когда выпячивание по объему сопоставимо с полостью самого левого желудочка, требуют проведения операции. При этом операция может быть выполнена как без разреза сердечной стенки, так и на открытом сердце с использованием аппарата искусственного кровообращения (АИК).
Методика операции заключается в ушивании аневризмы, в укреплении (пластике) аневризмы другими тканями, либо в резекции аневризмы.
- В первом случае выпячивание не вскрывается, а как бы погружается в стенку сердца с помощью швов, фиксирующих его к самому миокарду. Такая операция применяется при средних размерах аневризмы, которая не сильно выпячивается кнаружи и не сильно возвышается над поверхностью сердца. Оперативный доступ не требует вскрытия стенки сердца.
- Во втором случае аневризма не удаляется, а к стенке сердца подшивается лоскут из диафрагмы, питание которого осуществляется с помощью сосудистой ножки. Разреза стенки сердца не требуется, а операция применима при средних размерах аневризмы, которая диффузно охватывает миокард, и также не сильно возвышается над наружной поверхностью сердца. Оперативный доступ к диафрагме и к сердцу осуществляется посредством разреза грудной клетки в шестом межреберье слева с вскрытием плевральной и перикардиальной полостей.
- Резекция аневризмы является радикальным (то есть удаляющим аневризму насовсем) методом лечения – стенку аневризмы иссекают, удаляют ее часть и ушивают специальными швами. Операция проводится на открытом сердце, с применением АИК. После оперативного доступа и накладывания швов на аневризматический мешок важно как можно быстрее вскрыть купол аневризмы и наложить швы (обычно кардиохирург выполняет данную манипуляцию за 40-60 секунд). Оставшееся время занимает ушивание дефекта в стенке сердца и наложение диафрагмального лоскута.
После операции пациент несколько дней должен находиться в кардиохирургическом отделении с целью наблюдения и предупреждения постоперационных осложнений.
Аневризмы ЛЖ незначительных размеров обычно не представляют опасности для жизни пациента, хотя в редких случаях могут провоцировать тромбоэмболические осложнения вследствие формирования пристеночных тромбов в полости сердца, которые током крови разносятся по другим артериям и могут стать причиной инфаркта, инсульта, тробоэмболии легочной или брызжеечной артерий (ТЭЛА и мезентериального тромбоза).
Осложнения при аневризмах средних и гигантских размеров встречаются чаще, и заключаются в следующем:
- Тромбоэмболические осложнения,
- Прогрессирование хронической сердечной недостаточности, развитие острой сердечной недостаточности,
- Разрыв аневризмы, приводящий к быстрой гибели пациента.
Профилактикой осложнений является своевременное выявление роста аневризмы, регулярное обследование у врача, а также своевременное выявление показаний для оперативного лечения.
Осложнения после кардиохирургического вмешательства встречаются редко и заключаются в развитии тромбоэмболии, воспалительных процессов в постоперационной ране, а также в рецидиве аневризматического выпячивания при погружении или пластике аневризмы. Профилактикой является тщательное наблюдение за больным в раннем (в условиях стационара), а также в постоперационном периодах (в условиях поликлиники).
Прогноз при аневризме после инфаркта определяется, исходя из ее размеров и локализации. Так, аневризмы небольших размеров, диффузно локализующиеся на передней стенке ЛЖ или аневризмы верхушки левого желудочка, не требующие оперативного лечения, характеризуются благоприятным прогнозом для жизни и здоровья пациента.
Аневризмы средних и гигантских размеров часто являются причиной тяжелой сердечной недостаточности и тромбоэмболий, поэтому без лечения в данном случае прогноз неблагоприятный. После операции прогноз улучшается, так как у 90% пациентов качество жизни повышается, а пятилетняя выживаемость увеличивается.
источник
Постинфарктная аневризма левого желудочка (ПИАЛЖ) — это ограниченный участок истонченной рубцовой или фиброзно-мышечной ткани с выпячиванием сердечной стенки в этой области. Функционально представляет собой зону миокарда потерявшего способность к сокращениям, локальные движения которой могут быть двух видов: акинез и дискинез. Ряд исследований показывают, что зона аневризмы может включать в себя также и гипокинетичные участки стенки левого желудочка (ЛЖ).
Наличие у больного ПИАЛЖ не может не влиять на его исходный статус, и как следствие на течение анестезии и гемодинамические реакции в ответ на введение препаратов.
Чаще всего ПИАЛЖ развивается при больших трансмуральных инфарктах миокарда на фоне окклюзии передней межжелудочковой ветви (ПМЖВ). Поэтому наиболее частая локализация — это передняя, переднебоковая и верхушечная снижению общей сократительной способности миокарда, ФВ и ударного объема (УО).
Перегрузка давлением и объемом, испытываемые миокардом ЛЖ в процессе эволюции ОИМ, также оказывают влияние на сопряженные неинфарцированные участки. Данная биомеханическая модель сердечной недостаточности, предложенная Mann и Bristow, описывает изменение геометрических соотношений в ЛЖ, которые в свою очередь приводят к структурным изменениям в миокарде и активируют нейрогурмональную регуляцию гомеостаза.
Обычно концентрация катехоламинов в крови прямо пропорциональна степени дисфункции ЛЖ. Первоначально увеличение СВ происходит за счет увеличения частоты сердечных сокращений (ЧСС) и сократимости. Однако в условиях нарушенной перфузии миокарда это приводит к повышению потребности миокарда в кислороде и дальнейшему ухудшению систолической функции ЛЖ. В дальнейшем происходит вазоконстрикция, позволяющая поддержать артериальное давление (АД). Обусловленное вазоконстрикцией повышение общего периферического сосудистого сопротивления (ОПСС) снижает СВ и усугубляет недостаточность ЛЖ.
Постоянная симпатическая активация при хронической сердечной недостаточности (ХСН) уменьшает чувствительность адренорецепторов к катехоламинам, количество этих рецепторов и запасы катехоламинов в сердце. Однако сердце становится более зависимым от катехоламинов, циркулирующих в крови. Множество циркулирующих и тканевых белков, и пептидов (норэпинефрин, ангиотензин, эндотелии, альдостерон, фактор некроза опухоли, интерлейкины), образуются уже в начальной стадии повреждения.
Кроме того, длительный чрезмерный выброс этих биологически активных веществ может существенно усилить экспрессию генов, изменяя синтез белка в миоцитах и фибробластах. Адренергическая, ренин-ангиотензиновая (РААС) и система цитокинов активизируются системно и местно в миокарде в ответ на снижение СВ. Их системное воздействие приводит к перераспределению кровотока от кожи, почек, кишечника и скелетной мускулатуры к сердцу и головному мозгу.
Гипоперфузия почек активирует РААС. Происходит задержка натрия и воды. Кроме того, альдостерон, являясь мощным вазоконстриктором, увеличивает ОПСС и постнагрузку на ЛЖ, еще больше ухудшая его функцию. Порочный круг замыкается.
Основой развития ХСН при ИБС является именно ремоделирование ЛЖ, происходящее на всех уровнях структурной организации сердца — молекулярном, генном, клеточном, интерстициальном и сопровождающееся изменением размера, формы и функции сердца после повреждения миокарда.
В сравнении с больными ИБС без ПИАЛЖ в случае наличия постинфарктной аневризмы отмечается увеличение КДО, КСО, т. е. отмечается прогрессивное увеличение полости ЛЖ в обе фазы сердечного цикла. Причиной диастолической дисфункции является неэластичность дилатированной стенки аневризмы, что негативно влияет на диастолическое наполнение ЛЖ и увеличивает конечно-диастолическое давление в левом желудочке (КДДЛЖ).
Вследствие повышения КДДЛЖ и уровня катехоламинов неповрежденный миокард в перирубцовых зонах демонстрирует гиперконтрактильность, что в дальнейшем приводит к гипертрофии миокарда. Компенсаторно развивается гипердинамическая реакция не вовлеченных в патологический процесс сегментов (чаще всего базальных), что в свою очередь ведет к дополнительному растяжению стенок желудочка.
Процесс дилатации ЛЖ прямо связан с величиной миокардиального стресса (напряжение стенок желудочка). Расширение полости ЛЖ, приводит к нарушению его геометрии и, вследствие этого, к повышению внутрижелудочкового давления и усугублению миокардиального стресса с возрастанием потребления миокардом кислорода. Компенсаторная гипертрофия сохранившегося миокарда носит эксцентрический характер и должного увеличения массы миокарда не происходит.
По закону Лапласа (T = Pr/2h), при постоянном давлении (Р) в желудочке увеличение радиуса кривизны (r) и снижение толщины стенки (h), в зоне инфаркта приводят к увеличению напряжения мышечных волокон (Т) и к дальнейшему растяжению пораженной инфарктом стенки ЛЖ. Изменение формы полости ЛЖ имеет тенденцию к образованию сферического ЛЖ, что в итоге отрицательно влияет на гемодинамику и работу сердца.
В дальнейшем для постинфарктной аневризмы характерны глобальные гемодинамические сдвиги. Это прежде всего сниженные ударный объем (УО) и сердечный индекс (СИ). Интегральный показатель сократительной способности миокарда ФВ также снижается по мере увеличения размеров ЛЖ.
Выключение части миокарда из эффективной работы сердца приводит к снижению систолической функции. Морфологические изменения в миокарде обусловливают значительные изменения механических свойств тканей, архитектоники миокарда, приводят к различного рода деформациям, возникающим при асинергичной кинетике стенок, нарушению стереотомических соотношений в полости желудочка.
Изменение геометрии ЛЖ создает новые условия для внутрисердечной гемодинамики. Другими словами, создаются условия для прогрессирования ишемии и диастолической дисфункции. Увеличение КДО и КДДЛЖ приводит к усилению напряжения на стенки камеры желудочка и вторичной механической деформации не только в систолу, но и в диастолу. Следующее за этим нарастание дилатации ЛЖ значительно снижает сократительную способность миокарда и замыкает порочный круг развития сердечной недостаточности.
При увеличении конечно-диастолического размера (КДР) ЛЖ больше 5,5 см ударный объем продолжает нарастать. «Пороговым» значением компенсаторного увеличения конечно-диастолического объема (КДО) ЛЖ считают показатель в пределах 182,7±3,28 мл. После превышения этой «границы» последующая дилатация ЛЖ становится дезадаптивной.
Компенсаторно развивается гипердинамическая реакция не вовлеченных в патологический процесс сегментов (чаще всего базальных), что в свою очередь ведет к дополнительному растяжению стенок желудочка.
С помощью ЭхоКГ в 1995 г. Т. Kawata и соавт. измерили ДЛА и КДДЛЖ (ДЛП) и отметили его снижение после реконструктивных вмешательств на ЛЖ, а в 2006 г. аналогичное исследование было проведено Т. Isomura.
За счет парадоксального движения стенок аневризмы в каждую фазу систолы образуется остаточный объем крови, что и снижает УО и СИ, а также при наличии различных нарушений ритма сердца способствует тромбообразованию в левых отделах сердца.
Часто отмечается нарушение контрактильности сокращающейся части ЛЖ, обусловленное ухудшением миокардиального кровотока. Это можно объяснить тем, что, с одной стороны, гипертрофированный миокард обладает ограниченным вазодилатационным резервом, особенно в условиях атеросклероза коронарных артерий, а с другой, вследствие увеличения КДДЛЖ происходит снижение коронарного пер- фузионного давления (КПД).
Рядом авторов показано, что реперфузия инфарктзависимой коронарной артерии в первые 2 нед после развития инфаркта миокарда при спонтанной реперфузии вследствие тромболизиса или перкутанной ангиопластики улучшает доставку фибробластов к поврежденному миокарду, способствуя или предотвращая развитие аневризмы ЛЖ.
Кроме этого, часть жизнеспособного миокарда может находится в состоянии гибернации (спячки). Гибернация представляет собой адаптационный механизм, позволяющий миокарду не погибнуть в состоянии недостаточного кровоснабжения, но при этом функциональные способности резко нарушены.
Терминами «спящий, или гибернирующий, миокард» (hibernating) описывается состояние дисфункции ЛЖ в покое, вызванной его длительной гипоперфузией, которая полностью или частично исчезает после улучшения коронарного кровообращения и/или снижения потребности миокарда в кислороде. Сложилось представление, что при гибернации кардиомиоциты остаются жизнеспособными в течение длительного времени и даже через несколько лет функция ЛЖ может восстановиться. У больных, перенесших ИМ, гибернация может обнаруживаться как в зоне кровоснабжения коронарной артерией, связанной с инфарктом, так и на более отдаленных участках.
Также особенностью ПИАЛЖ является наличие митральной регургитации, обусловленной дилатацией ЛЖ, митрального кольца и ишемической дисфункцией папиллярных мышц. Это может оказаться причиной дальнейшего увеличение объема ЛЖ и снижения насосной функции сердца. D.A. Cooley, L. Mickleborough выявили уменьшение степени митральной регургитации после коррекции аневризмы ЛЖ.
Снижение насосной функции сердца, диастолическая дисфункция левого желудочка и сопутствующая митральная недостаточность способствуют повышению давления в малом круге кровообращения. Большинство исследователей сходятся во мнении, что основным звеном развития легочной гипертензии является нарушение оттока крови из легких за счет первичного нарушения сократимости левого желудочка. Это повышает КДДЛЖ, среднее давление в левом предсердии, легочных венах, а также в системе легочных капилляров, артериол и артерий.
Развитие описанных выше процессов приводит к клиническим проявлениям признаков левожелудочковой сердечной недостаточности (СН), к которой в последствие вторично может присоединиться и правожелудочковая.
В ответ на снижение СВ включаются различные компенсаторные механизмы (повышение симпатического тонуса, увеличение преднагрузки, активация РААС, гипертрофия желудочков), которые позволяют первоначально компенсировать дисфункцию желудочков, но при прогрессировании СН они усугубляют нарушения работы сердца.
Медикаментозная терапия, подавляющая нейрогормональную активацию, имеет тенденцию замедлять, но не в состоянии остановить процесс ремоделирования.
Увеличение размера ЛЖ не только отражает его неспособность справляться с венозным возвратом, но и также позволяет максимально повысить УО. Даже при сниженной ФВ увеличение КДО позволяет некоторое время поддерживать УО на приемлемом уровне. Нарастание венозного застоя, обусловленного скоплением крови перед ЛЖ и чрезмерным его перерастяжением, приводит к развитию легочной гипертензии, сначала венозной, а затем и артериальной. Таким образом, ДЛА является важным критерием функционального состояния ЛЖ и его повышение происходит с появлением первых признаков СН.
J.A. Goldstein и соавт., изучая связь функции правого желудочка при пораженной правой коронарной артерии, отметили значительное нарушение функции правого желудочка, приводящее к снижению преднагрузки левых отделов сердца. В процессе исследования авторы отметили значительное влияние сократительной способности правого желудочка на дискинез межжелудочковой перегородки. Лучшая функция правого предсердия позволяет создавать оптимальное давление в ПЖ и влиять на гемодинамику левых отделов через снижение дискинеза межжелудочковой перегородки.
Функциональное состояние правого желудочка (ПЖ) у больных с ПИАЛЖ также имеет большое значение. Нарушение систолической функции ПЖ у больных с тяжелыми формами ИБС в настоящее время можно считать установленным фактом. Сейчас полностью пересмотрен взгляд на ПЖ как на простой «проводник» крови из малого круга кровообращения в большой. Изменение систолической и диастолической функции ПЖ оказывает значимое влияние на детерминанты производительности ЛЖ. Снижение СИ практически всегда сопровождается уменьшением фракции выброса ПЖ. Это прежде всего связано с расстройствами внутрисердечной гемодинамики, повышением общелегочного сосудистого сопротивления (ОЛС) и нарушением межжелудочковых соотношений за счет вовлечения в процесс МЖП (ее рубцового изменения или за счет зон гибернирующего миокарда).
Нарушения ритма в виде желудочковой экстрасистолии (ЖЭ), пароксизмальной желудочковой тахикардии (ЖТ) и фибрилляции желудочков (ФЖ) — также фактор риска, который следует иметь в виду анестезиологу при проведении анестезиологического пособия у больных с ПИАЛЖ. В 80% случаях перирубцовая зона субэндокардиальной части — это зона re-entry — основного механизма развития аритмий у таких пациентов. Однако, если нарушения ритма имели место в доопрационном периоде, то, как правило, больные поступают на фоне приема антиаритмиков (бета-блокаторы, кордарон) и серьезных нарушениях ритма во время операции, в частности во время индукции и в доперфузионном периоде, что встречается крайне редко.
Тромбоз полости аневризмы, встречающийся до 40% случаев, трудно рассматривать как фактор риска для кардиоанестезиолога, особенно в доперфузионном периоде. Но в ряде случаев, когда имеются рыхлые тромботические массы с фрагментацией, после пуска кровотока возможна эмболия в различные органы. В том числе и попадание эмболов в коронарные артерии, что приводит к развитию интраоперационного инфаркта миокарда и острой сердечной недостаточности.
На течение постперфузионного периода не может не влиять характер выполненной коррекции ПИАЛЖ. Изменение объема и геометрии ЛЖ, несомненно, влияет на гемодинамику и некоторые хирургические аспекты представляют для кардиоанестезиолога несомненный интерес.
Хирургическая коррекция постинфаркгной аневризмы преследует следующие цели.
- Снижение КДО за счет удаления не сокращающейся, парадоксально пульсирующей части стенки ЛЖ и как следствие этого увеличение ФВ и уменьшение степени СН.
- Сопутствующая реваскуляризация миокарда.
- Уменьшение работы сохранной части миокарда ЛЖ.
- Снижение степени относительной митральной недостаточности за счет уменьшения объема полости ЛЖ.
- Устранение очагов аритмии, локализующихся в области рубца.
В разные годы были предложены различные виды пластик ПИАЛЖ. Но до сих пор ведутся поиски способов наиболее адекватной коррекции аневризм сердца. Неудовлетворенность результатами линейной пластики привела к появлению новых методов: септопластика, реконструкция полости ЛЖ по Jatane, операция типа «сэндвич», эндовентрикулопластика с использованием рубцово-измененной МЖП и, наконец, эндовентрикулопластика синтетической заплатой (Dor, Бокерия).
Большое внимание уделяется коррекции парадоксальной подвижности МЖП, так как аневризматически измененная перегородка продолжает нарушать контрактильную функцию ЛЖ.
В последние годы хирургами НЦ ССХ был предложен новый термин для операции реконструкции ПИАЛЖ — редукционная вентрикулопластика, подчеркивающее два важных механизма: редукцию полости ЛЖ и его пластическое ремоделирование с созданием оптимальной эллиптической конфигурации. Все это в сочетании с реваскуляризацией миокарда позволяет ликвидировать ишемическую дисфункцию вне зоны аневризмы.
Таким образом, линейная пластика применяется в настоящее время только при ограниченных аневризмах верхушечной локализации, метод Jatane — при передневерхушечных аневризмах без обширного рубцового поражения МЖП, реконструкция ЛЖ с использованием заплаты из рубцово-измененной МЖП — только при относительно небольших аневризмах и отсутствии пристеночного тромбоза. Редукционная вентрикулопластика с использованием синтетической заплаты показана при больших ПИАЛЖ с обширным вовлечением МЖП, резким снижением ФВ и массивным тромбозом полости ЛЖ.
Выбор методики реконструкции ЛЖ остается за хирургом, для кардиоанестезиолога главными моментами является степень уменьшения полости ЛЖ (КДО) и реваскуляризация миокарда.
Исходя из всего вышесказанного, проблемы анестезиологического пособия у больных ИБС с резко сниженной контрактильностью миокарда, в частности у больных с ПИАЛЖ, нуждаются в более детальном изучении. Наибольший интерес представляют патофизиологические закономерности изменения гемодинамики во время операции, знание которых позволит кардиоанестезиологу более грамотно подойти к выбору препаратов для анестезии.
Наконец, необходимо разработать патогенетически обоснованные показания к назначению кардиотонических препаратов при адекватной волемической нагрузке в раннем постперфузионном периоде у больных после коррекции ПИАЛЖ.
источник
Аневризма левого желудочка (АЛЖ) — это мешковидный тип рубцовой ткани, который располагается на сердечной мышце. Из-за изменений он выпирает наружу и истончается. Это приводит к изменениям в работе сокращения мышц или полной остановке сокращений. Такие проблемы возникают в области верхушки сердца или его верхней части. Инфаркт миокарда диагностируется чаще у мужчин от 40 до 70 лет, чем у женщин того же возраста.
Мышечная ткань состоит из гладкомышечных волокон, основной функцией которых является сокращение. Для нормальной работы им необходима бесперебойная подача обогащенной кислородом крови посредством артерий. Если в них происходит закупорка, поступление кислорода сокращается, и в этом участке происходит гипоксия (острая нехватка). Вследствие гипоксии ткань становится «мягкой» и не способной выдерживать кровеносное давление.
Тромбы могут формироваться вследствие перенесенного острого инфаркта миокарда. Важно соблюдать режим лечения во время начальной стадии развития инфаркта и не усложнять процесс заживления после инфарктного рубца. Физические нагрузки в это время противопоказаны.
Другими причинами возникновения АЛЖ могут быть:
- инфекционные заболевания тяжелой формы;
- травмы сложных форм;
- прямое ранение (выстрел, удар острым предметом);
Этот вид патологии возникает из-за разрушения структуры миокарда. При повышении артериального давления происходит растяжение и последующее истощение стенок.
Аневризмы классифицируются по нескольким признакам, благодаря которым ставится точный диагноз. Проявление симптомов проходит в острой, подострой и хронической формах. Они проявляются в разный период после перенесению приступа. Самой сложной для диагностирования является хроническая форма, схожая по симптомам с обострением сердечной недостаточности.
Структура аневризмы бывает ложной, функциональной и истинной и устанавливается в зависимости от вида клеток. Также заболевание разнится по форме проявления. Диффузная форма (выпячивание с углублением) чаще всего встречается во врачебной практике, а грибовидная (изменение большого участка) и расслаивающаяся (несколько аневризм на 1 месте) — встречаются редко.
Появление следующих симптомов служит следствием перенесенного приступа:
- проявляется частыми аритмиями, усиливающимися в лежачем положении;
- ноющая боль в груди, которая может быть под левой лопаткой;
- появление одышки при незначительных физических нагрузках, перерастающих в приступы удуший;
- шумы в сердце.
- появление частой слабости, повышение температуры;
- повышенная потливость и набухание вен на шее;
- аневризма верхушки левого желудочка приводит к постоянным отекам;
Однако симптоматика заболевания не является специфичной, по этим симптомам не всегда можно определить эту проблему, так как они могут служить признакам и других расстройств.
Если перечисленные симптомы есть, то лучше проконсультироваться у врача. Диагностика заболевания начинается с опроса пациента и сбора анамнеза с помощью лабораторных анализов (анализ крови, мочи). Также выяснить причину возникших проблем помогает радиоизотопная вентрикулография, определяющая размер и локацию дефекта мышцы.
Проводится рентген грудной клетки, указывающий точные размеры сердца.
Стандартным методом исследования является топография сердца, с ее помощью можно обнаружить наличие перебоев в работе органа. Максимально информативным способом обследования являются компьютерные томографии сердца. Их существует несколько типов, зависящих от использования разных видов спиралей. Для четкой картины протекания болезни они служат дополнением к УЗИ. Собрав все необходимые показатели, кардиолог устанавливает курс лечения.
Оно может быть выжидательным или операционным. Если размеры аневризмы небольшие, и угрозы для жизни нет, то за пациентом устанавливается динамическое наблюдение. Раз в несколько месяцев больному нужно проводить диагностические процедуры (посещение врача и компьютерные обследования). Это лечение является профилактикой развития хронической недостаточности и помогает предотвратить осложнение.
Если размеры выпячивания оказываются большими, или симптомы протекания болезни обострены, и это сказывается на качестве жизни пациента, то может потребоваться хирургическое вмешательство. Существует несколько методик их проведения:
- Ушивание аневризмы. Используется при средних размерах выпячивания, которое не вскрывается, а погружается в стенку. При этом фиксируется миокард.
- Пластика другими тканями. Проводится в том случае, когда ремоделирование сердца — средних размеров и находится невысоко от наружной поверхности органа. Измененная область не удаляется, а подшивается к диафрагме (которая питается с помощью сосудистой ножки). Доступ осуществляется благодаря разрезу грудной клетки.
- Резекция — самый радикальный метод, это удаление аневризмы посредством ее иссечения и ушивания специальными швами. Операция проводится при открытом доступе к сердцу с применением АИК. Процесс вскрытия купола и наложения швов должен проходить максимально быстро, хирургу дается 1 минута на проведение всей процедуры.
Осложнениями послеоперационного вмешательства могут быть: тромбоэмболии, усугубленное обострение хронических проблем с сердцем, разрыв области выпячивания (приводит к скорой смерти пациента). Они встречаются редко в хирургической практике. Проблемы послеоперационного восстановления чаще заключаются в воспалительных процессах заживания шва или рецидиве появления аневризмы. Для безопасности жизни пациента наблюдение происходит в стационарном режиме, сразу после операции, и послеоперационном ведении в поликлинике.
С аневризмой левого желудочка срок жизни может быть разным, все зависит от ее размеров и месторасположения. При небольших размерах и расположении в верхней части левого желудочка она не является прямой угрозой для жизни, не требует срочного хирургического вмешательства и дает благоприятный прогноз для здоровья пациента. Лечение носит выжидательный характер с незначительным медикаментозным сопровождением.
При средних и гигантских размерах аневризма левого желудочка сердца прогноз дает менее оптимистичный. Иногда является причиной появления острой сердечной недостаточности и тромбоэмболии. Лечится только при кардиохирургическом вмешательстве. Операция помогает повысить пятилетнюю выживаемость до 80% и оптимизировать качество жизни больного. Следствием смертельного исхода в 60% случаев являются повторные инфаркты.
На прогноз влияет дальнейшая работа сердечной мышцы. Из-за ушивания во время операции, размеры желудочка уменьшаются, что может повлиять на способность перекачивания нужного количества крови. Такая проблема называется синдромом небольшого выброса. Но даже при ее наличии срок жизни составляет более 8 лет.
Многие люди живут с подобными проблемами и ведут нормальный образ жизни. Своевременное обращение к специалисту и правильная постановка диагноза помогают сохранить здоровье.
источник
Аневризма сердца (aneurysma cordis) — ограниченное выпячивание истонченного участка стенки сердца. Чаще всего развивается в результате инфаркта миокарда. Значительно реже встречаются врожденные, инфекционные, травматические, послеоперационные аневризмы сердца. Травматические аневризмы возникают из-за перенесенных закрытых или открытых травм сердца. К этой же группе относятся аневризмы, возникающие после операций при врожденных пороках сердца.
В подавляющем числе случаев аневризма сердца является осложнением после перенесенного инфаркта миокарда (чаще трансмурального). До 25% пациентов с инфарктом могут быть подвержены этому заболеванию.
Опасными осложнениями хронической аневризмы сердца являются гангрена конечности, инсульт, инфаркт почки, ТЭЛА, повторный инфаркт миокарда. При разрыве аневризмы сердца наступает мгновенная смерть.
По времени возникновения аневризмы делят на острые (1-2 неделя от начала развития инфаркта миокарда), подострые (3-6 недель) и хронические. Чаще всего постинфарктные аневризмы локализуются на переднебоковой стенке и на верхушке левого желудочка, в 50-65% случаев распространяются на передне-перегородочную область.
Аневризма левого желудочка диагностируется столь часто по причине максимального давления крови именно в этом желудочке. До 50% поверхности левого желудочка может пострадать в результате патологического процесса.
Аневризма задней стенки левого желудочка наблюдается у 2-8% больных. Нередко в полости аневризмы обнаруживаются тромбы, однако частота тромбоэмболических осложнений не более 13%.
Клинические проявления зависят от размеров и локализации аневризмы.
Острой аневризме сердца соответствуют следующие симптомы:
Подострая аневризма сердца проявляется быстро прогрессирующими симптомами недостаточности кровообращения.
Хроническую аневризму сердца характеризуют:
- ярко выраженные признаки сердечной недостаточности (одышка, стенокардия покоя и напряжения, ощущение перебоев в работе сердца, на поздних этапах — набухание вен шеи, отеки, и др.)
- фиброзный перикардит, вызывающий спаечные процессы в грудной полости.
При хронической аневризме сердца может развиться тромбоэмболический синдром (чаще поражаются подвздошный и бедренно-подколенный сегменты, плечеголовной ствол, артерии мозга, почек, легких, кишечника.
Среди опасных осложнений хронической аневризмы сердца можно назвать гангрену конечности, инсульт, инфаркт почки, ТЭЛА, повторный инфаркт миокарда.
В ряде случаев возможен разрыв хронической аневризмы сердца. Он происходит на 2-9 день после инфаркта миокарда и приводит к мгновенному летальному исходу. Клинические проявления разрыва аневризмы сердца: внезапная резкая бледность (которая быстро сменяется цианотичностью кожных покровов), холодный пот, переполнение вен шеи кровью, потеря сознания, похолодание конечностей, шумное, хриплое, поверхностное дыхание.
У 50% больных выявляется патологическая прекордиальная пульсация.
ЭКГ-признаки неспецифичны — выявляется «застывшая» картина острого трансмурального инфаркта миокарда, могут быть нарушения ритма (желудочковая экстрасистолия) и проводимости (блокада левой ножки пучка Гиса).
ЭХО-КГ позволяет визуализировать полость аневризмы, определить ее размеры и локализацию, выявить наличие пристеночного тромба.
Жизнеспособность миокарда в зоне хронической аневризмы сердца определяется посредством стресс-ЭхоКГ и ПЭТ.
С помощью рентгенографии органов грудной клетки представляется возможным выявить кардиомегалию, застойные процессы в кровообращении.
Применяются также рентгеноконтрастной вентрикулографии, МРТ и МСКТ сердца для определения размеров аневризмы сердца, выявления тромбоза ее полости.
С целью дифференциальной диагностики заболевания от целомической кисты перикарда, митрального порока сердца, опухолей средостения может быть назначено зондирование полостей сердца, коронарография.
Консервативными методами лечения аневризму сердца устранить невозможно, и при появлении первых признаков сердечной недостаточности ставится вопрос об операции. Основной метод лечения аневризмы сердца — это хирургическое иссечение и ушивание дефекта сердечной стенки. В некоторых случаях проводится укрепление стенки аневризмы с помощью полимерных материалов.
В предоперационном периоде назначаются сердечные гликозиды, антикоагулянты, гипотензивные средства, кислородотерапия, оксигенобаротерапия. Пациентам рекомендуется строго ограничивать физическую активность.
В кардиологическом отделении «МедикСити» есть все необходимое оборудование для проведения комплексной диагностики широкого спектра кардиологических заболеваний. Прием ведут врачи-кардиологи высокой квалификации, прошедшие профессиональные стажировки в России и за рубежом.
Также Вы можете воспользоваться представленными ниже формами для того, чтобы задать вопрос нашему специалисту, записаться на прием в клинику или заказать обратный звонок. Задайте вопрос или укажите проблему, с которой Вы хотели бы к нам обратиться, и в самое ближайшее время мы свяжемся с Вами для уточнения информации.
источник
Развитие опасного постинфарктного осложнения — аневризмы левого желудочка. Современные подходы к лечению
Болезни сердца, при которых поражается миокард желудочковых камер, осложняются рядом необратимых вторичных заболеваний. Одним из подобных состояний является развитие рубцовой ткани, определяющей снижение всех функций левого желудочка.
Опасность патологии выражается в возможной тромбоэмболии, усугублении сердечной недостаточности и угрозе летального исхода.
Код по МКБ-10: I25.3.
Четко ограниченная рубцовая ткань левого желудочка, не участвующая в сокращении мышечных волокон, называется аневризмой. Патология характеризуется спадением или парадоксальным движением пораженного участка во время систолы и диастолы.
По времени возникновения выделяют следующие виды патологии:
- Врожденные (дивертикулы) – первичные;
- Приобретенные – вторичные.
Приобретенные делят по причинному заболеванию, морфологии, механизму и локализации.
- Коронарогенные – при патологии венечных артерий;
- Некоронарогенные – вследствие болезней миокарда;
- Посттравматические (в том числе послеоперационные и постинфарктные аневризмы левого желудочка).
По механизму:
- Истинные – представлены растянутым участком миокарда;
- Ложные – представлены гематомой, ограниченной перикардом.
По форме выделяют следующие разновидности:
- Мешковидные — имеют шейку, тело и купол;
- Диффузные — плавно переходят в здоровый миокард.
Существует четыре типа локализации аневризмы:
- В области верхушки – аневризма поражает нижнюю часть левого желудочка, заканчивающуюся куполообразным сужением;
- Передне-перегородочная – аневризма передней стенки левого желудочка, выходит за пределы верхушки и захватывает нижнюю часть межжелудочковой перегородки;
- Базального отдела – аневризма расположена снизу на задней стенке левого желудочка;
- Передняя – локализована спереди и частично распространяется на верхушку.
По течению выделяют острую, подострую и хроническую стадии (формы):
- Острая – стенка желудочка представлена участком некротизированного миокарда. Данная форма длится 1-2 недели и сопровождается выраженной болью, лихорадкой, слабостью;
- Подострая – от 3 до 8 недель. Представлена утолщенным эндокардом со скоплением эластических волокон. Клиника стертая, болевой синдром неяркий, лихорадка не характерна;
- Хроническая аневризма левого желудочка — начинается с 9 недели. Представлена нерастяжимой грубоволокнистой соединительной тканью. Симптомы определяются первичным заболеванием и сердечной недостаточностью.
Врожденные аневризмы (5% больных) развиваются во внутриутробном периоде под действием внешних факторов, приводящих к мутации генов.
Приобретенные образуются вследствие следующих причин:
- Атеросклероза венечных сосудов;
- Ревматоидного артрита;
- Инфекционного эндокардита;
- Саркоидоза;
- Трансмурального инфаркта (более 90% случаев);
- Кардиомиопатии;
- Вирусных миокардитов;
- Сифилиса.
Выделяют две последовательные фазы развития:
- Раннюю дилатацию (некроз и разволокнение);
- Позднее ремоделирование (формирование рубца).
Длится 2-14 дней. Сразу после ишемии стенка миокарда становится гладкой, место повреждения перекрывается тромбом.
К концу 1-2 суток клетки теряют структуру и некротизируются под действием ферментов. Коллагеновые волокна истончаются, поэтому подвергшийся некрозу участок (в последующем – стенка аневризмы) испытывает постоянное систолическое давление крови. Это приводит к прогрессирующему растяжению и увеличению пораженной зоны.
Большая часть крови поступает не в большой круг кровообращения, а в образованное выпячивание. Это приводит к усугублению ишемии и снижению фракции выброса.
Начинается с 3-4 недели. На месте ишемии развивается регенераторная ткань, которая постепенно замещается соединительными волокнами. Образовавшийся рубец предотвращает растяжимость миокарда, останавливая увеличение некротизированной зоны. Из-за вовлечения в процесс нервных волокон в данную фазу развиваются короткие цепочки нервного возбуждения, провоцирующие приступы аритмии.
Появление плотного рубца, четко отграниченного от здоровой ткани – конечный этап ремоделирования.
Матриксные металлопротеиназы – ферменты, участвующие в процессах рубцового перерождения миокарда. Они представлены белками, которые вырабатываются регенераторными клетками в ответ на повреждение.
Матриксные металлопротеиназы предназначены для разрушения омертвевшей зоны желудочка. Под их действием в фазу ранней дилатации нарушается анатомическая структура коллагеновых волокон. Ферменты способствуют разрушению участка некроза, на месте которого формируется новая соединительная ткань.
Течение длительное и медленно прогрессирующее. Наличие аневризмы приводит к падению фракции выброса. Уменьшение поступления крови в аорту провоцирует артериальную гипертензию. Впоследствии это вызывает нарушение проводимости и сократительной функции сердца. В течение года у большинства пациентов развиваются вторичные осложнения, самым частым из которых выступает аритмия. Следствием аритмии является повышенное тромбообразование.
Симптомы неспецифичны. Классическая триада представлена:
- Одышкой;
- Болевым синдромом;
- Ощущением перебоев и частого сердцебиения.
Одышка носит смешанный характер и проявляется затруднением как вдоха, так и выдоха. Болевой синдром развивается по типу стенокардии – в пределах 10-15 минут после физической нагрузки. Ощущение перебоев обусловлено развивающейся аритмией и может носить приступообразный или постоянный характер.
Другие проявления:
- Обмороки;
- Отеки;
- Снижение толерантности к физической нагрузке;
- Бессонница;
- Внезапная сердечная смерть.
Среди ранних осложнений наиболее значимы:
Для подтверждения диагноза используется комплекс визуализирующих обследований – ЭКГ, вентрикулоангиография, рентгенография грудной клетки, УЗИ (ЭХО), КТ, МРТ, радионуклидная ангиография. Выявляют следующие признаки заболевания:
- Рентгенография – расширение тени сердца влево, увеличение дуги левого желудочка;
- ЭКГ – подъем зубца Т и появление патологического зубца Q;
- Вентрикулоангиография– выявление парадоксальной подвижности в области одной из стенок желудочка;
- УЗИ сердца – обнаружение рубцовой ткани, присердечной гематомы, тромбообразования. Метод позволяет также подтвердить снижение фракции выброса;
- КТ (МРТ) – истончение стенки аневризмы, локальный отек (в острую фазу инфаркта), пристеночные тромбы;
- Радионуклидный метод – позволяет выявить аневризму по богатому накоплению радионуклидного препарата.
У части пациентов при отсутствии жалоб определяется относительно благоприятный прогноз. Такие больные проходят динамическое наблюдение и лечатся по поводу сопутствующих заболеваний.
В остальных ситуациях лечение хирургическое. Показания:
- Перенесенное аорто-коронарное шунтирование;
- Аритмия;
- Снижение сократительной функции сердца;
- Сердечная недостаточность;
- Угроза разрыва по рубцу;
- Болевой синдром;
- Снижение фракции выброса;
- Риск развития тампонады.
Выполняемое вмешательство носит название «хирургическое ремоделирование миокарда» и представляет собой восстановление анатомической целостности левожелудочковой камеры. Все варианты операции проводятся при кардиоплегии (отключении сердца из системного кровотока).
- После общего обезболивания проводится срединный разрез на уровне грудины (срединная стернотомия).
- Вскрывается грудная полость, затем — перикард.
- Левый желудочек осматривается, после чего выполняется вертикальный разрез.
- Рубцовую ткань аневризмы подвергают тщательному осмотру.
- Обнаруженные тромботические массы удаляют вместе с рубцом.
- Стенки вскрытого желудочка ушивают двумя слоями швов.
- Операция дополняется пластикой двустворчатого клапана и венечных артерий.
- Вмешательство заканчивается наложением швов, а также сопоставлением краев грудины.
- Линейная пластика (Cooley). Представляет собой восстановление анатомической структуры стенки двухрядным линейным швом. После удаления тромботических масс аневризму иссекают, не доходя до границ здоровой ткани 2.5-3 см. Герметизации полости сердца добиваются линейным обвивным швом.
- Кисетная пластика (Jatene). При поражении исключительно верхушки применяется кисетный способ. Аневризма удаляется. По краю полученного кругового отверстия прошивается круговой шов, который затягивают по типу тканного мешочка. Поверх него накладывается еще один шов (двухрядный) для профилактики послеоперационных расхождений.
- Циркулярная пластика заплатой (Cooley). Используется при поражении задней и нижней стенок. Рубцовую ткань удаляют, не доходя до зоны здорового миокарда 9-10 мм. На получившееся отверстие накладывают заплату из инертного безопасного материала и подшивают ее к стенкам отверстия. Поверх циркулярного шва накладывают обвивной.
- Эндовентрикулярная пластика заплатой (Dor). Используется при обширной области поражения. Рубцовую ткань удаляют на всем протяжении, после чего получившееся отверстие затягивают круговым швом. Со стороны полости (изнутри) обвивным швом подшивают заплату из перикарда или синтетического материала. Над заплатой дополнительно проводят однорядный шов, защищающий от послеоперационного разрыва.
В исключительных случаях вышеперечисленные операции еще больше нарушают анатомию сердца. Тогда им предпочитают менее радикальные вмешательства:
- Использование шаблонного баллона для восстановления полости левого желудочка;
- Применение удлиненной и суженной заплаты;
- Укорочение миокарда позади сосочковых мышц.
Операция проходит успешно в 77-80% случаев. Пятилетняя выживаемость больных составляет 60-70%, десятилетняя – 55%. Повторное образование аневризмы не наблюдается.
Качество жизни снижается ввиду низкой толерантности к физическим нагрузкам, однако при постоянном самоконтроле и диспансеризации функции сердца у части больных улучшаются.
Аневризмы левого желудочка представляют собой группу патологических образований, которые различаются по времени и причинам возникновения. Патология наиболее характерна для лиц пожилого возраста, перенесших крупноочаговый инфаркт.
Несвоевременная диагностика заболевания может привести к фибрилляции желудочков и летальным осложнениям. В большинстве случаев рекомендовано оперативное лечение; его результаты и прогноз определяются возрастом больного, типом хирургического вмешательства и сопутствующими заболеваниями.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Патологии сердца, являющегося своеобразным двигателем всего организма, врачи не зря относят к категории наиболее опасных для жизни человека. Считавшиеся ранее болезнями пожилых людей, они имеют малоприятную тенденцию к снижению возраста пациентов. Некоторые патологии с довольно большим процентом летальных исходов, такие как аневризма сердца, могут развиваться как у взрослых людей, так и у новорожденных. А это уже сигнал к тому, чтобы узнать о данной патологии как можно больше, чтобы по возможности предупредить ее развитие.

Статистика утверждает, что заболеванию в большей степени подвержены мужчины после 40 лет. Тем не менее, от патологии не застрахован никто, даже маленькие детки, у которых аневризма сердца может быть врожденной.
В подавляющем большинстве случаев аневризму диагностируют в области передне-боковой стенки и верхушки левого желудочка сердца. Аневризма правого желудочка, правого предсердия, задней стенки левого желудочка, межжелудочковой перегородки и аорты сердца считаются более редким диагнозом.
Самой частой и опасной причиной развития слабости сердечной мышцы является перенесенный в прошлом инфаркт миокарда (по разным сведениям от 90 до 95% всех случаев болезни). Именно с ним связаны от 5 до 15% случаев аневризмы левого желудочка сердца. Если брать общее число случаев межжелудочковой аневризмы и патологии левого желудочка, то они составляют порядка 15-25% от всего числа пациентов.

В большинстве случаев аневризма сердца развивается в течение трех месяцев после перенесенного инфаркта миокарда, однако этот период может растянуться и до полугода. Поскольку вероятность инфаркта наиболее высока в области левого желудочка и перегородки, отделяющей левый желудочек от правого, то и аневризма в большинстве случаев образуется именно там.
Аневризма сердца в этой ситуации развивается вследствие деформирования при инфаркте миокарда участка сердечной мышцы левого желудочка и происходящего в ней в дальнейшем процесса некротизации тканей. Такой вид аневризмы врачи называют аневризмой левого желудочка сердца. Если же наблюдается выпячивание перегородки между желудочками, то речь идет об аневризме межжелудочковой перегородки сердца.
Но инфаркт миокарда не является единственной причиной появления ослабленных участков мышечной ткани в сердце. Такому положению дел могут содействовать и другие причины, способные повлиять на работоспособность сердца и развитие в нем аневризмы.
К таким причинам относятся:
- патология, которая сама по себе развивается вследствие гипоксии миокарда, и называется ишемической болезнью сердца,
- заболевание воспалительного характера, затрагивающее миокард, которое имеет чаще всего вирусную или инфекционную этиологию (миокардит).
- патология, связанная с устойчиво повышенным артериальным давлением, именуемая в медицинских кругах артериальной гипертензией,
- травмы сердечной мышцы (последствия аварий, падения с высоты, ударов острыми предметами и т.д.), а также ранения в сердце, полученные во время выполнения боевых действий или в мирное время. Здесь речь идет о посттравматической аневризме, при которой интервал между травматическим событием и началом болезни может составлять даже порядка 10-20 лет.
Спровоцировать развитие аневризмы сердца могут также чрезмерные физические нагрузки в течение пары месяцев после инфаркта. По этой причине людям, перенесшим инфаркт врачи рекомендуют воздержаться от активных занятий спортом или выполнения тяжелой физической работы по дому или на производстве.

Факторами риска развития аневризмы различных участков сердца можно считать:
- Различные инфекционные патологии, приводящие к деформации сосудистых стенок и нарушению тока крови в них, например:
- венерические заболевания (преимущественно сифилис), нарушающие работу и целостность множества систем организма,
- воспалительные процессы, охватывающие эндокард сердца, и негативно влияющие на способность мышц активно сокращаться (эндокардит),
- тяжелая инфекционная болезнь под названием туберкулез, вызывающая осложнения на различные органы и системы организмы,
- ревматическая болезнь.
- Вредные привычки, такие как табакокурение и злоупотребление спиртными напитками, которые отрицательно воздействуют на всю сердечно-сосудистую систему.
- Операции на сердце и их последствия (например, послеоперационные осложнения, вызванные использованием некачественных материалов, низкой квалификацией хирурга или особенностями организма больного, которые не были в свое время учтены врачом, развитие тахикардии или повышение давления крови в желудочке в послеоперационном периоде и т.д.).
- Отрицательное воздействие на миокард некоторых веществ, вызывающих его интоксикацию и воспалительные процессы в мышце (в таком случае речь идет о токсическом миокардите). Такое случается, если человек чрезмерно увлекается спиртным, при избытке тиреоидных гормонов, при патологиях почек и подагре, характеризующихся повышением в крови пациента уровня мочевой кислоты, при попадании в организм веществ, которые плохи ним переносятся (лекарства, вакцины, яды насекомых и т.д.).
- Системные болезни, при которых в организме пациента начинают вырабатываться антитела к «чужеродным» клеткам сердечной мышцы. В таком случае причиной аневризмы сердца может стать красная волчанка или дерматомиозит.
- Кардиосклероз – болезнь, при которой происходит постепенное замещение мышечной ткани соединительной, уменьшающей резистентность сердечной стенки. Причины данной патологии так до конца и не изучены.
- Облучение органов грудной полости. Чаще всего происходит во время проведения лучевой терапии при опухолях с локализацией в области грудины.
Кроме прочего, аневризма сердца может носить и врожденный характер, с чем зачастую сталкиваются врачи, диагностируя данную патологию у детей. Здесь можно выделить 3 фактора, обуславливающих развитие данной болезни:
- Наследственный фактор. Болезнь может передаваться по наследству. Риск данной патологии значительно возрастает, если у родственников малыша была аневризма сердца или сосудов.
- Генетический фактор. Наличие хромосомных аномалий и связанных с ними качественных или количественных дефектов соединительной ткани. Например, при болезни Марфана имеет место системная недостаточность соединительной ткани в организме ребенка, прогрессирующая по мере взросления.
- Врожденные аномалии строения тканей сердца, например, частичная замена в миокарде мышечной ткани соединительной, неспособной удерживать давление крови. Такие нарушения строения сердца у ребенка зачастую связаны с проблематичным течением беременности у матери (курение, алкоголизм, прием запрещенных во время беременности лекарств, инфекционные болезни у беременной, такие как грипп, корь и др., воздействие радиации, вредные условия труда и пр.).

Чтобы понять, что такое аневризма сердца, нужно немного углубиться в анатомию и вспомнить, что же представляет собой человеческий мотор – сердце.
Итак, сердце — это ни что иное, как один из множества органов в нашем организме. Внутри он полый, а его стенки состоят из мышечной ткани. Сердечная стенка состоит из 3 слоев:
- эндокард (внутренний эпителиальный слой),
- миокард (средний мышечный слой),
- эпикард (наружный слой, представляющий собой соединительную ткань).
Внутри сердца имеется сплошная перегородка, которая делит его на две части: левую и правую. Каждая из частей в свою очередь разделена на предсердие и желудочек. Предсердие и желудочек каждой части сердца соединены между собой специальным отверстием с клапаном, открытым с сторону желудочков. Двухстворчатый клапан левой стороны принято называть митральным, а трехстворчатый с правой стороны – трикуспидальным.
Кровь из левого желудочка поступает в аорту, а из правого – в легочную артерию. Обратному току крови препятствуют полулунные клапаны.
Работа сердца заключается в постоянном ритмичном сокращении (систола) и расслаблении (диастола) миокарда, т.е. происходит попеременное сокращение предсердий и желудочков, проталкивающих кровь в коронарные артерии.
Все вышеописанное характерно для здорового органа. Но если под влиянием некоторых причин участок мышечной части сердца истончается, он становится не в силах сопротивляться давлению крови внутри органа. Утратив способность к сопротивлению (обычно вследствие недостаточного снабжения кислородом, снижения мышечного тонуса или нарушения целостности миокарда) такой участок начинает выделяться на фоне всего органа, выпячиваясь наружу и в некоторых случаях провисая в виде мешочка диаметром от 1 до 20 см. Такое состояние и называется аневризмой сердца.
Давление крови на стенки сердца остается равномерным и постоянным. Но здоровая часть мышечной стенки может его сдерживать, а ослабленная (деформированная) уже нет. Если нарушается работоспособность и резистентность перегородки, разделяющей желудочки или предсердия двух половинок сердца, она также может выпячиваться в правую сторону (поскольку физиологически обусловлено, что левый желудочек работает больше правого), но уже внутри органа.
Ишемизированая мышечная стенка утрачивает способность нормально сокращаться, оставаясь преимущественно в расслабленном состоянии, что не может не повлиять на ток крови и питание всего организма, а это в свою очередь приводит к появлению других опасных для здоровья и жизни симптомов.
Итак, мы разобрались, что же такое сердце и как возникает столь опасная сердечная патология как аневризма определенных участков сердца. И даже выяснили, что наиболее «популярной» причиной развития данного заболевания является другая опасная для жизни патология сердца – инфаркт миокарда, в результате которого на главной сердечной мышце образуются некротизированные области и рубцы, нарушающие снабжение мышцы кислородом и питательными веществами и снижающие ее резистентность.

То, что аневризма сердца может иметь различные размеры, локализацию и причины развития патологии, обуславливает значительные отличия в проявлении заболевания у разных людей. Тем не менее, для того, чтобы захватить болезнь в самом начале, не ожидая разрастания аневризмы до критических размеров (клинически значимым является снижение резистентности мышцы даже на небольшом участке в 1 см), нужно знать и обращать внимание хотя бы на те симптомы, которые свойственны любому из видов аневризмы сердца.
К первым признакам, по которым определяется аневризма сердца любой локализации, можно отнести:
- Боли в области сердца или чувство тяжести (давления) за грудиной слева. Боли носят приступообразный характер. Когда человек отдыхает и спокоен, боль утихает.
- Недомогание и слабость, ставшие следствием недопоставки кислорода нервно-мышечной системе. Это происходит из-за уменьшения объема перегоняемой крови вследствие недостаточной сократительной функции миокарда на участке аневризмы.
- Нарушения сердечного ритма, называемые аритмией, и ощущение сильного биения сердца, которое в нормальном состоянии человек не чувствует (по жалобам пациентов, сильно колотится сердце). Причиной такого состояния является недостаточная проводимость нервных импульсов в области аневризмы и большая нагрузка на больной орган. Аритмии усиливаются под воздействием стресса или больших физических нагрузок.
- Нарушения ритма дыхания, затрудненное дыхание или попросту одышка, которая при остром течении болезни может сопровождаться приступами сердечной астмы и отеком легких. Высокое давление внутри сердца постепенно передается сосудам, снабжающим кровью легкие. Вследствие этого нарушается обмен кислорода и человеку становится труднее дышать. Отсюда и сбитый дыхательный ритм.
- Бледный оттенок кожных покровов. Причиной опять же выступает нарушение поставки кислорода к тканям организма. В первую очередь ресурсы направляются к жизненно важным органам (головной мозг, сердце, почки), а кожа остается менее насыщенной кровью.
- Холодные конечности и быстрое их замерзание, связанное с нарушением кровообращения.
- Снижение чувствительности кожи, появление «мурашек».
- Сухой приступообразный кашель, не связанный с простудой или инфекцией. Его еще называют сердечным. Может быть следствием застойных явлений в легочных сосудах, так и появиться в результате сдавливания легкого аневризмой больших размеров.
- Усиление потоотделения.
- Вертиго, или, по-народному, головокружения, которые могут возникать с различной частотой.
- Отеки, которые можно наблюдать как на лице, так и на руках или ногах.
- Лихорадка в течение длительного времени (при острой аневризме).
- Сильное наполнение кровью вен в области шеи, вследствие чего они становятся более заметными.
- Сиплый голос.
- Скопление жидкости в брюшной или плевральной полости, увеличение печени, сухой перикардит, представляющий собой воспалительный процесс в сердечной сумке (перикарде), сопровождающийся фиброзными изменениями, нарушение проходимости различных кровеносных сосудов (можно обнаружить вовремя диагностических мероприятий при хронической аневризме).
На симптоматику аневризмы сердца могут накладываться различные проявления других имеющихся патологий сердечно-сосудистой и дыхательной систем, что заметно затрудняет диагностику заболевания. Да и сами симптомы в зависимости от размера аневризмы могут быть выражены в различной степени. При небольшой или врожденной аневризме сердца заболевание длительное время может вообще протекать без каких-либо подозрительных симптомов и напомнить о себе значительно позже.
Как уже упоминалось, самой распространенной формой патологии миокарда считается аневризма левого желудочка сердца. Именно этот участок нагружен работой более других. Испытывая наибольшую нагрузку, левый желудочек более склонен к повреждениям вследствие инфаркта миокарда. А следовательно и аневризму на нем обнаруживают чаще всего. Этому могут способствовать также травмы сердца или инфекционные патологии.
Во время диагностических мероприятий врач может наблюдать выпячивание стенки левого желудочка. Чаще всего местом расположения аневризмы левого желудочка сердца является передняя его стенка. Но нередки случаи болезни, где местом локализации аневризмы (выпячивания) становится верхушка сердца с левой стороны.
Такая патология не характерна для детей в силу отсутствия у данной категории пациентов причин, которые могут привести к развитию данной болезни.
Реже у пациентов встречается аневризма сосудов сердца. Это может быть как аневризма восходящей аорты сердца, так и выпячивание стенки синусов аорты.
В первом случае болезнь вызывают преимущественно воспалительные процессы, возникающие как следствие заболеваний инфекционной природы. Жалобы пациентов сводятся к ноющим болям в груди, одышке и отекам различной локализации вследствие сдавливания выпирающей стенкой аорты проходящей рядом полой вены.
Аневризму синусов аорты связывают с уменьшением просвета коронарных артерий, в результате чего под давлением крови ослабленная в силу некоторых причин стенка начинает провисать, оказывая давление на правую часть сердца. Благо, патологии сосудов сердца, связанные с ослаблением из стенок, встречаются нечасто.
Аневризма межжелудочковой перегородки встречается не так уж и часто, поскольку относится к числу врожденных болезней сердца. Правда, не во всех случаях она обнаруживается во время беременности или сразу после рождения ребенка. Бывает, что врожденное недоразвитие перегородки между желудочками сердца вызывает выпячивание аневризмы спустя некоторое время.
Чаще всего данная патология выявляется случайно, в частности при проведении эхокардиографии, ведь ей свойственно бессимптомное течение.
Аневризма может выбрать местом своей дислокации и другие области сердца (правый желудочек или предсердие, заднюю стенку левого желудочка), но такое случается довольно редко.

Как бы это странно не звучало, но болезни сердца свойственны не только пожилым и зрелым людям. Данными патологиями могут страдать также молодые люди, подростки и даже совсем маленькие детки.
Патологическое выпячивание участка сердечной мышцы у детей связывают с пороками развития одного или нескольких клапанов сердца, межжелудочковой или межпредсердной перегородки, в результате чего на этом месте образуется аневризма.
Такая редкая патология, как аневризма межпредсердной перегородки, которая может напомнить о себе даже во взрослом возрасте, возникает еще во внутриутробном периоде из-за недоразвития или изменения структуры перегородки сердца, разделяющей левое и правое предсердие. По аналогии образуется и аневризма межжелудочковой перегородки.
В детском возрасте эти виды болезней сердца встречаются довольно редко (не более 1 % от всех пациентов), тем не менее, они представляют большую опасность для жизни ребенка. Хорошо, если патология будет выявлена еще во время проведения УЗИ беременной женщины. Тогда ребенка после его рождения сразу же ставят на учет к кардиологу, и после того, как малышу исполнится годик, его начинают готовить к операции по удалению аневризмы.
Вероятность развития аневризмы сердца выше у детей, родившихся с малым весом, и недоношенных детей. Это связано с тем, что пороки сердца у этих категорий детей встречаются значительно чаще, и связанны они скорее с недоразвитием мышечной или сосудистой системы сердца.
Пока ребенок мал, врожденная аневризма сердца может себя никак не проявлять, но по мере взросления и увеличения двигательной активности, а значит и нагрузки на сердце, могут появляться следующие симптомы:
- разлитая боль в области грудной клетки,
- одышка и затрудненное дыхание после физических нагрузок,
- появление периодических болей в области сердца,
- беспричинный кашель без выделения мокроты,
- быстрая утомляемость, слабость и сонливость,
- срыгивание при кормлении (у грудничков), тошнота (у старших деток),
- головные боли при активном движении, головокружения,
- сильная потливость независимо от температуры воздуха.
Во время диагностики врачи определяют и такие проявления болезни, как
- ненормальная пульсация в области 3 ребра слева, при прослушивании напоминает звук качающихся волн,
- тромбы, придерживающиеся стенок крупных артерий сердца, возникающие из-за нарушения кровообращения,
- аритмии, как следствие занятий спортом и стрессов.
Особую опасность, как для взрослых, так и для детей представляет разрыв аневризмы сердца вследствие сильного истончения мышечных стенок. Именно поэтому детям с таким диагнозом врачи запрещают заниматься спортом, поскольку это связано со значительным увеличением нагрузки на сердечную мышцу. В дальнейшем пациентам советуют вести здоровый образ жизни, избегать стрессовых ситуаций и придерживаться рационального питания.

источник