Расслаивающая аневризма аорты – дефект внутренней оболочки аневризматически расширенной аорты, сопровождающийся образованием гематомы, продольно расслаивающей сосудистую стенку с формированием ложного канала. Расслаивающая аневризма аорты проявляется внезапной интенсивной болью, мигрирующей по ходу расслоения, подъемом артериального давления, признаками ишемии сердца, головного и спинного мозга, почек, внутреннего кровотечения. Диагноз расслоения сосудистой стенки основан на данных ЭхоКГ, КТ и МРТ грудной/брюшной аорты, аортографии. Лечение осложненной аневризмы включает интенсивную медикаментозную терапию, резекцию поврежденного участка аорты с последующей реконструктивной пластикой.
Расслаивающая аневризма аорты – продольное расслоение стенки аорты в дистальном или проксимальном направлении на различном протяжении, обусловленное разрывом ее внутренней оболочки и проникновением крови в толщу дегенеративно-измененного среднего слоя. Расширение аорты при расслаивании ее стенки может носить умеренный характер или отсутствовать, поэтому расслаивающую аневризму аорты часто называют расслоением аорты.
Большинство аневризм локализуются в наиболее гемодинамически уязвимых зонах аорты: около 70% — в восходящем отделе в нескольких сантиметрах от аортального клапана, 10% случаев – в дуге, 20% — в нисходящем отделе аорты дистальнее устья левой подключичной артерии. Расслаивающая аневризма в кардиологии относится к угрожающим жизни состояниям с риском массивного кровотечения при разрыве аорты или острой ишемии жизненно важных органов (сердца, мозга, почек и др.) при окклюзии магистральных артерий. Обычно расслоение аневризмы аорты возникает в возрасте 60-70 лет, у мужчин в 2-3 раза чаще, чем у женщин.
Причинами патологии являются заболевания и состояния, приводящие к дегенеративным изменениям мышечных и эластичных структур средней оболочки аорты (медиа). Пожилой возраст пациентов (старше 60-70 лет), травмы грудной клетки, III триместр беременности у женщин старше 40 лет считаются факторами риска расслоения аневризмы аорты. К основным причинам относятся:
- Стабильно повышенное АД. Основной риск расслоения аорты связан с длительной артериальной гипертензией (70-90% случаев), сопровождающейся гемодинамическим напряжением и хронической травматизацией аорты.
- Наследственные дефекты соединительной ткани. Расслаивающая аневризма может развиваться как осложнение синдромов Марфана, Тернера, Элерса-Данлоса.
- Болезни сердца и сосудов. В группе риска — пациенты с аортальными пороками, коарктацией аорты, выраженным атеросклерозом аорты, системными васкулитами.
- Перенесенные кардиохирургические операции и манипуляции. В ранний и поздний послеоперационный период после хирургических вмешательств на сердце и аорте (протезирования аортального клапана, резекции аорты) существует повышенный риск расслаивания аневризм. Ятрогенные расслаивающие аневризмы связаны с техническими погрешностями при выполнении аортографии и баллонной дилатации, канюляции аорты для обеспечения искусственного кровообращения.
Первичным патогенетическим звеном в большинстве случаев является надрыв интимы с последующим образованием внутристеночной гематомы. Примерно в 10% случаев расслаивающую аневризму аорты может инициировать кровоизлияние в медиа при спонтанном разрыве капилляров, разветвляющихся в стенке аорты. Распространение интрамуральной гематомы в пределах медиа обычно сопровождается последующим разрывом интимы, но может происходить без него (в 3-13% случаев). В редких случаях расслоение аорты может наблюдаться при пенетрации атеросклеротической язвы.
Согласно классификации ДеБейки, определяют 3 типа расслоения:
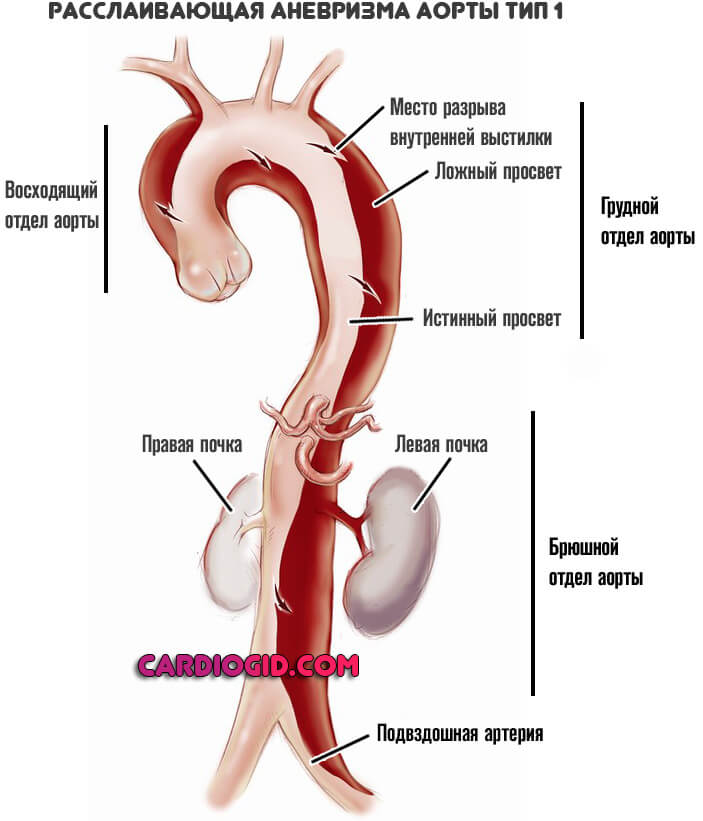
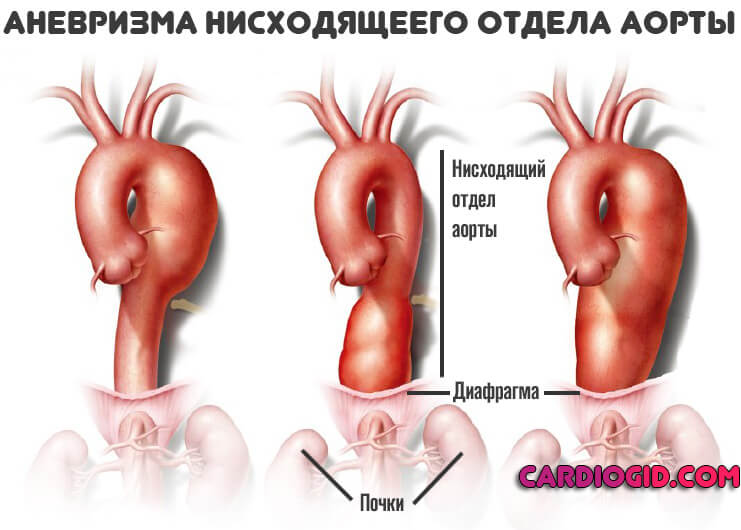
- I – надрыв интимы в восходящем сегменте аорты, расслоение распространяется до грудного и брюшного отделов;
- II – место надрыва и расслоение ограничено восходящим отделом аорты,
- III – надрыв интимы в нисходящей аорте, расслоение может распространяться до дистальных отделов брюшной аорты, иногда ретроградно на дугу и восходящую часть.
Стэнфордская классификация выделяет расслаивающие аневризмы аорты типа A — с проксимальным расслоением, затрагивающим ее восходящий отдел, и типа B — с дистальным расслоением дуги и нисходящей части аорты. Тип A характеризуется более высокой частотой развития ранних осложнений и высокой догоспитальной летальностью. По течению расслаивающие аневризмы аорты могут быть острыми (от нескольких часов до 1-2 дней), подострыми (от нескольких дней до 3-4 недель) и хроническими (несколько месяцев).
Клиническая картина заболевания обусловлена наличием и протяженностью расслоения аорты, внутристеночной гематомой, сдавлением и окклюзией ветвей аорты, ишемией жизненно важных органов. Различают несколько вариантов развития расслаивающей аневризмы аорты: образование обширной непрорвавшейся гематомы; расслоение стенки и прорыв гематомы в просвет аорты; расслоение стенки и прорыв гематомы в окружающие аорту ткани; разрыв аорты без расслоения стенки.
Для расслаивающей аневризмы аорты характерно внезапное начало с имитацией симптомов различных сердечно-сосудистых, неврологических, урологических заболеваний. Расслоение аорты проявляется резким нарастанием раздирающей, нестерпимой боли с широкой областью иррадиации (за грудиной, между лопатками и по ходу позвоночника, в эпигастральной области, пояснице), мигрирующей по ходу расслоения. Отмечается повышение артериального давления с последующим спадом, асимметрия пульса на верхних и нижних конечностях, обильное потоотделение, слабость, синюшность, двигательное беспокойство. Большая часть больных с расслаивающей аневризмой аорты умирает от развития осложнений.
Неврологическими проявлениями патологии могут служить ишемическое поражение головного или спинного мозга (гемипарез, параплегия), периферическая нейропатия, нарушения сознания (обморок, кома). Расслаивающая аневризма восходящей аорты может сопровождаться ишемией миокарда, сдавлением органов средостения (появлением охриплости, дисфагии, одышки, синдрома Горнера, синдрома верхней полой вены), развитием острой аортальной регургитации, гемоперикарда, тампонады сердца. Расслоение стенок нисходящей грудной и брюшной части аорты выражается развитием тяжелой вазоренальной гипертензии и острой почечной недостаточности, острой ишемии органов пищеварения, мезентериальной ишемии, острой ишемии нижних конечностей.
При подозрении на расслаивающую аневризму аорты необходима срочная и точная оценка состояния больного. Основными методами диагностики, позволяющими визуализировать поражение аорты, являются рентгенография грудной клетки, ЭхоКГ (трансторакальная и чреспищеводная), УЗДГ, МРТ и КТ грудной/брюшной аорты, аортография.
- Рентгенография грудной клетки. Выявляет признаки спонтанного расслоения аорты: расширение аорты и верхнего средостения (в 90% случаев), деформацию тени контуров аорты или средостения, наличие плеврального выпота (чаще слева), снижение или отсутствие пульсации расширенной аорты.
- ЭхоКГ. Трансторакальная или чреспищеводная эхокардиография помогают определить состояние грудной аорты, выявить отслоившийся лоскут интимы, истинный и ложный каналы, оценить состоятельность аортального клапана, распространенность атеросклеротического поражения аорты.
- Томография. Выполнение КТ и МРТ при расслаивающей аневризме аорты требует стабильного состояния больного для транспортировки и проведения процедуры. КТ применяют для обнаружения интрамуральной гематомы, пенетрации атеросклеротических язв грудного отдела аорты. МРТ позволяет без использования внутривенного введения контрастного вещества точно определить локализацию разрыва интимы, направление расслоения по направлению кровотока в ложном канале, оценить вовлеченность основных ветвей аорты, состояние аортального клапана.
- Аортография. Является инвазивным, но высокочувствительным методом исследования расслаивающей аневризмы аорты; позволяет увидеть место начального надрыва, локализацию и протяженность расслоения, истинный и ложный просветы, наличие проксимальной и дистальной фенестрации, степень состоятельности аортального клапана и коронарных артерий, целостность ветвей аорты.
Необходимо проводить дифференциальную диагностику расслаивающей аневризмы аорты с острым инфарктом миокарда, окклюзией мезентеральных сосудов, почечной коликой, инфарктом почки, тромбоэмболией бифуркации аорты, острой аортальной недостаточностью без расслоения аорты, нерасслаивающей аневризмой грудной или брюшной аорты, инсультом, опухолью средостения.
Больных с осложненной аневризмой аорты экстренно госпитализируют в отделение кардиохирургии. Консервативная терапия показана при любых формах заболевания на начальном этапе лечения с целью остановки прогрессирования расслоения сосудистой стенки, стабилизации состояния больного. Проводится:
- Интенсивная терапия. Направлена на купирование болевого синдрома (путем введения ненаркотических и наркотических анальгетиков), выведение из шокового состояния, снижение артериального давления. Проводится мониторинг гемодинамики, сердечного ритма, диуреза, ЦВД, давления в легочной артерии. При клинически значимой гипотонии важно быстрое восстановление ОЦК за счет внутривенной инфузии растворов.
- Медикаментозное лечение. Является основным у большинства больных с неосложненными расслаивающими аневризмами типа B (с дистальным расслоением), при стабильном изолированном расслоении дуги аорты и стабильном неосложненном хроническом расслоении. При неэффективности проводимой терапии, прогрессировании расслоения и развитии осложнений, а также больным с острым проксимальным расслоением стенки аорты (типа A) сразу же после стабилизации состояния показано экстренное оперативное вмешательство.
- Оперативное лечение. При расслаивающей аневризме аорты выполняют резекцию поврежденного участка аорты с надрывом, удаление интимального лоскута, ликвидацию ложного просвета и восстановление иссеченного фрагмента аорты (иногда одномоментную реконструкцию нескольких ветвей аорты) методом протезирования или сближения концов. В большинстве случаев операция выполняется в условиях искусственного кровообращения. По показаниям осуществляют вальвулопластику или протезирование аортального клапана, реимплантацию коронарных артерий.
При отсутствии лечения расслаивающей аневризмы аорты летальность высокая, в течение первых 3 месяцев может достигать 90%. Послеоперационная выживаемость при расслоении типа A составляет 80%, типа B – 90%. Долгосрочный прогноз в целом благоприятный: десятилетняя выживаемость составляет 60%. Профилактика формирования расслаивающей аневризмы аорты заключается в контроле за течением сердечно-сосудистых заболеваний. Предупреждение расслоения аорты включает наблюдение кардиолога, мониторинг артериального давления и уровня холестерина крови, периодическое УЗДГ или УЗДС аорты.
источник
А натомические дефекты сосудистых структур представляют колоссальную опасность для здоровья и жизни пациента. Включают в себя гетерогенную группу патологических процессов.
Проблема в том, что в большинстве своем указанные расстройства имеют латентное, вялое течение и не отличаются симптомами.
До определенного момента невозможно обнаружить проблему, если обращать внимание только на субъективные ощущения. Требуется качественная инструментальная диагностика.
Расслаивающая аневризма аорты — это нарушение целостности отдельных внутренних слоев сосуда, а затем тотальную деструкцию выстилки с развитием массивного кровотечения и гибелью больного в считанные секунды.
Частота или встречаемость процесса минимальна, в практике обнаруживается не более 1% пациентов с подобным страшным диагнозом.
Общая летальность близится к 40% даже при раннем выявлении патологии. Что связано с некоторыми трудностями оперативной коррекции (например, неудачная локализация дефекта или же множественное вовлечение участков).
Расслаивающаяся аневризма аорты имеет сложное происхождение. Речь не об одном факторе, а о целой группе нарушений органического плана.
Крайне редко это первичная патология. Много чаще говорят о вторичном типе, то есть таком, который обусловлен сторонними заболеваниями. Всего выделяют три механизма развития указанной проблемы.
Первый касается роста давления в системе. Изменение показателей АД вызывает стремительное изнашивание сосудов, снижается качество кровотока, начинаются дистрофические процессы.
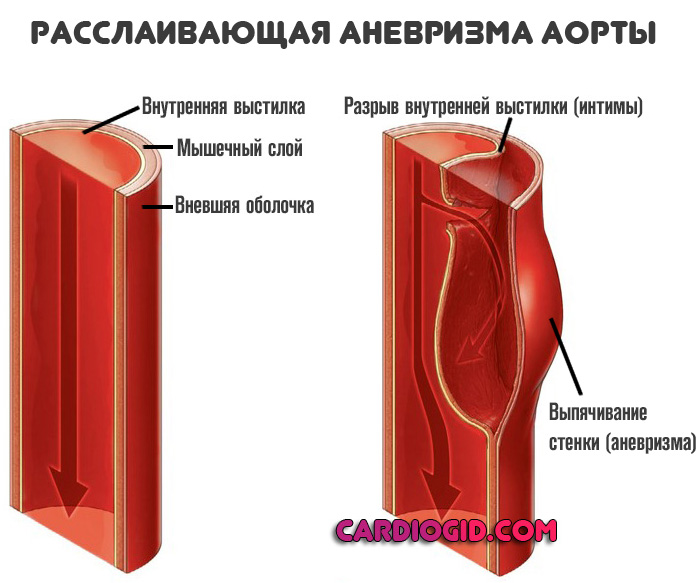
Внутренняя выстилка и мышечный слой аорты истончаются, наружная оболочка не приспособлена для противодействия большим нагрузкам.
Второй весомый механизм — атеросклероз. Как правило, самостоятельного значения не имеет и идет в комплексе с ростом артериального давления, что объяснимо.
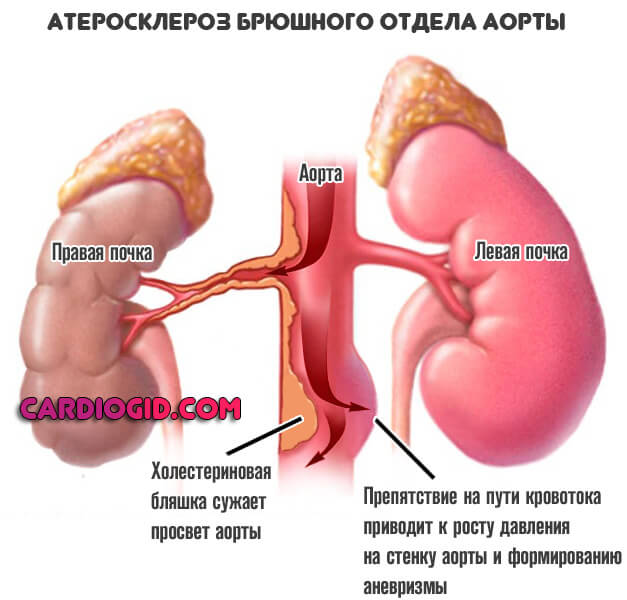
Закупорка просвета аорты холестериновой бляшкой или же стеноз (сужение) крупнейшей артерии приводит к невозможности нормального тока крови.
Организм отвечает на подобные препятствия усилением сердечной деятельности и ростом давления. Что и приводит уже по понятным причинам к дистрофии сосуда, деструкции стенок и повышает вероятность стеночного выпячивания.
Третий механизм имеет аутоиммунное происхождение. Возможны воспалительные процессы во внутреннем слое аорты, прямая деструкция стенок. Также встречается рубцевание просвета, образование фибриновых тяжей, препятствующих нормальному кровотоку.
Далее процесс идет по идентичной схеме. Рост давления в системе приводит к дистрофии (истончению стенки). Сосуд становится податливым, аномально пластичным.
Мышечный слой оказывается не способен поддерживать аорту в стабильном состоянии, противодействовать негативным факторам.
Потому происходит продавливание сосуда в одну из сторон или сразу по всему диаметру с развитием мешковидного или диффузного (веретенообразного) дефекта.
Уже на этом этапе возможен разрыв аневризмы и смерть от массивного кровотечения. Второй вариант — дальнейшая деструкция стенок.
Сначала жидкая соединительная ткань разрушает интиму (внутреннюю выстилку), затем просачивается в мышечный слой, потом в область наружной оболочки, пока не спровоцирует нарушения целостности и массивного кровотечения.
Полный «цикл» развития патологии, от старта до летального исхода составляет от 1 недели до 2 месяцев.
Известны случаи полугодового выживания, но это редкость и конец все равно идентичен. Без лечения спонтанного регресса не происходит, летального результата не избежать.
Как таковая типизация рассматриваемого дефекта не разработана, что связано с довольно малой распространенностью расслаивающей аневризмы аорты.
Основная классификация нарушения по локализации проводится по Де Бейки. Согласно ей выделяют три места расслоения:
- Первый тип. Порок расположен в восходящей части сосуда, может диффузно, экспансивно охватывать сразу группу участков (грудной и брюшной). Представляет собой наиболее встречаемый тип. При массивном поражении прогноз изначально хуже, потому как возрастает сложность предполагаемой операции.
- Второй тип. Отклонение локализуется строго изолированно, в восходящей части аорты. Также представляет трудности для хирурга, открытый доступ проблематичен, потому как мобилизовать сосуд непросто, слишком много тканей.
- Третий тип. Поражает нисходящий отдел аорты и брюшную часть включительно.
Существует упрощенная Стенфордская классификация. Согласно ей выделяют расслоение аневризмы, берущее начало в восходящем отделе аорты — тип (а) и в нисходящей части, тип (б).
Возможно подразделение расстройства также по симптомам (острое, хроническое), течению, размерам выпячивания (крайне запутанный критерий).
Универсальных методов подразделения нет. Врачей в первую очередь интересует диаметр патологического образования, скорость его прогрессирования и локализация.
Выяснение деталей позволяет снизить риски для пациента благодаря четкой, тщательной проработки оперативной стратегии.
Возможны два варианта течения расслаивающей аневризмы. Первый — острое. Представлено генерализовнанными признаками. Полная клиническая картина развивается в считанные секунды, отличается высокой тяжестью.
Продолжительность эпизода составляет несколько минут и менее, после чего наступает потеря сознания и гибель от массивного внутреннего кровотечения.
- Сильная, невыносимая боль. Располагается в области брюшины, спину, в грудной клетке. Зависит от локализации патологического процесса и его типа. Возникает внезапно, не купируется ничем. Вынуждает пациента принять положение лежа и не двигаться. Или же сесть.
- Потливость, бледность кожных покровов, выраженная одышка, слабость, тошнота, цианоз носогубного треугольника, спутанность сознания, предобморочное состояние. Так называемая коллаптоидная реакция. Объективно сопровождается падением уровня артериального давления.
- До становления описанного состояния возникает стремительный рост АД, на короткий промежуток времени.
Это типичные проявления. Прочие симптомы расслаивающей аневризмы аорты представлены ситуативными моментами, которые встречаются не у всех и не в каждом случае. Вероятность определяется в 1-15%.
- Боли в ногах, ощущение бегания мурашек, невозможность устоять, ходить.
- Почечная дисфункция. Сопровождается коликами в пояснице, задержкой мочи.
- Метеоризм, дискомфорт в животе. Причина кроется в нарушении соответствующего кровотока.
- Слабость мышц. Парезы, параличи. При снижении трофики нервных тканей спинного мозга.
- Боли в грудной клетке, отклонения ритма от нормального (по типу ускорения или урежения ЧСС), выраженная одышка.
- Потеря сознания. Сильная головная боль. При вовлечении в патологический процесс мозга, церебральных структур.
Расслаивающая аневризма грудного отдела аорты представлена наиболее полной клинической картиной.
Хроническая форма встречается примерно в 60% случаев. В то время как на долю острой приходится 20%. Остальные 20% определяются промежуточным типом.
- Боли в животе, запоры, диспепсические явления, артериальная гипертензия, которая не снимается препаратами и никак не реагирует на терапию. Встречается при поражении соответствующего одноименного отдела аорты.
- Дисфагия (невозможность глотать), нарушения голоса, процесса говорения, дыхания. По причине компрессии нервных тканей и самих систем, расположенных в грудной клетке. При значительных размерах аневризмы или же отклонения гемодинамики.
- Болевой синдром. Расположен в проекции сердца. Напоминает стенокардические или таковые при инфаркте. Однако это ложное впечатление.
- Отеки. В основном периферические. Страдают нижние и верхние конечности. Лицо.
- Посинение дермальных слоев. Возникает при компрессии вен, сопровождается ростом давления, одышкой.
- Нарушения зрения по типу потемнения, тумана в поле видимости.
- Наконец, обнаруживаются обмороки. Частые, пациента трудно вывести из подобного состояния.
Симптомы расслоения аневризмы, многообразны, но без должной подготовки и даже с таковой, но вне инструментальной диагностики определить, что стало причиной расстройства невозможно.
В некоторых клинических случаях, особенно сложных, патологический процесс маскируется столь хорошо, что даже по окончании обследования сказать что-либо конкретное не представляется возможным.
В основе развития расслаивающей аневризмы лежат врожденные и приобретенные патологии (соотношение — 30% против 70%).
Первые представлены соединительнотканными дефектами (синдром Морфана и прочие), анатомическими изменениями по типу стеноза аортального клапана, иных явлений. Они не обязательно провоцируют именно рассматриваемое расстройство. Вариантов множество.
Вторая группа отклонений многочисленна. Если ранжировать заболевания по встречаемости, обнаружится такая картина:
- Атеросклероз и гипертония. Также симптоматическое, стабильное повышение уровня давления в кровеносном русле. В сочетании они особенно опасны.
- Ятрогенный фактор. То есть врачебное вмешательство лечебного или диагностического плана. В основном — катетеризация аорты. Реже открытые или эндоваскулярные операции.
- Васкулиты вирусного, грибкового, бактериального, аутоиммунного (неинфекционного) рода. Сопровождаются воспалением сосудистых стенок, их деструкцией, рубцеванием.
- Перенесенные травмы грудной клетки. Особенно, если была вовлечена аорта.
Эндокринные факторы встречаются, но много реже. Обычно расслаивающая аневризма манифестирует в период беременности, на ранних сроках или в 3-й триместр. Настораживающим признаком оказывается тяжелый токсикоз.
В остальных случаях, если нет возможности определиться с фактором развития отклонения, говорят об идиопатической форме расстройства.
Выявить причину необходимо. Потому как даже после успешного хирургического вмешательства, полного восстановления, при самом благоприятном исходе ни один врач не даст гарантии отсутствии рецидива в будущем. Ведь патогенный фактор никуда не девается.
Среди редко встречающихся причин называют и сторонние инфекционные заболевания. Возможна транспортировка агентов в аорту, развитие воспаления и деструкции стенок.
Генетические врожденные синдромы генерализованного плана (например, Дауна) могут проявляться тем же неочевидным на первый взгляд образом.
Есть и предрасполагающие моменты, которые увеличивают риски развития расстройства: принадлежность к мужскому полу ( представители сильной половины человечества страдают рассматриваемым дефектом втрое чаще ), возраст от 55 лет и свыше (в связи с естественными процессами старения и воздействием накопленного груза заболеваний).
Выявление патологии ложится на плечи сосудистого хирурга. В основном. К кардиологу обратиться также можно, однако, это не профильный специалист. Обследование проводится в срочном порядке, времени на раздумья нет.
Примерный список мероприятий:
- Устный опрос больного. Направлен на выявление симптомов, выстраивание понятной клинической картины. Представляет собой основу.
- Сбор анамнеза. Перенесенные заболевания, образ жизни, семейная история (некоторые расстройства, особенно сопряженные с дефектами соединительной ткани передаются по наследству и повышают риски).
- Выслушивание сердечного звука. Аускультация. В 80% случаев обнаруживается синусовый шум над участочком локализации аневризмы.
- Рентгенография грудной клетке. Морально устаревшее исследование, дает минимум информации, но в рамках диагностики запущенных форм патологического процесса может оказаться полезным.
- Эхокардиография. УЗИ сердца и окружающих структур. Используется для визуализации грудного отдела аорты.
- Ультрасонография. Основная методика диагностики. Позволяет выявить дефект любой части крупнейшей артерии.
- МРТ-ангиография. Для визуализации тканей. Использовать контраст не имеет смысла, потому как кровь сама по себе хорошо усиливает рисунок. Компьютерная методика (КТ) применяется реже, она более предпочтительна в деле оценки состояния костных тканей.
После проведения тщательного обследования нужно начинать восстановление. Времени обычно не много.
Терапия строго хирургическая. Смысла в консервативных способах нет. Они не возымеют эффекта, зато время будет безвозвратно утрачено, а значит и шансы пациента на выживание и полное восстановление снизятся.
Открытым доступом. Суть заключается в иссечении аномальной, измененной области и ее ушивании. При необходимости проводится протезирование, либо эндоваскулярное вмешательство.
Хирургическое вмешательство представляет трудности, требует высокой квалификации врача. Порой дело осложняется «неудачной» локализацией дефекта.
Обязательное условие — лечение патологии, которая стала причиной расслаивающей аневризмы. Если речь о гипертонии — показаны специализированные средства (ингибиторы АПФ, бета-блокаторы, диуретики, лекарства центрального действия, антагонисты кальция).
При врожденных или приобретенных пороках проводится еще одна операция. Параллельно, как правило, несколько вмешательство не назначается, вопрос решается на усмотрение доктора.
Атеросклероз требует приема статинов, медикаментов, для растворения бляшек и выведения избытков холестерина.
Необходимо скорректировать образ жизни:
- Отказаться от курения, спиртного, психостимуляторов (наркотики), самовольного приема любых препаратов.
- Правильное питание (меньше животных жиров и соль до 7 граммов в сутки).
- Полноценный сон (не менее 7 часов за ночь).
- Адекватная, посильная физическая активность (оптимум — плавание или же прогулки неспешным шагом на свежем воздухе).
Соблюдение всех рекомендаций специалиста позволяет добиться максимального эффекта.
Лечение аневризмы проводится оперативными методами. Прочих вариантов не существует, потому терять время, надеяться на спонтанное самовосстановление не нужно.
Зависит от этапа, локализации дефекта, общего состояния здоровья пациента, первопричины аномалии и прочих факторов.
При раннем обнаружении и возможности «удобного» доступа к пороку — благоприятный. В остальных ситуациях — спорный.
Однозначно негативный только при разрыве образования. Шансы есть всегда. Опускать руки не стоит.
Общая летальность патологического процесса составляет порядка 40%, плюс-минус несколько процентов.
Без лечения смерть наступает в перспективе недели, максимум месяца. В исключительных ситуациях — полугода. Но это, скорее, казуистика, единичные случаи.
Основное и самое угрожающее последствие — разрыв аневризмы. С массивным кровотечением, гибелью человека. Тот же эффект наблюдается при прогрессирующем расслоении аорты в области мешотчатого или диффузного образования. Исход всегда один и тот же.
В процессе развития самого заболевания возможны грозные осложнения, спровоцированные сторонними явлениями.
Например, асфиксия вследствие компрессии дыхательных структур, инсульт, инфаркт на фоне недостаточного кровообращения в указанных тканях.
Расслаивающая аневризма аорты — смешанный патологический процесс. Сопровождается аномальным изменением крупнейшей артерии, деструкцией стенок.
Заканчивается смертью без лечения всегда . Единственный шанс на восстановление — своевременно провести операцию. Прогноз в такой ситуации благоприятный.
источник
Аорта — это самый крупный, мощный кровеносный сосуд человеческого тела. Мощный, посему, казалось, его ничего «не берет». Тем не менее, аневризма аорты — бич современной кардиоваскулярной хирургии. В нормальном состоянии у взрослых женщин и мужчин диаметр просвета восходящей части аорты составляет около 3 см, нисходящей — 2,5 см, брюшного сегмента этого крупного сосуда еще меньше — 2 см. Диагноз аневризмы оглашают только в том случае, если диаметр пораженной аорты увеличивается в 2 и больше раза в сравнении с нормой.
Аневризма — это аномальная выпуклость, возникающая на стенках артерии. Стенки артерий достаточно толстые и прочные, мышечные волокна, из которых они состоят, позволяют выдерживать интенсивное давление крови. Однако при наличии слабого участка в стенке артерии давление вызывает распирание этого участка, таким образом формируется аневризма.
Аневризма аорты может развиваться в двух частях этой артерии:
- брюшная часть, проходящая через нижнюю часть брюшной полости — аневризма брюшной аорты;
- аневризма грудной аорты, развивающаяся в области грудной полости. Этот вид аневризмы встречается реже, однако оба вида одинаково опасны для здоровья и жизни человека.
В зависимости от внешнего вида аневризма может быть:
1. веретенообразной
2. мешковидной.
Небольшие аневризмы обычно не представляют никакой угрозы. Тем не менее, они способны увеличить риск: образования атеросклеротических бляшек в месте аневризмы, которые вызывают дальнейшее ослабление стенок артерии; образования и отрыва тромба, следовательно, повышения риска инсульта; увеличения размеров аневризмы, а значит, сжатия близлежащих органов, что вызывает болевые ощущения; разрыва аневризмы.
Основным осложнением аневризм любой локализации является их расслоение с последующим возможным разрывом (летальность — 90%).
Причины и факторы риска
Основными причинами аневризмы являются заболевания и состояния, способствующие снижению прочности и эластичности сосудистой стенки:
- атеросклероз стенки аорты (по различным данным, от 70 до 90%); воспаление аорты (аортит) сифилитического, гигантоклеточного, микотического характера;
- травматическое повреждение;
- врожденные системные заболевания соединительной ткани (например, синдром Марфана или Элерса — Данлоса);
- аутоиммунные заболевания (неспецифическийаортоартериит);
- ятрогенные причины, обусловленные лечебными манипуляциями (реконструктивные операции на аорте и ее ветвях, катетеризация сердца, аортография).
Факторы риска развития атеросклероза и образования аневризмы:
- мужской пол (частота встречаемости аневризм у мужчин в 2–14 раз выше, чем у женщин);
- курение (при скрининговой диагностике 455 человек в возрасте от 50 до 89 лет в отделении сосудистой хирургии Московского областного научно-исследовательского клинического института были выявлено, что 100% пациентов с аневризмами абдоминального отдела аорты имели стаж курения более 25 лет, а в результате Уайтхолльского исследования доказано, что жизнеугрожающие осложнения аневризм у курильщиков возникают в 4 раза чаще, чем у некурящих);
- возраст старше 55 лет;
- отягощенный семейный анамнез;
- длительная артериальная гипертензия (АД выше 140/90 мм рт. ст.);
- гиподинамия;
- избыточная масса тела;
- повышение уровня холестерина крови.
Также говорят о расслаивающей аневризме, формирующейся вследствие разрыва внутренней оболочки с последующим ее расслоением и образованием второго ложного канала для кровотока.
В зависимости от локализации и протяженности расслоения выделяют 3 типа патологии:
1. Расслоение начинается в восходящей части аорты, продвигается по дуге (50%).
2. Расслоение происходит только в восходящей части аорты (35%).
3. Расслоение начинается в нисходящей части аорты, продвигается вниз (чаще) или вверх (реже) по дуге (15%).
В зависимости от давности процесса расслаивающая аневризма может быть:
острой (1–2 дня от момента появления дефекта эндотелия);
подострой (2–4 недели);
хронической (4–8 недель и более, до нескольких лет).
СИМПТОМЫ АНЕВРИЗМЫ АОРТЫ
Аневризма аорты проявляется по-разному — главным образом это зависит от размеров аневризматического мешочка и его местонахождения (ниже — наглядная клиническая картина на примере аневризмы синуса Вальсальвы). В ряде случаев никаких симптомов не наблюдается вообще (в частности, до разрыва аневризмы, но это уже будет другой диагноз), что затрудняет заблаговременную диагностику.
Самые частые жалобы со стороны больных при аневризме восходящего фрагмента аорты:
боль в грудной клетке (в области сердца или за грудиной) — из-за того, что аневризматическое выпячивание надавливает на близко расположенные органы и ткани, а также из-за давления тока крови на истонченную и немощную стенку; одышка, усиливающаяся со временем; ощущение сердцебиения («Словно что-то колотится в груди» — комментарий пациентов); головокружение; при больших размерах аневризмы беспокоят атаки головных болей, отечность мягких тканей лица и верхней половины туловища — из-за развития так называемого синдрома верхней полой вены (потому как аневризма давит на верхнюю полую вену).
Для аневризмы дуги аорты характерны:
- затруднение глотания (из-за давления на пищевод);
- сиплость голоса, иногда покашливание — в случае, если аневризма давит на возвратный нерв, который «отвечает» за голос;
- внезапно увеличенное слюноотделение и редкий пульс — если давление распространяется на блуждающий нерв, контролирующий слюноотделение и частоту пульса;
- натужное дыхание, а позже и одышка в случае сдавливания трахеи и бронхов огромной аневризмой;
- односторонние пневмонии — если аневризма, давя на корень легкого, мешает его нормальной вентиляции, то, как следствие, возникает застой в легких, при присоединении инфекции перетекающий в воспаление легких.
При аневризме нисходящей части аорты появляются:
- боли в левой руке (иногда до самих пальцев) и лопатке;
- при давлении на межреберные артерии может развиться недостаточность кислородного питания спинного мозга, из-за этого неминуемы парезы и параличи;
- в случае постоянного длительного давления большой аневризмы на позвонки возможно даже их смещение;
- в более легких случаях из-за давления на межреберные нервы и артерии — боли, как при радикулите или невралгиях.
Самые частые жалобы при аневризме брюшного сегмента аорты:
- ощущение переполнения желудка и тяжести в эпигастрии (верхнем этаже живота), которое больной поначалу пытается объяснить перееданием или патологией желудка;
- отрыжка;
- в ряде случаев — рвота рефлекторного характера (появляется как реакция на давление аневризмы аорты на близко расположенные органы и ткани);
- при пальпировании прощупывается напряженное, похожее на опухоль пульсирующее образование. Иногда больные самостоятельно могут выявить у себя эту пульсацию.
ДИАГНОСТИКА АНЕВРИЗМЫ АОРТЫ И ЕЕ УСЛОЖНЕНИЙ
Аневризма аорты в период до разрыва имеет довольно скудные клинические проявления: шумы, которые слышны при аускультации; врач выслушивает не только грудную клетку, но и брюшную полость; опухолевидное пульсирующее образование, которое находят при глубокой, но осторожной пальпации (иногда в самом деле расценивается как опухоль, так как довольно плотное на ощупь); непонятный дискомфорт в месте образования аневризматического выпячивания.
Поэтому для уточнения патологии, пока она не «разродилась» опасными усложнениями, применяют инструментальные методы диагностики: рентгеноскопия и рентгенография грудной клетки и брюшной полости — при них визуализируется опухолевидное образование (его пульсацию видно при рентгеноскопии); эхокардиография — при подозрении на аневризму восходящей аорты; ультразвуковая допплерография (УЗДГ) — при признаках аневризмы других участков аорты; КТ и МРТ.
ЛЕЧЕНИЕ И ОПЕРАЦИЯ ПРИ АНЕВРИЗМЕ АОРТЫ
Если поставлен диагноз аневризмы, но не наблюдается ее прогрессирования — врачи берут на вооружение консервативную тактику: дальнейшее внимательное наблюдение сосудистого хирурга и кардиолога — контролирование общего состояния, артериального давления, пульса, повторное выполнение электрокардиографии и других более информативных методов, чтобы уследить за возможным прогрессированием аневризмы и вовремя заметить предпосылки для осложнений аневризмы; гипотензивная терапия — для того, чтобы уменьшить давление крови на истонченную стенку аневризмы; антикоагулянтное лечение — чтобы профилактировать образование кровяных сгустков и возможной последующей тромбоэмболии средних и мелких сосудов; снижение количества холестерина в крови (с помощью как медикаментозной терапии, так и диеты). К хирургическому вмешательству прибегают в таких случаях: большие по размеру аневризмы (не менее 4 см в диаметре) или при быстром увеличении размеров (на полсантиметра за полгода); осложнения, которые угрожают жизни пациента — разрыв аневризмы и другие; осложнения, которые хоть и не критичны с точки зрения летального исхода, но резко понижают качество жизни больного — например, надавливание на близлежащие органы и ткани, что вызывает болевой синдром, чувство одышки, рвоту, отрыжку и тому подобные симптомы.
ПРОГНОЗ ПРИ АНЕВРИЗМЕ АОРТЫ
Аневризма аорты — нозология, которая должна постоянно находиться под усиленным контролем со стороны врачей. Причина — возможные осложнения, которые в большинстве случаев угрожают жизни человека. Со временем морфологически аневризма прогрессирует (измененная стенка становится все тоньше и тоньше, выпячивание увеличивается). Жизнь и здоровье больному можно сберечь только благодаря тщательнейшему наблюдению за течением болезни и в случае необходимости — безотлагательному оперативному вмешательству.
ПРОФИЛАКТИЧЕСКИЕ МЕРЫ
Профилактика, благодаря которой можно предупредить возникновение аневризмы аорты у здоровых людей, неспецифическая (то есть, действенны не только в случае этой патологии) и включает в себя: полный отказ от курения; снижение норм алкоголя до уровня «только на праздники», а лучше полный отказ; занятия физкультурой и спортом; устранение факторов, вызывающих подъем артериального давления (стрессы, заболевания почек); излечение и предупреждение патологии, которая способствует образованию аневризмы аорты (атеросклероз); моментальная настороженность при внезапном, на первый взгляд необъяснимом появлении перебоев в работе сердца, ЖКТ и дыхательной системы и незамедлительное обследование у профильных специалистов, чтобы исключить аневризму аорты; регулярные качественные, а не для «галочки», профосмотры у сосудистого хирурга и кардиолога. Если аневризма аорты уже имеется в наличии, профилактические мероприятия показаны для того, чтобы предупредить усложнения этого заболевания: грамотно подобранная антикоагулянтная терапия, чтобы предотвратить образование тромбов в просвете аневризмы; значительное снижение физнагрузок — иначе они могут вызвать перенапряжение истонченной стенки аневризмы, что обернется ее разрывом; иногда необходим полный отказ от физических нагрузок до того момента, пока врач уточнит диагноз и оценит риск; антигипертензивное лечение — благодаря ему удается избежать нарастания давления тока крови на истонченную стенку аневризмы, которая может разорваться в любой момент; тщательный психологический контроль — у некоторых пациентов к разрыву аневризмы аорты подталкивали даже незначительные стрессовые ситуации.
источник
Опубликовано в журнале:
Визуализация в клинике »» N13, Декабрь 1998 Ultrasound imaging in the diagnosis of aortic dissecting aneurism
О.Ю. Атьков, Д.М. Атауллаханова, В.Е. Синицын, С.К. Терновой, Т.В. Балахонова
Atkov O.Yu., Ataullakhanova D.M., Sinitsyn V.E., Ternovoy S.K., Balahonova T.V.
Институт клинической кардиологии им А.Л. Мясникова Российского кардиологического научно-производственного комплекса МЗ РФ, Москва
Cardiology Research Complex, Ministry of Health of the Russian Federation, Moscow
Анализируется случай расслаивающей аневризмы аорты. Ддя уточнения диагноза и определения начала и протяженности отслойки интимы использовался комплекс современных визуализирующих методов — трансторакальная и чреспищеводная ЭхоКГ, а также электронно-лучевая томография. Продемонстрирована высокая диагностическая значимость примененных методов.
Analyzed is the case of aortic dissecting aneurism. Improvement of the diagnosis and determination of the origin and expanse of intima detachment were performed with a set of present-day imaging techniques including transthoracic and transesophageal echocardiography and electron-beam CT. A high diagnostic virtue of these techniques was demonstrated. («Визуализация в клинике», 1998, 13: 51-54)
Ключевые слова: ультразвуковая диагностика, расслаивающая аневризма аорты, эхокардиография, чреспищеводная ЭхоКГ, электронно-лучевая томография.
Key words: ultrasound imaging, aortic dissection, echocardiography, transesophageal echocardiography, electron-beam CT.
Расслаивание аневризмы аорты — самое частое из неотложных состояний, связанных с заболеванием аорты, которое заканчивается летальным исходом у половины больных уже в первые 48 часов. Многообразие клинических проявлений расслаивания аневризмы аорты (РАА) ведет к диагностическим ошибкам. По данным большинства исследователей, правильный диагноз ставится лишь в 50% случаев. Уменьшение летальности в последнее десятилетие связано со значительным улучшением диагностики и совершенствованием хирургических методов лечения.
Различают три типа РАА по классификации De Bakey в зависимости от места расположения отслоившейся интимы [4]:
тип I — восходящая аорта, дуга и нисходящий отдел аорты,
тип II — восходящая аорта,
тип III — нисходящая аорта.
Золотым стандартом среди диагностических методов считался и все еще считается метод контрастной аортографии. В то же время это довольно дорогой инвазивный метод, опасный своими осложнениями. Именно поэтому клиницисты не всегда используют его при подозрении на РАА, особенно при отсутствии клинических проявлений или при атипичной симптоматике.
Этим объясняется большой интерес к разработке неинвазивных методов диагностики РАА. Весьма привлекательна и удобна для этой цели эхокардиография. По имеющимся в литературе сообщениям, трансторакальная эхокардиография (ТЭхоКГ) позволяет выявлять 80% РАА со специфичностью 95% [1]. В настоящее время особую роль в диагностике РАА отводят чреспищеводной эхокардиографии (ЧПЭхоКГ), которую считают одним из наиболее информативных и точных методов [2, 3]. Так, по данным многоцентрового исследования [5], охватывающего 164 пациента с предполагаемым РАА, диагностическая чувствительность и специфичность ЧПЭхоКГ составили соответственно 94% и 98%, что не уступает аналогичным показателям компьютерной томографии (83% и 100% соответственно) и аортографии (88% и 94% соответственно). Кроме того, метод ЧПЭхоКГ является относительно недорогим, полуинвазивным, не сопровождается облучением пациента и не требует введения контраста. ЧПЭхоКГ можно проводить непосредственно у постели больного, при необходимости даже интраоперационно, или осуществлять с ее помощью мониторирование хирургических операций, причем длительно. Возможно повторное наблюдение.
В данном сообщении мы описываем случай применения ультразвуковых методов для установления диагноза PAA и точной локализации места его расположения.
12 декабря 1997 г. у больного У., 40 лет, впервые в жизни без провоцирующих факторов развился интенсивный приступ болей за грудиной. Вызванная бригада скорой помощи на основании данных ЭКГ не выявила ишемических изменений в миокарде. От госпитализации больной отказался. Боль продолжалась четверо суток, В последующем с помощью ЭхоКГ была обнаружена аневризма восходящего отдела аорты. Боль в грудной клетке больше не возникала. Со слов больного, несколько лет назад он перенес травму грудной клетки (удар).
2 марта 1998 г. больной поступил в НИИ кардиологии им А.Л. Мясникова. При поступлении состояние больного было удовлетворительным, жалоб не предъявлял. Аускультативно над всей поверхностью сердца выслушивался систолический шум, над аортой — грубый систоло-диастолический шум. Пульс на a. radialis слева хорошего наполнения, справа — резко ослаблен, ЧСС 60-70 ударов в мин. Отмечалась асимметрия артериального давления: на левой руке 120/80 мм рт. ст., на правой руке — 80/60 мм рт. ст.).
С целью уточнения диагноза больному проведено ультразвуковое исследование сердца и сосудов, ЧПЭхоКГ и электронно-лучевая томография (ЭЛТ).
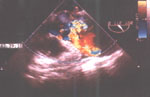
При проведении трансторакальной ЭхоКГ из парастернальной позиции по длинной оси выявлено, что левый желудочек (ЛЖ) расширен: КДР — 6.6 см, КСР — 4.4 см (норма 5.5 см и 3.5 см соответственно). Сократительная способность миокарда ЛЖ удовлетворительная. Аорта в области аортального кольца не расширена, диаметр ее равен 3.5 см (норма до 3.7 см). Восходящий отдел аорты выше места прикрепления створок аортального клапана расширен до 6.0 см (аневризма). По задней стенке аорты определяется двойной контур, что позволило предположить наличие PAA (рис. 1). При допплеровском исследовании сердца из верхушечной позиции (пятикамерный срез) в выходном тракте ЛЖ зарегистрирован регургитирующий поток 2-й степени. Из-за плохого ультразвукового окна цветовое допплеровское картирование сердца затруднено.
Таким образом, по данным ТЭхоКГ, у пациента обнаружены расслаивающая аневризма восходящего отдела аорты с развитием относительной недостаточности аортального клапана 2-й ст. и расширение ЛЖ.
Для уточнения состояния аортального клапана, выявления границ отслоившейся интимы и определения объема и особенностей предстоящего оперативного вмешательства, в том числе на клапане, была проведена ЧП ЭхоКГ.
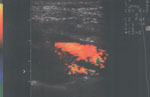
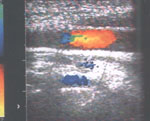
Под местной анестезией 10%-ным раствором лидокаина после внутривенного введения 2 мл раствора реланиума выполнена ЧП ЭхоКГ. Створки аортального клапана оказались неизмененными, аорта в области клапана не расширена, диаметр ее здесь равен 3.5 см. В 2 см от места прикрепления створок аортального клапана визуализируется отслоившаяся интима (рис. 2) с формированием ложной аневризмы в области задней стенки. Диаметр аорты в этой области составляет 6.2 см. При цветовом допплеровском картировании в нижней части отслоившейся интимы обнаружено отверстие размером 2.4 см (рис. 3) Отслойка интимы распространяется до дистального отдела дуги аорты, диаметр которой не превышает 3.5 см. Нисходящий отдел аорты не изменен и не расширен (2.6 см).
Таким образом, по данным ЧПЭхоКГ, диагностирована РАА в восходящем отделе с распространением и на дистальный отдел дуги.
При исследовании экстракраниального отдела брахиоцефальных артерий методом дуплексного сканирования и цветового допплеровского картирования потока выявлено расслоение брахиоцефального ствола с формированием двух каналов (рис. 4). Первый из них диаметром 10 мм переходит в правую сонную артерию, кровоток в которой не изменен. Второй канал диаметром 2.3 мм переходит в подключичную артерию, где определяется кровоток с повышенной скоростью и элементами турбулентности. Направление кровотока по правой позвоночной артерии ретроградное, что является признаком развития постоянной формы синдрома позвоночно-подключичного обкрадывания (рис. 5).
Таким образом, отслоение интимы аорты у данного больного распространялось на брахиоцефальный ствол, что, по-видимому, и привело к ослаблению пульса на a. radialis и снижению артериального давления справа.
Для уточнения данных, полученных с помощью ультразвуковых методов исследования, была проведена электронно-лучевая томография (ЭЛТ) на аппарате «Imatron», модель С-150 (США ) с синхронизацией по ЭКГ. Время выполнения одного среза составляло 100 мс. Все исследование было осуществлено в течение одной тридцатисекундной задержки дыхания. Толщина срезов и расстояние между их центрами равнялось 3 мм. ЭЛТ выполняли до и после внутривенного болюсного введения 120 мл неионного рентгеноконтрастного препарата Омнипак, содержащего 350 мг йода/мл, фирмы Никомед (Норвегия) со скоростью 3.5 мл/сек.
Рис. 1. Трансторакальная ЭхоКГ. Парастернальная позиция. Одномерное исследование аорты. Аорта расширена, по задней стенке определяется двойной контур (отслоившаяся интима).
Fig. 1. Transthoracic echocardiography: parasternal position, one-dimensional investigation. The enlarged aorta has a double contour along the posterior wall (detached intima).
Рис. 2. Чреспищеводная ЭхоКГ. Двухмерное изображение аорты по длинной оси. Стрелками показана отслоившаяся интима.
Fig. 2. Transesophageal echocardiography: two-dimensional image of the aorta along the long axis. Arrows point at the detached intima.
Рис. 3. Чреспищеводная ЭхоКГ. Двухмерное изображение аорты по длинной оси. Цветовое допплеровское картирование. Видно (желтый цвет) движение крови по каналу, образованному отслоившейся интимой.
Fig. 3. Transesophageal echocardiography: two-dimensional image of the aorta along the long axis. Color Doppler. Yellow is a blood flow along the channel formed by the detached intima.
Рис. 4. Исследование брахиоцефального ствола в цветовом допплеровском режиме. Отчетливо видно существование двух потоков.
Fig. 4. Investigation of the brachycephal column. Color Doppler. Two flows are easily observable.
Рис. 5. Правая общая сонная и позвоночная артерии в цветовом допплеровском режиме. Кровоток в общей сонной артерии направлен к мозгу, в позвоночной артерии — от мозга.
Fig. 5. The right common carotid and vertebral arteries in color Doppler. Blood is running toward the brain in the common carotid artery and in the opposite direction in the vertebral artery.
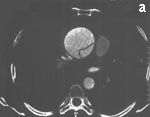
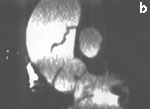
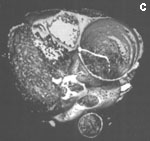
На основании серии поперечных срезов на рабочей станции выполнялись многоплоскостные и объемные реконструкции. По данным ЭЛТ, сразу за кольцом аортального клапана, диаметр которого составлял 3.0 см, начинается аневризматическое расширение восходящей аорты, достигающее 6.3 см в диаметре на границе между проксимальной и средней ее третями. Диаметр дуги аорты 3.5 см, нисходящей аорты — 3.3 см. Начиная от уровня синусов Вальсальвы, видна отслоившаяся интима, имеющая извитой ход и формирующая ложный канал вдоль задне-левой стенки аорты (рис. 6 а, b, с). Расслоение переходит на дугу аорты и заканчивается в ее дистальной трети. В нижней части отслоившейся интимы видна фенестрация размером около 2.5 см; в дистальном отделе дуги имеется второй разрыв интимы диаметром около 2.0 см. Тромботические массы в просвете ложного канала отсутствуют. При анализе состояния сосудов, отходящих от дуги аорты, обнаружен переход расслоения на устье брахиоцефального ствола.
Таким образом, данные ЭЛТ также свидетельствуют о наличии аневризмы восходящей аорты и ее расслоении (II тип) с вовлечением устья брахиоцефального ствола.
На основании клинических и инструментальных исследований был поставлен диагноз: расслаивающая аневризма восходящего отдела аорты (II тип по De Bakey) с распространением на брахиоцефальный ствол. Недостаточность аортального клапана 2-й степени.
Особенностью представленного наблюдения является распространение расслоения интимы на брахиоцефальный ствол с образованием двух каналов. Кроме того, несмотря на столь значительные изменения, больной не только остался жив, но и пребывал в удовлетворительном состоянии в течение нескольких месяцев после возникновения расслоения аневризмы.
Заключая, можно подчеркнуть, что ультразвуковые методы исследования позволили диагностировать расслаивающую аневризму аорты, определить место начала отслойки интимы, ее распространенность, что было подтверждено ЭЛТ. Это дает возможность рекомендовать использование ультразвуковых методов для диагностики РАА.
Рис. 6. Электронно-лучевая томография.
а — срез в поперечной плоскости. В просвете аорты, заполненном контрастным препаратом, видна отслоившаяся интима,
b — реконструкция в сагиттальной плоскости. Визуализируется проксимальный разрыв отслоившейся интимы,
с — трехмерная реконструкция.
Fig. 6. Electron-beam СТ.
а — cross section. The detached intima can be observed in the aortic lumen filled with a contrast agent,
b — reconstruction in the sagittal plane. Proximal rupture of the detached intima can be visualized,
с — three-dimensional reconstruction.
источник
Под расслаивающей аневризмой аорты (расслоение аорты) понимают образование дефекта (разрыва) внутренней оболочки стенки аорты с последующим поступлением крови в дегенеративно измененный средний слой, образованием внутристеночной гематомы и продольным расслоением стенки аорты на внутренний и наружный слои с формированием дополнительного внутрисосудистого канала (ложного просвета). Расслоение чаще происходит в дистальном (антеградном) направлении, реже — в проксимальном (ретроградном). Аневризма (расширение аорты) может формироваться в случае значительного расширения ложного просвета, однако, само по себе расширение аорты в ряде случаев носит умеренный характер или отсутствует.Клиническая картина заболевания определяется 3 патологоанатомическими факторами, лежащими в основе расслоения: расслоением стенки аорты, развитием обширной внутристеночной гематомы и сдавлением или отрывом ветвей аорты, снабжающих жизненно важные органы (сердце, головной и спинной мозг, почки), с последующей их ишемией. Само по себе внезапное расслоение аорты вызывает боль.
Образование внутристеночной гематомы в области восходящей аорты приводит к сдавлению коронарных артерий, сужению выходного отдела ЛЖ, острой недостаточности кровообращения, проксимальной коарктации. Обширная внутристеночная гематома, вмещающая большое количество крови, создает своеобразный «олигемический синдром».
Симптомы расслоения аорты могут быть разнообразны, т.к. расслоение — процесс динамичный и начальная картина заболевания может отличаться от финальной. Они могут имитировать практически все сердечно-сосудистые, неврологические, хирургические и урологические заболевания.
Ведущим и самым частым (в 90-96% случаев) синдромом расслоения аорты является боль (кроме больных с нарушением сознания). Боль отличается необычайной интенсивностью, возникает внезапно, с максимальной выраженностью в начале расслоения, в отличие от инфаркта миокарда (ИМ), где она постепенно нарастает. В некоторых случаях боль может становиться невыносимой. Боль имеет раздирающий, разрывающий, простреливающий характер, может быть мигрирующей от места возникновения по направлению расслоения, может в начале сопровождаться вагусными проявлениями, тошнотой, рвотой, повышением АД. Локализация боли при РА определяется местом начала расслоения. Боль за грудиной, спереди грудной клетки, имитирующая ИМ, характерна для проксимального расслоения (более 90% случаев), особенно если оно распространяется на корень и вызывает сдавление коронарных артерий. При дальнейшем расслоении (1тип) боль перемещается в межлопаточное пространство, затем смещается вдоль позвоночника. Мигрирующая боль по пути распространения расслаивающей гематомы отмечается у 17-70% больных. Боль в шее, глотке, челюсти, лице, зубах указывает на вовлечение восходящей аорты и дуги. Боль в грудной клетке сзади, спине, нижних конечностях характерна для дистального расслоения, при этом она первоначально локализуется в межлопаточном пространстве. Отсутствие боли в межлопаточном пространстве достаточное свидетельство против дистального расслоения. При распространении расслоения аорты I и II типов на брюшную аорту боль локализуется в эпигастрии, гипогастрии, пояснице, имитируя острые заболевания желудочно-кишечного тракта, урологические заболевания.
Асимптомное (безболевое) течение (кроме больных с нарушением сознания) может быть у больных с хроническим расслоением.
Менее частыми первоначальными признаками расслоения аорты (в связи или без связи с болью) могут быть:
— симптомы ишемии головного или спинного мозга, периферическая нейропатия, синкопэ без локальной неврологической симптоматики (в 4-5%), которые чаще связаны с разрывом расслоенной аорты в перикард или плевральную полость;
— аортальная недостаточность и острая недостаточность кровообращения;
— ишемия органов пищеварения;
— остановка сердца и внезапная смерть.
Данные объективного осмотра при расслоении аорты вариабельны и, в той или иной степени, связаны с локализацией аорты и степенью вовлечения сердечно-сосудистой системы. В других случаях, даже при наличии обширного расслоения, объективные данные могут быть невыраженными или вообще отсутствовать.
1) АГ в начале заболевания (при возможной клинической картине шока) наблюдается чаще при дистальном расслоении (в 80-90% случаев), реже — при проксимальном. Артериальная гипотензия — чаще при проксимальном расслоении. Причинами ее чаще является тампонада сердца, либо внутриплевральный или внутриперитониальный разрыв аорты.
2) Асимметрия пульса (снижение его наполнения или отсутствие) и АД на верхних или нижних конечностях наблюдается у половины больных с проксимальным и у 15% — с дистальным РА (при вовлечении бедренной или подключичной артерий). Сужение обусловлено либо распространением расслоения аорты на ту или иную артерию, с уменьшением истинного просвета, либо проксимальной обструкцией интимальным лоскутом лежащего выше устья вовлеченной артерии. Хотя наличие асимметрии пульса у больного с острой болью предполагает РА, возможны ошибочные трактовки.
3) Аортальная регургитация с диастолическим шумом аортальной недостаточности — важный признак проксимального расслоения — встречается у 50-75% больных. Шум может иметь музыкальный оттенок, лучше выслушивается вдоль правого края грудины. Он может быть нарастающим, убывающим, различной интенсивности, в зависимости от величины АД. При тяжелой аортальной недостаточности могут быть периферические признаки: быстрый, скачущий и высокий пульс и большое пульсовое давление. В некоторых случаях при развитии застойной сердечной недостаточности, вследствие остро развившейся аортальной недостаточности, диастолический шум может быть едва уловим или отсутствовать.
4) Неврологические нарушения встречаются в 6-19% всех расслоений аорты и включают в себя цереброваскулярные нарушения, периферическую нейропатию, нарушения сознания, параплегии. Цереброваскулярные нарушения встречаются в 3-6% случаев, вследствие вовлечения безымянной или левой общей сонной артерии. Реже могут быть нарушения сознания или даже кома.
При вовлечении спинальных артерий (чаще при дистальном расслоении) могут быть параплегии или парапарезы вследствие ишемии спинного мозга.
5) Более редкими проявлениями расслоений аорты могут быть: ИМ, инфаркт почек и др. В 1-2% случаев проксимального расслоения могут вовлекаться устья коронарных артерий и развиваться вторичный ИМ (чаще — задний/нижний, вследствие более частого поражения правой коронарной артерии). Из-за наличия симптомов расслоений аорты инфаркт миокарда может клинически не проявляться. С другой стороны, при ЭКГ острого ИМ может быть не распознано расслоение аорты, а применение тромболизиса может привести к фатальным последствиям. Поэтому при заднем/нижнем инфаркте миокарда следует не забывать о возможности РА и до проведения тромболизиса некоторые авторы считают необходимым провести рентгенологическое исследование для исключения расслоения аорты.
Распространение расслоения на брюшную аорту может вызвать различные сосудистые нарушения: ишемию и инфаркты почек, приводя к тяжелой АГ и острой почечной недостаточности мезентериальную ишемию и инфаркты соответствующей области (в 3-5% расслоений аорты); острую ишемию нижних конечностей (при распространении расслоения на подвздошные артерии).
6) Клиническим проявлением расслоения аорты могут быть плевральные выпоты, чаще слева, вследствие либо вторичной экссудативной реакции вокруг пораженной аорты, либо в результате разрыва или просачивания крови в плевральную полость.
7) Очень редкими проявлениями расслоений аорты могут быть:
— пульсация грудинно-ключичного сочленения
— сдавление трахеи и бронхов с явлениями стридора или бронхоспазма
— кровохарканье при разрыве в трахеобронхиальное дерево
— рвота кровью при разрыве в пищевод
— синдром верхней полой вены
— атриовентрикулярная блокада (при вовлечении перегородки)
— лихорадка неясного генеза, обусловленная воздействием пирогенных субстанций из гематомы или связанного с ней выпота
— шумы, обусловленные разрывом расслоенной аорты в полости предсердий или правого желудочка с развитием сердечной недостаточности.
При подозрении на расслоение аорты важно быстро и точно верифицировать диагноз.
Рентгенография органов грудной клетки, не являясь методом верификации диагноза, тем не менее, может первой выявить признаки, подозрительные на расслоение аорты. Данные рентгенологического обследования не являются специфичными, но могут дать основание для проведения других методов исследования. Основными рентгенологическими признаками, указывающими на возможность РА, являются:
I. Расширение тени аорты (в 81 -90% случаев, по нашим данным), лучше выявляемое в левой косой проекции (иногда локальное выпячивание в области расслоения, реже — расширение верхнего средостения). Расширение тени аорты было выявлено у 50% больных с расслоением I типа (- и у 10% — III типа. Отмечалась неровность контуров нисходящей аорты, деформация ее тени.
2. Сепарация (отделение) кальцинированной интимы в области выпячивания от адвентиция более, чем на 1 см (в норме — до 0,5 см) — предположительный, но также не диагностический признак.
3. Изменение тени контуров аорты или средостения при сравнении с данными предыдущего исследования.
4. Отклонение трахеи или плевральный выпот (чаще левосторонний).
5. Резкое снижение или отсутствие пульсации ненормально широкой аорты. Хотя большинство больных с РА имеет один или более рентгенологических признаков, у 12% пациентов имеется неизмененная рентгенограмма. Отсутствие изменений при ренгенографии не позволяет исключить диагноз расслоения аорты.
Электрокардиография в 12 стандартных отведениях выявляет неспецифические для РА признаки гипертрофии левого желудочка и связанные с ней изменения (депрессия сегмента ST, отрицательный зубец Т). У 1/3 пациентов ЭКГ остается нормальной. Тем не менее, снятие ЭКГ важно по двум причинам:
— отсутствие изменений на ЭКГ у больного с выраженным болевым синдромом в грудной клетке является опорным дифференциально-диагностическим критерием РА с ИМ;
— наличие на ЭКГ признаков ОИМ (чаще нижней локализации) при сопоставлении с данными рентгенографии позволяет не только предположить у больного расслоение аорты, но и указывает на вовлечение коронарных артерий.
Лабораторные признаки не очень показательны в диагностике расслоений аорты:
а. анемия — при значительной секвестрации крови в ложном канале или разрыве в полости;
б. небольшой (умеренный) нейтрофильный лейкоцитоз (до 12-14 тыс./мм3);
в. повышение ЛДГ и билирубина (из-за гемолиза крови в ложном канале);
г. нормальный уровень КФК и трансаминаз;
д. изредка возможно развитие ДВС-синдрома.
По данным объективных и рутинных методов обследования, диагноз расслоения аорты может быть поставлен только у 62% пациентов. Остальные в начале заболевания имеют признаки ишемии миокарда, застойной недостаточности кровообращения, нерасслаивающей аневризмы грудной или брюшной аорты, симптомы аортального стеноза, ТЭЛА и др. Среди этих больных с первоначально недиагносцированным расслоением аорты, у 2/3 расслоений аорты было диагносцировано другими методами исследования, использованными для решения прочих клинических вопросов. У 1/3 диагноз быть поставлен только на аутопсии.
Основными методами диагностики расслоений аорты в настоящее время считают методы, позволяющие визуализировать аорту:
— контрасгно-усиливающая компьютерная томография (КТ)
— ядерно-магнитный резонанс (ЯМР)
— трансторакальная и трансэзофагеальная эхокардиография.
Каждая методика имеет свои преимущества и недостатки. Выбор метода зависит от возможности и опыта.
Аортография долгое время рассматривалась как стандартный и единственно точный высокочувствительный метод диагностики расслоений аорты. Прямыми признаками расслоения аорты при аортографии являются: визуализация двух просветов (истинного и ложного), интимального лоскута, а непрямыми — деформация просвета аорты, расширение и деформация ее стенки, ненормальное отхождение сосудистых ветвей, наличие аортальной регургитации. Аортография позволяет:
1. определить протяженность расслоения
2. выявить вовлеченность ветвей аорты
3. определить место начального разрыва и точное место проксимальной фенестрации
4. наличие или отсутствие дистальной фенестрации
5. оценить степень состоятельности аортального клапана и коронарных артерий.
Однако, ложный просвет, чаще выявляющийся в нисходящей аорте, в 10-15% случаев тромбируется; истинный просвет при этом сужен. При трансфеморальном доступе катетер может не попасть в истинный просвет аорты. Выявить наличие интимального лоскута (т.е. отслоенную внутреннюю оболочку между истинным и ложным просветом) удается у 1/3 больных.
Недостатком аортографии является возможность получения ложно-отрицательных результатов, что случается при слабой контрастированности ложного просвета (из-за его возможного тромбоза), одинаково равномерном контрастировании обоих каналов, малом и локальном расслоении.
К сложностям применения данного метода следует отнести риск инвазивной процедуры и введения контрастного вещества (его непереносимость), невозможность выполнения аортографии у нестабильных (нетранспортабельных) больных. Кроме того, введение альтернативных диагностических методик показало, что чувствительность и специфичность аортографии составляет 77-88% и 95%, соответственно. Так, ложный ход визуализируется у 87% больных, интимальный лоскут — у 70% и место начального разрыва интимы — лишь у 50% пациентов с расслоениями аорты.
Эхокардиография является доступным и неинвазивным методом диагностики РА. По литературным данным трансторакальная эхокардиография позволяет выявить 80% расслоений аорты. В настоящее время особую роль в диагностике расслоений аорты отводят чреспищеводной ЭхоКГ (чувствительность метода составляет 95%, а специфичность-75%), являющейся методикой выбора при нестабильном состоянии больного, т.к. может быть быстро выполнена у постели больного, в операционной, непосредственно перед оперативным вмешательством, не требует прекращения мониторного наблюдения и проводимых терапевтических мероприятий. Эхокардиография позволяет визуализировать расширение луковицы аорты, увеличение толщины стенок аорты, функцию аортального клапана, определить подвижный лоскут в просвете аорты, а также дает дополнительную информацию о сердечных структурах и функции.
При отсутствии возможности проведения чреспищеводной ЭхоКГ, методом выбора является компьютерная томография с введением контраста. При контрастно-усиленной КТ расслоение аорты определяется по наличию двух различных просветов, видимо разделенных интимальным лоскутом, либо по различной скорости (степени) контрастного затемнения. Метод обладает чувствительностью 83-94% и специфичностью 87-100%.
Преимуществами КТ являются: неинвазивность, хотя и требуется в/в введение контраста; доступность; возможность установить диагноз расслоения аорты в случае тромбоза ложного просвета; возможность устанавливать наличие перикардиального выпота.
Основные недостатки КТ: относительно невысокая чувствительность в отношении диагностики расслоений аорты; невозможность в 1/3 случаев выявить интимальный лоскут; редкость установления места начального разрыва; невозможность выявить наличие аортальной регургитации и вовлечение сосудистых ветвей.
ЯМР является неинвазивной методикой, не требующей в/в введения контраста, при этом дающей высококачественное изображение в нескольких плоскостях. ЯМР облегчает распознавание РА, позволяет выявить вовлеченность ветвей, а также диагностировать расслоение аорты у пациентов с предшествующими заболеваниями аорты. Чувствительность и специфичность метода — около 98%, при этом, чувствительность составляет 88% для установки места интимального разрыва и аортальной регургитации, 98% — для диагностики наличия тромбоза и 100% — для выявления перикардиального выпота. Необычайно высокая точность делает ЯМР современным «золотым стандартом» в диагностике РА, особенно у стабильных больных и с хроническим расслоением.
Однако, у метода все же есть ряд недостатков: ЯМР противопоказан больным с пейсмейкером, при наличии определенного типа сосудистых скрепок, некоторыми старыми типами протезирования металлическими искусственными клапанами; не является широко доступным методом. Некоторые авторы считают относительным противопоказанием к проведению ЯМР нестабильное состояние больного, требующее в/в назначения гипотензивных препаратов и мониторинга АД.
Лечение при расслоении аорты направлено на остановку прогрессирования расслаивающей гематомы.
Боль должна быть купирована в/в введением морфина.
Для уменьшения сердечного выброса и снижения скорости изгнания ЛЖ, применяют b-блокаторы в возрастающих дозах до снижения ЧСС 60-80 в мин.
При наличии противопоказаний к применению b-блокаторов (брадикардия, АВ-блокада, бронхоспазм), сейчас все чаще применяются антагонисты кальциевых каналов. Нифедипин сублингвалыю может быть применим немедленно, пока будут приготовлены к введению другие препараты. Недостатком нифедипина является слабое отрицательное инотропное и хронотропное действия, в связи с чем могут быть применены дилтиазем и верапамил.
При неэффективности бета-блокаторов может быть применен нитропруссид натрия в дозе 0,5-10 мг/кг*мин в/в.
При рефракторной гипертензии, в результате вовлечения почечных артерий, наиболее эффективно применение ингибиторов АПФ (эналаприл — 0,625 мг внутривенно каждые 4-6 ч. с постепенным увеличением дозы).
При гипотензии следует думать о возможности тампонады сердца, разрыве аорты, что, по возможности, требует быстрого восстановления ОЦК. При рефракторной гипотензии предпочтительно использовать норадреналин, мезатон. Допамин используется для улучшения функции почек и только в малых дозах.
При стабилизации состояния больного немедленно проводятся диагностические исследования для верификации диагноза. При нестабильном состоянии больного предпочтительно выполнение ТЭЭ, на фоне непрерывающегося мониторинга и терапевтических мероприятий.
Дальнейшая тактика определяется типом расслоения.
источник