«ФАРМАТЕКА»; Актуальные обзоры; № 13; 2012; стр. 9-14.
Д.Т. Абдурахманов
Кафедра терапии и профболезней ГБОУ ВПО «Первый МГМУ им. И.М. Сеченова» Минздравсоцразвития РФ, Москва
Обсуждается проблема железодефицитной анемии (ЖДА), развивающейся в т. ч. при заболеваниях желудочно-кишечного тракта. Представлены сведения, касающиеся причин возникновения ЖДА, патогенеза, симптоматики, диагностики и лечения данной патологии. Особое внимание уделено препарату Феринжект (железа карбоксимальтозат), который применяется в комплексной терапии пациентов с ЖДА, обусловленной воспалительными заболеваниями кишечника.
Ключевые слова: железодефицитная анемия, дефицит железа, ферротерапия, железа карбоксимальтозат
The article discusses the problem of iron deficiency anemia (IDA), which develops against the background of many diseases, including gastrointestinal diseases. The data on the causes of IDA, pathogenesis, symptoms, diagnosis and treatment of this disease are presented. Particular attention is paid to the drug Ferinject (ferric carboxymaltosate) used for the treatment of IDA in patients with inflammatory bowel diseases.
Key words: iron deficiency anemia, iron deficiency, ferrotherapy, ferric carboxymaltosate
Наиболее частая в популяции причина анемии — дефицит железа в организме. По данным отчета Всемирной организации здравоохранения (ВОЗ) о состоянии здоровья за 2002 г., железодефицитная анемия (ЖДА) входит в десятку глобальных факторов риска развития нетрудоспособности. Так, показано, что ЖДА встречается среди 30 % населения планеты [1]. В США ЖДА наблюдается среди 5-12 % небеременных женщин и 1-5 % мужчин [2].
Метаболизм железа в организме
Общее количество железа в организме взрослого человека составляет около 3,5-4,0 г, в среднем 50 и 40 мг/кг у мужчин и женщин соответственно. Основная часть железа входит в состав гемоглобина эритроцитов (около 2,5 г), значительная часть железа (около 0,5—1,0 г) депонируется в составе ферритина или входит в состав гемсодержащих и других ферментов (миоглобина, каталазы, цитохромов) организма (около 0,4 г) и небольшая часть железа (0,003—0,007 г) находится в связанном с трансферрином состоянии в крови.
Баланс железа в организме поддерживается соответствием количества поступающего железа его потерям. В пище железо присутствует в составе гема или как негемовое железо. Ежедневно с пищей (стандартный пищевой рацион) в организм человека поступает 10—20 мг железа, из которого в норме в кишечнике всасывается около 10 % (от 3 до 15 %), что компенсирует суточные потери железа, главным образом при слущивании эпителиальных клеток. Организм обеспечивает баланс железа в организме, регулируя процесс его всасывания в кишечнике. В случае развития дефицита железа организм увеличивает процент всасываемого железа (может достигать 25 %), при избытке — уменьшает [3]. В этом процессе ключевое значение придают гепсидину — белку, который синтезируется в печени. Поступление с пищей или выведение железа, как правило, вне контроля организма.
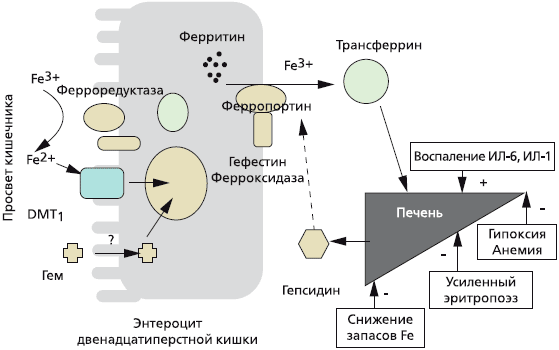
Около 25—30 мг железа ежедневно реутилизируется после разрушения (вследствие старения) эритроцитов в селезенке и поступает снова в костный мозг для синтеза новых эритроцитов. Железо, которое всасывается в кишечнике, предварительно на поверхности энтероцита восстанавливается с участием ферроредуктаз из трехвалентного (Fe 3+ ) в двухвалентнтное (Fe 2+ ), затем с помощью специфического переносчика — транспортера двухвалентных металлов (DMT1) поступает в цитоплазму [4]. Железо в составе гема (содержится в мясе, рыбе) всасывается напрямую. В дальнейшем двухвалентное железо с помощью другого переносчика, ферропортина (также мобилизует железо из ферритина), секретируется в кровь, где снова окисляется до трехвалентного (при участии белка гефестина) и связывается с плазменным белком трансферрином [5]. Трансферрин осуществляет транспорт железа в костный мозг, где оно утилизируется для синтеза эритроцитов, или преимущественно в печень, где железо депонируется в составе ферритина (рис. 1) [6].
При снижении запасов железа, гипоксии, анемии, усиленном эритропоэзе в печени снижается синтез гепсидина, что усиливает всасывание железа в кишечнике, при хроническом воспалении синтез гепсидина в печени увеличивается и, соответственно, всасывание железа в кишечнике снижается.
Рис 1. Регуляция всасывания железа в кишечнике [Guidi G.C., Santonastaso C.L., 2010]
Ферритин — ключевой белок, отражающий запасы железа в организме. Он депонирует железо в нетоксической форме, которое при необходимости мобилизуется. В среднем одна молекула ферритина содержит до 4500 атомов железа. Главным образом железо депонируется в печени, костном мозге и селезенке. Снижение уровня ферритина в сыворотке крови является достаточно надежным показателем дефицита железа в организме, его увеличение, как правило, указывает на перегрузку организма железом. В то же время необходимо помнить, что ферритин относится к белкам острой фазы воспаления, поэтому увеличение его содержания в крови может быть следствием активного воспалительного процесса, а не телько избытка железа. В ряде случаев некоторые злокачественные опухоли обладают способностью синтезировать и секретировать в кровь большое количество ферритина (в рамках паранеопластического синдрома). В норме содержание ферритина в сыворотке крови составляет 30-300 нг/мл.
Причины железодефицитной анемии
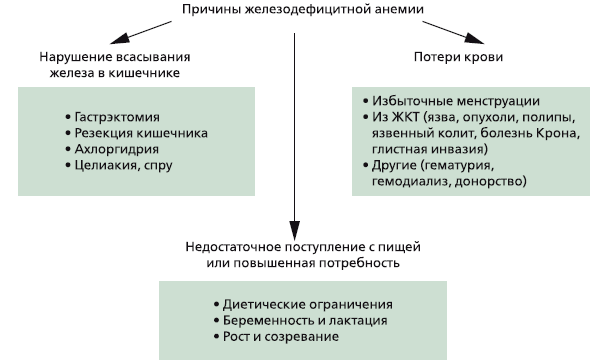
Выделяют три глобальные причины развития дефицита железа в организме (рис. 2):
1. Недостаточное поступление с пищей или повышенная потребность.
2. Нарушение всасывания железа в кишечнике.
3. Хронические потери крови.
Рис 2. Основные причины железодефицитной анемии
В популяции наиболее частой причиной ЖДА является недостаточное поступление с пищей: по данным ВОЗ, от четверти до трети населения в мире хронически голодают из-за нехватки продуктов питания, особенно мясной пищи. Однако в клинической практике среди основных причин ЖДА выделяют хронические потери крови, прежде всего из желудочно-кишечного тракта.
Клиническая картина
При ЖДА наблюдаются общие для всех анемий проявления циркуляторно-гипоксического синдрома:
Кроме того могут встречаться специфические признаки тканевого дефицита железа:
Диагностика
Лабораторная диагностика ЖДА основана на изучении обмена железа и выявлении его дефицита. Выделяют ряд признаков, указывающих на железодефицитный характер анемии (табл. 1).
Лабораторные признаки дефицита железа и ЖДА
| Параметры | Значения при ЖДА | Норма | |
| Железо сыворотки, мкг/дл | 3 | 5 | Примечание. НПВС — нестероидные противовоспалительные средства. Среди причин ЖДА (почти 30-50 % всех случаев) прежде всего рассматривают острые или хронические кровопотери из ЖКТ. Основной причиной ЖДА у женщин до менопаузы являются беременность и менструации, у женщин после менопаузы и у мужчин — хронические (латентные) потери крови из ЖКТ. Анализ кала на скрытую кровь — основной скрининговый метод выявления скрытого желудочно-кишечного кровотечения (тест положительный при выделении не менее 10 мл крови в сутки). При потере не менее 30 мл крови в сутки тест на скрытую кровь бывает положительным в 93 % случаев [8]. Наиболее часто при хронической ЖДА и особенно в случаях положительного результата кала на скрытую кровь выполняют эзофагогастродуодено- (ЭФГДС) и колоноскопию. В 5-10 % случаев анемий, связанных с заболеваниями ЖКТ, при ЭФГДС и колоноскопии не удается выявить очага поражения [9]. В 25 % случаев это обусловлено небольшим размером пораженного участка, который обнаруживается при повторном осмотре, в остальных случаях необходимо обследование тонкой кишки. В последние годы наиболее часто для выявления источника кровотечения из тонкой кишки используется беспроводная капсульная эндоскопия. В 10-17 % случаев причиной ЖДА у мужчин и женщин старше 40 лет являются онкологические заболевания ЖКТ; прежде всего колоректальный рак. ЖДА в течение длительного времени может быть единственным проявлением рака толстой кишки правосторонней локализации, при этом размер опухоли обычно превышает 3 см. Другая наиболее частая причина ЖДА -язвенная болезнь желудка и двенадцатиперстной кишки. При скрытых кровопотерях, обусловленных поражением тонкой кишки, наиболее часто в возрасте до 40 лет выявляют опухоли (лимфому, карциноид, аденокарциному, полипоз), ангиоэктазию артерий (Dieulafoy’s поражение), целиакию и болезнь Крона, в возрасте старше 40 лет -патологию сосудов различной природы и прием НПВС. У трети больных воспалительными заболеваниями кишечника (болезнь Крона, язвенный колит) выявляется анемия, имеющая сложный генез (сочетание ЖДА и анемии хронических заболеваний). При этом дефицит железа становится следствием нескольких причин: Лечение Суточная терапевтическая доза элементарного железа при лечении ЖДА для взрослых составляет в среднем 100— 200 мг в 2—3 приема. Поливитаминные комплексы, содержащие железо, не рекомендуют в качестве лечения ЖДА, т. к. они содержат недостаточное количество железа либо оно плохо всасывается в кишечнике. При адекватном лечении уже в течение первых 3 суток наблюдается увеличение числа ретикулоцитов в крови, на 7—10-й день отмечается ретикулоцитарный криз (пик ретикулоцитоза). К 3—4-й неделе лечения имеет место увеличение уровня гемоглобина на 20 г/л. Прием препаратов железа необходимо продолжать еще в течение 3—6 месяцев после нормализации уровня гемоглобина — пока насыщение трансферрина железом не превысит 30 % и концентрация ферритина не достигнет 50 нг/мл (показатель восстановления тканевых запасов железа). Среди 20—30 % пациентов в результате приема препаратов железа отмечаются различные диспептические расстройства (тошнота, дискомфорт в эпигастрии, диарея или запор). Риск развития желудочно-кишечных расстройств можно снизить, принимая препарат во время еды или на ночь, а также при постепенном увеличении дозы. Среди причин неэффективности пероральных форм железа рассматривают целый ряд факторов [10]: недостаточное поступление железа; Нарушение всасывания железа: Продолжающиеся потери крови или повышенная потребность в железе: Сопутствующие заболевания или состояния: Неправильный диагноз или наличие других причин анемии: Выделяют следующие показания к парентеральному введению, преимущественно внутривенному, препаратов железа: Основная опасность при парентеральном введении железа — развитие тяжелых аллергических реакций, включая анафилактических шок с летальным исходом, которые наблюдаются в 0,6—1,0 % случаев. Данные реакции, в основном, характерны для препаратов железа, содержащих декстран. Среди парентеральных препаратов железа широкое распространение, особенно в комплексной терапии воспалительных заболеваний кишечника, получили сахарат железа и железа карбоксимальтозат (Феринжект), которые в отличие от декстрана железа ассоциируются с минимальным риском развития анафилактических и других аллергических реакций [11—13]. Так, в 2011 г. были опубликованы результаты рандомизированного контролируемого исследования применения железа карбоксимальтозата пациентами с железодефицитной анемией, обусловленной воспалительными заболеваниями кишечника (FERGIcor — a Randomized Controlled Trial on Ferric Carboxymaltose for Iron Deficiency Anemia in Inflammatory Bowel Disease) [14]. В исследовании сравнивали эффективность и безопасность нового режима фиксированной дозы железа карбоксимальтозата (Феринжекта) и индивидуально рассчитываемых доз сахарата железа (СЖ) для пациентов с воспалительными заболеваниями кишечника и ЖДА. В исследование были включены 485 пациентов с ЖДА (уровень ферритина ЛИТЕРАТУРА источник В последние годы мы уже немного забыли о таких тяжелых проблемах со здоровьем, как язвенная болезнь желудка и двенадцатиперстной кишки. Во многом это объясняется ставшими действительно лучше средствами диагностики и новыми препаратами для лечения. Тем не менее, большое количество людей продолжают страдать от язв в желудке. А количество новых выявляемых случаев рака желудка в России составляет 40.000 каждый год, из них 51% людей умирает в течение года.
Поэтому даже при «обычных» на первый взгляд симптомах, таких как тяжесть и дискомфорт вверху живота, легкие болезненные ощущения вверху живота, изжога, отрыжка – обязательно нужно, чтобы врач осмотрел живот. После этого станет более ясно, есть ли опасность и риски развития язвы, нужно или не нужно делать гастроскопию, и возможно, сразу можно будет начать лечение.
Почему? Потому что, язва фактически представляет собой большую и глубокую рану на стенке желудка. Конечно, оттуда выделяется какое-то количество крови. Это может быть и большое кровотечение, которым будут заниматься уже хирурги, и вам самим захочется вызвать скорую помощь. Или это может быть небольшое «подкравливание», которое приводит к значительной потери крови, железа и гемоглобина из организма. Длительная потеря небольших количеств железа не успевает, ни при каких условиях, восполниться из пищи! Поэтому дефицит железа в организме накапливается. Появляется слабость, усталость, утомляемость, снижается внимание, кожа становится бледной. Могут даже начать ломаться ногти или выпадать волосы. А вот эти симптомы уже никто не будет связывать с язвой и анемией. Возникает порочный круг. Язва приводит к потере железа, без железа язва не может зажить даже при лечении. Кроме того сама язва и воспаление в желудке препятствуют поступлению железа в организм. И понеслось – у кого на сколько железа хватит?! Лечить анемию при язвенной болезни нужно обязательно, поскольку дефицит железа будет ухудшать заживление слизистой оболочки желудка и самого язвенного дефекта. Все препараты железа, существовавшие до недавнего времени имели побочные эффекты на желудок. И врачи находились в тупике – нужно восполнить уровень железа в организме, а когда мы его добавляем, ситуация в желудке ухудшается. До недавнего времени было так, пока не появилось первое лекарство с железом, не оказывающее побочных эффектов. Это железо, заключенное в специальную липосомальную оболочку (препарат Сидерал Форте). Им можно восстановить уровень железа в организме, даже при язве в желудке, двенадцатиперстной кишке, и даже в толстом и тонком кишечнике (например, при хроническом колите). И лечение анемии должно проводиться одновременно с лечением самой язвы. Для этого существует много разных вариантов лечения, в том числе лекарства, снижающие выработку соляной кислоты в желудке. Одним из наиболее эффективных средств, позволяющих значительно быстрее заживить язву, является Ребамипид. Он стимулирует выработку наших собственных противовоспалительных и заживляющих веществ простагландинов. Поэтому «зарастание» или рубцевание язвы происходит быстрее. Если же при обследовании выявили злобную бактерию Хеликобактер, тогда обязательным будет прием 2-х антибиотиков, чтобы убрать ее из организма.
Сергей Вялов, врач-гастроэнтеролог в GMS Clinic, к.м.н. Член Американской гастроэнтерологической ассоциации (AGA) и Российской гастроэнтерологической ассоциации (РГА) источник *Импакт фактор за 2017 г. по данным РИНЦ Журнал входит в Перечень рецензируемых научных изданий ВАК. Гастродуоденальные кровотечения в последнее десятилетие лидируют среди осложнений язвенной болезни [1,4,5]. Большое число работ по этой теме посвящено вопросам гемостаза, прогнозированию повторных кровотечений, выбору метода гемостаза, способам медикаментозной профилактики рецидива [1,4,6]. В этих же источниках отмечен факт поздней госпитализации с момента первого эпизода кровотечения, особенно в тех случаях, когда оно немассивное. Постгеморрагические анемии наблюдаются у большинства больных с длительными сроками неинтенсивного желудочно–кишечного кровотечения (ЖКК), нередко служат веским аргументом в пользу госпитализации пациентов без угрозы рецидива ЖКК и диктуют выбор способа лечения. При успешном консервативном лечении на фоне первичного эндоскопического гемостаза и отсутствии рецидивов в ранние (до 5 сут.) и поздние сроки актуальным является восстановление гемостазиологических показателей крови, которые влияют на сроки заживления и качество рубцевания язвенного дефекта. Особенно важно это у тех пациентов, у которых язвенное ЖКК появляется на фоне хронической анемии или другой патологии [2,3,9]. Активность регенерации слизистой при язвенных поражениях зависит от транспорта кислорода к тканям эритроцитами. Ведущим патогенетическим звеном постгеморрагических анемий является уменьшение общего объема крови, особенно ее циркулирующей фракции, что ведет к гипоксии, сдвигам кислотно–основного состояния, дисбалансу ионов в клетках и вне их. В зависимости от скорости кровопотери выделяют острую и хроническую постгеморрагические анемии [8,10]. источник Язвенная болезнь 12-ти перстной кишки — заболевание двенадцатиперстной кишки хронического рецидивирующего характера, сопровождающееся образованием дефекта в ее слизистой оболочке и расположенных под ней тканях. Проявляется сильными болями в левой эпигастральной области, возникающими через 3-4 часа после еды, приступами «голодных» и «ночных» болей, изжогой, отрыжкой кислотой, часто рвотой. Наиболее грозные осложнения — кровотечение, прободение язвы и ее злокачественное перерождение. Язвенная болезнь двенадцатиперстной кишки – это хроническое заболевание, характеризующееся возникновением язвенных дефектов слизистой ДПК. Протекает длительно, чередуя периоды ремиссии с обострениями. В отличие от эрозивных повреждений слизистой, язвы представляют собой более глубокие дефекты, проникающие в подслизистый слой стенки кишки. Язвенная болезнь двенадцатиперстной кишки встречается у 5-15 процентов граждан (статистика колеблется в зависимости от региона проживания), чаше встречается у мужчин. Язва двенадцатиперстной кишки в 4 раза более распространена, чем язва желудка.
Однако инфицирование хеликобактериями не всегда приводит к развитию заболевания, в большинстве случаев имеет место бессимптомное носительство. Факторы, способствующие развитию язвенной болезни двенадцатиперстной кишки:
Язвы двенадцатиперстной кишки, возникающие в результате приема лекарственных средств или сопутствующие гастриноме, являются симптоматическими и не входят в понятие язвенной болезни. Язвенная болезнь различается по локализации:
По клинической форме различают острую (впервые выявленную) и хроническую язвенную болезнь. По фазе выделяют периоды ремиссии, обострения (рецидив) и неполной ремиссии или затухающего обострения. Язвенная болезнь может протекать латентно (без выраженной клиники), легко (с редкими рецидивами), среднетяжело (1-2 обострения в течение года) и тяжело (с регулярными обострениями до 3х и более раз в год). Непосредственно язва двенадцатиперстной кишки различается по морфологической картине: острая или хроническая язва, небольшого (до полусантиметра), среднего (до сантиметра), крупного (от одного до трех сантиметров) и гигантского (более трех сантиметров) размера. Стадии развития язвы: активная, рубцующаяся, «красного» рубца и «белого» рубца. При сопутствующих функциональных нарушениях гастродуоденальной системы также отмечают их характер: нарушения моторной, эвакуаторной или секреторной функции. У детей и лиц пожилого возраста течение язвенной болезни иногда практически бессимптомное либо с незначительными проявлениями. Такое течение чревато развитием тяжелых осложнений, таких как перфорация стенки ДПК с последующим перитонитом, скрытое кровотечение и анемия. Типичная клиническая картина язвенной болезни двенадцатиперстной кишки – это характерный болевой синдром. Боль чаще всего умеренная, тупая. Выраженность боли зависит от тяжести заболевания. Локализация, как правило, с эпигастрии, под грудиной. Иногда боль может быть разлитой в верхней половине живота. Возникает зачастую ночью (в 1-2 часа) и после продолжительных периодов без приема пищи, когда желудок пуст. После приема пищи, молока, антацидных препаратов наступает облегчение. Но чаще всего боль возобновляется после эвакуации содержимого желудка. Боль может возникать по несколько раз в день на протяжении нескольких дней (недель), после чего самостоятельно проходить. Однако с течением времени без должной терапии рецидивы учащаются, и интенсивность болевого синдрома увеличивается. Характерна сезонность рецидивов: обострения чаще возникают весной и осенью. Основные осложнения язвы двенадцатиперстной кишки – это пенетрация, перфорация, кровотечение и сужение просвета кишки. Язвенное кровотечение возникает, когда патологический процесс затрагивает сосуды желудочной стенки. Кровотечение может быть скрытым и проявляться только нарастающей анемией, а может быть выраженным, кровь может обнаруживаться в рвоте и проявляться при дефекации (черный или с кровавыми прожилками кал). В некоторых случаях произвести остановку кровотечения можно в ходе эндоскопического исследования, когда источник кровотечения иногда удается прижечь. Если язва глубокая и кровотечение обильное – назначают хирургическое лечение, в остальных случаях лечат консервативно, корректируя железодефицит. При язвенном кровотечении пациентам прописан строгий голод, питание парентеральное.
Это – экстренное состояние, которое без должной медицинской помощи ведет к развитию шока и смерти. Перфорация язвы – это показание к срочному оперативному вмешательству. Пенетрация язвы – это глубокий дефект, поражающий стенку кишки с проникновением в смежные органы (печень или поджелудочную железу). Проявляется интенсивной болью колющего характера, которая может локализоваться в правом или левом подреберье, иррадиировать в спину в зависимости от месторасположения пенетрации. При изменении положения боль усиливается. Лечение в зависимости от тяжести консервативное, либо – при отсутствии результата – оперативное. Стеноз двенадцатиперстной кишки возникает при выраженном отеке изъязвленной слизистой или формировании рубца. При сужении просвета возникает непроходимость (полная или частичная) двенадцатиперстной кишки. Зачастую она характеризуется многократной рвотой. В рвотных массах определяется пища, принятая задолго до приступа. Также из симптоматики характерна тяжесть в желудке (переполнение), отсутствие стула, вздутие живота. Регулярная рвота способствует снижению массы тела и обменным нарушениям, связанным с недостаточностью питательных веществ. Чаще всего консервативное лечение ведет к уменьшению отечности стенок и расширению просвета, но при грубых рубцовых изменениях стеноз может приобрести постоянный характер и потребовать оперативного вмешательства.
Наиболее информативным методом диагностики является гастроскопия – эндоскопическое исследование слизистых оболочек желудка и двенадцатиперстной кишки. Оно дает детальную информацию о локализации язвы и ее морфологических особенностях, выявляет кровотечение и рубцовые изменения. При эндоскопическом исследовании возможно произвести биопсию тканей желудка и ДПК для гистологического исследования. При рентгенологическом обследовании с контрастным веществом язвенная болезнь двенадцатиперстной кишки проявляется, как дефект стенки (бариевая смесь проникает в язву и это видно на рентгенограмме), обнаруживается стеноз кишки, перфорации и пенетрации язв. Для выявления инфицированности хеликобактериями применяют ПЦР-диагностику и уреазный дыхательный тест. При лабораторном исследовании крови можно обнаружить признаки анемии, которая говорит о наличии внутреннего кровотечения. На скрытую кровь исследуют также каловые массы. Лечение язвы двенадцатиперстной кишки проводится строго по назначению врача-гастроэнтеролога, самолечение недопустимо в связи с тем, что самостоятельный прием препаратов, способствующих избавлению от боли ведет стуханию симптоматики и латентному развитию заболевания, что грозит осложнениями. Медикаментозная терапия язвенной болезни двенадцатиперстной кишки включает в себя меры по эрадикации Helicobacter и заживлению язвенных дефектов (чему способствует понижение кислотности желудочного сока). Для подавления хеликобактерной инфекции применяют антибиотики широкого спектра действия (метронидазол, амоксициллин, кларитромицин), проводят антибиотикотерапию с течение 10-14 дней. Для снижения секреторной деятельности желудка оптимальными препаратами являются ингибиторы протонной помпы – омепразол, эзомепразол, ланзопразол, рабепразол. С той же целью применяют средства, блокирующие Н2-гистаминовые рецепторы слизистой желудка: ранитидин, фамотидин. В качестве средств, понижающих кислотность желудочного содержимого, применяют антациды. Гелевые антациды с анестетиками эффективны и в качестве симптоматически препаратов – облегчают боль, обволакивая стенку кишки. Для защиты слизистой применяют гастропротективные средства: сукральфат, препараты висмута, мизопростол. При неэффективности консервативного лечения или в случае развития опасных осложнений прибегают к оперативному лечению. Операция заключается в иссечении или ушивании язвы двенадцатиперстной кишки. При необходимости для понижения секреции проводят ваготомию. Меры профилактики развития язвенной болезни двенадцатиперстной кишки:
Неосложненная язвенная болезнь при должном лечении и соблюдении рекомендаций по диете и образу жизни имеет благоприятный прогноз, при качественной эрадикации – заживление язв и излечение. Развитие осложнений при язвенной болезни утяжеляет течение и может вести к угрожающим жизни состояниям. источник
Железодефицитная анемия – наиболее частая форма анемий в гастроэнтерологии, и причиной ее развития являются кровотечения, нарушения всасывания железа, диетические ограничения. Ряд хронических заболеваний пищеварительной системы сопровождается развитием анемии различной степени тяжести. Анемия может являться первым признаком основного заболевания, в частности, опухолевого процесса пищевого канала, а также быть причиной снижения качества жизни пациентов. Выделяют три глобальные причины развития дефицита железа в организме:
Заболевания желудочно-кишечного тракта являются одной из основных причин развития железодефицитной анемии, что обусловлено нарушением всасывания железа в кишечнике или его потерями вследствие эрозивно-язвенных, опухолевых или аутоиммунных воспалительных поражений слизистой оболочки кишечника. Перечень заболеваний пищеварительного тракта, сопровождающихся развитием анемии, достаточно широк. Причиной железодефицитных состояний часто выступают болезни верхних отделов желудочно-кишечного тракта и толстой кишки. Одной из важных причин развития железодефицитной анемии является нарушение процессов всасывания железа в двенадцатиперстной кишке и проксимальном отделе тощей кишки. Различные заболевания тонкой кишки, сопровождающиеся синдромом мальабсорбции (энтерит, амилоидоз, целиакея, идеопатическая стеаторея), а также оперативные вмешательства на желудке и тонкой кишке (состояние после тотальной гастроэктомии, субтотальной резекции желудка, ваготомии с гастроэктомией, резекция тонкой кишки) приводят к развитию дефицита железа. Накапливаются данные о потенциальной связи инфекции H. pylory с железодефицитной анемией, которая может быть следствием скрытых кровотечений при эрозивном гастрите и язвенной болезни, нарушение всасывания железа при хеликобактерном атрофическом пангастрите, а также снижения содержания аскорбиновой кислоты в желудке и конкурентного захвата и утилизации железа самой бактерией. Таким образом, эрадикация H. pylory может стать еще одним подходом к лечению железодефицитной анемии в отсутствии других явных ее причин. Этиологическим фактором анемии может стать прием нестероидных противовоспалительных препаратов (НПВП). Врачам хорошо известна возможность как массивных, так и скрытых кровотечений из эрозий и язв желудка и двенадцатиперстной кишки при НПВП-гастропатии. Однако, железодефицитная анемия может быть следствием НПВП-энтеропатии, другими клиническими проявлениями которой могут служить гипоальбуминемия, мальабсорбция и наличие измененной крови в кале. Причиной нарушения всасывания гемопоэтических факторов являются и заболевания тонкой кишки. К ним можно отнести целиакию (половина пациентов с неясной этиологией железодефицитной анемии, резистентной к терапии препаратами железа), резекцию участка тонкой кишки, синдром избыточного бактериального роста в тонкой кишке, диабетическую энетропатию, амилоидоз, склеродермию, болезнь Уиппла, туберкулез, лимфому тонкой кишки, тропическое спру, паразитарные заболевания (лямблиоз) и гельминтозы (дифиллоботриоз). Воспалительные заболевания кишечника, прежде всего, неспецифический язвенный колит и болезнь Крона, часто сопровождаются развитием анемии. Ведущими механизмами при этом выступают кровопотеря у пациентов с язвенным колитом и болезнью Крона, а также мальабсорбция при вовлечении в процесс тощей и подвздошной кишки при болезни Крона. Ведущей причиной анемии при патологии нижних отделов желудочно-кишечного тракта, особенно у пациентов старше 50 лет, служит колоректальный рак. Хроническая кровопотеря наблюдается при полипах толстой кишки, дивертикулезе, ишемическом колите, геморрое и анальных трещинах. Анемический синдром часто делает необходимым тщательное обследование желудочно-кишечного тракта. Для уточнения вида анемии проводят исследования общего и биохимического анализа крови. Среди причин железодефицитной анемии (почти 30-50% всех случаев) прежде всего рассматривают острые или хронические кровопотери из желудочно-кишечного тракта. Причины железодефицитной анемии Как показали результаты открытого мультицентрового исследования, проведенного в Украине в 2008 году и базировавшиеся на анализе 1299 историй болезней больных железодефицитной анемией, основной причиной развития были эрозивно-язвенные поражения пищевого канала (44,58%) и заболевания, сопровождающиеся синдромом мальабсорбции. Циррозы печени являлись причиной железодефицитной анемии в 10,39% случаев, воспалительные заболевания кишечника – 4,54% больных. Диагностируется железодефицитная анемия у больных с гастроэнтерологическими заболеваниями по совокупности анамнестических данных (указания на оперативные вмешательства на желудке или кишечнике, прием нестероидных или гормональных противовоспалительных препаратов, антикоагулянтов и антиагрегантов, язвенный анамнез, наличие хронических заболеваний печени и воспалительных заболеваний кишечника и т.д.), клинических проявлений (наличие специфического сидеропенического синдрома, проявляющегося сухостью и истончением кожи, ангулярный хейлит, дисфагия, ломкость ногтей, их поперечная исчерченность, вогнутость ногтевой пластинки, извращение вкуса и обоняния, симптом «голубых склер», мышечная слабость) и лабораторных показателей. Диагностика анемии основывается, главным образом, на данных лабораторных исследований, в первую очередь – на результатах клинического исследования крови с определением концентрации гемоглобина. |




 Современная теория развития язвенной болезни считает ключевым фактором в ее возникновении инфекционное поражение желудка и двенадцатиперстной кишки бактериями Helicobacter Pylori. Эта бактериальная культура высевается при бактериологическом исследовании желудочного содержимого у 95% больных с язвой двенадцатиперстной кишки и у 87% пациентов, страдающих язвенной болезнью желудка.
Современная теория развития язвенной болезни считает ключевым фактором в ее возникновении инфекционное поражение желудка и двенадцатиперстной кишки бактериями Helicobacter Pylori. Эта бактериальная культура высевается при бактериологическом исследовании желудочного содержимого у 95% больных с язвой двенадцатиперстной кишки и у 87% пациентов, страдающих язвенной болезнью желудка. Перфорация язвы двенадцатиперстной кишки (как правило, передней стенки) приводит к проникновению ее содержимого в брюшную полость и воспалению брюшины – перитониту. При прободении стенки кишки обычно возникает резкая режуще-колющая боль в эпигастрии, которая быстро становится разлитой, усиливается при смене положения тела, глубоком дыхании. Определяются симптомы раздражения брюшины (Щеткина-Блюмберга) – при надавливании на брюшную стенку, а потом резком отпускании боль усиливается. Перитонит сопровождается гипертермией.
Перфорация язвы двенадцатиперстной кишки (как правило, передней стенки) приводит к проникновению ее содержимого в брюшную полость и воспалению брюшины – перитониту. При прободении стенки кишки обычно возникает резкая режуще-колющая боль в эпигастрии, которая быстро становится разлитой, усиливается при смене положения тела, глубоком дыхании. Определяются симптомы раздражения брюшины (Щеткина-Блюмберга) – при надавливании на брюшную стенку, а потом резком отпускании боль усиливается. Перитонит сопровождается гипертермией. При опросе выявляется характер болевого синдрома, его связь с приемами пищи, сезонность приступов, сопутствующая симптоматика. При дуоденальном зондировании получают данные о состоянии среды ДПК.
При опросе выявляется характер болевого синдрома, его связь с приемами пищи, сезонность приступов, сопутствующая симптоматика. При дуоденальном зондировании получают данные о состоянии среды ДПК. Анемия В практике гастроэнтеролога анемический синдром встречается достаточно часто. При этом основными видами анемий у пациентов с патологией органов пищеварения являются железодефицитная и В12-фолиеводефицитная анемии. В патогенезе анемий при заболеваниях желудочно-кишечного тракта ведущими механизмами выступают хроническая кровопотеря и нарушение всасывания гемопоэтических факторов.
Анемия В практике гастроэнтеролога анемический синдром встречается достаточно часто. При этом основными видами анемий у пациентов с патологией органов пищеварения являются железодефицитная и В12-фолиеводефицитная анемии. В патогенезе анемий при заболеваниях желудочно-кишечного тракта ведущими механизмами выступают хроническая кровопотеря и нарушение всасывания гемопоэтических факторов.