Наследственные гемолитические анемии — результат врожденного дефекта гемоглобина, ферментов или мембран эритроцитов. Соответственно выделяют три группы наследственных гемолитических анемий:
- Гемоглобинопатии (серповидноклеточная анемия, гемоглобинопатия HbSC).
- Ферментопатии (анемии при недостаточности глюкозо-6-фосфат дегидрогеназы).
- Мембранопатии (наследственный микросфероцитоз, овалоцитоз и пойкилоцитоз).
Серповидноклеточная анемия — наследственное заболевание системы крови, характеризующееся генетическим дефектом, в результате которого происходит нарушение строения белка гемоглобина (гемоглобинопатия). Образующийся при этом аномальный гемоглобин S (HbS) отличается по своим электрофизиологическим свойствам от нормального гемоглобина (HbA) здорового человека, в результате чего изменяются и сами эритроциты, приобретая характерную удлиненную форму, под микроскопом напоминающую серп (отсюда и название заболевания).
Серповидноклеточная анемия — заболевание, развивающееся у гомозигот по аллелю, кодирующему гемоглобин S, имеющий структурные аномалии молекулы гемоглобина и способный к полимеризации при отдаче кислорода или снижении его парциального давления. В эритроцитах образуются волокна (тактоиды), формирующие студенистую сеть, изменяющие форму эритроцитов на серповидную и повышающие их жесткость, что затрудняет прохождение эритроцитов по мелким сосудам. Как следствие возникает закупорка этих сосудов, и развиваются многочисленные инфаркты в селезенке, легких, почках и головном мозге.
Заболевание проявляется обычно в детском возрасте. Характерны бледность, утомляемость, задержка роста, повышенная чувствительность к инфекциям. В результате хронического гемолиза развиваются желтуха и желчнокаменная болезнь.
Характерными симптомами анемии являются трофические язвы голеней, приапизм, повторные инфаркты легких, хроническое легочное сердце, некроз почечных сосочков, обусловленные ухудшением реологических свойств крови. Возможно развитие кровоизлияний в сетчатку с последующими рубцеванием и отслойкой сетчатки.
Заболевание является хроническим. Течение заболевания нередко осложняется инфекцией, в частности сальмонеллезом, приводящим к остеомиелиту. Иногда возникает асептический некроз головки бедренной кости. Тяжелым осложнением и у детей, и у взрослых является инсульт.
Нередко развиваются угрожающие жизни больных острые кризы. Самый частый из них — болевой криз. Боль локализуется в спине, конечностях и ребрах, длится несколько дней или недель, сопровождается лихорадкой, но концентрация гемоглобина в крови нормальная. Возможно развитие острого синдрома грудной клетки, проявляющегося болью в грудной клетке, легочными инфильтратами и гипоксией.
У детей, а иногда и у взрослых, со спленомегалией развиваются секвестрационные кризы, характеризующиеся депонированием крови в селезенке и сопровождающиеся артериальной гипотонией и шоком, падением концентрации гемоглобина в крови.
Редко развиваются гемолитические кризы, характеризующиеся вторичной желтухой и снижением концентрации гемоглобина в крови.
При вирусной инфекции (обычно парвавирусе В19) развиваются апластические кризы, сопровождающиеся резким снижением гемоглобина и уменьшением количества ретикулоцитов в периферической крови.
Сходные клинические проявления имеет гемоглобинопатия HbSC. Она протекает менее тяжело, но с выраженной спленомегалией.
Гемоглобин S при серповидноклеточной анемии выявляют после обработки эритроцитов метабисульфатом натрия, что приводит к отдаче кислорода. С помощью электрофореза (более точный метод) можно количественно определить гемоглобин S и отличить гомозиготную от гетерозиготной анемии или от других аномалий строения гемоглобина.
Гемоглобин при серповидноклеточной анемии снижен до 50–100 г/л, при гетерозиготности по HbS его уровень нормальный. Средний эритроцитарный объем может быть увеличенным, наблюдается непрямая гипербилирубинемия и нейтрофильный лейкоцитоз, количество тромбоцитов повышено.
В мазках периферической крови выявляют серповидные эритроциты, иногда тельца Говела–Жолли и мишеневидные эритроциты.
Специфическим методом лечения является лечение гидроксимочевиной, повышающей уровень фетального гемоглобина и снижающей уровень гемолиза. Эффективность препарата усиливается назначением эритропоэтина. Этот метод лечения применяют только больным с тяжелой анемией.
Основное лечение направлено на предупреждение острых и хронических осложнений. Не следует допускать обезвоживания, длительного пребывания на большой высоте.
Детям от 3-х месяцев до 5 лет показано введение менингококковой вакцины и вакцины против Haemophilus influenza типа В. Детям старше 5 лет назначают профилактическую терапию пенициллином по 125–250 мг внутрь ежедневно. В случае лихорадки срочно проводят интенсивную противомикробную терапию.
Всем больным с хронической гемолитической анемией назначают фолиевую кислоту 1 мг внутрь 1 раз в сутки.
При болевом кризе в/в вводят жидкость и проводят обезболивающую терапию анальгетиками. Наиболее эффективны длительные инфузии морфина. Но следует помнить о склонности больных с рецидивирующим болевым синдромом к наркотической зависимости. Переливание крови не устраняет боль, повторные же переливания могут привести к гемосидерозу.
При остром синдроме грудной клетки проводят ингаляции кислорода и инфузионную терапию и назначают антибиотики широкого спектра действия (цефтриаксон и эритромицин). При снижении РаО2 в крови ниже 60 мм рт. ст. проводят обменное переливание крови.
Лечение секвестрационного криза направлено на восстановление гемодинамики. Основным лечением апластического криза является трансфузионная терапия.
Лечение остеомиелита проводят с учетом результата бактериологического исследования биопсийного материала. Трофические язвы голени лечат возвышенным положением нижних конечностей, интенсивными местными воздействиями и при отсутствии эффекта проводят трансфузионную терапию и пересадки полнослойных лоскутов кожи. Приапизм устраняется регидратационной терапией или хирургической декомпрессией.
Излечение от серповидноклеточной анемии у некоторых больных возможно с помощью аллотрансплантации костного мозга. Но отбор для этого лечения сложен и широко не применяется. В настоящее время интенсивно развиваются методы генотерапии.
Ферментопатические гемолитические анемии — группа заболеваний, обусловленных дефицитом активности эритроцитарных ферментов. Врожденный дефицит ферментов (пируваткиназы, глюкозо-6-фосфатизомеразы, гексокиназы, глюкозо-6-фосфатдегидрогеназы) приводит к развитию анемии. Чаще всего встречается дефицит глюкозо-6-фосфатдегидрогеназы.
Нормальные эритроциты защищены от действия окислителей за счет метаболизма глюкозы по пентозофосфатному пути, являющемуся источником восстановленного глутатиона, препятствующего окислению сульфгидрильных групп гемоглобина и мембраны эритроцитов. Образующиеся свободные радикалы кислорода при контакте с токсинами или лекарствами в эритроцитах резко увеличивают метаболизм глюкозы по этому пути.
При недостаточности глюкозо-6-фосфатдегидрогеназы в эритроцитах не образуется необходимое количество восстановленного глутатиона, что приводит к окислению сульфгидрильнх групп гемоглобина с образованием телец Гейнца и мембран эритроцитов и развитию хронического или эпизодического гемолиза.
Гем глюкозо-6-фосфатдегидрогеназы расположен на Х-хромосоме. Поэтому недостаточность глюкозо-6-фосфатдегидрогеназы наследуется сцеплено с Х-хромосомой главным образом у мужчин — выходцев из Африки, Средиземноморья и Китая. У женщин заболевание наблюдается редко.
Гемолитические кризы — основное клиническое проявление этой ферментопатической анемии — развиваются обычно быстро, в течение нескольких часов и только под действием провоцирующих факторов. К ним относятся лекарственные средства (сульфаниламиды, хинин, нитрофурантоин, аспирин, феназопиридин), инфекции и бобы, принимаемые с пищей.
Содержание глюкозо-6-фосфатдегидрогеназы снижено главным образом в стареющих эритроцитах, и они более подвержены гемолизу. В момент криза в мазках периферической крови выявляются тельца Гейнца. Характерно быстрое снижение гематокрита, повышение в плазме концентрации свободного гемоглобина и непрямого билирубина и снижение уровня гаптоглобина. Гемолитический криз проходит быстро, обычно самостоятельно после разрушения старых эритроцитов.
К концу первых суток тельца Гейнца удаляются селезенкой. После их удаления в крови появляются эритроциты с полукруглыми краевыми дефектами («укусы» эритроцитов), фрагменты эритроцитов и небольшое количество микросфероцитов. После криза уровень глюкозо-6-фосфатдегидрогеназы может нормализоваться за счет преобладания в крови популяции молодых эритроцитов. Активность фермента следует определить через 1,5–2 мес после криза.
Основное внимание следует уделить профилактике гемолитических кризов: лечению инфекции, исключению приема некоторых лекарственных средств и употребления в пищу бобов. Гемотрансфузии проводят по строгим показателям. Во время кризов с гемоглобинурией проводят адекватную гидратацию для поддержания нормальной функции почек.
Мембранопатии — наследственные заболевания, характеризующиеся структурными аномалиями белков эритроцитов, приводящими к нарушениям структуры их мембран и внесосудистому гемолизу. Различают три формы наследственных мембранопатий: микросфероцитоз, овалоцитоз и стоматоцитоз.
Заболевание наследуется в большинстве случаев по аутосомно-доминантному типу и характеризуется дефектом одного из белков цитоскелета эритроцитов, приводящим к потере части их мембраны с уменьшением отношения площади к объему. Эритроциты превращаются в микросфероциты, имеющие средний диаметр меньше 6,3 мкм и среднюю толщину больше 2,1 мкм.
Наследственный микросфероцитоз может выявиться как у детей, так и у взрослых. У больных находят синдром анемии, желтуху и спленомегалию. Желтуха сопровождается образованием пигментных камней в желчном пузыре и желчевыводящих путях даже у детей. В костном мозге развивается гиперплазия эритроидного ростка.
Анемия нормохромная, умеренная (гемоглобин 90–100 г/л). В мазке крови выявляют микросфероциты — мелкие клетки без центрального просветления. Характерна способность микросфероцитов к гемолизу в гипотонических растворах меньшей концентрации в отличие от нормальных эритроцитов. Секвестрация микросфероцитов происходит в селезенке.
Диагностическое значение имеет спонтанный гемолиз — число эритроцитов, разрушившихся после инкубации крови в течение 48 ч. У здоровых людей он не превышает 4%, у больных с наследственным микросфероцитозом достигает 15–50%. Спонтанный гемолиз при добавлении в кровь глюкозы резко снижается. Прямая проба Кумбса отрицательная в отличие от аутоиммунной гемолитической анемии, при которой она положительна.
Клиническое выздоровление наступает после спленэктомии, хотя микроцитоз остается, но гемолиз значительно уменьшается. С профилактической целью назначают длительно фолиевую кислоту (1 мг/сут внутрь). При наличии желчнокаменной болезни после спленэктомии решается вопрос о холецистэктомии.
Наследственный овалоцитоз — заболевание, сопровождающееся появлением в крови большого количества овалоцитов. В периферической крови здоровых лиц количество их составляет 5–10%, а у больных колеблется от 25 до 90%. Овалоцитоз наследуется по аутосомно-доминантному типу.
Ведущее значение в патогенезе заболевания имеет структурная аномалия спектрина, приводящая к образованию измененного цитоскелета эритроцитов. Возможна недостаточность белка 4,1 цитоскелета, связывающего спектрин и актин. В результате имеющие двояковогнутую форму диски эритроцитов после прохождения микроциркуляторного русла становятся овальными и не восстанавливают свою прежнюю форму. Овалоциты разрушаются главным образом в селезенке.
У большинства больных овалоцитоз обнаруживается случайно при исследовании периферической крови или проявляется легким гемолизом с нормальной концентрацией гемоглобина (больше 120 г/л). Концентрация гемоглобина может быть сниженной. У 10–15% больных выявляется тяжелое течение заболевания, характеризующееся интенсивным гемолизом. Концентрация гемоглобина снижается до 90–100 г/л и ниже, продолжительность жизни половины эритроцитов составляет 5 сут. В периферической крови обнаруживают микроовалоциты, пойкилоциты и шизоциты.
Лечение наследственного овалоцитоза аналогично лечению наследственного микросфероцитоза. Основное значение имеет спленэктомия, устраняющая гемолиз.
Наследственный стомацитоз — заболевание, при котором эритроциты имеют специфическую форму — выпуклые с одной стороны и вогнутые с другой и имеют щелевидное пространство в окрашенном мазке крови.
Существует две формы эритроцитов:
- гипергидратированные стоматоциты (гидроциты) с высоким содержанием ионов натрия и воды и низкой средней концентрацией гемоглобина;
- дегидратированные стоматоциты (ксероциты) с низким содержанием ионов натрия и воды, и высокой средней концентрацией гемоглобина.
Гидроциты выглядят в окрашенных мазках крови как типичные стоматоциты, а ксероциты сморщенные и имеют вид мишеней. Стоматоциты имеют укороченную продолжительность жизни.
Клиника наследственного стоматоцитоза проявляется спленомегалией и легким гемолизом. Спленэктомия полностью гемолиз не устраняет.
источник
Гемолитические анемии (ГА) — это анемии, обусловленные усиленным разрушением эритроцитов — гемолизом. ГА различаются по механизму развития гемолиза, внутриклеточный или внутрисосудистый; течению заболевания: скорость развития анемии может варьировать от нескольких минут или часов до нескольких дней, носить постоянный или рецидивирующий характер; методом диагностики и лечения.
К ГА с внутриклеточным механизмом гемолиза относятся:
1. наследственная мембранопатия эритроцитов (микросфероцитоз – болезнь Минковского-Шоффара, элиптоцитоз, стоматоцитоз, акантоцитоз);
2. врожденные ферментопатии эритроцитов (кроме дефицита Г-6-ФД);
3. наследственная гемоглобинопатии (талассемии, серповидно-клеточные анемии);
4. иммунные ГА, кроме гемолизиновой формы аутоиммунной ГА;
5. анемии при гиперспленизме.
К ГА с внутрисосудистым механизмом гемолиза относятся:
1. врожденная ГА, с дефицитом Г-6-ФД (фавизм);
2. пароксизмальноя ночная гемоглобинурия болезнь Маркиафавы-Микели);
3. гемолизиновая форма аутоиммунной ГА;
4. приобретенные неиммунные ГА: микроангиопатические, обусловленные механическим повреждением эритроцитов при протезировании сосудов или клапанов сердца, стенозе аортального клапана, злокачественной гипертензии, ДВС-синдроме, гемолитико-уремическом синдроме, гемангиомах; токсические – при отравлении гемолитическими ядоми: уксусной кислотой, пчелиным, змеиным; при разрушении эритроцитов – паразитоми (малярия).
В стернальном пунктате: резкая гиперплазия эритроидного ростка; на высоте гемолитического криза, если возникает относительная недо- статочность фолиевой кислоты, появляются признаки мегало -бластического кроветворения.
Наследственные гемолитичесие анемии, связанные с нарушением структуры мембраны эритроцитов (мембранопатии )
Мембранные дефекты (наследственный сфероцитоз, эллиптоцитоз) – дефект Na + -K + -АТФазы ® набухание эритроцитов ® осмотически нестойкие ® гемолиз в селезенке
— микросфероцитоз (б-нь Минковского-Шоффара) – снижение осмотической резистентности
— овалоцитоз – снижение осмотической резистентности
— стоматоцитоз – нарушение белковой структуры мембраны (Na активно поступает в клетку)
— акантоцитоз, эхиноцитоз — дефект липидной части мембраны при а-b-липопротеинемии
Наследственные гемолитические анемии, связанные с нарушением структуры или синтеза
гемоглобина (гемоглобинопатии)
— Талассемии (количественные гемоглобинопатии)
— Гемоглобинопатии (известно более 300 заболеваний, обусловленных точечными мутациями генов глобина)
— Серповидноклеточная анемии (полимеризация HbS деформация эритроцита хронический гемолиз;
— HbC, HbE, HbO и смешанные формы – синдром «серповидноклеточной анемии» (менее тяжелые)
— a-талассемия – дефект синтеза a-цепи (отсутствует мРНК в гене a-цепи глобина). Выделено 4 гена в зависимости от нарушения, выделяют 4 типа (от бессимптомного течения до внутриутробной гибели плода);
— b-таласемия – отсутствие или нарушение строения b-цепи (мРНК мало или дефектная). Выделяют 2 вида:
— гомозиготная – большая таласемия, анемия Кули (тяжелое течение, больные трансфузионнозависимые);
— гетерозиготная – малая талассемия (легкая форма, с редкими кризами)
Диагностика: высокое содержание HbF и HbA2
При количественных гемоглобинопатиях (таласемиях) отмечается снижение синтеза определенной цепи глобина, приводящее к нарушению баланса количества различных цепей глобина, при этом структура цепей не нарушена. В крови больных талассемией обнаруживаются гипо-хромные мишеневидные эритроциты, повышено содержание HbF до 90% (в норме0,5-2%) и HbA2 более3,5% (при норме 1,5-3,5%).
Диагностика ГА, обусловленных гемоглобинопатиями, основана:
a) на исследовании эритроцитов в мазках крови при световой микроскопии и выявлении их характерных морфологических изменений;
b) на выявлении аномальных форм Hb при его электрофоретическом исследовании.
Гемоглобинопатии могут быть структурными, когда нарушается структура Hb – при серповидно-клеточной анемии вместо HbA в эритроцитах присутствует HbS, в котором в 6 положении β-цепи глутаминовая кислота заменяется на валин. Это приводит к изменению свойств Hb. HbS имеет меньшую электрофоретическую подвижность, менее растворим, чем HbA. Выпадая в осадок и превращаясь в гель, он изменяет форму эритроцита. Серповидные эритроциты не могут проходить через капиллярное русло и разрушаются.
Наследственные гемолитические анемии, связанные, с дефицитом ферментов эритроцитов (энзимопатии)
— Дефекты ферментов мембраны и цитоплазмы
— дефицит Г6ФДГ (более 100 подтипов заболевания) – острые кризы
Диагностика ГА этой группы основана на исследовании активности ферментов эритроцитов.
При дефиците Г-6-ФД имеет место внутрисосудистый гемолиз, для которого характерно наличие свободного гемоглобина в плазме крови. Поэтому сыворотка крови больных при стоянии приобретает коричневый цвет за счет образования метгемоглобина. Моча может окрашиваться в черный цвет за счет выделяющегося гемоглобина, метгемоглобина, гемосидерина, уробилина. При специальной суправитальной окраске (нильским синим, метиловым фиолетовым или кристалл-виолетом) в эритроцитах обнаруживаются тельца Гейнца — Эрлиха.
Приобретенные гемолитические анемии
- ГА, обусловленне воздействием АТ
- Болезнь Маркиафавы-Микели (параксизмальная ночная гемоглобинурия)
- ГА, связанные с механическим повреждением эритроцитов.
Иммунные гемолитические анемии – это группа заболеваний, при которых эритроциты крови или эритрокариоциты костного мозга разрушаются антителами, образовавшимися в организме или поступившими извне.
Иммунные ГА делятся на 4 группы.
a) гемолитическая анемия плода и новорожденного – заболевание, связанное с антигенной несовместимостью эритроцитов матери и плода чаще по резус-фактору и группе крови;
b)посттранфузионные ГА, связанные с переливанием несовместимых эритроцитов донора, которые разрушаются имеющимися у реципиента атителами.
2. Трансиммунные ГА – связаны с разрушением эритроцитов плода антителами, поступающими через плаценту от матери, страдающей аутоиммунной ГА, в кровь плода, имеющего те же антигены, что и у матери.
3. Гетероиммунные ГА – обусловленные выработкой антител к чужеродным антигенам:
a) при фиксировании лекарств (ПАСК, феноцетин, пенициллин) на поверхности собственных неизмененных эритроцитов;
b) при фиксировании вирусов на поверхности собственных неизмененных эритроцитов;
c) при изменении антигенной структуры собственных эритроцитов под воздействием лекарств, вирусных инфекций и других факторов.
4. Аутоиммунные ГА – обусловленные выработкой антител к собственным неизмененным антигенам эритроидных клеток.
Аутоиммунные гемолитические анемии
Аутоиммунные ГА – сравнительно часто встречающееся заболевание. Регистрируется с частотой 1случай на 75000-80000 населения в год.
Аутоиммунные гемолитические анемии (АИГА) подразделяются :
A. По принципу клеточной направленности:
— АИГА с антителами к антигенам эритрокариоцитов костного мозга;
— АИГА с антителами к антигенам эритроцитов периферической крови;
B. По принципу связи с другими заболеваниями:
— симптоматические АИГА – при острыхи хронических лимфолейкозах, миеломной болезни, лимфогранулематозе, тимоме, системной красной волчанке, хроническом гепатите, неспецифическом язвенном колите, инфекционном мононуклеозе и пр.
C. По серологическому принципу:
— АИГА, связанные с неполными тепловыми агглютининами;
— АИГА, связанные с тепловыми геиолизинами;
— АИГА, связанные с полными холодовыми агглютининами;
— АИГА, связанные с двухфазными холодовыми агглютининами.
Диагноз АИГА основывается на выявлении аутоантител при проведении пробы Кумбса.
При помощи прямой пробы Кумбса определяют антитела, фиксированные на эритроцитах – антиглобулиновые антитела втупают во взаимодействие с иммуноглобулинами эритроцитов и вызывают их агглютинацию. Положительная прямая проба Кумбса отмечается у большинства больных АИГА, ее выраженность тесно коррелирует с количеством IgG, фиксированного на эритроцитах.
Отрицательная проба Кумбса не исключает диагноз АИГА и может быть следствием недостаточного количества антител (менее 500 молекул IgG на эритроците) при нетяжелом хроническом течении заболевания, при обострении, когда после гемолитического криза многие эритроциты разрушены, при гормональной терапии. Кроме того, недостаточное отмывание эритроцитов при выполнении пробы приводит к тому, что на поверхности эритроцитов остаются сывороточные иммуноглобулины, нейтролизующие антиглобулиновую сыворотку; часть антител с поверхности эритроцитов может теряться в процессе отмывания.
Непрямая проба Кумбса, выявляет антиэритроцитарные антитела, циркулирующие в сыворотке крови, не имеет большого значения для диагностики АИГА. Она положительна у большинства лиц, которым длительно применялись гемотрансфузии.
Более чувствительной является агрегат-гемагглютинационная проба. Ее чувствительность выше чувствительности пробы Кумбса в 64-128 раз. Значительно более чувствительный анти-антиглобулиновый вариант агрегат-гемагглютинационной пробы – в 1000 раз превышает чувствительность пробы Кумбса. Однако, из-за трудоемкости эти методы редко применяются в клинической практике.
Установлено, что от класса иммуноглобулинов может зависеть острота гемолиза, место преимущественной деструкции эритроцитов. При одновременном участии в патологическом процессе нескольких классов иммуноглобулинов отмечается усиление гемолиза. Использование иммуноферментного анализа позволяет выявить иммуноглобулины на поверхности эритроцитов, определить их класс и тип, оценить их количество. В настоящее время применяется гелевый тест, аналогичный пробе Кумбса, но более чувствительный. Метод не требует отмывания эритроцитов, так как гель разделяет эритроциты и плазму.
При гемолизиновой форме АИГА сыворотка крови больного вызывает гемолиз эритроцитов донора, в крови обнаруживаются гемолизины, имеются признаки внутрисосудистого гемолиза.
источник
Мембранопатии (микросфероцитоз, овалоцитоз, эллиптоцитоз).
Ферментопатии (дефицит ферментов гликолиза, пентозофосфатного цикла, системы глютатиона).
Гемоглобинопатии (Талассемия, серповидноклеточная анемия).
Мембранопатии – заболевания, наследуемые по аутосомно-доминантному типу, при которых время жизни эритроцитов уменьшено в связи с дефектом белков или липидов их оболочки.
Сфероцитоз – заболевание, в основе которого лежит дефект белка спектрина мембраны эритроцитов.
Дефектная мембрана становится проницаемой для ионов натрия, что приводит к накоплению в эритроцитах воды. Клетки приобретают сферическую форму, теряется их способность к деформации при прохождении в капиллярах. Такие эритроциты частично
элиминируются, частично повреждаются в селезенке.
Для клиники характерны три синдрома: анемический, желтухи и спленомегалии.
Анемия проявляется обычно в подростковом возрасте. Тяжелое ее течение наблюдается в раннем детском возрасте, особенно у новорожденных и может приводить к нарушениям физического и умственного развития, гипогонадизму.
Для желтухи характерно увеличение содержания непрямого билирубина в сыворотке крови. Степень ее зависит от степени разрушения эритроцитов и функциональной способности печени выводить билирубин в желчь. При небольшом гемолизе желтуха может не выявляться. Повышенное выведение билирубина с желчью обусловливает частое осложнение сфероцитоза – образование камней в желчном пузыре и протоках. В результате застоя желчи развиваются билиарный гепатит и цирроз. Анемия в сочетании с желтухой обусловливают лимонно-желтую окраску кожи у больных. Моча имеет темную окраску (увеличение образования и выведения уробилиногена), за счет увеличения образования стеркобилиногена кал также имеет темно-коричневую окраску.
Спленомегалия обычно умеренная, обусловлена гиперплазией.
Для наследственного сфероцитоза характерны деформации скелета – башенный череп, высокое небо, широкая переносица, аномалии глаз, зубов, отосклероз.
Под влиянием инфекций может развиться гемолитический криз, проявляющийся резким ухудшением состояния, повышением температуры тела, увеличение тяжести анемии, желтухи, нарастание уробилинурии. Опасным осложнением является гипопластический криз.
В периферической крови – умеренной степени нормохромная анемия, в случае развития гемолитического или гипопластического криза уровень гемоглобина может снижаться до 20-30 г/л. ЦП обычно близок к 1.Эритроциты имеют характерную форму – они шарообразны, без центрального просветления (сфероциты). Количество ретикулоцитов увеличивается, при гипопластическом кризе отсутствует.Во время гемолитического криза возможен лейкоцитоз со сдвигом влево.
Для сфероцитоза характерно снижение осмотической стойкости эритроцитов, одновременно повышен аутогемолиз и удлинена кислотная эритрограмма.
В костном мозге – компенсаторная гиперплазия красного ростка с выраженной эритронормобластической реакцией. При гипопластическом кризе – эритробластопения.
В плазме крови повышено содержание непрямого билирубина. Высокая билирубинемия (выше 120 мМ/л) и появление прямого билирубина могут свидетельствовать о заболевании печени и механической желтухе.
Уровень уробилиногена в моче иногда повышается, чаще нормальный (зависит от функции печени), увеличивается образование стеркобилина.
Продолжительность жизни меченых эритроцитов больных сфероцитозом в крови здоровых людей уменьшена.
Дифференцируют сфероцитоз с заболеваниями, сопровождающимися желтухой и спленомегалией (гепатиты, цирроз печени, гипербилирубинемия Жильбера) и анемиями, при которых наблюдается симптоматический сфероцитоз (аутоиммунная гемолитическая анемия, дизэритропоетическая анемия).
Единственным эффективным методом лечения является спленэктомия, после нее остаются сфероциты, но ликвидируется анемия (удаляется орган, в котором разрушаются дефектные эритроциты). Больные становятся практически здоровыми. Больным в возрасте до 25 лет рекомендуется удаление селезенки вне зависимости от уровня гемоглобина во избежание тяжелых осложнений.
Показаниями к спленэктомии независимо от возраста являются:
Наличие гемолитических и гипопластических кризов.
Осложнение заболевания ЖКБ с приступами печеночной колики или холестатическим гепатитом.
Переливание эритроцитарной массы – только по жизненным показаниям.
Ферментопатии – рецессивно наследуемый дефект активности одного из ферментов, участвующих в гликолизе, пентозофосфатном цикле или системе глутатиона.
Патогенез анемии при дефекте ферментов гликолиза связан с нарушением образования АТФ в эритроцитах, жизнеспособность которых снижается, изменяется ионный состав и они разрушаются макрофагами селезенки и печени. Дефект активности ферментов пентозофосфатного цикла или системы глутатиона вызывает изменения липидов мембраны, которая неспособна противостоять действию окислителей. После приема некоторых препаратов (сульфаниламиды, антималярийные, производные изоникотиновой кислоты), бобов такие эритроциты гемолизируются.
Клиника – Анемия различной степени выраженности, желтуха, спленомегалия.
Основной критерий для дифференциальной диагностики – обнаружение ферментного дефекта эритроцитов.
Лечение необходимо лишь в случаях выраженной анемии, особенно при гемолитических кризах и соответствует принципам терапии ДВС-синдрома при внутрисосудистом гемолизе. При постоянном хроническом гемолизе частичный эффект дает спленэктомия.
Обычно энзимопатии протекают благоприятно, хотя не излечиваются. Больные должны находиться на диспансерном учете, с осторожностью принимать препараты, вызывающие гемолиз.
Гемоглобинопатии – заболевания, обусловленные нарушениями скорости синтеза одной или нескольких полипептидных цепей глобина (талассемии), и анемии, вызванные изменением первичной структуры полипептидных цепей, что приводит к нарушению стабильности и функции гемоглобина (гемоглобинопатии с наличием аномального гемоглобина).
Талассемии –наследственные заболевания, вызванные делецией генов, кодирующих синтез цепей гемоглобина. Различают α- и β-талассемию (в зависимости от нарушения синтеза α- и β-цепей). Талассемия может быть гомозиготной (β 0 –талассемия) или гетерозиготной (β + –талассемия) в зависимости от делеции одного или двух генов из пары генов, кодирующих синтез β-цепей. Реже встречается α-талассемия с нарушением синтеза α-цепей. Поскольку синтез α-цепей кодируют 2 пары генов, возможны разные варианты заболевания. Отсутствие всех 4 генов делает плод нежизнеспособным.
Клиника талассемии представляет собой клиническую картину гемолитической анемии с внутриклеточным гемолизом различной степени тяжести. Анемия имеет гипохромный характер с явлениями неэффективного эритропоеза и гемосидероза. Развивается желтуха с увеличением непрямого билирубина. Увеличивается селезенка, часто печень. Эритроциты гипозромны, выражены анизоцитоз, пойкилоцитоз, мишеневидные формы, базофильная пунктация эритроцитов. Степень анемии зависит от тяжести гемолиза: при большой талассемии уровень гемоглобина 30-40 г/л, при малой -90-100 г/л. ЦП снижен – 0,5-0,8. Содержание ретикулоцитов значительно повышено, могут появляться эритро- и нормобласты. Осмотическая резистентность эритроцитов повышена, что является скрининговым тестом на талассемию.
В костном мозге значительно повышен эритропоез, но количество гемоглобинизированных форм невелико (неэффективный эритропоез), увеличивается число сидеробластов.
Уровень железа в сыворотке нормальный или повышен, но десферальвый тест указывает на повышенный запас железа в организме, не используемого для образования гемоглобина. Содержание непрямого билирубина в крови увеличивается, развивается уробилинурия, усилено выделение стеркобилина с калом.
Гомозиготная (болезнь Кули, большая) β-талассемия клинически проявляется к концу 1 года жизни ребенка. При тяжелой форме больные умирают на первом году жизни, при средней тяжести – доживают до периода полового созревания, при легкой, диагностируемой на втором году жизни, больные доживают до зрелого возраста. Кожа больных бледная, с серовато-желтым оттенком, скелет деформирован (монголоидные черты лица, квадратный череп), ребенок отстает в физическом развитии. В костях свода черепа при рентгенологическом исследовании – утолщение пластин и трабекул губчатой кости за счет усиления кроветворения. Живот увеличен в объеме за гепатоспленомегалии. При более легкой форме течения развиваются ЖКБ, гемосидероз, трофическая язва, вторичные инфекции, нарушения кровообращения.
Гетерозиготная (малая) β-талассемия — протекает более легко
Клиническое течение α-талассемии зависит от количества отсутствующих генов. При гомозиготной форме наступает внутриутробная смерть плода с явлениями водянки мозга, гепатоспленомегалией. Гетерозиготная α-талассемия протекает в виде гемолитической анемии средней тяжести или легкой формы с гипохромной анемией, желтухой, спленомегалией.
В подозрительных на талассемию случаях необходимо определение типа гемоглобина с использованием электрофореза на различных носителях, в неясных случаях – изучение скорости синтеза цепей гемоглобина по включению меченых аминокислот.
Лечение – при гомозиготной талассемии основным методом лечения являются повторные взвеси эритроцитов (отмытые или размороженные) вначале каждые 2-3 дня до повышения уровня гемоглобина, затем поддерживаюшие трансфузии (каждые 3-4 недели), чтобы уровень гемоглобина составлял 90-100 г/л. Необходимо вводить десферал для выведения избытка железа. Препараты железа категорически противопоказаны. При беременности, инфекциях назначается фолиевая кислота.
Гемоглобинопатии – наследственные гемолитические анемии, обусловленные наличием аномальных гемоглобинов вследствие замещения одной или нескольких аминокислот в полипептидных цепях глобина. В настоящее время известно более 150 аномальных гемоглобинов, чаще замещение происходит в β-цепи. Гемоглобинопатии – наследственные заболевания, обусловленные точечными мутациями в генах, кодирующих образование цепей глобина, или чаще наследуются как доминантный аутосомный признак.
В большинстве случаев аномальные гемоглобины стабильны в гомо- и гетерозиготном состоянии и обнаруживаются случайно. Некоторые замещения аминокислот приводят к изменению конфигурации цепей глобина, нарушению их взаимосвязи, силы прикрепления гема. Эти гемоглобинопатииимеют клинические проявления: гемоглобинопатия S (серповидно-клеточная анемия), обусловленная резким уменьшением растворимости НвS в условиях гипоксии. Это приводит к деформации эритроцитов (феномен серповидности, дрепаноцитоз), которые не могут проходить через мелкие капилляры, что вызывает стаз, гипоксию, микротромбоз, некоторые дрепаноциты быстро разрушаются в селезенке. В других случаях в аномальном гемоглобине (НвМ) происходит быстрое окисление железа гемма с образованием метгемоглобина, в котором гемоглобин стойко соединен с кислородом, что приводит к развитию цианоза и полицитемии. Клиника гкмолитической анемии развивается также у больных, у которых аномальный гемоглобин является нестабильным и выпадает в осадок в эритроците.
Гомозиготная серповидно-клеточная анемия диагностируется с половины первого года жизни, когда фетальный гемоглобин начинает замещаться НвS. Проявляется умеренной гемолитической анемией и тяжелым тромбозом различных органов. Характерно поражение костно-суставной системы: припухлость и болезненность суставов кистей, стоп, голеней, некрозы головок бедренных костей. Наблюдаются инфаркты легких, головного мозга, сетчатки, печени, почек, селезенки, брыжейки с соответствующей клинической картиной, возникают язвы на голенях, иногда приапизм. Дети не доживают до юношеского возраста. На фоне осложнений (инфекции, сосудисто-тромботические процессы) у больных развиваются гемолитические кризы с острым внутрисосудистым гемолизом, гипопластические кризы, секвестрационные кризы, связанные с удалением из кровообращения во внутренние органы большого количества эритроцитов.
При гетерозиготной серповидно-клеточной аномалии признаки заболевания в обычных условиях отсутствуют, появляясь только в период гипоксии (при пневмонии, наркозе, подводном плавании или подъеме на высоту). Серповидность эритроцитов проявляется в условиях гипоксии при проведении специальных проб (с метабисульфитом натрия или после наложения жгута на палец).
При наличии в крови нестабильных гемоглобинов с помощью специальной окраски в эритроцитах обнаруживают множественные тельца-включения вследствие выпадения в осадок нестабильного гемоглобина или тельца Гейнца.
Для уточнения характера гемоглобинопатии проводят электорофорез гемоглобина. Точно установить тип аномального гемоглобина можно путем исследования его первичной структуры.
Лечение серповидноклеточной анемии в основном симптоматическое. Трансфузионная терапия (отмытые эритроциты, заменное переливание эритроцитарной взвеси) проводится при тяжелой анемии. Для уменьшения серповидности рекомендуется оксигенотерапия, гемодилюция ощелачивающими растворами. При явлениях гиперспленизма – спленэктомия. При тромботических кризах назначают болеутоляющие, сосудорасширяющие и седативные препараты, обеспечивают прием достаточного количества жидкости внутрь и в виде инфузии солевых растворов.
В связи с неэффективным гемопоезом необходимо введение фолиевой кислоты, для профилактики гемосидероза – десферал.
источник
Наследственные гемолитические анемии относятся к эндоэритроцитарным ГА возникают в результате наследования:
1) дефектов структуры мембран эритроцитов (мембранопатии, или эритроцитопатии);
2) патологических типов гемоглобинов (гемоглобинопатии);
3) дефицита ферментов (ферментопатии, или энзимопатии).
К мембранопатиямотносятся гемолитические анемии, обусловленные генетическим дефектом белковой или липидной структуры мембраны, цитоскелета эритроцитов.
Клеточная мембрана эритроцита состоит из двойного липидного слоя, на ее поверхности эксперессированы антигены. Цитоскелет эритроцитов состоит из спектрина, актина, белка полос 4.1, 4.2 и анкирина. Цитоскелет обеспечивает эритроциту двояковогнутую форму и необходимую деформируемость, что позволяет ему проходить через отверстия диаметром 2,5-3 мкм.
Наследственные дефекты спектрина и ассоциированных с ним белков (например, анкирина) сопровождаются увеличением риска нарушения целостности мембраны в условиях выраженной гипоксии, сопряженной с дефицитом АТФ и увеличением содержания катионов кальция в клетках.
К белковозависимым мембранопатиям относятнаследственный микросфероцитоз (болезнь Минковского-Шоффара), эллиптоцитоз (овалоцитоз), стоматоцитоз.
К липидозависимым мембранопатиям – наследственный акантоцитоз.
Болезнь Минковского-Шоффара(микросфероцитоз) –наследуется аутосомно-доминантно и встречается только среди представителей белой расы. Мембранопатия обусловлена снижением содержания и изменением структуры примембранных белков эритроцитов (спектрина и анкирина), нарушением взаимодействия их с другими белками мембраны эритроцита, что приводит к повышению ее проницаемости, гипергидратации клеток. Реже болезнь вызвана дефектами других подмембранных белков цитоскелета – протеина 4.2 и белка третьей полосы. Эритроциты приобретают сферическую форму, при этом уменьшается их диаметр (до 5,4 мкм) – развивается микросфероцитоз.
Снижение деформируемости микросфероцитов приводит к их внутриклеточному гемолизу (в синусоидах селезенки) развивается спленомегалия. Продолжительность жизни микросфероцитов составляет 8-15 суток. Это заболевание является одной из важнейших причин врожденной гемолитической желтухи.
Эллиптоцитоз (овалоцитоз) также наследуется аутосомно-доминантно. Мембранопатия обусловлена дефектом мембранного белка 4.1. Образуются эритроциты овальной или элиптической формы (до 25-75 % от общего количества эритроцитов).
 |  |
Стоматоцитоз наследуется аутосомно-доминантно. В основе заболевания лежит нарушение структуры мембраны. Эритроцитыв центре содержат неокрашенный участок в виде светлой полосы, напоминающей рот (от греч. stoma – рот).
 |
Акантоцитоз наследуется аутосомно-рецессивно. Заболевание связано с нарушением липидного обмена. Снижение содержания триглицеридов, фосфолипидов в крови отражается на липидном составе мембран. Нарушения в эритроцитах способствуют снижению текучести мембран и изменению их формы. Эритроциты приобретают выпячивания мембраны различного размера (шпоровидные клетки).
 |
Этиология синдрома может быть разнообразной: от наследственной абеталипопротеинемии до приобретенных нарушений липопротеинового метаболизма – при печеночной недостаточности, стеаторее, авитаминозе E и голодании.
В группу мембранопатий должна быть переквалифицирована пароксизмальная ночная гемоглобинурия, или болезнь Маркиафава-Микели, обусловленная дефектом мембраны эритроцитов, вследствие чего эритроциты приобретают повышенную чувствительность к действию комплемента. Проявляется ночной гемоглобинурией. Причиной является дефицит гликанинозитолфосфатида – липополисахарида, обеспечивающего абсорбцию ингибиторов комплемента. Предполагается, что вследствие активации системы комплемента альтернативным путем под влиянием ацидоза и гиперкапнии во сне развитивается гемолиз. В патологический процесс вовлекаются гранулоциты и тромбоциты.
Мембранопатии могут иметь приобретенный характер (при авитаминозе E – липидной части).
Гемоглобинопатии (гемоглобинозы)возникают либо вследствие дефицита синтеза глобина, либо его структурной аномальности.
Гемоглобин представляет собой тетрамер, состоящий из двух цепей глобина типа α и двух цепей другого типа (β, γ или δ), соединенных с четырьмя молекулами гема.
К нормальным типам гемоглобина относятся: HbA (α2β2 – основной гемоглобин взрослого, 97%), HbA2 (α2δ2 – минорный гемоглобин взрослого, 2%) и HbF (α2γ2 – фетальный гемоглобин, 1%).
Известно более 50 видов заболеваний с образованием патологических типов гемоглобинов. Выделяют две основные группы наследственных нарушений образования гемоглобина:
Ø одиночные аминокислотные замены в структуре глобина (серповидноклеточная анемия) и
Ø уменьшение выработки глобиновых цепей (талассемия или средиземноморская анемия).
Для наследственных гемоглобинопатий характерна фетализация гемоглобина.
Серповидно-клеточная анемия(СКА) – заболевание, связанное с синтезом патологического гемоглобина S.
Гемоглобин S образуется в результате точечной мутации в гене β-цепи, приводящей к замене в 6-м положении глутаминовой кислоты на валин. Наследуется заболевание по типу неполного доминирования. Данная гемоглобинопатия наиболее распространена у лиц, проживающих в «малярийном поясе» (Средиземноморье, Средняя Азия, Америка, Африка, центральная Индия.
Свойства гемоглобинов А и S различны в концентрированных растворах: дезоксигенированный гемоглобин S в 50 раз менее растворим, чем HbA. Это лежит в основе временного образования внутри эритроцитов геля и серповидного изменения формы красных клеток при гипоксии (pО2
Дата добавления: 2018-08-06 ; просмотров: 212 ; ЗАКАЗАТЬ РАБОТУ
источник
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Гемолитическая анемия (ГА) — малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии— анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические — анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом — обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще — Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий — талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
источник
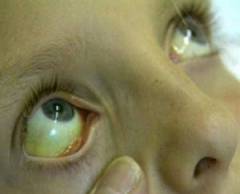
Поскольку симптомокомплекс гемолитических анемий одинаков для большинства вызвавших их причин, огромное значение приобретает правильно собранный анамнез, а также дополнительные лабораторные и параклинические исследования.
Лечение гемолитических анемий должно проводиться лишь после установления окончательного диагноза, однако далеко не всегда это представляется возможным ввиду высоких темпов разрушения эритроцитов и недостаточности времени на постановку диагноза. В таких случаях на первый план выступают мероприятия, направленные на жизнеобеспечение пациента, такие как переливание донорской крови, плазмаферез, эмпирическое лечение антибактериальными препаратами и глюкокортикоидными гормональными препаратами.
Интересные факты
- Среднее количество железа, содержащееся в крови взрослого человека, составляет порядка 4 грамм.
- Суммарное количество эритроцитов в теле взрослого человека в пересчете на сухую массу составляет в среднем 2 кг.
- Регенераторная способность эритроцитарного ростка костного мозга достаточно велика. Однако, для того чтобы регенераторные механизмы успели активизироваться, требуется длительное время. По этой причине хронический гемолиз значительно легче переносится пациентами, чем острый, даже если при этом уровень гемоглобина достигает 40 – 50 г\л.
Нормальный эритроцит обладает рядом параметров, которые обеспечивают успешное выполнение им своих функций.
Основными параметрами эритроцитов являются:
- форма двояковогнутого диска;
- средний диаметр — 7,2 – 7,5 мкм;
- средний объем — 90 мкм 3 ;
- длительность «жизни» — 90 – 120 дней;
- нормальная концентрация у мужчин — 3,9 – 5,2 х 10 12 \л;
- нормальная концентрация у женщин — 3,7 – 4,9 х 10 12 \л;
- нормальная концентрация гемоглобина у мужчин — 130 – 160 г\л;
- нормальная концентрация гемоглобина у женщин — 120 – 150 г\л;
- гематокрит (соотношение форменных элементов крови к жидкой ее части) у мужчин — 0,40 – 0,48;
- гематокрит у женщин — 0,36 – 0,46.
Изменение формы и размера эритроцитов отрицательно отражается на их функции. Например, уменьшение размеров эритроцита свидетельствует о меньшем содержании гемоглобина в нем. В таком случае количество эритроцитов может быть в норме, но, тем не менее, анемия будет присутствовать, поскольку общий уровень гемоглобина будет снижен. Увеличение диаметра эритроцита часто свидетельствует о мегалобластной B12-дефицитной или фолиеводефицитной анемии. Присутствие в анализе крови эритроцитов разного диаметра называется анизоцитозом.
Правильная форма эритроцита с точки зрения физиологии имеет большое значение. Во-первых, она обеспечивает наибольшую площадь соприкосновения эритроцита с сосудистой стенкой во время прохождения по капилляру, а соответственно и высокую скорость газообмена. Во-вторых, измененная форма эритроцитов часто свидетельствует о низких пластических свойствах цитоскелета эритроцита (система белков, организованных в сеть, поддерживающую необходимую форму клетки). Вследствие изменения нормальной формы клетки происходит преждевременное разрушение таких эритроцитов при прохождении через капилляры селезенки. Присутствие в периферической крови эритроцитов различной формы именуется пойкилоцитозом.
Цитоскелет эритроцита является системой микротрубочек и микрофиламентов, придающих эритроциту ту или иную форму. Микрофиламенты состоят из трех видов белков — актина, миозина и тубулина. Данные белки способны активно сокращаться, изменяя форму эритроцита для осуществления необходимой задачи. Например, для прохождения через капилляры эритроцит вытягивается, а по выходу из узкого участка снова принимает первоначальную форму. Данные преобразования происходят при использовании энергии АТФ (аденозинтрифосфат) и ионов кальция, являющихся пусковым фактором в перестройке цитоскелета.
Еще одной особенностью эритроцита является отсутствие ядра. Данное свойство крайне выгодно с эволюционной точки зрения, поскольку позволяет более рационально использовать пространство, которое бы занимало ядро, и вместо него поместить в эритроцит большее количество гемоглобина. Более того, ядро значительно бы ухудшило пластические свойства эритроцита, что недопустимо, учитывая, что данная клетка должна проникать через капилляры, диаметр которых в несколько раз меньше ее собственного.
Гемоглобин является макромолекулой, заполняющей 98% объема зрелого эритроцита. Он располагается в ячейках цитоскелета клетки. Подсчитано, что в среднем эритроците содержится приблизительно 280 – 400 миллионов молекул гемоглобина. Он состоит из белковой части – глобина и небелковой части – гема. Глобин, в свою очередь, состоит из четырех мономеров, два из которых мономеры α (альфа) и остальные два – мономеры β (бета). Гем является сложной неорганической молекулой, в центре которой располагается железо, способное окисляться и восстанавливаться в зависимости от условий среды. Основной функцией гемоглобина является захват, транспортировка и высвобождение кислорода и углекислого газа. Данные процессы регулируются кислотностью среды, парциальным давлением газов крови и другими факторами.
Различают следующие виды гемоглобина:
- гемоглобин А (HbA);
- гемоглобин А2 (HbA2);
- гемоглобин F (HbF);
- гемоглобин Н (HbH);
- гемоглобин S (HbS).
Гемоглобин А является наиболее численной фракцией, доля которой составляет 95 – 98%. Данный гемоглобин является нормальным, а его строение соответствует описанному выше. Гемоглобин А2 состоит из двух цепей α и двух цепей δ (дельта). Данный тип гемоглобина не менее функционален, чем гемоглобин А, однако его доля составляет всего 2 – 3% . Гемоглобин F является детской или фетальной фракцией гемоглобина и встречается в среднем до 1 года. Непосредственно после рождения фракция такого гемоглобина наиболее высока и составляет 70 – 90%. К концу первого года жизни фетальный гемоглобин разрушается, а его место занимает гемоглобин А. Гемоглобин Н встречается при талассемии, при этом он формируется из 4-х мономеров β. Гемоглобин S является диагностическим признаком серповидноклеточной анемии.
Мембрана эритроцита состоит из двойного липидного слоя, пронизанного различными белками, выполняющими роль насосов для разнообразных микроэлементов. К внутренней поверхности мембраны прикрепляются элементы цитоскелета. На внешней поверхности эритроцита располагается большое количество гликопротеидов, выполняющих роль рецепторов и антигенов – молекул, определяющих уникальность клетки. На сегодняшний день на поверхности эритроцитов обнаружено более 250 видов антигенов, наиболее изученными из которых являются антигены системы АВ0 и системы резус-фактора.
По системе АВ0 различают 4 группы крови, а по резус-фактору – 2 группы. Открытие данных групп крови ознаменовало начало новой эры в медицине, поскольку позволило производить переливание крови и ее компонентов пациентам со злокачественными заболеваниями крови, массивными кровопотерями и др. Также благодаря переливанию крови значительно возросла выживаемость пациентов после массивных хирургических вмешательств.
По системе АВ0 различают следующие группы крови:
- агглютиногены (антигены на поверхности эритроцитов, которые при контакте с одноименными агглютининами вызывают осаждение красных кровяных телец) на поверхности эритроцитов отсутствуют;
- присутствуют агглютиногены А;
- присутствуют агглютиногены В;
- присутствуют агглютиногены А и В.
По наличию резус-фактора различают следующие группы крови:
- резус-положительная – 85% населения;
- резус-отрицательная – 15% населения.
Несмотря на тот факт, что, теоретически, переливая полностью совместимую кровь от одного пациента другому анафилактических реакций быть не должно, периодически они случаются. Причиной такого осложнения является несовместимость по остальным типам эритроцитарных антигенов, которые, к сожалению, практически не изучены на сегодняшний день. Кроме того, причиной анафилаксии могут быть некоторые компоненты плазмы – жидкой части крови, Поэтому согласно последним рекомендациям международных медицинских гидов переливание цельной крови не приветствуется. Вместо этого переливаются компоненты крови – эритроцитарная масса, тромбоцитарная масса, альбумины, свежезамороженная плазма концентраты факторов свертывания и т. д.
Упомянутые ранее гликопротеиды, расположенные на поверхности мембраны эритроцитов, формируют слой, называющийся гликокаликсом. Важной особенностью данного слоя является отрицательный заряд на его поверхности. Поверхность внутреннего слоя сосудов также имеет отрицательный заряд. Соответственно, в кровеносном русле эритроциты отталкиваются от стенок сосуда и друг от друга, что предотвращает образование кровяных сгустков. Однако стоит произойти повреждению эритроцита или ранению стенки сосуда, как отрицательный их заряд постепенно сменяется на положительный, здоровые эритроциты группируются вокруг места повреждения, и формируется тромб.
Понятие деформируемости и цитоплазматической вязкости эритроцита тесно сопряжено с функциями цитоскелета и концентрацией гемоглобина в клетке. Деформируемостью называется способность эритроцита клетки произвольно изменять свою форму для преодоления препятствий. Цитоплазматическая вязкость обратно пропорциональна деформируемости и возрастает вместе с увеличением содержания гемоглобина по отношению к жидкой части клетки. Увеличение вязкости происходит при старении эритроцита и является физиологическим процессом. Параллельно с увеличением вязкости происходит уменьшение деформируемости.
Тем не менее, изменение данных показателей может иметь место не только при физиологическом процессе старения эритроцита, но еще и при многих врожденных и приобретенных патологиях, таких как наследственные мембранопатии, ферментопатии и гемоглобинопатии, которые более подробно будут описаны далее.
Эритроцит, как и любая другая живая клетка, нуждается в энергии для успешного функционирования. Энергию эритроцит получает при окислительно-восстановительных процессах, происходящих в митохондриях. Митохондрии сравниваются с электростанциями клетки, поскольку преобразуют глюкозу в АТФ в ходе процесса, именуемого гликолизом. Отличительной способностью эритроцита является то, что его митохондрии образуют АТФ только путем анаэробного гликолиза. Иными словами, данные клетки не нуждаются в кислороде для обеспечения своей жизнедеятельности и поэтому доставляют тканям ровно столько кислорода, сколько получили при прохождении через легочные альвеолы.
Несмотря на то, что об эритроцитах сложилось мнение как об основных переносчиках кислорода и углекислого газа, помимо этого они выполняют еще ряд важных функций.
Второстепенными функциями эритроцитов являются:
- регуляция кислотно-щелочного равновесия крови посредством карбонатной буферной системы;
- гемостаз – процесс, направленный на остановку кровотечения;
- определение реологических свойств крови – изменение численности эритроцитов по отношению к общему количеству плазмы приводит к сгущению или разжижению крови.
- участие в иммунных процессах – на поверхности эритроцита находятся рецепторы для прикрепления антител;
- пищеварительная функция – распадаясь, эритроциты высвобождают гем, самостоятельно трансформирующийся в свободный билирубин. В печени свободный билирубин превращается в желчь, использующуюся для расщепления жиров пищи.
Эритроциты образуются в красном костном мозге, проходя через многочисленные стадии роста и созревания. Все промежуточные формы предшественников эритроцитов объединяются в единый термин – эритроцитарный росток.
По мере созревания предшественники эритроцита претерпевают изменение кислотности цитоплазмы (жидкой части клетки), самопереваривание ядра и накопление гемоглобина. Непосредственным предшественником эритроцита является ретикулоцит – клетка, в которой при рассмотрении под микроскопом можно встретить некоторые плотные включения, являвшиеся некогда ядром. Ретикулоциты циркулируют в крови от 36 до 44 часов, за которые они избавляются от остатков ядра и заканчивают синтез гемоглобина из остаточных цепей матричной РНК (рибонуклеиновой кислоты).
Регуляция созревания новых эритроцитов осуществляется посредством прямого механизма обратной связи. Веществом, стимулирующим рост числа эритроцитов, является эритропоэтин – гормон, вырабатываемый паренхимой почек. При кислородном голодании выработка эритропоэтина усиливается, что приводит к ускорению созревания эритроцитов и в конечном итоге – восстановлению оптимального уровня насыщения тканей кислородом. Второстепенная регуляция деятельности эритроцитарного ростка осуществляется посредством интерлейкина-3, фактора стволовых клеток, витамина В12, гормонов (тироксин, соматостатин, андрогены, эстрогены, кортикостероиды) и микроэлементов (селен, железо, цинк, медь и др.).
По истечении 3 – 4 месяцев существования эритроцита происходит его постепенная инволюция, проявляющаяся выходом внутриклеточной жидкости из него по причине износа большинства транспортных ферментных систем. Вслед за этим происходит уплотнение эритроцита, сопровождающееся снижением его пластических свойств. Снижение пластических свойств ухудшает проходимость эритроцита через капилляры. В конечном итоге такой эритроцит попадает в селезенку, застревает в ее капиллярах и разрушается лейкоцитами и макрофагами, располагающимися вокруг них.
После разрушения эритроцита в кровеносное русло выделяется свободный гемоглобин. При скорости гемолиза менее 10% от общего числа эритроцитов в сутки гемоглобин захватывается белком под названием гаптоглобин и оседает в селезенке и внутреннем слое сосудов, где разрушается макрофагами. Макрофаги уничтожают белковую часть гемоглобина, но высвобождают гем. Гем под действием ряда ферментов крови трансформируется в свободный билирубин, после чего транспортируется в печень белком альбумином. Наличие в крови большого количества свободного билирубина сопровождается появлением желтухи лимонного оттенка. В печени свободный билирубин связывается с глюкуроновой кислотой и выделяется в кишечник в виде желчи. При наличии препятствия оттоку желчи она поступает обратно в кровь и циркулирует в виде связанного билирубина. В таком случае также появляется желтуха, однако более темного оттенка (слизистые и кожные покровы оранжевого или красноватого цвета).
После выхода связанного билирубина в кишечник в виде желчи происходит его восстановление до стеркобилиногена и уробилиногена при помощи кишечной флоры. Большая часть стеркобилиногена превращается в стеркобилин, который выделяется с калом и окрашивает его в коричневый цвет. Остаточная часть стеркобилиногена и уробилиноген всасывается в кишечнике и поступает обратно в кровоток. Уробилиноген трансформируется в уробилин и выделяется с мочой, а стеркобилиноген повторно поступает в печень и выводится с желчью. Данный цикл с первого взгляда может показаться бессмысленным, однако, это заблуждение. Во время повторного попадания продуктов распада эритроцитов в кровь осуществляется стимуляция активности иммунной системы.
При увеличении скорости гемолиза от 10% до 17 – 18% от общего числа эритроцитов в сутки резервов гаптоглобина становится недостаточно, для того чтобы захватывать высвобождающийся гемоглобин и утилизировать его путем, описанным выше. В таком случае свободный гемоглобин с током крови поступает в почечные капилляры, отфильтровывается в первичную мочу и окисляется до гемосидерина. Затем гемосидерин поступает во вторичную мочу и выводится из организма.
При крайне выраженном гемолизе, темпы которого превышают 17 – 18% от общего количества эритроцитов в сутки, гемоглобин поступает в почки в слишком большом количестве. Из-за этого не успевает происходить его окисление и в мочу поступает чистый гемоглобин. Таким образом, определение в моче избытка уробилина является признаком легкой гемолитической анемии. Появление гемосидерина свидетельствует о переходе в среднюю степень гемолиза. Обнаружение гемоглобина в моче говорит о высокой интенсивности разрушения эритроцитов.
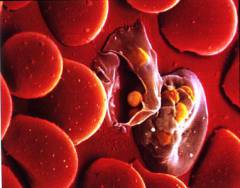
Гемолитические анемии классифицируются на врожденные и приобретенные.
Различают следующие виды врожденных гемолитических анемий:
- мембранопатии;
- ферментопатии;
- гемоглобинопатии.
Различают следующие виды приобретенных гемолитических анемий:
- иммунные гемолитические анемии;
- приобретенные мембранопатии;
- анемии из-за механического разрушения эритроцитов;
- гемолитические анемии, вызванные инфекционными агентами.
Как описывалось ранее, нормальной формой эритроцита является форма двояковогнутого диска. Такая форма соответствует правильному белковому составу мембраны и позволяет эритроциту проникать через капилляры, диаметр которых в несколько раз меньше диаметра самого эритроцита. Высокая проникающая способность эритроцитов, с одной стороны, позволяет им максимально эффективно выполнять основную свою функцию – обмен газов между внутренней средой организма и внешней средой, а с другой стороны – избегать избыточного их разрушения в селезенке.
Дефект определенных белков мембраны приводит к нарушению ее формы. С нарушением формы происходит снижение деформируемости эритроцитов и как следствие усиленное их разрушение в селезенке.
На сегодняшний день различают 3 вида врожденных мембранопатий:
- акантоцитоз
- микросфероцитоз
- овалоцитоз
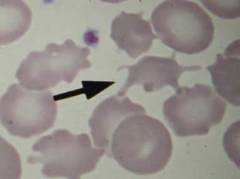
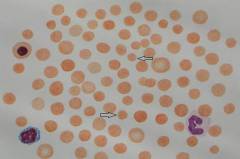
С детства у таких пациентов происходит гипертрофия эритроцитарного костномозгового ростка, компенсирующая гемолиз. Поэтому при микросфероцитозе чаще наблюдается легкая и средней тяжести анемия, появляющаяся преимущественно в моменты ослабления организма вирусными заболеваниями, недостаточным питанием или интенсивным физическим трудом.
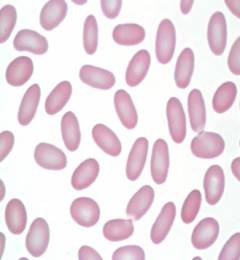
Эритроцит содержит ряд ферментов, при помощи которых поддерживается постоянство его внутренней среды, осуществляется переработка глюкозы в АТФ и регуляция кислотно-щелочного баланса крови.
Соответственно вышеуказанным направлениям различают 3 вида ферментопатий:
- дефицит ферментов, участвующих в окислении и восстановлении глутатиона (см. ниже);
- дефицит ферментов гликолиза;
- дефицит ферментов, использующих АТФ.
Глутатион является трипептидным комплексом, участвующим в большинстве окислительно-восстановительных процессов организма. В частности, он необходим для работы митохондрий – энергетических станций любой клетки, в том числе и эритроцита. Врожденные дефекты ферментов, участвующих в окислении и восстановлении глутатиона эритроцитов, приводят к снижению скорости продукции молекул АТФ – основного энергетического субстрата для большинства энергозависимых систем клетки. Дефицит АТФ приводит к замедлению обмена веществ эритроцитов и их скорому самостоятельному уничтожению, называемому апоптозом.
Гликолиз является процессом распада глюкозы с образованием молекул АТФ. Для осуществления гликолиза необходимо присутствие ряда ферментов, которые многократно преобразуют глюкозу в промежуточные соединения и в итоге высвобождают АТФ. Как указывалось ранее, эритроцит является клеткой, не использующей кислород для образования молекул АТФ. Такой тип гликолиза является анаэробным (безвоздушным). В результате из одной молекулы глюкозы в эритроците образуется 2 молекулы АТФ, использующиеся для поддержания работоспособности большинства ферментных систем клетки. Соответственно врожденный дефект ферментов гликолиза лишает эритроцит необходимого количества энергии для поддержания жизнедеятельности, и он разрушается.
АТФ является универсальной молекулой, окисление которой высвобождает энергию, необходимую для работы более чем 90% ферментных систем всех клеток организма. Эритроцит также содержит множество ферментных систем, субстратом которых является АТФ. Высвобождаемая энергия расходуется на процесс газообмена, поддержание постоянного ионного равновесия внутри и снаружи клетки, поддержание постоянного осмотического и онкотического давления клетки, а также на активную работу цитоскелета и многое другое. Нарушение утилизации глюкозы как минимум в одной из вышеупомянутых систем приводит к выпадению ее функции и дальнейшей цепной реакции, итогом которой является разрушение эритроцита.
Гемоглобин – молекула, занимающая 98% объема эритроцита, ответственная за обеспечение процессов захвата и высвобождения газов, а также за их транспортировку от легочных альвеол к периферическим тканям и обратно. При некоторых дефектах гемоглобина эритроциты значительно хуже осуществляют перенос газов. Кроме того, на фоне изменения молекулы гемоглобина попутно изменяется и форма самого эритроцита, что также отрицательно отражается на длительности их циркуляции в кровеносном русле.
Различают 2 вида гемоглобинопатий:
- количественные – талассемии;
- качественные – серповидноклеточная анемия или дрепаноцитоз.
Талассемии являются наследственными заболеваниями, связанными с нарушением синтеза гемоглобина. По своей структуре гемоглобин является сложной молекулой, состоящей из двух альфа-мономеров и двух бета-мономеров, связанных между собой. Альфа цепь синтезируется с 4-х участков ДНК. Цепь бета – с 2-х участков. Таким образом, при возникновении мутации в одном из 6 участков снижается или прекращается синтез того мономера, ген которого поврежден. Здоровые гены продолжают синтез мономеров, что со временем приводит к количественному преобладанию одних цепей над другими. Те мономеры, которые оказываются в избытке, образуют непрочные соединения, функция которых значительно уступает нормальному гемоглобину. Соответственно той цепи, синтез которой нарушен, выделяют 3 основных типа талассемий – альфа, бета и смешанная альфа-бета талассемия. Клиническая картина зависит от количества мутировавших генов.
Серповидноклеточная анемия является наследственным заболеванием, при котором вместо нормального гемоглобина А формируется аномальный гемоглобин S. Данный аномальный гемоглобин значительно уступает в функциональности гемоглобину А, а также изменяет форму эритроцита на серповидную. Такая форма приводит к разрушению эритроцитов в срок от 5 до 70 дней в сравнении с нормальной длительностью их существования – от 90 до 120 дней. В результате в крови появляется доля серповидных эритроцитов, величина которой зависит от того, является мутация гетерозиготной или гомозиготной. При гетерозиготной мутации доля аномальных эритроцитов редко достигает 50%, а больной испытывает симптомы анемии только при значительной физической нагрузке или в условиях сниженной концентрации кислорода в атмосферном воздухе. При гомозиготной мутации все эритроциты больного являются серповидными и поэтому симптомы анемии проявляются с рождения ребенка, а болезнь характеризуется тяжелым течением.
При данном типе анемий разрушение эритроцитов происходит под действием иммунной системы организма.
Различают 4 типа иммунных гемолитических анемий:
- аутоиммунные;
- изоиммунные;
- гетероиммунные;
- трансиммунные.
При аутоиммунных анемиях собственный организм пациента вырабатывает антитела к нормальным эритроцитам крови вследствие сбоя в работе иммунной системы и нарушения распознавания лимфоцитами своих и чужих клеток.
Изоиммунные анемии развиваются при переливании пациенту крови несовместимой по АВ0 системе и резус-фактору или, иными словами, крови другой группы. В данном случае накануне перелитые эритроциты разрушаются клетками иммунной системы и антителами реципиента. Аналогичный иммунный конфликт развивается при положительном резус-факторе в крови плода и отрицательном – в крови беременной матери. Такая патология именуется гемолитической болезнью новорожденных детей.
Гетероиммунные анемии развиваются в случае появления на мембране эритроцита чужеродных антигенов, признаваемых иммунной системой пациента как чужеродные. Чужеродные антигены могут появиться на поверхности эритроцита в случае употребления некоторых медикаментов или после перенесенных острых вирусных инфекций.
Трансиммунные анемии развиваются у плода, когда в организме матери присутствуют антитела против эритроцитов (аутоиммунная анемия). В данном случае мишенью иммунной системы становятся как эритроциты матери, так и эритроциты плода, даже если не выявляется несовместимость по резус-фактору, как при гемолитической болезни новорожденных.
К данной группе заболеваний относят:
- маршевую гемоглобинурию;
- микроангиопатическую гемолитическую анемию;
- анемию при пересадке механических клапанов сердца.
Маршевая гемоглобинурия, исходя из названия, развивается при длительном маршировании. Форменные элементы крови, находящиеся в ступнях, при длительном регулярном сдавлении подошв подвергаются деформации и даже разрушаются. В результате в кровь выделяется большое количество несвязанного гемоглобина, который выделяется с мочой.
Микроангиопатическая гемолитическая анемия развивается из-за деформации и последующего разрушения эритроцитов при острых гломерулонефритах и синдроме диссеминированного внутрисосудистого свертывания. В первом случае по причине воспаления почечных канальцев и соответственно окружающих их капилляров просвет их сужается, а эритроциты деформируются при трении с их внутренней оболочкой. Во втором случае во всей кровеносной системе происходит молниеносная агрегация тромбоцитов, сопровождающаяся образованием множества фибриновых нитей, перекрывающих просвет сосудов. Часть эритроцитов сразу застревает в образовавшейся сети и образует множественные тромбы, а оставшаяся часть на высокой скорости проскальзывает через данную сеть, попутно деформируясь. В результате деформированные таким образом эритроциты, называющиеся «венценосными», какое-то время еще циркулируют в крови, а затем разрушаются самостоятельно или при прохождении через капилляры селезенки.
Анемия при пересадке механических клапанов сердца развивается при столкновении эритроцитов, двигающихся с высокой скоростью, с плотным пластиком или металлом, из которого состоит искусственный клапан сердца. Темпы разрушения зависят от скорости кровотока в области клапана. Гемолиз усиливается при совершении физической работы, эмоциональных переживаниях, резком повышении или снижении артериального давления и повышении температуры тела.
Таким образом, гемолитическая анемия может развиться по следующим причинам:
- попадание в кровь различных токсинов и ядов (ядохимикаты, пестициды, укусы змей и т. д.);
- механическое разрушение эритроцитов (во время многочасового хождения, после имплантации искусственного клапана сердца и др.);
- синдром диссеминированного внутрисосудистого свертывания;
- различные генетические аномалии строения эритроцитов;
- аутоиммунные болезни;
- паранеопластический синдром (перекрестное иммунное уничтожение эритроцитов вместе с опухолевыми клетками);
- осложнения после переливания донорской крови;
- заражение некоторыми инфекционными болезнями (малярия, токсоплазмоз);
- хронический гломерулонефрит;
- тяжелые гнойные инфекции, сопровождающиеся сепсисом;
- инфекционный гепатит B, реже С и D;
- беременность;
- авитаминозы и др.

Анемический синдром проявляется следующими симптомами:
- бледность кожных покровов и слизистых оболочек;
- головокружение;
- выраженная общая слабость;
- скорая утомляемость;
- одышка при обычной физической нагрузке;
- сердцебиение;
- частый пульс и др.
Гемолитический синдром проявляется следующими симптомами:
- желтушно-бледный окрас кожных покровов и слизистых оболочек;
- моча темно-коричневого, вишневого или алого цвета;
- увеличение размеров селезенки;
- болезненность в левом подреберьи и др.
Гемолиз эритроцитов бывает двух видов. Первый вид гемолиза называется внутриклеточным, то есть разрушение эритроцитов происходит в селезенке посредством поглощения дефектных эритроцитов лимфоцитами и фагоцитами. Второй вид гемолиза называется внутрисосудистым, то есть разрушение эритроцитов имеет место в кровеносном русле под действием циркулирующих в крови лимфоцитов, антител и комплемента. Определение вида гемолиза крайне важно, поскольку дает исследователю подсказку, в каком направлении далее продолжать поиски причины разрушения красных кровяных телец.
Подтверждение внутриклеточного гемолиза осуществляется при помощи следующих лабораторных показателей:
- гемоглобинемия – наличие свободного гемоглобина в крови вследствие активного разрушения эритроцитов;
- гемосидеринурия – наличие в моче гемосидерина – продукта окисления в почках избыточного гемоглобина;
- гемоглобинурия – наличие в моче неизмененного гемоглобина, признака крайне высокой скорости разрушения эритроцитов.
Подтверждение внутрисосудистого гемолиза осуществляется при помощи следующих лабораторных анализов:
- общий анализ крови – снижение количества эритроцитов и\или гемоглобина, увеличение количества ретикулоцитов;
- биохимический анализ крови – увеличение общего билирубина за счет непрямой фракции.
- мазок периферической крови – при различных способах окраски и фиксации мазка определяется большинство аномалии строения эритроцита.
При исключении гемолиза исследователь переключается на поиск иной причины анемии.
Причин развития гемолиза огромное множество, соответственно их поиск может занять непозволительно много времени. В таком случае необходимо максимально детально выяснить анамнез заболевания. Иными словами, требуется выяснить места, которые посещал пациент в последние полгода, где работал, в каких условиях жил, очередность появления симптомов заболевания, интенсивность их развития и многое другое. Такая информация может оказаться полезной для сужения круга поиска причин гемолиза. При отсутствии таковой информации осуществляется ряд анализов на определение субстрата наиболее частых заболеваний, приводящих к разрушению эритроцитов.
Анализами второго этапа диагностики являются:
- прямой и непрямой тест Кумбса;
- циркулирующие иммунные комплексы;
- осмотическая резистентность эритроцитов;
- исследование активности ферментов эритроцита (глюкоза-6-фосфатдегидрогназа (Г-6-ФДГ), пируваткиназа и др.);
- электрофорез гемоглобина;
- проба на серповидность эритроцитов;
- проба на тельца Гейнца;
- бактериологический посев крови;
- исследование «толстой капли» крови;
- миелограмма;
- проба Хема, проба Хартмана (сахарозная проба).
Прямой и непрямой тест Кумбса
Данные тесты осуществляются с целью подтверждения или исключения аутоиммунной гемолитической анемии. Циркулирующие иммунные комплексы косвенно свидетельствуют об аутоиммунной природе гемолиза.
Осмотическая резистентность эритроцитов
Снижение осмотической резистентности эритроцитов чаще развивается при врожденных формах гемолитических анемий, таких как сфероцитоз, овалоцитоз и акантоцитоз. При талассемии, напротив, наблюдается увеличение осмотической резистентности эритроцитов.
Исследование активности ферментов эритроцитов
С данной целью сначала осуществляют качественные анализы на наличие или отсутствие искомых ферментов, а затем прибегают к количественным анализам, осуществляемым при помощи ПЦР (полимеразной цепной реакции). Количественное определение ферментов эритроцитов позволяет выявить их снижение по отношению к нормальным значениям и диагностировать скрытые формы эритроцитарных ферментопатий.
Электрофорез гемоглобина
Исследование осуществляется с целью исключения как качественных, так и количественных гемоглобинопатий (талассемий и серповидноклеточной анемии).
Проба на серповидность эритроцитов
Сутью данного исследования является определение изменения формы эритроцитов по мере снижения парциального давления кислорода в крови. В случае если эритроциты принимают серповидную форму, то диагноз серповидноклеточной анемии считается подтвержденным.
Проба на тельца Гейнца
Целью данной пробы является обнаружение в мазке крови специальных включений, являющихся нерастворимым гемоглобином. Данная проба осуществляется для подтверждения такой ферментопатии как дефицит Г-6-ФДГ. Однако нужно помнить, что тельца Гейнца могут появиться в мазке крови при передозировке сульфаниламидов или анилиновых красителей. Определение данных образований осуществляется в темнопольном микроскопе или в обычном световом микроскопе при специальном окрашивании.
Бактериологический посев крови
Бак-посев проводится с целью определения видов циркулирующих в крови инфекционных агентов, которые могут взаимодействовать с эритроцитами и вызывать их разрушение прямым путем или посредством иммунных механизмов.
Исследование «толстой капли» крови
Данное исследование проводится с целью выявления возбудителей малярии, жизненный цикл которых тесно сопряжен с разрушением эритроцитов.
Миелограмма
Миелограмма является результатом пункции костного мозга. Данный параклинический метод позволяет выявить такие патологии как злокачественные заболевания крови, которые посредством перекрестной иммунной атаки при паранеопластическом синдроме разрушают и эритроциты. Помимо этого в пунктате костного мозга определяется разрастание эритроидного ростка, что свидетельствует о высоких темпах компенсаторной продукции эритроцитов в ответ на гемолиз.
Проба Хема. Проба Хартмана (сахарозная проба)
Обе пробы проводятся с целью определения длительности существования эритроцитов того или иного пациента. Для того чтобы ускорить процесс их разрушения, тестируемый образец крови помещают в слабый раствор кислоты или сахарозы, а затем оценивают процент разрушенных эритроцитов. Проба Хема считается положительной при разрушении более 5% эритроцитов. Проба Хартмана считается положительной, когда разрушается более 4% эритроцитов. Положительная проба свидетельствует о пароксизмальной ночной гемоглобинурии.
Помимо представленных лабораторных тестов для установления причины гемолитической анемии могут быть проведены другие дополнительные тесты и инструментальные исследования, назначаемые специалистом в области того заболевания, которое предположительно является причиной гемолиза.
Лечением первичных идиопатических (неясной причины) гемолитических анемий, а также вторичных гемолитических анемий вследствие заболеваний системы крови занимается врач-гематолог. Лечение вторичных гемолитических анемий по причине других заболеваний выпадает на долю того специалиста, в поле деятельности которого находится данное заболевание. Таким образом, анемию, вызванную малярией, будет лечить врач-инфекционист. Аутоиммунную анемию будет лечить врач-иммунолог или аллерголог. Анемию вследствие паранеопластического синдрома при злокачественной опухоли будет лечить онкохирург и т. д.
Основой лечения аутоиммунных болезней и, в частности, гемолитической анемии являются глюкокортикоидные гормоны. Они применяются длительное время – сначала для купирования обострения гемолиза, а затем в качестве поддерживающего лечения. Поскольку глюкокортикоиды обладают рядом побочных действий, то для их профилактики осуществляется вспомогательное лечение витаминами группы B и препаратами, снижающими кислотность желудочного сока.
Помимо снижения аутоиммунной активности большое внимание должно уделяться профилактике ДВС-синдрома (нарушение процесса свертываемости крови), в особенности при средней и высокой интенсивности гемолиза. При низкой эффективности глюкокортикоидной терапии препаратами последней линии лечения являются иммунодепрессанты.
| Медикамент | Механизм действия | Способ применения |
| Преднизолон | Является представителем глюкокортикоидных гормонов, обладающих наиболее выраженным противовоспалительным и иммуносупрессивным действием. | 1 – 2 мг\кг\сутки внутривенно, капельно. При выраженном гемолизе дозу препарата увеличивают до 150 мг\сутки. После нормализации показателей гемоглобина дозу медленно снижают до 15 – 20 мг\сутки и продолжают лечение еще 3 – 4 месяца. После этого дозу снижают по 5 мг каждые 2 – 3 дня до полной отмены препарата. |
| Гепарин | Является прямым антикоагулянтом короткого действия (4 – 6 часов). Данный препарат назначается для профилактики ДВС-синдрома, часто развивающегося при остром гемолизе. Применяется при нестабильном состоянии пациента для более совершенного контроля свертываемости. | 2500 – 5000 МЕ подкожно каждые 6 часов под контролем коагулограммы. |
| Надропарин | Является прямым антикоагулянтом длительного действия (24 – 48 часов). Назначается пациентам со стабильным состоянием для профилактики тромбоэмболических осложнений и ДВС. | 0,3 мл\сутки подкожно под контролем коагулограммы. |
| Пентоксифиллин | Периферический вазодилататор с умеренным антиагрегантным действием. Увеличивает поступление кислорода к периферическим тканям. | 400 – 600 мг\сутки в 2 – 3 приема внутрь в течение минимум 2 недель. Рекомендуемая длительность лечения 1 – 3 месяца. |
| Фолиевая кислота | Относится к группе витаминов. При аутоиммунной гемолитической анемии используется с целью восполнения его запасов в организме. | Лечение начинают с дозы 1 мг\сутки, а затем увеличивают ее до появления стойкого клинического эффекта. Максимальная суточная доза – 5 мг. |
| Витамин В12 | При хроническом гемолизе запасы витамина В12 постепенно истощаются, что приводит к увеличению диаметра эритроцита и снижению его пластических свойств. Во избежание данных осложнений осуществляется дополнительное назначение данного препарата. | 100 – 200 мкг\сутки внутримышечно. |
| Ранитидин | Назначается с целью снижения агрессивного действия преднизолона на слизистую желудка посредством снижения кислотности желудочного сока. | 300 мг\сутки в 1 – 2 приема внутрь. |
| Хлористый калий | Является внешним источником ионов калия, которые вымываются из организма в процессе лечения глюкокортикоидами. | 2 – 3 г в сутки под ежедневным контролем ионограммы. |
| Циклоспорин А | Препарат из группы иммунодепрессантов. Применяется в качестве последней линии лечения при неэффективности глюкокортикоидов и спленэктомии. | 3 мг\кг\сутки внутривенно, капельно. При выраженных побочных эффектах осуществляется отмена препарата с переходом к другому иммунодепрессанту. |
| Азатиоприн | Иммунодепрессант. | 100 – 200 мг\сутки в течение 2 – 3 недель. |
| Циклофосфамид | Иммунодепрессант. | 100 – 200 мг\сутки в течение 2 – 3 недель. |
| Винкристин | Иммунодепрессант. | 1 – 2 мг\неделю капельно в течение 3 – 4 недель. |
При дефиците Г-6-ФДГ рекомендуется избегать применения препаратов, входящих в группу риска. Тем не менее, при развитии острого гемолиза на фоне данного заболевания осуществляется немедленная отмена препарата, вызвавшего разрушение эритроцитов, и при острой необходимости переливается отмытая донорская эритроцитарная масса.
При тяжелых формах серповидноклеточной анемии или талассемии, требующих частых переливаний крови, назначается Дефероксамин – препарат, связывающий избыток железа и выводящий его из организма. Таким образом осуществляется профилактика гемохроматоза. Еще одним выходом для пациентов с тяжелой формой гемоглобинопатий является пересадка костного мозга от совместимого донора. При успешности данной процедуры существует вероятность значительного улучшения общего состояния пациента, вплоть до полного выздоровления.
В случае, когда гемолиз выступает в качестве осложнения определенного системного заболевания и является вторичным, все лечебные мероприятия должны быть направлены на излечение заболевания, ставшего причиной разрушения красных кровяных телец. После излечения первичного заболевания прекращается и разрушение эритроцитов.
При гемолитической анемии наиболее практикующейся операцией является спленэктомия (удаление селезенки). Данная операция показана при первом рецидиве гемолиза после проведенного лечения глюкокортикоидными гормонами аутоиммунной гемолитической анемии. Помимо этого спленэктомия является предпочтительным методом лечения таких наследственных форм гемолитических анемий как сфероцитоз, акантоцитоз, овалоцитоз. Оптимальным возрастом, при котором рекомендуется удаление селезенки в случае вышеперечисленных заболеваний, является возраст 4 – 5 лет, однако в индивидуальных случаях операция может быть проведена и в более раннем возрасте.
Талассемия и серповидноклеточная анемия длительное время может лечиться посредством переливания донорских отмытых эритроцитов, однако при наличии признаков гиперспленизма, сопровождающегося снижением количества и остальных клеточных элементов крови, операция по удалению селезенки является оправданной.

Первичная профилактика идиопатических аутоиммунных анемий не производится за отсутствием причин таковых.
Первичная профилактика вторичных аутоиммунных анемий заключается в:
- избегании сопутствующих инфекций;
- избегании нахождения в среде с низкой температурой при анемии с холодовыми антителами и с высокой температурой при анемии с тепловыми антителами;
- избегании укусов змей и нахождении в среде с высоким содержанием токсинов и солей тяжелых металлов;
- избегании употребления медикаментов из расположенного ниже списка при дефиците фермента Г-6-ФДГ.
При дефиците Г-6-ФДГ гемолиз вызывают следующие медикаменты:
- антималярийные средства — примахин, памахин, пентахин;
- обезболивающие и жаропонижающие — ацетилсалициловая кислота (аспирин);
- сульфаниламиды — сульфапиридин, сульфаметоксазол, сульфацетамид, дапсон;
- другие антибактериальные препараты — хлорамфеникол, налидиксовая кислота, ципрофлоксацин, нитрофураны;
- противотуберкулезные средства — этамбутол, изониазид, рифампицин;
- препараты других групп — пробенецид, метиленовый синий, аскорбиновая кислота, аналоги витамина К.
Вторичная профилактика заключается в своевременной диагностике и соответствующем лечении инфекционных заболеваний, способных вызвать обострение гемолитических анемий.
источник