Гиперхромная анемия – группа заболеваний крови с цветовым показателем выше 1,15, характеризующихся нарушением функции кроветворения.
Гиперхромная макроцитарная анемия включает в себя следующие заболевания:
Причина В12-дефицитной анемии – недостаток витамина В12 в организме. Это может быть связано с нарушением режима питания и несбалансированным рационом, в котором недостаточно витамина В12. Также заболевание развивается при недостаточной выработке фактора всасывания витамина В12. Препараты для лечения гиперхромных анемий подбираются врачом, в зависимости от ее типа и причины.
Признаки анемии, вызванной недостатком витамина В12, можно объединить в три синдрома: анемический (слабость, головокружение, шум в ушах), гастроэнтерологический (похудение, тошнота, запоры, ярко-красный язык) и неврологический (онемение конечностей, мышечная слабость, судороги).
Диагноз ставится на основании анализа крови, который показывает снижение уровня эритроцитов и лейкоцитов, дефектное развитие эритроцитов, повышенный уровень билирубина. Изучение костного мозга определяет наличие крупных эритроцитов с ядерными остатками.
Средства для лечения гиперхромной анемии, вызванной дефицитом витамина В12, подбираются с учетом основного заболевания, которое является причиной анемии. Также нужно ликвидировать факторы, спровоцировавшие В12-дефицитную анемию.
Применяют при гиперхромной анемии цианокобаламин (витамин В12), который вводится больному внутримышечно. Если есть угроза жизни пациента, требуется переливание эритроцитарной массы.
Лечение гиперхромной анемии, вызванной дефицитом витамина В12, заключается также в правильном питании. Больному нужно есть мясо, рыбу, печень, сыр и другие продукты, содержащие витамин В12 и другие микроэлементы, необходимую для нормального функционирования организма.
Заболевание развивается из-за недостаточного поступления фолиевой кислоты в организм или нарушения ее всасывания в ЖКТ. Фолиеводефицитная анемия может возникнуть в результате нарушения питания, алкоголизма, заболеваниях печени, беременности и грудного вскармливания.
Пациенты жалуются на плохое самочувствие, а именно на слабость, головокружение, учащенное сердцебиение, быструю утомляемость. У больного наблюдается бледный цвет кожи и губ и ярко-красный язык. Гастроэнтерологические и неврологические симптомы при фолиеводефицитной анемии, в отличие от В12-дефицитной анемии, отсутствуют.
Анализ крови при дефиците фолиевой кислоты выявляет снижение уровня гемоглобина, числа эритроцитов, тромбоцитов и лейкоцитов. Диагноз подтверждается после определения уровня фолиевой кислоты в эритроцитах.
Необходимо вылечить основное заболевание, ставшее причиной фолиеводефицитной анемии. Пациенту необходимо пропить курс фолиевой кислоты для восполнения ее дефицита в организме. Если же в организме больного имеется нарушение функции всасывания фолиевой кислоты, то препарат придется принимать всю жизнь.
Миелодиспластическим синдромом называется группа заболеваний, при которых происходит нарушение образования клеток крови в костном мозге.
Синдром может возникнуть спонтанно или вследствие облучения и использования химиопрепаратов.
При миелодиспластическом синдроме у пациентов наблюдается быстрая утомляемость, одышка и учащенное сердцебиение при малейших физических нагрузках, головокружение и другие симптомы анемии. Также диагноз может быть случайно установлен при лечении других заболеваний, например, тромбоза.
Диагностика миелодиспластического синдрома подразумевает тщательный анализ крови и исследование костного мозга. Метод лечения зависит от возраста пациента, наличия у него каких-либо заболеваний и риска перехода миелодиспластического синдрома в острый лейкоз. Проводится внутривенное вливание эритроцитарной и тромбоцитарной массы, проводится иммунотерапия при помощи антитимоцитарного глобулина или циклоспорина А, назначаются препараты, индуцирующие дифференцировку клеток, проводится химиотерапия. Эти методы не имеют долгосрочного эффекта и помогают только продлить жизнь. Полностью достичь выздоровления можно только при помощи трансплантации костного мозга.
НОВЫЙ СПЕЦИАЛИСТ- КОСМЕТОЛОГ
С 01 марта в нашем центре ведет прием новый специалист- врач косметолог Юлия Олеговна Чубарова. Юлия Олеговна проводит уходовые процедуры на профессиональной косметике Cell Fusion, Holy Land (атравматическая чистка лица), УЗ и комбинированные чистки лица, микротоковую терапию, фотоомоложение, сеансы лазерной биоревитализации, фотоэпиляцию, процедуры плазмолифтинг, а также инъекционную биоревитализацию, мезотерапию и контурную пластику. Запись на БЕСПЛАТНУЮ КОНСУЛЬТАЦИЮ и процедуры предварительная — по тел.регистратуры, а также в форме zapis@mcprofessor.ru.
подробнее »
НОВЫЕ ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
С 10 12 18 в нашем центре дополнительно вводятся следующие исследования крови:
Гастропанель, Альфа-фетопротеин, маркер CA 72-4, Трансферрин, Anti-HAV антитела, Аполипопротеин А1, Аполипопротеин В, D-димер.
Посевы на Ureaplasma species, Гемолитический стрептококк группы А, Аэробную и факультативно- анаэробную флору, Грибы Candida Asp., Cryptococcus.
Обращаем Ваше внимание, что анализы крови сдаются ежедневно без записи, начиная с 09 утра (расписание работы процедурного кабинета в разделе Запись на прием). Посевы сдаются только в составе приема специалистов, отдельного забора на данные исследования нет.
подробнее »
источник
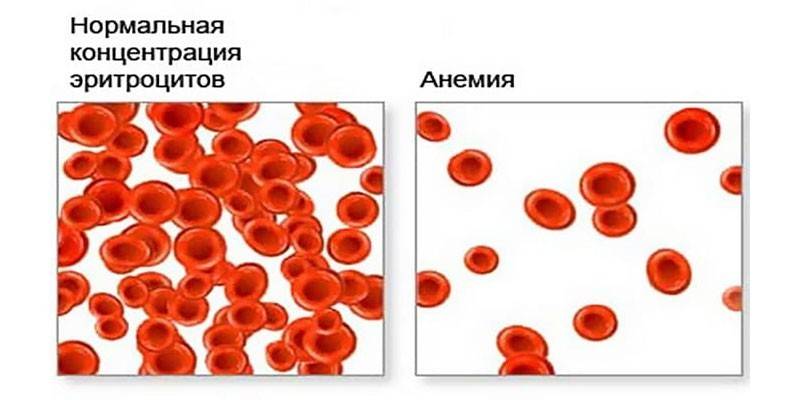
Понижение уровня гемоглобина в крови, преимущественно на фоне падения числа эритроцитов, в медицине известно как анемия – заболевание, являющееся симптомом разных патологических состояний. Одной из разновидностей анемии является гиперхромная, особенно часто поражающая лиц зрелого и преклонного возраста. Почему она возникает и как ее лечить?
Заболевание, известное большинству людей как малокровие, в официальной медицине названное «анемия», связано с падением уровня гемоглобина. При гиперхромной форме одновременно с этим снижается количество здоровых эритроцитов и появляются дефектные: содержащие в себе избыток железа. Благодаря этому веществу кровяные тельца становятся пресыщены гемоглобином, поэтому срединное просветление у них закрыто алым цветом (это видно при лабораторном исследовании анализов). Существует 2 вида анемии гиперхромной:
- Мегалобластная (макроцитарная) – характеризуется нарушением синтеза ДНК и РНК, что приводит к появлению очень крупных эритроцитов (мегалобластов и мегалоцитов) в костном мозге. Такая анемия может передаться по наследству.
- Немегалобластная – синтез ДНК в норме, костный мозг не продуцирует мегалобласты, но дефектные эритроциты присутствуют.
Большинство врачей не считают анемию самостоятельным заболеванием, поскольку она может развиться на фоне первичного поражения системы крови или при иных патологиях, никак с этим не связанных. По этой причине отсутствует строгая нозологическая классификация и, помимо уже упомянутого деления гиперхромного типа на 2 вида, существует группировка по состояниям, которым она соответствует:
- Витамин В12-дефицитная (пернициозная) анемия – болезнь Аддисона-Бирмера, злокачественное малокровие, обусловленное нехваткой витамина В12. Характеризуется образованием в костном мозге незрелых мегалобластов, может проявляться неврологическими расстройствами.
- Фолиеводефицитная анемия – тоже пернициозная, только возникает при дефиците фолиевой кислоты.
- Миелодиспластический синдром – характеризуется цитопенией (дефицит 1-ого или нескольких видов кровяных телец) в периферической крови, дисплазией (неправильным развитием) костного мозга. Заболевание склонно к переходу в острую форму лейкоза (недоброкачественное поражение системы кроветворения), тяжело поддается лечению (преимущественно проводится поддерживающая терапия). По официальной статистике 80% пациентов с миелодиспластическим синдромом старше 60-ти лет.
Дефицит витамина В12 (цианокобаламин) и фолиевой кислоты являются самыми распространенными отправными точками к развитию анемии гиперхромного типа, но эти состояния могут возникать под воздействием целого ряда факторов. Конкретный перечень причин для каждой ситуации свой. Нехватку цианокобаламина провоцируют:
- патологические процессы в подвздошной кишке, при которых происходит нарушение усвояемости питательных веществ за счет плохого всасывания ее стенками;
- инфекционные патологии кишечника, тоже нарушающие процесс всасывания витаминов;
- глисты – ленточные черви и бактерии активно поглощают витамин В12;
- атрофический гастрит, при котором в париетальных клетках желудка наблюдается недостаточный синтез внутреннего фактора Касла (фермент, который переводит цианокобаламин из неактивной формы в усваивающуюся).
У анемии гиперхромного типа, которая возникает как результат дефицита фолиевой кислоты, провоцирующие факторы выглядят иначе. Зачастую с таким состоянием сталкиваются женщины во время беременности, поскольку вся фолиевая кислота идет на строительство нервной трубки плода. Влияние могут оказывать и:
- алкоголизм;
- заболевания печени (особенно гепатит, цирроз, печеночная недостаточность).
Отдельно врачами упоминается гиперхромная макроцитарная анемия, которая носит наследственный характер (аутосомно-рецессивная передача – от родителей) и развивается на фоне генетических мутаций, а у женщин предпосылкой к ее возникновению является и прием гормональных препаратов. Если не рассматривать отдельные разновидности анемии, при которой у эритроцитов появляются гиперхромные ядра, в число общих причин можно включить:
- длительное голодание или нерациональное питание (с дефицитом витаминов и микроэлементов в пище);
- курение;
- наличие опухолей;
- инфекции (особенно ВИЧ) и вирусы;
- регулярная большая потеря крови во время менструации;
- рак желудка, гастрэктомия (его полное вырезание);
- гипотиреоз (дефицит гормонов щитовидной железы);
- прием лекарственных препаратов (Метформин, Неомицин, Дифенин);
- частые расстройства кишечника.
Заболевание имеет внешние и внутренние проявления: последние подразумевают изменения общего самочувствия, которые не всегда специфичны и не дают возможности поставить точный диагноз. К таким симптомам гиперхромного малокровия относятся:
- повышенная сонливость, усталость;
- снижение работоспособности;
- потеря концентрации внимания.
Данная клиническая картина характерна большинству случаев анемии, поэтому болезнь распознается исключительно после проведения лабораторных исследований. Если течение более тяжелое, могут добавиться:
- тахикардия (учащенный пульс);
- одышка при минимальных физических нагрузках (даже после быстрой ходьбы);
- шум в ушах (не постоянный);
- нарушения сна;
- потеря аппетита;
- головные боли;
- снижение либидо (полового влечения).
Почти во всех случаях гиперхромного малокровия можно наблюдать изменения во внешности: кожные покровы бледнеют, кожа истончается, становится сухой, на руках может приобрести желтоватый оттенок. В волосах появляется ранняя седина. Общая клиническая картина выраженной анемии дополняется следующими симптомами:
- потеря веса;
- расстройство зрения и слуха;
- тошнота, рвота;
- потеря вкуса, отсутствие влечения к ранее любимым продуктам и блюдам;
- мышечная слабость;
- онемение нижних конечностей;
- чувство зябкости;
- покраснение языка до малинового цвета, поверхность становится блестящей.
Лица, у которых гиперхромная анемия сочетается с миелопластическим синдромом, часто испытывают головокружения, повышенную утомляемость. Не исключены боли за грудиной при сильном сердцебиении и одышке. При сильном поражении нервной системы у пациента нарушается чувствительность пальцев (на ногах и руках), могут случаться потеря сознания, судороги. Артериальное давление преимущественно пониженное, печень увеличена (прощупывается при пальпации).
Авитаминоз по фолиевой кислоте для будущей матери – распространенное явление, поскольку этот элемент (вместе с цианокобаламином) требуется для полноценной жизнедеятельности плода. Потребность в витаминах В9 и В12 у беременной вырастает в 2 раза. При стремительном развитии и тяжелом течении анемия может спровоцировать преждевременные роды, недостаточный вес новорожденного, отслоение плаценты, внутриутробные кровотечения.
У детей анемия, при которой наблюдается гиперхромия эритроцитов, может привести к отставанию в развитии умственном и физическом, снижении защитных сил организма (ребенок будет часто подхватывать ОРВИ, тяжело переносить даже простуду). У взрослых распространенным осложнением анемии являются дефицит кислорода в крови, поражения нервной системы, на фоне чего возникают:
- гипоксия (кислородное голодание) мозга;
- ухудшение памяти и мышления;
- отмирание клеток головного мозга и нарушения работы его сосудов;
- сердечная недостаточность (может окончиться летальным исходом).
Отсутствие специфической клинической картины для анемии любого типа повышает значимость диагностических мероприятий для уточнения заболевания. Общий анализ крови является первичной проверкой, по результатам которой можно увидеть изменения в структуре эритроцитов (форма и размеры клеток), обнаружить ядерные тельца Жолли. При наличии подозрений на гиперхромное малокровие врач дополнительно назначает:
- биохимическое исследование крови – для определения уровня билирубина, сывороточного уровня железа;
- рентгеноскопию ОБП (органов брюшной полости);
- УЗИ органов пищеварения;
- иммунологическое исследование – помогает выявить антитела, которые специфичны против антигенов цитоплазмы париетальных клеток желудка и внутреннего фактора Касла.
Для легких форм гиперхромного малокровия основу терапевтической схемы составляет коррекция рациона питания, особенно если проблема кроется в дефиците фолиевой кислоты или витамина В12. Дополнительно за день важно принимать с едой 8 мг железа. Меню базируется на следующих продуктах:
- печень куриная, говяжья (2-3 раза в неделю);
- гречневая крупа;
- рыба (особенно треска);
- мясо (желательно ввести в рацион кролика);
- куриные яйца;
- сыры;
- бобовые культуры.
Обязательно употребление свежих овощей и фруктов, дополняющих список полезных при анемии продуктов. От острой и жареной пищи стоит отказаться, поскольку она раздражает пищеварительную систему. Кофеин тоже исключен, поскольку он мешает усваиваться железу. Такой диеты следует придерживаться несколько месяцев (в некоторых случаях – больше года), она актуальна для всех стадий заболевания, но не исключена индивидуальная коррекция рациона под конкретную клиническую картину. Медикаментозное лечение зависит от причин анемии и ее течения:
- Терапия легких дефицитных состояний начинается с назначения Цианокобаламина: синтетического аналога витамина В12, который принимается перорально или вводится внутримышечно. Если спустя 1-1,5 недели после начала его использования положительной динамики не наблюдается, врач выписывает Фолиевую кислоту (таблетки), Фемибион. В некоторых случаях проводится одновременное лечение обоими препаратами.
- При средней степени выраженности анемии Цианокобаламин или Оксикобаламин (более сильный препарат для тяжелых случаев) вводятся внутривенно и на 5-8 день отслеживается уровень ретикулоцитов: их количество должно возрасти на 20-30%.
- По необходимости назначаются препараты железа – Мальтофер, Гемофер (таблетки, инъекции), особенно если заболевание диагностировано у ребенка.
- Во время беременности (или после родов, если состояние не улучшается) врач может назначить пациентке внутривенное введение витаминных препаратов, начиная с больших доз. После они уменьшаются, а инъекционная форма заменяется на пероральную.
Восстановление показателей крови происходит быстро: уже через месяц можно видеть результат, а неврологические нарушения устраняются медленнее и могут требовать дополнительных препаратов. Если начальную (легкую) форму гиперхромного малокровия можно лечить амбулаторно (дома), то средняя и тяжелая требуют помещения пациента в стационар, где ему будут делать инъекции лекарственных средств и постоянно отслеживать состояние. Несколько моментов лечения таких случаев анемии:
- Резкое нарушение гемодинамики, падение гемоглобина ниже 70 г/л (тяжелая форма анемии) требуют немедленной гемотрансфузии – переливания крови.
- При миелодиспластическом синдроме обязательны госпитализация, гемотрансфузия (переливаются эритроцитарная и тромбоцитарная массы, зачастую с замещением клеток) и внутривенное введение препаратов, ускоряющих деление кровяных телец, чтобы предотвратить лейкоз.
- Если лечение подразумевает инъекционное введение лекарственных средств одновременно с приемом таблеток, такой курс длится 2-3 месяца. После раз в неделю делают 1 укол, оставляя таблетки, а через 2 месяца их ставят с частотой 1 раз в 14 дней. Основной формой лечения не тяжелых состояний являются таблетки.
Лечение анемии гиперхромной длится от полугода до года, дефицитные состояния за этот срок полностью устраняются. При миелодиспластическом синдроме терапия стационарная, прогноз неутешительный, поскольку препараты только способствуют увеличению срока жизни и сдвигают момент ремиссии. Шансы на исключение летального исхода возникают только при пересадке костного мозга.
Соблюдение принципов здорового питания, поддержание хорошего уровня витаминов В9 и В12, железа – самый простой и важный способ защиты от гиперхромного малокровия, особенно для беременных. Диета, используемая для его лечения, одновременно носит и профилактический характер. Дополнительно стоит:
- регулярно посещать гастроэнтеролога;
- заниматься спортом;
- отказаться от курения;
- не контактировать с ядохимикатами;
- гулять на свежем воздухе;
- своевременно лечить инфекционные заболевания, выводить паразитов;
- принимать витаминно-минеральные комплексы.
источник
Гиперхромные анемии (цветовой показатель выше 1.05) делятся на две разновидности:
1) мегалобластные (при мегалобластных анемиях по разным причинам нарушен синтез ДНК и РНК, поэтому в костном мозге появляются особого вида клетки — мегаблобласты):
К мегалобластным анемиям также относят:
- анемию при миелодиспластическом синдроме (МДС),
- лекарственную анемию, вызванную разными препаратами:
- 5-фторурацил (лечение злокачественных опухолей),
- азатиоприн (лечение аутоиммунных заболеваний),
- метотрексат (лечение злокачественных опухолей и ревматических заболеваний),
- гидроксимочевина (лечение опухолей кроветворной ткани),
- противосудорожные препараты (лечение эпилепсии),
- зидовудин (лечение ВИЧ-инфекции).
2) немегалобластные (здесь синтез ДНК нормальный, а в костном мозге нет мегалобластов):
- при болезнях печени,
- алкоголизме,
- гипотиреозе (сниженной функции щитовидной железы),
- опухолях,
- апластической анемии (об этих анемиях читайте дальше в разделе нормохромных анемий),
- миелопролиферативных заболеваниях (полицитемия, лейкозы и др.). Название произошло от греч. myelos — спинной мозг, англ. proliferation — размножение.
На этой странице я расскажу только о мегалобластных анемиях:
- В12–дефицитная анемия,
- фолиеводефицитная анемия,
- миелодиспластический синдром.
Витамин B12 необходим для синтеза ДНК в клетках, поэтому от дефицита B12 в первую очередь страдают быстро обновляющиеся ткани — все клетки крови и эпителий желудочно-кишечного тракта (это напоминает острую лучевую болезнь, которая вызывается ионизирующим излучением). При нехватке B12 эритроцитов в крови становится мало, а гемоглобина в них — много. В костном мозге появляется большое количество мегалобластов (это крупные клетки, являющиеся далекими предками эритроцитов), поэтому В12–дефицитная и фолиеводефицитная анемия относятся к мегалобластным. Помимо поражения костного мозга и ЖКТ, нехватка витамина B12 также приводит к накоплению в организме токсической метилмалоновой кислоты, которая нарушает функционирование нервной ткани. [И здесь тоже можно провести любопытные параллели с острой лучевой болезнью: при высокой дозе облучения так же поражается головной мозг с развитием церебральной формы острой лучевой болезни].
Нормальный (I) и мегалобластный (III) тип эритропоэза.
Эритропоэз — образование эритроцитов.
Источник: http://bono-esse.ru/blizzard/Lab/Anemia/morfologia_kinetika_eritropoeza.html
В организме имеется значительный запас витамина В12, которого хватает на 3-5 лет. Однако всасывание этого витамина является сложным и многоступенчатым процессом. При резком нарушении всасывания развивается болезнь Аддисона-Бирмера (В12–дефицитная анемия). Лечить эту анемию раньше не умели, течение было неблагоприятным и через некоторое время из-за падения гемоглобина до 30–40 г/л всё заканчивалось комой и смертью больного, поэтому анемию назвали злокачественной (пернициозной).
Частота В12-дефицитной анемии увеличивается с возрастом — от 0.1% у молодых до 4% лиц старше 75 лет. Причин дефицита витамина B12 много, но самая частая — атрофический гастрит (воспалительные изменения в слизистой оболочке желудка с уменьшением ее массы, объёма и выполняемых функций).
Для дефицита В12 характерно поражение нервной системы в виде фуникулярного миелоза (это дегенерация задних и боковых столбов спинного мозга) с развитием нарушений чувствительности [онемение, покалывание, чувство жара] и постепенным распространением от пальцев ног и рук к туловищу, а затем с присоединением двигательных нарушений [слабость мышц ног и рук, недержание мочи и кала, апатия, депрессия, психозы]).
Обратите внимание, что у большой части пациентов (28–40%) дефицит витамина В12 проявлется ТОЛЬКО поражением нервной системы, то есть единственным признаком дефицита В12 являются неврологические и психиатрические симптомы. При отсутствии лечения через несколько месяцев эти нарушения станут необратимыми. Поскольку дефицит витамина B12 широко распространен (до 4% среди лиц старше 75 лет), нетрудно догадаться, что многие больные не получают необходимой помощи своевременно, хотя лечение очень простое и дешевое — инъекции витамина B12 подкожно, внутримышечно или внутривенно. Рекомендуется проверять на дефицит витамина B12 всех пациентов психиатрических стационаров и всех людей старше 65 лет.
До сих пор не создан диагностический тест, являющий «золотым стандартом» диагностики B12-фолиеводефицитной анемии.
Предварительный диагноз B12-фолиеводефицитной анемии ставится на основании:
- общего анализа крови (гиперхромная анемия, нет ретикулоцитоза [повышенного уровня ретикулоцитов], число лейкоцитов и тромбоцитов также снижено),
- мазка периферической крови (неравномерность размера и дефекты развития эритроцитов),
Картина периферической крови при B12-фолиеводефицитной анемии.
- симптомы анемии и обострение кардиологических проблем (выше риск инфаркта миокарда и инсульта), ведь болеют чаще всего старые люди;
- поражение ЖКТ: боль, жжение в языке, снижение аппетита, похудение;
- неврологические симптомы: «мурашки по телу» (парестезии), скованность ног, неустойчивость, спастическая походка;
- психиатрические симптомы: неуравновешенность, изменение личности, снижение памяти, слабоумие, психозы, депрессия.
По возможности в крови определяют концентрацию витаминов B12 и B9, но их уровень мало специфичен, поскольку может повышаться и снижаться при разных состояниях (болезни печени, прием контрацептивов и др.). В сложных случаях делают пункцию грудины (мазок костного мозга), но эта процедура не является рутинным (простым, обыденным) исследованием.
До сих пор окончательный диагноз B12-фолиеводефицитной анемии ставится по результатам пробного лечения. Сперва назначается витамин B12 (цианокобаламин = оксикобаламин). Если на 2-14-й день лечения в крови резко увеличивается число ретикулоцитов (ретикулоцитарный криз) с пиком на 5-8-й день, то ставится окончательный диагноз B12-дефицитной анемии. Если такого криза нет, лечение продолжают фолиевой кислотой (см. рисунок). Категорически запрещается начинать лечение с фолиевой кислоты, поскольку это может усилить поражение нервной системы. Также нельзя начинать пробное лечение перед планируемой пункцией костного мозга, поскольку установлено, что для исчезновения мегалобластоза в костном мозге и нарастания уровня ретикулоцитов в крови достаточно всего одной инъекции витамина B12, B9 или преднизолона.
Алгоритм диагностики мегалобластных анемий.
Источник: Л. Б. Филатов «Анемии (клиника, диагностика, лечение)».
Пробное лечение витамином B12 является в современной медицине ярким примером древнего принципа «diagnosis ex juvantibus» (экс ювАнтибус, от лат. ex — исходя из, juvanus — помогающий), то есть диагностики по результатам лечения. Этот принцип «авось поможет» является вынужденной мерой, применяемой при значительных диагностических затруднениях и условии, что лечение не навредит пациенту. Этиология заболевания подтверждается эффективностью этиотропного лечения.
Второе название фолиевой кислоты — витамин B9. Дефицит фолиевой кислоты тоже характерен для пожилых людей:
- в 65-74 года — у 10%,
- у лиц старше 75 лет — в 20%.
Разумеется, часть пациентов с дефицитом витамина B9 имеет сопутствующий дефицит B12. Стандартных запасов фолиевой кислоты в организме достаточно на 4 месяца.
Обе анемии (В12– и фолиеводефицитная) практически не отличимы друг от друга, за исключением единственной особенности — поражение нервной системы в виде фуникулярного миелоза характерно только для дефицита В12.
Итак, лечение дефицита фолиевой кислоты можно начинать, только будучи уверенным, что нет дефицита витамина B12. При правильном лечении фолиевой кислотой ретикулоцитарный криз развивается через 5–8 дней от начала лечения.
На схеме диагностики мегалобластных анемий указан также миелодиспластический синдром. Что это такое?
Кроветворение (гемопоэз) делится на лимфопоэз (образование лимфоцитов — разновидности лейкоцитов) и миелопоэз (образование всех остальных форменных элементов крови). Дисплазия — нарушение развития.
Миелодиспластический синдром — это нарушение образования в костном мозге будущих клеток крови, в основе которого лежит генетическая поломка в одной из стволовых кроветворных клеток. В результате мутантная кроветворная клетка из разряда «бластных» (см. рисунок) получает какое-то преимущество перед остальными, активно делится и постепенно ее ущербные, но долгоживущие потомки целиком «заполняют» костный мозг, вытесняя все остальные нормальные клеточные линии. [Вам это ничего из жизни не напоминает?] В будущем, по мере накопления «свежих» генетических мутаций, миелодиспластический синдром может трансформироваться в острый лейкоз (злокачественная опухоль кроветворной системы с увеличением количества «бластных» клеток в костном мозге).
Этапы нормального кроветворения.
Миелодиспластический синдром возникает обычно у пожилых людей (60-85 лет). Средняя заболеваемость составляет 3-4 новых случая на 100 тыс. населения в год (среди людей старше 70 лет — 15 случаев на 100 тыс.)
Если вы хотите узнать больше про миелодиспластический синдром, рекомендую ознакомиться с понятной брошюрой «Сущность миелодиспластических синдромов» (PDF, 350 кб), созданной в 2002 году Международным фондом апластическoй анемии и МДС. Она предназначена специально для пациентов и членов их семей.
источник
Сущность Biz-дефицитной анемии (В12ДА) состоит в нарушении образования дезоксирибонуклеиновой кислоты (ДНК) в связи с нехваткой в организме витамина Bi2 (цианокобаламина), что приводит к нарушению кроветворения, появлению в костном мозге мегалобластов, внутри-костномозговому разрушению эритрокариоцитов, снижению количества эритроцитов и гемоглобина, лейкопении, нейтропении и тромбоцитопении, а также к изменению ряда органов и систем (пищеварительный тракт, ЦНС).
Этиология.В12ДА встречается значительно реже, чем ЖДА, и может быть вызвана следующими причинами:
1) нарушением секреции гастромукопротеина («внутренний фактор»)
при наследственно обусловленной атрофии желез желудка (пернициозная
анемия, или болезнь Аддисона — Бирмера), при органических заболева
ниях желудка (полипоз, рак), после гастрэктомии;
2) повышением расхода витамина Bi2 (инвазия широкого лентеца, ак
тивация кишечной микрофлоры при дивертикулезах тонкой кишки);
3) нарушением всасывания витамина Bi2 (органические заболевания
кишечника — спру, илеит, рак, состояние после резекции кишки, наслед
ственное нарушение всасывания — болезнь Имерслунд—Гресбека);
4) нарушением транспорта витамина Вп (дефицит транскобаламина);
5) образованием антител к «внутреннему фактору» или комплексу
«внутренний фактор» + витамин В12-
Сходную с В12ДА гиперхромную анемию вызывает дефицит фолиевой кислоты, который возникает при: 1) повышенном расходе (беременность); 2) вскармливании детей козьим молоком; 3) нарушении всасывания (органические заболевания кишечника, алкоголизм); 4) приеме некоторых лекарственных препаратов (противосудорожные, противотуберкулезные препараты, фенобарбитал, контрацептивы и др.).
Патогенез.Витамин В(2 состоит из двух коферментов — метилкоба-ламина и дезоксиаденозилкобаламина. Дефицит первого кофермента обусловливает нарушение синтеза ДНК, вследствие чего деление и созревание клеток красного ряда нарушаются, они избыточно растут, не утрачивая ядра. Большие клетки, содержащие ядра, называются мегалобласта-ми, они не созревают до мегалоцитов (гигантские эритроциты без ядер), легко гемолизируются, еще находясь в костном мозге. Дефицит витамина В(2 вызывает нарушение роста клеток лейкоцитарного и тромбоцитарного рядов, но это не так заметно сказывается на морфологии и количестве клеток, как нарушения эритропоэза.
При недостатке второго кофермента нарушается обмен жирных кислот, вследствие чего в организме происходит накопление токсичных продуктов пропионовой и метилмалоновой кислот: развивается поражение заднебоко-вых канатиков спинного мозга — фуникулярный миелоз (схема 26).
Клиническая картина.Проявления В^ДА, как это вытекает из схемы патогенеза, складываются из следующих синдромов: 1) циркуляторно-ги-поксического (при достаточной выраженности анемии и кислородного голодания тканей); 2) гастроэнтерологического; 3) неврологического; 4) гематологического (анемия гиперхромного типа).
Кроме этих синдромов, клиническая картина будет определяться также заболеванием, на основе которого развилась В^ДА.
На I этапе диагностического поиска при достаточно выраженной анемии могут наблюдаться симптомы, обусловленные циркуляторно-ги-поксическим синдромом (слабость, повышенная утомляемость, одышка при физической нагрузке, болевые ощущения в области сердца, сердцебиения). В случае нерезкого кислородного голодания тканей эти жалобы могут отсутствовать. Снижение аппетита, отвращение к мясу, боли в кончике языка и жжение, чувство тяжести в эпигастрии после еды, чередование поносов и запоров обусловлены поражением пищеварительного тракта и, в частности, выраженной секреторной недостаточностью желудка. При поражении ЦНС больные жалуются на головную боль, неустойчивую походку, зябкость, чувство онемения в конечностях, ощущение «ползания
| Схема 26. Патогенез В12-дефицитной анемии |
мурашек». Выраженность этих жалоб не всегда соответствует степени анемии, в период ремиссии заболевания жалобы могут отсутствовать. Весьма существенно, если все перечисленные жалобы предъявляет немолодой человек, в этих случаях вероятность В12ДА повышается.
В семейном анамнезе у больных с предполагаемой В12ДА могут быть больные с данным заболеванием. Злоупотребление алкоголем может быть одной из причин развития анемии.
Данные анамнеза могут помочь в предположении патогенетического варианта анемии. Развитие анемии после пребывания больного возле больших водоемов и употребления в пищу сырой или недостаточно обработанной рыбы заставляет предположить в качестве возможной причины дифилло-ботриоз. Если заболевание возникло у пожилого человека, страдающего хроническим гастритом, и развивается медленно, то можно думать о В12ДА. В случае, если симптомы со стороны пищеварительного тракта сочетаются со снижением массы тела и быстро прогрессируют, следует предположить в качестве причины заболевания злокачественное новообразование.
Наконец, сведения об успешном лечении больного витамином Bf2 позволяют с большой уверенностью рассматривать имеющуюся симптоматику как проявление В^ДА.
На II этапе диагностического поиска симптомы могут быть обусловлены поражением пищеварительного тракта и ЦНС. Кроме того, ряд неспецифических признаков повышает вероятность предположения о наличии у больного В12ДА. Так, бледность кожных покровов в сочетании с небольшой иктеричностью склер и одутловатостью лица наблюдается при В12ДА. Масса тела таких больных, как правило, нормальная или повышенная. Однако снижение массы тела может указывать на злокачествен-
ную опухоль как возможную причину ВпДА. Аналогичное значение имеет обнаружение увеличенного плотного лимфатического узла (метастаз опухоли?). Циркуляторно-гипоксический синдром проявляется так же, как и при ЖДА (расширение границ сердца влево, тахикардия, систолический шум, шум «волчка» на яремных венах).
Несомненное диагностическое значение имеет обнаружение при исследовании пищеварительного тракта признаков глоссита: сглаженные сосочки вплоть до полной их атрофии («полированный» язык). Печень несколько увеличена, может прощупываться селезенка. Однако все эти симптомы не являются обязательными для В12ДА. Отмечаются нарушения глубокой чувствительности, нижний спастический парапарез (картина псевдотабеса). Следует заметить, что изменения нервной системы наблюдаются далеко не во всех случаях, так что их отсутствие не исключает диагноза В12ДА.
Таким образом, данные II этапа в сочетании с анамнестическими данными и жалобами больного, хотя и выявляют ряд основных симптомов В12ДА, но дают основание лишь заподозрить эту форму болезни. Окончательный диагноз ставят после проведения серии лабораторных исследований.
На III этапе диагностического поиска при исследовании периферической крови выявляют следующие признаки: снижение количества эритроцитов (менее 310 12 /л), повышение цветового показателя (более 1,1), среднего содержания гемоглобина в эритроците (более 34 пг) и среднего объема эритроцита (более 120 мкм 3 ). Эритроцитометрическая кривая сдвинута вправо — увеличено количество макроцитов, появляются мега-лоциты — эритроциты диаметром более 12 мкм. Форма эритроцитов изменена — пойкилоцитоз. Встречаются единичные мегалобласты.
Дополнительный признак — появление нейтрофилов с гиперсегмен-тированными ядрами.
Если в картине периферической крови не обнаруживают характерных признаков, то производят стерналъную пункцию. Последняя позволяет выявить в костном мозге мегалобластический тип кроветворения.
Важным является определение содержания сывороточного железа: при ВпДА оно может быть в норме или повышено в связи с усиленным гемолизом эритроцитов. В этих случаях увеличено содержание непрямого билирубина. При исследовании желудочного сока часто выявляется гиста-миноустойчивая ахилия (характерный признак анемии Аддисона — Бирме-ра), эндоскопически — атрофия слизистой оболочки желудка.
Другие инструментальные методы исследования помогают обнаружить признаки миокардиодистрофии (развивается на фоне выраженной анемии), а также уточнить этиологию заболевания.
Диагностика. В диагностике В12ДА выделяют два этапа: 1) доказательство дефицита витамина Вп как причины анемии; 2) выявление причин дефицита витамина Bi2.
Критериями ВпДА являются: 1) снижение содержания эритроцитов (менее 3,0-10 12 /л); 2) повышение цветового показателя (более 1,1); 3) повышение содержания гемоглобина в эритроцитах (более 34 пг); 4) увеличение среднего объема эритроцита (более 120 мкм 3 ); 5) сдвиг эритроцитомет-рической кривой вправо (увеличение количества макроцитов, появление ме-галоцитов — эритроцитов диаметром более 12 мкм); 6) появление в мазках пунктата костного мозга элементов мегалобластного кроветворения; 7) по-
вышение содержания сывороточного железа (более 30,4 мкмоль/л); 8) снижение радиоактивности мочи после приема витамина Bi2, меченного радиоактивным кобальтом.
Для выявления причины анемии следует проводить рентгенологическое и эндоскопическое исследование пищеварительного тракта (опухоль желудка, дивертикулез тонкой кишки), гельминтологическое исследование (инвазия широким лентецом), функциональное исследование печени с биопсией (хронический гепатит, цирроз), исследование нейтрального жира в кишечнике (спру).
В12ДА следует дифференцировать от фолиеводефицитной анемии. При дефиците фолиевой кислоты наблюдается макроцитарная гиперхром-ная анемия, а в костном мозге могут обнаруживаться мегалобласты. Следует отметить, что дефицит фолиевой кислоты встречается значительно реже. В отличие от В12ДА при фолиеводефицитной анемии содержание фолиевой кислоты в сыворотке, а также в эритроцитах снижено. Кроме того, при окраске препарата костного мозга ализарином красным окрашиваются только мегалобласты, связанные с дефицитом В^, и не окрашиваются мегалобласты, связанные с дефицитом фолиевой кислоты.
Течение. Заболевание может резко обостриться. В таких случаях развивается коматозное состояние: потеря сознания, снижение температуры тела и АД, одышка, рвота, арефлексия, непроизвольное мочеиспускание. Между развитием коматозного состояния и падением уровня гемоглобина нет четких коррелятивных отношений (у больных с резко сниженным содержанием гемоглобина не наблюдается комы). Главную роль в патогенезе комы играют быстрый темп и степень снижения гемоглобина, резкая ишемия и гипоксия ЦНС.
Формулировка развернутого клинического диагнозаучитывает: 1) этиологию В12ДА (отдельно следует выделять такую форму анемии, как болезнь Аддисона — Бирмера); 2) стадию процесса (рецидив — ремиссия); 3) выраженность отдельных синдромов (обычно при наличии неврологических расстройств, обусловленных фуникулярным миелозом).
Лечение.Комплекс лечебных мероприятий при В12ДА следует проводить с учетом этиологии, выраженности анемии и наличия неврологических нарушений. При лечении следует ориентироваться на следующие положения:
• Непременным условием лечения В12ДА при глистной инвазии явля
ется дегельминтизация (для изгнания широкого лентеца назначают
фенасал по определенной схеме или экстракт мужского папоротни
ка).
• При органических заболеваниях кишечника и поносах следует при
менять ферментные препараты (панзинорм, фестал, панкреатин), а
также закрепляющие средства (карбонат кальция в сочетании с дер-
матолом).
• Нормализация кишечной флоры достигается приемом ферментных
препаратов (панзинорм, фестал, панкреатин), а также подбором
диеты, способствующей ликвидации синдромов гнилостной или
бродильной диспепсии.
• Сбалансированное питание с достаточным содержанием витаминов
белка, безусловным запрещением алкоголя — непременное условие
лечения Bir и фолиеводефицитной анемии.
• Патогенетическая терапия осуществляется с помощью парентерального введения витамина Bi2 (ликвидация его дефицита), а также нормализации измененных показателей центральной гемодинамики и нейтрализации антител к гастромукопротеину («внутреннему фактору») или комплексу гастромукопротеин + витамин В^ (корти-костероидная терапия). Цианкобаламин (витамин Вп) вводят ежедневно внутримышечно в дозе 200 — 500 мкг 1 раз в день в течение 4 — 6 нед до наступления гематологической ремиссии. Критериями гематологической реакции являются резкое увеличение количества ретикулоцитов в периферической крови — ретикулоцитарный криз, трансформации мегалобластического кроветворения в нормобласти-ческое. Появление ретикулоцитарного криза на 5 —б-й день лечения является ранним критерием эффективности его. В процессе лечения цианкобаламином количество эритроцитов нарастает быстрее, чем содержание гемоглобина, в связи с этим цветовой показатель обычно снижается. После нормализации костномозгового кроветворения и состава крови (обычно через 1,5 — 2 мес) витамин вводят 1 раз в неделю в течение 2 — 3 мес, затем в течение полугода 2 раза в месяц в тех же дозах, что и в начале курса). В дальнейшем больных ставят на диспансерный учет; профилактически им вводят витамин Bi2 1 — 2 раза в год короткими курсами по 5 — 6 инъекций или ежемесячно по 200 — 500 мкг (пожизненно).
При симптомах фуникулярного миелоза витамин Вп вводят в значительных дозах — 500 — 1000 мкг ежедневно в течение 10 дней, а затем 1—3 раза в неделю до исчезновения неврологической симптоматики.
Гемотрансфузии проводят лишь при значительном снижении гемоглобина и проявлении симптомов коматозного состояния. Рекомендуется вводить эритроцитную массу по 250 — 300 мл (5 — 6 трансфузий).
Преднизолон (20 — 30 мг/сут) рекомендуется при аутоиммунной природе заболевания.
Прогноз.В настоящее время применение витамина Bt2 сделало прогноз В12ДА благоприятным. При адекватной терапии больные живут длительное время.
Профилактика.Мер первичной профилактики не существует. У лиц, имеющих перечисленные ранее этиологические факторы, следует периодически исследовать кровь для своевременного выявления анемии.
Дата добавления: 2014-11-20 ; Просмотров: 494 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
✓ Статья проверена доктором
При повышенном объёме эритроцитов, когда увеличивается и степень насыщения крови гемоглобином (цветовой показатель больше 1,1), развивается патология, определяющаяся в медицине, как гиперхромная макроцитарная анемия. Данная патология отмечается при проблемах с функциями органов кроветворения, причиной которых могут быть различные заболевания.
Малокровие развивается несколькими путями. Во-первых, как итог нарушений в создании нормальных эритроцитов и синтеза гемоглобина. Так происходит, если в организме недостаёт железа, витамина B12, фолиевой кислоты или из-за патологий красного костного мозга. Причина анемии может скрываться в переизбытке аскорбиновой кислоты, которая блокирует выработку B12, необходимого для производства крови.
Во-вторых, малокровие возникает из-за потерь красных кровяных клеток при острых кровотечениях во время травм или оперативных вмешательств. Хотя если кровотечения хронически, то причиной анемии, скорее будет, недостаток железа.
И третий механизм, приводящий к анемии, — быстрое, меньше 120 суток, разрушение красных кровяных телец. Иногда разрушению эритроцитов предшествует приём значительных доз уксуса.
Специалисты определяют первопричины возникновения патологии и её клиническую картину в зависимости от вида.
Внимание! Основную группу риска гиперхромной анемии составляют мужчины и женщины после сорока лет.
Уровень эритроцитов при гиперхромной анемии
Данный недуг определяется характерными признаками и симптомами:
- Бледность кожного покрова, ускоренно седеют волосы, порой кожный покров становится с желтоватым оттенком, утончается.
- Быстрая утомляемость, слабость плохая концентрация внимания.
- Слизистая меняет свой внешний вид, бледнеет или желтеет.
- Головокружение.
- Одышка — при более выраженных формах, сердцебиение.
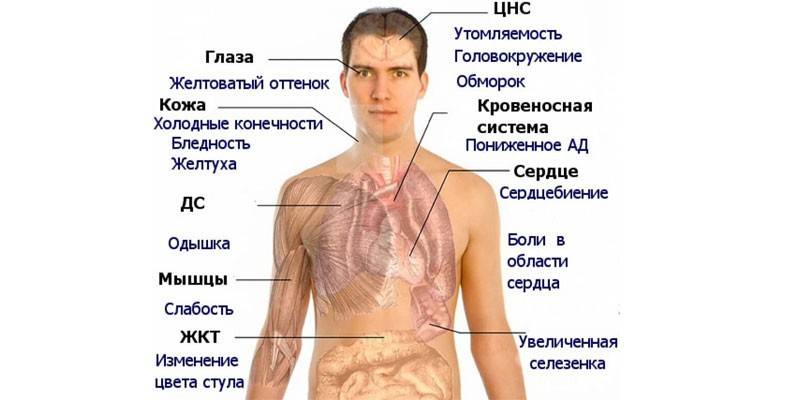
Клинические проявления анемии
Особое внимание следует обращать именно на язык, поскольку он становится блестящим и с гладкой поверхностью (это симптоматика недостатка В12 и фолиевой кислоты). Затем на данном органе начнут возникать красные пятна, что характеризуются болезненностью. Спустя некоторое время пятен становится настолько много, что они сливаются воедино. Таким образом, язык кажется ярко-красным. При движении языком может возникнуть болевой синдром. У больного атрофируются вкусовые качества. Именно эта симптоматика характерна для пернициозной гипертонии.
Это важно! Нужно исключить из рациона питания острую пищу, поскольку ее употребление будет крайне болезненным.
Проявление анемии на ногтях
Иногда малокровие никак не выражается, поэтому его случайно обнаруживают во время лабораторных анализов крови у тех, кто ни на что не жаловался. Вышеприведённая симптоматика характерна для большинства анемий, но у различных типов малокровия наблюдаются отличия в зависимости от причины возникновения. Например, чувствительность нарушается из-за недостатка витамина В12, а желтуха возникает при гемолитической анемии.
Состояние гиперхромного малокровия может быть выявлено в нескольких случаях:
- Дефицит витамина В12.
- Недостаток фолиевой кислоты.
- Миелодиспластический синдром.
Обратите внимание! Чаще всего гиперхромная анемия диагностируется при недостатке В12.
Роль фолиевой кислоты в организме
В зависимости от недостатка тех или иных веществ диагностируется вид гиперхромной анемии.
Она встречается реже, чем железодефицитная анемия. В Нидерландах, Скандинавии, Северной Америке более частотна, чем на юге, востоке Европы и Дальнем Востоке. Этим типом малокровия болеют люди сорока-пятидесяти лет. Часто его симптоматика стёрта, так как в рамка антианемической терапии врачи назначают Цианокобаламин, который после первого укола уже нормализует выработку витамина В12.
Причиной возникновения этого вида анемии являются болезни ЖКТ, снижающие выработки вещества:
- длительное неполноценное питание, вегетарианцы;
- атрофический гастрит провоцирует гиперхромию. Объясняется он проблемами с продукцией гастромукопротеина – он нужен для усвоения витамина. Следовательно, развивается пернициозная анемия;
- резекция желудка или его удаление;
- ожоги желудочной слизистой;
- недуги, связанные с тонким и толстым кишечниками, приводят к нарушениям всасывающих функций стенок органов;
- инфекционные патологии кишечника;
- глистное поражение.
- хронический панкреатит и синдром Золлингера-Эллисона;
- целиакия, опухоли и т.д.
Причины гиперхромной анемии
Симптоматика данного вида анемии имеет свои особенности:
- Общие проявления анемии (мы их описали выше).
- Гастроэнтерологический синдром (похудение, тяжесть и боли в эпигастрии, болезненность в языке (язык Гюнтера), запоры, поносы.
- Неврологический синдром (онемение, боли в ногах и руках, «ватные ноги», снижение обоняния, слуха, зрения). Характерен только для В12-дефицитной анемии.
Если говорить о гиперхромной анемии, что развивается на фоне недостатка фолиевой кислоты, то она объясняется следующими причинами:
- регулярное употребление алкоголя, что приводит к поражению печеночных клеток;
- вирусы гепатита;
- беременность и несоблюдение рациона питания.
При малокровии данного типа неврологический синдром не наблюдается, но больные жалуются на общие проявления анемического синдрома в дополнение к нему возникают и гастроэнтерологические проблемы. Разграничение В12-анемии и недостаточности фолиевой кислоты происходит по результатам анализов крови после приёма Цианокобаламином: в первом случае через 4-5 дней лечения «ретикулоцитарный криз» отсутствует, его появление диагностирует фолиеводефицитную анемию и адекватность назначенного лечения.
Справка! Если анемия развивается на фоне недостатка фолиевой кислоты, то не исключено, что ее придется принимать на протяжении оставшейся жизни.
Если у человека диагностирована легкая форма недуга, то ее можно быстро компенсировать корректировкой рациона питания. Для этого его обогащают мясопродуктами. Особое внимание следует обратить на печень, именно в ней содержится наибольшее количество полезных веществ, что улучшают состояние больного при анемии.
При дефицитных состояниях В12 необходим прием Цианокобаламина – специальный препарат, синтетического характера. По мере тяжести течения недуга, врач определяет дозировки. Если диагностируется неврологические симптомы, то Цианокобаламин назначается инъекционно по 1000 мкг ежедневно внутримышечно в течение 10 дней, после чего, переходят на стандартную дозу – по 500 мкг в сутки. При отсутствии нарушении со стороны нервной системы дозировка — 500 мкг/день ежедневно. Длительность приёма от месяца до полутора. Если речь о поддерживающей терапии, то такая же доза принимается раз в неделю в течение жизни.
Лечение недостатка фолиевой кислоты происходит таблетками по 5 мг 3 раза в день в течение месяца — полутора. Поддерживающая терапия не предусмотрена.
Если одновременно диагностированы два вида анемии. При обеих формах анемий и недейственности консервативной терапии по жизненным показателям делают трансфузию концентрата определенного вида эритроцитов (например, для выведения из анемической комы).
После курса терапии пациента отправляют на анализ крови, чтобы подтвердить присутствие ретикулоцитоза. Также необходимо наблюдение нервной системы, которая восстанавливается дольше всего.
Эффективность терапии проверяется через неделю применения. То есть, если спустя семь дней, после применения синтетических препаратов не произошло улучшение самочувствия больного, то курс считается не действующим либо была произведена неправильная диагностика.
Это важно! Если анемия находится в тяжелой стадии, то человеку потребуется переливание эритроцитарной массы.
Дифференциация анемии происходит по показателям применения витамина В12, если после курса лечения им не было отмечено никаких положительных результатов, то причиной гиперхромной анемии является недостаток фолиевой кислоты.
Гиперхромная анемия может проявляться в комплексе с миелодиспластическим синдромом, в который входит группа заболеваний, характеризующаяся дефицитом одного или нескольких видов кровяных клеток (цитопения), нарушением их производства и возможностью трансформации в острый лейкоз. Одна из причин возникновения патологии — проведение лучевых облучений, химиотерапии, сильнодействующее лечение опухолевидных образований костного мозга, лейкоз. Кроме того, возникновению МДС способствует профессиональные особенности (воздействие бензола), алкоголь, курение, склонность к спонтанным кровотечениям.
Таким образом, кроветворение подвергается сильному токсическому воздействию. Помимо тяжелой симптоматики основного недуга, у пациента возникает дополнительно:
- Сильная одышка даже при отсутствии физической нагрузки.
- Чрезмерная утомляемость.
- Постоянные головокружения, возникновение тахикардии.
Точный диагноз устанавливается только после полноценного обследования крови, так как МДС может быть вторичным и возникнуть как следствие какой-либо тяжелого хронического или острого заболевания. В общем виде МДС характерна цитопения — снижение уровня гемоглобина, нейтрофилов, тромбоцитов. В зависимости от недостатка тех или иных элементов крови и устанавливается диагноз.
Наиболее частые симптомы анемии
Поскольку данный синдром часто возникает у пожилых людей, ему сопутствуют различные заболевания — сердца (инфаркты, ИБС, проблемы с клапанами), поражения, печени, легких, почек и опухолевидные образования.
Если больной своевременно обратился к специалисту с последующим компетентным назначением лечения, то можно избежать осложнений недуга и проявления тяжких последствий в виде комы. Стоит отметить, что терапия будет сложной, поскольку больной должен находиться под бдительным наблюдением специалиста, соблюдать назначенную схему приема лекарственных средств. Но в целом при диагностике бессимптомной цитопении врачи занимают выжидательную позицию: если нет тревожащих признаков, то пациент проходит регулярное обследование.
При миелодиспластическом синдроме лечебная терапия проводится курсами, поскольку длительного эффекта не наблюдается. Таким образом, можно продлевать ремиссию и сохранять нормальное самочувствие пациента. Для полного восстановления и выздоровления терапии будет не достаточно, поэтому потребуется пересадка костного мозга.
Крайне важно своевременно начать лечение анемии, чтобы исключить дальнейшие осложнения со здоровьем. Когда диагноз гиперхромная анемия ставится ребенку, то высока вероятность, того, что при отсутствии лечения малыш будет заметно отставать в развитии от своих сверстников. На фоне патологии у ребенка могут развиваться различные заболевания, объясняется это потерей аппетита и заметным снижением функций иммунной системы.
Мегалобластные (гиперхромные) анемии
Для беременной заболевание не менее опасно, поскольку при отсутствии своевременной помощи может спровоцировать преждевременные роды, а в лучшем случае – маловесие новорожденного. Для предотвращения таких последствий женщине необходимо консультироваться с ведущим врачом.
Среди общих последствий отмечается недостаток кислорода в крови, кардиомиопатия, тахикардия, сердечная недостаточность. Очень важно вовремя пролечить анемию, поскольку сердечная недостаточность может закончиться смертельным исходом.
источник
Железодефицитная анемия (малокровие) обычно рассматривают скорее в качестве симптома другого заболевания или в виде состояния, возникающего при недостаточной концентрации в организме железа.
Причины и факторы, способствующие развитию анемического синдрома:
- Развивается болезнь у маленьких детей и взрослых, соблюдающих строгую диету, если они не получают необходимого количества железа с едой.
- На фоне нарушений в пищеварительной системе. Известно, что всасывание микроэлементов происходит в тонкой кишке (верхние отделы) и в желудке. А тем более, после удаления части желудка, способность пищеварительной системы к абсорбции нарушается.
- Анемический синдром может развиться из-за больших потерь крови. Это является основной причиной железодефицитных состояний. Часто синдром возникает у женщин из-за больших потерь крови во время обильной менструации и у тех, кто страдает от язвы пищеварительного тракта, рака желудка, геморроя, новообразований в толстой кишке.
- Сокращение времени жизни эритроцитов в крови или быстрое их разрушение. В норме срок жизни эритроцита – 4 месяца. В некоторых случаях причиной гемолиза является патология селезенки. Развивается гемолитическая или серповидно-клеточная анемия. При таком заболевании организмом вырабатывается аномальный гемоглобин.
При подозрении на анемию, важно оперативно обратится за помощью к специалисту. Врач поможет выявить причины и способы лечения болезни. Синдром приводит к снижению иммунитета, к упадку сил, ограничению работоспособности. Также анемия может стать важным сигналом о развитии других патологий и серьезных проблем в работе отдельных органов и их систем.
Диагноз ставят по анализу крови, а лечение, как правило, заключается в восстановлении количества железа с помощью лек. препаратов. Лекарства используют внутрь или вводят с помощью инъекций.
| Пол, возраст | Порог Нb (Г/Л) | Порог Нb (Г/%) |
| Дети от 3 месяцев до 5 лет | 110 | 11,0 |
| Дети от 5 до 12 лет | 115 | 11,5 |
| Дети от 12 до 15 лет | 120 | 12,0 |
| Мужчины от 15 лет | 130 — 160 | 13,0 — 16,0 |
| Женщины от 15 лет | 120 — 140 | 12,0 — 14,0 |
| Беременные женщины | 110 | 11,0 |
Можно выделить 3 основных механизма развития анемии:
- Вследствие нарушения процесса образования эритроцитов и образования гемоглобина. Такого рода механизм можно проследить при недостаточном поступлении железа, фолиевой кислоты и витамина В12, при заболеваниях костного мозга. Иногда дефицитное состояние может возникнуть из-за приема сверхбольших доз витамина С. При приеме сверх доз аскорбиновой к-ты происходит блокировка витамина В12 и нарушение процессов кроветворения.
- Острая потеря эритроцитов. Обычно – это последствия острых кровотечений, операций и травм. При хронических кровотечениях в небольших объемах причиной анемии выступает не просто потеря эритроцитов, но и недостаток железа на фоне хронической утраты крови.
- Анемический синдром — последствия от ускоренного разрушения эритроцитов крови. При нормальной работе костного мозга и иных органов кроветворения эритроциты живут порядка 4 месяцев, а затем разрушаются. При гемолитической анемии, гемоглобинопатии и так далее скорость разрушения эритроцитов выше, чем их производства. Иногда процесс протекает под влиянием внешних стимулов, химических веществ (уксус).
Рассмотрим различные виды у взрослых. Анемия является симптомом, а не отдельным заболеванием и может возникать при ряде болезней. Они, как правило, связаны с первичным поражением кроветворной системы или не зависят от нее. Невозможно провести четкую нозологическую классификацию анемий. Для этого используют принцип практической целесообразности. И в результате заболевание делят по единому классификационному признаку – по цветовому показателю.
Падение уровня гемоглобина в крови чаще всего наблюдают при одновременном снижении количества и качества эритроцитов. Любой вид анемии непременно приводит к снижению эффективности дыхательной функции крови, возникновению кислородного голодания тканей. Обычно это видно по бледности кожных покровов, слабости, высокой утомляемости, головным болям, головокружении, одышке, учащенному ритму сердца и т.д.
Врач назначает рутинное исследование мазка крови, в процессе анализа морфолог обязан указать на отклонения размера эритроцитов. Уменьшение может быть, как в меньшую (микроцитарная анемия), так и большую сторону (макроцитарная). Однако, если необходимую оценку производят без специальных микрометров, то она является весьма субъективной.
Анемии, которые могут развиться при болезнях почек, гипопластические, АХЗ и острую постгеморрагическую относят к нормоцитарным. Макроцитарные анемии бывают нормо- и гиперхромными, а микроцитарные – гипохромными.
Намного информативнее автоматический анализ крови, при котором соблюдается четкая стандартизация важных показателей. Учитывают средний корпускулярный объем (СКО), который можно измерить в фемтолитрах (fl, фл). Нормальное значение СКО составляет 80-90 фл и называется нормоцитозом. Если показатель повышен до 95 и более – то фиксируют развитие макроцитоза. При снижении менее 80 фл ставят диагноз микроцитоз. Есть у автоматического метода и свои недостатки: достаточно дорогое и чуткое оборудование, которому необходимо соответствующее обслуживание.
При замене цветового показателя на СКО не нарушается привычная классификация анемий по цветовому показателю. Анемии подразделяют на группы по различным признакам. Классификацию, как правило, основывают на удобстве и практической значимости для постановки диагноза.
Цветовой показатель покажет степень насыщения эритроцита гемоглобином. У здорового человека ЦП колеблется 0,86 до 1,1. В зависимости от него различают такие анемии:
- Гипохромная анемия, если ЦП меньше 0,86 (по некоторым классификациям ниже 0,8). При таких анализах ставят диагноз талассемия или железодефицитная анемия.
- При нормохромной анемии ЦП колеблется в пределах 0,86 — 1,1. В таком случае у пациента наблюдается постгеморрагическая анемии, гемолитические анемии, апластические анемии, неопластические заболевания костного мозга, внекостномозговые опухоли, анемия из-за снижения темпов выработки и количества эритропоэтина.
- Гиперхромная анемия – при ЦП более 1,1. Такие показатели характерны для фолиеводефицитной анемии, а также витамин B12-дефицитной анемии, для миелодиспластического синдрома.
Проводится в зависимости от выраженности снижения уровня гемоглобина в крови. Классификация по степени тяжести предполагает:
- легкую степень (когда уровень гемоглобина ниже нормы, но остается на уровне более 90 грамм на литр);
- среднюю степень тяжести (когда гемоглобин 70-90 г/л);
- тяжелую степень (когда уровень гемоглобина остается меньше 70 грамм на литр).
Разделение степени анемии по уровню гемоглобина достаточно распространено. Чаще всего именно по гемоглобину подтверждают диагноз, а потом уже проводят более детальную диагностику.
Характеризуется незначительным падением количества гемоглобина в крови. Обычно проявляются следующие симптомы:
- усталость;
- апатия;
- общее недомогание;
- часто развивается у беременных.
Как уже упоминалось выше, анемия 1 степени фиксируется, если уровень микроэлементов в крови ниже нормы, но выше 90 г на л.
Также первая степень заболевания часто поражает маленьких детей, появившихся на свет при многоплодной беременности или недоношенными. У детей постарше – это паразитические заболевания или погрешности в питании. Анемия легкой степени тяжести проще поддается лечению. Обычно рекомендуют соблюдать диету и усиленно питаться. При легкой степени анемии в рацион необходимо включать различные микроэлементы и витамины, в первую очередь – железо и витамин В12.
Анемия 2 степени или средней степени тяжести возникает не только при снижении уровня гемоглобина до 70 г/л. Возникает головокружение и головные боли, одышка, частое сердцебиение, трудности с дыханием. Дети часто болеют, у них наблюдается бледность губ и кожи. При 2 степени анемии может возникнуть кислородное голодание плода, снижается сократительная способность миокарда. Лечение медикаментозное + диета, следует больше находится и гулять по свежему воздуху.
На этой стадии острая анемия несет опасность для жизни человека. При 3 степени наблюдается ломкость ногтей и волос, острое снижение защитных сил организма, онемение конечностей, проблемы с сердцем и сосудами. Ребенок начинает часто болеть.
Особенно тяжелыми будут последствия такого симптома у беременных женщин. Это может негативно отразится на плоде, у матери развиться дистрофические изменения матки и плаценты. Анемия 3 степени лечится в стационаре, с переливанием эритроцитарной массы и другими видами медикаментозного лечения.
Основным признаком такого разделения принято считать количество молодых эритроцитов (ретикулоциты) в периферической картине крови. В норме показатель колеблется от 0,5 до 2%.
- Арегенераторную анемию (например, апластическая анемия) — ретикулоциты отсутствуют.
- Гипорегенераторная (витамин B12-дефицитная анемия или железодефицитная анемия) – ретикулоциты ниже 0,5%.
- Регенераторная или норморегенераторная (постгеморрагическая) — ретикулоциты 0,5 — 2%.
- Гиперрегенераторная (гемолитические анемии) — количество ретикулоцитов больше 2%.
Такая классификация основывается на различных механизмах развития анемии, как патологического процесса.
- Ассоциированные с дефицитом Fe — железодефицитные анемии.
- Гемолитические анемии — связанные с повышенным разрушением эритроцитов.
- Гис-гемолитические анемии — при нарушении кровообразования, протекающего в красном костном мозге.
- Постгеморрагические анемии — при острой или хронической кровопотере.
- В12- и фолиеводефицитные анемии.
Мегалобластные анемии: миокардит гемолитический и пернициозная анемия.
Гипохромия — это общее название для разных форм анемии, при которых цветовой показатель крови, вследствие недостатка гемоглобина, меньше 0,8. Не включена в список нозологических единиц. В анализе крови средний показатель для гемоглобина при таком состоянии меньше 30 пикограмм, а средняя концентрация гемоглобина в эритроците составляет менее 330 г на литр. Меняется не только цвет, но и диаметр (макро- или микроцитоз) и форма. Чаще всего при такого рода патологии красной крови кровяные тельца приобретают вид колец с бледно-красной серединой и темно-красными краями (обесцвечиваются).
Патологические формы эритроцитов могут возникать вследствие:
- Железодефицитной анемии при кровопотерях (геморрагическая), нарушении усвоения железа, при невынашивании плода и т.д.
- Хронического отравления свинцом.
- Талассемии – нарушения нормального процесса синтеза полипептидных цепей в структуре гемоглобина.
- Нарушения синтеза и утилизации порфиринов.
- Гиповитаминоза В6.
- При нарушении обмена вещества, хронических воспалительных процессах неинфекционного и инфекционного генезиса.
Дизэритропоэтическая анемия – целая группа достаточно редко встречающихся заболеваний крови, которые возникают из-за нарушения процессов эритропоэза. При этом, большая часть молодых эритроцитов погибает сразу после образования в костном мозге, а количество нормоцитов значительно снижается. Такого рода расстройство предполагает качественный, количественный, кинетический или совмещенный характер нарушения эритропоэза.
Следует упомянуть такую разновидность заболевания — гиперхромная макроцитарная анемия или малокровие. При котором также наблюдают снижение числа эритроцитов и уровня гемоглобина в единичном объеме крови. Как правило, при такого рода нарушениях параллельно дают сбой сердце и сосуды.
По коду МКБ-10 — D62 острая постгеморрагическая анемия. Такой симптом возникает после кровопотери. Подразделяют на острую постгеморрагическую анемию и хроническую постгеморрагическую анемию. Острая анемия развивается после острых и обильных кровотечений, хронические анемии возникают после длительных несильных кровотечений.
Во время быстрой кровопотери значительно снижается объем циркулирующей крови. В ответ на такое событие происходит компенсаторная реакция, которая заключается в возбуждении симпатического отдела нервной системы и рефлекторного спазма сосудов. Пульс ускоряется и ослабевает. Сосуды кожи и мышц максимально сужаются, кровь приливает к сосудам мозга, коронарным сосудам, что поддерживает снабжение кровью жизненно важных органов. При прогрессировании процесса начинает развиваться постгеморрагический шок.
Характерным клиническим симптомом постгеморрагической анемии является острая сосудистая недостаточность из-за гиповолемии (опустошение сосудистого русла). Внешне это проявляется ортостатическим коллапсом, одышкой, учащенным сердцебиением. В первые минуты кровопотери уровень гемоглобина может даже быть высоким, но после поступления тканевой жидкости в русло сосудов данный показатель снижается, даже если кровотечение уже прекратилось. Цветовой показатель остается в норме, одновременно происходит утрата эритроцитов и железа, нормохромная анемия. Ко вторым суткам увеличивается число ретикулоцитов, максимальных показателей достигает на 4-7 день (гиперрегенераторная анемия).
Диагноз ставят на основании клинических признаков и лабораторных показателей, повышения уровня остаточного азота, если кровотечение происходила в верхних отделах ЖКТ. Самое важное при такой нормохромной анемии – это устранить саму кровопотерю, восполнить устраненный объем крови эритроцитарной массой и гепарином (до 60% утраченной крови), кровезаменителями (5% р-р Альбумина, Раствор Рингера, Реополиглюкин).
При постановке диагноза постгеморрагическая анемия необходимо учитывать сведения о произошедшей острой кровопотере при наличии внешнего кровотечения. После массивного внутреннего диагноз основывают на клинических признаках и, в обязательном порядке, лабораторных пробах (Вебера, Грегерсена). Основанием для постановки диагноза также послужит рост уровня остаточного азота при кровотечении из верхнего отдела пищеварительного тракта.
После того, как кризис и острый период миновали, пациенту назначают препараты железа, витамины группы В, Е и С. Такая терапия производится в течение 6 месяцев. При утрате более 50% от объема циркулирующей крови — прогноз неблагоприятный.
Состояние может развиться в результате снижения поступления в организм фолиевой кислоты или нарушения процессов ее всасывания в пищеварительном тракте. Лечение заключается в дополнительном приеме недостающего вещества.
В отличии от патологии, ассоциированной с недостатком В12, фолиеводефицитная анемия диагностируется значительно реже.
Одной из основных причин фолиеводефицитной анемии является недостаточное содержание фолиевой к-ты в рационе. Следует помнить, что нужно включать в свое ежедневное меню больше зелени и печени. Также на здоровье значительно влияет алкогольная интоксикация, беременность, злокачественные новообразования, некоторые дерматиты, гемолиз.
Такого вида заболевания возникает при нарушении всасывания (например, при целиакии), под действием лекарственных средств, Метотрексата, Триамтерена, противосудорожных средств, барбитуратов, Метформина и др. Значительно повышается нужна организма в фолиевой кислоте после гемодиализа и при болезнях печени.
Также на здоровье оказывает влияние дефицит цианокобаламина и его кофермента – метилкобаламина. В таких условиях не происходит трансформации фолиевой кислоты в коферментную форму. В результате нарушается процесс нормального клеточного деления, начинают страдать клетки кроветворной ткани, которые ранее активно размножались. Тормозятся процессы созревания и размножения эритроцитов, сокращается их продолжительность жизни. Изменения касаются и лейкоцитов, возникает лейкопения и тромбоцитопения.
Далее в результате неправильного митоза появляются гигантские клетки эпителия пищевого канала и развиваются воспалительные процессы в слизистой оболочке, стоматиты, гастриты, эзофагиты, энтерит. Еще больше усугубляется первичное нарушения секреции и процесс всасывания внутреннего фактора, усиливается дефицит витаминов. Возникает порочный круг.
Из-за возникшего недостатка цианокобаламина, в организме начинают накапливаться продукты обмена, которые токсичны для нервных клеток. В волокнах тем временам начинают синтезироваться жирные кислоты уже с искаженной структурой. Наблюдается плавное изменение качества клеток спинного мозга и поражаются периферические и черепные нервные сплетения, развивается неврологическая симптоматика.
При таком виде анемии, как правило симптомы у пациента наблюдаются стандартные: высокая утомляемость, учащенное сердцебиение, бледность ногтей и губ, ярко-красный язык. На начальных стадиях отследить признаки поражения НС и ЖКТ практически невозможно. По результатам обследования выявляется гиперхромная макроцитарная анемия, лейкопения, тромбоцитопения. А лечение с помощью витамина В12 не вызывает улучшений лабораторных показателей. Диагноз можно подтвердить с помощью определения уровня сывороточной фолиевой к-ты и в эритроцитах. В норме ее содержание составляет от 100 до 450 нг/л. При фолиеводефицитной анемии концентрация фолиевой кислоты в эритроцитах значительно снижается.
Если проводят анализ периферической картины крови, то отмечают гиперхромную (макроцитарную) анемию при общем снижении уровня гемоглобина и эритроцитов. Непрямой билирубин меняется редко.
В качестве профилактики и для лечения фолиеводефицитной анемии должны назначить фолиевую кислоту в дозе 1 мг/сут, внутрь. Если есть необходимость врач может увеличить дозу. Улучшения должны наступать через в течение 3-4 суток, в том числе проходить должны и неврологические симптомы. В противном случае приходится говорить о недостатке именно витамина В12, а не фолиевой к-ты.
Обязательно проводить профилактику недостатка фолиевой к-ты у беременных женщин и пациентов, принимающих некоторые группы лек. препаратов. Для профилактики назначают 5 мг вещества в сутки.
Относится к виду витаминодефицитных (мегалобластных) анемий, которые возникают при недостаточном поступлении в организм витамина В12 (цианокобаламина). В результате В12-дефицитной анемии поражается кроветворная функция, нервная и пищеварительная система. В отличие от фолиеводефицитной В12-анемии, она развивается в преклонном или старческом возрасте, чаще всего у мужской половины. Проявляется заболевание постепенно.
Человек, страдающий В12-дефицитной анемией, будет испытывать общие симптомы: слабость, пониженная работоспособность, одышка, головокружение, жжение за грудиной, боли в ногах и языке, парестезии, шаткость походки. Такие симптомы будут сочетаться с желтушным цветом кожи, глосситом, незначительным увеличением печени и селезенки, негромким систолическим шумом, глухостью тонов сердца. Нередко поражается и нервная система, развивается комбинированный склероз или фуникулярный миелоз, нарушается чувствительность, полиневрит, атрофия мышц, паралич нижних конечностей.
Развивается анемия из-за недостатка витамина В12, из-за несбалансированности питания, голодания, алкоголизма и отсутствия аппетита. Также синдром может наблюдаться на фоне мальабсорбции, целиакии, изменений в слизистой оболочке кишечника, спру, лимфомы кишечника, болезни Крона, регионарного илеита, из-за длительного приема противосудорожных препаратов.
Вероятность развития В12-дефицитной анемии будет выше при беременности, гемолитической анемии, псориазе, эксфолиативном дерматите. При приеме алкоголя, препаратов–антагонистов фолатов, врождённых нарушениях метаболизма и атрофическом гастрите также может наблюдаться это заболевание.
Как правило, поставить диагноз В12-дефицитная анемия можно без особых проблем. Это может сделать гематолог, невролог, нефролог или гастроэнтеролог по результатам общего и биохимического анализа крови, наличию метилмалоновой кислоты. Также проводят УЗИ брюшной полости и исследование всасывания витамина В12 с помощью радиоизотопов. По показаниям можно провести аспирационную биопсию костного мозга.
Лечение проводят витамином В12 внутримышечно. В течение 1-1,5 месяцев используют поддерживающую дозу. Если уровень гемоглобина упал менее 60 г на л, при нарушении гемодинамики и угрозе анемической комы проводят трансфузии эритроцитов.
В качестве профилактики при заболеваниях, сопровождающихся нарушением всасывания витамина В12, а также после операций нужно под контролем содержания витамина В12 в моче и крови применять профилактические и лечебные курсы витаминотерапии.
Что это такое простыми словами? Это процесс ускоренного разрушения красных кровяных телец, он сопровождается значительным ростом уровня прямого билирубина в крови. Заболевание встречается достаточно редко.
Общим признаком можно считать ускоренное разрушение эритроцитов, сопровождающееся с одной стороны анемией и повышенным образованием продуктов распада эритроцитов, а с другой – реактивно усиленным эритропоэзом.
Аутоиммунная гемолитическая анемия, как правило вызвана генетическими дефектами мембран эритроцитов, что вызывает их повышенное разрушение. Аутоиммунное заболевание и гемолиз эритроцитов при приобретенных анемиях наступает под действием внутренних факторов или каких-либо факторов окружающей среды.
На развитие иммунных гемолитических анемий влияют посттрансфузионные реакции, вакцинации, прием некоторых препаратов (сульфаниламидов, анальгетиков, противомалярийных лекарств, производных нитрофуранового ряда). Также такой симптом может проявляться при гемобластозах, аутоиммунных патологиях (НЯК, СКВ), инфекционных болезнях (мононуклеоз, вирусная пневмония, сифилис, токсоплазмоз).
Гемолитические анемии можно поделить на два обширные группы заболеваний: приобретенные и врожденные.
Формы наследственных заболеваний:
- Эритроцитарные мембранопатии, такие как анемия Минковского-Шоффара или болезнь Минковского-Шоффара (микросфероцитоз), акантоцитоз, овалоцитоз, вызванные аномалиями в структуре мембран эритроцитов. Отметим, что сфероцитоз – самый распространенный вид среди патологий (микросфероцитоз).
- Энзимопении, вызванные дефицитом некоторых ферментов (пируваткиназа, глюкозо-6-фосфатдегидрогеназа).
- Гемоглобинопатии, возникшие из-за качественных нарушений структуры гемоглобина или изменения соотношения его нормальных форм.
Приобретенные гемолитические анемии делят на:
- Приобретенные мембранопатии (шпороклеточная анемия, болезнь Маркиафавы-Микели).
- Изо- и аутоиммунные, вызванные действием антител.
- Токсические, возникшие вследствие воздействия ядов, токсинов или других хим. агентов.
- Анемии, ассоциированные с механическими повреждениями в структуре эритроцитов.
Рост концентрации остаточных следов после распада эритроцитов в организме внешне будет проявляться желтухой лимонного оттенка. Также будет наблюдаться повышение концентрации в крови непрямого билирубина и железа. Отмечается уробилинурия и плейохромия кала и желчи. При внутрисосудистом гемолизе дополнительно развивается гипергемоглобинемия, гемоглобинурия, гемосидеринурия. Об усилении эритропоэза говорит ретикулоцитоз и полихроматофилия в составе периферической крови, либо эритронормобластоз костного мозга.
Если у пациента не микросфероцитарная анемия, обусловленная наследственным сфероцитозом или эллиптоцитозом, то необходимо, прежде всего проводить адекватную терапию заболевания, вызвавшего причину гемолитической анемии.
Для лечения обычно применяют:
- медикаменты (например, Десферал);
- спленэктомию;
- трансфузию эритроцитов при кризе;
- ГСК при аутоимунных заболеваниях в средней дозировке.
Апластическая анемия — заболевание, которое относят к категории миелодисплазий. При таком заболевании происходит резкое угнетение или прекращение роста и созревания клеток в костном мозге, еще называемое панмиелофтизом.
Типичными симптомами болезни являются: лейкопения, анемия, лимфопения и тромбоцитопения. Сам термин впервые появился в начале 20 века. Такое заболевание имеет достаточно тяжелое течение и без лечения (в том числе медикаментозного препаратом Атгам) имеет неблагоприятный прогноз.
Очень долго эту болезнь рассматривали в качестве синдрома, объединяющего различные патологические состояния в костном мозгу. В настоящее время термин «апластическая анемия» выделяется в качестве самостоятельной нозологической единицы. Его следует четко разграничивать от синдрома гипоплазии в кроветворной системе.
Апластическая анемия может быть вызвана различными причинами:
- химическими агентами, бензолом, солями тяжелых металлов и так далее;
- ионизирующим излучением;
- приемом некоторых лекарств, цитостатиков, НПВС, Анальгина, Мерказолила, Левомицетина;
- вирусами;
- наличием других аутоиммунных заболеваний.
Также существует форма апластической анемии, передающейся по наследству — анемия Фанкони. Лечение болезни заключается в приеме иммунодепрессантов и проведении пересадки костного мозга.
При серповидно-клеточной анемии человека происходит нарушение строения белка гемоглобина, он приобретает нетипичное кристаллическое строение, в виде серпа. Такую форму называют S-гемоглобином. Заболевание связывают с мутацией НВВ-гена, из-за которой в костном мозге начинает синтезироваться аномальный вид S-гемоглобина, в шестом положении в В-цепи вместо глутаминовой кислоты находится валин. Происходит полимеризация S-гемоглобина, образуются длинные тяжи, эритроциты приобретают форму серпа.
Тип наследования серповидноклеточной анемии – аутосомно-рецессивный при неполном доминировании. У гетерозиготных носителей в эритроцитах находится примерно равное количество гемоглобина А и S. Носители сами не болеют, а выявить серповидные эритроциты можно случайно при проведении лабораторного обследования. Симптомы же могут и вовсе не проявляться. Иногда такие люди начинают ощущать недомогание при гипоксии или тяжелом обезвоживании.
У гомозигот в крови есть только гемоглобин S, заболевание протекает достаточно тяжело. У таких больных высокий уровень степени разрушенных эритроцитов в селезенке, значительно короче срок жизни, часто проявляются признаки хронической недостаточности кислорода.
Такой вид анемии достаточно распространен в регионах, где высокий уровень заболеваемости малярией. У таких больных выше устойчивость к разным штаммам малярийного плазмодия. Поэтому столь вредные аллели часто проявляются у жителей Африки.
Симптомы сильно различаются и их можно наблюдать у детей уже с 3-х месячного возраста. Анемия может приводить к потере сознания, меньшей выносливости, вызвать желтуху. У младенцев наблюдается худоба, слабость, искривление конечностей, удлиненность туловища, изменения в строение черепа и зубов. Также у больных детей повышенная склонность к развитию сепсиса. У подростков наблюдают задержку развития на 2-3 года. Женщины, как правило, способны к зачатию и рождению ребенка.
Мегалобластная анемия (болезнь Аддисона-Бирмера, В12-дефицитная, пернициозная) — заболевание, вызванное недостатком фолиевой кислоты или витамина В12. Происходит это из-за недостатка веществ в пище или при заболеваниях пищеварительного тракта. Также мегалобластическая анемия может возникнуть при врожденных нарушениях процессов синтеза ДНК, приобретенных патологиях и из-за приема некоторых лекарств (антиметаболитов, противосудорожных).
При постоянном недостатке фолиевой кислоты и В12 развивается хроническая анемия, эритроциты изменяют свою форму и размеры. Более легкие стадии иногда протекают бессимптомно, далее начинают уже проявляться внешние признаки. Такое дефицитное состояние часто также называют пернициозной анемией. Заболевание получило статус анемии хронических заболеваний, так как проявляется у пациентов после 60 лет и у перенесших гепатит больных, при энтерите и раке кишечника. Подробнее о такого рода анемиях описано выше.
Развивается вследствие эндогенного В12-авитаминоза, вызванного атрофией желез фундального отдела желудка, которые в норме должны вырабатывать гастромукопротеин. В результате нарушаются процессы всасывания витамина В12 и возникает злокачественная анемия «пернициозного» типа. Чаще всего такой диагноз ставят в возрасте от 50 лет.
Болезнь сопровождается нарушениями нервной, сердечно-сосудистой, кроветворной и пищеварительной системы. Больные обычно жалуются на одышку, общую слабость, отечность ног, боли в сердце, «мурашки» по стопам и кистям, жгучие боли в языке и шаткость походки. По лабораторным показателям наблюдают анемию гиперхромного типа, лейкопению, тромбоцитопению.
Сидеробластная анемия также имеет название сидероахрестическая анемия (САА), железорефрактерная, железонасыщенная или сидеробластическая. Это патологическое состояние нарушений процесса синтеза микроэлементов и кроветворения, чаще всего – железа. Эритроциты содержат малое количество железа, из-за того, что микроэлемент активно расходуется костным мозгом и начинает накапливаться во внутренних органах. Заболевание развивается на фоне недостаточного содержания протопорфирина.
Выделяют две формы болезни:
- пиридоксин-зависимую, возникающую вследствие дефицита пиридоксальфосфата;
- пиридоксин-резистентную, развивающуюся из-за ферментного дефекта (дефицита гемсинтетазы).
Приобретенные формы сидероахрестической анемии чаще наблюдаются в пожилом возрасте, но болезнь не наследуется от родителей. Часто такого рода анемия развивается, как побочный эффект от лечения препаратами от туберкулеза или истощении пиридоксальфосфата при отравлении свинцом, при алкоголизме, миелопролиферативных болезнях крови, кожной порфирии. Встречаются и идиопатические формы САА.
Это редкое, передающееся по наследству заболевание. Анемия Фанкони встречается у 1 из 350000 детей. Наибольшее распространение заболевание получила среди евреев-ашкеназов и жителей Южной Африки.
Возникает из-за наличия дефектов в белковых кластерах, отвечающих за процесс репарации ДНК. Для заболевания характерная высокая ломкость у хромосом, наличие у пациентов старше 40 лет миелоидного лейкоза и апластической анемии.
Для новорожденных с таким недугом характерны врожденные дефекты развития, необычная пигментация, низкорослость, аномалии развития скелета и некоторые неврологические симптомы (косоглазие или недоразвитость одного из глаз, глухота, умственная отсталость), аномалии развития внутренних органов. К сожалению, в среднем такие пациенты живут не более 30 лет.
У диагноза неуточненная анемия код по МКБ-10 D64.9. Это первичный диагноз, который уточняется после проведения обследования у врача, так как он является вторичным признаком какого-либо основного заболеваний. Прежде всего следует исключить возможность кровопотери вследствие травм, хирургических вмешательств, внутренних кровотечений, далее проводится лабораторная диагностика.
По международной классификации МКБ-10 для миелодиспластического синдрома:
- D46.0 Рефрактерная анемия без сидеробластов, так обозначенная;
- D46.1 Рефрактерная анемия с сидеробластами;
- D46.2 Рефрактерная анемия с избытком бластов;
- D46.3 Рефрактерная анемия с избытком бластов с трансформацией;
- D46.4 Рефрактерная анемия неуточненная;
- D46.7 Другие миелодиспластические синдромы;
- D46.9 Миелодиспластический синдром неуточненный.
Приставка «рефрактерная» означает устойчивость заболевания к приему витаминов, препаратов железа, соблюдению диеты. Чаще всего такого вида анемия является наиболее распространенным видом миелодиспластического синдрома. Из-за нарушений процессов созревания бластов в крови значительно понижено содержание гемоглобина, проявляются признаки острого лейкоза. Примерно у 40% пациентов с миелодиспластическим синдромом проявляется рефрактерная анемия. Чаще всего гемоглобинопатия такого рода развивается у пациентов от 50 лет.
Заболевание можно считать промежуточным этапом между рефрактерной анемией и острым лейкозом. Как правило, болезнь проявляется снижением уровня гемоглобина и общей слабостью. Если у больного не нашли других причин для таких изменений картины крови, то основной задачей врачей становится дообследовать пациента и максимально затормозить наступление острого лейкоза.
Что за болезнь талассемия? Это наследуемое по рецессивному типу заболевание, развивающееся из-за снижения синтеза полипептидных цепей в структуре гемоглобина. В зависимости от того, какой мономер перестал нормально синтезироваться различают альфа-, бета-талассемию и дельта-талассемию. Также болезнь классифицируют по степени клинических проявлений, разделяют на тяжелую, легкую и среднюю.
Альфа-талассемия ассоциирована мутациями в генах HBA2 и HBA1. Альфа-цепь кодируется четырьмя локусами и, в зависимости от количества аномальных – различают разные степени тяжести заболевания. Симптомы и течение гемоглобинопатии варьируют от легкой до тяжелой степени гипохромной микроцитарной анемии.
Бета-талассемия существует в двух наиболее распространенных вариантах: малая (minor) и CD8(-AA) – большая (наиболее тяжелая форма заболевания). Анемия развивается из-за мутаций обоих аллелей бета-глобина, когда гемоглобин А начинает вытесняться гемоглобином F. Обычно малая талассемия имеет легкое течение и лечение не требуется.
Согласно Википедии, анемия Даймонда-Блекфена представляет собой наследственную форму красноклеточной аплазии с точно не выявленным типом наследования. Предполагают, что заболевание имеет аутосомно-доминантный тип наследования, который встречается у одной четвертой всех больных. У таких больных обычно проявляются проявления анемии в течение первого года жизни, слабость, бледность, повышенная утомляемость, снижение количества эритроцитов в плазме крови.
Диагноз ставят по общему анализу крови, показателям уровня эритропоэтинов, микроскопии и биопсии костного мозга. Лечению болезнь поддается плохо, назначают ГКС, гемотрансфузии.
Повышение концентрации свободного гемоглобина в плазме крови называют гемоглобинемией. Заболевание возникает вследствие приобретенных и врожденных заболеваний эритроцитов, при повышенном их разрушении. Симптом может проявиться после неправильно проведенного переливания крови, из-за воздействия паразитарных и инфекционных факторов (сепсиса, вирусной инфекции, малярии), после сильного переохлаждения, отравления ядами, бензином, уксусной кислотой, грибами. Проявляется внешне это гиперемией кожных покровов и слизистой, повышением концентрации гемоглобина и билирубина в крови.
Существуют настолько разные причины заболевания, что выявить некоторые из них можно только после проведения лабораторных исследований. Часто бывает, что показатели гемоглобина в норме, а железо низкое. Недуг может наблюдаться при недостатке витаминов группы В, фолиевой к-ты. Малокровие у человека возникает вследствие различных травм и обильных внутренних или внешних кровотечений.
Такой диагнозе женщине могут поставить, если уровень гемоглобина в крови падает ниже 120 г на литр. В целом у женщин, из-за некоторых физиологических особенностей выше склонность к данному недугу. Ежемесячные кровопотери во время менструации, когда в течение недели женщина может потерять до 100 мл крови, беременность, лактация и снижение концентрации ферритина – самые распространенные причины анемии. Часто заболевание развивается из-за психосоматики, когда у женщины депрессивное состояние, она плохо питается, редко выходят на свежий воздух, не занимается спортом или во время климакса, когда происходят глобальные изменения в физиологии женщины.
У мужской половины данный диагноз ставится, если уровень гемоглобина снизился менее 130 г на л. По статистике заболевание возникает реже. Чаще всего из-за каких-то хронических заболеваний, нарушений работы органов и их систем (язвенная болезнь, геморрой, эрозии в кишечнике, доброкачественные и злокачественные новообразования, паразиты, апластическая анемия). Существуют и генетические причины (анемия Фанкони) заболевания, которые не связаны с полом.
Малокровие проявляется по-разному, в зависимости от конкретного вида заболевания. Известно, что при малокровии у человека уменьшается количество эритроцитов, изменяется их строение, содержание железа в крови, падает гемоглобин. Ткани человека испытывают недостаток кислорода и это оказывает влияние на общее состояние и внешний вид человека.
Общие признаки анемии, следующие:
- значительно сниженная работоспособность, общая слабость;
- раздражительность, повышенная утомляемость, сильная сонливость;
- шум в ушах и головные боли, «мушки» перед глазами, головокружения;
- дизурия;
- непреодолимое желание полакомится мелом или известью;
- постоянная одышка;
- тонкие и ломкие волосы, ногти, сухая, неэластичная кожа;
- стенокардия, низкое артериальное давление;
- шум в ушах и частые обмороки;
- изменение цвета стула, желтуха, бледность;
- ломота в теле и суставах, мышечная слабость.
Также существуют специфические симптомы малокровия, характерные для той или ной разновидности:
- Железодефицитная анемия. Для данного диагноза характерная парорексия, у пациента появляется сильное желание жевать мел, землю, бумаги и прочие несъедобные материалы. Можно также выделить койлонихию, трещинки в уголках рта, заеды, воспаленный язык. Иногда может повыситься температура до субфебрильной.
- Основным симптомом В12-дефицитной анемии можно назвать покалывание в конечностях, нестойкость походки, скованность и стесненность в движениях, низкое чувство осязания. У пациента снижаются когнитивные способности, могут возникать галлюцинации. В крайне тяжелых случаях может развиться паранойя или шизофрения.
- Характерным симптомом серповидноклеточной анемии может быть слабость, приступообразные боли в брюшной полости и суставах.
- При отравлении свинцовыми отходами у пострадавшего наблюдаются характерные темно-синие линии на деснах, тошнота и болезненные ощущения в области живота.
- Хроническое разрушение эритроцитов может быть симптомом злокачественной опухоли. В таком состоянии развивается проступающая желтуха, язвы и ссадины на ногах, покраснение мочи. Часто образуются камни в желчном пузыре.
Поставить точный диагноз гемолитическая, мегалобластная или апластическая анемия можно после проведения дифференциальной диагностики. Диф. диагностика проводится по соответствующим таблицам и результатам лабораторных исследований.
источник