Материалы представлены из учебного пособия РУДН
Анемии. Клиника, диагностика и лечение / Стуклов Н.И., Альпидовский В.К., Огурцов П.П. – М.: ООО «Медицинское информационное агентство», 2013. – 264 с.
Копирование и тиражирование материалов без указания авторов запрещено и преследуется по закону.
Апластическая анемия (АА) – заболевание, являющееся следствием исчезновения или резкого уменьшения в костном мозге полипотентных стволовых клеток, количество которых снижается до 1% и ниже, что приводит к опустошению или аплазии костного мозга. Морфологически это проявляется панцитопенией в анализах периферической крови, отсутствием кроветворных клеток в пунктате костного мозга.В крови панцитопения характеризуется лейкопенией за счет нейтропении с относительным лимфоцитозом, отсутствием ретикулоцитов. При обнаружении таких изменений необходимо обязательно исключить все возможные причины аплазии (вирусные инфекции, злокачественные заболевания, заболевания крови (лимфопролиферативные заболевания), системные коллагенозы, контакт с химическими веществами, радиация), у взрослых провести трепанобиопсиюдля гистологического исследования костного мозга.
АА впервые была описана Эрлихом в 1888 году. Частота АА составляет 2 – 4 случая на 1 млн. населения в США и Европе, тогда как в некоторых странах Восточной Азии АА встречается значительно чаще. Так, в Таиланде и Японии заболеваемость АА составляет 11 – 14 случаев на 1 млн. населения.
АА наиболее часто выявляется в двух возрастных группах: 20 – 25 лет и старше 60 лет. Статистически значимая разница в частоте заболеваемости между мужчинами и женщинами отсутствует.
АА могут быть врожденными, но чаще носят приобретенный характер. Врожденные, генетически обусловленные АА впервые были описаны Фанкони в 1927 году.
Врожденные АА клинически проявляются недостаточностью костного мозга в первые годы жизни ребенка и нередко сочетаются с такими врожденными дисплазиями, как диспигментация кожи, гипоплазия почек и селезенки, отсутствие или гипоплазия лучевой кости, микроцефалия, врожденные пороки сердца и умственное или половое недоразвитие. Кариологические исследования при этом варианте АА часто выявляют различные хромосомные нарушения. Среди детей с анемией Фанкони отмечается также высокая частота заболеваемости острым лейкозом и другими неоплазиями.
При вторичных АА костномозговая недостаточность обусловлена либо прямым токсическим воздействием радиации или химических соединений на стволовые клетки, либо аберрантным ответом, обусловленным вирусными инфекциями (гемофагоцитарный синдром). Наиболее частыми заболеваниями, провоцирующими развитие АА, являются злокачественные заболевания, заболевания крови (лимфопролиферативные заболевания), системные коллагенозы. Увеличение периферических лимфоузлов, печени и селезенки не характерно дляАА. Более того, обнаружение увеличенной селезенки на ранней стадии заболевания ставит под сомнение диагноз АА, свидетельствует в пользу гепатит-ассоциированной аплазии. Однако, длительное течение заболевания может сопровождаться увеличением печени и селезенки вследствие посттрансфузионного гемосидероза. В случаях с выявленной причиной АА, такое состояние необходимо рассматривать, как вторичную аплазию кроветворения.
Истинной (идиопатической приобретенной) АА является состояние, связанное сгибелью неизмененных стволовых клеток. При идиопатических формах, при которых причина, обусловившая аплазию костного мозга неясна, предполагается Т-клеточно-опосредованная деструкция полипотентных стволовых гемопоэтических клеток костного мозга. У больных с идиопатической формой АА в крови обнаружено повышенное количество активированных цитотоксических Т-лимфоцитов, повышенная выработка γ-интерферона и фактора некроза опухоли, которые вызывают гибель собственных стволовыхклеток костного мозга. Причем причина аутосенсибилизации Т-лимфоцитов противсобственных стволовых клеток остается неясной.
Классификация апластических анемий.
1. Идиопатические апластические анемии
— врожденная (анемия Фанкони)
2. Вторичные апластические анемии, вызванные:
— лекарственными препаратами (хлорамфинекол, нестероидные противовоспалительные препараты, противосудорожные средства, цитотоксические препараты)
— вследствие воздействия ионизирующей радиации
— химическими воздействиями (бензол и его производные, пестициды, лакокрасочные материалы)
— вирусными инфекциями (Эпштейн-Барр, гепатиты, парвавирус, цитомегаловирус, ВИЧ)
— аутоиммуными заболеваниями (СКВ, эозинофильный фасциит, гипериммуноглобулинемия)
— другими причинами (беременность, тимома)
Все клинические проявления АА являются следствием костномозговой недостаточности, интенсивность их зависит от выраженности и скорости прогрессирования панцитопении.Течение АА может быть острым, подострым и хроническим.
У больных АА обычно имеется анемический синдром в сочетании с геморрагиями на коже, слизистых оболочках и инфекционными осложнениями. Доминирующие симптомы АА отличаются в зависимости от сроков развития заболевания.
Известно, что эритроциты циркулируют в периферической крови в течение 3 – 4 месяцев, поэтому симптомы анемии могут развиваться только при длительном угнетении кроветворения более 1 – 2 месяцев. В результате продолжительного отсутствия продукции эритроцитов происходит постепенное снижение концентрации гемоглобина на 25 – 50%, то есть до 90 – 70 г/л, что может быть причиной появления симптомов анемии.
Наоборот, при быстрой гибели подавляющего числа стволовых клеток уже через неделю истощается гемопоэз, прекращается продукция тромбоцитов и лейкоцитов, а количество циркулирующих эритроцитов остается нормальным. Далее ещё в течение недели происходит снижение количества тромбоцитов, что приводит к появлению геморрагического синдрома, на фоне полного отсутствия анемических жалоб. До появления кровоточивости организм компенсирует недостаток тромбоцитов за счет имеющихся, которые в норме жизнеспособны в среднем 10 – 11 суток. Причем, снижение тромбоцитов в циркуляции происходит раньше на несколько дней, чем появление геморрагий, так как основное их количество представлено пристеночным пулом, который составляет основную массу тромбоцитов периферической крови и расходуется медленнее. Геморрагический синдром при тромбоцитопении связан с неадекватной трофикой и повреждением эндотелия, повышенной ломкостью мелких сосудов и проявляется кровоточивостью слизистых (носовые, маточные кровотечения), петехиальными высыпаниями на коже. Считается, что угрожающим для жизни состоянием является кожный геморрагический синдром на верхней половине туловища, особенно на лице, при котором резко повышается риск кровоизлияния в головной мозг.
Что касается лейкоцитов, в особенности нейтрофилов, то их количество снижается наиболее интенсивно. Срок жизни гранулоцитов не более недели, причем в периферической крови они циркулируют несколько дней, затем поступают в окружающие ткани, где осуществляют основную фагоцитарную функцию. Поэтому даже на фоне полного отсутствия нейтрофилов в периферической крови (агранулоцитоза) инфекционные осложнения наступают не сразу, а, как правило, через 5 – 7 дней, и имеют свои особенности. У таких больных часто имеет место высокая лихорадка при отсутствии источника инфекции. Так, при одышке не удается прослушать хрипы, при болях в животе крайне размыты симптомы раздражения брюшины. Для установки диагноз пневмонии и перитонита в таком случае крайне важны инструментальные методы исследования (рентгенологические и ультразвуковые), при использовании которых можно увидеть инфильтрацию ткани легких, появление уровней жидкости в кишечнике при его атонии, утолщение стенки кишки и другие. У больных с агранулоцитозом при появлении лихорадки крайне высок риск развития септического шока в связи с отсутствием барьерной функции лейкоцитов. Такие больные при развитии лихорадки в обязательном порядке нуждаются в исследовании крови на стерильность. Мало того, диагноз сепсиса при агранулоцитозе может устанавливаться даже вопреки классическому определению сепсиса, то есть без наличия «первичного очага». Наиболее частой причиной сепсиса при агранулоцитозе является «нормальная» флора кишечника (сапрофиты или условно патогенные бактерии).
При остром течении АА имеют место бурно прогрессирующий геморрагический синдром, обусловленный глубокой тромбоцитопенией, и тяжелые инфекционные осложнения вследствие почти полного отсутствия гранулоцитов. Больные с подобным течением АА, требуют экстренной госпитализации в гематологическое отделение и проведение антибактериальной, заместительной, часто интенсивной терапии, специализированного лечения. Без адекватной помощи, такие пациенты, как правило, погибают в течение нескольких дней или недель от появления первых признаков заболевания.
При среднетяжелом (подостром) течении АА слабость и повышенная утомляемость длительно остаются основными жалобами больного, затем из-за тромбоцитопении могут появиться симптомы геморрагического диатеза.
Для вторичных АА, которые клинически могут проявлять себя спустя недели и даже месяцы после контакта с этиологическим фактором, более свойственно хроническое течение. При вторичной АА чаще, чем при идиопатической форме, развивается ремиссия заболевания и может наступить полное выздоровление после прекращения действия этиологического фактора.
Картина периферической крови у 90% больных АА характеризуется панцитопенией: анемией, лейко- и тромбоцитопенией.
Анемия носит нормохромный характер. Число ретикулоцитов снижено до 0 – 0,3%.
Лейкопения обусловлена гранулоцитопенией, причем содержание лимфоцитов обычно не изменено, что создает впечатление лимфоцитоза, который при АА носит относительный характер. Выраженность лейкопении во многом определяет тяжесть течения заболевания: число лейкоцитов 9 /л наблюдается больных с тяжелой АА, число лейкоцитов 9 /л – при сверхтяжелой АА.
Тромбоцитопения обнаруживается уже на ранних этапах заболевания и является наиболее стойким гематологическим симптомом.
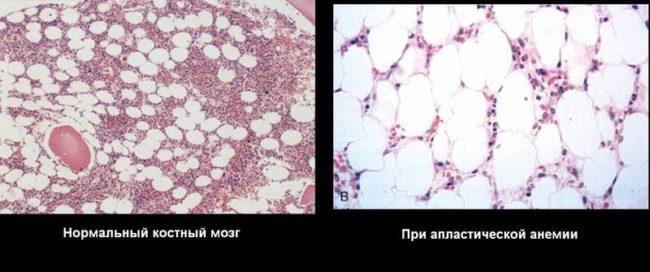
Пунктат костного мозга в подавляющем большинстве случаев очень беден, т.е. содержит небольшое количество гемопоэтических клеток, большинство из которых – лимфоциты. Однако, поскольку процесс аплазии костного мозга происходит неравномерно и отдельные очаги нормального кроветворения сохраняются, можно получить деятельный костный мозг с почти нормальным клеточным составом (при панцитопении в анализе периферической крови!). Все это позволяет сделать заключение о том, что миелограмма при АА не имеет определяющего диагностического значения.
Ключевым методом для диагностики АА у взрослых является гистологическое исследование костного мозга. Для проведения этого исследования проводят трепанобиопсию, результаты которой при АА говорят о тотальном преобладании жировой ткани над деятельным костным мозгом.
При биохимическом исследовании крови у большинства больных АА выявляется высокий уровень сывороточного железа, повышение уровней ЛДГ и трансаминаз, повышенное содержание эритропоэтина.
Диагноз АА основывается на сочетании панцитопении периферической крови, снижении клеточности костного мозга при стернальной пункции и обнаружении жирового костного мозга при его гистологическом исследовании, при этом исключаются другие причины развития аплазии кроветворения.
Критерии панцитопении: Hb 9 /л, тромбоциты 9 /л.
Классификация АА по степени тяжести указана в таблице.
Классификация АА по степени тяжести
Форма заболевания
— пациент не отвечает критериям тяжелой и сверхтяжелой форм;
источник
Апластическая анемия — редкое заболевание, ведь на 1 млн человек приходится всего 5 пациентов, страдающих от недуга. Тем не менее, появление патологии становится неприятным сюрпризом для ничего не подозревающего человека. Как помочь больному в этой нелёгкой ситуации?
Апластическая анемия — патология крови, которая связана с угнетением в костном мозге ростка кровяных телец. Это приводит к нарушению выработки лейкоцитов, тромбоцитов и эритроцитов — важных клеток крови.
В результате снижения количества кровяных клеток снижается степень защиты организма, что делает пациента уязвимым для инфекций. Ситуация усугубляется недостатком кислорода в организме, что становится причиной развития дистрофических изменений во внутренних органах.
Заболевание встречается как у мужчин, так и у женщин. Смертность достигает 60–70%.
Угнетение костного мозга характерно не только для апластической анемии, поэтому заболевание могут путать со следующими патологиями:
- пароксизмальной ночной гемоглобинурией — отсутствие некоторых белков, что приводит к недостаточности клеток костного мозга;
- агранулоцитозом — снижение уровня лейкоцитов, однако анемия отсутствует, а количество тромбоцитов остаётся в норме.
поэтому обязательно обращают внимание на другие патологические изменения, присутствующие в организме.
Апластическую анемию разделяют на приобретённые и наследственные формы. Подобный вид представлен следующими случаями:
- острый тип — заболевание возникает внезапно и быстро прогрессирует;
- подострая анемия — развитие продолжается в течение 1–6 месяцев, протекает плавно;
- хронический тип — продолжительность более полугода, заболевание постепенно прогрессирует.
Врождённые апластические анемии представлены такими разновидностями:
- анемия Фанкони — патология, характеризующаяся наличием врождённых аномалий развития внутренних органов и угнетением функции кроветворения;
- анемия Эстрена-Дамешека — представлена поражением функции кроветворения, но аномальные изменения со стороны внутренних органов отсутствуют.
Существует ещё одна форма — синдром Даймонда-Блекфена (парциальная красноклеточная анемия), при котором снижается выработка эритроцитов.
Согласно классификации болезней МКБ-10, рассматриваемое заболевание относится в группу других анемий, имеющих код D61. Допускаются следующие уточнения:
- D0 — конституциональная форма, сюда же относятся и другие наследственные типы;
- D1 — медикаментозная форма (дополнительно присваивается код лекарства, если есть необходимость в его идентификации);
- D2 — форма, вызванная внешними причинами;
- D3 — идиопатический тип, при котором причины возникновения анемии неизвестны;
- D8 — другие анемии с уточнёнными факторами;
- D9 — анемия имеет неуточненную форму.
Согласно данным статистики, установить точную причину развития апластической анемии не удаётся в 50–70% случаев. Наиболее изучены врождённые типы:
- при анемии Даймонда-Блекфена выявлены мутации генов 1, 13, 16 и 9;
- при анемии Фанкони обнаружены изменения в парных хромосомах 1 и 7.
Кроме того, выделяют внутренние и внешние причины развития апластической анемии. К внутренним факторам относятся:
- изменения в иммунной системе — связано с потерей регулирующей роли тимуса;
- нарушения в эндокринной системе — обнаружена связь заболевания с кистами яичников (у женщин) и ухудшением деятельности щитовидной железы.
Влияние нарушений эндокринной системы на формирование апластической анемии доказано исследователями. Было установлено, что у пациенток, находящиеся в интересном положении и страдающие от заболевания, наступала длительная ремиссия, если беременность прерывалась по медицинским показателям.
Привести к образованию анемии могут и внешние факторы:
- инфекции: цитомегаловирус, вирусы герпеса, гепатита C, Эпштейна-Барра, а также перенесённые заболевания: мононуклеоз, грипп;
- препараты: антибиотики (Тетрациклин, Стрептомицин), цитостатики (Треосульфан, Мелфан), сульфаниламиды (Сульфаэтидол, Сульфален), противотуберкулёзные лекарства (Рифампицин, Изониазид);
- проникающая радиация;
- химические агенты: нефтепродукты, ртуть.
Учёные придерживаются мнения, что помимо воздействия одного или нескольких факторов у больного человека вырабатывается определённая реакция на антигены.
Признаки заболевания зависят от формы анемии, а также возраста появления первых симптомов. Например, в детском возрасте первые проявления возникают в 4 года. Ребёнок начинает жаловаться на усталость, частые головные боли. Одновременно снижаются защитные механизмы организма, поэтому малыш часто болеет, нередко появляются кровотечения из носа.
По мере развития апластической анемии возникают новые признаки. Что свидетельствует о поражении остальных систем организма. В результате формируются 3 синдрома с соответствующими признаками:
- анемический;
- геморрагический;
- токсико-инфекционный.
| Синдром | Симптомы |
| Геморрагический синдром |
|
| Анемический синдром |
|
| Токсико-инфекционный |
|
Изучение анамнеза заболевания — первая мера, позволяющая установить факт наличия заболевания. Врач опрашивает больного, устанавливая частоту и время появления признаков, присутствие других признаков. Имеет большое значение и анализ жизни пациента, так как можно выявить возможные причины.
При осмотре больного выявляют пониженное артериальное давление, учащённый пульс и бледный оттенок кожи. В некоторых местах на слизистых оболочках и кожных покровах могут присутствовать незначительные кровоизлияния.
Для получения полной информации о патологии прибегают к помощи инструментальных и лабораторных методов диагностики:
- Анализ крови. Наблюдается снижение уровня гемоглобина, количество тромбоцитов, лейкоцитов и эритроцитов тоже ниже нормы.
- Биохимический анализ крови. Применяется для обнаружения поражённых органов, изучают уровень глюкозы, холестерина, мочевой кислоты и креатинина.
- Анализ мочи. Обнаруживают проявления инфекций (лейкоциты и микроорганизмы в моче), а также признаки кровотечения.
- Пункция костного мозга. Выявляют замещение предшественников клеток крови на рубцовую или жировую ткань.
- Ультразвуковая диагностика. Позволят отследить поражение других органов.
- Электрокардиография. Диагностируют нарушение питания сердца и увеличенную частоту сокращений органа.
- Трепанобиопсия позволяет охарактеризовать состояние костного мозга.
| Общий анализ крови | Биохимический анализ крови |
|
|
Лечение апластической анемии — сложный и комплексный процесс, требующий активного участия врача и пациента. Для медикаментозной терапии могут применяться следующие группы лекарств:
- Антибиотики (Амикацин, Цефтриаксон, Тобрамицин). Назначаются при присоединении бактериальной инфекции.
- Цитостатики (Имуран, Метотрексат, Циклофосфан). Назначают для лечения приобретённых форм апластической анемии.
- Иммунодепрессанты (Метилпреднизолон, Дексаметазон). Уменьшают реакцию иммунитета, позволяя костному мозгу вырабатывать кровяные клетки.
- Стимуляторы кроветворения (Нейпоген, Лейкин). Усиливают выработку кровяных клеток костным мозгом.
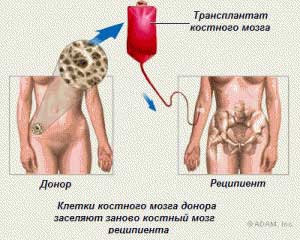
Единственным радикальным способом, позволяющим взять под контроль апластическую анемию и получить положительный результат, является трансплантация костного мозга. Такая методика наиболее эффективная в молодом возрасте, но есть одна сложность — материал для пересадки должен быть совместим или частично совместим с антигенным составом костного мозга больного. В этом случае лучше всего подходит ближайший родственник пациента.
Перед пересадкой применяют химиотерапию, направленную на угнетение защитных свойств организма пациента. Подобная мера связана с необходимость предотвратить отторжение пересаженных клеток.
Для лечения патологии, сопровождающейся низким значением эритроцитов или тромбоцитов, можно применять переливание крови. Методика не позволяет избавить от апластической анемии, но заболевание будет взято под контроль специалистов, что положительно скажется на самочувствии больного.
Прогноз жизни пациента завит от применяемых методов лечения и времени обнаружения патологии. При отсутствии лечения около 90% пациентов умирают в течение 1 года развития патологии.
Наиболее благоприятный вариант представлен пересадкой костного мозга — такое лечение позволило прожить более 5 лет 90% больных, прошедших эту процедуру. Однако, подобное мероприятие достаточно дорогое, поэтому не всем по карману подобная процедура.
При отсутствии возможности проведения пересадки клеток спинного мозга, но с условием, что осуществляется адекватное лечение, примерно 50% больных живут больше 5 лет.
Апластическая анемия — опасное заболевание, требующее много усилий от врачей и пациента. Патологию сложно устранить, но это не означает, что больной заранее проиграл — успех зависит от его действий и настроя.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
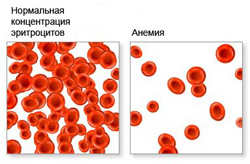
Эритроциты формируются в красном костном мозге из белковых фракций и небелковых компонентов под воздействием эритропоэтина (синтезируется почками). Эритроциты в течение трех дней обеспечивают транспорт, главным образом, кислорода и углекислого газа, а также питательных веществ и продуктов метаболизма от клеток и тканей. Срок жизни эритроцита сто двадцать дней, после чего он разрушается. Старые эритроциты накапливаются в селезенке, где утилизируются небелковые фракции, а белковые поступают в красный костный мозг, участвуя в синтезе новых эритроцитов.
Вся полость эритроцита наполнена белком, гемоглобином, в состав которого входит железо. Гемоглобин придает эритроциту красную окраску, а также помогает ему переносить кислород и углекислый газ. Его работа начинается в легких, куда эритроциты поступают с током крови. Молекулы гемоглобина захватывают кислород, после чего обогащенные кислородом эритроциты направляются сначала по крупным сосудам, а затем и по мелким капиллярам к каждому органу, отдавая клеткам и тканям необходимый для жизни и нормальной деятельности кислород.
Анемия ослабляет способность организма к газовому обмену, за счет сокращения числа эритроцитов нарушается транспортировка кислорода и углекислого газа. Вследствие этого у человека могут наблюдаться такие признаки анемии как чувство постоянной усталости, упадок сил, сонливость, а также повышенная раздражительность.
Анемия является проявлением основного заболевания и не является самостоятельным диагнозом. Многие болезни, включая инфекционные заболевания, доброкачественные или злокачественные опухоли могут быть связаны с анемией. Именно поэтому анемия является важным признаком, который требует проведения необходимых исследований для выявления основной причины, которая привела к ее развитию.
Тяжелые формы анемии вследствие тканевой гипоксии могут привести к серьезным осложнениям, таким как шоковые состояния (например, геморрагический шок), гипотония, коронарная или легочная недостаточность.
- по механизму развития;
- по степени тяжести;
- по цветному показателю;
- по морфологическому признаку;
- по способности костного мозга к регенерации.
| По патогенезу анемия может развиться вследствие кровопотери, нарушения образования эритроцитов или из-за их выраженного разрушения. По механизму развития выделяют:
|
- потеря крови (острые или хронические кровотечения);
- повышенное разрушение эритроцитов (гемолиз);
- уменьшенное производство эритроцитов.
Также следует заметить, что в зависимости от вида анемии причины ее возникновения могут отличаться.
Факторы, влияющие на развитие анемии
- гемоглобинопатии (изменение строения гемоглобина наблюдается при талассемии, серповидноклеточной анемии);
- анемия Фанкони (развивается вследствие имеющегося дефекта в кластере белков, которые отвечают за восстановление ДНК);
- ферментативные дефекты в эритроцитах;
- дефекты цитоскелета (клеточный каркас, располагающийся в цитоплазме клетки) эритроцита;
- врожденная дизэритропоэтическая анемия (характеризуется нарушением образования эритроцитов);
- абеталипопротеинемия или синдром Бассена-Корнцвейга (характеризуется нехваткой бета-липопротеина в клетках кишечника, что ведет к нарушению всасываемости питательных веществ);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (вследствие нарушения клеточной мембраны эритроциты принимают шарообразную форму).
- дефицит железа;
- дефицит витамина B12;
- дефицит фолиевой кислоты;
- дефицит аскорбиновой кислоты (витамин С);
- голодание и недоедание.
Хронические заболевания и новообразования
- почечные заболевания (например, туберкулез печени, гломерулонефрит);
- заболевания печени (например, гепатит, цирроз);
- заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, атрофический гастрит, неспецифический язвенный колит, болезнь Крона);
- коллагеновые сосудистые болезни (например, системная красная волчанка, ревматоидный артрит);
- доброкачественные и злокачественные опухоли (например, миома матки, полипы в кишечнике, рак почек, легких, кишечника).
- вирусные заболевания (гепатит, инфекционный мононуклеоз, цитомегаловирус);
- бактериальные заболевания (туберкулез легких или почек, лептоспироз, обструктивный бронхит);
- протозойные заболевания (малярия, лейшманиоз, токсоплазмоз).
Ядохимикаты и медикаментозные средства
- неорганический мышьяк, бензол;
- радиация;
- цитостатики (химиотерапевтические препараты, используемые для лечения опухолевых заболеваний);
- антибиотики;
- нестероидные противовоспалительные средства;
- антитиреоидные препараты (снижают синтез гормонов щитовидной железы);
- противоэпилептические препараты.
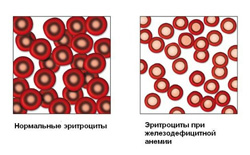
Для железодефицитной анемии характерно снижение эритроцитов, гемоглобина и цветового показателя.
Железо — это жизненно важный элемент, участвующий во многих метаболических процессах организма. У человека с весом семьдесят килограмм запас железа в организме составляет примерно четыре грамма. Данное количество поддерживается благодаря сохранению баланса между регулярными потерями железа из организма и его поступлением. Для поддержания равновесия суточная потребность железа составляет 20 – 25 мг. Большая часть поступающего железа в организм затрачивается на его нужды, остальное депонируется в виде ферритина или гемосидерина и при необходимости расходуется.
Нарушение поступления железа в организм
- вегетарианство вследствие неупотребления белков животного происхождения (мясо, рыба, яйца, молочные продукты);
- социально-экономическая составляющая (например, недостаточно денег для полноценного питания).
Нарушение усвоения железа
Всасывание железа происходит на уровне слизистых желудка, поэтому такие заболевания желудка как гастриты, язвенная болезнь или резекция желудка приводят к нарушению всасывания железа.
Повышенная потребность организма в железе
- беременность, в том числе многоплодная беременность;
- период лактации;
- подростковый возраст (за счет быстрого роста);
- хронические заболевания, сопровождающиеся гипоксией (например, хронический бронхит, пороки сердца);
- хронические нагноительные заболевания (например, хронические абсцессы, бронхоэктатическая болезнь, сепсис).
Потери железа из организма
- легочные кровотечения (например, при раке легких, туберкулезе);
- желудочно-кишечные кровотечения (например, язва желудка и двенадцатиперстной кишки, рак желудка, рак кишечника, варикозное расширение вен пищевода и прямой кишки, неспецифический язвенный колит, глистные инвазии);
- маточные кровотечения (например, преждевременная отслойка плаценты, разрыв матки, рак матки или шейки матки, прервавшаяся внематочная беременность, миома матки);
- почечные кровотечения (например, рак почек, туберкулез почек).
Питание при анемии
В питании железо делится на:
- гемовое, которое поступает в организм с продуктами животного происхождения;
- негемовое, которое поступает в организм с продуктами растительного происхождения.
Следует заметить, что гемовое железо усваивается в организме значительно лучше, нежели негемовое.
Количество железа на сто миллиграмм
Продукты питания
животного
происхождения
- печень;
- язык говяжий;
- мясо кролика;
- индюшатина;
- гусиное мясо;
- говядина;
- рыба.
- 9 мг;
- 5 мг;
- 4,4 мг;
- 4 мг;
- 3 мг;
- 2,8 мг;
- 2,3 мг.
Продукты питания растительного происхождения
- сушеные грибы;
- свежий горох;
- гречка;
- геркулес;
- свежие грибы;
- абрикосы;
- груша;
- яблоки;
- сливы;
- черешня;
- свекла.
- 35 мг;
- 11,5 мг;
- 7,8 мг;
- 7,8 мг;
- 5,2 мг;
- 4,1 мг;
- 2,3 мг;
- 2,2 мг;
- 2,1 мг;
- 1,8 мг;
- 1,4 мг.
При соблюдении диеты также следует увеличить потребление продуктов, содержащих витамин C, а также белок мяса (они повышают усвояемость железа в организме) и снизить потребление яиц, соли, кофеина и кальция (они уменьшают всасываемость железа).
Медикаментозное лечение
При лечении железодефицитной анемии больному параллельно с диетой назначается прием препаратов железа. Данные лекарственные средства предназначены для восполнения дефицита железа в организме. Они выпускаются в виде капсул, драже, инъекций, сиропов и таблеток.
Доза и длительность лечения подбирается индивидуально в зависимости от следующих показателей:
- возраста пациента;
- степени тяжести заболевания;
- причины, вызвавшей железодефицитную анемию;
- на основе результатов анализов.
Препараты железа принимаются за один час до еды или через два часа после приема пищи. Данные лекарственные средства нельзя запивать чаем или кофе, так как снижается всасываемость железа, поэтому их рекомендуется запивать водой или соком.
Принимать внутрь по одному грамму три – четыре раза в сутки.
Принимать по одной таблетке в день, с утра за тридцать минут до приема пищи.
Принимать по одной таблетке один – два раза в день.
Данные препараты рекомендуется назначать совместно с витамином C (по одной таблетке один раз в день), так как последний увеличивает всасываемость железа.
Препараты железа в виде инъекций (внутримышечных или внутривенных) применяются в следующих случаях:
- при тяжелой степени анемии;
- если анемия прогрессирует, несмотря на принимаемые дозы железа в виде таблеток, капсул или сиропа;
- если у больного имеются заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, неспецифический язвенный колит, болезнь Крона), так как принимаемый препарат железа может усугубить имеющееся заболевание;
- перед оперативными вмешательствами с целью ускоренного насыщения организма железом;
- если у пациента имеется непереносимость препаратов железа при их приеме внутрь.
Хирургическое лечение
Хирургическое вмешательство производится при наличии у больного острого или хронического кровотечения. Так, например, при желудочно-кишечном кровотечении может применяться фиброгастродуоденоскопия или колоноскопия с выявлением области кровотечения и последующей его остановкой (например, удаляется кровоточащий полип, коагулируется язва желудка и двенадцатиперстной кишки). При маточных кровотечениях, а также при кровотечениях в органах, находящихся в брюшной полости, может применяться лапароскопия.
При необходимости больному может быть назначено переливание эритроцитарной массы для восполнения объема циркулирующей крови.

В норме витамин В12 поступает в организм с пищевыми продуктами. На уровне желудка В12 связывается с продуцируемым в нем белком, гастромукопротеидом (внутренний фактор Касла). Данный белок защищает поступивший в организм витамин от негативного воздействия микрофлоры кишечника, а также способствует его усвоению.
Комплекс гастромукопротеид и витамин В12 доходит до дистального отдела (нижний отдел) тонкого кишечника, где происходит распад этого комплекса, всасывание витамина В12 в слизистый слой кишечника и дальнейшее поступление его в кровь.
Из кровяного русла данный витамин поступает:
- в красный костный мозг для участия в синтезе эритроцитов;
- в печень, где происходит его депонирование;
- в центральную нервную систему для синтеза миелиновой оболочки (покрывает аксоны нейронов).
Клиническая картина В12 и фолиево-дефицитной анемии основывается на развитии у больного следующих синдромов:
- анемический синдром;
- желудочно-кишечный синдром;
- невралгический синдром.
| |
Данные симптомы развиваются вследствие атрофических изменений слизистого слоя ротовой полости, желудка и кишечника. |
|
- снижение уровня эритроцитов и гемоглобина;
- гиперхромия (выраженная окраска эритроцитов);
- макроцитоз (увеличенный размер эритроцитов);
- пойкилоцитоз (различная форма эритроцитов);
- при микроскопии эритроцитов выявляются кольца Кебота и тельца Жолли;
- ретикулоциты снижены или в норме;
- снижение уровня лейкоцитов (лейкопения);
- повышение уровня лимфоцитов (лимфоцитоз);
- снижение уровня тромбоцитов (тромбоцитопения).
В биохимическом анализе крови наблюдается гипербилирубинемия, а также снижение уровня витамина В12.
При пункции красного костного мозга выявляется повышение мегалобластов.
Больному могут быть назначены следующие инструментальные исследования:
- исследование желудка (фиброгастродуоденоскопия, биопсия);
- исследование кишечника (колоноскопия, ирригоскопия);
- ультразвуковое исследование печени.
Данные исследования помогают выявить атрофические изменения слизистой оболочки желудка и кишечника, а также обнаружить заболевания, которые привели к развитию В12-дефицитной анемии (например, злокачественные образования, цирроз печени).
Все больные госпитализируются в отделение гематологии, где проходят соответствующее лечение.
Питание при В12-дефицитной анемии
Назначается диетотерапия, при которой увеличивается потребление продуктов, богатых витамином В12.
Суточная норма витамина В12 составляет три микрограмма.
Количество витамина В12 на сто миллиграмм
Медикаментозное лечение
Медикаментозное лечение назначается больному по следующей схеме:
- В течение двух недель больной ежедневно получает по 1000 мкг Цианокобаламина внутримышечно. За две недели у пациента исчезает неврологическая симптоматика.
- В течение последующих четырех – восьми недель больной получает по 500 мкг ежедневно внутримышечно для насыщения депо витамина В12 в организме.
- Впоследствии больной пожизненно получает внутримышечные инъекции один раз в неделю по 500 мкг.
Во время лечения одновременно с Цианокобаламином больному могут назначить прием фолиевой кислоты.
Больной В12-дефицитной анемией должен пожизненно наблюдаться у гематолога, гастролога и семейного врача.
Фолиевая кислота (витамин B9) является водорастворимым витамином, который отчасти продуцируется клетками кишечника, но в основном должен поступать извне для восполнения необходимой для организма нормы. Суточная норма фолиевой кислоты составляет прием 200 – 400 мкг.
В пищевых продуктах, а также в клетках организма фолиевая кислота находится в форме фолатов (полиглутаматы).
Фолиевая кислота играет большую роль в организме человека:
- участвует в развитии организма во внутриутробном периоде (способствует формированию нервной проводимости тканей, кровеносной системы плода, предупреждает развитие некоторых пороков развития);
- участвует в росте ребенка (например, в первый год жизни, в период полового созревания);
- влияет на процессы кроветворения;
- совместно с витамином В12 участвует в синтезе ДНК;
- препятствует образованию тромбов в организме;
- улучшает процессы регенерации органов и тканей;
- участвует в обновлении тканей (например, кожи).
Абсорбция (всасывание) фолатов в организме осуществляется в двенадцатиперстной кишке и в верхнем отделе тонкого кишечника.
При фолиеводефицитной анемии у больного наблюдается анемический синдром (такие симптомы как повышенная утомляемость, сердцебиение, бледность кожных покровов, снижение работоспособности). Неврологический синдром, а также атрофические изменения слизистой оболочки ротовой полости, желудка и кишечника при данном виде анемии отсутствуют.
Также у больного может наблюдаться увеличение размеров селезенки.
При общем анализе крови наблюдаются следующие изменения:
- гиперхромия;
- снижение уровня эритроцитов и гемоглобина;
- макроцитоз;
- лейкопения;
- тромбоцитопения.
В результатах биохимического анализа крови наблюдается снижение уровня фолиевой кислоты (менее 3 мг/мл), а также повышение непрямого билирубина.
При проведении миелограммы выявляется повышенное содержание мегалобластов и гиперсегментированных нейтрофилов.
Питание при фолиеводефицитной анемии играет большую роль, больному необходимо ежедневно потреблять продукты, богатые фолиевой кислотой.
Следует заметить, что при любой кулинарной обработке продуктов фолаты разрушаются приблизительно на пятьдесят процентов и более. Поэтому для обеспечения организма необходимой суточной нормой продукты рекомендуется употреблять в свежем виде (овощи и фрукты).
| Продукты питания | Наименование продуктов | Количество железа на сто миллиграмм |
| Продукты питания животного происхождения |
|
|
| Продукты питания растительного происхождения |
|
|
Медикаментозное лечение фолиеводефицитной анемии включает прием фолиевой кислоты в количестве от пяти до пятнадцати миллиграмм в сутки. Необходимую дозировку устанавливает лечащий врач в зависимости от возраста пациента, тяжести течения анемии и результатов исследований.
Профилактическая доза включает прием одного – пяти миллиграмм витамина в сутки.
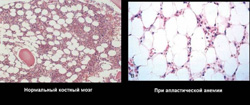
Апластическая анемия может быть врожденной или приобретенной.
Клинические проявления апластической анемии зависят от степени выраженности панцитопении.
При апластической анемии у больного наблюдаются следующие симптомы:
- бледность кожных покровов и слизистых;
- головная боль;
- учащенное сердцебиение;
- одышка;
- повышенная усталость;
- отеки на ногах;
- десневые кровотечения (вследствие снижения уровня тромбоцитов в крови);
- петехиальная сыпь (красные пятна на коже маленьких размеров), синяки на коже;
- острые или хронические инфекции (вследствие снижения уровня лейкоцитов в крови);
- изъязвления орофарингеальной зоны (поражается слизистая полости рта, язык, щеки, десна и глотка);
- желтушность кожных покровов (симптом поражения печени).
При биохимическом анализе крови наблюдается:
- повышение сывороточного железа;
- насыщение трансферрина (белок, переносящий железо) железом на 100%;
- повышение билирубина;
- повышение лактатдегидрогеназы.
При пункции красного мозга и последующем гистологическом исследовании выявляются:
- недоразвитие всех ростков (эритроцитарный, гранулоцитарный, лимфоцитарный, моноцитарный и макрофагальный);
- замещение костного мозга жировым (желтый костный мозг).
Среди инструментальных методов исследований больному может быть назначено:
- ультразвуковое исследование паренхиматозных органов;
- электрокардиография (ЭКГ) и эхокардиография;
- фиброгастродуоденоскопия;
- колоноскопия;
- компьютерная томография.
При правильно подобранном поддерживающем лечении состояние пациентов с апластической анемией существенно улучшается.
При лечении апластической анемии больному назначаются:
- иммунодепрессивные препараты (например, Циклоспорин, Метотрексат);
- глюкокортикостероиды (например, Метилпреднизолон);
- антилимфоцитарный и антитромбоцитарный иммуноглобулины;
- антиметаболиты (например, Флударабин);
- эритропоэтин (стимулирует образование эритроцитов и стволовых клеток).
Немедикаментозное лечение включает:
- трансплантацию костного мозга (от совместимого донора);
- переливание компонентов крови (эритроциты, тромбоциты);
- плазмаферез (механическое очищение крови);
- соблюдение правил асептики и антисептики с целью предотвращения развития инфекции.
Также при тяжелом течении апластической анемии больному может понадобиться хирургическое лечение, при котором производится удаление селезенки (спленэктомия).
В зависимости от эффективности проводимого лечения у больного при апластической анемии может наблюдаться:
- полная ремиссия (затухание или полное исчезновение симптомов);
- частичная ремиссия;
- клиническое улучшение;
- отсутствие эффекта от лечения.
|
|
|
|

Гемолитическая анемия может развиться вследствие наследственных или приобретенных заболеваний.
По локализации гемолиз может быть:
- внутриклеточным (например, аутоиммунная гемолитическая анемия);
- внутрисосудистым (например, переливание несовместимой крови, диссеминированное внутрисосудистое свертывание).
У пациентов с легкой степенью гемолиза уровень гемоглобина может быть нормальным, если производство эритроцитов соответствует темпу их разрушения.
Преждевременное разрушение эритроцита может быть связано со следующими причинами:
- внутренними мембранными дефектами эритроцитов;
- дефектами структуры и синтеза белка гемоглобина;
- ферментативными дефектами в эритроците;
- гиперспленомегалией (увеличение размеров печени и селезенки).
Наследственные заболевания могут вызвать гемолиз в результате отклонений мембраны эритроцита, ферментативных дефектов и отклонений гемоглобина.
Существуют следующие наследственные гемолитические анемии:
- энзимопатии (анемии, при которых наблюдается недостаток фермента, дефицит глюкозо-6-фосфатдегидрогеназы);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (эритроциты неправильной шарообразной формы);
- талассемия (нарушение синтеза полипептидных цепей, входящих в строение нормального гемоглобина);
- серповидно-клеточная анемия (изменение строения гемоглобина приводит к тому, что эритроциты принимают серпообразную форму).
Приобретенные причины гемолитической анемии включают иммунные и не иммунные нарушения.
Иммунные нарушения характеризуются аутоиммунной гемолитической анемией.
Не иммунные нарушения могут быть вызваны:
- ядохимикатами (например, пестициды, бензол);
- лекарственными средствами (например, противовирусные препараты, антибиотики);
- физическим повреждением;
- инфекциями (например, малярия).
Гемолитическая микроангиопатическая анемия приводит к производству фрагментированных эритроцитов и может быть вызвана:
- дефектным искусственным сердечным клапаном;
- диссеминированным внутрисосудистым свертыванием;
- гемолитическим уремическим синдромом;
- тромбоцитопенической пурпурой.
Симптомы и проявления гемолитической анемии разнообразны и зависят от вида анемии, степени компенсации, а также от того, какое лечение получал больной.
Следует заметить, что гемолитическая анемия может протекать бессимптомно, а гемолиз выявляться случайно во время обычного лабораторного тестирования.
При гемолитической анемии могут наблюдаться следующие симптомы:
- бледность кожи и слизистых;
- ломкость ногтей;
- тахикардия;
- учащение дыхательных движений;
- снижение артериального давления;
- желтушность кожных покровов (из-за увеличения уровня билирубина);
- на ногах могут наблюдаться язвы;
- гиперпигментация кожи;
- желудочно-кишечные проявления (например, боль в животе, нарушение стула, тошнота).
Следует заметить, что при внутрисосудистом гемолизе у больного наблюдается дефицит железа из-за хронической гемоглобинурии (наличие гемоглобина в моче). Вследствие кислородного голодания нарушается сердечная функция, что приводит к развитию у пациента таких симптомов как слабость, тахикардия, одышка и стенокардия (при тяжелой форме анемии). Из-за гемоглобинурии у больного также наблюдается потемнение мочи.
Длительный гемолиз может привести к развитию желчных камней вследствие нарушения обмена билирубина. При этом пациенты могут жаловаться на боль в животе и бронзовый цвет кожи.
В общем анализе крови наблюдается:
- снижение уровня гемоглобина;
- снижение уровня эритроцитов;
- увеличение ретикулоцитов.
При микроскопии эритроцитов выявляется их серпообразная форма, а также кольца Кебота и тельца Жолли.
В биохимическом анализе крови наблюдается повышение уровня билирубина, а также гемоглобинемия (увеличение свободного гемоглобина в плазме крови).
Также необходимо сдать анализ мочи на выявление наличия гемоглобинурии.
При пункции костного мозга наблюдается выраженная гиперплазия эритроцитарного ростка.
Существует много видов гемолитической анемии, поэтому лечение может отличаться в зависимости от причины, вызвавшей анемию, а также от типа гемолиза.
При лечении гемолитической анемии больному могут назначаться следующие препараты:
- Фолиевая кислота. Профилактическая доза фолиевой кислоты назначается, потому что активный гемолиз может потреблять фолат и впоследствии привести к развитию мегалобластоза.
- Глюкокортикостероиды (например, Преднизолон) и иммунодепрессанты (например, Циклофосфан). Данные группы препаратов назначаются при аутоиммунной гемолитической анемии.
- Переливание эритроцитарной массы. Больному индивидуально подбираются отмытые эритроциты, так как существует высокий риск разрушения перелитой крови.
Спленэктомия
Спленэктомия может быть первоначальным вариантом в лечении некоторых типов гемолитической анемии, таких как, например, наследственный сфероцитоз. В других случаях, например, при аутоиммунной гемолитической анемии, спленэктомия рекомендуется тогда, когда другие методы лечения потерпели неудачу.
Терапия препаратами железа
При гемолитической анемии применение препаратов железа в большинстве случаев противопоказано. Это связано с тем, что уровень железа при данной анемии не снижается. Однако если у больного наблюдается постоянная гемоглобинурия, то происходит существенная потеря железа из организма. Поэтому при выявлении дефицита железа пациенту может быть назначено соответствующее лечение.
Проявления анемии будут зависеть от следующих факторов:
- какое количество крови было потеряно;
- с какой скоростью происходит кровопотеря.
Симптомами постгеморрагической анемии являются:
- слабость;
- головокружение;
- бледность кожных покровов;
- сердцебиение;
- одышка;
- тошнота, рвота;
- сечение волос и ломкость ногтей;
- шум в ушах;
- мелькание мушек перед глазами;
- жажда.
При острой кровопотере у больного может развиться геморрагический шок.
Выделяют четыре степени геморрагического шока.
источник