Термином «анемия» обозначают патологические состояния, характеризующиеся уменьшением содержания гемоглобина (Гб) и/или количества эритроцитов (Эр) в единице объема крови.
Анемический синдром выявляется в любом возрасте и является одной из самых распространенных патологий. Если учитывать все анемии не только как нозологические формы, но и анемический синдром при различных заболеваниях, то масштабы проблемы столь широки, что ее иногда характеризуют, как «скрытую эпидемию» («Анемия — скрытая эпидемия», 2004). Анемия выявляется у 15-20% беременных, а по некоторым данным — у 40% будущих матерей.
В зависимости от уровня гемоглобина выделяют анемию тяжелой (уровень гемоглобина 75 г/л и ниже), умеренной или средней (гемоглобин 80-100 г/л) и легкой (100-110 г/л) степени тяжести.
- Этиологически они подразделяются на анемии, обусловленные внутри-эритроцитарными факторами — обычно врожденными (аномалии мембраны, ферментопатии, гемоглобинопатии), и анемии, обусловленные внеэри-троцитарными факторами — обычно приобретенными.
- В зависимости от размеров эритроцитов — микроцитарные анемии (средний объем эритроцитов МСУ 3 ), нормоцитарные (СДЭ = 7-8 мкм;МСУ = 80-100 мкм 3 ) и макроцитарные (МСУ более 95-100 мкмЗ) МСУ анемии.
- В зависимости от степени насыщения гемоглобином — гипохромные (с цветовым показателем — ЦП — менее 0,85 и средней концентрацией гемоглобина в эритроцитах — МСНС — ниже 30 г/дл), нормохромные (ЦП = 0,9-1,1; МСНС = 30-38 г/дл) и гиперхромные (ЦП выше 1,1; МСНС более 38 г/дл) анемии.
- В зависимости от сохранности и адекватности реакции костного мозга на снижение уровня гемоглобина и эритроцитов, определяемого по числу ретикулоцитов, анемии могут быть разделены на гипорегенераторные (при уровне ретикулоцитов менее 1-1,2% при наличии анемии), связанные с нарушением продукции эритроцитов в костном мозге, а также нормо-или гиперрегенераторные (уровень ретикулоцитов повышен умеренно или значительно — до 20-30% и более. Повышение числа ретикулоцитов указывает на то, что малокровие, скорее всего, обусловлено гемолизом (т. е. повышенным разрушением эритроцитов) или кровотечением.
С учетом ведущего механизма развития строятся патогенетические классификации, примером которых может быть следующий вариант группировки анемий по патогенетическому механизму (Воробьев П. А., 2001):
- Железодефицитные анемии.
- Анемии, связанные с нарушением синтеза тема: сидероахрестические, дефицит гемсинтетазы.
- Анемии, связанные с нарушением синтеза ДНК — мегалобластные анемии.
- Анемии, обусловленные нарушением транспорта железа — атрансферри-немия.
- Гемолитические анемии.
- Анемии, связанные с костномозговой недостаточностью.
- Анемии, связанные с нарушением регуляции эритропоэза (повышение уровня ингибиторов эритропоэза).
зависят от степени снижения кислород-насыщающей способности крови, степени изменения общего объема крови, проявлений основного заболевания, которое приводит к развитию анемии и способности сердечно-сосудистой и дыхательной систем компенсировать анемию.
Многообразные клинико-гематологические проявления анемий можно разделить на две основные группы: симптомы, возникновение которых связано с гипоксией (так называемые неспецифические симптомы) и симптомы, характерные только для определенной анемии.
К общеанемическим симптомам, составляющим общеанемический синдром, относят слабость, бледность кожи и слизистых, одышку, тахикардию, головокружение, головную боль, снижение умственной концентрации, сонливость. Практически для всех видов анемий характерны симптомы со стороны сердечно-сосудистой системы, которые проявляются наличием шума в сердце, обычно систолического характера, который выслушивается в области легочной артерии. При тяжелой анемии шумы могут определяться в области митрального и трехстворчато го клапанов. Эти шумы легко дифференцируются от шумов, возникающих при органических поражениях сердца. При анемиях часто наблюдается ритм галопа пресистолического и протодиастолического типов. Изменения ЭКГ проявляются в депрессии интервала 8Т с 17-образной деформацией 8Т сегмента, изменении продолжительности электрической систолы (интервал С>Т), нарушении предсердно-желудочковой проводимости. При тяжелых анемиях (уровень НЬ ниже 60 -70 г/л) может наблюдаться фибрилляция предсердий.
При диагностике анемий важно выяснить особенности начала заболевания. Так постепенное начало чаще связано с нарушением продукции эритроцитов, острое — чаще наблюдается при повышенном разрушении красных кровяных клеток. Следует отметить имевшиеся провоцирующие факторы (вирусные инфекции, химические и физические факторы и др.), что может свидетельствовать в пользу определенного вида анемий (аутоиммунных, фер-ментопатий и т. д.).
Для установления патогенеза анемии при оценке показателей «красной крови» обращают внимание на так называемые, эритроцитарные параметры (индексы), отражающие размеры эритроцитов и степень их насыщения гемоглобином, количество ретикулоцитов и морфологические характеристики эритроидных клеток, которые отмечает врач-лаборант при просмотре мазка крови.
Снижение МСУ характерно для микроцитарных — железодефицитной анемии (ЖДА), талассемии. Причиной макроцитарной анемии, характеризующейся повышением показателя МСУ, могут быть мегалобластные анемии или нарушения, не связанные с нарушенным синтезом ДНК. Так причиной макроцитоза могут стать хронические заболевания печени, хронические заболевания почек, курение, гипо- и гипертиреоидизм.
Гипохромия эритроцитов выявляется в случаях, когда снижение Гб выражено сильнее, чем уменьшение числа Эр. Чаще всего это происходит при нарушениях процессов синтеза гемоглобина (при железодефицитной анемии, талассемии, свинцовом отравлении) и сидеробластной анемии (нарушение утилизации запасов железа). Как нормохромные, обычно характеризуются гемолитические анемии и анемии, связанные с гипопластическим состоянием костного мозга в частности. Гиперхромия — повышенная насыщенность гемоглобином цитоплазмы клеток характерна для макро- и мегалоцитов.
Гипорегенераторные анемии со сниженным или нормальным уровнем ретикулоцитов наблюдаются при дефиците железа, анемии при хронических заболеваниях или миелодисплазии. Значительное повышение числа ретикулоцитов указывает на то, что малокровие, вероятее всего, обусловлено гемолизом или кровотечением.
Важную информацию можно получить при оценке морфологических особенностей эритроцитов. Наличие макро- и особенно мегалоцитоза эритроцитов типично для Вр и фолиево-дефицитной анемии. Сфероциты встречаются при аутоиммунном гемолизе или наследственном сфероцитозе, шизоциты — фраг-ментированные эритроциты, расщепленные фибриновыми нитями — при микроангиопатиях (тромботической тромбоцитопенической пурпуре или диссемини-рованном внутрисосудистом свертывании — ДВС). Мишеневидные («таргетные») клетки в небольшом количестве появляются в крови при ряде гемоглобинопатии, при патологии печени, но наиболее характерны для талассемии, при которой их процентное содержание может быть значительным. Появление базофиль-ной пунктации эритроцитов характерно для свинцовых отравлений, талассемии и других дизэритропоэтических анемиях.
Ядерные формы эритроцитов (нормобласты или эритрокариоциты) наблюдаются при эритробластической анемии, инфильтрации костного мозга, гемолизе, гипоксии.
Дальнейшие исследования проводятся для уточнения предполагаемого варианта анемии и включают в себя биохимические, иммунологические и другие виды анализов.
Существуют определенные группы больных, относящихся к группам риска по развитию того или иного вида малокровия, которых желательно обследовать регулярно в порядке скрининга с целью выявления предрасположенности к анемии или ранних стадий анемии и проведения соответствующих профилактических и лечебных мероприятий.
Железодефщитная анемия (ЖДА) — наиболее распространенная форма анемий. Социальная значимость данной патологии определяется частой встречаемостью ЖДС среди женщин детородного возраста и детей, неблагоприятным влиянием железодефщита нарост и развитие детей и подростков, снижением работоспособности и ухудшением качества жизни взрослых, зависимостью частоты заболеваемости от ряда социальных факторов (уровня жизни, образования, здравоохранения).
Основные причины развития дисбаланса обмена железа в организме, ведущего к железодефицитным состояниям:
- Потери крови, особенно меноррагии или кровотечения из желудочно-кишечного тракта (ЖКТ) при эзофагите, пептической язве, карциноме, колите, дивертикулите, геморрое.
- Неадекватное питание, приводящее к развитию ЖДА у детей и подростков, реже у взрослых.
- Глистные инвазии и связанные с ними ЖК-кровопотери.
- Мальабсорбция (например, при кишечных заболеваниях).
К группам повышенного риска развития железодефицита относятся:
- Дети: потребности в железе при быстром росте часто превышают его поступление.
- Девочки в подростковом возрасте.
- Женщины: некомпенсированные потери железа во время менструаций, беременности, родов, гиперполименоррее.
- Доноры без компенсации потерь железа.
- Пожилые люди вследствие хронических гастроинтестинальных заболеваний и питания, содержащего мало мясных продуктов. Определенную роль в развитии заболевания играет геликобактерная инфекция.
Клиническая картина заболевания складывается из неспецифических проявлений общеанемического синдрома и проявлений тканевого дефицита железа — так называемого сидеропенического синдрома. Как правило, отмечается сухость кожи, характерный алебастровый или зеленоватый оттенок кожных покровов, а также голубоватый оттенок склер («симптом голубых склер»), как отражение дистрофических изменений роговицы в условиях дефицита железа, повышенная ломкость ногтей и волос. Возможно появление поперечной ис-черченности ногтевой пластинки и специфические «ложкообразные» их изменения — койлонихии. У больных имеется выраженная общая слабость, которая может не соответствовать степени анемии, и мышечная слабость, обусловленная нарушением синтеза миоглобина. Может выявляться дисфагия, извращение вкуса и обоняния с пристрастием к необычным запахам, «заеды» в углах рта (ангулярный стоматит), сглаженность сосочков языка, дизурические явления, недержание мочи при смехе, кашле.
Железодефицитная анемия сопровождается многочисленными осложнениями в течение беременности и родов как у матери, так и у плода, включая невынашивание беременности, кровотечение в родах.
Поскольку заболевание развивается медленно (месяцы и даже годы), клинические проявления обычно сглажены и больные адаптированы ко многим проявлениям.
Для анализов крови при ЖДА характерно наличие гипохромной микро-цитарной анемии, отмечается анизоцитоз эритроцитов. При оценке мазка крови обращает на себя внимание бледность эритроцитов, встречаются эритроциты в виде колец с широким просветлением в центре (анулоциты). При глубокой анемии отмечается выраженный анизоцитоз и пойкилоцитоз эритроцитов, могут появляться единичные мишеневидные клетки. Количество ретикулоцитов обычно в норме, т.к. регенераторная способность эритроидного ростка костного мозга сохранена. Транзиторный ретикулоцитоз может наблюдаться при выраженной кровопотере или при приеме препаратов железа незадолго до проведения анализов. У отдельных больных возможна умеренная лейкопения и может отмечаться тромбоцитопения (чаще у детей) или тромбоцитоз.
ЖДА диагностируется при сниженном уровне сывороточного железа ( 69 мкмоль/л (ОЖСС). Процент насыщения трансферрина железом (Кнас) 100 фл).
Заболевание обусловлено малъабсорбцией В/2 в результате атрофического гастрита и отсутствия секреции внутреннего желудочного фактора (перни-циозная анемия, болезнь Аддисона-Бирмера), гастрэктомия; алиментарный дефицит (в частности, у вегетарианцев); иногда болезни терминального отдела подвздошной кишки (болезнь Крона) или ее резекция; слепая петля; дивертикул; глистные инвазии (ВурМНоЪо1гшгп).
В12 содержится в печени и всех животных продуктах. Имеются запасы витамина в организме.
Нередко В12-ДА ассоциирована с заболеваниями щитовидной железы (до 25%), витилиго, болезнью Аддисона, карциномой желудка.
В клинической картине заболевания наряду с общеанемическими симптомами могут присутствовать признаки поражения центральной и периферической нервной системы, ЖКТ, что проявляется такими нарушениями, как: парестезии; периферическая нейропатия, нарушение позиционной и вибрационной чувствительности; нейропсихиатрические отклонения; глоссит — болезненный красный язык; диаррея.
Важно отметить, что неврологическая симптоматика (симптоматика так называемого «фуникулярного миелоза») может опережать развитие анемии.
Возможна умеренная желтушиость (лимонный оттенок кожи), умеренная спленомегалия и билирубинемия за счет непрямой фракции в связи с гемолизом (преимущественно внутрикостномозговым), нередко сопровождающим В12-ДА. Диагностика. Основное значение в диагностике ВП-ДА принадлежит морфологическим исследованиям крови и костного мозга. Анемия носит характер макроцитарной нормо- или гиперхромной, гипорегенераторной анемии. Отмечается анизо-, пойкилоцитоз, базофильная зернистость эритроцитов за счет наличия элементов РНК. В эритроцитах обнаруживаются остатки ядра в виде телец Жолли, колец Кебота. В клиническом анализе крови могут быть лейко-и тромбоцитопения, обычно умеренные, а также морфологические изменения гранулоцитов и тромбоцитов (формы больших размеров, гиперсегментация ядер нейтрофилов). Для уточнения диагноза показаны дополнительные исследования, включая исследование костного мозга для подтверждения мегалобластоид-ного типа кроветворения.
Имеются методы определения концентрации В]2 в сыворотке крови, что служит отражением запасов кобаламина в организме. Указанием на клинически значимый дефицит витамина Вр является его существенно сниженный сывороточный уровень.
У части больных могут обнаруживаться антитела к париетальным клеткам желудка или антитела к внутреннему фактору (специфические для пернициоз-ной анемии). В таких случаях иногда информативен тест Шиллинга, который назначается для определения, является ли дефицит В12 следствием мальабсорбции или отсутствия внутреннего фактора путем сравнения пропорции содержания в оральной дозе (1 мкг) радиоактивного В|2 с экскретируемым с мочой — при и без дополнительного назначения внутреннего фактора. Концентрация гомоци-стеина у больных с дефицитом В12 и дефицитом фолатов повышена.
Дифференциальная диагностика проводится с другими видами анемий, в первую очередь — макроцитарных, а также с фолиеводефицитной анемией. Понятие макроцитарной анемии отражает увеличенный размер эритроцитов, причиной которого могут быть нарушения, не связанные с синтезом ДНК. Дефицит витамина В12 следует отличать от таких заболеваний, как апластическая анемия, рефрактерная анемия или миелодиспластический синдром (МДС). Макроцитар-ную анемию с панцитопенией могут вызывать как гипо- так и гипертиреоидизм, а также алкоголизм, хронические заболевания печени. Причиной макроцитоза могут стать хронические заболевания почек и курение. Большое число ретику-лоцитов может повышать показатель МСУ, поскольку ретикулоциты являются крупными клетками. Вследствие этого гемолитическая анемия иногда ошибочно принимается за мегалобластную. В сложных случаях основным методом исследования является исследование костного мозга.
В лечении Вр-ДА важным моментом является устранение причины дефицита. Проводится заместительная терапия цианкобаламином до нормализации гематологических показателей или при ЦНС симптомах — пока не завершится восстановление. Большинству больных требуется поддерживающая терапия умеренными дозами В[2 на протяжении длительного времени (до полугода), а при неустранимости причины дефицита — в течение жизни. Предвестником начала улучшения является значительный ретикулоцитоз (как правило, после 4-5 дней) — ретикулоцитарный криз. Поскольку гемопоэз активизируется в ходе лечения, может быть необходимо дополнительное назначение препаратов железа. В трансфузиях эритроцитарной массы обычно необходимости нет.
Возможно полное гематологическое и неврологическое восстановление.
Причины низких фолатов — бедная диета (например, у алкоголиков), повышение потребности в фолатах (беременность, гемолиз, дизеритропоэз, опухоли, длительный гемодиализ), мальабсорбция, особенно при заболеваниях кишечника, тропическая спру, медикаменты (ряд противосудорожных препаратов, антагонист фолатов — метатрексат и др).
Фолаты содержатся в зеленых овощах, фруктах, печени и синтезируется кишечными бактериями. Запасы в организме истощаются относительно быстро при недостаточном поступлении.
Клиническая картина аналогична В]2-ДА, за исключением неврологических нарушений. Дефицит фолатов у матери также связан с дефектами нервной трубки у плода.
Диагностика. Картина крови и костного мозга не отличается от таковой при В12-ДА.
Для диагностики и дифференциальной диагностики используется определение уровня фолатов и В12 в сыворотке, а также фолатов эритроцитов.
При смешанных В]2-фолиеводефицитных формах анемии или неверной диагностике ФДА назначение одних фолатов может способствовать проявлению или ухудшению течения подострой комбинированной дегенерации спинного мозга.
Лечение. При ФДА проводится заместительная терапия фолиевой кислотой в виде перорального препарата. Терапия проводится под контролем показателей гемограммы (уровень гемоглобина и эритроцитов, эритроцитарные параметры, появление ретикулоцитарного криза) до нормализации показателей красной крови. При невозможности полного устранения факторов, способствующих развитию дефицита фолатов, в дальнейшем проводятся профилактические курсы терапии.
Прогноз благоприятный при адекватном лечении анемии и устранении причины заболевания.
Профилактика фолиеводефицитной анемии
Первичные профилактические мероприятия включают в себя наблюдение за лицами из групп риска, коррекцию диеты и назначение профилактических доз фолиевой кислоты при заболеваниях и состояниях, способствующих развитию ФДА. В частности, группу риска составляют больные эпилепсией, поскольку противосудорожные препараты являются потенциальными индукторами печеночных ферментов, а увеличение их активности приводит к ускоренному распаду фолатов и возникновению фолиеводефицитной мегалобластной анемии. Поэтому больных эпилепсией и пациентов, принимающих препараты из группы антиметаболитов, таких как метатрексат, необходимо регулярно обследовать для своевременного обнаружения анемии и проведения соответствующих мероприятий.
Гемолизом называют преждевременное разрушение эритроцитов. Он может происходить непосредственно в циркуляции (внутрисосудистый гемолиз) или в ретикулоэндотелиалъной системе (внесосудистый).
Причины гемолиза могут быть как генетически обусловленными, так и приобретенными. Генетические:
- Патология мембраны: врожденный сфероцитоз, эллиптоцитоз.
- Патология гемоглобина: серповидноклеточная болезнь — серповиднокле-точная анемия (СКВ = СКА), талассемия.
- Энзимные дефекты: дефицит глюкозо-фосфат дегидрогеназы (Г6 ФД), дефицит пируваткиназы и др.
- Иммунные: либо изоиммунные (гемолитическая болезнь новорожденных, посттрансфузионные реакции реакции гемолитического типа), аутоиммунные (обусловленные тепловыми или Холодовыми антителами), лекарственно-индуцированные.
- Неиммунные: травматические (кардиальный гемолиз, микроангиопатиче-ская анемия), инфекционные (малярия, септицемия), патология мембраны (па-роксизмальная ночная гемоглобинурия), заболевания печени.
Признаки гемолиза:
- Клинические: желтушность кожи, потемнение мочи, гепатоспленомегалия и др.
- Лабораторные:
— Связанные с повышенным разрушением эритроцитов:
— Повышение уровня билирубина (неконъюгированного);
— Увеличение содержания уробилина в моче;
— Снижение уровня гаптоглобина в сыворотке (связывает свободный гемоглобин).
— Связанные с повышенной продукцией эритроцитов:
— Гиперплазия костного мозга с расширением эритроидного ростка.
При установлении диагноза и проведении дифференциальной диагностики у больных гемолитическими анемиями необходимо обратить внимание на данные анамнеза (семейная история, национальная принадлежность, желтухи, гематурия, прием препаратов, ранее выявлявшейся анемии), на желтушность, гепатоспленомегалию, костные деформации (стигмы при наследственной патологии, особенности черепа при талассемии и др.), язвы на ногах (наблюдаются при СКВ, иногда при сфероцитозе).
Из лабораторных исследований показательными являются общий анализ крови с ретикулоцитами, уровень билирубина и фракционный его состав, ЛДГ, гаптоглобин (снижение уровня — показатель внутрисосудистого гемолиза), уро-билиноген мочи. Мазки крови могут показать полихромазию, макроцитоз, сфероцитоз, эллиптоцитоз, фрагментированные или серповидные клетки, мишене-видные клетки (характерны для талассемии). На следующем этапе проводятся специальные исследования, такие как тест Кумбса, определение гемосидерина мочи (индикатор хронического внутрисосудистого гемолиза). Аномалии мембраны могут быть подтверждены тестами на осмотическую стойкость. Электрофорез гемоглобина определяет варианты гемоглобина. Когда другие причины исключены, проводятся исследования ферментов.
Аутоиммунная гемолитическая анемия (АИГА) — анемия, при которой укорочение длительности жизни эритроцитов является результатом воздействия аутоантител против антигенов (мембранных белков) эритроцитов.
Частота встречаемости — около 1:100 000 населения.
Гемолиз может быть обусловлен тепловыми или Холодовыми антителами.
АИГА может быть самостоятельным заболеванием или выявляться при системных заболеваниях соединительной ткани, патологии щитовидной железы, синдроме Фишера—Эванса (нарушение иммунной регуляции с иммунной тромбоцито-лейкопенией, анемией в сочетании с рядом других нарушений). Известна ВИЧ-ассоциированная АИГА, вторичные АИГА вследствие микоплазменных, пневмококковых инфекций. Возможно появление аутоантител в результате повторных гемотрансфузий, беременностей. Холодовые агглютинины могут продуцироваться микоплазмой и ЭБВ.
Выделяют острую и хроническую формы. Для большинства случаев характерно острое начало с возможным переходом в хроническую форму. В зависимости от серологического варианта различают АИГА с полными и неполными антителами, с тепловыми и Холодовыми антителами, гемолизиновые формы.
Пароксизмальная холодовая гемоглобинурия (синдром Доната-Ландштей-нера), как правило, наблюдается после перенесенных вирусных инфекций и в поздних стадиях сифилиса.
В клинической картине
сочетаются симптомы анемии и гемолиза: потемнение мочи, иктеричность кожи и склер, лихорадка, боли в животе, умеренная гаштоспленомегалия. Особенностью холодовой АИГА является обострение хронической анемии на холоде, частое сочетание с синдромом Рейно или акро-цианозом. Гемолизиновые формы нередко сопровождаются гемоглобинурией и другими признаками острого внутрисосудистого гемолиза.
Диагностика.
Анемия, как правило, нормохромная нормоцитарная, характерен ретикулоцитоз, часто выраженный. Могут встречаться сфероциты в небольшом количестве. Возможен лейкоцитоз со сдвигом лейкоцитарной формулы плево, умеренный тромбоцитоз. Характерно повышение непрямого билирубина, эритроидная гиперплазия костного мозга. Увеличивается уровень лактатдеги-дрогеначы (ЛДГ) сыворотки. Уровень сывороточного железа в норме или повышен, гаптоглобина — в норме или снижен.
Дифференциальная диагностика
проводится с другими видами анемий, в первую очередь — гемолитическими, вторичными анемиями, болезнью Жиль-бера. Задача врачей общей практики — заподозрить данный вид анемии и провести первичную диагностику. Уточнение варианта и лечение обычно проводится в специализированных учреждениях.
Основным диагностическими тестом является положительный прямой анти-глобулиновый тест (проба Кумбса), определяющий антитела или комплемент на поверхности эритроцитов. Дополнительно проводится непрямой тест Кумбса, определяющий антитела в сыворотке.
В лечении аутоиммунных форм гемолитической анемии основное место принадлежит глюкокортикостероидам (ГК). У пациентов с острым гемолизом может использоваться внутривенный иммуноглобулин, обычно в сочетании с ГК.
При отсутствии эффекта от консервативной терапии возможно проведение спленэктомии, эффективность которой при данной патологии составляет около 70%. Из иммуносупрессивных препаратов при неэффективности обычной терапии в лечении АИГА используется азатиаприн, цитостатики (винкаалкалоиды, циклофосфамид), циклоспорин А.
Основой лечения симптоматических анемий является лечение базового заболевания.
Профилактика аутоиммунной гемолитической анемии
Первичные профилактические мероприятия заключаются в лечении основных заболеваний, при которых может возникнуть АИГА.
Вторичная прфилактика. Пациентам, страдающим АИГА для предотвращения усиления гемолиза и развития гемолитических кризов рекомендуется избегать провоцирующих факторов: переохлаждения при Холодовых формах, вирусных инфекций — при всех вариантах заболевания и др. Пациентам, которым произведена спленэктомия, учитывая развитие иммунодефицита, показано введение пневмококковой вакцины. Эта рекомендация в первую очередь относится к детям и лицам, имеющим дополнительные показания к вакцинации (по эпидемиологической обстановке и др.).
Наследственный сфероцитоз (НС) — цитоскелетная аномалия, обусловленная нарушением структуры спектрина. Результатом таких аномалий является потеря способности эритроцитов к деформации, нарушается работа Ш+/К+ — насоса мембраны, происходит преждевременная (не по мере старения) сферуляция эритроцитов, укорочение продолжительности жизни красных кровяных клеток и разрушение их клетками селезенки. Длительность жизни эритроцитов укорачивается до 12-14 дней.
Обусловлено мутациями в генах, кодирующих мембранные белки цитоске-лета эритроцитов. Наследование аутосомно-доминантное (проявляется анемией легкой и средней степени тяжести) или рецессивное (клинически проявляется в тяжелой форме).
Характеризуется гемолитической анемией, спленомегалией и наличием эритроцитов сферической формы в периферической крови. Болезнь может протекать скрыто.
НС основывается на наличии у пациента характерных морфологических изменений эритроцитов и признаков гемолиза. Показатели насыщения эритроцитов гемоглобином и уровень сывороточного железа обычно в норме, за исключением тех случаев, когда на фоне длительно существующего гемолиза в организме развивается железодефицитное состояние.
В костном мозге отмечается компенсаторное усиление эритропоэза.
Дифференциальный диагноз
проводится с желтухами другой этиологии (инфекционным гепатитом, обструктивной желтухой, синдромом Жильбера и др.), иммунной гемолитической анемией, микроангиопатической гемолитической анемией, спленомегалиями другой этиологии. При дифференциальной диагностике наряду с выявлением морфологически измененных эритроцитов, отрицательной пробой Кумбса и другими лабораторными данными, немаловажное значение может иметь тщательно собранный семейный анамнез и обследование родственников больного для выявления у них признаков НС.
При клинически компенсированном состоянии больного, отсутствии значимого гемолиза и анемии терапия обычно ограничивается симптоматическими средствами, в том числе направленными на профилактику развития желчекаменной болезни (желчегонные, фитотерапия, рациональная диета). При тяжелом гемолизе с выраженной анемией и при апластических кризах с низким уровнем гемоглобина производятся трансфузии эритроцитарной массы.
Одним методом терапии у больных сфероцитарной анемией является спле-нэктомия. Оперативное лечение показано больным с наличием гемолитической анемии средней и тяжелой степени или ее осложнений, в том числе при наличии желчнокаменной болезни, особенно у лиц молодого возраста. В результате удаления селезенки прекращается или значительно уменьшается гемолиз эритроцитов, увеличивается продолжительность их жизни.
Первичная профилактика
при НС, как и при других наследственных заболеваниях, заключается в генетическом консультировании и планировании семьи.
Вторичная профилактика.
Поскольку у значительной части пациентов заболевание протекает в скрытой или клинически компенсированной форме, то основные мероприятия по вторичной профилактике направлены на устранение проявлений хронической интоксикации, компенсацию повышенного расхода необходимых для кроветворения веществ и предупреждение таких осложнений, как раннее развитие желчнокаменной болезни. В связи с этим показано полноценное питание, прием поливитаминов с микроэлементами, желчегонных средств, ежегодный УЗИ-контроль состояния желчевыводящих путей.
Как и при других формах хронических гемолитических анемий у больных НС нередко развивается дефицит фолатов, в связи с чем этой категории больных профилактически назначается фолиевая кислота.
Анемии могут быть обусловлены подавленным (гипотастическим) состоянием кроветворения за счет токсических и радиационных воздействий, развития реактивного фиброза в костном мозге при ряде заболеваний или в результате самостоятельных заболеваний — гипопластической (апластической) анемии, парциальной красноклеточной аплазии.
Апластическая анемия — тяжелое заболевание кроветворной системы, которое характеризуется панцитопенией в периферической крови и гипоклеточ-ным костным мозгом.
Заболевание редкое: от 2-3 до 10-20 случаев на млн населения в год. Наблюдается во всех возрастных группах. Большая частота встречаемости заболевания отмечается на Дальнем Востоке, в Японии, Таиланде.
Причинами развития заболевания могут быть цитотоксические препараты, радиация, лекарственные препараты (золото, хлорамфеникол), промышленные токсины, вирусы (гепатит). Этиологический фактор в половине случаев не выявляется — идиопатические формы. Выделяют врожденную форму — анемию Фанкони — генетически обусловленное заболевание с гиперчувствительностью к ДНК-повреждающим воздействиям и повышенной склонностью к развитию опухолевых заболеваний.
Современная концепция патогенеза АА предполагает связь между развитием аплазии кроветворения и дефектом стволовых клеток с нарушением их проли-феративной активности с участием иммуноопосредованных механизмов, нарушением регуляции гемопоэза иммунокомпетентными лимфоидными клетками.
Выделяют острую и хроническую формы заболевания, а также тяжелую апластическую анемию (тАА) и АА умеренной степени тяжести (нетяжелая апластическая анемия — нАА). ТАА определяется при наличии 2 любых из перечисленных критериев по данным периферической крови:
- Гранулоцитов менее 0,5 х 109/л
- Тромбоцитов менее 20 х 109/л
- Ретикулоцитов менее 1% (с коррекцией по гематокриту) в сочетании с аплазией костного мозга по данным трепанобиоптатов (клеточность костного мозга не более 30% от нормы).
Клинические проявления
заболевания обусловлены анемическим и геморрагическим синдромом.
Диагноз ставится на основании выявления характерных изменений в анализах крови и костном мозге с отсутствием признаков клонального гемопоэза. Осноиой диагностики является гистологическое исследование костного мозга.
Анемия нормохромного характера, количество ретикулоцитов снижено, как проянлспие I шюрегенераторного характера анемии.
И мпелограмме снижено количество ядросодержащих элементов, снижено суммарное процентное содержание клеточных элементов гранулопоэза и эритропоэза, нередко отмечается высокое относительное число лимфоцитов, значительно уменьшено содержание мегакариоцитов. В гистологических препаратах трепанопрепаратов подвздошной кости выявляется аплазия костного мозга с замещением кроветворной ткани жировой.
Содержание железа в сыворотке крови нормально или повышено.
Дифференциальный диагноз
проводится с гипопластическими вариантами гемобластозов (миелодиспластический синдром — МДС, острый лейкоз, су-блейкемический миелоз), вторичными — симптоматическими аплазиями, наблюдающимися при заболеваниях печени, ряде опухолевых заболеваний.
Пациентам с АА проводится иммуносупрессивная терапия, включающая глюкокортикоидные гормоны (ГК), антилимфоцитарный (АЛГ) или антитимоцитарный (АТГ) иммуноглобулин, циклоспорин-А (цА). Методом выбора в терапии тАА у пациентов до 40 лет является трансплантация костного мозга (ТКМ). Такая терапия позволяет получить ремиссии у 70 -80%. Проводится также симптоматическая терапия, направленная на коррекцию анемического и геморрагического синдромов, профилактику и лечение возможных инфекционных и иных осложнений.
Прогноз заболевания в первую очередь зависит от глубины аплазии и тяжести заболевания, а также своевременности и активности проводимой терапии.
Основные причины смерти больных — геморрагические и инфекционные осложнения, прогрессирование аплазии при безуспешной терапии.
Первичные профилактические мероприятия предусматривают прекращение контакта с факторами, обладающими гемодепрессивными свойствами, ограничение использования лекарственных препаратов с миелосупрессивными свойствами. Так, в ряде стран прекращено применение препарата левомецитин (хлорамфеникол), поскольку была показана связь приема данного лекарственного средства с повышением частоты развития аплазии кроветворения. При развитии АА на фоне беременности целесообразно ее прерывание.
Вторичная профилактика.
Пациенты с ремиссией заболевания должны оставаться под наблюдением с регулярным контролем показателей гемограммы, поскольку возможны рецидивы заболевания, как под воздействием неблагоприятных факторов, так и спонтанные.
источник
Железодефицитная анемия — анемия, вызванная недостатком железа в организме в результате нарушения баланса между его поступлением, использованием и потерей. Это самый распространенный вид анемии (80% всей заболеваемости анемиями).
Этиология. Наиболее частой причиной развития железодефицитной анемии (ЖДА) являются повторные и длительные, иногда массивные однократные кровотечения, приводящие к потере железа вместе с эритроцитами. Чаще всего это наблюдается при маточных, реже — желудочно-кишечных, почечных, легочных кровотечениях, при геморрагическом синдроме (см. «Постгеморрагическая анемия«).
ЖДА может возникать при нарушении поступления железа с пищей (при кормлении детей только коровьим или козьим молоком) и повышенном расходе железа в период роста, созревания организма, при беременности, лактации. Кроме того, причиной развития ЖДА служит снижение всасывания железа при заболеваниях пищевого канала (гипоацидный гастрит, хронический энтерит) или резекции его отделов, а также нарушение транспорта железа (гипотрансферринемия при поражении печени, наследственная атрансферринемия 3 ), его утилизации из резервов 4 (при инфекции, интоксикации, глистной инвазии) и депонировании (при гепатитах, циррозе печени).
Патогенез. Экзогенный или эндогенный дефицит железа в организме характеризуется уменьшением и постепенным истощением резервов железа, что проявляется исчезновением гемосидерина в макрофагоцитах печени и селезенки, снижением до 2—5% в костном мозге количества сидеробластов (клетки, содержащие железо в виде гранул ферритина; их число в норме — 20—40%). В крови понижается концентрация сывороточного железа (гипосидеремия достигает 1,8—2,7 мкм/л вместо 12,5—30,4 мкм/л в норме) и степень насыщения им трансферрина, что приводит к уменьшению транспорта железа в костный мозг. Нарушается включение железа в эритроцитарные клетки, снижается синтез гема в гемоглобине и некоторых железосодержащих и железозависимых ферментов (каталазы, глутатионпероксидазы) в эритроцитах, что повышает их чувствительность к гемолизирующему действию окислителей. Увеличивается неэффективный эритропоэз вследствие возросшего гемолиза эритрокариоцитов в костном мозге и эритроцитов в крови. Продолжительность жизни эритроцитов уменьшается.
В организме при железодефицитной анемии возникают компенсаторные реакции — усиление абсорбции железа в пищевом канале, повышение концентрации трансферрина, гиперплазия эритроцитарного ростка, увеличение интенсивности гликолиза и активности 2,3-дифосфоглицерата в эритроцитах, способствующее лучшей отдаче кислорода тканям. Однако эти реакции оказываются недостаточными, чтобы восполнить дефицит железа в организме и улучшить кислородтранспортную функцию крови при уменьшении общего количества эритроцитов и содержания в них гемоглобина. Возникают морфологические изменения в эритроцитарных клетках костного мозга: гипохромия, связанная с недостаточной гемоглобинизацией, преобладание базофильных нормобластов над ацидофильными в костном мозге, микроцитоз, деструкция ядерных клеток (нарушение митоза, кариорексис, вакуолизация цитоплазмы эритробластов и нормобластов).
Наряду с патологическими изменениями эритропоэза дефицит железа в организме приводит к уменьшению миоглобина и активности железосодержащих ферментов тканевого дыхания. Следствием гемической и тканевой гипоксии при железодефицитной анемии являются атрофические и дистрофические процессы в тканях и органах, особенно выраженные в пищевом канале (глоссит, гингивит, кариес зубов, поражение слизистой оболочки пищевода, атрофический гастрит с ахилией) и сердце (дистрофия миокарда).
Картина крови. Железодефицитная анемия — это анемия с эритробластическим типом кроветворения, гипохромная с низким цветовым показателем (0,6 и меньше). Количество гемоглобина снижается в большей степени, чем число эритроцитов. Для мазка крови характерны гипохромия, «тени» эритроцитов, анулоциты, микроцитоз, пойкилоцитоз. Количество ретикулоцитов зависит от регенераторной способности эритроцитарного ростка (регенераторная или чаще гипорегенераторная анемия).
В12— И ФОЛИЕВОДЕФИЦИТНАЯ АНЕМИЯ
В12— и фолиеводефицитная анемия — анемия, связанная с нарушением синтеза нуклеиновых кислот и заменой эритробластического типа кроветворения мегалобластическим вследствие недостатка в организме цианокобаламина (витамина В12) и фолиевой кислоты (мегалобластная анемия).
Этиология. По этиологии эти анемии могут быть приобретенными и наследственными. Причины, общие для В12— и фолиеводефицитной анемий, следующие:
1. недостаток этих витаминов в пище (вскармливание грудных детей козьим молоком, сухими молочными смесями);
2. нарушение всасывания витаминов в тонкой кишке (при резекции тощей кишки или поражении ее опухолью, множественными дивертикулами, при тропическом спру, дифиллоботриозе, алкоголизме);
3. повышенное расходование витаминов при беременности (когда эмбриональный тип кроветворения у плода сменяется эритробластическим, увеличивается потребление плодом цианокобаламина и фолиевой кислоты матери);
4. нарушение депонирования витаминов при диффузном поражении печени (гепатит, цирроз). Кроме того, дефицит цианокобаламина возникает в результате нарушения образования внутреннего фактора Касла — мукопротеида (транскоррина) — при наследственном дефекте выработки его клетками желез желудка, при поражении слизистой оболочки желудка опухолью, сифилитической гуммой, большими дозами алкоголя, при резекции желудка, разрушений мукопротеида аутоантителами.
Причиной возникновения пернициозной анемии (злокачественной, анемии Аддисона — Бирмера), являющейся разновидностью В12-дефицитной анемии, могут быть генетически детерминированный дефицит транскоррина (наследуется по аутосомно-рецессивному типу) или же аутоиммунный процесс, о чем свидетельствует обнаружение у больных в сыворотке и желудочном соке антител (IgG, IgA) к антигенам цитоплазмы париетальных клеток, реже — к внутреннему фактору.
Патогенез. При дефиците цианокобаламина (его кофермента — метилкобаламина) не происходит превращения фолиевой кислоты в ее коферментную форму — тетрагидрофолиевую кислоту, без которой невозможен синтез тимидинмонофосфата, входящего в состав ДНК. Нарушается клеточное деление и прежде всего страдают активно размножающиеся клетки кроветворной ткани. В костном мозге задерживается размножение и созревание эритрокариоцитов., эритробластический тип кроветворения заменяется мегалобластическим, возрастает неэффективный эритропоэз, укорачивается продолжительность жизни эритроцитов. Вследствие нарушения кроветворения и гемолиза эритроцитов развивается анемия, при которой клетки патологической регенерации и эритроциты с признаками дегенерации появляются не только в костном мозге, но и в крови. Изменение лейко- и тромбоцитопоэза проявляется уменьшением числа лейкоцитов и тромбоцитов, выраженной атипией клеток.
Возникновение атипичного митоза и гигантских клеток эпителия пищевого канала приводит к развитию воспалительно-атрофических процессов в слизистой оболочке его отделов (глоссит, стоматит, эзофагит, ахилический гастрит, энтерит). Это усугубляет первичное нарушение секреции и всасывания внутреннего фактора и, следовательно, усиливает дефицит витаминов (порочный круг).
В результате недостатка цианокобаламина (его кофермент дезоксиаденозилкобаламин участвует в образовании янтарной кислоты из метилмалоновой кислоты) в организме накапливается метилмалоновая кислота, токсичная для нервных клеток, а в нервных волокнах синтезируются жирные кислоты с измененной структурой, что отражается на образовании миелина и ведет к повреждению аксона. Развивается дегенерация задних и боковых столбов спинного мозга (фуникулярный миелоз), поражаются черепные и периферические нервы с развитием многообразной неврологической симптоматики.
Картина крови. В12— и фолиеводефицитные анемии — это анемии с мегалобластическим типом кроветворения, гиперхромные, макроцитарные. Содержание эритроцитов и гемоглобина в крови при этих анемиях может резко снижаться, однако цветовой показатель выше 1 (1,4—1,8) в связи с наличием в крови больших по объему мегалобластов и мегалоцитов, насыщенных гемоглобином.
В мазке крови появляются клетки патологической регенерации костного мозга — мегалоциты (интенсивно окрашенные клетки диаметром 10—12 мкм и более, не имеющие центрального просветления, несколько овальной формы) и единичные мегалобласты (крупные клетки размером 12—15 мкм с базофильной, полихроматофильной или ацидофильной цитоплазмой и нежносетчатым, обычно эксцентрично расположенным ядром). Существует точка зрения, согласно которой мегалобласты и мегалоциты при В12— и фолиеводефицитных анемиях не идентичны эмбриональным клеткам эритроцитарного ряда и только внешне похожи на них. В крови встречается много дегенеративно измененных эритроцитов: пойкилоцитоз, анизоцитоз, гиперхромные мегало- и макроциты, мегалоциты с включениями в виде телец Жолли, колец Кебота, эритроциты с базофильной зернистостью. Уменьшается количество клеток физиологической регенерации (ретикулоциты, полихроматофилы), так как в костном мозге наблюдается раздражение эритроцитарного ростка с преобладанием мегалобластического эритропоэза на фоне угнетения эритробластического кроветворения. Наблюдается лейко- и тромбоцитопения с атипическими клетками (например, гигантские полисегментированные нейтрофильные гранулоциты размером 20—30 мкм, с 8—10 сегментами).
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: При сдаче лабораторной работы, студент делает вид, что все знает; преподаватель делает вид, что верит ему. 8975 — 

источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
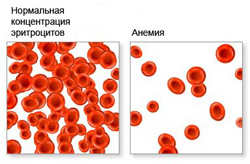
Эритроциты формируются в красном костном мозге из белковых фракций и небелковых компонентов под воздействием эритропоэтина (синтезируется почками). Эритроциты в течение трех дней обеспечивают транспорт, главным образом, кислорода и углекислого газа, а также питательных веществ и продуктов метаболизма от клеток и тканей. Срок жизни эритроцита сто двадцать дней, после чего он разрушается. Старые эритроциты накапливаются в селезенке, где утилизируются небелковые фракции, а белковые поступают в красный костный мозг, участвуя в синтезе новых эритроцитов.
Вся полость эритроцита наполнена белком, гемоглобином, в состав которого входит железо. Гемоглобин придает эритроциту красную окраску, а также помогает ему переносить кислород и углекислый газ. Его работа начинается в легких, куда эритроциты поступают с током крови. Молекулы гемоглобина захватывают кислород, после чего обогащенные кислородом эритроциты направляются сначала по крупным сосудам, а затем и по мелким капиллярам к каждому органу, отдавая клеткам и тканям необходимый для жизни и нормальной деятельности кислород.
Анемия ослабляет способность организма к газовому обмену, за счет сокращения числа эритроцитов нарушается транспортировка кислорода и углекислого газа. Вследствие этого у человека могут наблюдаться такие признаки анемии как чувство постоянной усталости, упадок сил, сонливость, а также повышенная раздражительность.
Анемия является проявлением основного заболевания и не является самостоятельным диагнозом. Многие болезни, включая инфекционные заболевания, доброкачественные или злокачественные опухоли могут быть связаны с анемией. Именно поэтому анемия является важным признаком, который требует проведения необходимых исследований для выявления основной причины, которая привела к ее развитию.
Тяжелые формы анемии вследствие тканевой гипоксии могут привести к серьезным осложнениям, таким как шоковые состояния (например, геморрагический шок), гипотония, коронарная или легочная недостаточность.
- по механизму развития;
- по степени тяжести;
- по цветному показателю;
- по морфологическому признаку;
- по способности костного мозга к регенерации.
| По патогенезу анемия может развиться вследствие кровопотери, нарушения образования эритроцитов или из-за их выраженного разрушения. По механизму развития выделяют:
|
- потеря крови (острые или хронические кровотечения);
- повышенное разрушение эритроцитов (гемолиз);
- уменьшенное производство эритроцитов.
Также следует заметить, что в зависимости от вида анемии причины ее возникновения могут отличаться.
Факторы, влияющие на развитие анемии
- гемоглобинопатии (изменение строения гемоглобина наблюдается при талассемии, серповидноклеточной анемии);
- анемия Фанкони (развивается вследствие имеющегося дефекта в кластере белков, которые отвечают за восстановление ДНК);
- ферментативные дефекты в эритроцитах;
- дефекты цитоскелета (клеточный каркас, располагающийся в цитоплазме клетки) эритроцита;
- врожденная дизэритропоэтическая анемия (характеризуется нарушением образования эритроцитов);
- абеталипопротеинемия или синдром Бассена-Корнцвейга (характеризуется нехваткой бета-липопротеина в клетках кишечника, что ведет к нарушению всасываемости питательных веществ);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (вследствие нарушения клеточной мембраны эритроциты принимают шарообразную форму).
- дефицит железа;
- дефицит витамина B12;
- дефицит фолиевой кислоты;
- дефицит аскорбиновой кислоты (витамин С);
- голодание и недоедание.
Хронические заболевания и новообразования
- почечные заболевания (например, туберкулез печени, гломерулонефрит);
- заболевания печени (например, гепатит, цирроз);
- заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, атрофический гастрит, неспецифический язвенный колит, болезнь Крона);
- коллагеновые сосудистые болезни (например, системная красная волчанка, ревматоидный артрит);
- доброкачественные и злокачественные опухоли (например, миома матки, полипы в кишечнике, рак почек, легких, кишечника).
- вирусные заболевания (гепатит, инфекционный мононуклеоз, цитомегаловирус);
- бактериальные заболевания (туберкулез легких или почек, лептоспироз, обструктивный бронхит);
- протозойные заболевания (малярия, лейшманиоз, токсоплазмоз).
Ядохимикаты и медикаментозные средства
- неорганический мышьяк, бензол;
- радиация;
- цитостатики (химиотерапевтические препараты, используемые для лечения опухолевых заболеваний);
- антибиотики;
- нестероидные противовоспалительные средства;
- антитиреоидные препараты (снижают синтез гормонов щитовидной железы);
- противоэпилептические препараты.
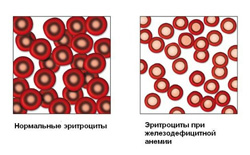
Для железодефицитной анемии характерно снижение эритроцитов, гемоглобина и цветового показателя.
Железо — это жизненно важный элемент, участвующий во многих метаболических процессах организма. У человека с весом семьдесят килограмм запас железа в организме составляет примерно четыре грамма. Данное количество поддерживается благодаря сохранению баланса между регулярными потерями железа из организма и его поступлением. Для поддержания равновесия суточная потребность железа составляет 20 – 25 мг. Большая часть поступающего железа в организм затрачивается на его нужды, остальное депонируется в виде ферритина или гемосидерина и при необходимости расходуется.
Нарушение поступления железа в организм
- вегетарианство вследствие неупотребления белков животного происхождения (мясо, рыба, яйца, молочные продукты);
- социально-экономическая составляющая (например, недостаточно денег для полноценного питания).
Нарушение усвоения железа
Всасывание железа происходит на уровне слизистых желудка, поэтому такие заболевания желудка как гастриты, язвенная болезнь или резекция желудка приводят к нарушению всасывания железа.
Повышенная потребность организма в железе
- беременность, в том числе многоплодная беременность;
- период лактации;
- подростковый возраст (за счет быстрого роста);
- хронические заболевания, сопровождающиеся гипоксией (например, хронический бронхит, пороки сердца);
- хронические нагноительные заболевания (например, хронические абсцессы, бронхоэктатическая болезнь, сепсис).
Потери железа из организма
- легочные кровотечения (например, при раке легких, туберкулезе);
- желудочно-кишечные кровотечения (например, язва желудка и двенадцатиперстной кишки, рак желудка, рак кишечника, варикозное расширение вен пищевода и прямой кишки, неспецифический язвенный колит, глистные инвазии);
- маточные кровотечения (например, преждевременная отслойка плаценты, разрыв матки, рак матки или шейки матки, прервавшаяся внематочная беременность, миома матки);
- почечные кровотечения (например, рак почек, туберкулез почек).
Питание при анемии
В питании железо делится на:
- гемовое, которое поступает в организм с продуктами животного происхождения;
- негемовое, которое поступает в организм с продуктами растительного происхождения.
Следует заметить, что гемовое железо усваивается в организме значительно лучше, нежели негемовое.
Количество железа на сто миллиграмм
Продукты питания
животного
происхождения
- печень;
- язык говяжий;
- мясо кролика;
- индюшатина;
- гусиное мясо;
- говядина;
- рыба.
- 9 мг;
- 5 мг;
- 4,4 мг;
- 4 мг;
- 3 мг;
- 2,8 мг;
- 2,3 мг.
Продукты питания растительного происхождения
- сушеные грибы;
- свежий горох;
- гречка;
- геркулес;
- свежие грибы;
- абрикосы;
- груша;
- яблоки;
- сливы;
- черешня;
- свекла.
- 35 мг;
- 11,5 мг;
- 7,8 мг;
- 7,8 мг;
- 5,2 мг;
- 4,1 мг;
- 2,3 мг;
- 2,2 мг;
- 2,1 мг;
- 1,8 мг;
- 1,4 мг.
При соблюдении диеты также следует увеличить потребление продуктов, содержащих витамин C, а также белок мяса (они повышают усвояемость железа в организме) и снизить потребление яиц, соли, кофеина и кальция (они уменьшают всасываемость железа).
Медикаментозное лечение
При лечении железодефицитной анемии больному параллельно с диетой назначается прием препаратов железа. Данные лекарственные средства предназначены для восполнения дефицита железа в организме. Они выпускаются в виде капсул, драже, инъекций, сиропов и таблеток.
Доза и длительность лечения подбирается индивидуально в зависимости от следующих показателей:
- возраста пациента;
- степени тяжести заболевания;
- причины, вызвавшей железодефицитную анемию;
- на основе результатов анализов.
Препараты железа принимаются за один час до еды или через два часа после приема пищи. Данные лекарственные средства нельзя запивать чаем или кофе, так как снижается всасываемость железа, поэтому их рекомендуется запивать водой или соком.
Принимать внутрь по одному грамму три – четыре раза в сутки.
Принимать по одной таблетке в день, с утра за тридцать минут до приема пищи.
Принимать по одной таблетке один – два раза в день.
Данные препараты рекомендуется назначать совместно с витамином C (по одной таблетке один раз в день), так как последний увеличивает всасываемость железа.
Препараты железа в виде инъекций (внутримышечных или внутривенных) применяются в следующих случаях:
- при тяжелой степени анемии;
- если анемия прогрессирует, несмотря на принимаемые дозы железа в виде таблеток, капсул или сиропа;
- если у больного имеются заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, неспецифический язвенный колит, болезнь Крона), так как принимаемый препарат железа может усугубить имеющееся заболевание;
- перед оперативными вмешательствами с целью ускоренного насыщения организма железом;
- если у пациента имеется непереносимость препаратов железа при их приеме внутрь.
Хирургическое лечение
Хирургическое вмешательство производится при наличии у больного острого или хронического кровотечения. Так, например, при желудочно-кишечном кровотечении может применяться фиброгастродуоденоскопия или колоноскопия с выявлением области кровотечения и последующей его остановкой (например, удаляется кровоточащий полип, коагулируется язва желудка и двенадцатиперстной кишки). При маточных кровотечениях, а также при кровотечениях в органах, находящихся в брюшной полости, может применяться лапароскопия.
При необходимости больному может быть назначено переливание эритроцитарной массы для восполнения объема циркулирующей крови.

В норме витамин В12 поступает в организм с пищевыми продуктами. На уровне желудка В12 связывается с продуцируемым в нем белком, гастромукопротеидом (внутренний фактор Касла). Данный белок защищает поступивший в организм витамин от негативного воздействия микрофлоры кишечника, а также способствует его усвоению.
Комплекс гастромукопротеид и витамин В12 доходит до дистального отдела (нижний отдел) тонкого кишечника, где происходит распад этого комплекса, всасывание витамина В12 в слизистый слой кишечника и дальнейшее поступление его в кровь.
Из кровяного русла данный витамин поступает:
- в красный костный мозг для участия в синтезе эритроцитов;
- в печень, где происходит его депонирование;
- в центральную нервную систему для синтеза миелиновой оболочки (покрывает аксоны нейронов).
Клиническая картина В12 и фолиево-дефицитной анемии основывается на развитии у больного следующих синдромов:
- анемический синдром;
- желудочно-кишечный синдром;
- невралгический синдром.
| |
Данные симптомы развиваются вследствие атрофических изменений слизистого слоя ротовой полости, желудка и кишечника. |
|
- снижение уровня эритроцитов и гемоглобина;
- гиперхромия (выраженная окраска эритроцитов);
- макроцитоз (увеличенный размер эритроцитов);
- пойкилоцитоз (различная форма эритроцитов);
- при микроскопии эритроцитов выявляются кольца Кебота и тельца Жолли;
- ретикулоциты снижены или в норме;
- снижение уровня лейкоцитов (лейкопения);
- повышение уровня лимфоцитов (лимфоцитоз);
- снижение уровня тромбоцитов (тромбоцитопения).
В биохимическом анализе крови наблюдается гипербилирубинемия, а также снижение уровня витамина В12.
При пункции красного костного мозга выявляется повышение мегалобластов.
Больному могут быть назначены следующие инструментальные исследования:
- исследование желудка (фиброгастродуоденоскопия, биопсия);
- исследование кишечника (колоноскопия, ирригоскопия);
- ультразвуковое исследование печени.
Данные исследования помогают выявить атрофические изменения слизистой оболочки желудка и кишечника, а также обнаружить заболевания, которые привели к развитию В12-дефицитной анемии (например, злокачественные образования, цирроз печени).
Все больные госпитализируются в отделение гематологии, где проходят соответствующее лечение.
Питание при В12-дефицитной анемии
Назначается диетотерапия, при которой увеличивается потребление продуктов, богатых витамином В12.
Суточная норма витамина В12 составляет три микрограмма.
Количество витамина В12 на сто миллиграмм
Медикаментозное лечение
Медикаментозное лечение назначается больному по следующей схеме:
- В течение двух недель больной ежедневно получает по 1000 мкг Цианокобаламина внутримышечно. За две недели у пациента исчезает неврологическая симптоматика.
- В течение последующих четырех – восьми недель больной получает по 500 мкг ежедневно внутримышечно для насыщения депо витамина В12 в организме.
- Впоследствии больной пожизненно получает внутримышечные инъекции один раз в неделю по 500 мкг.
Во время лечения одновременно с Цианокобаламином больному могут назначить прием фолиевой кислоты.
Больной В12-дефицитной анемией должен пожизненно наблюдаться у гематолога, гастролога и семейного врача.
Фолиевая кислота (витамин B9) является водорастворимым витамином, который отчасти продуцируется клетками кишечника, но в основном должен поступать извне для восполнения необходимой для организма нормы. Суточная норма фолиевой кислоты составляет прием 200 – 400 мкг.
В пищевых продуктах, а также в клетках организма фолиевая кислота находится в форме фолатов (полиглутаматы).
Фолиевая кислота играет большую роль в организме человека:
- участвует в развитии организма во внутриутробном периоде (способствует формированию нервной проводимости тканей, кровеносной системы плода, предупреждает развитие некоторых пороков развития);
- участвует в росте ребенка (например, в первый год жизни, в период полового созревания);
- влияет на процессы кроветворения;
- совместно с витамином В12 участвует в синтезе ДНК;
- препятствует образованию тромбов в организме;
- улучшает процессы регенерации органов и тканей;
- участвует в обновлении тканей (например, кожи).
Абсорбция (всасывание) фолатов в организме осуществляется в двенадцатиперстной кишке и в верхнем отделе тонкого кишечника.
При фолиеводефицитной анемии у больного наблюдается анемический синдром (такие симптомы как повышенная утомляемость, сердцебиение, бледность кожных покровов, снижение работоспособности). Неврологический синдром, а также атрофические изменения слизистой оболочки ротовой полости, желудка и кишечника при данном виде анемии отсутствуют.
Также у больного может наблюдаться увеличение размеров селезенки.
При общем анализе крови наблюдаются следующие изменения:
- гиперхромия;
- снижение уровня эритроцитов и гемоглобина;
- макроцитоз;
- лейкопения;
- тромбоцитопения.
В результатах биохимического анализа крови наблюдается снижение уровня фолиевой кислоты (менее 3 мг/мл), а также повышение непрямого билирубина.
При проведении миелограммы выявляется повышенное содержание мегалобластов и гиперсегментированных нейтрофилов.
Питание при фолиеводефицитной анемии играет большую роль, больному необходимо ежедневно потреблять продукты, богатые фолиевой кислотой.
Следует заметить, что при любой кулинарной обработке продуктов фолаты разрушаются приблизительно на пятьдесят процентов и более. Поэтому для обеспечения организма необходимой суточной нормой продукты рекомендуется употреблять в свежем виде (овощи и фрукты).
| Продукты питания | Наименование продуктов | Количество железа на сто миллиграмм |
| Продукты питания животного происхождения |
|
|
| Продукты питания растительного происхождения |
|
|
Медикаментозное лечение фолиеводефицитной анемии включает прием фолиевой кислоты в количестве от пяти до пятнадцати миллиграмм в сутки. Необходимую дозировку устанавливает лечащий врач в зависимости от возраста пациента, тяжести течения анемии и результатов исследований.
Профилактическая доза включает прием одного – пяти миллиграмм витамина в сутки.
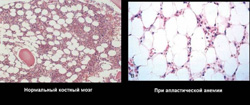
Апластическая анемия может быть врожденной или приобретенной.
Клинические проявления апластической анемии зависят от степени выраженности панцитопении.
При апластической анемии у больного наблюдаются следующие симптомы:
- бледность кожных покровов и слизистых;
- головная боль;
- учащенное сердцебиение;
- одышка;
- повышенная усталость;
- отеки на ногах;
- десневые кровотечения (вследствие снижения уровня тромбоцитов в крови);
- петехиальная сыпь (красные пятна на коже маленьких размеров), синяки на коже;
- острые или хронические инфекции (вследствие снижения уровня лейкоцитов в крови);
- изъязвления орофарингеальной зоны (поражается слизистая полости рта, язык, щеки, десна и глотка);
- желтушность кожных покровов (симптом поражения печени).
При биохимическом анализе крови наблюдается:
- повышение сывороточного железа;
- насыщение трансферрина (белок, переносящий железо) железом на 100%;
- повышение билирубина;
- повышение лактатдегидрогеназы.
При пункции красного мозга и последующем гистологическом исследовании выявляются:
- недоразвитие всех ростков (эритроцитарный, гранулоцитарный, лимфоцитарный, моноцитарный и макрофагальный);
- замещение костного мозга жировым (желтый костный мозг).
Среди инструментальных методов исследований больному может быть назначено:
- ультразвуковое исследование паренхиматозных органов;
- электрокардиография (ЭКГ) и эхокардиография;
- фиброгастродуоденоскопия;
- колоноскопия;
- компьютерная томография.
При правильно подобранном поддерживающем лечении состояние пациентов с апластической анемией существенно улучшается.
При лечении апластической анемии больному назначаются:
- иммунодепрессивные препараты (например, Циклоспорин, Метотрексат);
- глюкокортикостероиды (например, Метилпреднизолон);
- антилимфоцитарный и антитромбоцитарный иммуноглобулины;
- антиметаболиты (например, Флударабин);
- эритропоэтин (стимулирует образование эритроцитов и стволовых клеток).
Немедикаментозное лечение включает:
- трансплантацию костного мозга (от совместимого донора);
- переливание компонентов крови (эритроциты, тромбоциты);
- плазмаферез (механическое очищение крови);
- соблюдение правил асептики и антисептики с целью предотвращения развития инфекции.
Также при тяжелом течении апластической анемии больному может понадобиться хирургическое лечение, при котором производится удаление селезенки (спленэктомия).
В зависимости от эффективности проводимого лечения у больного при апластической анемии может наблюдаться:
- полная ремиссия (затухание или полное исчезновение симптомов);
- частичная ремиссия;
- клиническое улучшение;
- отсутствие эффекта от лечения.
|
|
|
|

Гемолитическая анемия может развиться вследствие наследственных или приобретенных заболеваний.
По локализации гемолиз может быть:
- внутриклеточным (например, аутоиммунная гемолитическая анемия);
- внутрисосудистым (например, переливание несовместимой крови, диссеминированное внутрисосудистое свертывание).
У пациентов с легкой степенью гемолиза уровень гемоглобина может быть нормальным, если производство эритроцитов соответствует темпу их разрушения.
Преждевременное разрушение эритроцита может быть связано со следующими причинами:
- внутренними мембранными дефектами эритроцитов;
- дефектами структуры и синтеза белка гемоглобина;
- ферментативными дефектами в эритроците;
- гиперспленомегалией (увеличение размеров печени и селезенки).
Наследственные заболевания могут вызвать гемолиз в результате отклонений мембраны эритроцита, ферментативных дефектов и отклонений гемоглобина.
Существуют следующие наследственные гемолитические анемии:
- энзимопатии (анемии, при которых наблюдается недостаток фермента, дефицит глюкозо-6-фосфатдегидрогеназы);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (эритроциты неправильной шарообразной формы);
- талассемия (нарушение синтеза полипептидных цепей, входящих в строение нормального гемоглобина);
- серповидно-клеточная анемия (изменение строения гемоглобина приводит к тому, что эритроциты принимают серпообразную форму).
Приобретенные причины гемолитической анемии включают иммунные и не иммунные нарушения.
Иммунные нарушения характеризуются аутоиммунной гемолитической анемией.
Не иммунные нарушения могут быть вызваны:
- ядохимикатами (например, пестициды, бензол);
- лекарственными средствами (например, противовирусные препараты, антибиотики);
- физическим повреждением;
- инфекциями (например, малярия).
Гемолитическая микроангиопатическая анемия приводит к производству фрагментированных эритроцитов и может быть вызвана:
- дефектным искусственным сердечным клапаном;
- диссеминированным внутрисосудистым свертыванием;
- гемолитическим уремическим синдромом;
- тромбоцитопенической пурпурой.
Симптомы и проявления гемолитической анемии разнообразны и зависят от вида анемии, степени компенсации, а также от того, какое лечение получал больной.
Следует заметить, что гемолитическая анемия может протекать бессимптомно, а гемолиз выявляться случайно во время обычного лабораторного тестирования.
При гемолитической анемии могут наблюдаться следующие симптомы:
- бледность кожи и слизистых;
- ломкость ногтей;
- тахикардия;
- учащение дыхательных движений;
- снижение артериального давления;
- желтушность кожных покровов (из-за увеличения уровня билирубина);
- на ногах могут наблюдаться язвы;
- гиперпигментация кожи;
- желудочно-кишечные проявления (например, боль в животе, нарушение стула, тошнота).
Следует заметить, что при внутрисосудистом гемолизе у больного наблюдается дефицит железа из-за хронической гемоглобинурии (наличие гемоглобина в моче). Вследствие кислородного голодания нарушается сердечная функция, что приводит к развитию у пациента таких симптомов как слабость, тахикардия, одышка и стенокардия (при тяжелой форме анемии). Из-за гемоглобинурии у больного также наблюдается потемнение мочи.
Длительный гемолиз может привести к развитию желчных камней вследствие нарушения обмена билирубина. При этом пациенты могут жаловаться на боль в животе и бронзовый цвет кожи.
В общем анализе крови наблюдается:
- снижение уровня гемоглобина;
- снижение уровня эритроцитов;
- увеличение ретикулоцитов.
При микроскопии эритроцитов выявляется их серпообразная форма, а также кольца Кебота и тельца Жолли.
В биохимическом анализе крови наблюдается повышение уровня билирубина, а также гемоглобинемия (увеличение свободного гемоглобина в плазме крови).
Также необходимо сдать анализ мочи на выявление наличия гемоглобинурии.
При пункции костного мозга наблюдается выраженная гиперплазия эритроцитарного ростка.
Существует много видов гемолитической анемии, поэтому лечение может отличаться в зависимости от причины, вызвавшей анемию, а также от типа гемолиза.
При лечении гемолитической анемии больному могут назначаться следующие препараты:
- Фолиевая кислота. Профилактическая доза фолиевой кислоты назначается, потому что активный гемолиз может потреблять фолат и впоследствии привести к развитию мегалобластоза.
- Глюкокортикостероиды (например, Преднизолон) и иммунодепрессанты (например, Циклофосфан). Данные группы препаратов назначаются при аутоиммунной гемолитической анемии.
- Переливание эритроцитарной массы. Больному индивидуально подбираются отмытые эритроциты, так как существует высокий риск разрушения перелитой крови.
Спленэктомия
Спленэктомия может быть первоначальным вариантом в лечении некоторых типов гемолитической анемии, таких как, например, наследственный сфероцитоз. В других случаях, например, при аутоиммунной гемолитической анемии, спленэктомия рекомендуется тогда, когда другие методы лечения потерпели неудачу.
Терапия препаратами железа
При гемолитической анемии применение препаратов железа в большинстве случаев противопоказано. Это связано с тем, что уровень железа при данной анемии не снижается. Однако если у больного наблюдается постоянная гемоглобинурия, то происходит существенная потеря железа из организма. Поэтому при выявлении дефицита железа пациенту может быть назначено соответствующее лечение.
Проявления анемии будут зависеть от следующих факторов:
- какое количество крови было потеряно;
- с какой скоростью происходит кровопотеря.
Симптомами постгеморрагической анемии являются:
- слабость;
- головокружение;
- бледность кожных покровов;
- сердцебиение;
- одышка;
- тошнота, рвота;
- сечение волос и ломкость ногтей;
- шум в ушах;
- мелькание мушек перед глазами;
- жажда.
При острой кровопотере у больного может развиться геморрагический шок.
Выделяют четыре степени геморрагического шока.
источник