Нарушение, развивающееся в организме и характеризующееся снижением общего количество гемоглобина и эритроцитов, называется анемией. При этом важным моментом является то, что если уменьшение количества гемоглобина является обязательным моментом, то уровень эритроцитов может оставаться в пределах нормальных показателей. Такое состояние не относится к самостоятельным заболеваниям, в большинстве случаев оно лишь указывает на какую-либо имеющуюся патологию в организме.
Эритроциты — это красные клетки крови. Их формирование происходит в области красного костного мозга под воздействием специфического вещества, которое называется эритропоэтином. Продолжительность жизни эритроцитарных клеток в обычном состоянии находится в пределах ста двадцати дней, после чего они подвергаются разрушению в структурах селезенки. Именно эритроциты отвечают за перемещение углекислого газа и кислорода в организме за счет имеющегося в них гемоглобина. Гемоглобин — это белок, придающий эритроцитарным клеткам красную окраску и имеющий в своем составе железо. Он способен захватывать молекулы кислорода и доставлять их к внутренним органам с током крови. От внутренних органов, в свою очередь, он забирает углекислый газ. В том случае, если развивается анемия, происходит постепенное возникновение тканевой гипоксии, которая сопровождается характерными симптомами.
Существует разделение анемий на несколько форм, которые выделяются на основании механизма их развития:
- Постгеморрагическая форма — обусловлена возникающей в организме кровопотерей, которая может иметь острый или хронический характер;
- Дефицитная форма — формируется в результате недостаточного поступления в организм определенных веществ, которые принимают непосредственное участие в образовании эритроцитов и гемоглобина;
- Гемолитическая форма — характеризуется повышенной скоростью разрушения эритроцитарных клеток;
- Апластическая форма — имеет место в том случае, если отмечается угнетение процесса кроветворения в структурах красного костного мозга.
Кроме этого, анемия классифицируется на три степени тяжести. Легкая степень сопровождается снижением уровня гемоглобина не ниже 90 грамм на литр. Средняя степень устанавливается в том случае, если показатель гемоглобина находится в диапазоне от 89 до 70 грамм на литр. Тяжелая степень характеризуется уровнем гемоглобина ниже 69 грамм на литр.
Как мы уже сказали, гемолитическая анемия представляет собой патологическое состояние, при котором в силу определенных причин происходит слишком быстрое разрушение эритроцитов. В результате такого разрушения отмечается высвобождение в кровь непрямого билирубина, что приводит к появлению желтухи.
Согласно статистике, такой патологический процесс встречается примерно у одного процента от всего населения. В нормальном состоянии жизненный цикл эритроцитов составляет от ста до ста двадцати дней. При данном нарушении эритроцитарные клетки погибают примерно через двадцать одни сутки или еще раньше.
Гемолитические анемии разделяются на врожденную разновидность и приобретенную разновидность. Врожденная разновидность имеет место в том случае, если у ребенка при рождении имеются различные нарушения со стороны структуры эритроцитов или гемоглобина. Кроме этого, в некоторых случаях уже при рождении отмечается недостаток определенных ферментов, которые отвечают за жизненный цикл эритроцитов.
Приобретенная разновидность наиболее часто развивается вследствие аутоиммунных нарушений в организме. Другими словами, собственный иммунитет начинает разрушать эритроциты. Помимо этого, в формировании такого патологического состояния могут играть роль отравление ядохимикатами и некоторыми видами лекарственных препаратов. В группе риска также находятся люди, систематически подвергающиеся избыточным физическим нагрузкам и перенесшие тяжелые инфекционные заболевания.
Гемолитическая анемия сопровождается бледной окраской кожи и видимых слизистых оболочек, а также желтухой. В некоторых случаях отмечается развитие гепатоспленомегалии. Больной человек предъявляет жалобы на учащение сердечных сокращений и появление одышки. Иногда присутствуют различные симптомы со стороны желудочно-кишечного тракта. Важным моментом является то, что люди с данным нарушением всегда испытывают повышенную слабость и быструю утомляемость.
Апластическая анемия формируется в результате того, что костный мозг в силу каких-либо причин начинает менее активно функционировать, что приводит к снижению количества синтезируемых эритроцитов. Такая патология характеризуется наиболее тяжелым течением, однако она встречается не так часто. Статистика утверждает о том, что ежегодно данное состояние диагностируется у двух человек на один миллион населения.
Возникновение апластической анемии может быть обусловлено различными генетическими дефектами. В этом случае мы говорим о врожденной разновидности. Если рассматривать причины приобретенной разновидности, то можно сказать о том, что свою роль здесь играют аутоиммунные процессы, перенесенные инфекции, прием некоторых видов лекарственных препаратов, отравление химическими соединениями, а также воздействие лучевого фактора.
Апластическая анемия характеризуется довольно быстро нарастающей общей слабостью и недомоганием, приступами головокружения и одышки. Отмечается бледность кожных покровов. Важным моментом при этой анемии является наличие геморрагического синдрома, который проявляется повышенной кровоточивостью десен, кровоизлияниями на коже, а также маточными и желудочно-кишечными кровотечениями. Очень часто к такому патологическому процессу присоединяются различные инфекционные осложнения.
Анемия, протекающая в апластической форме, лечится с помощью назначения курса иммуносупрессивной терапии. В сочетании с заместительными гемотрансфузионными мероприятиями это дает хороший эффект. При гемолитической форме могут использоваться глюкокортикостероиды и иммунодепрессивные препараты. В некоторых случаях показано удаление селезенки.
Принципы профилактики сводятся к исключению необоснованного назначения лекарственных препаратов, к избеганию контактов с агрессивными химическими веществами, а также к повышению иммунитета для предупреждения инфекционных заболеваний.
источник
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Гемолитическая анемия (ГА) — малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии— анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические — анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом — обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще — Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий — талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
источник
приобретенные
| Токсическая гемолитические яды, соединения мышьяка, свинца; возбудители инфекций: гемолитический стрептококк, малярийный плазмодий) | Иммунная (перелива-ние несов-местимой крови; Rh-несов-местимость крови матери и плода | Механическая (механическое повреждение эритроцитов при протезировании сосудов и клапанов сердца | Приобретенная (соматические мутации при образовании аутоантител против собственных эритроцитов под влиянием вирусов и лекарств с образованием патологических популяций эритроцитов с нарушенной мембраной |
Наследственная гемолитическая анемия— наследственный микросфероцитоз или болезнь Минковского-Шоффара. Неполноценность эритроцитов при болезни Минковского-Шоффара обусловлена генуинной недостаточностью синтеза АТФ, необходимого для поддержания двояковогнутой формы эритроцитов. При снижении содержания АТФ ниже 10 % от нормы эритроциты теряют ионы калия, в них поступает избыточное количество ионов Nа + и воды, эритроциты изменяют свою форму и превращаются в сфероциты. Кроме того, понижается их осмотическая резистентность, что связано с уменьшением содержания в мембране актомиозиноподобного белка, падением количества фосфолипидов и холестерина. Эритроциты живут 2-3 недели. Селезенка увеличена у всех больных, а печень — у половины пациентов.
Картина крови при наследственных гемолитических анемиях. Отмечается усиленная регенерация эритроцитарного ростка. При частых гемолитических кризисах может быть регенераторная анемия. В мазке крови, наряду с регенеративными формами (высокий ретикулоцитоз — до 50-60 %, полихроматофилия, ядерные формы эритроцитов), находится дегенеративно измененные эритроциты малого размера —
Отечная формахарактеризуется общими выраженными отеками, кожа плода бледная, полупрозрачная, в полостях тела — транссудат. Сердце, печень, селезенка значительно увеличены, почки полнокровны. Мягкая мозговая оболочка и ткань мозга отечны и полнокровны.
При анемической формевыражены общая бледность покровов и малокровие внутренних органов. В печени и селезенке — умеренный эритробластоз. Изменения головного мозга менее выражены, чем при отечной форме.
Желтушная формахарактеризуется желтухой покровов, подкожно-жирового слоя и интимы крупных сосудов. Количество непрямого биллирубина в сыворотке крови достигает 20-40 мг %. Ядра головного мозга прокрашены в охряно-желтый цвет. Тяжесть поражения усугубляется гипоксией из-за повреждений мелких сосудов.
Аналогично, но менее выраженно, протекает гемолитическая желтуха при несовместимости групп крови плода и матери.
Картина крови при приобретенных гемолитических анемиях. Приобретенная гемолитическая анемия может быть по типу кроветворения нормобластической, по регенераторной способности костного мозга — регенераторной, по цветовому показателю — нормо- или гиперхромной.
Степень уменьшения количества эритроцитов и гемоглобина зависит от интенсивности гемолиза. В мазке крови обнаруживают клетки физиологической регенерации и дегенеративно измененные эритроциты (пойкилоцитоз, анизоцитоз). Появление большого количества эритробластов и нормобластов характерно для гемолитической болезни новорожденных. Профилактика — обменное переливание крови отца или введение матери антирезусных антител.
Аутоиммунные гемолитические анемиивозникают при изменении антигенной структуры мембраны эритроцитов при переохлаждении, ожогах, инфекциях и действии лекарственных препаратов. В патогенезе главным является разрушение эритроцитов, образование аутоантител, стимуляция иммунного ответа и образуется порочный круг (самая опасная анемия). Лечение этого процесса — подавление иммунного ответа гормонами и иммунодепрессантами.
Патогенез и гематологическая характеристика. Гемолиз эритроцитов происходит внутри сосудов с образованием непрямого биллирубина. Развивается желтуха. Цветовой показатель может быть в норме или повышен. Размер эритроцитов — нормоциты и умеренный макроцитоз, пойкилоцитоз. Повышена регенерация эритроцитов, гипер- или нормохромия, повышена регенерация эритроцитов.
Анемии вследствие нарушения кровообразования. Витамин В12— и фолиеводефицитные анемии- это анемии, связанные с нарушением синтеза нуклеиновых кислот и заменой нормобластического типа кроветворения мегалобластическим из-за недостатка в организме витамина В12 и фолиевой кислоты.
В патогенезевитаминВ12-и-фолиеводефицитной анемии различают 3 основные ветви:
а) нарушение костномозгового кроветворения (что ведет к гипоксии);
б) нарушение миелинизации нервных волокон (нарушения чувствительности от парестезий до синдрома демиелинизации);
в) желудочно-кишечные (нарушение образования сосочков языка — глоссит, патология пристеночного пищеварения).
Дефицит витамина В12 и фолиевой кислоты, участвующих в образовании тимина, входящего в состав ДНК, снижает скорость ее образования. Нарушение клеточного деления приводит к формированию крупных клеток крови: мегалоцитов, мегалобластов, гигантских мегакариоцитов. Созревание мегалобластов до мегалоцитов сопровождается нарушением энуклеации — об этом свидетельствуют появление в мегалоцитах телец Жолли (остатки ядра) и колец Кебота (остатки ядерной оболочки). Наличие большого количества мегалобластов и мегалоцитов, насыщенных гемоглобином, обуславливает гиперхромию (ЦП>1,5).
Картина крови. Витамин В12-и-фолиеводефицитная анемия — это анемия мегалобластическая, гиперхромная, диспластическая, макроцитарная. В мазке крови появляются мегалобласты — клетки патологической регенерации костного мозга и мегалоциты (крупные клетки с базофильной, полихроматофильной или оксифильной цитоплазмой, для которых характерна ранняя гемоглобинизация). В крови встречается много дегенеративно измененных эритроцитов: пойкилоцитоз, анизоцитоз с микроцитозом, гипохромные эритроциты, мегалоциты с патологическими включениями. Уменьшается количество клеток физиологической регенерации (ретикулоциты, полихроматофилы), т.к. в костном мозге наблюдается раздражение эритроцитарного ростка с преобладанием мегалобластического типа кроветворения над нормобластическим. Наблюдается тромбоцитопения и лейкоцитопения с атипическими клетками.
Железодефицитная анемия (сидеропеническая) — это анемия, вызванная недостатком железа в организме в результате нарушения баланса между его поступлением, потреблением и потерей. Это самый распространенный вид анемии (80-90 % всех анемий). Недостаток железа в организме проявляется исчезновением гемосидерина в клетках печени и селезенки, снижением количества сидеробластов и сидероцитов в костном мозге. В крови уменьшается содержание сывороточного железа и степень насыщения им трансферрина (белка-переносчика железа), что ведет к снижению транспорта железа в костный мозг. Нарушается включение железа в эритроцитарные клетки, при этом снижается синтез гема и глобина, уменьшается активность некоторых ферментов в эритроцитах, что вызывает повышение их чувствительности к окислителям (т.к. неполноценность ферментативных процессов ведет к неустойчивости клеточных мембран), эритроциты подвергаются гемолизу под действием окислителей и продолжительность жизни эритроцитов уменьшается.
Картина крови. Железодефицитная анемия — это нормобластическая, гипохромная анемия (из-за недостаточной гемоглобинизации). В мазке крови наблюдается анизоцитоз (микроцитоз), пойкилоцитоз, шизоцитоз — обломки эритроцитов. Количество ретикулоцитов зависит от регенерирующей способности костного мозга (анемия может быть сначала регенераторной, а затем гипорегенераторной).
Железорефрактерная анемия —(рефрактерный — невосприимчивый)- сидероахрестическая, сидеробластическая, железонасыщенная анемия — обширная группа анемических состояний с высоким содержанием сывороточного железа, костномозговым сидеробластозом (отложение органических и неорганических соединений железа) и рефрактерностью к лечению железом. Анемии могут быть наследственными и приобретенными.
Этиология и патогенез связаны с нарушением активности ферментных систем, участвующих в биосинтезе гема. Наследственные анемии встречаются почти исключительно у мальчиков и молодых мужчин, приобретенные первичные формы чаще у пожилых лиц обоего пола, а вторичные — в любом возрасте.
Картина крови: выраженная анемия (возможно снижение гемоглобина до 3 г%, эритроцитов до 1 млн в микролитре). Процент ретикулоцитов в пределах нормы. Величина эритроцитов в норме или несколько завышена за счет макроцитов. Нередко отмечается клеточный диморфизм с наличием двух популяций эритроцитов: гипохромно-микроцитарной и нормохромно-макроцитарной. Лечение и прогноз зависит от формы анемии.
Не нашли то, что искали? Воспользуйтесь поиском:
источник
Вид работы: Контрольная
Формат работы: Word
Год сдачи: 2017г.
Работа сдавалась 1 раз
Предмет:
Медицина
Оценка работы:
Вы можете быть полностью уверены в том, что работа «Мегалобластический тип кроветворения при гемолитических анемиях обусловлен» является уникальной, исключающей плагиат и дублирование, использование данной работы (Контрольная) не может вызвать проблем при последующей сдаче и защите.
Ответ к тесту
661. Д
662. В
663. А
664. Д
665. А
666. Г
667. Д
668. Д
669. Г
670. А
671. Г
672. Д
673. Г
674. Г
675. Б
676. В
677. А
678. В
679. Г
680. Д
661. Цитохимические исследования бластных клеток позволяют установить:
А) принадлежность их к определенным клеточным линиям гемопоэза
Б) степень дифференцировки бластных клеток
В) принадлежность клеток к опухолевому клону
Г) все перечисленное
Д) нет правильного ответа
662. Иммунофенотипирование бластных клеток позволяет определить:
А) принадлежность их к определенным клеточным линиям гемопоэза
Б) степень дифференцировки бластных клеток
В) принадлежность клеток к опухолевому клону
Г) все перечисленное
Д) верны пункты А и Б
663. Среднее содержание гемоглобина в эритроците повышено при:
А) мегалобластной анемии
Б) железодефицитной анемии
В) анемии при злокачественных опухолях
Г) все перечисленное верно
Д) все перечисленное неверно
664. Средний объем эритроцита увеличен:
А) железодефицитная анемия
Б) талассемия
В) гемоглобинопатии
Г) В12- дефицитная анемия
Д) все перечисленное верно
665. Анизоцитоз эритроцитов отмечается при:
А) макроцитарной анемии
Б) миелодиспластическом синдроме
В) железодефицитной анемии
Г) метастазах новообразований в костный мозг
Д) все перечисленное верно
666. Для В12 – дефицитных анемий характерны:
А) тромбоцитоз
Б) анизохромия
В) нейтрофильный лейкоцитоз со сдвигом влево
Г) лейкопения с нейтропенией и относительным лимфоцитозом
Д) все перечисленное
667. Причиной гиперсегментации нейтрофилов не может быть:
А) дефицит фолиевой кислоты
Б) дефицит витамина В-12
В) наследственные аномалии сегментации нейтрофилов
Г) дефицит железа
Д) хронический миелолейкоз
668. Для выявления зернисто-сетчатой субстанции ретикулоцитов рекомендуется краситель:
А) бриллиант — крезиловый синий
Б) азур 1
В) азур 2
Г) метиленовый синий
Д) все перечисленное верно
669. Резкое снижение количества миелокариоцитов в костном мозге наблюдается при:
А) анемии Фанкони
Б) цитостатической болезни
В) миелотоксическом агранулоцитозе
Г) всех перечисленных болезнях
Д) ни при одном из перечисленных
670. Признаками мегалобластического кроветворения могут наблюдаться при:
А) аутоиммунной гемолитической анемии
Б) эритромиелозе
В) дифиллоботриозе
Г) раке желудка
Д) всех перечисленных заболеваниях
671. Мегалобластический тип кроветворения при гемолитических анемиях обусловлен:
А) дефицитом витамина В12
Б) нарушением кишечной абсорбции витамина В12 и фолиевой кислоты
В) В12 – ахрестическим состоянием
Г) повышенной потребностью в фолиевой кислоте или витамине В-12 из-за с интенсивного эритропоэза
Д) всеми перечисленными причинами
672. Белковой частью гемоглобина является:
А) альбумин
Б) трасферрин
В) церулоплазмин
Г) глобин
Д) гаптоглобин
673. У взрослого человека можно получить методом электрофореза виды гемоглобинов:
А) Hb H и Hb F
Б) Hb A, Hb A-2, Hb F
В) Hb A, Hb E
Г) Hb S, Hb A, Hb F
Д) Hb A, Hb D, Hb S
674. Основным типом гемоглобина взрослого человека является:
А) Hb P
Б) Hb F
В) Hb A
Г) Hb S
Д) Hb D
675. Патологическим типом гемоглобина не является:
А) Hb F
Б) Hb S
В) Hb M
Г) Hb C
Д) все перечисленное
676. Аномальным гемоглобином называется:
А) гемоглобин с измененной структурой гема
Б) гемоглобин с включением липидов
В) гемоглобин с измененной структурой глобина
Г) гемоглобин со снижением сродства к кислороду
Д) гемоглобин с увеличением сродства к кислороду
677. Синтез в эритроцитах гемоглобина «S» сопровождается развитием:
А) апластической анемии
Б) гипохромной анемии
В) мегалобластной анемии
Г) серповидно-клеточной анемии
Д) нормохромной анемии
678. Для эритроцитов с аномальным гемоглобином характерно:
А) изменение сродства к кислороду
Б) изменение резистентности эритроцитов
В) изменение растворимости гемоглобина
Г) снижение устойчивости на внешние факторы
Д) все перечисленное
679. Талассемия – это:
А) качественная гемоглобинопатия
Б) наличие аномального гемоглобина
В) количественная гемоглобинопатия
Г) структурная гемоглобинопатия
Д) гемоглобинобинурия
680. При бета-талассемии наблюдается:
А) увеличение синтеза бета-цепей глобина
Б) снижение синтеза бета-цепей глобина
В) увеличение синтеза гамма-цепей глобина
Г) снижение синтеза альфа-цепей глобина
Д) снижение синтеза гемоглобина
Цены на готовые работы 2017 года
Контрольная — 30 бел.руб.
Курсовая — 60 бел.руб.
Дипломная — 150 бел.руб.
План быстрого получения работы:
шаг 1. Нажать на кнопку «Заказать» и в открывшемся окне заполните ваши данные;
шаг 2. На ваш email адрес вы получите письмо с указанием методов оплаты;
шаг 3. После оплаты (в отделении банка, карточкой или электронным платежем) отпишитесь нам и через 2-4 часа получаете на ваш адрес оплаченную работу.
Наши контакты (Беларусь):
+(375)-29-290-0487 (MTS)
+(375)-25-788-2562 (Life)
время работы с 12.00ч. до 19.00ч.
Данная работа Мегалобластический тип кроветворения при гемолитических анемиях обусловлен (Контрольная) по предмету (Медицина), была выполнена по индивидуальному заказу специалистами нашей компании и прошла свою успешную защиту. Работа — Мегалобластический тип кроветворения при гемолитических анемиях обусловлен по предмету Медицина отражает свою тему и логическую составляющую ее раскрытия, раскрыта сущность исследуемого вопроса, выделены основные положения и ведущие идеи данной темы.
Работа — Мегалобластический тип кроветворения при гемолитических анемиях обусловлен, содержит: таблицы, рисунки, новейшие литературные источники, год сдачи и защиты работы – 2017 г. В работе Мегалобластический тип кроветворения при гемолитических анемиях обусловлен (Медицина) раскрывается актуальность темы исследования, отражается степень разработанности проблемы, на основании глубокой оценки и анализе научной и методической литературы, в работе по предмету Медицина рассмотрен всесторонне объект анализа и его вопросы, как с теоретической, так и практической стороны, формулируется цель и конкретные задачи рассматриваемой темы, присутствует логика изложения материала и его последовательность.
Для получения работы или по возникшим вопросам относительно данной работы Мегалобластический тип кроветворения при гемолитических анемиях обусловлен нажмите по кнопке Заказать работу и заполните все поля формы. Большая просьба, аккуратно заполнять и указывать все данной (ВУЗ, страну, email и телефон), ваши пожелания и требования к работе. При написании данной работы (Мегалобластический тип кроветворения при гемолитических анемиях обусловлен) используется только свежая литература. Научный подход и профессионализм работников нашей компании позволяют провести качественное выполнение работы Мегалобластический тип кроветворения при гемолитических анемиях обусловлен, в результате чего полученные работы защищают на «отлично».
Если вас не устраивает само содержание или структура работы: Мегалобластический тип кроветворения при гемолитических анемиях обусловлен по предмету (Медицина) обращайтесь, работа изменяется и оформляется под ВУЗ полностью бесплатно. Наши специалисты проконсультируют вас по любому вопросу, связанным с данной работой по телефону или e-mail.
Контрольная — Мегалобластический тип кроветворения при гемолитических анемиях обусловлен оформлена по ГОСТу и готова к распечатке и сдаче на кафедру.
Оплатить работу (Контрольная — Мегалобластический тип кроветворения при гемолитических анемиях обусловлен) можно через: почтовое отделение, банк или электронным платежом, для всех жителей Беларуси и России.
Работа высылается в среднем по истечении 2-4 часа после оплаты и получении от Вас e-mail с реквизитами оплаты.
Расценки соответственно: контрольная работа или тесты – 30 руб, курсовая работа – 60 руб., диплом – 150 руб. Все реквизиты будут указанны в ответном письме.
Консультирование и объяснения по выполненной дипломной или курсовой работе производится на бесплатной основе.
Все наши гарантии относительно работы Мегалобластический тип кроветворения при гемолитических анемиях обусловлен по предмету Медицина (Контрольная) служат для одной цели — чтобы Вы были уверенны в том, что обратившись к нам в компанию получите желаемый результат и высокую оценку.
источник
- Наследственная форма гемолитической анемии, обусловленная нарушением мембраны эритроцитов
- Наследственная форма гемолитической анемии, обусловленная нарушением активности ферментов эритроцитов
- Наследственная форма гемолитической анемии, обусловленная нарушением синтеза или структуры гемоглобина
- Анемия, обусловленная влиянием антител
- Анемия, обусловленная изменением структуры мембраны, вызванной соматической мутацией
- Анемия, обусловленная механическим повреждением оболочки эритроцитов
- Анемия, вызванная химическим повреждением эритроцитов
- Анемия, вызванная дефицитом витаминов (фолиевой кислоты и цианокобаламина)
- Анемия, вызванная разрушением эритроцитов паразитами
Болезнь Минковского-Шоффара (наследственный микросфероцитоз) – группа наследственных гемолитических анемий, характеризующихся образованием микросфероцитов (шаровидных эритроцитов) и обусловленных дефектом протеинов цитоскелета эритроцитов. При этом эритроциты теряют часть мембраны, уменьшается соотношение площади поверхности к объему, в результате чего эритроцит превращается в микросфероцит. Как правило, патология наследуется по аутосомно-доминантному признаку. Распространенность наследственного микросфероцитоза составляет примерно 1 случай на 1000-4500 человек.
При наследственном микросфероцитозе генетические нарушения влияют на протеины цитоскелета, преимущественно на те, которые объединяют цитоскелет с мембраной эритроцита. У большинства больных отмечается значительный дефицит спектрина, и только в некоторых случаях этот дефицит обусловлен генетическими дефектами самого спектрина.
Главные признаки наследственного микросфероцитоза – анемия, желтуха, спленомегалия (увеличенная селезенка). Анемия возникает из-за внутриклеточного распада эритроцитов. Желтуха развивается посредством непрямой гипербилирубинемии, может быть непостоянной и, как правило, слабо выражена у детей раннего возраста. Повышенное содержание билирубина в желчи часто является причиной образования пигментных желчных камней (даже у детей). Увеличение селезенки (спленомегалия) отмечается практически во всех случаях. При системных инфекционных патологиях интенсивность гемолиза может увеличиваться, в результате чего развивается спленомегалия.
Тяжелые формы наследственного микросфероцитоза характеризуются деформацией скелета: изменение расположения зубов, акрокефалия (башенный череп), высокое верхнее небо, микрофтальмия (уменьшение глазного яблока). В некоторых случаях отмечаются укороченные мизинцы. Могут образовываться трофические язвы на ногах.
Наследственный микросфероцитоз сопровождается апластическими кризами, которые провоцируются инфекцией (особенно парвовирусной).
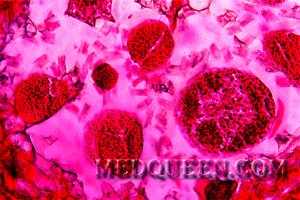
Микросфероцитоз – характерное изменение формы эритроцитов при этой патологии. При анализе мазка крови в биологическом материале наблюдаются микросфероциты в виде мелких клеток без центрального просветления (см рисунок 1). Отметим, что обнаружение микросфероцитов в мазках не всегда является признаком наследственного сфероцитоза.
Рисунок 1. Наследственный микросфероцитоз. Микросфероциты в мазке периферической крови (окр. по Романовскому-Гимзе, ув. ×100)
Такой признак обнаруживается при аутоиммунной гемолитической анемии с неполными тепловыми агглютинами, при наследственных дизэритропоэтической анемии. Средний объем эритроцитов, как правило, остается в норме или незначительно снижен. Показатель среднего содержания гемоглобина в эритроцитах в норме или незначительно повышен. Средняя концентрация гемоглобина в эритроцитах повышена почти у 50% пациентов.
Количественным показателем сферичности эритроцитов является осмотическая устойчивость (она снижена). Уровень ретикулоцитов в крови при гемолитическом кризе может значительно повышаться. Миелограмма показывает резкое раздражение красного ростка. Дифференциальный диагноз проводят с аутоиммунной гемолитической анемией, для которой характерна положительная проба Кумбса, отсутствие этой патологии среди родственников пациента и отсутствие данных о начале заболевания в детском возрасте.
Основной метод лечения анемии при наследственном микросфероцитозе – спленэктомия, с помощью которой устраняется анемия; при этом нельзя устранить морфологический дефект эритроцитов.
Наследственная гемолитическая анемия, обусловленная дефицитом глюкозо-6-фосфат дегидрогеназы эритроцитов – наиболее распространенная ферментопатия эритроцитов из группы ферментопатий пентозофосфатного пути метаболизма глюкозы. Глюкозо-6-фосфатдегидрогеназа эритроцитов – олигомер (в зависимости от условий может быть димер или тетрамер), который состоит из субъединиц с молекулярной массой 56 000 D. По данным ВОЗ (Всемирной организации здравоохранения) во всем мире количество людей, страдающих этой патологией, составляет более 200 млн. Наиболее широкое распространение этого заболевания характерно для Средиземноморского региона (Сицилия, Греция, Сардиния), негроидной расы, жителей Ближнего и Дальнего востока.
Клиническая картина при наследственной форме гемолитической анемии полиморфна: степень тяжести патологии может колебаться от гемолитической анемии, возникающей спонтанно после рождения, до гемолитических кризов. Гемолитический криз, который может провоцироваться метаболическим ацидозом или гипогликемией, развивается за несколько часов. В тяжелых случаях у больного развивается гемоглобинурия и шок. Также наблюдаются желтуха, моча приобретает бурый или черный цвет, одышка, диарея, рвота, снижение артериального давления, развивается тяжелая анемия, увеличиваются печень (гепатомегалия) и селезенка (спленомегалия).
Тяжелый гемолитический криз может спровоцировать развитие ДВС-синдрома (диссеминированного внутрисосудистого свертывания крови). Некоторые пациенты не переносят конские бобы (Viciafaba), после употребления которых происходит молниеносное развитие гемолитического криза (это явление также известно, как фовизм или примахиновая анемия).
Дефицит глюкозо-6-фосфат дегидрогеназы эритроцитов необходимо подозревать во всех случаях острого гемолиза, особенно у лиц негроидной расы и жителей средиземноморского региона. Диагноз подтверждается путем проведения лабораторных анализов. Острый гемолиз характеризуется быстрым снижением гематокрита с одновременным повышением уровня гемоглобина и непрямого гемоглобина, а также снижением уровня гаптоглобина. Анализ мазка крови показывает наличие фрагментов эритроцитов. Основой диагностики считается качественное (при необходимости – количественное) определение активности глюкозо-6-фосфат дегидрогеназы эритроцитов. У пациентов с вариантом «А-» явление аномального гемолиза проходит, как правило, самостоятельно – такие больные не нуждаются в специальном лечении. В случае развития тяжелого гемолитического криза необходимо проводить форсированный диурез, профилактику ДВС-синдрома, плазмаферез (с целью удаления продуктов гемолиза).
В случае возникновения качественной гемоглобинопатии происходит изменение аминокислотной последовательности цепей глобина. Талассемия (количественная гемоглобинопатия) характеризуется снижением образования цепей глобина без изменения их цепей. Нужно отметить, что разница между качественной и количественной гемоглобинопатиями не абсолютна.
Талассемия (анемия Кули) – группа патологий, обусловленных генетическим нарушением синтеза одной из цепей глобина. В норме процесс синтеза глобиновых цепей сбалансирован, поэтому свободных цепей глобина нет. В случае нарушения синтеза одной из цепей глобина баланс нарушается, образуются лишние цепи, которые агрегируют и откладываются в эритрокариоцитах. Среди жителей Средиземноморья наиболее распространена β-талассемия.
«Большая талассемия» (болезнь Кули, β-талассемия) – наследственная гемолитическая анемия, впервые описанная американскими педиатрами-гематологами Томасом Бентоном Кули (Thomas Benton Cooley) и Ли (P. Lee) в статье «Серия случаев спленомегалии у детей с анемией и необычными изменениями костей» («A Series of Cases of Splenomegaly in Children, with Anemia and Peculiar Bone Changes»), где были приведены случаи у выходцев из стран Средиземноморья. Для анемии Кули характерна тяжелая степень течения с самого детства, задержка роста и изменения костей в результате увеличения объема костного мозга, возникающие в случае отсутствия соответствующего лечения). Также при этой патологии у больного наблюдаются гепатомегалия, спленомегалия, гиперспленизм, деформации черепа (монголоидное лицо, башенный череп); желтуха, бледность и отложение меланина придают коже особый медный оттенок. Кроме этого, наблюдается перегрузка железом сердца, легких, печени, поджелудочной железы и других органов эндокринной системы, переломы костей, сдавления периферических нервов, разного рода инфекционные осложнения.
Результаты лабораторных исследований периферической крови показывают гипохромную анемию, ретикулоцитоз, мишеневидные эритроциты (см рис 2-4).
Рисунок 02. Анемия Кули (большая талассемия). Периферическая кровь. Микроцитоз, выраженная гипохромия, мишеневидные нормобласты и эритроциты (окр. по Романовскому-Гимзе, ув. ×100)
Рисунок 03. Анемия Кули (большая талассемия). Периферическая кровь (окр. по Романовскому-Гимзе, ув. ×50)
Рисунок 04. Анемия Кули (большая талассемия). Периферическая кровь. Множественные мишеневидные эритроциты (окр. по Романовскому-Гимзе, ув. ×100)
Миелограмма демонстрирует раздражение «красного ростка» и повышение количества сидеробластов. Также наблюдается повышение осмотической резистентности эритроцитов и количества билирубина за счет непрямой фракции. В крови повышается содержание железа и ферритина, развивается гемосидероз (чрезмерное отложение гемосидерина в тканях) внутренних органов. При гомозиготной β-талассемии необходимо проводить пренатальную диагностику – забор клеток плода из амниотической жидкости на предмет выявления мутации генов, отвечающих за кодирование β-цепи глобина, с применением метода полимеразной цепной реакции.
Без соответствующего лечения больные анемией Кули умирают в детском возрасте. Продлить жизнь, предупредить деформации костей и задержку роста можно путем регулярных трансфузий эритроцитарной массы (лучше переливать отмытые или размороженные эритроциты) при условии поддержания достаточно высокого уровня гемоглобина. В случае значительной спленомегалии и явлениях гиперспленизма больному показана спленэктомия (удаление селезенки). С целью предотвращения развития гемосидероза пациентам периодически назначают Деферазирокс (Эксиджад) или Дефероксамин (Десферал). Излечение возможно при аллогенной трансплантации костного мозга.
Серповидноклеточная анемия обусловлена носительством гемоглобина, который меняет свою структуру в условиях гипоксии. Самой распространенной аномалией структуры гемоглобина является гемоглобинопатия Sα2β26 глу+вал. При гомозиготном носительстве можно говорить о серповидноклеточной анемии; при гетерозиготном носительстве – серповидноклеточная аномалия. Патология наследуется по аутосомно-доминантному признаку. При серповидноклеточной анемии наблюдается мутация, в результате которой в цепи глобина глутаминовая кислота заменяется валином. В результате растворимость гемоглобина S при отдаче кислорода снижается, что приводит к образованию геля.
Серповидноклеточная анемия наиболее распространена среди населения Центральной Африки, Турции, Индии, Кубы. У больных диагностируется анемия, тромботические осложнения, поражения костей и суставов (отмечаются некрозы плечевой и бедренной костей). Кроме этого, тромбозы осложняются инфарктами (сердца, легких, почек, селезенки, головного мозга), приступами сильной боли в области живота. У детей отмечаются нарушения физического (отставание в росте) и полового развития, ночное недержание мочи, нарушение зрения (тромбозы сосудов сетчатки). Также могут развиваться гемолитический, апластический и секвестрационные кризы, при этом в селезенке происходит резкое накопление эритроцитов, что вызывает гиповолемический шок и резкое снижение уровня гемоглобина.
Для анализов крови при апластической анемии характерны низкий уровень гемоглобина, наличие серповидных эритроцитов (рисунок 5), базофильная пунктация эритроцитов, их мишеневидность, повышение уровня ретикулоцитов и непрямого билирубина. Миелограмма демонстрирует раздражение «красного ростка».
Рисунок 5. Серповидноклеточная анемия. Периферическая кровь. Серповидные и мишеневидные эритроциты. выраженная гипохромия эритроцитов (окр. по Романовскому-Гимзе, ув. ×100)
В качестве лечения применяют адекватную инфузионную терапию, переливания эритроцитарной массы, оксигенотерапии.
К приобретенным гемолитическим анемиям относится группа заболеваний разного патогенеза, которые объединяет внутрисосудистый гемолиз (гемолиз эритроцитов в периферической крови). В зависимости от механизма эритролиза приобретенная гемолитическая анемия может носить иммунный и неиммунный характер. Но, несмотря на разные патогенетические механизмы, клинические признаки этих анемий часто совпадают.
Гемолитическая анемия у пациентов с протезированными клапанами сердца и сосудами развивается примерно в 10% случаев при протезированном аортальном клапане. При использовании стеллитовых запирательных элементов частота гемолиза незначительно увеличивается (по сравнению с селиконовыми). Также некоторое увеличение частоты гемолиза отмечается при наличии околоклапанной регургитации и при малом диаметре клапана. Биопротезы (свиные клапаны) в редких случаях являются причиной механического гемолиза. Гораздо реже причиной гемолиза может быть также протезированный митральный клапан, так как трансклапанный градиент давления в этом случае ниже.
Гемолиз протезированными клапанами происходит в результате одновременного действия сразу нескольких факторов:
- Значительная сила сдвига, которая при турбулентном токе крови действует на мембрану эритроцитов, особенно когда под высоким давлением кровь проходит через маленькое отверстие (например, при околоклапанной регургитации)
- Отложения фибрина на участках неплотного прилегания кольца клапана к тканям сердца
- Прямое механическое повреждение эритроцитов при закрытии запирательного элемента
Значительное разрушение эритроцитов может наблюдаться после закрытия дефекта межпредсердной перегородки типа ostium primum заплатой из синтетического материала. Умеренное сокращение жизни эритроцитов с легкой анемией или без нее может наблюдаться при значительном обызвествлении аортального клапана. Механический гемолиз обнаруживается также у пациентов, перенесших аортокоронарное и аортобедренное шунтирование.
Тяжелые случаи механического гемолиза сопровождаются тяжелой анемией, ретикулоцитозом, обнаруживаются фрагментированные эритроциты (шизоциты), гемоглобинемия и гемоглобинурия, повышается активность лактатдегидрогеназы, снижается уровень гаптоглобина. Выведение железа из организма с мочой в виде гемосидерина или гемоглобина может вызвать дефицит железа в организме. В случае развития дефицита железа пациенту назначается пероральный прием препаратов железа. Терапия препаратами железа способствует повышению уровня гемоглобина и способствует снижению сердечного выброса и снижению интенсивности гемолиза. Отметим, что ограничение физической активности также способствуют снижению интенсивности распада эритроцитов. Если предпринимаемые меры не приводят к желаемому результату, нужно полностью устранить околоклапанную регургитацию или заменить протез.
источник
Гемолитическая анемия — анемия, возникающая, когда разрушение эритроцитов преобладает над их образованием.
Классификация. По этиологии гемолитические анемии подразделяются на приобретенные и наследственные. В свою очередь в зависимости от этиологических факторов, вызвавших гемолиз эритроцитов, приобретенные гемолитические анемии делятся на токсические, обусловленные действием экзогенных и эндогенных гемолитических ядов; иммунные (гетеро-, изо-, аутоиммунные), когда гемолиз происходит под влиянием комплекса антиген — антиэритроцитарное антитело; механические— при механическом повреждении эритроцитов; мембранопатии, связанные с соматической мутацией пролиферирующих клеток эритроцитарного ряда и образованием популяции эритроцитов с дефектом структуры мембраны.
На основании того, какие генетические нарушения привели к усилению гемолиза эритроцитов, наследственные гемолитические анемии подразделяют на наследственные мембранопатии, ферментопатии и гемоглобинопатии, вызванные генетическими дефектами структуры мембраны, активности ферментов эритроцитов и синтеза гемоглобина. Имеется две разновидности наследственных гемоглобинопатий: анемии, связанные с нарушением синтеза цепей глобина, и анемии, обусловленные наследственным дефектом первичной структуры цепей глобина.
Этиология приобретенных гемолитических анемий. Токсическая гемолитическая анемия может развиться под влиянием гемолитических ядов (соединения мышьяка, свинца, нитробензол, фенилгидразин; алкоголь, желчные кислоты, токсические продукты азотистого обмена; змеиный, грибной, пчелиный яды и др.), а также при действии возбудителей инфекционных и паразитарных заболеваний (гемолитический стрептококк, анаэробная инфекция, малярийный плазмодий, лейшмания).
Иммунная (гетеро-, изо-, аутоиммунная) гемолитическая анемия развивается при переливании несовместимой крови; резус-несовместимости матери и плода; образовании аутоантител против собственных эритроцитов при изменении их антигенных свойств под влиянием лекарственных препаратов, вирусов, МО или в результате соматической мутации иммуноцитов, когда возникает «запретный» клон лимфоцитов, продуцирующих антитела к нормальным антигенам эритроцитов (при лейкозе, системной красной волчанке и др.).
Механическое повреждение эритроцитов может возникнуть при протезировании кровеносных сосудов и клапанов сердца, длительном марше или беге по твердому грунту (маршевая гемоглобинурия), спленомегалии.
Причиной приобретенной мембранопатии может стать соматическая мутация эритробластов под действием вирусов, МО, лекарственных препаратов с образованием
патологической популяции эритроцитов, у которых нарушается структура мембраны и повышается чувствительность к комплементу (паро- ксизмальная ночная гемоглобинурия).
Патогенез. Механизм гемолиза при приобретенной гемолитической анемии заключается в повреждении структуры мембран эритроцитов. Одни гемолитические факторы (например, механические) оказывают прямое повреждающее действие, другие (мышьяковистый водород, нитриты), являясь сильными окислителями, вызывают сначала метаболические, а затем функциональные и структурные изменения в мембране и строме эритроцитов, приводящие к их гемолизу. Многие гемолитические яды биологического происхождения обладают ферментной активностью (лецитиназная активность стрепто-, стафилолизинов, яда насекомых и змей), разрушая лецитин мембран. При иммунных гемолитических анемиях IgG и IgM присоединяют к эритроцитарной мембране комплемент, который при этом активируется и вызывает ее ферментативный лизис.
Под влиянием гемолитических агентов в мембранах эритроцитов образуются поры, через которые из клетки выходят ионы калия, фосфаты, а ионы натрия поступают в клетку. Вследствие сдвигов ионного баланса вода проникает в эритроцит, который при этом набухает, приобретает сферическую форму, его клеточная поверхность уменьшается, снижается способность к деформации. Такие сфероциты не могут пройти через межэндотелиальные поры синусов селезенки и фагоцитируются селезеночными макрофагоцитами. Когда объем эритроцита достигает критического (146 % первоначального), а размер пор мембраны превышает 6 нм, наступает гемолиз с выходом гемоглобина в плазму.
Гемолиз эритроцитов при приобретенных гемолитических анемиях происходит преимущественно в кровеносном русле. Однако при резус- конфликте (гемолитическая болезнь новорожденных) антирезусные агглютинины, образовавшиеся в организме резус-отрицательной матери, вызывают гемолиз резус-положительных эритроцитов плода или новорожденного не только внутри сосудов, но и в печени и селезенке (внутриклеточный гемолиз).
При наследственной гемолитической анемии гемолиз обусловлен снижением осмотической и механической резистентности эритроцитов с генетически детерминированными нарушениями структуры мембраны, метаболизма, синтеза гемоглобина.
Так, при наследственной мембранопатии (микросфероцитарная гемолитическая анемия или болезнь Минковского—Шоффара с аутосомно-доминантным наследованием) генетический дефицит в мембране эритроцитов Са п -зависимой АТФазы и фосфолипидов приводит к повышению проницаемости мембраны. В клетки поступают ионы натрия и вода, эритроциты превращаются в сфероциты с резко пониженной способностью деформироваться при прохождении через синусы селезенки. Отрыв части оболочки у таких эритроцитов ведет к образованию микросфероцитов с укороченной продолжительностью жизни (8 — 14 дней вместо 120 дней в норме) в связи с захватом их макрофагоцитами селезенки и печени (внутриклеточный гемолиз).
При наследственной ферментопатии, например глюкозо-6- фосфатдегидрогеназодефицитной анемии (доминантное, сцепленное с X- хромосомой наследование), острый внутрисосудистый гемолиз эритроцитов, возникающий при приеме лекарств с высокой окислительной способностью (противомалярийные препараты, фтивазид и др.), обусловлен повреждением клеточных мембран перекисями, так как в эритроцитах с дефицитом Г-6-ФДГ понижено содержание восстановленного глутатиона (антиоксиданта).
Внутриклеточный гемолиз эритроцитов при наследственной гемоглобинопатии связан с синтезом аномального или не свойственного данному возрасту гемоглобина. Так, при серповидно- клеточной анемии образуется HbS (в (3-цепи глобина глутаминовая кислота заменена валином), который в восстановленном состоянии выпадает в кристаллы и вызывает деформацию эритроцитов (серповидная форма); гипоксия способствует усилению гемолиза таких эритроцитов. Следствием массивного гемолиза эритроцитов является анемия с нарушением дыхательной функции крови и развитием гипоксии. Образовавшийся при распаде эритроцитов гемоглобин циркулирует в крови (гемоглобинемия) и соединяется с гаптоглобином в крупномолекулярный комплекс, не проходящий через почечный фильтр. Если же содержание свободного гемоглобина в плазме превышает 20,9 ммоль/л (337 г/л) или исходный уровень гаптоглобина низкий, тогда не связанный с последним гемоглобин начинает выделяться с мочой (гемоглобинурия). Частично гемоглобин поглощается клетками макрофагоцитарной системы и расщепляется в них до гемосидерина. Гемосидероз селезенки, почек, печени, костного мозга сопровождается реактивным разрастанием соединительной ткани и нарушением функций этих органов. Повышенное образование из гемоглобина желчных пигментов обусловливает развитие гемолитической желтухи. Кроме того, внутрисосудистый распад эритроцитов может привести к появлению тромбов и нарушению кровоснабжения тканей, отсюда — трофические язвы конечностей, дистрофические изменения в селезенке, печени, почках. В результате поступления в сосудистое русло большого количества эритроцитарного тромбопластина возможно развитие ДВС-синдрома.
Картина крови. Приобретенная гемолитическая анемия по типу кроветворения является эритробластической, по степени регенерации костного мозга — регенераторной, по цветовому показателю — нормо- или гипохромной, реже — ложногиперхромной (вследствие абсорбции гемоглобина на эритроцитах). Степень уменьшения количества эритроцитов и гемоглобина зависит от интенсивности гемолиза. В мазке крови обнаруживаются клетки физиологической регенерации и дегенеративно измененные эритроциты (пойкилоцитоз; разорванные, фрагментированные эритроциты, анизоцитоз). Появление большого количества эритробластов и нормобластов характерно для гемолитической болезни новорожденных.
При наследственной гемолитической анемии отмечается усиленная регенерация эритроцитарного ростка часто с неэффективным эритропоэзом, когда в костнбм мозге разрушаются ядерные формы эритроцитов. В мазке крови наряду с регенеративными формами (высокий ретикулоцитоз, полихроматофилия, единичные ядерные формы эритроцитов) находятся дегенеративно измененные клетки (микросферо- циты при болезни Минковского — Шоффара, серповидные при S- гемоглобинопатии, мишеневидные, базофильно пунктированные — при талассемии). При частых гемолитических кризах может возникнуть гипорегенераторная анемия.
источник