ЖДА — заболевание, обусловленное истощением запасов железа в организме, что влечет за собой нарушение синтеза железосодержащих белков.
Заболевание проявляется снижением концентрации гемоглобина в крови и трофическими расстройствами в тканях.
По МКБ-10 D50 Железодефицитная анемия.
Эпидемиология. По данным экспертов ВОЗ, на земном шаре 700—800 млн человек страдают ЖДА или скрытым дефицитом железа.
Этиология.
Основные причины возникновения ЖДА:
1. Хронические и острые кровопотери (гиперполименорея, язвенная болезнь желудка, ДПК; опухоли желудка; опухоли тонкой кишки; опухоли толстой кишки; грыжа пищеводного отверстия диафрагмы; эзофагит; эрозивный гастрит; болезнь Крона; дивертикулез; геморрой, донорство). 2. Повышенная потребность в железе: период роста детей и подростков, беременные и кормящие женщины.
3. Нарушения всасывания железа в тонком кишечнике, аутоиммунный атрофический гастрит.
4. Алиментарные ЖДА развиваются при уменьшении в пищевом рационе продуктов, содержащих железо.
Патогенез. Истощение запасов железа ведет к уменьшению синтеза гемоглобина в эритрокариоцитах костного мозга, что приводит к снижению его концентрации, а затем и числа эритроцитов в единице объема крови.
Адаптационными механизмами являются увеличение сердечного выброса и усиленное высвобождение кислорода в тканях, происходящее в результате повышенной концентрации в эритроцитах 2-3-дифосфоглицировой кислоты.
При дефиците железа нарушается работоспособность мышц.
Причиной функциональной недостаточности мышц является сниженная активность железосодержащих ферментов, основное значение при этом отводится истощению запаса а-глицерофосфатдегидрогеназы.
При тяжелом дефиците железа могут развиться неврологические нарушения, извращение вкусовых ощущений и восприятия запахов, трофические нарушения (повышенная ломкость и выпадение волос, ломкость ногтей, сухость кожи, ангулярный стоматит и атрофический глоссит).
Клиническая картина. Клиническая картина складывается из проявлений сидеропенического синдрома, связанного с дефицитом железосодержащих ферментов, участвующих в окислительно-восстановительных процессах. Жалобы на слабость, головокружения, обмороки, сердцебиение, одышку, мышечную слабость, головную боль, парестезии.
Поражение кожи и слизистых (сухость и атрофичность кожи, ломкость ногтей и волос, выпадение волос, трещины слизистых).
Извращение вкуса и запахов (пристрастие к употреблению в пищу мела, зубной пасты, глины, сырой крупы, сырого кофе, неочищенных семян подсолнечника; пристрастие к запаху бензина, керосина, лака для ногтей (ацетон), запаху сырой глины, извести.
Неврологические нарушения: нарушение глотания твердой пищи, недержание мочи. При объективном осмотре — бледность кожи и слизистых оболочек, кожа сухая, истонченная, ногти уплощаются, а иногда становятся вогнутыми (ложкообразными) — койлонихии, явления ангулярного стоматита в углах губ и покраснение языка, сглаженность его сосочков.
Анемия носит гипохромный микроцитарный характер.
Количество ретикулоцитов — в пределах нормы.
Количество лейкоцитов, тромбоцитов и лейкоцитарная формула не изменены.
При тяжелом дефиците железа наряду с выраженной гипохромной (микроцитарной) анемией могут отмечаться легкая нейтропения и, реже, тромбоцитопения.
У взрослых больных с ЖДА средней или тяжелой степени могут наблюдаться умеренные тромбоцитозы.
ЖДА чаще бывают легкой или средней степени тяжести.
Диагностика. Основные критерии ЖДА: низкий цветовой показатель (0,6—0,7); гипохромия эритроцитов; анизоцитоз (уменьшенные по величине эритроциты) и пойкилоцитоз (изменение формы эритроцитов); снижение уровня сывороточного железа (менее 12 мкмоль/л); повышение общей железосвязывающей способности сыворотки (более 56 мкмоль/л); снижение содержания ферритина в сыворотке; клинические проявления гипосидероза (непостоянный признак); эффективность препаратов железа.
Наличие анемии гипохромного характера заставляет в первую очередь подозревать у больного ЖДА (все ЖДА также являются гипохромными!).
Однако факт гипохромии сам по себе не исключает других патогенетических вариантов анемий (не все гипохромные анемии являются железодефицитными!).
Так, например, гипохромная анемия может возникать при дефекте синтеза НЬ в результате нарушения включения в его молекулу железа при нормальном или даже повышенном уровне железа в сыворотке крови. Различать эти состояния и, тем самым, верифицировать ЖДА позволяет исследование содержания железа в сыворотке, которое следует выполнять обязательно до назначения больным лекарственных препаратов железа или проведения трансфузий эритроцитов.
Об этом должны быть осведомлены врачи, средний медицинский персонал (медицинские сестры, лаборанты), а также сами пациенты.
Наряду с определением содержания железа в сыворотке крови важным лабораторным показателем, определяемым при ЖДА, является общая железосвязывающая способность сыворотки, отражающая степень «голодания» сыворотки и насыщения белка трансферрина железом.
Общая железосвязывающая способность сыворотки при ЖДА всегда повышена в отличие от других гипохромных анемий, связанных не с дефицитом железа, а с нарушением его включения в молекулу гемоглобина или с перераспределением железа из эритроидных клеток в клетки макрофагальной системы (например, при активных воспалительных процессах).
Десфераловый тест (выделение железа с мочой) при ЖДА — ниже 0,2 мг/сут.
Снижение уровня железосодержащего белка ферритина — существенный диагностический критерий ЖДА с высокой специфичностью.
Ферритин характеризует величину запасов железа в организме.
Поскольку истощение запасов железа — обязательный этап формирования ЖДА, то уровень ферритина является одним из специфических признаков железодефицитного характера гипохромных анемий.
Следует, однако, иметь в виду, что наличие сопутствующего активного воспалительного процесса у больных ЖДА может маскировать гипоферритинемию.
Дополнительными методами определения запасов железа в организме могут быть подсчет числа эритроидных клеток костного мозга, содержащих гранулы железа (сидеробластов), и количество железа в моче после введения препаратов, связывающих железо, например, десфериоксиамина.
Количество сидеробластов при ЖДА значительно снижено, вплоть до полного их отсутствия, а содержание железа в моче после введения десфериоксиамина не увеличивается.
Патоморфология костного мозга. Картина гемопоэза в костном мозге у больных ЖДА мало чем отличается от таковой у здоровых лиц.
Может иметь место небольшая гиперплазия эритроидного ростка. Выявляется резкое снижение или полное отсутствие запасов железа в стромальных и макрофагальных элементах костного мозга, а также резкое уменьшение количества сидеробластов.
Дифференцировать ЖДА необходимо от других вариантов гипохромных анемий. Гипохромные микроцитарные анемии могут также наблюдаться при талассемии, сидеробластной анемии, пароксизмальной ночной гемоглобинурии, отравлении свинцом.
Дифференциальный диагноз ЖДА с малой талассемией проводится на основании отсутствия в случае последней лабораторных признаков дефи- цита железа и наличия патологического гемоглобина при электрофорезе гемоглобина.
Дифференциальный диагноз с сидеробластной анемией (вариант миелодиспластического синдрома) — на основании наличия в костном мозге более 20% сидеробластов.
При хроническом отравлении свинцом имеют место специфические включения в эритроцитах.
Гипохромная (чаще нормоцитарная, реже микроцитарная) анемия наблюдается на фоне хронических инфекционных и воспалительных заболеваний.
Гипохромная анемия на фоне хронических заболеваний развивается вследствие увеличения воспалительных цитокинов и роста продукции гепсидина, блокирующего процесс освобождения железа из депо.
Таким образом, для гипохромных анемий на фоне хронических заболеваний характерны следующие лабораторные показатели: нормальный или повышенный уровень ферритина в сочетании с пониженным содержанием сывороточного железа и трансферрина.
Лечение.
Важно выявить и по возможности устранить причину дефицита железа (оперативное лечение опухоли желудка, кишечника, лечение энтерита, коррекция алиментарной недостаточности и др.).
Для успешного лечения ЖДА должны быть использованы только лекарственные формы железа, восполнить необходимое количество железа путем поступления его из пищи даже теоретически невозможно из-за ограничения всасывания.
Из лекарственных источников у больных с ЖДА всасывание железа возрастает как минимум в 10 раз по сравнению со всасыванием железа из пиши, т. е. составляет 20—25 мг/суг.
При таком уровне всасывания повышение содержания гемоглобина происходит примерно на 1% вдень.
В ряде случаев радикальное устранение причины ЖДА не представляется возможным, например, при продолжающихся меноррагиях, наследственных геморрагических диатезах, проявляющихся носовыми кровотечениями, у беременных и в некоторых других ситуациях.
В таких случаях основное значение приобретает патогенетическая терапия железосодержащими лекарственными препаратами.
В клинической практике лекарственные препараты железа применяют внутрь или парентерально. Путь введения препарата у больных ЖДА определяется конкретной клинической ситуацией.
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний препараты железа следует назначать внутрь.
Лечение железодефицитной анемии продолжают до нормализации уровня гемоглобина в крови, затем в течение нескольких месяцев применяют препараты железа в меньших дозах для восстановления его запасов в депо.
В настоящее время все препараты железа можно разделить на две группы: ионные железосодержащие препараты (солевые, полисахаридные соединения железа) и неионные соединения, к которым относятся препараты гидроксид-полимальтозного комплекса трехвалентного железа.
Данная классификация основана на различии механизмов всасывания железа из ионных и неионных соединений.
Всасывание железа из ионных соединений происходит преимущественно в двухвалентной форме, так как активность утилизации железа из препаратов, содержащих соли трехвалентного железа, жестко лимитируется определенным уровнем рН желудочного сока (при высокой кислотности желудочного сока образуются труднорастворимые гидроксиды железа).
Вследствие этого наиболее часто используются двухвалентные солевые препараты железа, обладающие хорошей растворимостью, высокой диссоциационной способностью.
Следует отметить, что при своем восстановлении в трехвалентное железо в слизистой оболочке ЖКТ двухвалентные соли железа образуют свободные радикалы, обладающие повреждающим эффектом.
Именно с этим связаны побочные явления, наблюдающиеся при ферротерапии солями двухвалентного железа (гастроинтестинальные расстройства — боль, тошнота, рвота, диарея).
Препараты нового поколения, представляющие собой многомолекулярные комплексы гидроокиси трехвалентного железа, практически лишены этого побочного эффекта, так как не требуют восстановления и соответственно не вызывают образования свободных радикалов.
Они намного лучше переносятся, практически не сопровождаются гастроинтестинальными расстройствами и более безопасны.
При этом по биодоступности они не уступают препаратам солей двухвалентного железа.
При жедезодефицитных состояниях для синтеза НЬ требуется 50—100 мг железа ежедневно.
Поскольку при пероральном применении препаратов железа абсорбироваться может только 25% принятой дозы, то для быстрой коррекции недостатка железа в организме его необходимо применять в дозе 200—400 мг вдень.
При появлении желудочно-кишечных расстройств возможно снижение дозы железа, однако в этом случае дефицит железа устраняется медленнее.
Железа глюконат назначают внутрь, после еды, по 4-6 таблеток в день; железа сульфат — после еды, по 0,3—0,5 г 3—4 раза в день.
Железа фумарат — натощак по 1 капсуле вдень; при недостаточном эффекте возможен прием по I капсуле 2 раза в день.
Прием продолжают и после нормализации картины крови. Продолжительность насыщающего курса терапии не менее 1-1,5 мес.
Железа хлорид принимают по 4-6 мг/кг массы тела в сутки, дозу делят на 3—4 приема.
Мальтофер — 100 мг 2—3 раза в день.
Феррум Лек — 100 мг 2-3 таблетки в день.
Основными принципами лечения препаратами железа для приема внутрь являются следующие:
— назначение препаратов железа с достаточным содержанием двухвалентного железа;
— назначение препаратов железа, содержащих вещества, усиливающие всасывание железа;
— нежелательность одновременного приема пищевых веществ и лекарственных препаратов, уменьшающих всасывание железа;
— нецелесообразность одновременного назначения витаминов группы В, В12, фолиевой кислоты без специальных показаний;
— избегать назначения препаратов железа внутрь при наличии признаков нарушения их всасывания в кишечнике;
— достаточная продолжительность насыщающего курса терапии (не менее 1 — 1,5 мес);
— необходимость проведения поддерживающей терапии препаратами железа после нормализации показателей гемоглобина в соответствующих ситуациях.
Лечение пероральными препаратами следует проводить до нормализации содержания гемоглобина, а затем еще в течение 2 мес в половинной дозе для пополнения запасов железа в депо.
Длительное бесконтрольное применение больших доз может привести к гемосидерозу внутренних органов.
Препараты для парентерального введения необходимо использовать лишь у отдельных больных. Чаще используют препараты феррум-лек для в/м введения (полиизомальтоза) и для в/в (натрий-сахаратный комплекс); ектофер (сорбитовый цитратный комплекс) для в/м и венофер (сахарат железа) для в/в введения.
В одной ампуле каждого из названных препаратов содержится 100 мг железа.
Показания для парентерального лечения препаратами железа: нарушение всасывания в кишечнике при тяжелых энтеритах; обширная резекция тонкой кишки; невозможность приема пероральных препаратов железа.
Применение парентеральных препаратов железа не позволяет реально сократить сроки лечения и ускорить подъем концентрации гемоглобина до желаемого уровня.
Ограничивают использование парентеральных препаратов железа высокий риск развития анафилактических реакций, гемосидероза внутренних органов и болезненных, нередко абсцедирующих инфильтратов в местах введения препарата.
Побочные действия при лечении препаратами железа: гиперемия лица, тошнота, головокружение, головная боль, кожные аллергические реакции. Реже — рвота, диарея, боли в животе, в спине, тахикардия, транзиторное снижение АД.
При в/м введении возможно развитие абсцессов в месте инъекции. Противопоказаны препараты железа при гемохроматозе, повышенной чувствительности к железу.
Парентерально нельзя назначать препараты железа при АГ, тяжелой коронарной недостаточности, аллергических заболеваниях кожи, выраженных нарушениях функций печени и почек.
Препараты железа окрашивают кал в темный цвет и иногда могут маскировать кровотечение; могут вызывать потемнение зубов.
Прогноз. При правильном лечении прогноз при ЖДА благоприятный.
Профилактика. Основным контингентом, нуждающимся в профилактике ЖДА, являются женщины с гиперполименореей.
Каждая девушка с момента установления менструального цикла нуждается в профилактическом приеме препаратов железа, если менструальное кровотечение продолжается более 5 дней без образования сгустков крови или более 3 дней с образованием сгустков крови.
Используются пероральные препараты железа в дозе 300 мг/сут, в течение 5 дней ежемесячно.
При наличии дополнительных показаний для этого могут быть использованы пероральные контрацептивы, имеющие специальную добавку препарата железа.
источник
Принципы лечения железодефицитной анемии:
— Диетой нельзя вылечить железодефицитную анемию.
— Применение лекарственных средств, строго соответствующих определенному патогенетическому варианту анемии, то есть используются только препараты железа.
— Используются преимущественно препараты орального применения.
— Лечение адекватно высокими суточными дозами одного препарата с хорошей переносимостью.
— Назначение трансфузии эритроцитов только по жизненным показаниям, в том числе больным старших возрастных групп с прогрессирующей стенокардией, декомпенсацией кровообращения и общемозговыми гипоксическими расстройствами.
— Оценка эффекта лечения по клинико-лабораторным признакам, в том числе по ретикулоцитарному кризу.
— Использование препаратов с оптимальным соотношением «затраты/эффективность» позволяет минимизировать затраты на лечение.
Рациональная терапевтическая тактика подразумевает:
— Начало лечения с момента выявления железодефицитной анемии до достижения полной клинико-гематологической ремиссии; при необходимости — проведение поддерживающей (профилактической) терапии.
— Устранение причин (заболеваний) железодефицитной анемии.
Основой заместительной терапии дефицита железа при лечении железодефицитной анемии являются препараты железа. В настоящее время используются две группы препаратов железа — содержащие двухвалентное и трехвалентное железо. В связи с тем что железо из большинства современных железосодержащих препаратов хорошо всасывается в кишечнике, в подавляющем большинстве случаев возможно применение лекарственных препаратов железа внутрь. Парентерально препараты железа назначаются только по специальным показаниям, к которым относятся:
— наличие патологии кишечника с нарушением всасывания (тяжелые энтериты, синдром недостаточности всасывания, резекция тонкого кишечника и др.);
— абсолютная непереносимость препаратов железа при приеме внутрь (тошнота, рвота) даже при приеме препаратов разных групп, не позволяющая продолжать дальнейшее лечение;
— необходимость быстрого насыщения организма железом, например, когда больным с железодефицитной анемией планируются оперативные вмешательства;
— лечение больных эритропоэтином, при котором лимитирующим фактором эффективности является недостаточное количество запасов и циркулирующего железа.
Из лекарственной формы всасывается не более 10 — 12% содержащегося в ней железа. При тяжелой степени дефицита железа показатель всасываемости железа может возрастать до трех раз. Повышению биодоступности железа способствует присутствие аскорбиновой и янтарной кислот, фруктозы, цистеина и других акселераторов, а также использование в ряде препаратов специальных матриц, замедляющих высвобождение железа в кишечнике (уровень убедительности доказательства В). Всасывание железа может уменьшаться под влиянием некоторых содержащихся в пище веществ (танин чая, фосфорная кислота, фитин, соли кальция, молоко), а также при одновременном применении ряда медикаментов (тетрациклиновые препараты, альмагель, фосфалюгель, препараты кальция, левомицетин, пеницилламин и др.). Эти вещества не влияют на всасывание железа из полимальтозного комплекса гидроокиси железа. Для снижения вероятности побочных эффектов препараты солей железа принимают до еды.
Расчет суточного количества препарата (СКП) для пероральных препаратов железа выполняют по следующей формуле:
где НСД — необходимая суточная доза двухвалентного или трехвалентного
(не элементарного) железа (у взрослых — 200 мг в сутки, у
детей — 30 — 100 мг в сутки);
СЖП — содержание двухвалентного или трехвалентного (не
элементарного) железа в единице препарата (таблетке, капсуле,
капле раствора, миллилитре сиропа или раствора).
Расчет ориентировочной курсовой дозы препарата железа, назначаемого парентерально, может быть произведен по формуле с учетом массы тела больного и уровня гемоглобина, отражающего степень дефицита железа:
А = М х (Нb — Нb ) х 0,24 + D, (5)
где А — количество железа в мг;
Hb — нормативная величина гемоглобина для массы тела менее 35 кг
1 130 г/л, более 35 кг — 150 г/л;
HB — уровень гемоглобина у пациента в г/л;
D — расчетная величина депо железа для массы тела менее
35 кг — 15 мг/кг, для массы тела более 35 кг — 500 мг.
Оптимальная суточная доза для препаратов железа при лечении железодефицитной анемии должна соответствовать необходимой суточной дозе и рассчитывается:
— железа в составе препаратов солей железа, составляет для детей до 3-х лет — 5 — 8 мг двухвалентного железа на кг массы тела в сутки, старше 3-х лет — 100 — 120 мг двухвалентного железа в сутки, взрослых — 200 мг двухвалентного железа в сутки;
— железа в препаратах полимальтозатного комплекса гидроксида железа (трехвалентного железа) для недоношенных детей 2,5 — 5 мг на кг массы тела, детей до года — 25 — 50 мг, 1 — 12 лет 50 — 100 мг, старше 12 лет 100 — 300 мг, взрослых — 200 — 300 мг.
Применение меньших доз препаратов не дает адекватного клинического эффекта. При латентном дефиците железа или для насыщения депо после окончания курса терапии применяются половинные относительно лечебных дозы препаратов.
У взрослых больных парентерально вводится не более 200 мг железа в сутки, по особым показаниям, капельно, до 500 мг в сутки. У детей суточная доза 25 — 50 мг в зависимости от возраста, препарат вводят струйно, медленно — не менее 10 минут. Максимально допустимая разовая доза — 7 мг железа на кг массы тела вводится 1 раз в неделю.
Контроль эффективности терапии является обязательным компонентом рационального применения железосодержащих препаратов. В первые дни лечения проводится оценка субъективных ощущений, на 5 — 8-й день обязательно определение ретикулоцитарного криза (2 — 10-кратное увеличение числа ретикулоцитов по сравнению с исходным значением). На 3-й неделе оценивают прирост гемоглобина и числа эритроцитов. Отсутствие ретикулоцитарного криза свидетельствует либо об ошибочном назначении препарата, либо о назначении неадекватно малой дозы.
Нормализация уровня гемоглобина, исчезновение гипохромии происходит обычно к концу первого месяца лечения (при адекватных дозах препаратов). Однако с целью насыщения депо рекомендуется применение половинной дозы железосодержащих препаратов на протяжении еще 4 — 8 недель. Насыщение депо определяется с помощью комплексного биохимического исследования. При отсутствии этих методов лечение проводится эмпирически.
Среди побочных эффектов на фоне перорального применения препаратов железа наиболее часто возникают диспепсические расстройства (анорексия, металлический вкус во рту, чувство переполнения желудка, давления в эпигастрии, тошнота, рвота), запоры, иногда — диарея. Развитие запоров связано с образованием в кишечнике сернистого железа, являющегося активным ингибитором функции толстого кишечника. У некоторых больных, особенно у детей, при применении препаратов солей железа происходит коричневатое окрашивание эмали зубов. Не имеет клинического значения часто появляющееся темное окрашивание стула.
При парентеральном введении препаратов железа могут возникать реакции: местные — флебиты, венозный спазм, потемнение кожи в месте инъекции, постинъекционные абсцессы и общие — гипотония, загрудинные боли, парестезии, боли в мышцах, артралгии, лихорадка. При передозировке возможно перенасыщение железом с развитием гемосидероза. В месте инъекций возможна малигнизация.
Двухвалентное железо очень часто входит в состав комплексных витаминных препаратов. Однако доза железа в этом случае незначительна, и в связи с этим они не могут быть использованы для лечения железодефицитных состояний (уровень убедительности доказательства А).
источник
Н.И. Стуклов, Е.Н. Семенова
ФГБОУ ВПО Российский университет дружбы народов, Москва
Рассмотрен современный взгляд на проблему железодефицитной анемии (ЖДА) с точки зрения эпидемиологии, этиологии, патогенеза. Описаны известные в настоящее время механизмы регуляции обмена железа, приведены наиболее важные данные литературы и результаты собственных исследований. Основываясь на рекомендациях по лечению больных ЖДА, авторы представляют описанный в литературе и собственный клинический опыт использования железосодержащих препаратов и рассматривают полученные результаты. В рамках статьи авторы объясняют механизмы низкой эффективности лечения при ЖДА и предлагают способы решения проблемы с учетом опубликованных в литературе последних научных исследований.
Ключевые слова: анемия; обмен железа; сидеропенический синдром; лечение железодефицитной анемии.
N.I. Stuklov, E.N. Semenova
Russian University of People’s Friendship, Moscow, Russia
Modern views of epidemiology, etiology and pathogenesis of iron deficiency anemia are considered. Mechanisms of iron metabolism regulation are described based on the most important literature data and the results of the authors ’ research. The authors present their own and literature clinical experience of using iron-containing drugs with reference to the existing recommendations on the treatment of iron deficiency anemia. Causes of low treatment efficiency are discussed and the ways to address this problem are proposed based on the published results of clinical research.
Key words: anemia; iron metabolism; sideropenic syndrome; treatment of iron deficiency anemia.
Анемии (греч. αναιμια — бескровие) определяются как ряд клинических состояний, связанных со снижением уровня гемоглобина менее 120 г/л у женщин и менее 130 г/л у мужчин; (ВОЗ, 2001) и (или) гематокрита ( менее 36,4% соответственно), что обусловлено уменьшением количества эритроцитов или содержания гемоглобина в них [1]. В настоящее время железодефицитная анемия (ЖДА) является самым распространенным состоянием, связанным со снижением уровня гемоглобина, поэтому ее признают государственной проблемой более чем в 100 странах мира, где разрабатываются программы, направленные на профилактику и снижение заболеваемости. ЖДА чаще выявляется у представителей наиболее социально значимых и незащищенных слоев населения — у женщин детородного возраста и детей. Количество больных анемией в указанных группах, по данным ВОЗ (2001), превышает 1 млрд [2]. В итоге ЖДА является причиной роста материнской и детской смертности [3].
Регуляция обмена железа.
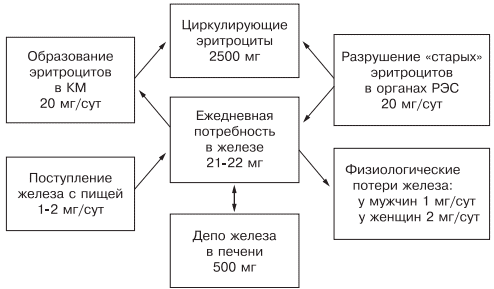
Ежедневно организму для нормальной жизнедеятельности требуется 20—25 мг железа, причем экзогенного железа необходимо только 1— 2 мг: женщинам — 2 мг (из-за физиологической кровопотери), а мужчинам — 1—1,5 мг. Около 20 мг железа поступает из «старых» разрушенных эритроцитов, столько же расходуется на синтез нового гемоглобина.
Железо накапливается в органах ретикулоэндотелиальной системы (до 500 мг), остальные запасы железа на 70% сосредоточены в гемоглобине, что и обусловливает развитие ЖДА при хронической кровопотере (рис. 1).
Рис. 1. Схема обмена железа.
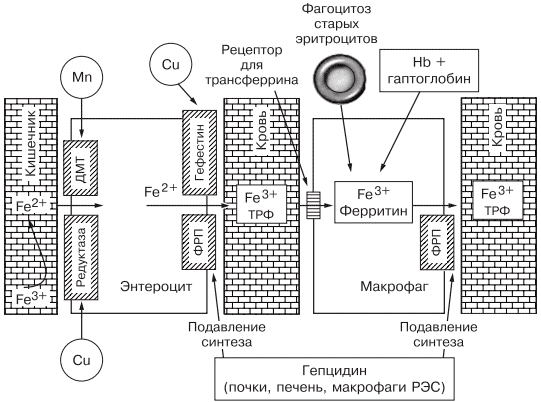
Всасывание железа происходит в верхних отделах тонкой кишки, причем этот процесс требует участия множества белков. В основном до 70—80% железа усваивается в двухвалентном состоянии (гемовое железо, содержащееся в основном в мясе, меньше — в печени и рыбе). При поступлении в кишечник растительного трехвалентного железа с помощью медьзависимой ферроредуктазы на апикальной мембране энтероцитов или под действием витамина С оно восстанавливается до двухвалентного. Двухвалентное железо через марганецзависимые белки — транспортеры двухвалентных металлов (ДМТ — двухвалентный металлотранспортер) поступает в энтероцит, а затем через белок ферропортин на базальной мембране — в кровь, где с помощью медьзависимых феррооксидаз (гефестина, расположенного на базальной мембране и связанного с ферропортином, и церулоплазмина, находящегося в плазме) окисляется до трехвалентного состояния, чтобы связаться с транспортным белком — трансферрином (рис. 2). Только очень незначительная часть железа, образуя комплекс с муцином, может поступить в энтероциты путем пиноцитоза [4, 5].
Рис. 2. Схема регуляции обмена железа.
Универсальным регулятором метаболизма железа является гепцидин [6—9], который блокирует транспорт железа, причем этот механизм реализуется с помощью регуляции активности белка ферропортина, т.е. путем воздействия на высвобождение железа из клеток кишечника и макрофагов ретикулоэндотелиальной системы [10—13]. Увеличение количества железа в организме ведет к стимуляции синтеза гепцидина, что уменьшает абсорбцию железа в кишечнике и его транспорт в циркуляцию. В свою очередь уменьшение абсорбции железа в кишечнике ведет к угнетению синтеза гепцидина в печени и по обратной связи — к восстановлению захвата железа из пищи и кишечника (см. рис. 2) [14—18]. Помимо железорегуляторной функции, гепцидин оказывает выраженное бактерицидное действие, является белком воспаления, его уровень повышается при инфекционных, воспалительных, опухолевых заболеваниях, блокируя выход железа в кровь [6]. Такой эффект гепцидина отрицательно влияет на рост бактерий, опухолей, блокирует избыточный воспалительный процесс. В работе, проведенной в 2011 г. [19], доказана роль гепцидина как основного фактора развития ЖДА у женщин с гинекологическими заболеваниями без патологической кровопотери. Показатели гепцидина в указанной группе составили 108,75 ± 40,08 нг/л (референсные значения 60— 85 нг/л), что обусловило резкое уменьшение содержания ферропортина — 0,43 ± 0,21 нг/л (референсные значения 3,1 ± 0,2 нг/л) и привело к нарушению поступления железа из кишечника в кровь [19].
Железо, которое остается внутри клеток, депонируется в виде ферритина, количество которого в крови прямо пропорционально содержанию железа в депо [20].
Клиническая картина и диагностические критерии.
Дефицит железа приводит к нарушению синтеза гемоглобина в эритрокариоцитах костного мозга, уменьшению содержания миоглобина в мышцах, активности цитохромов и каталаз в митохондриях клеток, миелопероксидазы в нейтрофилах [21—23].
В настоящее время выделяют несколько этапов развития дефицита железа [5, 24].
1. Предрасположенность к развитию дефицита железа (вегетарианство, подростковый возраст в сочетании с нарушением менструального цикла у девочек, частые роды, наличие хронических болезней желудочно-кишечного тракта — ЖКТ, заболеваний женской репродуктивной системы, связанных с кровопотерей).
2. Предлатентный дефицит железа. На этой стадии нет никаких лабораторных критериев дефицита железа, однако можно определить повышение абсорбции трехвалентного железа в ЖКТ, которое может превышать 50% (в норме 10—15%).
3. Латентный дефицит железа характеризуется развитием сидеропенического синдрома и уменьшением запасов железа в организме (по данным лабораторных исследований).
4. ЖДА. Диагноз устанавливается при уровне гомоглобина менее 120 г/л у женщин и 130 г/л у мужчин. Выделяют следующие стадии ЖДА:
В основе патологии эритропоэза при дефиците железа лежит нарушение синтеза гема, в результате которого уменьшается количество гемоглобина в эритрокариоцитах костного мозга, что проявляется на первом этапе гипохромией эритроцитов, а в дальнейшем — развитием гипохромной микроцитарной анемии.
Клинические проявления ЖДА связаны с развитием как сидеропенического синдрома, для которого характерны выраженная мышечная слабость, нарушение целостности слизистых оболочек, кожи, ее придатков (ломкость и расслаивание ногтей, выпадение волос), снижение иммунитета, так и непосредственно симптомов анемии (головокружение, мелькание «мушек» перед глазами, сонливость, снижение работоспособности).
Наиболее характерным лабораторным признаком ЖДА являются гипохромия, микроцитоз эритроцитов, анизоцитоз. О гипохромии эритроцитов свидетельствуют цветовой показатель менее 0,8, среднее содержание гемоглобина в эритроците менее 28 пг, средняя концентрация гемоглобина в эритроците менее 290 г/л. О микроцитозе говорят, когда средний диаметр эритроцита менее 7 мкм, а средний объем эритроцита — менее 80 фл [21, 22, 24].
Параметры обмена железа широко используются в клинической практике, но в связи с отсутствием четко определенных значений, доказывающих наличие ЖДА, высокой стоимостью исследования и большим количеством больных их применение не всегда оправдано. Так, показатель ферритина сыворотки (ФС) как единственный маркер, отражающий запасы железа в организме и используемый для верификации и дифференциальной диагностики ЖДА, по мнению разных исследователей [5, 20], варьирует от 15 до 100 мкг/л. Известно, что показатель ФС является положительным маркером воспаления, а количество его определяется белково-синтетической функцией печени. В настоящее время для установления диагноза ЖДА принято считать достоверным показатель ФС менее 30 мкг/л [25]. Уровень такого транспортного белка, как трансферрин, как правило, повышен при недостатке железа, однако при наличии инфекции его содержание уменьшается и не может использоваться в диагностике ЖДА [26]. Тем более изменчивы такие параметры обмена железа, как железосвязывающая способность (общая и латентная) и коэффициент насыщения трансферрина железом, так как они рассчитываются исходя из содержания трансферрина и сывороточного железа, а последний показатель вообще не имеет связи с содержанием железа в организме и зависит от времени, в которое проведено исследование, и приема пищи [21]. Значения коэффициента насыщения трансферрина железом у больных ЖДА, по опубликованным данным, могут составлять от 15 до 20%. Наиболее точным методом диагностики ЖДА в настоящее время считается подсчет растворимых рецепторов для трансферрина, однако этот метод не используется в качестве рутинного из-за отсутствия единого способа детекции, высокой стоимости исследования, невозможности интерпретировать результат при наличии любых пролиферативных процессов [26].
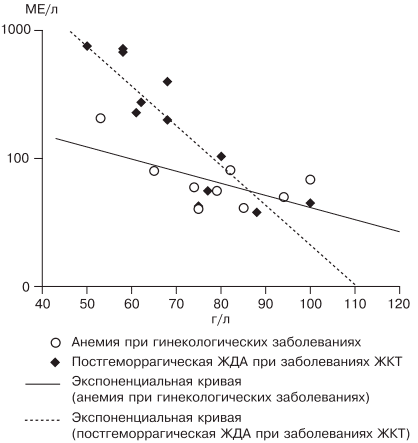
Наиболее частыми причинами ЖДА являются как физиологические, так и патологические состояния. В группу риска развития ЖДА входят недоношенные дети, так как у них не успевает сформироваться депо железа, и подростки, которым требуется больше железа в связи с быстрым ростом организма [27]. Наиболее часто ЖДА развивается при беременности. В период беременности, родов и лактации в среднем расходуется до 1000 мг железа, что в 2 раза больше его запасов в депо [28]. Репродуктивный возраст у женщин связан с повышенной потерей железа при менструациях; этот недостаток компенсируется увеличением всасывания железа в ЖКТ, что в настоящее время объясняется изменением влияния гепцидина. При наличии гиперполименореи, однако, такой баланс нарушается в связи с увеличением кровопотери [29, 30], при сопутствующих заболеваниях ЖКТ нарушается всасывание железа и развивается ЖДА [6, 19]. Часто у женщин меноррагии имеют органические причины: полипы, эндометрит, миома матки, аденомиоз, открывающийся в полость матки; мало того, такие заболевания, как миома матки и дисплазия шейки матки, оказывают влияние на развитие анемии и без патологической кровопотери [5, 19, 30]. Указанный механизм связан с увеличением содержания гепцидина в крови и снижением активности эритропоэза, доказанным синдромом неадекватной выработки эритропоэтина. В настоящее время продукцию эритропоэтина принято считать неадекватной при отношении определяемого эритропоэтина к предполагаемому (О/П log эритропоэтина менее 0,9) [28, 31]. Так, В.А. Бурлевым и Е.Н. Коноводовой [32] при обследовании женщин с миомой матки выявлено отношение О/П log эритропоэтина менее 0,8, а при обследовании гинекологических больных с анемией без нарушения менструальной функции в 2011 г. отношение О/П log эритропоэтина составило 0,89 (рис. 3). Для всех женщин с диагностированной ЖДА необходимо обязательное обследование у гинеколога. В случае обнаружении ЖДА у мужчин, наоборот, показано исключение заболеваний ЖКТ.
Рис. 3. Зависимость между уровнем гемоглобина и сывороточного эритропоэтина (логарифмическая шкала и экспоненциальные кривые) у больных с постгеморрагической ЖДА при заболеваниях ЖКТ (предполагаемый эритропоэтин) и анемии при гинекологических заболеваниях (определяемый эритропоэтин) [5].
Помимо повышенной потребности в железе и хронической кровопотери, патологическими состояниями, способными вызывать развитие ЖДА, являются различные нарушения всасывания железа и поступления его с пищей (в том числе и обусловленные вегетарианством), нарушения транспорта железа (гипотрансферринемии при заболеваниях печени и наследственные атрансферринемии) [21].
Таким образом, гипохромная микроцитарная анемия, особенно при наличии характерной для сидеропенического синдрома клинической картины, даже без исследования обмена железа может определяться как ЖДА при условии полноценного клинического и инструментального обследования больного и установления причины ее развития [5].
Лечение.
Современная тактика лечения при ЖДА в настоящее время направлена на устранение этиологического фактора и восполнение запасов железа в организме [4, 5]. Наиболее оправдано более физиологическое пероральное применение препаратов железа; парентерально препараты можно использовать только при доказанном дефиците железа. Перорально следует назначать препараты железа в высоких дозах (от 200 до 300 мг/сут), что, однако, может приводить к возникновению диспепсических явлений, поэтому (особенно в детской и акушерской практике) рекомендуется постепенное повышение дозы до терапевтической, а при достижении нормальных значений уровня гемоглобина — ее снижение [20].
Степень абсорбции двухвалентных солей железа в несколько раз выше, чем трехвалентных, так как они пассивно диффундируют через каналы ДМТ-белков [33], поэтому препараты, содержащие двухвалентное железо, дают быстрый эффект и нормализуют уровень гемоглобина в среднем через 1—2 мес, а нормализация депо железа происходит уже через 3—4 мес от начала лечения в зависимости от степени тяжести анемии и дозы препарата. Препараты, содержащие железо в трехвалентном состоянии, требуют более длительного применения, а в случае дефицита меди в организме будут неэффективны. Нормализация уровня гемоглобина при лечении препаратом трехвалентного железа наступит только через 2—4 мес, а нормализация показателей депо железа — через 5—7 мес от начала терапии [5, 19, 33]. Степень абсорбции отражается и на частоте развития побочных эффектов. Уменьшить нежелательное влияние таблетированных препаратов железа на ЖКТ можно, принимая их во время еды, но при этом уменьшается всасывание железа. Лучше (но также с потерей эффективности) использовать формы с замедленным высвобождением, так как часть препарата будет высвобождаться в нижних отделах ЖКТ, где железо практически не всасывается [34]. Несмотря на рекомендации ВОЗ по применению для лечения ЖДА препаратов двухвалентного железа как более эффективных, препараты с низкой биодоступностью на основе трехвалентного железа активно применяются благодаря их лучшей переносимости.
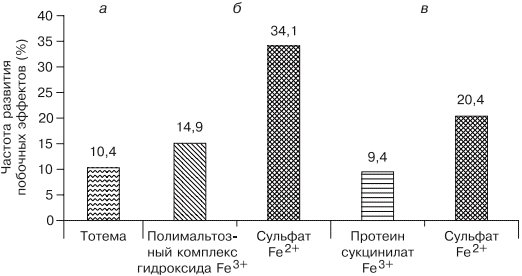
В современной клинической практике используются различные варианты сочетаний двухвалентного железа с витаминами С, В9, В12, что позволяет минимизировать побочные эффекты и одновременно повысить эффективность терапии, однако переносимость такого лечения до настоящего времени была основным лимитирующим фактором [20, 33]. Анализ переносимости различных препаратов железа более чем у тысячи пациентов показал, что современная жидкая форма двухвалентного железа (препарат тотема, лаборатория Иннотек Интернасиональ, Франция) по количеству побочных эффектов не превышает таковые у трехвалентного (рис. 4) [4]. Такой эффект достигается равномерным распределением препарата по слизистой оболочке желудка и его высокой биодоступностью. Двухвалентное железо равномерно и максимально эффективно проникает в энтероциты и, не накапливаясь в них, поступает в кровь. Это обусловлено наличием в составе препарата меди и марганца, которые входят в состав ДМТ-белков и гефестина, окисляющего железо, что способствует наилучшему его метаболизму (см. рис. 2) [33]. Помимо этого, указанные металлы участвуют в работе системы антиоксидантов, наиболее важными составляющими которой являются Cu, Zn-супероксиддисмутаза, Mn-супероксиддисмутаза (в митохондриях), каталаза, глутатионпероксидаза и глутатион. При уменьшении антиоксидантной защиты происходит сдвиг в сторону избыточного накопления свободных радикалов, что обусловливает их повреждающее действие на клетки. Следует понимать, что процесс активации перекисного окисления липидов запускается ионами двухвалентного железа, что проявляется частым развитием побочных эффектов при лечении препаратами железа. Наличие меди и марганца в составе тотемы уменьшает образование свободных радикалов, что улучшает переносимость препаратов железа [37].
Пациентам с заболеваниями ЖКТ назначать препараты железа перорально следует с осторожностью, причем острые заболевания, такие как язва желудка и двенадцатиперстной кишки, эрозивный гастрит, являются противопоказаниями; также не следует использовать указанный метод лечения у больных с заболеваниями тонкой кишки (болезнь Крона, целиакия, мальабсорбция) или отсутствием ее части.
Рис. 4. Сравнение результатов исследований безопасности применения различных железосодержащих препаратов.
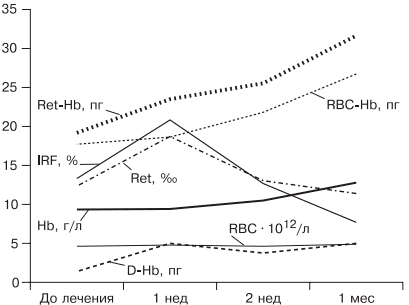
При лечении больных ЖДА остро стоит вопрос оценки эффективности терапии, так как часто ЖДА диагностируется у соматически тяжелых больных с крайне низким уровнем гемоглобина. Попытки ранней диагностики, как правило, связаны с исследованием количества ретикулоцитов [38], однако в настоящее время такой подход не является доказательным, так как часто ретикулоцитоз возникает компенсаторно при наличии кровотечения. В работе [5, 9] показано, что наиболее достоверными показателями, указывающими на хороший эффект препаратов железа, служат появление молодых форм ретикулоцитов и увеличение дельты гемоглобина (разницы между средним содержанием гемоглобина в ретикулоците и эритроците) уже через 1 нед после начала лечения (рис. 5).
Рис. 5. Динамика гемоглобина эритроцитов (RBC), количества ретикулоцитов (Ret), фракции незрелых ретикулоцитов (IRF-) среднего содержания гемоглобина в эритроците (RBC-Hb), среднего содержания гемоглобина в ретикулоците (Ret-Hb), дельты гемоглобина (D-Hb) при лечении ЖДА в течение 1 мес.
Основным критерием положительного ответа на терапию ЖДА является прирост уровня гемоглобина через 1 мес после начала применения препаратов железа, однако рекомендации разных организаций по этому вопросу не согласуются друг с другом. Минимальным приростом уровня гемоглобина в периферической крови для признания терапии эффективной является его увеличение более чем на 10 г/л за 1 мес (Центр по контролю и профилактике заболеваний в США) [39]. В нашем исследовании, проведенном при лечении 61 пациентки с гинекологической патологией и заболеваниями ЖКТ, у которых лечение привело к полному восстановлению показателей гемоглобина и обмена железа, прирост уровня гемоглобина в течение первого месяца составил от 10 до 50 г/л с медианой прироста 30 г/л [19]. Поэтому с учетом большого количества сопутствующих заболеваний у больных ЖДА и доказанной роли гепцидина в нарушении метаболизма железа за оптимальный критерий оценки эффективности терапии лучше принять прирост уровня гемоглобина более 10 г/л за 1 мес [5].
При отсутствии прироста уровня гемоглобина, согласно указанным критериям, необходимо обязательно исследовать обмен железа, провести диагностический поиск, исключить другой механизм развития анемии. При подтверждении абсолютного дефицита железа и отсутствии злокачественной опухоли следует перейти на парентеральное применение препаратов железа со строго рассчитанной терапевтической дозой. При назначении препаратов парентерально предпочтение следует отдавать внутривенному пути введения. Наиболее часто в настоящее время используются венофер (100 мг в 5 мл), космофер, феринъект (50 мг в 1 мл). За один раз, как правило, вводят 100—200 мг, но, используя феринъект, это количество можно увеличить до 1000 мг. Эти препараты должны применяться только при наличии показаний, доказанном абсолютном дефиците железа и невозможности перорального применения. Существенным недостатком парентерального применения является то, что необходимо использовать строго рассчитанное количество препарата, врач может назначать препараты только в условиях стационара, применение препаратов ограничено из-за наличия большого количества тяжелых побочных реакций (анафилактический шок, аллергические реакции, передозировка железа, системный гемосидероз, локальный гемосидероз тканей). Кроме того, как правило, есть ограничения парентерального применения препаратов при беременности, особенно в ранние сроки.
В случае отсутствия гипоферритинемии есть основания проводить лечение анемии с использованием препаратов рекомбинантного человеческого эритропоэтина, эффективность которого доказана при терапии ЖДА в поздние сроки беременности [28] и у больных с миомой матки [40, 41]. Такую тактику необходимо выбирать у больных с доказанными хроническими воспалительными или инфекционными заболеваниями, доброкачественными опухолями при наличии синдрома неадекватной степени тяжести анемии выработки эритропоэтина [5, 19, 28].
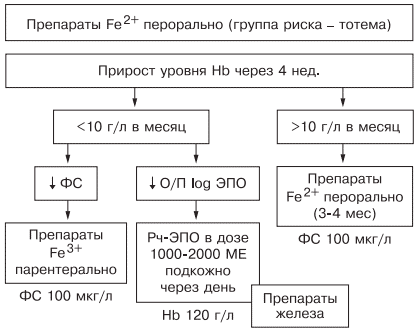
Таким образом, оптимальным у больных с наличием гипохромной микроцитарной анемии является выявление причины развития дефицита железа, после чего следует начинать лечение. Если есть сомнения в железодефицитном характере анемии, лучше проверить обмен железа, подтвердив диагноз ЖДА низкими показателями ФС и насыщения трансферрина железом. Далее следует устранить хроническое заболевание, остановить кровотечение, убрать погрешности в диете и начать пероральный прием препаратов железа (с обязательным учетом противопоказаний). Лечение следует начинать с двухвалентных препаратов железа. При наличии хронических воспалительных, пролиферативных, инфекционных заболеваний лучше использовать жидкую лекарственную форму (препарат тотема), содержащую в своем составе глюконат двухвалентного железа, медь и марганец. Через 1 мес следует определить прирост уровня гемоглобина и если он выше 10 г/л в месяц — продолжить лечение, если нет — пересмотреть диагноз (рис. 6).
Рис. 6. Схема лечения ЖДА.
При использовании препаратов железа необходимо ориентироваться на показатель ФС, целевое значение которого должно составлять около 100 мкг/л, после чего можно остановить лечение (поздние критерии эффективности терапии [39]). При пероральном приеме препаратов достаточно подтвердить нормализацию содержания ФС через 3 мес терапии, при назначении препаратов железа внутривенно этот показатель необходимо проверять каждую неделю. Лечение препаратами рекомбинантного человеческого эритропоэтина опасно из-за возможности развития эритроцитоза и тромботических осложнений, поэтому ориентироваться прежде всего необходимо на уровень гемоглобина, целевая концентрация которого не должна превышать 120 г/л [42].
Таким образом, ЖДА представляет собой важную социально значимую проблему, а ее диагностика и лечение до сих пор являются трудной задачей. Только выполнение современных рекомендаций позволит существенно повысить качество и эффективность оказания медицинской помощи больным ЖДА.
Сведения об авторах:
Российский университет дружбы народов, Москва
Кафедра госпитальной терапии с курсом клинической лабораторной диагностики Стуклов Николай Игоревич — д-р мед. наук, проф. кафедры; руководитель курса гематологии;
Семенова Елена Николаевна — учебный мастер кафедры.
источник

Рассмотрены подходы к лечению железодефицитной анемии у женщин. Во многих случаях внутривенный путь введения железа является гораздо более эффективным, в отличие от перорального приема, так как обеспечивает возможность быстрого насыщения организма дефицит
Approaches to treatment of iron-deficiency anemia in women were considered. In many cases, the method of intravenous iron administration is much more effective than oral intake, as it provides for fast saturation of the organism with lacking iron. Most of all, it is important in treatment of anemia against the background of chronic diseases.
Анемия — патологическое состояние, характеризующееся уменьшением концентрации гемоглобина и нередко сопровождающееся снижением числа эритроцитов в единице объема крови [1]. Согласно данным Минздрава РФ за последние 10 лет частота анемий увеличилась в 6,3 раза, причем наиболее распространенной является железодефицитная анемия (ЖДА) (около 90% всех анемий). ЖДА — это гипохромная микроцитарная анемия, возникающая вследствие снижения содержания железа в организме и представляющая собой самостоятельную нозологическую форму [2].
В клинической практике наиболее распространена следующая классификация анемий:
1) анемия, обусловленная острой кровопотерей (постгеморрагические);
2) анемия вследствие нарушения продукции эритроцитов (апластические, железодефицитные, мегалобластные, сидеробластные и др.);
3) анемия вследствие повышенного разрушения эритроцитов (гемолитические).
В зависимости от выраженности снижения уровня гемоглобина выделяют три степени тяжести анемии:
- легкая — уровень гемоглобина выше 90 г/л;
- средняя — гемоглобин в пределах 90–70 г/л;
- тяжелая — уровень гемоглобина менее 70 г/л.
Распространенность у женщин детородного возраста железодефицитных состояний (ЖДС) в некоторых регионах Российской Федерации достигает 30–60%, а согласно данным Всемирной организации здравоохранения в мире общее число лиц с дефицитом железа составляет около 600 млн человек [3]. ЖДС выступают причиной увеличения восприимчивости к острым респираторным вирусным инфекциям и снижения работоспособности.
В гинекологии различают три стадии ЖДС в организме:
- Прелатентный дефицит железа — скрытый дефицит железа, организм аккумулирует железо при помощи ферритина — железосодержащего белка. Если его показатель низкий, то говорят о наличии прелатентного дефицита железа.
- Латентный дефицит железа — на данной стадии, наряду с ферритином, истощаются тканевые запасы железа при оптимальных показателях гемоглобина, не наблюдается клинических симптомов дефицита железа, в кишечнике происходит компенсаторное повышение всасывания железа, активность железосодержащих ферментов постепенно снижается.
- Явный дефицит железа характеризуется уменьшением числа эритроцитов и снижением уровня гемоглобина, который входит в состав эритроцитов и представляет собой вещество, транспортирующее кислород к тканям организма из легких, развитием дистрофических изменений в органах и тканях, а также повышенным количеством протопорфирина в эритроцитах [2, 4].
Высокая распространенность анемий среди женщин связана с тем, что женский организм испытывает всегда недостаток железа из-за регулярных кровопотерь. Человеческий организм устроен так, что может восстановить из пищи лишь 2 мг этого минерала в сутки, при условии полноценного питания (употребления в пищу достаточного количества овощей и мяса) [2]. Таким образом, менструальные кровопотери, несмотря на свою «объективность», могут послужить причиной развития дефицита железа в организме женщины. Во время менструаций нормальная кровопотеря составляет 30–50 мл, организм при этом теряет от 15 мг железа [4, 5]. А в случае если менструации обильные и длятся свыше 7 дней, то потери железа составляют более 50 мг. Как следствие, в таких случаях потребность в железе возрастает во много раз [6].
Дефицит железа наблюдается чаще у женщин в возрасте 30–40 лет. Как правило, это происходит в процессе беременности и кормления грудью (как плод, так и грудной ребенок непосредственно получают железо от матери). Также нельзя забывать о потере крови в течение родов. Женщины могут не подозревать о наличии у себя подобной проблемы, хотя регулярно сдают анализ крови во время беременности. Недостаток железа в организме диагностируется, к сожалению, лишь на третьей стадии. Большинство женщин достаточно быстро утомляются и чувствуют разбитыми себя уже при незначительном снижении уровня ферритина. В организме при недостатке железа возникает головокружение и головные боли.
Для того чтобы пополнить запасы железа и при нормальном эритропоэзе восстановить кровопотерю, достаточно содержащегося в пище железа. При заместительной гормональной терапии стимулирующими эритропоэз препаратами адекватное поступление в организм железа оптимизирует назначенное лечение. Следует отметить, что во многих случаях внутривенный путь введения железа более эффективен, чем пероральный, так как обеспечивает возможность быстрого насыщения организма необходимым ему железом [7]. Это особенно важно при лечении анемии, протекающей на фоне хронических заболеваний. Внутривенный путь введения железа помогает преодолеть блокировку всасывания железа из желудочно-кишечного тракта (ЖКТ) и создать его запас в организме.
ЖДА в настоящее время является социальным заболеванием с достаточно широкой распространенностью. У беременных женщин представляет собой состояние, обусловленное сокращением содержания железа в костном мозге и сыворотке крови в связи с его большими затратами на формирование фетоплацентарного комплекса, а также перераспределением в пользу плода. Естественным следствием дефицита железа выступает нарушение образования гемоглобина с развитием как гипохромной анемии, так и трофических расстройств тканей.
ЖДА остается серьезной патологией в современной гинекологии, так как частота данного заболевания не снижается. У беременных частота анемии варьирует в пределах 15–80%, а у 98% женщин анемия во время беременности носит выраженный железодефицитный характер [2, 8].
Сбалансировать в женском организме содержание железа способны только железосодержащие препараты.
Нехватка ферментов, содержащих в своем составе железо, может в организме беременной женщины вызвать разнообразные трофические изменения. Наряду с этими изменениями наблюдается появление трещин в уголках рта, желтизна ладоней, ногти становятся хрупкими, выпадают волосы и др. Это заболевание иногда проявляется «экзотическими» гастрономическими пристрастиями. В тяжелой форме развития дефицита железа может наблюдаться понижение или повышение артериального давления, отечность, сердцебиение, а также сердечная недостаточность. Повышается объем циркулирующей крови, возрастает потребность в кислороде, и, как следствие, дефицит железа осложняет ход беременности и родов, что в свою очередь крайне негативно влияет на развитие плода.
К основным факторам риска возникновения и развития у беременных ЖДА относят наличие до беременности хронических заболеваний или анемии, хронические заболевания внутренних органов или инфекционные болезни, многоплодие, ранний токсикоз, уровень гемоглобина меньше 120 г/л в I триместре, длительность менструаций в течение нескольких лет до беременности более 5 дней [9].
Ежесуточно женщина потребляет с пищей от 10 до 20 мг железа, из которых полностью усваивается менее 2 мг, а за время менструации до 75% здоровых женщин теряют от 20 до 30 мг железа [10, 11]. Данное количество железа не может усвоиться даже при его большом содержании в пище. Таким образом, возникает дисбаланс, приводящий к развитию анемии.
При беременности, родах и кормлении грудью совокупная потеря железа составляет приблизительно 1 г, и для того чтобы пополнить запас железа исключительно из пищевых источников, женскому организму требуется примерно 4 года. Следовательно, если женщина рожает ребенка повторно в этот срок, у нее неизбежно развивается дефицит железа [5].
Современные клинические рекомендации включают в себя необходимость приема железосодержащих препаратов всем беременным во II и III триместрах гестации. Для взрослых небеременных женщин суточная доза (18 мг железа) в наиболее редких случаях покрывается исключительно за счет питания [4, 9]. Именно поэтому к началу беременности практически у половины всех женщин резервы железа минимальны.
Согласно современным данным, в конце гестационного процесса дефицит железа развивается без исключения у всех беременных как в скрытой, так и в явной форме. Главным образом это связано с тем, что беременность всегда сопровождается дополнительными потерями железа: 320–500 мг железа расходуется на возросший клеточный метаболизм и прирост гемоглобина, 50 мг железа — на увеличение размеров матки, 100 мг железа — на построение плаценты, 400–500 мг железа — на потребности плода [6].
В итоге плод с учетом запасного фонда обеспечивается в достаточном количестве железом, но у беременных при этом часто развиваются ЖДС различной степени тяжести. Для оценки соответствия запаса железа норме определяется уровень ферритина сыворотки крови, который при своих значениях менее 30 мкг/л считается сниженным.
Сниженная дородовая концентрация гемоглобина (особенно дефицит железа) выступает фактором риска послеродовых кровотечений, коррелируя с тяжестью состояния женщины на ее фоне. Применяя в дородовый период препараты внутривенного железа для коррекции ЖДА, врачи стремятся минимизировать как риск развития кровотечений, так и потребность переливания препаратов крови в перинатальный период. В постнатальный период (от 0 до 6 месяцев) дефицит железа отмечается у 13% матерей, а у 10% женщин диагностируют анемию. Пероральные формы препаратов железа при этом достаточно медленно действуют и часто не дают необходимого эффекта [2, 11].
Внутривенное железо, бесспорно, выступает безопасной альтернативой, снижая как необходимость переливаний крови, так и их объем. Лечение с помощью внутривенных препаратов железа позволяет достичь существенного увеличения запасов железа и значительно повысить концентрацию гемоглобина в крови.
За исключением тяжелых случаев, ЖДА лечится во время беременности амбулаторно. Врачи для ее лечения назначают прием лекарственных средств с содержанием данного элемента. Как правило, их употребляют длительное время (от 15 недель до 6 месяцев). Уровень гемоглобина в крови поднимается плавно, не ранее третьей недели от начала лечения. Показатель приходит в норму примерно через 2 месяца от начала терапии [9, 11]. Одновременно улучшается состояние здоровья и самочувствие женщины. Однако важно не прерывать курс лечения, так как при увеличении срока беременности плод также растет и его потребности в железе, соответственно, тоже повышаются.
Не стоит забывать и о предстоящих женщине родах, которые, в свою очередь, влекут значительную растрату сил и кровопотерю. Далее наступает период грудного кормления ребенка, вызывающий также нехватку железа. Поэтому специалисты рекомендуют в послеродовой период продолжать поддерживающее лечение с помощью препаратов железа еще 6 месяцев [11, 12]. Для того чтобы определить недостаток железа в женском организме вовремя, симптомы следует рассматривать как в комплексе, так и по отдельности.
Современные исследования показали высокую потребность в переливании компонентов крови пациенткам с тяжелыми маточными кровотечениями, что повышает стоимость госпитализации и снижает в целом качество жизни. Пероральный прием железосодержащих препаратов в целях устранения ЖДС у женщин с меноррагиями позволяет избежать трансфузий эритромассы во всех известных случаях, кроме выраженного падения уровня гемоглобина, когда пероральные формы не могут полностью компенсировать потери железа [12].
На сегодняшний день в России, к сожалению, широкое распространение получили лекарства, содержащие большое количество железа при расчете на одну таблетку. Токсические эффекты терапии, проявляющиеся при этом, считались неизбежными, и с целью их предотвращения, как правило, рекомендовался прием лекарственного средства во время еды для связки свободных ионов железа и предотвращения тем самым их отрицательного влияния на ЖКТ. Парадокс очевиден: рекомендовались значительные дозы железа, связывание железа белками пищи одновременно с этим снижало во много раз его поступление. Терапевтический эффект в результате не зависел никаким образом от высокой дозы железа в лекарстве [5, 6].
При выборе содержащего железо препарата необходимо учитывать ряд факторов. Так как ионизированное железо из ЖКТ всасывается исключительно в двухвалентной форме и огромную роль в данном процессе играет аскорбиновая кислота, то крайне важно наличие ее в препарате. В гемопоэзе большое значение принадлежит фолиевой кислоте, которая усиливает нуклеиновый обмен. Также для нормального обмена фолиевой кислоты важен цианокобаламин, выступающий ключевым фактором при формировании из нее активной формы.
Дефицит данных веществ, возникающий достаточно часто при связанных с кровопотерями анемиях, приводит к нарушениям синтеза ДНК в кроветворных клетках, в то время как включение данных компонентов в лекарственное средство повышает активную абсорбцию в кишечнике железа и его дальнейшую утилизацию, освобождает дополнительное число ферритина и трансферрина [13]. Как следствие, скорость синтеза гемоглобина увеличивается, а эффективность терапии как ЖДА, так и других ЖДС повышается.
Единственным препаратом железа для внутривенного введения в СССР был Феррум Лек. В России для внутривенного восполнения дефицита железа разрешены следующие препараты: Венофер, КосмоФер и Ликферр (из них отечественный Венофер). Во многих странах используются препараты нового поколения с усовершенствованными характеристиками — Феринжект (железа карбоксимальтозат), Ферумокситол (наночастицы оксида супермагнитного железа) и Монофер (железа (III) гидроксид олигоизомальтозат 1000) [5, 13, 14].
Датская фармацевтическая компания, являющаяся мировым экспертом в разработке железосодержащих препаратов, создала новый высокоэффективный препарат железа для внутривенного использования, с минимальными ограничениями при назначении. Организация работает над клиническими программами с целью дальнейшего подтверждения безопасности, эффективности и удобства применения Монофера как современного средства лечения ЖДА.
Препарат Монофер (железа (III) гидроксид олигоизомальтозат 1000) был создан на базе технологии матричной структуры с чередующимися фрагментами олигоизомальтозата 1000 и железа (III) гидроксида, за счет чего обеспечивается низкая токсичность препарата [14, 15]. Благодаря низкой токсичности Монофер может быть назначен в высокой дозе, создавая возможность коррекции ЖДС всего за один визит.
К основным факторам безопасности Монофера можно отнести: отсутствие тест-дозы, низкий риск анафилактических реакций, минимальный риск токсичности, обусловленный наличием в составе препарата свободного железа. Удобство применения Монофера основано на возможности высокой (до 20 мг/кг) и быстрой (до 60 мин) скорости инфузии за счет низкой токсичности препарата [15].
Матричная структура препарата включает прочно связанное и стабильное железо, способствуя медленному и контролируемому высвобождению железосодержащих белков биоактивного железа с минимальным риском токсичности из-за присутствия свободного железа (рис.) [10].
Препараты железа нового поколения имеют в своем составе меньшее содержание свободного железа, в отличие от старых препаратов железа. Монофер предоставляет для каждого пациента с ЖДА удобную дозировочную линейку в виде:
- внутривенной капельной инфузии: 200–1000 мг (назначается 1 раз в неделю до полного достижения восстановления дефицита железа):
а) 11–20 мг/кг — 60 минут (необходимо добавить от 100 до 500 мл стерильного раствора NaCl 0,9%);
б) 6–10 мг/кг — 30 минут;
в) 0–5 мг/кг — 15 минут;
- внутривенной болюсной инъекции: 100–200 мг в неделю до 3 раз (скорость — 50 мг/мин). Может быть также растворен в 10–20 мл стерильного раствора 0,9% NaCl [12].
Если необходимость пациента в восполнении железа превышает показатель 20 мг/кг, доза Монофера должна быть обязательно разделена и назначена с временным интервалом, как минимум, в одну неделю. Инфузии препарата более 1000 мг назначаются исключительно в госпитальных условиях. Препарат должен назначаться больным с диагнозом ЖДА, подтвержденным соответствующими лабораторными данными (результаты определения концентрации гематокрита и гемоглобина, ферритина сыворотки, количества эритроцитов и их параметров — среднего содержания в эритроците гемоглобина, среднего объема эритроцита или средней концентрации в эритроците гемоглобина).
Следует отметить, что в одном шприце Монофер можно смешивать исключительно со стерильным физиологическим раствором. Другие терапевтические препараты и растворы для введения добавлять запрещено, так как существует риск не только преципитации, но и другого фармацевтического взаимодействия.
Важно избегать проникновения препарата в околовенозное пространство, поскольку его попадание за границы сосуда приводит к коричневому окрашиванию кожи и некрозу тканей. В случае развития подобных осложнений для ускорения вывода железа и предотвращения его более глубокого проникновения в близлежащие ткани рекомендуется нанести гепаринсодержащий препарат на место инъекции (мазь или гель наносят не втирая, легкими движениями) [16].
Противопоказания к применению препарата:
- не связанная с дефицитом железа анемия (например, гемолитическая анемия);
- высокая чувствительность к активному веществу и входящим в состав препарата вспомогательным веществам;
- наличие различных признаков перегрузки железом (гемосидероз, гемохроматоз) или нарушение процессов утилизации железа;
- ревматоидный артрит в сочетании с симптомами активности воспалительных процессов;
- цирроз и гепатит печени (стадия декомпенсации);
- бактериемия;
- детский возраст менее 18 лет (по причине недостаточности доказанных данных о безопасности и эффективности) [3].
Препараты железа, вводимые парентерально, могут вызвать реакции повышенной чувствительности, в частности анафилактический шок, в связи с риском развития аллергических реакций у больных экземой, поливалентной аллергией, бронхиальной астмой, аллергическими реакциями на другие парентеральные препараты железа, с системной красной волчанкой, острыми и хроническими инфекционными заболеваниями, ревматоидным артритом и др. применение препарата ограничено. Также возможны эпизоды внезапного значительного снижения артериального давления при высокой скорости введения Монофера.
Таким образом, применение препарата рекомендовано в клинически оправданных случаях. Важно тщательно оценить отношение польза/риск для решения вопроса о использовании Монофера при беременности. Если для матери предполагаемая польза превышает риск для плода, то лечение можно проводить во II и III триместрах беременности. Не рекомендуется применение препарата в I триместре беременности [3, 17].
Выделение Монофера с грудным молоком на сегодняшний день не установлено. Следовательно, препарат в период лактации можно применять.
Монофер не должен одновременно назначаться с различными лекарственными формами железа для приема внутрь, так как их совместное употребление способствует сокращению всасывания железа из ЖКТ. Лечение пероральными препаратами железа начинают не ранее чем спустя 5 дней после последней инъекции. Препарат отличается хорошей переносимостью и обладает низкой токсичностью. В связи с этим риск передозировки минимален. Однако передозировка может развиваться из-за острой перегрузки железом или кумуляции железа и выражается симптоматикой гемосидероза. Контроль содержания в организме железа проводят, определяя степень концентрации ферритина.
Полученные результаты исследований показали, что профилактика анемии у женщин препаратом Монофер способствует сокращению частоты развития различных заболеваний, ассоциированных с дефицитом железа [18]. Кроме того, на фоне отсутствия ЖДА исчезает циркуляторная и гемическая гипоксия, что, в свою очередь, предупреждает развитие метаболических расстройств и приводит к уменьшению частоты осложнений, таких как фетоплацентарная недостаточность, гестоз, преждевременные роды и аномалии родовой деятельности. Отсутствие у препарата тяжелых побочных эффектов и удобный режим дозирования указывают на хорошую переносимость Монофера.
Таким образом, среди основных преимуществ Монофера в гинекологии можно выделить следующие: широкий спектр показаний для назначения, удобное дозирование и высокий профиль безопасности. Применение Монофера обеспечивает высокую эффективность как профилактики, так и лечения ЖДА.
На сегодняшний день существует большая доказательная база различных клинических исследований, подтверждающих эффективность и безопасность внутривенного введения железа при разнообразии клинических ситуаций, связанных с различными ЖДС. Анализ исследований, позволяющих сравнить результаты пероральной и внутривенной форм приема железа, свидетельствует о равной или более высокой эффективности последней формы. Также в современных исследованиях подчеркиваются такие недостатки пероральной формы введения железосодержащих препаратов, как побочные эффекты, несоблюдение предписаний врача, низкий уровень всасывания, а также и невозможность оперативного возмещения потери железа и поддержания его адекватной концентрации, характерных для пациенток с продолжающейся кровопотерей.
Внедрение в клиническую практику гидроксида изомальтозата 1000, не требующего тестовой дозы, с возможностью парентерального введения за короткое время высоких доз, несет в себе дополнительные преимущества в терапии препаратами, вводимыми внутривенно железа. Также, в отличие от пероральной формы, именно внутривенный путь введения препаратов железа позволяет преодолеть анемию, развивающуюся на фоне хронических заболеваний.
- Куликов А. Ю., Скрипник А. Р. Фармакоэкономический анализ лекарственного препарата «Монофер» в лечении железодефицитной анемии // Фармакоэкономика: теория и практика. 2016, 4: 183–186.
- Лебедев В. А., Пашков В. М. Принципы терапии железодефицитной анемии у гинекологических больных // Трудный пациент. 2013, 11: 3–7.
- Nordfjeld K., Andreasen H. Pharmacokinetics of iron isomaltoside 1000 in patients with inflammatory bowel disease // Drug. Des. Devel. Therapy. 2012, 6: 43–51.
- Малкоч А. В., Анастасевич Л. А., Филатова Н. Н. Железодефицитные состояния и железодефицитная анемия у женщин детородного возраста // Лечащий Врач. 2013; 4: 37–41.
- Мубаракшина О. А., Сомова М. Н., Любавская С. С. Фармакологическая коррекция дефицита железа и магния в период беременности. Воронежская государственная медицинская академия им. Н. Н. Бурденко. 2014; 4: 52–60.
- Подзолкова Н. М., Нестерова А. А. Железодефицитная анемия беременных // Русcкий медицинский журнал. 2003, 5: 326–331.
- Morrison J., Patel S. T., Watson W. Assessment of the prevalence and impact of anemia on women hospitalized for gynecologic conditions associated with heavy uterine bleeding // J. Reprod. Med. 2008, 5: 323–330.
- Протопопова Т. А. Железодефицитная анемия и беременность // Русский медицинский журнал. 2012; 17: 862–867.
- Чушков Ю. В. Современные возможности коррекции дефицита железа в акушерстве и гинекологии // Гинекология. 2011; 6: 44–47.
- Bhandari S. A hospital-based cost minimization study of the potential financial impact on the UK health care system of introduction of iron isomaltoside 1000 // Clin Risk Manag. 2011, 7: 103–113.
- Дворецкий Л. И. Алгоритмы диагностики и лечения анемий // Русcкий медицинский журнал. 2003, 8: 427–433.
- Coyne D. From anemia trials to clinical practice: understanding the risks and benefits when setting goals for therapy // Semin Dial. 2008, 21: 212–216.
- Лебедев В. А., Пашков В. М. Принципы терапии железодефицитной анемии у гинекологических больных // Трудный пациент. 2013, 11: 3–7.
- Gupta D. R., Larson D. S., Thomsen L. L. Pharmacokinetics of Iron Isomaltoside1000 in Patients with Stage 5 Chronic Kidney Disease on Dialysis Therapy. 2013, 03: 4172/2157–7609.
- Hildebrant P., Brunn N. et al. Effects of administration of iron isomaltoside 1000 in patients with chronic heart failure. A pilot study. Transfusion Alternatives in Transfusion Medicine // 2010, 11: 131–137.
- Locatelli F. Iron treatment and the TREAT trial // NDT +. 2011, 4: 13–15.
- Pasricha S. R., Flecknoe-Brown S. C. Diagnosis and management of iron deficiency anaemia: a clinical update. 2010, 9: 50–62.
- Philip A. Kalra, Sunil Bhandari, Sanjiv Saxena. A randomized trial of iron isomaltoside 1000 versus oral iron in non-dialysis-dependent chronic kidney disease patients with anaemia // Nephrol Dial Transplant. 2015, 3: 1–10.
А. З. Хашукоева* , 1 , доктор медицинских наук, профессор
М. И. Агаева*
М. З. Дугиева*, доктор медицинских наук
Т. Н. Сухова**
Л. И. Абдурахманова*
* ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ОСП РГНКЦ ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Современные подходы к лечению железодефицитной анемии у больных с гинекологической патологией/ А. З. Хашукоева, М. И. Агаева, М. З. Дугиева, Т. Н. Сухова, Л. И. Абдурахманова
Для цитирования: Лечащий врач №12/2017; Номера страниц в выпуске: 23-29
Теги: женщины, железо, внутривенные препараты
источник
.jpg)