ЖДА — заболевание, обусловленное истощением запасов железа в организме, что влечет за собой нарушение синтеза железосодержащих белков.
Заболевание проявляется снижением концентрации гемоглобина в крови и трофическими расстройствами в тканях.
По МКБ-10 D50 Железодефицитная анемия.
Эпидемиология. По данным экспертов ВОЗ, на земном шаре 700—800 млн человек страдают ЖДА или скрытым дефицитом железа.
Этиология.
Основные причины возникновения ЖДА:
1. Хронические и острые кровопотери (гиперполименорея, язвенная болезнь желудка, ДПК; опухоли желудка; опухоли тонкой кишки; опухоли толстой кишки; грыжа пищеводного отверстия диафрагмы; эзофагит; эрозивный гастрит; болезнь Крона; дивертикулез; геморрой, донорство). 2. Повышенная потребность в железе: период роста детей и подростков, беременные и кормящие женщины.
3. Нарушения всасывания железа в тонком кишечнике, аутоиммунный атрофический гастрит.
4. Алиментарные ЖДА развиваются при уменьшении в пищевом рационе продуктов, содержащих железо.
Патогенез. Истощение запасов железа ведет к уменьшению синтеза гемоглобина в эритрокариоцитах костного мозга, что приводит к снижению его концентрации, а затем и числа эритроцитов в единице объема крови.
Адаптационными механизмами являются увеличение сердечного выброса и усиленное высвобождение кислорода в тканях, происходящее в результате повышенной концентрации в эритроцитах 2-3-дифосфоглицировой кислоты.
При дефиците железа нарушается работоспособность мышц.
Причиной функциональной недостаточности мышц является сниженная активность железосодержащих ферментов, основное значение при этом отводится истощению запаса а-глицерофосфатдегидрогеназы.
При тяжелом дефиците железа могут развиться неврологические нарушения, извращение вкусовых ощущений и восприятия запахов, трофические нарушения (повышенная ломкость и выпадение волос, ломкость ногтей, сухость кожи, ангулярный стоматит и атрофический глоссит).
Клиническая картина. Клиническая картина складывается из проявлений сидеропенического синдрома, связанного с дефицитом железосодержащих ферментов, участвующих в окислительно-восстановительных процессах. Жалобы на слабость, головокружения, обмороки, сердцебиение, одышку, мышечную слабость, головную боль, парестезии.
Поражение кожи и слизистых (сухость и атрофичность кожи, ломкость ногтей и волос, выпадение волос, трещины слизистых).
Извращение вкуса и запахов (пристрастие к употреблению в пищу мела, зубной пасты, глины, сырой крупы, сырого кофе, неочищенных семян подсолнечника; пристрастие к запаху бензина, керосина, лака для ногтей (ацетон), запаху сырой глины, извести.
Неврологические нарушения: нарушение глотания твердой пищи, недержание мочи. При объективном осмотре — бледность кожи и слизистых оболочек, кожа сухая, истонченная, ногти уплощаются, а иногда становятся вогнутыми (ложкообразными) — койлонихии, явления ангулярного стоматита в углах губ и покраснение языка, сглаженность его сосочков.
Анемия носит гипохромный микроцитарный характер.
Количество ретикулоцитов — в пределах нормы.
Количество лейкоцитов, тромбоцитов и лейкоцитарная формула не изменены.
При тяжелом дефиците железа наряду с выраженной гипохромной (микроцитарной) анемией могут отмечаться легкая нейтропения и, реже, тромбоцитопения.
У взрослых больных с ЖДА средней или тяжелой степени могут наблюдаться умеренные тромбоцитозы.
ЖДА чаще бывают легкой или средней степени тяжести.
Диагностика. Основные критерии ЖДА: низкий цветовой показатель (0,6—0,7); гипохромия эритроцитов; анизоцитоз (уменьшенные по величине эритроциты) и пойкилоцитоз (изменение формы эритроцитов); снижение уровня сывороточного железа (менее 12 мкмоль/л); повышение общей железосвязывающей способности сыворотки (более 56 мкмоль/л); снижение содержания ферритина в сыворотке; клинические проявления гипосидероза (непостоянный признак); эффективность препаратов железа.
Наличие анемии гипохромного характера заставляет в первую очередь подозревать у больного ЖДА (все ЖДА также являются гипохромными!).
Однако факт гипохромии сам по себе не исключает других патогенетических вариантов анемий (не все гипохромные анемии являются железодефицитными!).
Так, например, гипохромная анемия может возникать при дефекте синтеза НЬ в результате нарушения включения в его молекулу железа при нормальном или даже повышенном уровне железа в сыворотке крови. Различать эти состояния и, тем самым, верифицировать ЖДА позволяет исследование содержания железа в сыворотке, которое следует выполнять обязательно до назначения больным лекарственных препаратов железа или проведения трансфузий эритроцитов.
Об этом должны быть осведомлены врачи, средний медицинский персонал (медицинские сестры, лаборанты), а также сами пациенты.
Наряду с определением содержания железа в сыворотке крови важным лабораторным показателем, определяемым при ЖДА, является общая железосвязывающая способность сыворотки, отражающая степень «голодания» сыворотки и насыщения белка трансферрина железом.
Общая железосвязывающая способность сыворотки при ЖДА всегда повышена в отличие от других гипохромных анемий, связанных не с дефицитом железа, а с нарушением его включения в молекулу гемоглобина или с перераспределением железа из эритроидных клеток в клетки макрофагальной системы (например, при активных воспалительных процессах).
Десфераловый тест (выделение железа с мочой) при ЖДА — ниже 0,2 мг/сут.
Снижение уровня железосодержащего белка ферритина — существенный диагностический критерий ЖДА с высокой специфичностью.
Ферритин характеризует величину запасов железа в организме.
Поскольку истощение запасов железа — обязательный этап формирования ЖДА, то уровень ферритина является одним из специфических признаков железодефицитного характера гипохромных анемий.
Следует, однако, иметь в виду, что наличие сопутствующего активного воспалительного процесса у больных ЖДА может маскировать гипоферритинемию.
Дополнительными методами определения запасов железа в организме могут быть подсчет числа эритроидных клеток костного мозга, содержащих гранулы железа (сидеробластов), и количество железа в моче после введения препаратов, связывающих железо, например, десфериоксиамина.
Количество сидеробластов при ЖДА значительно снижено, вплоть до полного их отсутствия, а содержание железа в моче после введения десфериоксиамина не увеличивается.
Патоморфология костного мозга. Картина гемопоэза в костном мозге у больных ЖДА мало чем отличается от таковой у здоровых лиц.
Может иметь место небольшая гиперплазия эритроидного ростка. Выявляется резкое снижение или полное отсутствие запасов железа в стромальных и макрофагальных элементах костного мозга, а также резкое уменьшение количества сидеробластов.
Дифференцировать ЖДА необходимо от других вариантов гипохромных анемий. Гипохромные микроцитарные анемии могут также наблюдаться при талассемии, сидеробластной анемии, пароксизмальной ночной гемоглобинурии, отравлении свинцом.
Дифференциальный диагноз ЖДА с малой талассемией проводится на основании отсутствия в случае последней лабораторных признаков дефи- цита железа и наличия патологического гемоглобина при электрофорезе гемоглобина.
Дифференциальный диагноз с сидеробластной анемией (вариант миелодиспластического синдрома) — на основании наличия в костном мозге более 20% сидеробластов.
При хроническом отравлении свинцом имеют место специфические включения в эритроцитах.
Гипохромная (чаще нормоцитарная, реже микроцитарная) анемия наблюдается на фоне хронических инфекционных и воспалительных заболеваний.
Гипохромная анемия на фоне хронических заболеваний развивается вследствие увеличения воспалительных цитокинов и роста продукции гепсидина, блокирующего процесс освобождения железа из депо.
Таким образом, для гипохромных анемий на фоне хронических заболеваний характерны следующие лабораторные показатели: нормальный или повышенный уровень ферритина в сочетании с пониженным содержанием сывороточного железа и трансферрина.
Лечение.
Важно выявить и по возможности устранить причину дефицита железа (оперативное лечение опухоли желудка, кишечника, лечение энтерита, коррекция алиментарной недостаточности и др.).
Для успешного лечения ЖДА должны быть использованы только лекарственные формы железа, восполнить необходимое количество железа путем поступления его из пищи даже теоретически невозможно из-за ограничения всасывания.
Из лекарственных источников у больных с ЖДА всасывание железа возрастает как минимум в 10 раз по сравнению со всасыванием железа из пиши, т. е. составляет 20—25 мг/суг.
При таком уровне всасывания повышение содержания гемоглобина происходит примерно на 1% вдень.
В ряде случаев радикальное устранение причины ЖДА не представляется возможным, например, при продолжающихся меноррагиях, наследственных геморрагических диатезах, проявляющихся носовыми кровотечениями, у беременных и в некоторых других ситуациях.
В таких случаях основное значение приобретает патогенетическая терапия железосодержащими лекарственными препаратами.
В клинической практике лекарственные препараты железа применяют внутрь или парентерально. Путь введения препарата у больных ЖДА определяется конкретной клинической ситуацией.
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний препараты железа следует назначать внутрь.
Лечение железодефицитной анемии продолжают до нормализации уровня гемоглобина в крови, затем в течение нескольких месяцев применяют препараты железа в меньших дозах для восстановления его запасов в депо.
В настоящее время все препараты железа можно разделить на две группы: ионные железосодержащие препараты (солевые, полисахаридные соединения железа) и неионные соединения, к которым относятся препараты гидроксид-полимальтозного комплекса трехвалентного железа.
Данная классификация основана на различии механизмов всасывания железа из ионных и неионных соединений.
Всасывание железа из ионных соединений происходит преимущественно в двухвалентной форме, так как активность утилизации железа из препаратов, содержащих соли трехвалентного железа, жестко лимитируется определенным уровнем рН желудочного сока (при высокой кислотности желудочного сока образуются труднорастворимые гидроксиды железа).
Вследствие этого наиболее часто используются двухвалентные солевые препараты железа, обладающие хорошей растворимостью, высокой диссоциационной способностью.
Следует отметить, что при своем восстановлении в трехвалентное железо в слизистой оболочке ЖКТ двухвалентные соли железа образуют свободные радикалы, обладающие повреждающим эффектом.
Именно с этим связаны побочные явления, наблюдающиеся при ферротерапии солями двухвалентного железа (гастроинтестинальные расстройства — боль, тошнота, рвота, диарея).
Препараты нового поколения, представляющие собой многомолекулярные комплексы гидроокиси трехвалентного железа, практически лишены этого побочного эффекта, так как не требуют восстановления и соответственно не вызывают образования свободных радикалов.
Они намного лучше переносятся, практически не сопровождаются гастроинтестинальными расстройствами и более безопасны.
При этом по биодоступности они не уступают препаратам солей двухвалентного железа.
При жедезодефицитных состояниях для синтеза НЬ требуется 50—100 мг железа ежедневно.
Поскольку при пероральном применении препаратов железа абсорбироваться может только 25% принятой дозы, то для быстрой коррекции недостатка железа в организме его необходимо применять в дозе 200—400 мг вдень.
При появлении желудочно-кишечных расстройств возможно снижение дозы железа, однако в этом случае дефицит железа устраняется медленнее.
Железа глюконат назначают внутрь, после еды, по 4-6 таблеток в день; железа сульфат — после еды, по 0,3—0,5 г 3—4 раза в день.
Железа фумарат — натощак по 1 капсуле вдень; при недостаточном эффекте возможен прием по I капсуле 2 раза в день.
Прием продолжают и после нормализации картины крови. Продолжительность насыщающего курса терапии не менее 1-1,5 мес.
Железа хлорид принимают по 4-6 мг/кг массы тела в сутки, дозу делят на 3—4 приема.
Мальтофер — 100 мг 2—3 раза в день.
Феррум Лек — 100 мг 2-3 таблетки в день.
Основными принципами лечения препаратами железа для приема внутрь являются следующие:
— назначение препаратов железа с достаточным содержанием двухвалентного железа;
— назначение препаратов железа, содержащих вещества, усиливающие всасывание железа;
— нежелательность одновременного приема пищевых веществ и лекарственных препаратов, уменьшающих всасывание железа;
— нецелесообразность одновременного назначения витаминов группы В, В12, фолиевой кислоты без специальных показаний;
— избегать назначения препаратов железа внутрь при наличии признаков нарушения их всасывания в кишечнике;
— достаточная продолжительность насыщающего курса терапии (не менее 1 — 1,5 мес);
— необходимость проведения поддерживающей терапии препаратами железа после нормализации показателей гемоглобина в соответствующих ситуациях.
Лечение пероральными препаратами следует проводить до нормализации содержания гемоглобина, а затем еще в течение 2 мес в половинной дозе для пополнения запасов железа в депо.
Длительное бесконтрольное применение больших доз может привести к гемосидерозу внутренних органов.
Препараты для парентерального введения необходимо использовать лишь у отдельных больных. Чаще используют препараты феррум-лек для в/м введения (полиизомальтоза) и для в/в (натрий-сахаратный комплекс); ектофер (сорбитовый цитратный комплекс) для в/м и венофер (сахарат железа) для в/в введения.
В одной ампуле каждого из названных препаратов содержится 100 мг железа.
Показания для парентерального лечения препаратами железа: нарушение всасывания в кишечнике при тяжелых энтеритах; обширная резекция тонкой кишки; невозможность приема пероральных препаратов железа.
Применение парентеральных препаратов железа не позволяет реально сократить сроки лечения и ускорить подъем концентрации гемоглобина до желаемого уровня.
Ограничивают использование парентеральных препаратов железа высокий риск развития анафилактических реакций, гемосидероза внутренних органов и болезненных, нередко абсцедирующих инфильтратов в местах введения препарата.
Побочные действия при лечении препаратами железа: гиперемия лица, тошнота, головокружение, головная боль, кожные аллергические реакции. Реже — рвота, диарея, боли в животе, в спине, тахикардия, транзиторное снижение АД.
При в/м введении возможно развитие абсцессов в месте инъекции. Противопоказаны препараты железа при гемохроматозе, повышенной чувствительности к железу.
Парентерально нельзя назначать препараты железа при АГ, тяжелой коронарной недостаточности, аллергических заболеваниях кожи, выраженных нарушениях функций печени и почек.
Препараты железа окрашивают кал в темный цвет и иногда могут маскировать кровотечение; могут вызывать потемнение зубов.
Прогноз. При правильном лечении прогноз при ЖДА благоприятный.
Профилактика. Основным контингентом, нуждающимся в профилактике ЖДА, являются женщины с гиперполименореей.
Каждая девушка с момента установления менструального цикла нуждается в профилактическом приеме препаратов железа, если менструальное кровотечение продолжается более 5 дней без образования сгустков крови или более 3 дней с образованием сгустков крови.
Используются пероральные препараты железа в дозе 300 мг/сут, в течение 5 дней ежемесячно.
При наличии дополнительных показаний для этого могут быть использованы пероральные контрацептивы, имеющие специальную добавку препарата железа.
источник
Н.И. Стуклов, Е.Н. Семенова
ФГБОУ ВПО Российский университет дружбы народов, Москва
Рассмотрен современный взгляд на проблему железодефицитной анемии (ЖДА) с точки зрения эпидемиологии, этиологии, патогенеза. Описаны известные в настоящее время механизмы регуляции обмена железа, приведены наиболее важные данные литературы и результаты собственных исследований. Основываясь на рекомендациях по лечению больных ЖДА, авторы представляют описанный в литературе и собственный клинический опыт использования железосодержащих препаратов и рассматривают полученные результаты. В рамках статьи авторы объясняют механизмы низкой эффективности лечения при ЖДА и предлагают способы решения проблемы с учетом опубликованных в литературе последних научных исследований.
Ключевые слова: анемия; обмен железа; сидеропенический синдром; лечение железодефицитной анемии.
N.I. Stuklov, E.N. Semenova
Russian University of People’s Friendship, Moscow, Russia
Modern views of epidemiology, etiology and pathogenesis of iron deficiency anemia are considered. Mechanisms of iron metabolism regulation are described based on the most important literature data and the results of the authors ’ research. The authors present their own and literature clinical experience of using iron-containing drugs with reference to the existing recommendations on the treatment of iron deficiency anemia. Causes of low treatment efficiency are discussed and the ways to address this problem are proposed based on the published results of clinical research.
Key words: anemia; iron metabolism; sideropenic syndrome; treatment of iron deficiency anemia.
Анемии (греч. αναιμια — бескровие) определяются как ряд клинических состояний, связанных со снижением уровня гемоглобина менее 120 г/л у женщин и менее 130 г/л у мужчин; (ВОЗ, 2001) и (или) гематокрита ( менее 36,4% соответственно), что обусловлено уменьшением количества эритроцитов или содержания гемоглобина в них [1]. В настоящее время железодефицитная анемия (ЖДА) является самым распространенным состоянием, связанным со снижением уровня гемоглобина, поэтому ее признают государственной проблемой более чем в 100 странах мира, где разрабатываются программы, направленные на профилактику и снижение заболеваемости. ЖДА чаще выявляется у представителей наиболее социально значимых и незащищенных слоев населения — у женщин детородного возраста и детей. Количество больных анемией в указанных группах, по данным ВОЗ (2001), превышает 1 млрд [2]. В итоге ЖДА является причиной роста материнской и детской смертности [3].
Регуляция обмена железа.
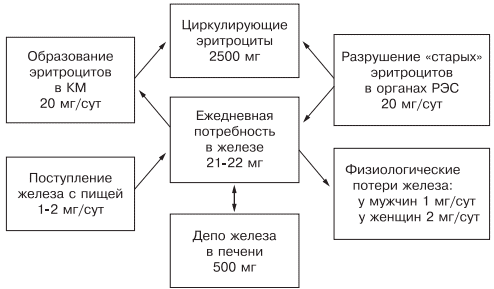
Ежедневно организму для нормальной жизнедеятельности требуется 20—25 мг железа, причем экзогенного железа необходимо только 1— 2 мг: женщинам — 2 мг (из-за физиологической кровопотери), а мужчинам — 1—1,5 мг. Около 20 мг железа поступает из «старых» разрушенных эритроцитов, столько же расходуется на синтез нового гемоглобина.
Железо накапливается в органах ретикулоэндотелиальной системы (до 500 мг), остальные запасы железа на 70% сосредоточены в гемоглобине, что и обусловливает развитие ЖДА при хронической кровопотере (рис. 1).
Рис. 1. Схема обмена железа.
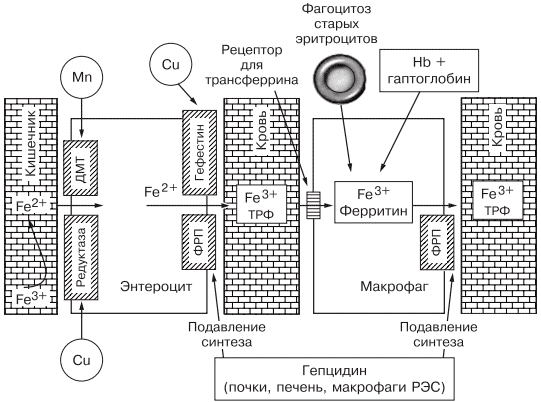
Всасывание железа происходит в верхних отделах тонкой кишки, причем этот процесс требует участия множества белков. В основном до 70—80% железа усваивается в двухвалентном состоянии (гемовое железо, содержащееся в основном в мясе, меньше — в печени и рыбе). При поступлении в кишечник растительного трехвалентного железа с помощью медьзависимой ферроредуктазы на апикальной мембране энтероцитов или под действием витамина С оно восстанавливается до двухвалентного. Двухвалентное железо через марганецзависимые белки — транспортеры двухвалентных металлов (ДМТ — двухвалентный металлотранспортер) поступает в энтероцит, а затем через белок ферропортин на базальной мембране — в кровь, где с помощью медьзависимых феррооксидаз (гефестина, расположенного на базальной мембране и связанного с ферропортином, и церулоплазмина, находящегося в плазме) окисляется до трехвалентного состояния, чтобы связаться с транспортным белком — трансферрином (рис. 2). Только очень незначительная часть железа, образуя комплекс с муцином, может поступить в энтероциты путем пиноцитоза [4, 5].
Рис. 2. Схема регуляции обмена железа.
Универсальным регулятором метаболизма железа является гепцидин [6—9], который блокирует транспорт железа, причем этот механизм реализуется с помощью регуляции активности белка ферропортина, т.е. путем воздействия на высвобождение железа из клеток кишечника и макрофагов ретикулоэндотелиальной системы [10—13]. Увеличение количества железа в организме ведет к стимуляции синтеза гепцидина, что уменьшает абсорбцию железа в кишечнике и его транспорт в циркуляцию. В свою очередь уменьшение абсорбции железа в кишечнике ведет к угнетению синтеза гепцидина в печени и по обратной связи — к восстановлению захвата железа из пищи и кишечника (см. рис. 2) [14—18]. Помимо железорегуляторной функции, гепцидин оказывает выраженное бактерицидное действие, является белком воспаления, его уровень повышается при инфекционных, воспалительных, опухолевых заболеваниях, блокируя выход железа в кровь [6]. Такой эффект гепцидина отрицательно влияет на рост бактерий, опухолей, блокирует избыточный воспалительный процесс. В работе, проведенной в 2011 г. [19], доказана роль гепцидина как основного фактора развития ЖДА у женщин с гинекологическими заболеваниями без патологической кровопотери. Показатели гепцидина в указанной группе составили 108,75 ± 40,08 нг/л (референсные значения 60— 85 нг/л), что обусловило резкое уменьшение содержания ферропортина — 0,43 ± 0,21 нг/л (референсные значения 3,1 ± 0,2 нг/л) и привело к нарушению поступления железа из кишечника в кровь [19].
Железо, которое остается внутри клеток, депонируется в виде ферритина, количество которого в крови прямо пропорционально содержанию железа в депо [20].
Клиническая картина и диагностические критерии.
Дефицит железа приводит к нарушению синтеза гемоглобина в эритрокариоцитах костного мозга, уменьшению содержания миоглобина в мышцах, активности цитохромов и каталаз в митохондриях клеток, миелопероксидазы в нейтрофилах [21—23].
В настоящее время выделяют несколько этапов развития дефицита железа [5, 24].
1. Предрасположенность к развитию дефицита железа (вегетарианство, подростковый возраст в сочетании с нарушением менструального цикла у девочек, частые роды, наличие хронических болезней желудочно-кишечного тракта — ЖКТ, заболеваний женской репродуктивной системы, связанных с кровопотерей).
2. Предлатентный дефицит железа. На этой стадии нет никаких лабораторных критериев дефицита железа, однако можно определить повышение абсорбции трехвалентного железа в ЖКТ, которое может превышать 50% (в норме 10—15%).
3. Латентный дефицит железа характеризуется развитием сидеропенического синдрома и уменьшением запасов железа в организме (по данным лабораторных исследований).
4. ЖДА. Диагноз устанавливается при уровне гомоглобина менее 120 г/л у женщин и 130 г/л у мужчин. Выделяют следующие стадии ЖДА:
В основе патологии эритропоэза при дефиците железа лежит нарушение синтеза гема, в результате которого уменьшается количество гемоглобина в эритрокариоцитах костного мозга, что проявляется на первом этапе гипохромией эритроцитов, а в дальнейшем — развитием гипохромной микроцитарной анемии.
Клинические проявления ЖДА связаны с развитием как сидеропенического синдрома, для которого характерны выраженная мышечная слабость, нарушение целостности слизистых оболочек, кожи, ее придатков (ломкость и расслаивание ногтей, выпадение волос), снижение иммунитета, так и непосредственно симптомов анемии (головокружение, мелькание «мушек» перед глазами, сонливость, снижение работоспособности).
Наиболее характерным лабораторным признаком ЖДА являются гипохромия, микроцитоз эритроцитов, анизоцитоз. О гипохромии эритроцитов свидетельствуют цветовой показатель менее 0,8, среднее содержание гемоглобина в эритроците менее 28 пг, средняя концентрация гемоглобина в эритроците менее 290 г/л. О микроцитозе говорят, когда средний диаметр эритроцита менее 7 мкм, а средний объем эритроцита — менее 80 фл [21, 22, 24].
Параметры обмена железа широко используются в клинической практике, но в связи с отсутствием четко определенных значений, доказывающих наличие ЖДА, высокой стоимостью исследования и большим количеством больных их применение не всегда оправдано. Так, показатель ферритина сыворотки (ФС) как единственный маркер, отражающий запасы железа в организме и используемый для верификации и дифференциальной диагностики ЖДА, по мнению разных исследователей [5, 20], варьирует от 15 до 100 мкг/л. Известно, что показатель ФС является положительным маркером воспаления, а количество его определяется белково-синтетической функцией печени. В настоящее время для установления диагноза ЖДА принято считать достоверным показатель ФС менее 30 мкг/л [25]. Уровень такого транспортного белка, как трансферрин, как правило, повышен при недостатке железа, однако при наличии инфекции его содержание уменьшается и не может использоваться в диагностике ЖДА [26]. Тем более изменчивы такие параметры обмена железа, как железосвязывающая способность (общая и латентная) и коэффициент насыщения трансферрина железом, так как они рассчитываются исходя из содержания трансферрина и сывороточного железа, а последний показатель вообще не имеет связи с содержанием железа в организме и зависит от времени, в которое проведено исследование, и приема пищи [21]. Значения коэффициента насыщения трансферрина железом у больных ЖДА, по опубликованным данным, могут составлять от 15 до 20%. Наиболее точным методом диагностики ЖДА в настоящее время считается подсчет растворимых рецепторов для трансферрина, однако этот метод не используется в качестве рутинного из-за отсутствия единого способа детекции, высокой стоимости исследования, невозможности интерпретировать результат при наличии любых пролиферативных процессов [26].
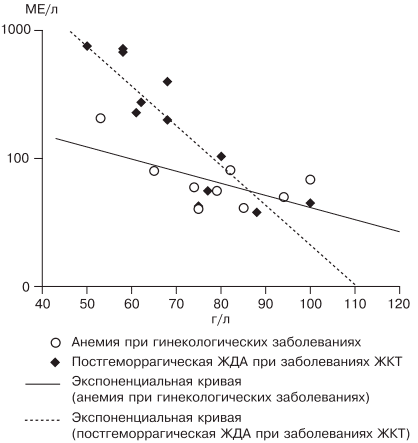
Наиболее частыми причинами ЖДА являются как физиологические, так и патологические состояния. В группу риска развития ЖДА входят недоношенные дети, так как у них не успевает сформироваться депо железа, и подростки, которым требуется больше железа в связи с быстрым ростом организма [27]. Наиболее часто ЖДА развивается при беременности. В период беременности, родов и лактации в среднем расходуется до 1000 мг железа, что в 2 раза больше его запасов в депо [28]. Репродуктивный возраст у женщин связан с повышенной потерей железа при менструациях; этот недостаток компенсируется увеличением всасывания железа в ЖКТ, что в настоящее время объясняется изменением влияния гепцидина. При наличии гиперполименореи, однако, такой баланс нарушается в связи с увеличением кровопотери [29, 30], при сопутствующих заболеваниях ЖКТ нарушается всасывание железа и развивается ЖДА [6, 19]. Часто у женщин меноррагии имеют органические причины: полипы, эндометрит, миома матки, аденомиоз, открывающийся в полость матки; мало того, такие заболевания, как миома матки и дисплазия шейки матки, оказывают влияние на развитие анемии и без патологической кровопотери [5, 19, 30]. Указанный механизм связан с увеличением содержания гепцидина в крови и снижением активности эритропоэза, доказанным синдромом неадекватной выработки эритропоэтина. В настоящее время продукцию эритропоэтина принято считать неадекватной при отношении определяемого эритропоэтина к предполагаемому (О/П log эритропоэтина менее 0,9) [28, 31]. Так, В.А. Бурлевым и Е.Н. Коноводовой [32] при обследовании женщин с миомой матки выявлено отношение О/П log эритропоэтина менее 0,8, а при обследовании гинекологических больных с анемией без нарушения менструальной функции в 2011 г. отношение О/П log эритропоэтина составило 0,89 (рис. 3). Для всех женщин с диагностированной ЖДА необходимо обязательное обследование у гинеколога. В случае обнаружении ЖДА у мужчин, наоборот, показано исключение заболеваний ЖКТ.
Рис. 3. Зависимость между уровнем гемоглобина и сывороточного эритропоэтина (логарифмическая шкала и экспоненциальные кривые) у больных с постгеморрагической ЖДА при заболеваниях ЖКТ (предполагаемый эритропоэтин) и анемии при гинекологических заболеваниях (определяемый эритропоэтин) [5].
Помимо повышенной потребности в железе и хронической кровопотери, патологическими состояниями, способными вызывать развитие ЖДА, являются различные нарушения всасывания железа и поступления его с пищей (в том числе и обусловленные вегетарианством), нарушения транспорта железа (гипотрансферринемии при заболеваниях печени и наследственные атрансферринемии) [21].
Таким образом, гипохромная микроцитарная анемия, особенно при наличии характерной для сидеропенического синдрома клинической картины, даже без исследования обмена железа может определяться как ЖДА при условии полноценного клинического и инструментального обследования больного и установления причины ее развития [5].
Лечение.
Современная тактика лечения при ЖДА в настоящее время направлена на устранение этиологического фактора и восполнение запасов железа в организме [4, 5]. Наиболее оправдано более физиологическое пероральное применение препаратов железа; парентерально препараты можно использовать только при доказанном дефиците железа. Перорально следует назначать препараты железа в высоких дозах (от 200 до 300 мг/сут), что, однако, может приводить к возникновению диспепсических явлений, поэтому (особенно в детской и акушерской практике) рекомендуется постепенное повышение дозы до терапевтической, а при достижении нормальных значений уровня гемоглобина — ее снижение [20].
Степень абсорбции двухвалентных солей железа в несколько раз выше, чем трехвалентных, так как они пассивно диффундируют через каналы ДМТ-белков [33], поэтому препараты, содержащие двухвалентное железо, дают быстрый эффект и нормализуют уровень гемоглобина в среднем через 1—2 мес, а нормализация депо железа происходит уже через 3—4 мес от начала лечения в зависимости от степени тяжести анемии и дозы препарата. Препараты, содержащие железо в трехвалентном состоянии, требуют более длительного применения, а в случае дефицита меди в организме будут неэффективны. Нормализация уровня гемоглобина при лечении препаратом трехвалентного железа наступит только через 2—4 мес, а нормализация показателей депо железа — через 5—7 мес от начала терапии [5, 19, 33]. Степень абсорбции отражается и на частоте развития побочных эффектов. Уменьшить нежелательное влияние таблетированных препаратов железа на ЖКТ можно, принимая их во время еды, но при этом уменьшается всасывание железа. Лучше (но также с потерей эффективности) использовать формы с замедленным высвобождением, так как часть препарата будет высвобождаться в нижних отделах ЖКТ, где железо практически не всасывается [34]. Несмотря на рекомендации ВОЗ по применению для лечения ЖДА препаратов двухвалентного железа как более эффективных, препараты с низкой биодоступностью на основе трехвалентного железа активно применяются благодаря их лучшей переносимости.
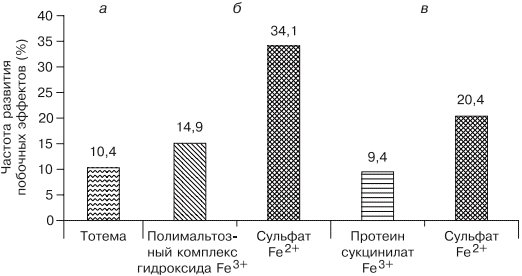
В современной клинической практике используются различные варианты сочетаний двухвалентного железа с витаминами С, В9, В12, что позволяет минимизировать побочные эффекты и одновременно повысить эффективность терапии, однако переносимость такого лечения до настоящего времени была основным лимитирующим фактором [20, 33]. Анализ переносимости различных препаратов железа более чем у тысячи пациентов показал, что современная жидкая форма двухвалентного железа (препарат тотема, лаборатория Иннотек Интернасиональ, Франция) по количеству побочных эффектов не превышает таковые у трехвалентного (рис. 4) [4]. Такой эффект достигается равномерным распределением препарата по слизистой оболочке желудка и его высокой биодоступностью. Двухвалентное железо равномерно и максимально эффективно проникает в энтероциты и, не накапливаясь в них, поступает в кровь. Это обусловлено наличием в составе препарата меди и марганца, которые входят в состав ДМТ-белков и гефестина, окисляющего железо, что способствует наилучшему его метаболизму (см. рис. 2) [33]. Помимо этого, указанные металлы участвуют в работе системы антиоксидантов, наиболее важными составляющими которой являются Cu, Zn-супероксиддисмутаза, Mn-супероксиддисмутаза (в митохондриях), каталаза, глутатионпероксидаза и глутатион. При уменьшении антиоксидантной защиты происходит сдвиг в сторону избыточного накопления свободных радикалов, что обусловливает их повреждающее действие на клетки. Следует понимать, что процесс активации перекисного окисления липидов запускается ионами двухвалентного железа, что проявляется частым развитием побочных эффектов при лечении препаратами железа. Наличие меди и марганца в составе тотемы уменьшает образование свободных радикалов, что улучшает переносимость препаратов железа [37].
Пациентам с заболеваниями ЖКТ назначать препараты железа перорально следует с осторожностью, причем острые заболевания, такие как язва желудка и двенадцатиперстной кишки, эрозивный гастрит, являются противопоказаниями; также не следует использовать указанный метод лечения у больных с заболеваниями тонкой кишки (болезнь Крона, целиакия, мальабсорбция) или отсутствием ее части.
Рис. 4. Сравнение результатов исследований безопасности применения различных железосодержащих препаратов.
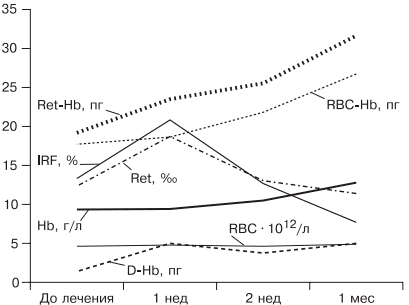
При лечении больных ЖДА остро стоит вопрос оценки эффективности терапии, так как часто ЖДА диагностируется у соматически тяжелых больных с крайне низким уровнем гемоглобина. Попытки ранней диагностики, как правило, связаны с исследованием количества ретикулоцитов [38], однако в настоящее время такой подход не является доказательным, так как часто ретикулоцитоз возникает компенсаторно при наличии кровотечения. В работе [5, 9] показано, что наиболее достоверными показателями, указывающими на хороший эффект препаратов железа, служат появление молодых форм ретикулоцитов и увеличение дельты гемоглобина (разницы между средним содержанием гемоглобина в ретикулоците и эритроците) уже через 1 нед после начала лечения (рис. 5).
Рис. 5. Динамика гемоглобина эритроцитов (RBC), количества ретикулоцитов (Ret), фракции незрелых ретикулоцитов (IRF-) среднего содержания гемоглобина в эритроците (RBC-Hb), среднего содержания гемоглобина в ретикулоците (Ret-Hb), дельты гемоглобина (D-Hb) при лечении ЖДА в течение 1 мес.
Основным критерием положительного ответа на терапию ЖДА является прирост уровня гемоглобина через 1 мес после начала применения препаратов железа, однако рекомендации разных организаций по этому вопросу не согласуются друг с другом. Минимальным приростом уровня гемоглобина в периферической крови для признания терапии эффективной является его увеличение более чем на 10 г/л за 1 мес (Центр по контролю и профилактике заболеваний в США) [39]. В нашем исследовании, проведенном при лечении 61 пациентки с гинекологической патологией и заболеваниями ЖКТ, у которых лечение привело к полному восстановлению показателей гемоглобина и обмена железа, прирост уровня гемоглобина в течение первого месяца составил от 10 до 50 г/л с медианой прироста 30 г/л [19]. Поэтому с учетом большого количества сопутствующих заболеваний у больных ЖДА и доказанной роли гепцидина в нарушении метаболизма железа за оптимальный критерий оценки эффективности терапии лучше принять прирост уровня гемоглобина более 10 г/л за 1 мес [5].
При отсутствии прироста уровня гемоглобина, согласно указанным критериям, необходимо обязательно исследовать обмен железа, провести диагностический поиск, исключить другой механизм развития анемии. При подтверждении абсолютного дефицита железа и отсутствии злокачественной опухоли следует перейти на парентеральное применение препаратов железа со строго рассчитанной терапевтической дозой. При назначении препаратов парентерально предпочтение следует отдавать внутривенному пути введения. Наиболее часто в настоящее время используются венофер (100 мг в 5 мл), космофер, феринъект (50 мг в 1 мл). За один раз, как правило, вводят 100—200 мг, но, используя феринъект, это количество можно увеличить до 1000 мг. Эти препараты должны применяться только при наличии показаний, доказанном абсолютном дефиците железа и невозможности перорального применения. Существенным недостатком парентерального применения является то, что необходимо использовать строго рассчитанное количество препарата, врач может назначать препараты только в условиях стационара, применение препаратов ограничено из-за наличия большого количества тяжелых побочных реакций (анафилактический шок, аллергические реакции, передозировка железа, системный гемосидероз, локальный гемосидероз тканей). Кроме того, как правило, есть ограничения парентерального применения препаратов при беременности, особенно в ранние сроки.
В случае отсутствия гипоферритинемии есть основания проводить лечение анемии с использованием препаратов рекомбинантного человеческого эритропоэтина, эффективность которого доказана при терапии ЖДА в поздние сроки беременности [28] и у больных с миомой матки [40, 41]. Такую тактику необходимо выбирать у больных с доказанными хроническими воспалительными или инфекционными заболеваниями, доброкачественными опухолями при наличии синдрома неадекватной степени тяжести анемии выработки эритропоэтина [5, 19, 28].
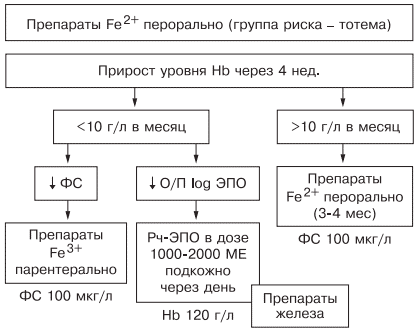
Таким образом, оптимальным у больных с наличием гипохромной микроцитарной анемии является выявление причины развития дефицита железа, после чего следует начинать лечение. Если есть сомнения в железодефицитном характере анемии, лучше проверить обмен железа, подтвердив диагноз ЖДА низкими показателями ФС и насыщения трансферрина железом. Далее следует устранить хроническое заболевание, остановить кровотечение, убрать погрешности в диете и начать пероральный прием препаратов железа (с обязательным учетом противопоказаний). Лечение следует начинать с двухвалентных препаратов железа. При наличии хронических воспалительных, пролиферативных, инфекционных заболеваний лучше использовать жидкую лекарственную форму (препарат тотема), содержащую в своем составе глюконат двухвалентного железа, медь и марганец. Через 1 мес следует определить прирост уровня гемоглобина и если он выше 10 г/л в месяц — продолжить лечение, если нет — пересмотреть диагноз (рис. 6).
Рис. 6. Схема лечения ЖДА.
При использовании препаратов железа необходимо ориентироваться на показатель ФС, целевое значение которого должно составлять около 100 мкг/л, после чего можно остановить лечение (поздние критерии эффективности терапии [39]). При пероральном приеме препаратов достаточно подтвердить нормализацию содержания ФС через 3 мес терапии, при назначении препаратов железа внутривенно этот показатель необходимо проверять каждую неделю. Лечение препаратами рекомбинантного человеческого эритропоэтина опасно из-за возможности развития эритроцитоза и тромботических осложнений, поэтому ориентироваться прежде всего необходимо на уровень гемоглобина, целевая концентрация которого не должна превышать 120 г/л [42].
Таким образом, ЖДА представляет собой важную социально значимую проблему, а ее диагностика и лечение до сих пор являются трудной задачей. Только выполнение современных рекомендаций позволит существенно повысить качество и эффективность оказания медицинской помощи больным ЖДА.
Сведения об авторах:
Российский университет дружбы народов, Москва
Кафедра госпитальной терапии с курсом клинической лабораторной диагностики Стуклов Николай Игоревич — д-р мед. наук, проф. кафедры; руководитель курса гематологии;
Семенова Елена Николаевна — учебный мастер кафедры.
источник
Железодефицитная анемия часто является лишь симптомом другого продолжающегося процесса заболевания, поэтому всегда необходимо определить ее причины, а после диагностики включить адекватное лечение. Учитывая симптомы, можно подобрать лечение железодефицитной анемии.
Почти 3,5 миллиарда человек, главным образом из развивающихся стран, страдают железодефицитной анемией. В России дефицитом железа страдают около 4% мужчин и 10% женщин. Это самый распространенный тип анемии в мире. Каждый год он приводит к гибели 850 000 человек.
Следует помнить, что симптомы железодефицитной анемии у женщин с аменореей требуют лечения, а также диагностики кровопотери в органах. Предполагается, что в 9% пациенты старше 65 лет с железодефицитной анемией могут иметь симптомы рака.
Типичный для железодефицитной анемии результат периферической крови с микроцитозом и гипохромией может также возникать при других типах анемии (например, при талассемии, анемии хронических заболеваний, сидеробластической анемии) и при отравлении свинцом. Поэтому необходимо точно диагностировать и корректировать соответствующее лечение.
Важнейшим элементом в лечении пациентов с железодефицитной анемией является определение причины дефицита этого элемента. Принципом лечения железодефицитной анемии является не только диагностика причины, но и пополнение запасов железа (0,5-1,0 г железа). Для достижения этой цели необходимо продолжать лечение железом в течение примерно 3-6 месяцев после отмены анемии.
Большинству пациентов лечение пероральными препаратами железа достаточно. На рынке существует много таких препаратов для лечения железодефицитной анемии у женщин: начиная с простых солей железа (например, сульфата, глюконата) и заканчивая формами длительного высвобождения.
Отдельные препараты железа отличаются содержанием элементарного железа. Средняя доза составляет около 150-200 мг элементарного железа в день, что определяет количество таблеток, которые пациент должен принимать в течение дня. Например, в случае препаратов глюконата железа, содержащих 0,0232 г ионов железа, пациент должен принимать 6 таблеток, в то время как при приеме препаратов сульфата железа, содержащих 0,1 г железа, — 2 таблетки.
Только сбалансированное и полноценное питание поможет добиться успехов в лечении железодефицитной анемии у детей. В некоторых случаях полезно кормить ребенка детским питанием с дополнительным содержанием железа.
Чтобы вылечить железодефицитную анемию у ребенка народными средствами, необходимо включить в его рацион травы: крапиву, шиповник, мяту и другие.
Некоторые препараты, доступные на рынке, также содержат аскорбиновую кислоту, которая облегчает поглощение железа. Следует помнить, что пациенты с нарушенной желудочно-кишечной проходимостью должны использовать препараты, которые быстро всасываются. Современное лечение железодефицитной анемии имеет альтернативы.
Пероральные препараты железа следует принимать натощак. Некоторые продукты, особенно содержащие танин (чай, какао), оксалаты, фитаты (крупы, орехи), фосфаты (сладкие напитки), могут ухудшить усвоение железа. Избегайте приема пероральных добавок железа с лекарствами, которые повышают рН в желудке.
Препараты железа могут вызвать раздражающие симптомы желудочно-кишечного тракта (тошноту, рвоту, диарею, запор, боль в животе).
В нормальных условиях через 4-7 дней после начала лечения наблюдается увеличение количества ретикулоцитов и (примерно через месяц) концентрации гемоглобина.
Наиболее распространенной причиной отсутствия ответа на лечение является несоблюдение терапевтических рекомендаций. Нарушение лечения также может быть вызвано нарушением абсорбции железа или неправильным диагнозом, включая непризнанную инфекцию Helicobacter pylori. Чтобы подтвердить нарушения абсорбции, необходимо провести измерение концентрации железа после введения препарата сульфата железа как лекарства при лечении железодефицитной анемии. Увеличение концентрации ниже 100 мкг указывает на аномальное поглощение. В нормальных условиях наблюдается увеличение в 20-30 раз относительно начальной концентрации.
При лечении железодефицитной анемии внутривенно применяют препараты только пациентам, не переносящим оральные формы или имеющим нарушения усвоения железа в желудочно-кишечном тракте. Этот тип лечения часто необходим пациентам, получающим эритропоэз-стимулирующие факторы.
У пациентов, получавших внутривенные препараты железа, рекомендуемая доза железа должна определяться на основе следующей формулы: масса тела (кг) х 2,4 х (концентрация целевого гемоглобина — концентрация гемоглобина пациента в настоящее время, г / дл) + 500 мг (или 1000).
Выбор препарата для внутривенного использования определяет тактику введения данной дозы — пациенты получают одну дозу сразу или несколько раз в более низких дозах. Вторая стратегия предпочтительна, например, пациентам, получавшим гемодиализ.
Важным осложнением использования внутривенных препаратов для лечения железодефицитной анемии являются анафилактические реакции, особенно часто при лечении декстраном железа. Поэтому вначале инфузии всегда следует вводить небольшую контрольную дозу (25 мг). В настоящее время уходят от внутримышечного введения препаратов железа. Эти инъекции были относительно болезненными, вызывая обесцвечивание и стерильные абсцессы в месте инъекции.
Лечение переливанием концентрата эритроцитов — это стандарт лечения железодефицитной анемии для пациентов с симптоматическим заболеванием, например, в форме сердечно-сосудистой недостаточности и, следовательно, требует немедленного вмешательства. Схема лечения железодефицитной анемии направлена на устранение последствий болезни.
Железодефицитная анемия по-прежнему является серьезной медицинской проблемой. Важно правильно идентифицировать ее причины, а затем решить, как лечить железодефицитную анемию предпочтительно на стадии дефицита, а не на стадии полномасштабной анемии. Успех лечения в значительной степени зависит от участия пациента в процессе заживления.
источник
Железодефицитная анемия — наиболее распространенный вид малокровия. По разным данным на него приходится от 80 до 90% всех анемий. Медицинские наблюдения говорят, что 30% взрослых людей имеют недостаток железа. У пожилых — 60%. Болезнь более распространена среди женского населения.
В Международной классификации болезней (МКБ-10) железодефицитную анемию можно найти в классе «Болезни крови… Анемии, связанные с питанием». Присвоенные коды предусматривают:
- вторичную форму анемии из-за хронической кровопотери (D 50.0);
- другие виды, в том числе неуточненные (D 50.8 и D 50.9).
Клинические классификации более удобны для понимания механизма заболевания и выбора лечения.
Установлено, что механизм заболевания связан с дефицитом минерала железа в крови. Его роль трудно преувеличить. Ведь из всего количества 70% непосредственно заняты в построении гемоглобина. Это значит, что железо — незаменимый материал для удержания эритроцитами молекул кислорода и последующего процесса переноса от легочных пузырьков в ткани.
Любой вариант недостатка железа приводит к снижению синтеза гемоглобина и кислородному голоданию всего организма.
Важно не только поступление минерала с пищей (в организме железо не вырабатывается), но и правильный процесс его усвоения и переноса.
За всасывание молекул железа из 12-перстной кишки отвечает специальный белок (трансферрин). Он доставляет Fe в костный мозг, где синтезируются эритроциты. Организм образует «склад» в печеночных клетках для быстрого восполнения в случае острого недостатка. Запасы хранятся в виде гемосидерина.
Если разложить все железосодержащие формы по частям, то получится следующее:
- 2/3 приходится на гемоглобин;
- на запасы в печени, селезенке и костном мозге в виде гемосидерина — 1 г;
- на транспортную форму (сывороточное железо) — 30,4 ммоль/л;
- на дыхательный фермент цитохромоксидазу — 0,3 г.
Накопление начинается во внутриутробном периоде. Плод забирает часть железа у материнского организма. Анемия матери опасна для формирования и закладки внутренних органов у ребенка. А после рождения малыш должен получать его только с пищей.
Выведение излишков минерала происходит с мочой, калом, через потовые железы. У женщин с подросткового возраста до климактерического периода есть еще путь менструальных кровотечений.
В сутки выводится около 2 г железа, значит поступать с пищей должно не меньшее количество.
От правильного функционирования этого механизма зависит поддержание нужного баланса для обеспечения тканевого дыхания.
Причины железодефицитной анемии упрощенно можно представить следующим образом:
- недостаток поступления железа;
- повышенный вывод;
- некомпенсированный расход;
- затрудненный перенос из кишечника в органы кроветворения.
Повышенный расход образуется:
- при большой физической нагрузке у спортсменов, при усиленных тренировках;
- у беременных женщин, в период лактации;
- при обильном потоотделении в жару, высокой лихорадке.
Нормы в 2 г становится недостаточно.
Заболевания кишечника, связанные с поносами и нарушенной всасываемостью, способствуют недостатку усвоения железа из пищи. Подобные осложнения разной степени тяжести ожидаемы после операций удаления части желудка, двенадцатиперстной кишки. Потому что именно в желудке и 12-перстной кишке происходит соединение железа с соляной кислотой и связывание его белком-переносчиком трансферрином. Значительное влияние оказывает состояние поджелудочной железы. При панкреатитах функция всасывания нарушается.
Наиболее распространенной причиной считается хроническая кровопотеря. Она сначала протекает скрытно (латентный период), затем вызывает клинические признаки. Источниками подобной кровопотери являются:
- желудок и кишечник (язвенная болезнь, некротический колит, анальные трещины, варикозные вены пищевода и геморрой, злокачественные опухоли);
- заболевание половых органов у женщин (дисфункциональные маточные кровотечения, опухоли матки, эндометриоз);
- длительное кровохарканье (туберкулез легких, злокачественная опухоль в легочной ткани или бронхах, бронхоэктазы);
- кровь в моче (мочекаменная болезнь, поликистоз почек, злокачественная опухоль, полипы);
- частые носовые кровотечения (при гипертонии, сосудистой патологии).
Недостаточное поступление с пищей – наиболее частая причина развития железодефицитной анемии в детском и подростковом периоде, у вегетарианцев, у лиц, принуждающих себя к полуголодным диетам.
Выявлены генетические последствия для родившихся девочек от матерей, имевших анемию во время беременности: у девочек возможны ранние проявления железодефицитного состояния.
При длительных хронических инфекциях (туберкулез, сепсис, бруцеллез) молекулы железа захватываются клетками иммунитета, а в крови обнаруживается недостаток.
Железодефицитная анемия никак не проявляется при начальном латентном течении заболевания. Клинические симптомы маскируются разными другими состояниями и не вызывают подозрений у пациента.
Наиболее часто «задним числом» обнаруживаются:
- нарастающая слабость,
- головокружения,
- повышенная утомляемость,
- головные боли.
Эти проявления беспокоят при физической нагрузке, нервном напряжении.
Более выражена симптоматика основного заболевания, способствующего анемии.
В дальнейшем состояние утяжеляется: появляется сонливость, нарушение трудоспособности, шум в голове, бледность кожи. С такими жалобами пациенты вынуждены обратиться к врачу.
Для точной диагностики анемии врач должен сопоставить клинические симптомы с показателями крови.
Общий анализ крови выявляет сниженный уровень эритроцитов, низкий цветной показатель, недостаточное содержание гемоглобина.
- Определяется численность эритроцитов у женщин менее 3,7 x 10¹² /л, у мужчин менее 4,0 x 10¹² /л.
- Цветной показатель — условное расчетное содержание гемоглобина в одном эритроците, говорит о полноценности синтезированных клеток крови. В норме показатель составляет 0,85 – 1,05. В зависимости от его величины, анемии различают на нормохромную, гиперхромную (насыщенность превышает 1,05) и гипохромную (показатель ниже 0,85 говорит о «некачественных» эритроцитах).
- Допускается нижний уровень гемоглобина для мужчин 130 г/л, для женщин 120 г/л.
Концентрация железа в сыворотке крови определяется биохимическими методами — нижней нормальной границей служит 12 – 32 мкмоль/л для мужчин, 10 – 30 для женщин.
Способность трансферрина связывать и переносить железо называют железосвязывающей функцией сыворотки крови. В норме она составляет у мужчин 54 – 72 мкмоль/л, у женщин — 45 – 63. При железодефицитных состояниях показатель возрастает.
Уровень ферритина крови (белок, превращающий железо из двухвалентного в нерастворимое трехвалентное, которое в дальнейшем накапливается) показывает правильность процесса усвоения железа, способность организма к накоплению. Его норма — 12 – 300 нг/мл для мужчин и 12 – 150 для женщин. При анемии он снижается даже в легкой степени заболевания.
Для полной диагностики важны все показатели.
Определение степени клинических проявлений необходимо для решения вопроса о лечении, выбора препарата, способа введения. Наиболее простая классификация анемии по уровню гемоглобина.
Выделяют 3 степени тяжести:
- при легкой показатель гемоглобина снижен, но остается около 90 г/л;
- при средней гемоглобин держится в границах от 90 до 70 г/л;
- при тяжелой гемоглобин составляет меньше 70 г/л.
Другой вариант учитывает клинические проявления анемии:
- первая степень — клинические симптомы отсутствуют;
- вторая степень — умеренно выражены слабость, головокружение;
- третья — имеются все клинические симптомы анемии, нарушена трудоспособность;
- четвертая — представляет собой тяжелое состояние прекомы;
- пятая — носит название «анемическая кома», длится несколько часов и приводит к летальному исходу.
Легкую форму дефицита железа можно лечить специальной диетой при условии отсутствия поражения желудка, кишечника, поджелудочной железы.
При этом важно учитывать, что железо из белков и жиров пищи усваивается лишь на 1/4 — 1/3 часть, а из фруктово-овощного состава — на 80%. Оказалось, значительную роль играют витамины, которых в овощах и фруктах больше, чем в мясе. Особо важное значение придается содержанию в продуктах витаминов группы В и фолиевой кислоты, витамина С.
Продукты, содержащие повышенный уровень железа: говяжий язык, мясо курицы, индейки, печень, морская рыба, крупа гречки и пшено, яйца, зелень. Фрукты: яблоки, персики, хурма, айва и ягоды черники.
Добавить витамин С можно за счет смородины, цитрусовых, щавеля, капусты.
Рекомендуется ограничить продукты, нарушающие всасывание железа: черный сорт чая, молоко во всех видах.
Современная терапия препаратами железа проводится, начиная со второй степени железодефицитной анемии. Лекарства должны соответствовать требованиям по компенсации и восстановлению кроветворения. Лечение препаратами железа применяется, когда одной диетой этого достичь невозможно.
Учитывая то, что главным способом усвоения железа является поступление через кишечник, преимущества в терапии отдаются таблеткам. Результативность внутримышечного введения ниже, чем при приеме таблетированных препаратов. При лечении препаратами в инъекциях чаще обнаруживаются побочные нежелательные эффекты.
Для терапевтического воздействия достаточно от 80 до 160 мг железа в чистом виде (320 мг сульфата). Контроль за дозировкой проводится врачом.
Таблетки рекомендуется глотать не разжевывая, запивать достаточным количеством воды.
Все лекарства делят на препараты двухвалентного железа и трехвалентного. Их отличия требуют дополнить лечение в первом случае витамином С, во втором — аминокислотами.
Популярные препараты двухвалентного железа:
- Сорбифер дурулес,
- Тардиферрон Феррофольгамма,
- Ферретаб,
- Актиферрин,
- Тотема,
- Гемофер пролонгатум (сульфат).
Лекарства из трехвалентного железа:
При беременности и в период лактации лечение обязательно согласовывается с гинекологом и педиатром.
Побочное действие препаратов проявляется в:
- болях в эпигастральной области, длительных запорах;
- темном налете на зубах после приема таблеток или сиропа;
- аллергических реакциях.
Народные средства можно использовать в дополнении к общему комплексу лечения.
- В домашних условиях можно приготовить и смешать в равных объемах соки свеклы, редьки и моркови. Рекомендовано принимать по столовой ложке до еды курсом 3 месяца.
- Отвар шиповника, клевера настаивается после получасового кипячения. Можно пить вместо чая.
- Крапиву отваривают одну или в сочетании с корнями одуванчика и цветами тысячелистника. Для вкуса можно добавить немного меда.
- Тертый хрен с медом рекомендован для беременных по чайной ложке перед едой.
- Заготовленная черная смородина с сахаром позволит уберечь всю семью от анемии.
Для применения этих способов существует одно противопоказание: аллергическая реакция на компоненты.
Профилактика железодефицитной анемии требует соблюдения баланса в питании. Никакие диеты нельзя применять без потерь для организма. Увлечение вегетарианством, голоданием может вызвать выраженную патологию. На фоне переедания мяса и отсутствия в пище фруктов и овощей тоже невозможно сохранить здоровье.
Особое значение имеет диагностика и лечение хронических кровотечений (носовых, геморроидальных, менструальных). Воспитание мальчиков и девочек не должно строиться на «стыдных» болезнях. Во взрослом состоянии мы имеем мужчин, категорически отказывающихся от осмотра проктолога и поступающих на госпитализацию в неоперабельной форме рака, и женщин, доводящих себя диетами до полной анорексии. Не упускайте возможность вовремя восполнить дефицит железа и вернуть здоровье.
источник
Лечение железодефицитной анемии у детей должно быть комплексным. Этиологическое лечение предусматривает устранение причин, приводящих к развитию дефицита железа.
- Отсутствие лабораторного подтверждения дефицита железа.
- Сидероахрестические анемии.
- Гемолитические анемии.
- Гемосидероз и гемохроматоз.
- Инфекция, вызванная грамотрицательной флорой (энтеробактерии, синегнойная палочка, клебсиелла являются сидерофильными микроорганизмами и используют железо в процессах роста и размножения).
Обычно самочувствие больных улучшается уже через несколько дней после начала терапии препаратами железа. Значимое увеличение уровня гемоглобина при применении препаратов железа через рот наблюдается в среднем через 3 нед от начала лечения, при парентеральном введении препаратов железа прирост показателей гемоглобина происходит быстрее, чем при назначении препаратов внутрь. Препаратом выбора для лечения тяжелых форм железодефицитной анемии у детей является феррум лек, позволяющий быстро получить клинико-гематологический эффект. У некоторых больных сроки нормализации содержания гемоглобина при применении препаратов внутрь затягиваются до 6-8 нед, что может быть связано с выраженностью анемии и степенью истощения запасов железа или с тем, что причина железодефицитной анемии сохраняется или устранена не полностью. Если спустя 3 нед от начала лечения содержание гемоглобина не повышается, необходимо выяснить причину неэффективности лечения.
При железодефицитной анемии возможно использование фитотерапии. Назначают фитосбор: листья крапивы двудомной, череды трехраздельной, земляники лесной и черной смородины; высушенные листья указанных растений смешивают в равных частях, 1 столовую ложку измельченных листьев заливают стаканом кипятка, настаивают в течение 2 ч, процеживают и принимают по 1/3 стакана 3 раза в день натощак, в течение 1,5 мес ежедневно. Весьма желательно принимать настой листьев медуницы лекарственной, шпината огородного, одуванчика, плодов шиповника.

Важными звеньями комплексной терапии являются правильная организация режима и питания. Эффективной лечебно-профилактической мерой является длительное пребывание на свежем воздухе.
Дети нуждаются в щадящем режиме: ограничение физической нагрузки, дополнительный сон, благоприятный психологический климат, следует освободить их от посещения детского учреждения, беречь от простудных заболеваний.
Дети старшего возраста освобождаются от занятий физкультурой до выздоровления, при необходимости им предоставляют дополнительный день, свободный от занятий в школе.
Особое внимание следует уделить сбалансированному питанию, нормализации аппетита, желудочной секреции и обмену веществ. Без урегулирования этих процессов нельзя надеяться на эффективность медикаментозной терапии.
Назначение полноценного питания больным железодефицитной анемией имеет большое значение. Необходимо устранить имеющиеся дефекты вскармливания и назначить рациональное питание, по основным пищевым ингредиентам соответствующее возрастным показателям.
Содержание железа (мг) в продуктах питания (в 100 г)
Детям раннего возраста, страдающим анемией, находящимся на естественном вскармливании, прежде всего следует отрегулировать питание матери, а в случае необходимости провести коррекцию питания ребенка. Детям, страдающим анемией, первый прикорм необходимо вводить на 2-4 нед раньше, ч е м здоровым (то есть с 3, 5 — 4 мес). Первым прикормом обязательно должны быть блюда, богатые солями железа: картофель, свекла, морковь, капуста, кабачки и др. В рацион питания должны входить фруктово-ягодные соки, тертые яблоки. Уже с первым прикормом детям, больным анемией, можно давать телячью или говяжью печень. Печеночные блюда необходимо давать в протертом виде, смешивая с овощным пюре. Начиная с б мес, в рацион питания можно вводить мясные блюда в виде фарша. Из рациона следует исключить белые каши (манную, рисовую, толокняную), отдавая предпочтение гречневой, ячменной, перловой, из проса. Варить каши следует на воде или, лучше, на овощном отваре.
При построении диеты у детей старшего возраста необходимо учитывать, что лучше всего всасывается в пищеварительном тракте гемовое железо, содержащееся в мясных блюдах. Значительно хуже усваивается солевое железо, входящее в состав овощей и фруктов. В пищевом рационе целесообразно несколько повысить квоту белка (примерно на 10 % от возрастной нормы) за счет увеличения в рационе белковых продуктов животного происхождения; количество углеводов в рационе больного должно соответствовать возрастной норме, количество жиров следует несколько ограничить. При анемии показано достаточное введение фруктовых и овощных соков и отваров, у детей старшего возраста можно использовать минеральные воды. Целесообразно использование вод из источников с типом слабоминерализованных железо-сульфатно-гидрокарбонатномагниевых вод, в которых железо находится в хорошо ионизированной форме и легко всасывается в кишечнике. К источникам такого типа относятся минеральные источники Железноводска, Ужгорода, Марциальных вод в Карелии. Необходимо учитывать, что компенсация дефицита железа и коррекция железодефицитной анемии с помощью пищевого железа не могут быть достигнуты, о чем обяхзательно информируют родителей пациента, которые нередко предпочитают медикаментозным препаратам «пищевую коррекцию».
Для улучшения деятельности ЖКТ назначают ферменты.

Проводится препаратами железа, которые назначаются внутрь или парентерально.
Препараты железа — основные лекарства для лечения железодефицитной анемии, они представлены многочисленными формами препаратов железа для приёма внутрь (капли, сироп, таблетки).
Для расчёта необходимого количества препарата необходимо знать содержание элементарного железа (Fe 2+ или Fe 3+ ) в данной лекарственной форме препарата (капле, таблетке, драже, флаконе) и объём упаковки.
Выбор препарата железа — прерогатива врача. Врач выбирает препарат в соответствии с финансовыми возможностями пациента или его родителей, переносимостью препарата и собственным опытом применения препарата железа.
Вместе с тем каждый врач должен быть информирован об имеющейся в мировой практике тенденции смены солевых препаратов железа, часто демонстрирующих низкую комплаиентность, на препараты нового поколения — гидроксид полимальтозный комплекс трёхвалентного железа (Мальтофер \ Феррум-Лек).
Список некоторых препаратов железа для приёма внутрь
Состав препарата (в одном драже, таблетке, в 1 мл капель или сиропа)
Содержание элементарного железа
Железа сульфат (актиферрин)
Сульфат железа 113,85 мг, D.L-серин 129 мг в 1 капсуле
Капсулы, в блистере 10 капсул, по 2 и 5 блистеров в упаковке
Железа сульфат (актиферрин)
Сульфат железа 47,2 мг, D.L-серин 35,6 мг, глюкоза и фруктоза 151,8 мг, калия сорбат 1 мг в 1 мл капель
Капли для приёма внутрь, 30 мл во флаконе
Железа сульфат (актиферрин)
Сульфат железа 171 мг, D.L-серин 129 мг, глюкоза, фруктоза в 5 мл сиропа
Железа (III) гидроксид полимальтозат (мальтофер)
Гидроксид- полимальтозный комплекс
Раствор для приёма внутрь, 30 мл во флаконе с капельницей
Fe 3+ 50 мг в 1 мл раствора (20 капель)
Железа (III) гидроксид полимальтозат + фолиевая кислота (мальтофер Фол)
Гидроксид-полимальтозный комплекс, фолиевая кислота 0,35 мг в 1 таблетке
Жевательные таблетки, 10 таблеток в блистере, по 3 блистера в упаковке
Fe 3+ : 100 мг в 1 таблетке
Железа (III) гидроксид полимальтозат (мальтофер)
Жевательные таблетки, в блистере 10 таблеток, по 3 и 50 блистеров в упаковке
Fe 3+ : 100 мг в 1 таблетке
Железа (III) гидроксид полимальтозат (мальтофер)
Железа сульфат + аскорбиновая кислота (Сорбифер Дурулес)
Сульфат железа 320 мг, аскорбиновая кислота 60 мг
Таблетки, покрытые оболочкой, по 30 и 50 таблеток во флаконе
Fe 3+ : 100 мг в 1 таблетке
Железа сульфат (тардиферон)
Сульфат железа 256,3 мг, мукопротеоза 80 мг, аскорбиновая кислота 30 мг
Таблетки, покрытые оболочкой, 10 таблеток в блистере, 3 блистера в упаковке
В 10 мл раствора: 50 мг глюконата железа, 1,33 мг глюконата марганца, 0,7 мг глюконата меди, глицерол, глюкоза, сахароза, лимонная кислота, цитрат натрия и др.
Раствор для приёма внутрь, ампулы по 10 мл, по 20 шт. в упаковке
Железа фумарат + фолиевая кислота (ферретаб комл)
Фумарат железа 154 мг, фолиевая кислота 0,5 мг
Капсулы, 10 капсул в блистере, 3 блистера в упаковке
Железа сульфат + аскорбиновая кислота (ферроплекс)
Сульфат железа 50 мг, аскорбиновая кислота 30 мг
Глюконат железа 300 мг в 1 таблетке
Таблетки, покрытые оболочкой, в блистере 10 таблеток, 1 блистер в упаковке
Фумарат железа 350 мг в 1 калсупе
Железа (III) гидроксид полимальтозат (Феррум Лек)
10 таблеток в стрипе, 3 стрипа в упаковке
Железа (III) гидроксид полимальтозат (Феррум Лек)
Протеин сукцинилат железа 800 мг в 15 мл
Раствор для приёма внутрь, 15 мл во флаконе, 10 флаконов в упаковке
Поливитамин + минеральные соли (фенюльс)
Сульфат железа 150 мг, аскорбиновая кислота 50 мг, рибофлавин 2 мг, тиамин 2 мг, никотинамид 15 мг, пиридоксина гидрохлорид 1 мг, пантотеновая кислота 2,5 мг
Капсулы, 10 капсул в блистере, 1 блистер в упаковке
В большинстве случаев, кроме специальных показаний, лечение железодефицитной анемии проводится препаратами для внутреннего применения. Наиболее целесообразно применять препараты, содержащие двухвалентное железо. Эти соединения хорошо всасываются и дают высокий темп прироста гемоглобина. При выборе препарата для детей раннего возраста необходимо учитывать степень токсичности и форму выпуска. Предпочтение отдают препаратам в жидкой форме. При назначении препаратов железа внутрь необходимо учитывать некоторые общие принципы.
- Лучше назначать препараты железа между приемами пищи. Пища ведет к разведению и снижению концентрации железа, а, кроме того, некоторые элементы пищи (соли, кислоты, щелочи) образуют с железом нерастворимые соединения. К ним относятся препараты, содержащие фосфор, фитин. Железо, принятое в вечерние часы, продолжает всасываться в ночное время.
- Применять препараты железа следует в сочетании с веществами, улучшающими его всасывание: аскорбиновая, лимонная, янтарная кислоты, сорбит. В лечебный комплекс включают средства, ускоряющие синтез гемоглобина — медь, кобальт; витамины В1, В2, В6, С, А — для улучшения регенерации эпителия; витамин Е — для предотвращения чрезмерной активации свободнорадикальных реакций. Дозы витаминов В1, В2, С соответствуют суточной потребности, доза витамина В6 превышает суточную потребность в 5 раз. Комплекс витаминов следует принимать через 15-20 мин после еды, а препараты железа — через 20-30 мин после их приема.
- Для предупреждения диспепсических явлений рекомендуется, по показаниям, применять ферменты — панкреатин, фестал.
- Курс лечения должен быть длительным. Лечебные дозы применяются до достижения нормального уровня гемоглобина в крови, то есть 1,5-2 мес, а затем в течение 2- 3 мес возможно назначение профилактических доз для пополнения запасов железа.
- Необходимо учитывать переносимость препарата. При плохой переносимости можно заменить препарат, начать лечение с малой дозы, постепенно повышая ее до переносимой и эффективной.
- Не следует назначать препараты железа одновременно с препаратами, уменьшающими его всасывание: препараты кальция, антациды, тетрациклины, левомицетин.
- Необходимо рассчитывать потребность в железе для каждого больного. При расчете длительности лечения следует учитывать содержание элементарного железа в препарате и его всасывание.
Оптимальная суточная доза элементарного железа составляет 4-6 мг/кг. При этом необходимо иметь в виду, что прирост гемолобина у больных железодефицитной анемией может быть обеспечен поступлением в организм от 30 до 100 мг двухвалентного железа в сутки. Учитывая, что при развитии железодефицитной анемии всасывание железа увеличивается на 25-30 % (при нормальных запасах всасывается 3-7 % железа), необходимо назначать от 100 до 300 мг двухвалентного железа в сутки. Применение более высоких суточных доз не имеет смысла, поскольку объем всасывания при этом не увеличивается. Таким образом, минимальная эффективная суточная доза составляет 100 мг элементарного железа, а максимальная — около 300 мг внутрь. Выбор суточной дозы в данном диапазоне определяется индивидуальной переносимостью препаратов железа и их доступностью.
При передозировке препаратов железа отмечают нежелательные эффекты: диспепсические расстройства (тошнота, рвота, понос) прямо пропорциональны количеству невсосавшегося железа в желудочно-кишечном тракте; инфильтрат на месте внутримышечного введения; гемолиз эритроцитов из-за активации свободнорадикальных реакций, повреждения клеточных мембран.
Недостатки применения солевых препаратов железа при лечении больных железодефицитными анемиями:
- опасность передозировки, вплоть до отравлений, вследствие негибкого дозирования, пассивного, неконтролируемого всасывания;
- выраженный металлический вкус и окрашивание эмали зубов и дёсен, иногда стойкое;
- взаимодействие с пищей и другими препаратами;
- частый отказ пациентов от лечения (30-35% больных, начавших лечение).
Врачи обязаны предупреждать пациентов или их родителей о возможных отравлениях солевыми препаратами железа. Отравления препаратами железа составляют всего 1,6% всех случаев отравлений у детей, но в 41,2% случаев заканчиваются летальным исходом.
Свойства и преимущества препаратов на основе гидроксидполимальтозного комплекса:
- высокая эффективность;
- высокая безопасность: нет риска передозировки, интоксикации и отравления;
- отсутствие потемнения зубов и дёсен;
- приятный вкус, нравится детям;
- отличная переносимость, определяющая регулярность лечения;
- отсутствие взаимодействия с медикаментами и продуктами питания;
- антиоксидантные свойства;
- существование лекарственных форм для всех возрастных групп (капли, сироп, жевательные таблетки, разовые ампулы, препарат железа с фолиевой кислотой для беременных).
Парентеральные (внутримышечные, внутривенные) препараты железа показаны:
- при тяжёлой форме железодефицитной анемии (около 3% больных);
- при непереносимости препаратов железа для приёма внутрь;
- при язвенной болезни или операциях на ЖКТ, даже в анамнезе;
- при необходимости быстрого насыщения организма железом.
Общая курсовая доза железа для парентерального введения рассчитывается по формуле:
Fe (мг) = Р х (78 — 0,35 х Нb), где Р- вес пациента в килограммах; Нb — содержание гемоглобина в г/л у больного.
Парентерально не следует вводить более 100 мг железа в сутки, дающих полное насыщение трансферрина. У детей до 2 лет суточная доза вводимого парентерально железа составляет 25-50 мг, у детей старше 2 лет — 50-100 мг.
Парентеральное введение железа значительно сложнее и опаснее перорального вследствие возможного развития аллергических реакций и инфильтратов (при внутримышечном введении), а также токсичности ионизированного железа и опасности его чрезмерных отложений в тканях при передозировке, поскольку оно при этом практически не выводится из организма. Железо является капилляротоксическим ядом и при парентеральном введении на фоне пониженного уровня трансферрина в крови увеличивается фракция свободного железа, что приводит к снижению тонуса артериол и венул, повышается их проницаемость, уменьшается общее периферическое сопротивление и объем циркулирующей крови, падает артериальное давление. При передозировке железа рекомендуется введение антидота — десферала (дефероксамина) в дозе 5-10 г внутрь или 60-80 мг/кг в сутки внутримышечно или внутривенно капельно.
Характеристика препаратов железа для парентерального применения (назначаются только после определения железо-комплекса крови и верификации диагноза железодефицитной анемии)
источник