Эта болезнь часто встречается при патологиях внутренних органов. Нередко она возникает когда женщина беременна или у ребёнка начинается период активного роста, нарушены процессы всасывания в кишечнике или есть серьёзное наследственное заболевание. Для диагностирования анемии врачи берут кровь из вены больного и проводят её лабораторное исследование.
Врачи используют для диагностирования заболевания несколько способов:
- Общее исследование (определение объёма жидкости, уровень гемоглобина, вычисление формулы лейкоцитов)
- Биохимия крови (уровень железа, трансферрина, Витамина В2, билирубина и других показателей в организме).
- Анализ на скрытую кровь в каловых массах (помогает понять есть ли кровотечение в желудочно-кишечном тракте).
Методы исследования можно разделить на несколько разновидностей:
- общий
- биохимический анализ
- исследование на скрытую кровь
Самый универсальный и распространённый способ исследования. Он не подразумевает больших затрат и на то, чтобы исследовать кровь не нужно много времени. С его помощью можно понять состояние системы кроветворения.
Брать его можно двумя способами: из пальца (путём прокола пальца одноразовой иглой, если необходим один анализ) или из вены (рука затягивается жгутом, забор осуществляется одноразовым шприцем, такой анализ используется сразу для нескольких исследований, а объем исследуемой жидкости больше).
С помощью такого анализа можно понять сколько в крови химических веществ и какого состояние внутренних органов, какие в организме пациента есть недуги.
Анализ проводится на десятки показателей, среди них концентрация сывороточного железа, уровень ферритина, общая железосвязывающая способность сыворотки.
Анна Поняева. Закончила нижегородскую медицинскую академию (2007-2014) и Ординатуру по клинико-лабораторной диагностике (2014-2016).Задать вопрос>>
Причиной такого явления может стать наличие у пациента болезни Крона, язвенной болезни, опухоли в ЖКТ и ряд других заболеваний.
При кровотечении из нижних отделов кишечника кал окрашивается в ярко-алый цвет, а из верхних отделов кровь в каловых массах становится тёмной, почти чёрной.
Если такие явления однократные, то они не ведут к появлению ЖДА, а если они длительные или периодические, то несут большой вред организму пациента.
Забор анализа осуществляется в утреннее время до приёма больным пищи. Дополнительно палец дезинфицируют, прокол делают одноразовой иглой.
Ручной анализ крови предполагает исследование на:
- СОЭ
- концентрацию гемоглобина
- лейкоциты и эритроциты
- мазок
Для ручного исследования берут аппарат и капилляры Панченкова, раствор лимоннокислого натрия (5%), стекло, спирт и другие вспомогательные средства.
СОЭ исследуют методом выдувания жидкости на стекло из капилляра Панченкова на часовое стекло и замера этой скорости.
Для концентрации уровня гемоглобина используется колометрический способ исследования. Жидкость помещают в специальный раствор и сравнивают цвет со стандартом гемометром Сали.
Для получения уровня эритроцитов и лейкоцитов её дополняют раствором соли или уксусной кислоты и помещают в счётную камеру.
Понимая, сколько составляет уровень эритроцитов в крови и концентрацию гемоглобина можно понять насыщение эритроцита.
Для вычисления используется формула: ( уровень полученного гемоглобина* уровень полученных эритроцитов)/ (нормальный уровень гемоглобина* нормальный уровень эритроцитов).
Палец вытирается и на предметное стекло берётся мазок из свежевыступившей капли жидкости. Стекло наклоняют так, что она растеклась, мазок должен просвечивать, потом его фиксируют с помощью метилового спирта. После этого лаборант проводит его окрашивание по Романовскому-Гимзе в течение получаса.
Подсчёт ретикулоцитов берётся там: специалист считает попавшие в обзор узла зрения 1000 эритроцитов и считают сколько ретикулитов. Это количество делят на 10 и сравнивают с нормальным показателем.
Похожим образом считают и лейкоцитное значение крови у пациента.
Уже сейчас на вооружении многих лабораторий стоят специальные автоматические приборы — гематологические анализаторы крови.
Такой аппарат заправляют реактивами, он работает от розетки. Внутрь прибора ставится пробка со взятой у пациента кровью. Аппарат обрабатывает полученный анализ и выдаёт бланк с результатами.
Сложности у такой машины возникают только с расчётом лейкоцитарной формулы, обычные модели могут производить расчёт только общего количества.
Автомат не считает только недоразвитые нейтрофилы.
Их считают врачи, изучая мазок крови.
Биохимический анализ крови помогает выявить ряд серьёзных заболеваний, например, патологии почек, печени, проблемы со щитовидной железой. Анализ показывает концентрацию и уровень конкретных химических веществ в субстанции. Изучив содержимое крови и сопоставив их с нормальными значениями можно узнать о наличии той или иной болезни в организме. Назначает этот анализ лечащий врач и пишет в направлении перечень тех веществ, уровень которых нужно определить. Анализ назначают при болезнях сердечно-сосудистой системы, болезнях ЖКТ и других патологиях. Такое исследование помогает сделать правильную диагностику.
Для изучения берётся крови из вены в области локтя. Если к ней нет доступа, то можно осуществить забор с другого места. Перед пункцией место прокола обрабатывается антисептиком.
За 8 часов до забора крови нельзя пить, есть. За 2 дня до исследования пациент обязан исключить алкогольные напитки и жирные блюда из своего меню.
Не рекомендуется нервничать, сильно нервничать и физически напрягаться.
Этот метод считается самым универсальным и распространённым. Его проходят не только для выявления заболеваний, но и на профосмотрах, в школах, в армии.
Он показывает сколько в субстанции лейкоцитов, гемоглобина, уровень СОЭ, цветовой показатель и другие жизненно важные показатели.
Такой анализ покажет реакцию организма на процессы, которые происходят в организме пациента. Забор крови осуществляется в утреннее время. За 4 часа до него нужно отказаться от приёма пищи и воды. Для исследования используется кровь из пальца, реже делается пункция вены.
Посмотрите видео про общий анализ крови
источник
Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день.
Гипохромная болезнь анемия включает в себя группу разных видов анемий, характеризующихся недостатком гемоглобина, вследствие чего изменяются цветовые показатели крови. Малокровие происходит по причине недостатка железа, что не обязательно может быть вызвано из-за неправильного питания — чаще ситуация происходит из-за наследственных патологий, когда нарушается всасываемость данного элемента. Гипохромная анемия у детей наблюдается достаточно часто, что связано недостаточной выработкой железа.
Гипохромная анемия характеризуется пониженным уровнем эритроцитов. Цветовой количественный показатель в этом случае составит меньше 0.8. Сами эритроциты могут приобретать другие размеры и отклонения в форме. Красные кровяные тельца поддаются обесцвечиванию, становятся похожими на кольцо, имеющее просветление посередине и по краям темную окантовку. Недостаток железосодержащего белка (гемоглобина), содержащегося в кровяных клетках, заканчивается кислородным голоданием, включая органы и ткани.
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Эритроциты тоже имеют важнейшее значение в транспортировке кислорода по организму. Нормальный газообмен будет реализован в организме только в том случае, когда вырабатываемые эритроциты полноценны и содержат достаточное количество гемоглобина. Кислородное голодание грозит тем, что органы и другие функциональные элементы организма перестают выполнять свое назначение. Все это может привести к серьезным осложнениям. Заболевание такого характера может сопутствовать любому нарушению или поражению крови. Люди, страдающие от пониженного уровня гемоглобина, гораздо сильнее подвержены кишечным инфекциям и ОРЗ.
Гипохромная анемия бывает с различным течением и провоцирующими факторами. Выделяют такие виды заболевания:
- Железодефицитная — вызвана недостатком гемоглобина и количества эритроцитов, трофических расстройств, сбоями в формировании структуры тканей;
- Железонасыщенная или сидероахрестическая — концентрация железа в плазме нормальная или даже повышенная, но присутствует сбой относительно его состава в молекуле гемоглобина;
- Железоперераспределительная — железо в плазме крови перемещается с нарушениями;
- Смешанного генеза — смешанная форма заболевания.
При каждом из видов отклонений должна проводиться соответствующая диагностика и назначаться необходимое лечение. Всем видам гипохромной анемии присущи различные симптомы и проявления.
Железодефицитная анемия характеризуется двумя видами синдромов — анемическим и сидеропеническим. Анемическому синдрому при данном заболевании присущи: общее чувство слабости, головокружения, упадок физической активности, одышка и др. Сидеропенический синдром проявляется поражением эпителия, включая эпителий ЖКТ, могут появляться трещинки в уголках рта, трудности при глотании сухой пищи, чувство жжения в языке. Зубы могут утрачивать блеск и быстро поддаваться разрушениям. Проявления со стороны кожи — множественные микротрещины, ломкость ногтей, сухость и выпадение волос.
В зависимости от уровня гемоглобина и других определяющих факторов, может быть в легкой, средней и тяжелой степени. Однако клинические проявления тяжести заболевания не всегда будут соответствовать степени тяжести по показателям лабораторного обследования. Основные причины железодефицитной анемии:
- Ребенок был недоношен и вследствие этого имеет низкие запасы железа при рождении;
- Дети, рожденные от матери с данным заболеванием, также его будут иметь;
- Многоплодная беременность также приводит к низкому запасу железа с рождения;
- Если у матери было в последние месяцы беременности или при родах кровотечение, то у ребенка вероятно будет железодефицитная анемия.
Кроме этого поступление железа в организм может нарушаться из-за вегетарианства, однообразной диеты, содержащей большое количество жиров, рака желудка и других факторов, нарушающих всасывание железа.
Железонасыщенная гипохромная анемия имеет причины в виде нарушенной молекулы гемоглобина, в которую не включено железо в правильной форме. Причем сам уровень железа может быть в норме или повышенный. Основные причины:
- Сбой синтеза гема, вызванный вследствии недостачи протопорфирина;
- Наследственный фактор;
- Свинцовое отравление;
- Долгосрочный прием туберкулостатических препаратов;
- Продолжительное употребление алкогольных напитков.
Пациенты с сидероахрестической анемией, вызванной патологией наследственного характера, имеют симптомы такого вида, как бледность, постоянное чувство упадка сил, сниженной способностью к нагрузкам физического типа, возможны случае и появлением красноты на зубной эмали. Заболевание приводит к снижению памяти, проблемам со сном. В случае с избытком железа и откладыванием его в печени, возможно осложнение в виде цирроза. Также железо может концентрироваться в поджелудочной железе, вызывая сахарный диабет.
Гипохромная железораспределительная анемия лечение требует для налаживания процессов перемещения железа по плазме крови, так как заболевание связанно с нарушениями в данных процессах. При этом железо сосредотачивается в определенных местах хранения и не распределяется нужным образом по организму.
Для нормального гемопоэза среднестатистическому организму требуется 25 мг железа ежесуточно. Из кишечника всасывается всего 1-1.5 мг, основная же часть поступает за счет повторной высокоэффективной реутилизации. Железораспределительная анемия может развиваться из-за следующих болезней:
- Сепсис;
- Хроническая или острая форма инфекционных воспалительных заболеваний;
- Туберкулез;
- Саркоидоз;
- Ревматоидный артрит;
- Болезнь почек, вызванная употреблением алкоголя и др.
Из-за этих заболеваний происходит накопление железа в отдельных частях организма.
Для того, чтобы достоверно определить, что это такое и на каком уровне заболевание спрогрессировало в организме, проводится обязательный внешний осмотр у врача, включая сбор анамнеза. Прежде чем начинать лечиться, следует пройти развернутый анализ крови, чтобы точно оценить уровень гемоглобина в крови, включая количество эритроцитов и цветовой показатель. Благодаря клиническому анализу возможно рассмотреть лейкоцитарную формулу и оценить скорость оседания эритроцитов. Благодаря всем полученным показателям можно будет определить особенности смешанной анемии и назначить необходимые для лечения препараты.
У детей заболевание может быть в латентной и железодефицитной формах. Для латентной будет характерна изолированная задержка железа в тканях с отсутствием анемии. Данная форма заболевания часто начинает лечиться у детей в младшем возрасте. Большое значение в дисбалансе имеет неправильное питание у ребенка, если отклонение не вызвано наследственным характером. Назначаемые при этом препараты компенсируют недостаток железа и направленны на нормализацию состояния.
Зачастую монохромный вид анемии появляется в период полового созревания, что больше всего проявляется у девушек. Все дело в том, что в этот время появляется усиленная потребность в железе, может снижаться иммунитет. Не последняя роль отводится гормонам. В случае нарастания железодефицитной анемии у ребенка может усиливаться вялость, появляться жалобы на чувство головокружения и усиленную одышку.
источник
Наиболее характерным лабораторным признаком железодефицитной анемии является гипохромная анемия. Хотя она наблюдается не только при дефиците железа, но и при ряде состояний, при которых содержание железа в организме повышено, железодефицитная анемия — самая частая форма гипохромной анемии.
Содержание гемоглобина при железодефицитной анемии может колебаться от 20—30г/л (2—3г%) до 110г/л (11г%) в зависимости от выраженности дефицита железа. Содержание эритроцитов может быть нормальным, а может быть сниженным до 1,5—2•10 12 /л 2 .
Мерой степени гипохромии является цветовой показатель, или среднее содержание гемоглобина в эритроците. Цветовой показатель рассчитывают по формуле:
где А — содержание гемоглобина в граммах на 1 л; В — число эритроцитов, деленное на 10 12 . Например, при содержании гемоглобина 50г/л (5г%), а эритроцитов 3•10 12 /л цветовой показатель равен:
В норме цветовой показатель колеблется от 0,85 до 1,05. В мировой литературе значительно более широко используется другой показатель — среднее содержание гемоглобина в одном эритроците. Этот показатель определяется делением содержания гемоглобина в граммах на 1 л на число эритроцитов в 1 л. Например, при содержании гемоглобина 50 г/л (5 г%) и эритроцитов 3•10 12 следует делить 50 (содержание гемоглобина в граммах на 1 л) на 3•10 12 . При этом мы получаем ответ в 10 –12 г. Можно разделить 50 на 3. Тогда получим ответ в пикограммах —16,6 пг. В норме в одном эритроците содержится 27—35 пг гемоглобина. Для перевода цветового показателя в среднюю концентрацию гемоглобина (в пикограммах) цветовой показатель следует помножить на 33,3.
Для гипохромной анемии характерно снижение цветового показателя и соответственно снижение средней концентрации гемоглобина.
Часто лаборатория дает неверное определение цветового показателя, что связано прежде всего с неправильным подсчетом эритроцитов. До настоящего времени во многих лабораториях для их подсчета используется фотометрический метод. Уже давно было установлено [Воробьев А. И., 1959], что фотометрический метод дает очень большую ошибку подсчета эритроцитов в случае их необычной величины и формы. Метод подсчета эритроцитов в фотоколориметре не должен применяться. Вторая причина ошибки — это использование старых методов для подсчета содержания гемоглобина. Большую ошибку при определении гемоглобина дает гемометр Сали. Его не рекомендуется применять в практической работе. Непригодны для практического определения гемоглобина методы, которыми содержание гемоглобина определяется в аммиачном или содовом растворе. Окраска такого раствора изменяется, оптическая плотность снижается и ошибка в определении гемоглобина становится очень большой.
Для определения гемоглобина, особенно у больных анемией, следует использовать цианметгемоглобиновый метод, а для определения содержания эритроцитов — камерный метод подсчета или определение эритроцитов на приборах, регистрирующих прохождение через пункт подсчета одного эритроцита (целлоскоп или подобный ему прибор).
При неправильном определении содержания гемоглобина или эритроцитов врач получает из лаборатории неверный подсчет цветового показателя, и нередко у больных с выраженной железодефицитной анемией, по данным лаборатории, цветовой показатель оказывается ошибочно близким к 1,0.Однако при просмотре мазка крови определяются гипохромные эритроциты.
Кроме гипохромии эритроцитов, для железодефицитной анемии характерна неодинаковая их величина со склонностью к микроцитозу. При дефиците железа выражен пойкилоцитоз, эритроциты бывают самой различной формы (рис. 2, 3).На рис. 4видно, что гипохромные эритроциты по сравнению с нормальными (рис. 5)действительно «худые», лишенные гемоглобина, занимающего значительный объем.
При железодефицитной анемии уменьшено не только содержание гемоглобина, но и эритроцитов.
Рис. 2. Морфология эритроцитов при железодефицитной анемии. Х900.
Рис. 3.Эритроциты здорового человека. Х900.
Рис. 4. Морфология эритроцитов при дефиците железа, обнаруживаемая в сканирующем электронном микроскопе. В центре видны дискоциты с широкой ямкой и крутыми невысокими краями. х3000 (по А. А. Можиной).
Рис. 5. Нормальные эритроциты, двояковогнутые дискоциты, имеющие правильную округлую или слегка овальную форму. Виден микроцит (7). х3000 (по А. А. Можиной).
Это снижение количества эритроцитов может быть объяснено, с одной стороны, снижением при этой болезни пролиферации ядерных эритроидных элементов по сравнению с нормой [Шостка Г. Д., 1970;Канаев С. В., 1973;Осипова Л. А., 1978];а с другой стороны, усилением неэффективного эритропоэза. В норме в костном мозге разрушается 5—10%эритрокариоцитов, не достигнув периода созревания. При железодефицитной анемии величина неэффективного эритропоэза значительно возрастает [Pollycove, 1964;Brunstrometal., 1968]. Эти данные были получены по косвенным расчетам: было показано, что скорость появления радиоактивного железа в эритроцитах периферической крови при железодефицитной анемии меньше, чем в норме. Это было объяснено тем, что железо вначале захватывается одним эритрокариоцитом, затем он погибает в процессе дифференциации, железо попадает в другой или в третий, который созревает до стадии зрелых эритроцитов. Кроме того, имеются данные о некотором укорочении продолжительности жизни эритроцитов при железодефицитной анемии. Тем не менее главным в генезе анемии является все же нарушение образования гемоглобина, поэтому цветовой показатель при железодефицитной анемии остается низким.
Содержание ретикулоцитов при железодефицитных анемиях может быть в пределах нормы (до 12‰), но иногда бывает несколько повышенным. Следует помнить, что уровень ретикулоцитов у этих больных может быть повышенным, если они получали препараты железа до исследования ретикулоцитов. Повышение уровня ретикулоцитов может говорить также о значительном кровотечении у больного.
Содержание лейкоцитов при железодефицитной анемии имеет тенденцию к снижению чаще всего за счет умеренного снижения содержания нейтрофилов (Е. Н. Михайлова). Содержание тромбоцитов в большинстве случаев железодефицитной анемии оказывается в пределах нормы или реже повышено, особенно при какой-либо кровопотере. Однако опубликовано несколько случаев умеренной тромбоцитопении —40—70•10 9 /л (40000—70000в 1мкл) у больных железодефицитной анемией. После лечения препаратами железа количество тромбоцитов у этих больных стало нормальным [Sonnerborn, 1974;Sahudetal., 1974].
В костном мозге при железодефицитной анемии существенных патологических признаков определить не удается. Количество клеток в 1мкл костного мозга, как правило, нормальное. В гистологическом препарате соотношение между кроветворным костным мозгом и жиром не изменено. Иногда отмечается умеренная гиперплазия. При цитологическом исследовании костного мозга в некоторых случаях обнаруживается умеренное преобладание красного ростка. Для железодефицитной анемии, так же как и для других форм гипохромной анемии, характерно нарушение гемоглобинизации эритрокариоцитов. Увеличено количество базофильных и полихроматофильных эритрокариоцитов за счет уменьшения количества оксифильных форм. Количество мегакариоцитов — в пределах нормы или увеличено в случае выраженных кровотечений.
Характерной особенностью костного мозга при железодефицитной анемии является снижение количества сидеробластов — эритрокариоцитов, содержащих гранулы железа. В норме 20—40%эритрокариоцитов костного мозга содержат единичные гранулы. При железодефицитной анемии гранул практически выявить не удается. Исследование сидеробластов костного мозга помогает в трудных случаях диагностики, когда нет полной уверенности в диагнозе.
Среди биохимических методов диагностики железодефицитных анемий наиболее широко используется метод определения сывороточного железа.
В 1927г.Barkanпредложил определять железо сыворотки роданитным методом. Это было большим прогрессом в тот период, так как в какой-то мере объективизировало диагноз. Однако вскоре после этого появились новые органические реактивы, с помощью которых можно получить окрашенные комплексные соединения с железом. Ортофенантролиновый метод, примененный для определения железа сывороткиHeilmeyer,Plotnerв 1937г., а затемBarkan,Walkerв 1940г., фактически полностью вытеснил старый роданитный метод. Действительно, комплексное соединение железа с роданитом быстро диссоциирует, оно очень непрочное. Интенсивность окраски комплексного соединения железа с роданитом резко снижается через 15мин, тогда как окраска ортофенантролинового комплекса сохраняется несколько дней. Роданитный метод фактически не дает возможности использовать современную фотометрическую аппаратуру, что резко снижает его точность. Окраска роданитного комплекса во многом зависит от примесей и прежде всего фосфата. Поэтому роданитные методы определения железа сыворотки в настоящее время нигде в мире не применяются.
Вскоре после ортофенантролинового метода был предложен метод, в котором использовался a-ai-дипиридил,дающий с железом стойкий комплекс (Ramsey). Но окраска этого комплекса, так же как и комплекса железа с ортофенантролином, слабая, поэтому разница окраски между нормой и патологией невелика. В связи с этим ортофенантролиновый и -дипиридиловыйметоды определения железа дают большую ошибку.
В 1951г. был предложен очень чувствительный реактив на железо— батофенантролин —4,7-дифенил-1,10-фенантролин (Case). Этот реактив образует с железом комплекс, который дает окраску в 2раза более интенсивную, чем комплекс с ортофенантролином и-1-дипиридилом. К тому же эта окраска стойкая, практически не меняется в течение нескольких дней. Поэтому для определения железа сыворотки в настоящее время используются только батофенантролиновые методики. Предложен ряд методов с применением батофенантролина в качестве комплексообразователя [Peterson,1953;Kok,Wild, 1960;Henryetа1., 1958].
В нашей стране наиболее широко используется метод, предложенный Henryс соавт., а также его модификация, на которой основано определение железа в наборах, которые выпускаются в ЧССР.
Необходимо упомянуть о двух очень важных обстоятельствах. Во-первых, кровь следует брать в специальную пробирку, пропаренную или тщательно вымытую дважды дистиллированной водой, причем вторая перегонка воды должна быть проведена через стеклянное оборудование. Это связано с тем, что обычная дистиллированная вода, которая перегоняется через металлический дистиллятор, содержит следы металла, который при подогревании в кислой среде может перейти в ионизированную форму и завысить результаты исследования. Обычно процедурные сестры получают из биохимических лабораторий специальные пробирки, куда забирают кровь для исследования сывороточного железа. Во-вторых, больной, у которого исследуют содержание железа сыворотки, не должен принимать препаратов железа по крайней мере 5дней. Если он принимает препараты железа, содержание железа сыворотки за счет этого повышается и не отражает его запасов. Это одна из наиболее частых ошибок. Нам нередко приходится сталкиваться с тем, что диагноз железодефицитной анемии отвергается из-за нормального содержания железа сыворотки, определенного на фоне приема внутрь или инъекций препаратов железа.
Нормальное содержание железа сыворотки —12.5—30,4мкмоль/л (70—170мкг%) 3 . В среднем, по нашим данным, содержание железа сыворотки 22,1±1,3мкмоль/л (123±7мкг%). Содержание железа сыворотки при выраженной железодефицитной анемии снижается до 1,8—5,4мкмоль/л (10—30мкг%). При нерезко выраженной железодефицитной анемии содержание железа сыворотки снижается до 7,2—10,8мкмоль/л (40—60мкг%).
Кроме исследования сывороточного железа, для изучения запасов железа принято определять железосвязывающую способность сыворотки. В норме примерно 1/3 трансферрина насыщена железом, а 2/3 его свободны и могут присоединять значительное количество железа. Говоря о железосвязывающей способности сыворотки, мы имеем в виду не абсолютное количество трансферрина, а количество железа, которое может связываться с трансферрином. Количество железа, способное связаться 100мл сыворотки, раньше измеряли в микрограммах, в настоящее время количество железа, которое способен связать 1л сыворотки, измеряют в микромолях.
Существует несколько методов определения железосвязывающей способности сыворотки.
Прибавление железа к сыворотке повышает интенсивность окраски за счет насыщения железотрансферринового комплекса, но лишь до известных пределов, пока весь имеющийся трансферрин не соединится с железом. Чем больше трансферрина, тем больше интенсивность окраски, тем больше оптическая плотность на спектрофотометре или фотоколориметре. На этом принципе основан метод, предложенный Rath, Finch (1949), Ventura (1952). Этот метод усовершенствован М. М. Щербой (1965). При помощи этого метода определяется ненасыщенная железосвязывающая способность сыворотки, т. е. выясняется, сколько железа (кроме того, которое уже связано с белком) может связаться еще. Метод чрезвычайно прост, однако страдает значительной неточностью. Разница между нормой и патологией невелика, мешает мутность сыворотки. Поэтому в настоящее время данную группу методов применяют редко. Значительно шире используют принципиально отличные методы.
К исследуемой сыворотке прибавляют избыток железа, одна часть которого связывается с трансферрином, а другая — остается свободной. Каким-либо адсорбентом поглощают часть железа, не связавшуюся с белком, а затем все неадсорбированное железо, т. е. связанное с белком, определяют аналитически, как при определении железа сыворотки. Для адсорбции железа Ramsey использовал карбонат магния. Еще лучше адсорбируется железо ионообменными смолами: в методе Генри и др. применяют ионообменную смолу амберлит IRA-401. Для связывания с белком используют железоаммонийную соль лимонной кислоты.
В норме, по нашим данным, общая железосвязывающая способность сыворотки колеблется от 30,6до84,6мкмоль/л (от 70до 470мкг%). Среднее значение —70,4,4,1 мкмоль/л (391±23мкг%).
Вычитая количество железа сыворотки из общей железосвязывающей способности, мы узнаем ненасыщенную или латентную железосвязывающую способность. В среднем, по нашим данным, латентная железосвязывающая способность равна 50,2 ±4мкмоль/л (279±22 мкг%). Есть еще один производный показатель — это коэффициент насыщения, т. е. процент, который составляет железо сыворотки от общей железосвязывающей способности сыворотки. В норме он колеблется от 16до 54,составляя в среднем 31,2±1,7.
Для железодефицитной анемии считается характерным увеличение общей железосвязывающей способности сыворотки, значительное увеличение латентной железосвязывающей способности и резкое снижение процента насыщения трансферрина. Следует только отметить, что хотя в среднем в группе больных имеет место повышение общей железосвязывающей способности, у отдельных больных общая железосвязывающая способность может оставаться нормальной. Считается, что определение общей железосвязывающей способности в какой-то мере дает возможность определить запасы железа в организме. Однако определение содержания сывороточного железа и железосвязывающая способность сыворотки не всегда отражают запасы железа в организме. Так, например, при анемии, связанной с инфекцией и воспалением, снижается содержание железа сыворотки при нормальных запасах железа в организме.
Для оценки запасов железа может быть использован десфераловый тест. Десферал (десфероксамин) — комплексен, избирательно выводящий ион железа из организма. Это вещество — продукт метаболизма актиномицетовStreptomycespilosus— выпускает фирма «Ciba» (Швейцария). 100весовых частей десферала способны связать 8,5части трехвалентного железа.
В настоящее время известно, что источником железа, входящего в комплекс с десфералом, не может быть ни гемоглобин, ни трансферрин. Имеется определенный параллелизм между содержанием железа в запасах в виде ферритина и гемосидерина и количеством железа, выделяемого с мочой после введения десферала. Десферал связывает железо ферритина легче, чем гемосидерина.
В моче здоровых людей содержится от 0,04до0,3мг железа (в пересчете на суточную мочу). Определение железа в моче не отражает содержания железа в запасах. Для изучения запасов железа больному вводят 500мг десферала, после чего определяют содержание железа в суточной моче. После введения десферала, по нашим данным [Аполлонова Л. А., Идельсон Л. И., 1970], в норме за сутки выводится 0,6—1,3мг железа. У больных железодефицитной анемией после введения десферала содержание железа в моче значительно меньше, чем в норме. У некоторых больных оно снижается до 0,2мг в сутки и менее.
Следует помнить, что хотя имеется определенный параллелизм между содержанием железа в запасах, точного соответствия между содержанием железа в запасах и содержанием его в моче после введения десферала быть не может. Lipschitzс соавт. изучили обмен железа между ферритином и десфералом. Ферритин, меченный 59 Fe, вводили крысам. Он быстро поглощался печенью. Через несколько дней меченое железо оказывалось в составе гемоглобина. У животных, получавших десферал, радиоактивное железо выделялось с мочой, однако включение его в клетки костного мозга не менялось. В случае же активации эритропоэза у животных кровопусканием при введении десферала значительно уменьшалось включение 59 Feв гемоглобин. Известно [Hallberg,Hedenberg, 1965;Belcezzak, 1966], что десферал не вступает в комплекс с железом, связанным с трансферрином. По даннымLipschitzс соавт., у животных с посттрансфузионной полицитемией и гемосидерозом выведение железа с мочой после введения десферала уменьшается. Можно предположить, что десферал не комплексируется с железом запасов в случае угнетения эритропоэза полицитемией, следовательно, скорее всего десферал комплексируется не с железом, входящим в состав ферритина, а захватывает железо в момент перехода его из запасов в трансферриновую форму. Вероятно, имеется промежуточная лабильная форма железа между ферритином и трансферрином, состав которой пока неизвестен. При введении животным термически поврежденных эритроцитов с меченным 59 Feгемоглобином последующее введение десферала приводит к выведению с мочой значительного количества 59 Fe. Вероятно, это железо мобилизуется из фракции, образующейся при распаде гемоглобина, перед тем как железо комплексируется с трансферрином.
Следовательно, используя десфераловый тест, следует помнить, что выделение железа с мочой отражает не только характеристику запасов железа в организме, но и степень активности эритропоэза и степень распада эритроцитов.
В настоящее время для оценки запасов железа в организме используют метод определения ферритина сыворотки. Хотя ферритин — это белок, содержащийся в тканях, давно уже было установлено, что он появляется в сыворотке при некрозе печени [Reissrnann,Dietrich, 1956], однако в тот период использовались недостаточно чувствительные методы определения ферритина. В последние годы были разработаны очень чувствительные методы определения ферритина сыворотки и установлено, что у всех здоровых людей в сыворотке имеется определенное количество ферритина. Для определения сывороточного ферритина используют радиоиммунологические методы исследования. При этом в одних методах используют меченые антитела к ферритину [Addisonetal., 1972], а в других — меченый ферритин [Marcus,Linberg, 1975]. В норме, по даннымJacobs, содержание ферритина чаще всего колеблется в пределах 12—300мкг/л. У здоровых женщин, по даннымCookс соавт., содержание ферритина в среднем составляет около 34мкг/л, а у мужчин — около 94мкг/л. А. А. Замчий с соавт.(1979),исследовав 50здоровых лиц, представил следующие нормы: у мужчин —106±21,5 мкг/л и у женщин —65±18,6мкг/л.
По данным Siimesс соавт., при железодефицитной анемии содержание ферритина сыворотки колеблется от 1,5до 9мкг/л.
Метод определения ферритина сыворотки в настоящее время считается одним из лучших методов определения запасов железа в организме. Он пока не нашел широкого применения из-за отсутствия в широкой медицинской сети необходимых реактивов и оборудования. Содержание ферритина сыворотки не всегда отражает запасы железа. Оно зависит также от скорости освобождения ферритина из тканей и скорости освобождения ферритина из плазмы.
При железодефицитных анемиях повышено содержание протопорфирина эритроцитов. Это повышение связано прежде всего с тем, что при низком уровне железа протопорфирину не с чем связываться и он накапливается в эритроцитах. Кроме того, при железодефицитной анемии несколько увеличен синтез протопорфирина [Идельсон Л. И., 1968;Lichtman,Feldman. 1963].
В норме содержание протопорфирина эритроцитов колеблется от 18до 89мкмоль/л (10—50мкг%). При железодефицитной анемии, по нашим данным, содержание протопорфирина в среднем составляло 191±18мкмоль/л (106±10мкг%). У большинства больных содержание протопорфирина повышено, но у 20% больных было в пределах нормы. Кроме того, этот тест не строго специфичен. Содержание протопорфирина повышено при свинцовом отравлении в связи с нарушением активности фермента гемсинтетазы, связывающего железо с протопорфирином. Повышено содержание протопорфирина при различных формах гемолитических анемий в связи с тем, что в ретикулоцитах идет повышенный синтез порфиринов. Резко повышено содержание протопорфирина при наследственном заболевании — эритропоэтической протопорфирии [Идельсон Л. И., 1968].
источник
Цветной показатель крови является одним из наиболее основных показателей клинического анализа крови. Он показывает количество находящегося гемоглобина в одном эритроците, что дает свои результате при обследовании различных заболеваний. Средняя норма такого количества не должна превышать пределы от 0,86 до 1,05. Но, не смотря на это, нужно четко понимать, что цветовой показатель отражает не точное количество, а общее. Поэтому, достаточно часто встречаются случаи, когда анализ показывает норму, а на самом деле гемоглобин ниже допустимого. Такой результат носит название существующего заболевания нормохромная анемия.
Она бывает двух видов – апластическая и гемолитическая, соответственно и причины возникновения разные.
Цветовой показатель крови может быть повышен при наличии такого заболевания, как В-12-дефицитной анемии. У таких пациентов анализы приходят достаточно неутешительные, что сразу не всегда позволяет выявить наличие причины. Что касается низкого цветного уровня, то он существует при железодефицитной анемии, циррозе печени или же при наличии злокачественных опухолей. В медицинских терминах данное нарушение именуется как гипохромия. Можно выделить основные заболевания, которые возникают при наличии низкого цветового показателя в крови. Это:
При наличии высокого цветового показателя в крови выше 1,1 могут присутствовать такие заболевания, как:
- рак;
- полипоз желудка;
- дефицит витамина В12 в организме;
- дефицит фолиевой кислоты.

Так же есть и обратная связь нарушения, которая характеризуется не продуктивной работой костного мозга и выработкой малого — ниже нормы — количества эритроцитов. Это называется апластическая анемия.
В медицине существует определенная формула, которая помогает провести расчет и определить цветной показатель в крови. Цветовой показатель крови можно рассчитать таким образом:
Ц.П.= (Hb*3) /первые 3 цифры количества Er
Из этой формулы следует, что:
- Ц.П. – это цветовой коэффициент;
- Hb – уровень содержания гемоглобина;
- Er – количество эритроцитов.
Так как норма должна быть не ниже 0,86 и не выше 1,15, то следуя такому расчету можно получить соответствующие результаты данного анализа. Самостоятельно это сделать, конечно, невозможно. Для этого необходимо специальное медицинское оборудование и знания. Таким образом, получив данный расчет, может идти речь о том или ином диагнозе. Чаще всего это либо гипохромная анемия, либо нормохромная, или же гиперхромная.
При наличии того или иного вида, назначается соответствующее дополнительное обследование, что позволяет определить полную картину заболевания. Цветной показатель в крови не может быть понижен или повышен на пустом месте. Этому что-то предшествовало и врач должен выяснить причину.
В первую очередь необходимо обратить внимание на свое питание, а точнее оно должно быть как можно больше сбалансированным. Это отражается и на уровне гемоглобина, ведь если его количество ниже положенного, то организм начинает страдать. В этом случае необходимо есть больше витаминов, сбалансированных витаминами А, Группы В, С и Е. Это могут быть различные овощи и фрукты, белковое мясо, и минимум жареной и жирной пищи.
Если у вас понижен цветовой коэффициент, то врачи могут вам порекомендовать пить каждый день красные соки или немного красного вина. Ешьте как можно больше тех продуктов, которые богаты на железо и цинк. Так же не рекомендуется пить кофе и лучше бросить все вредные привычки.
Стоит отметить, что данную патологию в основном не лечат определенными препаратами, за исключением, если цветовой уровень плазмы слишком сильно понижен и требуется срочная помощь больному. Во всех других случаях, рекомендуется просто следить за своим образом жизни и за сбалансированным питанием. Тогда все результаты анализов и других заборов будут нормальными и удовлетворительными для здоровой жизни. В частности речь идет о физических нагрузках и поддержании стабильной работы кардио-системы.
источник
Анемия. Виды анемий: железодефицитная, гемолитическая, В12 дефицитная, апластическая. Причины, диагностика, степени анемии.
Анемия или пониженное количество гемоглобина в крови, а в просторечии – «малокровие». Практически каждый человек хотя бы один раз сталкивался с такой формулировкой, особенно женщины. Что же означает этот пугающий термин? Почему возникает данное состояние организма? Чем опасна анемия? Как вовремя распознать её на начальных этапах?
Анемия – это патологическое состояние организма, при котором наблюдается снижение количества гемоглобина и эритроцитов ниже нижних границ нормы. Причем уменьшение содержания гемоглобина является обязательным признаком анемии, в отличие от снижения количества эритроцитов. То есть снижение концентрации гемоглобина при анемии есть всегда, а снижение количества эритроцитов может и не быть. Однако в некоторых случаях при анемии выявляются патологические формы эритроцитов (не двояко – вогнутые).
Анемия – это не самостоятельное заболевание, а следствие основной патологии, потому, выявление сниженного уровня эритроцитов и гемоглобина, требует проведения тщательной диагностики для выявления причины!
Гидремия – разжижение крови.
Такое состояние возможно при поступлении в кровоток тканевой жидкости при схождении отека, обильном питье. Гидремия – это псевдоанемия.
Сгущение крови
Сгущение крови может происходить вследствие потери жидкой части крови, что происходит при сильном обезвоживании. Обезвоживание наблюдается в результате сильной рвоты, поноса, обильного потения. Однако в этом случае за счет сгущения крови количество гемоглобина и эритроцитов может быть в пределах нормальных значений. В таких ситуациях говорят о наличии скрытой анемии.
Специфические и неспецифические признаки анемии – что относится к ним?
В первую очередь рассмотрим, как же проявляется анемия. Существуют неспецифические проявления и специфические. Неспецифические проявления называются так, потому что эти признаки общие для всех видов анемий. Специфические же проявления строго индивидуальны и характерны только для каждого конкретного вида анемии.Сейчас мы рассмотрим только неспецифические проявления, а специфические укажем при рассмотрении видов анемий.
Итак, к неспецифическим признакам анемий, относят следующие симптомы:
- бледность кожи и слизистых оболочек
- слабость
- головокружение
- шум в ушах
- головные боли
- быстрая утомляемость
- сонливость
- одышка
- анорексия (патологическая потеря аппетита или отвращение к пище)
- нарушение сна
- нарушения менструального цикла вплоть до полного прекращения менструаций (аменореи)
- импотенция
- тахикардия (увеличение частоты сердечных сокращений)
- шумы в сердце (усиление сердечного толчка, систолический шум на верхушке сердца)
- сердечная недостаточность
- при снижении количества гемоглобина менее 50 г/л возможно развитие ацидоза (закисление крови)
- снижение содержания гемоглобина ниже нормальных показателей
- снижение содержания эритроцитов ниже нормы
- изменение цветного показателя
- изменение содержания лейкоцитов и тромбоцитов
Виды анемий – постгеморрагическая, гемолитическая, дефицитная и гипопластическая
Анемии могут вызываться совершенно разными причинами, поэтому принято все анемии делить по различным признакам, в том числе по причинам, их вызывающим. Согласно причинам (патогенезу) выделяют три вида анемии: постгеморрагические, гемолитические и связанные с нарушением кровообразования (дефицитные и гипопластические). Что это значит? Разберем подробнее.
Постгеморрагические анемии связаны с острой или хронической кровопотерей (кровотечение, ранение).
Гемолитические – развиваются в связи с усиленным разрушением эритроцитов.
Дефицитные анемии вызваны недостатком витаминов, железа или других микроэлементов, которые необходимы для кроветворения.
Гипопластические анемии – это самый тяжелый вид анемий и связан он с нарушением кроветворения в костном мозгу.
- По степени тяжести. Существует три степени тяжести анемии – легкая, средняя и тяжелая в зависимости от содержания гемоглобина и эритроцитов в крови:
| Степень тяжести | Гемоглобин, г/л | Эритроциты, Т/л | ||||||||||||||||||||||
| Легкая | > 100 г/л | > 3 Т/л | ||||||||||||||||||||||
| Средняя | 100 – 66 г/л | 3 – 2 Т/л | ||||||||||||||||||||||
| Тяжелая | 1,05) и гипохромные (ЦП 8,0 микрон) и мегалобластные (СДЭ > 9,5 микрон). Нормоцитарные анемии характеризуются нормальным диаметром эритроцитов, микроцитарные – уменьшенным диаметром эритроцитов, а макроцитарные и мегалобластные связаны с увеличением диаметра эритроцитов. К нормоцитарным анемиям относят – острую постгеморрагическую и большинство гемолитических анемий; к микроцитарным – железодефицитную анемию, микросфероцитоз и хроническую постгеморрагическую анемию. Макроцитарные анемии – это гемолитическая болезнь новорожденных, фолиево дефицитная анемии. Мегалоцитарная – В12 дефицитнаяанемия.
Мы рассмотрели, на какие типы, и по каким признакам классифицируют анемии. Перейдем к рассмотрению, как проявляются отдельные виды анемий, какие изменения при этом наблюдаются в крови и в организме человека в целом.
Симптомы острой постгеморрагической анемии, картина крови Симптомами острой постгеморрагической анемии являются такие признаки: бледность, резкое головокружение, обмороки, частый пульс, холодный пот, снижение температуры тела, иногда рвота. Потеря крови более 30% от исходного уровня является критической и опасна для жизни. Диагностика постгеморрагической острой анемии В крови увеличивается количество ретикулоцитов более 11%, также появляются «незрелые» эритроциты и эритроциты с измененной формой клетки. Со стороны лейкоцитов наблюдается увеличение их общего количества выше 12 Г/л, а в лейкоцитарной формуле идет сдвиг влево. В последующие два месяца после острой кровопотери происходит восстановление показателей эритроцитов и гемоглобина. Однако восстановление количества эритроцитов и содержания гемоглобина связано с расходованием фонда железа в организме и может повлечь за собой развитие железодефицита. Поэтому в период восстановления после кровопотери необходимо соответствующее питание, то есть в рационе должны быть продукты с высоким содержанием железа (например, гранаты, гречка, печень и т.д.). Принципы лечения острой постгеморрагической анемии Лечение острой постгеморрагической анемии должно проводиться в условиях стационара и быть направлено на восстановление количества циркулирующей крови, количества форменных элементов крови и поддержание этих показателей. В первую очередь необходимо остановить кровотечение. Затем в зависимости от количества кровопотери применяют переливание крови, эритроцитарной массы и кровезаменителей. Симптомы хронической постгеморрагической анемии Симптомы хронической постгеморрагической анемии такие же, как при железодефицитной анемии. Какие же это симптомы? Итак, признаками хронической постгеморрагической анемии являются: кожа «алебастрового» оттенка (очень белая, бледная), извращение обоняния (непереносимость запахов или, наоборот, тяга к каким-либо запахам), изменение вкуса, одутловатость лица, пастозность голеней, ломкость волос и ногтей, сухость, шершавость кожи. Также возможно образование койлонехий – истонченных и уплощенных ногтей. Помимо этих внешних признаков возможно появление одышки, тошноты, головокружения, учащения пульса, слабости, утомляемости, субфебрильной температуры (до 37° С) и прочее. Из-за дефицита железа могут проявляться нарушения со стороны желудочно-кишечного тракта – кариес, глоссит, сниженная кислотность желудочного сока, а также непроизвольное мочеиспускание при смехе, потливость. Диагностика хронической постгеморрагической анемии В крови при хронической постгеморрагической анемии появляются слабо окрашенные эритроциты маленького размера, овальные эритроциты, снижено общее количество лейкоцитов, а в лейкоцитарной формуле наблюдается незначительный лимфоцитоз. В сыворотке крови концентрация железа ниже нормы – 9,0 мкмоль/л, также ниже нормального содержание меди, кальция, витаминов А, В, С, но, однако, повышена концентрация цинка, марганца и никеля в крови. Причины хронической постгеморрагической анемии Почему же возникает такое состояние – хроническая постгеморрагическая анемия? Причины этого явления следующие:
Лечение хронической постгеморрагической анемии Именно в силу причин, приводящих к развитию хронической постгеморрагической анемии, при лечении этого состояния, прежде всего, необходимо устранить причину хронической кровопотери.Затем необходимо сбалансированное питание, содержащее продукты с высоким содержанием железа, фолиевой кислоты и витаминов. В случае тяжелой анемии необходимо принимать препараты железа (сорбифер, феррум-лек) в виде таблеток или инъекций, препараты фолиевой кислоты, витамин В12 в виде таблеток или в виде инъекций. Наиболее эффективными препаратами для восстановления уровня железа в организме являются таблетированные препараты, которые выпускаются различными фирмами. В силу этого в аптеках представлен широкий выбор препаратов железа. При выборе препарата необходимо обращать внимание на содержание железа в одной таблетке и биологическую доступность данного препарата. Препараты железа необходимо принимать совместно с аскорбиновой кислотой и фолиевой кислотой, поскольку в такой комбинации происходит наилучшее усвоение железа. Однако при выборе препарата и дозы необходимо обязательно проконсультироваться с врачом. Гемолитические анемии – это группа анемий, при которых процессы разрушения эритроцитов преобладают над процессами их производства. Иными словами разрушение эритроцитов происходит быстрее, чем образуются новые клетки, взамен разрушенных. Гемолитические анемии могут быть наследственными и приобретенными. Наследственные гемолитические анемии это:
Симптомы гемолитических анемий Общим признаком всех гемолитических анемий является желтуха. Желтуха появляется вследствие того, что при разрушении эритроцитов выделяется в кровь большое количество билирубина, который и приводит к данному симптому. Помимо желтухи имеются следующие признаки, общие для всех гемолитических анемий – увеличение печени и селезенки, увеличение концентрации билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев». В связи с тем, что наиболее широкое распространение среди наследственных гемолитических анемий имеют серповидно – клеточная анемия и талассемия, более подробно рассмотрим именно их.
Серповидно – клеточная анемия вызвана тем, что синтезируется молекула гемоглобина с дефектом. Такие дефектные молекулы гемоглобина собираются в веретенообразные кристаллы (тактоиды), которые растягивают эритроцит, придавая ему серповидную форму. Такие серповидные эритроциты мало пластичны, повышают вязкость крови и закупоривают мелкие кровеносные сосуды. Кроме этого своими острыми концами такие эритроциты протыкают друг друга и разрушаются. Симптомы серповидно–клеточной анемии Серповидно – клеточная анемия внешне проявляется следующими признаками:
Диагностика серповидно–клеточной анемии В анализе крови сниженное количество гемоглобина (50 – 80 г/л) и эритроцитов (1 – 2 Т/л), увеличение ретикулоцитов до 30% и более. В мазке крови видны серповидные эритроциты и эритроциты с тельцами Жолли и кольцами Кабо. Лечение серповидно-клеточной анемии Основной принцип лечения данного вида анемии –это недопущение гемолитических кризов. Данный эффект достигается тем, что человек избегает гипоксических состояний – присутствия в разреженном воздухе, в местах с низким содержанием кислорода и прочее. Используют переливание эритроцитарной массы или кровезаменителей.
Талассемия возникает вследствие нарушения скорости образования гемоглобина. Такой незрелый гемоглобин не стабилен, в результате чего он выпадает в эритроцитах в виде включений – телец, а весь эритроцит приобретает внешний вид мишеневидной клетки. Талассемия – это тяжелое наследственное заболевание, которое невозможно вылечить, а можно лишь облегчить ее проявления. Симптомы талассемии
Диагностика талассемии В крови обнаруживаются мишеневидные эритроциты, увеличенное количество ретикулоцитов, снижение концентрации гемоглобина до 20 г/л, а эритроцитов до 1 Т/л. Также наблюдаются уменьшение количества лейкоцитов и тромбоцитов. Итак, мы рассмотрели основные виды наследственных гемолитических анемий, которые передаются от родителей к детям. Перейдем к рассмотрению приобретенных гемолитических анемий, которые возникают вследствие наличия провоцирующего фактора. Приобретенные гемолитические анемии, иммунные и не иммунные анемии Прежде всего, необходимо отметить, что приобретенные гемолитические анемии могут развиваться при участии иммунной системы (иммунные) или без ее участия (не иммунные). К анемиям, развивающимся при участии иммунной системы, относятся вирусная, сифилитическая анемия и гемолитическая болезнь новорожденных. Не иммунные гемолитические анемии – это болезнь Маркиафавы – Микелли, а также анемии, возникшие вследствие длительной маршевой ходьбы, отравления алкоголем, кислотами, солями тяжелых металлов, ядами змей, насекомых и грибов. При ожогах, составляющих более 20% поверхности тела, недостатке витамина Е и малярии, также развивается не иммунная гемолитическая анемия.
Лечение этих видов анемии, как правило, не требуется. Гемолитическая болезнь новорожденного, причины развития, симптомы заболевания, степени тяжести.
В настоящее время проводится профилактика гемолитической болезни новорожденных путем отслеживания наличия антител у матери. Если у матери выявляются антитела, то лечение проводят в стационаре. При этом производят вливание антирезусных иммуноглобулинов. Признаки не иммунных гемолитических анемий, лабораторные симптомы Не иммунные гемолитические анемии имеют следующие признаки – желтуха,увеличенные печень и селезенка,повышенная концентрация билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев».В картине крови отмечается наличие эритроцитов различной формы и размеров, ретикулоцитоз до 30% и выше, сниженное количество лейкоцитов и тромбоцитов. Такие анемии сами по себе не требуют отдельного и особенного лечения, так как в первую очередь необходимо убрать фактор, вызывающий эту анемию (яды змей, соли тяжелых металлов и т.д.). Анемии, вызванные нарушением кровообразования, делятся на две большие группы – дефицитные анемии и гипопластические. Дефицитные анемии связаны с дефицитом необходимых для кроветворения элементов. К дефицитным анемиям относят – железодефицитную анемию, железорефрактерную анемию, В12 – дефицитную и фолиево дефицитную. Гипопластические анемии вызваны гибелью клеток – предшественниц в костном мозгу. Гипопластические анемии могут быть наследственными (анемия Фанкони, анемия Эстрена – Дамешика, анемия Блекфэрна — Даймонда) и приобретенными. Приобретенные гипопластические анемии развиваются либо сами по себе вследствие неизвестной причины, либо на фоне имеющегося заболевания — лучевой болезни, инфекций, повреждений иммунитета. Для большинства людей больший интерес представляют дефицитные анемии, которые могут возникнуть практически у каждого человека. Поэтому наиболее подробно остановимся именно на этом виде анемий.
Причины железодефицитной анемии Железодефицитная анемия возникает в следующих случаях:
Симптомы железодефицитной анемии Клинически железодефицитная анемия проявляется тремя основными синдромами – гипоксическим, сидеропеническим и анемическим. Что это за синдромы? Чем характеризуется каждый из них?Синдром – это устойчивая совокупность симптомов. Итак, гипоксический синдром характеризуется одышкой, головными болями, шумом в ушах, быстрой утомляемостью, сонливостью и тахикардией; анемический синдром выражается в уменьшении содержания количества эритроцитов и гемоглобина. Сидеропенический синдром напрямую связан с уменьшением количества железа в организме и проявляется так: нарушение питания кожи, ногтей, волос – кожа «алебастрового» оттенка, сухость и шершавость кожи, ломкие волосы и ногти. Затем присоединяетсяизвращение вкуса и обоняния (желание есть мел, вдыхать запах мытых бетонных полов и т.д.). Возможно появление осложнений со стороны желудочно-кишечного тракта – кариеса, дисфагии, снижения кислотности желудочного сока, непроизвольного мочеиспускания (в тяжелых случаях), потливости. Диагностика железодефицитной анемии В крови наблюдается снижение содержания гемоглобина до 60 – 70 г/л, эритроцитов до 1,5 – 2 Т/л, также снижено количество или вовсе отсутствуют ретикулоциты. Появляются эритроциты различных форм и размеров. Концентрация сывороточного железа ниже нормы. Лечение железодефицитной анемии В основе лечения железодефицитной анемии лежат принципы устранения причины ее возникновения – лечение заболеваний желудочно – кишечного тракта, а также введение сбалансированного пищевого рациона. В диете должны присутствовать продукты с высоким содержанием железа (печень, мясо, молоко, сыр, яйца, злаки и т.д.). Однако главным средством восстановления количества железа в организме на начальном этапе являются лекарственные препараты железа. В большинстве случаев такие лекарства назначают в виде таблеток. В тяжелых случаях прибегают к внутримышечным или внутривенным инъекциям. В лечении данной анемии используют, например, такие препараты: сорбифер, феррум-лек, тардиферон, тотема и другие. Выбор различных лекарственных средств, в том числе комбинированных, очень широк. При выборе необходимо консультироваться с врачом. Обычно, суточная доза для профилактики и лечения анемии легкой степени составляет 50-60 мг железа, для лечения анемии средней тяжести – 100-120 мг железа в сутки. Лечение анемии тяжелой степени проводят в стационаре и применяют препараты железа в виде инъекций. Затем переходят на таблетированные формы. Препараты железа вызывают потемнение стула, однако в данной ситуации это нормально.Если препарат железа вызывает неприятные ощущения в желудке, то его необходимо заменить.
Железорефрактерную анемию также называют сидеробластной или сидероахристической. Железорефрактерная анемия развивается на фоне нормального содержания железа в сыворотке крови и недостатка ферментов, которые участвуют в синтезе гемоглобина. То есть основная причина железорефрактерной анемии – нарушение процессов «усвоения» железа. Симптомы железорефрактерной анемии, что такое гемосидероз? Проявляется железорефрактерная анемия одышкой, головными болями, головокружением, шумом в ушах, быстрой утомляемостью, сонливостью, нарушениями сна и тахикардией. Из-за высокого содержания железа в крови тканях наблюдается гемосидероз.Гемосидероз – это отложение железа в органах и тканях вследствие его избытка. При гемосидерозе развивается недостаточность сердечно – сосудистой системы вследствие отложения железа в сердечной мышце, сахарный диабет, поражение легких и увеличиваются размеры печени и селезенки. Кожа приобретает землянистый оттенок. Диагностика железорефрактерной анемии, что такое сидеробласты? Цветной показатель крови снижен до 0,6 – 0,4, присутствуют эритроциты различных форм и размеров, количество гемоглобина и эритроцитов ниже нормы. Имеются изменения и в костном мозгу – появляются клетки – сидеробласты. Сидеробласты – это клетки, имеющие вокруг ядра венчик из железа. В норме таких клеток в костном мозгу 2,0 – 4,6%, а при железорефрактерной анемии их количество может доходить до 70%. Лечение железорефрактерной анемии Лечения, которое смогло бы устранить ее совсем, на сегодняшний день нет. Возможно применение заместительной терапии – вливание эритроцитарной массы и кровезаменителей.
Во-первых, что такое В12? В12 – это витамин, который имеет также название цианкобаламин. Цианкобаламин содержится в основном в продуктах животного происхождения – мясо, печень, почки, молоко, яйца, сыр. Уровень витамина В12 необходимо постоянно поддерживать употреблением соответствующих продуктов, поскольку происходят его естественные физиологические потери с калом и желчью. Причины В12 дефицитной анемии Итак, В12 – дефицитная анемия – это анемия, возникающая вследствие недостаточности витамина В12. Недостаток витамина В12 может быть вызван недостаточным его поступлением с пищей или нарушением его усвоения в желудочно-кишечном тракте. Недостаточное поступление цианкобаламина с пищей возможно у строгих вегетарианцев. Также недостаток В12 может проявиться при повышении потребности в нем у беременных женщин, кормящих матерей, раковых больных. Неусвоение витамина В12, поступающего с пищей в достаточном количестве, происходит при заболеваниях желудка, тонкого кишечника (дивертикулы, глисты) и лечении противосудорожными средствами или оральными контрацептивами. Симптомы В12 дефицитной анемии Симптомы проявления В12 – дефицитной анемии характеризуются нарушениями в центральной нервной системе и желудочно-кишечном тракте. Итак, рассмотрим эти две большие группы симптомов:
Диагностика В12 дефицитной анемии В системе крови происходит переход на мегалобластический тип кроветворения. Это означает, что в крови появляются гигантские эритроциты с укороченным сроком жизни, ярко окрашенные эритроциты без просветления в центре, грушевидные и овальные эритроциты с тельцами Жолли и кольцами Кабо. Также появляются гигантские нейтрофилы, уменьшается количество эозинофилов (вплоть до полного отсутствия), базофилов и общего количества лейкоцитов. В крови повышена концентрация билирубина, в связи с чем, может наблюдаться легкая желтушность кожи и склер глаз. Лечение В12 дефицитной анемии В первую очередь необходимо вылечить заболевания желудочно-кишечного тракта и наладить сбалансированное питание, с достаточным содержанием витамина В12. Применение курса инъекций витамина В12 быстро нормализует кроветворение в костном мозгу, а далее необходимо постоянное, регулярное поступление с пищей достаточного количества витамина В12.
Симптомы фолиеводефицитной анемии При фолиево дефицитной анемии страдает желудочно-кишечный тракт, поэтому и проявления данной анемии связаны с нарушениями работы желудочно-кишечного тракта. Наблюдается появление повышенной чувствительности к кислой пище, глоссита, трудностей глотания, атрофии слизистой желудка, увеличения размеров печени и селезенки. Лечение фолиеводефицитной анемии Для лечения данного вида анемии применяют таблетки фолиевой кислоты и нормализуют рацион питания, в котором должны быть продукты, содержащие достаточное количество фолиевой кислоты.
Симптомы гипопластических анемий Гипопластические анемии могут быть наследственными или приобретенными, однако все подвиды данного типа анемий характеризуются одинаковыми проявлениями. Рассмотрим эти симптомы:
Причины, вызывающие развитие гипопластической анемии Какие же причины способны вызывать подобное поражение костного мозга? Наследственные анемии, соответственно, передаются по наследству, а вот приобретенные? Все факторы, способные приводить к развитию гипопластической анемии, делятся на экзогенные (внешние) и эндогенные (внутренние). В таблице приведены основные экзогенные и эндогенные причины, способные вызвать развитие гипопластической анемии.
Принципы лечения гипопластических анемий Лечение гипопластических анемий находится строго в компетенции врача – гематолога. Могут применяться различные методы стимулирования кроветворения, или пересадка костного мозга. Итак, мы рассмотрели все основные виды анемий. Конечно, их гораздо больше, однако мы не можем объять необъятное. При появлении каких-либо признаков анемии необходимо своевременно обратиться к врачу. И регулярно сдавать анализ крови на содержание гемоглобина. источник |

 Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.
Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.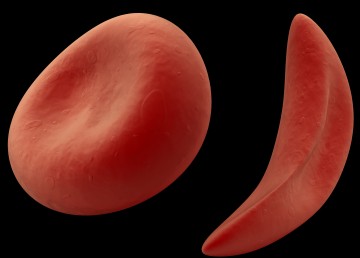 Причины серповидно–клеточной анемии
Причины серповидно–клеточной анемии Талассемия – причины заболевания
Талассемия – причины заболевания Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы.
Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы.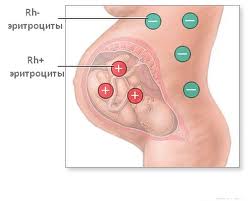 Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.
Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.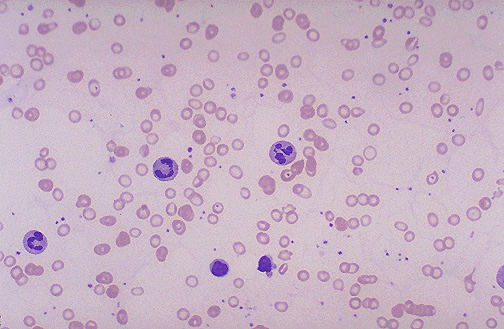 Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты.
Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты. Причина железорефрактерной анемии
Причина железорефрактерной анемии Что такое В12? Где содержится этот витамин?
Что такое В12? Где содержится этот витамин? Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12.
Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12. Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.
Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.