Лечение анемии у детей должно назначаться педиатром после тщательного обследования.
Очень важно, чтобы лечение охватывало три направления:
- устранение причины анемии;
- нормализацию режима питания малыша;
- восполнение дефицита железа в организме.
Правильное питание малыша является одной из составляющих лечения. Для грудных детей – это молоко матери. Грудное молоко полезное по двум причинам: оно не только содержит железо в легкоусвояемой форме, но и улучшает его всасывание из других продуктов, которые ребенок получает вместе с молоком.
Если ребенок находится на искусственном вскармливании, его необходимо кормить адаптированными молочными смесями, специально предназначенными для детей с анемией (обогащенные железом).
! При выборе смесей обязательно проконсультируйтесь с педиатром, так как эти смеси относятся к категории лечебных
Даже с хорошими запасами железа в организме, у детей к 5-6 месяцам они заканчиваются, формируется необходимость получать железо из еды, а значит, нужно вводить прикорм.
Детям с анемией рекомендовано вводить прикорм на 2-4 недели раньше установленного срока. Мясной прикорм следует вводить в 6 месяцев. Лучше отказаться от таких каш, как манная и рисовая. Для детей с анемией больше подходят гречневая, ячменная, просяная каши.
Продукты, содержащие наибольшее количество железа: печень, язык, почки, яичный желток, морская капуста, гречка, персики, устрицы, лесные орехи, шпинат, отруби.
Для начала необходимо ознакомиться с тем, какие продукты содержат железо и как правильно их совмещать, чтобы железо лучше усваивалось организмом ребенка.
- Известно, что продукты, богатые витамином С, способствуют лучшему усвоению железа из пищи.
- Мясо, птица, рыба содержат достаточно железа, которое хорошо усваивается
- Можно сказать, что порция мяса с овощами – не только сытная, но и полезная еда.
- Яблоки и кислые фрукты улучшают всасывание железа.
- Если Вы любите печь, то добавляйте в муку тонкого помола отруби, в которых содержится множество активных веществ и водорастворимых элементов.
Также есть ряд продуктов, которые не следует давать детям вместе с железосодержащей пищей — это ингибиторы абсорбции железа:
- чай и кофе (перерыв между основным приемом пищи должен составлять не менее 1 часа);
- молоко и молочные продукты, если их употреблять вместе с остальной едой;
- грудные дети лучше усваивают железо, если между кормлением грудью и приемом твердой пищи проходит не менее 1 часа.
У детей с анемией восстановление уровня гемоглобина только за счет диеты представляется довольно сложным, так как процент усвоения железа из еды составляет 1-20%, а у лекарственных препаратов он гораздо выше – 30-40%.
Диета при коррекции анемии, как правило, назначается одновременно с препаратами железа.
- Профилактика анемии у детей начинается еще во время беременности мамы. В этот период крайне важно соблюдать все рекомендации врача относительно питания и образа жизни.
- Грудное вскармливание также является гарантом правильного развития ребенка.
- У детей, которые находятся на смешанном и искусственном вскармливании, необходим адекватный подбор смеси.
- Профилактика также включает в себя полноценное питание, своевременное введение прикорма, физическую активность, прогулки на свежем воздухе, внимательное отношение родителей к здоровью ребенка.
Для лечения железодефицитной анемии используются препараты железа.
- Лечение должно быть назначено врачом после обследования и постановки диагноза. Препарат и дозирование рассчитывается индивидуально, а родителям рекомендуется точно следовать инструкции.
- Не занимайтесь самолечением.
При приеме препаратов железа возможны такие побочные явления как тошнота и рвота, о такой реакции необходимо сообщить врачу. При абсолютной непереносимости сиропов и таблеток врач может назначить раствор железа в уколах.
Вместе с препаратами железа, врач может назначить прием поливитаминов. Довольно часто, дефицит витаминов и микроэлементов бывает комплексным, поэтому и лечение должно быть одновременным.
Эффективность лечение определяют результаты анализа крови, который необходимо повторно сдать через несколько недель после начала лечения.
! Интерпретировать анализы может только врач
Хотя гемоглобин может нормализироваться уже через 3-5 недель после начала лечения, препараты, как правило, нужно принимать не менее 3 месяцев. Это связано с тем, что железо должно не только усвоиться, но и пополнить депо (запасы) в организме ребенка.
К современным железосодержащим препаратам с доказанной эффективностью относится препарат Тотема, в котором содержится глюконат железа, марганец глюконат и медь глюконат. Марганец и медь необходимы для повышения эффективности всасывания железа в процессе синтеза гемоглобина и переноса кислорода. Тотема выпускается в ампулах из коричневого стекла, защищающего железо в препарате. Принимается препарат внутрь в виде раствора. Тотема особенна тем, что для нормализации уровня гемоглобина, его можно применять у детей, начиная с 1 месяца.
источник
Правильное питание при анемии для пациентов направлено на восстановление процесса кроветворения и нормализацию состава крови. Помимо употребления продуктов, богатых железом, при анемии важно больше времени проводить на свежем воздухе, полноценно отдыхать и соблюдать остальные правила, предусмотренные вашим лечащим врачом.
Если у вас была диагностирована лёгкая стадия малокровия, тогда лечение будет заключаться только в соблюдении диеты. При средней и тяжёлой формах используются дополнительно медикаменты, витамины и другие полезные вещества в виде лекарственных препаратов. Но соблюдать правила диеты всё равно нужно и дальше.
В диетотерапии, направленной против малокровия, есть свои правила, особенности, ограничения и рекомендации. Даже полезные продукты могут оказать негативное воздействие на ваш организм. Потому старайтесь употреблять только то, что одобрят ваш лечащий врач и диетолог.
Чтобы не называть целый перечень продуктов, которые нельзя есть во время диеты против анемии или следует ограничить, рассмотрим наиболее вредные вещества.
Больным нужно избегать употребления:
Эти вещества способствуют тому, что нарушается всасываемость железа. Потому если у вас обнаружена железодефицитная форма малокровия, как самая распространённая в мире (95% всех случаев анемии), то ограничивайте в рационе продукты, содержание эти компоненты.
Кальций необходим каждому, особенно детям в период их роста и развития. Но, кроме пользы, кальций нарушает процессы всасывания. Наибольшая его концентрация в молочной продукции, потому не стройте диету, основываясь на ней.
Оксалаты являются ещё одним компонентом, который мешает нормальному всасыванию железа. Они содержатся в орехах (грецких), бобовых культурах, цельном зерне, шпинате, шоколаде и прочих продуктах. Хотя тут есть выход из ситуации. Если вы любите бобовые, просто замочите их в воде, выдержав 12 часов. Это заметно снизит негативное воздействие на организм, позволив насладиться блюдами из этих продуктов.
Полифенолы считаются главными ингибиторами всасывания. Наибольшая концентрация в чёрных сортах чая и кофе. Какао и некоторые травяные чаи тоже придётся ограничить. Никакого кофе, ведь он на 60% способен блокировать всасываемость организмом железа.
Чтобы правильно питаться при анемии, вам необходимо отказаться от наиболее вредной и опасной пищи. Старайтесь не употреблять в пищу большое количество жиров. Они способствуют угнетению процессов образования крови. Суточная норма жиров составляет до 80 грамм.
Это ограничение относится к чистому животному жиру, жирным сортам рыбы. Если вы будете питаться диетическим мясом и птицей, то принесёте только пользу своему организму. А опасный жир стоит заменить растительными маслами.
Из названия понятно, что причиной развития железодефицитной анемии выступает нехватка в организме такого вещества, как железо. Чтобы справиться с проблемой, нужно обеспечить кровь этим элементом через продукты, которые его содержат.
К причинам развития патологии относят:
- плохое питание;
- чрезмерную физическая активность и усталость;
- длительное голодание;
- соблюдение строгих диет;
- внутренние кровотечения;
- злокачественные новообразования.
В последних двух случаях простой корректировкой рациона проблему не решить. Здесь придётся обращаться за помощью и заниматься сложным длительным лечением.
Если же причины не связаны с опасными патологиями, тогда восстановить образование крови и вернуть человека к нормальному самочувствию поможет правильно построенная диета.
Здесь есть несколько основных правил питания, которых нужно придерживаться.
- Употребление продуктов, богатых железом, при анемии способствует восстановлению количества этого вещества в крови. Поднимается гемоглобин и восстанавливается хорошее самочувствие;
- Железосодержащие продукты при анемии употребляют в виде белковой пищи (не больше 120 грамм в сутки), фруктов и различных овощей. Количество жиров снижается до 40 грамм. Обязательно делается упор на ягоды, зелень и свежие соки.
- При диетической терапии соблюдайте правило, которое предусматривает одновременное употребление железосодержащих блюд и витамина С. Последний помогает нормализовать всасываемость и усвоение вещества в организме человека.
- Поскольку молочные продукты кушать нужно из-за наличия в них кальция, сделайте их отдельным приёмом пищи. Иначе кальций не позволит железу усваиваться.
Только квалифицированные специалисты могут точно сказать своим пациентам, что есть при анемиях. Это объясняется необходимостью сначала сдать анализы, провести некоторые исследования и определить причины развития малокровия.
Строить диеты самостоятельно не рекомендуется. Путём анализов следует определить, чего в организме не хватает, в каких веществах ощущается нехватка, и на какие продукты есть аллергия.
Хотя заболевание встречается реже по сравнению с детьми, но при анемии у взрослых патология протекает сложнее, и на лечение уходит больше времени. В основном к такому состоянию приводят тяжёлые физические нагрузки, сильная утомляемость на работе вместе с отсутствием нормального, разнообразного и сбалансированного питания.
Для них питание при анемии основано на повышении количества потребляемого белка, необходимых микроэлементов и витаминов. Что нужно есть и в каком количестве, скажет лечащий врач. Для взрослых рекомендуется соблюдение такой суточной схемы:
- не более 120 граммов белка в течение дня;
- максимум 40 грамм жира в сутки;
- до 450 грамм углеводов, потребляемых за день;
- средний показатель калорийности составляет от 2,5 до 3 тысяч ккал.
Для получения всего необходимого еда взрослого человека с малокровием должна включать фрукты и овощи. Упор делается на:
Этот список условный. В него включены продукты, богатые на железо и его соединения. Но у каждого взрослого могут иметься свои индивидуальные противопоказания, аллергия и непереносимость.
Питание при анемии у женщин, которые находятся в положении, будет отличаться. Среди беременных малокровие считается довольно распространённым нарушением, которое способно негативно влиять на рост и развитие плода. Это потенциально высокая угроза для ребёнка.
Диета при анемии является частью комплексной терапии, рекомендованной для беременных при выявлении этого заболевания. Кроме правильно подобранных продуктов, в состав терапии входит приём лекарственных препаратов и витаминов.
Развитие малокровия объясняется несколькими причинами:
- растёт потребность организма в питательных веществах из-за развития плода;
- организм мамы является единственным источником питания для малыша;
- объём циркулирующей крови увеличивается, из-за чего растёт и количество клеток крови.
Не зря существует фраза, что беременные питаются за двоих. Это так, потому прежнего количества пищи уже недостаточно для нормального функционирования женского организма и растущего внутри него плода.
Диета беременной основывается на:
Будьте осторожными с каждым из продуктов, поскольку многие из них выступают потенциальными аллергенами. Прежде чем есть цитрусовые, некоторые овощи, ягоды и рыбу, проконсультируйтесь со своим врачом. Он даст рекомендации по подбору наиболее полезной и безопасной для малыша пищи.
Если малокровие обусловлено дефицитом витаминов группы В, тогда придётся отказаться от молока, яиц и всего мясного.
При анемии у пожилых людей есть свои особенности составления рациона. Малокровие считается распространённой патологией людей преклонного и старческого возраста. Это объясняется началом малоподвижного образа жизни, целым букетом хронических заболеваний и сокращением функций и дееспособности иммунной системы.
Здесь врачи дают важные рекомендации касательно того, как питаться. Важно не допускать приступов голода, но и не переедать. То есть кушать следует регулярно, но небольшими порциями.
Такое правило связано с тем, что органы и системы начинают стареть. Физиологически пищеварительная система не способна работать так же, как у молодых людей. Потому переедания перегружают систему, а голодание отрицательно сказывается на дальнейшей усвояемости еды.
Нет конкретных запретов на употребление пищи. Но упор лучше сделать на:
- качественное нежирное мясо;
- молочные продукты;
- фрукты;
- зелень;
- свежие сезонные ягоды и овощи.
Важно получать все необходимые витамины при анемии в достаточном количестве. Потому ошибкой считается переход на вегетарианское меню. Пожилой организм не может быстро и эффективно перестроиться под новый вариант питания, потому это негативно отразится на его состоянии.
Постарайтесь есть по 2 – 4 яйца за неделю, употреблять больше гречки, свёклы и капусты. А вот от бобовых стоит отказаться, ведь они плохо усваиваются организмом в этом возрасте.
Хорошим решением станет измельчение полезных растительных продуктов с помощью блендера или мясорубки. Это позволит есть такую пищу людям, у которых проблемы с пищеварением или слабые зубы. Перетёртая и измельчённая еда быстрее переваривается, на неё затрачивается меньше сил и энергии.
С едой для детей проблем намного меньше. Им можно давать больше разнообразных продуктов. Важно организовать разнообразное и аппетитное меню, чтобы у ребёнка возникало желание съесть что-нибудь полезное и вкусненькое.
Удостоверьтесь, что за сутки ваш ребёнок съедает:
Если малокровие находится в средней стадии, тогда от большого количества жиров лучше отказаться. Вместо них включите продукты, богатые на железо, витамины А, В и С. Отлично подойдут печень, язык, бобовые, крупы, пюре из овощей и рагу. Если вы правильно и оригинально приготовите эти продукты, дети будут кушать их с огромным удовольствием.
Для компенсации недостающего витамина А добавьте в повседневный рацион морскую рыбу. А витамин В получают из говядины, чернослива и бобовых.
Если дети отказываются кушать печень, тогда придётся идти на небольшие хитрости. Для этого её измельчают, добавляя в пюре, кашу и прочие блюда. Взрослым детям рекомендуется делать домашние печёночные паштеты и готовить из печени запеканки. Жарить её не рекомендуется.
Проблема малокровия характерна для той категории детей, которые придерживаются слишком однообразного питания. Нет ничего плохого в том, что ребёнок любит вкусные мясные сосиски с макаронами из твёрдых сортов, йогурты или другие полезные блюда. Некоторые могут есть такое по несколько раз в день. Родителям проще, поскольку ничего выдумывать не приходится. Но в однообразном рационе наблюдается нехватка ряда витаминов, минералов и микроэлементов, которые можно получить только из других продуктов, которые дети не едят.
Ещё одной распространённой ошибкой родителей при коррекции меню для детей при малокровии является попытка заставить кушать то или иное блюдо. Когда малыша заставляют что-то съесть, это ещё больше отталкивает его от пищи. Лучше попробуйте приготовить что-то вместе, позвольте ему принять участие в готовке. Разносящиеся ароматы будут стимулировать питание, а участие в процессе заставить сильно захотеть попробовать то, что он приготовил своими руками.
Суть правильного питания при возникновении малокровия или анемии у людей разного возраста состоит в разнообразии меню. Используйте разную вкусную и аппетитную еду. Список продуктов обширный, что позволяет выбирать оптимальный перечень блюд для своей диеты.
Правильное питание не является панацеей против анемии. Чтобы справиться с этим заболеванием, нужно определить первопричину его развития. Избавившись от неё, вы сможете вернуться к нормальной жизни, устранить неприятные симптомы и восстановить все функции своего организма. Полезная пища способна поддерживать состояние здоровья и частично компенсировать нехватку ряда витаминов, минералов и микроэлементов. Хотя иногда без помощи лекарственных препаратов не обойтись.
Правильная и здоровая пища полезна всегда и для всех. Придерживаясь правил питания, можно предотвратить целый ряд опасных патологий и заболеваний, включая малокровие. Но заметив первые же признаки анемии, сразу обращайтесь за помощью к квалифицированному врачу. Только он поставит точный диагноз и даст конкретные рекомендации по лечению и питанию для борьбы с недугом.
Спасибо всем вам за внимание! Обязательно подписывайтесь, не забывайтесь оставлять комментарии, задавать интересующие вас вопросы и приглашать к обсуждению своих друзей!
источник
Анемию и анемический синдром, вызываемый многими причинами, можно упомянуть среди наиболее часто встречающихся патологических состояний, с которыми ежедневно приходится сталкиваться педиатрам общей практики. В эту группу входят различные заболевания
Анемию и анемический синдром, вызываемый многими причинами, можно упомянуть среди наиболее часто встречающихся патологических состояний, с которыми ежедневно приходится сталкиваться педиатрам общей практики. В эту группу входят различные заболевания и патологические состояния, характеризующиеся уменьшением содержания гемоглобина и/или эритроцитов в единице объема крови, приводящие к нарушению снабжения тканей кислородом. Применяются следующие лабораторные критерии анемии (Н. П. Шабалов, 2003). В зависимости от возраста детей уровень гемоглобина составляет:
- 0–1 сутки жизни — 3+ . Лактоферрин в грудном молоке содержится в виде насыщенной и ненасыщенной форм. Соотношение форм лактоферрина меняется в зависимости от периода лактации. В течение первых 1–3 мес жизни превалирует насыщенная железотранспортная форма лактоферрина. Наличие специфических рецепторов к лактоферрину на эпителиальных клетках слизистой оболочки кишечника способствует адгезии с ними лактоферрина и более полной его утилизации. Кроме того, лактоферрин, связывая лишнее, не всосавшееся в кишечнике железо, лишает условно-патогенную микрофлору необходимого для ее жизнедеятельности микроэлемента и запускает неспецифические бактерицидные механизмы. Установлено, что бактерицидная функция иммуноглобулина A реализуется только в присутствии лактоферрина.
Физиологические потери железа с мочой, потом, калом, через кожу, волосы и ногти не зависят от пола и составляют 1–2 мг в сутки, у женщин во время менструации — 2–3 мг в сутки. У детей потеря железа составляет 0,1–0,3 мг в сутки, возрастая до 0,5–1,0 мг в сутки у подростков.
Ежедневная потребность детского организма в железе составляет 0,5–1,2 мг в сутки. У детей раннего возраста в связи с быстрыми темпами роста и развития наблюдается повышенная потребность в железе. В этот период жизни запасы железа быстро истощаются из-за усиленного его потребления из депо: у недоношенных детей к 3-му месяцу, у доношенных — к 5–6-му мес жизни. Для обеспечения нормального развития ребенка в суточном рационе новорожденного должно содержаться 1,5 мг железа, а у ребенка 1–3 лет — не менее 10 мг.
Дефицит железа у детей приводит к росту инфекционной заболеваемости органов дыхания и ЖКТ. Железо необходимо для нормального функционирования структур головного мозга, при его недостаточном содержании нарушается нервно-психическое развитие ребенка. Установлено, что у детей, имевших в младенчестве железодефицитную анемию, в возрасте 3–4 лет определяются нарушения передачи нервных импульсов от центров головного мозга к органам слуха и зрения из-за нарушения миелинизации и, как следствие этого, нарушение проводимости нервов.
Причины железодефицитных состояний у детей очень разнообразны. Основной причиной ЖДА у новорожденных считается наличие ЖДА или скрытого дефицита железа у матери во время беременности. К антенатальным причинам относят также и осложненное течение беременности, нарушение маточно-плацентарного кровообращения, фетоматеринские и фетоплацентарные кровотечения, синдром фетальной трансфузии при многоплодной беременности. Интранатальными причинами дефицита железа являются: фетоплацентарная трансфузия, преждевременная или поздняя перевязка пуповины, интранатальные кровотечения из-за травматических акушерских пособий или аномалий развития плаценты или пуповины. Среди постнатальных причин сидеропенических состояний на первое место выступает недостаточное поступление железа с пищей. При этом более всего страдают новорожденные, находящиеся на искусственном вскармливании неадаптированными молочными смесями, коровьим и козьим молоком. Другими постнатальными причинами ЖДА являются: повышенная потребность организма в железе; потери железа, превышающие физиологические; заболевания ЖКТ, синдром нарушенного кишечного всасывания; дефицит запасов железа при рождении; анатомические врожденные аномалии (дивертикул Меккеля, полипозы кишечника); употребление продуктов, тормозящих абсорбцию железа.
В группе риска всегда находятся недоношенные дети и дети, родившиеся с очень большой массой, дети с лимфатико-гипопластическим типом конституции.
У детей первого года жизни к дефициту железа чаще всего приводит несбалансированная диета, в частности вскармливание исключительно молоком, вегетарианство, недостаточное употребление мясных продуктов.
К сидеропении способны приводить кровотечения различной этиологии. Источником этого могут быть: грыжа пищеводного отверстия диафрагмы, варикозное расширение вен пищевода, желудочно-кишечные язвы, опухоли, дивертикулы, язвенный колит, геморроидальные узлы, а также кровотечения из мочеполового тракта и дыхательных путей. Прием некоторых медикаментов, таких как нестероидные противовоспалительные препараты, салицилаты, кумарины, глюкокортикостероиды, также может привести к потере железа. Дефицит железа всегда сопутствует заболеваниям, сопровождающимся нарушениями кишечного всасывания (энтериты, болезнь Крона, паразитарные инвазии и др.). Дисбактериоз кишечника также препятствует нормальному перевариванию пищи и тем самым снижает способность организма усваивать железо. Кроме того, может иметь место нарушение транспорта железа из-за недостаточной активности и снижения содержания трансферрина в организме.
Распознать причину развития ЖДА в каждом конкретном случае чрезвычайно важно. Ориентация на нозологическую диагностику необходима, так как в большинстве случаев при лечении анемии можно воздействовать и на основной патологический процесс.
ЖДА проявляется общими симптомами. Один из главных и видимых признаков — бледность кожных покровов, слизистых оболочек, конъюнктив глаз. Обращают на себя внимание общая вялость, капризность, плаксивость, легкая возбудимость детей, снижение общего тонуса организма, потливость, отсутствие или снижение аппетита, поверхностный сон, срыгивание, рвота после кормления, понижение остроты зрения. Выявляются изменения со стороны мышечной системы: ребенок с трудом преодолевает физические нагрузки, отмечается слабость, утомляемость. У детей первого года жизни может наблюдаться регресс моторных навыков.
Во втором полугодии жизни и у детей старше года наблюдаются признаки поражения эпителиальной ткани — шершавость, сухость кожи, ангулярный стоматит, болезненные трещины в уголках рта, глоссит или атрофия слизистой оболочки ротовой полости, ломкость и тусклость волос, их выпадение, матовость и ломкость ногтей, разрушение зубов (кариес), отставание в физическом и психомоторном развитии.
В зависимости от степени тяжести заболевания выявляются симптомы поражения органов и систем: сердечно-сосудистой — в виде функционального шума в сердце, тахикардии; нервной системы — в виде головных болей, головокружений, обмороков, ортостатических коллапсов. Возможно увеличение размеров печени, селезенки. Со стороны ЖКТ наблюдается затрудненное глотание, вздутие кишечника, диарея, запоры, извращение вкуса — желание есть глину, землю.
Диагноз ЖДА ставится на основании клинической картины, лабораторных признаков анемии и дефицита железа в организме: гипохромная (цветовой показатель 3+ (мальтофер, мальтофер фол, феррум лек). Эти соединения имеют большую молекулярную массу, что затрудняет их диффузию через мембрану слизистой кишечника. Они поступают из кишечника в кровь в результате активного всасывания. Это объясняет невозможность передозировки препаратов в отличие от солевых соединений железа, всасывание которых происходит по градиенту концентрации. Взаимодействия их с компонентами пищи и лекарственными препаратами не происходит, что позволяет использовать неионные соединения железа, не нарушая режим питания и терапии сопутствующей патологии. Их применение существенно снижает частоту развития побочных эффектов, обычно наблюдаемых при назначении пероральных препаратов железа (тошнота, рвота, диарея, запоры и др.). Кроме того, у детей раннего возраста большое значение имеет лекарственная форма препарата. В этом возрасте удобно использовать капли и сиропы, что обеспечивает в том числе возможность точного дозирования препаратов и не вызывает негативного отношения ребенка.
При назначении любых препаратов железа необходимо рассчитывать индивидуальную потребность в нем для каждого пациента, исходя из того, что оптимальная суточная доза элементарного железа составляет 4–6 мг/кг. Среднесуточная доза железа при лечении ЖДА составляет 5 мг/кг. Применение более высоких доз не имеет смысла, поскольку объем всасывания железа не увеличивается.
Применение парентеральных препаратов железа показано для быстрого достижения эффекта при анемии тяжелой степени; патологии ЖКТ, сочетающейся с нарушением всасывания; неспецифическом язвенном колите; хроническом энтероколите; при тяжелой непереносимости оральных форм препаратов. На сегодняшний день в Российской Федерации для внутривенного введения разрешен только один препарат — венофер (сахарат железа), для внутримышечного может использоваться феррум лек.
Необходимо помнить, что у детей раннего возраста дефицит железа никогда не бывает изолированным и часто сочетается с недостаточностью витаминов С, В12, В6, РР, А, Е, фолиевой кислоты, цинка, меди и др. Это связано с тем, что алиментарная недостаточность и нарушенное кишечное всасывание, приводящие к дефициту железа, влияют и на насыщаемость данными микронутриентами. Поэтому в комплексную терапию ЖДА необходимо включать поливитаминные препараты.
Об эффективности терапии ЖДА можно судить уже через 7–10 дней по увеличению ретикулоцитов в 2 раза по сравнению с исходным количеством (так называемый ретикулоцитарный криз). Также оценивается прирост гемоглобина, который должен составлять 10 г/л и более в неделю. Соответственно, достижение целевого уровня гемоглобина наблюдается в среднем через 3–5 нед от начала терапии в зависимости от тяжести анемии. Однако лечение препаратами железа должно проводиться в достаточных дозах и длительно (не менее 3 мес) даже после нормализации уровня гемоглобина, с тем чтобы пополнить запасы железа в депо.
Если же в течение 3–4 нед не наблюдается значимого улучшения показателей гемоглобина, то необходимо выяснить, почему лечение оказалось неэффективным. Наиболее часто речь идет: о неадекватной дозе препарата железа; продолжающейся или неустановленной кровопотере; наличии хронических воспалительных заболеваний или новообразований; сопутствующем дефиците витамина В12; неверном диагнозе; глистной инвазии и других паразитарных инфекциях.
Противопоказаниями к назначению препаратов железа являются:
- отсутствие лабораторного подтверждения дефицита железа;
- сидероахрестические анемии;
- гемолитические анемии;
- гемосидероз и гемохроматоз;
- инфекция, вызванная грамотрицательной флорой (энтеробактерии, синегнойная палочка, клебсиелла).
При развитии тяжелых анемий, сопровождаемых угнетением эритропоэза и снижением продукции эритропоэтина, показано назначение препаратов рекомбинантного человеческого эритропоэтина (рчЭПО). Особое значение имеет применение рчЭПО при развитии ранней анемии недоношенных, которая развивается на втором месяце жизни и встречается, по данным различных авторов, в 20–90% случаев. Назначение препаратов рчЭПО (рекормон, эпрекс, эпокрин) приводит к резкой активизации эритропоэза и, как следствие, к значительному возрастанию потребностей в железе.
Поэтому применение рчЭПО является показанием к назначению препаратов железа, как правило, парентеральных. В настоящее время в Российской Федерации разрешены к применению a- и b-эпоэтины, которые вошли в список дополнительного лекарственного обеспечения. Назначeние рчЭПО позволяет в большинстве случаев избежать гемотрансфузий, при которых велика вероятность осложнений (трансфузионные реакции, сенсибилизация и пр.). Предпочтительным способом введения препаратов рчЭПО, особенно в раннем детском возрасте, является подкожный. Подкожный способ введения более безопасный и экономичный, так как для достижения эффекта необходимы меньшие дозы, чем при внутривенном введении. До недавнего времени в странах Евросоюза и в Российской Федерации для лечения гипорегенераторных анемий у детей использовались в основном β-эритропоэтины, которые при подкожном введении не вызывали значимых побочных реакций в отличие от a-эритропоэтинов, при подкожном введении которых был велик риск развития красноклеточной аплазии. Наиболее широкое распространение среди β-эритропоэтинов получил препарат рекормон (Ф. Хоффманн-Ля Рош), который удобен в применении и приводит к быстрому повышению уровня эритроцитов и ретикулоцитов, не влияя на лейкопоэз, повышает уровень гемоглобина, а также скорость включения железа в клетки.
С 2004 г. в европейских странах разрешено подкожное введение a-эритропоэтинов, среди которых в нашей стране наиболее часто используются эпрекс (Янсен-Силаг) и эпокрин (Сотекс-ГосНИИ ОЧБ).
Целью лечения рчЭПО является достижение показателей гематокрита 30–35% и устранение необходимости переливаний крови. Значения целевой концентрации гемоглобина могут варьировать в зависимости от дней и месяцев жизни ребенка, однако не могут быть ниже 100–110 г/л. В зависимости от дозы целевые значения концентрации гемоглобина и гематокрита достигаются примерно через 8–16 нед лечения рчЭПО.
С целью профилактики ЖДА рчЭПО назначается недоношенным новорожденным, родившимся с массой тела 750–1500 г до 34-й недели беременности.
Лечение эритропоэтином должно начинаться как можно раньше и продолжаться 6 нед. Препарат рекормон вводят подкожно в дозе 250 МЕ/кг 3 раза в неделю. Однако необходимо учитывать, что чем меньше возраст ребенка, тем более высокие дозы эритропоэтина ему требуются, поэтому доза может быть увеличена.
Как было сказано выше, терапия рчЭПО приводит к резкому возрастанию потребления железа, поэтому в большинстве случаев, особенно у недоношенных детей, одновременно с повышением гематокрита снижается содержание ферритина в сыворотке. Быстрое расходование запасов железа в организме может привести к ЖДА. Поэтому всем больным, получающим терапию рчЭПО, показано назначение препаратов железа. Терапия препаратами железа должна продолжаться до нормализации уровня сывороточного ферритина (не менее 100 мкг/мл) и насыщения трансферрина (не менее 20%). Если концентрация ферритина в сыворотке сохраняется стойко ниже 100 мкг/мл или есть другие признаки дефицита железа, дозу железа следует увеличить, в том числе с использованием парентеральных препаратов.
Профилактика ЖДА у детей раннего возраста включает в себя: антенатальную (правильный режим и питание беременной, своевременное выявление и лечение анемии беременной, превентивное назначение препаратов железа женщинам из групп риска по развитию ЖДА); постнатальную (соблюдение гигиенических условий жизни ребенка, длительное грудное вскармливание и своевременное введение прикормов, адекватный выбор смеси для детей, находящихся на смешанном и искусственном вскармливании, профилактика развития у ребенка рахита, гипотрофии и ОРВИ). В профилактическом назначении препаратов железа нуждаются:
- женщины репродуктивного возраста, страдающие обильными и длительными менструальными кровотечениями;
- постоянные доноры;
- беременные, особенно повторные беременности, следующие с коротким интервалом;
- женщины с дефицитом железа в период лактации.
Профилактическое назначение препаратов железа показано детям из групп риска по развитию ЖДА:
- недоношенные дети (с 2-месячного возраста);
- дети от многоплодной беременности, осложненных беременностей и родов;
- крупные дети с высокими темпами прибавки массы и роста;
- дети с аномалиями конституции;
- страдающие атопическими заболеваниями;
- находящиеся на искусственном вскармливании неадаптированными смесями;
- с хроническими заболеваниями;
- после кровопотерь и хирургических вмешательств;
- с синдромом мальабсорбции.
Доза железа, назначаемого с профилактической целью, зависит от степени недоношенности ребенка:
- для детей с массой тела при рождении менее 1000 г — 4 мг Fe /кг/день;
- для детей с массой тела при рождении от 1000 до 1500 г — 3 мг Fe/кг/день;
- для детей с массой тела при рождении от 1500 до 3000 г — 2 мг Fe/кг/день.
Значимость проблемы ЖДА у детей раннего возраста обусловлена ее большой распространенностью в популяции и частым развитием при различных заболеваниях, что требует постоянной настороженности врачей любых специальностей. Тем не менее на современном этапе в арсенале врача имеется достаточно диагностических и лечебных возможностей для раннего выявления и своевременной коррекции сидеропенических состояний.
- Анемии у детей/под ред. В. И. Калиничевой. Л.: Медицина, 1983. 360 с.
- Анемии у детей: диагностика и лечение/под ред. А. Г. Румянцева, Ю. Н. Токарева. М., 2000. 128 с.
- Аркадьева Г. В. Диагностика и лечение железодефицитных анемий. М., 1999. 59 с.
- Белошевский В. А. Железодефицит у взрослых, детей и беременных. Воронеж, 2000. 121 с.
- Борисова И. П., Скобин В. Б., Павлов А. Д. Раннее назначение рекомбинантного эритропоэтина у недоношенных детей/7-й Национальный конгресс «Человек и лекарство». М., 2000. С. 125.
- Вахрамеева С. Н., Денисова С. Н. Латентная форма железодефицитной анемии беременных женщин и состояние здоровья их детей//Российский вестник перинатологии и педиатрии. 1996. № 3. С. 26–29.
- Дворецкий Л. И., Воробьев П. А. Дифференциальный диагноз и лечение при анемическом синдроме. М.: Ньюдиамед, 1994. 24 с.
- Дворецкий Л. И. Железодефицитные анемии//Русский медицинский журнал. 1997. № 19. С. 1234–1242.
- Идельсон Л. И. Гипохромные анемии. М.: Медицина, 1981. 190 с.
- Казакова Л. М., Макрушин И. М. Иммунитет при дефиците железа// Педиатрия. 1992. № 10–12. С. 54–59.
- Казюкова Т. В., Самсыгина Г. А., Левина А. А. Дефицит железа у детей: проблемы и решения//Consilium medicum. 2002. С. 17–19.
- Малаховский Ю. Е., Манеров Ф. К., Сарычева Е. Г. Легкая форма железодефицитной анемии и латентный дефицит железа — пограничные состояния у детей первых двух лет жизни//Педиатрия. 1988. № 3. С. 27–34.
- Папаян А. В., Жукова Л. Ю. Анемии у детей: руководство для врачей. СПб.: Питер, 2001. 382 с.
- Пригожина Т. А. Эффективность рекомбинантного эритропоэтина в комплексной профилактике и лечении ранней анемии недоношенных: автореф. дис. . канд. мед. наук. М., 2001. 19 с.
- Румянцев А. Г., Морщакова Е. Ф. Павлов А. Д. Эритропоэтин. Биологические свойства. Возрастная регуляция эритропоэза. Клиническое применение. М., 2002. С. 137–144; 266–270.
- Румянцев А. Г., Морщакова Е. Ф., Павлов А. Д. Эритропоэтин в диагностике, профилактике и лечении анемий. М., 2003. 568 с.
- Сергеева А. И., Султанова К. Ф., Левина А. А. и др. Показатели метаболизма железа у беременных женщин и детей раннего возраста//Гематология и трансфузиология. 1993. № 9–10. С. 30–33.
- Тетюхина Л. Н., Казакова Л. М. Профилактика дефицита железа как мера по снижению заболеваемости детей//Педиатрия. 1987. № 4. С. 72–73.
- Dallman P. R., Looker A. C., Johnson C. L. et al. Iron Nutrition in Health and Disease. Eds. Hallberg L., Asp N. G. Libbey; London. 1996; 65–74.
- Messer Y., Escande B. Erytropoietin and iron in the anemia of prematurity. TATM 1999; 15–17.
- Ohls R. K. The use of erythropoetin in neonatoles//Clin Perinatol. 2000; 20 (3): 681–696.
- Ulman J. The role of erythropoietin in erythropoiesis regulation in fetuses and newborn infants//Ginekol. Pol. 1996; 67:205–209.
Л. А. Анастасевич, кандидат медицинских наук
А. В. Малкоч, кандидат медицинских наук
РГМУ, Москва
источник
Анемия у детей в большинстве случаев оказывается железодефицитной и обуславливается дефицитом железа в организме, возникающим ввиду нарушений его поступления с пищей, усвоения в кишечнике или излишних потерь.
Возникновению анемии, в большинстве случаев, предшествует возникновение скрытого недостатка железа, который рассматривается как функциональное нарушение и выражается уменьшением резервного запаса железа в организме и понижением его уровня в тканях, при этом — отсутствием анемии.
Главная причина железодефицитной анемии, по ВОЗ — это несбалансированная диета, бедная железом. Значительно реже железодефицитная анемия у детишек развивается из-за различных кровотечений, (такая анемия называется — хроническая постгеморрагическая, или из-за глистных инвазий (в регионах с низкой культурой).
- Недостаток железа в организме ребеночка при его рождении.
- Недостаток железа ввиду несбалансированной диеты.
- Увеличение потребности организма ребеночка в железе из-за активного роста.
- Потеря железа организмом, превышающая физиологическую потерю.
К алиментарно-зависимым факторам анемии у детей можно отнести
- Недостаток железа в употребляемой пище.
- Пониженная всасываемость железа в ЖКТ.
- У детишек до года причиной анемии может быть возрастание потерь железа ввиду мелких кровотечений в ЖКТ, вызванных преждевременным прикормом детей кефиром и коровьим молоком.
У подростков мужского пола причиной анемии- могут быть разные болезни ЖКТ: язвенное кровотечение, полипоз, ангиоматоз или опухоль ЖКТ, неспецифический язвенный колит, Меккелев дивертикул, кровотечения из геморроидальных вен.
У девочек-подростков и девушек главной причиной постгеморрагической ЖДА являются маточные кровотечения, а болезни ЖКТ отодвигаются на второй план. Половые различия следует учесть при определении причин ЖДА.
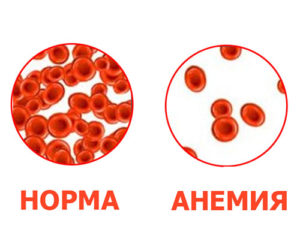
- Уменьшение уровня гемоглобина — Hb (ниже 110 г/л).
- Небольшое понижение числа эритроцитов (меньше 3,8 × 1012/л).
- Уменьшение цветового показателя (меньше 0,85).
- Возрастание скорости оседания эритроцитов (СОЭ, больше 10-12 мм/ч).
- Пониженное или нормальное число ретикулоцитов (10-20‰).
- Кроме этого, лаборант отмечает морфологические особенности эритроцитов — пойкилоцитоз и анизоцитоз.
В общих анализах крови, проводимых с помощью автоматического анализатора крови, кроме изменения указанных выше показателей, меняется серия эритроцитарных индексов.
Уменьшается средний объем эритроцита (mean corpuscular volume — MCV, меньше 80 фл),
Среднее содержание Hb в эритроците (mean corpuscular hemoglobin — MCH, меньше 26 пг),
Средний уровень Hb в эритроците (mean corpuscular hemoglobin concentration — MCHC, меньше 320 г/л),
Увеличивается степень анизоцитоза эритроцитов (red cell distribution width — RDW, больше 14%).
В биохимических анализах крови обращают внимание на
Понижение количества железа в сыворотке крови — СЖ (меньше 12,5 мкмоль/л).
Возрастание общей железосвязывающей способности сыворотки — ОЖСС (больше 69 мкмоль/л).
Уменьшение процента насыщения трансферрина железом — НТЖ (менее 17%).
Понижение количества сывороточного ферритина СФ (меньше 30 нг/мл или мкг/л).
Сейчас стало возможным определять растворимые трансферриновые рецепторы, концентрация их при дефиците железа возрастает (более 2,9 мкг/мл).
- Устранить причину, вызвавшую болезнь (скорректировать питание, выявить и устранить источник кровопотери).
- Возместить недостающее железо организму.
- Назначаются железосодержащие лекарства, т.к. возмещение недостатка железа в организме другими методами невозможно.
- Используются в первую очередь железосодержащие лекарства для внутреннего применения.
- Дозы железосодержащих лекарств подбираются индивидуально с учетом возраста больного, его массы и плана лечения.
- Продолжительность лечения должна быть при анемиях первой (легкой) ст. — 3 мес, при анемиях второй (средней) ст. 4,5 мес, и при анемиях третьей (тяжёлой) степени — полгода.
- В процессе лечения должны восполниться резервы железа в депо, что можно определить по нормализации уровня сывороточного ферритина.
- Необходим обязательный контроль эффективности лечения железосодержащими лекарствами.
В РФ терапию ЖДА проводят по Протоколу «Железодефицитная анемия» утвержденному МЗ России от 22.10.2004г.
В терапии ЖДА у детишек есть особенности, которые учитываются в терапевтических протоколах. Например, назначение детям до 3х лет солевых железосодержащих лекарств в дозировках 5-8 мг/кг веса в день, как это рекомендует протокол, приводит к токсическим явлениям у некоторых детей. Поэтому, детям до 3х лет рекомендуемая ежедневная дозировка железосодержащих лекарств 3 мг/кг, детишкам после 3х лет — 5 мг/кг.
 Железодефицитная анемия у детей Лекарства для приёма внутрь
Железодефицитная анемия у детей Лекарства для приёма внутрь
Железосодержащие лекарства для терапии ЖДА можно условно подразделить на ионные-солевые (двухвалентные) и лекарства на основе гидроксид полимальтозного комплекса (трёхвалентные).
К препаратам 2х валентного железа относятся актиферрин, сорбифер, ферроплекс, фенюльс.
К препаратам 3х валентного железа на основе гидроксид полимальтозного комплекса относятся: мальтофер, феррум-лек, железо полимальтозное, ферри.
Современные научные исследования доказывают, что эффект от препаратов 2х и 3х валентоного железа в лечении ЖДА одинаков.
- Частые передозировки и иногда отравления лекарством из-за неконтролируемости организмом пассивного всасывания железа.
- Вступление в реакцию с прочими лекарствами и едой.
- Характерный привкус металла во рту после приёма лекарства.
- Коричневая или фиолетовая окраска десен и эмали зубов, как правило проходящая со временем, в редких случаях стойкая.
- Высокий процент отказов родителей от лечения (до трети приступивших к лечению).
Большей части побочных эффектов нет у препаратов трёхвалентного железа на основе гидроксид полимальтозного комплекса
- Они безопасны.
- Риск передозировок, интоксикаций, отравлений отсутствует.
- Не дают окрашивания десен и зубов.
- Не имеют металлического привкуса.
- Хорошо переносятся.
- Не вступают во взаимодействие с прочими лекарствами и продуктами.
- Обладают антиоксидантными свойствами.
- Пациенты реже отказываются от лечения.
Парентеральные (внутривенные и внутримышечные) железосодержащие лекарства применяются тогда, когда есть противопоказания к назначению железосодержащих лекарств для внутреннего приема или они не дают эффекта.
- Тяжелых формах ЖДА (на сегодняшний день они встречаются редко, менее чем у 3% больных анемией).
- Аллергии на пероральные железосодержащие лекарства.
- Неэффективности железосодержащих лекарств для приема внутрь.
- Наличии у детей язвы желудка или 12-перстной кишки или операций на ЖКТ в прошлом.
- Хронические болезни кишечника у пациента (болезнь Крона язвенный колит).
- Хронические болезни почек (в преддиализный и диализный периоды) если они отягощаются анемией.
- Наличие противопоказаний к переливанию эритроцитной массы.
- Наличие необходимости скорого насыщения организма железом.
Внутримышечно или внутривенно препараты железа, как правило делают, 1-3 раза в неделю. При терапии парентеральными железосодержащими лекарствами нельзя превышать общий дефицит железа, который можно рассчитать по формуле Ганзони.
Общий дефицит железа, мг = Масса тела больного, кг × (Hb (норма), г/л — Hb больного, г/л) × 0,24 + Депо железа, мг.
Коэффициент 0,24 = 0,0034 × 0,07 × 1000:
содержание железа в Hb — приблизительно 0,34%;
объем крови — 7% массы тела;
1000 — перевод граммов в миллиграммы.
Депо железа у пациентов с массой тела:
менее 35 кг — 15 мг/кг, целевая концентрация Hb — 130 г/л;
более 35 кг — 500 мг, целевая концентрация Hb — 150 г/л.
В этой формуле учитывается железо в депо, которое составляет более трети общего количества железа в организме. Понижение резервов железа в депо можно определить по количеству сывороточного ферритина.
Возможны побочные эффекты при введении железа парентерально местные (жжение, зуд) и общие (аллергические). При парентеральном введении железа требуется наблюдение за больным, применение тестовой дозы лекарства до начала терапии, точный расчет дозы лекарства.
Чтобы лечение парентеральными железосодержащими препаратами стало безопасным и эффективным для ребенка следует выполнять следующие принципы лечения
- Применять современные парентеральные железосодержащие лекарства с низкой токсичностью, без возможных анафилактических реакций, представляющих угрозу для жизни ребеночка.
- Определить общий дефицит железа в организме ребенка до начала лечения.
- Прекратить терапию после того, как общий дефицит железа в организме восполнится, для того чтобы избежать перенасыщения железом опасного для ребенка.
- Соблюдать технику внутримышечных инъекций и внутривенных инфузий железосодержащих лекарств.
- Строго соблюдать инструкцию к парентеральным препаратам железа, если рекомендуется ввести пробную дозу до начала терапии.
- Терапию следует проводить в интервале безопасных доз, т. к. побочные эффекты парентеральных железосодержащих лекарств дозозависимы.
- Ретикулоцитарная реакция: к концу первой, началу второй недели с начала терапии железосодержащими лекарствами число ретикулоцитов увеличивается на 2-3% или 20-30‰ если сравнивать с их числом до лечения.
- Увеличение уровня Hb к концу месяца терапии на 10 г/л и гематокрита на 3% если сравнивать с начальными цифрами до лечения.
- Купирование проявлений анемии через 1-1,5 мес с начала лечения.
- Восполнение дефицита железа в тканях в депо через 3-6 мес с начала терапии, что можно определить по нормализации уровня СФ (более 30 нг/мл).
- Неправильная постановка диагноза железодефицитная анемия у детей.
- Неадекватная доза железосодержащих лекарств.
- Недостаточная продолжительность терапии ЖДА.
- Невыполнение назначений врача родителями ребенка.
- Наличие у ребенка трудностей всасывания железа в ЖКТ.
- Непереносимость ребенком выбранного лекарства.
Если диагноз ЖДА поставлен верно, то эффект от терапии препаратами железа обязательно будет. Если нет ретикулоцитарной реакции, которая характеризует первый эффект от лечения, и нет возрастания уровня Hb на 10 г/л и гематокрита на 3% после месяца терапии, то нужно прекратить прием лекарств и обдумать диагноз, т. к., существует вероятность, что у ребенка — не ЖДА.
Устойчивость ЖДА к терапии железосодержащими лекарствами часто вызвана неправильно подобранной дозой или анемия не имеет ничего общего с недостатком железа.
Недавно описана новая форма ЖДА, называемая железорефрактерной (iron-refractory iron deficiency anemia — IRIDA). Она наследуется по аутосомно-рецессивному типу. Терапия IRIDA железосодержащими лекарствами для приёма внутрь неэффективна, некоторый эффект получается при использовании парентеральных железосодержащих лекарств.
При ЖДА, в большинстве случаев, нет показаний для переливаний эритроцитной массы. Даже в тяжелых случаях, ЖДА успешно лечится пероральными, внутримышечными или внутривенными железосодержащими лекарствами. Риски от переливания эритроцитной массы для борьбы с ЖДА значительно превышает пользу от него.

Ежесуточные потребности взрослого в железе — 1-2 мг, ребеночка — 0,5-1,2 мг. Стандартный суточный рацион питания содержит от 5 до 15 мг железа. В ЖКТ усваивается 10-15% железа из пищи.
Главные пищевые источники железа — это продукты, содержащие гемовое железо: мясо (говядина, баранина, курятина), рыба, творог. Важнее не содержание железа в продукте, а его биодоступность. Негемовое железо, из растительных продуктов: овощей, фруктов, злаков обладает низкой биодоступностью, т.е. из этих продуктов железо хуже всасывается.
Для всасывания железа нужны некоторые условия: аскорбиновая кислота улучшает всасываемость железа, а танин, имеющийся в чае, или фитаты, которые есть в некоторых продуктах, уменьшают её. При ЖДА усвоение железа в 12-перстной кишке значительно увеличивается.
Для профилактики ЖДА американская академия педиатрии рекомендует следующее
- Здоровые доношенные детишки до 4х месяцев обладают достаточными резервами железа в организме.
- После 4х месяцев, если ребеночек вскармливается только грудью, ему необходимы препараты железа в дозировке 1 мг/кг в день, из-за малого содержания железа в материнском молоке — до введения прикорма.
- Для детишек на смешанном вскармливании — рекомендации аналогичны.
- Детишки, вскармливающиеся адаптированными молочными смесями получают с пищей достаточно железа и дополнительного назначения им железосодержащих лекарств не требуется.
- Цельное коровье молоко не рекомендуется давать детишкам до года.
- Детишкам от 6-12 мес требуется 11 мг железа ежедневно, его они должны получить с питанием. В прикорм нужно включать красное мясо и овощи богатые железом.
- Дети 1-3 лет нуждаются в 7 мг железа в день, в их рационе обязательно должно быть красное мясо, овощи, богатые железом и фрукты, богатые аскорбиновой кислотой.
- Все дети, родившиеся до срока, находящиеся на грудном или смешанном вскармливании, требуют назначения им железосодержащих лекарств в дозах не меньше 2 мг/ кг в день с 1 месяца жизни до введения прикорма.
- А недоношенных и маловесных детишек, вскармливающихся искусственно нужно кормить обогащенными железом молочными смесями.
- Дети из социально-неблагополучных семей, семей с низким доходом.
- Недоношенные дети или дети с низким весом при рождении.
- Дети, которых кормят только грудью после 4-месячного возраста без прикорма или приема ребенком препаратов железа.
- Дети, которых кормят до года цельным коровьим молоком или пищей бедной железом.
- Недостаточность питания, задержка роста и веса.
- Увеличенные потребности в железе, обусловленные состоянием организма.
Диспансерное наблюдение за детьми и подростками с ЖДА осуществляется в нашей стране на протяжении 1-го года со дня постановки диагноза.
Проводится контроль самочувствия и общего состояния ребенка. Общий анализ крови контролируется ежемесячно, после нормализации показателей — 1 раз в 3 месяца. Перед снятием ребена с диспансерного учета назначают общий анализ крови, который должен быть нормальным
Проф. прививки деткам с ЖДА разрешены. Для их проведения не требуется нормализация уровня Hb. Проф прививки детей с нетяжелыми анемиями проводятся по календарю т.к. число иммунных клеток у таких детей достаточное.
Это всё про анемия у детей. Желаю Вам здоровья!
источник
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК — 2018
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «25» апреля 2019 года
Протокол №64
Железодефицитная анемия – приобретенное заболевание из группы дефицитных анемий, возникает при дефиците железа, сопровождающееся микроцитарной, гипохромной, норморегенераторной анемией, клиническими проявлениями которой являются сочетание сидеропенического и анемического синдромов.
| МКБ-10 | |
| Код | Название |
| D50 | Железодефицитная анемия |
| D50.0 | Хроническая постгеморрагическая анемия |
Дата разработки/пересмотра протокола: 2013 год (пересмотр в 2018 г.)
Сокращения, используемые в протоколе:
| АХБ | – | анемия при хронических болезнях |
| ВОЗ | – | Всемирная организация здравоохранения |
| ГПК | – | гидросидполимальтозный комплекс |
| ЖДА | – | железодефицитная анемия |
| ЖКТ | – | желудочно-кишечный тракт |
| ЛДЖ | – | латентный дефицит железа |
| МСНС | – | средняя концентрация гемоглобина в эритроците |
| НТЖ | – | коэффициент насыщения трансферрина железом |
| ОЖСС | – | общая железосвязывающая способность |
| СЖ | — | сывороточное железо |
| СФ | – | сывороточный ферритин |
| ЦП | – | цветовой показатель |
| ЭГДС | – | эзофагогастродуоденоскопия |
| Hb | – | гемоглобин |
| МСН | – | содержание гемоглобина в эритроците |
| MCV | – | средний объем эритроцитов |
| RDW | – | степень анизоциотоза эритроцитов |
Пользователи протокола: врачи общей практики, педиатры, гематологи
Категория пациентов: дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты, которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы и анамнез:
Для анемического синдрома характерны следующие симптомы:
· снижение аппетита;
· шум в ушах;
· мелькание мушек перед глазами;
· плохая переносимость физических нагрузок;
· слабость, вялость, головокружение, раздражительность;
· обмороки;
· одышка;
· снижение работоспособности;
· снижение когнитивных функций;
· снижение качества жизни;
Физикальное обследование
Клинические проявления ЖДА представляют совокупность двух синдромов: сидеропенического и анемического.
Для сидеропенического синдрома характерны следующие симптомы:
· изменения кожи: сухость, появление маленьких пигментных пятен цвета «кофе с молоком», бледность кожи;
· изменения слизистых оболочек: «заеды» в углу рта, глоссит, атрофический гастрит и эзофагит; видимых слизистых оболочек;
· диспептические явления со стороны ЖКТ;
· изменения волос – раздваивание кончика, ломкость и выпадение вплоть до гнездной алопеции;
· изменения ногтей – поперечная исчерченность ногтей больших пальцев рук (в тяжелых случаях и ног), ломкость, расслаивание на пластинки;
· изменение обоняния – пристрастие больного к резким запахам лака, краски ацетона, выхлопных газов автомобиля, концентрированных духов;
· изменения вкуса – пристрастие больного к глине, мелу, сырому мясу, тесту, пельменям и др.;
· боли в икроножных мышцах, изменение тонуса мышц в виде тенденции к гипотонии, гипотония мышц мочевого пузыря с развитием недержания мочи;
· расширение границ сердца, приглушенность сердечных тонов, тахикардия, систолический шум на верхушке сердца.
· Считается, что наличие 4-х симптомов и более из перечисленных выше патогномонично для латентного дефицита железа (ЛДЖ) и ЖДА.
Лабораторные исследования:
Имеется 3 возможности лабораторной диагностики ЖДА:
· ОАК, выполненный «ручным» методом — снижение концентрации Hb (менее 110 г/л), небольшое снижение количества эритроцитов (менее 3,8 х 1012/л), снижение ЦП (менее 0,85), увеличение СОЭ (более 10-12 мм/час), нормальное содержание ретикулоцитов (10-20‰). Дополнительно врач-лаборант описывает анизоцитоз и пойкилоцитоз эритроцитов. ЖДА это микроцитарная, гипохромная, норморегенераторная анемия.
· ОАК, выполненный на автоматическом анализаторе клеток крови — снижаются средний объем эритроцита – MCV (менее 80 фл), среднее содержание Hb в эритроците – MCН (менее 26 пг), средняя концентрация Hb в эритроците – МСНС (менее 320 г/л), повышается степень анизоцитоза эритроцитов – RDW (более 14%).
· Биохимический анализ крови — снижение концентрации сывороточного железа (менее 12,5 мкмоль/л), повышение общей железосвязывающей способности сыворотки (более 69 мкмоль/л), снижение коэффициента насыщения трансферрина железом (менее 17%), снижение сывороточного ферритина (менее 30 нг/мл). В последние годы появилась возможность определения растворимых трансферриновых рецепторов (рТФР), количество которых в условиях дефицита железа увеличивается (более 2,9 мкг/мл).
Инструментальные исследования: нет
Диагностический алгоритм: (схема)
Дифференциальный диагноз и обоснование дополнительных исследований:
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Мегалобластные анемии | снижается количество эритроцитов и гемоглобина, наблюдаются лейкопения и тромбоцитопения. Кроме того, при обоих типах анемий может развиваться гемолитический синдром | Исследование периферической и венозной крови; миелограмма | При ЖДА не бывает гиперхромной анемии с макроцитозом эритроцитов. Длительность жизни эритроцитов при мегалобластной анемии снижается. Возможное понижение лейкоцитов и тромбоцитов при мегалобластной анемии, когда как при ЖДА данные показатели в норме. Особенности миелограммы (наличие редукции красного кроветворного ростка, а не гиперплазия мегалобластов). |
| Апластическая анемия | Анемический синром, геморрагический синдром на фоне тромбоцитопении, симптомы интоксикации. | Исследование периферической и венозной крови, миелограммы, общего анализа мочи, имунофенотипирова ние периферической крови на ПНГ клон. | При ЖДА в миелограмме не отмечается сокращение всех трех ростков кроветворения, нет жирового перерождение костного мозга. Отрицательный ПНГклон. |
| Талассемия | гипохромная анемия, анизоцитоз эритроцитов, наличие мишеневидных форм эритроцитов (пятно гемоглобина в центре клетки, напоминающее мишень). При этом содержание сывороточного железа нормальное или повышенное. Компенсаторная гиперплазия костного мозга ведёт к нарушениям в строении лицевого черепа. Череп может стать квадратным, башенным; нос приобретает седловидную форму; нарушается прикус и расположение зубов. Отмечается желтушность кожи и слизистых оболочек. Селезёнка и печень увеличены. Больные подвержены инфекционным заболеваниям. Рано начавшаяся анемия обуславливает физическое и умственное недоразвитие ребёнка. | Исследование периферической и венозной крови, миелограммы, генетическое исследование, УЗИ органов брюшной полости, портальной вены, проба Кумбса, определение типов гемоглобина. | Нет генетических мутаций, форма эритроцитов не изменена; сывороточное железо обычно снижено; нет костной деформации; нет желтушного синдрома; отсутствие гепатоспленомегалии; физическое и умственное развитие ребенка соответствуют возрасту. |
| Сидеробластные анемии | нарушение синтеза гема и митохондриальная дисфункция: неэффективный эритропоэз, высокое содержание железа в крови и гемосидероз внутренних органов. В костном мозге образуются эритроциты малого размера, в которых снижено содержание гемоглобина, а железо откладывается внутри клеток, затем выходит в кровь и оседает в тканях внутренних органов. | клинический анализ крови; пункция костного мозга, сывороточное железо, УЗИ Органов брюшной полости; генетическое исследование | При ЖДА снижено сывороточное железо в крови; нет гемохроматоза; отсутствие генетических мутаций |
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Немедикаментозное лечение:
- Устранение этиологических факторов;
- Рациональное лечебное питание (для новорожденных – грудное естественное вскармливание, а при отсутствии молока у матери – адаптированные молочные смеси, обогащенные железом. Своевременное введение прикорма, мяса, субпродуктов, гречневой и овсяной круп, фруктовых и овощных пюре, твердых сортов сыра; уменьшение приема фосфатов, танина, кальция, которые ухудшают всасывание железа).
Медикаментозное лечение
В настоящее время в нашей стране используется терапевтический план лечения ЖДА пероральными препаратами железа, суточные дозы которых представлены в таблице.
Возрастные терапевтические дозы пероральных препаратов железа для лечения ЖДА у детей.
| Возраст ребенка | Суточная доза элементарного железа |
| Ионные железосодержащие препараты (солевые, полисахаридные соединения железа) | |
| Дети до 3-х лет | 3 мг/кг |
| Дети старше 3-х лет | 45-60 мг |
| Подростки | до 120 мг |
| Неионные соединения т.е. препараты, представленные гидроксид-полимальтозным комплексом трехвалентного железа | |
| Любой возраст | 5 мг/кг |
| Лекарственная группа | Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности | |||||||||
| Монокомпонентные препараты железа | ||||||||||||
| Глюконат железа | Глюконат железа 300 мг | по 1–3 табл. в день | III C | |||||||||
| Сульфат железа | Сульфат железа табл. 256.3 мг (80 мг железа), Сульфат железа 325 мг (105 мг иона (II) железа (Fe 2+ )) | Детям старше 6 лет до 15 лет назначают по 1 капсуле ежедневно. Подросткам с 15 лет в начале терапии обычно назначают по 1 капсуле 1-2 раза в сутки | III C | |||||||||
| Комбинированные препараты | ||||||||||||
| Железа (II) сульфат сухой + Аскорбиновая кислота 60 мг | Сульфат железа таб.320 мг+аскорбиновая кислота 60 мг | по 1 табл. 1–2 раза в день | III C | |||||||||
| Препараты железа (III) валентные | ||||||||||||
| Железа (III) гидроксид полимальтозат | Железа (III) гидроксид полимальтозат 400 мг (100 мг эл.железа) Таб. 375 мг (100 мг эл.железа) | По 100 — 300 мг железа (1 — 3 таблетки) ежедневно | IIB | |||||||||
| Препараты железа для парентерального введения | ||||||||||||
| Железа оксида сахарат | Железо III гидроксид сахарозный комплекс 540 мг (железа 20 мг); | |||||||||||
Железа (III) гидроксида сахарозного комплекса 333,0 мг (эквивалентно элементарному железу) 20,0 мг
В/в медленно (0,2 мл/мин) в дозе 100–200 мг железа (2–4 мл), предпочтительно разведенного в 10–20 мл 0,9% раствора натрия хлорида или 5% раствора глюкозы. Начальная доза препарата составляет 25 мг железа или 0,5 мл раствора, которая вводится в/в медленно в течение 1–2 мин
в/в (внутривенно) капельно (инфузионно) 1000 мг железа 1 раз в неделю.
Дальнейшее ведение:
Диспансерное наблюдение за детьми и подростками с ЖДА проводится в течение 1-го года с момента установления диагноза, контролируются самочувствие и общее состояние больного. Перед снятием больного с диспансерного наблюдения выполняется общий анализ крови, все показатели которого должны быть в пределах нормы.
Медицинской, физической и психологической реабилитации больных после излечения от ЖДА не требуется.
Индикаторы эффективности лечения:
- улучшение аппетита, самочувствия, физической активности, настроения;
- нормализация цвета кожи и видимых слизистых;
- нормализация Hb, ретикулоцитов.
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ: см. Амбулаторный уровень
Хирургическое вмешательство: нет
Дальнейшее ведение: см. Амбулаторный уровень
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации: нет
Показания для экстренной госпитализации:
- анемия III степени тяжести;
- необходимость парентерального введения препаратов железа.
- Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2018
- 1) Dado DN, Loesch EB, Jaganathan SP A Case of Severe Iron Deficiency Anemia Associated with Long-Term Proton Pump Inhibitor Use Curr Ther Res Clin Exp. 2017 Jan 21;84:1-3 2) Тарасова И.С. Разработка и научное обоснование скрининга железодефицитных состояний у подростков: Автореф. дис. д-ра мед. наук. — М.— 67 с. 3) Тарасова И.С., Чернов В.М., Лаврухин Д.Б., Румянцев А.Г. Становление менструальной функции как фактор риска развития анемии // Гематология и трансфузиология. — 2014. — Т. 55, № 4. — С. 3-7. 4) Baker R.D., Greer F.R. Committee on Nutrition American Academy of Pediatrics. Diagnosis and prevention of iron deficiency and iron-deficiency anemia in infants and young children (0-3 years of age) // Pediatrics. — 2014. — Vol. 126, N5. — P. 1040-1050. 5) Детская гематология. Клинические рекомендации / Под ред. А.Г. Румянцева, А.А. Масчана, Е.В. Жуковской. Авторы: Айзенберг В.Л., Балашов Д.Н., Биккулова Д.Ш., Вдовин В.В., Володин Н.Н., Демихов В.Г., Демихова Е.В., Евдокимова М.А., Жарков П.А., Журина, О.Н., Зозуля Н.И., Инякова Н.В., Карачунский А.И., Клипинина Н.В., Копылов К.Г., Кузминова Ж.А., Кумирова Э.В., Кумскова М.А., Лазарев В.В., Луговская С.А., Лукина Е.А., Лунякова Е.А., Масчан М.А., Морщакова Е.Ф., Мякова Н.В., Новичкова Г.А., Орлов А.Б., Панкратьева Л.Л., Полевиченко Е.В., Птушкин В.В., Румянцева Ю.В., Самочатова Е.В., Свирин П.В., Сигарева И.А., Скворцова Ю.В., Скобин В.Б., Сметанина Н.С., Спиридонова Е.А., Стефаненко Е.А., Тарасова И.С., Хаин А.Е., Хамин И.Г., Харькин А.В., Хачатрян Л.А., Цветаева Н.В., Цыпин Л.Е., Чернов В.М., Щербина А.Ю., Щукин В.В. — М.: ГЭОТАР-Медиа, 2015. — 656 с. 6) Auerbach M, Deloughery T. Single-dose intravenous iron for iron deficiency: a new paradigm. Hematology Am Soc Hematol Educ Program 2016; 2016:57. 7) Auerbach M, Deloughery T. Single-dose intravenous iron for iron deficiency: a new paradigm. Hematology Am Soc Hematol Educ Program 2016; 2016:57. 8) Krayenbuehl PA, Battegay E, Breymann C, et al. Intravenous iron for the treatment of fatigue in nonanemic, premenopausal women with low serum ferritin concentration. Blood 2011; 118:3222. 9) Sharma R, Stanek JR, Koch TL, et al. Intravenous iron therapy in non-anemic iron-deficient menstruating adolescent females with fatigue. Am J Hematol 2016; 91:973. 10) Vaucher P, Druais PL, Waldvogel S, Favrat B. Effect of iron supplementation on fatigue in nonanemic menstruating women with low ferritin: a randomized controlled trial. CMAJ 2012; 184:1247. 11) Pittori C, Buser A, Gasser UE, et al. A pilot iron substitution programme in female blood donors with iron deficiency without anaemia. Vox Sang 2011; 100:303. 12) Burden RJ, Morton K, Richards T, et al. Is iron treatment beneficial in, iron-deficient but non-anaemic (IDNA) endurance athletes? A systematic review and meta-analysis. Br J Sports Med 2015; 49:1389. 13) Achebe MM, Gafter-Gvili A. How I treat anemia in pregnancy: iron, cobalamin, and folate. Blood 2017; 129:940. 14) Gomollón F, Gisbert JP. Intravenous iron in inflammatory bowel diseases. Curr Opin Gastroenterol 2013; 29:201. 15) Jimenez K, Gasche C, Auerbach M. On both sides of the ocean. Blood Transfus 2016; 14:197. 16) Lee T, Clavel T, Smirnov K, et al. Oral versus intravenous iron replacement therapy distinctly alters the gut microbiota and metabolome in patients with IBD. Gut 2017; 66:863. 17) García-López S, Bocos JM, Gisbert JP, et al. High-dose intravenous treatment in iron deficiency anaemia in inflammatory bowel disease: early efficacy and impact on quality of life. Blood Transfus 2016; 14:199. 18) Reinisch W, Chowers Y, Danese S, et al. The management of iron deficiency in inflammatory bowel disease—an online tool developed by the RAND/UCLA appropriateness method. Aliment Pharmacol Ther 2013; 38:1109.Gasche C, Evstatiev R, Haas T, et al. [Diagnosis and treatment of iron deficiency and anaemia in inflammatory bowel diseases. Consensus of the Austrian IBD Working Party]. Z Gastroenterol 2011; 49:627. 19) Auerbach M, Adamson JW. How we diagnose and treat iron deficiency anemia. Am J Hematol 2016; 91:31. 20) Kim YW, Bae JM, Park YK, et al. Effect of Intravenous Ferric Carboxymaltose on Hemoglobin Response Among Patients With Acute Isovolemic Anemia Following Gastrectomy: The FAIRY Randomized Clinical Trial. JAMA 2017; 317:2097. 21) Khalafallah AA, Yan C, Al-Badri R, et al. Intravenous ferric carboxymaltose versus standard care in the management of postoperative anaemia: a prospective, open-label, randomised controlled trial. Lancet Haematol 2016; 3:e415. 22) Johansson PI, Rasmussen AS, Thomsen LL. Intravenous iron isomaltoside 1000 (Monofer®) reduces postoperative anaemia in preoperatively non-anaemic patients undergoing elective or subacute coronary artery bypass graft, valve replacement or a combination thereof: a randomized double-blind placebo-controlled clinical trial (the PROTECT trial). Vox Sang 2015; 109:257. 23) Froessler B, Palm P, Weber I, et al. The Important Role for Intravenous Iron in Perioperative Patient Blood Management in Major Abdominal Surgery: A Randomized Controlled Trial. Ann Surg 2016; 264:41. 24) Serrano-Trenas JA, Ugalde PF, Cabello LM, et al. Role of perioperative intravenous iron therapy in elderly hip fracture patients: a single-center randomized controlled trial. Transfusion 2011; 51:97.
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
- Омарова Кулян Омаровна – доктор медицинских наук, профессор, гематолог АО «Национальный центр педиатрии и детской хирургии».
- Манжуова Ляззат Нурбапаевна – кандидат медицинских наук, заведующий отделением онкологии №1 АО «Национальный центр педиатрии и детской хирургии».
- Нургалиев Даир Жванышевич – доктор медицинских наук, руководитель отдела онкогематологии и трансплантации гемопоэтических стволовых клеток КФ «UMC» «Национальный научный центр материнства и детства».
- Ашимова Разита Беймбетовна – онкогематолог, отделение онкологии №1 КФ «UMC» Национальный научный центр материнства и детства.
- Ихсанова Алина Кайратовна – онкогематолог, отделение онкологии №1 КФ «UMC» Национальный научный центр материнства и детства.
- Суров Владимир Константинович – клинический фармаколог отдела госпитальной фармации АО «Национальный Центр Нейрохирургии».
Указание на отсутствие конфликта интересов: нет.
- Абдрахманова Сагира Токсанбаевна. – доктор медицинских наук, профессор кафедры детских болезней НАО «Медицинский университет Астана».
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
источник






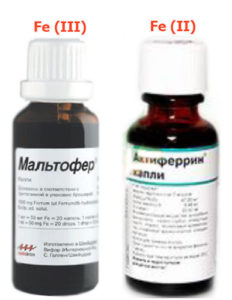 Железодефицитная анемия у детей Лекарства для приёма внутрь
Железодефицитная анемия у детей Лекарства для приёма внутрь