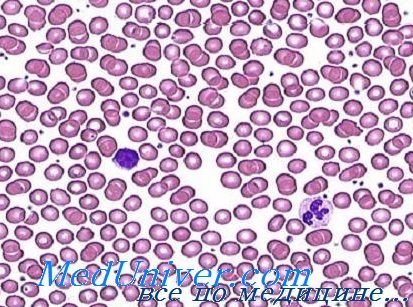
Периферическая кровь при железодефицитной анемии. Свойственные крови морфологические изменения заключаются в микроцитозе и гипохромии. Однако эти признаки отражают длительную недостаточность железа, сочетающуюся с тяжелой анемией. Исходно, когда в процессе гемоглобиногенеза отмечается отрицательное влияние недостаточного подвоза железа в костный мозг, кроветворение начинает приспосабливаться к новым условиям. По началу сокращается объем эритроцитов.
Микроцитоз и нормохромия обычное явление у женщин при показателе гемоглобина от 9 до 10 г на 100 мл. Гипохромия развивается, когда показатель уровня гемоглобина падает до меньших значений, причем вначале она умеренная, а затем становится все более выраженной. При тяжелой форме анемии эритроциты имеют кольчатый аспект (аннулоциты) или обретают вид клеток-мишень. Пойкилоцитоз наблюдается лишь при тяжелых формах анемии (Дачие и сотр.).
Показатели эритроцитов свидетельствуют о небольшом объеме (менее 80 мкг3), о количестве гемоглобина менее 27 пг и о средней концентрации гемоглобина на каждый эритроцит (менее 30 г/100/мл.). В принципе число ретикулоцитов в норме или немного больше; лишь е редких случаях их число занижено. Число эритроцитов обычно нормальное или немного меньшее нормы. Вот почему определение не дает точную справку о тяжести анемии. В отдельных случаях, особенно у детей, число эритроцитов превышает 5 млн/мм3. Следует отметить, что, при железодефицитной анемии увеличивается устойчивость эритроцитов к гипотонии.
Наиболее часто число лейкоцитов укладывается в норму. При длительной недостаточности железа развивается умеренная гранулоцитопения. В некоторых случаях выявляются гиперсегментированные нейтрофилы. Их появление при недостатке железа можно объяснить развитием вторичной недостаточности фолиевокислых солей или витамина В12 (Брукнер и сотр.).
В большинстве случаев показатель численности тромбоцитов высокий, однако еше не разработано четкое объяснение этому явлению. Высказана мысль о возможности появления тромбоцитоза в результате активной кровоточивости. В случаях тяжелой или длительной анемии отмечена умеренная тромбоцитопения, обратимая после проведения железотерапии.
У страдающих железодефицитной анемией количество клеточной массы в костном мозге выше нормы. Рост показателя костномозговых клеток объясняется увеличением числа эритробластов. Последние, в частности полихроматофильные и оксифильные меньших размеров, чем нормальные эритробласты в связи с сокращением количества цитоплазмы. Исследование мазка в условиях железодефицитной анемии выявляет не только малые размеры эритробластов, но также их нерегулярный, «изорванный» контур. В таких клетках были описаны аспекты дисэритропоэза и кариорексиса, почкования ядер, в некоторых случаях многоядерность и ядерные фрагменты.
Непосредственное исследование, без окраски, размозженных на стекле зерен костного мозга не выявляет наличие аггрегатов мелких, нерегулярных, золотистых, характерных гемосидерину частиц. Окраска по Перлсу выявляет отсутствие запасного железа в макрофагах и наличие менее 10% сидеробластов (Дачие и сотр.). В целях определения заболевания железодефицитной анемией этот тест представляет наибольшее диагностическое значение.
Сывороточное железо при железодефицитной анемии. Концентрация железа в сыворотке всегда меньше 50 мкг/100 мл., причем в отдельных случаях она не больше 10 мкг/100 мл. Общая связывающая способность железа (ОССЖ), отражающая количество находящегося в кровотоке трансферина, чаще завышена и лишь в редких случаях укладывается в норму или занижена. У больных с заниженной ОССЖ возможно вмешательство и других факторов, например гипопротеинемии (McGibbon и Mollin5). Насыщение трансферином (железо сыворотки/ОССЖ х 100) в любом случае меньше 16%, однако встречаются и случаи 1%-ой насыщенности.
Следует обратить особое внимание на интерпретацию насыщения трансферином у женщин на последнем квартале беременности. У последних насыщение трансферином менее 16% не всегда указывает на наличие недостатка железа. Объяснение такому явлению следует искать в повышении количества трансферина, что характерно беременным независимо от возможного дефицита железа.
Показатель свободного протопорфирина эритроцитов (СПЭ) в принципе характеризуется высокими значениями — более 70 мкг/100 мл. а в отдельных случаях даже больше 300 мкг/мл. При этом следует обратить внимание на тот факт, что на повышение уровня СПЭ влияет больше продолжительность железо дефицита, чем его интенсивность (Dameshek).
Показатель феритина в сыворотке — растворимой формы находящегося в запасе железа—составляет менее 12 мкг/л. у женщин и детей раннего возраста и менее 35 мкг/л. у мужчин. Существует четкая взаимосвясь сывороточного феритина и количеством железа выявляемого в костном мозге и печени путем окраски по Перлсу.
Кинетика железа. В процессе выявления недостатка железа кинетика последнего не применяется как текущий метод. При использовании этого метода обнаруживается весьма быстрый клиренс железа плазмы, перенос железа в костный мозг и его расход нормальными или увеличенными эритроцитами, при этом интенсивность и скорость метаболизма железа эритроцитов больше нормы. Эти данные свидетельствуют о наличии неэффективного кроветворения в условиях недостатка железа:
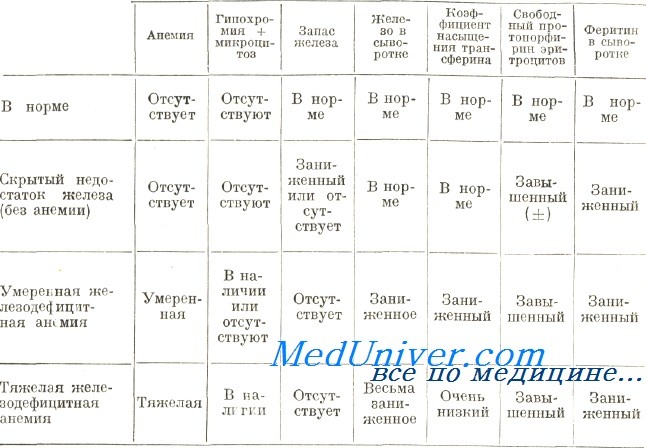
Диагностирование тяжелой железодефицитной анемии по клиническим и лабораторным данным дело несложное, при этом сделанное определение подтверждается терапевтическим испытанием. Осложнения появляются при мало выраженной форме анемии и нечетких клинических и лабораторных признаках. Ниже в таблице приведены морфологические, биохимические и цитохимические данные, на основе которых дифференцируются этапы недостатка железа.
Элементы лабораторного диагноза стадий железной недостаточности
Железодефицитную анемию следует отличать от остальных видов гипохромной анемии. Среди последних, на втором месте по частоте после железодефицитной анемии, находится бета-талассемия (по данным приема для страдающих болезнями крови при Центре гематологии). Учитывая тяжесть заболевания, ранный возраст страдающего и характерную клиническую картину тяжелая бета-талассемия (анемия Кули) распознается без затруднений.
В противоположность этому легкая форма бета-талассемии в отдельных случаях не различима от железодефицитной анемии по клиническим признакам и результатам морфологического исследования крови. Возможные кровоточивость в анамнезе, наблюдаемые в слизистых оболочках и роговых образованиях изменения, равно как и бледность сыворотки подсказывают диагноз железодефицитной анемии. Гипохромия и микроцитоз общее, для обеих групп явление, однако при талассемии они выделяются более ярко.
Отмечаем, что, при талассемии, более характерной чертой микроцитоза это не сокращенный диаметр эритроцитов, а их значительно уменьшенная толщина (микроплатициты). Вот почему выраженная гипохромия с показателем гемоглобина примерно 10 г/100 мл или более подсказывает диагноз талассемии. Также, при железодефицитной анемии с более 8 г/100 мл гемоглобина пойкилоцитоз единичное явление, в то время как при талассемии наблюдается часто. В условиях талассемии выраженный микроцитоз отражается ростом численности эритроцитов, по сравнению с железодефицитной анемией.
Что касается остальных лабораторных данных следует не забывать, что при талассемии чаще наблюдаются такие признаки, как повышенное число ретикулоцитов, полихроматофильных эритроцитов и наличие точечно-базофильных красных кровяных клеток, к тому же осмотическая устойчивость последних больше.
В связи со сказанным для различения этих двух заболеваний наибольшую ценность представляют тесты метаболизма железа. В принципе, при талассемии показатель железа в крови характеризуется нормальными или завышенными значениями. Редко, у больных с хронической кровоточивостью развивается гипосидеремия. В таких случаях ОССТЖ, показатель которой при талассемии отличается низкими значениями (обычно менее 250 мкг/100 мл), увеличивается до нормы и даже более.
За исключением случаев, осложненных недостатком железа, костномозговые запасы железа при талассемии укладываются в норму или несколько больше. В отдельных случаях количество железа в митохондриях нормобластов очень велико, что создает аспект кольчатых сидеробластов.
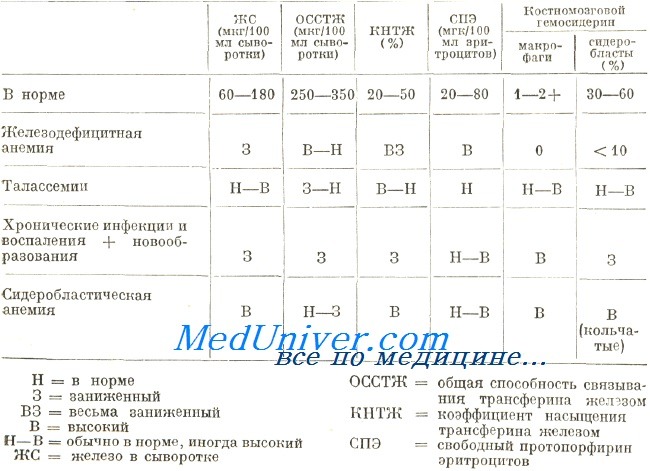
Анемия с многонедельным течением, развивающаяся при инфекциях и хронических воспалениях, в принципе носит нормоцитный и нормохромный характер, причем эта характеристика действительна и в отношение анемий, наблюдаемых при свежих новообразованиях. Но после длительного течения в условиях этих заболеваний анемия становится микроцитной и гииохромной. В подобном случае различение этой анемии от железодефицитной возможна путем выявления первичного заболевания, в частности посредством лабораторных исследований. Морфологическое исследование крови не представляет данные, способствующие дифференциальному диагнозу.
Элементы дифференциальной диагностики при гипохромной анемии
Концентрация железа в сыворотке невелика в обеих группах заболеваний, в то время как показатель ОССТЖ в принципе высокий при железодефицитной анемии и низкий при хронических воспалениях и новообразованиях. По этой причине коэффициент насыщенности трансферина меньше у страдающих железодефицитной анемией. Обследование дополняется определением гемосидерина на костномозговом мазке. В костном мозге страдающих хроническим воспалением и новообразованием содержатся макрофаги, загруженные гемосидерином, который всегда отсутствует в условиях железодефицитной анемии. При обоих заболеваниях сидеробласты обнаруживаются в малом количестве или совсем отсутствуют.
В процессе, диагностирования возникают затруднения и в случае сидеробластической анемии. Тем не менее, в условиях сидеробластической анемии, эритроциты отличаются частным видом. На мазге различаются две популяции эритроцитов, из них одна микроцитная и гипохромная) другая — макроцитная и нормохромная («частичная гипохромия»). Дифференциальная диагностика основывается на определении метаболизма железа, который, при сидеробластической анемии, отражает нормальную или завышенную сидеремию, нормальную или низкую ОССТЖ и высокий показатель гемосидерина в костном мозге с наличием кольчатых сидеробластов.
Из гемолитических анемий наличие гипохромии отмечается при гемоглобинопатиях К, КС, Е, Кёлн. В отдельных случаях наблюдаются клетки мишень. Высокие показатели сидеремии и гемосидерина в костном мозге исключают возможность наличия железодефицитной анемии. Гемолитическая анемия с хроническим внутрисосудистым гемолизом, в частности ночной пароксизмальной гемоглобинурией сочетается с характерной для железодефицитной анемии картиной. Дифференциация возможна по признакам гемолиза и данным лабораторных анализов специфических ночной пароксизмальной гемоглобинурии.
После проведения курса лечения витамином В12 или фолиевой кислотой сидеремия и запасы железа быстро сокращаются под влиянием ускоренного эритропоэза. Это сокращение четко выражено у женщины с небольшим запасом железа. Дифференциальная диагностика представляет трудности, поскольку признаки мегалобластоза в костном мозге исчезают после проведения специфической терапии. В таком случае наиболее важным представляется исследование мазка крови, выявляющее наличие макроцитоза с нормохромией и гиперсегментирование нейтрофилов.
Нередко исследование мазка крови страдающего недостатком железа указывает на наличие нормохромии. Вот почему представляется важной постановка дифференциального диагноза по сравнению с группой нормохромных анемий. Отсутствие костномозгового гемосидерина характеризует железодефицитную анемию, даже при ее умеренной форме.
Необходимо отметить, что в условиях истинной полицитемии, эритроциты нередко гипохромные уже при первом обследовании врача, до вскрытия вен. К тому же обнаруживается невысокая сидеремия и отсутствие костномозгового запаса железа. Тем не менее истинная полицитемия отличается характерной клинической и лабораторной симптоматологией.
источник
Красные кровяные тельца, которые называются эритроцитами, содержат в себе гемоглобин. Этот белок является очень важным для организма, ведь именно он отвечает за процесс обмена железом, также транспортирует кислород к каждой клеточке нашего тела. Но при каких показателях анемия диагностируется у человека? Это происходит в том случае, когда количество эритроцитов и уровень гемоглобина начинают стремительно снижаться.
О том, что в организме начинает протекать такое заболевание, как малокровие, можно узнать по определенным симптомам, но только лабораторные исследования крови помогут специалисту действительно засвидетельствовать этот факт и установить тип малокровия и степень его тяжести.
Для того чтобы специалист мог установить максимально точный диагноз протекающего недуга, пациенту необходимо сдать несколько анализов:
- Общий анализ крови.
- Расширенный анализ крови.
- Биохимический анализ крови.
Если дополнительные анализы могут назначаться специалистом по требованию, то общий анализ крови является обязательным. Основным признаком малокровия будет сниженный уровень гемоглобина. Также учитывается цветовое изменение эритроцитов при анемии. Оптимальный его показатель составляет не ниже 0,8, но при малокровии он всегда будет падать.
Также гемограмма при анемиях (тот же общий анализ крови) позволяет установить специалисту степень тяжести малокровия:
- Легкая степень. Гемоглобин снижается до 90 г/л.
- Средняя степень. Концентрация гемоглобина снижается до 70 г/л.
- Тяжелая степень. Гемоглобин опустился ниже 70 г/л.
Расшифровка картины результатов общего анализа крови будет включать следующие моменты:
- Количество красных кровяных телец.
- Уровень лейкоцитов. Они выполняют защитную функцию в теле человека.
- Тромбоциты. Это бесцветные и очень мелкие клетки в крови. Они отвечают за процесс свертывания крови, а также является первой помощью при повреждениях.
- Гемоглобин. Является белком, основу которого составляет железо. Именно гемоглобин придает эритроцитам их нормальный цвет, а также переносит кислород по кровеносной системе.
- СОЭ. Этот показатель свидетельствует о скорости оседания эритроцитов. На основании полученных результатов, специалист может оценить уровень свертываемости крови.
- Цветовой показатель. Он позволяет оценить содержание гемоглобина в каждом эритроците.
Исходя из полученных результатов, специалист может диагностировать форму недуга, а также назначить правильное лечение малокровия. Стоит отметить, что общий анализ крови необходимо сдавать не только при проявлениях симптоматики малокровия. Если делать это систематически, то можно быстрее среагировать на протекающий недуг и пресечь любые осложнения.
Также общий анализ крови позволяет специалист определит размер эритроцитов, их форму и цветовой показатель. Анизоцитоз при анемии будет свидетельствовать о том, что размер эритроцитов отдалился от нормы. Если диагностировано серьезное отклонение, то без оперативного лечения могут возникнуть серьезные осложнения.
Чаще всего у пациентов диагностируется железодефицитная анемия. Вместе с этим, отмечается анемия и тромбоцитоз, который и возникает в результате резкого снижения железа, что может быть спровоцировано сильными кровотечениями или обычными процессами, протекающими во время беременности.
На основании этого анализа, специалист может судить о патогенности процесса, который протекает в организме пациента. Если СОЭ повышен при анемии, то это свидетельствует о сниженном гемоглобине в эритроцитах. Показатели скорости оседания эритроцитов практически всегда зависят от уровня гемоглобина. Это значит, что если уровень гемоглобина увеличен, то СОЭ буден снижен. Если у пациента диагностируется низкий уровень гемоглобина, но высокий показатель оседания эритроцитов, то специалисты диагностируют развитие патогенного процесса в организме пациента. Если быстро компенсировать дефицит гемоглобина, то всего за несколько дней можно нормализировать положение.
Ретикулоцитами называют клетки эритроидного ряда, которые являются основной для создания будущих эритроцитов. Трансформация одной клетки в другую происходит в результате влияния определенного гормона – эритропоэтина. Если же эритроциты начинают быстро разрушаться, то костный мозг начинает вырабатывать ретикулоциты в больших количествах, чтобы компенсировать недостачу.
Специалисты проверяют ретикулоцитоз при анемиях для того, чтобы оценить состояние костного мозга, почек, а также патогенный процесс разрушения эритроцитов. Стоит отметить, что увеличение количества этих клеток не всегда является негативным проявлением.
источник
Железодефицитная анемия – синдром, обусловленный недостаточностью железа и приводящий к нарушению гемоглобинопоэза и тканевой гипоксии. Клинические проявления представлены общей слабостью, сонливостью, пониженной умственной работоспособностью и физической выносливостью, шумом в ушах, головокружениями, обморочными состояниями, одышкой при нагрузке, сердцебиением, бледностью. Гипохромная анемия подтверждается лабораторными данными: исследованием клинического анализа крови, показателей сывороточного железа, ОЖСС и ферритина. Терапия включает лечебную диету, прием препаратов железа, в некоторых случаях – трансфузию эритроцитарной массы.
Железодефицитная (микроцитарная, гипохромная) анемия – анемия, обусловленная нехваткой железа, необходимого для нормального синтеза гемоглобина. Её распространенность в популяции зависит от половозрастных и климатогеографических факторов. По обобщенным сведениям, гипохромной анемией страдает около 50% детей раннего возраста, 15% женщин репродуктивного возраста и около 2% мужчин. Скрытый тканевой железодефицит выявляется практически у каждого третьего жителя планеты. На долю микроцитарной анемии в гематологии приходится 80–90% всех анемий. Поскольку железодефицит может развиваться при самых различных патологических состояниях, данная проблема актуальна для многих клинических дисциплин: педиатрии, гинекологии, гастроэнтерологии и др.
Ежесуточно с потом, калом, мочой, слущенными клетками кожи теряется около 1 мг железа и примерно столько же (2-2,5 мг) поступает в организм с пищей. Дисбаланс между потребностями организма в железе и его поступлением извне или потерями способствует развитию железодефицитной анемии. Железодефицит может возникать как при физиологических условиях, так и в результате ряда патологических состояний и быть обусловлен как эндогенными механизмами, так и внешними воздействиями:
Чаще всего анемия вызывается хронической потерей крови: обильными менструациями, дисфункциональными маточными кровотечениями; желудочно-кишечными кровотечениями из эрозий слизистой желудка и кишечника, гастродуоденальных язв, геморроидальных узлов, анальных трещин и др. Скрытая, но регулярная кровопотеря отмечается при гельминтозах, гемосидерозе легких, экссудативном диатезе у детей и др.
Особую группу составляют лица с болезнями крови — геморрагическими диатезами (гемофилией, болезнью Виллебранда), гемоглобинурией. Возможно развитие постгеморрагической анемии, вызванной одномоментным, но массивным кровотечением при травмах и операциях. Гипохромная анемия может возникать вследствие ятрогенных причин — у доноров, часто сдающих кровь; пациентов с ХПН, находящихся на гемодиализе.
К факторам алиментарного порядка относятся анорексия, вегетарианство и следование диетам с ограничением мясных продуктов, плохое питание; у детей — искусственное вскармливание, позднее введение прикорма. Снижение абсорбции железа характерно для кишечных инфекций, гипоацидного гастрита, хронического энтерита, синдрома мальабсорбции, состояния после резекции желудка или тонкой кишки, гастрэктомии. Значительно реже железодефицитная анемия развивается вследствие нарушения транспортировки железа из депо при недостаточной белково-синтетической функции печени – гипотрансферринемиях и гипопротеинемиях (гепатитах, циррозе печени).
Ежедневная потребность в микроэлементе зависит от пола и возраста. Наиболее высока необходимость в железе у недоношенных, детей раннего возраста и подростков (в связи с высокими темпами развития и роста), женщин репродуктивного периода (в связи с ежемесячными менструальными потерями), беременных (в связи с формированием и ростом плода), кормящих мам (в связи с расходом в составе молока). Именно эти категории являются наиболее уязвимыми в отношении развития железодефицитной анемии. Кроме того, повышение потребности и расхода железа в организме наблюдается при инфекционных и опухолевых заболеваниях.
По своей роли в обеспечении нормального функционирования всех биологических систем железо является важнейшим элементом. От уровня железа зависит поступление кислорода к клеткам, протекание окислительно-восстановительных процессов, антиоксидантная защита, функционирование иммунной и нервной систем и пр. В среднем содержание железа в организме находится на уровне 3-4 г. Более 60% железа (>2 г) входит в состав гемоглобина, 9% — в состав миоглобина, 1% — в состав ферментов (гемовых и негемовых). Остальное железо в виде ферритина и гемосидерина находится в тканевом депо – главным образом, в печени, мышцах, костном мозге, селезенке, почках, легких, сердце. Примерно 30 мг железа непрерывно циркулирует в плазме, будучи частично связанным основным железосвязывающим белком плазмы – трансферрином.
При развитии отрицательного баланса железа мобилизуются и расходуются запасы микроэлемента, содержащиеся в тканевых депо. На первых порах этого бывает достаточно для поддержания адекватного уровня Hb, Ht, сывороточного железа. По мере истощения тканевых резервов компенсаторно увеличивается эритроидная активность костного мозга. При полном истощении эндогенного тканевого железа его концентрация начинает снижаться в крови, нарушается морфология эритроцитов, уменьшается синтез гема в гемоглобине и железосодержащих ферментов. Страдает кислородтранспортная функция крови, что сопровождается тканевой гипоксией и дистрофическими процессами во внутренних органах (атрофический гастрит, миокардиодистрофия и др.).
Железодефицитная анемия возникает не сразу. Вначале развивается предлатентный железодефицит, характеризующийся истощением только запасов депонированного железа при сохранности транспортного и гемоглобинового пула. На этапе латентного дефицита отмечается уменьшение транспортного железа, содержащегося в плазме крови. Собственно гипохромная анемия развивается при уменьшении всех уровней метаболических запасов железа – депонированного, транспортного и эритроцитарного. В соответствии с этиологией различают анемии: постгеморрагические, алиментарные, связанные с повышенным расходом, исходным дефицитом, недостаточностью резорбции и нарушением транспорта железа. По степени выраженности железодефицитные анемии подразделяются на:
- Легкие (Нb 120-90 г/л). Протекают без клинических проявлений или с их минимальной выраженностью.
- Среднетяжелые (Нb 90-70 г/л). Сопровождаются циркуляторно-гипоксическим, сидеропеническим, гематологическим синдромами умеренной степени выраженности.
- Тяжелые (Нb
Циркуляторно-гипоксический синдром обусловлен нарушением синтеза гемоглобина, транспорта кислорода и развитием гипоксии в тканях. Это находит свое выражение в ощущении постоянной слабости, повышенной утомляемости, сонливости. Пациентов преследует шум в ушах, мелькание «мушек» перед глазами, головокружения, переходящие в обмороки. Характерны жалобы на сердцебиение, одышку, возникающую при физической нагрузке, повышенную чувствительность к низким температурам. Циркуляторно-гипоксические нарушения могут усугублять течение сопутствующей ИБС, хронической сердечной недостаточности.
Развитие сидеропенического синдрома связано с недостаточностью тканевых железосодержащих ферментов (каталазы, пероксидазы, цитохромов и др.). Этим объясняется возникновение трофических изменений кожных покровов и слизистых оболочек. Чаще всего они проявляются сухостью кожи; исчерченностью, ломкостью и деформацией ногтей; повышенным выпадением волос. Со стороны слизистых оболочек типичны атрофические изменения, что сопровождается явлениями глоссита, ангулярного стоматита, дисфагии, атрофического гастрита. Может возникать пристрастие к резким запахам (бензина, ацетона), искажение вкуса (желание есть глину, мел, зубной порошок и пр.). Признаками сидеропении также служат парестезии, мышечная слабость, диспепсические и дизурические расстройства. Астеновегетативные нарушения проявляются раздражительностью, эмоциональной неустойчивостью, снижением умственной работоспособности и памяти.
Поскольку в условиях железодефицита IgA теряет свою активность, больные становятся подвержены частой заболеваемости ОРВИ, кишечными инфекциями. Пациентов преследует хроническая усталость, упадок сил, снижение памяти и концентрации внимания. Длительное течение железодефицитной анемии может привести к развитию миокардиодистрофии, распознаваемой по инверсии зубцов Т на ЭКГ. При крайне тяжелом железодефиците развивается анемическая прекома (сонливость, одышка, резкая бледность кожи с цианотичным оттенком, тахикардия, галлюцинации), а затем – кома с потерей сознания и отсутствием рефлексов. При массивной стремительной кровопотере возникает гиповолемический шок.
На наличие железодефицитной анемии может указывать внешний вид больного: бледная, с алебастровым оттенком кожа, пастозность лица, голеней и стоп, отечные «мешки» под глазами. При аускультации сердца обнаруживается тахикардия, глухость тонов, негромкий систолический шум, иногда – аритмия. С целью подтверждения анемии и определения ее причин проводится лабораторное обследование.
- Лабораторные тесты. В пользу железодефицитного характера анемии свидетельствует снижение гемоглобина, гипохромия, микро- и пойкилоцитоз в общем анализе крови. При оценке биохимических показателей отмечается снижение уровня сывороточного железа и концентрации ферритина (60 мкмоль/л), уменьшение насыщения трансферрина железом (
- Инструментальные методики. Для установления причины хронической кровопотери должно быть проведено эндоскопическое обследование ЖКТ (ЭГДС, колоноскопия,), рентгенодиагностика (ирригоскопия, рентгенография желудка). Обследование органов репродуктивной системы у женщин включает УЗИ малого таза, осмотр на кресле, по показаниям — гистероскопию с РДВ.
- Исследование пунктата костного мозга. Микроскопия мазка (миелограмма) показывает значительное снижение количества сидеробластов, характерное для гипохромной анемии. Дифференциальная диагностика направлена на исключение других видов железодефицитных состояний — сидеробластной анемии, талассемии.
К основным принципам терапии железодефицитной анемии относятся устранение этиологических факторов, коррекция рациона питания, восполнение железодефицита в организме. Этиотропное лечение назначается и проводится специалистами гастроэнтерологами, гинекологами, проктологами и др.; патогенетическое – гематологами. При железодефицитных состояниях показано полноценное питание с обязательным включением в рацион продуктов, содержащих гемовое железо (телятины, говядины, баранины, мяса кролика, печени, языка). Следует помнить, что усилению ферросорбции в ЖКТ способствуют аскорбиновая, лимонная, янтарная кислота. Ингибируют всасывание железа оксалаты и полифенолы (кофе, чай, соевый протеин, молоко, шоколад), кальций, пищевые волокна и др. вещества.
Вместе с тем, даже сбалансированная диета не в состоянии устранить уже развившийся недостаток железа, поэтому больным с гипохромной анемией показана заместительная терапия ферропрепаратами. Препараты железа назначаются курсом не менее 1,5-2-х месяцев, а после нормализации уровня Hb проводится поддерживающая терапия в течение 4-6 недель половинной дозой препарата. Для фармакологической коррекции анемии используются препараты двухвалентного и трехвалентного железа. При наличии витальных показаний прибегают к гемотрансфузионной терапии.
В большинстве случаев гипохромная анемия подается успешной коррекции. Однако при неустраненной причине железодефицит может рецидивировать и прогрессировать. Железодефицитная анемия у детей раннего и младшего возраста может вызывать задержку психомоторного и интеллектуального развития (ЗПР). В целях профилактики железодефицита необходим ежегодный контроль параметров клинического анализа крови, полноценное питание с достаточным содержанием железа, своевременная ликвидация источников кровопотери в организме. Следует учитывать, что лучше всего усваивается железо, содержащееся в мясе и печени в форме гема; негемовое железо из растительной пищи практически не усваивается – в этом случае оно сначала должно восстановиться до гемового при участии аскорбиновой кислоты. Лицам групп риска может быть показан профилактический прием железосодержащих препаратов по назначению специалиста.
источник
Среди различных анемических состояний железодефицитные анемииявляются самыми распространенными и составляют около 80% всех анемий.
Железодефицитная анемия— гипохромная микроцитарная анемия, развивающаяся вследствие абсолютного уменьшения запасов железа в организме. Железодефицитная анемия возникает, как правило, при хронической потере крови или недостаточном поступлении железа в организм.
По данным Всемирной организации здравоохранения, каждая 3-я женщина и каждый 6-й мужчина в мире (200 миллионов человек) страдают железодефицитной анемией.
Обмен железа
Железо является незаменимым биометаллом, играющим важную роль в функционировании клеток многих систем организма. Биологическое значение железа определяется его способностью обратимо окисляться и восстанавливаться. Это свойство обеспечивает участие железа в процессах тканевого дыхания. Железо составляет лишь 0,0065% массы тела. В организме мужчины с массой тела 70 кг содержится примерно 3,5 г (50 мг/кг массы тела) железа. Содержание железа в организме женщины с массой тела 60 кг составляет примерно 2,1 г (35 мг/кг массы тела). Соединения железа имеют различное строение, обладают характерной только для них функциональной активностью и играют важную биологическую роль. К наиболее важным железосодержащим соединениям относятся: гемопротеины, структурным компонентом которых является гем (гемоглобин, миоглобин, цитохромы, каталаза, пероксидаза), ферменты негеминовой группы (сукцинатдегидрогеназа, ацетил-КоА-дегидрогеназа, ксантиноксидаза), ферритин, гемосидерин, трансферрин. Железо входит в состав комплексных соединений и распределено в организме следующим образом:
— гемовое железо — 70%;
— депо железа — 18% (внутриклеточное накопление в форме ферритина и гемосидерина);
— функционирующее железо — 12% (миоглобин и содержащие железо энзимы);
— транспортируемое железо — 0,1% (железо, связанное с трансферрином).
Различают два вида железа: гемовое и негемовое. Гемовое железо входит в состав гемоглобина. Оно содержится лишь в небольшой части пищевого рациона (мясные продукты), хорошо всасывается (на 20-30%), на его всасывание практически не влияют другие компоненты пищи. Негемовое железо находится в свободной ионной форме — двухвалентного (Fe II) или трехвалентного железа (Fe III). Большая часть пищевого железа — негемовое (содержится преимущественно в овощах). Степень его усвоения ниже, чем гемового, и зависит от целого ряда факторов. Из продуктов питания усваивается только двухвалентное негемовое железо. Чтобы «превратить» трехвалентное железо в двухвалентное, необходим восстановитель, роль которого в большинстве случаев играет аскорбиновая кислота (витамин С). В процессе всасывания в клетках слизистой оболочки кишечника закисное железо Fe2+ превращается в окисное Fe3+ и связывается со специальным белком-носителем — трансферрином, который осуществляет транспорт железа к гемопоэтическим тканям и местам депонирования железа.
Накопление железа осуществляется белками ферритином и гемосидерином. При необходимости железо может активно освобождаться из ферритина и использоваться для эритропоэза. Гемосидерин является производным ферритина с более высоким содержанием железа. Из гемосидерина железо освобождается медленно. Начинающийся (прелатентный) дефицит железа можно определить по сниженной концентрации ферритина еще до исчерпания запасов железа, при еще сохраняющейся нормальной концентрации железа и трансферрина в сыворотке крови.
Основной этиопатогенетический фактор развития железодефицитной анемии — дефицит железа. Наиболее частыми причинами возникновения железодефицитных состояний являются:
1. потери железа при хронических кровотечениях (наиболее частая причина, достигающая 80%):
— кровотечения из желудочно-кишечного тракта: язвенная болезнь, эрозивный гастрит, варикозное расширение эзофагеальных вен, дивертикулы толстой кишки, инвазии анкилостомы, опухоли, НЯК, геморрой;
— длительные и обильные менструации, эндометриоз, фибромиома;
— макро- и микрогематурия: хронический гломеруло- и пиелонефрит, мочекаменная болезнь, поликистоз почек, опухоли почек и мочевого пузыря;
— носовые, легочные кровотечения;
— потери крови при гемодиализе;
— неконтролируемое донорство;
2. недостаточное усваивание железа:
— резекция тонкого кишечника;
— хронический энтерит;
— синдром мальабсорбции;
— амилоидоз кишечника;
3. повышенная потребность в железе:
— интенсивный рост;
— беременность;
— период кормления грудью;
— занятия спортом;
4. недостаточное поступление железа с пищей:
— новорожденные;
— маленькие дети;
— вегетарианство.
Рекомендуемая ежедневная норма поступления железа с пищей: для мужчин — 12 мг, для женщин — 15 мг (для беременных — 30 мг).
Патогенетически развитие железодефицитного состояния можно условно разделить на несколько стадий:
1. прелатентный дефицит железа (недостаточность накопления) — отмечается снижение уровня ферритина и снижение содержания железа в костном мозге, повышена абсорбция железа;
2. латентный дефицит железа (железодефицитный эритропоэз) — дополнительно снижается сывороточное железо, повышается концентрация трансферрина, снижается содержание сидеробластов в костном мозге;
3. выраженный дефицит железа = железодефицитная анемия — дополнительно снижается концентрация гемоглобина, эритроцитов и гематокрит.
В период скрытого дефицита железа появляются многие субъективные жалобы и клинические признаки, характерные для железодефицитных анемий. Пациенты отмечают общую слабость, недомогание, снижение работоспособности. Уже в этот период могут наблюдаться извращение вкуса, сухость и пощипывание языка, нарушение глотания с ощущением инородного тела в горле, сердцебиение, одышка.
При объективном обследовании пациентов обнаруживаются «малые симптомы дефицита железа»: атрофия сосочков языка, хейлит, сухость кожи и волос, ломкость ногтей, жжение и зуд вульвы. Все эти признаки нарушения трофики эпителиальных тканей связаны с тканевой сидеропенией и гипоксией.
Больные железодефицитной анемией отмечают общую слабость, быструю утомляемость, затруднение в сосредоточении внимания, иногда сонливость. Появляются головная боль, головокружение. При тяжелой анемии возможны обмороки. Эти жалобы, как правило, зависят не от степени снижения гемоглобина, а от продолжительности заболевания и возраста больных.
Железодефицитная анемия характеризуется также изменениями кожи, ногтей и волос. Кожа обычно бледная, иногда с легким зеленоватым оттенком (хлороз) и с легко возникающим румянцем щек, она становится сухой, дряблой, шелушится, легко образуются трещины. Волосы теряют блеск, сереют, истончаются, легко ломаются, редеют и рано седеют. Специфичны изменения ногтей: они становятся тонкими, матовыми, уплощаются, легко расслаиваются и ломаются, появляется исчерченность. При выраженных изменениях ногти приобретают вогнутую, ложкообразную форму (койлонихия). У больных железодефицитной анемией возникает мышечная слабость, которая не наблюдается при других видах анемий. Ее относят к проявлениям тканевой сидеропении. Атрофические изменения возникают в слизистых оболочках пищеварительного канала, органов дыхания, половых органов. Поражение слизистой оболочки пищеварительного канала — типичный признак железодефицитных состояний.
Отмечается снижение аппетита. Возникает потребность в кислой, острой, соленой пище. В более тяжелых случаях наблюдаются извращения обоняния, вкуса (pica chlorotica): употребление в пищу мела, известки, сырых круп, погофагия (влечение к употреблению льда). Признаки тканевой сидеропении быстро исчезают после приема препаратов железа.
Основные ориентиры в лабораторной диагностике железодефицитной анемии следующие:
1. Среднее содержание гемоглобина в эритроците в пикограммах (норма 27-35 пг) снижено. Для его вычисления цветовой показатель умножают на 33,3. Например, при цветовом показателе 0,7 х 33,3 содержание гемоглобина равно 23,3 пг.
2. Средняя концентрация гемоглобина в эритроците снижена; в норме она составляет 31-36 г/дл.
3. Гипохромия эритроцитов определяется при микроскопии мазка периферической крови и характеризуется увеличением зоны центрального просветления в эритроците; в норме соотношение центрального просветления к периферическому затемнению равно 1:1; при железодефицитной анемии — 2+3:1.
4. Микроцитоз эритроцитов — уменьшение их размеров.
5. Разная по интенсивности окраска эритроцитов — анизохромия; наличие как гипо-, так и нормохромиых эритроцитов.
6. Разная форма эритроцитов — пойкилоцитоз.
7. Количество ретикулоцитов (при отсутствии кровопотери и периода ферротерапии) при железодефицитной анемии остается в норме.
8. Содержание лейкоцитов также в пределах нормы (за исключением случаев кровопотери или онкопатологии).
9. Содержание тромбоцитов чаще остается в пределах нормы; умеренный тромбоцитоз возможен при кровопотере в момент обследования, а содержание тромбоцитов уменьшается, когда в основе железодефицитной анемии лежит кровопотеря вследствие тромбоцитопении (например, при ДВС-синдроме, болезни Верльгофа).
10. Уменьшение количества сидероцитов вплоть до их исчезновения (сидероцит — это эритроцит, содержащий гранулы железа). С целью стандартизации изготовления мазков периферической крови рекомендуется использовать специальные автоматические устройства; образующийся при этом монослой клеток повышает качество их идентификации.
Биохимический анализ крови:
1. Снижение содержания железа в сыворотке крови (в норме у мужчин 13-30 мкмоль/л, у женщин 12-25 мкмоль/л).
2. ОЖСС повышена (отражает количество железа, которое может быть связано за счет свободного трансферрина; ОЖСС в норме — 30-86 мкмоль/л).
3. Исследование трансферриновых рецепторов иммуноферментным методом; их уровень повышен у больных железодефицитной анемией (у больных анемией хронических заболеваний — в норме или снижен, несмотря на аналогичные показатели обмена железа.
4. Латентная железосвязывающая способность сыворотки крови повышена (определяется путем вычитания из показателей ОЖСС показателя содержания сывороточного железа).
5. Процент насыщения трансферрина железом (отношение показателя железа сыворотки крови к ОЖСС; в норме 16-50%) снижен.
6. Уровень сывороточного ферритина тоже снижен (в норме 15-150 мкг/л).
Вместе с тем у больных железодефицитной анемией увеличено количество трансферриновых рецепторов и повышен уровень эритропоэтина в сыворотке крови (компенсаторные реакции кроветворения). Объем секреции эритропоэтина обратно пропорционален величине кислородтранспортной емкости крови и прямо пропорционален кислородному запросу крови. Следует учитывать, что уровень сывороточного железа выше в утренние часы; перед началом и во время менструации он выше, чем после менструации. Содержание железа в сыворотке крови в первые недели беременности выше, чем в последнем ее триместре. Уровень сывороточного железа повышается на 2-4-й день после лечения железосодержащими препаратами, а затем снижается. Значительное потребление мясных продуктов накануне исследования сопровождается гиперсидеремией. Эти данные необходимо учитывать при оценке результатов исследования сывороточного железа. Не менее важно соблюдать технику лабораторного исследования, правила забора крови. Так, пробирки, в которые собирают кровь, предварительно должны быть промыты соляной кислотой и бидистиллированной водой.
Исследование миелограммы выявляет умеренную нормобластическую реакцию и резкое снижение содержания сидеробластов (эритрокариоцитов, содержащих гранулы железа).
О запасах железа в организме судят по результатам десфералевой пробы. У здорового человека после внутривенного введения 500 мг десфераля выводится с мочой от 0,8 до 1,2 мг железа, в то время как у больного с железодефицитной анемией выведение железа снижается до 0,2 мг. Новый отечественный препарат дефериколиксам идентичен десфералю, но дольше циркулирует в крови и поэтому точнее отражает уровень запасов железа в организме.
С учетом уровня гемоглобина железодефицитная анемия, как и другие формы анемий, подразделяются на анемию тяжелой, средней и легкой степени. При железодефицитной анемии легкой степени концентрация гемоглобина ниже нормы, но более 90 г/л; при железодефицитной анемии средней степени содержание гемоглобина менее 90 г/л, но более 70 г/л; при тяжелой степени железодефицитной анемии концентрация гемоглобина менее 70 г/л. Вместе с тем клинические признаки тяжести анемии (симптомы гипоксического характера) не всегда соответствуют степени тяжести анемии по лабораторным критериям. Поэтому предложена классификация анемий по степени выраженности клинических симптомов.
По клиническим проявлениям выделяют 5 степеней тяжести анемий:
1. анемия без клинических проявлений;
2. анемический синдром умеренной выраженности;
3. выраженный анемический синдром;
4. анемическая прекома;
5. анемическая кома.
Умеренная степень тяжести анемии характеризуется общей слабостью, специфическими признаками (например, сидеропеническими или признаками дефицита витамина В12); при выраженной степени тяжести анемии появляются сердцебиение, одышка, головокружение и др. Прекоматозное и коматозное состояния могут развиться в считанные часы, что особенно характерно для мегалобластной анемии.
Современные клинические исследования показывают, что среди больных железодефицитной анемией наблюдается лабораторная и клиническая гетерогенность. Так, у части больных с признаками железодефицитной анемии и сопутствующими воспалительными и инфекционными заболеваниями уровень сывороточного и эритроцитарного ферритина не снижается, однако после ликвидации обострения основного заболевания их содержание падает, что свидетельствует об активации макрофагов в процессах расходования железа. У части больных уровень эритроцитарного ферритина даже повышается, особенно у больных с длительным течением железодефицитной анемии, что приводит к неэффективному эритропоэзу. Иногда наблюдаются повышение уровня сывороточного железа и эритроцитарного ферритина, снижение трансферрина сыворотки крови. Предполагается, что в этих случаях нарушен процесс передачи железа в гемсинтезирующие клетки. В некоторых случаях определяется одновременно дефицит железа, витамина В12 и фолиевой кислоты.
Таким образом, даже уровень сывороточного железа не всегда отражает степень дефицита железа в организме при наличии других признаков железодефицитной анемии. Только уровень ОЖСС при железодефицитной анемии всегда повышен. Поэтому, ни один биохимический показатель, в т.ч. ОЖСС, нельзя рассматривать как абсолютный диагностический критерий при железодефицитной анемии. В то же время морфологическая характеристика эритроцитов периферической крови и компьютерный анализ основных параметров эритроцитов являются решающими в скрининговой диагностике железодефицитной анемии.
Диагностика железодефицитных состояний затруднена в случаях, когда содержание гемоглобина остается в норме. Железодефицитная анемия развивается при наличии тех же факторов риска, что и при железодефицитной анемии, а также у лиц с повышенной физиологической потребностью в железе, прежде всего у недоношенных детей в раннем возрасте, у подростков с быстрым увеличением роста и массы тела, у доноров крови, при алиментарной дистрофии. На первой стадии дефицита железа клинические проявления отсутствуют, а дефицит железа определяют по содержанию гемосидерина в макрофагах костного мозга и по абсорбции радиоактивного железа в ЖКТ. На второй стадии (латентный дефицит железа) наблюдается увеличение концентрации протопорфирина в эритроцитах, уменьшается количество сидеробластов, появляются морфологические признаки (микроцитоз, гипохромия эритроцитов), уменьшается среднее содержание и концентрация гемоглобина в эритроцитах, снижаются уровень сывороточного и эритроцитарного ферритина, насыщение трансферрина железом. Уровень гемоглобина в этой стадии остается достаточно высоким, а клинические признаки характеризуются снижением толерантности к физической нагрузке. Третья стадия проявляется явными клиническими и лабораторными признаками анемии.
Обследование больных с железодефицитной анемией
Для исключения анемий, имеющих общие черты с железодефицитной анемией, и выявления причины дефицита железа необходимо полное клиническое обследование больного:
Общий анализ кровис обязательным определением количества тромбоцитов, ретикулоцитов, изучением морфологии эритроцитов.
Биохимический анализ крови: определение уровня железа, ОЖСС, ферритина, билирубина (связанного и свободного), гемоглобина.
Во всех случаях необходимо исследовать пунктат костного мозгадо назначения витамина В12 (прежде всего, для дифференциальной диагностики с мегалобластной анемией).
Для выявления причины железодефицитной анемии у женщин обязательна предварительная консультация гинеколога с целью исключения заболеваний матки и ее придатков, а у мужчин — осмотр проктолога для исключения кровоточащего геморроя и уролога для исключения патологии предстательной железы.
Известны случаи экстрагенитального эндометриоза, например в дыхательных путях. В этих случаях наблюдается кровохарканье; фибробронхоскопия с гистологическим исследованием биоптата слизистой оболочки бронха позволяет установить диагноз.
В план обследования входят также рентгенологическое и эндоскопическое исследование желудка и кишечника с целью исключения язв, опухолей, в т.ч. гломических, а также полипов, дивертикула, болезни Крона, язвенного колита и т.д. При подозрении на легочный сидероз проводят рентгенографию и томографию легких, исследование мокроты на альвеолярные макрофаги, содержащие гемосидерин; в редких случаях необходимо гистологическое исследование биоптата легких. При подозрении на патологию почек необходимы общий анализ мочи, исследование сыворотки крови на мочевину и креатинин, по показаниям — ультразвуковое и рентгенологическое исследование почек. В ряде случаев приходится исключать эндокринную патологию: микседему, при которой дефицит железа может развиться вторично вследствие поражения тонкой кишки; ревматическую полимиалгию — редкое заболевание соединительной ткани у пожилых женщин (реже — у мужчин), характеризуется болью в мышцах плечевого или тазового пояса без каких-либо объективных изменений в них, а в анализе крови — анемия и увеличение СОЭ.
Дифференциальная диагностика железодефицитных анемий
При постановке диагноза железодефицитной анемии необходимо проводить дифференциальный диагноз с другими гипохромными анемиями.
Железоперераспределительные анемии — достаточно частая патология и по частоте развития занимает второе место среди всех анемий (после железодефицитной анемии). Она развивается при острых и хронических инфекционно-воспалительных заболеваниях, сепсисе, туберкулезе, ревматоидном артрите, болезнях печени, онкологических заболеваниях, ИБС и др. Механизм развития гипохромной анемии при этих состояниях связан с перераспределением железа в организме (оно находится преимущественно в депо) и нарушением механизма реутилизации железа из депо. При вышеперечисленных заболеваниях происходит активация макрофагальной системы, когда макрофаги в условиях активации прочно удерживают железо, тем самым нарушая процесс его реутилизации. В общем анализе крови отмечается умеренное снижение гемоглобина (
Основным отличием от железодефицитной анемии являются:
— повышенный уровень ферритина сыворотки, что свидетельствует о повышенном содержании железа в депо;
— уровень сывороточного железа может сохраняться в пределах нормальных значений или быть умеренно сниженным;
— ОЖСС остается в пределах нормальных значений либо снижается, что говорит об отсутствии Fe-голодания сыворотки.
Железонасыщенные анемии развиваются в результате нарушения синтеза гема, которое обусловлено наследственностью либо может быть приобретенным. Гем образуется из протопорфирина и железа в эритрокариоцитах. При железонасыщенных анемиях происходит нарушение активности ферментов, участвующих в синтезе протопорфирина. Следствием этого является нарушение синтеза гема. Железо, которое не было использовано для синтеза гема, депонируется в виде ферритина в макрофагах костного мозга, а также в виде гемосидерина в коже, печени, поджелудочной железе, миокарде, в результате чего развивается вторичный гемосидероз. В общем анализе крови будет регистрироваться анемия, эритропения, снижение цветового показателя.
Для показателей обмена железа в организме характерно повышение концентрации ферритина и уровня сывороточного железа, нормальные показатели ОЖСС, повышение насыщения трансферрина железом (в некоторых случаях достигает 100 %). Таким образом, основными биохимическими показателями, позволяющими оценить состояние обмена железа в организме, являются ферритин, железо сыворотки, ОЖСС и % насыщения трансферрина железом.
Использование показателей обмена железа в организме дает возможность врачу-клиницисту:
— выявить наличие и характер нарушений обмена железа в организме;
— выявить наличие дефицита железа в организме на доклинической стадии;
— проводить дифференциальную диагностику гипохромных анемий;
— оценить эффективность проводимой терапии.
Во всех случаях железодефицитной анемии необходимо установить непосредственную причину возникновения данного состояния и по возможности ликвидировать ее (чаще всего устранить источник кровопотери или провести терапию основного заболевания, осложнившегося сидеропенией).
Лечение железодефицитной анемии должно быть патогенетически обоснованным, комплексным и нацеленным не только на ликвидацию анемии как симптома, но и на ликвидацию дефицита железа и восполнение его запасов в организме.
Программа лечения железодефицитной анемии:
— устранение причины железодефицитной анемии;
— лечебное питание;
— ферротерапия;
— профилактика рецидивов.
Больным железодефицитными анемиями рекомендуется разнообразная диета, включающая мясные продукты (телятина, печень) и продукты растительного происхождения (бобы, сою, петрушку, горох, шпинат, сушеные абрикосы, чернослив, гранаты, изюм, рис, гречневую крупу, хлеб). Однако невозможно добиться противоанемического эффекта только диетой. Если даже больной будет питаться высококалорийными продуктами, содержащими животный белок, соли железа, витамины, микроэлементы,- можно достичь всасывания железа не более 3-5 мг в сутки. Необходимо применение препаратов железа. В настоящее время в распоряжении врача имеется большой арсенал лекарственных препаратов железа, характеризующихся различным составом и свойствами, количеством содержащегося в них железа, наличием дополнительных компонентов, влияющих на фармакокинетику препарата, различных лекарственных форм.
Согласно рекомендациям, разработанным ВОЗ, при назначении препаратов железа предпочтение отдают препаратам, содержащим двухвалентное железо. Суточная доза должна достигать у взрослых 2 мг/кг элементарного железа. Общая длительность лечения не менее трех месяцев (иногда до 4-6 месяцев). Идеальный железосодержащий препарат должен обладать минимальным количеством побочных эффектов, иметь простую схему применения, наилучшее соотношение эффективность/цена, оптимальное содержание железа, желательно наличие факторов, усиливающих всасывание и стимулирующих гемопоэз.
Показания к парентеральному введению препаратов железа возникают при непереносимости всех пероральных препаратов, нарушении всасывания (неспецифический язвенный колит, энтерит), язвенной болезни желудка и двенадцатиперстной кишки в период обострения, при тяжелой анемии и жизненной необходимости быстрого восполнения дефицита железа. Об эффективности препаратов железа судят по изменениям лабораторных показателей в динамике. К 5-7 дню лечения увеличивается количество ретикулоцитов в 1,5-2 раза по сравнению с исходными данными. Начиная с 10-го дня терапии повышается содержание гемоглобина.
Учитывая прооксидантное и лизосомотропное действие препаратов железа, их парентарельное введение можно сочетать с внутривенным капельным введением реополиглюкина (400 мл — один раз в неделю), который позволяет защитить клетку и избежать перегрузки макрофагов железом. Учитывая значительные изменения функционального состояния мембраны эритроцита, активацию перекисного окисления липидов и снижение антиоксидантной защиты эритроцитов при железодефицитной анемии, необходимо в схему лечения вводить антиоксиданты, мембраностабилизаторы, цитопротекторы, антигипоксанты, такие как a-токоферол до 100-150 мг в сутки (либо аскорутин, витамин А, витамин С, липостабил, метионин, милдронат и др.), а также сочетать с витаминами В1, В2, В6, В15, липоевой кислотой. В некоторых случаях целесообразно применение церулоплазмина.
Список препаратов, которые применяют при лечении железодефицитной анемии:
— Жектофер (Jectofer);
— Конферон (Conferon);
— Мальтофер (Maltofer);
— Сорбифер дурулес (Sorbifer durules);
— Тардиферон (Tardiferon);
— Ферамид (Ferramidum);
— Ферро-градумет (Ferro-gradumet);
— Ферроплекс (Ferroplex);
— Ферроцерон (Ferroceronum);
— Феррум лек (Ferrum lek).
— Тотема (tothema)
— Периодическое наблюдение за картиной крови;
— употребление пищи с высоким содержанием железа (мясо, печень и др.);
— профилактический прием препаратов железа в группах риска.
— оперативная ликвидация источников кровопотерь.
источник
Вид анемии в зависимости от МСV
Патогенетический вариант анемии
Гетерозиготная талассемия, при хронических болезнях
ЖДА, серповидноклеточная, бета-талассемия, гемоглобин Н фрагментация эритроцитов (два пика на гистограмме)*
При хронических болезнях, энзимопатии эритроцитов, гемоглобинопатии, наследственный сфероцитоз, острая постгеморрагическая, при хроническом миелолейкозе, при цитостатической миелодепрессии
Смешанный дефицит (ЖДА и В12), сидеробластные, миелофиброз
Апластичекая анемия, миелодиспластический синдром
Аутоиммунная гемолитическая, мегалобластная
*Гистограмма графически отражает частоту встречаемости эритроцитов разного объема и является аналогом кривой Прайс-Джонса. Обычно гистограмма имеет форму одиночного пика.
Повышение количества ретикулоцитов более 3%
Снижение количества ретикулоцитов менее 0,5%
Мембранопатии, энзимопатии, нестабильность гемоглобина, промежуточная форма талассемии, микроангиопатические гемолитические анемии
Апластическая анемия, В12-дефицитная анемия, фолиеводефицитная анемия, ЖДА тяжелая, врожденная дизэритропоэтическая анемия*, большая форма талассемии*, сидеробластные анемии*, пароксизмальная ночная гемоглобинурия
*Количество ретикулоцитов может быть повышенным, но не соответствовать степени гемолиза.
Наследственный сфероцитоз, аутоиммунная гемолитическая анемия, криз дефицита Г-6-ФД, нестабильный гемоглобин
Наследственный элиптоцитоз, может быть при ЖДА, талассемии, мегалобластной анемии, миелофиброзе, миелофтизе, миелодиспластическом синдроме, дефиците пируваткиназы
Талассемия, гемоглобин С, заболевания печени
Шизоциты (фрагментация эритроцитов)
Механические гемолитические анемии
Анемии при заболеваниях печени, абета-липопротеинемии
Врожденный и приобретенный стоматоцитоз
Анизохромия, пойкилоцитоз (эхиноциты, шизоциты)
Анемии при хронической почечной недостаточности
Макроовалоцитоз (мегалоцитоз), тельца Жолли, кольца Кабо
Тельца Гейнца в эритроцитах
Железодефицитная анемия (ЖДА) – полиэтиологичное заболевание, являющееся результатом снижения общего содержания железа в организме и характеризующееся прогрессирующими микроцитозом и гипохромией эритроцитов.
По данным литературы, 90% случаев анемий вызваны дефицитом железа. 43% детей до 4 лет и 37% дошкольников и школьников в возрасте 5 — 12 лет в мире страдают железодефицитным состоянием (ЖДС). Частота ЖДА у детей в среднем по России достигает 12%, а в раннем возрасте по разным регионам – от 15% до 47,8% (Хотимченко С.А., Алексеева И.А., Батурин А.К.,1999). Предрасполагают к развитию ЖДС у детей от 6 месяцев до 3 лет высокие темпы роста, функциональная незрелость пищеварительной системы, однообразность питания, частые интеркуррентные заболевания, дисфункции желудочно-кишечного тракта, дефекты вскармливания.
Метаболизм железа определяется потребностью в этом нутриенте, содержанием и биодоступностью его в пищевом рационе, утилизацией в желудочно-кишечном тракте, транспортом к клеткам, синтезом железопротеинов, потерями (выделением с калом и мочой). Сидеропения может развиться вследствие недостаточного поступления железа с пищей, нарушения его утилизации или повышенных потерь. Существуют четыре группы причин ЖДА у детей.
1. Снижение депонирования железа в антенатальном периоде. В первом полугодии жизни алиментарное железо, поступающее в минимальных количествах с молоком, важной роли в эритропоэзе младенца не играет. Гемопоэз осуществляется преимущественно за счет депо железа, создание которого у плода в виде ферритина идет с ранних сроков гестации, интенсивно нарастая в позднем фетальном периоде. 70% гемового железа у детей до двух лет имеет материнское происхождение. Обеспеченность плода ферритином зависит от содержания железа в организме женщины и состояния фетоплацентарного барьера. Имеются убедительные данные о снижении тканевого железа плаценты и сывороточного железа в пуповине новорожденного при сидеропении у матери. Предрасполагают к развитию ЖДС у женщины кровопотери, чаще связанные с менометроррагиями, повторные беременности и роды, несбалансированное питание. Гестозы, обострения хронических воспалительных процессов во второй половине беременности нарушают функции фетоплацентарного барьера и затрудняют утилизацию железа плодом. Недоношенные и новорожденные дети от многоплодной беременности всегда имеют низкий уровень депонированного железа. В перинатальном периоде предрасполагает к снижению депонированного железа постгеморрагические анемии новорожденных.
2. Алиментарный дефицит — наиболее частая причина развития ЖДС. Суточная потребность организма в железе зависит от возраста, пола, физической активности, потерь и составляет для младенцев до 3 месяцев — 4 мг, в первом полугодии жизни — 7 мг, для детей в возрасте от 7 месяцев до 6 лет — 10 мг, у школьников препубертатного возраста – 12 мг, у юношей – 15 мг, у девушек – 18 мг. Обеспеченность организма железом связана как с его содержанием в пищевом рационе, так и с биодоступностью. К продуктам, богатым железом, относятся красное мясо, печень, икра осетровых рыб, некоторые крупы (греча, пшено, овес), фрукты (черника, голубика, персики, яблоки, хурма и др.). В женском молоке концентрация железа не превышает 2 — 4 мг/л, в коровьем – 1 мг/л. Содержание железа в рационе питания является одним из важнейших, но не единственным фактором, определяющим нормальную обеспеченность организма человека этим нутриентом. Гемовое железо, поступающее из продуктов животного происхождения (мяса, рыбы, домашней птицы) в виде комплексных форм, связанных с порфириновым кольцом (гемоглобин, миоглобин) и другими белками (ферритин, гемосидерин), хорошо всасывается в кишечнике и усваивается до 15 — 35% от общего объёма, содержащегося в пищевых продуктах. Железо, входящее в состав ряда специфических белков (лактоферрин молока, овотрансферрин и фосфовитин яйца), всасывается хуже, за исключением грудного молока, биодоступность нутриента в котором составляет 50%. Из растительных пищевых продуктов человек получает железо в виде солей, фитоферритина, в комплексах с органическими кислотами. Усвояемость негемового железа не превышает 2 — 5%. Уровень всасывания железа зависит от индивидуальных потребностей в нем, обеспеченности им организма, его источника и содержания в пище, а также от наличия в этом продукте лиганд, усиливающих или ингибирующих процессы утилизации. Гемовое железо обладает высокой абсорбционной способностью вследствие того, что его усвояемость, как правило, не связана с действием других веществ, содержащихся в рационе. Негемовое железо всасывается намного хуже, поскольку на его усвояемость влияет ряд соединений, входящих в состав пищевых продуктов.
Большое значение в процессе абсорбции железа принадлежит количественному и качественному составу белка. Лица с низкой обеспеченностью белком имеют дефицит железа, что объясняется достаточно большим содержанием хорошо усвояемого гемового железа в белковых продуктах, образованием с нутриентом легко абсорбируемых комплексов некоторыми аминокислотами. Добавление в рацион продуктов животного происхождения способно увеличивать всасывание железа из овощей в 2 — 3 раза. При белковой недостаточности резко уменьшается утилизация железа эритроцитами, что приводит к снижению концентрации гемоглобина.
Органические кислоты (лимонная, яблочная, винная) соединяются с негемовым железом в хорошо растворимые комплексы. В то же время целый ряд соединений, содержащихся в соевых продуктах, чае, кофе, шпинате, молоке (фитаты, танин, фосфопротеины, оксалаты), образуют с железом плохо растворимые комплексы и тем самым тормозят его всасывание.
Хорошо изучена роль гиповитаминозов в развитии ЖДА. Аскорбиновая кислота активно участвует в процессах всасывания негемового железа в кишечнике, восстанавливая трехвалентное железо в биодоступную двухвалентную форму. Образуя хелатные комплексы в кислой среде желудка и поддерживая в растворимой форме негемовое железо, поступающее в щелочную среду тонкой кишки, витамин С устраняет ингибирующий эффект фитатов и танина, которые создают эти комплексы в щелочной среде. Утилизация железа повышается как при добавлении чистой аскорбиновой кислоты, так и продуктов с высоким ее содержанием. Предполагается, что аскорбиновая кислота необходима для модулирования синтеза ферритина. Аскорбиновая кислота увеличивает освобождение железа из макрофагов, и тем самым способствует эритропоэзу.
К развитию анемии может приводить недостаток рибофлавина. В условиях нарушения метаболизма рибофлавина, с нарастанием его тканевого дефицита формируется синдром избыточной потери железа с мочой, снижается накопление в печени, что, возможно, обусловлено блокадой поступления железа из кишечника. Дефицит пиридоксина отражается на состоянии аминокислотного обмена (лизина, гистидина, метионина), специфически участвующих в процессах всасывания железа в кишечнике и синтезе гемоглобина.
Значение в развитии анемии имеет нарушение метаболизма многих микроэлементов: меди, марганца, никеля, цинка, селена и др. Медь является кофактором различных ферментов, участвующих, в том числе, в метаболизме железа. Исследования на животных показали, что церуллоплазмин необходим для транспорта железа трансферрином. Кроме того, ионы меди участвуют в синтезе гема в митохондриях, поэтому дефицит меди в организме приводит к устойчивой к лечению ферропрепаратами анемии и нейтропении.
Экзогенный дефицит цинка, описанный впервые A.S. Prasad в 1963 году и названый болезнью Прасада, характеризуется наличием карликовости, гипогонадизма и ЖДА.
Одним из важных патогенетических звеньев анемических состояний является дисбаланс в системе “перекисное окисление липидов (ПОЛ) – антиоксиданты”. Установлено, что активация процессов липопероксидации на фоне угнетения антиоксидантных ресурсов организма сопровождает практически все анемии. Это, в свою очередь, приводит к усилению мембранодеструкции, накоплению в крови токсических продуктов ПОЛ. Лечение ферропрепаратами инициирует гиперпродукцию свободных радикалов, вызывая оксидативный стресс. Наиболее биологически значимым ферментом антиоксидантного звена (АОЗ) является супероксиддисмутаза – фермент содержащий цинк. Кроме того, обладая постоянной валентностью, цинк предотвращает окисление SH-групп ионами железа и меди.
Особую значимость проблема ЖДС приобретает в эндемичных по дефициту некоторых микроэлементов (например, селена) регионах. Известна роль селена в обеспечении адекватного ответа со стороны ферментативного АОЗ за счет включения в структуру глутатионпероксидазы (ГПО). Установлено, что при ЖДА у детей раннего возраста в условиях селенодефицита имеется нарушение фосфолипидного состава мембран и снижение активности антиоксидантных ферментов эритроцитов, приводящее к усилению их перекисного гемолиза (Баранова Т.А., 2004).
Таким образом, одной из ведущих причин развития ЖДА является нерациональное питание. Предрасполагают к сидеропении раннее искусственное вскармливание младенцев, особенно неадаптированными молочными смесями, несвоевременное введение прикормов; дефицит в рационе мясных продуктов, свежих овощей и фруктов на фоне преобладание злаков, бобовых и молока в рационе детей старше года, отсутствие коррекции питания в эндемичных по дефициту отдельных микроэлементов регионах.
3. Заболевания желудочно-кишечного тракта (гастриты, энтериты, врожденные и приобретенные энтеропатии с синдромом нарушенного всасывания) приводят к нарушению утилизации железа
4. Хронические кровопотери, возможно обусловленные эрозивным гастроэнтероколитом, диафрагмальной грыжей, варикозом вен пищевода, полипозом или телеангиэктазиями кишечника, дивертикулом, геморрагическими диатезами, гематурией, менометроррагиями, идиопатическим гемосидерозом легких, некоторыми паразитарными инвазиями. У детей первого года жизни, вскармливаемых нативным коровьим молоком, часто возникают диапедезные кровотечения в кишечнике.
ЖДА предшествует латентный дефицит железа, протекающий бессимптомно и характеризующийся уменьшением количества резервного железа. Поскольку микроэлемента поступает в организм недостаточно, то потребляется резервное железо, поступающее в циркулирующую кровь. Первоначально используется ферритин макрофагов, как более мобильная фракция, а затем – гемосидерин, компартмент железа. Отрицательный баланс железа приводит к усилению абсорбции микроэлемента в кишечнике и увеличению синтеза трансферрина. Освобождаемое железо из резервного компартмента позволяет поддерживать сывороточное железо на физиологическом уровне, но сывороточный ферритин при этом снижается. Если дефицит железа не восполняется, то развивается ЖДА. По данным российский педиатров, частота латентного дефицита железа среди детей первых двух лет жизни достигает 73% (Румянцев А.Г., Чернов В.М., 2001) и вероятность его перехода в анемию высока.
Клиническая картина ЖДА состоит из двух ведущих синдромов: анемического и сидеропенического. Анемический синдром проявляется бледностью кожных покровов и слизистых оболочек, физической и умственной утомляемостью, снижением работоспособности, тахикардией, головокружением, приглушенностью тонов и систолическим шумом при аускультации сердца. Для сидеропенического синдрома характерны дистрофические изменения кожи и ее придатков в виде выпадения волос, ломкости, исчерченности ногтей, койлонихий (ложкообразных ногтей) а также атрофические поражения слизистых оболочек пищевода, желудка, кишечника, рецепторов носа и языка, сопровождающиеся извращением вкуса и обоняния, гингивитом, ангулярным стоматитом, дисфагией, диспепсией, вторичным синдромом мальабсорбции. Часто отмечаются мышечные гипотония и боли вследствие дефицита миоглобина. Следует отметить, что клинические симптомы дегенеративных поражений кожи и слизистых оболочек желудочно-кишечного тракта выражены у взрослых и детей старшего возраста, что связано, по-видимому, с длительным дефицитом железа. В раннем возрасте преобладают диспепсические расстройства, метеоризм, снижение аппетита, затруднения при глотании твердой пищи, мышечная гипотония, в том числе диафрагмы, приводящая к опущению печени и селезенки, определяемой пальпаторно. У детей старшего возраста нередко появляется снижение тонуса мышц мочевого пузыря, что ведет к неудержанию мочи при смехе и кашле.
Лабораторная диагностика. 1. Гемограмма характеризуется гипохромной, микроцитарной, регенераторной анемией, с нормальным или повышенным числом эритроцитов в начале болезни. При прогрессировании железодефицита и снижении эффективности эритропоэза количество эритроцитов и ретикулоцитов падает и повышается на фоне ферротерапии. При оценке гемограммы, выполненной с помощью гематологического анализатора, выявляются снижение MCV, MCH, MCHC и типичное для ЖДА значительное увеличение RDW, показывающую анизоцитоз клеток. Осмотическая резистентность эритроцитов (ОРЭ) в норме или повышена.
2. При биохимическом исследовании крови определяются основные диагностические критерии ЖДС: уменьшается содержания сывороточного ферритина (СФ) – ниже 30 нг/л; повышается уровень общей железосвязывающей способности сыворотки (ОЖСС) – выше 60 мкмоль/л; понижается количество сывороточного железа (СЖ) – менее 12,5 мкмоль/л и насыщение трансферрина железом (НТЖ) – ниже 25%. При падении коэффициента НТЖ ниже 16% эффективный эритропоэз невозможен, что сопровождается эритропенией и ретикулоцитопенией. Латентный дефицит железа диагностируется на основании снижения концентрации СФ и повышения ОЖСС.
3. Необходимости проведения миелограммы для диагностики ЖДА нет. Морфология клеток костного мозга при дефиците железа характеризуется нормобластной гиперплазией с преобладанием полихроматофильных или оксифильных нормобластов с уменьшением объема цитоплазмы, со снижением процента сидеробластов и гемосидерина в клетках до полного его отсутствия.
Диагностический алгоритм ЖДА включает: 1) тщательный сбор анамнеза (выяснение предрасполагающих факторов к дефициту железа);
2) клиническое исследование пациента (отсутствие желтухи, лимфо-пролиферативного синдрома, гепатоспленомегалии, наличие признаков сидеропении);
3) оценку гемограммы (гипохромная, микроцитарная, регенераторная анемия при отсутствии изменений со стороны лейкограммы, содержания тромбоцитов, сдвигов СОЭ).
4) оценку эффекта от терапии препаратами железа через 2 – 3 недели (ретикулоцитоз, тенденция к нарастанию гемоглобина).
Во всех остальных случаях проводится диагностика в большем объеме, направленная на исключение других причин анемических состояний.
В таблице 7 отражены дифференциально-диагностические лабораторные критерии анемий при алиментарном дефиците железа, нарушениях его утилизации и реутилизации.
источник