Гемолитические анемии – это группа анемий, которые характеризуются снижением продолжительности жизни эритроцитов и их ускоренным разрушением (гемолиз, эритроцитолиз) либо внутри кровеносных сосудов, либо в костном мозге, печени или селезенке.
В норме средняя продолжительность жизни эритроцитов составляет 110–120 суток. При гемолитической анемии жизненный цикл красных клеток крови укорачивается в несколько раз и составляет 15–20 суток. Процессы разрушения эритроцитов преобладают над процессами их созревания (эритропоэза), в результате чего в крови снижается концентрация гемоглобина, уменьшается содержание эритроцитов, т. е. развивается анемия. Другими общими признаками, характерными для всех видов гемолитических анемий, являются:
- лихорадка с ознобом;
- боли в животе и пояснице;
- нарушения микроциркуляции;
- спленомегалия (увеличение селезенки);
- гемоглобинурия (присутствие в моче гемоглобина);
- желтуха.
Гемолитической анемией страдает примерно 1% населения. В общей структуре анемий на долю гемолитических приходится 11%.
Гемолитические анемии развиваются либо под воздействием внеклеточных (внешних) факторов, либо в результате дефектов эритроцитов (внутриклеточные факторы). В большинстве случаев внеклеточные факторы являются приобретенными, а внутриклеточные – врожденными.
К внутриклеточным факторам относятся аномалии мембран эритроцитов, ферментов или гемоглобина. Все эти дефекты являются наследуемыми, за исключением пароксизмальной ночной гемоглобинурии. В настоящее время описано свыше 300 заболеваний, связанных с точечными мутациями генов, кодирующих синтез глобинов. В результате мутаций изменяется форма и мембрана эритроцитов, увеличивается их подверженность гемолизу.
Более обширную группу представляют внеклеточные факторы. Эритроциты находятся в окружении эндотелия (внутренняя оболочка) кровеносных сосудов и плазмы. Присутствие в плазме инфекционных агентов, токсических веществ, антител способно вызывать изменения в стенках эритроцитов, приводящие к их разрушениям. По такому механизму развивается, например, аутоиммунная гемолитическая анемия, гемолитические трансфузионные реакции.
Дефекты эндотелия кровеносных сосудов (микроангиопатии) также способны повреждать эритроциты, приводя к развитию микроангиопатической гемолитической анемии, у детей протекающей остро, в виде гемолитико-уремического синдрома.
Стать причиной гемолитической анемии может и прием некоторых лекарственных препаратов, в частности, противомалярийных средств, анальгетиков, нитрофуранов и сульфаниламидов.
Все гемолитические анемии подразделяются на приобретенные и врожденные. К врожденным, или наследственным формам относятся:
- эритроцитарные мембранопатии – результат аномалий строения эритроцитарных мембран (акантоцитоз, овалоцитоз, микросфероцитоз);
- энзимопении (ферментопении) – связаны с недостатком в организме определенных ферментов (пируваткиназы, глюкозо-6-фосфатдегидрогеназы);
- гемоглобинопатии – обусловлены нарушением структуры молекулы гемоглобина (серповидноклеточная анемия, талассемия).
Наиболее часто встречающейся в клинической практике наследственной гемолитической анемией является болезнь Минковского – Шоффара (микросфероцитоз).
Приобретенные гемолитические анемии, в зависимости от вызвавших их причин, делятся на следующие виды:
- приобретенные мембранопатии (шпороклеточная анемия, пароксизмальная ночная гемоглобинурия);
- изоиммунные и аутоиммунные гемолитические анемии – развиваются в результате повреждения эритроцитов собственными или полученными извне антителами;
- токсические – ускоренное разрушение эритроцитов происходит из-за воздействия на них бактериальных токсинов, биологических ядов или химических веществ;
- гемолитические анемии, связанные с механическими повреждениями эритроцитов (маршевая гемоглобинурия, тромбоцитопеническая пурпура).
Для всех видов гемолитических анемий характерны:
- анемический синдром;
- увеличение селезенки;
- развитие желтухи.
При этом каждый отдельный вид заболевания обладает особенностями.
Наиболее часто встречающейся в клинической практике наследственной гемолитической анемией является болезнь Минковского – Шоффара (микросфероцитоз). Она отслеживается в нескольких поколениях семьи и наследуется по аутосомно-доминантному типу. Генетическая мутация приводит к недостаточному содержанию в мембране эритроцитов определенного типа белков и липидов. В свою очередь это вызывает изменения в размерах и форме эритроцитов, их преждевременное массивное разрушение в селезенке. Микросфероцитарная гемолитическая анемия может манифестировать у пациентов в любом возрасте, но чаще всего первые симптомы гемолитической анемии возникают в 10–16 лет.
Заболевание может протекать с разной выраженностью. У некоторых больных отмечается субклиническое течение, а у других развиваются тяжелые формы, сопровождающиеся частыми гемолитическими кризами, которые имеют следующие проявления:
- повышение температуры тела;
- озноб;
- общая слабость;
- головокружение;
- боли в пояснице и животе;
- тошнота, рвота.
Основным симптомом микросфероцитоза является разной степени выраженности желтуха. Из-за высокого содержания стеркобилина (конечного продукта обмена гема) кал интенсивно окрашивается в темно-коричневый цвет. У всех пациентов, страдающих микросфероцитарной гемолитической анемией, увеличивается селезенка, а у каждого второго увеличивается и печень.
Микросфероцитоз повышает риск образования в желчном пузыре конкрементов, т. е. развития желчнокаменной болезни. В связи с этим нередко возникают желчные колики, а при закупорке желчного протока камнем – обтурационная (механическая) желтуха.
В клинической картине микросфероцитарной гемолитической анемии у детей присутствуют и другие признаки дисплазии:
- брадидактилия или полидактилия;
- готическое небо;
- аномалии прикуса;
- седловидная деформация носа;
- косоглазие;
- башенный череп.
У пациентов пожилого возраста из-за разрушения эритроцитов в капиллярах нижних конечностей возникают устойчивые к традиционной терапии трофические язвы стоп и голеней.
Гемолитические анемии, связанные с дефицитом определенных ферментов, обычно манифестируют после приема некоторых медикаментов или перенесенного интеркуррентного заболевания. Их характерными признаками являются:
- бледная желтуха (бледный цвет кожи с лимонным оттенком);
- сердечные шумы;
- умеренно выраженная гепатоспленомегалия;
- темный цвет мочи (обусловлен внутрисосудистым распадом эритроцитов и выделением с мочой гемосидерина).
При тяжелом течении заболевания возникают ярко выраженные гемолитические кризы.
К врожденным гемоглобинопатиям относятся талассемия и серповидноклеточная анемия. Клиническая картина талассемии выражена следующими симптомами:
- гипохромная анемия;
- вторичный гемохроматоз (связан с частыми гемотрансфузиями и необоснованным назначением железосодержащих препаратов);
- гемолитическая желтуха;
- спленомегалия;
- холелитиаз;
- поражение суставов (артрит, синовит).
Серповидноклеточная анемия протекает с рецидивирующими болевыми кризами, умеренно выраженной гемолитической анемией, повышенной восприимчивостью больного к инфекционным заболеваниям. Основными симптомами являются:
- отставание детей в физическом развитии (особенно мальчиков);
- трофические язвы нижних конечностей;
- умеренная желтуха;
- болевые кризы;
- апластические и гемолитические кризы;
- приапизм (не связанная с половым возбуждением самопроизвольная эрекция полового члена, сохраняющаяся несколько часов);
- холелитиаз;
- спленомегалия;
- аваскулярные некрозы;
- остеонекроз с развитием остеомиелита.
Из приобретенных гемолитических анемий чаще всего встречаются аутоиммунные. К их развитию приводит выработка иммунной системой пациентов антител, направленных против собственных эритроцитов. Т. е. под влиянием некоторых факторов происходит нарушение деятельности иммунной системы, в результате которой она начинает воспринимать собственные ткани как чужеродные и разрушать их.
При аутоиммунной анемии гемолитические кризы развиваются внезапно и остро. Их возникновению могут предшествовать предвестники в виде артралгий и/или субфебрильной температуры тела. Симптомами гемолитического криза являются:
- повышение температуры тела;
- головокружение;
- резкая слабость;
- одышка;
- сердцебиение;
- боли в пояснице и эпигастрии;
- быстрое нарастание желтухи, не сопровождающейся зудом кожи;
- увеличение селезенки и печени.
Существуют формы аутоимунных гемолитических анемий, при которых пациенты плохо переносят холод. При переохлаждении у них развивается гемоглобинурия, холодовая крапивница, синдром Рейно (сильный спазм артериол пальцев).
Особенностями клинической картины токсических форм гемолитических анемий являются:
- быстропрогрессирующая общая слабость;
- высокая температура тела;
- рвота;
- сильная боль в пояснице и животе;
- гемоглобинурия.
На 2-3 сутки от начала заболевания у больного начинает нарастать уровень билирубина в крови и развивается желтуха, а еще через 1-2 дня возникает гепаторенальная недостаточность, проявляющаяся анурией, азотемией, ферментемией, гепатомегалией.
Еще одной формой приобретенной гемолитической анемии является гемоглобинурия. При этой патологии происходит массовое разрушение эритроцитов внутри кровеносных сосудов и гемоглобин попадает в плазму, а затем начинает выделяться с мочой. Основным симптомом гемоглобинурии является темно-красный (иногда черный) цвет мочи. Другими проявлениями патологии могут стать:
Гемолиз эритроцитов при гемолитической болезни плода и новорожденных связан с проникновением в кровоток плода через плаценту антител из крови матери, т. е. по патологическому механизму данная форма гемолитической анемии относится к изоиммунным заболеваниям.
В норме средняя продолжительность жизни эритроцитов составляет 110–120 суток. При гемолитической анемии жизненный цикл красных клеток крови укорачивается в несколько раз и составляет 15–20 суток.
Гемолитическая болезнь плода и новорожденного может протекать по одному из следующих вариантов:
- внутриутробная гибель плода;
- отечная форма (иммунная форма водянки плода);
- желтушная форма;
- анемическая форма.
Общими признаками, характерными для всех форм этого заболевания, являются:
- гепатомегалия;
- спленомегалия;
- увеличение в крови эритробластов;
- нормохромная анемия.
Обследование пациентов с гемолитическими анемиями проводится гематологом. При опросе пациента выясняют частоту образования гемолитических кризов, их тяжесть, а также уточняет наличие подобных заболеваний в семейном анамнезе. В ходе осмотра пациента обращают внимание на окраску склер, видимых слизистых оболочек и кожных покровов, пальпируют живот с целью выявления возможного увеличения печени и селезенки. Подтвердить гепатоспленомегалию позволяет УЗИ органов брюшной полости.
Изменения в общем анализе крови при гемолитической анемии характеризуются гипо- или нормохромной анемией, ретикулоцитозом, тромбоцитопенией, лейкопенией, увеличением СОЭ.
Большое диагностическое значение при аутоиммунных гемолитических анемиях имеет положительная проба Кумбса (наличие в плазме крови или прикрепленных к поверхности эритроцитов антител).
В ходе биохимического исследования крови определяют увеличение активности лактатдегидрогеназы, наличие гипербилирубинемии (преимущественно за счет увеличения непрямого билирубина).
В общем анализе мочи выявляют гемоглобинурию, гемосидеринурию, уробилинурию, протеинурию. В кале отмечается повышенное содержание стеркобилина.
При необходимости выполняют пункционную биопсию костного мозга с последующим гистологическим анализом (обнаруживают гиперплазию эритроидного ростка).
Гемолитической анемией страдает примерно 1% населения. В общей структуре анемий на долю гемолитических приходится 11%.
Дифференциальная диагностика гемолитических анемий проводится со следующими заболеваниями:
- гемобластозы;
- гепатолиенальный синдром;
- портальная гипертензия;
- цирроз печени;
- гепатиты.
Подходы к лечению гемолитических анемий определяются формой заболевания. Но в любом случае первостепенной задачей является устранение гемолизирующего фактора.
Схема терапии гемолитического криза:
- внутривенное вливание растворов электролитов и глюкозы;
- трансфузия свежезамороженной плазмы крови;
- витаминотерапия;
- назначение антибиотиков и/или кортикостероидов (по показаниям).
При микросфероцитозе показано хирургическое лечение – удаление селезенки (спленэктомия). После оперативного вмешательства у 100% пациентов наступает стойкая ремиссия, так как повышенный гемолиз эритроцитов прекращается.
Терапия аутоиммунных гемолитических анемий проводится глюкокортикоидными гормонами. При ее недостаточной эффективности может потребоваться назначение иммунодепрессантов, противомалярийных препаратов. Резистентность медикаментозной терапии является показанием к проведению спленэктомии.
При гемоглобинурии проводят трансфузию отмытых эритроцитов, инфузию растворов плазмозаменителей, назначают антиагреганты и антикоагулянты.
Лечение токсических форм гемолитических анемий требует введения антидотов (при их наличии), а также использования методов экстракорпоральной детоксикации (форсированный диурез, перитонеальный диализ, гемодиализ, гемосорбция).
Гемолитические анемии могут приводить к развитию следующих осложнений:
При своевременно начатом и адекватном лечении гемолитических анемий прогноз в целом благоприятный. При присоединении осложнений он значительно ухудшается.
Профилактика развития гемолитических анемий включает следующие мероприятия:
- медико-генетическое консультирование пар при наличии в семейном анамнезе указаний на случаи гемолитической анемии;
- определение на этапе планирования беременности группы крови и резус-фактора будущей матери;
- укрепление иммунной системы.
Видео с YouTube по теме статьи:
Образование: окончила Ташкентский государственный медицинский институт по специальности лечебное дело в 1991 году. Неоднократно проходила курсы повышения квалификации.
Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
источник
Процесс разрушения эритроцитов называется гемолизом. В организме здорового человека постоянно происходит так называемый физиологический гемолиз вследствие естественного старения эритроцитов.
Продолжительность жизни эритроцитов в среднем колеблется от 100 до 130 дней. При наличии дефекта эритроцитов или в результате воздействия на них различных патологических факторов жизненный цикл эритроцитов укорачивается. Именно это и является характерным признаком гемолитических анемий.
Гемолитические анемии – это группа заболеваний, при которых разрушение эритроцитов происходит быстрее, чем их выработка костным мозгом. При этой патологии наблюдается уменьшение количества эритроцитов и концентрации гемоглобина вследствие укорочения жизни эритроцитов. При этом костный мозг не реагирует на анемический синдром.
Гемолитические анемии разделяют по признаку врожденности и приобретенности. Врожденные формы патологии связаны с дефектами структуры и функции эритроцитов.
Приобретенные гемолитические анемии развивается в результате влияния факторов окружающей среды:
- инфекции вирусные и бактериальные – малярия, анаэробный сепсис;
- интоксикации гемолитическими ядами – фосфор, мышьяк, змеиный яд, грибной яд;
- сильное воздействие физических факторов – переохлаждение, ожоги;
- переливание несовместимой крови;
- вакцинация;
- психоэмоциональное напряжение;
- физические нагрузки;
- лекарственные средства – хинин, сульфаниламиды, антибиотики.
Приобретенная гемолитическая анемия может быть спровоцирована многими инфекционными болезнями: корь, краснуха, эпидемический паротит, ангина и другие.
Основные формы врожденных (наследственных) гемолитических анемий:
- гемолитические анемии, связанные с нарушением мембраны эритроцита – мембранопатии;
- гемолитические анемии, связанные с нарушением активности ферментов эритроцитов – ферментопатии;
- гемолитические анемии, связанные с нарушением структуры или синтеза гемоглобина – гемоглобинопатии.
Из врожденных гемолитических анемий наиболее часто встречается болезнь Минковского-Шоффара.
Болезнь Минковского-Шоффара (микросфероцитоз, сфероцитоз)
Сфероцитоз – это группа врожденных гемолитических анемий, характеризующихся появлением шаровидных эритроцитов (микросфероцитов) вследствие дефекта белков мембраны эритроцита.
При мембранопатии этого вида эритроциты уменьшаются в размере за счет своей сферичности. Изменения в структуре белков клеточной мембраны приводят к ее натяжению. Вместо двояковогнутых дисков (такую форму имеют здоровые эритроциты) образуются сферы. Это в свою очередь сопровождается нарушением способности эритроцитов к деформации. Эритроциты не могут пройти через красную пульпу селезенки, теряют часть мембраны в селезенке, увеличивая орган в размерах. В результате в крови появляются совершенно круглые эритроциты.
Основные признаки микросфероцитоза – анемия, желтуха, увеличение селезенки. При тяжелых формах патологии этого вида у больных отмечаются деформации скелета: башенный череп, уменьшение глазного яблока, высокое верхнее нёбо, изменяется расположение зубов. У некоторых больных бывают укорочены мизинцы. Иногда возникают трофические язвы ног.
Единственным методом лечения анемии при микросфероцитозе является удаление селезенки. Показанием к хирургической операции являются:
- анемия тяжелой степени;
- кризовое течение анемии;
- значительное повышение билирубина;
- боли в правом подреберье, связанные с наличием камней в желчном пузыре;
- значительное увеличение селезенки;
- отставание у детей в развитии.
После удаления селезенки обычно уменьшается симптоматика болезни (устраняется анемия), но дефект эритроцитов остается.
Распространенность заболевания составляет 1 случай на 1000 – 4500 человек.
Овалоцитоз (эллиптоцитоз)
Овалоцитоз – редкое врожденное заболевание, при котором эритроциты имеют характерную овальную форму.
Выраженная анемия наблюдается нечасто. Из-за повышенного разрушения эритроцитов может наблюдаться образование желчных камней. Это вызывает необходимость удаления желчного пузыря. В случае этой операции рекомендуется провести одномоментно и удаление селезенки даже в отсутствие выраженной анемии.
Стоматоцитоз
Стоматоцитоз характеризуется уменьшением центрального просветления в эритроците до размеров щели. Причиной является нарушение проницаемости мембраны эритроцитов для одновалентных катионов при сохраненной проницаемости для двухвалентных катионов и анионов.
Мембранопатия этого вида может быть следствием врожденного дефекта и нередко наблюдается в течение двух недель после приема алкоголя.
Лечение наследственной патологии этого вида – хирургическая операция по удалению селезенки. Это уменьшает, но не устраняет процесс разрушения эритроцитов. Однако существует опасность тромботических осложнений у больных, перенесших операцию. Эти осложнения плохо купируются лекарственными средствами.
Среди всех случаев недостаточности ферментов более 95 % случаев приходится на недостаточность пируваткиназы. Остальные ферментопатии встречаются крайне редко, в основном в отдельных семьях.
Дефицит пируваткиназы
Фермент пируваткиназа – один из заключительных ферментов гликолиза. При его недостаточности происходит дегидратация и сморщивание эритроцитов. Уменьшение количества воды в эритроцитах затрудняет отдачу кислорода гемоглобином.
При недостаточности пируваткиназы описано много мутаций, приводящих к замене одних аминокислот на другие в молекуле фермента. Поэтому клинические и лабораторные проявления дефицита пируваткиназы характеризуются большим многообразием – от тяжелых гемолитических кризов до бессимптомного течения.
У больных отмечается:
- анемия;
- желтуха;
- увеличение селезенки;
- увеличение печени;
- камни в желчном пузыре;
- иногда трофические язвы голеней.
Гемолитические кризы могут быть вызваны инфекцией, возникать в период менструации, при беременности.
Лечение патологии этого вида не разработано. Удаление селезенки дает лишь некоторый эффект. Во время проведения хирургической операции у больных с камнями в желчном пузыре одновременно удаляют и его.
Дефицит глюкозо-6-фосфатдегидрогеназы (Г-6-ФДГ) – фавизм
Распространенность этого вида гемолитической анемии высока среди представителей негроидной расы – у 10 % чернокожего населения США. В белой расе патология встречается значительно реже.
Разрушение эритроцитов развивается в тот момент, когда они контактируют с лекарственными препаратами, вызывающими образование перекиси водорода, окисление гемоглобина и мембран эритроцитов. Такими лекарствами являются:
- примахин,
- салицилаты,
- сульфаниламиды,
- нитрофураны,
- фенацетин,
- некоторые производные витамина К.
Аналогичным эффектом могут обладать и конские бобы.
Разрушается обычно 25 % циркулирующих эритроцитов, редко – больше. Лица, имеющие дефект глюкозо-6-фосфатдегидрогеназы, должны исключить применение указанных лекарственных средств.
Гемолитические кризы, не спровоцированные приемом лекарственных средств, наблюдаются при лихорадках, острых вирусных и бактериальных инфекциях, при диабетическом ацидозе (смещении кислотно-щелочного баланса организма в сторону увеличения кислотности).
Заболевание возникает неожиданно. Могут наблюдаться невыраженная желтуха, присутствие крови в моче, могут быть и острые нарушения функции почек.
Гемоглобинопатии – это группа наследственных заболеваний, обусловленных присутствием в эритроцитах дефектных глобинов. Существует достаточно большое число различных видов этой патологии. Из всех видов гемоглобинопатий чаще других встречаются серповидноклеточная анемия и талассемия.
Талассемия
Талассемия – наиболее распространенный вид гемоглобинопатий, наиболее частая врожденная аномалия у человека. Это патология, связанная с нарушением баланса в скорости синтеза различных цепей глобина. Причем сами по себе эти цепи являются нормальными.
Выделяют β-талассемию и α-талассемию, что соответствует снижению синтеза определенной цепи глобина. Клинические проявления заболевания при всех формах сходны, но варьируют по своей выраженности: при малой форме они менее выражены, при большой талассемии признаки заболевания максимальны.
При заболевании присутствуют общие симптомы наследственных гемолитических анемий:
- выраженные изменения лицевого скелета, черепа, длинных трубчатых костей, что сопровождается их переломами;
- сильно замедленное физическое и половое развитие ребенка;
- низкий рост.
Постоянное разрушение эритроцитов развивает цирроз печени, сердечную недостаточность, желчекаменную болезнь. Характерно увеличение селезенки, иногда до значительных размеров.
Малая талассемия не нуждается в лечении. Лечение большой талассемии направлено на устранение проявлений гемохроматоза – нарушение обмена железа с накоплением его в тканях и органах. Назначаются препараты для связывания и ускорения выведения железа из организма.
При сильном увеличении селезенки выполняется операция по ее удалению. Это уменьшает степень гемолиза.
Серповидноклеточная анемия (гемоглобиноз S)
Серповидноклеточная анемия характеризуется изменением структуры эритроцита. Он принимает серповидную форму и не может проходить через капиллярное русло. Повышается вязкость крови, замедляется кровоток в микроциркуляторном русле, вызывая инфаркты органов.
Исторически серповидноклеточная анемия оказалась первой болезнью, при которой было продемонстрировано присутствие у пациента другого, отличного от нормального, гемоглобина. Это гемоглобин S. Серповидноклеточная анемия встречается практически только у чернокожих жителей Африки.
Различают гетерозиготную и гомозиготную форму серповидноклеточной анемии.
Основная часть пациентов болеет в гетерозиготной форме. Больной практически здоров до момента попадания в условия напряжения кислорода в артериальной крови: подъем в горы, полет на самолете, тяжелая физическая нагрузка. При этом развивается тяжелый гемолитический криз с характерными проявлениями вплоть до полного отсутствия урины в мочевом пузыре (острая анурия) и смерти.
У гетерозиготных больных даже без тяжелых гемолитических кризов наблюдается поражение почек в виде выделения мочи постоянно низкого удельного веса и периодического спонтанного присутствия крови в моче.
Прогноз патологии этого вида в целом благоприятный. Многие больные и не подозревают о наличии у них гемоглобинопатии.
Пациенты с гомозиготной формой патологии имеют тяжелую гемолитическую анемию. Тяжелые кризы происходят на фоне инфекции. Характерные жалобы:
- боль в трубчатых костях, в кистях и стопах;
- эпизодические боли в суставах с лихорадкой;
- нарушение кровоснабжения головки бедренной кости.
Могут быть приступы болей в животе психогенной природы, болей в спине, инсульты. В большинстве случаев имеют место тяжелые инфекции, прогрессирует дыхательная и почечная недостаточность. Иногда возникает аномально длительная болезненная эрекция полового члена, не связанная с сексуальным возбуждением. Изменения кроветворения приводят к нарушениям строения скелета.
При необходимости больным переливают донорские эритроциты. Особенно важно это при беременности или при подготовке больных к операции. Переливание эффективно при длительно незаживающих язвах на ногах.
Основные формы приобретенных гемолитических анемий:
- анемии, связанные с воздействием антител – аутоиммунные;
- анемии, связанные с изменением структуры мембраны в связи с соматической мутацией – пароксизмальная ночная гемоглобинурия (болезнь Маркиафавы-Микели);
- анемии, связанные с механическим повреждением оболочки эритроцитов с появлением фрагментированных эритроцитов (шистоцитов) – протезы клапанов, маршевая гемоглобинурия;
- анемии, обусловленные химическим повреждением эритроцитов – воздействие гемолитических ядов (свинец, тяжелые металлы, органические кислоты, змеиный яд), малярия; клострилиальный, стафилококковый, стрептококковый сепсис;
- анемии, обусловленные недостатком витаминов;
- анемии, обусловленные разрушением эритроцитов паразитами.
Примером приобретенной гемолитической анемии являются гемолитическая болезнь плода и новорожденного при несовместимости матери и плода по резус-фактору, острая гемолитическая анемия при осложнениях после переливания крови, вызванная несовместимостью группы крови.
Аутоиммунные гемолитические анемии связаны с появлением в крови больного антител против эритроцитов. Эти виды патологии связаны с тепловыми антителами – при лимфопролиферативных заболеваниях, опухолях; с холодовыми антителами – при инфекциях.
Гемолитическая анемия с тепловыми антителами (идиопатическая аутоимунная)
Встречается чаще у женщин, являясь самой частой гемолитической анемией. Заболевание начинается остро, манифестирует гемолитическим кризом, нередко тяжелым. Уровень гемоглобина снижается за считанные часы до 20 – 30 г/л.
Тепловые антитела появляются:
- при системной красной волчанке;
- при хроническом лимфолейкозе, лимфомах;
- после приема некоторых лекарственных средств – а-метилдопа, L-дофа.
Нередко причиной появления антител становятся пенициллины, цефалоспорины. В этих случаях антитела направлены против комплекса антибиотик-мембрана эритроцита и исчезают вскоре после отмены препаратов.
Течение заболевания может быть и хроническим. Патология может возникнуть и на фоне полного здоровья. Этот вид анемии сложно определить. Диагноз подтверждается постановкой прямой пробы Кумбса, выполняемой при t 37°С.
Лечение лекарственных форм гемолитической анемии начинают с отмены препарата, вызвавшего гемолиз. В первые часы заболевания целесообразно проведение плазмафереза. Эффективность глюкортикостероидных лекарств при этой форме анемии не подтверждена.
Для лечения аутоиммунной гемолитической анемии назначают большие дозы стероидов (100 мг преднизолона в сутки), что в 30% случаев позволяет достичь стойкой ремиссии заболевания. В случае рецидива или невозможности быстрого (в течение нескольких недель) прекращения стероидной терапии показано удаление селезенки. Операция эффективна у 30 % больных.
В случае неэффективности описанных методов лечения назначают длительную стероидную терапию. Иногда прибегают к применению циклоспорина, цитостатиков.
Болезнь холодовых антител
Болезнь холодовых антител – это гемолитическая анемия, вызванная антителами (холодовые агглютинины), вступающими в реакцию при температуре ниже 37° и даже ниже 30° С.
Клинически проявляется:
- острой формой, нередко связанной с инфекцией – микоплазменной, инфекционным мононуклеозом;
- хронической – при идиопатическом варианте, при хроническом лимфолейкозе и других заболеваниях лимфатических тканей.
В клинической картине наряду с признаками гемолитической анемии (обычно умеренной), нередко наблюдаются синюшность кожи и боли в кончиках пальцев при снижении температуры окружающей среды (синдром Рейно).
При анемии этого вида необходимо избегать переохлаждения.
Для пароксизмальной ночной гемоглобинурии характерны гемолитические кризы и эпизоды появления гемоглобина в моче.
Причина заболевания, вероятно, связана с приобретенным дефектом строения мембраны эритроцита, приводящим к повышенной чувствительности к гемолитическим агентам. Дефект является результатом соматической мутации, возможно, на уровне стволовых клеток.
Клиническая картина – хроническая гемолитическая анемия с периодическими гемолитическими кризами (гемоглобин может снижаться до 30 – 50 г/л), с появлением утром желтухи и мочи почти черного цвета за счет гемоглобинурии.
Болеют преимущественно лица среднего возраста. Кризы провоцируются инфекциями, приемом препаратов железа, вакцинациями, физической нагрузкой, иногда менструациями.
Клинические проявления гемолитической анемии зависят от выраженности гемолиза: от острых, угрожающих жизни состояний до слабых симптомов, которые могут проявляться только увеличением количества билирубина в сыворотке крови и увеличением селезенки при нормальном гемоглобине.
Основные клинические признаки гемолитической анемии:
- общий анемический синдром – слабость, утомляемость, бледность, головокружение, сердцебиение, одышка;
- специфический синдром гемолиза – желтушное окрашивание склер, кожи, темное окрашивание кала, темная моча, темно-красная, черная моча.
Для гемолитической анемии характерно образование билирубиновых камней в желчном пузыре, увеличение в размерах селезенки, печени.
Острые гемолитические анемии могут привести к резкому обострению признаков разрушения эритроцитов. Гемолитический криз развивается со следующими симптомами:
- высокая температура;
- слабость;
- головные боли, головокружение;
- боли в животе, спине, пояснице;
- тошнота, рвота;
- резкое учащенное сердцебиение;
- одышка;
- бледность кожных покровов с желтушным оттенком;
- желтушность белка склер;
- снижение артериального давления;
- лихорадка;
- моча приобретает почти черный цвет;
- в некоторых случаях расстройства сознания, судороги.
В сыворотке крови обнаруживается непрямой билирубин, в моче – белок и свободный гемоглобин. Общий анализ крови указывает на резкую анемию со снижением эритроцитов и гемоглобина, повышение уровня молодых, незрелых эритроцитов, чрезмерное увеличение содержания лейкоцитов.
Диагностика проводится на основе лабораторных анализов и других инструментов (смотри Таблицу 1).
Таблица 1
| Методы диагностики | Результаты исследований |
| Клинический анализ крови | Нормохромная (реже гипохромная – при талассемии), гиперрегенераторная (с ретикулоцитозом), нормобластическая анемия |
| Биохимический анализ крови | Гипербилирубинемия за счет непрямого билирубина. Может быть повышение уровня сывороточного железа. При поражении почек – повышение креатинина, мочевины (азотемия) |
| Общий анализ мочи | Уробилинурия, а при внутрисосудистом гемолизе – гемоглобинурия |
| Проба Кумбса с выявлением тепловых или холодовых агглютиногенов | Положительная – при аутоиммунном генезе |
| Проба Хэма | Выявление повышенной чувствительности эритроцитов к комплементу при болезни Маркиафавы-Миккели |
| Проба на осмотическую резистентность эритроцитов | Выявление патологических фракций гемоглобина НвF, НвS, НвА2, НвН – при наследственных гемоглобинопатиях |
| Электрофорез гемоглобина | |
| Стернальная пункция | Гиперплазия эритроидного ростка |
| Генетические исследования |
Острая гемолитическая анемия может иметь следующие варианты лечения:
- применение кортикостероидных препаратов;
- переливание эритроцитарной массы;
- хирургическая операция по удалению селезенки;
- проведение противоинтоксикационной терапии.
Лечение гемолитической анемии зависит от ее формы и описано выше в разделах.
источник
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
Гемолитическая анемия (ГА) — малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.
Центральным звеном патогенеза ГА является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. При аутоиммунном механизме анемии происходит образование антиэритроцитарных АТ (тепловых, холодовых), которые вызывают ферментативный лизис мембраны эритроцитов. Токсические вещества, являясь сильнейшими окислителями, разрушают эритроцит за счет развития метаболических, функциональных и морфологических изменений оболочки и стромы красных кровяных телец. Механические факторы оказывают прямое воздействие на клеточную мембрану. Под влиянием этих механизмов из эритроцитов выходят ионы калия и фосфора, а внутрь поступают ионы натрия. Клетка разбухает, при критическом увеличении ее объема наступает гемолиз. Распад эритроцитов сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии— анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические — анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом — обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Энзимопенические анемии связаны с недостатком определенных ферментов эритроцитов (чаще — Г-6-ФД, глутатион-зависимых ферментов, пируваткиназы и др). Гемолитическая анемия может впервые заявлять о себе после перенесенного интеркуррентного заболевания или приема медикаментов (салицилатов, сульфаниламидов, нитрофуранов). Обычно заболевание имеет ровное течение; типична «бледная желтуха», умеренная гепатоспленомегалия, сердечные шумы. В тяжелых случаях развивается ярко выраженная картина гемолитического криза (слабость, рвота, одышка, сердцебиение, коллаптоидное состояние). В связи с внутрисосудистым гемолизом эритроцитов и выделением гемосидерина с мочой последняя приобретает темный (иногда черный) цвет. Особенностям клинического течения гемоглобинопатий — талассемии и серповидно-клеточной анемии посвящены самостоятельные обзоры.
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Токсические анемии протекают с прогрессирующей слабостью, болями в правом подреберье и поясничной области, рвотой, гемоглобинурией, высокой температурой тела. Со 2-3 суток присоединяется желтуха и билирубинемия; на 3-5 сутки возникает печеночная и почечная недостаточность, признаками которых служат гепатомегалия, ферментемия, азотемия, анурия. Отдельные виды приобретенных гемолитических анемий рассмотрены в соответствующих статьях: «Гемоглобинурия» и «Тромбоцитопеническая пурпура», «Гемолитическая болезнь плода».
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
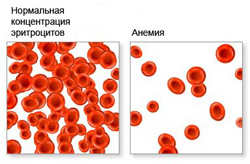
Эритроциты формируются в красном костном мозге из белковых фракций и небелковых компонентов под воздействием эритропоэтина (синтезируется почками). Эритроциты в течение трех дней обеспечивают транспорт, главным образом, кислорода и углекислого газа, а также питательных веществ и продуктов метаболизма от клеток и тканей. Срок жизни эритроцита сто двадцать дней, после чего он разрушается. Старые эритроциты накапливаются в селезенке, где утилизируются небелковые фракции, а белковые поступают в красный костный мозг, участвуя в синтезе новых эритроцитов.
Вся полость эритроцита наполнена белком, гемоглобином, в состав которого входит железо. Гемоглобин придает эритроциту красную окраску, а также помогает ему переносить кислород и углекислый газ. Его работа начинается в легких, куда эритроциты поступают с током крови. Молекулы гемоглобина захватывают кислород, после чего обогащенные кислородом эритроциты направляются сначала по крупным сосудам, а затем и по мелким капиллярам к каждому органу, отдавая клеткам и тканям необходимый для жизни и нормальной деятельности кислород.
Анемия ослабляет способность организма к газовому обмену, за счет сокращения числа эритроцитов нарушается транспортировка кислорода и углекислого газа. Вследствие этого у человека могут наблюдаться такие признаки анемии как чувство постоянной усталости, упадок сил, сонливость, а также повышенная раздражительность.
Анемия является проявлением основного заболевания и не является самостоятельным диагнозом. Многие болезни, включая инфекционные заболевания, доброкачественные или злокачественные опухоли могут быть связаны с анемией. Именно поэтому анемия является важным признаком, который требует проведения необходимых исследований для выявления основной причины, которая привела к ее развитию.
Тяжелые формы анемии вследствие тканевой гипоксии могут привести к серьезным осложнениям, таким как шоковые состояния (например, геморрагический шок), гипотония, коронарная или легочная недостаточность.
- по механизму развития;
- по степени тяжести;
- по цветному показателю;
- по морфологическому признаку;
- по способности костного мозга к регенерации.
| По патогенезу анемия может развиться вследствие кровопотери, нарушения образования эритроцитов или из-за их выраженного разрушения. По механизму развития выделяют:
|
- потеря крови (острые или хронические кровотечения);
- повышенное разрушение эритроцитов (гемолиз);
- уменьшенное производство эритроцитов.
Также следует заметить, что в зависимости от вида анемии причины ее возникновения могут отличаться.
Факторы, влияющие на развитие анемии
- гемоглобинопатии (изменение строения гемоглобина наблюдается при талассемии, серповидноклеточной анемии);
- анемия Фанкони (развивается вследствие имеющегося дефекта в кластере белков, которые отвечают за восстановление ДНК);
- ферментативные дефекты в эритроцитах;
- дефекты цитоскелета (клеточный каркас, располагающийся в цитоплазме клетки) эритроцита;
- врожденная дизэритропоэтическая анемия (характеризуется нарушением образования эритроцитов);
- абеталипопротеинемия или синдром Бассена-Корнцвейга (характеризуется нехваткой бета-липопротеина в клетках кишечника, что ведет к нарушению всасываемости питательных веществ);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (вследствие нарушения клеточной мембраны эритроциты принимают шарообразную форму).
- дефицит железа;
- дефицит витамина B12;
- дефицит фолиевой кислоты;
- дефицит аскорбиновой кислоты (витамин С);
- голодание и недоедание.
Хронические заболевания и новообразования
- почечные заболевания (например, туберкулез печени, гломерулонефрит);
- заболевания печени (например, гепатит, цирроз);
- заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, атрофический гастрит, неспецифический язвенный колит, болезнь Крона);
- коллагеновые сосудистые болезни (например, системная красная волчанка, ревматоидный артрит);
- доброкачественные и злокачественные опухоли (например, миома матки, полипы в кишечнике, рак почек, легких, кишечника).
- вирусные заболевания (гепатит, инфекционный мононуклеоз, цитомегаловирус);
- бактериальные заболевания (туберкулез легких или почек, лептоспироз, обструктивный бронхит);
- протозойные заболевания (малярия, лейшманиоз, токсоплазмоз).
Ядохимикаты и медикаментозные средства
- неорганический мышьяк, бензол;
- радиация;
- цитостатики (химиотерапевтические препараты, используемые для лечения опухолевых заболеваний);
- антибиотики;
- нестероидные противовоспалительные средства;
- антитиреоидные препараты (снижают синтез гормонов щитовидной железы);
- противоэпилептические препараты.
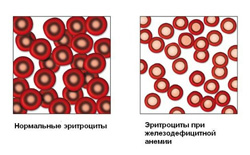
Для железодефицитной анемии характерно снижение эритроцитов, гемоглобина и цветового показателя.
Железо — это жизненно важный элемент, участвующий во многих метаболических процессах организма. У человека с весом семьдесят килограмм запас железа в организме составляет примерно четыре грамма. Данное количество поддерживается благодаря сохранению баланса между регулярными потерями железа из организма и его поступлением. Для поддержания равновесия суточная потребность железа составляет 20 – 25 мг. Большая часть поступающего железа в организм затрачивается на его нужды, остальное депонируется в виде ферритина или гемосидерина и при необходимости расходуется.
Нарушение поступления железа в организм
- вегетарианство вследствие неупотребления белков животного происхождения (мясо, рыба, яйца, молочные продукты);
- социально-экономическая составляющая (например, недостаточно денег для полноценного питания).
Нарушение усвоения железа
Всасывание железа происходит на уровне слизистых желудка, поэтому такие заболевания желудка как гастриты, язвенная болезнь или резекция желудка приводят к нарушению всасывания железа.
Повышенная потребность организма в железе
- беременность, в том числе многоплодная беременность;
- период лактации;
- подростковый возраст (за счет быстрого роста);
- хронические заболевания, сопровождающиеся гипоксией (например, хронический бронхит, пороки сердца);
- хронические нагноительные заболевания (например, хронические абсцессы, бронхоэктатическая болезнь, сепсис).
Потери железа из организма
- легочные кровотечения (например, при раке легких, туберкулезе);
- желудочно-кишечные кровотечения (например, язва желудка и двенадцатиперстной кишки, рак желудка, рак кишечника, варикозное расширение вен пищевода и прямой кишки, неспецифический язвенный колит, глистные инвазии);
- маточные кровотечения (например, преждевременная отслойка плаценты, разрыв матки, рак матки или шейки матки, прервавшаяся внематочная беременность, миома матки);
- почечные кровотечения (например, рак почек, туберкулез почек).
Питание при анемии
В питании железо делится на:
- гемовое, которое поступает в организм с продуктами животного происхождения;
- негемовое, которое поступает в организм с продуктами растительного происхождения.
Следует заметить, что гемовое железо усваивается в организме значительно лучше, нежели негемовое.
Количество железа на сто миллиграмм
Продукты питания
животного
происхождения
- печень;
- язык говяжий;
- мясо кролика;
- индюшатина;
- гусиное мясо;
- говядина;
- рыба.
- 9 мг;
- 5 мг;
- 4,4 мг;
- 4 мг;
- 3 мг;
- 2,8 мг;
- 2,3 мг.
Продукты питания растительного происхождения
- сушеные грибы;
- свежий горох;
- гречка;
- геркулес;
- свежие грибы;
- абрикосы;
- груша;
- яблоки;
- сливы;
- черешня;
- свекла.
- 35 мг;
- 11,5 мг;
- 7,8 мг;
- 7,8 мг;
- 5,2 мг;
- 4,1 мг;
- 2,3 мг;
- 2,2 мг;
- 2,1 мг;
- 1,8 мг;
- 1,4 мг.
При соблюдении диеты также следует увеличить потребление продуктов, содержащих витамин C, а также белок мяса (они повышают усвояемость железа в организме) и снизить потребление яиц, соли, кофеина и кальция (они уменьшают всасываемость железа).
Медикаментозное лечение
При лечении железодефицитной анемии больному параллельно с диетой назначается прием препаратов железа. Данные лекарственные средства предназначены для восполнения дефицита железа в организме. Они выпускаются в виде капсул, драже, инъекций, сиропов и таблеток.
Доза и длительность лечения подбирается индивидуально в зависимости от следующих показателей:
- возраста пациента;
- степени тяжести заболевания;
- причины, вызвавшей железодефицитную анемию;
- на основе результатов анализов.
Препараты железа принимаются за один час до еды или через два часа после приема пищи. Данные лекарственные средства нельзя запивать чаем или кофе, так как снижается всасываемость железа, поэтому их рекомендуется запивать водой или соком.
Принимать внутрь по одному грамму три – четыре раза в сутки.
Принимать по одной таблетке в день, с утра за тридцать минут до приема пищи.
Принимать по одной таблетке один – два раза в день.
Данные препараты рекомендуется назначать совместно с витамином C (по одной таблетке один раз в день), так как последний увеличивает всасываемость железа.
Препараты железа в виде инъекций (внутримышечных или внутривенных) применяются в следующих случаях:
- при тяжелой степени анемии;
- если анемия прогрессирует, несмотря на принимаемые дозы железа в виде таблеток, капсул или сиропа;
- если у больного имеются заболевания желудочно-кишечного тракта (например, язва желудка и двенадцатиперстной кишки, неспецифический язвенный колит, болезнь Крона), так как принимаемый препарат железа может усугубить имеющееся заболевание;
- перед оперативными вмешательствами с целью ускоренного насыщения организма железом;
- если у пациента имеется непереносимость препаратов железа при их приеме внутрь.
Хирургическое лечение
Хирургическое вмешательство производится при наличии у больного острого или хронического кровотечения. Так, например, при желудочно-кишечном кровотечении может применяться фиброгастродуоденоскопия или колоноскопия с выявлением области кровотечения и последующей его остановкой (например, удаляется кровоточащий полип, коагулируется язва желудка и двенадцатиперстной кишки). При маточных кровотечениях, а также при кровотечениях в органах, находящихся в брюшной полости, может применяться лапароскопия.
При необходимости больному может быть назначено переливание эритроцитарной массы для восполнения объема циркулирующей крови.

В норме витамин В12 поступает в организм с пищевыми продуктами. На уровне желудка В12 связывается с продуцируемым в нем белком, гастромукопротеидом (внутренний фактор Касла). Данный белок защищает поступивший в организм витамин от негативного воздействия микрофлоры кишечника, а также способствует его усвоению.
Комплекс гастромукопротеид и витамин В12 доходит до дистального отдела (нижний отдел) тонкого кишечника, где происходит распад этого комплекса, всасывание витамина В12 в слизистый слой кишечника и дальнейшее поступление его в кровь.
Из кровяного русла данный витамин поступает:
- в красный костный мозг для участия в синтезе эритроцитов;
- в печень, где происходит его депонирование;
- в центральную нервную систему для синтеза миелиновой оболочки (покрывает аксоны нейронов).
Клиническая картина В12 и фолиево-дефицитной анемии основывается на развитии у больного следующих синдромов:
- анемический синдром;
- желудочно-кишечный синдром;
- невралгический синдром.
| |
Данные симптомы развиваются вследствие атрофических изменений слизистого слоя ротовой полости, желудка и кишечника. |
|
- снижение уровня эритроцитов и гемоглобина;
- гиперхромия (выраженная окраска эритроцитов);
- макроцитоз (увеличенный размер эритроцитов);
- пойкилоцитоз (различная форма эритроцитов);
- при микроскопии эритроцитов выявляются кольца Кебота и тельца Жолли;
- ретикулоциты снижены или в норме;
- снижение уровня лейкоцитов (лейкопения);
- повышение уровня лимфоцитов (лимфоцитоз);
- снижение уровня тромбоцитов (тромбоцитопения).
В биохимическом анализе крови наблюдается гипербилирубинемия, а также снижение уровня витамина В12.
При пункции красного костного мозга выявляется повышение мегалобластов.
Больному могут быть назначены следующие инструментальные исследования:
- исследование желудка (фиброгастродуоденоскопия, биопсия);
- исследование кишечника (колоноскопия, ирригоскопия);
- ультразвуковое исследование печени.
Данные исследования помогают выявить атрофические изменения слизистой оболочки желудка и кишечника, а также обнаружить заболевания, которые привели к развитию В12-дефицитной анемии (например, злокачественные образования, цирроз печени).
Все больные госпитализируются в отделение гематологии, где проходят соответствующее лечение.
Питание при В12-дефицитной анемии
Назначается диетотерапия, при которой увеличивается потребление продуктов, богатых витамином В12.
Суточная норма витамина В12 составляет три микрограмма.
Количество витамина В12 на сто миллиграмм
Медикаментозное лечение
Медикаментозное лечение назначается больному по следующей схеме:
- В течение двух недель больной ежедневно получает по 1000 мкг Цианокобаламина внутримышечно. За две недели у пациента исчезает неврологическая симптоматика.
- В течение последующих четырех – восьми недель больной получает по 500 мкг ежедневно внутримышечно для насыщения депо витамина В12 в организме.
- Впоследствии больной пожизненно получает внутримышечные инъекции один раз в неделю по 500 мкг.
Во время лечения одновременно с Цианокобаламином больному могут назначить прием фолиевой кислоты.
Больной В12-дефицитной анемией должен пожизненно наблюдаться у гематолога, гастролога и семейного врача.
Фолиевая кислота (витамин B9) является водорастворимым витамином, который отчасти продуцируется клетками кишечника, но в основном должен поступать извне для восполнения необходимой для организма нормы. Суточная норма фолиевой кислоты составляет прием 200 – 400 мкг.
В пищевых продуктах, а также в клетках организма фолиевая кислота находится в форме фолатов (полиглутаматы).
Фолиевая кислота играет большую роль в организме человека:
- участвует в развитии организма во внутриутробном периоде (способствует формированию нервной проводимости тканей, кровеносной системы плода, предупреждает развитие некоторых пороков развития);
- участвует в росте ребенка (например, в первый год жизни, в период полового созревания);
- влияет на процессы кроветворения;
- совместно с витамином В12 участвует в синтезе ДНК;
- препятствует образованию тромбов в организме;
- улучшает процессы регенерации органов и тканей;
- участвует в обновлении тканей (например, кожи).
Абсорбция (всасывание) фолатов в организме осуществляется в двенадцатиперстной кишке и в верхнем отделе тонкого кишечника.
При фолиеводефицитной анемии у больного наблюдается анемический синдром (такие симптомы как повышенная утомляемость, сердцебиение, бледность кожных покровов, снижение работоспособности). Неврологический синдром, а также атрофические изменения слизистой оболочки ротовой полости, желудка и кишечника при данном виде анемии отсутствуют.
Также у больного может наблюдаться увеличение размеров селезенки.
При общем анализе крови наблюдаются следующие изменения:
- гиперхромия;
- снижение уровня эритроцитов и гемоглобина;
- макроцитоз;
- лейкопения;
- тромбоцитопения.
В результатах биохимического анализа крови наблюдается снижение уровня фолиевой кислоты (менее 3 мг/мл), а также повышение непрямого билирубина.
При проведении миелограммы выявляется повышенное содержание мегалобластов и гиперсегментированных нейтрофилов.
Питание при фолиеводефицитной анемии играет большую роль, больному необходимо ежедневно потреблять продукты, богатые фолиевой кислотой.
Следует заметить, что при любой кулинарной обработке продуктов фолаты разрушаются приблизительно на пятьдесят процентов и более. Поэтому для обеспечения организма необходимой суточной нормой продукты рекомендуется употреблять в свежем виде (овощи и фрукты).
| Продукты питания | Наименование продуктов | Количество железа на сто миллиграмм |
| Продукты питания животного происхождения |
|
|
| Продукты питания растительного происхождения |
|
|
Медикаментозное лечение фолиеводефицитной анемии включает прием фолиевой кислоты в количестве от пяти до пятнадцати миллиграмм в сутки. Необходимую дозировку устанавливает лечащий врач в зависимости от возраста пациента, тяжести течения анемии и результатов исследований.
Профилактическая доза включает прием одного – пяти миллиграмм витамина в сутки.
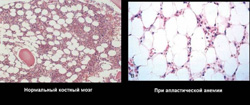
Апластическая анемия может быть врожденной или приобретенной.
Клинические проявления апластической анемии зависят от степени выраженности панцитопении.
При апластической анемии у больного наблюдаются следующие симптомы:
- бледность кожных покровов и слизистых;
- головная боль;
- учащенное сердцебиение;
- одышка;
- повышенная усталость;
- отеки на ногах;
- десневые кровотечения (вследствие снижения уровня тромбоцитов в крови);
- петехиальная сыпь (красные пятна на коже маленьких размеров), синяки на коже;
- острые или хронические инфекции (вследствие снижения уровня лейкоцитов в крови);
- изъязвления орофарингеальной зоны (поражается слизистая полости рта, язык, щеки, десна и глотка);
- желтушность кожных покровов (симптом поражения печени).
При биохимическом анализе крови наблюдается:
- повышение сывороточного железа;
- насыщение трансферрина (белок, переносящий железо) железом на 100%;
- повышение билирубина;
- повышение лактатдегидрогеназы.
При пункции красного мозга и последующем гистологическом исследовании выявляются:
- недоразвитие всех ростков (эритроцитарный, гранулоцитарный, лимфоцитарный, моноцитарный и макрофагальный);
- замещение костного мозга жировым (желтый костный мозг).
Среди инструментальных методов исследований больному может быть назначено:
- ультразвуковое исследование паренхиматозных органов;
- электрокардиография (ЭКГ) и эхокардиография;
- фиброгастродуоденоскопия;
- колоноскопия;
- компьютерная томография.
При правильно подобранном поддерживающем лечении состояние пациентов с апластической анемией существенно улучшается.
При лечении апластической анемии больному назначаются:
- иммунодепрессивные препараты (например, Циклоспорин, Метотрексат);
- глюкокортикостероиды (например, Метилпреднизолон);
- антилимфоцитарный и антитромбоцитарный иммуноглобулины;
- антиметаболиты (например, Флударабин);
- эритропоэтин (стимулирует образование эритроцитов и стволовых клеток).
Немедикаментозное лечение включает:
- трансплантацию костного мозга (от совместимого донора);
- переливание компонентов крови (эритроциты, тромбоциты);
- плазмаферез (механическое очищение крови);
- соблюдение правил асептики и антисептики с целью предотвращения развития инфекции.
Также при тяжелом течении апластической анемии больному может понадобиться хирургическое лечение, при котором производится удаление селезенки (спленэктомия).
В зависимости от эффективности проводимого лечения у больного при апластической анемии может наблюдаться:
- полная ремиссия (затухание или полное исчезновение симптомов);
- частичная ремиссия;
- клиническое улучшение;
- отсутствие эффекта от лечения.
|
|
|
|

Гемолитическая анемия может развиться вследствие наследственных или приобретенных заболеваний.
По локализации гемолиз может быть:
- внутриклеточным (например, аутоиммунная гемолитическая анемия);
- внутрисосудистым (например, переливание несовместимой крови, диссеминированное внутрисосудистое свертывание).
У пациентов с легкой степенью гемолиза уровень гемоглобина может быть нормальным, если производство эритроцитов соответствует темпу их разрушения.
Преждевременное разрушение эритроцита может быть связано со следующими причинами:
- внутренними мембранными дефектами эритроцитов;
- дефектами структуры и синтеза белка гемоглобина;
- ферментативными дефектами в эритроците;
- гиперспленомегалией (увеличение размеров печени и селезенки).
Наследственные заболевания могут вызвать гемолиз в результате отклонений мембраны эритроцита, ферментативных дефектов и отклонений гемоглобина.
Существуют следующие наследственные гемолитические анемии:
- энзимопатии (анемии, при которых наблюдается недостаток фермента, дефицит глюкозо-6-фосфатдегидрогеназы);
- наследственный сфероцитоз или болезнь Минковского-Шоффара (эритроциты неправильной шарообразной формы);
- талассемия (нарушение синтеза полипептидных цепей, входящих в строение нормального гемоглобина);
- серповидно-клеточная анемия (изменение строения гемоглобина приводит к тому, что эритроциты принимают серпообразную форму).
Приобретенные причины гемолитической анемии включают иммунные и не иммунные нарушения.
Иммунные нарушения характеризуются аутоиммунной гемолитической анемией.
Не иммунные нарушения могут быть вызваны:
- ядохимикатами (например, пестициды, бензол);
- лекарственными средствами (например, противовирусные препараты, антибиотики);
- физическим повреждением;
- инфекциями (например, малярия).
Гемолитическая микроангиопатическая анемия приводит к производству фрагментированных эритроцитов и может быть вызвана:
- дефектным искусственным сердечным клапаном;
- диссеминированным внутрисосудистым свертыванием;
- гемолитическим уремическим синдромом;
- тромбоцитопенической пурпурой.
Симптомы и проявления гемолитической анемии разнообразны и зависят от вида анемии, степени компенсации, а также от того, какое лечение получал больной.
Следует заметить, что гемолитическая анемия может протекать бессимптомно, а гемолиз выявляться случайно во время обычного лабораторного тестирования.
При гемолитической анемии могут наблюдаться следующие симптомы:
- бледность кожи и слизистых;
- ломкость ногтей;
- тахикардия;
- учащение дыхательных движений;
- снижение артериального давления;
- желтушность кожных покровов (из-за увеличения уровня билирубина);
- на ногах могут наблюдаться язвы;
- гиперпигментация кожи;
- желудочно-кишечные проявления (например, боль в животе, нарушение стула, тошнота).
Следует заметить, что при внутрисосудистом гемолизе у больного наблюдается дефицит железа из-за хронической гемоглобинурии (наличие гемоглобина в моче). Вследствие кислородного голодания нарушается сердечная функция, что приводит к развитию у пациента таких симптомов как слабость, тахикардия, одышка и стенокардия (при тяжелой форме анемии). Из-за гемоглобинурии у больного также наблюдается потемнение мочи.
Длительный гемолиз может привести к развитию желчных камней вследствие нарушения обмена билирубина. При этом пациенты могут жаловаться на боль в животе и бронзовый цвет кожи.
В общем анализе крови наблюдается:
- снижение уровня гемоглобина;
- снижение уровня эритроцитов;
- увеличение ретикулоцитов.
При микроскопии эритроцитов выявляется их серпообразная форма, а также кольца Кебота и тельца Жолли.
В биохимическом анализе крови наблюдается повышение уровня билирубина, а также гемоглобинемия (увеличение свободного гемоглобина в плазме крови).
Также необходимо сдать анализ мочи на выявление наличия гемоглобинурии.
При пункции костного мозга наблюдается выраженная гиперплазия эритроцитарного ростка.
Существует много видов гемолитической анемии, поэтому лечение может отличаться в зависимости от причины, вызвавшей анемию, а также от типа гемолиза.
При лечении гемолитической анемии больному могут назначаться следующие препараты:
- Фолиевая кислота. Профилактическая доза фолиевой кислоты назначается, потому что активный гемолиз может потреблять фолат и впоследствии привести к развитию мегалобластоза.
- Глюкокортикостероиды (например, Преднизолон) и иммунодепрессанты (например, Циклофосфан). Данные группы препаратов назначаются при аутоиммунной гемолитической анемии.
- Переливание эритроцитарной массы. Больному индивидуально подбираются отмытые эритроциты, так как существует высокий риск разрушения перелитой крови.
Спленэктомия
Спленэктомия может быть первоначальным вариантом в лечении некоторых типов гемолитической анемии, таких как, например, наследственный сфероцитоз. В других случаях, например, при аутоиммунной гемолитической анемии, спленэктомия рекомендуется тогда, когда другие методы лечения потерпели неудачу.
Терапия препаратами железа
При гемолитической анемии применение препаратов железа в большинстве случаев противопоказано. Это связано с тем, что уровень железа при данной анемии не снижается. Однако если у больного наблюдается постоянная гемоглобинурия, то происходит существенная потеря железа из организма. Поэтому при выявлении дефицита железа пациенту может быть назначено соответствующее лечение.
Проявления анемии будут зависеть от следующих факторов:
- какое количество крови было потеряно;
- с какой скоростью происходит кровопотеря.
Симптомами постгеморрагической анемии являются:
- слабость;
- головокружение;
- бледность кожных покровов;
- сердцебиение;
- одышка;
- тошнота, рвота;
- сечение волос и ломкость ногтей;
- шум в ушах;
- мелькание мушек перед глазами;
- жажда.
При острой кровопотере у больного может развиться геморрагический шок.
Выделяют четыре степени геморрагического шока.
источник