О том, что это такое – пернициозная анемия, большинство больных узнает в кабинет врача после сдачи анализов крови. В обычной жизни с этим термином люди, как правило, не сталкиваются. Пернициозная анемия – это заболевание, которое характеризуется нарушением кроветворения на фоне снижения в организме витамина В12. Также пернициозную анемию называют В12-дефицитной анемией или болезнью Аддисона-Бирмера.
По МКБ10 пернициозной анемии присвоен код D51.0, а по МКБ 9 – код 281.0.
На фоне снижения уровня витамина В12 в организме, костный мозг заменяет нормальные клетки-предшественники эритроцитов клетками очень больших размеров (мегалобласты). Они не имеют возможности дальнейшего перерождения в эритроциты, что приводит к снижению их численности. Если вовремя не начать лечение, то у человека разовьется анемия и начнется процесс дегенерации нервной ткани.
Впервые мир узнал о пернициозной анемии в 1855 году благодаря трудам ученого Аддисона. Он называл это заболевание идиопатической анемией, то есть анемией неясного генеза.
Более подробно описал данное нарушение ученый по фамилии Бример, что произошло в 1868 году. Именно он дал заболеванию название, которое дошло в неизменном виде до наших времен. Пернициозная анемия означает злокачественная анемия.
На протяжении долгого времени эта болезнь считалась неизлечимой. Однако в 1926 году ученые Майнот и Мерфи установили, что от пернициозной анемии можно избавиться, для чего нужно употреблять в пищу сырую печень. В то время этот инновационный способ лечения так и называли печеночной терапией.
Следующим ученым, который продолжил изучать проблему пернициозной анемии, является У. Б. Касл. Основываясь на научных трудах своих предшественников, он установил, что кроме соляной кислоты и пепсина, организм человека вырабатывает еще один внутренний фактор, содержащий мукоиды и пептиды. Производится это вещество в слизистой оболочке желудка. Именно этот внутренний фактор соединяется с витамином В12, поступающим извне в нестабильный, но подвижный комплекс. Он проникает в плазменную часть крови, по ней поступает в печень и оседает в ней в виде белково-В12-витаминного комплекса. Именно это соединение принимает активное участие в процессе кроветворения. Каслу удалось определить, что у людей, которые страдают от В12-дефицитной анемии, отсутствует именно третий внутренний фактор (фактор Касла), который продуцируется в слизистой оболочке желудка. Однако на то время, ученому не удалось установить, что внешним фактором является именно витамин В12.
Об этом стало известно только в 1948 году благодаря ученым Риксу и Смиту.
Нельзя назвать В12-дефицитную анемию заболеванием редким. Оно диагностируется у каждого 110-180 человека из 100 000 людей. Больше всего людей с В12-дефицитной анемией проживает в Скандинавии и в Великобритании. Причем преимущественно – это пациенты достаточно зрелого возраста. Однако, если в семье прослеживается отягощенный анамнез, то развиваться пернициозная анемия может и в молодом возрасте. Женщины от В12-дефицитной анемии страдают чаще мужчин. На 10 заболевших женщин приходится 7 представителей мужского пола.
Пернициозная анемия может иметь три степени тяжести:
При снижении уровня гемоглобина в крови до 90-110 г/л анемия считается легкой.
При падении уровня гемоглобина в крови до 70-90 г/л говорят об анемии средней степени тяжести.
Если уровень гемоглобина падает ниже отметки в 70 г/л, то анемия имеет тяжелое течение.
В зависимости от того, что послужило причиной развития пернициозной анемии, различают следующие ее формы:
Алиментарная (нутритиновая) анемия, которая чаще всего диагностируется у детей в раннем возрасте. Однако может наблюдаться данное нарушение и у взрослых людей, которые преднамеренно ограничивают свой рацион в продуктах животного происхождения. Также в группе риска находятся недоношенные дети, дети, находящиеся на искусственном вскармливании и дети, питающиеся козьим молоком.
Классическая пернициозная анемия, которая развивается на фоне атрофических процессов в слизистой оболочке желудка. Это приводит к тому, что клетки органа не в состоянии вырабатывать внутренний фактор.
Ювенильная пернициозная анемия, которая манифестирует при функциональной недостаточности фундальных желез. Они становятся не в состоянии вырабатывать гландулярный мукопротеин. При этом слизистая оболочка желудка работает как положено. Если начать лечение ювенильной анемии, то можно добиться полного выздоровления.
Также различают семейную пернициозную анемию (болезнь Ольги Имерслунд). Она развивается при нарушении транспортировки и всасывания витамина В12 в кишечнике. Ярким диагностическим признаком такого нарушения будет появление в моче белка.
Причины, которые способны приводить к развитию пернициозной анемии могут быть следующими:
Атрофический фундальный гастрит, резекция желудка и кишечника, экзокринная недостаточность поджелудочной железы, нарушение микрофлоры кишечника, болезнь Крона, гастринома – все эти заболевания приводят к тому, что витамин В12 не в состоянии нормально всасываться в кровь. В результате у человека развивается пернициозная анемия.
Погрешности в питании, связанные с недостаточным употреблением мясных продуктов, яиц, кисломолочных напитков также являются частой причиной развития пернициозной анемии. В группе риска находятся вегетарианцы и люди, придерживающиеся строгих диет.
Заражение лентецом. Этот паразит селится в тонком кишечнике человека и потребляет значительные объемы витамина В12 для удовлетворения собственных нужд. Заболевание, которое вызывает этот ленточный червь, носит название дифиллоботриоз. Заразиться паразитом можно при употреблении в пищу свежей рыбы. Чаще всего встречается дифиллоботриоз в северных странах. Также спровоцировать развитие пернициозной анемии могут патогенные бактерии, которые проникают в тонкий кишечник, либо начинают там размножаться при появлении в нем фистул и дивертикул.
Сбои в транспортировке витамина В12. Подобное нарушение носит врожденный характер, при котором в организме отсутствует транспортный белок транскобаламин II, он отвечает за связывание и транспортировку в витамина В12. Еще одно врожденное заболевание, которое приводит к развитию пернициозной анемии – это синдром Имерслунд-Гресбека.
Частой причиной развития В12-дефицитоной анемии выступают аутоиммунные заболевания. У 90% больных удается обнаружить в крови аутоантитела, которые атакуют клетки желудка, ответственные за выработку соляной кислоты и внутренний фактор Касла. Хотя подобные антитела могут быть выявлены и у здоровых людей в 5-10% случае. У 60% пациентов с пернициозной анемией обнаруживаются аутоантитела к самому внутреннему фактору Касла.
Ежедневно человек должен получать с продуктами питания 6-9 мкг витамина В12. Около 2-5 мкг этого вещества выводится из организма, а 4 мкг в нем задерживаются, откладываясь про запас. Депо организма содержит достаточное количество витамина В12, для того, чтобы обеспечивать им потребности человека на протяжении нескольких лет (при условии, что извне он перестанет поступать).
В организме витамин В12 присутствует в форме метилкобаламина (отвечает за нормальную продукцию эритроцитов) и 5-дезоксиаденозилкобаламина (принимает участие в обменных процессах в ЦНС и в периферической нервной системе).
Если в организме снижается уровень метилкобаламина, то у больного развивается мегалобластный тип кроветворения. Это неполноценные эритроциты, которые не в состоянии транспортировать кислород и очень быстро разрушаются. Как итог, у человека развивается анемия со всеми ее негативными последствиями.
Если в организме не хватает 5-дезоксиаденозилкобаламина, то происходит сбой в обмене жирных кислот. В нем начинают скапливаться вредные кислоты (метилмалоновая и пропионовая). Они обладают разрушительным воздействием на нейроны головного и спинного мозга, не дают вырабатываться миелину, которые покрывает нервные стволы. Поэтому при пернициозной анемии страдает нервная система человека.
Симптомы, которые характеризуют пернициозную анемию:
Анемический синдром: усиление слабости и утомляемости, отсутствие возможности выполнять прежние объемы работы. У больного повышается температура тела до отметки в 37-37,5 градусов, часто возникают головокружения, могут случаться обмороки. Усиливается одышка, возникает она даже в состоянии покоя. Появляется шум в ушах, перед глазами могут периодически «летать мушки». Кожные покровы приобретают неестественную бледность, могут отдавать некоторой желтизной. Лицо слегка отекает. При выслушивании тонов сердца, можно обнаружить систолические шумы. Если анемия прогрессирует, то это сопряжено с риском развития миокардиодистрофии и сердечной недостаточности.
Гастроэнтерологический синдром – это тошнота, запоры, рвота, отсутствие желания употреблять пищу, похудание. Язык больного воспаляется, начинает болеть, становится яркого малинового цвета, его поверхность блестит, будто отполированная (гунтеровский глоссит). В уголках рта формируются «заеды». Если выполнить ФГДС, то можно обнаружить атрофию слизистой оболочки желудка.
Неврологический синдром: мышечная слабость, изменение походки, онемение конечностей. Судороги и отсутствие чувствительности наблюдается при поражении спинного и головного мозга. Сухожильные рефлексы усиливаются, положительным становится симптом Ромберга и рефлекс Бабинского. Развиваются признаки, характерные для фуникулярного миелоза.
Кроме того, человек становится нервным, все время находится в апатии. Также страдает мочеполовая система с развитием импотенции и недержанием мочи. В тяжелых случаях могут возникать галлюцинации, ухудшаться цветовое восприятие (желтый и синий цвет).
Основные диагностические мероприятия:
Опрос пациента, сбор анамнеза, в том числе, изучение семейной истории болезни.
Физикальный осмотр с оценкой кожных покровов, прослушиванием пульса, измерением артериального давления и осмотром ротовой полости для выявления глоссита.
Назначение лабораторных тестов.
К методам лабораторной диагностики относят:
Забор крови на общий анализ. При анемии будет обнаружено снижение уровня эритроцитов, их увеличение в размерах, снижение количества ретикулоцитов, гемоглобина, тромбоцитов (тромбоциты становятся больше в диаметре). Данные цветового показателя крови при пернициозной анемии превышают значения в 1,05, при норме 0,86-1,05.
Забор мочи на анализ, что дает сведения о сопутствующих заболеваниях. Также это исследование дает некоторую информацию о наследственных формах пернициозной анемии.
Забор крови на биохимический анализ. На анемию будет указывать снижение уровня витамина В12, повышение уровня билирубина (продукт распада эритроцитов) и железа (оно остается невостребованным). Также можно отметить увеличение уровня фермента под названием лактат-дегидрогеназа, который отвечает за ускорение химических реакций в организме.
В ряде случаев для уточнения диагноза, выполняют пункцию костного мозга. На пернициозную анемию будет указывать мегалобластический тип кроветворения и быстрая выработка эритроцитов.
К вспомогательным диагностическим методикам относят:
ЭКГ. Это исследование дает информацию о ЧСС и нарушениях сердечного ритма.
ФГДС. Осмотр слизистой оболочки кишечника и желудка с помощью эндоскопа позволяет обнаружить на них патологические изменения.
Рентген желудка, ультразвуковое обследование внутренних органов.
Неврологический осмотр, прохождение МРТ.
Тест Шиллинга позволяет определить, всасывается ли витамин В12 в организме. Для этого пациенту предлагают выпить радиоактивный раствор витамина В12, а спустя некоторое время ему предлагают внушительную дозу обычного витамина В12. После этого собирают мочу на анализ и подсчитывают, какое количество меченого витамина за сутки было выведено организмом. Если его почками выводится мало, то значит в кишечнике он всасывает в недостаточном количестве.
Терапия заболевания должна основываться на причинах, которые спровоцировали его развитие.
Для лечения могут быть использованы следующие препараты:
Витамин В12 для восполнения его дефицита в организме. Подкожно вводят препарат 1 раз в сутки в дозировке 200-500 мкг. Курс длится 1-1,5 месяцев. Затем на протяжении 3 месяцев препарат вводят 1 раз в 7 дней. Затем еще на протяжении 6 месяцев его вводят в установленной дозировке 2 раза в 30 дней. Ожидать результатов можно спустя 2 месяца от начала лечения, хотя это во многом зависит от индивидуальных особенностей организма.
Празиквантел для избавления от паразитарной инфекции.
Глюкокортикостероиды для подавления аутоиммунной реакции.
Патогенетическое лечение заболеваний органов пищеварения.
Обязательно нужно назначить пациенту лечебную диету с включением в меню кисломолочных продуктов, красного мяса, печени, яиц и морепродуктов.
При тяжелом течении анемии возможно переливание эритроцитарной массы.
Меры профилактики пернициозной анемии:
Рацион человека должен быть сбалансированным.
Все болезни, которые способствуют развитию анемии, должны быть своевременно пролечены.
Если человек перенес резекцию желудка или кишечника, то ему нужно пожизненно принимать витамин В12 в поддерживающей дозировке.
Автор статьи: Шутов Максим Евгеньевич | Врач-гематолог
Образование: В 2013 году закончен Курский государственный медицинский университет и получен диплом «Лечебное дело». Спустя 2 года окончена ординатура по специальности «Онкология». В 2016 году пройдена аспирантура в Национальном медико-хирургическом центре имени Н. И. Пирогова.
Как быстро и просто понизить артериальное давление?
7 тревожных симптомов боли в животе
Анемия – это низкое содержание в крови функционально полноценных красных клеток (эритроцитов), такое состояние ещё называют низким гемоглобином (читайте подробнее в статье: причины и симптомы низкого гемоглобина). Анемия может развиться у человека, который страдает множеством других болезней.
Чтобы установить диагноз анемия, необходимо сдать кровь на анализ. Это исследование позволит не только определить, что у человека развивается анемия, но и уточнить тип нарушения, а также степень его тяжести. Благодаря лабораторным исследованиям можно установить даже незначительные отклонения от нормы.
При анемии назначают препараты железа, которые позволяют перекрыть нехватку этого микроэлемента в организме. В результате, гемоглобин повышается до нормальных значений. Препараты для лечения железодефицитной анемии может назначить только доктор.
Анемия является распространенным нарушением, которое обнаруживают у каждого 7 жителя России. При этом многие люди даже не подозревают о том, что в их крови снижен уровень гемоглобина и эритроцитов. Анемия, зачастую, дает о себе знать такими симптомами, как повышенная утомляемость и усталость.
Анемия, или как ее называют в народе, «малокровие» — это состояние, характеризующееся снижением уровня гемоглобина и/или эритроцитов в крови. Большинство пациентов, узнав о своем диагнозе, задаются вопросом о том, как лечить анемию в домашних условиях. Именно об этом пойдет речь в статье.
источник
Анемия — это заболевание, характеризующееся понижением концентрации гемоглобина в крови. Сегодня поговорим о пернициозной анемии, также кратко рассмотрим и другие виды анемии (классификации и степени тяжести).
Анемия пернициозная — это серьезная патология, развивающаяся вследствие дефицита в организме витамина В12. Данное заболевание имеет несколько названий: злокачественное малокровие, болезнь Аддисона-Бирмера, мегалобластная анемия, В12-дефицитная анемия.
В 1855 году английский доктор Томас Аддисон впервые описал данную болезнь. В 1872 году немецкий врач Антон Бирмер изучил недуг более подробно. Именно он назвал заболевание пернициозной, или злокачественной анемией. Однако в то время не было известно, какое необходимо лечение для анемии данного типа. И только лишь в 1926 году группой врачей было установлено, что признаки недуга полностью исчезают после введения в рацион больного сырой печени. Эти же специалисты доказали, что в основе такой болезни лежит состояние, при котором желудок по причине врожденной патологии не способен секретировать особое вещество (фактор Кастла), помогающее всасывать в кишечнике витамин В12. За данное открытие ученые были удостоены Нобелевской премии.
Какие бывают виды анемии? Данный недуг развивается по различным причинам, различна может быть и история болезни. Анемия подразделяется на следующие виды:
Постгеморрагическая — заболевание развивается на фоне острой или хронической кровопотери (ранение, кровотечение).
Гемолитическая — возникновение патологии связано с усиленным разрушением эритроцитов.
Дефицитная — развивается болезнь вследствие недостатка необходимых для кроветворения веществ (железа, витаминов и других микроэлементов).
Гипопластическая — наиболее тяжелый вид анемии, возникает данное состояние в результате нарушения кроветворения в костном мозгу.
Помимо вышеописанной классификации, врачи-клиницисты различают заболевание и по степени тяжести. Данный показатель зависит от концентрации гемоглобина. Заболевание анемия степени тяжести имеет следующие:
легкая — содержание гемоглобина в 1-м литре крови составляет 100-120 г для мужчин и 90-110 г/л для женщин;
средняя — количество гемоглобина для мужчин составляет 80-100 г/л, для женщин — 70-90 г/л;
тяжелая — уровень гемоглобина опускается ниже вышеуказанных границ.
Перед тем как ответить на вопрос: «Как лечить анемию пернициозную?», необходимо выяснить, что способствовало его возникновению. Данный недуг может развиться по различным причинам. Как уже говорилось выше, основной из них является недостаточное содержание витамина В12 в организме. Также пернициозная анемия может развиться в результате:
длительного применения лекарств, которые способствуют снижению кислотности желудка;
аутоиммунного поражения внутреннего фактора Кастла;
заражения ленточными червями;
токсического воздействия медикаментов и химических веществ на стенки желудка;
Как проявляется пернициозная анемия? Симптомы могут быть и явными, и косвенными. К явным признакам болезни Аддисона-Бирмера относятся:
ярко-красный (алый) язык, который из-за деформации рецепторов становится «лакированным»;
нарушение функций нервной системы;
желудочная ахилия — состояние, при котором в желудочном соке отсутствует соляная кислота и ферменты;
наличие патологических эритроцитов, малокровие;
образование в костном мозге неестественно крупных клеток (мегалобластов) вместо эритроцитов.
Косвенными симптомами недуга выступают:
слабость, сонливость, снижение жизненного тонуса;
болезненные ощущения во рту и на языке;
снижение веса, потеря аппетита.
Данные признаки патологии развиваются наиболее часто. В редких случаях пернициозная анемия может проявляться:
Заболевание может развиться у беременных женщин. Пернициозная анемия возникает в результате недостаточного поступления в организм будущей матери фолиевой кислоты и цианокобаламина. При этом в крови происходит снижение уровня эритроцитов, а вот гемоглобин остается в норме или повышается. Недуг развивается достаточно медленно, и, чтобы поставить диагноз «анемия пернициозная» на ранней стадии, необходимо провести клиническое исследование крови. Поэтому своевременное проведение всех анализов, назначенных врачом, крайне важно. Проявляется недуг бледностью кожи, слабостью, повышенной утомляемостью, позже присоединяются расстройства пищеварения. Крайне редко наблюдается поражение нервной системы, может наблюдаться незначительное снижение чувствительности в конечностях.
При беременности пернициозная анемия обязательно должна быть вылечена, так как в большинстве случаев патология может спровоцировать отслойку плаценты, риск преждевременных родов и рождение мертвого ребенка.
Лечение заболевания проводят по общей схеме.
Чаще всего данный недуг развивается у детей, имеющих наследственные патологии пищеварительной системы, вследствие которых нарушено всасывание витамина В12. В редких случаях у ребенка пернициозная анемия может возникнуть при грудном вскармливании матерью-вегетарианкой. Анализ крови дает возможность поставить правильный диагноз уже на третьем месяце жизни, симптомы патологии начинают проявляться только по достижении ребенком 3-х-летнего возраста. При осмотре врач может обнаружить сухость и шелушение кожных покровов, глоссит, увеличение селезенки. Наблюдается расстройство пищеварения, снижается аппетит. В особо тяжелых случаях ребенок может отставать в развитии.
Наиболее явное проявление патологии наблюдается в составе крови. Как правило, у всех больных в сыворотке обнаруживается низкая концентрация витамина В12. Для всасывания витамина требуется дополнительное введение внутреннего фактора. Также проводят исследование мочи, так как сравнительный анализ состава мочи и крови дает возможность поставить диагноз более точно.
Очень важно обнаружить первопричину заболевания. Специалисты проводят исследование желудочно-кишечного тракта для возможного обнаружения гастритов, язв и других патологий, вследствие которых могло быть нарушено усваивание витамина В12.
Если диагностирована пернициозная анемия, лечение проводят при помощи введения таких медикаментов, как средства «Оксикобаламин» или «Цианокобаламин». Препараты вводят методом инъекций. Прежде всего, необходимо концентрацию витамина В12 довести до нормальных значений, позже количество инъекций сокращают, и введенное лекарство оказывает только поддерживающий эффект. После проведенной терапии больным придется постоянно следить за уровнем витамина и периодически проходить профилактический курс инъекций препарата.
В некоторых случаях в ходе лечения у больных может наблюдаться снижение концентрации железа в организме. Происходит это, как правило, по прошествии 3-6 месяцев лечения. В такой ситуации требуется дополнительное введение медикаментов, восстанавливающих уровень железа.
При успешной терапии все проявления недуга постепенно исчезают. Длительность восстановительного периода может составлять 6 месяцев. Содержание витамина В12 нормализуется спустя 35-70 дней после начала лечебных мероприятий.
В процессе лечения устраняется невропатия, у всех пациентов исчезает недержание мочи и другие признаки. Зрение, которое было нарушено в результате атрофии зрительного нерва, к сожалению, не восстанавливается. Но если нарушение зрения возникло вследствие кровоизлияний желтого пятна, то восстановление происходит достаточно быстро.
Следует иметь в виду, что в некоторых случаях после лечения могут развиваться такие серьезные заболевания, как токсический зоб, микседема, рак желудка. Однако случается это достаточно редко (не более, чем в 5% случаев).
Как лечить анемию пернициозную, мы выяснили, но не следует забывать и о сбалансированном питании. Ежедневный рацион должен содержать достаточное количество витаминов и белков. Обязательно следует регулярно употреблять говядину, мясо кролика, морепродукты, яйца, кисломолочные продукты, бобовые. Количество жиров в рационе рекомендуется ограничить, так как они притормаживают процессы кроветворения в костном мозге. Также следует отказаться от курения и употребления алкогольных напитков. Для успешного лечения крайне важны положительные эмоции и поддержка родных и близких. Относитесь внимательно к своему организму, регулярно сдавайте анализы и незамедлительно реагируйте на малейшие изменения в состоянии здоровья.
источник
ПЕРНИЦИОЗНАЯ АНЕМИЯ (anaemia perniciosa; лат. perniciosa гибельная, губительная; анемия; син.: злокачественная анемия, болезнь Аддисона — Бирмера, B12-дефицитная анемия, мегалобластная анемия) — тяжелая прогрессирующая анемия, возникающая при нарушении усвоения витамина B12, поступающего с пищей, вследствие пониженной (или при отсутствии) секреции внутреннего желудочного фактора.
Первое описание П. а. под названием «тяжелое первичное малокровие» принадлежит Кумбу (J. S. Combe, 1822). Т. Аддисон в 1855 г. описал болезнь под названием «идиопатическая анемия», а А. Бирмер (см.) в 1872 г. — группу больных, страдавших «прогрессирующей пернициозной анемией».
Возможность излечения П. а. путем назначения особой диеты (сырой печени) установлена Дж. Майнотом и У. Мерфи в 1926 г.; открытие в 1929 г. У. Каслом внутреннего желудочного фактора (см. Касла факторы) и в 1948 г. Смитом (E. L. Smith) и Риккесом (E. L. Rickes) «антипернициозного» витамина B12 — цианокобаламина (см.) способствовало выявлению патогенеза П. а. и его успешному лечению.
П. а. встречается гл. обр. у лиц старше 40 лет; чаще болеют мужчины. Известны редкие случаи заболевания детей на почве однообразного вскармливания козьим молоком или сухими молочными смесями. Заболеваемость П. а., по данным разных исследователей, составляет от 20 до 60 на 10 000 населения.
В классификации анемий (см.) выделяют B12— (фолиево) дефицитные анемии. В действительности комбинированный дефицит витамина B12 и фолиевой к-ты встречается редко, чаще наблюдается изолированный дефицит витамина B12 и реже — дефицит фолиевой к-ты.
Ведущим фактором в этиологии П. а. является эндогенная недостаточность витамина B12, возникающая вследствие нарушения его всасывания в результате снижения или полного прекращения секреции внутреннего желудочного фактора (гастромукопротеи-на), необходимого для связывания и последующей абсорбции витамина B12. П. а. может возникнуть в результате поражения жел.-киш. тракта, напр, воспалительным или злокачественным процессом, а также после субтотального или тотального удаления желудка и после обширной резекции части тонкого кишечника. В редких случаях П. а. развивается при нормальной секреции внутреннего желудочного фактора и обусловлена врожденным отсутствием транскобаламина II (белка плазмы крови), с которым витамин B12 связывается и доставляется в печень и красный костный мозг, или отсутствием в кишечнике белкового акцептора витамина B12, необходимого для поступления витамина B12 из кишечника в кровеносное русло. На роль генетического фактора указывают случаи семейных заболеваний, а также возникновение П. а. на почве врожденного нарушения секреции внутреннего желудочного фактора, наследуемого по аутосомно-рецессивному типу. Об участии иммунных механизмов при П. а. свидетельствует наличие в сыворотке крови у большинства больных П. а. и их родственников антител, направленных против париетальных гландулоцитов желудка, а также антител (IgG) против внутреннего желудочного фактора, к-рые определяются как в париетальных гландулоцитах (при гастробиопсии), так и в цитоплазме плазматических клеток красного костного мозга авторадиографией (см.). О существовании аутоиммунных процессов говорят случаи сочетания П. а. с тиреоидитом Хасимото (см. Хасимото болезнь), при этом одновременно присутствуют антитиреоидные антитела и антитела к париетальным гландулоцитам желудка. Аутоиммунный генез П. а. подтверждает успешное применение кортикостероидов. В ряде случаев П. а. возникает без участия специфических антител.
Нарушение кроветворения (см.) характеризуется мегалобластозом красного костного мозга с поражением всех трех ростков кроветворения — эритроидного, гранулоцитарного и мегакариоцитарного. Особенностью мегалобластического эритроцитопоэза является его неэффективность, обусловленная резким нарушением процессов дифференциации эритроидных клеток, в результате которого в красном костном мозге происходит накопление аномальных эритроидных клеток — промегалобластов и мегалобластов. Мегалобластический эритроцитопоэз обусловлен резким снижением активности В ^-зависимых энзимов, участвующих в метаболизме фолатов (солей фолиевой к-ты), необходимых для синтеза ДНК; в частности, снижение активности метилтрансферазы сопровождается кумуляцией в клетках неактивного метилтетрагидрофолата и снижением синтеза ДНК, что приводит к нарушению клеточного деления и развитию мегалобластоза.
Повышенная «интрамедуллярная смертность» мегалобластов, выявляемая при биопсии костного мозга в виде интенсивного эритрофагоцитоза и гемосидероза (см.), ведет к резкому снижению продукции эритроцитов, т. е. к анемии. В то же время в результате повышенного распада гемоглобинизированных мегалобластов (полихроматофильных и оксифильных) возникают симптомы гемолитической анемии (см.) — не-конъюгированная гипербилирубинемия, плейохромия (увеличенное содержание пигментов) желчи, уробилинурия, повышенное выделение стеркобилина с калом. Не исключена возможность участия антител в костномозговом разрушении эрит-рокариоцитов.
Смертельные случаи в связи с успешным лечением П. а. встречаются крайне редко. При вскрытии умерших в остром периоде болезни выявляется общее малокровие, желтушность кожи, серозных и слизистых оболочек, жировая дистрофия миокарда, печени, почек. Кровь в сердце и крупных сосудах жидкая, водянистая. Вследствие выраженной гиперплазии кроветворных элементов и исчезновения жира костный мозг плоских костей, а также диафизов и эпифизов трубчатых костей очень сочный, малиново-красного цвета. Характерны атрофические изменения в жел.-киш. тракте.
Сосочки языка, особенно в области корня, атрофичны, сглажены. Слизистая оболочка языка содержит красноватые участки воспаления, располагающиеся чаще по краям и на кончике, иногда афтозные высыпания, трещины (картина так наз. гунтеровского глоссита). Сходные изменения могут наблюдаться в слизистой оболочке десен, щек, мягкого неба, глотки, пищевода. Постоянно выявляется атрофия слизистой оболочки желудка, наиболее выраженная в области дна; складки слизистой оболочки сглажены или не определяются, стенка желудка истончена, в некоторых случаях имеются полипозные разрастания. Атрофические изменения могут наблюдаться также в слизистой оболочке кишечника. Размеры селезенки — в пределах или несколько больше нормы. Печень увеличена незначительно, плотновата. Вследствие отложения гемосидерина ткань селезенки, печени, иногда почек на разрезе имеет ржавый оттенок. Лимф, узлы небольшие, мягкие. В некоторых: случаях макроскопически в спинном мозге выявляются мелкие очаги некроза с размягчением. Иногда находят мелкоточечные кровоизлияния в. серозных и слизистых оболочках, в коже.
Микроскопически в красном костном мозге отмечается выраженная гиперплазия клеток эритроидного ряда с наличием среди них большого количества мегалобластов — крупных клеток, имеющих нежноячеистую структуру ядра с отчетливо видимыми ядрышками и широкую зону базофильной или полихрома-тофильной цитоплазмы. Число клеток лейкоцитопоэза несколько снижено. Мегакариоциты содержатся в достаточном или уменьшенном количестве. Наблюдаются выраженные дистрофические изменения и распад клеток, особенно эритроидного ряда, обилие эритро-и сидерофагов. В слизистой оболочке желудка выявляется картина атрофического гастрита, имеется значительное уменьшение количества желез и железистых клеток, особенно обкладочных. Клетки уменьшены в размерах, пикнотичны, уплощены, вследствие чего просвет желез расширен. Возрастает количество слизеобразующих железистых клеток, встречаются участки кишечной метаплазии поверхностного эпителия. Строма слизистой оболочки склерозирована, инфильтрирована лимфоцитами, плазматическими клетками, единичными сегментоядерными нейтрофильными гранулоцитами (рис.). Изменения наиболее выражены в дне желудка, однако интенсивность их может варьировать в различных участках слизистой оболочки. Атрофические изменения не подвергаются обратному развитию при лечении витамином B12 и сохраняются в период ремиссии заболевания.
При биопсии слизистой оболочки тонкой кишки выявляются укорочение кишечных ворсинок, дистрофические изменения железистых клеток со снижением в них фигур митозов в криптах, лимфоидно-плазмоцитарная инфильтрация стромы. После лечения витамином B12 эти изменения могут исчезнуть. Наряду с атрофическими изменениями наблюдается дистрофия нервных волокон языка, нервных клеток подслизистого сплетения (plexus submucosus, s. Meissneri) и мышечно-кишечного сплетения (plexus myen-tericus, s. Auerbachi).
Характерны дистрофические изменения в задних и боковых столбах спинного мозга, преимущественно в шейном отделе, выражающиеся в очаговом набухании с последующим распадом миелиновых нервных волокон. Слияние мелких очагов приводит к образованию больших участков поражения. В некоторых случаях наблюдаются дистрофические изменения черепно-мозговых (черепных, Т.) и периферических нервов. Имеет место гемосидероз костного мозга, селезенки, печени, лимф, узлов, почек, выраженный в различной степени. В селезенке, лимф, узлах нередко встречаются очаги экстрамедуллярного кроветворения.
Клиническая картина проявляется симптомами поражения жел.-киш. тракта, нервной системы и кроветворной ткани. Постепенно появляются слабость, утомляемость, сердцебиение, одышка при физической нагрузке. Многие из больных в течение ряда лет жалуются на диспептические расстройства, возникшие в результате желудочной ахилии, которая может быть обнаружена за несколько лет до развития малокровия, при этом желудочный сок не содержит внутреннего желудочного фактора. В 1 — 2% случаев П. а. начинается с явлений стенокардии.
Как правило, заболевание протекает с обострениями, за которыми следуют ремиссии. Внешний вид больного при обострении процесса характеризуется бледностью с лимонно-желтым оттенком кожи и субиктеричностыо склер. Больные склонны к ожирению. Печень, как правило, увеличена, мягкая. Иногда пальпируется плотная селезенка. Температура изредка субфебрильная. Выслушиваются функциональные (анемические) сердечные шумы; на ЭКГ — снижение зубца T во всех отведениях, уширение желудочного комплекса.
У некоторых больных обнаруживается гунтеровский глоссит: вначале преобладают воспалительные явления («ошпаренный» язык), в дальнейшем — атрофические («лакированный» язык). Воспалительно-атрофические изменения могут распространиться на десны, слизистую оболочку щек, мягкого неба, глотки и пищевода; в последнем случае возникает дисфагия (синдром Плахммера — Винсона). Эти явления, кроме ахилии, исчезают в период ремиссии. При гастроскопии (см.) выявляется гнездная, реже тотальная атрофия слизистой оболочки желудка.
Поражение ц. н. с. клинически проявляется симптомами спинального паралича (спастический парапарез с повышенными рефлексами и клонусами) и табетическими симптомами (парестезии, опоясывающие боли, снижение рефлексов вплоть до полной арефлексии, нарушение вибрационной и глубокой чувствительности, сенсорная атаксия, расстройство функций тазовых органов). Реже наблюдаются поражения черепно-мозговых нервов, гл. обр. зрительного, слухового, обонятельного. Типична центральная скотома (см.) с потерей зрения, быстро восстанавливающегося под влиянием лечения витамином B12.
При обострении П. а. в крови отмечается Гиперхромная анемия; для нее характерно уменьшение количества эритроцитов, к-рые отличаются насыщенностью гемоглобином, достигают в диам. 12—15 мкм; цветной показатель равен 1,4—1,8. Встречаются эритроциты с остатками ядер (тельца Жолли), митотического веретена (кольца Кебота), с базофильной пунктацией, поли-хроматофилы, пойкилоциты, шизо-циты, а также ядерные формы эритроидных клеток — мегалобласты. Количество лейкоцитов уменьшено за счет гранулоцитопении; обнаруживаются миело- и метамиелоциты, гигантские палочко- и сегментоядерные нейтрофилы, содержащие до 12 и более сегментов. Обмечается тромбоцитопения, встречаются гигантские пластинки (мегатромбоциты). Содержание витамина B12 в крови снижено при нормальном или повышенном уровне фолатов в эритроидных клетках (так наз. метилтетрагидрофо-латный блок) и при повышенном содержании сывороточного железа. В период ремиссии картина крови постепенно нормализуется.
В случаях легкого течения П. а. у 80—90% больных, по данным М. П. Невского, наблюдаются астенические нарушения (см. Астенический синдром).
У одних больных преобладают эмоционально-гиперестетическая слабость, утомляемость, рассеянность, неустойчивость внимания, чувство разбитости, подавленно-слезливое настроение, гиперестезия; у других — раздражительность, недовольство, легкая возбудимость, повышенная требовательность. Ипохондрические высказывания у больных с П. а. (см. Ипохондрический синдром) часто связаны с реальными соматическими расстройствами. В случаях ирогредиентно текущей П. а., особенно сопровождаемой симптомами фуникулярного миелоза (см.), возникают острые и затяжные психозы, частота которых, по данным ряда исследователей, колеблется от 4 до 10%. Психозы чаще встречаются у женщин в возрасте от 40 до 60 лет. Начальные расстройства определяются астенией, продолжительность которой в случаях острого течения составляет недели, а в затяжных — месяцы. В последующем при остром течении чаще всего развивается делирий (см. Делириозный синдром), реже — сумеречное помрачение сознания (см.) или аменция (см. Аментивный синдром). Утяжеление психических нарушений приводит к развитию сопора и комы (см.).
При психозах с затяжным течением вслед за астенией возникают аффективные расстройства, чаще всего в форме депрессии (см. Депрессивные синдромы). Преобладают тревожно-ажитированные состояния с отрывочным бредом преследования и обвинения, вербальными иллюзиями (см.) и галлюцинациями (см.). В ряде случаев возникает депрессия со страхом. Реже встречаются маниакальные состояния с эйфорией и сниженной критикой (см. Маниакальные синдромы). При утяжелении клин, картины развивается галлюцинаторно-параноидное состояние (см. Параноидный синдром), при к-ром могут возникать выраженные тактильные галлюцинации. Особенность психических расстройств при П. а. заключается в изменчивости их интенсивности и смене одних расстройств другими на протяжении коротких отрезков времени. В тех случаях, когда такое «мерцание» психических расстройств отсутствует, затянувшийся психоз исчерпывается одним каким-либо состоянием, напоминая шизофрению (см.) или маниакально-депрессивный психоз (см.). На отдаленных этапах затяжных психозов могут возникать делириозные состояния. В ряде случаев их появление — признак возможного смертельного исхода, связанного с основным заболеванием. Психозы в случаях легкого течения П. а. могут смениться преходящими симптомами снижения уровня личности, а в случаях тяжелого течения наблюдается возникновение различного по тяжести и проявлениям психоорганического синдрома (см.).
Тяжелым осложнением П. а. является Пернициозная кома (coma perniciosum), возникающая вследствие быстрой анемизации, приводящей к гипоксии и ишемии головного мозга (в частности, области III желудочка). При этом наблюдается потеря сознания, арефлексия, падение температуры тела и АД, одышка, рвота, непроизвольное мочеиспускание.
Диагноз устанавливают на основании клин, данных, характерной картины крови и результатов исследования костномозгового пунктата.
Дифференциальный диагноз П. а. с другими мегалоб л астными, в частности фолиево-дефицитными, анемиями проводят на основе теста Шиллинга, заключающегося в том, что у больного П. а. введенный внутрь радиоактивный витамин B12 и одновременно парентерально не радиоактивный витамин B12 (1000 мкг) определяются в моче лишь в минимальных количествах, что указывает на нарушенную абсорбцию витамина B12, которая связана либо с нарушением секреции внутреннего желудочного фактора, либо с нарушением кишечного всасывания витамина B12; в последнем случае прием концентрата внутреннего желудочного фактора не улучшает абсорбцию витамина B12. П. а. дифференцируют с симптоматическими мегалобласт-ными (пернициозноподобными) анемиями, возникающими при опухолях желудка, дивертикулах и опухолях тонкой и слепой кишок, а также с агастральной, анентеральной и глистной B12-дефицитной анемиями (см. Анемия), при которых мегалобластная анемия развивается в результате нарушения секреции внутреннего желудочного фактора или абсорбции витамина B12 в кишечнике. П. а. дифференцируют также с системными заболеваниями, напр, эритромиелозом (см. Лейкозы), для которого характерны мегалобластоз костного мозга при повышенном содержании витамина B12 в крови (до 1000 нг/мл и выше) и отсутствие терапевтического эффекта от введения витамина B12 (так наз. B12-ахрестическая анемия).
При обострении ежедневно вводят витамин B12 (по 100—200 мкг) в течение 1-й недели до ретикулоцитарного криза, который обычно наступает на 5-й день от начала введения витамина B12 и характеризуется увеличенным содержанием ретикулоцитов. В дальнейшем те же дозы вводят через день в течение 4—5 недель до наступления гематол, ремиссии, которая определяется нормализацией периферической крови и костномозгового кроветворения и восстановлением нормального содержания витамина B12 в крови, причем нормализация крови начинается вслед за ретикулоцитарным кризом и завершается через 4—6 недель; нормализация костномозгового кроветворения (трансформация мегалобластиче-ского эритроцитопоэза в нормобласти-ческий) начинается немедленно после введения витамина B12 и завершается через 48—72 часа; содержание витамина B12 в крови восстанавливается постепенно. В период ремиссии исчезают клин, симптомы, включая неврологические. При фуникулярном миелозе вводят массивные дозы витамина B12 (500—1000 мкг) ежедневно в течение 7—10 дней, в дальнейшем два раза в неделю до исчезновения неврологических симптомов.
При психозах в зависимости от клин, картины применяют психотропные средства. При быстро прогрессирующей тяжелой пернициозной анемии (угрожающая Пернициозная кома) показано переливание эритроцитной массы (см. Переливание крови).
Прогноз при своевременно начатом лечении благоприятный.
Профилактика. Для предупреждения обострений П. а. производят инъекции витамина B12 по 50—100 мкг еженедельно в течение 1 года и в дальнейшем 1 раз в 2 недели в течение всей жизни.
Библиография: Абрамов М. Г. Гематологический атлас, с. 14, М., 1979; Боткин С. П. О пернициозной анемии, Еженед. клин, газ., Мб, с. 81, 1884; 0 н ж е, Курс клиники внутренних болезней и клинические лекции, т. 2, с. 80, М., 1950; Гольдберг А. И. Агастриче-ские В!г-дефицитные анемии, Томск, 1962, библиогр.; Давыдовокий И. В. Патологическая анатомия и патогенез болезней человека, т. 2, М., 1958; Кассирский И. А. иАлексеев Г. А. Клиническая гематология, с. 174, М., 1970; JI ю м о т Г. Н. К вопросу психозов при пернициозной анемии, в кн.: Вопр, клиники, патогенеза и тер. психич. заболев., под ред. В. М. Банщикова и И. А. Шишкина, с. 437, М., 1972; Невский М. П. К вопросу о психозах при пернициозной анемии, Труды психиат, клиники им. G. С. Корсакова, в. 8, с.391, М., 1945; Салу пере В. Проблема хронического гастрита, Таллин, 1978; Димитров Д. Я. Анемии на бремен-ните, София, 1974; Addison Th. Anaemia, disease of the supra-renal capsules, Lond. med. Gaz., v. 43, p. 517, 1849; Besangon F. L’an6mie pernicieuse, P., 1955; B i e г m e г A. Form von prog-ressiver pernicioser AnSmie, KorrespBl. schweiz. Arz., Bd 2, S. 15, 1872; G a s t-1 e W. B. a. Townsend W. G. Observations on the etiologic relationship of ac-hylia gastrica to pernicious anemia, Amer. J. med. Sci., v. 178, p. 764, 1929; G o m b e J. S. History of a case of anaemia, Trans, med.-chir. Soc. Edinb., v. 1, p. 194, 1824; Foroozan P. a. Trier J. S. Mucosa of the small intestine in pernicious anemia, New Engl. J. Med., v. 277, p. 553, 1967; K a ss L. Pernicious anemia, Philadelphia a. o., 1976, bibliogr.; Minot G. R. a. Murphy W. P. Treatment of pernicious anemia by a special diet, J. Amer, med. Ass., v. 87, p. 470, 1926; P o r o t A. Manuel alphab6tique de psychiatrie, p. 275, P., 1969; R i с k e s E. L. a. o. Crystalline vitamin Bt2, Science, v. 107, p. 396, 1948; Schneider С. Uber Geistesstorungen bei pernizioser Anamie, Nervenarzt, S. 286, 1929; Shulman R. Psychiatric aspects of pernicious anaemia, Brit. med. J., v. 3, p. 266, 1967; Smith E. L.Purification of anti-pernicious anaemia factors from liver, Nature (Lond.), v. 161, p. 638, 1948; Taylor K. B. Inhibition of intrinsic factor by pernicious anaemia sera, Lancet, v. 2, p.gl06, 1959; Taylor R. T., Hanna M. L. a. H u 11 o n J. J. 5-met-hyltetrahydrofolate homocysteine cobala-min methyltransferase in human bone marrow and its relationship to pernicious anemia, Arch. Biochem., v. 165, p. 787, 1974; Williams W. J. Hematology, p. 266. N. Y., 1977. v ’
Г. А. Алексеев; М. П. Хохлова (пат. ан.), H. Г. Шуме кий (псих.).
источник
Пернициозная анемия — это специфическая форма мегалобластной анемии, вызываемая аутоиммунным гастритом и сопутствующей недостаточностью продукции внутреннего фактора, приводящей к дефициту витамина B12. Рассмотрим метаболизм витамина В12, т.к. это поможет сравнить пернициозную анемию с другими анемиями, возникающими вследствие дефицита витамина В12.
Нормальный метаболизм витамина B12. Витамин B12 — это комплексное металлоорганическое соединение, известное как кобаламин. В обычных условиях человек полностью зависит от витамина B12, поступающего с пищей (небольшое количество витамина B12 вырабатывает микрофлора кишечника). Растения и овощи содержат мало витамина В12, и строго вегетарианская или макробиотическая диета не обеспечивает организм человека этим важным витамином. Ежедневная потребность в витамине В12 — 2-3 мкг.
Диета, включающая продукты животного происхождения, содержит значительно большее количество витамина. Как правило, подобная диета обеспечивает накопление витамина В12 в печени в количестве, достаточном на несколько лет.
Для абсорбции витамина B12 необходимо наличие внутреннего фактора, который секретируют париетальные клетки слизистой оболочки фундального отдела желудка. Витамин В12 высвобождается в желудке из комплекса с белками пищи под действием пепсина и связывается с кобалофилином — быстрым связывающим белком слюны (R-белком). В двенадцатиперстной кишке связанный витамин В12 высвобождается под действием панкреатических протеаз. Затем он связывается с внутренним фактором.
Этот комплекс транспортируется в подвздошную кишку, где подвергается эндоцитозу энтероцитами, экспрессирующими на поверхности рецепторы внутреннего фактора. В этих клетках витамин В12 связывается с главным белком-носителем, транскобаламином II, и секретируется в плазму. Транскобаламин II доставляет витамин B12 в печень и другие клетки организма, в том числе в быстро пролиферирующие клетки костного мозга и желудочно-кишечного тракта. В дополнение к этому основному пути существует также недостаточно изученный альтернативный механизм.
Этим путем может абсорбироваться до 1% витамина B12, поступающего с пищей, что делает возможным лечение пернициозной анемии высокими дозами витамина В12 per os.
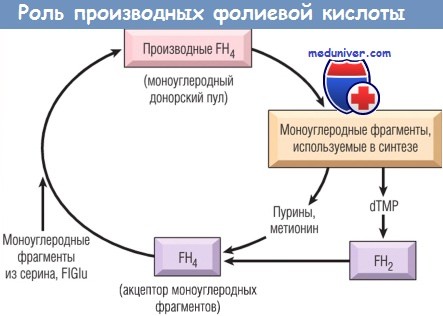
dTMP — дезокситимидинмонофосфат; FH2 — дигидрофолиевая кислота;
FH4 — тетрагидрофолиевая кислота; FIGIu — формиминоглутамат.
а) Биохимические функции витамина В12. У человека известны только две реакции, в которых необходимо участие витамина В12. В одной из них метилкобаламинслужит незаменимым кофактором при превращении гомоцистеина в метионин под влиянием метионинсинтазы. В этой реакции метилкобаламин отдает метильную группу, которая восстанавливается из N5-метилтетрагидрофолиевой кислоты (N5-метилFH4), главной формы фолиевой кислоты в плазме. В той же реакции N5-метил-FH4 превращается в тетрагидрофолиевую кислоту (FH4). FH4 играет кардинальную роль, т.к. она необходима (в виде производного N5,10-метилен-FН4) для превращения дезоксиуридинмонофосфата в дезокситимидинмонофосфат, непосредственный предшественник ДНК.
Предполагается, что фундаментальной причиной нарушения синтеза ДНК при дефиците витамина B12 служит сниженная доступность FH4, большая часть которой остается в виде N5-метил-FH4. Дефицит FH4 может усиливать дефицит внутренних фолатов из-за отсутствия синтеза метаболически активных полиглутамилированных форм. Это обусловлено участием витамина В12 в синтезе метионина, который переносит углеродные группы, необходимые для образования фолатполиглутаматов. Каковым бы ни был механизм, отсутствие фолатов — первейшая причина анемии при дефиците витамина B12, поскольку введение фолиевой кислоты улучшает состояние пациентов. Неврологические осложнения, обусловленные дефицитом витамина В12, менее понятны, т.к. введение фолиевой кислоты их не устраняет.
Другая известная реакция, зависимая от витамина B12, — изомеризация метилмалонил-кофермента А в сукцинил-кофермент А, для которой необходим аденозилкобаламин в качестве простетической группы метилмалонил-кофермент А-мутазы. Дефицит витамина B12 приводит к повышению уровня метилмалоновой кислоты в плазме и моче. Прерывание этой реакции с последующим накоплением метилмалоната и пропионата может привести к образованию и включению аномальных жирных кислот в липиды нейронов. Предполагают, что эта биохимическая аномалия способствует разрушению миелина и тем самым вызывает неврологические осложнения при дефиците витамина В12.
Однако такая гипотеза вызывает сомнения, т.к. у некоторых пациентов с наследственным дефицитом метилмалонил-кофермент А-мутазы, у которых осложнения обусловлены метилмалонил-ацидемией, отсутствуют неврологические осложнения, наблюдаемые при дефиците витамина B12.
б) Распространение. Пернициозная анемия часто наблюдается у представителей европеоидной расы, особенно в Скандинавских странах, но встречается и у представителей других рас. Средний возраст заболевших составляет 60 лет; болезнь редко возникает у лиц моложе 30 лет. Предполагается генетическая предрасположенность, но тип наследования не установлен. У многих больных обнаруживают антитела к разнообразным аутоантигенам.
в) Патогенез. Считается, что пернициозная анемия возникает в результате аутоиммунной реакции, мишенью которой служит слизистая оболочка желудка. Гистологически определяют хронический атрофический гастрит, характеризующийся утратой париетальных клеток, выраженным инфильтратом, состоящим из лимфоцитов и плазматических клеток, и мегалобластными изменениями клеток слизистой оболочки, подобными наблюдаемым у эритроидных клеток-предшественников.
У многих пациентов присутствуют аутоантитела трех типов. Около 75% пациентов имеют антитела типа I, блокирующие связывание витамина В12 с внутренним фактором. Эти антитела присутствуют и в плазме, и в желудочном соке. Антитела типа II препятствуют связыванию комплекса «внутренний фактор-витамин B12» с рецепторами в подвздошной кишке. Антитела типа II определяются у значительной части больных пернициозной анемией. Антитела типа III есть у 85-90% пациентов. Эти антитела распознают а- и b-субъединицы протонной помпы, которая в норме локализуется в микроворсинках каналикулярной системы париетальных клеток желудка. Эти антитела неспецифичны для пернициозной анемии, поскольку обнаруживаются у 50% пожилых с идиопатическим хроническим гастритом, не ассоциированным с пернициозной анемией.
Аутоантитела имеют диагностическую ценность, однако не являются первичной причиной патологии желудка. Скорее всего, поражение слизистой оболочки желудка инициирует ответ аутореактивных Т-клеток, которые продуцируют аутоантитела, усиливающие повреждение эпителия желудка. Когда общее количество клеток, секретирующих внутренний фактор, падает ниже порогового уровня (а также истощается резерв витамина B12), развивается анемия. В экспериментах на животных с аутоиммунным гастритом, опосредованным Т-клетками CD4+, образуются аутоантитела, напоминающие аутоантитела при пернициозной анемии. Это подтверждает первостепенную роль Т-клеточного иммунитета. Как правило, пернициозная анемия сочетается с другими аутоиммунными заболеваниями, особенно аутоиммунным тиреоидитом и воспалением надпочечников.
Склонность к развитию множественных аутоиммунных заболеваний, включая пернициозную анемию, обусловлена специфическими вариантами последовательности NALP1 — гена врожденного иммунного рецептора, картированного на хромосоме 17р13.
Дефицит витамина В12 ассоциируется не только с пернициозной анемией, но и с другими заболеваниями. Большинство из них связано с нарушением абсорбции витамина B12. При ахлоргидрии и нарушении секреции пепсина (что наблюдается у некоторых пожилых) витамин B12 с трудом отделяется от белков пищи. После резекции желудка внутренний фактор не поступает в подвздошную кишку. При утрате экзокринной функции поджелудочной железы витамин B12 не может высвобождаться из комплекса R-B12. Резекция подвздошной кишки или ее диффузное заболевание может удалить или повредить участок абсорбции комплекса IF-B12. Ленточные черви способны конкурировать с организмом-хозяином за витамин В12 и индуцировать его дефицит.
В некоторых ситуациях, например во время беременности, при гипертиреозе, хронической инфекции и диссеминированной злокачественной опухоли, повышенная потребность в витамине В12 может вызвать относительный дефицит его даже при нормальной абсорбции.
г) Морфология. Результаты исследования костного мозга и крови при пернициозной анемии сходны с описанными ранее для всех межобластных анемий. В желудке обычно обнаруживается диффузный хронический гастрит. Наиболее характерным изменением является атрофия фундальных желез желудка, захватывающая как главные, так и париетальные клетки, причем последние практически отсутствуют. Железистые эпителиальные клетки замещены секретирующими слизь бокаловидными клетками, напоминающими клетки, которые выстилают толстую кишку. Эта форма метаплазии носит название интестинализации. Некоторые клетки и их ядра увеличиваются в 2 раза, межобластные изменения аналогичны таковым в костном мозге. Со временем язык может стать гладким, лоснящимся, мясистым (атрофический глоссит).
Атрофия слизистой оболочки желудка и метапластические изменения обусловлены аутоиммунитетом, а не дефицитом витамина В12, поэтому парентеральное введение витамина В12 корригирует межобластные изменения в костном мозге и эпителиальных клетках пищеварительного тракта, но атрофические изменения в желудке и ахлоргидрия продолжают персистировать.
Поражения центральной нервной системы обнаруживаются в 75% случаев полностью развившейся пернициозной анемии, однако могут быть и в отсутствие явных гематологических изменений. Значимые изменения обнаруживаются в спинном мозге, где происходит демиелинизация дорсальных и латеральных путей, иногда с последующей утратой аксонов. Эти изменения приводят к спастическому параличу, сенсорной атаксии и тяжелым парестезиям в нижних конечностях. Реже происходят дегенеративные изменения в ганглиях задних корешков и периферических нервах (см. главу 28).
д) Клинические признаки. Вначале пернициозная анемия протекает без явных симптомов, поэтому к моменту обращения пациента к врачу анемия часто уже имеет тяжелую степень. В отсутствие лечения заболевание прогрессирует.
Признаки, на основании которых ставят диагноз «пернициозная анемия»:
(1) мегалобластная анемия от умеренной до тяжелой степени;
(2) лейкопения с присутствием гиперсегментированных гранулоцитов;
(3) низкий уровень витамина B12 в сыворотке;
(4) повышенный уровень гомоцистеина и метилмалоновой кислоты в сыворотке.
Диагноз подтверждается резким увеличением количества ретикулоцитов и возвращением уровня гематокрита к норме начиная приблизительно с 5-го дня после парентерального введения витамина В12. Антитела к внутреннему фактору, содержащиеся в сыворотке, высокоспецифичны для пернициозной анемии. Наличие антител к внутреннему фактору в большей степени свидетельствует о пернициозной анемии, чем наличие или отсутствие дефицита потребления витамина B12.
Лица с атрофическими или метапластическими изменениями слизистой оболочки желудка, ассоциированными с пернициозной анемией, подвержены повышенному риску развития карциномы желудка. Как было указано ранее, у лиц с дефицитом витамина В12 уровень гомоцистеина в сыворотке повышен. Такое повышение — фактор риска развития атеросклероза и тромбоза, и есть мнение, что дефицит витамина B12 повышает частоту сосудистой патологии. При парентеральной или высокодозной терапии витамином B12 per os анемию удается излечить, а периферические неврологические изменения начинают регрессировать или по меньшей мере не прогрессируют. Однако изменения слизистой оболочки желудка и риск развития рака желудка сохраняются.
источник
Пернициозная анемия (мегалобластная анемия, B12-дефицитная анемия или болезнь Аддисона-Бирмера) — заболевание, которое возникает в результате нарушения кроветворения при дефиците в организме витамина В12.
| МКБ-10 | D51.0 |
|---|---|
| МКБ-9 | 281.0 |
| eMedicine | med/1799 |
| DiseasesDB | 9870 |
| MedlinePlus | 000569 |
| OMIM | 261100; 613839 |
| MeSH | D000752 |
При недостатке витамина В12 в костном мозге обычные клетки-предшественники эритроцитов замещаются мегалобластами – аномально крупными клетками, которые не способны трансформироваться в эритроциты. При отсутствии лечения у больного развивается анемия и дегенерация нервов.
Впервые пернициозную анемию описал Аддисон в 1855 г., охарактеризовав заболевание как «идиопатическую анемию» (анемия неясного происхождения).
Подробная клинико-анатомическая характеристика болезни принадлежит Бирмеру (1868 г.) Именно Бример дал заболеванию название «пернициозная анемия», т.е. злокачественная анемия.
Долгое время заболевание считалось неизлечимым, но в 1926 г. Майнотом и Мерфи было сделано открытие — пернициозную анемию можно излечить с помощью сырой печени (печеночная терапия). Это открытие и последующие работы американского гематолога и физиолога У. Б. Касла легли в основу современных представлений о патогенезе данного заболевания.
У. Б. Касл установил, что в норме у человека вырабатывается не только соляная кислота и пепсин, но и третий (внутренний) фактор – состоящее из пептидов и мукоидов комплексное соединение, которое выделяется мукоцитами (клетками слизистой оболочки желудка). Это соединение образует с внешним фактором (витамином В12) лабильный комплекс, который после поступления в плазму крови образует накапливающийся в печени белково-В12-витаминный комплекс. Данный комплекс принимает участие в кроветворении. У. Б. Касл выявил отсутствие у больных пернициозной анемией выделения в желудке внутреннего фактора, но химическую природу внешнего фактора не установил.
Вещество (витамин B12), играющее роль внешнего фактора, было установлено в 1948 г. Риксом и Смитом.
Заболевание встречается достаточно часто – частота распространения составляет 110 -180 больных на 100 000 населения. Наиболее подвержены заболеванию жители Великобритании и Скандинавского полуострова.
В большинстве случаев пернициозной анемией болеют люди, которые принадлежат к старшей возрастной группе (наблюдается у 1% лиц старше 60 лет). При наличии семейной предрасположенности к заболеванию болезнь выявляется в более молодом возрасте.
У женщин заболевание наблюдается чаще (10:7 в соотношении с лицами мужского пола).
Пернициозная анемия в зависимости от количества гемоглобина в крови больных подразделяется на:
- легкую степень заболевания, которая диагностируется при гемоглобине от 90 до 110 г/л;
- анемию средней степени тяжести, выявляющуюся при гемоглобине от 90 до 70 г/л;
- тяжелую анемию, при которой в крови содержится менее 70 г/л гемоглобина.
В зависимости от причины развития В12-дефицитной анемии выделяют:
- Пищевую или нутритивную анемию (развивается у детей раннего возраста). Наблюдается при недостатке витамина В12 в рационе (вегетарианцы, недоношенные дети и дети, вскармливаемые молочным порошком или козьим молоком).
- Классическую В12-дефицитную анемию, связанную с атрофией слизистой желудка и отсутствием «внутреннего» фактора.
- Ювенильную В12-дефицитную анемию, развивающуюся из-за функциональной недостаточности вырабатывающих гландулярный мукопротеин фундальных желез. Слизистая желудка и секреция соляной кислоты сохранены. Данное заболевание носит обратимый характер.
Отдельно выделяют семейную В12-дефицитную анемию (болезнь Ольги Имерслунд), которая вызывается нарушением транспорта и всасывания в кишечнике витамина В12. У больных при данном заболевании выявляется белок в моче (протеинурия).
Пернициозная анемия развивается в организме:
- В результате нарушения всасывания витамина В12, которое возникает при атрофическом фундальном гастрите, частичной резекции (удаление) желудка и тотальной гастрэктомии, экзокринной недостаточности поджелудочной железы, тонкокишечном дисбактериозе, синдроме Золингера-Эллисона, заболеваниях конечного отдела подвздошной кишки (болезнь Крона и др.).
- При нарушении поступления витамина В12, которое вызвано отсутствием в рационе мяса, яиц и молочных продуктов (вегетарианство, голодание).
- При конкурентном поглощении витамина В12, которое возникает при инвазии широким лентецом (дифиллоботриоз) – видом ленточных червей, паразитирующих в тонком кишечнике. Инфицирование происходит при употреблении в пищу необработанной рыбы. Развитие пернициозной анемии в результате дифиллоботриоза наблюдается преимущественно в северных странах (например, 3% от общего числа данного заболевания, выявленного в Финляндии). Также наблюдается конкурентное поглощение при заселении тонкой кишки микроорганизмами (тонкая кишка в норме стерильна, поскольку микроорганизмы, попавшие с пищей или при рефлюксе через илеоцекальный клапан, находятся в ней транзитом). Постоянная бактериальная флора в тонкой кишке формируется при наличии анатомических аномалий (фистулы, дивертикулы и др.).
- В результате нарушения транспорта витамина В12. Возникает при врожденном отсутствии витамина В12-связывающих компонентов (врожденный, транзиторный и парциальный дефицит транспортного белка транскобаламина II) и при синдроме Имерслунд-Гресбека (возникает в результате нарушения транспорта витамина В12 к клеткам эпителия кишечника).
К причинам заболевания относится и аутоиммунный фактор — у 90% больных выявлено наличие циркулирующих аутоантител к клеткам желудка, которые секретируют соляную кислоту и внутренний фактор Кастла (присутствуют и у 5—10% здоровых людей), а у 60% больных – антитела к внутреннему фактору Касла.
В норме с пищей в организм человека поступает 6-9 мкг витамина В12 в сутки (2-5 мкг выводится, а около 4 мкг задерживается в организме). Поскольку запасы витамина В12 в организме значительны, злокачественное малокровие развивается только спустя длительный период (около 4 лет) после прекращения его поступления или нарушения его усвоения.
Недостаточность цианокобаламина (витамина В12) приводит к дефициту его коферментных форм – метилкобаламина и 5-дезоксиаденозилкобаламина. Метилкобаламин необходим для нормального протекания процессов образования эритроцитов, а 5-дезоксиаденозилкобаламин обеспечивает метаболические процессы, протекающие в ЦНС и периферической нервной системе.
При дефиците метилкобаламина синтез нуклеиновых кислот и незаменимых аминокислот нарушается и развивается мегалобластный тип кроветворения. Эритроциты в процессе образования и созревания принимают форму мегалобластов и мегалоцитов, которые быстро разрушаются и не способны выполнять кислородтранспортную функцию. В результате в периферической крови значительно сокращается количество эритроцитов и развивается анемический синдром.
Недостаточное количество 5-дезоксиаденозилкобаламина вызывает нарушение обмена жирных кислот, которые провоцируют накапливание в организме токсичных метилмалоновой и пропионовой кислот. Эти кислоты оказывают повреждающее воздействие на нейроны головного и спинного мозга, способствуют нарушению синтеза миелина и дегенерации миелинового слоя, поэтому пернициозная анемия сопровождается поражением нервной системы.
Пернициозная анемия проявляется:
- Анемическим синдромом, который сопровождается общей слабостью, снижением работоспособности, субфебрилитетом, головокружениями, обморочными состояниями. Синдром также проявляется одышкой, которая возникает даже при незначительных нагрузках, шумом в ушах и мельканием «мушек» перед глазами. Кожа становится бледной со слегка желтоватым оттенком, а лицо приобретает одутловатость. При аускультации сердца могут выявляться систолические шумы, а при длительном течении анемии развивается миокардиодистрофия и сердечная недостаточность.
- Гастроэнтерологическим синдромом, который сопровождается тошнотой и рвотой, снижением аппетита и массы тела, запорами. Возникает также гунтеровский глоссит (меняется структура языка из-за недостатка витамина В12), при котором язык приобретает малиновый или ярко-красный оттенок, а его поверхность становится сглаженной, «лакированной». Больной при этом испытывает в языке ощущение жжения. Возможно развитие ангулярного (локализующегося в углах рта) стоматита. Желудочная секреция в значительной степени снижена, при гастроскопии выявляются атрофические изменения слизистой желудка.
- Неврологическим синдромом. При дефиците витамина В12 наблюдается слабость мышц, походка становится неустойчивой, ноги – скованными, больной испытывает онемение конечностей. Длительный дефицит витамина В12 приводит к поражениям спинного и головного мозга (исчезает вибрационная, болевая и тактильная чувствительность, возникают судороги). Осмотр невролога позволяет выявить повышение сухожильных рефлексов, наличие симптома Ромберга (потеря равновесия при закрытых глазах) и рефлекса Бабинского (разгибание I пальца стопы во время штрихового раздражения кожи наружного края подошвы), признаки фуникулярного миелоза.
Мегалобластная анемия может сопровождаться раздражительностью, пониженным настроением, нарушением мочеиспускания. Иногда развивается импотенция и расстройства зрения.
При повреждениях головного мозга возможно нарушение восприятия желтого и синего цветов, в редких случаях наблюдаются галлюцинации и другие нарушения психики.
Пернициозная анемия диагностируется при помощи:
- Анализа жалоб пациента и анамнеза заболевания, во время которого врач уточняет длительность заболевания, наличие наследственных и сопутствующих заболеваний и т.д.
- Данных физикального осмотра. Во время осмотра врач обращает внимание на оттенок кожных покровов, пульс и артериальное давление (при В12-дефицитной анемии пульс часто учащенный, а АД снижено). Обязательно осматривается язык.
- Данных лабораторных анализов.
Лабораторные анализы включают:
- Анализ крови, который позволяет выявить снижение количества эритроцитов, увеличение их размера, снижение клеток-предшественников эритроцитов (ретикулоцитов), пониженный уровень гемоглобина, пониженное содержание тромбоцитов и их увеличение в размерах. Также выявляется изменение цветного показателя (соотношение первых трех цифр количества эритроцитов и увеличенного в 3 раза уровня гемоглобина) в сторону увеличения – при норме от 0,86 до 1,05 при пернициозной анемии это соотношение превышает 1,05.
- Анализ мочи, который позволяет выявить сопутствующие заболевания (пиелонефрит и др.), а также предположить наследственную форму болезни.
- Биохимический анализ крови, позволяющий выявить снижение содержания в крови витамина В12, определить уровень холестерина, мочевой кислоты, глюкозы, обнаружить креатинин (продукт распада белка). Мегалобластная анемия часто сопровождается повышением уровня билирубина, образующегося при распаде эритроцитов, уровня железа в результате уменьшения его использования при образовании новых эритроцитов и уровня ускоряющего химические реакции фермента лактат-дегидрогеназы.
Для исследования костного мозга под общим наркозом в области передних и задних остей подвздошной кости делают пункцию (для исключения искажений данных исследование проводится до назначения витамина В12). Анализ миелограммы позволяет обнаружить мегалобластический тип кроветворения и усиленное образование эритроцитов.
- ЭКГ, позволяющую обнаружить увеличенную частоту сердечных сокращений и в некоторых случаях нарушения ритма сердца.
- Гастроскопию, позволяющую выявить отсутствие соляной кислоты в желудочном соке (ахлоргидрию) и атрофический гастрит, затрагивающий отделы, в которых происходит секреция соляной кислоты и пепсина. Поскольку клетки желудочного эпителия выглядят при цитологическом исследовании как атипичные, проводят дифференциальную диагностику с раком желудка.
- Рентгенографию желудка, УЗИ органов брюшной полости.
- МРТ головного мозга и осмотр невролога.
Оценка всасывания витамина В12 проводится при помощи теста Шиллинга. Больной принимает внутрь радиоактивный витамин В12, а через несколько часов ему парентерально вводится «ударная» доза немеченного витамина. Затем измеряется содержание радиоактивного витамина в суточной моче. При сохранной функции почек снижение его выделения свидетельствует о снижении всасывания в кишечнике витамина В12.
Лечение мегалобластной анемии направлено на устранение причины заболевания и нормализацию кроветворения. Терапия включает:
- Лечение заболеваний ЖКТ (при аутоиммунном поражении желудка назначаются глюкокортикостероиды), сбалансированный рацион питания, в который включают кисломолочные продукты, говядину, морепродукты, яйца и мясо кролика.
- Применение празиквантела или фенасала при дифиллоботриозе.
- Восполнение дефицита витамина В12.
Пернициозная анемия лечится введением цианокобаламина (витамин В12) на протяжение 4 – 6 недель подкожно 1 раз в день по 200 — 500 мгк. Затем витамин вводят раз в неделю (курс 3 месяца), а потом переходят к инъекциям 2 раза в месяц на протяжении полугода (доза не меняется).
Нормализация кроветворения наступает приблизительно спустя 2 месяца после начала лечения (точные сроки зависят от тяжести анемии).
Переливание эритроцитарной массы проводится только при анемической коме или тяжелой степени анемии.
Профилактика заболевания сводится к:
- полноценному питанию;
- своевременному лечению заболеваний, вызывающих дефицит витамина В12;
- приему поддерживающей дозы цианокобаламина после удаления части желудка или кишечника.
источник