«ФАРМАТЕКА»; Актуальные обзоры; № 13; 2012; стр. 9-14.
Д.Т. Абдурахманов
Кафедра терапии и профболезней ГБОУ ВПО «Первый МГМУ им. И.М. Сеченова» Минздравсоцразвития РФ, Москва
Обсуждается проблема железодефицитной анемии (ЖДА), развивающейся в т. ч. при заболеваниях желудочно-кишечного тракта. Представлены сведения, касающиеся причин возникновения ЖДА, патогенеза, симптоматики, диагностики и лечения данной патологии. Особое внимание уделено препарату Феринжект (железа карбоксимальтозат), который применяется в комплексной терапии пациентов с ЖДА, обусловленной воспалительными заболеваниями кишечника.
Ключевые слова: железодефицитная анемия, дефицит железа, ферротерапия, железа карбоксимальтозат
The article discusses the problem of iron deficiency anemia (IDA), which develops against the background of many diseases, including gastrointestinal diseases. The data on the causes of IDA, pathogenesis, symptoms, diagnosis and treatment of this disease are presented. Particular attention is paid to the drug Ferinject (ferric carboxymaltosate) used for the treatment of IDA in patients with inflammatory bowel diseases.
Key words: iron deficiency anemia, iron deficiency, ferrotherapy, ferric carboxymaltosate
Наиболее частая в популяции причина анемии — дефицит железа в организме. По данным отчета Всемирной организации здравоохранения (ВОЗ) о состоянии здоровья за 2002 г., железодефицитная анемия (ЖДА) входит в десятку глобальных факторов риска развития нетрудоспособности. Так, показано, что ЖДА встречается среди 30 % населения планеты [1]. В США ЖДА наблюдается среди 5-12 % небеременных женщин и 1-5 % мужчин [2].
Метаболизм железа в организме
Общее количество железа в организме взрослого человека составляет около 3,5-4,0 г, в среднем 50 и 40 мг/кг у мужчин и женщин соответственно. Основная часть железа входит в состав гемоглобина эритроцитов (около 2,5 г), значительная часть железа (около 0,5—1,0 г) депонируется в составе ферритина или входит в состав гемсодержащих и других ферментов (миоглобина, каталазы, цитохромов) организма (около 0,4 г) и небольшая часть железа (0,003—0,007 г) находится в связанном с трансферрином состоянии в крови.
Баланс железа в организме поддерживается соответствием количества поступающего железа его потерям. В пище железо присутствует в составе гема или как негемовое железо. Ежедневно с пищей (стандартный пищевой рацион) в организм человека поступает 10—20 мг железа, из которого в норме в кишечнике всасывается около 10 % (от 3 до 15 %), что компенсирует суточные потери железа, главным образом при слущивании эпителиальных клеток. Организм обеспечивает баланс железа в организме, регулируя процесс его всасывания в кишечнике. В случае развития дефицита железа организм увеличивает процент всасываемого железа (может достигать 25 %), при избытке — уменьшает [3]. В этом процессе ключевое значение придают гепсидину — белку, который синтезируется в печени. Поступление с пищей или выведение железа, как правило, вне контроля организма.
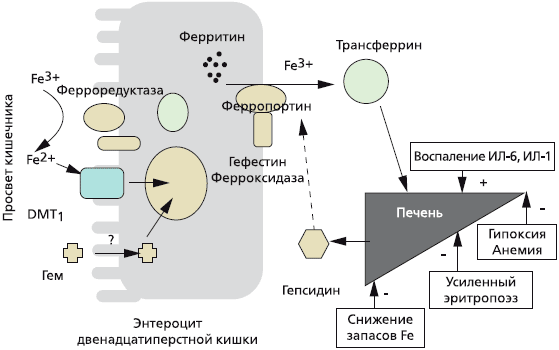
Около 25—30 мг железа ежедневно реутилизируется после разрушения (вследствие старения) эритроцитов в селезенке и поступает снова в костный мозг для синтеза новых эритроцитов. Железо, которое всасывается в кишечнике, предварительно на поверхности энтероцита восстанавливается с участием ферроредуктаз из трехвалентного (Fe 3+ ) в двухвалентнтное (Fe 2+ ), затем с помощью специфического переносчика — транспортера двухвалентных металлов (DMT1) поступает в цитоплазму [4]. Железо в составе гема (содержится в мясе, рыбе) всасывается напрямую. В дальнейшем двухвалентное железо с помощью другого переносчика, ферропортина (также мобилизует железо из ферритина), секретируется в кровь, где снова окисляется до трехвалентного (при участии белка гефестина) и связывается с плазменным белком трансферрином [5]. Трансферрин осуществляет транспорт железа в костный мозг, где оно утилизируется для синтеза эритроцитов, или преимущественно в печень, где железо депонируется в составе ферритина (рис. 1) [6].
При снижении запасов железа, гипоксии, анемии, усиленном эритропоэзе в печени снижается синтез гепсидина, что усиливает всасывание железа в кишечнике, при хроническом воспалении синтез гепсидина в печени увеличивается и, соответственно, всасывание железа в кишечнике снижается.
Рис 1. Регуляция всасывания железа в кишечнике [Guidi G.C., Santonastaso C.L., 2010]
Ферритин — ключевой белок, отражающий запасы железа в организме. Он депонирует железо в нетоксической форме, которое при необходимости мобилизуется. В среднем одна молекула ферритина содержит до 4500 атомов железа. Главным образом железо депонируется в печени, костном мозге и селезенке. Снижение уровня ферритина в сыворотке крови является достаточно надежным показателем дефицита железа в организме, его увеличение, как правило, указывает на перегрузку организма железом. В то же время необходимо помнить, что ферритин относится к белкам острой фазы воспаления, поэтому увеличение его содержания в крови может быть следствием активного воспалительного процесса, а не телько избытка железа. В ряде случаев некоторые злокачественные опухоли обладают способностью синтезировать и секретировать в кровь большое количество ферритина (в рамках паранеопластического синдрома). В норме содержание ферритина в сыворотке крови составляет 30-300 нг/мл.
Причины железодефицитной анемии
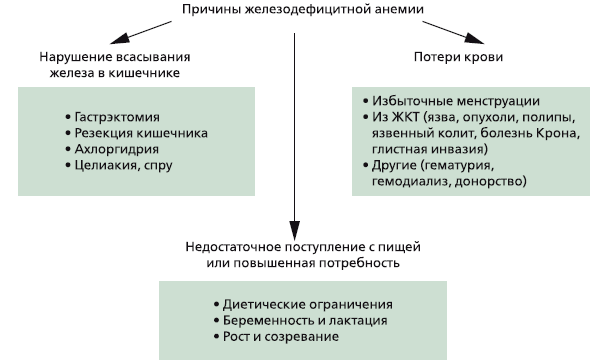
Выделяют три глобальные причины развития дефицита железа в организме (рис. 2):
1. Недостаточное поступление с пищей или повышенная потребность.
2. Нарушение всасывания железа в кишечнике.
3. Хронические потери крови.
Рис 2. Основные причины железодефицитной анемии
В популяции наиболее частой причиной ЖДА является недостаточное поступление с пищей: по данным ВОЗ, от четверти до трети населения в мире хронически голодают из-за нехватки продуктов питания, особенно мясной пищи. Однако в клинической практике среди основных причин ЖДА выделяют хронические потери крови, прежде всего из желудочно-кишечного тракта.
Клиническая картина
При ЖДА наблюдаются общие для всех анемий проявления циркуляторно-гипоксического синдрома:
Кроме того могут встречаться специфические признаки тканевого дефицита железа:
Диагностика
Лабораторная диагностика ЖДА основана на изучении обмена железа и выявлении его дефицита. Выделяют ряд признаков, указывающих на железодефицитный характер анемии (табл. 1).
Лабораторные признаки дефицита железа и ЖДА
| Параметры | Значения при ЖДА | Норма | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Железо сыворотки, мкг/дл | 3 | 5 | Примечание. НПВС — нестероидные противовоспалительные средства. Среди причин ЖДА (почти 30-50 % всех случаев) прежде всего рассматривают острые или хронические кровопотери из ЖКТ. Основной причиной ЖДА у женщин до менопаузы являются беременность и менструации, у женщин после менопаузы и у мужчин — хронические (латентные) потери крови из ЖКТ. Анализ кала на скрытую кровь — основной скрининговый метод выявления скрытого желудочно-кишечного кровотечения (тест положительный при выделении не менее 10 мл крови в сутки). При потере не менее 30 мл крови в сутки тест на скрытую кровь бывает положительным в 93 % случаев [8]. Наиболее часто при хронической ЖДА и особенно в случаях положительного результата кала на скрытую кровь выполняют эзофагогастродуодено- (ЭФГДС) и колоноскопию. В 5-10 % случаев анемий, связанных с заболеваниями ЖКТ, при ЭФГДС и колоноскопии не удается выявить очага поражения [9]. В 25 % случаев это обусловлено небольшим размером пораженного участка, который обнаруживается при повторном осмотре, в остальных случаях необходимо обследование тонкой кишки. В последние годы наиболее часто для выявления источника кровотечения из тонкой кишки используется беспроводная капсульная эндоскопия. В 10-17 % случаев причиной ЖДА у мужчин и женщин старше 40 лет являются онкологические заболевания ЖКТ; прежде всего колоректальный рак. ЖДА в течение длительного времени может быть единственным проявлением рака толстой кишки правосторонней локализации, при этом размер опухоли обычно превышает 3 см. Другая наиболее частая причина ЖДА -язвенная болезнь желудка и двенадцатиперстной кишки. При скрытых кровопотерях, обусловленных поражением тонкой кишки, наиболее часто в возрасте до 40 лет выявляют опухоли (лимфому, карциноид, аденокарциному, полипоз), ангиоэктазию артерий (Dieulafoy’s поражение), целиакию и болезнь Крона, в возрасте старше 40 лет -патологию сосудов различной природы и прием НПВС. У трети больных воспалительными заболеваниями кишечника (болезнь Крона, язвенный колит) выявляется анемия, имеющая сложный генез (сочетание ЖДА и анемии хронических заболеваний). При этом дефицит железа становится следствием нескольких причин: Лечение Суточная терапевтическая доза элементарного железа при лечении ЖДА для взрослых составляет в среднем 100— 200 мг в 2—3 приема. Поливитаминные комплексы, содержащие железо, не рекомендуют в качестве лечения ЖДА, т. к. они содержат недостаточное количество железа либо оно плохо всасывается в кишечнике. При адекватном лечении уже в течение первых 3 суток наблюдается увеличение числа ретикулоцитов в крови, на 7—10-й день отмечается ретикулоцитарный криз (пик ретикулоцитоза). К 3—4-й неделе лечения имеет место увеличение уровня гемоглобина на 20 г/л. Прием препаратов железа необходимо продолжать еще в течение 3—6 месяцев после нормализации уровня гемоглобина — пока насыщение трансферрина железом не превысит 30 % и концентрация ферритина не достигнет 50 нг/мл (показатель восстановления тканевых запасов железа). Среди 20—30 % пациентов в результате приема препаратов железа отмечаются различные диспептические расстройства (тошнота, дискомфорт в эпигастрии, диарея или запор). Риск развития желудочно-кишечных расстройств можно снизить, принимая препарат во время еды или на ночь, а также при постепенном увеличении дозы. Среди причин неэффективности пероральных форм железа рассматривают целый ряд факторов [10]: недостаточное поступление железа; Нарушение всасывания железа: Продолжающиеся потери крови или повышенная потребность в железе: Сопутствующие заболевания или состояния: Неправильный диагноз или наличие других причин анемии: Выделяют следующие показания к парентеральному введению, преимущественно внутривенному, препаратов железа: Основная опасность при парентеральном введении железа — развитие тяжелых аллергических реакций, включая анафилактических шок с летальным исходом, которые наблюдаются в 0,6—1,0 % случаев. Данные реакции, в основном, характерны для препаратов железа, содержащих декстран. Среди парентеральных препаратов железа широкое распространение, особенно в комплексной терапии воспалительных заболеваний кишечника, получили сахарат железа и железа карбоксимальтозат (Феринжект), которые в отличие от декстрана железа ассоциируются с минимальным риском развития анафилактических и других аллергических реакций [11—13]. Так, в 2011 г. были опубликованы результаты рандомизированного контролируемого исследования применения железа карбоксимальтозата пациентами с железодефицитной анемией, обусловленной воспалительными заболеваниями кишечника (FERGIcor — a Randomized Controlled Trial on Ferric Carboxymaltose for Iron Deficiency Anemia in Inflammatory Bowel Disease) [14]. В исследовании сравнивали эффективность и безопасность нового режима фиксированной дозы железа карбоксимальтозата (Феринжекта) и индивидуально рассчитываемых доз сахарата железа (СЖ) для пациентов с воспалительными заболеваниями кишечника и ЖДА. В исследование были включены 485 пациентов с ЖДА (уровень ферритина ЛИТЕРАТУРА источник Железодефицитная анемия – клинико-гематологический синдром, обусловленный недостатком железа в организме человека, что влечет нарушение нормального синтеза гемоглобина и гипоксию тканей. Патология широко распространена. По статистическим данным, у 8-10% женщин детородного возраста диагностируется железодефицитная анемия, а у 30% женщин – латентный дефицит железа. В раннем детском возрасте признаки железодефицитной анемии выявляются у каждого второго ребенка. В структуре всех анемий на долю железодефицитной приходится 90%. В основе развития железодефицитной анемии лежит отрицательный баланс обмена железа. К этому могут приводить разные факторы, но чаще всего причиной дефицита железа становится хроническая кровопотеря:
Другие причины кровопотери:
Нередко железодефицитная анемия развивается и у пациентов с хронической почечной недостаточностью, находящихся на программном гемодиализе.
Недостаток железа в организме также может сформироваться в результате недостаточного поступления его из пищи по следующим причинам:
Ряд заболеваний и патологических состояний органов пищеварительной системы может приводить к нарушению всасывания железа и развитию железодефицитной анемии:
Железодефицитная анемия развивается и у пациентов, страдающих хроническими гепатитами или циррозом печени. В данном случае нарушается транспорт железа из депо. Железодефицитная анемия может также появиться на фоне повышенной потребности в железе (в период полового созревания, беременности либо лактации) или при значительных потерях этого элемента (при онкологических, инфекционных заболеваниях). В зависимости от причины железодефицитные анемии делятся следующим образом:
По степени выраженности лабораторных и клинических признаков железодефицитные анемии бывают:
Железодефицитная анемия легкой степени в большинстве случаев протекает без-каких либо клинических проявлений или с минимальной их выраженностью. Тяжелая форма сопровождается развитием гематологического, сидеропенического и циркуляторно-гипоксического синдромов. В течении железодефицитной анемии выделяют несколько стадий:
В клинической картине железодефицитной анемии выделяют синдромы:
Развитие циркуляторно-гипоксического синдрома обусловлено нарушением синтеза гемоглобина, в результате чего страдает транспорт кислорода и развивается тканевая гипоксия. Клинически это проявляется:
Механизм развития сидеропенического синдрома связан с дефицитом железосодержащих тканевых ферментов (цитохромов, пероксидазы, каталазы). Недостаток названных ферментов становится причиной наблюдаемых на фоне железодефицитной анемии трофических расстройств со стороны слизистых оболочек и кожных покровов. Признаки сидеропенического синдрома:
Астеновегетативный синдром характеризуется эмоциональной лабильностью, повышенной раздражительностью, ухудшением памяти, снижением работоспособности. Клиническая картина железодефицитной анемии у детей неспецифична, преобладает один из следующих синдромов:
Диагностика состояния, а также определение степени его тяжести осуществляются по результатам лабораторных исследований. Для железодефицитной анемии характерны следующие изменения:
Для эффективного лечения железодефицитной анемии важно установить причину, ее вызвавшую. С целью обнаружения источника хронической кровопотери показано проведение:
В сложных диагностических случаях выполняют пункцию красного костного мозга с последующим гистологическим и цитологическим исследованием полученного пунктата. Значительное снижение в нем сидеробластов свидетельствует о наличии железодефицитной анемии. Дифференциальная диагностика проводится с другими видами гипохромных анемий (талассемией, сидеробластной анемией). Принципы терапии железодефицитной анемии:
Важную роль играет диетотерапия. В рацион включают язык, печень, мясо кролика, баранину, говядину, телятину – продукты, богатые гемовым железом. Для улучшения всасывания железа из желудочно-кишечного тракта необходимы аскорбиновая, янтарная и лимонная кислоты, которые в большом количестве содержатся в свежих фруктах и ягодах. Исключают шоколад, молоко, соевый протеин, чай, кофе, поскольку они ингибируют всасывание железа. Но только лишь диетой восполнить уже образовавшийся дефицит железа невозможно. Пациенты с железодефицитной анемией проходят заместительную терапию ферропрепаратами длительным курсом (не менее 2-2,5 месяцев). При тяжелой форме железодефицитной анемии и выраженном циркуляторно-гипоксическом синдроме возникают показания к проведению гемотрансфузии. Возникающие на фоне железодефицитной анемии циркуляторно-гипоксические нарушения ухудшают течение сопутствующих заболеваний сердечно-сосудистой и дыхательных систем. При железодефицитных состояниях происходит снижение активности IgA; в результате у пациентов зачастую возникают кишечные и респираторные инфекции. На фоне длительного течения тяжелой формы железодефицитной анемии у больных может развиться миокардиодистрофия. Прогноз благоприятный при условии своевременной коррекции дефицита железа и устранения причины развития анемии. Профилактика железодефицитной анемии включает:
Видео с YouTube по теме статьи: Образование: окончила Ташкентский государственный медицинский институт по специальности лечебное дело в 1991 году. Неоднократно проходила курсы повышения квалификации. Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа. Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья! источник Железодефицитная анемия – синдром, обусловленный недостаточностью железа и приводящий к нарушению гемоглобинопоэза и тканевой гипоксии. Клинические проявления представлены общей слабостью, сонливостью, пониженной умственной работоспособностью и физической выносливостью, шумом в ушах, головокружениями, обморочными состояниями, одышкой при нагрузке, сердцебиением, бледностью. Гипохромная анемия подтверждается лабораторными данными: исследованием клинического анализа крови, показателей сывороточного железа, ОЖСС и ферритина. Терапия включает лечебную диету, прием препаратов железа, в некоторых случаях – трансфузию эритроцитарной массы. Железодефицитная (микроцитарная, гипохромная) анемия – анемия, обусловленная нехваткой железа, необходимого для нормального синтеза гемоглобина. Её распространенность в популяции зависит от половозрастных и климатогеографических факторов. По обобщенным сведениям, гипохромной анемией страдает около 50% детей раннего возраста, 15% женщин репродуктивного возраста и около 2% мужчин. Скрытый тканевой железодефицит выявляется практически у каждого третьего жителя планеты. На долю микроцитарной анемии в гематологии приходится 80–90% всех анемий. Поскольку железодефицит может развиваться при самых различных патологических состояниях, данная проблема актуальна для многих клинических дисциплин: педиатрии, гинекологии, гастроэнтерологии и др. Ежесуточно с потом, калом, мочой, слущенными клетками кожи теряется около 1 мг железа и примерно столько же (2-2,5 мг) поступает в организм с пищей. Дисбаланс между потребностями организма в железе и его поступлением извне или потерями способствует развитию железодефицитной анемии. Железодефицит может возникать как при физиологических условиях, так и в результате ряда патологических состояний и быть обусловлен как эндогенными механизмами, так и внешними воздействиями: Чаще всего анемия вызывается хронической потерей крови: обильными менструациями, дисфункциональными маточными кровотечениями; желудочно-кишечными кровотечениями из эрозий слизистой желудка и кишечника, гастродуоденальных язв, геморроидальных узлов, анальных трещин и др. Скрытая, но регулярная кровопотеря отмечается при гельминтозах, гемосидерозе легких, экссудативном диатезе у детей и др. Особую группу составляют лица с болезнями крови — геморрагическими диатезами (гемофилией, болезнью Виллебранда), гемоглобинурией. Возможно развитие постгеморрагической анемии, вызванной одномоментным, но массивным кровотечением при травмах и операциях. Гипохромная анемия может возникать вследствие ятрогенных причин — у доноров, часто сдающих кровь; пациентов с ХПН, находящихся на гемодиализе. К факторам алиментарного порядка относятся анорексия, вегетарианство и следование диетам с ограничением мясных продуктов, плохое питание; у детей — искусственное вскармливание, позднее введение прикорма. Снижение абсорбции железа характерно для кишечных инфекций, гипоацидного гастрита, хронического энтерита, синдрома мальабсорбции, состояния после резекции желудка или тонкой кишки, гастрэктомии. Значительно реже железодефицитная анемия развивается вследствие нарушения транспортировки железа из депо при недостаточной белково-синтетической функции печени – гипотрансферринемиях и гипопротеинемиях (гепатитах, циррозе печени). Ежедневная потребность в микроэлементе зависит от пола и возраста. Наиболее высока необходимость в железе у недоношенных, детей раннего возраста и подростков (в связи с высокими темпами развития и роста), женщин репродуктивного периода (в связи с ежемесячными менструальными потерями), беременных (в связи с формированием и ростом плода), кормящих мам (в связи с расходом в составе молока). Именно эти категории являются наиболее уязвимыми в отношении развития железодефицитной анемии. Кроме того, повышение потребности и расхода железа в организме наблюдается при инфекционных и опухолевых заболеваниях. По своей роли в обеспечении нормального функционирования всех биологических систем железо является важнейшим элементом. От уровня железа зависит поступление кислорода к клеткам, протекание окислительно-восстановительных процессов, антиоксидантная защита, функционирование иммунной и нервной систем и пр. В среднем содержание железа в организме находится на уровне 3-4 г. Более 60% железа (>2 г) входит в состав гемоглобина, 9% — в состав миоглобина, 1% — в состав ферментов (гемовых и негемовых). Остальное железо в виде ферритина и гемосидерина находится в тканевом депо – главным образом, в печени, мышцах, костном мозге, селезенке, почках, легких, сердце. Примерно 30 мг железа непрерывно циркулирует в плазме, будучи частично связанным основным железосвязывающим белком плазмы – трансферрином. При развитии отрицательного баланса железа мобилизуются и расходуются запасы микроэлемента, содержащиеся в тканевых депо. На первых порах этого бывает достаточно для поддержания адекватного уровня Hb, Ht, сывороточного железа. По мере истощения тканевых резервов компенсаторно увеличивается эритроидная активность костного мозга. При полном истощении эндогенного тканевого железа его концентрация начинает снижаться в крови, нарушается морфология эритроцитов, уменьшается синтез гема в гемоглобине и железосодержащих ферментов. Страдает кислородтранспортная функция крови, что сопровождается тканевой гипоксией и дистрофическими процессами во внутренних органах (атрофический гастрит, миокардиодистрофия и др.). Железодефицитная анемия возникает не сразу. Вначале развивается предлатентный железодефицит, характеризующийся истощением только запасов депонированного железа при сохранности транспортного и гемоглобинового пула. На этапе латентного дефицита отмечается уменьшение транспортного железа, содержащегося в плазме крови. Собственно гипохромная анемия развивается при уменьшении всех уровней метаболических запасов железа – депонированного, транспортного и эритроцитарного. В соответствии с этиологией различают анемии: постгеморрагические, алиментарные, связанные с повышенным расходом, исходным дефицитом, недостаточностью резорбции и нарушением транспорта железа. По степени выраженности железодефицитные анемии подразделяются на:
Циркуляторно-гипоксический синдром обусловлен нарушением синтеза гемоглобина, транспорта кислорода и развитием гипоксии в тканях. Это находит свое выражение в ощущении постоянной слабости, повышенной утомляемости, сонливости. Пациентов преследует шум в ушах, мелькание «мушек» перед глазами, головокружения, переходящие в обмороки. Характерны жалобы на сердцебиение, одышку, возникающую при физической нагрузке, повышенную чувствительность к низким температурам. Циркуляторно-гипоксические нарушения могут усугублять течение сопутствующей ИБС, хронической сердечной недостаточности. Развитие сидеропенического синдрома связано с недостаточностью тканевых железосодержащих ферментов (каталазы, пероксидазы, цитохромов и др.). Этим объясняется возникновение трофических изменений кожных покровов и слизистых оболочек. Чаще всего они проявляются сухостью кожи; исчерченностью, ломкостью и деформацией ногтей; повышенным выпадением волос. Со стороны слизистых оболочек типичны атрофические изменения, что сопровождается явлениями глоссита, ангулярного стоматита, дисфагии, атрофического гастрита. Может возникать пристрастие к резким запахам (бензина, ацетона), искажение вкуса (желание есть глину, мел, зубной порошок и пр.). Признаками сидеропении также служат парестезии, мышечная слабость, диспепсические и дизурические расстройства. Астеновегетативные нарушения проявляются раздражительностью, эмоциональной неустойчивостью, снижением умственной работоспособности и памяти. Поскольку в условиях железодефицита IgA теряет свою активность, больные становятся подвержены частой заболеваемости ОРВИ, кишечными инфекциями. Пациентов преследует хроническая усталость, упадок сил, снижение памяти и концентрации внимания. Длительное течение железодефицитной анемии может привести к развитию миокардиодистрофии, распознаваемой по инверсии зубцов Т на ЭКГ. При крайне тяжелом железодефиците развивается анемическая прекома (сонливость, одышка, резкая бледность кожи с цианотичным оттенком, тахикардия, галлюцинации), а затем – кома с потерей сознания и отсутствием рефлексов. При массивной стремительной кровопотере возникает гиповолемический шок. На наличие железодефицитной анемии может указывать внешний вид больного: бледная, с алебастровым оттенком кожа, пастозность лица, голеней и стоп, отечные «мешки» под глазами. При аускультации сердца обнаруживается тахикардия, глухость тонов, негромкий систолический шум, иногда – аритмия. С целью подтверждения анемии и определения ее причин проводится лабораторное обследование.
К основным принципам терапии железодефицитной анемии относятся устранение этиологических факторов, коррекция рациона питания, восполнение железодефицита в организме. Этиотропное лечение назначается и проводится специалистами гастроэнтерологами, гинекологами, проктологами и др.; патогенетическое – гематологами. При железодефицитных состояниях показано полноценное питание с обязательным включением в рацион продуктов, содержащих гемовое железо (телятины, говядины, баранины, мяса кролика, печени, языка). Следует помнить, что усилению ферросорбции в ЖКТ способствуют аскорбиновая, лимонная, янтарная кислота. Ингибируют всасывание железа оксалаты и полифенолы (кофе, чай, соевый протеин, молоко, шоколад), кальций, пищевые волокна и др. вещества. Вместе с тем, даже сбалансированная диета не в состоянии устранить уже развившийся недостаток железа, поэтому больным с гипохромной анемией показана заместительная терапия ферропрепаратами. Препараты железа назначаются курсом не менее 1,5-2-х месяцев, а после нормализации уровня Hb проводится поддерживающая терапия в течение 4-6 недель половинной дозой препарата. Для фармакологической коррекции анемии используются препараты двухвалентного и трехвалентного железа. При наличии витальных показаний прибегают к гемотрансфузионной терапии. В большинстве случаев гипохромная анемия подается успешной коррекции. Однако при неустраненной причине железодефицит может рецидивировать и прогрессировать. Железодефицитная анемия у детей раннего и младшего возраста может вызывать задержку психомоторного и интеллектуального развития (ЗПР). В целях профилактики железодефицита необходим ежегодный контроль параметров клинического анализа крови, полноценное питание с достаточным содержанием железа, своевременная ликвидация источников кровопотери в организме. Следует учитывать, что лучше всего усваивается железо, содержащееся в мясе и печени в форме гема; негемовое железо из растительной пищи практически не усваивается – в этом случае оно сначала должно восстановиться до гемового при участии аскорбиновой кислоты. Лицам групп риска может быть показан профилактический прием железосодержащих препаратов по назначению специалиста. источник Железодефицитная анемия (ЖДА) — одно из наиболее часто диагностируемых патологических состояний кровеносной системы, да и вообще самый распространенный вид анемии.
Для того чтобы остановить прогрессирование заболевания и избежать осложнений, необходимо выявить первопричины его появления и своевременно начать лечение. Анемия характеризуется пониженным содержанием в кровеносной системе человека красных кровяных телец — эритроцитов, и, как следствие, падением гемоглобина. Если низкий уровень этих элементов связан с недостатком железа в организме, то в данном случае речь идет о железодефицитной анемии (ЖДА). Как правило, патология не является самостоятельным заболеванием. В большинстве случаев железодефицитная анемия возникает вслед за какими-либо другими негативными изменениями в организме человека.
Дефицит железа плохо сказывается на жизнеспособности человека в целом. Кроме того, развитие этой недостаточности чревато сбоями в образовании эритроцитов, а также нарушением реакций окисления и восстановления, механизма деления клеток и нормального течения некоторых других реакций. Железо является основой гемоглобина, выполняющего функции снабжения кислородом всех тканей и органов в теле человека, а также играющего важную роль в синтезе белка и гормонов. Если дефицит железа не восполняется в течение длительного времени, у пациента начинает развиваться анемический синдром. Причины развития железодефицитной анемии могут заключаться в нехватке железа, поступающего в организм извне, или в сбоях потребляющих его процессов, ведь самостоятельно организм человека не может вырабатывать этот микроэлемент. Ими могут стать:
Железодефицитная анемия у детей может развиваться в результате различных патологий при беременности, раннему переходу на искусственное кормление, ускоренным темпом роста (в случае недоношенности плода). Усиленная потребность организма в железе и является главным провоцирующим фактором для развития железодефицитной анемии. Она может быть связана с такими жизненными процессами, как:
Патогенез этой разновидности анемии выражается двумя основными периодами:
Классификация заболевания по причинам возникновения выделяет следующие виды:
Классификация по уровню гемоглобина разделяет заболевание на виды в зависимости от тяжести:
Позднее начинает проявляться общеанемический синдром, явственность которого определяется тяжестью анемии и способностью организма к сопротивлению. Наличие у пациента следующих признаков может свидетельствовать о заболевании железодефицитной анемией:
Железодефицитная анемия у детей и взрослых может быть установлена любым специалистом, однако детальная диагностика, направленная на выявление причин, и лечение данного заболевания должны проводиться врачом-гематологом. Обследования пациента включают в себя:
По мнению врачей при лечении железодефицитной анемии у взрослых и детей нельзя ограничиваться только медикаментами. Восполнять дефицит важного микроэлемента лучше и проще всего при помощи здоровой пищи и правильно подобранной диеты. Ежедневная норма железа, которую должен содержать рацион – не менее 20 мг. Следует отметить, что лечение этого заболевания будет неэффективным, если не принять мер по устранению первичной патологии, вызвавшей дефицит железа. Для профилактики болезни каждому человеку следует каждый год проводить лабораторный анализ показателей крови, комплексно питаться и, при необходимости, вовремя устранять возможные причины значительной кровопотери.
Сбалансированный рацион играет основную роль в профилактике и лечении ЖДА. При составлении диеты следует учитывать, что железо качественнее усваивается, если его прием осуществляется в совокупности с витамином C. При этом этот микроэлемент лучше всего всасывается кишечником, если он содержится в продуктах животного происхождения (до 3 раз больше по сравнению с растительными продуктами). Рейтинг продуктов, которые являются лидерами по количеству содержания железа, которые обязательно должны быть включены в лечебно-профилактическую диету при железодефицитной анемии:
Для более эффективного усвоения железа рекомендуется употреблять следующие препараты и витамины (в допустимых дозах):
Несмотря на то, что железодефицитная анемия у детей грудного возраста развивается достаточно редко (за исключением случаев, когда у мамы присутствует это заболевание), следует отметить что в этом случае заболевание особенно опасно. Нехватка железа у детей может обернуться серьезными нарушениями в физическом развитии, потому требует оперативного восполнения. Лечение железодефицитной анемии в этом возрасте осуществляется путем строгой диеты и тщательного контроля над ежедневным рационом кормящей матери, а также пересмотром прикорма малыша, если он уже имеется. Правильное питание является необходимым этапом в лечении и профилактике ЖДА, однако оно не может компенсировать недостаток нужного микроэлемента в организме самостоятельно, и потому врачи рекомендуют пациентам принимать медикаментозные препараты. Чаще всего назначаются лекарства в виде таблеток, реже, в случаях сбоев в работе кишечника – парентеральное введение. Лекарственные препараты при железодефицитной анемии должны употребляться длительным курсом (в течение нескольких недель или месяцев). Все они предназначены для приведения в норму основных показателей при анализе крови и устранения симптомов болезни. Наиболее часто применяемые из них:
Перед применением лекарственных средств необходимо проконсультироваться с врачом, неграмотное употребление может привести к переизбытку железа, что также чревато негативными последствиями и осложнениями. В сложных случаях заболевания анемией может возникнуть необходимость в проведении операции по переливанию эритроцитов. Данная процедура может понадобиться при наличии серьезной угрозы жизни больного и должна быть проведена в минимально возможный промежуток времени. Показанием для назначения переливания эритроцитов может стать:
Для успешного проведения этой процедуры и отсутствия осложнений очень важно, чтобы кровь донора идеально подходила пациенту по всем лабораторным показателям. Степень сложности такого заболевания, как железодефицитная анемия на сегодняшний день является достаточно низкой. При своевременном обнаружении симптомов и проведении качественно диагностики этот недуг может быть полностью устранен без каких-либо последствий. В некоторых случаях развитие осложнений при лечении ЖДА может произойти. Причинами для этого могут послужить следующие факторы:
Возможные осложнения данного заболевания это:
Данные виды осложнений представляют наибольшую угрозу для пациентов детского и преклонного возраста. источник
Железодефицитная анемия является самой распространенной патологией системы крови и самой часто встречаемой анемией. По данным ВОЗ (всемирной организации здравоохранения), более 2 миллиардов людей на планете имеют дефицит железа в организме. Несколько чаще данным недугом страдают женщины, что связано с беременностью, кормлением грудью, а также периодической кровопотерей во время менструаций. Интересные факты
Размер зрелого эритроцита колеблется в пределах от 7,5 до 8,3 микрометров (мкм). Он имеет форму двояковогнутого диска, которая поддерживается благодаря наличию в клеточной мембране эритроцита особого структурного белка – спектрина. Такая форма обеспечивает максимально эффективный процесс газообмена в организме, а наличие спектрина позволяет эритроцитам видоизменяться при прохождении через мельчайшие кровеносные сосуды (капилляры) и после этого восстанавливать свою первоначальную форму. Более 95% внутриклеточного пространства эритроцита заполнено гемоглобином – веществом, состоящим из белка глобина и небелкового компонента – гема. Молекула гемоглобина состоит из четырех глобиновых цепей, в центре каждой из которых находится гем. Каждый эритроцит содержит более 300 миллионов молекул гемоглобина. За транспортировку кислорода в организме отвечает небелковая часть гемоглобина, а именно атом железа, входящего в состав гема. Обогащение крови кислородом (оксигенация) происходит в легочных капиллярах, при прохождении через которые каждый атом железа присоединяет к себе 4 молекулы кислорода (формируется оксигемоглобин). Оксигенированная кровь разносится по артериям ко всем тканям организма, где происходит переход кислорода к клеткам органов. Взамен из клеток выделяется углекислый газ (побочный продукт клеточного дыхания), который присоединяется к гемоглобину (формируется карбгемоглобин) и по венам транспортируется к легким, где выделяется в окружающую среду вместе с выдыхаемым воздухом. Помимо переноса дыхательных газов, дополнительными функциями эритроцитов являются:
В организме человека эритроциты формируются из так называемых стволовых клеток. Эти уникальные клетки образуются на стадии эмбрионального развития. Они содержат ядро, в котором находится генетический аппарат (ДНК – дезоксирибонуклеиновая кислота), а также множество других органелл, обеспечивающий процессы их жизнедеятельности и размножения. Стволовые клетки дают начало всем клеточным элементам крови. Для нормального процесса эритропоэза необходимы:
Образование эритроцитов (эритропоэз) начинается в конце 3 недели эмбрионального развития. На ранних этапах внутриутробного развития красные клетки крови образуются, в основном, в печени и селезенке. Примерно на 4 месяце беременности происходит миграция стволовых клеток из печени в полости костей таза, черепа, позвонков, ребер и других, в результате чего в них формируется красный костный мозг, который также принимает активное участие в процессе кроветворения. После рождения ребенка кроветворная функция печени и селезенки угнетается, и костный мозг остается единственным органом, обеспечивающим поддержание клеточного состава крови. В процессе превращения в эритроцит, стволовая клетка претерпевает целый ряд изменений. Она уменьшается в размерах, постепенно теряет ядро и практически все органеллы (в результате чего дальнейшее ее деление становится невозможным), а также накапливает гемоглобин. Конечным этапом эритропоэза в красном костном мозге является ретикулоцит (незрелый эритроцит). Он вымывается из костей в периферический кровоток, и в течение суток происходит его созревание до стадии нормального эритроцита, способного в полной мере выполнять свои функции. Средняя продолжительность жизни красных клеток крови составляет 90 – 120 дней. По истечении этого периода их клеточная мембрана становится менее пластичной, в результате чего теряет способность обратимо деформироваться при прохождении через капилляры. «Старые» эритроциты захватываются и разрушаются особыми клетками иммунной системы – макрофагами. Данный процесс происходит, в основном, в селезенке, а также (в значительно меньшей степени) в печени и красном костном мозге. Незначительно малая доля эритроцитов разрушается непосредственно в сосудистом русле. При разрушении эритроцита из него выделяется гемоглобин, который быстро распадается на белковую и небелковую части. Глобин подвергается ряду превращений, в результате чего формируется пигментный комплекс желтого цвета – билирубин (несвязанная форма). Он нерастворим в воде и весьма токсичен (способен проникать в клетки организма, нарушая процессы их жизнедеятельности). Билирубин быстро транспортируется в печень, где связывается с глюкуроновой кислотой и выводится вместе с желчью. Небелковая часть гемоглобина (гем) также подвергается разрушению, в результате чего происходит выделение свободного железа. Оно токсично для организма, поэтому быстро связывается с трансферрином (транспортным белком крови). Большая часть железа, выделяющегося при разрушении эритроцитов, транспортируется в красный костный мозг, где повторно используется для синтеза эритроцитов.
В организме взрослого человека содержится около 4 грамм железа. Эта цифра варьирует в зависимости от пола и возраста. Концентрация железа в организме составляет:
Основными местами содержания железа в организме являются:
Кроме того, железо входит в состав целого ряда других белковых ферментов (цитохромов, каталазы, редуктазы). Они участвуют в окислительно-восстановительных процессах в организме, в процессах клеточного деления и регуляции многих других реакций. Дефицит железа может привести к недостатку данных ферментов и появлению соответствующих нарушений в организме. Всасывание железа в организме человека происходит преимущественно в двенадцатиперстной кишке, при этом все железо, поступающее в организм, принято разделять на гемовое (двухвалентное, Fe +2 ), содержащееся в мясе животных и птиц, в рыбе, и негемовое (трехвалентное, Fe +3 ), основным источником которого являются молочные продукты и овощи. Важным условием, необходимым для нормального всасывания железа, является достаточное количество соляной кислоты, входящей в состав желудочного сока. При уменьшении ее количества всасывание железа значительно замедляется. Всосавшееся железо связывается с трансферрином и транспортируется в красный костный мозг, где используется для синтеза эритроцитов, а также к органам-депо. Запасы железа в организме представлены, в основном, ферритином – комплексом, состоящим из белка апоферритина и атомов железа. Каждая молекула ферритина содержит в среднем 3 – 4 тысячи атомов железа. При снижении концентрации данного микроэлемента в крови, происходит выделение его из ферритина и использование для нужд организма. Скорость всасывания железа в кишечнике строго ограничена и не может превышать 2,5 мг в сутки. Этого количества достаточно лишь для того, чтобы восстанавливать ежедневные потери данного микроэлемента, которые в норме составляют около 1 мг у мужчин и 2 мг у женщин. Следовательно, при различных патологических состояниях, сопровождающихся нарушением всасывания железа либо повышенными его потерями, может развиться дефицит данного микроэлемента. При снижении концентрации железа в плазме уменьшается количество синтезируемого гемоглобина, в результате чего образующиеся эритроциты будут иметь меньшие размеры. Кроме того, нарушаются процессы роста эритроцитов, что приводит к уменьшению их количества.
Причиной дефицита железа в организме может быть:
Нарушение питания может привести к развитию железодефицитной анемии как у детей, так и у взрослых. Основными причинами недостаточного поступления железа в организм являются:
У новорожденных и детей грудного возраста потребности в железе полностью покрываются при кормлении грудным молоком (при условии, что мать не страдает железодефицитным состоянием). Если же слишком рано переводить ребенка на искусственное вскармливание, у него также могут появиться симптомы дефицита железа в организме. В нормальных, физиологических условиях может возникать повышенная потребность в железе. Это характерно для женщин во время беременности и в период кормления грудью. Несмотря на то, что определенная часть железа в период беременности сохраняется (ввиду отсутствия менструальных кровотечений), потребность в нем увеличивается в несколько раз.
Организм ребенка получает от матери все необходимые питательные вещества, в том числе и железо. Однако при наличии определенных заболеваний у матери или плода, возможно рождение ребенка с дефицитом железа. Причиной врожденного дефицита железа в организме может быть:
В любом из вышеперечисленных случаев концентрация железа в крови новорожденного значительно ниже нормы, и симптомы железодефицитной анемии могут проявляться уже с первых недель жизни. Всасывание железа в двенадцатиперстной кишке возможно лишь при нормальном функциональном состоянии слизистой оболочки данного отдела кишечника. Различные заболевания желудочно-кишечного тракта могу повреждать слизистую оболочку и значительно снижать скорость поступления железа в организм. К уменьшению всасывания железа в двенадцатиперстной кишке может привести:
Нарушение образования данного транспортного белка может быть связано с различными наследственными заболеваниями. Симптомов дефицита железа у новорожденного не будет, так как он получал данный микроэлемент из организма матери. После рождения основным способом поступления железа в организм ребенка является всасывание в кишечнике, однако из-за недостатка трансферрина всосавшееся железо не может быть доставлено к органам-депо и к красному костному мозгу и не может использоваться в синтезе эритроцитов. Так как трансферрин синтезируется только в клетках печени, различные ее поражения (цирроз, гепатиты и другие) также могут привести к уменьшению концентрации данного белка в плазме и развитию симптомов железодефицитной анемии. Одноразовая потеря большого количества крови обычно не приводит к развитию железодефицитной анемии, так как запасов железа в организме достаточно, чтобы возместить потери. В то же время при хронических, длительных, часто незаметных внутренних кровотечениях организм человека может терять по несколько миллиграмм железа ежедневно, на протяжении нескольких недель или даже месяцев. Причиной хронической кровопотери может быть:
Если причина кровопотери не будет своевременно выявлена и устранена, высока вероятность развития железодефицитной анемии у больного, так как всасывающееся в кишечнике железо способно лишь покрывать физиологические потребности в данном микроэлементе. Прием некоторых лекарственных препаратов может нарушать процессы всасывания и утилизации железа в организме. Обычно это происходит при длительном приеме больших доз медикаментов. Препаратами, которые могут вызвать дефицит железа в организме, являются:
Во избежание развития железодефицитной анемии принимать данные препараты следует только по назначению врача, строго соблюдая дозировку и длительность использования.
Проявлениями железодефицитной анемии являются:
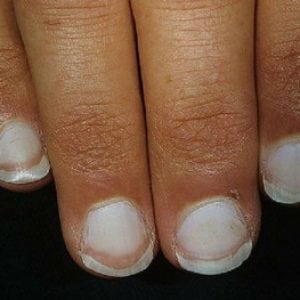
Как говорилось ранее, железо входит в состав множества ферментов, участвующих в процессах клеточного дыхания и деления. Дефицит данного микроэлемента приводит к повреждению кожи — она становится сухой, менее эластичной, шелушится и трескается. Кроме того, привычный красный или розоватый оттенок слизистым оболочками и коже придают эритроциты, которые находятся в капиллярах данных органов и содержат оксигенированный гемоглобин. При снижении его концентрации в крови, а также в результате уменьшения образования эритроцитов, может отмечаться бледность кожных покровов. Волосы истончаются, теряют привычный блеск, становятся менее прочными, легко ломаются и выпадают. Рано появляется седина. Поражение ногтей является весьма специфичным проявлением железодефицитной анемии. Они истончаются, приобретают матовый оттенок, расслаиваются и легко ломаются. Характерной является поперечная исчерченность ногтей. При выраженном дефиците железа может развиться койлонихия – края ногтей приподымаются и изгибаются в обратную сторону, приобретая ложкообразную форму. Слизистые оболочки относятся к тканям, в которых процессы клеточного деления происходят максимально интенсивно. Вот почему их поражение является одним из первых проявлений дефицита железа в организме. При железодефицитной анемии поражается:
Как уже говорилось, слизистая оболочка языка богата вкусовыми рецепторами, расположенными преимущественно в сосочках. При их атрофии могут появляться различные вкусовые нарушения, начиная со снижения аппетита и непереносимости некоторых видов продуктов (обычно кислой и соленой пищи), и заканчивая извращением вкуса, пристрастием к поеданию земли, глины, сырого мяса и других несъедобных вещей. Нарушения обоняния могут проявляться обонятельными галлюцинациями (ощущением запахов, которых на самом деле нет) либо пристрастием к непривычным запахам (лака, краски, бензина и другим). Склонность к инфекционным заболеваниям
Важно отметить, что лечение железодефицитной анемии будет неэффективным, если не выявить и не устранить причину ее возникновения. В диагностике железодефицитной анемии применяется:
Первое, что должен сделать врач при подозрении на железодефицитную анемию – это тщательно опросить и обследовать пациента. Врач может задать следующий вопросы:
Во время обследования врач оценивает:
Это первый анализ, назначаемый всем пациентам при подозрении на анемию. Он позволяет подтвердить или опровергнуть наличие анемии, а также дает косвенную информацию о состоянии кроветворения в красном костном мозге. Кровь для общего анализа может браться из пальца или из вены. Первый вариант более подходит в том случае, если общий анализ является единственным лабораторным исследованием, назначенным пациенту (когда достаточно небольшого количества крови). Перед взятием крови кожу пальца всегда обрабатывают ватой, смоченной в 70% спирте, чтобы избежать занесения инфекции. Прокол производится специальной одноразовой иглой (скарификатором) на глубину 2 – 3 мм. Кровотечение в данном случае несильное и полностью останавливается практически сразу после взятия крови. В том случае, если планируется выполнять сразу несколько исследований (например, общий и биохимический анализ) – берут венозную кровь, так как ее легче получить в больших количествах. Перед забором крови на среднюю треть плеча накладывается резиновый жгут, что приводит к наполнению вен кровью и облегчает определение их местоположения под кожей. Место прокола также должно быть обработано спиртовым раствором, после чего медсестра одноразовым шприцем прокалывает вену и набирает кровь для анализа. Полученную одним из описанных методов кровь направляют в лабораторию, где она исследуется в гематологическом анализаторе – современном высокоточном приборе, имеющемся в большинстве лабораторий мира. Часть полученной крови окрашивают специальными красителями и исследуют в световом микроскопе, что позволяет визуально оценить форму эритроцитов, их строение, а при отсутствии или неисправности гематологического анализатора – произвести подсчет всех клеточных элементов крови. При железодефицитной анемии мазок периферической крови характеризуется:
В ходе данного исследования удается установить концентрацию различных химических веществ, находящихся в крови. Это дает информацию о состоянии внутренних органов (печени, почек, костного мозга и других), а также позволяет выявить множество заболеваний. Существует несколько десятков биохимических показателей, определяемых в крови. В данном разделе будут описаны только те из них, которые имеют значение в диагностике железодефицитной анемии.
Данное исследование заключается в прокалывании одной из костей организма (обычно грудины) специальной полой иглой и заборе нескольких миллилитров вещества костного мозга, которое потом исследуется под микроскопом. Это позволяет напрямую оценить выраженность изменения структуры и функции органа. В начале заболевания никаких изменений в пунктате костного мозга не будет. При развитии анемии может отмечаться разрастание эритроидного ростка кроветворения (увеличения количества клеток-предшественниц эритроцитов). Для выявления причины железодефицитной анемии применяется:
Причиной появления крови в кале (мелены) может стать кровотечение из язвы, распад опухоли, болезнь Крона, неспецифический язвенный колит и другие заболевания. Обильные кровотечения легко определяются визуально по изменению цвета каловых масс на ярко-красный (при кровотечении из нижних отелов кишечника) или черный (при кровотечении из сосудов пищевода, желудка и верхнего отдела кишечника). Массивные однократные кровотечения практически не приводит к развитию железодефицитной анемии, так как быстро диагностируются и устраняются. Опасность в этом плане представляют длительные, небольшие по объему кровопотери, возникающие при повреждении (или изъязвлении) мелких сосудов желудочно-кишечного трата. В таком случае выявить кровь в кале возможно только с помощью специального исследования, которое назначается во всех случаях анемии неясного генеза. С целью выявления опухолей или язв желудка и кишечника, которые могли стать причиной хронического кровотечения, применяется рентген с контрастом. В роли контраста используется вещество, которое не поглощает рентгеновские лучи. Обычно это взвесь бария в воде, которую пациент должен выпить непосредственно перед началом исследования. Барий покрывает слизистые оболочки пищевода, желудка и кишечника, в результате чего на рентгеновском снимке становится четко различима их форма, контур и различные деформации. Перед проведением исследования необходимо исключить прием пищи в течение последних 8 часов, а при исследовании нижних отделов кишечника назначаются очистительные клизмы. В данную группу включен ряд исследований, суть которых заключается во введении в полости организма специального аппарата с видеокамерой на одном конце, подсоединенной к монитору. Этот метод позволяет визуально исследовать слизистые оболочки внутренних органов, оценить их строение и функцию, а также выявить опухоль или кровотечение. С целью установления причины железодефицитной анемии используется:
При выявлении заболевания различных систем и органов гематолог может привлекать специалистов из других областей медицины с целью постановки более точного диагноза и назначения адекватного лечения. Для выявления причины железодефицитной анемии может понадобиться консультация:
Основным направлением в терапии данного заболевания является использование препаратов железа. Диетотерапия, хотя и является важным этапом лечения, не в состоянии самостоятельно восполнить дефицит железа в организме. Методом выбора являются таблетированные формы препаратов. Парентеральное (внутривенное или внутримышечное) введение железа назначается в случае, если невозможно полноценное всасывание данного микроэлемента в кишечнике (например, после удаления части двенадцатиперстной кишки), необходимо быстро восполнить запасы железа (при массивной кровопотере) либо при развитии побочных реакций от применения пероральных форм препарата.
Рекомендуемые дозы:
Перерыв между двумя последующими приемами железа должен составлять не менее 6 часов, так как в этот период клетки кишечника невосприимчивы к новым дозам препарата. Длительность лечения – 4 – 6 месяцев. После нормализации уровня гемоглобина переходят на поддерживающую дозу (30 – 50 мг/сутки) еще на 2 – 3 месяца. | Критериями эффективности лечения являются:
Данные критерии используются для контроля эффективности лечения всеми препаратами железа. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сорбифер Дурулес | Одна таблетка препарата содержит 320 мг сульфата железа и 60 мг аскорбиновой кислоты, которая улучшает всасывание данного микроэлемента в кишечнике. | Принимать внутрь, не разжевывая, за 30 минут до еды, запивая стаканом воды. Рекомендуемые дозы:
После нормализации уровня гемоглобина переходят на поддерживающую терапию (20 – 50 мг 1 раз в сутки). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ферро-фольгамма | Комплексный медикамент, который содержит:
Данный препарат назначается женщинам во время беременности (когда повышается риск развития дефицита железа, фолиевой кислоты и витаминов), а также при различных заболеваниях желудочно-кишечного тракта, когда нарушается всасывание не только железа, но и многих других веществ. | Принимать внутрь, за 30 минут до еды, по 1 – 2 капсулы 2 раза в день. Период лечения – 1 – 4 месяца (в зависимости от основного заболевания). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Феррум Лек | Препарат железа для внутривенного введения. | Внутривенно, капельно, медленно. Перед введением препарат необходимо разбавить в растворе хлорида натрия (0,9%) в пропорции 1:20. Доза и длительность применения определяются лечащим врачом индивидуально в каждом конкретном случае. При внутривенном введении железа высок риск передозировки, поэтому данная процедура должна выполняться только в условиях стационара под контролем специалиста. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Важно помнить, что некоторые лекарственные средства (и другие вещества) могут в значительной степени ускорять либо замедлять скорость всасывания железа в кишечнике. Применять их совместно с препаратами железа стоит осторожно, так как это может привести к передозировке последних, или, наоборот, к отсутствию лечебного эффекта.
| Медикаменты, способствующие всасыванию железа | Вещества, препятствующие всасыванию железа |
|
|
При неосложненном течении и правильно проводимом лечении необходимости в данной процедуре нет.
Показаниями к переливанию эритроцитов являются:
- массивная кровопотеря;
- снижение концентрации гемоглобина менее 70 г/л;
- стойкое снижение систолического артериального давления (ниже 70 миллиметров ртутного столба);
- предстоящее хирургическое вмешательство;
- предстоящие роды.
Эритроциты следует переливать максимально короткий промежуток времени, пока не будет устранена угроза жизни пациента. Данная процедура может осложниться различными аллергическими реакциями, поэтому перед ее началом необходимо провести целый ряд тестов на определение совместимости крови донора и реципиента.

Причиной затруднений в лечении железодефицитной анемии может быть:
- неправильно выставленный диагноз;
- неустановленная причина дефицита железа;
- поздно начатое лечение;
- прием недостаточных доз препаратов железа;
- нарушение режима приема медикаментов или диеты.
При нарушениях в диагностике и лечении заболевания возможно развитие различных осложнений, некоторые из которых могут представлять опасность для здоровья и жизни человека.
Осложнениями железодефицитной анемии могут быть:
- Отставание в росте и развитии. Данное осложнение характерно для детей. Оно обусловлено ишемией и связанными с ней изменениями в различных органах, в том числе в ткани головного мозга. Отмечается как задержка физического развития, так и нарушение интеллектуальных способностей ребенка, которые при длительном течении заболевания могут оказаться необратимыми.
- Анемическая кома. Развитие комы обусловлено критическим снижением доставки кислорода к головному мозгу. Внешне это проявляется потерей сознания, отсутствием реакции на речь и болевые раздражители. Кома является опасным для жизни состоянием, требующим срочной медицинской помощи.
- Развитие недостаточности внутренних органов. При длительном дефиците железа и наличии анемии могут поражаться практически все органы человека. Наиболее характерным является развитие сердечной недостаточности, почечной недостаточности и печеночной недостаточности.
- Инфекционные осложнения. Часто рецидивирующие инфекции могут сопровождаться поражением внутренних органов и развитием сепсиса (попадания гноеродных бактерий в кровоток и ткани организма), что особенно опасно у детей и людей пожилого возраста.
источник


 Железодефицитная анемия (ЖДА) – заболевание крови, вызываемое недостаточным поступлением железа в организм либо нарушением процессов его утилизации. ЖДА не является первичным заболеванием, а всегда обусловлена какой-либо патологией. Дефицит железа в организме приводит к нарушению процессов кроветворения – нарушается синтез гемоглобина в эритроцитах, в результате чего снижается их количество и функциональные способности.
Железодефицитная анемия (ЖДА) – заболевание крови, вызываемое недостаточным поступлением железа в организм либо нарушением процессов его утилизации. ЖДА не является первичным заболеванием, а всегда обусловлена какой-либо патологией. Дефицит железа в организме приводит к нарушению процессов кроветворения – нарушается синтез гемоглобина в эритроцитах, в результате чего снижается их количество и функциональные способности. Анемия – это патологическое состояние, характеризующееся уменьшением концентрации эритроцитов и гемоглобина в крови. Если развитие данного состояния обусловлено недостаточным поступлением железа в красный костный мозг и связанным с этим нарушением эритропоэза, то анемия называется железодефицитной.
Анемия – это патологическое состояние, характеризующееся уменьшением концентрации эритроцитов и гемоглобина в крови. Если развитие данного состояния обусловлено недостаточным поступлением железа в красный костный мозг и связанным с этим нарушением эритропоэза, то анемия называется железодефицитной. Железодефицитная анемия может развиться как в результате недостаточного поступления железа в организм, так и при нарушении процессов его использования.
Железодефицитная анемия может развиться как в результате недостаточного поступления железа в организм, так и при нарушении процессов его использования.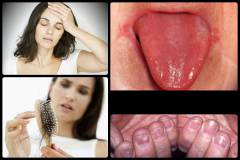 Симптомы данного заболевания обусловлены, недостатком железа в организме и нарушением кроветворения в красном костном мозге. Стоит отметить, что дефицит железа развивается постепенно, поэтому в начале заболевания симптоматика может быть довольно скудной. Латентный (скрытый) дефицит железа в организме может привести к появлению симптомов сидеропенического (железодефицитного) синдрома. Несколько позже развивается анемический синдром, тяжесть которого обусловлена уровнем гемоглобина и эритроцитов в организме, а также скоростью развития анемии (чем быстрее она развивается, тем выраженнее будут клинические проявления), компенсаторными возможностями организма (у детей и пожилых людей они менее развиты) и наличием сопутствующих заболеваний.
Симптомы данного заболевания обусловлены, недостатком железа в организме и нарушением кроветворения в красном костном мозге. Стоит отметить, что дефицит железа развивается постепенно, поэтому в начале заболевания симптоматика может быть довольно скудной. Латентный (скрытый) дефицит железа в организме может привести к появлению симптомов сидеропенического (железодефицитного) синдрома. Несколько позже развивается анемический синдром, тяжесть которого обусловлена уровнем гемоглобина и эритроцитов в организме, а также скоростью развития анемии (чем быстрее она развивается, тем выраженнее будут клинические проявления), компенсаторными возможностями организма (у детей и пожилых людей они менее развиты) и наличием сопутствующих заболеваний. Врач любой специальности может заподозрить наличие анемии у человека, основываясь на внешних проявлениях данного заболевания. Однако установлением вида анемии, выявлением ее причины и назначением соответствующего лечения должен заниматься врач-гематолог. В процессе диагностики он может назначить целый ряд дополнительных лабораторных и инструментальных исследований, а при необходимости привлечь специалистов из других областей медицины.
Врач любой специальности может заподозрить наличие анемии у человека, основываясь на внешних проявлениях данного заболевания. Однако установлением вида анемии, выявлением ее причины и назначением соответствующего лечения должен заниматься врач-гематолог. В процессе диагностики он может назначить целый ряд дополнительных лабораторных и инструментальных исследований, а при необходимости привлечь специалистов из других областей медицины.