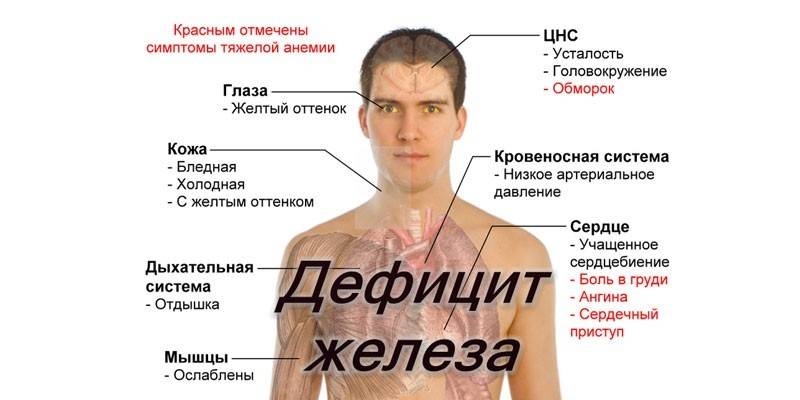
При необходимости профилактики или лечения уже существующей железодефицитной анемии пациенту назначаются препараты железа. Симптомы опасного заболевания могут развиваться в любом возрасте, при беременности, лактации, неправильном рационе. В таких ситуациях врачи прописывают сиропы, капсулы, растворы на основе солей или гидроксида железа.
Чтобы врач смог назначить препараты с железом пациенту, он должен диагностировать железодефицитную анемию. Она развивается по следующим причинам:
- Хронические кровотечения – на их долю выпадает 80% всех случаев развития заболеваний. К ним относятся поражения желудочно-кишечного тракта при язве, геморрое, опухолях, эрозивном гастрите, дивертикулезе кишечника. У женщин анемия развивается вследствие обильных месячных, миомы матки, кровотечений. У всех остальных причина связана с легочными, носовыми потерями крови, пиелонефритом, мочекаменной болезнью, злокачественными опухолями мочевого пузыря и почек.
- Хронические воспалительные заболевания – при наличии в организме очага воспаления железо депонируется, что приводит к его скрытому дефициту. Вместо формирования гемоглобина элемент просто копится в депо и не расходуется.
- Беременность, грудное вскармливание, физические нагрузки, интенсивный рост детей, активные занятия спортом – все эти состояния вызывают повышенную потребность в микроэлементе.
- Нарушение усвоения железа – состояние, сопровождающее некоторые болезни, например, синдром мальабсорбции, амилоидоз кишечника, хронический энтерит, резекция тонкой кишки.
- Неправильный и плохо сбалансированный рацион питания – такое характерно для новорожденных и маленьких детей, вегетарианцев.
Препараты при железодефицитной анемии назначаются, если есть отклонения от нормы в потреблении железа. Его суточные показатели:
Потребность железа в сутки, мг
Вне зависимости от того, сколько железа содержит пища, за сутки кишечником всасывается не более 2 мг микроэлемента при условии, что человек здоров. За сутки взрослый мужчина с волосами и эпителием теряет около 1 мг железа, а женщина при месячных – 1,5 мг. При условии нормального питания в депо мужчины попадает 1 мг микроэлемента, женщины – 0,5 мг. При плохом питании, хронических болезнях, обильных месячных железо полностью расходуется, так начинается развиваться анемия.
Для нормализации выработки гемоглобина назначают пероральные препараты железа. Врач смотрит на анализы, прописывает курс длиной несколько месяцев для пополнения депо. Женщинам детородного возраста для профилактики анемии необходимо принимать витамины или биологически активные добавки с добавлением железа (200 мг чистого элемента в сутки) семь дней месячных в течение каждого месяца.
На начальных стадиях развития железодефицитной анемии признаки не проявляются. Со временем они развиваются в следующие:
- Слабость, вялость, быстрая утомляемость.
- Головокружение, потеря аппетита и вкуса.
- Бледность и сухость кожи, ломкость волос, слоение ногтей.
- Чрезмерное выпадение волос.
- Трещины в уголках рта.
- Одышка, учащенное сердцебиение.
- Сглаженность вкусовых сосочков на языке.
- У беременных может появиться странное пристрастие – есть мел или землю.
Препараты для лечения железодефицитной анемии содержат двухвалентное или трехвалентное железо. Соли первого соединения поглощаются клетками слизистой оболочки органов желудочно-кишечного тракта. Это происходит путем связывания апоферритина в энтероцитах с ионами. Из-за этого препараты солей сульфата, глюконата, фумарата, лактата, сукцината и глутамата обладают повышенной биодоступностью и доступной ценой.
К недостаткам солей двухвалентного железа относятся высокий уровень желудочно-кишечных побочных эффектов, снижение доступности при сочетании с лекарствами, танинами, антацидами. Средства назначают только натощак, их передозировка грозит острым отравлением, особенно у детей младшего возраста. Гематологи рекомендуют не более 200 мг препаратов в сутки (в пересчете на элементарное железо), а для беременных – 100-120 мг.
Соли трехвалентного железа менее предпочтительны, потому что для поглощения ионов они должны восстановиться до двухвалентного элемента. Это приводит к меньшей биодоступности препаратов. Еще одной причиной сложности приема становятся легкий гидролиз солей в верхних отделах тонкого кишечника, образование малорастворимых гидроксидов и снижение их усвояемости.
Препараты железа для внутривенного введения менее предпочтительны по сравнению с таблетками, драже, каплями, капсулами и сиропами. Лучшие средства для лечения железодефицитной анемии:
Препараты железа при анемии
Форма железа, концентрация
2 таблетки ежедневно, курсом 3-4 месяца
Сульфат, 113 мг на капсулу
Хлорид, сульфат, 325 на 1 шт.
1-2 шт. ежедневно курсом до 12 недель
150-300 мг в день в 2-3 приема
Протеинсукцинилат, 800 на флакон
По 1-2 флакона в два приема каждый день
900 за 20 флаконов по 15 мл
Таблетки, капли, сироп, пероральный и парентеральный растворы
Гидроксид полимальтозат, 100 на шт.
Гидроксид полиизомальтазат, 100 на 1 мл
100-200 мг трижды в неделю
Гидроксид полимальтозат, 41,6 на мл
Раствор для внутривенного введения
Гидроксид сахарозный комплекс, 540 на мл
Раствор для внутримышечного и внутривенного введения
Гидроксид декстран, 50 на мл
100-200 мг дважды в неделю внутримышечно
Гидроксид сахарозный комплекс, 25 на мл
Железо в ампулах для инъекций для детей не назначается, если только у них не обнаружена тяжелая железодефицитная анемия. Ребенку прописываются драже, сиропы или капли. Их прием помогает улучшить кровоснабжение кислородом сосудов головного мозга. От рождения и до двух лет можно применять Гемофер, Мальтофер, Актиферрин. С 2 до 5 лет малышам дают сиропы Ферронал, Актиферрин, Феррум Лек. Они снабжены мерным колпачком для удобного измерения лекарства. Дети старше пяти лет могут принимать таблетки. Они не окрашивают эмаль зубов в желтый цвет.
Преимущество следует отдать капсулам с защитной оболочкой Актиферрин, Гемофер, Феррум Лек, Тардиферон. Дозировка назначается врачом, но не должна превышать 3 мг на кг веса в сутки. Длительность курса составит 2-6 месяцев. Таблетки глотаются целиком, их нельзя разжевывать, но можно запивать водой. Во время лечения следует обогатить детский рацион питания мясом, фруктами, овощами. Если препараты содержит двухвалентное железо, в питание включают продукты, богатые витамином С, трехвалентное – аминокислотами.
Если у будущей матери диагностирована анемия, ей следует обратиться к врачу за назначением лекарственного препарата. Лечение производится стандартными средствами, при выборе которых учитывается дефицит витамина В12, аллергологический анамнез. Чтобы лечение было эффективным, беременной женщине нужно скорректировать свое питание – включить в него бобовые, отруби, овсянку, гречку, сухофрукты.
Для профилактики анемии назначают 30-40 мг железа в сутки в третьем триместре. При склонности к анемии профилактика проводится на 12-14 и 21-25 неделях – во время этого 30-40 мг микроэлемента принимается 2-3 раза еженедельно. Если обнаружена устойчивая железодефицитная анемия, женщине необходимо пропивать по 100-200 мг препаратов ежедневно. При условии, что беременная страдала от анемии и до зачатия, во время вынашивания ребенка необходимо пить по 200 мг средств. Во время лактации прием продолжается.
Чтобы железосодержащие препараты при анемии эффективно помогли в борьбе с заболеванием, нужно знать особенности их приема. Врачи рекомендуют придерживаться следующих правил:
- Нельзя назначать препараты самостоятельно, менять дозировку. Иначе это грозит осложнениями и отравлением. При беременности прием лекарств сопровождается строгим контролем врача.
- Парентерально средства используются при операциях на органах пищеварительного тракта, удалении части желудка или кишечника, при обострении язвы, панкреатите, энтерите, неспецифическом язвенном колите.
- Запрещено сочетать препараты железа со средствами на основе кальция, антибиотиками тетрациклинами, антацидами, Левомицетином.
- Если в процессе терапии пациент страдает от диспепсии, ему прописывают ферментные препараты Фестал, Панкреатин.
- Улучшать всасывание железа могут сорбит, аскорбиновая, лимонная, янтарная кислоты, медь, витамины В6, В1, А, Е, кобальт.
- Железосодержащие препараты желательно принимать между приемами еды.
- Если на фоне лечения у пациента проявляются негативные симптомы, лекарство заменяют.
- Анемия лечится назначением первоначальной минимальной дозы с постепенным ее повышением. Процесс терапии длительный – сначала 2 месяца дозы лечебные, потом 2-3 месяца они профилактические.
- Примерная суточная дозировка для взрослого человека – 180-200 мг ежедневно. Примерно за три недели железодефицитная анемия корректируется наполовину, а через два месяца она излечивается.
- Если у пациента отмечается непереносимость средства, то замена его другим препаратом железа при анемии не поможет – отрицательно действует элемент. В таком случае лекарство принимают после еды или снижают дозировку, увеличивая курс лечения до полугода.
У железосодержащих медикаментов существуют свои противопоказания. Их нельзя применять при следующих состояниях:
- лейкоз, онкология крови;
- апластическая, гемолитическая анемия;
- хронические заболевания печени, почек;
- одновременный прием с антацидами, тетрациклинами, препаратами кальция, пищевыми продуктами, богатыми кальцием, кофеином, клетчаткой.
Таблетированные и другие формы железосодержащих средств могут приводить к побочным действиям. Чаще они проявляются со стороны желудочно-кишечного тракта, при приеме двухвалентных солей. К побочным реакциям относятся:
- тошнота, рвота, боль в желудке;
- снижение аппетита, расстройства стула, метеоризм, запор;
- слабость, головные, мышечные боли, головокружение;
- сыпь на коже, зуд;
- боли в суставах;
- металлический привкус во рту;
- тахикардия, гипотензия;
- потемнение кала;
- покраснение кожи лица;
- отек, краснота при уколе, повышение температуры;
- анафилактический шок;
- лимфаденопатия.
источник
Железодефицитная анемия (малокровие) обычно рассматривают скорее в качестве симптома другого заболевания или в виде состояния, возникающего при недостаточной концентрации в организме железа.
Причины и факторы, способствующие развитию анемического синдрома:
- Развивается болезнь у маленьких детей и взрослых, соблюдающих строгую диету, если они не получают необходимого количества железа с едой.
- На фоне нарушений в пищеварительной системе. Известно, что всасывание микроэлементов происходит в тонкой кишке (верхние отделы) и в желудке. А тем более, после удаления части желудка, способность пищеварительной системы к абсорбции нарушается.
- Анемический синдром может развиться из-за больших потерь крови. Это является основной причиной железодефицитных состояний. Часто синдром возникает у женщин из-за больших потерь крови во время обильной менструации и у тех, кто страдает от язвы пищеварительного тракта, рака желудка, геморроя, новообразований в толстой кишке.
- Сокращение времени жизни эритроцитов в крови или быстрое их разрушение. В норме срок жизни эритроцита – 4 месяца. В некоторых случаях причиной гемолиза является патология селезенки. Развивается гемолитическая или серповидно-клеточная анемия. При таком заболевании организмом вырабатывается аномальный гемоглобин.
При подозрении на анемию, важно оперативно обратится за помощью к специалисту. Врач поможет выявить причины и способы лечения болезни. Синдром приводит к снижению иммунитета, к упадку сил, ограничению работоспособности. Также анемия может стать важным сигналом о развитии других патологий и серьезных проблем в работе отдельных органов и их систем.
Диагноз ставят по анализу крови, а лечение, как правило, заключается в восстановлении количества железа с помощью лек. препаратов. Лекарства используют внутрь или вводят с помощью инъекций.
| Пол, возраст | Порог Нb (Г/Л) | Порог Нb (Г/%) |
| Дети от 3 месяцев до 5 лет | 110 | 11,0 |
| Дети от 5 до 12 лет | 115 | 11,5 |
| Дети от 12 до 15 лет | 120 | 12,0 |
| Мужчины от 15 лет | 130 — 160 | 13,0 — 16,0 |
| Женщины от 15 лет | 120 — 140 | 12,0 — 14,0 |
| Беременные женщины | 110 | 11,0 |
Можно выделить 3 основных механизма развития анемии:
- Вследствие нарушения процесса образования эритроцитов и образования гемоглобина. Такого рода механизм можно проследить при недостаточном поступлении железа, фолиевой кислоты и витамина В12, при заболеваниях костного мозга. Иногда дефицитное состояние может возникнуть из-за приема сверхбольших доз витамина С. При приеме сверх доз аскорбиновой к-ты происходит блокировка витамина В12 и нарушение процессов кроветворения.
- Острая потеря эритроцитов. Обычно – это последствия острых кровотечений, операций и травм. При хронических кровотечениях в небольших объемах причиной анемии выступает не просто потеря эритроцитов, но и недостаток железа на фоне хронической утраты крови.
- Анемический синдром — последствия от ускоренного разрушения эритроцитов крови. При нормальной работе костного мозга и иных органов кроветворения эритроциты живут порядка 4 месяцев, а затем разрушаются. При гемолитической анемии, гемоглобинопатии и так далее скорость разрушения эритроцитов выше, чем их производства. Иногда процесс протекает под влиянием внешних стимулов, химических веществ (уксус).
Рассмотрим различные виды у взрослых. Анемия является симптомом, а не отдельным заболеванием и может возникать при ряде болезней. Они, как правило, связаны с первичным поражением кроветворной системы или не зависят от нее. Невозможно провести четкую нозологическую классификацию анемий. Для этого используют принцип практической целесообразности. И в результате заболевание делят по единому классификационному признаку – по цветовому показателю.
Падение уровня гемоглобина в крови чаще всего наблюдают при одновременном снижении количества и качества эритроцитов. Любой вид анемии непременно приводит к снижению эффективности дыхательной функции крови, возникновению кислородного голодания тканей. Обычно это видно по бледности кожных покровов, слабости, высокой утомляемости, головным болям, головокружении, одышке, учащенному ритму сердца и т.д.
Врач назначает рутинное исследование мазка крови, в процессе анализа морфолог обязан указать на отклонения размера эритроцитов. Уменьшение может быть, как в меньшую (микроцитарная анемия), так и большую сторону (макроцитарная). Однако, если необходимую оценку производят без специальных микрометров, то она является весьма субъективной.
Анемии, которые могут развиться при болезнях почек, гипопластические, АХЗ и острую постгеморрагическую относят к нормоцитарным. Макроцитарные анемии бывают нормо- и гиперхромными, а микроцитарные – гипохромными.
Намного информативнее автоматический анализ крови, при котором соблюдается четкая стандартизация важных показателей. Учитывают средний корпускулярный объем (СКО), который можно измерить в фемтолитрах (fl, фл). Нормальное значение СКО составляет 80-90 фл и называется нормоцитозом. Если показатель повышен до 95 и более – то фиксируют развитие макроцитоза. При снижении менее 80 фл ставят диагноз микроцитоз. Есть у автоматического метода и свои недостатки: достаточно дорогое и чуткое оборудование, которому необходимо соответствующее обслуживание.
При замене цветового показателя на СКО не нарушается привычная классификация анемий по цветовому показателю. Анемии подразделяют на группы по различным признакам. Классификацию, как правило, основывают на удобстве и практической значимости для постановки диагноза.
Цветовой показатель покажет степень насыщения эритроцита гемоглобином. У здорового человека ЦП колеблется 0,86 до 1,1. В зависимости от него различают такие анемии:
- Гипохромная анемия, если ЦП меньше 0,86 (по некоторым классификациям ниже 0,8). При таких анализах ставят диагноз талассемия или железодефицитная анемия.
- При нормохромной анемии ЦП колеблется в пределах 0,86 — 1,1. В таком случае у пациента наблюдается постгеморрагическая анемии, гемолитические анемии, апластические анемии, неопластические заболевания костного мозга, внекостномозговые опухоли, анемия из-за снижения темпов выработки и количества эритропоэтина.
- Гиперхромная анемия – при ЦП более 1,1. Такие показатели характерны для фолиеводефицитной анемии, а также витамин B12-дефицитной анемии, для миелодиспластического синдрома.
Проводится в зависимости от выраженности снижения уровня гемоглобина в крови. Классификация по степени тяжести предполагает:
- легкую степень (когда уровень гемоглобина ниже нормы, но остается на уровне более 90 грамм на литр);
- среднюю степень тяжести (когда гемоглобин 70-90 г/л);
- тяжелую степень (когда уровень гемоглобина остается меньше 70 грамм на литр).
Разделение степени анемии по уровню гемоглобина достаточно распространено. Чаще всего именно по гемоглобину подтверждают диагноз, а потом уже проводят более детальную диагностику.
Характеризуется незначительным падением количества гемоглобина в крови. Обычно проявляются следующие симптомы:
- усталость;
- апатия;
- общее недомогание;
- часто развивается у беременных.
Как уже упоминалось выше, анемия 1 степени фиксируется, если уровень микроэлементов в крови ниже нормы, но выше 90 г на л.
Также первая степень заболевания часто поражает маленьких детей, появившихся на свет при многоплодной беременности или недоношенными. У детей постарше – это паразитические заболевания или погрешности в питании. Анемия легкой степени тяжести проще поддается лечению. Обычно рекомендуют соблюдать диету и усиленно питаться. При легкой степени анемии в рацион необходимо включать различные микроэлементы и витамины, в первую очередь – железо и витамин В12.
Анемия 2 степени или средней степени тяжести возникает не только при снижении уровня гемоглобина до 70 г/л. Возникает головокружение и головные боли, одышка, частое сердцебиение, трудности с дыханием. Дети часто болеют, у них наблюдается бледность губ и кожи. При 2 степени анемии может возникнуть кислородное голодание плода, снижается сократительная способность миокарда. Лечение медикаментозное + диета, следует больше находится и гулять по свежему воздуху.
На этой стадии острая анемия несет опасность для жизни человека. При 3 степени наблюдается ломкость ногтей и волос, острое снижение защитных сил организма, онемение конечностей, проблемы с сердцем и сосудами. Ребенок начинает часто болеть.
Особенно тяжелыми будут последствия такого симптома у беременных женщин. Это может негативно отразится на плоде, у матери развиться дистрофические изменения матки и плаценты. Анемия 3 степени лечится в стационаре, с переливанием эритроцитарной массы и другими видами медикаментозного лечения.
Основным признаком такого разделения принято считать количество молодых эритроцитов (ретикулоциты) в периферической картине крови. В норме показатель колеблется от 0,5 до 2%.
- Арегенераторную анемию (например, апластическая анемия) — ретикулоциты отсутствуют.
- Гипорегенераторная (витамин B12-дефицитная анемия или железодефицитная анемия) – ретикулоциты ниже 0,5%.
- Регенераторная или норморегенераторная (постгеморрагическая) — ретикулоциты 0,5 — 2%.
- Гиперрегенераторная (гемолитические анемии) — количество ретикулоцитов больше 2%.
Такая классификация основывается на различных механизмах развития анемии, как патологического процесса.
- Ассоциированные с дефицитом Fe — железодефицитные анемии.
- Гемолитические анемии — связанные с повышенным разрушением эритроцитов.
- Гис-гемолитические анемии — при нарушении кровообразования, протекающего в красном костном мозге.
- Постгеморрагические анемии — при острой или хронической кровопотере.
- В12- и фолиеводефицитные анемии.
Мегалобластные анемии: миокардит гемолитический и пернициозная анемия.
Гипохромия — это общее название для разных форм анемии, при которых цветовой показатель крови, вследствие недостатка гемоглобина, меньше 0,8. Не включена в список нозологических единиц. В анализе крови средний показатель для гемоглобина при таком состоянии меньше 30 пикограмм, а средняя концентрация гемоглобина в эритроците составляет менее 330 г на литр. Меняется не только цвет, но и диаметр (макро- или микроцитоз) и форма. Чаще всего при такого рода патологии красной крови кровяные тельца приобретают вид колец с бледно-красной серединой и темно-красными краями (обесцвечиваются).
Патологические формы эритроцитов могут возникать вследствие:
- Железодефицитной анемии при кровопотерях (геморрагическая), нарушении усвоения железа, при невынашивании плода и т.д.
- Хронического отравления свинцом.
- Талассемии – нарушения нормального процесса синтеза полипептидных цепей в структуре гемоглобина.
- Нарушения синтеза и утилизации порфиринов.
- Гиповитаминоза В6.
- При нарушении обмена вещества, хронических воспалительных процессах неинфекционного и инфекционного генезиса.
Дизэритропоэтическая анемия – целая группа достаточно редко встречающихся заболеваний крови, которые возникают из-за нарушения процессов эритропоэза. При этом, большая часть молодых эритроцитов погибает сразу после образования в костном мозге, а количество нормоцитов значительно снижается. Такого рода расстройство предполагает качественный, количественный, кинетический или совмещенный характер нарушения эритропоэза.
Следует упомянуть такую разновидность заболевания — гиперхромная макроцитарная анемия или малокровие. При котором также наблюдают снижение числа эритроцитов и уровня гемоглобина в единичном объеме крови. Как правило, при такого рода нарушениях параллельно дают сбой сердце и сосуды.
По коду МКБ-10 — D62 острая постгеморрагическая анемия. Такой симптом возникает после кровопотери. Подразделяют на острую постгеморрагическую анемию и хроническую постгеморрагическую анемию. Острая анемия развивается после острых и обильных кровотечений, хронические анемии возникают после длительных несильных кровотечений.
Во время быстрой кровопотери значительно снижается объем циркулирующей крови. В ответ на такое событие происходит компенсаторная реакция, которая заключается в возбуждении симпатического отдела нервной системы и рефлекторного спазма сосудов. Пульс ускоряется и ослабевает. Сосуды кожи и мышц максимально сужаются, кровь приливает к сосудам мозга, коронарным сосудам, что поддерживает снабжение кровью жизненно важных органов. При прогрессировании процесса начинает развиваться постгеморрагический шок.
Характерным клиническим симптомом постгеморрагической анемии является острая сосудистая недостаточность из-за гиповолемии (опустошение сосудистого русла). Внешне это проявляется ортостатическим коллапсом, одышкой, учащенным сердцебиением. В первые минуты кровопотери уровень гемоглобина может даже быть высоким, но после поступления тканевой жидкости в русло сосудов данный показатель снижается, даже если кровотечение уже прекратилось. Цветовой показатель остается в норме, одновременно происходит утрата эритроцитов и железа, нормохромная анемия. Ко вторым суткам увеличивается число ретикулоцитов, максимальных показателей достигает на 4-7 день (гиперрегенераторная анемия).
Диагноз ставят на основании клинических признаков и лабораторных показателей, повышения уровня остаточного азота, если кровотечение происходила в верхних отделах ЖКТ. Самое важное при такой нормохромной анемии – это устранить саму кровопотерю, восполнить устраненный объем крови эритроцитарной массой и гепарином (до 60% утраченной крови), кровезаменителями (5% р-р Альбумина, Раствор Рингера, Реополиглюкин).
При постановке диагноза постгеморрагическая анемия необходимо учитывать сведения о произошедшей острой кровопотере при наличии внешнего кровотечения. После массивного внутреннего диагноз основывают на клинических признаках и, в обязательном порядке, лабораторных пробах (Вебера, Грегерсена). Основанием для постановки диагноза также послужит рост уровня остаточного азота при кровотечении из верхнего отдела пищеварительного тракта.
После того, как кризис и острый период миновали, пациенту назначают препараты железа, витамины группы В, Е и С. Такая терапия производится в течение 6 месяцев. При утрате более 50% от объема циркулирующей крови — прогноз неблагоприятный.
Состояние может развиться в результате снижения поступления в организм фолиевой кислоты или нарушения процессов ее всасывания в пищеварительном тракте. Лечение заключается в дополнительном приеме недостающего вещества.
В отличии от патологии, ассоциированной с недостатком В12, фолиеводефицитная анемия диагностируется значительно реже.
Одной из основных причин фолиеводефицитной анемии является недостаточное содержание фолиевой к-ты в рационе. Следует помнить, что нужно включать в свое ежедневное меню больше зелени и печени. Также на здоровье значительно влияет алкогольная интоксикация, беременность, злокачественные новообразования, некоторые дерматиты, гемолиз.
Такого вида заболевания возникает при нарушении всасывания (например, при целиакии), под действием лекарственных средств, Метотрексата, Триамтерена, противосудорожных средств, барбитуратов, Метформина и др. Значительно повышается нужна организма в фолиевой кислоте после гемодиализа и при болезнях печени.
Также на здоровье оказывает влияние дефицит цианокобаламина и его кофермента – метилкобаламина. В таких условиях не происходит трансформации фолиевой кислоты в коферментную форму. В результате нарушается процесс нормального клеточного деления, начинают страдать клетки кроветворной ткани, которые ранее активно размножались. Тормозятся процессы созревания и размножения эритроцитов, сокращается их продолжительность жизни. Изменения касаются и лейкоцитов, возникает лейкопения и тромбоцитопения.
Далее в результате неправильного митоза появляются гигантские клетки эпителия пищевого канала и развиваются воспалительные процессы в слизистой оболочке, стоматиты, гастриты, эзофагиты, энтерит. Еще больше усугубляется первичное нарушения секреции и процесс всасывания внутреннего фактора, усиливается дефицит витаминов. Возникает порочный круг.
Из-за возникшего недостатка цианокобаламина, в организме начинают накапливаться продукты обмена, которые токсичны для нервных клеток. В волокнах тем временам начинают синтезироваться жирные кислоты уже с искаженной структурой. Наблюдается плавное изменение качества клеток спинного мозга и поражаются периферические и черепные нервные сплетения, развивается неврологическая симптоматика.
При таком виде анемии, как правило симптомы у пациента наблюдаются стандартные: высокая утомляемость, учащенное сердцебиение, бледность ногтей и губ, ярко-красный язык. На начальных стадиях отследить признаки поражения НС и ЖКТ практически невозможно. По результатам обследования выявляется гиперхромная макроцитарная анемия, лейкопения, тромбоцитопения. А лечение с помощью витамина В12 не вызывает улучшений лабораторных показателей. Диагноз можно подтвердить с помощью определения уровня сывороточной фолиевой к-ты и в эритроцитах. В норме ее содержание составляет от 100 до 450 нг/л. При фолиеводефицитной анемии концентрация фолиевой кислоты в эритроцитах значительно снижается.
Если проводят анализ периферической картины крови, то отмечают гиперхромную (макроцитарную) анемию при общем снижении уровня гемоглобина и эритроцитов. Непрямой билирубин меняется редко.
В качестве профилактики и для лечения фолиеводефицитной анемии должны назначить фолиевую кислоту в дозе 1 мг/сут, внутрь. Если есть необходимость врач может увеличить дозу. Улучшения должны наступать через в течение 3-4 суток, в том числе проходить должны и неврологические симптомы. В противном случае приходится говорить о недостатке именно витамина В12, а не фолиевой к-ты.
Обязательно проводить профилактику недостатка фолиевой к-ты у беременных женщин и пациентов, принимающих некоторые группы лек. препаратов. Для профилактики назначают 5 мг вещества в сутки.
Относится к виду витаминодефицитных (мегалобластных) анемий, которые возникают при недостаточном поступлении в организм витамина В12 (цианокобаламина). В результате В12-дефицитной анемии поражается кроветворная функция, нервная и пищеварительная система. В отличие от фолиеводефицитной В12-анемии, она развивается в преклонном или старческом возрасте, чаще всего у мужской половины. Проявляется заболевание постепенно.
Человек, страдающий В12-дефицитной анемией, будет испытывать общие симптомы: слабость, пониженная работоспособность, одышка, головокружение, жжение за грудиной, боли в ногах и языке, парестезии, шаткость походки. Такие симптомы будут сочетаться с желтушным цветом кожи, глосситом, незначительным увеличением печени и селезенки, негромким систолическим шумом, глухостью тонов сердца. Нередко поражается и нервная система, развивается комбинированный склероз или фуникулярный миелоз, нарушается чувствительность, полиневрит, атрофия мышц, паралич нижних конечностей.
Развивается анемия из-за недостатка витамина В12, из-за несбалансированности питания, голодания, алкоголизма и отсутствия аппетита. Также синдром может наблюдаться на фоне мальабсорбции, целиакии, изменений в слизистой оболочке кишечника, спру, лимфомы кишечника, болезни Крона, регионарного илеита, из-за длительного приема противосудорожных препаратов.
Вероятность развития В12-дефицитной анемии будет выше при беременности, гемолитической анемии, псориазе, эксфолиативном дерматите. При приеме алкоголя, препаратов–антагонистов фолатов, врождённых нарушениях метаболизма и атрофическом гастрите также может наблюдаться это заболевание.
Как правило, поставить диагноз В12-дефицитная анемия можно без особых проблем. Это может сделать гематолог, невролог, нефролог или гастроэнтеролог по результатам общего и биохимического анализа крови, наличию метилмалоновой кислоты. Также проводят УЗИ брюшной полости и исследование всасывания витамина В12 с помощью радиоизотопов. По показаниям можно провести аспирационную биопсию костного мозга.
Лечение проводят витамином В12 внутримышечно. В течение 1-1,5 месяцев используют поддерживающую дозу. Если уровень гемоглобина упал менее 60 г на л, при нарушении гемодинамики и угрозе анемической комы проводят трансфузии эритроцитов.
В качестве профилактики при заболеваниях, сопровождающихся нарушением всасывания витамина В12, а также после операций нужно под контролем содержания витамина В12 в моче и крови применять профилактические и лечебные курсы витаминотерапии.
Что это такое простыми словами? Это процесс ускоренного разрушения красных кровяных телец, он сопровождается значительным ростом уровня прямого билирубина в крови. Заболевание встречается достаточно редко.
Общим признаком можно считать ускоренное разрушение эритроцитов, сопровождающееся с одной стороны анемией и повышенным образованием продуктов распада эритроцитов, а с другой – реактивно усиленным эритропоэзом.
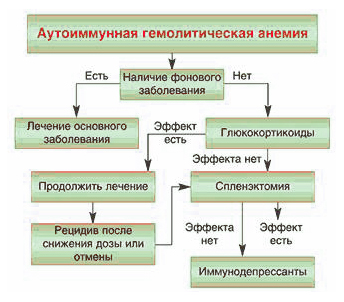
Аутоиммунная гемолитическая анемия, как правило вызвана генетическими дефектами мембран эритроцитов, что вызывает их повышенное разрушение. Аутоиммунное заболевание и гемолиз эритроцитов при приобретенных анемиях наступает под действием внутренних факторов или каких-либо факторов окружающей среды.
На развитие иммунных гемолитических анемий влияют посттрансфузионные реакции, вакцинации, прием некоторых препаратов (сульфаниламидов, анальгетиков, противомалярийных лекарств, производных нитрофуранового ряда). Также такой симптом может проявляться при гемобластозах, аутоиммунных патологиях (НЯК, СКВ), инфекционных болезнях (мононуклеоз, вирусная пневмония, сифилис, токсоплазмоз).
Гемолитические анемии можно поделить на два обширные группы заболеваний: приобретенные и врожденные.
Формы наследственных заболеваний:
- Эритроцитарные мембранопатии, такие как анемия Минковского-Шоффара или болезнь Минковского-Шоффара (микросфероцитоз), акантоцитоз, овалоцитоз, вызванные аномалиями в структуре мембран эритроцитов. Отметим, что сфероцитоз – самый распространенный вид среди патологий (микросфероцитоз).
- Энзимопении, вызванные дефицитом некоторых ферментов (пируваткиназа, глюкозо-6-фосфатдегидрогеназа).
- Гемоглобинопатии, возникшие из-за качественных нарушений структуры гемоглобина или изменения соотношения его нормальных форм.
Приобретенные гемолитические анемии делят на:
- Приобретенные мембранопатии (шпороклеточная анемия, болезнь Маркиафавы-Микели).
- Изо- и аутоиммунные, вызванные действием антител.
- Токсические, возникшие вследствие воздействия ядов, токсинов или других хим. агентов.
- Анемии, ассоциированные с механическими повреждениями в структуре эритроцитов.
Рост концентрации остаточных следов после распада эритроцитов в организме внешне будет проявляться желтухой лимонного оттенка. Также будет наблюдаться повышение концентрации в крови непрямого билирубина и железа. Отмечается уробилинурия и плейохромия кала и желчи. При внутрисосудистом гемолизе дополнительно развивается гипергемоглобинемия, гемоглобинурия, гемосидеринурия. Об усилении эритропоэза говорит ретикулоцитоз и полихроматофилия в составе периферической крови, либо эритронормобластоз костного мозга.
Если у пациента не микросфероцитарная анемия, обусловленная наследственным сфероцитозом или эллиптоцитозом, то необходимо, прежде всего проводить адекватную терапию заболевания, вызвавшего причину гемолитической анемии.
Для лечения обычно применяют:
- медикаменты (например, Десферал);
- спленэктомию;
- трансфузию эритроцитов при кризе;
- ГСК при аутоимунных заболеваниях в средней дозировке.
Апластическая анемия — заболевание, которое относят к категории миелодисплазий. При таком заболевании происходит резкое угнетение или прекращение роста и созревания клеток в костном мозге, еще называемое панмиелофтизом.
Типичными симптомами болезни являются: лейкопения, анемия, лимфопения и тромбоцитопения. Сам термин впервые появился в начале 20 века. Такое заболевание имеет достаточно тяжелое течение и без лечения (в том числе медикаментозного препаратом Атгам) имеет неблагоприятный прогноз.
Очень долго эту болезнь рассматривали в качестве синдрома, объединяющего различные патологические состояния в костном мозгу. В настоящее время термин «апластическая анемия» выделяется в качестве самостоятельной нозологической единицы. Его следует четко разграничивать от синдрома гипоплазии в кроветворной системе.
Апластическая анемия может быть вызвана различными причинами:
- химическими агентами, бензолом, солями тяжелых металлов и так далее;
- ионизирующим излучением;
- приемом некоторых лекарств, цитостатиков, НПВС, Анальгина, Мерказолила, Левомицетина;
- вирусами;
- наличием других аутоиммунных заболеваний.
Также существует форма апластической анемии, передающейся по наследству — анемия Фанкони. Лечение болезни заключается в приеме иммунодепрессантов и проведении пересадки костного мозга.
При серповидно-клеточной анемии человека происходит нарушение строения белка гемоглобина, он приобретает нетипичное кристаллическое строение, в виде серпа. Такую форму называют S-гемоглобином. Заболевание связывают с мутацией НВВ-гена, из-за которой в костном мозге начинает синтезироваться аномальный вид S-гемоглобина, в шестом положении в В-цепи вместо глутаминовой кислоты находится валин. Происходит полимеризация S-гемоглобина, образуются длинные тяжи, эритроциты приобретают форму серпа.
Тип наследования серповидноклеточной анемии – аутосомно-рецессивный при неполном доминировании. У гетерозиготных носителей в эритроцитах находится примерно равное количество гемоглобина А и S. Носители сами не болеют, а выявить серповидные эритроциты можно случайно при проведении лабораторного обследования. Симптомы же могут и вовсе не проявляться. Иногда такие люди начинают ощущать недомогание при гипоксии или тяжелом обезвоживании.
У гомозигот в крови есть только гемоглобин S, заболевание протекает достаточно тяжело. У таких больных высокий уровень степени разрушенных эритроцитов в селезенке, значительно короче срок жизни, часто проявляются признаки хронической недостаточности кислорода.
Такой вид анемии достаточно распространен в регионах, где высокий уровень заболеваемости малярией. У таких больных выше устойчивость к разным штаммам малярийного плазмодия. Поэтому столь вредные аллели часто проявляются у жителей Африки.
Симптомы сильно различаются и их можно наблюдать у детей уже с 3-х месячного возраста. Анемия может приводить к потере сознания, меньшей выносливости, вызвать желтуху. У младенцев наблюдается худоба, слабость, искривление конечностей, удлиненность туловища, изменения в строение черепа и зубов. Также у больных детей повышенная склонность к развитию сепсиса. У подростков наблюдают задержку развития на 2-3 года. Женщины, как правило, способны к зачатию и рождению ребенка.
Мегалобластная анемия (болезнь Аддисона-Бирмера, В12-дефицитная, пернициозная) — заболевание, вызванное недостатком фолиевой кислоты или витамина В12. Происходит это из-за недостатка веществ в пище или при заболеваниях пищеварительного тракта. Также мегалобластическая анемия может возникнуть при врожденных нарушениях процессов синтеза ДНК, приобретенных патологиях и из-за приема некоторых лекарств (антиметаболитов, противосудорожных).
При постоянном недостатке фолиевой кислоты и В12 развивается хроническая анемия, эритроциты изменяют свою форму и размеры. Более легкие стадии иногда протекают бессимптомно, далее начинают уже проявляться внешние признаки. Такое дефицитное состояние часто также называют пернициозной анемией. Заболевание получило статус анемии хронических заболеваний, так как проявляется у пациентов после 60 лет и у перенесших гепатит больных, при энтерите и раке кишечника. Подробнее о такого рода анемиях описано выше.
Развивается вследствие эндогенного В12-авитаминоза, вызванного атрофией желез фундального отдела желудка, которые в норме должны вырабатывать гастромукопротеин. В результате нарушаются процессы всасывания витамина В12 и возникает злокачественная анемия «пернициозного» типа. Чаще всего такой диагноз ставят в возрасте от 50 лет.
Болезнь сопровождается нарушениями нервной, сердечно-сосудистой, кроветворной и пищеварительной системы. Больные обычно жалуются на одышку, общую слабость, отечность ног, боли в сердце, «мурашки» по стопам и кистям, жгучие боли в языке и шаткость походки. По лабораторным показателям наблюдают анемию гиперхромного типа, лейкопению, тромбоцитопению.
Сидеробластная анемия также имеет название сидероахрестическая анемия (САА), железорефрактерная, железонасыщенная или сидеробластическая. Это патологическое состояние нарушений процесса синтеза микроэлементов и кроветворения, чаще всего – железа. Эритроциты содержат малое количество железа, из-за того, что микроэлемент активно расходуется костным мозгом и начинает накапливаться во внутренних органах. Заболевание развивается на фоне недостаточного содержания протопорфирина.
Выделяют две формы болезни:
- пиридоксин-зависимую, возникающую вследствие дефицита пиридоксальфосфата;
- пиридоксин-резистентную, развивающуюся из-за ферментного дефекта (дефицита гемсинтетазы).
Приобретенные формы сидероахрестической анемии чаще наблюдаются в пожилом возрасте, но болезнь не наследуется от родителей. Часто такого рода анемия развивается, как побочный эффект от лечения препаратами от туберкулеза или истощении пиридоксальфосфата при отравлении свинцом, при алкоголизме, миелопролиферативных болезнях крови, кожной порфирии. Встречаются и идиопатические формы САА.
Это редкое, передающееся по наследству заболевание. Анемия Фанкони встречается у 1 из 350000 детей. Наибольшее распространение заболевание получила среди евреев-ашкеназов и жителей Южной Африки.
Возникает из-за наличия дефектов в белковых кластерах, отвечающих за процесс репарации ДНК. Для заболевания характерная высокая ломкость у хромосом, наличие у пациентов старше 40 лет миелоидного лейкоза и апластической анемии.
Для новорожденных с таким недугом характерны врожденные дефекты развития, необычная пигментация, низкорослость, аномалии развития скелета и некоторые неврологические симптомы (косоглазие или недоразвитость одного из глаз, глухота, умственная отсталость), аномалии развития внутренних органов. К сожалению, в среднем такие пациенты живут не более 30 лет.
У диагноза неуточненная анемия код по МКБ-10 D64.9. Это первичный диагноз, который уточняется после проведения обследования у врача, так как он является вторичным признаком какого-либо основного заболеваний. Прежде всего следует исключить возможность кровопотери вследствие травм, хирургических вмешательств, внутренних кровотечений, далее проводится лабораторная диагностика.
По международной классификации МКБ-10 для миелодиспластического синдрома:
- D46.0 Рефрактерная анемия без сидеробластов, так обозначенная;
- D46.1 Рефрактерная анемия с сидеробластами;
- D46.2 Рефрактерная анемия с избытком бластов;
- D46.3 Рефрактерная анемия с избытком бластов с трансформацией;
- D46.4 Рефрактерная анемия неуточненная;
- D46.7 Другие миелодиспластические синдромы;
- D46.9 Миелодиспластический синдром неуточненный.
Приставка «рефрактерная» означает устойчивость заболевания к приему витаминов, препаратов железа, соблюдению диеты. Чаще всего такого вида анемия является наиболее распространенным видом миелодиспластического синдрома. Из-за нарушений процессов созревания бластов в крови значительно понижено содержание гемоглобина, проявляются признаки острого лейкоза. Примерно у 40% пациентов с миелодиспластическим синдромом проявляется рефрактерная анемия. Чаще всего гемоглобинопатия такого рода развивается у пациентов от 50 лет.
Заболевание можно считать промежуточным этапом между рефрактерной анемией и острым лейкозом. Как правило, болезнь проявляется снижением уровня гемоглобина и общей слабостью. Если у больного не нашли других причин для таких изменений картины крови, то основной задачей врачей становится дообследовать пациента и максимально затормозить наступление острого лейкоза.
Что за болезнь талассемия? Это наследуемое по рецессивному типу заболевание, развивающееся из-за снижения синтеза полипептидных цепей в структуре гемоглобина. В зависимости от того, какой мономер перестал нормально синтезироваться различают альфа-, бета-талассемию и дельта-талассемию. Также болезнь классифицируют по степени клинических проявлений, разделяют на тяжелую, легкую и среднюю.
Альфа-талассемия ассоциирована мутациями в генах HBA2 и HBA1. Альфа-цепь кодируется четырьмя локусами и, в зависимости от количества аномальных – различают разные степени тяжести заболевания. Симптомы и течение гемоглобинопатии варьируют от легкой до тяжелой степени гипохромной микроцитарной анемии.
Бета-талассемия существует в двух наиболее распространенных вариантах: малая (minor) и CD8(-AA) – большая (наиболее тяжелая форма заболевания). Анемия развивается из-за мутаций обоих аллелей бета-глобина, когда гемоглобин А начинает вытесняться гемоглобином F. Обычно малая талассемия имеет легкое течение и лечение не требуется.
Согласно Википедии, анемия Даймонда-Блекфена представляет собой наследственную форму красноклеточной аплазии с точно не выявленным типом наследования. Предполагают, что заболевание имеет аутосомно-доминантный тип наследования, который встречается у одной четвертой всех больных. У таких больных обычно проявляются проявления анемии в течение первого года жизни, слабость, бледность, повышенная утомляемость, снижение количества эритроцитов в плазме крови.
Диагноз ставят по общему анализу крови, показателям уровня эритропоэтинов, микроскопии и биопсии костного мозга. Лечению болезнь поддается плохо, назначают ГКС, гемотрансфузии.
Повышение концентрации свободного гемоглобина в плазме крови называют гемоглобинемией. Заболевание возникает вследствие приобретенных и врожденных заболеваний эритроцитов, при повышенном их разрушении. Симптом может проявиться после неправильно проведенного переливания крови, из-за воздействия паразитарных и инфекционных факторов (сепсиса, вирусной инфекции, малярии), после сильного переохлаждения, отравления ядами, бензином, уксусной кислотой, грибами. Проявляется внешне это гиперемией кожных покровов и слизистой, повышением концентрации гемоглобина и билирубина в крови.
Существуют настолько разные причины заболевания, что выявить некоторые из них можно только после проведения лабораторных исследований. Часто бывает, что показатели гемоглобина в норме, а железо низкое. Недуг может наблюдаться при недостатке витаминов группы В, фолиевой к-ты. Малокровие у человека возникает вследствие различных травм и обильных внутренних или внешних кровотечений.
Такой диагнозе женщине могут поставить, если уровень гемоглобина в крови падает ниже 120 г на литр. В целом у женщин, из-за некоторых физиологических особенностей выше склонность к данному недугу. Ежемесячные кровопотери во время менструации, когда в течение недели женщина может потерять до 100 мл крови, беременность, лактация и снижение концентрации ферритина – самые распространенные причины анемии. Часто заболевание развивается из-за психосоматики, когда у женщины депрессивное состояние, она плохо питается, редко выходят на свежий воздух, не занимается спортом или во время климакса, когда происходят глобальные изменения в физиологии женщины.
У мужской половины данный диагноз ставится, если уровень гемоглобина снизился менее 130 г на л. По статистике заболевание возникает реже. Чаще всего из-за каких-то хронических заболеваний, нарушений работы органов и их систем (язвенная болезнь, геморрой, эрозии в кишечнике, доброкачественные и злокачественные новообразования, паразиты, апластическая анемия). Существуют и генетические причины (анемия Фанкони) заболевания, которые не связаны с полом.
Малокровие проявляется по-разному, в зависимости от конкретного вида заболевания. Известно, что при малокровии у человека уменьшается количество эритроцитов, изменяется их строение, содержание железа в крови, падает гемоглобин. Ткани человека испытывают недостаток кислорода и это оказывает влияние на общее состояние и внешний вид человека.
Общие признаки анемии, следующие:
- значительно сниженная работоспособность, общая слабость;
- раздражительность, повышенная утомляемость, сильная сонливость;
- шум в ушах и головные боли, «мушки» перед глазами, головокружения;
- дизурия;
- непреодолимое желание полакомится мелом или известью;
- постоянная одышка;
- тонкие и ломкие волосы, ногти, сухая, неэластичная кожа;
- стенокардия, низкое артериальное давление;
- шум в ушах и частые обмороки;
- изменение цвета стула, желтуха, бледность;
- ломота в теле и суставах, мышечная слабость.
Также существуют специфические симптомы малокровия, характерные для той или ной разновидности:
- Железодефицитная анемия. Для данного диагноза характерная парорексия, у пациента появляется сильное желание жевать мел, землю, бумаги и прочие несъедобные материалы. Можно также выделить койлонихию, трещинки в уголках рта, заеды, воспаленный язык. Иногда может повыситься температура до субфебрильной.
- Основным симптомом В12-дефицитной анемии можно назвать покалывание в конечностях, нестойкость походки, скованность и стесненность в движениях, низкое чувство осязания. У пациента снижаются когнитивные способности, могут возникать галлюцинации. В крайне тяжелых случаях может развиться паранойя или шизофрения.
- Характерным симптомом серповидноклеточной анемии может быть слабость, приступообразные боли в брюшной полости и суставах.
- При отравлении свинцовыми отходами у пострадавшего наблюдаются характерные темно-синие линии на деснах, тошнота и болезненные ощущения в области живота.
- Хроническое разрушение эритроцитов может быть симптомом злокачественной опухоли. В таком состоянии развивается проступающая желтуха, язвы и ссадины на ногах, покраснение мочи. Часто образуются камни в желчном пузыре.
Поставить точный диагноз гемолитическая, мегалобластная или апластическая анемия можно после проведения дифференциальной диагностики. Диф. диагностика проводится по соответствующим таблицам и результатам лабораторных исследований.
источник
Клинические симптомы, признаки и классификация анемий. Причины и последствия снижения количества эритроцитов, гемоглобина и гематокрита. Определение концентрации ферритина в сыворотке крови. Сравнительная характеристика железосодержащих препаратов.
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://allbest.ru
Государственное автономное образовательное учреждение среднего профессионального образования Республики Татарстан «Казанский медицинский колледж»
Средства для лечения анемий
Выполнила студентка группы5302-0
Состояния, которые сопровождаются снижением количества эритроцитов, концентрации гемоглобина и гематокрита, объединены общим понятием анемия.
Основные клинические симптомы анемии обусловлены снижением доставки кислорода к тканям. Существует множество возможных причин анемии, поэтому она не рассматривается как самостоятельное заболевание, а скорее, бывает проявлением какой-то другой болезни, которую необходимо выявить для того, чтобы лечение от него и от анемии было успешным.
Независимо от причины, анемия сопровождается снижением содержания гемоглобина в крови. Поэтому определение концентрации гемоглобина в крови играет важнейшую роль в диагностике анемий. Пониженное количество эритроцитов и гематокрита- признаки анемии.
Заключение о наличии анемии основывается на результатах определения концентрации гемоглобина и величины гематокрита в крови: для мужчин это снижение количества гемоглобина ниже 135 г/л и показателя гематокрита ниже 40%, для женщин ниже 115 г/л и ниже 35% соответственно. У детей уровень гемоглобина в норме ниже, чем у взрослых, поэтому анемию диагностируют при содержании гемоглобина менее 110 г/л. При анемиях содержание гемоглобина варьирует в широких пределах и зависит от степени ее выраженности. Чем ниже результат, тем анемия тяжелее. Снижение количества эритроцитов и гематокрита зависит не только от тяжести, но и от причины анемии.
Всасывание железа (главным образом, в виде его двухвалентной формы) происходит преимущественно в начальной части тонкого кишечника, однако оно имеет место и в других его отделах. Улучшает всасывание железа аскорбиновая кислота.
В желудке железо попадает сначала в клетки слизистой, где оно образует комплекс с белком апоферритином — ферритин. Железо, не соединившееся с апоферритином, поступает в плазму, там взаимодействует с трансферрином и в виде комплекса с ним транспортируется в костный мозг, клетки печени и другие клетки.
В крови содержится лишь небольшое количество ферритина, который высвобождается из разрушающихся клеток различных тканей. При дефиците железа его всасывание значительно увеличивается, при этом контроль за усвоением железа может быть нарушен, что приводит к его избытку и отложению в органах в виде гемосидерина. Нарушение всасывания наблюдается при патологии тонкого кишечника и гастроэктомии.
При этом в щелочном содержимом кишечника возможно образование нерастворимых соединений, например фосфата железа, в результате чего не усваиваются даже большие дозы назначаемых препаратов. Установлено, что железо может усваиваться в той или иной степени из всех его соединений, попадающих в желудок. Нарушение всасывания имеет место при одновременном назначении тетрациклина и десферроксамина. Дефицит железа проявляется гипохромной микроцитарной анемией.
Помимо снижения среднего объема эритроцитов и содержания в них гемоглобина уменьшена концентрация железа и ферритина в плазме, увеличена способность плазмы связывать железо, что обусловлено трансферрином.
Наиболее частыми клиническими признаками анемии являются:
1) Бледность кожных покровов и видимых слизистых оболочек
2) Утомляемость и сонливость
3) Одышка, особенно при физической нагрузке
4) Головокружение, обмороки
6) Учащение пульса, сердцебиение, тахикардия
· дефицитные анемии (железодефицитные анемии, В12 и фолиево-дефицитные анемии, белководефицитные и др.).
· постгеморрагические (острая постгеморрагическая и хроническая постгеморрагическая).
· гемолитические (наследственный сфероцитоз, талласемия, серповидноклеточная анемия и др.).
· гипорегенераторные (ретикулоцитов в крови меньше нормы — дефицитные анемии, хроническая постгеморрагическая анемия).
· гиперрегенераторные (гемолитические анемии, острая постгеморрагическая анемия).
· гипохромные (железодефицитные анемии)
· гиперхромные (В12 и фолиево-дефицитная анемия).
Следует иметь в виду, что при некоторых системных заболеваниях, протекающих с гипохромной анемией, содержание ферритина в плазме соответствует норме или повышено, что указывает на нарушенное усвоение железа, которое поступает в организм в достаточном количестве. В этом случае терапия препаратами железа не показана.
Также нет основания проводить такую терапию при гемолитической анемии.
Лечение препаратами железа проводится при дефиците его вследствие:
3) патологии желудочно-кишечного тракта с уменьшением всасывания железа и во время лечения тяжелой пернициозной анемии, когда запасы железа могут истощаться вследствие очень активного кроветворения.
При лечении препаратами железа в таблетках следует начинать с малых доз, повышая их через несколько дней во избежание передозировки и токсических реакций.
Все препараты содержат несколько видов солей железа. Чаще всего сульфат железа (феррокаль, тардиферон,ферроплекс и т.д.); аскорбинат железа, лактат железа, трехвалентное железо (очень редко).
Существует два показателя в выборе дозы препарата: общее содержание соли железа и содержание свободного железа. Например, гемостимулин содержит соли железа 240 мг, а свободного железа 50 мг; ферроплекс — соли 50 мг, свободного железа 10 мг. Дело в том, что при назначении препаратов железа доза рассчитывается не по солевому составу, а по содержанию свободного железа.
Минимальная суточная доза свободного железа должна составлять не менее 100 мг. Оптимальной суточной дозой является 150-200 мг. Если оптимальная доза хорошо переносится, то можно увеличить дозу до 300-400 мг (максимальная пероральная доза).
При этом обычно, скорость увеличения прироста железа в крови будет составлять 0.3 — 0.5 г% в сутки.
Если увеличивать дозу еще больше к положительному эффекту не приводит так как всасывание не увеличивается. Терапевтический диапазон доз составляет 100-400 мг. Выбор зависит от индивидуальной переносимости железа, выраженности анемии.
Обычно суточная доза делится на 3-4 приема. При назначении высоких доз (более 200 мг), то целесообразно делить такие дозы на 6-8 приемов, так как считается что переносимость высоких доз улучшается при дробном приеме.
Для того чтобы улучшить переносимость препаратов железа, улучшить их всасывание рекомендуют за час до приема препаратов железа принимать панкреатин, фестал и другие ферментные препараты. Можно применять мед. Если при приеме железа до еды появляются диспепсические расстройства, то можно назначать железо через 2 часа после еды.
Сульфат железа выпускается в таблетках по 0,2 г, которые содержат 60 мг элементарного железа. Назначают его по 0,2—0,6 г/сут. Феррамид — комплексное соединение железа с никотиновой кислотой (таблетки по 0,1 г). Назначают взрослым до 0,5 г/сут.
Сравнительная оценка переносимости различных препаратов затруднительна. Лучше начинать лечение с сульфата железа, при его плохой переносимости переходить на глюконат и т. д. Включение в терапию аскорбиновой кислоты улучшает усвоение железа и позволяет уменьшить назначаемую дозу.
При плохой переносимости указанных препаратов могут применяться соединения, из которых железо высвобождается медленно после прохождения привратника: феоспан особенно хорош для профилактики анемийбеременных. Ферроплекс — драже, содержащее 50 мг железа в виде его сульфата и 30 мг аскорбиновой кислоты.
Состав и форма выпуска: Активное вещество железо III (в форме комплекса с мальтозой). Раствор для в/м введения (1 мл — 0,05 г активного вещества) 2 мл в ампулах по 50 штук в упаковке. Активное вещество — железо III в форме сахарата. Раствор для в/в (1 мл — 0,02 г активного вещества) 5 мл в ампулах по 50 штук в упаковке.
Фармакологическое действие: Микроэлемент железо, входящее в состав препарата быстро восполняет нехватку этого элемента в организме, стимулирует эритропоэз. При курсовом применении препаратов железа происходит постепенная регрессия клинических (слабость, утомляемость, головокружение, тахикардия, болезненность и сухость кожных покровов) и лабораторных симптомов анемии.
Режим дозирования: При в/м применении Феррум лек вводят через день в средней разовой дозе 2 мл, максимальная суточная доза — 4 мл. В/в — дозу, кратность применения и длительность лечения устанавливают индивидуально.
Курсовая доза препарата для конкретного больного может быть вычислена по формуле: масса тела больного (кг) х концентрация гемоглобина в крови (г/100 мл) х 2,5.
Побочное действие: При парентеральном применении: гиперемия кожных покровов, головокружение, тошнота, боль в спине или животе, затруднение дыхания, аллергические реакции в виде сыпи, зуда.
· все виды анемий, не вызванные дефицитом железа
· повышенная чувствительность к препарату
Особые указания: В/в введение производят медленно, в положении больного лежа. Препараты железа для парентерального применения нельзя смешивать в одном шприце с другими лекарственными средствами. Прием препарата необходимо продолжать и после нормализации картины крови, для того чтобы восполнить депо железа в организме. С осторожностью препарат назначают при пептической язве, регионарном энтерите, язвенном колите.
Лекарственное взаимодействие: Феррум лек не следует принимать одновременно с антибиотиками тетрациклинового ряда.
Ферковен для внутривенного введения (ампулы по 5 мл) включает в себя сахарат железа, глюконат кобальта и раствор углеводов. В 1 мл препарата содержится 20 мг железа. Вводят его внутривенно в течение 10— 15 дней, сначала по 2 мл, начиная с 3-го дня по 5 мл, разводя изотоническим раствором.
Для поддержания эффекта затем переходят на прием препарата внутрь.
Возможны побочные явления в виде гиперемии лица, шеи, изредка приступов стенокардии.
Сорбитол железа (жектофер) представляет собой низкомолекулярный комплекс железо — сорбитол — цитрат и содержит в 2 мл препарата 100 мг железа. За сутки почками выводится 30% дозы с мочой темного цвета (она может темнеть позже за счет образования под влиянием бактерий сульфида железа).
Препарат увеличивает лейкоцитурию у больных с инфекцией мочевыводящих путей, что следует учитывать при его назначении. Сорбитол железа связывается с глобулинами плазмы, трансферрином и откладывается в костном мозге и печени, особенно в ее ретикулоэндотелии. Несвязанная часть железа выделяется с мочой.
Сорбитол железа вводится внутримышечно (инъекции часто болезненны). Возможны реакции на введение: головная боль, головокружение, тошнота, дезориентация, иногда непосредственно после введения препарата ощущается металлический вкус во рту.
Декстран железа (имферон) содержит в 1 мл 50 мг железа. Может вводиться как внутримышечно, так и внутривенно. Имеет высокую молекулярную массу и медленно всасывается из места введения в мышцу. Не исключено, что многократное введение препарата в один участок мышцы, где часть его длительно сохраняется, может способствовать канцерогенезу. Декстран железа не связывается с трансферрином и накапливается в основном в ретикулоэндотелии. Прием препаратов железа внутрь приводит к потемнению кала и может дать ложноположительные результаты проб на кровь в кале.
Терапия препаратами железа должна продолжаться до восстановления уровня гемоглобина и затем еще 2 мес. в меньших дозах для пополнения запасов железа в организме. Длительное лечение массивными дозами препаратов может привести к развитию гемосидероза.
При отсутствии достаточного терапевтического эффекта от приема препаратов внутрь (в связи с нарушением всасывания в кишечнике) назначают железо для парентерального введения.
Общая доза препарата для парентерального введения рассчитывается по специальным формулам. Введение декстрана железа может осложняться лихорадкой, крапивницей, артралгией, лимфаденопатией.
При терапии препаратами железа железодефицитной анемии реакция кроветворения в виде повышения ретикулоцитоза наблюдается в пределах 7 дней. Повышение уровня гемоглобина на 50% происходит приблизительно в течение 1 мес. Однако восстановление запасов железа происходит позже, в течение еще нескольких месяцев. Величина этих запасов оценивается по уровню ферритина плазмы, который повышается позже, чем содержание гемоглобина.
Большие дозы препаратов железа, принимаемых внутрь, могут вызвать диспептические явления вследствие раздражения (а иногда некроза) слизистой кишечника, особенно если доза железа превышает 180 мг/сут. При очень больших дозах может развиться коллапс и даже кома вследствие повреждения мозга и печени. анемия гемоглобин железосодержащий
Иногда у лиц, перенесших острое отравление с некрозами слизистой, позже (спустя 1—2 мес) развивается нарушение проходимости пищи в тонком кишечнике. Возможность такого отравления более вероятна у маленьких детей, так как препараты железа часто покрываются сладким, что делает их привлекательными для них.
При опасности острого отравления промывают желудок 1 % раствором соды, для связывания препаратов железа в желудочно-кишечном тракте назначают сырые яйца и молоко внутрь. Внутримышечно вводят 1—2 г десферроксиамина. Последний связывает железо с быстрым образованием ферроксамина, который выводится почками. Десферроксиамин применяют в общей дозе до 80 мг/кг массы тела в сутки.
При хронической перегрузке железом (у больных гемохроматозом, иногда при гемолитических анемиях и талассемии, требующих повторных переливаний крови) его приходится извлекать из организма с помощью кровопусканий (особенно при гемохроматозе). Одна венесекция (при отсутствии анемии) позволяет удалить 200 мг железа (500 мл крови) и может повторяться раз в неделю.
Прием препаратов железа внутрь приводит к потемнению кала и может дать ложноположительные результаты проб на кровь в кале.
Терапия препаратами железа должна продолжаться до восстановления уровня гемоглобина и затем еще 2 мес в меньших дозах для пополнения запасов железа в организме. Длительное лечение массивными дозами препаратов может привести к развитию гемосидероза.
Препараты железа назначают парентерально при плохой переносимости при приеме внутрь, нарушении всасывания в кишечнике (с отсутствием достаточного терапевтического эффекта от приема железа внутрь), по социальным показаниям. Общая доза препарата для парентерального введения рассчитывается по специальным формулам.
При терапии препаратами железа железодефицитной анемии реакция кроветворения в виде повышения ретикулоцитоза наблюдается в пределах 7 дней. Повышение уровня гемоглобина на 50% происходит приблизительно в течение 1 мес. Однако восстановление запасов железа происходит позже, в течение еще нескольких месяцев. Величина этих запасов оценивается по уровню ферритина плазмы.
Большие дозы препаратов железа, принимаемых внутрь, могут вызвать диспептические явления вследствие раздражения (а иногда некроза) слизистой кишечника, особенно если доза железа превышает 180 мг/сут. При очень больших дозах может развиться коллапс и даже кома вследствие повреждения мозга и печени.
При опасности острого отравления промывают желудок 1% раствором соды. Для связывания препаратов железа в желудочно-кишечном тракте назначают сырые яйца и молоко внутрь. Внутримышечно вводят 1-2 г (до 80 мг/кг в сутки) десферроксамина, который связывает железо и в виде ферроксамина выводится почками.
При хронической перегрузке железом (у больных гемохроматозом, иногда при гемолитических анемиях и талассемии, требующих повторных переливаний отмытых эритроцитов) приходится прибегать к кровопусканиям (особенно при гемохроматозе). Одна венесекция (при отсутствии анемии) позволяет удалить 200 мг железа (500 мл крови) и может повторяться раз в неделю.
Целесообразно назначение и микроэлементов (2—5 г в сутки): мед, кобальт, марганец. Они способствуют утилизации железа в организме, ускоряют биосинтез гемоглобина и стимулируют эритропоэз.
В некоторых случаях назначаются кортикостероидные и анаболические гормоны, которые способствуют более интенсивной утилизации железа эритробластами костного мозга.
Основными критериями эффективности терапии являются:
Повышение уровня железа в сыворотке крови, повышение концентрации гемоглобина, количества ретикулоцитов и эритроцитов. Нормализация гемоглобина еще не является основанием для отмены лечения, т. к. для пополнения запасов железа в органах и тканях необходима продолжительная поддерживающая терапия небольшими дозами того же препарата, которым был достигнут лечебный эффект.
Сравнительная характеристика железосодержащих препаратов для внутреннего применения
источник