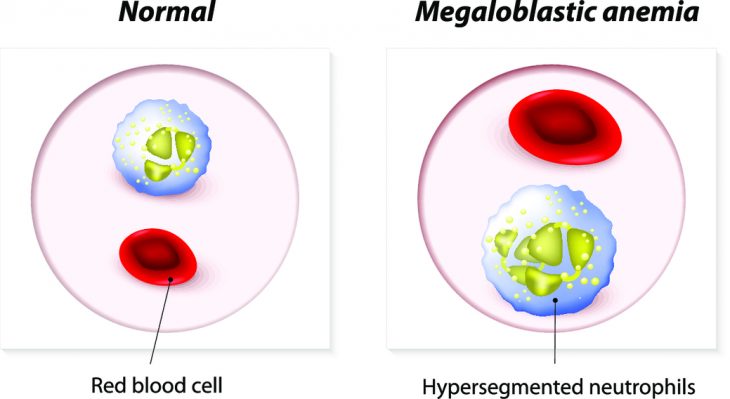
Одной из разновидностей анемий является мегалобластная, или В12-фолиеводефицитная анемия. Это заболевание, развивающееся вследствие нарушения процесса созревания эритроцитов в связи с нарушением синтеза в клетке РНК и ДНК, сопровождающееся наличием в костном мозге большого количества видоизмененных предшественников эритроцитов – мегалобластов.
Частота мегалобластной анемии составляет 9-10% всех случаев анемии. Страдают ею лица всех возрастов, однако у пожилых людей она встречается чаще, чем у молодых (4% и 0.1% соответственно). Мегалобластная анемия — это состояние, которое можно и нужно лечить. Причины, симптомы и лечение данного недуга рассмотрим в этой статье.
Причиной развития В12-фолиеводефицитной анемии является недостаток в организме витамина В12 (цианокобаламина) и фолиевой кислоты (витамина В9).
Дефицит фолиевой кислоты, как правило, возникает по следующим причинам:
- недостаточное поступление витамина с пищей при голодании;
- недостаточное всасывание его в кишечнике по причине различных заболеваний, таких как целиакия и другие энтеропатии;
- частичное или полное отсутствие у пациента тонкой кишки в результате резекции (удаления);
- повышенная потребность в витамине В9 в период беременности и кормления грудью, а также при некоторых формах гемолитических анемий, при эксфолиативном дерматите или в случае инвазии лентеца широкого — при дифиллоботриозе;
- повышенные потери его, например, при гемодиализе;
- хронические гепатиты, цирроз печени;
- хронический панкреатит;
- злоупотребление алкоголем;
- длительный прием некоторых медикаментов – комбинированных пероральных контрацептивов, противосудорожных препаратов, препаратов, замедляющих обмен веществ.
Причинами недостатка в организме цианокобаламина являются:
- вегетарианство;
- полипоз или рак дна желудка;
- хронический гастрит А;
- частичное или полное удаление желудка;
- синдром Золлингера-Эллисона;
- беременность и период кормления грудью;
- глистная инвазия;
- энтеропатии, в частности, целиакия;
- резекция тонкой кишки;
- болезнь Крона;
- цирроз печени и хронические гепатиты;
- недостаток фермента – транскобаламина II.
При дефиците в организма витаминов В9 и В12 нарушается синтез в клетках генетического материала – ДНК и РНК. Больше других при этом страдают клетки костного мозга и эпителия пищеварительного тракта – то есть клетки с высокой скоростью обновления. Клетки-предшественники эритроцитов теряют способность к дифференцировке (переходу из более молодых к более зрелым формам), однако их цитоплазма развивается, как и раньше: в результате образуются клетки огромных размеров, называемые мегалобластами.
Витамин В12 в организм человека поступает со всевозможными продуктами животного происхождения. Попадая в желудок, он связывается с особым веществом – гастромукопротеином, с которым продвигается по пищеварительному тракту далее – в тонкую кишку, где и всасывается. Суточная потребность в витамине В12 равна 3-7 мкг. Запасы его имеются в печени и составляют 3-5 мг. Потребность в фолиевой кислоте выше – 100 мкг в сутки, но и попадает в организм ее больше – при стандартной диете – 300-750 мкг. Запасы же витамина В9 составляют 5-10 мг.
Состоит витамин В12 из 2-х важных частей – коферментов. При недостатке первого нарушается синтез ДНК – нарушается созревание эритроидных клеток – формируется мегалобластный тип кроветворения. Помимо эритроцитов нарушается формирование лейкоцитов и тромбоцитов, однако эти изменения выражены в меньшей степени.
Также дефицит первого кофермента приводит к нарушению синтеза незаменимой аминокислоты – метионина, отвечающей за нормальную работу нервной системы. Вследствие недостатка второго кофермента в организме нарушается обмен жирных кислот – накапливаются токсичные вещества, частично поражающие спинной мозг – развивается состояние, называемое фуникулярный миелоз.
Подавляющее число мегалобластных анемий – В12-дефицитные. Клинические проявления их можно объединить в 4 группы – признаки поражения пищеварительного тракта, симптомы фуникулярного миелоза, циркуляторно-гипоксический синдром, психо-неврологические расстройства. Рассмотрим подробнее.
1. Признаки поражения пищеварительного тракта (возникают в связи с атрофией слизистой желудка, поражением слизистой верхнего отдела кишечника, недостаточной продукцией ферментов и вызванными этими изменениями нарушениями процессов переваривания и всасывания пищи):
- снижение аппетита;
- полное отвращение к мясной пище;
- пощипывание и боль кончика языка, нарушение вкуса, «лакированный» язык – эти симптомы объединили термином атрофический глоссит Хюнтера;
- тошнота, рвота;
- расстройства стула.
2. Симптомы фуникулярного миелоза:
- головная боль;
- ощущения покалывания, пощипывания, жжения в коже – парестезии;
- ощущение холода;
- шаткая, неустойчивая походка;
- ощущение онемения в конечностях;
- вялость в нижних конечностях;
- ограничение двигательной активности – парезы и, в особо тяжелых случаях, параличи.
3. Циркуляторно-гипоксический синдром:
- выраженная общая слабость;
- быстрая утомляемость;
- одышка при небольшой физической нагрузке или даже в покое;
- сердцебиение;
- разной интенсивности боли в области сердца;
- бледность, иногда – желтушность кожи.
4. Психо-неврологические расстройства:
- раздражительность;
- галлюцинации;
- судороги;
- сложность выполнения простых математических функций.
Заболевание, как правило, протекает в 2 стадии – субклиническую и клиническую. На первой стадии явные признаки гиповитаминоза отсутствуют, а пациенты предъявляют жалобы на легкое недомогание и незначительные диспепсические явления. Несмотря на отсутствие внешних клинических признаков снижение содержания витаминов в крови уже имеется. Когда истощаются запасы витаминов в организме либо же раньше, но после воздействия сильного провоцирующего фактора (например, на фоне психоэмоционального стресса или после серьезного оперативного вмешательства) заболевание вступает во вторую стадию – клиническую.
На фоне мегалобластной анемии обостряются и активно прогрессируют хронические соматические заболевания – стенокардия, аритмии. Появляются отеки.
Стоит отметить особенность течения мегалобластной анемии у пожилых лиц. Данная категория больных даже при достаточно низких значениях гемоглобина жалоб предъявляет мало, в то время как при железодефицитной анемии снижение этого показателя лишь до 110 г/л сопровождается значительным ухудшением состояния больного и множеством жалоб.
Врач заподозрит наличие анемии еще на этапе сбора жалоб, анамнеза и объективного обследования больного.
Обратят на себя внимание следующие изменения:
- бледность, иногда желтушность кожных покровов; цвет кожи при данном заболевании сравнивают с цветом пергамента;
- увеличенный в размере лакированный язык;
- при аускультации сердца – учащение его сокращений – тахикардия, систолический шум;
- при пальпации живота – увеличение селезенки – спленомегалия;
- при неврологическом обследовании – признаки фуникулярного миелоза.
В общем анализе крови отмечается снижение уровня гемоглобина и эритроцитов, повышение цветового показателя выше 1.1 (то есть, анемия – гиперхромная). У некоторых больных параллельно с эритропенией выявляется тромбо- и лейкопения. Также в крови определяются видоизмененные предшественники эритроцитов – мегалобласты, макроциты. Характерен анизоцитоз (изменение размеров клеток) и пойкилоцитоз (изменение их формы). В цитоплазме эритроцитов определяются специфичные элементы – кольца Кеббота и тельца Жолли. Также отмечается ретикулоцитопения.
Уровень витаминов В9 и/или В12 в сыворотке крови, конечно, ниже нормальных значений.
Поскольку мегалобластная анемия нередко сопровождается гемолизом эритроцитов, уровень железа в сыворотке крови не снижен, а находится в пределах нормы или же повышен. По этой же причине в сыворотке крови повышен и уровень свободного билирубина.
Для подтверждения диагноза проводят стернальную пункцию. В пунктате определяется мегалобластная трансформация костного мозга. Важно проводить пункцию до начала терапии больного витамином В12, так как уже через несколько часов после его введения состав костного мозга начинает возвращаться в норму, а через 1-2 суток проявления мегалобластного типа кроветворения исчезают вовсе.
Практически у всех больных помимо описанных выше изменений определяются атрофические изменения слизистой оболочки желудка, сниженное содержание соляной кислоты в нем – гипо- или даже ахлоргидрия.
В целом весь процесс обследования больного на предмет наличия у него мегалобластной анемии можно разделить на 3 этапа:
- Клинический анализ крови, в котором определяются вышеописанные, характерные для данного вида анемии, изменения.
- Определение уровня витаминов В9 и В12, стернальная пункция с последующим исследование пунктата.
- Установление причинного фактора анемии – подробное изучение данных анамнеза, обследование желудка (фиброгастроскопия, определение кислотности и так далее), кишечника, печени, определение наличия или отсутствия гельминтозов (исследование кала). Объем проводимых клинических исследований индивидуален для каждого больного и определяется конкретной клинической ситуацией.
В случае, если определена точная причина – этиологический фактор анемии, главным направление терапии является устранение его. Это может быть дегельментизация (если обнаружены глисты), удаление полипов или другой опухоли желудка хирургическим путем, адекватная терапия болезней кишечника, борьба с алкоголизмом и так далее.
Параллельно проведению этиологического лечения больному следует уделять много внимания питанию. Диета больного с мегалобластной анемией должна включать достаточное количество мясных и молочных продуктов, печени, листовых овощей, фруктов.
Суть патогенетической терапии заключается во введении парентеральным путем витамина В12 – цианокобаламина. Доза, необходимая для лечения, зависит от исходных показателей крови и варьируется в пределах 200-1000 мкг в сутки.

Обычно первый признак гематологической ремиссии появляется через 6-10 дней после начала терапии и представляет собой резкое – до 2-3% – повышение уровня ретикулоцитов. Это явление получило название «ретикулярный криз». В дальнейшем постепенно приходят в норму показатели гемоглобина, эритроцитов, а также лейкоцитов и тромбоцитов, снижается цветовой показатель.
Когда показатели общего анализа крови нормализуются, дозу цианокобаламина снижают до поддерживающей – вводят его по 100-200 мкг раз в 1-2 недели. Если у больного диагностирована анемия Аддисона-Бирмера, витамин В12 ему рекомендован пожизненно.
В отдельных случаях болезни – например, при уже развившемся фуникулярном миелозе – назначаются более высокие дозы витамина В12 – 800-1000 мг каждый день. Снижают дозу препарата лишь тогда, когда не только пришли в норму показатели периферической крови, но и полностью исчезла неврологическая симптоматика данного состояния.
В особо тяжелых клинических ситуациях – когда больной находится в прекоматозном состоянии либо уже впал в кому – ему назначают гемотрансфузии. Как правило, вводят отмытые эритроциты. При доказанном аутоиммунном механизме заболевания (такое имеет место быть у ряда больных) больному показано введение глюкокортикоидов в минимальных лечебных дозировках коротким курсом.
В случае дефицита фолиевой кислоты вводятся препараты, ее содержащие. Суточная доза препарата обычно равна 1-5 мг. Путь введения – пероральный.
Для профилактики рецидива заболевания в дальнейшем больному должны быть назначены профилактические курсы витамина В9, доза его при этом составляет треть от лечебной.
Среди мероприятий, уменьшающих риск развития данного вида анемии, следует отметить рациональное питание – употребление в пищу достаточного количества продуктов, содержащих витамины В9 и В12, борьбу с вредными привычками – в частности, с алкоголизмом, профилактику гельминтозов, своевременное лечение болезней пищеварительного тракта, введение витамина В12 больным после операции по удалению желудка или тонкой кишки.
При условии своевременного начала адекватного лечения прогноз при обоих видах мегалобластной анемии (и В12, и фолиеводефицитной) благоприятный.
Если вас беспокоят описанные выше признаки, или вы уже сдавали кровь и знаете, что у вас какая-то анемия, обратитесь к терапевту. После проведения дополнительной диагностики пациента с мегалобластной анемией направляют к гематологу, который и назначает лечение. Дополнительно часто требуется консультация невролога (при фуникулярном миелозе) и гастроэнтеролога (при нарушении пищеварения). Так как нередкой причиной анемии становятся болезни печени и глистные инвазии — рекомендован осмотр гепатолога и инфекциониста. Большое значение в лечении имеет питание, полезна будет консультация диетолога.
источник
Мегалобластные анемии являются результатом дефицита витамина В12 и фолиевой кислоты. Неэффективный гемопоэз поражает все клеточные линии, но в особенности эритроидную. Диагноз базируется на общем анализе крови, мазке периферической крови, в которых определяется макроцитарная анемия с анизоцитозом и пойкилоцитозом, большие овальные эритроциты (макроовалоциты), гиперсегментация нейтрофилов и ретикулоцитопения. Лечение направлено на устранение основной причины.
Макроцитами называют увеличенные эритроциты (MCV > 95II). Макроцитарные эритроциты обнаруживаются при различных заболеваниях, многие из которых не связаны с мегалобластозом и развитием анемии. Макроцитоз может быть обусловлен мегалобластами или другими увеличенными эритроцитами. Мегалобласты — это большие ядросодержащие предшественники эритроцитов, содержащие неконденсированный хроматин. Мегалобластоз предваряет развитие макроцитарной анемии.

Наиболее частой причиной межобластного кроветворения является нарушение утилизации витамина В12 или фолиевой кислоты. Другими причинами являются употребление лекарственных препаратов (обычно цитостатических или иммунодепрессантов), нарушающих синтез ДНК, и реже метаболические заболевания. В некоторых случаях этиология мегалобластоза неизвестна.

Мегалобластный тип кроветворения является результатом нарушения синтеза ДНК, приводя к появлению больших клеток с крупными ядрами. Во всех клеточных линиях имеет место нарушение созревания, при котором созревание цитоплазмы опережает созревание ядер, это приводит к появлению мегалобластов в костном мозге, прежде чем происходят изменения в крови. Нарушение гемопоэза вызывает костномозговую гибель клеток, делая эритропоэз неэффективным, и непрямую гипербилирубинемию и гиперурикемию. Поскольку нарушение созревания поражает все клеточные линии, определяется ретикулоцитопения, в более поздних стадиях лейкопения и тромбоцитопения. Большие овальные эритроциты (макроовалоциты) появляются в кровотоке. Характерны гиперсегментированные полиморфноядерные нейтрофилы, механизм образования которых неясен.

Анемия развивается исподволь и может быть бессимптомной, пока не станет выраженной. Дефицит витамина В12 может приводить к манифестации неврологической симптоматики, включая периферическую нейропатию, деменцию и подострую комбинированную дегенерацию. Дефицит фолиевой кислоты может вызвать развитие диареи, глоссита, потери веса.
Большинство макроцитарных (MCV > 95 fl/клетку) анемий являются межобластными. Немегалобластный макроцитоз проявляется при различных клинических состояниях, не все из которых ясны. Анемия обычно развивается по механизмам, не зависящим от макро-цитоза. Макроцитоз, обусловленный избытком мембраны эритроцитов, проявляется у больных с хроническим заболеванием печени, при котором нарушается этерификация холестерина. Макроцитоз с MCV от 95 до 105 95А/клетку проявляется при хроническом алкоголизме с отсутствием дефицита фолиевой кислоты. Умерено выраженный макроцитоз встречается при апластической анемии, особенно в период восстановления. Макроцитоз типичен и для миелоидисплазии. Вследствие того что эритроциты модифицируют свою форму в селезенке после выхода из костного мозга, макроцитоз может наблюдаться после спленэктомии, хотя эти изменения не ассоциированы с анемией.
Немегалобластный макроцитоз подозревается у больных с макроцитарной анемией, у которых после проведения исследований исключен дефицит витамина В12 и фолиевой кислоты. Макроовалоциты в мазке периферической крови и повышение RDW, что является типичным для классической мегалобластной анемии, могут отсутствовать. Если немегалобластный макроцитоз необъясним клинически (например, при наличии апластической анемии, хроническом заболевании печени или употреблении алкоголя) или при подозрении на миелодиплазию, необходимы выполнение цитогенетических исследований и изучение костного мозга, чтобы исключить наличие миелодисплазии. При немегалобластном макроцитозе в костном мозге мегалобласты не определяются, но при миелодисплазии и выраженном поражении печени характерны мегалобластоидные предшественники эритроцитов с плотными конденсатами хроматина, которые отличаются от обычных тонких нитей, характерных для мегалобластных анемий.
источник
Анемии, связанные с нарушением синтеза ДНК и РНК, — большая группа как наследственных, так и приобретенных заболеваний. Эти анемии объединяет присутствие в
костном мозге мегалобластов — своеобразных больших клеток красного ряда с нежной структурой и необычным расположением хроматина в ядре.
Синтез ДНК нарушается при дефиците витамина В12, фолиевой кислоты, некоторых редких наследственных заболеваниях.
Выделяют витамин В12-(фолиево)-дефицитную анемию. В связи с этим нередко больным с мегалобластной анемией назначают как витаминВ12, так и фолиевую кислоту. В действительности комбинированный дефицит витамина В12 и фолиевой кислоты наблюдается редко, лишь при нарушениях всасывания в кишечнике.
Анемии, возникающие в результате дефицита витамина В12 (пернициозные анемии)
Анемии, возникающие при недостатке в организме витамина В12, отличаются от других видов анемий появлением в костном мозге мегалобластов. Помимо этого, при данном типе анемии отмечаются снижение числа эритроцитов и гемоглобина, уменьшение количества тромбоцитов (тромбоцитопения), лейкоцитов (лейкопения) и нейтрофилов (нейтропения). Клинически пернициозная анемия проявляется всевозможными повреждениями слизистой оболочки желудочно-кишечного тракта атрофического характера, а также симптомами поражения нервной системы в виде фуникулярного миелоза.
Впервые пернициозная, или злокачественная, анемия была описана в 1849 г. Ориентировочно в это же время установили, что при пернициозной анемии наблюдается атрофический гастрит. Впоследствии было обнаружено, что при рассматриваемой болезни в костном мозге появляются крупные клетки со своеобразной структурой хроматина. Данные клетки получили название мегалобластов.
В 1926 г. Минот и Мерфи показали, что сырая печень эффективна при пернициозной анемии. В 1930 г. Кастл предположил, что в мясе содержится «внешний фактор», который объединяется с «внутренним фактором», при этом образуется какое-то вещество, которое всасывается и откладывается в печени. В дальнейшем, однако, стало ясно, что «внутренний фактор» необходим для всасывания «внешнего фактора» — витаминаВ12.
Внутренний фактор сохранил свое название до настоящего времени. Это гликопротеин. В присутствии витамина В12 две молекулы внутреннего фактора объединяются и образуют димер. 1 мг внутреннего фактора связывает 25 мг витаминаВ12. У человека внутренний фактор образуется в фундальной части и в области тела желудка. Он секретируется париетальными клетками желудка.
Витамин В12 содержится в мясе, яйцах, сыре, молоке, печени и почках. Витамин В12 в пище связан с белком. Он исчезает при кулинарной обработке, а также в желудке под влиянием протеолитических ферментов, после чего связывается с внутренним фактором. Комплекс витамин В12 — внутренний фактор связывается со специфическими рецепторами в нижней и средней частях подвздошной кишки. ВитаминВ12 всасывается медленно, его всасывание при помощи внутреннего фактора ограничено. У человека единовременно может всасываться не более 1,5 мкг витамина В12, или 6-9 мкг/сут. Незначительная часть витаминаВ12 (около 1%) может всосаться без внутреннего фактора в желудочном соке. Витамин В12 в крови связывается с белками плазмы -транскобаламинами, синтезируемыми в печени. Основное количество витамина В12 передается клеткам костного мозга.
Содержание витаминаВ12 в организме взрослого здорового человека составляет 2-5 мг. Печень — основной орган, в котором содержится витамин В12. Запасы витамина в организме настолько велики, что требуется 3-6 лет для развития дефицита витамина В12 при нарушении его всасывания. Потери витаминаВ12 с мочой и калом составляют у взрослого человека 2-5 мкг/сут. Так как из пищи всасывается не весь витамин В12, человек должен получать 3-7 мкг витамина в день.
У человека обнаружены две ферментные реакции, требующие участия витаминаВ12. Первая из этих реакций обеспечивает нормальное кроветворение, в ее ходе из уридин-монофосфата образуется тимидин-монофосфат, включаемый в ДНК. Без витамина В12 нарушается эта циклическая реакция, в результате чего нарушается синтез тимидин-монофосфата, а, следовательно, и ДНК.
Вторая реакция, в которой участвует витамин В12, не влияет на кроветворение. Эта реакция необходима для нормального обмена жирных кислот. В случае дефицита витамина В12 в организме нарушается процесс образования жирных кислот, что приводит к накоплению метилмалоновой кислоты, являющейся довольно токсичной.
Непосредственной причиной развития дефицита витаминаВ12 в организме является нарушение его всасывания. Всасывание нарушается при следующих условиях: снижении образования внутреннего фактора, воспалительных и атрофических заболеваниях тонкой кишки, всасывании значительного количества витаминаВ12 в кишечнике.
Самой распространенной причиной снижения интенсивности всасывания витаминаВ12 является атрофия слизистой оболочки желудка. Данная патология протекает с отсутствием секреция соляной кислоты, пепсина и внутреннего фактора. Атрофические изменения слизистой оболочки желудка могут быть следствием различных причин. Имеются сведения о роли наследственной предрасположенности в развитии витамин-В12-дефицитных анемий, возникающих в результате снижения секреции фактора Кастла. Среди родственников больных пернициозной анемией в 30% случаев также встречается данное заболевание. Описана аутосомно-рецессивная наследственная форма витаминВ12-дефицитной анемии у детей, связанная с отсутствием внутреннего фактора в желудочном соке. При этом у больных сохраняется нормальная секреция пепсина и соляной кислоты. У большинства больных пернициозной анемией в сыворотке крови обнаруживаются антитела, направленные против париетальных клеток желудка. Однако это еще не говорит о том, что витамин-В12-дефицитная анемия является заболеванием аутоиммунной природы. Такие же антитела обнаруживаются иногда при хроническом атрофическом гастрите без нарушения всасывания витамина В12. Более чем в половине случаев пернициозной анемии в сыворотке крови обнаруживаются антитела против внутреннего фактора.
Иногда витамин-В12-дефицитные анемии сочетаются с аутоиммунным тиреоидитом, гипогаммаглобулинемией (снижением в крови уровня у-глобулинов). В отличие от наследственной формы при аутоиммунной ювенильной (юношеской) форме витамин-В12-дефицитной анемии также нарушена секреция соляной кислоты и пепсина.
Нарушение секреции внутреннего фактора может стать следствием влияния на слизистую оболочку желудка разнообразных токсических веществ, например алкоголя, а особенно неразведенного спирта.
Таким образом, снижение образования внутреннего фактора может быть следствием различных причин, как наследственных, так и приобретенных. Витамин-В12-дефицитная анемия развивается после гастрэктомии (удаления желудка). После резекции 2/3 желудка количество внутреннего фактора обычно оказывается вполне достаточным для связывания витамина В12 и обеспечения его всасывания.
Вторая по частоте причина дефицита витамина В12 — нарушение его всасывания в кишечнике в связи с тяжелым хроническим энтеритом у лиц, перенесших резекцию тощей кишки, при целиакии, при тропической спру. Всасывание витамина В12 нарушается при снижении секреции трипсина.
В12-дефицитная анемия развивается в случае заражения широким лентецом. Это связано с тем, что данный паразит конкурентно поглощает большое количество витамина В12. Помимо этого, пернициозная анемия может развиваться при синдроме «слепой петли», что связано с появлением участков тонкого кишечника, в которых прохождение пищи либо затруднено, либо невозможно вообще. Такая ситуация возникает после наложения кишечных анастомозов. В этих участках большое количество кишечной микробной флоры поглощает витаминВ12. Такая же ситуация наблюдается при множественном дивертикулезе тонкой кишки.
Имеются описания ряда случаев дефицита транскобаламина II, в результате чего нарушена передача витамина В12 тканям, несмотря на его нормальное всасывание и содержание в организме.
Изменения в кроветворении и эпителиальных клетках связаны с нарушением образования тимидина и, следовательно, с нарушением деления клетки. Клетки увеличиваются в размерах и несколько напоминают клетки эмбриона. Это позволило предположить, что мегалобластное кроветворение — возврат к эмбриональному кроветворению. Мегалобластное кроветворение было представлено как вариант нормального кроветворения. В настоящее время сходство мегалобластов с эмбриональными красными ядерными клетками считают чисто внешним.
По всей вероятности, изменения в нервной системе имеют отношение к нарушению не синтеза ДНК, а обмена жирных кислот. Как пропионовая, так и метилмалоновая кислота, которые накапливаются при дефиците витаминаВ12, токсичны для нервной клетки. Кроме того, в нерве, полученном при биопсии у больного витамин-В12-дефицитной анемией, синтезируются жирные кислоты, отличные от нормальных. Различие в структуре жирных кислот может приводить к нарушению образования миелина, а затем и к повреждению самого аксона.
Независимо от того, какая из перечисленных выше причин привела к развитию у больного В12-дефицитной анемии, в клинической картине наблюдаются симптомы поражения пищеварительного тракта, нервной системы и кроветворной ткани. Больной предъявляет жалобы на повышенную утомляемость, вялость, слабость, чувство сердцебиения и одышку при легкой физической нагрузке. С течением времени такое состояние постепенно усугубляется. Большая часть больных рассматриваемой патологией на протяжении многих лет жалуются на диспепсические расстройства.
Чаще витамин-В12-дефицитная анемия развивается у пожилых людей, но возможна и у молодых.
Больные чаще бывают полными, с одутловатым, при выраженной анемии бледно-желтушным лицом. У большинства больных даже при тяжелой анемии выявляется легкая желтушность склер. Иногда при дефиците витамина В12 у больного повышена температура тела до 37,5°С. Некоторые больные жалуются на боли в языке. На языке обнаруживаются участки воспаления, иногда афты (небольшие поверхностные изъязвления слизистых оболочек), атрофия сосочков. Вопреки существующему представлению лишь у 1/4 больных с дефицитом витамина В12 имеются субъективные или объективные признаки глоссита (воспаления языка). Вообще глоссит при анемии -это не специфичный признак дефицита витамина В12, глоссит бывает и при железодефицитной анемии.
У ряда больных немного увеличена селезенка, а иногда и печень. Желудочная секреция у большинства больных с дефицитом витаминаВ12 резко снижена. Если причиной дефицита витаминаВ12 служит приобретенное нарушение секреции внутреннего фактора, то в желудочном соке отсутствуют соляная кислота и пепсин. При дефиците витамина В12 вследствие нарушения кишечного всасывания или инвазии широким лентецом секреция соляной кислоты, как правило, снижается, однако сильные активаторы желудочной секреции могут ее усиливать.
При рентгеноскопии желудка нередко обнаруживают нарушения эвакуаторной деятельности, уплощенные и сглаженные складки. При фиброгастродуоденоскопии устанавливают атрофию слизистой оболочки желудка, подтверждаемую данными гистологического исследования.
Одним из характерных признаков дефицита витаминаВ12 является поражение нервной системы, которое принято называть фуникулярным миелозом. Наиболее ранними симптомами являются нарушение чувствительности с постоянными легкими болевыми ощущениями, напоминающими покалывание булавками, ощущение холода, «ватных» ног, ползания мурашек, онемение в конечностях. Реже бывают опоясывающие боли. Довольно часто беспокоит выраженная мышечная слабость, возможна атрофия мышц. К явлениям полиневрита присоединяется поражение спинного мозга. Нижние конечности поражаются в первую очередь, чаще симметрично. При прогрессировании процесса нарушаются поверхностная чувствительность, способность отличать холодное от горячего, снижается болевая чувствительность. Поражение может распространяться на живот и даже выше. Руки поражаются реже и меньше, чем ноги. В тяжелых случаях нарушается вибрационная и глубокая чувствительность. У некоторых больных теряются обоняние, слух, нарушается вкус. В редких случаях у больных могут отмечаться тяжелые трофические нарушения, расстройство функции тазовых органов.
У некоторых лиц, страдающих данным заболеванием, возникают разнообразные психические нарушения, бред, слуховые и зрительные галлюцинации, описаны эпилептические приступы. В самых тяжелых случаях наблюдаются выраженное истощение, исчезновение рефлексов, стойкие параличи нижних конечностей.
При дефиците витаминаВ12 наблюдается анемия, чаще гиперхромная (с повышенным насыщением эритроцитов гемоглобином), реже нормохромная, цветовой показатель может повышаться до 1,3, но в большинстве случаев он близок к единице. Эритроциты
большие, часто овальной формы, во многих обнаруживаются остатки ядра (тельца Жолли, кольца Кебота). Нередко в периферической крови обнаруживаются эритрокариоциты. Количество ретикулоцитов у большинства больных снижено или нормальное, количество лейкоцитов снижается главным образом за счет снижения количества нейтрофилов. Количество тромбоцитов также часто снижено. Иногда снижение количества тромбоцитов выражено в значительной степени, но их функция при этом, как правило, не нарушена и кровоточивость возникает крайне редко. В костном мозге обнаруживается раздражение красного ростка.
Витамин-В12-дефицитную анемию сопровождает умеренная гипербилирубинемия (увеличение содержания билирубина в крови). Билирубин повышается за счет непрямой фракции, содержание которой может достигать 28-47 мкмоль/л. Повышение содержания билирубина главным образом связано с внутрикостномозговым распадом эритрокариоцитов, содержащих гемоглобин. Кроме того, продолжительность жизни периферических эритроцитов несколько укорочена по сравнению с нормой.
Содержание сывороточного железа, как правило, нормальное, хотя до начала лечения может быть несколько повышенным. В период лечения в связи с быстрой утилизацией содержание железа в сыворотке снижается, однако это снижение не говорит о малых запасах железа.
Диагностика и дифференциальная диагностика
Обнаружение анемии в сочетании с лейкопенией и тромбоцитопенией у человека пожилого возраста дает основание заподозрить у него витамин-В12-дефицитную анемию. Предположение подкрепляют небольшая желтушность склер, боли в языке, нарушения чувствительности. Однако эти признаки не обязательны, иногда они появляются лишь при выраженном дефиците витамина.
Дефициту витаминаВ12 свойственны макроцитоз (крупный размер клеток) и анизоцитоз эритроцитов, гиперхромия (увеличенное насыщение эритроцита гемоглобином), овальная форма клеток, наличие в эритроцитах телец Жолли.
При выявлении у больного цитопении (малого количества форменных элементов) с высоким или нормальным цветовым показателем необходима пункция костного мозга. В миелограмме выявляются признаки мегалобластной анемии.
Дифференциальная диагностика витамин-В12-дефицитной анемии проводится с другими анемиями, при которых также снижается содержание лейкоцитов и тромбоцитов и есть признаки повышенного разрушения эритроцитов, к которым в первую очередь относятся повышение содержания билирубина и увеличение селезенки.
Повышенное разрушение эритроцитов сочетается с панцитопенией (низкое содержание всех форменных элементов крови), болезни Маркиафавы — Микели. При аутоиммунной панцитопении снижение количества тромбоцитов встречается чаще и приводит к развитию геморрагического синдрома, что отличает это заболевание от анемии при дефиците витаминаВ12. Также при аутоиммунной панцитопении чаще повышено содержание ретикулоцитов, а при дефиците витамина В12 оно обычно снижено. В костном мозге при дефиците витамина В12 выявляются мегалобласты, тогда как при аутоиммунной панцитопении чаще обнаруживаются нормальные эритрокариоциты.
При болезни Маркиафавы — Микели обычно обнаруживается внутрисосудистое разрушение эритроцитов, что проявляется выделением черной мочи, появлением в ней
гемосидерина, повышением содержания свободного гемоглобина в плазме. Внутрисосудистое разрушение эритроцитов нехарактерно для мегалобластных анемий. В связи с постоянным выделением с мочой гемосидерина при болезни Маркиафавы -Микели чаще снижается содержание железа, и анемия бывает гипохромной, а не гиперхромной, как при мегалобластных анемиях.
Наибольшие трудности в дифференциальной диагностике возникают у больных, которые лечились небольшим количеством витамина В12 (1-2 инъекции). У этих больных еще не успевает повыситься уровень гемоглобина, но уже исчезают из костного мозга типичные мегалобласты, а в периферической крови выявляется ретикулоцитоз (увеличение количества ретикулоцитов).
Мегалобласты могут исчезнуть также под влиянием фолиевой кислоты, поэтому нельзя принимать больным с неясными анемиями препараты, содержащие фолиевую кислоту (ундевит, декамевит, гендевит, пентовит). Это иногда дает основание для неправильной диагностики аутоиммунной гемолитической анемии.
При обнаружении в костном мозге большого количества мегалобластов возникает вопрос о причине мегалобластной анемии. Выявление ахилии (отсутствие соляной кислоты и фермента пепсина в желудочном соке), атрофии слизистой оболочки желудка у пожилого человека или у молодого, употреблявшего неразведенный этанол, позволяет думать о нарушении секреции внутреннего фактора.
Для диагностики дефицита витамина В12 используют микробиологические методы определения содержания витамина В12 в сыворотке. К таким методам относится рост ряда микроорганизмов — Escherichia coli, Euglena gracillis, Lactobacillis, Leichmannii, который непосредственным образом зависит от количества данного витамина. Рост Escherichia coli зависит не только от витамина В12, поэтому рекомендуют пользоваться двумя другими микроорганизмами.
ВитаминВ12 в сыворотке можно определять радиоиммунологическими методами. Нормальное содержание витаминаВ12 в сыворотке составляет 200-1000 пг/мл, при его дефиците количество снижается до 10-150 пг/мл. Используется витаминВ12, помеченный радиоактивным кобальтом. Всасывание изучают либо по радиоактивности кала после приема витамина, либо по включению помеченного витамина в клетки печени, либо по суммарному счету радиоактивности тела. Очень широко применяется метод Шиллинга. Указанный метод заключается в том, что больному дают помеченный витамин В12, а затем вводят 1000 мкг нерадиоактивного витамина В12. В норме более 10% принятого радиоактивного витамина должно выделиться с мочой. При нарушении всасывания витамина В12 радиоактивность в моче может не появиться, и тогда думают о нарушении либо секреции внутреннего фактора, либо кишечного всасывания витамина. Если нарушена секреция внутреннего фактора, то прием внутрь совместно с концентратом внутреннего фактора приводит к нормализации всасывания витамина. При нарушении всасывания в кишке прием концентрата внутреннего фактора эффекта не дает.
Для диагностики дефицита витаминаВ12 в организме определяют метилмалоновую кислоту в моче.
Во всех случаях дефицита витамина В12 следует исключить заражение широким лентецом. В кале иногда выявляются обрывки стробилы, яйца паразита.
Необходимо также выяснить, не наложен ли у больного анастомоз с оставлением слепой петли. Важно выяснить объем операции, если у больного резецировалась часть желудка. Удаление желудка чаще приводит к витамин-В12-дефицитной анемии в связи с
отсутствием внутреннего фактора. При резекции 2/3 желудка дефицит витамина В12, как правило, не развивается.
При дефиците витаминаВ12 необходимы рентгенологическое исследование желудка и фиброгастродуоденоскопия для исключения рака желудка. Частое сочетание дефицита витамина В12 и рака желудка объясняется атрофией слизистой оболочки желудка при обоих видах патологии.
Дефицит витамина В12 приходится дифференцировать с дефицитом фолиевой кислоты. При дефиците фолиевой кислоты не бывает фуникулярного миелоза, желудочная секреция может быть снижена, однако атрофия слизистой оболочки желудка не характерна. Диагностике помогает исследование содержания фолиевой кислоты и витамина В12 в сыворотке, а также определение степени всасывания витамина В12 в желудочно-кишечном тракте.
Обнаружение в препарате костного мозга мегалобластов говорит о необходимости проведения дифференциальной диагностики с острым лейкозом, эритромиелозом.
Мегалобласты в костном мозге обнаруживаются при лечении цитостатическими препаратами (метотрексатом, цитозаром). Это связано с их влиянием на синтез ДНК.
Кроме описанных причин мегалобластных анемий, очень редко у детей бывают наследственные заболевания, обусловленные нарушением функции ряда ферментов, принимающих участие в синтезе пуриновых или пиримидиновых оснований. Все эти формы выявляются в раннем детстве, сопровождаются нарушением роста, умственного развития, иногда подагрой, глухотой и сахарным диабетом. Они не поддаются лечению ни витамином В12, ни фолиевой кислотой. При оротовой ацидурии в моче выявляются своеобразные кристаллы оротовой кислоты, что является качественной пробой при данной патологии.
Обнаружение мегалобластной анемии у маленьких детей требует разграничивать наследственные формы болезни и приобретенные, связанные с недостаточным поступлением в организм фолиевой кислоты.
При биопсии слизистой оболочки желудка не находят каких-либо спецефических изменений. Слизистая оболочка атрофична, лимфоциты, обнаруживаемые на ней, иногда содержат антитела к комплексу витамина В12 с внутренним фактором.
Основной метод лечения — парентеральное введение витамина В12 или назначение его внутрь в очень больших дозах (5-10 мг), иногда вместе с внутренним фактором. Однако при этом очень быстро вырабатываются антитела к чужеродному свиному белку, и всасывание нарушается.
Для парентерального введения применяют цианокобаламин и оксикобаламин. Водный раствор цианокобаламина очень быстро проникает в кровь, максимальная концентрация в сыворотке отмечается через 1,5-2 ч после введения. Введение 1 мг цианокобаламина значительно превышает количество, которое может связаться транскобаламинами плазмы.
Почти все введенное количество выводится с мочой, из 1 мг цианокобаламина в организме остается лишь 50-80 мкг.
Гидроксикобаламин из места инъекции всасывается так же быстро, как и цианокобаламин, концентрация его в сыворотке становится максимальной через 2 ч после введения. Однако в отличие от цианокобаламина гидроксикобаламин значительно лучше связывается с белком сыворотки. После введения 1 мг препарата в организме остается 2533%.
Для лечения витамин-В12-дефицитной анемии цианокобаламин назначают по 200-400 мкг 1 раз в сутки, а в тяжелой ситуации — 2 раза в сутки. Препарат вводят в течение 4-6 недель. Гидроксикобаламин достаточно вводить через день по 1 мг/сут. в течение 4 недель.
Имеются препараты длительного действия — комплексы витамина в виде масляной суспензии. Препарат поступает в кровь медленно, из 1 мг в организме остается 90-98%, однако после введения подобных препаратов остаются плохо рассасывающиеся уплотнения.
Фолиевая кислота при дефиците витамина В12 не показана. Более того, лечение одной фолиевой кислотой без витамина В12 может ухудшить состояние больного, усилить неврологическую симптоматику. Лечения препаратами железа не требуется, если нет дефицита железа. Такое сочетание встречается сравнительно редко.
На 3-4-й день от начала введения витамина В12 начинает увеличиваться содержание ретикулоцитов. Максимальный подъем ретикулоцитов выявляется на 5-8-й день и зависит от выраженности анемии.
После курса лечения необходим курс закрепляющей терапии. В течение 2 месяцев цианокобаламин вводят еженедельно, а затем постоянно 2 раза в месяц по 400-500 мкг. Оксикобаламин можно вводить реже — в течение 3 месяцев его вводят 1 раз в неделю, а затем постоянно 1 раз в месяц по 500 мкг.
Сразу после удаления желудка при нормальном уровне гемоглобина и эритроцитов лечение начинают с поддерживающих доз.
Переливания крови следует применять только при наличии жизненных показаний, к которым относятся коматозное состояние или резкое нарушение гемодинамики.
В случае заражения широким лентецом следует провести дегельминтизацию. С этой целью применяют фенасал в дозировке 2 гна ночь и повторно утром, запивая водой. Для повышения эффективности препарата на второй день назначают 0,5 г дихлорофена.
При фуникулярном миелозе назначают большие дозы витамина В12 (1000 мкг ежедневно). В настоящее время имеется особая форма витаминаВ12 -аденозилкобаламин, который участвует в обмене жирных кислот и при фуникулярном миелозе является гораздо эффективнее цианокобаламина и гидроксикобаламина. Препарат применяют по 500 мкг ежедневно. Так как это вещество не влияет на кроветворение, его следует применять парентерально с цианокобаламином или гидроксикобаламином.
Во всех случаях дефицита витаминаВ12 применение витамина должно привести к быстрому и стойкому улучшению. Неэффективность витамина В12 говорит о неправильном диагнозе.
Наследственные формы витамин-В12-дефицитной анемии, проявляющейся с детства. С детства проявляются формы витамин-В 12-дефицитной анемии, обусловленные наследственным нарушением секреции внутреннего фактора или всасывания витамина В12 и отсутствием белка плазмы, переносящего витамин В12, — транскобаламина.
Наследственное нарушение секреции внутреннего фактора наследуется аутосомно-рецессивно. В течение первого года у детей показатели крови нормальны. На втором году жизни появляются резкая слабость, понос, раздражительность. Ребенок худеет, исчезает аппетит, появляются восковая бледность, часто — желтизна склер и кожи. Иногда наступает атрофия слизистой оболочки языка с покраснением сосочков. Нередко увеличиваются печень и селезенка. Желудочная секреция может быть нормальной. При гистологическом исследовании обычно нет признаков атрофии слизистой оболочки желудка. Иногда резко снижаются спинальные рефлексы (вплоть до атаксии). Картина крови и костного мозга не отличается от таковой при других формах витамин-В 12-дефицитной анемии. Содержание витаминаВ12 в сыворотке снижается. Всасывание меченого витамина В12 также снижено. Прибавление нормального нейтрализованного желудочного сока или концентрата внутреннего фактора нормализует всасывание.
Синдром Имерслунд — Гресбека. Эта редкая наследственная форма проявляется мегалобластной анемией с нормальной или субнормальной желудочной секрецией, нормальным содержанием в желудке внутреннего фактора, нарушением всасывания витамина В12 без нарушения всасывания других веществ и в большинстве случаев протеинурией. Болезнь наследуется аутосомно-рецессивно. Болеют дети обоего пола. Чаще всего болезнь проявляется в возрасте до 2 лет, хотя иногда и значительно позже. Клинические и гематологические признаки такие же, как и при других формах витамин-В 12-дефицитной анемии. Имеется лишь один дополнительный симптом — протеинурия без каких-либо других изменений в моче. Она наблюдается у 90% больных с синдромом Имерслунд — Гресбека. Всасывание витамина В12 резко нарушено, хотя активность внутреннего фактора в желудочном соке больного нормальная. Прибавление желудочного сока здорового человека и концентрата внутреннего фактора не приводит к нормализации всасывания. Нарушение всасывания витаминаВ12 может быть связано с изменением структуры рецептора в тонкой кишке, присоединяющего комплекс витамина В12 с внутренним фактором, либо с процессом проникновения витаминаВ12 через энтероциты — клетки, выстилающие тонкую кишку. Протеинурия остается после лечения больных витаминомВ12, в период гематологической ремиссии. При гистологическом исследовании почек в большинстве случаев патологических изменений обнаружить не удается. В отдельных случаях выявляются признаки хронического мембранозного гломерулонефрита.
Дифференциальная диагностика достаточно трудна, в особенности в тех случаях, когда больной попадает под наблюдение в период ремиссии после комплексного лечения анемии. Постановке диагноза помогают выявление немотивированной небольшой протеинурии без других изменений в моче, а также исследование всасывания меченого витамина В12 и исследование костного мозга в период обострения до начала лечения.
Лечение не отличается от лечения других форм витамин-В 12-дефицитной анемии.
Наследственный дефицит транскобаламина II. Из 3 типов транскобаламина лишь транскобаламин II участвует в переносе витамина В12 в костный мозг. При дефиците этого белка развивается мегалобластная анемия, чаще у детей в возрасте нескольких недель. Анемия у всех больных резко выражена, отмечаются тромбоцитопения, нейтропения. Имеются все признаки витамин-В 12-дефицитной анемии (глоссит, поражение нервной системы). Содержание внутреннего фактора в желудочном соке нормально, нарушения всасывания витамина В12 не выявлено. Общая способность
сыворотки связывать витамин В12 у данной категории больных не нарушена из-за нормального количества транскобаламина I и III. Транскобаламина II в тех же сыворотках очень мало или совсем нет.
Лечение проводится большими дозами витамина В12 постоянно. Эффективно одновременное введение свежей донорской плазмы.
Анемии, связанные с дефицитом фолиевой кислоты
Анемии, обусловленные дефицитом фолиевой кислоты, независимо от причин этого дефицита сопровождаются появлением в костном мозге мегалобластов, разрушением эритрокариоцитов внутри костного мозга, панцитопенией (снижением количества всех форменных элементов крови), макроцитозом (большими размерами) и гиперхромией эритроцитов (большим насыщением гемоглобином), иногда психическими расстройствами.
У человека содержится 5-10 мг фолиевой кислоты в различных формах. В отличие от витамина В12, запасы которого могут истощиться при нарушении его поступления в организм лишь за несколько лет, запасы фолиевой кислоты исчерпываются за 4 месяца. Суточная потребность в фолиевой кислоте составляет 100-200 мкг и увеличивается во много раз при беременности, гемолитических анемиях. Общее количество поступающей фолиевой кислоты при полноценном питании составляет 500-600 мкг/сут. Фолаты широко представлены в различных пищевых продуктах, их много в печени, дрожжах, шпинате, мясе. Более 50% фолиевой кислоты может разрушиться при кулинарной обработке пищи.
Фолиевая кислота всасывается в верхнем отделе тонкой кишки. Способность кишечника всасывать фолиевую кислоту намного превышает суточную потребность в витамине. Имеется некоторое ограничение всасывания фолиевой кислоты: при введении фолиевой кислоты в дозе 0,01-0,1 мкг/мл около 50% всасывается за 20 мин, а при ее концентрации 10 мкг/мл всасывается около 23%.
Фолиевая кислота участвует в синтезе пиримидиновых оснований. Различные формы фолиевой кислоты включаются в ряд важнейших реакций.
Дефицит фолиевой кислоты, так же как и дефицит витамина В12, приводит к мегалобластной анемии. Всасывание фолиевой кислоты нарушено у лиц, перенесших удаление части тонкой кишки, особенно тощей, а также при нарушениях всасывания пищи. Дефицит фолиевой кислоты так же, как и дефицит витаминаВ12, наблюдается при синдроме слепой петли. Описаны редкие случаи наследственного нарушения транспорта фолиевой кислоты через стенку кишечника и в спинномозговую жидкость. Всасывание других веществ в кишечнике при этом не нарушено. Дефицит фолиевой кислоты наблюдается у новорожденных при недоношенности, нарушении кишечного всасывания, вскармливании козьим молоком, содержащим мало фолиевой кислоты.
Всасывание фолиевой кислоты нарушается у лиц, длительно принимающих противосудорожные препараты типа дифенина и фенобарбитала (люминала), а также у лиц, страдающих алкоголизмом.
Повышенный расход фолиевой кислоты при беременности может приводить к ее дефициту. Следует, однако, отметить, что у женщин, живущих в высокоразвитых странах, дефицит фолиевой кислоты в период беременности встречается в очень редких случаях. Он встречается при плохом питании и повышенной потребности в витамине, у беременных женщин, больных гемолитической анемией и расходующих в связи с этим большое количество фолиевой кислоты, злоупотреблявших алкоголем до беременности.
Больные с дефицитом фолиевой кислоты жалуются на общую слабость, головокружение. В отличие от больных с дефицитом витамина В12 боли в языке у них бывают редко. Нарушенной чувствительности и других признаков фуникулярного миелоза не наблюдается. Дефицит фолиевой кислоты встречается у детей, у молодых женщин. При нем обычно не бывает полноты, одутловатости лица, желтушность склер. В отличие от дефицита витамина В12 при дефиците фолиевой кислоты редко наблюдается атрофический гастрит, хотя понижение желудочной секреции бывает часто.
Для дефицита фолиевой кислоты, так же как для дефицита витамина В12, характерны появление в периферической крови макроцитоза, гиперхромной анемии, пониженное количество ретикулоцитов, тромбоцитопения и лейкопения. В костном мозге обнаруживаются мегалобласты.
Изменения в нервной системе при дефиците фолиевой кислоты отличаются от таковых при витамин-В 12-дефицитной анемии. У лиц, страдающих эпилепсией, дефицит фолиевой кислоты приводит к учащению и утяжелению приступов. Это особенно важно, поскольку прием противосудорожных препаратов, включая люминал, может приводить к нарушению всасывания фолиевой кислоты. Дефицит фолиевой кислоты приводит к обострению шизофрении, более тяжелым клиническим проявлениям и меньшей эффективности терапии.
Дефицит фолиевой кислоты может наблюдаться при мегалобластной анемии у новорожденных, у лиц, употребляющих противосудорожные препараты, злоупотребляющих алкогольными напитками, у беременных, которые страдают гемолитической анемией, у больных с тяжелым гемолитическим кризом.
Для дифференциальной диагностики между дефицитом витаминаВ12 и дефицитом фолиевой кислоты определяют содержание фолиевой кислоты в сыворотке и в эритроцитах микробиологическим методом. В качестве тест-микроба используют Streptococcus faecalis, Lactobacillus casei. Используется также радиоиммунологическое определение фолиевой кислоты. В норме содержание фолиевой кислоты в сыворотке колеблется, по данным разных авторов, от 3 до 25 нг/мл. Содержание фолиевой кислоты в эритроцитах колеблется в норме от 100 до 425 нг/мл. При дефиците фолиевой кислоты ее уровень снижается в сыворотке и в эритроцитах. При дефиците витамина В12 содержание фолиевой кислоты в сыворотке чаще повышается, в эритроцитах — понижается (незначительно) либо остается нормальным.
Для диагностики дефицита фолиевой кислоты применяют нагрузочный метод. Больной принимает 15 г гистидина, после чего определяют содержание его метаболита в моче. В норме с мочой выводится от 1 до 18 мг метаболита. При дефиците фолиевой кислоты за 8
ч после приема гистидина с мочой выделяется от 20 до 1500 мг конечного продукта обмена. Диагностике помогает также радиологическое исследование: при дефиците витамина В12, связанного с нарушением секреции внутреннего фактора, всасывание меченого витаминаВ12 нарушено, а при дефиците фолиевой кислоты витамин В12 всасывается нормально.
При дефиците фолиевой кислоты ее прием приводит к повышению содержания ретикулоцитов, а витамин В12 оказывается неэффективным. Следует отметить, что при дефиците витаминаВ12 прием фолиевой кислоты повышает уровень ретикулоцитов.
Проводится препаратами фолиевой кислоты в дозе 5-15 мг/сут., достаточной даже при нарушенном всасывании фолиевой кислоты. При выявлении дефицита фолиевой кислоты во время беременности или лактации следует назначать ту же дозу препарата, а после нормализации кроветворения ее можно уменьшить до 1 мг/сут. на весь период беременности и лактации.
Профилактика проводится у беременных, страдающих наследственными и приобретенными формами гемолитической анемии, талассемии. Доза фолиевой кислоты при этом должна быть не более 5 мг/сут.
Прогноз фолиеводефицитных анемий хороший. Обострения не наступают, если в период клинических улучшений проводится их профилактика.
Анемии, находящиеся в зависимости от наследственных нарушений активности ферментов, участвующих в синтезе пуриновых и пиримидиновых оснований
1. Наследственное нарушение активности ферментов, которые принимают участие в возникновении коферментных форм фолиевой кислоты. Впервые мегалобластная анемия была обнаружена у ребенка в возрасте 6 месяцев. Всасывание витамина В12 было нормальным.
2. Наследственное нарушение активности ферментов, участвующих в метаболизме оротовой кислоты. Тяжелая мегалобластная анемия наступает в результате наследственного нарушения образования уридин-5-фосфата из оротовой кислоты. Эта редкая форма нарушения пиримидинового синтеза, сопровождающаяся нарушением роста и задержкой умственного развития, была впервые описана в 1959 г.
3. При недостаточной активности ферментов, участвующих в образовании уридин-5-фосфата и оротидин-5-фосфата, развивается мегалобластная анемия. При этом содержание оротовой кислоты в моче увеличивается с 1,4-1,6 мг/сут. до 1 г/сут. В норме меченые тимидин, уридин и оротовая кислота включаются в молекулу ДНК. При оротовой ацидурии включение тимидина и уридина не меняется, включение оротовой
кислоты резко нарушается. В отличие от этого при дефиците витаминаВ12 и фолиевой кислоты нарушается включение в молекулу ДНК уридина и оротовой кислоты.
Наследственная мегалобластная анемия при синдроме Леш — Найана
Синдром Леш — Найана редкое наследственное заболевание. Наследование рецессивное, сцепленное с Х-хромосомой. Заболевание вызывает тяжелые клинические проявления, включающие нарушение психического развития, признаки тяжелого поражения спинного мозга, подагру и мегалобластную анемию.
Наследственная мегалобластная анемия при синдроме Роджерса. Впервые в 1969 г. Rogers с соавторами описали сложный наследственный синдром у девочки 11 лет -сахарный диабет, глухота, мегалобластная анемия. Данная анемия не поддавалась терапии ни витамином В12, ни фолиевой кислотой.
В том же году другие ученые описали аналогичное заболевание у девочки 12 лет, страдавшей с 3-летнего возраста сахарным диабетом, глухотой и мегалобластной анемией. Содержание гемоглобина снижалось до 60 г/л. После безрезультатной терапии витамином В12, фолиевой кислотой, пиридоксином, никотинамидом, пантотенатом, уридином применили тиамин в дозе 20 мг/сут. При этом им удалось добиться подъема содержания ретикулоцитов и нормализации показателей эритроцитов и лейкоцитов. Отмена тиамина привела к падению содержания гемоглобина. Повторное назначение тиамина вновь сопровождалось хорошим терапевтическим эффектом. Признаков гиповитаминоза В6 не было ни у первой, ни у второй больной.
источник
Мегалобластная анемия (МА) или как её также принято называть – пернициозная анемия (хотя такое название подразумевает дефицит исключительно витамина B12) – патология, отнесенная к группе приобретенных и/или передаваемых по наследству гематологических заболеваний, возникающих на почве нарушения синтеза рибонуклеиновой (РНК) или дезоксирибонуклеиновой кислоты (ДНК).
Для мегалобластных анемий весьма характерным признаком является изменение клеток эритроидного ряда: размера (большой), дифференцировки ядра и цитоплазмы (асинхронная), размещения хроматина в ядре (не свойственное нормальным клеткам).
Болезнь формируется по причине недостатка отдельных витаминов (в частности, B12 и B9). Это происходит потому, что синтез ДНК зависим от количества данных веществ в организме. Кроме этого, выработку дезоксирибонуклеиновой кислоты могут расстроить отдельные (редкие) наследственные аномалии ферментов, принимающих участие в биохимических процессах, влияющих на продукцию ДНК.
Типичными представителями этой гематологической патологии являются:
- B12-дефицитная анемия (болезнь Аддисона-Бирмера, пернициозная анемия, злокачественное малокровие) – самая частая форма. Она обусловлена недостатком цианокобаламина, может быть приобретенной по причине заболеваний верхнего отдела кишечника (тонкая кишка) либо передаваемой по наследству и зависимой от продукции и выделения внутреннего фактора (ВФ), либо от всасывания в кишечнике и отсутствия транспортного протеина, который переносит цианокобаламин (транскобаламин). Наследственная анемия становится заметной уже у детей младшего возраста;
- Фолиеводефицитная анемия (недостаток витамина B9) – наблюдается намного реже, нежели дефицит витамина B12, к тому же, изолированный дефицит фолиевой кислоты не ведет к столь серьезным последствиям, которые развиваются в отсутствие цианокобаламина;
- Сочетанный вариант – B12-фолиеводефицитная анемия. Комбинированная форма, обусловленная недостатком витаминов B12 и B9, встречается довольно редко и, как правило, возникает по причине нарушения всасывания данных веществ в кишечнике.
Почему так важно поступление достаточного количества цианокобаламина и фолиевой кислоты в организм человека? Все дело в том, что они принимают участие и играют не последнюю роль в транспортировке лабильных метильных групп метионина, в которых нуждается «строительство» ДНК. Как только уровень В12 снижается или он исчезает, эта реакция резко идет на спад, что сильно сказывается на созревании ядра. При сохраненной функции цитоплазмы, ядро делиться «не спешит» – этот процесс сильно запаздывает (происходит то, что называют «асинхронной дифференцировкой ядра и цитоплазмы»). В таких условиях сама клетка «пускается в рост» и приобретает огромные размеры.
Очевидно, что основным виновником развития патологии признается нарушение всасывания упомянутых выше витаминов в кишечнике. Какие предпосылки могут способствовать подобным нарушениям?
Гематологи обычно ссылаются на три основные причины:
- Отсутствие гликопротеина, называемого внутренним фактором (ВФ), и вырабатываемого специальными клетками тела и фундального отдела желудка. Неимение ВФ становится результатом аутоиммунного атрофического гастрита, в условиях которого начинают появляться «блокирующие» антитела (они не позволяют ВФ и цианокобакламину вступать во взаимодействие), а также антитела «связывающие» (эти АТ соединяются с внутренним фактором или с готовым блоком «ВФ + В12», инактивируя его);
- Заболевания тонкого кишечника (средней и нижней трети), где, собственно, и осуществляется всасывание цианокобаламина (гранулематозный энтерит – болезнь Крона, целиакия – непереносимость глютена, удаление большого участка тонкой кишки, новообразования);
- Появление конкурентов, «присваивающих» витамин В12, который был предназначен для всасывания. Например, конкурентами нормального всасывания может выступать широкий лентец либо бактерии, усиленно размножающиеся и забирающие питательные вещества при синдроме слепой кишечной петли (стаз тонкой кишки, застойная кишечная петля).
картина крови при мегалобластной анемии
Любая болезнь у разных людей может проявлять себя по-разному, однако в отношении мегалобластной анемии можно выделить ведущую триаду симптомов, которые будут иметь место практически у всех больных:
- Отсутствующее в норме мегалобластное кроветворение в костном мозге, дает значительные изменения в периферической крови. Анализ показывает:
мегалобласты и другие изменения в крови
- малокровие (анемия) – уменьшение количества красных клеток крови – эритроцитов и снижение уровня красного пигмента крови – гемоглобина;
- гиперхромию (насыщенная окраска увеличенных в размерах эритроцитов);
- пойкилоцитоз (изменение формы красных клеток крови);
- анизоцитоз: макроцитоз (клетки большого размера) и в большей степени – мегалоцитоз (размер красных кровяных телец может превышать 8, а то и 12 микрон);
- мегакариоцитоз – появление гигантских клеток костного мозга, имеющих большое ядро;
- нормобластоз – присутствие в мазках крови ядерных форм клеток эритроидного (красного) ряда (как известно, эритроциты, циркулирующие в периферической крови, ядра не имеют);
- в красных клетках крови замечаются остатки ядерной субстанции (включения в виде телец Жолли либо колец Кобота);
- в анализе крови также может быть снижено количество других форменных элементов: тромбоцитов, нейтрофилов, моноцитов.
- Клинически, а также при инструментальном обследовании, явно прослеживаются признаки поражения ЖКТ:
- теряется аппетит, снижается вес;
- атрофируется слизистая желудка;
- соляная кислота в желудочном соке полностью исчезает (ахлоргидрия), поскольку, вследствие атрофии слизистой, обкладочные клетки отмирают и перестают ее продуцировать (кислотность желудочного сока – 0).
- По причине недостатка цианокобаламина в течение длительного времени начинает испытывать страдания нервная система, что проявляется формированием фуникулярного миелоза (комбинированного склероза). Клинически – наблюдаются симптомы поражения спинного мозга:
- парестезии;
- нарушение чувствительности;
- парезы и параличи;
- выраженная мышечная слабость
Очевидно, что данная гематологическая патология, сопровождаемая непомерным увеличением красных клеток крови и изменением в их ядре, при прогрессировании и отсутствии адекватной терапии может сделать человека полным инвалидом. Нарушения образования миелина при дефиците В12 приводят к весьма серьезным последствиям: со временем теряется не только поверхностная, но и глубокая мышечная чувствительность, «отказывают ноги» (паралич нижних конечностей), органы таза перестают нормально функционировать (недержание мочи и кала, импотенция и т. д.). Не зря за пернициозной анемией сохранилось определение – «злокачественная».
Лечение мегалобластной анемии заключается в назначении ударных доз цианокобаламина в первые три дня (до 1000 γ в сутки), особенно, если появились признаки дегенеративных изменений спинного мозга (двигательные и чувствительные расстройства), затем дозу снижают до 400 – 500 γ каждый день до того, пока уровень гемоглобина не придет в норму. В среднем курс лечения продолжается месяц – полтора.
Фолиевую кислоту, как правило, одновременно не назначают, даже если имеет место ее дефицит при недостатке витамина B12 (применение фолиевой кислоты возможно только при изолированном варианте – фолиеводефицитной анемии, с которой, кстати, бороться намного легче и проще, нежели с недостатком кобаламина). Насколько эффективно назначенное лечение – покажет анализ, произведенный через 5-7 дней от начала терапии (увеличение количества молодых форм эритроцитов – ретикулоцитоз, является положительным признаком). Если же успеха от лечебных мероприятий не наблюдается, то необходимость продолжать диагностический поиск остается.
Следующим этапом лечения мегалобластной анемии является закрепляющая терапии, суть которой состоит в еженедельном введении 400 – 500 γ цианокобаламина в течение двух месяцев.
Переливание крови (эритроцитарной массы) назначается только в случаях, если значения гемоглобина падают ниже 50 г/л.
При выписке на домашний режим больной от врача получает рекомендации, касающиеся профилактики обострений болезни:
- Лечение хронических заболеваний, которые стали причиной формирования этой патологии;
- Коррекция диеты (отмена вегетарианства, насыщение рациона мясными продуктами, листовыми овощами и фруктами, содержащими данные вещества);
- Отмена лекарственных средств, признанных «виновниками» нарушения синтеза ДНК;
- Профилактические курсы витамина B12 (8 – 10 инъекций 1 раз в 6 месяцев на протяжении нескольких лет или всей оставшейся жизни, если причину заболевания никаким способом устранить невозможно).
Заподозрить мегалобластную анемию получается уже при первом общем анализе крови (ОАК). Поскольку даже самые современные («навороченные») анализаторы не способны уловить те морфологические изменения в эритроцитах (см. выше), которые свойственны данной патологии, то исследование не должно доверяться исключительно аппарату, пусть и самому «умному». Хотя и он, наверняка, обнаружит некоторые сдвиги в ОАК. Обычно любая, уважающая себя лаборатория, придерживается «золотых стандартов» и мазок в обязательном порядке просматривается врачом под микроскопом. Однако болезнь не принадлежит к случайным находкам, поэтому первичная диагностика опирается на жалобы пациента и клинические симптомы:
- Слабость, усталость, снижение общей физической активности и трудоспособности;
- Эпизодически наступающая темнота в глазах;
- Снижение уровня АД (гипотония);
- Частые головокружения и головные боли;
- Учащенное сердцебиение;
- Признаки изменения слизистой полости рта по типу глоссита;
- Возможно увеличение размеров селезенки (спленомегалия) и печени (гепатомегалия);
- Отеки ног;
- Склонность к поносам, хотя запоры также не исключены, то есть, эти неприятные состояния могут чередоваться между собой;
- Потеря аппетита, вкусовые нарушения, отсюда – снижение массы тела.
Далее последует более углубленная диагностика:
- Биохимический анализ крови (БАК) – он покажет повышение не конъюгированного (не связанного) билирубина, а также, скорее всего, изменение показателей сывороточного железа и значений лактатдегидрогеназы – ЛДГ;
- ФГДС (фиброгастродуоденоскопия), которая позволит определить состояние слизистой желудка (признаки атрофии);
- Пункция спинного мозга, поскольку лабораторные признаки похожи на таковые при гемолитической и апластической анемии;
- Дифференциальная диагностика – уточнение формы мегалобластной анемии (B12-дефицитная, недостаток фолиевой кислоты или комбинированный вариант).
Своевременная диагностика мегалобластной анемии очень важна для здоровья пациента, ведь опоздание или диагностическая ошибка (к счастью, она случается крайне редко) может привести к развитию анемической комы. Клиника ее довольно тяжела: больной не приходит в сознание, тяжело дышит, его пульс заметно учащен, артериальное давление снижено, кожные покровы отдают лимонным оттенком (при пернициозной анемии возможен усиленный гемолиз кровяных телец), возможно появление тонических и клонических судорог. Больной может погибнуть…
У детей мегалобластная анемия в наибольшей степени носит наследственный характер и имеет несколько форм:
- Расстройство всасывания цианокобаламина может быть обусловлено поражением эпителиального слоя тонкой кишки и отсутствием тетрагидрофолата в клетках, который является активной формой витамина B9 (при этом, содержание внутреннего фактора остается в норме);
- Мегалобластная анемия, вызванная наследственной недостаточностью внутреннего фактора, характеризуется уменьшением (иногда значительным) выделения ВФ обкладочными клетками слизистой желудка (тип наследования – аутосомно-рецессивный);
- Дефицит переносящего В12 белка – транскобаламина (аутосомно-рецессивное наследование) абсолютно не виден при исследовании плазмы крови (значения кобаламина остаются в пределах нормы), зато в тканях – глубочайший дефицит (для В12 нет «транспортного средства», чтобы проникнуть в ткани);
- Очень редкая форма, которая наблюдается у детей, достигших подросткового возраста – ювенильная пернициозная анемия.
У детей с наследственной формой симптомы (отказ от еды, рвота, сухость и шелушение кожных покровов, признаки атрофического глоссита, частые пневмонии) проявляются уже на первом втором, реже на третьем, году жизни.
Диагностика болезни преимущественно основывается на морфологическом исследовании периферической крови и костного мозга, где обнаруживаются признаки мегалобластного кроветворения.
Лечение, в принципе, как и у взрослых: симптоматическое и назначение цианокобаламина по схеме.
Кроме этого существует ряд очень редких врожденных заболеваний, для которых характерно нарушение выработки дезоксирибонуклеиновой кислоты, а в качестве главного симптома выступает мегалобластная анемия. Вот, к примеру, некоторые из них:
- Оротовая ацидурия – нарушение обмена пиримидинов;
- Тиамин-зависимая МА, природа которой так и остается невыясненной, хотя известно, что наследование идет по аутосомно-рецессивному пути;
- Врожденная мальабсорбция фолатов (аутосомно-рецессивный тип наследования) – расстройство всасывания фолатов в кишечном тракте и переноса их из кишечника в кровеносное русло и из кровотока через гематоэнцефалический барьер;
- Наследуемые по аутосомно-рецессивному типу врожденные расстройства обмена фолатов (например, недостаток активности фермента ДГФР – дигидрофолатредуктазы);
- Синдром Лиш-Найана (патологический ген находится в Х-хромосоме).
Некоторые из этих болезней задерживают умственное и физическое развитие, дают богатую неврологическую симптоматику. Практически все эти врожденные аномалии в каждом конкретном случае требуют своего отдельного лечения, поскольку витамин B12 оказывается просто неэффективным.
источник