Анемия определяется как снижение концентрации гемоглобина в периферической крови ниже показателя 120 г/л у женщин и 140 г/л у мужчин. Заболевание может протекать в разных формах, которые определяются по характерным признакам анемии.
Чтобы предотвратить анемию, необходима эффективная и слаженная работа почек, спинного мозга и питательных веществ в организме. Если хоть с одним из элементов этой системы что-то не так, возникает анемия.
Признаки анемии различны в зависимости от причины ее возникновения и тяжести патологии. На первый взгляд, может показаться, что у пациента обычная простуда или усталость. Но при появлении слабости, головокружения, бледности кожных покровов и слизистых оболочек, раздражительности можно предположить наличие анемии. При легкой форме анемии ее признаки могут какое-то время оставаться незамеченными, но становятся очевидными по мере ухудшения состояния, прогрессировании болезни.
В запущенной форме хроническая анемия проявляется одышкой, холодностью конечностей, нерегулярными менструациями или аменореей, замедленным заживлением ран, болью в груди, быстрым или нерегулярным пульсом, а также выпадением волос и ломкостью ногтей.
Нечастыми признаками анемии могут также быть обмороки, покалывания в руках и ногах (парестезии), низкое кровяное давление (при серьезной потере крови), низкая устойчивость к инфекции, болезненное учащенное сердцебиение (тахикардия), иногда увеличение селезенки.
Уменьшение количества красных кровяных клеток — еще не показатель анемии, потому что при некоторых ее разновидностях (например, гипохромная анемия) количество эритроцитов остается нормальным, но средняя концентрация гемоглобина низкая. Кроме того, образ жизни, рост, возраст и пол, могут существенно повлиять как на количество эритроцитов, так и на концентрацию гемоглобина. Если развитие анемии идет медленно, организм может адаптироваться к ней, вплоть до уровня гемоглобина 60 г/л.
При таком недуге, как анемия, в первую очередь, страдает иммунитет. Проблемы с иммунной системой отражаются на общем состоянии всего организма. И в данном случае возникшую простуду или вирусную инфекцию можно считать наименьшим злом, потому что хроническая анемия может способствовать развитию более серьезных заболеваний, например, сердечно—сосудистой системы, а также привести к нарушению работы центральной нервной системы.
Анемия особенно опасна для женщин «в положении». Она может привести к выкидышу, как на раннем, так и на позднем сроке, плацентарной недостаточности и даже преждевременным родам, что в результате может негативно повлиять на дальнейшее развитие малыша. Анемичные дети чаще подвержены простудам, могут отставать в физическом и умственном развитии.
Сама анемия является скорее состоянием (признаком) какого-либо недуга, а не самим заболеванием. Врачами анемия рассматривается либо в хронической, либо в острой форме. Хроническая анемия развивается в течение относительно длительного времени, в то время как острая анемия начинается внезапно. Только врач может определить наличие той или иной формы заболевания.
Хроническую анемию могут спровоцировать различные нарушения в работе органов и систем: функции костного мозга, печени, аутоиммунные состояния, почек, эндокринной и пищеварительной систем, а также инфекционные и онкологические заболевания, гельминтозы (инвазии паразитами).
Эритроциты живут в среднем 100 дней, поэтому организм постоянно меняет отмершие красные клетки на новые. Красные клетки (эритроциты) синтезируются в костном мозге. В качестве причины анемии, в первую очередь, рассматриваются кровотечение или расстройство процесса синтеза красных кровяных клеток в кости. Анемия встречается у взрослых и детей, но в преклонном возрасте она проявляется чаще. Примерно 10% населения страдает анемией, женщины в два раза чаще мужчин.
Существует множество заболеваний, которые вызывают хроническую анемию. Среди них:
- наружное кровотечение (кровоизлияние), вызванное менструацией, язвой;
- дефицит железа (костный мозг нуждается в железе для синтеза красных кровяных клеток);
- хронические заболевания (любое такое заболевание может привести к анемии);
- болезни почек (почки выделяют гормон эритропоэтин, необходимый для стимуляции эритропоэза — процесса образования эритроцитов);
- снижение чрезмерного объема крови при остром или хроническом кровотечении;
- чрезмерное разрушение эритроцитов при гемолитических заболеваниях;
- снижение эритропоэза из-за угнетенного синтеза нуклеопротеидов, которые в норме его стимулируют;
- дефицит железа в рационе питания;
- угнетение костного мозга (при отравлении);
- беременность (задержка воды и жидкостей во время беременности приводит к разжижению крови и уменьшению процентного содержания красных кровяных телец);
- плохое питание (витамины и минералы имеют жизненно важное значение для синтеза эритроцитов),
- алкоголизм (включая низкий уровень витаминов и минералов),
Другие причины являются менее распространенными. Среди них заболевания печени, нарушения свертываемости крови, инфекции, рак, артрит, дефицит ферментов, токсины или наследственные заболевания.
Лечение анемии основывается, в первую очередь, на устранение ее причины, потому что в некоторых случаях она угрожает жизни пациента и требует переливания крови.
Некоторыми лекарственными средствами и методами лечения анемии являются:
- железо (во время беременности, когда уровень железа в организме низкий),
- витаминные добавки (для покрытия потребности в фолиевой кислоты и витамина В 12)
- антибиотики, когда речь идет о инфекции.
Быстрее всего восстанавливаются молодые пациенты, в то время как для людей преклонного возраста необходимо более длительное лечение. И это связано с преобладанием у них хронических заболеваний. Анемия ухудшает почти все физиологические недомогания.
Профилактика анемии состоит в полноценном и сбалансированном питании, с употреблением мяса, молочных продуктов, овощей и фруктов. Эти продукты являются источником железа и витаминов, необходимых организму для выработки гемоглобина в крови.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Анемия при хроническом заболевании (анемия вследствие нарушения реутилизации железа) является мультифакториальной и часто сопровождается дефицитом железа. Для постановки диагноза обычно требуется наличие хронической инфекции, воспаления, рака, микроцитарной или погранично-нормоцитарной анемии, показателей сывороточного трансферрина и ферритина, которые определяются в значениях между типичными для железодефицитной анемии и сидеробластной анемии. Терапия направлена на лечение основного заболевания, а если оно носит необратимый характер, сводится к применению эритропоэтина.
Во всем мире анемия при хроническом заболевании является второй по распространенности. На ранних этапах эритроциты нормохромные, но с течением времени они становятся микроцитарными. Основной проблемой является неспособность эритроидного ряда костного мозга к пролиферации в ответ на анемию.

Этот тип анемии следует заподозрить при наличии хронического заболевания чаще инфекционного, воспалительного процесса (особенно ревматоидного артрита) или злокачественного новообразования, однако аналогичный процесс имеет место при любой инфекции или воспалении.

Выделяют три патофизиологических механизма:
- умеренное укорочение времени жизни эритроцитов по пока неясным причинам у больных раком или с хроническими гранулематозными инфекциями;
- нарушение эритропоэза вследствие снижения продукции ЭПО и ответа костного мозга на него;
- нарушение внутриклеточного метаболизма железа.
Ретикулярные клетки удерживают железо, полученное из старых эритроцитов, делая недоступным для синтеза гемоглобина; таким образом, невозможна компенсация анемии путем повышения продукции эритроцитов. Макрофагальные цитокины (например, IL-1, фактор некроза опухоли а, интерферон ) у больных с инфекцией, воспалительным процессом и раком вызывают или способствуют уменьшению продукции ЭПО и нарушают метаболизм железа.

Клинические проявления, как правило, те, которые определяют основное заболевание (инфекция, воспаление или злокачественное новообразование).

Анемия на фоне хронического заболевания предполагается у больных с микроцитарной или погранично-нормоцитарной анемией с хронической инфекцией, воспалением или раком. Если есть подозрение на хроническую анемию, необходимо исследовать сывороточное железо, трансферрин, рецептор трансферрина и сывороточный ферритин. Уровень гемоглобина обычно превышает 80 г/л, пока дополнительные процессы не приведут к прогрессированию анемии. Если в дополнение к хроническому заболеванию имеется железодефицитное состояние, уровень сывороточного ферритина обычно составляет менее 100 нг/мл, и, если при наличии инфекции, воспаления или злокачественного новообразования уровень ферритина несколько меньше 100 нг/мл, предполагается, что параллельно с вызванной хроническим заболеванием анемией имеется и железодефицит. Вместе с тем, учитывая возможность ложного повышения уровня сывороточного ферритина в качестве маркера острой фазы, в случаях высокого уровня сывороточного ферритина (> 100 нг/мл) в дифференциальной диагностике железодефицита и анемии на фоне хронического заболевания помогает определение рецептора сывороточного трансферрина.

источник
Опубликовано в журнале:
В мире лекарств »» №3 1999 ПРОФЕССОР А.В. ПИВНИК, РУКОВОДИТЕЛЬ ОТДЕЛЕНИЯ ХИМИОТЕРАПИИ ГЕМАТОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ И ИНТЕНСИВНОЙ ТЕРАПИИ ГЕМАТОЛОГИЧЕСКОГО НАУЧНОГО ЦЕНТРА РАМН
Анемия — уменьшение общего количества гемоглобина, чаще всего проявляющееся уменьшением его концентрации в единице объема крови. В большинстве случаев, за исключением железодефицитных состояний и талассемии, анемия сопровождается и снижением содержания эритроцитов в единице объема крови [1].
Хроническая железодефицитная анемия (ХЖДА) — клинико-гематологический синдром, характеризующийся нарушением синтеза гемоглобина вследствие дефицита железа и проявляющийся анемией и сидеропенией [2]. Основными причинами ХЖДА являются кровопотери и недостаток богатой гемом пищи — мяса и рыбы. Разберем основные моменты проблемы: обмен железа, диагностика ХЖДА, вопросы лечения и профилактики.
Обмен железа
У взрослого мужчины весом 70 кг содержится 4 г железа: в геме гемоглобина эритроцитов содержится 2500 мг, в запасах (ткани и паренхиматозные органы) — 1000 мг (у женщин около 300 мг), в миоглобине и дыхательных ферментах — 300 мг, в плазму поступают из разрушающихся стареющих эритроцитов и уходят для формирования эритрона 20 мг ежедневно, всасываются в кишечнике и теряются ежедневно 1-2 мг [3]. Железо в пище представлено железом гема и различными железосодержащими солями и комплексами [4]. В растительной пище это металлопротеины, растворимое железо и различные хелаты, уменьшающие его всасывание. В мясной пище не гемовое железо представлено ферритином гемосидерином и цитратом железа. Комплексы железа с белком и углеводами обрабатываются кислым содержимым желудка и двенадцатиперстной кишки и высвобождают железо в виде его солей.
Основная масса железа пищи представлена как его закись (трехвалентное железо), и любая соль окисного двухвалентного железа на воздухе спонтанно окисляется до закиси. В сильно кислой среде закись железа растворима, при ощелачивании желудочного содержимого (рН более 2) она превращается в нерастворимые полигидроксиды. В двенадцатиперстной и тощей кишке происходит максимальное всасывание закиси (трехвалентного) железа в виде хелатов — они удерживают его в растворимой форме — аскорбат, цитрат и другие органические кислоты и аминокислоты. Окись железа всасывается лучше закиси. Железо в просвете кишки находится в форме закиси (трехвалентного железа), связанной с хелатами. Оно связывается с муцином и остается в растворимой форме при ощелачивании среды.
Белки, связывающие железо, выявлены на мембране ворсинок тонкой кишки. Они представлены полипептидами интегрина. Другой белок — мобилферрин — образует комплексы с интегрином, которые «складируют» железо в цитоплазме энтероцита для последующего транспорта в кровоток.
Двухвалентное железо лучше, чем трехвалентное, всасывается из просвета кишки, так как при существующем рН оно остается растворимым. Мобилферрин, белок с молекулярной массой 56 кДа, переносит железо внутри клетки. Свойства этого белка очень близки описанному белку кальретикулину. Мультиполипептидный комплекс мобилферрина молекулярной массой 520 кДа известен как параферритин. Он связывает трехвалентное железо, соединенное с мобилферрином, и флавинмонооксигеназу и В2-микроглобулин с помощью никотинамидадениндинуклеотид фосфата и переводит закисное трехвалентное железо в окисное двухвалентное.
Железо гема всасывается из мяса более эффективно, чем неорганическое железо пищи и по другому механизму. Поэтому ХЖДА реже встречается в странах, где мясо существенно представлено в рационе. Продукты деградации глобина способствуют всасыванию железа из гема гемоглобина и миоглобина. Хелаты, уменьшающие всасывание неорганического железа из пищи, не влияют на всасывание гемового железа. Гем проникает в клетку кишечника как интактный металлопорфирин. Гем-оксигеназа расщепляет порфириновое кольцо, высвобождая железо. Оно связывается с мобилферрином и параферритином, который действует как ферриредуктаза. Конечным продуктом этой реакции является вновь образованный комплекс гема с белком. Через энтероциты железо, связанное с трансферрином, поступает в кровоток.
У позвоночных транспорт железа от места всасывания, хранения и утилизации обеспечивается гликопротеином плазмы — трансферрином. Он связывает железо прочно, но обратимо. Трансферрин связывается с клетками через собственные рецепторы на их мембране. Железо в клетках хранится в виде ферритина. У мужчин содержание железа равно 55 мг/кг веса, у женщин — 45 мг/кг веса. Трансферрин связывается с клетками при помощи рецепторов к нему, расположенных на мембранах всех клеток, кроме зрелых эритроцитов. Для клинических целей уровень трансферрина в плазме выражается в количестве железа, которое он может связать — это так называемая общая железосвязывающая способность плазмы. Уровень железа в плазме около 18 мкмоль/литр, а общая железосвязывающая способность 56 мкм/л, то есть трансферрин насыщен железом на 30%. При полном насыщении трансферрина в плазме начинает определяться низкомолекулярное железо; оно откладывается в печени и поджелудочной железе, вызывая их повреждение. Эритроциты циркулируют 120 дней, постепенно разрушаясь и возвращая железо гема в запасы и трансферрин. Физиологические потери железа приходятся на потерю через желудочно-кишечный тракт (не более 2 мл крови — не более 2 мг железа за сутки по определению с радиоактивным хромом), на менструации у женщин (около 30-40 мл в сутки), на одну беременность, роды и лактацию — 800 мг (Идельсон Л.И., [1], стр. 3-21). Таким образом, из пищи всасывается 1-1,5 мг железа в сутки, что при полном здоровье обеспечивает потребности взрослого человека.
Перед исследованием обмена железа обязательно исключение приема препаратов железа на 7-10 дней. Нормальные показатели красной крови (с пределами отклонений в полторы сигмы) для жителей СССР по Соколову В.В. и Грибовой И.А., 1972, [1]: эритроциты у мужчин 4,6 млн в микролитре (пределы 4-5,1), у женщин — 4,2 млн (3,7-4,7); гемоглобин у мужчин 148 г/л (132-164), у женщин — 130 г/л (115-145), ретикулоциты 0,7% (0,2-1,2). Perkins [5] приводит свои данные за 1998 г.: эритроциты у мужчин 4,5-5,9 млн в мкл, у женщин — 4,5-5,1; гемоглобин у мужчин 140-175 г/л, у женщин — 123-153 г/л, ретикулоциты 0,5-2,5%, средний объем эритроцита (MCV) 80-96 fL (фенталитр — один кубический микролитр), среднее содержание гемоглобина в эритроците (МСН) 27,5-33,2 пикограмм (пг), средняя концентрация гемоглобина в эритроцитах (МСНС) 334-355 г/л, гематокрит (VPRC) у мужчин 0,47, у женщин — 0,42; содержание железа в сыворотке у мужчин 13-30 мкмоль/л, у женщин — 12-25. Wharton [6] приводит средние показатели обмена железа у подростков обоего пола 12-15 лет: насыщение трансферрина 14%, ферритин сыворотки 12 мкг/л, протопорфирин эритроцитов 70 мкг/дл эритроцитов). Средний гемоглобин (с учетом двух сигм) у мальчиков 120 г/л и у девочек 115. Железодефицитной анемией признается состояние, при котором фиксируются не менее двух вышеперечисленных показателей обмена железа при уровне гемоглобина менее 115 г/л. Итак, выявление микроцитарной гипохромной анемии при микроскопии мазка периферической крови при низком содержании железа и ферритина в сыворотке крови служат надежными диагностическими признаками хронической железодефицитной анемии.
Мышечная слабость, нарушения вкуса и обоняния — желание есть необычную пищу (мел, штукатурку, глину, бумагу, сырые овощи, лед, сухие крупы др.), вдыхать обычно неприятные запахи (бензин, керосин, лаки и краски, влажный пепел табака и др.), появление «заед» в углах рта, тусклый цвет волос и их «сечение», затруднение при глотании твердой и жидкой пищи, эпизоды недержания мочи — вот набор жалоб, с которыми появляется женщина средних лет. Далее выясняется, что менструальный цикл нарушен — выявляется гиперполименоррея, нередки геморроидальные кровотечения. В анамнезе упоминаются несколько абортов и повторные роды с кровопотерей. При осмотре видны дистрофические изменения ногтей — они в форме ложек — койлонихии. Кожа и слизистые оболочки бледны. При длительной анемии у детей обнаруживаются дефекты иммунитета (частые простудные заболевания, гнойно-воспалительные изменения кожи и т.д.), расстройства памяти, нарушения интеллекта. У взрослых, особенно часто у пожилых, — кардиопатии с недостаточностью кровообращения.
Причина хронической железодефицитной анемии почти всегда — кровопотери, и желудочно-кишечный тракт занимает здесь первое место. Общее правило — анемия у мужчин всегда плохо, всегда опасно! Анемия у женщин — менее тревожно. Гинекологические кровопотери, обычно обильные и затянутые менструации — вторая по частоте причина малокровия, а у женщин — первая. В целях диагностики принято исследовать весь пищеварительный тракт, проводить осмотр полости рта, языка (телеангиоэктазии — болезнь Рандю-Ослера). Если в патогенез анемии вовлечен кишечник, то диагноз устанавливается только с помощью селективной ангиографии мезентериальных артерий). Проводится фиброскопия и биопсия слизистой оболочки пищевода (дивертикулы, рефлюкс-эзофагит, опухоли), желудка (язвы, полипы, опухоли, сосудистые аномалии), кишечника (дивертикулы — известен дивертикул Миккеля вблизи Трейцевой связки, воспалительные процессы, сосудистые поражения, опухоли, отсутствие части кишечника или желудка вследствие операций, «слепые» петли и карманы после неудачных резекций кишки). Пальцевое исследование прямой кишки — обязательная манипуляция по протоколу исследования больных анемиями. Столь же обязательны поиски кровососущих паразитов или их яиц в фекалиях. К редким причинам дефицита железа относятся изолированный легочный сидероз (аутоиммунный васкулт с кровотечением в легочную ткань) и механический гемолиз с потерей железа с мочей (гемосидерин) при оперативных хирургических дефектах протезирования клапанов сердца. Кровотечения в замкнутые полости также случаются редко, например, при эндометриозе с расположением циклически кровоточащего эндометрия в брюшной полости. Наиболее частая причина анемии у крепких рабочих — мужчин — геморроидальные кровотечения, о сути которых нередко впервые докладывает больному врач. У мальчиков-подростков неожиданной находкой случаются постбульбарные кровоточащие язвы двенадцатиперстной кишки.
Еще одна причина малокровия — проявление дефицита железа у девушек-подростков, когда реализуются сразу несколько причин: недополучение, вследствие недостатка железа у матери, быстрый рост и появление менструаций. Это — хлороз, «бледная немочь». Быстро и хорошо лечится пероральным приемом железа.
Основные положения: хроническая железодефицитная анемия
1) никогда не требуется переливаний эритроцитов;
2) практически никогда не нужно парентеральное введение железа (внтуримышечно и внутривенно);
3) нет необходимости ничего добавлять к препаратам железа внутрь — ни витаминов в инъекциях, ни соляной кислоты, ни глюкозы внутривенно, ни «стимуляторов кроветворения», ни пищевых добавок;
4) лечение проводится только длительным приемом препаратов двухвалентного железа внутрь в умеренных дозах, причем существенный прирост гемоглобина, в отличие от улучшения самочувствия, будет не скорым — через 4-6 недель
Обычно назначается любой препарат двухвалентного железа — чаще это сульфат железа — лучше его пролонгированная лекарственная форма, в средней лечебной дозе на несколько месяцев, затем доза снижается ло минимальной еще на несколько месяцев, а затем (если причина малокровия не устранена), продолжается прием поддерживающей минимальной дозы в течение недели ежемесячно многие годы. Так, эта практика хорошо оправдала себя при лечении тардиферроном женщин с хронической постгеморрагической железодефицитной анемией вследствие многолетней гиперполименорреи — одна таблетка утром и вечером 6 месяцев без перерыва, затем одна таблетка в день еще 6 месяцев, затем несколько лет каждый день в течение недели в дни месячных. Это дисциплинирует пациенток, не дает забыть сроки приема препарата и обеспечивает нагрузку железом при появлении затянутых обильных месячных в период климакса. Бессмысленным анахронизмом является определение уровня гемоглобина до и после месячных.
При агастральной (гастрэктомия по поводу опухоли) анемии хороший эффект дает прием минимальной дозы препарата постоянно много лет и введение витамина В12 по 200 гамм в день внутримышечно четыре недели подряд каждый год пожизненно.
Беременным с дефицитом железа и малокровием (небольшое снижение уровня гемоглобина и числа эритроцитов физиологично вследствие умеренной гидремии и не требует лечения) назначается средняя доза сульфата железа внутрь до родов и в период кормления грудью, если у ребенка не возникнет диаррея, что обычно случается редко.
Практика срочной госпитализации таких беременных женщин в отделения патологии беременности, назначения переливаний эритроцитов, плазмы, железа в инъекциях, витаминов, глюкозы — порочна. Она грозит инфицированием женщин гепатитами, изоиммунизацией компонентами крови, аллергическими реакциями, ненужными затратами, психологической дизадаптацией беременных.
Профилактика железодефицитных анемий сводится к полноценному питанию с потреблением животных белков, мяса, рыбы, контролю за возможными заболеваниями, о которых сказано выше. Показатель благосостояния государства — причины железодефицитных анемий: у богатых она носит постгеморрагический характер, а у бедных — алиментарный.
источник
Симптомы анемии формируются на фоне снижения гемоглобина. Норма этого вещества дискутабельна. Признаки малокровия прослеживаются у некоторых людей при показателе гемоглобина – 110 г/л.
У других пациентов клинических проявлений заболевания не прослеживаются при концентрации ниже 90 г/л. По классическим меркам анемическое состояние тяжелой степени наблюдается при уровне гемоглобина ниже 70 г/л.
Некоторые терапевты наблюдали идеальное состояние здоровья у пожилых пациентов при более низких цифрах данного показателя. Конечно, патологические симптомы заболевания на этом фоне проявляются, но они совместимы с жизнью.
Дискуссии на тему лабораторной нормы при малокровии продолжаются, но это не отменяет клинические проявления заболевания, требующие незамедлительного лечения.
Симптомы анемии отличаются на начальных и поздних стадиях. Прелатентная форма заболевания характеризуется следующими проявлениями:
- Снижение работоспособности;
- Общая утомляемость;
- Повышенная работоспособность;
- Шум в ушах;
- Головокружение;
- Ускорение частоты сокращений сердца;
- Одышка.
Жалоб у людей на ранней (латентной) стадии недуга немного. Чаще всего преобладает 2-3 из вышеописанных маркеров анемического состояния.
Признаки анемии зависят от биохимических изменений организма. При патологии страдают не только эритроциты. Наблюдается разрушение депо железа – ферритина, повышается уровень транспортного белка – трансферрина, происходит деструкция миоглобина . Эти процессы влияют на проявления недуга.
Какие признаки железодефицитной анемии при тяжелом течении:
- Тахикардия – учащение сердцебиения;
- Бледность кожи;
- Головокружение и головная боль;
- Сухость языка и отечность;
- Извращение вкуса (употребление мела и извести).
Симптомы анемии различаются в зависимости от вида болезни. Существует несколько его вариантов:
- Апластический;
- Железодефицитный;
- Гемолитический;
- Серповидно-клеточный;
- Шаровидный.
Рассмотрим, как распознать проявления малокровия у взрослых и детей по патологическим формам.
Признаки апластической анемии возникают на фоне нарушения образования эритроцитов костным мозгом. Специфические проявления заболевания:
- Постоянная утомляемость;
- Головокружение и общая слабость;
- Быстрая потеря веса и ухудшение аппетита;
- Кровотечения из носа и кишечника;
- Высокая температура;
- Образование язвенных дефектов ротовой полости.
Апластическая анемия наблюдается редко, поэтому ее клинические симптомы обнаруживаются поздно. Только на основе лабораторных анализов выявляются специфические изменения крови. Нарушение эритрогенеза костного мозга изучаются после исследования роста путем взятия биопсии из костей.
Признаки анемии гемолитической распознать можно по специфическому увеличению размеров печени и селезенки (гепатоспленомегалия). Они четко прослеживаются при выполнении ультразвукового исследования.
На латентной стадии болезни гемолиз (разрушение эритроцитов) определить сложно. Незначительный распад красных клеток компенсируется за счет повышения эритрогенеза в костном мозге.
Внутриклеточное разрушение эритроцитов осуществляется селезенкой, костным мозгом и печенью. Процесс необходим для получения железе из погибших красных клеток для обратной утилизации железа.
Внутрисосудистый вид недуга осуществляется непосредственно в сосудистом русле. Для такого типа болезни характерны следующие признаки анемии:
- Тахикардия;
- Потемнение мочи;
- Увеличение селезенки и печени;
- Одышка;
- Слабость и головокружение.
Из всех видов заболевания специфичными симптомами анемического состояния гемолитического типа является гепатоспленомегалия.
Признаки анемии при дефиците витамина B12 у женщин выражены сильнее, чем у мужчин. Нарушение метаболизма этого вещества имеет приобретенный и врожденный характер. Патология развивается медленно, поэтому у представителей сильной половины протекает без симптомов. У женщин на фоне менструаций усиливаются признаки болезни.
Генетическая предрасположенность приводит к появлению следующих симптомов B12 дефицитной анемии в детском возрасте:
- Боль внизу живота при поражении желудочно-кишечного тракта;
- Головные боли, нарушения памяти и другие неврологические заболевания;
- Нарушение эритрогенеза костного мозга.
Признаки анемии у женщин «завуалированы» менструальным циклом. Представительницы прекрасной половины некоторые проявления заболевания «списывают» на недомогание перед очередными месячными. Только когда проявления недуга становятся выраженными, они понимают, что симптомы не связаны с гормональной системой.
Проявления анемии у детей максимально выражены между 3 и 6-м месяцами. Если малыш недоношен, у него наблюдается дефицит железа уже на первых месяцах жизни.
Главные признаки анемического состояния у грудных детей:
- Сухость кожных покровов;
- Бледность;
- Образование трещин уголков рта, стоматит во рту;
- Блестящий язык;
- Неподвижность и быстрая утомляемость;
- Плаксивость.
Чтобы определить признаки анемического состояния у детей, необходимо провести лабораторные анализы и выявить снижение количества эритроцитов, низкий уровень гемоглобина.
Гипохромия крови у взрослых легкой степени не приводит к внешним клиническим проявлениям. На фоне патологии могут бледнеть кожные покровы. После физических нагрузок незначительно увеличивается частота сокращений сердца и ускоряется дыхательный ритм.
При средней степени патологии симптоматика анемического состояния крови у взрослых проявляется более четко. Только при тяжелой степени болезни наблюдаются признаки заболевания:
- Быстрая утомляемость;
- Затруднения глотания;
- Нарушение пищеварения;
- Выпадение волос;
- Ломкость ногтей;
- Общая слабость;
- Головокружение;
- Шум в ушах;
- Одышка.
Следует понимать, что признаки железодефицитной анемии у взрослых существуют на фоне другой патологии. Из-за этого их сложно диагностировать .
Симптоматика патологии у мужчин и женщин отличается в зависимости от причины недуга. У представителей сильной половины выносливость выше леди. Красавицы склонны к кровопотерям, поэтому на фоне обильных месячных патологические проявления анемического синдрома у них усиливаются.
Если у детей признаки анемии существуют постоянно и длительно, то у женщин они обостряются перед началом менструального цикла (речь идет о железодефицитных нормохромных вариантах патологии).
У взрослых нужно обратить внимание не внешние признаки заболевания:
- Дряблость кожи;
- Выпадение волос;
- Ломкость ногтей;
- Изменение вкусовых ощущений.
На фоне дефицита железа у человека вырастает потребность в использовании кислой, острой и соленой пищи.
Причины анемического синдрома: кровотечения (маточные, носовые, кишечные), заболевания печени и селезенки. Существуют лекарственные формы заболевания, токсичные формы. Под влиянием неблагоприятных факторов появляется апластический вариант болезни, гемолиз эритроцитов. При недостатке витамина B12 появляется пернициозная форма патологии.
При беременности анемический синдром при длительном и неконтролируемом состоянии человека приводит нарушению свертываемости крови.
Тяжелые степени болезни опасны летальным исходом. Когда болезнь выявлена на начальных стадиях, можно остановить летальный исход. Даже в этом случае лечение анемии длительное. Оно продолжается не менее 4 месяцев.
На протяжении всего курса следует контролировать состояние крови с помощью лабораторных анализов. Они позволяют при необходимости контролировать дозу препарата.
источник
Железодефицитная анемия (малокровие) обычно рассматривают скорее в качестве симптома другого заболевания или в виде состояния, возникающего при недостаточной концентрации в организме железа.
Причины и факторы, способствующие развитию анемического синдрома:
- Развивается болезнь у маленьких детей и взрослых, соблюдающих строгую диету, если они не получают необходимого количества железа с едой.
- На фоне нарушений в пищеварительной системе. Известно, что всасывание микроэлементов происходит в тонкой кишке (верхние отделы) и в желудке. А тем более, после удаления части желудка, способность пищеварительной системы к абсорбции нарушается.
- Анемический синдром может развиться из-за больших потерь крови. Это является основной причиной железодефицитных состояний. Часто синдром возникает у женщин из-за больших потерь крови во время обильной менструации и у тех, кто страдает от язвы пищеварительного тракта, рака желудка, геморроя, новообразований в толстой кишке.
- Сокращение времени жизни эритроцитов в крови или быстрое их разрушение. В норме срок жизни эритроцита – 4 месяца. В некоторых случаях причиной гемолиза является патология селезенки. Развивается гемолитическая или серповидно-клеточная анемия. При таком заболевании организмом вырабатывается аномальный гемоглобин.
При подозрении на анемию, важно оперативно обратится за помощью к специалисту. Врач поможет выявить причины и способы лечения болезни. Синдром приводит к снижению иммунитета, к упадку сил, ограничению работоспособности. Также анемия может стать важным сигналом о развитии других патологий и серьезных проблем в работе отдельных органов и их систем.
Диагноз ставят по анализу крови, а лечение, как правило, заключается в восстановлении количества железа с помощью лек. препаратов. Лекарства используют внутрь или вводят с помощью инъекций.
| Пол, возраст | Порог Нb (Г/Л) | Порог Нb (Г/%) |
| Дети от 3 месяцев до 5 лет | 110 | 11,0 |
| Дети от 5 до 12 лет | 115 | 11,5 |
| Дети от 12 до 15 лет | 120 | 12,0 |
| Мужчины от 15 лет | 130 — 160 | 13,0 — 16,0 |
| Женщины от 15 лет | 120 — 140 | 12,0 — 14,0 |
| Беременные женщины | 110 | 11,0 |
Можно выделить 3 основных механизма развития анемии:
- Вследствие нарушения процесса образования эритроцитов и образования гемоглобина. Такого рода механизм можно проследить при недостаточном поступлении железа, фолиевой кислоты и витамина В12, при заболеваниях костного мозга. Иногда дефицитное состояние может возникнуть из-за приема сверхбольших доз витамина С. При приеме сверх доз аскорбиновой к-ты происходит блокировка витамина В12 и нарушение процессов кроветворения.
- Острая потеря эритроцитов. Обычно – это последствия острых кровотечений, операций и травм. При хронических кровотечениях в небольших объемах причиной анемии выступает не просто потеря эритроцитов, но и недостаток железа на фоне хронической утраты крови.
- Анемический синдром — последствия от ускоренного разрушения эритроцитов крови. При нормальной работе костного мозга и иных органов кроветворения эритроциты живут порядка 4 месяцев, а затем разрушаются. При гемолитической анемии, гемоглобинопатии и так далее скорость разрушения эритроцитов выше, чем их производства. Иногда процесс протекает под влиянием внешних стимулов, химических веществ (уксус).
Рассмотрим различные виды у взрослых. Анемия является симптомом, а не отдельным заболеванием и может возникать при ряде болезней. Они, как правило, связаны с первичным поражением кроветворной системы или не зависят от нее. Невозможно провести четкую нозологическую классификацию анемий. Для этого используют принцип практической целесообразности. И в результате заболевание делят по единому классификационному признаку – по цветовому показателю.
Падение уровня гемоглобина в крови чаще всего наблюдают при одновременном снижении количества и качества эритроцитов. Любой вид анемии непременно приводит к снижению эффективности дыхательной функции крови, возникновению кислородного голодания тканей. Обычно это видно по бледности кожных покровов, слабости, высокой утомляемости, головным болям, головокружении, одышке, учащенному ритму сердца и т.д.
Врач назначает рутинное исследование мазка крови, в процессе анализа морфолог обязан указать на отклонения размера эритроцитов. Уменьшение может быть, как в меньшую (микроцитарная анемия), так и большую сторону (макроцитарная). Однако, если необходимую оценку производят без специальных микрометров, то она является весьма субъективной.
Анемии, которые могут развиться при болезнях почек, гипопластические, АХЗ и острую постгеморрагическую относят к нормоцитарным. Макроцитарные анемии бывают нормо- и гиперхромными, а микроцитарные – гипохромными.
Намного информативнее автоматический анализ крови, при котором соблюдается четкая стандартизация важных показателей. Учитывают средний корпускулярный объем (СКО), который можно измерить в фемтолитрах (fl, фл). Нормальное значение СКО составляет 80-90 фл и называется нормоцитозом. Если показатель повышен до 95 и более – то фиксируют развитие макроцитоза. При снижении менее 80 фл ставят диагноз микроцитоз. Есть у автоматического метода и свои недостатки: достаточно дорогое и чуткое оборудование, которому необходимо соответствующее обслуживание.
При замене цветового показателя на СКО не нарушается привычная классификация анемий по цветовому показателю. Анемии подразделяют на группы по различным признакам. Классификацию, как правило, основывают на удобстве и практической значимости для постановки диагноза.
Цветовой показатель покажет степень насыщения эритроцита гемоглобином. У здорового человека ЦП колеблется 0,86 до 1,1. В зависимости от него различают такие анемии:
- Гипохромная анемия, если ЦП меньше 0,86 (по некоторым классификациям ниже 0,8). При таких анализах ставят диагноз талассемия или железодефицитная анемия.
- При нормохромной анемии ЦП колеблется в пределах 0,86 — 1,1. В таком случае у пациента наблюдается постгеморрагическая анемии, гемолитические анемии, апластические анемии, неопластические заболевания костного мозга, внекостномозговые опухоли, анемия из-за снижения темпов выработки и количества эритропоэтина.
- Гиперхромная анемия – при ЦП более 1,1. Такие показатели характерны для фолиеводефицитной анемии, а также витамин B12-дефицитной анемии, для миелодиспластического синдрома.
Проводится в зависимости от выраженности снижения уровня гемоглобина в крови. Классификация по степени тяжести предполагает:
- легкую степень (когда уровень гемоглобина ниже нормы, но остается на уровне более 90 грамм на литр);
- среднюю степень тяжести (когда гемоглобин 70-90 г/л);
- тяжелую степень (когда уровень гемоглобина остается меньше 70 грамм на литр).
Разделение степени анемии по уровню гемоглобина достаточно распространено. Чаще всего именно по гемоглобину подтверждают диагноз, а потом уже проводят более детальную диагностику.
Характеризуется незначительным падением количества гемоглобина в крови. Обычно проявляются следующие симптомы:
- усталость;
- апатия;
- общее недомогание;
- часто развивается у беременных.
Как уже упоминалось выше, анемия 1 степени фиксируется, если уровень микроэлементов в крови ниже нормы, но выше 90 г на л.
Также первая степень заболевания часто поражает маленьких детей, появившихся на свет при многоплодной беременности или недоношенными. У детей постарше – это паразитические заболевания или погрешности в питании. Анемия легкой степени тяжести проще поддается лечению. Обычно рекомендуют соблюдать диету и усиленно питаться. При легкой степени анемии в рацион необходимо включать различные микроэлементы и витамины, в первую очередь – железо и витамин В12.
Анемия 2 степени или средней степени тяжести возникает не только при снижении уровня гемоглобина до 70 г/л. Возникает головокружение и головные боли, одышка, частое сердцебиение, трудности с дыханием. Дети часто болеют, у них наблюдается бледность губ и кожи. При 2 степени анемии может возникнуть кислородное голодание плода, снижается сократительная способность миокарда. Лечение медикаментозное + диета, следует больше находится и гулять по свежему воздуху.
На этой стадии острая анемия несет опасность для жизни человека. При 3 степени наблюдается ломкость ногтей и волос, острое снижение защитных сил организма, онемение конечностей, проблемы с сердцем и сосудами. Ребенок начинает часто болеть.
Особенно тяжелыми будут последствия такого симптома у беременных женщин. Это может негативно отразится на плоде, у матери развиться дистрофические изменения матки и плаценты. Анемия 3 степени лечится в стационаре, с переливанием эритроцитарной массы и другими видами медикаментозного лечения.
Основным признаком такого разделения принято считать количество молодых эритроцитов (ретикулоциты) в периферической картине крови. В норме показатель колеблется от 0,5 до 2%.
- Арегенераторную анемию (например, апластическая анемия) — ретикулоциты отсутствуют.
- Гипорегенераторная (витамин B12-дефицитная анемия или железодефицитная анемия) – ретикулоциты ниже 0,5%.
- Регенераторная или норморегенераторная (постгеморрагическая) — ретикулоциты 0,5 — 2%.
- Гиперрегенераторная (гемолитические анемии) — количество ретикулоцитов больше 2%.
Такая классификация основывается на различных механизмах развития анемии, как патологического процесса.
- Ассоциированные с дефицитом Fe — железодефицитные анемии.
- Гемолитические анемии — связанные с повышенным разрушением эритроцитов.
- Гис-гемолитические анемии — при нарушении кровообразования, протекающего в красном костном мозге.
- Постгеморрагические анемии — при острой или хронической кровопотере.
- В12- и фолиеводефицитные анемии.
Мегалобластные анемии: миокардит гемолитический и пернициозная анемия.
Гипохромия — это общее название для разных форм анемии, при которых цветовой показатель крови, вследствие недостатка гемоглобина, меньше 0,8. Не включена в список нозологических единиц. В анализе крови средний показатель для гемоглобина при таком состоянии меньше 30 пикограмм, а средняя концентрация гемоглобина в эритроците составляет менее 330 г на литр. Меняется не только цвет, но и диаметр (макро- или микроцитоз) и форма. Чаще всего при такого рода патологии красной крови кровяные тельца приобретают вид колец с бледно-красной серединой и темно-красными краями (обесцвечиваются).
Патологические формы эритроцитов могут возникать вследствие:
- Железодефицитной анемии при кровопотерях (геморрагическая), нарушении усвоения железа, при невынашивании плода и т.д.
- Хронического отравления свинцом.
- Талассемии – нарушения нормального процесса синтеза полипептидных цепей в структуре гемоглобина.
- Нарушения синтеза и утилизации порфиринов.
- Гиповитаминоза В6.
- При нарушении обмена вещества, хронических воспалительных процессах неинфекционного и инфекционного генезиса.
Дизэритропоэтическая анемия – целая группа достаточно редко встречающихся заболеваний крови, которые возникают из-за нарушения процессов эритропоэза. При этом, большая часть молодых эритроцитов погибает сразу после образования в костном мозге, а количество нормоцитов значительно снижается. Такого рода расстройство предполагает качественный, количественный, кинетический или совмещенный характер нарушения эритропоэза.
Следует упомянуть такую разновидность заболевания — гиперхромная макроцитарная анемия или малокровие. При котором также наблюдают снижение числа эритроцитов и уровня гемоглобина в единичном объеме крови. Как правило, при такого рода нарушениях параллельно дают сбой сердце и сосуды.
По коду МКБ-10 — D62 острая постгеморрагическая анемия. Такой симптом возникает после кровопотери. Подразделяют на острую постгеморрагическую анемию и хроническую постгеморрагическую анемию. Острая анемия развивается после острых и обильных кровотечений, хронические анемии возникают после длительных несильных кровотечений.
Во время быстрой кровопотери значительно снижается объем циркулирующей крови. В ответ на такое событие происходит компенсаторная реакция, которая заключается в возбуждении симпатического отдела нервной системы и рефлекторного спазма сосудов. Пульс ускоряется и ослабевает. Сосуды кожи и мышц максимально сужаются, кровь приливает к сосудам мозга, коронарным сосудам, что поддерживает снабжение кровью жизненно важных органов. При прогрессировании процесса начинает развиваться постгеморрагический шок.
Характерным клиническим симптомом постгеморрагической анемии является острая сосудистая недостаточность из-за гиповолемии (опустошение сосудистого русла). Внешне это проявляется ортостатическим коллапсом, одышкой, учащенным сердцебиением. В первые минуты кровопотери уровень гемоглобина может даже быть высоким, но после поступления тканевой жидкости в русло сосудов данный показатель снижается, даже если кровотечение уже прекратилось. Цветовой показатель остается в норме, одновременно происходит утрата эритроцитов и железа, нормохромная анемия. Ко вторым суткам увеличивается число ретикулоцитов, максимальных показателей достигает на 4-7 день (гиперрегенераторная анемия).
Диагноз ставят на основании клинических признаков и лабораторных показателей, повышения уровня остаточного азота, если кровотечение происходила в верхних отделах ЖКТ. Самое важное при такой нормохромной анемии – это устранить саму кровопотерю, восполнить устраненный объем крови эритроцитарной массой и гепарином (до 60% утраченной крови), кровезаменителями (5% р-р Альбумина, Раствор Рингера, Реополиглюкин).
При постановке диагноза постгеморрагическая анемия необходимо учитывать сведения о произошедшей острой кровопотере при наличии внешнего кровотечения. После массивного внутреннего диагноз основывают на клинических признаках и, в обязательном порядке, лабораторных пробах (Вебера, Грегерсена). Основанием для постановки диагноза также послужит рост уровня остаточного азота при кровотечении из верхнего отдела пищеварительного тракта.
После того, как кризис и острый период миновали, пациенту назначают препараты железа, витамины группы В, Е и С. Такая терапия производится в течение 6 месяцев. При утрате более 50% от объема циркулирующей крови — прогноз неблагоприятный.
Состояние может развиться в результате снижения поступления в организм фолиевой кислоты или нарушения процессов ее всасывания в пищеварительном тракте. Лечение заключается в дополнительном приеме недостающего вещества.
В отличии от патологии, ассоциированной с недостатком В12, фолиеводефицитная анемия диагностируется значительно реже.
Одной из основных причин фолиеводефицитной анемии является недостаточное содержание фолиевой к-ты в рационе. Следует помнить, что нужно включать в свое ежедневное меню больше зелени и печени. Также на здоровье значительно влияет алкогольная интоксикация, беременность, злокачественные новообразования, некоторые дерматиты, гемолиз.
Такого вида заболевания возникает при нарушении всасывания (например, при целиакии), под действием лекарственных средств, Метотрексата, Триамтерена, противосудорожных средств, барбитуратов, Метформина и др. Значительно повышается нужна организма в фолиевой кислоте после гемодиализа и при болезнях печени.
Также на здоровье оказывает влияние дефицит цианокобаламина и его кофермента – метилкобаламина. В таких условиях не происходит трансформации фолиевой кислоты в коферментную форму. В результате нарушается процесс нормального клеточного деления, начинают страдать клетки кроветворной ткани, которые ранее активно размножались. Тормозятся процессы созревания и размножения эритроцитов, сокращается их продолжительность жизни. Изменения касаются и лейкоцитов, возникает лейкопения и тромбоцитопения.
Далее в результате неправильного митоза появляются гигантские клетки эпителия пищевого канала и развиваются воспалительные процессы в слизистой оболочке, стоматиты, гастриты, эзофагиты, энтерит. Еще больше усугубляется первичное нарушения секреции и процесс всасывания внутреннего фактора, усиливается дефицит витаминов. Возникает порочный круг.
Из-за возникшего недостатка цианокобаламина, в организме начинают накапливаться продукты обмена, которые токсичны для нервных клеток. В волокнах тем временам начинают синтезироваться жирные кислоты уже с искаженной структурой. Наблюдается плавное изменение качества клеток спинного мозга и поражаются периферические и черепные нервные сплетения, развивается неврологическая симптоматика.
При таком виде анемии, как правило симптомы у пациента наблюдаются стандартные: высокая утомляемость, учащенное сердцебиение, бледность ногтей и губ, ярко-красный язык. На начальных стадиях отследить признаки поражения НС и ЖКТ практически невозможно. По результатам обследования выявляется гиперхромная макроцитарная анемия, лейкопения, тромбоцитопения. А лечение с помощью витамина В12 не вызывает улучшений лабораторных показателей. Диагноз можно подтвердить с помощью определения уровня сывороточной фолиевой к-ты и в эритроцитах. В норме ее содержание составляет от 100 до 450 нг/л. При фолиеводефицитной анемии концентрация фолиевой кислоты в эритроцитах значительно снижается.
Если проводят анализ периферической картины крови, то отмечают гиперхромную (макроцитарную) анемию при общем снижении уровня гемоглобина и эритроцитов. Непрямой билирубин меняется редко.
В качестве профилактики и для лечения фолиеводефицитной анемии должны назначить фолиевую кислоту в дозе 1 мг/сут, внутрь. Если есть необходимость врач может увеличить дозу. Улучшения должны наступать через в течение 3-4 суток, в том числе проходить должны и неврологические симптомы. В противном случае приходится говорить о недостатке именно витамина В12, а не фолиевой к-ты.
Обязательно проводить профилактику недостатка фолиевой к-ты у беременных женщин и пациентов, принимающих некоторые группы лек. препаратов. Для профилактики назначают 5 мг вещества в сутки.
Относится к виду витаминодефицитных (мегалобластных) анемий, которые возникают при недостаточном поступлении в организм витамина В12 (цианокобаламина). В результате В12-дефицитной анемии поражается кроветворная функция, нервная и пищеварительная система. В отличие от фолиеводефицитной В12-анемии, она развивается в преклонном или старческом возрасте, чаще всего у мужской половины. Проявляется заболевание постепенно.
Человек, страдающий В12-дефицитной анемией, будет испытывать общие симптомы: слабость, пониженная работоспособность, одышка, головокружение, жжение за грудиной, боли в ногах и языке, парестезии, шаткость походки. Такие симптомы будут сочетаться с желтушным цветом кожи, глосситом, незначительным увеличением печени и селезенки, негромким систолическим шумом, глухостью тонов сердца. Нередко поражается и нервная система, развивается комбинированный склероз или фуникулярный миелоз, нарушается чувствительность, полиневрит, атрофия мышц, паралич нижних конечностей.
Развивается анемия из-за недостатка витамина В12, из-за несбалансированности питания, голодания, алкоголизма и отсутствия аппетита. Также синдром может наблюдаться на фоне мальабсорбции, целиакии, изменений в слизистой оболочке кишечника, спру, лимфомы кишечника, болезни Крона, регионарного илеита, из-за длительного приема противосудорожных препаратов.
Вероятность развития В12-дефицитной анемии будет выше при беременности, гемолитической анемии, псориазе, эксфолиативном дерматите. При приеме алкоголя, препаратов–антагонистов фолатов, врождённых нарушениях метаболизма и атрофическом гастрите также может наблюдаться это заболевание.
Как правило, поставить диагноз В12-дефицитная анемия можно без особых проблем. Это может сделать гематолог, невролог, нефролог или гастроэнтеролог по результатам общего и биохимического анализа крови, наличию метилмалоновой кислоты. Также проводят УЗИ брюшной полости и исследование всасывания витамина В12 с помощью радиоизотопов. По показаниям можно провести аспирационную биопсию костного мозга.
Лечение проводят витамином В12 внутримышечно. В течение 1-1,5 месяцев используют поддерживающую дозу. Если уровень гемоглобина упал менее 60 г на л, при нарушении гемодинамики и угрозе анемической комы проводят трансфузии эритроцитов.
В качестве профилактики при заболеваниях, сопровождающихся нарушением всасывания витамина В12, а также после операций нужно под контролем содержания витамина В12 в моче и крови применять профилактические и лечебные курсы витаминотерапии.
Что это такое простыми словами? Это процесс ускоренного разрушения красных кровяных телец, он сопровождается значительным ростом уровня прямого билирубина в крови. Заболевание встречается достаточно редко.
Общим признаком можно считать ускоренное разрушение эритроцитов, сопровождающееся с одной стороны анемией и повышенным образованием продуктов распада эритроцитов, а с другой – реактивно усиленным эритропоэзом.
Аутоиммунная гемолитическая анемия, как правило вызвана генетическими дефектами мембран эритроцитов, что вызывает их повышенное разрушение. Аутоиммунное заболевание и гемолиз эритроцитов при приобретенных анемиях наступает под действием внутренних факторов или каких-либо факторов окружающей среды.
На развитие иммунных гемолитических анемий влияют посттрансфузионные реакции, вакцинации, прием некоторых препаратов (сульфаниламидов, анальгетиков, противомалярийных лекарств, производных нитрофуранового ряда). Также такой симптом может проявляться при гемобластозах, аутоиммунных патологиях (НЯК, СКВ), инфекционных болезнях (мононуклеоз, вирусная пневмония, сифилис, токсоплазмоз).
Гемолитические анемии можно поделить на два обширные группы заболеваний: приобретенные и врожденные.
Формы наследственных заболеваний:
- Эритроцитарные мембранопатии, такие как анемия Минковского-Шоффара или болезнь Минковского-Шоффара (микросфероцитоз), акантоцитоз, овалоцитоз, вызванные аномалиями в структуре мембран эритроцитов. Отметим, что сфероцитоз – самый распространенный вид среди патологий (микросфероцитоз).
- Энзимопении, вызванные дефицитом некоторых ферментов (пируваткиназа, глюкозо-6-фосфатдегидрогеназа).
- Гемоглобинопатии, возникшие из-за качественных нарушений структуры гемоглобина или изменения соотношения его нормальных форм.
Приобретенные гемолитические анемии делят на:
- Приобретенные мембранопатии (шпороклеточная анемия, болезнь Маркиафавы-Микели).
- Изо- и аутоиммунные, вызванные действием антител.
- Токсические, возникшие вследствие воздействия ядов, токсинов или других хим. агентов.
- Анемии, ассоциированные с механическими повреждениями в структуре эритроцитов.
Рост концентрации остаточных следов после распада эритроцитов в организме внешне будет проявляться желтухой лимонного оттенка. Также будет наблюдаться повышение концентрации в крови непрямого билирубина и железа. Отмечается уробилинурия и плейохромия кала и желчи. При внутрисосудистом гемолизе дополнительно развивается гипергемоглобинемия, гемоглобинурия, гемосидеринурия. Об усилении эритропоэза говорит ретикулоцитоз и полихроматофилия в составе периферической крови, либо эритронормобластоз костного мозга.
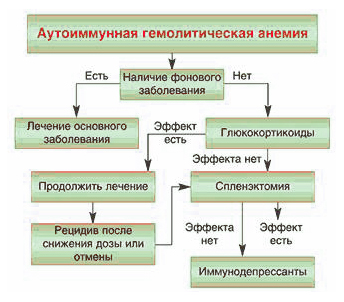
Если у пациента не микросфероцитарная анемия, обусловленная наследственным сфероцитозом или эллиптоцитозом, то необходимо, прежде всего проводить адекватную терапию заболевания, вызвавшего причину гемолитической анемии.
Для лечения обычно применяют:
- медикаменты (например, Десферал);
- спленэктомию;
- трансфузию эритроцитов при кризе;
- ГСК при аутоимунных заболеваниях в средней дозировке.
Апластическая анемия — заболевание, которое относят к категории миелодисплазий. При таком заболевании происходит резкое угнетение или прекращение роста и созревания клеток в костном мозге, еще называемое панмиелофтизом.
Типичными симптомами болезни являются: лейкопения, анемия, лимфопения и тромбоцитопения. Сам термин впервые появился в начале 20 века. Такое заболевание имеет достаточно тяжелое течение и без лечения (в том числе медикаментозного препаратом Атгам) имеет неблагоприятный прогноз.
Очень долго эту болезнь рассматривали в качестве синдрома, объединяющего различные патологические состояния в костном мозгу. В настоящее время термин «апластическая анемия» выделяется в качестве самостоятельной нозологической единицы. Его следует четко разграничивать от синдрома гипоплазии в кроветворной системе.
Апластическая анемия может быть вызвана различными причинами:
- химическими агентами, бензолом, солями тяжелых металлов и так далее;
- ионизирующим излучением;
- приемом некоторых лекарств, цитостатиков, НПВС, Анальгина, Мерказолила, Левомицетина;
- вирусами;
- наличием других аутоиммунных заболеваний.
Также существует форма апластической анемии, передающейся по наследству — анемия Фанкони. Лечение болезни заключается в приеме иммунодепрессантов и проведении пересадки костного мозга.
При серповидно-клеточной анемии человека происходит нарушение строения белка гемоглобина, он приобретает нетипичное кристаллическое строение, в виде серпа. Такую форму называют S-гемоглобином. Заболевание связывают с мутацией НВВ-гена, из-за которой в костном мозге начинает синтезироваться аномальный вид S-гемоглобина, в шестом положении в В-цепи вместо глутаминовой кислоты находится валин. Происходит полимеризация S-гемоглобина, образуются длинные тяжи, эритроциты приобретают форму серпа.
Тип наследования серповидноклеточной анемии – аутосомно-рецессивный при неполном доминировании. У гетерозиготных носителей в эритроцитах находится примерно равное количество гемоглобина А и S. Носители сами не болеют, а выявить серповидные эритроциты можно случайно при проведении лабораторного обследования. Симптомы же могут и вовсе не проявляться. Иногда такие люди начинают ощущать недомогание при гипоксии или тяжелом обезвоживании.
У гомозигот в крови есть только гемоглобин S, заболевание протекает достаточно тяжело. У таких больных высокий уровень степени разрушенных эритроцитов в селезенке, значительно короче срок жизни, часто проявляются признаки хронической недостаточности кислорода.
Такой вид анемии достаточно распространен в регионах, где высокий уровень заболеваемости малярией. У таких больных выше устойчивость к разным штаммам малярийного плазмодия. Поэтому столь вредные аллели часто проявляются у жителей Африки.
Симптомы сильно различаются и их можно наблюдать у детей уже с 3-х месячного возраста. Анемия может приводить к потере сознания, меньшей выносливости, вызвать желтуху. У младенцев наблюдается худоба, слабость, искривление конечностей, удлиненность туловища, изменения в строение черепа и зубов. Также у больных детей повышенная склонность к развитию сепсиса. У подростков наблюдают задержку развития на 2-3 года. Женщины, как правило, способны к зачатию и рождению ребенка.
Мегалобластная анемия (болезнь Аддисона-Бирмера, В12-дефицитная, пернициозная) — заболевание, вызванное недостатком фолиевой кислоты или витамина В12. Происходит это из-за недостатка веществ в пище или при заболеваниях пищеварительного тракта. Также мегалобластическая анемия может возникнуть при врожденных нарушениях процессов синтеза ДНК, приобретенных патологиях и из-за приема некоторых лекарств (антиметаболитов, противосудорожных).
При постоянном недостатке фолиевой кислоты и В12 развивается хроническая анемия, эритроциты изменяют свою форму и размеры. Более легкие стадии иногда протекают бессимптомно, далее начинают уже проявляться внешние признаки. Такое дефицитное состояние часто также называют пернициозной анемией. Заболевание получило статус анемии хронических заболеваний, так как проявляется у пациентов после 60 лет и у перенесших гепатит больных, при энтерите и раке кишечника. Подробнее о такого рода анемиях описано выше.
Развивается вследствие эндогенного В12-авитаминоза, вызванного атрофией желез фундального отдела желудка, которые в норме должны вырабатывать гастромукопротеин. В результате нарушаются процессы всасывания витамина В12 и возникает злокачественная анемия «пернициозного» типа. Чаще всего такой диагноз ставят в возрасте от 50 лет.
Болезнь сопровождается нарушениями нервной, сердечно-сосудистой, кроветворной и пищеварительной системы. Больные обычно жалуются на одышку, общую слабость, отечность ног, боли в сердце, «мурашки» по стопам и кистям, жгучие боли в языке и шаткость походки. По лабораторным показателям наблюдают анемию гиперхромного типа, лейкопению, тромбоцитопению.
Сидеробластная анемия также имеет название сидероахрестическая анемия (САА), железорефрактерная, железонасыщенная или сидеробластическая. Это патологическое состояние нарушений процесса синтеза микроэлементов и кроветворения, чаще всего – железа. Эритроциты содержат малое количество железа, из-за того, что микроэлемент активно расходуется костным мозгом и начинает накапливаться во внутренних органах. Заболевание развивается на фоне недостаточного содержания протопорфирина.
Выделяют две формы болезни:
- пиридоксин-зависимую, возникающую вследствие дефицита пиридоксальфосфата;
- пиридоксин-резистентную, развивающуюся из-за ферментного дефекта (дефицита гемсинтетазы).
Приобретенные формы сидероахрестической анемии чаще наблюдаются в пожилом возрасте, но болезнь не наследуется от родителей. Часто такого рода анемия развивается, как побочный эффект от лечения препаратами от туберкулеза или истощении пиридоксальфосфата при отравлении свинцом, при алкоголизме, миелопролиферативных болезнях крови, кожной порфирии. Встречаются и идиопатические формы САА.
Это редкое, передающееся по наследству заболевание. Анемия Фанкони встречается у 1 из 350000 детей. Наибольшее распространение заболевание получила среди евреев-ашкеназов и жителей Южной Африки.
Возникает из-за наличия дефектов в белковых кластерах, отвечающих за процесс репарации ДНК. Для заболевания характерная высокая ломкость у хромосом, наличие у пациентов старше 40 лет миелоидного лейкоза и апластической анемии.
Для новорожденных с таким недугом характерны врожденные дефекты развития, необычная пигментация, низкорослость, аномалии развития скелета и некоторые неврологические симптомы (косоглазие или недоразвитость одного из глаз, глухота, умственная отсталость), аномалии развития внутренних органов. К сожалению, в среднем такие пациенты живут не более 30 лет.
У диагноза неуточненная анемия код по МКБ-10 D64.9. Это первичный диагноз, который уточняется после проведения обследования у врача, так как он является вторичным признаком какого-либо основного заболеваний. Прежде всего следует исключить возможность кровопотери вследствие травм, хирургических вмешательств, внутренних кровотечений, далее проводится лабораторная диагностика.
По международной классификации МКБ-10 для миелодиспластического синдрома:
- D46.0 Рефрактерная анемия без сидеробластов, так обозначенная;
- D46.1 Рефрактерная анемия с сидеробластами;
- D46.2 Рефрактерная анемия с избытком бластов;
- D46.3 Рефрактерная анемия с избытком бластов с трансформацией;
- D46.4 Рефрактерная анемия неуточненная;
- D46.7 Другие миелодиспластические синдромы;
- D46.9 Миелодиспластический синдром неуточненный.
Приставка «рефрактерная» означает устойчивость заболевания к приему витаминов, препаратов железа, соблюдению диеты. Чаще всего такого вида анемия является наиболее распространенным видом миелодиспластического синдрома. Из-за нарушений процессов созревания бластов в крови значительно понижено содержание гемоглобина, проявляются признаки острого лейкоза. Примерно у 40% пациентов с миелодиспластическим синдромом проявляется рефрактерная анемия. Чаще всего гемоглобинопатия такого рода развивается у пациентов от 50 лет.
Заболевание можно считать промежуточным этапом между рефрактерной анемией и острым лейкозом. Как правило, болезнь проявляется снижением уровня гемоглобина и общей слабостью. Если у больного не нашли других причин для таких изменений картины крови, то основной задачей врачей становится дообследовать пациента и максимально затормозить наступление острого лейкоза.
Что за болезнь талассемия? Это наследуемое по рецессивному типу заболевание, развивающееся из-за снижения синтеза полипептидных цепей в структуре гемоглобина. В зависимости от того, какой мономер перестал нормально синтезироваться различают альфа-, бета-талассемию и дельта-талассемию. Также болезнь классифицируют по степени клинических проявлений, разделяют на тяжелую, легкую и среднюю.
Альфа-талассемия ассоциирована мутациями в генах HBA2 и HBA1. Альфа-цепь кодируется четырьмя локусами и, в зависимости от количества аномальных – различают разные степени тяжести заболевания. Симптомы и течение гемоглобинопатии варьируют от легкой до тяжелой степени гипохромной микроцитарной анемии.
Бета-талассемия существует в двух наиболее распространенных вариантах: малая (minor) и CD8(-AA) – большая (наиболее тяжелая форма заболевания). Анемия развивается из-за мутаций обоих аллелей бета-глобина, когда гемоглобин А начинает вытесняться гемоглобином F. Обычно малая талассемия имеет легкое течение и лечение не требуется.
Согласно Википедии, анемия Даймонда-Блекфена представляет собой наследственную форму красноклеточной аплазии с точно не выявленным типом наследования. Предполагают, что заболевание имеет аутосомно-доминантный тип наследования, который встречается у одной четвертой всех больных. У таких больных обычно проявляются проявления анемии в течение первого года жизни, слабость, бледность, повышенная утомляемость, снижение количества эритроцитов в плазме крови.
Диагноз ставят по общему анализу крови, показателям уровня эритропоэтинов, микроскопии и биопсии костного мозга. Лечению болезнь поддается плохо, назначают ГКС, гемотрансфузии.
Повышение концентрации свободного гемоглобина в плазме крови называют гемоглобинемией. Заболевание возникает вследствие приобретенных и врожденных заболеваний эритроцитов, при повышенном их разрушении. Симптом может проявиться после неправильно проведенного переливания крови, из-за воздействия паразитарных и инфекционных факторов (сепсиса, вирусной инфекции, малярии), после сильного переохлаждения, отравления ядами, бензином, уксусной кислотой, грибами. Проявляется внешне это гиперемией кожных покровов и слизистой, повышением концентрации гемоглобина и билирубина в крови.
Существуют настолько разные причины заболевания, что выявить некоторые из них можно только после проведения лабораторных исследований. Часто бывает, что показатели гемоглобина в норме, а железо низкое. Недуг может наблюдаться при недостатке витаминов группы В, фолиевой к-ты. Малокровие у человека возникает вследствие различных травм и обильных внутренних или внешних кровотечений.
Такой диагнозе женщине могут поставить, если уровень гемоглобина в крови падает ниже 120 г на литр. В целом у женщин, из-за некоторых физиологических особенностей выше склонность к данному недугу. Ежемесячные кровопотери во время менструации, когда в течение недели женщина может потерять до 100 мл крови, беременность, лактация и снижение концентрации ферритина – самые распространенные причины анемии. Часто заболевание развивается из-за психосоматики, когда у женщины депрессивное состояние, она плохо питается, редко выходят на свежий воздух, не занимается спортом или во время климакса, когда происходят глобальные изменения в физиологии женщины.
У мужской половины данный диагноз ставится, если уровень гемоглобина снизился менее 130 г на л. По статистике заболевание возникает реже. Чаще всего из-за каких-то хронических заболеваний, нарушений работы органов и их систем (язвенная болезнь, геморрой, эрозии в кишечнике, доброкачественные и злокачественные новообразования, паразиты, апластическая анемия). Существуют и генетические причины (анемия Фанкони) заболевания, которые не связаны с полом.
Малокровие проявляется по-разному, в зависимости от конкретного вида заболевания. Известно, что при малокровии у человека уменьшается количество эритроцитов, изменяется их строение, содержание железа в крови, падает гемоглобин. Ткани человека испытывают недостаток кислорода и это оказывает влияние на общее состояние и внешний вид человека.
Общие признаки анемии, следующие:
- значительно сниженная работоспособность, общая слабость;
- раздражительность, повышенная утомляемость, сильная сонливость;
- шум в ушах и головные боли, «мушки» перед глазами, головокружения;
- дизурия;
- непреодолимое желание полакомится мелом или известью;
- постоянная одышка;
- тонкие и ломкие волосы, ногти, сухая, неэластичная кожа;
- стенокардия, низкое артериальное давление;
- шум в ушах и частые обмороки;
- изменение цвета стула, желтуха, бледность;
- ломота в теле и суставах, мышечная слабость.
Также существуют специфические симптомы малокровия, характерные для той или ной разновидности:
- Железодефицитная анемия. Для данного диагноза характерная парорексия, у пациента появляется сильное желание жевать мел, землю, бумаги и прочие несъедобные материалы. Можно также выделить койлонихию, трещинки в уголках рта, заеды, воспаленный язык. Иногда может повыситься температура до субфебрильной.
- Основным симптомом В12-дефицитной анемии можно назвать покалывание в конечностях, нестойкость походки, скованность и стесненность в движениях, низкое чувство осязания. У пациента снижаются когнитивные способности, могут возникать галлюцинации. В крайне тяжелых случаях может развиться паранойя или шизофрения.
- Характерным симптомом серповидноклеточной анемии может быть слабость, приступообразные боли в брюшной полости и суставах.
- При отравлении свинцовыми отходами у пострадавшего наблюдаются характерные темно-синие линии на деснах, тошнота и болезненные ощущения в области живота.
- Хроническое разрушение эритроцитов может быть симптомом злокачественной опухоли. В таком состоянии развивается проступающая желтуха, язвы и ссадины на ногах, покраснение мочи. Часто образуются камни в желчном пузыре.
Поставить точный диагноз гемолитическая, мегалобластная или апластическая анемия можно после проведения дифференциальной диагностики. Диф. диагностика проводится по соответствующим таблицам и результатам лабораторных исследований.
источник