Гемолитическая анемия – это болезнь, которая характеризуется разрушением эритроцитов. При ней сокращается срок жизни эритроцитов. В норме они существуют около 120 дней.
Ежедневно около 1% красных клеток удаляется из крови. Количество погибших эритроцитов повышается на фоне гемолиза (разрушения). Из-за этого формируется гипоксия тканей головного мозга и внутренних органов.
Физиологически взамен погибших клеток из красного костного мозга в кровь выделяются молодые эритроциты и депо. Так происходит «омоложение» крови. При гемолитических состояниях (аутоиммунная, B12-дефицитная) – этот процесс нарушается.
Интенсивное разрушение красных клеток крови не уравновешивается образованием молодых форм. Расшифровка анализа крови в такой ситуации показывает ретикулоцитоз (повышенное количество несозревших эритроцитов).
Наличие ретикулоцитоза в лабораторных анализах подтверждает диагноз гемолитической анемии. Даже на фоне нормальной концентрации гемоглобина крови появление ретикулоцитов свидетельствует о наличии гемолиза.
Чтобы ответить на вопрос, опишем патогенез заболевания.
Первым признаком недуга является апластический (арегенераторный) криз. При нем формируется недостаточность костного мозга. На фоне патологии возникает раздражение эритроидного красного ростка. Арегенераторная гемолитическая анемия (апластическая) сопровождается снижением количества ретикулоцитов, поэтому расшифровка анализа крови не показывает специфических изменений.
Если пропустить начальную стадию заболевания, возникает тяжелая анемия гемолитического типа. Пациенты знают, выраженный гемолиз – это такое состояние, при котором возникает сильная слабость, не позволяющая выполнять обычную физическую нагрузку. При кризах человек может потерять сознание.
Аутоиммунная гемолитическая анемия – это разрушение эритроцитов, возникающее из-за поражения эритроидного ряда антителами иммунной системы. Причина этого заболевания неизвестна. Клинические эксперименты показали значительное влияние на возникновение патологии наследственных факторов.
Гемолиз – это такое состояние, которое сочетается с компенсаторной гиперплазией эритроидного ростка. На его фоне формируется уменьшение количества ретикулоцитов крови. При длительном течении болезни возникает тяжелая и угрожающая форма патологии. Сокращение сроков жизни красных клеток крови на этом фоне приводит к опасным состояниям и серьезным осложнениям.
Гемолиз – это состояние, при котором не только нарушен процесс образования эритроцитов в костном мозге, но и возникает нарушение работы внутренних органов.
При выраженной гемолитической анемии нарушается работоспособность печени, селезенки и почек. Они «забиваются» разрушенными частями красных клеток крови. При гемолитической анемии на фоне гемолиза образуются особые патологические виды гемоглобина:
Гаптоглобин образуется в печени и относится к классу альфа-глобулинов. Он имеет большую молекулу, которая не проникает через почечный фильтр. Последняя анатомическая структура «забивается», поэтому нарушается работоспособность почек. Функциональная способность мочевыделительной системы на этом фоне снижается. В результате поражаются почечные канальцы, что приводит к снижению экскреторной функции.
Комплекс гемоглобин-гаптоглобин накапливается в крови. При длительном существовании процесса резервы печени по синтезу гаптоглобина снижаются. Следствием состояние является накопление в крови токсических продуктов распада эритроцитов.
Продуктом катаболизма гема эритроцитов является билирубин. Он возникает на фоне разрушения этого белка в печени. За данный процесс отвечает фермент гемоксигеназа. Она содержится в селезенке, костном мозге, печени. Фермент приводит к разрушению альфа-метиленового мостика. Химическим веществом, формирующимся при данном процессе, является вердогемоглобин. Это продукт промежуточной стадии метаболизма билирубина (желтого пигмента). При его повышенном накоплении формируется не только токсическое поражение головного мозга, но и увеличивается риск образования камней желчного пузыря.
Следующим этапом процесса является образование биливердина с отщеплением железа. Фермент цитоплазматическая биливердин редуктаза приводит к превращению билирубина в биливердин. Определение этих веществ используется с целью изучения состояния гемолиза и выявления степени поражения печени.
Наблюдается накопление в сыворотке крови каждого из вышеописанных веществ. Билирубин и продукты его переработки в печени являются токсичными. Они приводят к гибели клеток головного мозга.
Токсические продукты в крови частично связываются белком гаптоглобин, что снижает их негативное влияние на организм. Резервные возможности печени по нейтрализации токсинов ограничены. При выраженной степени заболевания их будет недостаточно для предотвращения поражения головного мозга.
При гемолитических состояниях средней и большой степени выраженности белка гаптоглобина образуется мало, так как истощены резервы для его образования в печени. Интенсивный гемолиз приводит к разрушению красных кровяных клеток. Они выделяются с почками, поэтому у человека появляется моча цвета пива.
источник
Гемолитическая анемия – комплекс заболеваний, которые объединены в одну группу из-за того, что при всех из них снижается продолжительность жизни эритроцитов. Это способствует потере гемоглобина и приводит к гемолизу. Эти патологии схожи друг с другом, но их происхождение, течение и даже клинические проявления разнятся. Гемолитическая анемия у детей также имеет свои особенности.
Гемолиз представляет собой массовую гибель форменных элементов крови. По своей сути это патологический процесс, который может происходить в двух пространствах организма.
- Экстраваскулярно, то есть вне сосудов. Чаще всего очагами являются паренхиматозные органы – печень, почки, селезенка, а также красный костный мозг. Такой вид гемолиза протекает схоже с физиологическим;
- Интраваскулярно, когда кровяные клетки разрушаются в просвете кровеносных сосудов.
Массовая деструкция эритроцитов протекает с типичным симптомокомплексом, при этом проявления интраваскулярного и экстраваскулярного гемолиза различны. Они определяются при общем осмотре больного, помогут установить диагноз общий анализ крови и другие специфические тесты.
Нефизиологическая гибель красных клеток крови возникает по разным причинам, среди которых одно из самых главных мест занимает дефицит железа в организме. Однако это состояние следует разграничивать с нарушениями синтеза эритроцитов и гемоглобина, в чем помогают лабораторные анализы, клинические симптомы.
- Желтушность кожных покровов, которая отображается повышением общего билирубина и его свободной фракции.
- Несколько отдаленным проявлением становится повышенная вязкость и густота желчи с повышенной склонностью к камнеобразованию. Она также меняет свою окраску, поскольку содержание желчных пигментов увеличивается. Этот процесс обусловлен тем, что клетки печени стараются обезвредить избыток билирубина.
- Кал также меняет свою окраску, поскольку желчные пигменты «добираются» и до него, провоцируя рост показателей стеркобилина, уробилиногена.
- При экстраваскулярной гибели клеток крови повышается уровень уробилина, что отображается потемнением мочи.
- Общий анализ крови реагирует снижением эритроцитов, падением гемоглобина. Компенсаторно растут молодые формы клеток – ретикулоциты.
Разрушение эритроцитов происходит или в просвете кровеносных сосудов, или в паренхиматозных органах. Поскольку экстраваскулярный гемолиз по своему патофизиологическому механизму схож с нормальной гибелью эритроцитов в паренхиматозных органах, различие заключается лишь в его скорости, и он частично описан выше.
При разрушении эритроцитов внутри просвета сосудов развиваются:
- повышение свободного гемоглобина, кровь приобретает так называемый лаковый оттенок;
- изменение цвета мочи за счет свободного гемоглобина или гемосидерина;
- гемосидероз – состояние, когда железосодержащий пигмент откладывается в паренхиматозных органах.
По своей сути гемолитическая анемия представляет собой патологию, при котором продолжительность жизни эритроцитов значительно снижается. Это обуславливается большим количеством факторов, при этом они бывают внешними или внутренними. Гемоглобин во время деструкции форменных элементов частично разрушается, а частично приобретает свободную форму. Снижение гемоглобина менее 110 г/л указывает на развитие анемии. Крайне редко гемолитическая анемия имеет связь со снижением количества железа.
Внутренними факторами, способствующими развитию заболевания, служат аномалии строения кровяных клеток, а внешними – иммунные конфликты, инфекционные агенты, механические повреждения.
Заболевание может быть врожденным или приобретенным, при этом развитие гемолитической анемии после рождения ребенка называется приобретенным.
Врожденная разделяется на мембранопатии, ферментопатии и гемоглобинопатии, а приобретенная на иммунные, приобретенные мембранопатии, механические повреждения форменных элементов, по причине инфекционных процессов.
На сегодняшний день врачи не разделяют форму гемолитической анемии по месту деструкции эритроцитов. Наиболее часто фиксируется аутоиммунная. Также, большая часть всех фиксированных патологий этой группы приходится на долю приобретенных гемолитических анемий, при этом они характерны для всех возрастов, начиная с первых месяцев жизни. У детей следует проявить особую преднастороженность, поскольку эти процессы могут быть наследственными. Их развитие обусловлено несколькими механизмами.
- Появлением антиэритроцитарных антител, которые попадают извне. При гемолитической болезни новорожденных речь идет об изоиммунных процессах.
- Соматическими мутациями, что служит одним из триггеров хронической гемолитической анемии. Это не может стать генетическим наследственным фактором.
- Механическое повреждение эритроцитов возникает как результат воздействия тяжелых физических нагрузок или протезирования клапанов сердца.
- Гиповитаминоз, особую роль играет витамин Е.
- Малярийный плазмодий.
- Воздействие отравляющих веществ.
При аутоиммунных анемиях организм отвечает повышенной восприимчивостью к любым чужеродным белкам, а также имеет повышенную склонность к аллергическим реакциям. Это обусловлено увеличением активности собственной иммунной системы. В крови могут изменяться следующие показатели: специфические иммуноглобулины, количество базофилов и эозинофилов.
Аутоиммунные анемии характеризуются выработкой антител к нормальным кровяным клеткам, что приводит к нарушению распознавания своих клеток. Подвидом такой патологии является трансиммунная анемия, при которой мишенью иммунной системы плода становится материнский организм.
Для обнаружения процесса применяются тесты Кумбса. Они позволяют выявить циркулирующие иммунные комплексы, которые нет при полном здоровье. Лечением занимается аллерголог либо иммунолог.
Заболевание развивается по ряду причин, также они могут быть врожденными или приобретенными. Примерно 50% случаев заболевания остаются без выясненной причины, такая форма называется идиопатической. Среди причин гемолитической анемии важно выделить те, которые провоцируют процесс чаще других, а именно:
- переливание несовместимой крови при гемотрансфузиях, в том числе по резус-фактору;
- воздействие отравляющих веществ, токсические эффекты лекарственных препаратов;
- аномалии развития малышей, пороки сердца;
- лейкозы;
- изменения, провоцируемые жизнедеятельностью паразитов.
Под воздействием вышеперечисленных триггеров и наличии других пусковых механизмов форменные клетки разрушаются, способствуя появлению типичной для анемии симптоматики.
Клинические проявления гемолитической анемии достаточно обширные, но их характер всегда зависит от причины, вызвавшей заболевание, тот или иной его тип. Иногда патология проявляется лишь тогда, когда развивается криз или обострение, а ремиссия протекает бессимптомно, человек не предъявляет никаких жалоб.
Все симптомы процесса можно обнаружить только при декомпенсации состояния, когда имеет место выраженный дисбаланс между здоровыми, формирующимися и разрушенными форменными элементами крови, а костный мозг не справляется с возложенной на него нагрузка.
Классические клинические проявления представлены тремя симптомокомплексами:
- анемическим;
- желтушным;
- увеличение печени и селезенки – гепатоспленомегалия.
Обычно они развиваются при внесосудистой деструкции форменных элементов.
Серповидно-клеточная, аутоиммунная и другие гемолитические анемии проявляются такими характерными признаками.
- Повышенная температура тела, головокружение. Встречается при стремительном развитии заболевания в детском возрасте, а сама температура достигает 38С.
- Синдром желтухи. Появление этого признака обусловлено деструкцией эритроцитов, что приводит к повышению уровня непрямого билирубина, который перерабатывается печенью. Его высокая концентрация способствует росту стеркобилина и уробилина кишечника, за счет чего окрашивается кал, кожа, слизистые оболочки.
- По мере развития желтухи спленомегалия также развивается. Этот синдром достаточно часто протекает с гепатомегалией, то есть одновременно увеличиваются и печень, и селезенка.
- Анемия. Сопровождается снижением количества гемоглобина в крови.
Другими признаками гемолитической анемии бывают:
- болевые ощущения в эпигастрии, животе, поясничной области, почках, костях;
- инфарктоподобные боли;
- пороки развития детей, сопровождающиеся признаками нарушения внутриутробного формирования плода;
- изменение характера стула.
Диагностика гемолитической анемии проводится врачом-гематологом. Он устанавливает диагноз на основании данных, полученных при обследовании больного. Сначала происходит сбор анамнестических данных, уточняется наличие триггерных факторов. Врач оценивает степень бледности кожных покровов и видимых слизистых оболочек, проводит пальпаторное исследование органов живота, при котором можно определить увеличение печени, селезенки.
Следующим этапом служит лабораторное и инструментальное обследование. Проводится общий анализ мочи, крови, биохимическое обследование, при котором можно установить наличие в крови высокого уровня непрямого билирубина. Также выполняется УЗИ органов брюшной полости.
В особо тяжелых случаях назначается биопсия костного мозга, при которой можно определить, как развиваются эритроциты при гемолитической анемии. Важно провести правильную дифференциальную диагностику, чтобы исключить такие патологии, как вирусные гепатиты, гемобластозы, онкологические процессы, цирроз печени, механическую желтуху.
Каждая отдельно взятая форма заболевания требует своего подходу к лечению по причине особенностей возникновения. Важно сразу же устранить все гемолизирующие факторы, если речь идет о приобретенном процессе. Если лечение гемолитических анемий происходит во время криза, то больной должен получать большой объем гемотрансфузий – плазма крови, эритроцитарная масса, также проводят метаболическую и витаминотерапии, при этом особую роль играет компенсация дефицита витамина е.
Иногда возникает потребность назначения гормонов и антибиотиков. В случае установки диагноза микросфероцитоза единственным вариантом лечения является спленэктомия.
Аутоиммунные процессы подразумевают применение стероидных гормонов. Препаратом выбора считается преднизолон. Такая терапия снижает гемолиз, а иногда прекращает его полностью. Особо тяжелые случаи требуют назначение иммунодепрессантов. Если заболевание полностью резистентно к медикаментозным лекарственным средствам, врачи прибегают к удалению селезенки.
При токсической форме заболевания возникает необходимость в проведении дезинтоксикационной интенсивной терапии – гемодиализ, лечение антидотами, форсированный диурез при сохраненной работоспособности почек.
Как уже было сказано ранее, гемолитические анемии – группа патологических процессов, которая по своему механизму развития может значительно отличаться, но у всех заболеваний есть одна общая черта – гемолиз. Он происходит не только в кровяном русле, но и в паренхиматозных органах.
Первые признаки развития процесса зачастую не вызывают никаких подозрений у заболевших лиц. Если у ребенка малокровие развивается стремительно, то появляются раздражительность, быстрая утомляемость, плаксивость, а также бледность кожи. Эти признаки могут быть легко приняты за особенности характера малыша. Особенно если речь идет о часто болеющих детях. И это неудивительно, поскольку при наличии этой патологии люди подвержены развитию инфекционных процессов.
Основные симптомы анемии у детей – бледность кожи, которую необходимо дифференцировать с почечными патологиями, туберкулезом, интоксикацией различного генеза.
Главным признаком, который позволит определить наличие именно анемии без определения лабораторных показателей – при малокровии слизистые оболочки также приобретают бледный оттенок.
Основными осложнениями гемолитических анемий являются:
- самое страшное – анемическая кома и летальный исход;
- снижение показателей артериального давления, сопровождающееся учащенным пульсом;
- олигоурия;
- образование камней в желчном пузыре и желчевыводящих протоках.
Следует отметить, что некоторые пациенты отмечают обострение заболевания в холодное время года. Таким пациентам врачи рекомендуют не переохлаждаться.
Профилактические мероприятия бывают первичными и вторичными:
- первичные способствуют предотвращению развития заболевания;
- вторичные превентивные меры борются с обострениями патологии.
Если развивается анемия врожденная, то сразу нужно приступать ко вторичным мероприятиям. Единственный верный способ предупреждения заболевания – соблюдение принципов здорового образа жизни, отдавать предпочтение натуральным продуктам питания, своевременная терапия любых патологических процессов.
источник
Под термином «гемолитическая анемия» подразумевается группа наследственных или приобретенных заболеваний, которым свойственно повышенное внутрисосудистое или внутриклеточное разрушение эритроцитов. Гемолитическая анемия может быть иммунной, идиопатической и аутоиммунной. Но чаще всего встречаются именно аутоиммунные гемолитические анемии (АГА) – 1 случай на 75 тысяч населения.
Все аутоиммунные гемолитические анемии включают заболевания, характеризующиеся образованием антител к собственным антигенам эритроцитов.
Как и любое аутоиммунное заболевание, аутоиммунная анемия является результатом сбоя работы иммунной системы. Причиной такого сбоя может послужить мутация генов и повреждение цепочки ДНК под влиянием различных вредоносных факторов.
Как известно, ДНК – это молекула, которая обеспечивает хранение и передачу информации, а потому анемия может передаваться по наследству. Именно поэтому профилактика и успешное лечение аутоиммунной гемолитической анемии, прежде всего, заключаются в оптимизации работы иммунной системы.
В зависимости от причины развития аутоиммунная гемолитическая анемия может быть симптоматической и идиопатической. В первом случае она развивается как осложнение какого-либо иного заболевания. Во втором случае явной причины развития заболевания нет.
В зависимости от антител, атакующих эритроциты, данная болезнь классифицирует на 4 подвида. Итак, бывает аутоиммунная гемолитическая анемия:
- С неполными тепловыми агглютининами: когда эритроциты атакуют иммуноглобулины A и G – молекулы белкового происхождения. Заболевание, как правило, развивается быстро и остро. Основные симптомы: повышение температуры, общая слабость, одышка, боль в пояснице. Разрушение крови происходит в основном в селезенке;
- С тепловыми гемолизинами: разрушение эритроцитов происходит под действием гемолизинов (клеток, повреждающих клетки крови) в кровеносных сосудах. На фоне этого вида болезни повышается свертываемость крови, в результате чего у пациента образуются микротромбы, часто развивается острая почечная недостаточность;
- С полными холодовыми антителами: плохая переносимость холода – главный признак этой формы заболевания. Также больные жалуются на быструю утомляемость, слабость, одышку. Летом болезнь может вообще не давать о себе знать, но обостряется в холодное время года. Наиболее часто страдают люди преклонного возраста;
- С двухфазными антителами-гемолизинами – очень редкий вид анемии, для которого характерно закрепление двухфазного гемолизина на поверхности эритроцита. Данный процесс возможен только при холоде, поэтому гемолизу всегда предшествует переохлаждение.
Хроническая форма аутоиммунной гемолитической анемии обычно протекает практически бессимптомно, периодически обостряясь. На фоне ремиссии при пальпации определяется увеличение селезенки и печени, иногда возникает желтуха.
Развернутый анализ крови у больных АГА показывает увеличение СОЭ, нормальный уровень тромбоцитов, повышенный или нормальный гемоглобин. При обострении хронической анемии или при болезни в острой форме количество лейкоцитов увеличивается (в стадии ремиссии этот показатель находится в норме).
Диагностировать аутоиммунную гемолитическую анемию довольно сложно, для этого проводят ряд специфических диагностических исследований.
Лечение аутоиммунной гемолитической анемии проводят глюкокортикостероидными препаратами, чаще всего это преднизолон. Его назначают в суточной дозе 40-60 мг в течение трех недель. Если этот курс не приводит к ремиссии, дозировку медикамента увеличивают в два раза. К признакам ремиссии относят увеличение содержания в крови ретикулоцитов, после чего либо повышается и уровень гематокрита, либо хотя бы намечается тенденция к положительной динамике. Резистентность к такой схеме лечения считается плохим прогностическим признаком.
Поскольку прямой антиглобулиновый тест длительный период может оставаться положительным, даже несмотря на явные признаки улучшения состояния, больным рекомендуется проводить непрямой антиглобулиновый тест– он чутко реагирует на эффективность терапии.
В стадии ремиссии заболевания, а так же с целью предупреждения рецидивов суточную дозу кортикостероидов постепенно снижают на 2,5-5 мг в сутки и до полной отмены.
При отсутствии желаемого эффекта от терапии препаратами этой группы, а также при повышенной устойчивости к гормональным средствам пациентам, течение болезни у которых практически не поддается медикаментозной коррекции и сопровождается частыми рецидивами, рекомендуют спленэктомию – хирургическую операцию по удалению селезёнки. Такая радикальная мера позволяет значительно улучшить качество их жизни.
В случаях отсутствия результата от применения кортикостероидов больным также могут назначить иммуносупрессирующие медикаменты, к примеру, 6-меркантопурин (из расчета 2 мг на 1 кг веса в сутки) или азатиоприн (1,5-3,0 мг на кг/сутки).
При тяжелых гемолитических кризах, угрожающих жизни человека, показана инфузионная терапия: гемодез, индивидуально подобранная эритроцитарная масса. В некоторых случаях переливают плазму крови, замороженные или отмытые эритроциты. Иногда при аутоиммунной гемолитической анемии прибегают к методу плазмафереза и гемодиализу.
Стоит отметить, что кортикостероидные препараты проявляют малую терапевтическую эффективность при лечении гемолитических анемий, вызванных холодовыми антителами. По этой причине основу профилактики этой формы заболевания составляет предупреждение переохлаждения организма. При тяжелом течении болезни назначают иммуносупрессирующие лекарства (хлорбутин, циклофосфан и др.).
Лечение аутоиммунной гемолитической анемии в хронической стадии проводят преднизолоном в суточной дозировке 20-25 мг. По мере улучшения показателей крови дозу постепенно снижают до поддерживающей, которая составляет 5-10 мг/сутки.
Несмотря на довольно высокий уровень развития современной медицины, лечение всех видов гемолитических анемий – сложный процесс, а диагноз, к сожалению, часто неблагоприятный.
источник

Различают аутоиммунные анемии, проявляющиеся образованием холодовых и тепловых антител. Анемии с тепловыми антителами встречаются чаще и протекают преимущественно хронически, однако встречаются и острые формы.
Диагностика данной анемии не вызывает затруднений, поскольку в 90% случаев диагноз может быть установлен на основании стандартных анализов крови. Тем не менее, для установления степени выраженности аутоиммунного процесса может понадобиться стернальная пункция или трепанобиопсия.
Лечение заболевания достаточно сложно, поскольку часто приходится прибегать к операции по удалению селезенки и приему иммунодепрессантов. По статистике улучшение состояния наступает в 85 – 90% случаев, а полное излечение — менее, чем в 50%. Таким образом, более половины пациентов вынуждены постоянно следить за своим состоянием и при необходимости проходить очередной курс поддерживающего лечения. Учитывая то, что лечение кортикостероидами и иммунодепрессантами тяжело переносится организмом и вызывает ряд серьезных побочных эффектов, об аутоиммунной анемии складывается мнение как о тяжелом органическом заболевании.
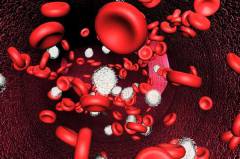
Различают следующие функции эритроцитов:
- газообмен;
- поддержание кислотно-щелочного равновесия;
- осуществление гемостаза;
- определение реологических свойств крови;
- участие в иммунных процессах.
Эритроциты являются единственными клетками организма, способными осуществлять транспорт газов. Осуществление данной функции связано с молекулами гемоглобина, заполняющими 98% внутренней среды клетки. Гемоглобин состоит из органической части – белка глобина и неорганической части – гемма. Данный комплекс способен в различных условиях среды связывать и высвобождать газы. В легочных альвеолах эритроциты выделяют углекислый газ и наполняются кислородом, а в периферических тканях, наоборот – выделяют кислород и наполняются углекислым газом. В среднем эритроцит совершает один оборот вокруг сердечно-сосудистой системы за 25 – 27 секунд. Таким образом, за одну минуту эритроцит совершит 2 цикла, за час – 120 циклов, за сутки — 2880 циклов.
Различают следующие фракции гемоглобина:
- гемоглобин А (НbA) – 95 – 98%;
- гемоглобин А2 (HbA2) – 2 – 3%
- гемоглобин F (HbF) – до 70 – 90% у новорожденных детей.
Наиболее распространенной фракцией гемоглобина является гемоглобин А, который в норме превалирует у взрослого населения. Значительно меньшую долю занимает гемоглобин А2, который обладает некоторыми структурными отличиями и появляется в эритроцитах периферической крови при попадании организма в определенные неблагоприятные для него условия. Гемоглобин F является исключительно детской фракцией, полностью отсутствующей у взрослых. Наиболее высокая его концентрация наблюдается в возрасте до 10 дней, после чего происходит постепенное снижение концентрации гемоглобина F вплоть до полного исчезновения в 1 год.
На клеточной мембране эритроцита находятся многочисленные рецепторы для присоединения лейкоцитов и белков системы комплемента, являющихся элементами пассивного и активного иммунитета.
Строение эритроцита во многом связано с его функциями. Как указывалось выше, эритроцит не содержит ядра, поскольку теряет его в процессе дифференциации. Такой путь развития имеет несколько преимуществ. В первую очередь, ядро занимает в среднем от 15 до 85% объема клетки. Соответственно при его устранении данное пространство может быть использовано более рационально. Во-вторых, отсутствие ядра приводит к исчезновению мишени для клеточных мутаций. В-третьих, отсутствие ядра приводит к увеличению деформируемости эритроцита, свойства, которое напрямую влияет на выполнение эритроцитом его функции, а также длительность его существования.
Занимательно, что эритроцит относится к немногим видам клеток, которые абсолютно не потребляют кислород. Необходимый АТФ (аденозинтрифосфат) клетки получают путем анаэробного (не требующего присутствия кислорода) расщепления молекул глюкозы. Таким образом, выходит, что эритроцит абсолютно не чувствителен к недостатку кислорода, но крайне чувствителен к дефициту глюкозы в крови. Поэтому длительное голодание может привести к самопроизвольному разрушению красных кровяных телец.
Мембрана эритроцита состоит из двойного слоя липидов, пронизанного различного рода транспортными белками. Данные белки предназначены для однонаправленного перемещения определенных ионов в клетку и за ее пределы. Бесперебойная работа транспортных белков поддерживает постоянный положительный заряд внутри клетки и отрицательный снаружи, что крайне важно для многих реакций, в которые вовлекаются эритроциты.
На внешней поверхности мембраны находятся тысячи гликопротеидных комплексов, выполняющих роль рецепторов для прикрепления различных веществ. Помимо этого рецепторы определяют групповую принадлежность красных кровяных телец. Таким образом, различают 4 основные группы крови по системе AB0 и 2 группы по наличию резус-антигена. Данные группы используются при переливании крови от доноров к реципиентам.
Считается, что переливание цельной крови или определенных ее компонентов допустимо при одинаковых группах крови донора и реципиента. Тем не менее, даже при совместимости крови по группе и резус-фактору могут возникать анафилактические реакции, сопровождающиеся шоковым состоянием и даже гибелью пациента. Этот факт объясняется несовместимостью эритроцитов по остальным типам антигенов, большинство из которых на сегодняшний день не изучены. Учитывая, что на поверхности эритроцитов находятся тысячи различных видов антигенов, а также то, что их количество увеличивается по мере взросления человека, можно с уверенностью сказать, что каждый житель планеты обладает уникальной кровью, не похожей на кровь любого другого живого существа.
Отдельного внимания заслуживают такие свойства эритроцита как цитоплазматическая вязкость и деформируемость. Цитоплазматическая вязкость является относительным показателем, отражающим концентрацию гемоглобина в эритроците. Лабораторно она соответствует цветовому индексу. Увеличение содержания гемоглобина и уменьшение содержания воды приводит к увеличению вязкости и наоборот. Деформируемость является способностью эритроцита изменять форму для прохождения через узкие кровеносные сосуды. Таким образом, данная клетка крови способна протискиваться через капилляры, диаметр которых в несколько раз меньше диаметра эритроцита.
Деформируемость эритроцита напрямую зависит от успешной работы цитоскелета. Цитоскелетом называется система микротрубочек и микрофиламентов, формирующая каркас клетки и, в конечном итоге, ее форму. В ячейках цитоскелета располагаются молекулы гемоглобина. Изменение формы цитоскелета является энергозависимым процессом, требующим достаточного уровня АТФ и глюкозы, поэтому их отсутствие приводит ригидности к застреванию эритроцитов в наиболее узких капиллярах селезенки и их разрушению макрофагами.
Деформируемость и вязкость напрямую связаны. Увеличение вязкости эритроцита сопровождается уменьшением его деформируемости. В процессе старения мембранные транспортные белки и белки цитоскелета эритроцита изнашиваются. Следствием этого является потеря эритроцитом жидкой части, сопровождающаяся увеличением его вязкости и незначительным округлением. Увеличение вязкости приводит к снижению деформируемости и затруднению прохождения данных клеток через сосуды селезенки. При достижении эритроцитом цитоплазматической вязкости равной концентрации гемоглобина 360 – 380 г\л происходит окончательное застревание эритроцита в селезенке и его разрушение клетками макрофагальной системы, расположенными вокруг капилляров.
Различают следующие клинические разновидности аутоиммунной анемии:
- идиопатическая (первичная);
- симптоматическая (вторичная).
В случае, когда выявляется объективная причина аутоиммунного разрушения красных кровяных телец, устанавливается диагноз вторичной аутоиммунной анемии. Когда причина не обнаруживается, но есть явные признаки иммунной агрессии по отношению к эритроцитам, выставляется диагноз первичной или идиопатической аутоиммунной анемии. Иными словами, такой диагноз является диагнозом исключения.
Различают следующие причины вторичных аутоиммунных анемий:
- острые и хронические лимфобластные лейкозы;
- неблагоприятный радиационный фон;
- паранеопластический синдром при иных злокачественных опухолях;
- болезни соединительной ткани (системная красная волчанка, ревматическая лихорадка, системная склеродермия и т. п.);
- некоторые инфекционные заболевания (микоплазмоз, цитомегаловирус);
- негематологические аутоиммунные заболевания (тиреоидит, болезнь Крона, саркоидоз и др.);
- сахарный диабет I типа;
- применение больших доз бета-лактамных антибиотиков (пенициллины и цефалоспорины);
Большое значение имеет температура окружающей среды, поскольку она определяет механизм, по которому будет протекать аллергическая реакция. Различают полные и неполные тепловые и холодовые антигены. Соответственно этому выделяют 4 типа атопических реакций. Различия в их механизмах достаточно сложны, поэтому основные моменты каждого типа будут переданы в соответствующих разделах.
При острых и хронических лейкозах происходит появление в крови лейкоцитов, замерших на определенных этапах развития. Данные лейкоциты не являются зрелыми, поэтому на их поверхности находятся не все антигены первого и второго комплекса гистосовместимости. Иными словами, данные лейкоциты не распознают некоторые клетки организма как свои и атакуют их. Таким образом, может развиться аутоиммунная реакция не только по отношению к эритроцитам, но еще и по отношению к любым другим клеткам организма.
Паранеопластический синдром является одной из частых причин аутоиммунных анемий. Причиной его развития является образование в организме злокачественной опухоли. Антигенный состав опухоли схож с антигенами на поверхности эритроцитов крови и клеток предшественниц эритроцитов в костном мозге. Клетки иммунной системы распознают злокачественную опухоль как инородное тело и атакуют ее. Вместе с тем под перекрестную атаку попадают и эритроциты, которые также разрушаются под действием лейкоцитов, антител и белков системы комплемента.
При таких болезнях соединительной ткани как ревматоидный артрит, склеродермия и системная красная волчанка всегда присутствует определенный аутоиммунный компонент. В крови определяются антитела к определенным клеткам организма и отдельным их частям – ядру, митохондриям, мембране и т. д. Часто мишенями для антител становятся и эритроциты. При этом в определенных случаях они являются первичными мишенями, то есть именно к ним изначально развается иммунная интолерантность. В остальных случаях эритроциты являются вторичными мишенями, поскольку поражаются перекрестно с другими клетками организма. Важно отметить, что при данных заболеваниях имеет место дефект одного или нескольких звеньев иммунной системы, а атакуемые эритроциты являются абсолютно здоровыми.
Некоторые инфекционные заболевания, а также прием антибиотиков, преимущественно бета-лактамного ряда (пенициллин, амоксиклав, аугментин, цефтриаксон и др.), сопровождаются развитием аутоиммунной анемии. Среди инфекционных заболеваний отмечались случаи анемии во время обострений цитомегаловирусной и микоплазменной инфекции. В одних случаях вирус проникает в ядро и встраивается в геном нормальной клетки. В иных случаях антигены вируса выставляются на поверхности эритроцитов. Для клеток иммунной системы данные антигены являются чужеродными, поэтому происходит развитие агрессии по отношению к ним, сопровождающееся разрушением клеток, на которых данные антигены находятся. Третий механизм развития связан с тем, что некоторые лекарственные вещества, химикаты и инфекционные агенты являются гаптенами – неполными аллергенами. Сами по себе они слишком малы для того, чтобы обратить на себя внимание иммунной системы, но при присоединении к рецепторам на поверхности эритроцитов их удельный вес возрастает, а вместе с тем возрастают и антигенные свойства, делая из гаптена полноценную мишень для атаки иммунной системы.
Негематологические аутоиммунные заболевания, такие как тиреоидит, терминальный илеит и первичный билиарный цирроз подразумевают нарушения в работе иммунной системы организма. В случае если воздействие, вызвавшее патологический сдвиг в иммунной системе, не устраняется, то не исключается появление и других аутоиммунных заболеваний вдобавок к уже существующим. При этих заболеваниях мишенями для клеток иммунной системы и антител могут быть как эритроциты, так и любые другие клетки организма.
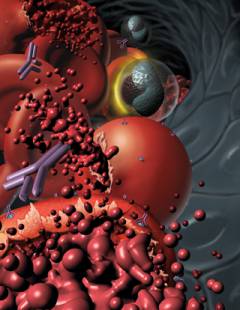
В результате появления на поверхности эритроцита чужеродных антигенов или вследствие нарушения распознавания иммунными клетками своих и чужих тканей происходит нарушение толерантности иммунной системы по отношению к красным кровяным тельцам. В результате образуются многочисленные клоны Т- лимфоцитов и В-лимфоцитов, призванных уничтожать собственные эритроциты. Т-лимфоциты атакуют эритроциты самостоятельно, а В-лимфоциты трансформируются в плазматические клетки, которые вырабатывают антитела. Процесс гемолиза (разрушение эритроцитов) может происходить как в кровеносном русле, так и в капиллярах селезенки. В первом случае гемолиз называется внутриклеточным, а во втором – внутрисосудистым.
Внутриклеточный гемолиз в селезенке развивается при участии макрофагов и Т-лимфоцитов. Эритроциты, проходя по капиллярам селезенки, значительно задерживаются. Снижение скорости их продвижения создает благоприятные условия для поглощения их иммунными клетками, расположенными вокруг капилляров селезенки. Параллельно с этим развивается процесс локального воспаления, сопровождающийся увеличением данного органа в размерах за счет выраженного отека. Отек приводит к сужению капилляров и еще большему замедлению продвижения эритроцитов. Таким образом, замыкается порочный круг, в котором эритроциты неуклонно подвергаются разрушению.
Внутрисосудистый гемолиз происходит при участии антител, Т-лимфоцитов и белков системы комплемента. Местом, в котором происходит уничтожение эритроцитов, является вся кровеносная система. Интенсивность гемолиза зависит от выраженности иммунного ответа, который может варьировать в зависимости от большого количества разнообразных факторов.
Итогом разрушения эритроцитов является высвобождение в кровеносное русло свободного гемоглобина. При скорости гемолиза менее 10% от общего числа эритроцитов в сутки гемоглобин захватывается белком под названием гаптоглобин и оседает в селезенке или на внутреннем слое сосудов. Оседая, он разрушается макрофагами. В процессе разрушения эритроцита макрофаги высвобождают все молекулы гемма, находившиеся в нем. Далее гемм самостоятельно трансформируется в свободный билирубин, проявляющийся появлением желтухи. Свободный билирубин при помощи белка крови альбумина транспортируется в печень, где он превращается в связанный (прямой) билирубин и выделяется в кишечник вместе с желчью.
В дальнейшем под влиянием флоры кишечника происходит восстановление прямого билирубина до стеркобилиногена и уробилиногена, всасывающегося обратно в кишечнике и выделяющегося с мочой. Большая часть стеркобилиногена выделяется с калом, окрашивая его в темно-коричневый цвет, а остаток всасывается обратно в кишечник, поступает в кровоток и повторно выводится с желчью. Совершая данный круг, стеркобилиноген параллельно тонизирует иммунную систему. Этим объясняется тот факт, что при механических (нарушение выделения желчи) и паренхиматозных (нарушение формирования желчи) желтухах, персистирующих более одной — двух недель, наступает снижение уровня иммунной резистентности организма.
При более высоких темпах гемолиза, превышающих 10% от общего числа эритроцитов в сутки, связывающей способности гаптоглобина оказывается недостаточно, и свободный гемоглобин поступает в почки. В почках гемоглобин окисляется до гемосидерина и в таком виде выводится с мочой. При темпах гемолиза, превышающих 18 – 20% общего числа эритроцитов в сутки, окисление гемоглобина в почечных канальцах не успевает происходить, и в моче обнаруживается чистый гемоглобин. Определение в моче цельных неизмененных эритроцитов не характерно для аутоиммунной анемии и говорит скорее об источнике кровотечения в лоханке, мочеточниках, мочевом пузыре, уретре или влагалище у женщин. Также неизмененные эритроциты могут появиться в анализе мочи при неправильном ее заборе в период обильных выделений во время менструации.
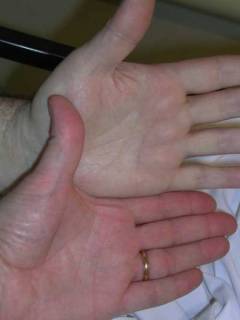
Проявлениями анемического синдрома являются:
- бледность кожных и слизистых покровов;
- головокружение;
- тошнота;
- сердцебиение;
- увеличение частоты сердечных сокращений;
- выраженная общая слабость;
- скорая утомляемость.
Проявлениями гемолитического синдрома являются:
- бледность кожных покровов с желтым оттенком, зависящим от выраженности гемолиза;
- увеличение размеров селезенки с умеренной болезненностью в левом подреберьи;
- окрашивание мочи в темно-коричневый, темно-вишневый или алый цвет;
- компенсаторное развитие ДВС синдрома (множественный полиорганный тромбоз, сопровождающийся длительно неостанавливающимися кровотечениями).
По степени прогрессии клинических признаков различают следующие виды течения аутоиммунной анемии:
- острое;
- подострое;
- хроническое.
Острое течение характерно для детского возраста, а также при наслоении сопутствующей вирусной инфекции.
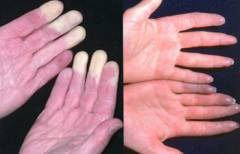
Подострым течением обладает чаще аутоиммунная анемия, развивающаяся посредством холодовых антител. Примечательным фактом данных анемий является усиление гемолиза при снижении температуры тканей организма, поэтому более выраженный гемолиз наблюдается на периферии. Такие анемии часто сопровождаются гипервискозным синдромом, проявлениями которого являются посинение и побледнение пальцев рук и ног при низких температурах (синдром Рейно), тромбофлебиты, длительно незаживающие трофические язвы и даже гангрена. Исчезновение симптоматики происходит при повышении температуры кожных покровов до физиологических значений.
Хроническое течение характерно для аутоиммунных анемий с вовлечением тепловых антител. Часто обострения сопровождаются повышением температуры тела, вызванной вирусными и бактериальными инфекциями. Тем не менее, по причине того, что в некоторых органах человека температура тела физиологически выше средних значений (печень, селезенка), гемолиз в них протекает постоянно, однако в умеренных масштабах.
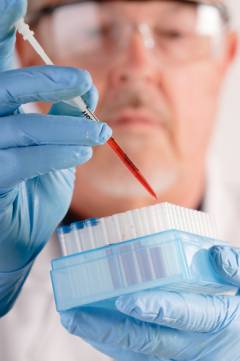
Наиболее важными лабораторными исследованиями являются:
- общий анализ крови (с тромбоцитами и ретикулоцитами (молодые формы эритроцитов));
- общий анализ мочи;
- биохимический анализ крови;
- прямая реакция Кумбса;
- иммуноферментный анализ (ELISA);
- стернальная пункция (пункция грудины);
- трепанобиопсия.
Забор крови для данного анализа осуществляется из любой периферической вены. Медицинский персонал, осуществляющий забор, должен использовать индивидуальные средства защиты, такие как резиновые перчатки, очки или прозрачные лицевые щитки. При помощи жгута перетягивается любая периферическая вена. Место прокола кожи тщательно обрабатывается антисептическими растворами 2 – 3 раза до отсутствия следов грязи и пота на ватном тампоне. Игла одноразового шприца вводится в вену под углом приблизительно в 30 градусов к поверхности кожи. После ощущения провала в полость сосуда игла фиксируется в данном положении, а поршень шприца оттягивается назад. Таким способом набирается кровь в шприц в необходимом количестве, обычно составляющем от 10 до 20 мл. После взятия крови игла извлекается, а место прокола кожи придавливается чистым ватным тампоном, смоченным антисептическим раствором, до остановки кровотечения.
| Показатель | Значение при аутоиммунной анемии | Значение в норме | Интерпретация |
| Гемоглобин | Менее 110г\л | Мужчины: 130 – 160 г\л Женщины: 120 – 150 г\л | Снижение гемоглобина в результате разрушения эритроцитов. |
| Эритроциты | Менее 3,5 х 10 12 \л | Мужчины: 3,9 – 5,2 х 10 12 \л Женщины: 3,7 – 4,9 х 10 12 \л | Снижение количества эритроцитов. |
| Цветовой индекс | 0, 85 – 1,1 | Норма: 0,85 – 1,05 | Нормальное или незначительно увеличенное заполнение эритроцитов гемоглобином. |
| Ретикулоциты | До 80% | Норма: 2 – 10% | Значительное увеличение количества молодых форм эритроцитов свидетельствует о высоких темпах компенсаторного восполнения количества данных клеток. |
| Размер эритроцитов | Анизоцитоз – наличие в кровеносном русле эритроцитов различных размеров | Нормоцитоз – нормальный размер эритроцитов: 7,2 – 7,5 мкм | Микроцитоз – диаметр эритроцита менее 7,2 мкм – по причине развивающегося со временем дефицита железа. Макроцитоз – диаметр эритроцита менее 7,5 мкм – по причине развивающегося дефицита витамина В12 и фолиевой кислоты. |
| Лейкоциты | 0,5 – 20 х 10 9 \л | Норма: 4 – 9 х 10 9 \л | Число лейкоцитов в крови зависит от сопутствующего заболевания, однако чаще определяется незначительное увеличение. |
| Тромбоциты | 100 – 320 х 10 9 \л | Норма: 180 – 320 х 10 9 \л | Нормальное или незначительное уменьшение числа тромбоцитов при сопутствующем вовлечении в аутоиммунный процесс тромбоцитарного ростка. |
| СОЭ (скорость оседания эритроцитов) | 2 – 25 мм\час | Мужчины: 2 – 10 мм\час Женщины: 2 – 15 мм\час | СОЭ зависит от заболевания, вызвавшего аутоиммунную анемию. |
| Цвет плазмы | Желтый | Прозрачный | Желтый цвет плазмы свидетельствует о повышении билирубина в крови. |
Соотношение различных видов лейкоцитов в лейкоцитарной формуле изменяется в соответствии с заболеванием, вызвавшим аутоиммунную анемию. При идиопатической анемии лейкоцитарная формула часто характеризуется увеличением доли лимфоцитов и моноцитов.
Правильный сбор мочи для анализа является своего рода гарантией получения объективного результата. Для сбора мочи необходимо, чтобы больной произвел гигиеническую обработку промежности и половых органов накануне сбора мочи. Первая порция мочи не собирается, поскольку является загрязненной эпителием и флорой мочевыводящих путей. Собирается только средняя порция мочи как наиболее чистая. Терминальная моча также не собирается, так как вытекает вследствие сжатия мочевого пузыря и поэтому также может содержать увеличенное количество эпителия.
| Показатель | Значение при аутоиммунной анемии | Значение в норме | Интерпретация |
| Относительная плотность | 1002 – 1030 | 1002 – 1030 с учетом возрастных колебаний | Относительная плотность мочи неизменна. Фильтрационная функция почек не нарушена. |
| Цвет | Темно-коричневый, темно-красный, алый | Соломенно-желтый | Темно-коричневый цвет свидетельствует о выделении с мочой избытка свободного билирубина. Темно-красный цвет говорит о появлении в моче гемосидерина при более высоких темпах гемолиза. Алая моча говорит о присутствии в ней свободного гемоглобина при крайне выраженном гемолизе. |
| Среда | Кислая или нейтральная | Кислая | Незначительное снижение кислотности мочи может свидетельствовать о повышении скорости почечной фильтрации. |
| Прозрачность | Прозрачная | Прозрачная | Прозрачность мочи визуально свидетельствует об отсутствии в ней большого количества белка, являющегося признаком воспалительного процесса. |
| Эпителий | Плоский: 2 – 3 в поле зрения у женщин и 0 – 1 в поле зрения у мужчин | Плоский: 2 – 3 в поле зрения у женщин и 0 – 1 в поле зрения у мужчин | Нормальное количество эпителия в моче свидетельствует о хорошем состоянии почек и мочевыводящей системы. |
| Лейкоциты | Отсутствуют | Отсутствуют | Отсутствие воспалительного процесса в мочеполовой системе. |
| Эритроциты | 2 – 3 неизмененных эритроцита в поле зрения у женщин и 0 – 1 у мужчин | 2 – 3 неизмененных эритроцита в поле зрения у женщин и 0 – 1 у мужчин | Отсутствие цельных эритроцитов в моче свидетельствует о целостности эпителиального покрова мочеполовой системы. Появление измененных эритроцитов или эритроцитарных цилиндров является признаком острого гломерулонефрита. |
| Гемосидерин | Может присутствовать | Отсутствует | Появление гемосидерина в моче является признаком высокой скорости гемолиза (более 10% от общего количества эритроцитов в сутки). Неблагоприятный прогноз. |
| Гемоглобин | Может присутствовать | Отсутствует | Появление в моче гемоглобина является признаком крайне высокой скорости гемолиза (более 18 – 20% от общего количества эритроцитов в сутки). Крайне неблагоприятный прогноз. |
Забор крови осуществляется аналогичным образом с общим анализом.
| Показатель | Значение при аутоиммунной анемии | Значение в норме | Интерпретация |
| Общий белок | Более 85 г\л | 65 – 85 г\л | Увеличение общего белка свидетельствует о воспалительных признаках в организме. |
| Общий билирубин | Более 20 ммоль\л | Менее 20,5 ммоль\л | Повышение общего билирубина. |
| Прямой билирубин | Менее 20,5 ммоль\л | Менее 20,5 ммоль\л | Прямой билирубин в норме, поскольку функция печени не страдает. |
| Непрямой билирубин | Более 17,5 ммоль\л. Часто увеличение в десятки раз | 0 – 17,5 ммоль\л | Увеличение непрямого билирубина, продукта метаболизма гемма из разрушенных эритроцитов. |
| Сывороточное железо | Увеличение в несколько раз | У женщин 10,7 – 32,2 мкмоль\л и 12,5 – 32,2 мкмоль\л у мужчин | Увеличение концентрации сывороточного железа говорит о высоких темпах разрушения эритроцитов. |
| Свободный гемоглобин | Присутствует | Отсутствует | Крайне высокие темпы гемолиза. |
| С-реактивный белок | Более 20 – 30 мг\л | 0 – 5мг\л | Увеличение С-реактивного белка является общим признаком воспаления в организме. |
Данная процедура осуществляется с целью исследования клеточного состава костного мозга. Проведение стернальной пункции может осуществляться как в условиях операционной, так и в условиях процедурного кабинета. Обезболивание производится по необходимости, чаще ингаляторными препаратами, такими как закись азота или пентрокс. Пациент находится в положении лежа на спине с руками вдоль тела.
Кожа над грудиной обрабатывается антисептическими растворами. При достижении необходимого уровня обезболивания медленными вращательными движениями осуществляется прокол грудины в области 2 – 3 грудино-реберного сочленения. Игла для прокола снабжена специальным ограничителем глубины ввода, который не позволяет ей пробить грудину и проникнуть в грудную полость. Резкое введение иглы также нежелательно, поскольку вносит риск соскальзывания ее с грудины и повреждения органов грудной полости.
После прокола поршень шприца оттягивается и в его полость поступает кровь богатая клетками костного мозга. В случаях, когда кровь не поступает, необходимо повторить прокол на 1 – 2 см ниже. После сбора 1 – 1,5 мл крови шприц извлекается, а образовавшееся отверстие тампонируется ватой и заклеивается лейкопластырем. После данной процедуры больной должен находиться в горизонтальном положении под наблюдением медицинского персонала еще как минимум 20 – 30 минут.
Содержимое шприца резким толчком высвобождается на предметное стекло. Из полученного количества пунктата изготавливают не менее 10 мазков, каждый из которых окрашивается специальным образом, а затем исследуется под микроскопом. Результат анализа выводится в специальный бланк, называемый миелограммой или медулограммой.
Для аутоиммунной анемии характерна гиперплазия красного костномозгового ростка, проявляющаяся увеличением клеток предшественников эритроцита более 25% от нормы. В некоторых случаях наблюдается снижение эритробластов и ретикулоцитов, объясняющееся крайне выраженной аутоиммунной активностью не только по отношению к эритроцитам, а еще и по отношению к его клеткам предшественникам в костном мозге.
Наряду с переливаниями крови необходимо проводить дезинтоксикацию крови для удаления продуктов распада эритроцитов, а также плазмаферез с целью снижения количества циркулирующих в крови антител. Наряду с этим осуществляется восстановление ионного равновесия, уровня глюкозы в крови и других жизненно важных показателей. Назначение прямых и непрямых антикоагулянтов предупреждает риск развития ДВС синдрома (синдрома диссеминированного внутрисосудистого свертывания крови), сопровождающего острую кровопотерю. Стимуляция и поддержание высокого уровня кроветворения осуществляется при помощи внешних вливаний витамина В 12 и фолиевой кислоты, истощающихся через некоторое время с условного момента начала заболевания.
После проведенного лечения вышеуказанными методами оценивается результат. Если заболевание полностью ликвидировалось, то лечение на данной стадии завершают. В случае возвращения симптомов заболевания через некоторое время после прекращения лечения прибегают к удалению селезенки. Если и после удаления селезенки не наступает ремиссии заболевания, то последней ступенью лечения становится иммуносупрессивная терапия.
Медикаментозное лечение является преимущественным при аутоиммунной анемии и осуществляется на всех этапах заболевания в качестве ведущего или вспомогательного.
| Медикамент | Механизм действия | Способ применения |
| Преднизолон | Является представителем глюкокортикоидных гормонов. Их действие заключается в угнетении всех иммунных процессов. Таким образом, происходит снижение уровня агрессии иммунной системы по отношению к собственным красным кровяным тельцам. | 1 мг\кг\сутки внутривенно, капельно. При сильно выраженном гемолизе дозу препарату увеличивают до 150 мг\сутки. После прохождения гемолитического криза дозу снижают до обычных значений и продолжают лечение до нормализации показателей гемоглобина и эритроцитов. Затем дозу постепенно снижают по 5 мг каждые 2 – 3 дня до полной отмены препарата. |
| Гепарин | Является прямым антикоагулянтом короткого действия (4 – 6 часов). Данный препарат назначается с целью предотвращения ДВС синдрома, вероятность которого возрастает при резком уменьшении числа циркулирующих в крови эритроцитов. | 2500 – 5000 МЕ подкожно каждые 6 часов под контролем коагулограммы. |
| Надропарин | Является прямым антикоагулянтом длительного действия (24 – 48 часов). Показания к назначению аналогичны гепарину. | 0,3 мл\сутки подкожно под контролем коагулограммы. |
| Пентоксифиллин | Обладает выраженным антиагрегантным эффектом (предотвращает слипание тромбоцитов), что так же применяется с целью снижения вероятности развития ДВС синдрома. Помимо этого препарат является периферическим вазодилататором, улучшающим кровоснабжение периферических тканей и тканей головного мозга. | 400 – 600 мг\сутки в 2 – 3 приема внутрь в течение минимум 2 недель. Рекомендуемая длительность лечения 1 – 3 месяца. |
| Фолиевая кислота | Является представителем группы витаминов, участвующих во многих процессах организма, в том числе и в формировании эритроцитов. Применяется при заболеваниях, связанных с ее активным использованием организмом. | Начальная доза для взрослого человека – 1 мг\сутки, внутрь. Увеличение дозы осуществляется при недостаточном терапевтическом эффекте. Максимально допустимая суточная доза – 5 мг. |
| Витамин В 12 | Участвует в процессе формирования зрелого эритроцита. При его дефиците размер эритроцита увеличивается, а его пластические свойства уменьшаются, что приводит к снижению длительности его существования. | 100 – 200 мкг\сутки, внутрь или внутримышечно под контролем гемограммы. |
| Ранитидин | Является Н2-антигистаминным препаратом, основной функцией которого является снижение продукции соляной кислоты желудком. Данные меры необходимы для компенсации побочного действия преднизолона на слизистую желудка, проявляющегося снижением образования защитной слизи и карбонатов. | По 150 мг 2 раза в сутки. Внутрь. |
| Хлористый калий | Назначается с целью компенсировать потерю организмом ионов калия, вызванной приемом глюкокортикоидов. | По 1 г 3 раза в сутки под ежедневным контролем ионограммы. |
| Циклоспорин А | Иммунодепрессант, применяющийся при недостаточности эффекта глюкокортикоидов и при спленэктомии. | 3 мг\кг\сутки внутривенно, капельно. При выраженных побочных эффектах осуществляется отмена препарата с переходом к другому иммунодепрессанту. |
| Азатиоприн | Иммунодепрессант. | 100 – 200 мг\сутки в течение 2 – 3 недель. |
| Циклофосфамид | Иммунодепрессант. | 100 – 200 мг\сутки в течение 2 – 3 недель. |
| Винкристин | Иммунодепрессант. | 1 – 2 мг\неделю капельно в течение 3 – 4 недель. |
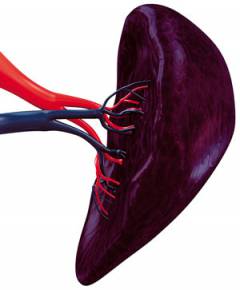
Спленэктомия осуществляется в условиях операционной при общем внутривенном обезболивании. В зависимости от хирургического доступа пациент находится в положении на спине или в положении лежа на правом боку. Классически обрабатывается операционное поле, после чего осуществляется разрез. Разрез может осуществляться по срединной линии при классической лапаротомии или в левом подреберье. Величина разреза зависит от предположительных размеров удаляемой селезенки. После открытия доступа к селезенке производится перевязка и отсечение коротких сосудов желудка. Далее зажимами и тупым концом скальпеля выделяется селезеночная артерия и вена, входящие в ворота селезенки. После выделения данные сосуды прочно перевязываются нерассасывающимся шовным материалом и отсекаются, а селезенка удаляется. После удаления селезенки необходимо произвести ревизию брюшной полости на наличие дополнительных селезенок, и при их обнаружении также их удалить. Такая аномалия развития встречается достаточно редко, однако незнание данного факта хирургом приведет к дальнейшим диагностическим ошибкам, поскольку после удаления селезенки будет ожидаться ремиссия заболевания, а ее происходить не будет по причине разрушения эритроцитов остаточными селезенками. После ревизии из раны удаляются весь инструментарий и салфетки и производится ее ушивание с оставлением дренажной трубки.

Прогноз заболевания во многом зависит от его формы. При первичной идиопатической аутоиммунной анемии полное выздоровление после лечения глюкокортикостероидными препаратами наступает в 5 – 10% случаев. Спленэктомия эффективна в 70 – 80% случаев. Иммуносупрессивная терапия восстанавливает уровень гемоглобина в 90 – 95% случаев, однако тяжело переносится пациентами и приводит к выраженному угнетению иммунитета и многочисленным септическим осложнениям. Прогноз вторичных симптоматических анемий зависит от успешности лечения вызвавшего анемию заболевания.
источник