Низкий гемоглобин обнаруживается у 80% людей. При этом женщины чаще мужчин страдают малокровием. Бежать в аптеку и покупать железосодержащие препараты — не совсем правильная тактика. Хотя в большинстве случаев анемия спровоцирована железодефицитом, при некоторых формах болезни такие лекарственные препараты не окажут лечебного эффекта.
Также стоит понимать, что анемия — это не самостоятельное заболевание, а всего лишь состояние, сопутствующее различным патологическим процессам в организме человека. Только устранив причинную патологию, можно нормализовать состав крови и предотвратить снижение гемоглобина в дальнейшем.
Анемия — это патологическое изменение состава крови, основным признаком которого является снижение показателя гемоглобина (Hb). Нижняя граница гемоглобина для женщин —120 г/л (беременные — 110 г/л). В зависимости от уровня падения Hb диагностируют степени анемии:
- Легкая (I степени) — гемоглобин 110-90, эритроциты более 3;
- Среднетяжелая (II степени) — Hb 90-70, эритроциты не менее 2;
- Тяжелая (III степени) — Hb ниже 70.
Важно! Показатели гемоглобина в пределах 120-110 г/л являются пограничными. В таких случаях через некоторое время проводится повторный анализ крови.
Для диагностики анемии значение имеют и другие показатели крови:
- Цветовой показатель — норма ЦП 0,86-1,1, определяет насыщенность эритроцитов гемоглобином;
- Ретикулоциты — молодые красные клетки в норме 0,2-2%, характеризуют регенеративную способность костного мозга;
- Количество эритроцитов — норма 3,7-4,7 х1012;
- Форма эритроцитов — при некоторых видах малокровия красные клетки серповидно изогнуты или имеют вид мишени;
- Диаметр эритроцитов — в норме 7.2 -8,0 микрон, изменяется при различных типах малокровия;
- Сывороточное железо — у здоровой женщины уровень 9,0-31,3 мкмоль/л;
- Ферритин (белок, участвующий в образовании Hb) — норма 10-120 мкг/л, определяет соотношение железа в печени и плазме крови;
- Железонасыщенность трансферина — характеризует процесс переноса железа из печени к костному мозгу, при анемии менее 16%;
- Сывороточная железосвязывающая способность — выявляет нарушения метаболизма железа (норма ОЖСС — 41-77).
Врачи выделяют три основные причины анемии:
- Потеря эритроцитов и Hb — является следствием острой (при травмах, операциях, обильных менструациях) и хронической кровопотери при язвенном поражении ЖКТ, глистных инвазиях и т. Д.;
- Нарушение созревания эритроцитов и образования гемоглобина — происходит при недостаточности вит. В12, С и В9 (фолиевой кислоты), железодефиците, патологии костного мозга, частичной резекции желудка;
- Стремительное разрушение эритроцитов — при воздействии ядов, уксуса, свинцовом отравлении, приеме сульфаниламидов, лимфолейкозе, циррозе печени и онкопатологии они живут менее 100 дней.
При диагностике малокровия следует отличать схожие состояния, при которых проявляются симптомы анемии у взрослых, но лечение кардинально отличается:
- Псевдоанемия — изменение показателей крови возникает вследствие избыточного поступления жидкости в кровяное русло (гидремия). Такие состояние наблюдается при лечении отеков мочегонными средствами, обильном питье.
- Скрытая анемия — результат обезвоживания организма. При длительной рвоте, поносах, обильном потении кровь сгущается, теряя жидкую часть. Хотя показатели крови остаются при этом в норме, женщина страдает от малокровия.
Каждый тип анемии имеет специфические проявления, их рассмотрим чуть позже. Однако для всех видов малокровия характерна следующие симптомы:
- Слабость и быстрая утомляемость;
- Головные боли и головокружение, особенно при подъеме с постели и натуживании;
- Потеря аппетита, нередко извращенный вкус или полное отвращение к пище;
- Постоянная сонливость с нарушением режима ночного сна;
- Звон в ушах, «мушки» перед глазами;
- Рассеянность, раздражительность, снижение памяти;
- Одышка при минимальных физических нагрузках и другие признаки сердечной недостаточности (боли в сердце, снижение а/д);
- Учащенная частота сокращений сердца (до 90уд/мин);
- Шум в сердце — выраженный сердечный толчок, систолические шумы на верхушке сердца;
- Нарушение менструального цикла, вплоть до отсутствия менструации;
- Снижение полового влечения.
Формирование эритроцитов и образование гемоглобина — очень сложный процесс, сбой может произойти на любом этапе. Поэтому медики четко разделяют анемические процессы по причине возникновения и изменениям показателей крови. Видов анемии достаточно много, рассмотрим лишь наиболее распространенные и самые опасные из них.
Название наиболее часто встречающегося типа малокровия отражает причину патологического состояния лишь с одной стороны. Железодефицитная анемия развивается как на фоне недостаточного поступления железа с пищей (жесткие диеты, вегетарианство, неполноценное питание, кишечные паразиты), так и при нарушении его усвоения (болезни ЖКТ) и повышенной потребности в микроэлементе (беременность, фаза активного роста в подростковом периоде). Клинически железодефицит проявляется следующими симптомами:
- Гипоксический синдром — сонливость, постоянная усталость, звон в ушах, головные боли, одышка и тахикардия.
- Анемический синдром — снижение Hb и количества эритроцитов. ретикулоциты отсутствуют или ниже нормы, снижена концентрация железа в сыворотке (меньше 9,0 мкмоль/л). ЦП ниже 0,8 (гипохромная анемия). Эритроциты малого диаметра (меньше 7,2 микрон), разной формы.
- Сидеропенический синдром — сухая «алебастровая» кожа, усиленное выпадение волос, ломкие ногти.
Пациентки с железодефицитом отмечают потливость, потерю аппетита, нередки тошнота и рвота. Зачастую возникает странная потребность есть мел, бумагу или землю, вдыхать запах краски, бензина.
Характерной чертой хронической недостаточности железа является койлонихия (тонкие вогнутые ногти) и появление на ногтевых пластинах продольных бороздок. В тяжелых случаях возникает ощущение комка в горле, гипоацидный гастрит и атрофические изменения его слизистой, тотальный кариес и стрессовое недержание мочи.
Сидеробластная анемия характеризуется нормальным или повышенным количеством железа в организме. Сбой происходит в процессе его усвоения при приеме медикаментов (Циклосерина, Изониазида, Пиразинамида, Хлорамфеникола), алкогольном и свинцовом отравлении.
Характерным признаком данного типа малокровия является гемосидероз — непереработанное в гемоглобин железо откладывается в различных тканях, провоцируя заболевания сердца, сахарный диабет, очаговое поражение легких, увеличение печени и селезенки. Кожа при этом приобретает серый, землистый оттенок. Лабораторное подтверждение сидеробластной анемии:
- Низкие показатели гемоглобина и эритроцитов;
- Цп снижен — 0,4-0,6;
- Большое количество эритроцитов малого диаметра, однако встречаются и очень большие клетки;
- Количество ретикулоцитов ниже нормы;
- Высокий ожсс — более 86 мкмоль/л;
- Завышенный показатель сывороточного железа и ферритина;
- В костном мозге высокий показатель сидеробластов (клетки, имеющие венчик из железа вокруг ядра) — 70% при норме 2,0-4,6%.
Причины анемии — недостаток витамина (вегетарианство, скудная пища), повышенная потребность в нем (беременность, период грудного вскармливания, онкология) и плохое его усвоение (хронические болезни ЖКТ, прием противосудорожных препаратов и оральная контрацепция).
При В12-дефицитной анемии возникают симптомы со стороны ЦНС — мурашки по телу, онемение конечностей, «ватные» ноги, шаткая походка, слабая память, судороги.
Недостаток вит. В12 проявляется внезапной тягой к кислой пище, легкой желтушностью кожи и склер, запорами, глосситом и проблематичным глотанием, атрофическим гастритом, гепато- и спленомегалией.
Характерный признак — «лакированный» малиновый язык, сглаживание сосочков и ощущение жжения. В крови:
- Малое количество эритроцитов и ретикулоцитов, низкий Hb;
- ЦП выше нормы — от 1,05;
- Гигантские эритроциты (мегабластная анемия — диаметр эритроцитов более 9,5 микрон), тромбоциты и нейтрофилы (количество их снижено);
- Высокий показатель сывороточного железа;
- Снижение общего уровня лейкоцитов и базофилов;
- Завышенный показатель билирубина.
Критический недостаток фолиевой кислоты возникает при несбалансированном питании (отказ от мяса), почечной недостаточности, патологии печени, алкоголизме и злостным курением. Повышенная потребность в вит. В9 у беременных и онкобольных, подростков и в период кормления грудью.
Важно! Обычно диагностируется сочетание недостаточности фолиевой кислоты и вит. В12. Фолиеводефицитная и В12-дефицитная анемия дают одинаковую симптоматику. В анализе крови фиксируются идентичные изменения.
Следует различать малокровие, спровоцированное острой кровопотерей (внезапное обильное кровотечение), и хроническую анемию (степень кровопотери нарастает постепенно при язвенной патологии ЖКТ, гельминтах, опухолях).
Острая постгеморрагическая анемия характеризуется стремительным ухудшением состояния больной: обморочное состояние и потеря сознания, снижение пульса и а/д, рвота, холодный пот, нарастающая бледность кожи. Потеря больше 30% объема крови является критическим. В анализе крови:
- В зависимости от кровопотери снижение Hb и эритроцитов;
- ЦП в норме;
- Ретикулоциты свыше 11%;
- Диаметр эритроцитов при острой кровопотере не изменен, форма клеток разная;
- Лейкоцитоз свыше 12 г/л, сдвиг влево;
- Содержание сывороточного железа нормальное.
При хроническом течении постгеморрагической анемии, наравне с общими симптомами, женщина отмечает извращенность обоняния, непривычные вкусовые потребности, одутловатость лица, тошноту и повышение температуры до 37,2ºС. Лабораторные изменения:
- ЦП и гемоглобин снижен;
- Эритроциты деформированы, малого диаметра (меньше 7,2 микрон);
- Низкое количество лейкоцитов с незначительным лимфоцитозом;
сывороточное железо меньше 9 мкмоль/л; - Малое количество в крови кальция, меди и вит. А, в, с;
- Высокие показатели цинка, никеля и марганца.
В группу гемолитических анемий входит несколько патологических состояний, с различными проявлениями и механизмом развития малокровия. Для всех заболеваний, приобретенных и врожденных, характерна желтушность кожи и высокий билирубин в крови, гепато- и спленомегалия, моча цвета «мясных помоев» и темный кал, лихорадка, болезненность во всем теле.
- Серповидноклеточная анемия — врожденная патология, при которой формируются вытянутые серповидные эритроциты. При этом повышается вязкость крови, увеличивается риск тромбоза сосудов. Гемолитический криз возникает при гипоксических состояниях (пребывание в горах, душном, людном месте). Ноги пациентки припухшие, покрыты трудно заживающими язвами. Многие женщины отмечают нарушение зрения. В крови на фоне низкого Hb (50-80 г/л) и малого количества эритроцитов (1-2 Т/л, серповидной формы, телца Жолли, кольца Кабо) наблюдается повышение ретикулоцитов более 30%.
- Талассемия — генетически обусловленное торможение синтеза гемоглобина приводит к образованию мишеневидных эритроцитов. Заболевание развивается в детском возрасте: деформируются кости черепа, отстает умственное и физическое развитие, разрез глаз по монголоидному типу, увеличенный размер печени и селезенки, гемосидероз, землистого цвета кожа. ЦП и сывороточное железо низкие.
- Иммунные гемолитические анемии (вирусная, сифилитическая) — симптоматически идентичны, различия лишь в признаках основного заболевания. В крови высокий билирубин, большое количество ретикулоцитов, эритроциты круглой (не вогнутой) формы. Гемоглобин нормальный или чуть снижен.
- Неиммунные гемолитические анемии — малокровие при отравлениях (спиртным, кислотами, грибами, змеиным ядом), ожогах (повреждено более 20% кожи), малярии, недостатке вит. Е и специфическая анемия Маркиафавы-Микелли. В крови ретикулоциты 30%, ЦП в норме и больше, разной формы эритроциты, лейкопения и тромбоцитопения.
Гипопластическая анемия — следствие приобретенного или наследственного нарушения кроветворной функции костного мозга, характеризуется снижением всех клеток крови и замещением костного мозга жировыми клетками.
Клиническая картина: в дополнение к общим анемическим симптомам возникают частые кровотечения, синяки без причины, кровоточивость десен, язвы на коже, во рту и в глотке.
Гипопластическая анемия развивается при вирусе герпеса, грибковом поражении, при белковой и витаминной недостаточности, воздействии облучения и высокочастотных токов, эндокринной патологии (болезни щитовидки, сахарный диабет, гиперфункция яичников), системных заболеваниях (ревматоидный артрит, волчанка).
Анемия — частая «спутница» беременности. Возрастающая потребность в железе и витаминах в большинстве случаев не может восполняться питанием. На 29-36 нед. беременности потребность в железе возрастает до 3,5 мг/сут, тогда как из пищи максимально усвоиться может лишь 2 мг/сут. Анемия у будущей матери диагностируется при показателях крови, вышедших за предельные границы:
- гемоглобин — 100г/л;
- эритроциты — в I триместре 4,2, во II триместре 3,5, в III триместре 3,9;
- ретикулоциты — 5-10%;
- ферритин — в I триместре не больше 90, во II триместре до 74, в III триместре 10-15.
Чаще всего в период вынашивания плода у женщины диагностируется железодефицитная, В12- и В9-дефицитная анемия. Симптомы анемии при беременности идентичны общим признакам малокровия. Низкий гемоглобин чреват развитием токсикоза и угрозой выкидыша, на поздних сроках высок риск преждевременных родов и масштабного послеродового кровотечения. После родов у анемичной мамы часто недостает молока. Однако еще большая опасность грозит будущему малышу:
- задержка внутриутробного развития;
- гипотрофия — малый вес;
- слабость иммунитета.
Нельзя исключать и развитие у ребенка гемолитической болезни новорожденных. Этот тип гемолитической анемии связан с разрушением эритроцитов вследствие несовместимости группы крови или резус-фактора крови матери и ребенка. У новорожденного отмечается желтуха (не всегда), отеки (асцит), бочкообразный живот, увеличение селезенки и печени. В крови гемоглобин от 150 г/л и ниже, высокий билирубин и количество ретикулоцитов.
Важно! Предупреждение гемолитической анемии у новорожденных проводится еще в период беременности. Женщинам, у которых обнаружены антитела, вливают антирезусные иммуноглобулины.
Лечебная тактика при малокровии напрямую зависит от типа анемии и ее степени тяжести. Не при каждом анемическом синдроме эффект даст прием железосодержащих препаратов.
- Железодефицитная анемия — при легкой и среднетяжелой степени назначаются таблетки Сорбифер, Феррум лек, Ферроградумет, раствор Тотема. При тяжелой анемии целесообразен прием Гино-Тардиферона (высокое содержание железа), Гемофер пролонгатум и инъекции Мальтофер, Венофер, Феррум лек (в дальнейшем пациентка переводится на пероральный прием лекарств). Гемоглобин нормализуется уже через 1 мес., однако курс продолжается до 3 мес.
- В12- и В9-дефицитиная анемия — обязателен сочетанный прием вит. группы В (лучший препарат — В-комплекс) и фолиевой кислоты. При одновременном железодефиците используются препараты Ферровит форте, Гино-Тардиферон, Ранферон-12 (содержат железо и необходимые витамины).
- Железорефрактерная анемия, талассемия — полностью устраняющего болезни лечения не существует. Улучшение состояния достигается при в/в вливаниях эритроцитарной массы и препаратов-кровезаменителей.
- Острая постгеморрагическая анемия — остановка кровотечения, переливание эритроцитарной массы, крови.
- Хроническое постгеморрагическое малокровие — лечение причинного заболевания, длительный прием таблетированных препаратов железа, усиленных витаминами.
- Серповидноклеточная анемия не излечивается, терапия направлена на профилактику гемолитических кризов и вливания растворов, содержащих нормальные эритроциты.
- Вирусная, сифилитическая анемии — гемоглобин самостоятельно восстанавливается после лечения основного заболевания.
- Неиммунные гемолитические анемии — устранение провоцирующего фактора (выведение токсинов и ядов из организма) обычно приводит и к нормализации гемоглобина.
- Гипопластическая анемия — препараты железа бесполезны, для улучшения состояния врачи-гематологи прибегают к различным методам стимуляции кроветворной функции: инъекции Эпокомб, Эпостим, Эпомакс, Аранесп. Улучшение состояния дают кортикостероиды (Преднизолон, Гидрокортизон, Дексаметазон) и анаболики (Нандролон, Анаполон). Однако эти препараты имеют массу побочных эффектов. В тяжелых случаях результат даст только трансплантация костного мозга.
Какой препарат лучше при анемии — выбор остается за лечащим врачом. Так как гиповитаминоз принимает крупный масштаб, логично назначать комплексные лекарства, содержащие железо и необходимые витамины. Повышение показателя гемоглобина спустя месяц не всегда означает выздоровление. Для стойкого результата лечение следует продолжать 2-3 мес.
Отличным дополнением к лекарственной терапии является диета. Большое содержание железа в сухофруктах, большинстве ягод и фруктов (земляника, слива, малина, виноград, клубника, гранат, персик, вишня), капусте и томатах, белых грибах, моркови и свекле, мясе (телятина, крольчатина) и субпродуктах, гречке и яичном желтке, грецких орехах и черном шоколаде.
Важно! Кофе и крепкий чай, курение — снижают гемоглобин.
Из народных антианемических рецептов наиболее эффективны:
- Смесь меда, грецких орехов, сушеных абрикосов (предварительно замочить в горячей воде, а затем промыть) и кишмиша в равных частях. Добавить измельченный лимон (с цедрой!). Принимать по 1 ст. л. трижды в день.
- Свежевыжатый морковно-свекольный сок — курсовое лечение 2-3 мес.
- Настой крапивы — на стакан кипятка необходимо 1 ст. л. сухого сырья.
Легкая и среднетяжелая анемия обычно проходит без последствий в течение 1-3 мес. Тяжелую степень малокровия часто приходится лечить в стационарных условиях с дальнейшими повторными курсами дома.
Наиболее неблагоприятный прогноз касается гипопластической (апластической) и серповидноклеточной анемии, талассэмии. Оптимистичные шансы врачи дают молодым пациенткам (до 30 лет) с легкой степенью снижения гемоглобина и хорошей переносимостью лечебных мероприятий.
источник
Анемия. Виды анемий: железодефицитная, гемолитическая, В12 дефицитная, апластическая. Причины, диагностика, степени анемии.
Анемия или пониженное количество гемоглобина в крови, а в просторечии – «малокровие». Практически каждый человек хотя бы один раз сталкивался с такой формулировкой, особенно женщины. Что же означает этот пугающий термин? Почему возникает данное состояние организма? Чем опасна анемия? Как вовремя распознать её на начальных этапах?
Анемия – это патологическое состояние организма, при котором наблюдается снижение количества гемоглобина и эритроцитов ниже нижних границ нормы. Причем уменьшение содержания гемоглобина является обязательным признаком анемии, в отличие от снижения количества эритроцитов. То есть снижение концентрации гемоглобина при анемии есть всегда, а снижение количества эритроцитов может и не быть. Однако в некоторых случаях при анемии выявляются патологические формы эритроцитов (не двояко – вогнутые).
Анемия – это не самостоятельное заболевание, а следствие основной патологии, потому, выявление сниженного уровня эритроцитов и гемоглобина, требует проведения тщательной диагностики для выявления причины!
Гидремия – разжижение крови.
Такое состояние возможно при поступлении в кровоток тканевой жидкости при схождении отека, обильном питье. Гидремия – это псевдоанемия.
Сгущение крови
Сгущение крови может происходить вследствие потери жидкой части крови, что происходит при сильном обезвоживании. Обезвоживание наблюдается в результате сильной рвоты, поноса, обильного потения. Однако в этом случае за счет сгущения крови количество гемоглобина и эритроцитов может быть в пределах нормальных значений. В таких ситуациях говорят о наличии скрытой анемии.
Специфические и неспецифические признаки анемии – что относится к ним?
В первую очередь рассмотрим, как же проявляется анемия. Существуют неспецифические проявления и специфические. Неспецифические проявления называются так, потому что эти признаки общие для всех видов анемий. Специфические же проявления строго индивидуальны и характерны только для каждого конкретного вида анемии.Сейчас мы рассмотрим только неспецифические проявления, а специфические укажем при рассмотрении видов анемий.
Итак, к неспецифическим признакам анемий, относят следующие симптомы:
- бледность кожи и слизистых оболочек
- слабость
- головокружение
- шум в ушах
- головные боли
- быстрая утомляемость
- сонливость
- одышка
- анорексия (патологическая потеря аппетита или отвращение к пище)
- нарушение сна
- нарушения менструального цикла вплоть до полного прекращения менструаций (аменореи)
- импотенция
- тахикардия (увеличение частоты сердечных сокращений)
- шумы в сердце (усиление сердечного толчка, систолический шум на верхушке сердца)
- сердечная недостаточность
- при снижении количества гемоглобина менее 50 г/л возможно развитие ацидоза (закисление крови)
- снижение содержания гемоглобина ниже нормальных показателей
- снижение содержания эритроцитов ниже нормы
- изменение цветного показателя
- изменение содержания лейкоцитов и тромбоцитов
Виды анемий – постгеморрагическая, гемолитическая, дефицитная и гипопластическая
Анемии могут вызываться совершенно разными причинами, поэтому принято все анемии делить по различным признакам, в том числе по причинам, их вызывающим. Согласно причинам (патогенезу) выделяют три вида анемии: постгеморрагические, гемолитические и связанные с нарушением кровообразования (дефицитные и гипопластические). Что это значит? Разберем подробнее.
Постгеморрагические анемии связаны с острой или хронической кровопотерей (кровотечение, ранение).
Гемолитические – развиваются в связи с усиленным разрушением эритроцитов.
Дефицитные анемии вызваны недостатком витаминов, железа или других микроэлементов, которые необходимы для кроветворения.
Гипопластические анемии – это самый тяжелый вид анемий и связан он с нарушением кроветворения в костном мозгу.
- По степени тяжести. Существует три степени тяжести анемии – легкая, средняя и тяжелая в зависимости от содержания гемоглобина и эритроцитов в крови:
| Степень тяжести | Гемоглобин, г/л | Эритроциты, Т/л | ||||||||||||||||||||||
| Легкая | > 100 г/л | > 3 Т/л | ||||||||||||||||||||||
| Средняя | 100 – 66 г/л | 3 – 2 Т/л | ||||||||||||||||||||||
| Тяжелая | 1,05) и гипохромные (ЦП 8,0 микрон) и мегалобластные (СДЭ > 9,5 микрон). Нормоцитарные анемии характеризуются нормальным диаметром эритроцитов, микроцитарные – уменьшенным диаметром эритроцитов, а макроцитарные и мегалобластные связаны с увеличением диаметра эритроцитов. К нормоцитарным анемиям относят – острую постгеморрагическую и большинство гемолитических анемий; к микроцитарным – железодефицитную анемию, микросфероцитоз и хроническую постгеморрагическую анемию. Макроцитарные анемии – это гемолитическая болезнь новорожденных, фолиево дефицитная анемии. Мегалоцитарная – В12 дефицитнаяанемия.
Мы рассмотрели, на какие типы, и по каким признакам классифицируют анемии. Перейдем к рассмотрению, как проявляются отдельные виды анемий, какие изменения при этом наблюдаются в крови и в организме человека в целом.
Симптомы острой постгеморрагической анемии, картина крови Симптомами острой постгеморрагической анемии являются такие признаки: бледность, резкое головокружение, обмороки, частый пульс, холодный пот, снижение температуры тела, иногда рвота. Потеря крови более 30% от исходного уровня является критической и опасна для жизни. Диагностика постгеморрагической острой анемии В крови увеличивается количество ретикулоцитов более 11%, также появляются «незрелые» эритроциты и эритроциты с измененной формой клетки. Со стороны лейкоцитов наблюдается увеличение их общего количества выше 12 Г/л, а в лейкоцитарной формуле идет сдвиг влево. В последующие два месяца после острой кровопотери происходит восстановление показателей эритроцитов и гемоглобина. Однако восстановление количества эритроцитов и содержания гемоглобина связано с расходованием фонда железа в организме и может повлечь за собой развитие железодефицита. Поэтому в период восстановления после кровопотери необходимо соответствующее питание, то есть в рационе должны быть продукты с высоким содержанием железа (например, гранаты, гречка, печень и т.д.). Принципы лечения острой постгеморрагической анемии Лечение острой постгеморрагической анемии должно проводиться в условиях стационара и быть направлено на восстановление количества циркулирующей крови, количества форменных элементов крови и поддержание этих показателей. В первую очередь необходимо остановить кровотечение. Затем в зависимости от количества кровопотери применяют переливание крови, эритроцитарной массы и кровезаменителей. Симптомы хронической постгеморрагической анемии Симптомы хронической постгеморрагической анемии такие же, как при железодефицитной анемии. Какие же это симптомы? Итак, признаками хронической постгеморрагической анемии являются: кожа «алебастрового» оттенка (очень белая, бледная), извращение обоняния (непереносимость запахов или, наоборот, тяга к каким-либо запахам), изменение вкуса, одутловатость лица, пастозность голеней, ломкость волос и ногтей, сухость, шершавость кожи. Также возможно образование койлонехий – истонченных и уплощенных ногтей. Помимо этих внешних признаков возможно появление одышки, тошноты, головокружения, учащения пульса, слабости, утомляемости, субфебрильной температуры (до 37° С) и прочее. Из-за дефицита железа могут проявляться нарушения со стороны желудочно-кишечного тракта – кариес, глоссит, сниженная кислотность желудочного сока, а также непроизвольное мочеиспускание при смехе, потливость. Диагностика хронической постгеморрагической анемии В крови при хронической постгеморрагической анемии появляются слабо окрашенные эритроциты маленького размера, овальные эритроциты, снижено общее количество лейкоцитов, а в лейкоцитарной формуле наблюдается незначительный лимфоцитоз. В сыворотке крови концентрация железа ниже нормы – 9,0 мкмоль/л, также ниже нормального содержание меди, кальция, витаминов А, В, С, но, однако, повышена концентрация цинка, марганца и никеля в крови. Причины хронической постгеморрагической анемии Почему же возникает такое состояние – хроническая постгеморрагическая анемия? Причины этого явления следующие:
Лечение хронической постгеморрагической анемии Именно в силу причин, приводящих к развитию хронической постгеморрагической анемии, при лечении этого состояния, прежде всего, необходимо устранить причину хронической кровопотери.Затем необходимо сбалансированное питание, содержащее продукты с высоким содержанием железа, фолиевой кислоты и витаминов. В случае тяжелой анемии необходимо принимать препараты железа (сорбифер, феррум-лек) в виде таблеток или инъекций, препараты фолиевой кислоты, витамин В12 в виде таблеток или в виде инъекций. Наиболее эффективными препаратами для восстановления уровня железа в организме являются таблетированные препараты, которые выпускаются различными фирмами. В силу этого в аптеках представлен широкий выбор препаратов железа. При выборе препарата необходимо обращать внимание на содержание железа в одной таблетке и биологическую доступность данного препарата. Препараты железа необходимо принимать совместно с аскорбиновой кислотой и фолиевой кислотой, поскольку в такой комбинации происходит наилучшее усвоение железа. Однако при выборе препарата и дозы необходимо обязательно проконсультироваться с врачом. Гемолитические анемии – это группа анемий, при которых процессы разрушения эритроцитов преобладают над процессами их производства. Иными словами разрушение эритроцитов происходит быстрее, чем образуются новые клетки, взамен разрушенных. Гемолитические анемии могут быть наследственными и приобретенными. Наследственные гемолитические анемии это:
Симптомы гемолитических анемий Общим признаком всех гемолитических анемий является желтуха. Желтуха появляется вследствие того, что при разрушении эритроцитов выделяется в кровь большое количество билирубина, который и приводит к данному симптому. Помимо желтухи имеются следующие признаки, общие для всех гемолитических анемий – увеличение печени и селезенки, увеличение концентрации билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев». В связи с тем, что наиболее широкое распространение среди наследственных гемолитических анемий имеют серповидно – клеточная анемия и талассемия, более подробно рассмотрим именно их.
Серповидно – клеточная анемия вызвана тем, что синтезируется молекула гемоглобина с дефектом. Такие дефектные молекулы гемоглобина собираются в веретенообразные кристаллы (тактоиды), которые растягивают эритроцит, придавая ему серповидную форму. Такие серповидные эритроциты мало пластичны, повышают вязкость крови и закупоривают мелкие кровеносные сосуды. Кроме этого своими острыми концами такие эритроциты протыкают друг друга и разрушаются. Симптомы серповидно–клеточной анемии Серповидно – клеточная анемия внешне проявляется следующими признаками:
Диагностика серповидно–клеточной анемии В анализе крови сниженное количество гемоглобина (50 – 80 г/л) и эритроцитов (1 – 2 Т/л), увеличение ретикулоцитов до 30% и более. В мазке крови видны серповидные эритроциты и эритроциты с тельцами Жолли и кольцами Кабо. Лечение серповидно-клеточной анемии Основной принцип лечения данного вида анемии –это недопущение гемолитических кризов. Данный эффект достигается тем, что человек избегает гипоксических состояний – присутствия в разреженном воздухе, в местах с низким содержанием кислорода и прочее. Используют переливание эритроцитарной массы или кровезаменителей.
Талассемия возникает вследствие нарушения скорости образования гемоглобина. Такой незрелый гемоглобин не стабилен, в результате чего он выпадает в эритроцитах в виде включений – телец, а весь эритроцит приобретает внешний вид мишеневидной клетки. Талассемия – это тяжелое наследственное заболевание, которое невозможно вылечить, а можно лишь облегчить ее проявления. Симптомы талассемии
Диагностика талассемии В крови обнаруживаются мишеневидные эритроциты, увеличенное количество ретикулоцитов, снижение концентрации гемоглобина до 20 г/л, а эритроцитов до 1 Т/л. Также наблюдаются уменьшение количества лейкоцитов и тромбоцитов. Итак, мы рассмотрели основные виды наследственных гемолитических анемий, которые передаются от родителей к детям. Перейдем к рассмотрению приобретенных гемолитических анемий, которые возникают вследствие наличия провоцирующего фактора. Приобретенные гемолитические анемии, иммунные и не иммунные анемии Прежде всего, необходимо отметить, что приобретенные гемолитические анемии могут развиваться при участии иммунной системы (иммунные) или без ее участия (не иммунные). К анемиям, развивающимся при участии иммунной системы, относятся вирусная, сифилитическая анемия и гемолитическая болезнь новорожденных. Не иммунные гемолитические анемии – это болезнь Маркиафавы – Микелли, а также анемии, возникшие вследствие длительной маршевой ходьбы, отравления алкоголем, кислотами, солями тяжелых металлов, ядами змей, насекомых и грибов. При ожогах, составляющих более 20% поверхности тела, недостатке витамина Е и малярии, также развивается не иммунная гемолитическая анемия.
Лечение этих видов анемии, как правило, не требуется. Гемолитическая болезнь новорожденного, причины развития, симптомы заболевания, степени тяжести.
В настоящее время проводится профилактика гемолитической болезни новорожденных путем отслеживания наличия антител у матери. Если у матери выявляются антитела, то лечение проводят в стационаре. При этом производят вливание антирезусных иммуноглобулинов. Признаки не иммунных гемолитических анемий, лабораторные симптомы Не иммунные гемолитические анемии имеют следующие признаки – желтуха,увеличенные печень и селезенка,повышенная концентрация билирубина в крови, темный цвет мочи и кала, лихорадка, ознобы, боли, моча цвета «мясных помоев».В картине крови отмечается наличие эритроцитов различной формы и размеров, ретикулоцитоз до 30% и выше, сниженное количество лейкоцитов и тромбоцитов. Такие анемии сами по себе не требуют отдельного и особенного лечения, так как в первую очередь необходимо убрать фактор, вызывающий эту анемию (яды змей, соли тяжелых металлов и т.д.). Анемии, вызванные нарушением кровообразования, делятся на две большие группы – дефицитные анемии и гипопластические. Дефицитные анемии связаны с дефицитом необходимых для кроветворения элементов. К дефицитным анемиям относят – железодефицитную анемию, железорефрактерную анемию, В12 – дефицитную и фолиево дефицитную. Гипопластические анемии вызваны гибелью клеток – предшественниц в костном мозгу. Гипопластические анемии могут быть наследственными (анемия Фанкони, анемия Эстрена – Дамешика, анемия Блекфэрна — Даймонда) и приобретенными. Приобретенные гипопластические анемии развиваются либо сами по себе вследствие неизвестной причины, либо на фоне имеющегося заболевания — лучевой болезни, инфекций, повреждений иммунитета. Для большинства людей больший интерес представляют дефицитные анемии, которые могут возникнуть практически у каждого человека. Поэтому наиболее подробно остановимся именно на этом виде анемий.
Причины железодефицитной анемии Железодефицитная анемия возникает в следующих случаях:
Симптомы железодефицитной анемии Клинически железодефицитная анемия проявляется тремя основными синдромами – гипоксическим, сидеропеническим и анемическим. Что это за синдромы? Чем характеризуется каждый из них?Синдром – это устойчивая совокупность симптомов. Итак, гипоксический синдром характеризуется одышкой, головными болями, шумом в ушах, быстрой утомляемостью, сонливостью и тахикардией; анемический синдром выражается в уменьшении содержания количества эритроцитов и гемоглобина. Сидеропенический синдром напрямую связан с уменьшением количества железа в организме и проявляется так: нарушение питания кожи, ногтей, волос – кожа «алебастрового» оттенка, сухость и шершавость кожи, ломкие волосы и ногти. Затем присоединяетсяизвращение вкуса и обоняния (желание есть мел, вдыхать запах мытых бетонных полов и т.д.). Возможно появление осложнений со стороны желудочно-кишечного тракта – кариеса, дисфагии, снижения кислотности желудочного сока, непроизвольного мочеиспускания (в тяжелых случаях), потливости. Диагностика железодефицитной анемии В крови наблюдается снижение содержания гемоглобина до 60 – 70 г/л, эритроцитов до 1,5 – 2 Т/л, также снижено количество или вовсе отсутствуют ретикулоциты. Появляются эритроциты различных форм и размеров. Концентрация сывороточного железа ниже нормы. Лечение железодефицитной анемии В основе лечения железодефицитной анемии лежат принципы устранения причины ее возникновения – лечение заболеваний желудочно – кишечного тракта, а также введение сбалансированного пищевого рациона. В диете должны присутствовать продукты с высоким содержанием железа (печень, мясо, молоко, сыр, яйца, злаки и т.д.). Однако главным средством восстановления количества железа в организме на начальном этапе являются лекарственные препараты железа. В большинстве случаев такие лекарства назначают в виде таблеток. В тяжелых случаях прибегают к внутримышечным или внутривенным инъекциям. В лечении данной анемии используют, например, такие препараты: сорбифер, феррум-лек, тардиферон, тотема и другие. Выбор различных лекарственных средств, в том числе комбинированных, очень широк. При выборе необходимо консультироваться с врачом. Обычно, суточная доза для профилактики и лечения анемии легкой степени составляет 50-60 мг железа, для лечения анемии средней тяжести – 100-120 мг железа в сутки. Лечение анемии тяжелой степени проводят в стационаре и применяют препараты железа в виде инъекций. Затем переходят на таблетированные формы. Препараты железа вызывают потемнение стула, однако в данной ситуации это нормально.Если препарат железа вызывает неприятные ощущения в желудке, то его необходимо заменить.
Железорефрактерную анемию также называют сидеробластной или сидероахристической. Железорефрактерная анемия развивается на фоне нормального содержания железа в сыворотке крови и недостатка ферментов, которые участвуют в синтезе гемоглобина. То есть основная причина железорефрактерной анемии – нарушение процессов «усвоения» железа. Симптомы железорефрактерной анемии, что такое гемосидероз? Проявляется железорефрактерная анемия одышкой, головными болями, головокружением, шумом в ушах, быстрой утомляемостью, сонливостью, нарушениями сна и тахикардией. Из-за высокого содержания железа в крови тканях наблюдается гемосидероз.Гемосидероз – это отложение железа в органах и тканях вследствие его избытка. При гемосидерозе развивается недостаточность сердечно – сосудистой системы вследствие отложения железа в сердечной мышце, сахарный диабет, поражение легких и увеличиваются размеры печени и селезенки. Кожа приобретает землянистый оттенок. Диагностика железорефрактерной анемии, что такое сидеробласты? Цветной показатель крови снижен до 0,6 – 0,4, присутствуют эритроциты различных форм и размеров, количество гемоглобина и эритроцитов ниже нормы. Имеются изменения и в костном мозгу – появляются клетки – сидеробласты. Сидеробласты – это клетки, имеющие вокруг ядра венчик из железа. В норме таких клеток в костном мозгу 2,0 – 4,6%, а при железорефрактерной анемии их количество может доходить до 70%. Лечение железорефрактерной анемии Лечения, которое смогло бы устранить ее совсем, на сегодняшний день нет. Возможно применение заместительной терапии – вливание эритроцитарной массы и кровезаменителей.
Во-первых, что такое В12? В12 – это витамин, который имеет также название цианкобаламин. Цианкобаламин содержится в основном в продуктах животного происхождения – мясо, печень, почки, молоко, яйца, сыр. Уровень витамина В12 необходимо постоянно поддерживать употреблением соответствующих продуктов, поскольку происходят его естественные физиологические потери с калом и желчью. Причины В12 дефицитной анемии Итак, В12 – дефицитная анемия – это анемия, возникающая вследствие недостаточности витамина В12. Недостаток витамина В12 может быть вызван недостаточным его поступлением с пищей или нарушением его усвоения в желудочно-кишечном тракте. Недостаточное поступление цианкобаламина с пищей возможно у строгих вегетарианцев. Также недостаток В12 может проявиться при повышении потребности в нем у беременных женщин, кормящих матерей, раковых больных. Неусвоение витамина В12, поступающего с пищей в достаточном количестве, происходит при заболеваниях желудка, тонкого кишечника (дивертикулы, глисты) и лечении противосудорожными средствами или оральными контрацептивами. Симптомы В12 дефицитной анемии Симптомы проявления В12 – дефицитной анемии характеризуются нарушениями в центральной нервной системе и желудочно-кишечном тракте. Итак, рассмотрим эти две большие группы симптомов:
Диагностика В12 дефицитной анемии В системе крови происходит переход на мегалобластический тип кроветворения. Это означает, что в крови появляются гигантские эритроциты с укороченным сроком жизни, ярко окрашенные эритроциты без просветления в центре, грушевидные и овальные эритроциты с тельцами Жолли и кольцами Кабо. Также появляются гигантские нейтрофилы, уменьшается количество эозинофилов (вплоть до полного отсутствия), базофилов и общего количества лейкоцитов. В крови повышена концентрация билирубина, в связи с чем, может наблюдаться легкая желтушность кожи и склер глаз. Лечение В12 дефицитной анемии В первую очередь необходимо вылечить заболевания желудочно-кишечного тракта и наладить сбалансированное питание, с достаточным содержанием витамина В12. Применение курса инъекций витамина В12 быстро нормализует кроветворение в костном мозгу, а далее необходимо постоянное, регулярное поступление с пищей достаточного количества витамина В12.
Симптомы фолиеводефицитной анемии При фолиево дефицитной анемии страдает желудочно-кишечный тракт, поэтому и проявления данной анемии связаны с нарушениями работы желудочно-кишечного тракта. Наблюдается появление повышенной чувствительности к кислой пище, глоссита, трудностей глотания, атрофии слизистой желудка, увеличения размеров печени и селезенки. Лечение фолиеводефицитной анемии Для лечения данного вида анемии применяют таблетки фолиевой кислоты и нормализуют рацион питания, в котором должны быть продукты, содержащие достаточное количество фолиевой кислоты.
Симптомы гипопластических анемий Гипопластические анемии могут быть наследственными или приобретенными, однако все подвиды данного типа анемий характеризуются одинаковыми проявлениями. Рассмотрим эти симптомы:
Причины, вызывающие развитие гипопластической анемии Какие же причины способны вызывать подобное поражение костного мозга? Наследственные анемии, соответственно, передаются по наследству, а вот приобретенные? Все факторы, способные приводить к развитию гипопластической анемии, делятся на экзогенные (внешние) и эндогенные (внутренние). В таблице приведены основные экзогенные и эндогенные причины, способные вызвать развитие гипопластической анемии.
Принципы лечения гипопластических анемий Лечение гипопластических анемий находится строго в компетенции врача – гематолога. Могут применяться различные методы стимулирования кроветворения, или пересадка костного мозга. Итак, мы рассмотрели все основные виды анемий. Конечно, их гораздо больше, однако мы не можем объять необъятное. При появлении каких-либо признаков анемии необходимо своевременно обратиться к врачу. И регулярно сдавать анализ крови на содержание гемоглобина. источник Анемия — клинико-гематологический синдром, характеризующийся уменьшением содержания гемоглобина в единице объема крови, чаще при одновременном уменьшении количества эритроцитов, что приводит к развитию кислородного голодания тканей. Принято считать анемией снижение уровня гемоглобина ниже 130 г/л и количества эритроцитов ниже 4 х 10 12 /л у мужчин и соответственно ниже 120 г/л и 3,7 х 10 12 /л у женщин. Классификация анемий Патогенетическая классификация анемий: I. Анемии вследствие кровопотери (постгеморрагические). II. Анемии вследствие нарушения образования эритроцитов и гемоглобина. 1. Железодефицитная анемия. 2. Мегалобластные анемии, связанные с нарушением синтеза ДНК. (В12— и фолиеводефицитные анемии) 3. Анемии, связанные с костномозговой недостаточностью (гипопластические). Ш. Анемии вследствие усиленного кроворазрушения (гемолитические). Классификация анемий по цветовому показателю: I. Анемия гипохромная, цв. показатель ниже 0,8. — тиреопривная анемия (при гипофункции щитовидной железы). II. Анемия нормохромная, цв. показатель 0,85-1,05: — анемия при хронической почечной недостаточности; — гипопластическая (апластическая) анемия; — лекарственная и лучевая цитостатическая болезнь; — анемия при злокачественных новообразованиях и гемобластозах; — анемия при системных заболеваниях соединительной ткани; — анемия при хроническом активном гепатите и циррозе печени; — гемолитическая анемия (кроме талассемий); — острая потгеморрагическая анемия. III. Анемия гиперхромная, цв. показатель выше 1,05: АНЕМИИ ВСЛЕДСТВИЕ НАРУШЕНИЯ ОБРАЗОВАНИЯ ЭРИТРОЦИТОВ И ГЕМОГЛОБИНА ЖЕЛЕЗОДЕФИЦИТНАЯ АНЕМИЯ Железодефицитная анемия — это анемия, обусловленная дефицитом железа в сыворотке крови, костном мозге и депо. Люди, страдающие скрытым дефицитом железа и железодефицитной анемией, составляют 15-20% населения Земли. Наиболее часто железодефицитная анемия встречается среди детей, подростков, женщин детородного возраста, пожилых людей. Общепринято выделять две формы железодефицитных состояний: латентный дефицит железа и железодефицитную анемию. Латентный дефицит железа характеризуется уменьшением количества железа в его депо и снижением уровня транспортного железа крови при нормальных показателях гемоглобина и эритроцитов. Основные сведения об обмене железа Железо в организме человека участвует в регуляции обмена веществ, в процессах переноса кислорода, в тканевом дыхании и оказывает огромное влияние на состояние иммунологической резистентности. Почти все железо в организме человека входит в состав различных белков и ферментов. Можно выделить две его основные формы: гемовое (входящее в состав гема – гемоглобин, миоглобин) и негемовое. Железо гема мясных продуктов всасывается без участия соляной кислоты. Однако ахилия может в определенной мере способствовать развитию железодефицитной анемии при наличии значительных потерь железа из организма и высокой потребности в железе. Всасывание железа осуществляется преимущественно в двенадцатиперстной кишке и верхних отделах тощей кишки. Степень всасывания железа зависит от потребности организма в нем. При выраженном дефиците железа всасывание его может происходить и в остальных отделах тонкого кишечника. При уменьшении потребности организма в железе происходит снижение скорости поступления его в плазму крови и увеличивается отложение в энтероцитах в виде ферритина, который элиминируется при физиологическом слущивании эпителиальных клеток кишечника. В крови железо циркулирует в комплексе с плазменным трансферином. Этот белок синтезируется преимущественно в печени. Трансферин захватывает железо из энтероцитов, а также из депо в печени и селезенке и переносит его к рецепторам на эритрокариоцитах костного мозга. В норме трансферин насыщен железом приблизительно на 30%. Комплекс трансферин-железо взаимодействует со специфическими рецепторами на мембране эритрокариоцитов и ретикулоцитов костного мозга, после чего путем эндоцитоза проникает в них; железо переносится в их митохондрии, где включается в протопрорфирин и таким образом участвует в образовании гема. Освободившийся от железа трансферин неоднократно участвует в переносе железа. Затраты железа на эритропоэз составляют 25 мг в сутки, что весьма значительно превышает возможности всасывания железа в кишечнике. В связи с этим для гемопоэза постоянно используется железо, освобождающееся при распаде эритроцитов в селезенке. Хранение (депонирование) железа осуществляется в депо — в составе белков ферритина и гемосидерина. Наиболее распространенная форма депонирования железа в организме — ферритин. Он представляет собой водорастворимый гликопротеиновый комплекс, состоящий из расположенного в центре железа, покрытого белковой оболочкой из апоферритина. Каждая молекула ферритина содержит от 1000 до 3000 атомов железа. Ферритин определяется почти во всех органах и тканях, но наибольшее его количество обнаруживается в макрофагах печени, селезенки, костного мозга, эритроцитах, в сыворотке крови, в слизистой оболочке тонкой кишки. При нормальном балансе железа в организме устанавливается своеобразное равновесие между содержанием ферритина в плазме и депо (прежде всего в печени и селезенке). Уровень ферритина в крови отражает количество депонированного железа. Ферритин создает запасы железа в организме, которые могут быстро мобилизоваться при повышении потребности тканей в железе. Другая форма депонирования железа — гемосидерин — малорастворимое производное ферритина с более высокой концентрацией железа, состоящее из агрегатов кристаллов железа, не имеющих апоферритиновой оболочки. Гемосидерин накапливается в макрофагах костного мозга, селезенки, в купферовских клетках печени. Физиологические потери железа Потеря железа из организма мужчин и женщин происходит следующими путями:
Указанными путями происходит выделение около 1 мг железа за сутки. Кроме того, у женщин детородного периода дополнительные потери железа возникают за счет менструаций, беременности, родов, лактации. Хронические кровопотери Хронические кровопотери являются одной из самых частых причин железодефицитной анемии. Наиболее характерны необильные, но длительные кровопотери, которые незаметны для больных, но постепенно снижают запасы железа и приводят к развитию анемии. Основные источники хронических кровопотерь Маточные кровопотери — самая частая причина железодефицитной анемии у женщин. У пациенток репродуктивного возраста чаще всего речь идет о длительных и обильных кровопотерях во время менструации. Нормальной считается менструальная кровопотеря, составляющая 30-60 мл (15-30 мг железа). При полноценном питании женщины (с включением мяса, рыбы и других железосодержащих продуктов) из кишечника максимально может всосаться ежедневно 2 мг, а за месяц — 60 мг железа и, следовательно, при нормальной менструальной кровопотере анемия не развивается. При большем объеме ежемесячной менструальной кровопотери разовьется анемия. Хронические кровотечения из желудочно-кишечного тракта — наиболее частая причина железодефицитной анемии у мужчин и неменструирующих женщин. Источниками желудочно-кишечных кровотечений могут являться эрозии и язвы желудка и 12-перстной кишки, рак желудка, полипоз желудка, эрозивный эзофагит, диафрагамальная грыжа, десневые кровотечения, рак пищевода, варикозное расширение вен пищевода и кардиального отдела желудка (при циррозе печени и других формах портальной гипертензии), рак кишечника; дивертикулярная болезнь желудочно-кишечного тракта, полипы толстого кишечника, кровоточащий геморрой. Кроме того, железо может теряться при носовых кровотечениях, при кровопотерях в результате заболеваний легких (при туберкулезе легких, бронхоэктазах, раке легкого). Ятрогенные кровопотери — это кровопотери, обусловленные врачебными манипуляциями. Это редкие причины железодефицитной анемии. К ним относятся частые кровопускания у больных полицитемией, кровопотери во время процедур гемодиализа у больных хронической почечной недостаточностью, а также донорство (приводит к развитию скрытого дефицита железа у 12% мужчин и 40% женщин, а при многолетнем стаже провоцирует развитие железодефицитной анемии). Повышенная потребность в железе Повышенная потребность в железе также может привести к развитию железодефицитной анемии. Беременность, роды и лактация — в эти периоды жизни женщины расходуется значительное количество железа. Беременность – 500 мг железа (300 мг – ребенку, 200 мг — плацента). В родах теряется – 50 – 100 мг Fe. При лактации теряется 400 — 700 мг Fe. Для восстановления запасов железа требуется не менее 2,5-3 лет. Следовательно, у женщин с интервалами между родами менее 2,5-3 лет легко развивается железодефицитная анемия. Период полового созревания и роста — довольно часто сопровождается развитием железодефицитной анемии. Развитие железодефицитной анемии обусловлено повышением потребности в железе в связи с интенсивным ростом органов и тканей. У девушек играют роль также и такие факторы, как появление кровопотерь вследствие менструаций и нерациональное питание в связи с желанием похудеть. Повышенная потребность в железе у больных В 12-дефицитной анемией может наблюдаться на фоне лечения витамином В12, что объясняется интенсификацией нормобластического кроветворения и использованием для этих целей больших количеств железа. Интенсивные занятия спортом в некоторых случаях могут способствовать развитию железодефицитной анемии, особенно если ранее имелся скрытый дефицит железа. Развитие анемии при интенсивных спортивных нагрузках обусловлено повышением потребности в железе при больших физических нагрузках, увеличением мышечной массы (и, следовательно, использованием большего количества железа для синтеза миоглобина). Недостаточное поступление железа с пищей Алиментарная железодефицитная анемия, обусловленная недостаточным поступлением железа с пищей, развивается у строгих вегетарианцев, у лиц с низким социально-экономическим уровнем жизни, у больных с психической анорексией. Нарушение всасывания железа Основными причинами, приводящими к нарушению всасывания железа в кишечнике и развитию вследствие этого железодефицитной анемии, являются: хронические энтериты и энтеропатии с развитием синдрома мальабсорбции; резекция тонкой кишки; резекция желудка по методу Бильрот II («конец в бок»), когда происходит выключение части 12-перстной кишки. При этом железодефицитная анемия часто сочетается в В12-(фолиево)-дефицитной анемией в связи с нарушением всасывания витамина В12 и фолиевой кислоты. Нарушения транспорта железа Железодефицитная анемия, обусловленная снижением содержания в крови трансферина и, следовательно, нарушением транспорта железа, наблюдается при врожденной гипо- и атрансферинемии, гипопротеинемиях различного генеза, появлении антител к трансферину. В основе всех клинических проявлений железодефицитной анемии лежит дефицит железа, который развивается в тех случаях, когда потери железа превышают его поступление с пищей (2 мг/сутки). Первоначально уменьшаются запасы железа в печени, селезенке, костном мозге, что получает отражение в снижении уровня ферритина в крови. На этой стадии происходит компенсаторное усиление всасывания железа в кишечнике и повышение уровня мукозного и плазменного трансферина. Содержание сывороточного железа еще не снижено, анемии нет. Однако в дальнейшем истощенные депо железа уже не способны обеспечить эритропоэтическую функцию костного мозга и, несмотря на сохраняющийся высокий уровень трансферина в крови, значительно снижаются содержание железа в крови (транспортное железо), синтез гемоглобина, развиваются анемия и последующие тканевые нарушения. При дефиците железа снижается активность железосодержащих и железозависимых ферментов в различных органах и тканях, а также уменьшается образование миоглобина. В результате указанных нарушений и снижения активности ферментов тканевого дыхания (цитохромоксидаз) наблюдаются дистрофические поражения эпителиальных тканей (кожи, ее придатков, слизистой оболочки, желудочно-кишечного тракта, нередко — мочевыводящих путей) и мускулатуры (миокарда и скелетной мускулатуры). Снижение активности некоторых железосодержащих ферментов в лейкоцитах нарушает их фагоцитарную и бактерицидную функции и угнетает защитные иммунные реакции. Классификация железодефицитной анемии 1 стадия — дефицит железа без клиники анемии (латентная анемия) 2 стадия —железодефицитная анемия с развернутой клинико-лабораторной картиной Степень тяжести 1. Легкая (содержание Нb 90-120 г/л) 2. Средняя (содержание Нb 70-90 г/л) 3. Тяжелая (содержание Нb ниже 70 г/л) Клиническая картина Клинические проявления железодефицитной анемии можно сгруппировать в два важнейших синдрома — анемический и сидеропенический. Анемический синдром Анемический синдром обусловлен снижением содержания гемоглобина и количества эритроцитов, недостаточным обеспечением тканей кислородом и представлен неспецифическими симптомами. Больные жалуются на общую слабость, повышенную утомляемость, снижение работоспособности, головокружение, шум в ушах, мелькание мушек перед глазами, сердцебиения, одышку при физической нагрузке, появление обморочных состояний. Может появляться снижение умственной работоспособности, памяти, сонливость. Субъективные проявления анемического синдрома вначале беспокоят больных при физической нагрузке, а затем и в покое (по мере роста анемии). При объективном исследовании обнаруживается бледность кожи и видимых слизистых оболочек. Нередко обнаруживается некоторая пастозность в области голеней, стоп, лица. Характерны утренние отеки — «мешки» вокруг глаз. Анемия обусловливает развитие синдрома миокардиодистрофии, который проявляется одышкой, тахикардией, часто аритмией, умеренным расширением границ сердца влево, глухостью тонов сердца, негромким систолическим шумом во всех аускультативных точках. При тяжелой и длительной анемии миокардиодистрофия может привести к выраженной недостаточности кровообращения. Железодефицитная анемия развивается постепенно, поэтому организм больного постепенно адаптируется и субъективные проявления анемического синдрома не всегда бывают ярко выражены. Сидеропенический синдром Сидеропенический синдром (синдром гипосидероза) обусловлен тканевым дефицитом железа, что приводит к снижению активности многих ферментов (цитохромоксидаза, пероксидаза, сукцинат-дегидрогеназа и др.). Сидеропенический синдром проявляется многочисленными симптомами:
Лабораторные данные Диагностика латентного дефицита железа Латентный дефицит железа диагностируется на основании следующих признаков:
При дефиците железа процент насыщения трансферина железом снижен. Диагностика железодефицитной анемии При снижении гемоглобинового фонда железа появляются характерные для железодефицитной анемии изменения в общем анализе крови:
Биохимический анализ крови — характерно снижение уровня сывороточного железа и ферритина. Могут отмечаться также изменения, обусловленные основным заболеванием. Лечение железодефицитной анемии Лечебная программа включает:
3.1. Устранение дефицита железа и анемии. 3.2. Восполнение запасов железа (терапию насыщения). 3.3. Противорецидивную терапию. 4. Профилактику железодефицитной анемии. 1. Устранение этиологических факторов Ликвидация дефицита железа и, следовательно, излечение железодефицитной анемии возможно только после устранения причины, ведущей к постоянному дефициту железа. 2. Лечебное питание При железодефицитной анемии больному показана диета, богатая железом. Максимальное количество железа, которое может всосаться из пищи в желудочно-кишечном тракте, — 2 г в сутки. Железо из продуктов животного происхождения всасывается в кишечнике в больших количествах, чем из растительных продуктов. Лучше всего всасывается двухвалентное железо, входящее в состав гема. Железо мяса всасывается лучше, а железо печени хуже, поскольку железо в печени содержится преимущественно в виде ферритина, гемосидерина, а также в виде гема. В малом количестве железо всасывается из яиц, фруктов. Лучше всего всасывается железо из телятины (22%), рыбы (11%). Из яиц, фасоли, фруктов всасывается лишь 3% железа. Для нормального кроветворения необходимо получать с пищей, кроме железа, также другие микроэлементы. Диета больного железодефицитной анемией должна включать 130 г белков, 90 г жира, 350 г углеводов, 40 мг железа, 5 мг меди, 7 мг марганца, 30 мг цинка, 5 мкг кобальта, 2 г метионина, 4 г холина, витамины групп В и С. При железодефицитной анемии может быть рекомендован также фито сбор, включающий листья крапивы, череды, земляники, черной смородины. Одновременно рекомендуется принимать отвар или настой плодов шиповника по 1 стакану в течение дня. Настой шиповника содержит железо и витамин С. 3. Лечение железосодержащими препаратами 3.1. Устранение дефицита железа Поступление железа с пищей способно восполнить лишь нормальную суточную его потерю. Применение препаратов железа является патогенетическим методом лечения железодефицитной анемии. В настоящее время применяются препараты, содержащие двухвалентное железо (Fe ++ ), так как оно значительно лучше всасывается в кишечнике. Препараты железа обычно применяются внутрь. Для обеспечения нарастающего повышения уровня гемоглобина необходимо принимать ежедневно такое количество железосодержащих препаратов, чтобы оно соответствовало суточной дозе двухвалентного железа от 100 мг (минимальная доза) до 300 мг (максимальная доза). Выбор суточной дозы в указанных дозах определяется преимущественно индивидуальной переносимостью препаратов железа и выраженностью дефицита железа. Назначать более 300 мг двухвалентного железа в сутки бесполезно, так как объем его всасывания при этом не возрастает. Препараты двухвалентного железа назначаются за 1 ч до еды или не ранее чем через 2 ч после еды. Для лучшего всасывания железа одновременно принимают аскорбиновую или янтарную кислоту, всасывание увеличивается также в присутствии фруктозы. Ферро-фольгамма (комплекс железа сульфата 100 мг + аскорбиновая к-та 100 мг + фолиевая к-та 5мг + цианокобаламин 10 мг). Принимают по 1-2 капс 3 раза в день после еды. Ферроплекс — комплекс железа сульфата и аскорбиновой кислоты, назначается по 2-3 драже 3 раза в день. Гемофер пролонгатум — препарат продленного действия (железа сульфата 325 мг), по 1-2 таблетки в день. Лечение железосодержащими препаратами проводится в максимально переносимой дозе до полной нормализации содержания гемоглобина, что происходит через 6-8 недель. Клинические признаки улучшения появляются значительно раньше (уже через 2-3 дня) по сравнению с нормализацией уровня гемоглобина. Это связано с поступлением железа в ферменты, дефицит которых обусловливает мышечную слабость. Содержание гемоглобина начинает возрастать на 2-3-й неделе от начала лечения. Железосодержащие препараты, как правило, принимают внутрь. При нарушении процессов всасывания железа из желудочно-кишечного тракта препараты назначают парентерально. 3.2. Восполнение запасов железа (терапия насыщения) Запасы железа (депо железа) в организме представлены железом ферритина и гемосидерина печени и селезенки. Для восполнения запасов железа после достижения нормального уровня гемоглобина проводят лечение железосодержащими препаратами в течение 3 месяцев в суточной дозе, которая в 2-3 раза меньше по сравнению с дозой, применявшейся на этапе купирования анемии. 3.3. Противорецидивная (поддерживающая) терапия При продолжающихся кровотечениях (например, обильных менструациях) показан прием препаратов железа короткими курсами по 7-10 дней ежемесячно. При рецидиве анемии показано проведение повторного курса лечения в течение 1-2 мес. 4. Профилактика железодефицитной анемии Лицам с ранее излеченной железодефицитной анемией при наличии условий, угрожающих развитием рецидива железодефицитной анемии (обильные менструации, фибромиома матки и др.) проводится профилактика анемии. Рекомендуется профилактический курс длительностью 6 недель (суточная доза железа 40 мг), затем проводятся два 6-недельных курса в год или прием 30-40 мг железа ежедневно в течение 7-10 дней после менструации. Кроме того, необходимо ежедневно употреблять не менее 100 грамм мяса. МЕГАЛОБЛАСТНЫЕ АНЕМИИ Мегалобластные анемии — это группа анемий, обусловленных нарушением синтеза ДНК в эритрокариоцитах вследствие дефицита витамина В12 и/или фолиевой кислоты и характеризующихся мегалобластным типом кроветворения. В12-дефицитная анемия Основные сведения о метаболизме витамина В12 Витамин В12 поступает в организм человека с пищей. Он содержится в мясе, печени, почках, яичном желтке, сыре, молоке, черной икре. В пище витамин В12 связан с белком. При кулинарной обработке пищи, а также в желудке под действием соляной кислоты и протеолитических ферментов витамин В12 высвобождается из пищи. Далее в желудке витамин В12 (внешний фактор Касла) соединяется с белками «R» (Rapid-binders). Затем комплекс «витамин В12 + белок «R»» поступает в 12-перстную кишку, где под влиянием протеолитических ферментов панкреатического сока белок «R» отщепляется и освободившийся В12 соединяется с гастромукопротеином (внутренний фактор Касла), поступившим сюда из желудка. Гастромукопротеин вырабатывается париетальными клетками в фундальной части и в области тела желудка. Щелочная среда содержимого 12-перстной кишки усиливает связь витамина В12 и гастромукопротеина. Гастромукопротеин защищает витамин В12 от воздействия протеолитических ферментов. Далее комплекс «витамин В12+ гастромукопротеин» продвигается по тонкому кишечнику и поступает в подвздошную кишку, где в присутствии ионов Са 2+ взаимодействует со специфическими рецепторами, после чего расщепляется, и витамин В12 поступает в митохондрии клеток слизистой оболочки. Отсюда витамин В12 проникает в кровь, где соединяется с транспортными белками — транскобаламинами и доставляется к печени и костному мозгу. В этих органах витамин В12 высвобождается из комплекса витамин В12 + транскобаламин. Часть комплекса элиминируется с желчью. В костном мозге витамин В12 используется для кроветворения, в печени — депонируется и в дальнейшем поступает при необходимости в кровь. Часть витамина В12 из печени в составе желчи снова поступает в 12-перстную кишку и в дальнейшем всасывается согласно вышеописанному механизму. При полноценном питании суточный рацион человека содержит до 30 мкг витамина В12. Суточная потребность в нем составляет 2-7 мкг. За сутки всасывается в кишечнике около 6-9 мкг витамина В12. В организме здорового человека содержится около 2-5 мг витамина В12. Основным органом, в котором содержится наибольшее количество кобаламина, является печень. Запасов витамина В12 в печени хватает на 3-5 лет после прекращения его всасывания. Свою биологическую роль витамин В12 выполняет в виде двух коферментов — метилкобаламина и дезоксиаденозилкобаламина. Превращение свободного витамина В12 в В12-коферменты протекает в несколько этапов при участии специфических ферментов. С помощью этих коферментов витамин В12 осуществляет две важнейшие реакции. Первая реакция протекает с участием кофермента метилкобаламина и обеспечивает созревание, развитие и размножение клеток системы кроветворения, прежде всего красного кроветворного ростка и эпителия желудочно-кишечного тракта. Вторая реакция — расщепление и синтез жирных кислот протекает с участием кофермента дезоксиаденозилкобаламина и обеспечивает превращение продукта метаболизма жирных кислот метилмалоновой кислоты в янтарную кислоту. Нормальный ход этой реакции обеспечивает оптимальный метаболизм миелина в нервной системе и требует присутствия активной формы фолиевой кислоты. Основные причины развития В12-дефицитной анемии: I. Нарушение секреции желудком «внутреннего фактора» — гастромукопротеина встречаются при атрофическом аутоиммунном гастрите с продукцией антител к париетальным клеткам и гастромукопротеину, тотальной гастрэктомии (реже — субтотальной резекции желудка), раке и полипозе желудка, токсическом действие высоких доз алкоголя на слизистую оболочку желудка. II. Нарушение всасывания витамина В12 в тонком кишечнике у больных с резекцией участка подвздошной кишки (более 60 см), при синдроме мальабсорбции различного генеза (ферментные энтеропатии, целиакия, тропическое спру, энтериты, болезнь Крона, амилоидоз кишечника), и лимфоме тонкой кишки. Замедлено всасывание В12 у больных хроническим панкреатитом с нарушением секреции трипсина. Снижают всасывание витамина В12 ряд лекарственных средств (колхицин, неомицин, бигуаниды, циметидин и др.). III. Конкурентное расходование витамина В12 встречается при инвазии глистами (широкий лентец, власоглав и др.). IV. Повышенный расход витамина В12наблюдается при многоплодной беременности, хронической гемолитической анемии, миелопролиферативных заболеваниях, новообразованиях, тиреотоксикозе. V. Нарушение поступления витамина В12 с пищей обусловлено неполноценным питанием или строгой вегетарианской диетой. VI. Снижение запасов витамина В12 имеет место при выраженном циррозе печени. При дефиците витамина В12 развиваются следующие нарушения. Недостаток кофермента витамина В12 метилкобаламина приводит к нарушению синтеза тимидина, включаемого в ДНК, вследствие этого нарушается синтез ДНК и процессы митоза в клетках организма. Наиболее значительно страдают быстрорастущие ткани — клетки костного мозга, эпителий желудочно-кишечного тракта. Клетки костного мозга утрачивают способность к нормальному созреванию. Особенно выражены нарушения со стороны красного кроветворного ростка. Появляется большое количество мегалобластов. Мегалобластный эритропоэз характеризуется задержкой созревания ядер эритрокариоцитов по сравнению со степенью гемоглобинизации цитоплазмы, сокращением продолжительности жизни красных кроветворных клеток, повышенным распадом мегалобластов в костном мозге. Эритропоэз при В12-дефицитной анемии становится неэффективным, что, подтверждается несоответствием между повышенным количеством эритрокариоцитов в костном мозге и резким снижением содержания ретикулоцитов в периферической крови, увеличением сывороточного железа и уменьшением включения радиоактивного железа в эритрокариоциты. Одновременно отмечаются нарушение и неэффективность гранулоцитопоэза и тромбоцитопоэза. Появляются гигантские формы тромбоцитов, гранулоцитов, увеличивается фагоцитоз нейтрофилов костномозговыми макрофагами. Могут появляться аутоантитела к нейтрофилам, что также способствует развитию нейтропении у больных В12— дефицитной анемией. Таким образом, дефицит витамина В12приводит к неэффективности гемопоэза с развитием мегалобластной анемии, лейкопении и тромбоцитопении. Кроме того, происходит нарушение созревания эпителиальных клеток желудочно-кишечного тракта, что обусловливает развитие атрофии слизистой оболочки желудка и тонкого кишечника. Недостаток кофермента витамина В12 дезоксиаденозилкобаламина приводит к нарушению обмена жирных кислот и накоплению в большом количестве токсичных для нервной системы метилмалоновой и пропионовой кислот. В отсутствие витамина В12 метилмалоновая кислота не превращается в янтарную кислоту. В результате развивается повреждение задних и боковых столбов спинного мозга, а также снижается синтез миелина в нервных волокнах. Клиническая картина Развитие заболевания характерно преимущественно для возраста 60-70 лет. Клиническая картина В12-дефицитной анемии характеризуется поражением трех систем: пищеварительной, кроветворной и нервной. Поражение пищеварительной системы У подавляющего большинства больных симптомы поражения системы органов пищеварения (прежде всего субъективные) могут быть наиболее ранними признаками заболевания. Больные жалуются на снижение или отсутствие аппетита, ощущение тяжести в подложечной области после еды, отрыжку съеденной пищей и воздухом, боль и жжение в языке, в области десен, губ, иногда в области прямой кишки. Указанные жалобы больных обусловлены развитием глоссита, атрофического гастрита и атрофическими изменениями слизистой оболочки кишечника. При осмотре полости рта обращают на себя внимание воспалительно-атрофические изменения слизистой оболочки полости рта и языка. Для В12-дефицитной анемии характерен гладкий «лакированный» язык с атрофированными сосочками, потрескавшийся, с участками воспаления ярко-красного цвета (воспаленным и красным может оказаться весь язык), иногда с изъязвлениями. Глоссит наблюдается только при значительном и длительном дефиците витамина В12, приблизительно у 25% больных. Глоссит характерен не только для В12-де-фицитной анемии, он может наблюдаться и при железодефицитной анемии. Слизистая оболочка полости рта бледна, могут отмечаться явления афтозного стоматита. При пальпации живота может определяться неинтенсивная боль в эпигастральной области, нередко — увеличение печени и селезенки. Поражение кроветворной системы Нарушение системы кроветворения является ведущим в клинической картине заболевания и характеризуется анемией различной степени выраженности. Больные предъявляют жалобы характерные для анемического синдрома. Кожа обычно бледная, очень часто с лимонно-желтым оттенком (в связи с гипербилирубинемией, обусловленной гемолизом). Иногда при В12— дефицитной анемии повышается температура тела (не выше 38°С). Поражение нервной системы Изменения нервной системы при В12-дефицитной анемии являются характерным признаком этого заболевания и, как правило, наблюдаются при тяжелом и длительном течении. Поражение нервной системы при В12-дефицитной анемии называется фуникулярным миелозом и характеризуется вовлечением в процесс задних и боковых столбов спинного мозга. Наступает демиелинизация, а затем дегенерация нервных волокон в спинном мозге и спинномозговых нервах. Больные жалуются на слабость в ногах, особенно при подъеме по лестнице, при быстрой ходьбе, ощущение ползания мурашек по ногам, онемение ног. Больным кажется, что они не чувствуют при ходьбе опоры под ногами. Создается впечатление, что нога наступает не на твердую землю, а на что-то рыхлое, мягкое, как вата. Указанные жалобы обусловлены нарушением проприоцептивной чувствительности. При преобладании поражения задних столбов нарушается глубокая, пространственная, вибрационная чувствительность; появляются сенсорная атаксия, затруднения при ходьбе; снижаются сухожильные рефлексы; наблюдается атрофия мышц нижних конечностей. Может наступить нарушение функции тазовых органов (недержание мочи, недержание кала). При поражения боковых столбов спинного мозга неврологическая симптоматика иная: развивается нижний спастический парапарез с резким повышением сухожильных рефлексов и тонуса мышц нижних конечностей; нарушение функции тазовых органов характеризуется задержкой мочеиспускания и дефекации. Лабораторные данные Исследование периферической крови и костного мозга имеют решающее значение в диагностике заболевания. Общий анализ крови. Характерно развитие гиперхромной макроцитарной анемии (цветовой показатель более 1,1). Изредка анемия может быть нормохромной. Эритроциты большие (макроциты), имеется анизоцитоз (разная величина эритроцитов, наряду с макроцитами имеются нормоциты), пойкилоцитоз (изменение формы эритроцитов). Во многих мегалоцитах (макроцитах) обнаруживаются остатки ядра (тельца Жолли, кольца Кебота), возможно наличие базофильной пунктуации. Часто в периферической крови обнаруживаются нормобласты, количество ретикулоцитов у большинства больных снижено или нормальное. Количество лейкоцитов снижено, определяются нейтропения, эозинопения, относительный лимфоцитоз. Для В12-дефицитной анемии чрезвычайно характерно появление больших сегментоядерных нейтрофилов с полисегментированным ядром. Количество тромбоцитов снижено, однако геморрагических проявлений, как правило, нет, потому что тромбоцитопения не достигает критической величины. Миелограмма. Характерными признаками В12-дефицитной анемии, позволяющими верифицировать диагноз, являются:
• изменение клеток миелоидного ряда — они увеличиваются в размерах, встречаются большие метамиелоциты (юные), палочкоядерные, сегментоядерные нейтрофилы; характерно появление гиперсегментированных нейтрофилов; • нарушение созревания мегакариоцитов, выражающееся в нарушении отшнуровки тромбоцитов (непостоянный признак). Биохимический анализ крови — специфических изменений не существует. Однако при В12-дефицитной анемии часто наблюдается гемолитический синдром, обусловленный внутрикостномозговым распадом эритрокариоцитов, а также укорочением продолжительности жизни периферических эритроцитов. Это проявляется неконъюгированной гипербилирубинемией. Возможно повышение содержания в крови ЛДГ, и ЛДГ2. Часто отмечается умеренное повышение содержания железа в сыворотке крови (при развитии гемолиза). Анализ мочи и кала — при развитии гемолиза в моче выявляется уробилин, в кале — увеличено количество стеркобилина. Инструментальные исследования Эзофагогастродуоденоскопия — наблюдаются атрофические изменения слизистой оболочки пищеварительного тракта. Характерно развитие диффузного атрофического гастрита, дуоденита, реже атрофического эзофагита. Исследование желудочной секреции — выявляется уменьшение количества желудочного сока, отсутствие соляной кислоты (ахилия) и пепсина, иногда снижение соляной кислоты. Рентгеноскопия желудка — обнаруживаются нарушения эвакуаторной функции желудка, уплощение и сглаженность складок слизистой оболочки. Диагностические критерии В12-дефицитной анемии: I. Основные диагностические критерии.
II. Дополнительные диагностические критерии. 1. Атрофический гастрит, отсутствие соляной кислоты, пепсина и гастромукопротеина в желудочном соке. 2. Обнаружение в крови антител к париетальным клеткам желудка, гастромукопротеину или комплексу «витамин В12 гастромукопротеин». 3. Ретикулоцитарный криз (на 5-7 день лечения В12 резко возрастает количество ретикулоцитов в периферической крови). Фолиево дефицитная анемия (ФДА) ФДА относится к группе мегалобластных анемий. Развитие мегалобластного типа кроветворения обусловлено тем, что при дефиците фолиевой кислоты нарушается влияние витамина В12 на синтез ДНК. Основные сведения о метаболизме фолиевой кислоты Фолиевая кислота водорастворимый, термолабильный витамин. В пищевых продуктах и в клетках организма фолиевая кислота содержится в виде фолиевокислых солей — полиглутаматов (фолатов). Фолаты содержатся в мясе, печени, растительных продуктах (шпинат, спаржа, салат, бобовые, овощи, фрукты, грибы), дрожжах, молоке. При кулинарной обработке, длительной варке более 50% фолатов разрушается, поэтому для обеспечения потребностей организма в фолатах необходимо употреблять свежие овощи и фрукты. Всасывание фолатов происходит в 12-перстной кишке и проксимальном отделе тощей кишки. В крови 5-метилтетрагидрофолат связывается с различными белками, поступает в печень и быстро пролиферирующие клетки костного мозга. Проникновение фолатов через мембрану и накопление их в клетке происходит с участием витамина В12. Фолиевая кислота участвует в следующих биохимических реакциях:
Показатели нормального обмена фолиевой кислоты: Суточная потребность в фолиевой кислоте — 100-200 мкг. Общее количество поступающей с пищей фолиевой кислоты при полноценном питании — 500-600 мкг/сут. Количество фолатов, всасывающихся в кишечнике — 400- 480 мкг/сут. Общее содержание фолатов в организме — 5-10 мг. Срок, в течение которого депо обеспечивает потребность в фолиевой кислоте при прекращении ее поступления в организм — 4-5 мес. Недостаточное поступление фолатов с пищей Алиментарная недостаточность фолатов частая причина ФДА. Она развивается при недостаточном употреблении в пищу овощей и фруктов, мяса и других продуктов, содержащих фолаты, а также при неправильной их кулинарной обработке. ФДА может развиваться у детей грудного возраста при вскармливании козьим молоком, различными питательными смесями, содержащими мало или совсем не содержащими фолатов; при исключении из рациона овощей, фруктов, мяса. Нарушение всасывания фолатов в тонком кишечнике Причины, обусловливающие нарушение всасывания фолатов в кишечнике, аналогичны тем, которые нарушают всасывание витамина B12: врожденные нарушения транспорта фолатов через стенку тонкой кишки; обширная резекция тонкой кишки, особенно тощей; энзимодефицитные энтеропатии; синдром мальабсорбции различного генеза; синдром «слепой кишки»; опухолевые заболевания тонкого кишечника. Повышенная потребность в фолатах Повышенная потребность в фолатах наблюдается у детей любого возраста, но особенно часто у детей первого года жизни, а также в периоды интенсивного роста, полового созревания. Повышенная потребность в фолатах характерна для беременности, хронических воспалительных заболеваний, хронических гемолитических анемий, эксфолиативного дерматита, злокачественных новообазований, в том числе гемобластозов. Хроническая алкогольная интоксикация Алкоголь нарушает всасывание фолатов в тонком кишечнике, поэтому хроническое злоупотребление алкоголем может приводить к ФДА. Повышенная потеря фолатов Может наблюдаться при тяжело протекающем циррозе печени (уменьшается депо фолатов в печени), гемодиализе, сердечной недостаточности. Прием лекарственных препаратов
Вышеприведенные этиологические факторы приводят к уменьшению образования активной формы фолиевой кислоты — 5,10-метилентетрагидрофолиевой кислоты. В итоге нарушается синтез ДНК в кроветворных клетках и развивается мегалобластная анемия. Клиническая картина Заболевание чаще всего развивается у детей, молодых людей и у беременных женщин. Больные предъявляют жалобы, характерные для анемии любого генеза — отмечается неспецифический анемический синдром. Однако, в отличие от В12-дефицитной анемии отсутствуют жалобы, обусловленные поражением нервной системы. При осмотре обращает на себя внимание бледность кожи, субиктеричность. При исследовании внутренних органов можно обнаружить небольшое увеличение селезенки (непостоянный признак) и синдром миокардиодистрофии (приглушенность сердечных тонов, негромкий систолический шум на верхушке, нарушение фазы реполяризации миокарда левого желудочка на ЭКГ в виде снижения амплитуды зубцов Т). В отличие от В12-дефицитной анемии для ФДА характерно отсутствие атрофического глоссита, атрофического гастрита и ахилии. Лабораторные данные Общий анализ крови — характерны те же признаки, что и при В12-дефицитной анемии. Биохимический анализ крови — может наблюдаться увеличение количества неконъюгированного билирубина (вследствие гемолиза эритроцитов), снижение содержания фолиевой кислоты в крови и эритроцитах. Миелограмма — характерна гиперплазия красного кроветворного ростка, появление большого количества мегалобластов, гиперсегментированных нейтрофилов. Проба с гистидином — больной принимает 15 г гистидина, после чего определяется экскреция с мочой формиминглутаминовой кислоты за 8 ч после приема гистидина. В норме основная часть гистидина превращается при участии фолиевой кислоты в глутаминовую кислоту, с мочой выводится от 1 до 18 мг формиминглутаминовой кислоты. При фолиеводефицитной анемии выделение формиминглутаминовой кислоты значительно увеличивается. Диагностические критерии ФДА. 1. Общий анализ периферической крови: гиперхромная анемия, макроцитоз эритроцитов, гиперсегментация нейтрофилов, лейкопения, тромбоцитопения. 2. Миелограмма — обнаружение мегалобластов, гиперсегментированных нейтрофилов. 3. Отсутствие глоссита, атрофического гастрита. 4. Отсутствие фуникулярного миелоза. 5. Нормальное содержание в крови витамина В12. 6. Сниженное содержание фолиевой кислоты в сыворотке крови и эритроцитах. 7. Нормальная суточная экскреция с мочой метилмалоновой кислоты. Лечение В12-дефицитной и ФДА К лечению В12 -дефицитной анемии витамином В12 можно приступать только после установления и верификации диагноза с помощью миелограммы. Даже 1-2 инъекции витамина В12, не устраняя синдром анемии, могут трансформировать мегалобластическое кроветворение в нормобластическое и сделать стернальную пункцию неинформативной. Лечение В12-дефицитной анемии проводится внутримышечными инъекциями витамина В12. Имеются два препарата витамина В12 — цианокобаламин и оксикобаламин. Цианокобаламин назначают по 400-500 мкг внутримышечно 1 раз в день (оксикобаламин по 1 мг/сут через день). Длительность курса лечения составляет 4-6 недель. На 3-4-й день от начала лечения витамином В12 начинается увеличение содержания ретикулоцитов в крови. После курса лечения назначается курс закрепляющей терапии: цианокобаламин вводят 1 раз в неделю в течение 2 месяцев, а затем постоянно 2 раза в месяц по 400-500 мкг. Оксикобаламин: в течение 3 месяцев его вводят 1 раз в неделю, а затем постоянно 1 раз в месяц по 500 мкг. При фуникулярном миелозе назначают большие дозы витамина В12 (1000 мкг ежедневно) в сочетании с коферментом витамина В12 кобамамидом (500 мкг 1 раз в день внутримышечно), который участвует в обмене жирных кислот и улучшает функциональное состояние спинного мозга и нервных волокон. Эта доза витамина В12 вводится до исчезновения клиники миелоза. Препараты фолиевой кислоты назначают лишь больным с ФДА. Назначают фолиевую кислоту внутрь в суточной дозе 5-15 мг. При В12-дефицитной анемии лечение фолиевой кислотой не показано. Лечение В12-дефицитной анемии проводится пожизненно, диспансерное наблюдение должно осуществляться постоянно. ГИПО И АПЛАСТИЧЕСКИЕ АНЕМИИ Гипо и апластические анемии — это нарушения гемопоэза, характеризующиеся редукцией эритроидного, миелоидного и мегакариоцитарного кроветворных ростков костного мозга и панцитопенией в крови, не сопровождающаяся гепатоспленомегалией, при отсутствии миелофиброза, острого лейкоза или миелодиспластического синдрома. Патоморфологической основой гипо и апластических анемий является резкое сокращение активного кроветворного костного мозга и замещение его жировой тканью. Заболевание встречается с частотой 5-10 случаев на 1 млн. жителей в год. В зависимости от этиологических факторов различают врожденную (наследственную) и приобретенную гипо- и апластическую анемию. В свою очередь приобретенная гипо- и апластическая анемия подразделяется на идиопатическую (с неизвестной этиологией) форму и форму с известными этиологическими факторами. Идиопатическая форма составляет 50-65% всех случаев апластической анемии. Известные этиологические факторы приобретенной апластической анемии: I. Химические факторы: бензол, неорганические соединения мышьяка, этилированный бензин (содержит тетраэтилсвинец, тяжелые металлы — ртуть, висмут и др.), хлорорганические соединения и т.д. II. Физические факторы: ионизирующая радиация и рентгеновское излучение. III. Лекарственные средства: антибиотики (хлорамфеникол, метициллин и др.), сульфаниламиды, нестероидные противовоспалительные средства (бутадион, индометацин, анальгин), препараты золота, мерказолил, цитостатики, антиаритмические средства (хинидин), гипотензивные средства (каптоприл, эналаприл; допегит) и др. IV. Инфекционные агенты: вирусы инфекционного мононуклеоза, гепатита, гриппа, Эпштейна-Барр, иммунодефицита человека, цитомегаловирусы, герпеса, эпидемического паротита. V. Иммунные заболевания: болезнь «трансплантат против хозяина», эозинофильный фасциит, тимома и карцинома тимуса. В настоящее время основными патогенетическими факторами апластической анемии считаются:
Поражение полипотентной стволовой гемопоэтической клетки — важнейший патогенетический фактор апластической анемии. Стволовая клетка является родоначальницей всех кроветворных клеток. При апластической анемии значительно снижается колониеобразующая способность костного мозга, нарушается пролиферация кроветворных клеток, в конечном итоге формируется синдром панцитопении — лейкопения, анемия, тромбоцитопения. Окончательно механизм угнетения активности полипотентной стволовой кроветворной клетки не выяснен. Поражение клеточного микроокружения стволовой кроветворной клетки. В настоящее время установлено, что на функциональное состояние стволовой кроветворной клетки и полипотентных клеток-предшественниц большое влияние оказывает микроокружение, т. е. строма костного мозга. Клетки микроокружения обуславливают деление и дифференцировку стволовых клеток. Основными клеточными компонентами микроокружения стволовой клетки являются остеобласты, фибробласты, эндостальные, адвентициальные, эндотелиальные и жировые клетки. В связи с большой ролью микроокружения в кроветворении, предложен термин «индуцирующее кроветворение микроокружение» (ИКМ). Для нормального развития гемопоэтических клеток нужны гемопоэтические факторы роста (ГФР) и колониестимулирующие факторы роста (КСФ) — гликопротеиновые гормоны, которых идентифицировано около двадцати. Под влиянием ГРФ и КСФ происходит деление и дифференцировка гемопоэтических клеток. При апластической анемии внутренний дефект полипотентной стволовой клетки является первичным нарушением, которое проявляется или усиливается при воздействии различных этиологических факторов на гемопоэтические клетки через изменение ИКМ. Большое значение в развитии апластической анемии придается иммунным механизмам. Предполагается, что происходит блокирование Т-лимфоцитами дифференциации стволовых клеток, образуются антитела к стволовым клеткам, эритроцитам, клеткам — предшественницам разных линий кроветворения, что приводит к депрессии гемопоэза. При взаимодействии гемопоэтических стволовых кроветворных клеток с активированными цитотоксическими Т-лимфоцитами и некоторыми цитокинами стимулируется апоптоз (запрограммированная клеточная смерть) стволовых клеток гемопоэза. При апластической анемии могут возникать нарушения ферментных систем в эритроцитах, что делает их гиперчувствительными к различным повреждающим факторам и приводит к их внутримозговому разрушению. Значительные изменения претерпевает метаболизм кроветворных клеток, вследствие чего клетки всех кроветворных ростков не усваивают в достаточной мере вещества необходимые для оптимального гемопоэза (железо, витамин В12). Снижение интенсивности пролиферации и дифференциации клеток красного ряда кроветворения, повышенное разрушение эритроцитов, неоптимальное использование железа и нарушение гемоглобинообразования приводят к накоплению в организме железа с отложением железосодержащих пигментов в различных органах и тканях (печени, селезенке, коже, миокарде, надпочечниках и др.) — т. е. развивается вторичный гемохроматоз. Классификация 1. Гипопластическая анемия с поражение всех трех кроветвроных ростков: 2. Парциальная гипопластическая анемия с избирательным поражением эритропоэза. III.Роль иммунных факторов в развитии анемии Клиническая картина Основная клиническая и лабораторная симптоматика приобретенной гипо- и апластической анемии с поражением всех трех кроветворных ростков костного мозга обусловлена тотальным угнетением гемопоэза, а также гипоксией органов и тканей и геморрагическим синдромом. Выраженность симптоматики зависит от степени тяжести и варианта течения анемии. Больные предъявляют жалобы характерные для анемического синдрома. Характерны кровоточивость (десневые, носовые, желудочно-кишечные, почечные, маточные кровотечения) и частые инфекционно-воспалительные заболевания. При острой форме симптомы развиваются быстро и течение заболевания с самого начала тяжелое. Но у большинства больных заболевание развивается достаточно медленно, постепенно, в определенной мере пациенты адаптируются к анемии. Заболевание обычно распознается при выраженной симптоматике. При осмотре больных обращает на себя внимание выраженная бледность кожи и видимых слизистых оболочек, часто с желтушным оттенком; геморрагические высыпания на коже, чаще в виде кровоподтеков различной величины. Часто на месте инъекций (внутримышечных, внутривенных, подкожных) образуются обширные гематомы. Геморрагическая сыпь локализуется преимущественно в области голеней, бедер, живота, иногда на лице. Могут наблюдаться кровоизлияния в конъюнктиву и видимые слизистые оболочки — губы, слизистую оболочку полости рта. Могут быть тяжелые носовые, желудочно-кишечные, почечные, легочные, маточные, внутрицеребральные кровотечения. Периферические лимфоузлы не увеличены. При исследовании внутренних органов могут обнаруживаться следующие изменения:
Нередко развивается гемосидероз внутренних органов вследствие повышенного разрушения неполноценных эритроцитов, снижения использования железа костным мозгом, нарушения синтеза гема, частых переливаний эритроцитарной массы. Лабораторные данные и инструментальные исследования Общий анализ крови — выраженное снижение количества эритроцитов и гемоглобина; анемия у большинства больных нормохромная, нормоцитарная; характерно отсутствие или резкое снижение количества ретикулоцитов (арегенераторная анемия); наблюдается лейкопения за счет гранулоцитопении с относительным лимфоцитозом; характерна тромбоцитопения. Таким образом, наиболее существенным лабораторным проявлением гипо- и апластической анемии является панцитопения. СОЭ увеличена. Биохимический анализ крови — содержание сывороточного железа повышено, процент насыщения железом трансферина значительно увеличен. Исследование стернального пунктата (миелограмма) — выраженное уменьшение клеток эритроцитарного и гранулоцитарного рядов, лимфоцитов и значительная редукция мегакариоцитарного ростка. В тяжелых случаях костный мозг выглядит «опустошенным», в стернальном пунктате можно обнаружить лишь единичные клетки. В костном мозге значительно увеличивается содержание железа, расположенного как внеклеточно, так и внутриклеточно. Диагностические критерии
• Увеличение содержания железа внутри эритрокариоцитов и внеклеточно.
1. Лечение глюкокортикоидами Глюкокортикоидная терапия наиболее эффективна, если гипопластическая анемия обусловлена аутоиммунными механизмами, появлением антител против клеток крови. Однако глюкокортикоиды применяются и при других вариантах депрессии костного мозга в связи со способностью стимулировать эритроцитарный, нейтрофильный и мегакариоцитарный ростки кроветворения. Суточная доза преднизолона составляет 1-2 мг/кг массы больного в сутки, чаще всего доза колеблется от 60 до 120 мг в сутки. Длительность терапии преднизолоном зависит от эффекта в первые 2 недели от начала лечения. Если есть эффект, то лечение преднизолоном продолжают с переходом на поддерживающие дозы 15-20 мг после значительного улучшения гемограммы. Если эффекта нет, то дальнейшее лечение преднизолоном (более 2 недель) бесполезно. Лечение преднизолоном может продолжаться от 4 недель до 3-4 мес. 2. Лечение анаболическими препаратами Анаболические стероидные препараты, с одной стороны, нивелируют катаболические эффекты глюкокортикоидов, с другой — стимулируют кроветворение. Назначают неробол по 20 мг/сут или более эффективный aнaполон (оксиметолон) по 200 мг/сут в течение 5-6 месяцев. Лечение анаболиками показано также после спленэктомии. 3. Лечение андрогенами Андрогены обладают анаболическим эффектом и стимулируют эритропоэз. Повышение уровня гемоглобина отмечается у 50% больных, нейтрофильных лейкоцитов — у 30%, тромбоцитов — у 25% больных. Суточные дозы андрогенов составляют 1-2 мг/кг, иногда — 3-4 мг/кг. Вводится тестостерона пропионат 5% раствор по 1 мл 2 раза в сутки или препарат продленного действия сустанон-250 1 раз в месяц (в 1 мл содержится 250 мг мужских половых гормонов). Эффект андрогенов наступает постепенно, поэтому лечение проводится длительно в течение нескольких месяцев. При уменьшении дозы или отмене андрогенов у некоторых больных возможно обострение заболевания. Лечение андрогенами проводится только мужчинам. 4. Лечение цитостатиками (иммунодепрессантами) Иммунодепрессантная терапия назначается лишь при отсутствии эффекта от других методов лечения у больных с аутоиммунной формой гипопластической анемии. Азатиоприн (имуран) по 0,05 г 2-3 раза в день с постепенным уменьшением дозы после получения эффекта. Длительность курса лечения может составить 2-3 месяца. 5. Спленэктомия Спленэктомия показана при отсутствии эффекта от глюкокортикоидов всем больным, если они не имеют септических осложнений. Положительный эффект спленэктомии наблюдается у 84% больных и обусловлен уменьшением продукции антител против кроветворных клеток, а также уменьшением секвестрации клеток крови. 6. Лечение антилимфоцитарным глобулином Лечение антилимфоцитарным глобулином рекомендуется при отсутствии эффекта от спленэктомии и других методов лечения. Препарат подавляет образование антител против клеток крови. Вводится внутривенно капельно по 120-160 мг антилимфоцитарного глобулина 1 раз в день в течение 10-15 дней. Иммуносупрессивная терапия с помощью антилимфоцитарного глобулина, умеренных доз глюкокортикоидов и андрогенов является методом выбора у больных апластической анемией, не имеющих HLA-идентичного донора, и которым, следовательно, не может быть произведена пересадка костного мозга. 7. Лечение циклоспорином Циклоспорин А — обладает иммунодепрессантным эффектом. Является эффективным средством лечения апластической анемии, гематологическая ремиссия достигается у 40-50% больных. Применяется внутрь в виде масляного раствора или в капсулах в дозе 4 мг/кг/сут в 2 приема. При отсутствии токсических явлений лечение может продолжаться в течение нескольких месяцев. 8. Пересадка костного мозга В настоящее время трансплантация костного мозга является основным методом лечения гипопластической анемии при отсутствии эффекта от других методов лечения. Производится пересадка подобранного и совместимого по HLA-системе костного мозга. Перед трансплантацией производится предварительная иммунодепрессия цитостатиками и облучением. Достижение ремиссия после миелотрансплантации отмечено у 80-90% больных с тяжелой апластической анемией. Наилучшие результаты получены у лиц не старше 30 лет. Трансплантацию следует применять не позднее 3 месяцев с момента установления диагноза тяжелой аплазии. 9. Лечение колониестимулирующцми факторами Колониестимулирующие факторы (КСФ) — это гликопротеиды, стимулирующие пролиферацию и дифференциацию клеток-предшественников различных типов. Препараты гранулоцитарного КСФ филграстим, ленограстим, нартограстим преимущественно стимулируют образование нейтрофилов; препараты гранулоцитарно-макрофагального КСФ молграмостим, сарграмостим, лейкомакс стимулируют продукцию эозинофилов, нейтрофилов, моноцитов. Основным показанием к назначению КСФ является нейтропения различной природы, в том числе при апластической анемии, повышающая риск развития угрожающих жизни инфекций. КСФ применяются в дополнение к другим методам терапии. Применяются рекомбинантные препараты КСФ внутривенно в дозе 5 мкг/кг/сут в течение 14 дней. 10. Трансфузии эритроцитов Показаниями к трансфузии эритроцитов являются выраженная анемия, признаки гипоксии мозга, гемодинамические нарушения. Частые переливания эритроцитов создают опасность развития гиперсидероза и депрессивного влияния на эритроцитопоэз. В связи с этим гемотрансфузии строго лимитируются уровнем гемоглобина. Его повышение до 80-90 г/л является достаточным для устранения гипоксии тканей. Если 250-450 мл эритроцитарной массы, перелитые в течение недели, поддерживают содержание гемоглобина на уровне 90-100 г/л, то более частые гемотрансфузии не нужны. 11. Десфералотерапия При гипопластической (апластической) анемии имеется значительное накопление железа в клетках гемопоэза, особенно эритропоэза. Это обусловлено депрессией гемопоэза, снижением утилизации железа, недостаточным образованием протопорфирина IX. Избыток железа может нарушать функцию клеток гемопоэза вплоть до их гибели. Поэтому в комплексную терапию гипопластической анемии включают препарат десферриоксалин (десферал), избирательно связывающий и выводящий из организмам человека трехвалентное железо. Препарат быстро выводится через почки в виде ферроксамина, придавая моче красноватый оттенок. Десферал вводят внутримышечно или внутривенно по 500 мг 2 раза в день в течение не менее 2-3 недель. После перерыва на 3-4 недели целесообразно провести еще 2-4 таких таких курса. У 50% больных после лечения десфералом показатели гемопоэза улучшаются. 12. Трансфузии тромбоцитов Переливание тромбоцитов производится при выраженном геморрагическом синдроме, обусловленном тромбоцитопенией. Переливаются тромбоциты, полученные от одного донора. 13. Лечение иммуноглобулином В последние годы для лечения гипопластических анемий рекомендуют внутривенное введение иммуноглобулина в дозе 400 мкг/кг массы тела в течение 5 дней подряд. Препарат стимулирует эритро- и тромбоцитопоэз. источник |


 Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.
Постгеморрагические анемии могут быть острыми и хроническими. Острая постгеморрагическая анемия развивается в ответ на скоротечную и большую кровопотерю, а хроническая – развивается в ответ на длительную кровопотерю в небольших количествах.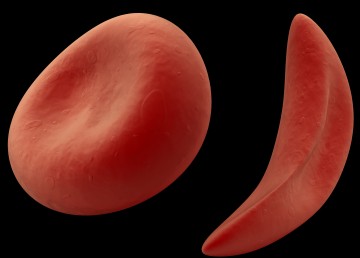 Причины серповидно–клеточной анемии
Причины серповидно–клеточной анемии Талассемия – причины заболевания
Талассемия – причины заболевания Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы.
Сифилитическая и вирусная иммунные гемолитические анемии проявляются одинаково. Эти виды анемии являются вторичными, то есть возникают на фоне уже имеющегося заболевания – сифилиса или вирусной инфекции.У этих людей наблюдается лихорадка, ознобы, боли в спине, слабость, одышка, кровь в моче, увеличение печени и селезенки. В крови увеличивается концентрация билирубина и количество ретикулоцитов, а вот содержание гемоглобина может быть в норме или немного снижено, появляются эритроциты круглой формы.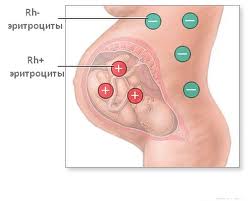 Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.
Гемолитическая болезнь новорожденных – это заболевание, которое возникает в результате конфликта эритроцитов матери и ребенка, которые имеют несовместимые антигены группы крови или резус – фактора. В таком случае антитела матери проникают к плоду через плаценту и вызывают разрушение эритроцитов у ребенка. Тяжесть гемолитической болезни новорожденных зависит от количества антител матери, которые проникают через плаценту к плоду. Поэтому беременные женщины с отрицательным резус – фактором крови регулярно сдают анализ крови на наличие именно таких антител. Если антитела обнаруживаются, значит необходимо соответствующее лечение. Ребенок с гемолитической болезнью новорожденных рождается с отеками, асцитом, имеет высокий тон крика и высокое содержание незрелых эритроцитов (эритробластов, нормоцитов и ретикулоцитов). Гемолитическая болезнь новорожденных классифицируется по степени тяжести на легкую, среднюю и тяжелую согласно количеству гемоглобина и билирубина в крови.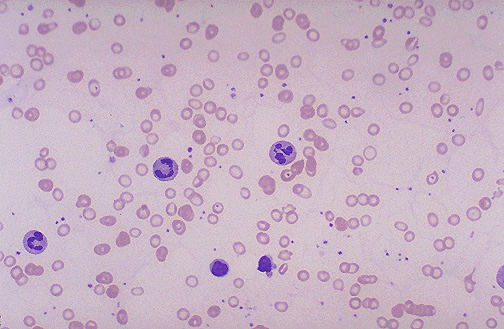 Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты.
Содержание железа в организме человека – 4 – 5 г или 0,000065% от массы тела. Из них 58% железа входит в состав гемоглобина. Железо может депонироваться (откладываться в запас) в печени, селезенке и костном мозгу. В то же самое время происходят физиологические потери железа с калом, мочой, потом, с менструацией и во время кормления грудью, поэтому необходимо включать в рацион питания железосодержащие продукты. Причина железорефрактерной анемии
Причина железорефрактерной анемии Что такое В12? Где содержится этот витамин?
Что такое В12? Где содержится этот витамин? Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12.
Витамин В9 –фолиевая кислота. В организм поступает с пищей – печень говяжья и куриная, салат, шпинат, спаржа, томаты, дрожжи, молоко, мясо. Витамин В9 способен накапливаться в печени. Таким образом, В9 – дефицитная анемия возникает вследствие недостатка фолиевой кислоты в организме человека. Недостаток фолиевой кислоты возможен при вскармливании детей козьим молоком, при длительной термической обработке пищи, у вегетарианцев, при недостаточном или несбалансированном питании. Также дефицит фолиевой кислоты наблюдается при повышенной потребности в ней у беременных, кормящих, недоношенных детей, подростков, раковых больных. К Вс – дефицитной анемии приводит наличие таких заболеваний как хроническая почечная недостаточность, заболевания печени. Возникновение дефицита фолиевой кислоты возможно и при нарушении всасывания данного витамина, что происходит при алкоголизме, приеме оральных контрацептивов и недостатке В12. Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.
Гипопластические анемии характеризуются уменьшением содержания в крови всех клеток (панцитопенией). Панцитопения связана с гибелью клеток – предшественниц в костном мозгу.