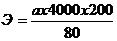Осмотическая резистентность эритроцитов — показатель устойчивости эритроцитов к осмотическому давлению. Стойкость ККТ определяется только путем диагностических мероприятий. Превышение или понижение нормы будет свидетельствовать о развитии определенного патологического процесса, а потому показатель следует всегда контролировать.
Осмотическая резистентность эритроцитов имеет свои минимальные и максимальные значения:
- максимум — воздействие гипотонического раствора натрия хлорида, когда в течение трех часов происходит гемолиз совершенно всех клеток;
- минимум — воздействие вещества другой концентрации, при которой происходит разрушение только минимально устойчивых клеток.
Следует отметить, что осмотическая резистентность эритроцитов будет зависеть от их возраста. Самая большая устойчивость у молодых ККТ как у самых плоских.
Определение осмотической резистентности эритроцитов осуществляется следующим образом:
- используется несколько стеклянных пробирок, в которые заливается раствор натрий хлорида разной концентрации — чаще всего от 0,7 до 22 %;
- в пробирки с раствором добавляют образцы крови, но только в одинаковом количестве;
- образцы помещают в условия комнатной температуры на 60 минут;
- по истечении срока пробирки с образцами центрифугируют;
- полученный после этого окрас жидкости будет указывать на показатели осмотической стойкости эритроцитов.
Если окрас жидкости розовый, это говорит о минимальной концентрации, а вот ярко-красный цвет будет говорить о максимальной. Норма для сферической резистентности эритроцита составляет 0,32–0,44 процента раствора натрия хлорида.
Норма для взрослого человека следующая:
- максимальная устойчивость — норма 0,32–0,34 %;
- минимальная осмотическая резистентность эритроцитов — 0,46–0,48 %.
Если норма не соблюдается, то есть показатели выше или ниже, это может свидетельствовать о развитии определенного патологического процесса в организме. Даже незначительное отклонение от нормы может указывать на довольно тяжелые патологические процессы в организме, поэтому осмотическое давление нужно обязательно контролировать.
Норма показателей может нарушаться вследствие определенных заболеваний как острого, так и хронического типа. Максимальные показатели резистентности могут наблюдаться в следующих случаях:
- атеросклероз;
- злокачественные новообразования в желудочно-кишечном тракте;
- талассемия;
- полицитемия, но только в некоторых случаях;
- спленэктомия;
- гемоглобинопатия;
- гемоглобиноз;
- застойная желтуха;
- врожденные заболевания крови;
- системные и аутоиммунные патологии.
Минимальная осмотическая резистентность может быть следствием таких патологических процессов:
- железодефицитная анемия;
- гемолитическая анемия у новорожденных;
- отравление тяжелыми металлами;
- обширная интоксикация организма;
- наследственная форма гемолитической анемии.
Небольшое отклонение от нормы может быть обусловлено такими заболеваниями:
Предрасполагающие факторы для снижения устойчивости ККТ:
- выработка шарообразных эритроцитов — генетическое отклонение;
- завершение жизненного цикла ККТ, что приводит к шарообразной форме;
- сердечно-сосудистые заболевания.
Определить, что именно привело к такому нарушению, можно только путем диагностических мероприятий. Поводом для начала обследования будет соответствующая клиническая картина.
Клиническая картина будет носить общий характер. Специфических симптомов, которые будут характерны только отклонению от нормы резистентности ККТ, нет.
Может присутствовать симптоматика такого характера:
- бледность кожных покровов;
- снижение веса без видимой причины;
- повышенная утомляемость и нарастающая слабость, что будет больше похоже на синдром хронической усталости;
- плохой аппетит;
- сонливость;
- обострение хронических заболеваний.
При наличии клинической картины нужно обращаться к врачу. Первоначально это врач общей практики, то есть терапевт. Далее обследованием занимаются гематолог и смежные специалисты.
Если диагностически будет установлено, что показатели ниже или выше допустимых, в обязательном порядке нужно проходить лечение, так как большая часть этиологических факторов представляет опасность не только для здоровья, но и для жизни пациента.
Лечение будет полностью основываться на первопричинной патологии. Терапевтические мероприятия могут быть как консервативными, так и радикальными. Прогноз носит исключительно индивидуальный характер.
источник
Анализ крови на осмотическую резистентность эритроцитов (ОРЭ) назначают нечасто. Это обследование обычно проходят при подозрении на гемолитическую анемию. Анализ помогает определить жизненный цикл и стойкость мембраны красных кровяных клеток. Такую диагностику обычно назначают врачи-гематологи. Исследование можно пройти далеко не во всех лабораториях. ОРЭ делают в специальных центрах по изучению болезней крови, а также в некоторых платных лабораториях («Вералаб», «Юнилаб» и т. д.) В ИНВИТРО осмотическую резистентность эритроцитов не определяют.
ОРЭ — это устойчивость красных кровяных клеток к разрушающим факторам: высокой или низкой температуре, химическим веществам, а также к механическому воздействию. Обычно в лабораторных экспериментах выявляют резистентность эритроцитов к хлористому натрию (NaCl). В ходе опытов важно выяснить, какая концентрация этого химиката вызывает разрушение эритроцитов. Это помогает выявить устойчивость мембран кровяных клеток к давлению и химическому воздействию соляного раствора (осмосу). Нормальные эритроциты могут сопротивляться. Они остаются прочными, а их оболочки — целыми. Это и называется осмотической резистентностью эритроцитов.
Иммунная система способна определять кровяные клетки, которые слабы и не могут сопротивляться воздействию. Со временем такие эритроциты выходят из организма.
Для определения осмотической резистентности эритроцитов проводят наблюдения за реакцией крови и раствора хлористого натрия. Эти ингредиенты смешивают в равных пропорциях.
Если концентрация раствора хлорида натрия равна 0,85%, то его называют изотоническим (или физраствором). При более низком содержании соли химикат называют гипотоническим, а при более высоком — гипертоническим. В изотоническом растворе эритроциты не разрушаются, в гипотоническом — набухают и распадаются, а в гипертоническом — сжимаются и погибают.
Метод определения осмотической резистентности эритроцитов связан с использованием гипотонических растворов концентрацией от 0,22 до 0,7%. В них помещают одинаковое количество крови. Эту смесь держат около часа при комнатной температуре, а затем подвергают обработке в центрифуге. При этом наблюдают за цветом жидкости. В начале процесса распада эритроцитов смесь становится слегка розовой, а при полном разрушении кровяных клеток — красной.
Таким образом, при определении осмотической резистентности эритроцитов получают 2 показателя: минимальный и максимальный.
Этот анализ помогает определить причину анемии. Кровь у пациента берут из вены. Специальной подготовки или соблюдения диеты перед анализом не требуется.
Норма показателя ОРЭ не зависит от возраста и пола пациента. Небольшое снижение этого значения наблюдается у пожилых людей, а повышение — у детей до 2 лет.
Нормой осмотической резистентности эритроцитов считается максимальный показатель — от 0,32 до 0,34% и минимальный — от 0,46 до 0,48%.
Это означает, что нормальные эритроциты проявляют наибольшую устойчивость в растворе концентрацией 0,32 — 0,34%, и наименьшую — в 0,43 — 0,48%.
В некоторых случаях ОРЭ может быть выше или ниже нормы. Повышение устойчивости мембран красных кровяных клеток наблюдается при гемолитической желтухе. При этом происходит повышение билирубина, и на оболочках эритроцитов откладывается холестерин. А также повышение ОРЭ бывает при аномалиях мембраны эритроцитов (сфероцитозе) и при нарушении строения гемоглобина (гемоглобинопатии).
Понижение осмотической резистентности эритроцитов встречается в следующих случаях:
- Болезни крови, удаление селезенки, массивные кровопотери.
- Сердечно-сосудистые патологии. При этом красные кровяные клетки по форме напоминают сферу и имеют плохую устойчивость к внешним воздействиям.
- Генетические аномалии, при которых эритроциты по форме похожи на шары. Такие измененные клетки имеют низкую резистентность.
- Большое количество старых эритроцитов, с высокой проницаемостью мембран. Это может быть связано с заболеваниями почек. Именно этот орган отвечает за вывод старых кровяных клеток из организма.
Однако нужно помнить, что при некоторых видах анемии показатель ОРЭ может оставаться нормальным. Например, при недостаточной активности фермента эритроцитов (Г-6-ФДГ) результат анализа будет в пределах допустимых границ. Но при этом у пациента наблюдаются все признаки анемии.
При исследовании проводят определение границ осмотической резистентности эритроцитов. Превышение или снижение этих показателей может означать патологию.
Верхняя граница ОРЭ в норме составляет не более 0,32%. Если резистентность становится меньше этого показателя, то это может свидетельствовать о следующих патологиях:
- гемоглобинопатия;
- желтуха застойного типа;
- операция удаления селезенки;
- талассемия;
- полицитемия;
- сильная потеря крови.
Если нижняя граница осмотической резистентности эритроцитов становится больше 0,48%, то это может быть при разных видах гемолитической анемии и после отравления свинцовыми соединениями.
При некоторых видах патологий крови границы ОРЭ могут расширяться. Так происходит при анемии, связанной с авитаминозом В12 и разрушении эритроцитов при остром гемолитическом кризе.
Осмотическая резистентность эритроцитов зависит от формы этих клеток. Резистентность значительно ниже у красных кровяных телец, имеющих выраженную сферическую или шарообразную форму. Такие клетки очень подвержены разрушению под воздействием различных факторов. Форма эритроцитов может быть наследственно обусловлена или являться следствием их старения.
На устойчивость эритроцитов влияет также их возраст. Самая высокая резистентность выявляется у молодых клеток, имеющих плоскую форму.
При отклонениях в анализе на ОРЭ всегда изменяется самочувствие пациентов. Больные жалуются на следующие симптомы:
- быструю утомляемость;
- общий упадок сил;
- сонливое состояние, постоянное желание прилечь;
- бледность кожи;
- ухудшение аппетита;
- беспричинное повышение температуры;
- похудение.
Такие проявления являются результатом кислородного голодания тканей. Обычно при отклонениях в анализе ОРЭ врач назначает дополнительные исследования, чтобы уточнить причину патологии. Если нарушения не являются следствием генетической болезни, то после курса терапии эритроциты приходят в норму.
При нарушениях резистентности эритроцитов больным назначают кортикостероидные гормоны, витамины (фолиевую кислоту), лекарства, содержащие железо. В тяжелых случаях, при частых обострениях заболевания делают хирургическую операцию по удалению селезенки.
Специфическая профилактика нарушений резистентности эритроцитов не разработана. Многие виды таких отклонений имеют наследственный характер. Таким пациентам требуется консультация генетика, чтобы больные не передали патологию своим детям. Нужны также профилактические меры, предотвращающие развитие гемолитического криза. Пациентам нужно обеспечивать условия для хорошего кроветворения. Необходим прием витаминов и препаратов для профилактики анемии, а также диета с достаточным содержанием железа. Это поможет избежать обострения гемолитических проявлений, а в некоторых случаях и улучшить результаты анализа ОРЭ.
источник
Красные кровяные тельца (или эритроциты) — наиболее многочисленные клетки крови. Особое устройство мембраны позволяет им захватывать молекулы кислорода в капиллярах легких и транспортировать его к тканям и органам. Однако при определенных патологиях структура оболочки эритроцитов становится менее устойчивой и легко разрушается. Такие изменения приводят к значительному уменьшению количества красных телец в крови и последующему нарушению кислородного обмена в тканях организма.
Способность мембран красных клеток крови противостоять разрушению под воздействием неблагоприятных факторов получила название резистентность. Особое значение при диагностике заболеваний имеет осмотическая резистентность (ОРЭ) — сохранение устойчивости оболочки клетки в условиях изменения концентрации растворенных солей в окружающей ее среде.
Клетки крови способны нормально функционировать в изотоническом растворе (содержание ионов NaCl не превышает 0,85%). Такая концентрация NaCl соответствует количеству ионов соли в сыворотке крови. Те растворы, которые содержат большее количество солей, называются гипертоническими, а меньшее — гипотонические. Мембраны клеток, помещенных в такие растворы, быстро разрушаются.
Эритроциты здорового человека способны выдерживать изменения осмотического давления, то есть обладать прочной оболочкой. Для определения стойкости мембран клеток крови используют следующую методику:
- В пробирки помещается раствор NaCl c разной степенью концентрации (начиная от самой большой — 0,7%, до наименьшей — 0,22%);
- В каждую пробирку добавляется небольшое количество крови (не более 0,02 мл);
- В течение следующего часа пробирки держат при температуре в 22-23°C;
- Полученные растворы центрифугируют и по цвету содержимого высчитывают примерное время начала разрушения клеток крови и момент их полного гемолиза;
Чуть розовый раствор свидетельствует о том, что эритроциты только начали разрушаться, тогда как ярко-красный цвет — знак того, что произошел полный распад клеток.
При помощи этого анализа определяют минимальную и максимальную осмотическую резистентность кровяных телец. Максимальная соответствует тому значению содержания NaCl, при котором происходит полное разрушение клеток крови. Минимальная же определяется тем количеством, при котором клетки разрушаются меньше всего.
Расчет значений осмотической резистентности позволит определить причину нехватки эритроцитов в крови пациента. Для проведения анализа кровь берется из вены и сразу же помещается в пробирку с антикоагулянтом, чтобы избежать ее свертывания. В каких-либо особых приготовлениях перед сдачей анализа нет необходимости — пациент может не менять привычный ему режим питания.
Для взрослого человека нормальными показателями являются следующие значения:
- минимальная резистентность — не выше 0,48%;
- максимальная — не ниже 0,32%
Следует помнить, что у маленьких детей показатели устойчивости значительно выше, чем у взрослых пациентов, в то время как у пожилых — немного ниже нормы.
Существует несколько факторов, которые могут повлиять на достоверность данных анализа:
- недавнее переливание крови;
- присутствие во взятом образце патогенных микроорганизмов, которые вызывают гемолиз клеток;
- некоторые заболевания, при которых количество зрелых эритроцитов в крови минимально (тяжелые формы анемии);
- наконец, человеческий фактор — неосторожное обращение с наполненными пробирками может привезти к преждевременному гемолизу;
Если вышеперечисленные причины отсутствовали, а результат анализа выходит за пределы нормы, то можно говорить о серьезном заболевании, за которым последуют значительные нарушения обмена веществ в организме.
ОРЭ менее 0,33% развивается в следующих ситуациях:
- значительные кровопотери;
- при талассемии (наследуемое заболевание, при котором нарушен синтез белков, входящих в состав гемоглобина);
- при спленэктомии (удалении части селезенки — органа, активно участвующем в процессах кроветворения);
- при полицитемии (нарушение функций кроветворных клеток костного мозга);
Резистентность более 0,48% связана с такими заболеваниями как:
- наследственная гемолитическая анемия (передающаяся по наследству патология, при которой организм активно разрушает свои же клетки крови);
- гемолитическая анемия новорожденных (диагностируется в течение первых дней жизни младенца. Может быть как наследственной, так и приобретенной);
- отравление солями тяжелых металлов;
Как правило, отклонения от нормальных показателей резистентности сигнализируют о сбоях в работе организма, причем чаще всего диагностируемые патологии носят наследственный характер.
Как правило, причиной снижения резистентности клеток становятся наследственные заболевания. Пациенты, столкнувшиеся с такой проблемой, могут обратиться к генетику, чтобы рассчитать возможность появления такого же заболевания у их детей. В остальных случаях профилактика снижения плотности мембраны клеток крови сводится к ведению здорового образа жизни, отсутствию вредных привычек, созданию наиболее благоприятных условий для процесса кроветворения.
Еще до проведения анализа, пациент может найти у себя признаки снижения устойчивости мембран кровяных телец. Вот основные проявления подобного отклонения:
- Сонливость;
- Угнетенное состояние;
- Значительное снижение массы тела;
- Анемичность слизистых оболочек;
- Повышенная температура тела;
- Отсутствие интереса к еде;
Перечисленные симптомы должны стать серьезным поводом для беспокойства. При их обнаружении следует немедленно записаться на прием к врачу и пройти полное обследование. Чем раньше будет поставлен диагноз, тем быстрее можно будет начать лечение и тем меньший вред будет нанесен организму.
Плотность мембраны зависит не только от возраста клеток, но и от их формы. Сформировавшийся эритроцит приобретает вид двояковогнутого диска, однако также могут встречаться и дегенеративные формы эритроцитов: сферические, звездчатые, полулунные, серповидные и т.д. Для разных заболеваний характерны свои изменения клеток крови. К примеру, при серповидно-клеточной анемии развиваются серповидные эритроциты, талассемия характеризуется появлением овальных клеток, большинство видов анемий проявляют себя появлением сфероцитов — эритроцитов сферической формы.
Нормальную устойчивость мембраны имеют лишь эритроциты в форме двояковогнутого диска. Красные клетки крови другой конфигурации менее жизнеспособны — их резистентность составляет 0,4-0,6% при обычных показателях в 0,32-0,48%. Кроме того, такие клетки, как правило, не способны качественно выполнять свои функции. Из патологических форм чаще всего встречаются овальные эритроциты. Такие клетки можно наблюдать не только при болезнях крови, но и у полностью здоровых людей, поскольку, чем старше становятся эритроциты, тем более округлыми они становятся.
Таким образом, наиболее устойчивыми клетками являются молодые, недавно сформировавшиеся эритроциты, отличающиеся наиболее выраженной дисковидной формой.
Методика расчета осмотической устойчивости нередко применяется при обнаружении гемоглобинопатии и прочих заболеваний крови и отличается эффективностью и простотой. Наиболее часто его применяют для обнаружения гемолитической анемии и онкогематологии (в том числе и у новорожденных).
источник
Нормальная максимальная осмотическая резистентность эритроцитов составляет 0,34— 0,32 %, а минимальная — 0,48—0,46 %.
Под осмотической резистентностью эритроцитов понимается их устойчивость по отношению к гипотоническим растворам натрия хлорида. Минимальная резистентность
эритроцитов определяется максимальной концентрацией гипотонического раствора натрия хлорида (в серии растворов с постепенно уменьшающейся концентрацией), при которой начинается гемолиз наименее устойчивых эритроцитов, находящихся в растворе в течение 3 ч; максимальная — минимальной концентрацией гипотонического раствора натрия хлорида, вызывающего в течение 3 ч гемолиз всех эритроцитов крови, помещенных в этот раствор.
Максимальная осмотическая резистентность ниже 0,32 % возможна после больших кро-вопотерь и спленэктомии, при гемоглобинозе С, застойных желтухах, а также в некоторых случаях полицитемии. Повышение осмотической резистентности эритроцитов ниже 0,32 % характерно для талассемии и гемоглобинопатии.
Минимальная осмотическая резистентность выше 0,48 % наблюдается при семейной гемолитической анемии, гемолитической анемии новорожденных и отравлении свинцом. Можно обнаружить небольшие изменения и при токсикозах, бронхопневмониях, туберкулезе, малярии, лейкемии, миелосклерозах, лимфогранулематозе, циррозе печени. Случаи расширения границ осмотической резистентности (одновременное понижение минимальной и повышение максимальной резистентности) наблюдаются в начале острого гемолитического криза и в остром периоде пернициозной анемии.
Кислотная резистентность эритроцитов (проба Хема)
В норме проба Хема отрицательная.
Кислотную резистентность определяют на основании различной кислотоустойчивости эритроцитов по отношению к НС1.
При анемии Маркиафавы и некоторых других гемолитических анемиях в подкисленной пробирке по сравнению с контролем обнаруживают ясный гемолиз.
В норме проба на серповидность эритроцитов отрицательная.
Пробу применяют для диагностики гемоглобинопатии. Гемоглобин S при понижении парциального давления кислорода кристаллизуется в форме тактоидов и придает эритроцитам форму серпа. Среди гемоглобинопатии чаще всего встречается серповидно-клеточная анемия, поэтому выявление эритроцитов в виде серпа позволяет установить этот вид анемии.
Эритроцитометрия — измерение диаметра эритроцитов. В процентном отношении диаметры эритроцитов у здоровых людей распределяются следующим образом: 5 мкм — 0,4 % всех эритроцитов; 6 мкм — 4 %; 7 мкм — 39 %; 8 мкм — 54 %; 9 мкм — 2,5 %. Графическое изображение соотношения содержания в крови эритроцитов с различными диаметрами называют эритроцитометрической кривой Прайс-Джонса, где по оси абсцисс откладывают величину диаметра эритроцитов (мкм), а по оси ординат — проценты эритроцитов соответствующей величины. В норме эритроцитометрическая кривая имеет правильную, с довольно узким основанием, почти симметричную форму (рис. 1.1).
Результаты эритроцитометрии важны для уточнения характера анемии. При железоде-фицитной анемии, как правило, возможны микроцитоз эритроцитов до 30—50 % всех эритроцитов и соответственно сдвиг эритроцитометрической кривой влево. Увеличение процента микроцитов наблюдается также при наследственном микросфероцитозе, талассемии, свинцовом отравлении. При микроцитозе и сфероцитозе эритроцитометрическая кривая растянута и неправильна, сдвинута влево, в сторону меньших диаметров.
Увеличение числа макроцитов является признаком макроцитарной анемии, наблюдающейся при В,2-дефицитных и фолиеводефицитных состояниях, при которых их содержание может достигать 50 % и более, при этом в небольшом числе (1—3 %) находят и мегалоциты (эритроциты с диаметром 12 мкм и более). При этих формах анемии эритроцитометрическая кривая имеет неправильную пологую форму с широким основанием и сдвинута вправо, т.е. в сторону больших диаметров. Макроцитоз эритроцитов может наблюдаться независимо от анемии при алкоголизме, диффузных поражениях печени.
1 2 3 4 5 6 7 8 9 10 11 12 13 14 Рис. 1.1. Эритроцитометрическая кривая Прайс-Джонса в норме.
Гистограмма распределения эритроцитов по объему, получаемая с помощью современных гематологических анализаторов, по сравнению с такой же по диаметру (кривая Прайс-Джонса) имеет ряд особенностей [Титов В.Н., Наумова И.Н., 1995]. Коэффициент вариации в 3 раза выше при определении объема, чем при определении диаметра. Если кривая распределения диаметров эритроцитов симметрична, то распределение клеток по объему будет иметь сдвиг вправо, пропорционально коэффициенту вариации. Если кривая распределения диаметров полимодальна (имеет несколько пиков), то гистограмма распределения эритроцитов по объему может оказаться унимодальной (одновариантной), что является недостатком автоматизированного метода.
источник
Вязкость крови
Возникает в результате сил трения между частицами крови, образующихся при ее движении. Величина вязкости зависит от количества и объема эритроцитов, тромбоцитов, лейкоцитов, концентрации белков, органических и неорганических веществ.
Основой определения вязкости крови является то, что скорость продвижения жидкости в одинаковых капиллярах при одной и той же температуре находится в зависимости только от силы внутреннего трения, т. е. от вязкости этой жидкости.
Вязкость дистиллированной воды составляет 1, по отношению к этой величине и определяется вязкость крови. В норме у мужчин вязкость крови – 4,3–5,3, у женщин – 3,9–4,9. Вязкость плазмы у женщин – 1,7–2,0, у мужчин – 1,9–2,3.
Исследование вязкости крови осуществляется при помощи вискозиметра, состоящего из двух одинаковых стеклянных капилляров, на поверхности которых имеются деления от 0 до 10.
Вязкость крови уменьшается при анемии, злокачественном малокровии.
Вязкость повышена при лейкемии, желтухе, пневмонии, полицитемии, нарушении сердечной деятельности.
Скорость оседания эритроцитов (СОЭ)
В пробирке с кровью, лишенной возможности свертываться, эритроциты медленно оседают на дно за счет того, что удельная масса эритроцитов (1096) выше удельной массы плазмы (1027). В норме СОЭ у здорового мужчины за первый час составляет 1–10 мм, у женщины – 2–15 мм, у новорожденного – 0–2 мм. СОЭ зависит от белкового состава плазмы крови: снижается при увеличении содержания в плазме альбумина и повышается при увеличении концентраций фибриногена, гаптоглобина, церулоплазмина и α– и β‑липопротеинов, а также парапротеинов – иммуноглобулинов, образующихся в избытке при некоторых патологических состояниях. СОЭ повышается при значительном уменьшении количества эритроцитов (гематокрита), так как при этом снижается вязкость крови; при увеличении гематокрита СОЭ снижается. При изменении формы эритроцитов (пойкилоцитозе) СОЭ снижается вследствие подавления агрегации эритроцитов. В физиологических условиях СОЭ ускоряется во время менструации, при беременности и после родов. СОЭ не является показателем, специфическим для определенного заболевания, его увеличение отмечается при наличии в организме инфекционно‑воспалительного процесса, системной воспалительной реакции, онкологического процесса. Замедление СОЭ наблюдается при эритремии, вторичных эритроцитозах, при значительном сгущении крови.
Осмотическую резистентность эритроцитов исследуют с использованием гипотонических растворов хлорида натрия. Нормальные величины: у здоровых – начало гемолиза при концентрации хлорида натрия 0,50–0,45 %, полный гемолиз – при концентрации 0,40–0,35 %. Понижение резистентности эритроцитов (появление гемолиза при более высоких, чем в норме, концентрациях хлорида натрия – 0,7–0,75 %) наблюдается при гемолитических несфероцитарных анемиях; наследственном микросфероцитозе. Повышение резистентности эритроцитов наблюдается при талассемии, гемоглобинопатиях.
Минимальная устойчивость эритроцитов выявляется наибольшей концентрацией раствора хлорида натрия, при которой начинают разрушаться менее устойчивые эритроциты, в течение трех часов пребывающие в растворе. Максимальная резистентность – наименьшей концентрацией гипотонического раствора, при которой в течение 3 ч разрушаются все эритроциты. У детей младше 2 лет минимальная устойчивость эритроцитов больше, чем у старших. У пожилых людей отмечаются цифры чуть ниже нормы (субнормальные).
Наибольшая осмотическая резистентность эритроцитов (ниже 0,32 %) наблюдается при большой потере крови, удалении селезенки (спленоэктомия), застойных желтухах, гемоглобинопатиях.
Наименьшая осмотическая устойчивость эритроцитов (выше 0,48 %) возможна при семейной гемолитической анемии, гемолитической анемии у новорожденных, свинцовых отравлениях. Небольшие изменения показателей могут иметь место при бронхопневмониях, токсикозах, малярии, туберкулезе, лимфогранулематозе, лейкемии, циррозе печени. Иногда регистрируются случаи снижения минимальной и увеличение максимальной резистентности (расширение границ осмотической устойчивости). Такое может быть в острой стадии пернициозной анемии и в начале гемолитического криза.
Для определения границ осмотической резистентности эритроцитов используют раствор натрия хлорида в уменьшающейся концентрации, которые затем смешивают с кровью. Концентрация того раствора, где начинается гемолиз (разрушение) эритроцитов (раствор окрашивается в розовый цвет над осевшими на дно эритроцитами), – это верхняя граница устойчивости. Нижняя граница резистентности эритроцитов – это та концентрация хлорида натрия, в которой разрушаются все эритроциты и раствор становится прозрачным.
Существует еще один метод определения осмотической резистентности эритроцитов – фотоколориметрический (с помощью специального аппарата – фотоколориметра).
Дата добавления: 2014-11-20 ; Просмотров: 993 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
Определением скорости оседания эритроцитов широко пользуются в клинике с диагностической целью. В норме СОЭ составляет в среднем 4-10 мм/ч (у новорожденных 2 мм/ч). Величина СОЭ меняется при многих заболеваниях и зависит от следующих факторов:
1. От количественного и качественного состава белков плазмы крови. Например, при воспалительных процессах и некоторых инфекционных заболеваниях увеличивается в крови содержание крупнодисперсных белков (глобулинов и фибриногена), что ведет к ускорению СОЭ.
В нормальной среде отрицательно заряженные эритроциты взаимно отталкиваются. Слабо заряженные крупнодисперсные белки, адсорбируясь на эритроцитах, уменьшают их поверхностный заряд, эритроциты начинают сближаться и быстрее оседают.
2. От вязкости крови и количества эритроцитов. Ускорение СОЭ отмечается при уменьшении вязкости крови (гидремия) снижении числа эритроцитов (анемия). С увеличением вязкости крови (обезвоживание) и количества эритроцитов (эритремия) СОЭ замедляется.
3. От содержания холестерина и лецитина в крови. Отмечено, что холестерин ускоряет СОЭ, так как адсорбируется на эритроцитах. Лецитин замедляет СОЭ.
4. От изменения относительной плотности эритроцитов. Например, при введении в кровь гипертонического раствора эритроциты теряют воду, сморщиваются, их относительная плотность увеличивается, СОЭ ускоряется. При гиперкапнии (асфиксия, сердечная декомпенсация) эритроциты, напротив, вбирают воду, их относительная плотность уменьшается, СОЭ замедляется.
Изменения осмотической резистентности эритроцитов
В изотоническом растворе (0,85% NаСl) эритроциты сохраняют свой объем, а в гипертоническом растворе теряют воду, сморщиваются. В гипотоническом растворе они поглощают воду, их объем увеличивается до определенного «критического» уровня, повышение которого сопровождается гемолизом, выходом гемоглобина в кровь. Если объем эритроцитов в изотоническом растворе принять за 100%, то критический объем эритроцитов человека составит 146%, кролика — 137%, овцы — 126%.
Осмотической резистентностью эритроцитов называют устойчивость их в гипотонических растворах. Минимальную осмотическую резистентность определяют по гипотоническому раствору хлористого натрия такой концентрации, при которой гемолизируются только наименее устойчивые эритроциты (в норме 0,44—0,46% раствора NаCl). Максимальная осмотическая резистентность соответствует раствору хлористого натрия, в котором полностью гемолизируются все эритроциты (в норме 0,32—0,28% раствора NaCl).
Осмотическая стойкость эритроцитов зависит от степени их зрелости, формы и от изменения состава плазмы. Форма эритроцитов характеризуется соотношением между его толщиной и диаметром. Это соотношение называется индексом сферичности и соответствует в норме 0,27— 0,28. Индекс сферичности может значительно превышать норму, например при наследственной сфероцитарной анемии, когда наследуются шаровидные эритроциты. При этом заболеваний отмечается резкое снижение осмотической стойкости эритроцитов, минимальная резистентность их равняется 0,6—0,7% NaCl. Сфероидную форму приобретают эритроциты, завершающие жизненный цикл. Более осмотически стойкими являются эритроциты, поступившие в кровоток из костного мозга, в особенности менее зрелые клетки (ретикулоциты, полихроматофилы), которые имеют уплощенную дисковидную форму и малый индекс сферичности
Виды и механизмы развития геморрагических диатезов. Патогенез изменений в органах полости рта при тромбоцитопениях и тромбоцитопатиях.
Диатезы геморрагические — это формы нарушений, характеризующиеся склонностью к кровоточивости.
Болезнь Вшлебранда — один из наиболее частых наследственных геморрагических диатезов.
Диспротромбш — геморрагические диатезы, обусловленные наследственным дефицитом некоторых факторов свертывания крови.
Дисфибриногенемии — наследственные молекулярные аномалии фибриногена. Они характеризуются либо замедлением свертывания этого белка под влиянием тромбина и тромбиноподобных ферментов, либо неправильным его превращением.
Геморрагические диатезы, обусловленные патологией тромбоцитов: тромбоцитопении и тромбоцитопатии.
Тромбоцитопеническая пурпура — сборная группа заболеваний, объединяемая по принципу единого механизма тромбоцитопении; укорочения жизни тромбоцитов, вызванного наличием антител к тромбоцитам или иным механизмом их разрушения.
Спленогенные тромбоцитопении — тромбоцитопении, обусловленные увеличением и повышением функции селезенки.
Тромбоцитопатии — заболевания, в основе которых лежит врожденная (чаще всего наследственная) или приобретенная качественная неполноценность тромбоцитов. При ряде тромбоцитопатии возможна непостоянная вторичная тромбоцитопения (обычно умеренная), обусловленная укорочением продолжительности жизни дефектных тромбоцитов.
Различают наследственные (семейные) формы с многолетней, начинающейся с детского возраста кровоточивостью и приобретенные формы, в большинстве своем вторичные (симптоматические). Большая часть наследственных форм связана с нарушениями строения и функций клеток крови либо с дефицитом или дефектом факторов свертывания крови, а также фактора Виллебранда, реже — с неполноценностью мелких кровеносных сосудов (телеангиэктазия, болезнь Ослера-Рандю).
Большинство приобретенных форм кровоточивости связано с синдромом-ДВС, иммунными поражениями сосудистой стенки (васкулит Шенлейна-Геноха, эритемы) и тромбоцитов (большинство тромбоцитопении), с нарушениями нормального кроветворения, токсико-инфекционным поражением кровеносных сосудов (геморрагические лихорадки, сыпной тиф и др.), заболеваниями печени и желтухой (ведущими к нарушению образования в печеночных клетках факторов свертывания крови), воздействием лекарственных препаратов, нарушающих свертывание крови (дезагреганты, антикоагулянты, фибринолитики), либо провоцирующих иммунные нарушения — тромбоцитопению, васкулиты. При многих перечисленных заболеваниях нарушения свертывания крови носят смешанный характер и резко усиливаются в связи с вторичным развитием синдрома-ДВС, чаще всего в связи с инфекционными, иммунными, разрушающими или опухолевыми (включая лейкозы) процессами.
По механизму развития различают следующие группы геморрагических диатезов:
• обусловленные нарушениями свертываемости крови;
• обусловленные нарушением тромбоцитарно-сосудистого свертывания (тромбоцитопении, тромбоцитопатии);
• обусловленные нарушениями свертываемости крови и механизма остановки кровотечения с помощью тромбоцитов (болезнь Виллебранда, ДВС-синдром, при белковых нарушениях, лучевой болезни и др.);
• обусловленные первичным поражением сосудистой стенки (наследственная телеангиэктазия Ослера-Рандю, гемангиомы, геморрагический васкулит Шенлейна-Геноха, эритемы, геморрагические лихорадки, гиповитаминозы С и В и др.).
В особую группу включают различные формы так называемой невротической, или имитационной, кровоточивости, вызываемой у себя самими больными вследствие расстройства психики. Ими наносятся механические повреждения ткани (нащипывание или насасывание синяков, травмирование слизистых оболочек и т. д.), тайно принимаются лекарственные препараты геморрагического действия (чаще всего антикоагулянтов непрямого действия — кумаринов, фенилина и др.), самоистязанием или садизмом на эротической почве и т. д.
Реже встречаются близкие к ДВС-синдрому заболевания, протекающие с выраженной лихорадкой, — тромботическая тромбоцито-пеническая пурпура (болезнь Мошкович) и гемолитико-уремический синдром.
При незначительной травматизации возникают кровоизлияния в кожу и подкожную клетчатку, носовые и маточные кровотечения, часто ошибочно расцениваемые как дисфункциональные, реже — желудочно-кишечные, внутричерепные. Кровоизлияния в полость суставов редки и поражают лишь единичные суставы, не ведут к глубоким нарушениям функции опорно-двигательного аппарата.
109. причины и механизмы развития предтромботических состояний. Понятие о тромбофилии.(этот вопрос не оч…все что нашла)
Тромбофилия — это патологическое состояние, характеризующееся нарушением системы свёртываемости крови при которой увеличивается риск развития тромбоза.
Тромботический синдром, или тромбофилия (от гр. thrombos — ком, сгусток, phileo — люблю) — состояние, характеризующееся чрезмерной (неадекватной) коагуляцией крови и тромбообразованием, ведущими к ишемии тканей и органов.
Причины тромботического синдрома • Повреждение стенок сосудов и сердца (например, при их механической травме, атерогенезе, васкулитах, ангиопатиях у пациентов с СД). • Патология форменных элементов крови (например, тромбоцитопатии, гемолиз эритроцитов, чрезмерное повышение адгезии и агрегации тромбоцитов и эритроцитов). • Патология факторов системы гемостаза. — Абсолютное или относительное преобладание эффектов прокоагулянтных факторов. — Недостаточность антикоагулянтных и фибринолитических факторов (например, при системном атеросклерозе, СД, гипертонической болезни, эн-дотоксинемиях, шоковых состояниях). Механизмы тромботического синдрома.. • Чрезмерная активация прокоагулянтов и проагрегантов. Наиболее частые причины. — Гиперлипопротеинемии. Липопротеины активируют фактор Хагемана (фактор свёртывания XII) и стимулируют активность протромбиназы. — Повышенный уровень антифосфолипидных AT (IgG, IgM) при анти-фосфолипидном синдроме. AT к анионным фосфолипидам стимулируют реакцию высвобождения из тромбоцитов, эндотелиоцитов, кардиомиоцитов и некоторых других клеток прокоагулянтов и их последующую активацию. Такой механизм тромбообразования выявляется, например, при СКВ и ишемической болезни сердца (ИБС). — Массированные травмы мягких тканей (например, при механическом повреждении органов, тканей, конечностей, синдроме длительного раздавливания), ожоги большой площади, шоковые состояния, сепсис. Основные механизмы гиперкоагуляции и тромботического синдрома • Увеличение концентрации в крови прокоагулянтов и проагрегантов (фибриногена, протромбина, акцелерина, проконвертина, тромбина и др.). + Наиболее частые причины. — Гиперкатехоламинемия. Катехоламины активируют процесс синтеза фибриногена (например, при патогенном стрессе или феохромоцитоме). — Гиперкортицизм (с гиперпродукцией глюкокортикоидов). Глюкокортикоиды стимулируют образование протромбина, проакцелерина, фибриногена. — Атеросклеротическое поражение стенок артерий. Потенцирует синтез фибриногена, протромбина, фактора Хагемана, антигемофилических глобулинов и др. — Септицемия. Стимулирует гиперпродукцию тканевого тромбопластина, + Последствия чрезмерной активации и/или увеличения в крови прокоагулянтов и проагрегантов: гиперкоагуляция белков крови, адгезия, агрегация и активация форменных элементов крови, образование единичных тромбов, генерализованный тромбоз (наблюдается при ДВС-синдроме). • Снижение содержания и/или угнетение активности антикоагулянтов и антиагрегантов. Наиболее частые причины. — Наследственный дефицит антитромбина. Характеризуется снижением синтеза антитромбина III, а также его сродства к гепарину. — Печёночная, почечная или панкреатическая недостаточность. Все эти состояния обусловливают снижение синтеза гепатоцитами антитромбина III. — Гиперлипопротеинемии. Обусловливают снижение уровня гепарина в крови (за счёт его адсорбции на поверхности форменных элементов крови и иммунных комплексов, например при СКВ или пурпуре Шёнляйна— Геноха). — Наследственная или приобретённая недостаточность протеинов С и S. Вторичный (приобретённый) дефицит этих белков наблюдается при печёночной недостаточности, СД, лейкозах, массивных травмах, респираторном дистресс-синдроме взрослых. • Уменьшение уровня и/или подавление активности фибринолитических агентов. Наиболее частые причины. — Подавление синтеза и выделение клетками в кровь активатора плазминогена. Наблюдается у пациентов с атеросклерозом, инфарктом миокарда, ревматоидным артритом). — Наследственная или приобретённая гиперпродукция антиплазминов. — Снижение продукции фактора XII (например, при васкулитах или ДВС-синдроме). Именно это послужило причиной смерти больного тромбофилией по фамилии Хагеман (его именем назван фактор XII).
Дата добавления: 2019-02-12 ; просмотров: 70 ; ЗАКАЗАТЬ РАБОТУ
источник
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 6 |
3. Дальнейший рост и прогрессия опухоли. Прогессия – нарастание различных признаков злокачественности независимо друг от друга. Предполагаемые механизмы те же, что и в 2-ой стадии.
Наличие причины и даже включение механизмов канцерогенеза сами по себе недостаточны для возникновения и развития опухолей: необходимо снижение антибластомной (противоопухолевой резистентности). Без этого условия, как правило, невозможно развитие опухоли.
Механизмы противоопухолевой резистентности условно разделены на три вида: антиканцерогенные – направлены на взаимодействие канцерогена с клетками; антитранформационные – направлены на предотвращение трансформации нормальной клетки в опухолевую; антицеллюлярные – адресованы этапу превращения отдельных опухолевых клеток в клеточную колонию – опухоль.
Цель: Изучение методов перевивки опухолей и свойств опухолевых клеток.
Опыт 1. Ознакомление с методом воспроизведения опухолей путем перевивки малигнизированной ткани.
Методика: Мышь с саркомой «Рокера» наркотизировать эфиром, выстричь шерсть над опухолью. Кожу смазать йодом, сделать разрез, извлечь кусочек опухоли. В стерильных условиях кусочек опухоли промыть физиологическим раствором в чашке Петри и тщательно измельчить ножницами. Полученную тканевую взвесь в небольшом количестве физиологического раствора набрать в шприц и ввести 0,3—0,5 мл под кожу интактной мыши с соблюдением асептики. Через несколько дней после трансплантации под кожей появляется уплотнение ткани, а спустя 2—3 недели опухоль достигает больших размеров, развивается общая интоксикация и животное погибает.
Объясните, какие свойства опухолевых клеток обеспечивают развитие саркомы у мыши-реципиента.
Опыт 2. Ознакомление с методом перевивки опухоли взвесью клеток.
Методика: Мышь с асцитной формой карциномы Эрлиха наркотизировать эфиром. Работу проводить в стерильных условиях. С помощью шприца из брюшной полости отсосать 0,2 мл асцитической жидкости с раковыми клетками и развести ее в 1 мл физиологического раствора. Ввести 0,2 мл разбавленной асцитической жидкости в асептических условиях внутрибрюшинно интактной мыши. У реципиента примерно через 10 дней накапливается асцитическая жидкость, а через 3 недели развивается общая интоксикация и животное погибает.
Объясните, какие свойства опухолевых клеток обеспечивают развитие карциномы у мыши-реципиента.
Раздел: Типовые патологические процессы.
Тема: Экстремальные состояния. Патогенез травматического шока. Кома. Коллапс.
Шок (удар, сотрясение) — тяжелый патологический процесс, сопровождающийся истощением жизненно важных функций организма и приводящий его на грань жизни и смерти из-за критического уменьшения капиллярного кровообращения в пораженных органах. Вследствие «шокогенного» воздействия организм или погибает или в результате сложного комплекса защитно-приспособительных реакций восстанавливает свои жизненные функции и выживает.
Шок — это длительное патологическое проявление системного характера, которое возникает в тот момент, когда первичное поражение по силе или по времени действия переходит «шоковый порог».
Упрощенная, обобщающая схема патофизиологии шокового состояния может быть представлена в следующем виде.
Шокогенные факторы обусловливают информацию, которая действует на гипоталамо-гипофизарную область, результатом усиления ее функции является повышение концентрации адреналина, норадреналина, кортизола в плазме. Эти химические факторы управляют вторичным распределением жидкостей и внутриклеточных ферментов. Возникает вазоконстрикция, которая является генерализованной, но неравномерной по интенсивности и длительности на различных территориях. Эта гемодинамическая реакция получила название «централизация кровообращения».
Начальный спазм возникает только там, где имеются мышечные клетки. Спазм обходит коронарную, гипофизо/тиреоидную, надпочечниковую и диафрагмальную области (сосуды этих областей не имеют альфа-адренергических рецепторов), но жертвует почками, кожными покровами, портальной областью и скелетной мускулатурой (в сосудах этих областей имеются альфа-адренорецепторы), следствием вазоконстрикции артериол является снижение гидростатического давления в области микроциркуляции.
В дальнейшем при повышении ацидоза снимается спазм в микроциркуляции в области прекапиллярных сфинктеров. Одновременно с этим начинаются метаболические расстройства.
При шоке позднее расслабление прекапиллярных сфинктеров благодаря ацидозу является ловушкой, поскольку открывается огромный шлюз. который со стороны венул остается закрытым и в котором задерживается количество жидкости, превышающей в 3-4 раза существующее в физиологических условиях. И это происходит в полный разгар гповолемии при существовании послекапиллярно-венулярной задержке.
Застой и ацидоз подготавливают почву для возникновения внутри сосудистого свертывания крови. Возникает тромбоз и дальнейшее нарушение микроциркуляции.
Коллапс – общее, быстро развивающееся состояние, возникающее в результате значительного несоответствия ОЦК ёмкости сосудистого русла. Характеризуется недостаточностью кровообращения, первично циркуляторной гипоксией, расстройством функций тканей, органов и систем.
Кома — состояние, характеризующееся глубокой потерей сознания в связи с резко выраженной степенью патологического торможения центральной нервной системы, отсутствием рефлексов на внешние раздражения и расстройством регуляции жизненно важных функций организма. Ведущим в патогенезе становится поражение центральной нервной системы. Ведущими патогенетическими звеньями являются гипоксия мозга, ацидоз, нарушения баланса электролитов и образования и выделения медиаторов в синапсах ЦНС. По происхождению различают: неврологические комы в связи с первичным поражением ЦНС, развивающиеся при инсультах, черепно-мозговых травмах, воспалениях и опухолях головного мозга и его оболочек; эндокринологические комы, возникающие как при недостаточности некоторых желез внутренней секреции (диабетическая, гипокортикоидная, гипопитуитарная, гипотиреоидная комы), так и при их гиперфункции (тиреотоксическая, гипогликемическая); токсические комы, возникающие при эндогенных (уремия, печёночная недостаточность, токсикоинфекции, панкреатит) и экзогенных (отравления алкоголем, барбитуратами, фосфорорганическими и другими соединениями) интоксикациях; комы, обусловленные нарушениями газообмена при различных видах гипоксии.
Цель занятия: изучить этиологию и патогенез экстремальных состояний – шок, кома, коллапс.
Опыт: Воспроизведение анафилактического шока у крысы.
Методика: За две недели до опыта провести сенсибилизацию крысы внутрибрюшинным введением лошадиной сыворотки (по 0.1-0.2 мл в течение 3 дней).
После фиксации наркотизированного нембуталом животного (в/м раствор нембутала, 40 мг/кг) посчитать частоту дыхания. Внутрибрюшинно ввести разрешающую дозу лошадиной сыворотки в количестве 0.7-1,0 мл, которая приводит к развитию шока. Через 15 мин от введения разрешающей дозы лошадиной сыворотки отметить изменения в поведении животного, характере дыхания (посчитать частоту дыхания)
На основании полученных данных сделать вывод о возможности экспериментального воспроизведения анафилактического шока, о механизмах его развития.
1. Воспаление. Этиология. Внешние признаки. Классификация воспаления.
2. Альтерация в очаге воспаления.
3. Медиаторы воспаления. Провоспалительные цитокины.
4. Эмиграция лейкоцитов в очаг воспаления. Роль медиаторов воспаления, молекул адгезии (селектинов, интегринов), хемоаттрактантов (фрагмента С5а, лейкотриена В4, фактора активации тромбоцитов, МСР-1, лимфотоксин).
5. Фагоцитоз. Бактерицидные механизмы.
6. Отек и экксудация при воспалении. Медиаторы воспаления.
7. Нарушения обмена веществ в очаге воспаления.
8. Пролиферативная фаза воспаления. Биологическая сущность воспалительного процесса.
9. Патогенез хронического воспаления.
10. Механизмы терморегуляции. Основные виды нарушений терморегуляции.
11. Определение понятия «лихорадка». Инфекционная и неинфекционная лихорадка. Основные отличия лихорадки от перегревания.
12. Виды пирогенов, их источники в организме.
13. . Участие первичных и вторичных пирогенов в патогенезе лихорадки. Роль интерлейкинов.
14. Стадии лихорадки. Механизмы терморегуляции на разных стадиях лихорадки. Механизмы антипиреза.
15. Нарушение функционального состояния важнейших систем жизнедеятельности организма при лихорадке.
16. . Биологическое значение лихорадки.
17. Понятие о пиротерапии. Принципы жаропонижающей терапии.
18. Механизмы клеточного деления. Патофизиология клеточного деления.
19. Понятие «опухолевый» рост. Этиология опухолей. Основные свойства кацерогеных веществ.
20. Классификация опухолей. Отличия злокачественных и доброкачественных опухолей. Свойства опухолевых клеток in vitro.
21. Многостадийность кацерогенеза. Особенности патогенеза стадий опухолевого процесса.
22. Понятие о протоонкогенах, онокогенах, онкобелках. Роль онкобелков в инициации опухолевого роста.
23. Функции генов-супрессоров клеточного деления. Роль генов-супрессоров в инициации опухолевого роста.
24. Роль в канцерогенезе генов, регулирующих репарацию ДНК и апоптоз.
25. Взаимоотношение опухоли и организма. Паранеопластический синдром. Механизмы противоопухолевой резистентности организма.
26. Механизмы резистентности опухоли к терапевтическим воздействиям.
27. Терминальные состояния. Клиническая и биологическая смерть.
28. Шок. Этиология шока. Значение исходного состояния и реактивности организма для исхода шока.
29. Общий патогенез шока. Стадии шока.
30. Изменение микроциркуляции, гемолимфоциркуляции при шоке.
31. Нарушение обмена веществ и функций жизненно важных органов при шоке.
32. Характерные особенности травматического шока.
33. .Кома. Виды коматозных состояний. Этиология и патогенез комы. Стадии комы.
34. Этиология и патогенез коллапса, обморока. Их отличие от шока.
Раздел: Типовые патологические процессы.
Тема: Расстройства водно-электролитного обмена. Отёки.
Вода в организме находится в разных секторах или компартментах.
Внутриклеточный сектор составляет около 55% всей воды и представлен связанной, свободной и адгезированной водой.
Внеклеточный сектор составляет около 45% всей воды организма и представлен плазменной, трансцеллюлярной, межклеточной и кристаллизационной водой.
Водный баланс – это равновесие между поступившей в организм (2,5 л/сут) и выделенной из организма водой (2,5 л/сут). Водный баланс зависит от трех процессов:
1) поступления в организм с пищей и водой,
2) образования воды при обмене веществ (эндогенная вода),
3) выведение воды из организма.
Различают положительный (поступление воды превышает ее выведение), отрицательный (выведение воды преобладает над ее поступлением) и нейтральный (количество поступившей и выводимой воды совпадает) водный баланс.
Типовые формы нарушения водного баланса называют дисгидриями.
Дисгидрии классифицируют с учетом трех критериев:
Первый критерий – содержание жидкости в организме. По содержанию жидкости в организме различают две формы дисгидрии:
1) гипогидратация (дегидратация) – уменьшение общего содержания воды в организме,
2) гипергидрадация – увеличение общего содержания воды в организме.
Второй критерий – осмоляльность внеклеточной жидкости. В зависимости от осмоляльности внеклеточной жидкости различают:
1) гипоосмолярную (осмоляльность плазмы крови менее 280 мОсм/кг),
2) гиперосмолярную (осмоляльность плазмы крови более 300 мОсм/кг),
3) изоосмолярную форму дисгидрии.
Третий критерий – сектор организма, в котором преимущественно нарушается водный обмен. Согласно этому критерию выделяют:
3) смешанную формы дисгидрии.
Для характеристики нарушений водного обмена используют термины:
1. Гиповолемия – уменьшение объема внеклеточной жидкости.
2. Гиперволемия – увеличение объема внеклеточной жидкости (интерстициальной и внутрисосудистой), как правило, сопровождающееся развитием отеков. Отеки – избыточное накопление жидкости в интерстициальном пространстве из-за нарушения обмена жидкости в системе капилляры-ткани.
Цель: Познакомиться с патогенетическими факторами развития типовых форм нарушения водного баланса.
Опыт 1. Изучение роли гидростатического давления в развитии скорости фильтрации.
Методика: В вертикально установленные стеклянные трубки (имитация гидростатического давления), нижняя часть которых закрыта полупроницаемым коллоидным мешочком (имитация биологической мембраны), до метки 20 и 40 налить дистиллированную воду. В мерные сосуды собрать профильтровавшуюся жидкость, отмечая объем жидкости, которая профильтровалась от меток 20 и 40 в течение 1 минуты.
Запротоколировать результаты. На основании полученных данных сделать вывод о роли гидростатического давления в развитии скорости фильтрации.
Опыт 2. Изучение роли осмотического давления в развитии дисгидрии у лягушек.
Методика: Подопытной лягушке в спинной лимфатический мешок ввести 0,2 мл 20% раствора поваренной соли, а контрольной — ту же дозу физиологического раствора. Взвесить обеих лягушек и поместить в сосуд с водой. Через 20 мин вновь взвесить.
Запротоколировать результаты. На основании полученных данных сделать вывод о роли повышения осмотического давления в развитии дисгидрии.
Опыт 3. Изучение роли РН в связывании воды гидролизатом коллагена.
Методика: Кусочки желатина (гидролизат коллагена) одного веса и размера поместить в три пробирки, наполненные 0,1 н раствором соляной кислоты, 0,1 н раствором едкого натрия и физиологическим раствором. Через 20 минут извлечь все три кусочка одновременно, высушить фильтровальной бумагой и взвесить.
Запротоколировать результаты. На основании полученных данных сделать вывод о роли рН в связывании воды гидролизатом коллагена.
Часть 2. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ
Раздел: Патофизиология органов и систем
Тема: Нарушение системы эритроцитов. Эритроцитоз. Анемии.
Эритрон – это морфо-функциональная единица системы крови, которая включает в себя органы эритропоэза, эритродиэреза, пул циркулирующих в крови эритроцитов, и механизмы регуляции между эритропоэзом и эритродиэрезом.
Анемия — патологический процесс, характеризующийся уменьшением содержания гемоглобина и (или) количества эритроцитов в единице объема крови в сочетании с изменением их качества.
Патогенетическая классификация анемий:
1. Анемии вследствие потери крови (постгеморрагические, дилюционные):
2. Анемия вследствие нарушения кровообразования (дизэритропоэтические):
а) анемия от дефицита гемопоэтических веществ:
— железодефицитные, хроническая постгеморрагическая
б) анемия вследствие угнетения или истощения костного мозга:
3. Анемия вследствие повышенного кроворазрушения (гемолитические):
а) наследственные – мембранопатии ( дефект оболочки эритроцитов);
-ферментопатии (недостаточность ферментативных систем, обеспечивающих жиснеспособность эритроцита);
б) приобретенные — аутоиммунные, изоиммунные ( в результате образования антител к эритроцитам );
Для мазка крови больного острой постгеморрагической анемией характерен нормобластический тип кроветворения, регенеративный сдвиг с появлением полихромотофильных эритроцитов, ретикулоцитов (при суправитальной окраске мазков основными красителями) и нормоцитов: оксифильных, полихроматофильных, базофильных.
Мазок крови больного хронической постгеморрагической анемией характеризуется нормобластическим типом кроветворения, гипохромией, с признаками дегенеративного сдвига: анизоцитозом и пойкилоцитозом.
Мазок крови больного В12-фолиеводефицитной анемией характеризуется мегалобластическим типом кроветворения, гиперхромией, признаками дегенеративного сдвига (анизоцитоз, пойкилоцитоз, в клетках — тельца Жолли, кольца Кебота).
Мазок крови больного гемолитической анемией характеризуется нормобластическим типом кроветворения: гипо-, изо — или гиперхромией. Признаки дегенеративного сдвига: анизоцитоз, пойкилоцитоз, базофильная пунктуация Признаки регенеративного сдвига: нормоциты оксифильные, полихроматофильные, базофильные и ретикулоциты, обнаруженные при суправитальной окраске мазка основными красителями.
Цель: Изучить количественные и качественные изменения в системе эритрона при патологии.
Опыт 1. Подсчет количества эритроцитов при постгеморрагической анемии.
Методика: Постгеморрагическая анемия воспроизводится у кролика повторным кровопусканием. Кровь для подсчета эритроцитов набрать из краевой вены уха кролика после прокола ее иглой. Кровь набрать в красный меланжер до метки 0,5 и довести физиологическим раствором до метки 101. Меланжер встряхивать в течение 2 мин, на 1/3 содержимое удалить и заправить сетку камеры Горяева. Подсчет эритроцитов произвести в 5 расчерченных больших квадратах по диагонали с использованием формулы:
где а — количество эритроцитов в пяти больших квадратах;
4000 — количество малых квадратов, объем которых составляет 1 мм3
200 — степень разведения крови;
80 — количество сосчитанных малых квадратов.
Сформулировать вывод об изменении содержания эритроцитов при постгеморрагической анемии.
Опыт 2. Подсчет количества ретикулоцитов при постгеморрагической анемии.
Методика: Исследуются готовые мазки крови, окрашенные бриллиант-крезилбау. Мазок рассмотреть под микроскопом, объектив иммерсионный, окуляр Х7. Ретикулоциты отличаются от эритроцитов наличием в их протоплазме синего цвета сеточки. Подсчитать 1000 эритроцитов, отметить, сколько из них ретикулоцитов.
Сделать вывод о содержании ретикулоцитов при постгеморрагической анемии.
Опыт 3. Изучение морфологической картины крови при постгеморрагической анемии.
Методика: Изучить готовый мазок крови под иммерсией. Зарисовать клетки крови, характерные для данного вида анемии.
Опыт 4. Изучение морфологической картины крови при гемолитической анемии.
Методика: Изучить готовый мазок крови под иммерсией. Зарисовать клетки крови, характерные для данного вида анемии.
Опыт 5. Изучение мазков крови больного B12-фолиеводефицитной анемии.
Методика: Изучить готовый мазок крови под иммерсией. Зарисовать клетки.
Раздел: Патофизиология органов и систем
Тема: Нарушение системы лейкоцитов.
Лейкон — морфо-функциональная единица системы крови, которая включает в себя органы лейкопоэза, зрелые лейкоциты в крови и тканях и механизмы регуляции, обеспечивающие баланс между лейкопоэзом и лейкодиерезом. Все качественные и количественные изменения в лейконе проявляются реактивными состояниями (лейкоцитозы, лейкопении, лейкемоидные реакции) и самостоятельными заболеваниями системы крови (лейкозы). Лейкоцитоз — увеличение общего количества лейкоцитов в единице объема крови свыше 9*109/л. Лейкемоидные реакции — особый тип реактивных состояний, для которых характерно в периферической крови наличие лейкоцитоза свыше 40*109 л с гиперрегенеративным сдвигом вплоть до бластов в сочетании с дегенеративными изменениями цитоплазмы и ядер лейкоцитов. Лейкопения — уменьшение количества лейкоцитов в периферической крови ниже 4,0*109/л. Лейкоз — опухоль, исходящая из кроветворных клеток с первичным поражением костного мозга. В основе патогенеза лейкоза лежит неконтролируемая пролиферация клеток. Мишенью опухолевой трансформации при лейкозе являются бипотентные и унипотентные клетки-предшественницы, реже стволовая кроветворная клетка. По морфологическому субстрату опухоли лейкозы разделяют на острые и хронические. Острым лейкозам свойственно нарушение механизма нормальной дифференцировки и созревания клеток, поэтому субстрат опухоли представлен бластными клетками. При хронических лейкозах опухолевые клетки сохраняют способность дифференцироваться до зрелых клеток.
Мазки крови при острым лейкозе характеризуются лейкемическим провалом, т. е. присутствием бластов и зрелых лейкоцитов. В мазках крови и костном мозге при хроническом миелоидном лейкозе обнаруживают базофильно-эозинофильную ассоциацию клеток, все стадии созревания гранулоцитов от миелобласта до сегментоядерных лейкоцитов (промиелоциты, миелоциты, метамиелоциты, палочкоядерные). В мазках крови и костного мозга при хроническом лимфолейкозе выявляют абсолютный лимфоцитоз (70-90% зрелых лимфоцитов), пролимфоциты, а в период бластного криза — лимфобласты. Патогномоничными являются клетки лейколиза (тени Боткина-Гумпрехта).
Цель: Изучить количественные и качественные нарушения в системе лейкона при реактивных состояниях и лейкозах.
Опыт 1. Подсчет количества лейкоцитов при постгеморрагической анемии.
Методика: Техника взятия венозной крови у крысы. Под нембуталовым наркозом (30 мг/кг) у крысы вызвать острую кровопотерю (15% от объема циркулирующей крови). Затем для подсчета количества лейкоцитов взять 0,1 мл венозной крови и поместить на часовое стекло, предварительно обработанное раствором гепарина (250 Ед. на 1 мл физиологического раствора).
Для подсчета количества лейкоцитов из капли крови, помещенной на часовое стекло, ровным столбиком набрать 20 мкл крови и поместить в пробирку с 0,4 мл 3% раствора уксусной кислоты. Кровь осторожно выдуть в раствор кислоты и, не смешивая содержимое пробирки, в верхнем слое раствора уксусной кислоты аккуратно промыть пипетку. После этой манипуляции содержимое пробирки перемешать между руками. Через 10-15 мин содержимое пробирки вновь тщательно перемешать, на стеклянной палочке каплю раствора лейкоцитов поместить под притертое стекло камеры Горяева. Через 3 минуты приступить к подсчету клеток. Под малым увеличением микроскопа окуляр х15, объектив х8 сосчитать клетки в 100 больших квадратах. Рассчитать количество лейкоцитов по формуле:
где а — количество лейкоцитов в 100 больших квадратах;
1/4000 — объем одного малого квадрата;
1600 — количество малых квадратов в 100 больших;
1/20 — степень разведения крови.
Полученную при подсчете цифру лейкоцитов перевести из внесистемной в системную величину, учитывая, что системной единицей объема является 1 литр.
Полученные результаты запротоколировать. Сделать вывод о характере количественных нарушений в лейконе при постгеморрагической анемии. Объяснить их механизмы развития.
Опыт 2. Подсчет лейкоцитарной формулы у больного с острым лейкозом.
Методика: Изучение мазка крови проводится с масляной иммерсионной системой. В окрашенных мазках дают оценку величины, формы, окраски и структуры клеток. При подсчете лейкоцитарной формулы нужно помнить, что различные виды лейкоцитов распределяются по стеклу неравномерно: более крупные клетки (моноциты, нейтрофилы) располагаются по периферии (вдоль верхнего и нижнего края мазка), а более легкие (лимфоциты) преобладают в центре мазка. Распространен следующий способ подсчета. По верхнему и нижнему краю мазка считают, передвигая мазок по зигзагообразной линии: 3 поля зрения по самому краю в горизонтальном направлении, затем по направлению к середине мазка, вновь направляют к краю, сосчитывают 3 поля зрения и т. д. В каждом участке двух мазков крови подсчитывают 50 клеток. Определив процентное соотношение видов лейкоцитов, зная их общее количество в крови, определяют лейкоцитарный профиль (абсолютное содержание каждого вида лейкоцитов в единице объема крови).
Пример. Общее количество лейкоцитов 6,0*109/л, лимфоцитов – 30%. Абсолютное содержание лимфоцитов в крови составляет 1,8*109/л.
Зарисовать клетки крови, сравнить полученные данные при подсчете лейкоцитарной формулы с нормальными показателями,
Опыт 3. Подсчет лейкоцитарной формулы у больного с хроническим лимфолейкозом. Методика: С помощью счетной машинки, подсчитать лейкоцитарную формулу готового мазка. Зарисовать клетки крови, сравнить полученные данные при подсчете лейкоцитарной формулы с нормальными показателями. Объяснить механизмы развития выявленных отклонений показетелей лейкограммы.
Опыт 4. Подсчет лейкоцитарной формулы больного с хроническим миелолейкозом.
Методика: С помощью счетной машинки, подсчитать лейкоцитарную формулу готового мазка. Зарисовать клетки, характерные для данного вида лейкоза. Запротоколировать результаты. Объяснить механизмы развития обнаруженных изменений. Сформулировать вывод о количественных и качественных нарушениях в лейконе при хроническом миелолейкозе.
Опыт 5. Подсчет лейкоцитарной формулы у лиц с воспалительными и инфекционными заболеваниями.
Методика: С помощью счетной машинки, подсчитать лейкоцитарную формулу готового мазка. Определить лейкоцитарный профиль лейкограммы.
Зарисовать клетки крови, сравнить полученные данные при подсчете лейкоцитарной формулы с нормальными показателями. Объяснить механизмы развития выявленных отклонений показетелей лейкограммы.
Раздел: Патофизиология органов и систем
Тема: Изменения физико-химических свойств крови
Физико-химические свойства крови могут быть оценены путем определения осмотической резистентности эритроцитов, гематокритной величины, белкового состава крови и компонентов свертывающей и противосвертывающей систем.
Гематокрит — это доля (%) от общего объема крови, которую составляют эритроциты. Гематокрит отражает соотношение эритроцитов и плазмы крови. Повышение гематокрита: эритремия; симптоматические эритроцитозы (врожденные пороки сердца, дыхательная недостаточность, гемоглобинопатии, новообразования почек, сопровождающиеся усиленным образованием эритропоэтина, поликистоз почек); гемоконцентрация при ожоговой болезни, перитоните, дегидратации организма (при выраженной диарее, неукротимой рвоте, повышенной потливости, диабете). Понижение гематокрита: анемия; гипергидратация; вторая половина беременности.
Резистентность эритроцитов — способность их противостоять различным разрушительным воздействиям: осмотическим, механическим, химическим, физическим.
В гипертонических растворах эритроциты теряют воду и сморщиваются, а в гипотонических — поглощают воду и набухают. При значительном набухании происходит гемолиз. Изотоническим раствором для эритроцитов является 0,85%-ный раствор хлорида натрия. В 0,48-0,44%-ных растворах NaCl разрушаются наименее резистентные эритроциты (минимальная осмотическая резистентность, верхняя граница резистентности). При концентрации 0,32-0,28% полностью гемолизируются все эритроциты (максимальная осмотическая резистентность, нижняя граница резистентности).
Уменьшение осмотической резистентности эритроцитов (повышение показателей минимальной и максимальной резистентности) наблюдается при гемолитической болезни новорожденных и наследственном микросфероцитозе, а также (в слабой степени выраженности) при токсикозах, бронхопневмониях, гемобластозах, циррозах печени и др. Увеличение осмотической резистентности эритроцитов имеет место при некоторых случаях полицитемии и железодефицитной анемии, а также при гемоглобинозе S и после массивных кровопотерь.
Система гемостаза — совокупность биологических и биохимических механизмов, которые, с одной стороны, участвуют в поддержании целостности кровеносных сосудов и сохранении жидкого состояния циркулирующей крови, а с другой — обеспечивают быструю закупорку поврежденных сосудов и купирование кровотечений.
Осуществляется гемостаз тремя взаимодействующими между собой морфофункциональными компонентами: стенками кровеносных сосудов, клетками крови (тромбоциты) и плазменными ферментными системами — свертывающей, фибринолитической (плазминовой), калликреин-кининовой и системой комплемента.
Многочисленные нарушения системы гемостаза подразделены на три группы:
1. Усиление свертываемости крови и тромбообразования — гипергоагуляция и развитие тромботического синдрома.
2. Уменьшение свертываемости крови и тромбообразования — гипокоагуляция и развитие геморрагических синдромов.
3. Фазное нарушение состояния системы гемостаза (ДВС-синдром).
Тромботический синдром, или тромбофилия — состояние, характеризующееся чрезмерной (неадекватной) коагуляцией крови и тромбообразованием, ведущими к ишемии тканей и органов.
Геморрагические заболевания и синдромы — патологические состояния, характеризующиеся повышенной кровоточивостью в результате недостаточности одного или нескольких элементов гемостаза. По происхождению различают следующие виды геморрагических заболеваний и синдромов: васкулиты, тромбоцитопении, тромбоцитопатии, коагулопатии, ДВС.
1. гиперкоагуляция и гиперагрегация;
2. коагулопатия и тромбоцитопатия потребления с активацией фибринолитической системы;
3. генерализация фибринолиза;
Цель: Познакомиться с некоторыми видами нарушения физико-химических свойств крови.
Опыт 1. Определение времени свертываемости крови при постгеморрагической анемии (метод Бюркера).
Методика: На часовое стекло поместить небольшую каплю дистиллированной воды и на нее капнуть каплю крови (в 2-3 раза больше), взятую из вены подопытного кролика. Отметить момент взятия крови. Через каждые 30 с, опуская стеклянную палочку в каплю, уловить образование нитей фибрина. Начало процесса свертывания крови – появление нитей фибрина, окончанием считается момент, когда вся капля крови тянется за палочкой.
Запротоколировать результаты. На основании полученных данных сформулировать вывод о характере нарушений свертываемости крови при постгеморрагической анемии.
Опыт 2. Определение времени рекальцификации плазмы при постгеморрагической анемии.
Методика: В пробирку, находящуюся в водяной бане при температуре 37˚С, ввести 0,2 мл 0,227% раствора хлорида кальция и 0,1 мл 0,85 % раствора хлорида натрия. Через 1 мин добавить 0,1 мл испытываемой плазмы, немедленно включить секундомер и заметить время образования сгустка фибрина. Исследование повторяют 2-3 раза и вычисляют средний результат. Нормальные величины: 60-120 с.
Запротоколировать результаты. На основании полученных данных сформулировать вывод о характере нарушений свертываемости крови при постгеморрагической анемии.
Опыт 3. Определение осмотической резистентности эритроцитов при постгеморрагической анемии.
Методика: Схема постановки реакции и получения концентрация гипотонического раствора хлорида натрия.
источник