Стенка кишечника содержит гладкие мышцы, сокращения которых обеспечивают передвижение пищи от его верхних отделов к нижним. Это так называемая перистальтика кишечника. В норме в течение 1 минуты участок тонкой или толстой кишки выполняет 15-18 перистальтических движений. Атония кишечника — это снижение или отсутствие перистальтики. Часто встречается в экономически развитых странах у людей с малоподвижным образом жизни и питающихся высококалорийной пищей.
Атония это функциональное состояние, и если устранить причину ее появления, то перистальтика кишечника возобновляется. Какой-то одной причины возникновения не существует, она может проявляться как самостоятельное заболевание, так и быть проявлением других заболеваний организма. Можно выделить несколько основных причинных факторов, приводящих к развитию атонии кишечника:
- малоподвижный образ жизни – приводит к снижению иннервации мышц стенок кишечника и уменьшению их перистальтики;
- неправильное питание – высококалорийная пища с низким содержанием клетчатки приводит к развитию атонии кишечника;
- постоянные стрессы – регуляция работы кишечника осуществляется центральной нервной системой, поэтому чрезмерная нагрузка на нее может вызвать сбой в иннервации мышц стенок кишечника (и в других органах тоже);
- лекарственные препараты (спазмолитики, морфиноподобные обезболивающие) – их длительное применение в высоких дозах приводит к атонии кишечника;
- дисбактериоз кишечника – изменение баланса нормальной микрофлоры кишечника приводит к нарушению пищеварения и выработке токсинов, снижающих перистальтику;
- некоторые кишечные инфекции;
- гельминтоз – паразитирование глистов в кишечнике происходит с выделением веществ, снижающих его перистальтику;
- употребление наркотиков из группы опиатов – наркотические производные мака попадая в организм, снижают тонус и расслабляют мышцы всех полых органов;
- злоупотребление алкоголем – за счет токсического воздействия алкоголя на нервную систему нарушается ее нормальная работа;
- курение – никотин вначале усиливает перистальтику кишечника, однако через некоторое время она снижается;
- опухоли кишечника – злокачественные новообразования в кишке выделяют токсины, воздействующие на центральную и вегетативную нервную систему, с нарушением их работы;
- генетическая предрасположенность – это состояние может передаваться по наследству от родителей к детям.
Механизм развития атонии кишечника заключается в снижении тонуса мышц стенок кишки, снижении перистальтики и передвижения пищевых масс. Это приводит к нарушению пищеварения, развитию гнилостных процессов в кишечнике, выработке токсинов, которые усугубляют это состояние.
Проявления этого состояния связаны в первую очередь с нарушением пищеварения и задержкой стула:
- склонность к запорам – стул у человека реже 1-го раза в сутки;
- плотный стул – консистенция стула становится каменистой, длительное нахождение каловых масс в толстом кишечнике приводит к тому, что вода из них полностью всасывается;
- вздутие живота – проявление нарушения полостного и пристеночного пищеварения в кишечнике с выделением газов;
- общая слабость, плохой сон;
- бледный, неестественный цвет лица;
- мраморный рисунок кожи;
- анемия (малокровия) – снижение концентрации гемоглобина происходит из-за того, что железо не усваивается организмом.
Диагностика данного состояния несложная, уже на основании симптомов можно заподозрить атонию кишечника. Более сложным является выявление причин заболевания, для этого проводится комплексная лабораторная и инструментальная диагностика.
Перед тем, как лечить атонию кишечника, вне зависимости от ее причины, важным мероприятием является выполнение рекомендаций по правильному питанию и образу жизни:
- питание – диета должна быть сбалансированной по калорийности (ее нужно снизить), предпочтительно употребление растительной пищи богатой клетчаткой (клетчатка сама по себе является стимулятором перистальтики), отказ от жирной, жареной, копченой пищи и сладостей;
- режим употребления пищи – нельзя допускать больших перерывов в питании, последний прием пищи должен быть не менее, чем за 2 часа до сна;
- борьба с малоподвижным образом жизни – динамические дозированные физические нагрузки полчаса в сутки значительно повышают тонус и перистальтику кишечника.
Медикаментозное лечение предполагает использование слабительных средств и препаратов, повышающий тонус мышц стенок кишечника и его перистальтику. К ним относятся:
- метоклопрамид – усиливает перистальтику, обладает противорвотным действием, выпускается в виде инъекций и таблеток;
- регулакс – растительный препарат травы сенны, обладает мягким слабительным действием, способствует выведению каловых масс из толстой кишки;
- прозерин – используется в условиях стационара при неэффективности других средств;
- амиридин – препарат, улучшающий нервно-мышечную передачу импульса, за счет чего он усиливает перистальтику кишечника, применяется только под контролем врача;
- панкреатин (или аналоги) – ферментный препарат, улучшающий переваривание пищи;
- эспумизан – средство уменьшающее вздутие кишечника за счет ослабления поверхностного натяжения пузырьков газа.
В домашних условиях при атонии кишечника используется отвар травы сенны. Однако стоит помнить, что при симптомах атонии кишечника лучше обратиться за консультацией к врачу гастроэнтерологу для полноценного обследования и выяснения причин этого состояния.
Железодефицитная анемия обычно рассматривается скорее как симптом другого заболевания или как состояние, а не как отдельное заболевание и обычно возникает, когда в организме недостаточный запас железа. Маленькие дети или взрослые, сидящие на строгой диете, могут получать недостаточное количество железа из пищи, что может привести к анемии. Может быть нарушена способность пищеварительной системы всасывать достаточно железа, что часто происходит в тех случаях, когда была удалена часть желудка. Анемия может наступать вследствие чрезмерной потери крови. Это относится к женщинам, у которых обильные менструации, а также к людям, страдающим от язвы желудка и двенадцатиперстной кишки, геморроя или рака желудка или толстой кишки.
Две другие формы анемии — это гемолитическая анемия, при которой красные кровяные клетки разрушаются слишком быстро, и серповидно-клеточная анемия, при которой организм вырабатывает аномальный гемоглобин.
Если вы подозреваете, что у вас анемия, очень важно быстро обратиться к врачу. Анемия может снизить сопротивляемость организма болезням, вызвать упадок сил, ограничить работоспособность. Анемия также может быть сигналом более серьезных медицинских проблем. Диагноз «анемия» ставится на основе анализа крови. Лечение анемии основывается на восстановлении количества железа в организме с помощью различных лекарственных препаратов (как для приема внутрь, так и инъекций).
Основной причиной анемии является недостаточность железа, витамина В12 или фолиевой кислоты. Анемия также может быть вызвана потерей крови из-за желудочно-кишечного кровотечения, которое может быть связано с приемом определенных препаратов, например, ацетилсалициловой кислоты (аспирина ) или ибупрофена, а также с раковыми заболеваниями.
Если вы отмечаете бледность, повышенную утомляемость и слабость, обмороки, одышку, учащенное сердцебиение, то следует обратиться к врачу. При анемии, вызванной недостатком фолиевой кислоты в пище, могут возникать стоматит (воспаление слизистой оболочки рта), воспаление языка, желтизна кожи, покалывания в руках и ногах.
Включите в ваш рацион как можно больше зеленых овощей, салата и зелени для получения достаточного количества фолиевой кислоты. Многие зерновые завтраки также содержат фолиевую кислоту. Пища, обогащенная железом, также может помочь при анемии. Следует избегать употребления напитков, содержащих кофеин (например, чая, кофе, колы), особенно во время еды, т.к. кофеин мешает всасыванию железа.
Женщинам с частыми или обильными менструальными кровотечениями, а также во время беременности следует обсудить со своим врачом возможность дополнительного приема препаратов железа.
Назначить анализы и другие виды обследования, для того чтобы оценить состояние пациента, определить причину анемии и прописать лечение.
— с недостаточностью железа, врач назначит препараты, содержащие железо, а определив причину анемии, примет меры для ее устранения.
— с недостаточностью витамина В12 вам назначат инъекции витамина В12.
— у детей анемия может быть связана с заражением кишечника паразитами или глистами, в этом случае сначала необходимо провести противопаразитарное лечение.
— при сильной потере крови врач в больнице может провести переливание крови.
Беременным с целью профилактики и лечения врач назначает препараты железа и фолиевую кислоту.
Ешьте продукты, богатые железом, например, фрукты, цельнозерновой хлеб, бобы, красное нежирное мясо, зеленые овощи, салат и зелень.
Проводите профилактику заражения глистами.
Избегайте длительного контакта с инсектицидами. химическими агентами, отравляющими и токсичными веществами, бензином и другими нефтепродуктами.
Пару слов о том, что такое синдром СРК. Каковы последствия этой болезни? Рассказать, что одним из последствий является анемия.
Почему? Пошаговая инструкция что делать, если диагностировали анемию из-за СРК.
Синдром раздраженного кишечника на сегодняшний день является одним из самых проблемных заболеваний в гастроэнтерологии. Это состояние по разным оценкам имеют около 10 процентов населения, то есть каждый 10-й из нас.
При этом симптомы достаточно мучительные и реально заставляют людей страдать. К счастью буквально недавно были разработаны новые стандарты диагностики и лечения этой болезни, которых ждали целых 10 лет!
Подозревать синдром раздраженного кишечника можно, если есть боли в животе, связанные с нарушением стула. Стул может быть жидкий или твердый, или иногда жидкий, или иногда твердый, или иногда такой, а в другие периоды времени другой.
То есть при наличии болей в животе чаще 1 раза в неделю и изменений стула можно думать о синдроме раздраженного кишечника.
Первое, что нужно сделать, если у вас возникли такие симптомы и сохраняются в течение месяца или дольше, это обратиться к врачу для проведения обследования. Обследование назначается в зависимости от состояния живота, может быть минимальным (какие-то общие анализы) или достаточно полным, включая колоноскопию.
В принципе, в зависимости от состояния могут быть использованы разным методы – ирригоскопия, компьютерная томография с двойным контрастированием, капсульная эндоскопия и другие, все решается индивидуально. Однако у многих пациентов даже не требуется дополнительное обследование.
Самое важное, что при синдроме раздраженного кишечника практически все анализы нормальные и не имеют отклонений от нормы, но живот продолжает болеть и проблемы со стулом сохраняются!
Если при синдроме раздраженного кишечника у вас нашли анемию или снижение гемоглобина, или снижение уровня железа, то дело плохо. Значит беспокоящий вас недуг вовсе не синдром раздраженного кишечника, а одно из воспалительных заболеваний кишечника!
Это может быть язвенный колит, болезнь Крона, дивертикулярная болезнь, полипоз кишечника или другие болезни. В такой ситуации обязательно нужен осмотр и дополнительное обследование, потому что болезнь может быть серьезной.
Для лечения воспалительных заболеваний кишечника, важно понимать какое именно воспаление возникло. От этого будет зависеть способ и длительность лечения. В любом случае, это будут достаточно специальные лекарства, которые назначит врач.
Для лечения анемии при воспалительных заболеваниях кишечника подходят не все лекарства, а вернее, подходит только одно – Сидерал Форте. Потому что в отличие от любого другого препарата железа он не имеет побочного действия на кишечник и даже при нарушении всасывания пищи в кишечнике железо из него попадет в организм.
Чтобы лечить синдром раздраженного кишечника важно быть уверенным, что нет других болезней кишечника. После этого можно приступать и к лечению. В зависимости от типа болей, частоты и консистенции стула используются разные варианты лечения.
При болях и запорах используется коррекция питания, специальная диета. Затем приступают к волокнам и осмотическим слабительным. При боли и диарее используются средства, замедляющие сокращения кишечника. Если же диарея сохранялась долго, более месяца, необходимо убирать из кишечника избыточный бактериальный рост и восстанавливать моторику кишечника.
При синдроме раздраженного кишечника также нарушается и чувствительность нервных волокон, расположенных в кишечнике. Именно поэтому боли могут восприниматься и чувствоваться намного сильнее, чем ситуация в кишечнике на самом деле. Самое сложное в лечении –
Для этого используются различные лекарства, действующие на специальные рецепторы.
Синдром раздраженного кишечника не смертельный, но очень мучительный.
Автор. Сергей Вялов, врач-гастроэнтеролог в GMS Clinic, к.м.н. Член Американской гастроэнтерологической ассоциации (AGA) и Российской гастроэнтерологической ассоциации (РГА)
источник
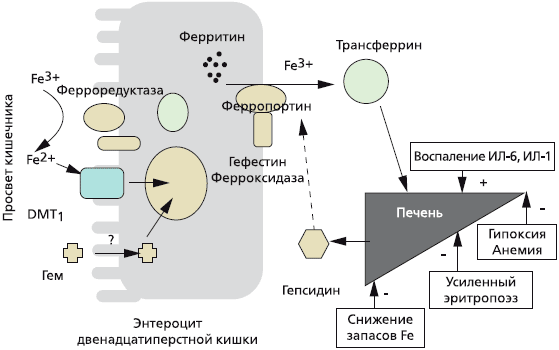
Железодефицитная анемия – наиболее частая форма анемий в гастроэнтерологии, и причиной ее развития являются кровотечения, нарушения всасывания железа, диетические ограничения. Ряд хронических заболеваний пищеварительной системы сопровождается развитием анемии различной степени тяжести. Анемия может являться первым признаком основного заболевания, в частности, опухолевого процесса пищевого канала, а также быть причиной снижения качества жизни пациентов.
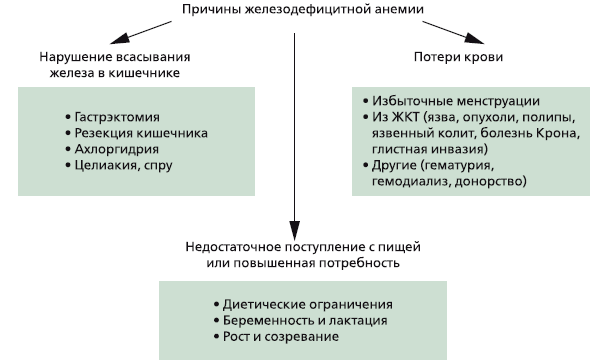
Выделяют три глобальные причины развития дефицита железа в организме:
- Недостаточное поступление с пищей или повышенная потребность.
- Нарушение всасывания железа в кишечнике.
- Хронические потери крови.
Заболевания желудочно-кишечного тракта являются одной из основных причин развития железодефицитной анемии, что обусловлено нарушением всасывания железа в кишечнике или его потерями вследствие эрозивно-язвенных, опухолевых или аутоиммунных воспалительных поражений слизистой оболочки кишечника.
Перечень заболеваний пищеварительного тракта, сопровождающихся развитием анемии, достаточно широк. Причиной железодефицитных состояний часто выступают болезни верхних отделов желудочно-кишечного тракта и толстой кишки.
Одной из важных причин развития железодефицитной анемии является нарушение процессов всасывания железа в двенадцатиперстной кишке и проксимальном отделе тощей кишки. Различные заболевания тонкой кишки, сопровождающиеся синдромом мальабсорбции (энтерит, амилоидоз, целиакея, идеопатическая стеаторея), а также оперативные вмешательства на желудке и тонкой кишке (состояние после тотальной гастроэктомии, субтотальной резекции желудка, ваготомии с гастроэктомией, резекция тонкой кишки) приводят к развитию дефицита железа.
Накапливаются данные о потенциальной связи инфекции H. pylory с железодефицитной анемией, которая может быть следствием скрытых кровотечений при эрозивном гастрите и язвенной болезни, нарушение всасывания железа при хеликобактерном атрофическом пангастрите, а также снижения содержания аскорбиновой кислоты в желудке и конкурентного захвата и утилизации железа самой бактерией. Таким образом, эрадикация H. pylory может стать еще одним подходом к лечению железодефицитной анемии в отсутствии других явных ее причин.
Этиологическим фактором анемии может стать прием нестероидных противовоспалительных препаратов (НПВП). Врачам хорошо известна возможность как массивных, так и скрытых кровотечений из эрозий и язв желудка и двенадцатиперстной кишки при НПВП-гастропатии. Однако, железодефицитная анемия может быть следствием НПВП-энтеропатии, другими клиническими проявлениями которой могут служить гипоальбуминемия, мальабсорбция и наличие измененной крови в кале.
Причиной нарушения всасывания гемопоэтических факторов являются и заболевания тонкой кишки. К ним можно отнести целиакию (половина пациентов с неясной этиологией железодефицитной анемии, резистентной к терапии препаратами железа), резекцию участка тонкой кишки, синдром избыточного бактериального роста в тонкой кишке, диабетическую энетропатию, амилоидоз, склеродермию, болезнь Уиппла, туберкулез, лимфому тонкой кишки, тропическое спру, паразитарные заболевания (лямблиоз) и гельминтозы (дифиллоботриоз).
Воспалительные заболевания кишечника, прежде всего, неспецифический язвенный колит и болезнь Крона, часто сопровождаются развитием анемии. Ведущими механизмами при этом выступают кровопотеря у пациентов с язвенным колитом и болезнью Крона, а также мальабсорбция при вовлечении в процесс тощей и подвздошной кишки при болезни Крона.
Ведущей причиной анемии при патологии нижних отделов желудочно-кишечного тракта, особенно у пациентов старше 50 лет, служит колоректальный рак. Хроническая кровопотеря наблюдается при полипах толстой кишки, дивертикулезе, ишемическом колите, геморрое и анальных трещинах.
Анемический синдром часто делает необходимым тщательное обследование желудочно-кишечного тракта. Для уточнения вида анемии проводят исследования общего и биохимического анализа крови.
Среди причин железодефицитной анемии (почти 30-50% всех случаев) прежде всего рассматривают острые или хронические кровопотери из желудочно-кишечного тракта.
Причины железодефицитной анемии
Как показали результаты открытого мультицентрового исследования, проведенного в Украине в 2008 году и базировавшиеся на анализе 1299 историй болезней больных железодефицитной анемией, основной причиной развития были эрозивно-язвенные поражения пищевого канала (44,58%) и заболевания, сопровождающиеся синдромом мальабсорбции. Циррозы печени являлись причиной железодефицитной анемии в 10,39% случаев, воспалительные заболевания кишечника – 4,54% больных.
Диагностируется железодефицитная анемия у больных с гастроэнтерологическими заболеваниями по совокупности анамнестических данных (указания на оперативные вмешательства на желудке или кишечнике, прием нестероидных или гормональных противовоспалительных препаратов, антикоагулянтов и антиагрегантов, язвенный анамнез, наличие хронических заболеваний печени и воспалительных заболеваний кишечника и т.д.), клинических проявлений (наличие специфического сидеропенического синдрома, проявляющегося сухостью и истончением кожи, ангулярный хейлит, дисфагия, ломкость ногтей, их поперечная исчерченность, вогнутость ногтевой пластинки, извращение вкуса и обоняния, симптом «голубых склер», мышечная слабость) и лабораторных показателей.
Диагностика анемии основывается, главным образом, на данных лабораторных исследований, в первую очередь – на результатах клинического исследования крови с определением концентрации гемоглобина.
| Параметры | Значения при ЖДА | Норма | |
| Железо сыворотки, мкг/дл | 3 | 5 | Примечание. НПВС — нестероидные противовоспалительные средства. Среди причин ЖДА (почти 30-50 % всех случаев) прежде всего рассматривают острые или хронические кровопотери из ЖКТ. Основной причиной ЖДА у женщин до менопаузы являются беременность и менструации, у женщин после менопаузы и у мужчин — хронические (латентные) потери крови из ЖКТ. Анализ кала на скрытую кровь — основной скрининговый метод выявления скрытого желудочно-кишечного кровотечения (тест положительный при выделении не менее 10 мл крови в сутки). При потере не менее 30 мл крови в сутки тест на скрытую кровь бывает положительным в 93 % случаев [8]. Наиболее часто при хронической ЖДА и особенно в случаях положительного результата кала на скрытую кровь выполняют эзофагогастродуодено- (ЭФГДС) и колоноскопию. В 5-10 % случаев анемий, связанных с заболеваниями ЖКТ, при ЭФГДС и колоноскопии не удается выявить очага поражения [9]. В 25 % случаев это обусловлено небольшим размером пораженного участка, который обнаруживается при повторном осмотре, в остальных случаях необходимо обследование тонкой кишки. В последние годы наиболее часто для выявления источника кровотечения из тонкой кишки используется беспроводная капсульная эндоскопия. В 10-17 % случаев причиной ЖДА у мужчин и женщин старше 40 лет являются онкологические заболевания ЖКТ; прежде всего колоректальный рак. ЖДА в течение длительного времени может быть единственным проявлением рака толстой кишки правосторонней локализации, при этом размер опухоли обычно превышает 3 см. Другая наиболее частая причина ЖДА -язвенная болезнь желудка и двенадцатиперстной кишки. При скрытых кровопотерях, обусловленных поражением тонкой кишки, наиболее часто в возрасте до 40 лет выявляют опухоли (лимфому, карциноид, аденокарциному, полипоз), ангиоэктазию артерий (Dieulafoy’s поражение), целиакию и болезнь Крона, в возрасте старше 40 лет -патологию сосудов различной природы и прием НПВС. У трети больных воспалительными заболеваниями кишечника (болезнь Крона, язвенный колит) выявляется анемия, имеющая сложный генез (сочетание ЖДА и анемии хронических заболеваний). При этом дефицит железа становится следствием нескольких причин: Лечение Суточная терапевтическая доза элементарного железа при лечении ЖДА для взрослых составляет в среднем 100— 200 мг в 2—3 приема. Поливитаминные комплексы, содержащие железо, не рекомендуют в качестве лечения ЖДА, т. к. они содержат недостаточное количество железа либо оно плохо всасывается в кишечнике. При адекватном лечении уже в течение первых 3 суток наблюдается увеличение числа ретикулоцитов в крови, на 7—10-й день отмечается ретикулоцитарный криз (пик ретикулоцитоза). К 3—4-й неделе лечения имеет место увеличение уровня гемоглобина на 20 г/л. Прием препаратов железа необходимо продолжать еще в течение 3—6 месяцев после нормализации уровня гемоглобина — пока насыщение трансферрина железом не превысит 30 % и концентрация ферритина не достигнет 50 нг/мл (показатель восстановления тканевых запасов железа). Среди 20—30 % пациентов в результате приема препаратов железа отмечаются различные диспептические расстройства (тошнота, дискомфорт в эпигастрии, диарея или запор). Риск развития желудочно-кишечных расстройств можно снизить, принимая препарат во время еды или на ночь, а также при постепенном увеличении дозы. Среди причин неэффективности пероральных форм железа рассматривают целый ряд факторов [10]: недостаточное поступление железа; Нарушение всасывания железа: Продолжающиеся потери крови или повышенная потребность в железе: Сопутствующие заболевания или состояния: Неправильный диагноз или наличие других причин анемии: Выделяют следующие показания к парентеральному введению, преимущественно внутривенному, препаратов железа: Основная опасность при парентеральном введении железа — развитие тяжелых аллергических реакций, включая анафилактических шок с летальным исходом, которые наблюдаются в 0,6—1,0 % случаев. Данные реакции, в основном, характерны для препаратов железа, содержащих декстран. Среди парентеральных препаратов железа широкое распространение, особенно в комплексной терапии воспалительных заболеваний кишечника, получили сахарат железа и железа карбоксимальтозат (Феринжект), которые в отличие от декстрана железа ассоциируются с минимальным риском развития анафилактических и других аллергических реакций [11—13]. Так, в 2011 г. были опубликованы результаты рандомизированного контролируемого исследования применения железа карбоксимальтозата пациентами с железодефицитной анемией, обусловленной воспалительными заболеваниями кишечника (FERGIcor — a Randomized Controlled Trial on Ferric Carboxymaltose for Iron Deficiency Anemia in Inflammatory Bowel Disease) [14]. В исследовании сравнивали эффективность и безопасность нового режима фиксированной дозы железа карбоксимальтозата (Феринжекта) и индивидуально рассчитываемых доз сахарата железа (СЖ) для пациентов с воспалительными заболеваниями кишечника и ЖДА. В исследование были включены 485 пациентов с ЖДА (уровень ферритина ЛИТЕРАТУРА источник Анемии являются довольно частым вторичным синдромом при гастроэнтерологических заболеваниях. Основными видами анемий, выявляемых у гастроэнтерологических больных, являются: железодефицитная анемия (ЖДА), анемия хронических заболеваний (АХЗ), гемолитическа Анемии являются довольно частым вторичным синдромом при гастроэнтерологических заболеваниях. Основными видами анемий, выявляемых у гастроэнтерологических больных, являются: железодефицитная анемия (ЖДА), анемия хронических заболеваний (АХЗ), гемолитическая анемия, В12— и фолиеводефицитная анемия, гипо-, апластические анемии. ЖДА — наиболее частая форма анемий в гастроэнтерологии, и причиной ее развития являются кровотечения, нарушения всасывания железа, диетические ограничения. Второй по распространенности после ЖДА в детской гастроэнтерологии является АХЗ, которая отличается достаточными запасами железа в организме, но снижением насыщения им трансферрина, сниженным или нормальным уровнем сывороточного железа. Причина развития АХЗ заключается в действии провоспалительных цитокинов (интерлейкина 1-альфа и интерлейкина 1-бета, фактора некроза опухоли альфа, гамма-интерферона и др.). Воспалительные заболевания кишечника Воспалительные заболевания кишечника (ВЗК), прежде всего, неспецифический язвенный колит (НЯК) и болезнь Крона (БК), часто сопровождаются развитием анемии. Частота анемии при ВЗК, по данным литературы, достаточно вариабельна и колеблется от 6% до 74% [17]. В большинстве исследований это значение составляет 35–50% [9, 12, 13, 19, 25, 27]. С несколько большей частотой анемия выявляется у больных НЯК. Так, S.?Schreiber и соавт. [26] сообщили о наличии анемии у 25% больных с БК и 37% больных с НЯК. В развитии анемии при ВЗК всегда играют роль несколько механизмов. Условно можно выделить следующие группы причин возникновения анемии при ВЗК [2, 4, 7, 13, 17, 18, 20]: Наиболее часто у больных ВЗК комбинируются АХЗ и железодефицитная анемия [1, 4, 17, 18], однако роль других факторов тоже велика и выраженность анемии может усиливаться вследствие повторных эпизодов кровотечения, дефицита витаминов и нутриентов, влияния лекарственных препаратов. Анемия хронических заболеваний была впервые описана Maxwell Wintrobe и George Cartwright в 1949 году. Основными критериями ее диагностики являются снижение уровня сывороточного железа и насыщения трансферрина железом при сохранных запасах железа в ретикулоэндотелиальной ткани (нормальный уровень ферритина). Успехи в расшифровке основных механизмов АХЗ привели к повышенному вниманию к этому виду анемии, в том числе и в педиатрии. Установлено, что на долю АХЗ приходится около 10–20% всех анемий. На сегодняшний день главным звеном в патогенезе АХЗ считается гиперпродукция провоспалительных цитокинов. Они приводят к угнетению синтеза эритропоэтина и значительно снижают его эффекты, направленные на усиление пролиферации и созревания эритроидных предшественников [1–4, 13]. Нарушение метаболизма железа при АХЗ во многом опосредовано экспрессией гепсидина. Гепсидин — это белок острой фазы воспаления, который синтезируется печенью в ответ на воздействие липополисахаридов бактерий и интерлейкина 6. Гепсидин снижает всасывание железа в двенадцатиперстной кишке, блокирует высвобождение железа из макрофагов и снижает способность красного костного мозга его усваивать. Недостаточное поступление железа в эритроидные клетки приводит к нарушению их созревания и снижению синтеза гема [3, 14]. Участие провоспалительных цитокинов в генезе АХЗ при ВЗК обусловлено как прямым их ингибирующим действием (в первую очередь, гамма-интерферона) на созревание эритроидных клеток и усилением процессов апоптоза, так и опосредованными эффектами: подавлением синтеза эритропоэтина, снижением чувствительности к нему эритроидных клеток, активацией синтеза гепсидина и нарушением утилизации железа, а также усилением свободно-радикальных реакций [5, 10, 14]. В течение последних двадцати лет в отделении гастроэнтерологии Российской детской клинической больницы (РДКБ) наблюдалось 155 пациентов с НЯК и 61 пациент с БК. Анемия выявлялась у 35% детей с НЯК и имела железодефицитный характер, обусловленный преимущественно хронической кровопотерей. В 69% случаев анемия была легкой степени, в 27% — среднетяжелой, а в 4% — тяжелой. Тяжесть анемии в значительной степени зависела от обширности поражения толстой кишки и выраженности язвенного процесса. Снижение уровня гемоглобина (110 г/л ≤ Hb А. В. Малкоч*, кандидат медицинских наук *РГМУ, **Российская детская клиническая больница, Москва источник Колит – это воспалительное заболевание толстой кишки, возникшее вследствие инфекционного, ишемического, лекарственного или иного поражения. Колиты протекают с болевым синдромом, расстройством пищеварения (запорами, поносами), метеоризмом, тенезмами. В рамках диагностики производится исследование кала (копрограмма, бакпосев, на гельминтов и простейших), ирригоскопия, колоноскопия с биопсией слизистой толстого кишечника. Лечение назначается с учетом этиологической формы болезни, включает диету, этиотропную (антибактериальную, противогельминтную и другую терапию), прием ферментов и эубиотиков, фитотерапию, физио- и бальнеотерапию. Колитами называют заболевания пищеварительной системы, характеризующиеся развитием воспаления в слизистой оболочке стенки толстой кишки. Различают острый и хронический колит. Для острого колита характерны боли в животе, метеоризм, наличие слизи и прожилок крови в кале, тошнота, позывы к акту дефекации. Могут развиться хроническая форма, язвенное поражение кишечника, кровотечения, иногда канцерофобия. Хронический колит представляет собой патологические изменения в строении слизистой оболочки в результате продолжительного воспалительного процесса и дистрофии пораженных тканей, в связи с которыми возникают нарушения моторной и секреторной функции толстого кишечника. Хронический колит — довольно часто встречающееся заболевание пищеварительного тракта, нередко воспаление толстой кишки сопровождается поражением тонкого кишечника. Порядка трети больных хроническим колитом отмечают в качестве причины его развития различные кишечные инфекции (чаще всего дизентерию и сальмонеллез). Во многих случаях заболевание развивается на фоне дисбактериоза (к примеру, после продолжительного курса антибиотикотерапии), в связи с неправильным питанием, склонностью к гиподинамии, злоупотреблением алкогольными напитками. Причины возникновения патологии могут быть связаны с нарушением режима и характера питания (неправильные пищевые привычки, нерегулярное нерациональное питание, злоупотребление алкоголем, прием некачественной пищи). Колиты могут возникать как осложнение заболеваний желудочно-кишечного тракта (хронического гастрита, панкреатита, гепатита), а также при пищевых отравлениях и заражении кишечными инфекциями. Прием многих лекарственных средств может оказывать негативное действие на кишечную флору, ятрогенный дисбактериоз может в свою очередь вызывать воспалительные процессы в толстом кишечнике. Кроме того, колитам могут поспособствовать препараты, нарушающие кислотно-щелочной баланс в просвете кишечника. Иногда причинами воспалительных заболеваний кишечника являются врожденные патологии развития и функциональная недостаточность. Колиты подразделяются на инфекционные (колит при шигеллезе, сальмонеллезе, микобактериоз, туберкулезный колит и т.д.), алиментарные (связанные с нарушениями питания), токсические экзогенные (при продолжительных интоксикациях парами ртути, соединениями фосфора, мышьяка и т. д.) и эндогенные (при интоксикации продуктами катаболизма, например, уратами при подагре), лекарственные (развившиеся после применения лекарственных средств: слабительных, аминогликозидов, антибиотиков). Выделяют также аллергические (аллергическая реакция на пищевые компоненты, лекарственные средства, некоторые бактерии или продукты их метаболизма) и механические (при хронических запорах, злоупотреблении клизмами, ректальными суппозиториями в результате регулярного механического раздражения слизистой) колиты. Зачастую имеет место несколько этиологических факторов, способствующих развитию воспаления в толстом кишечнике, тогда можно говорить о комбинированном колите. Для хронического воспаления характерны такие клинические проявления, как боль в животе, расстройство дефекации, тенезмы. Болевой синдром при колите характеризуется тупой ноющей болью в нижних и боковых частях живота (часто с левой стороны), либо больной не может достаточно четко локализовать источник боли (разлитая боль в животе). После еды обычно боль усиливается и ослабляется после дефекации и отхождения газов. Кроме того, провоцировать усиление боли может ходьба, тряска, очистительная клизма. Также может отмечаться чувство тяжести в животе, вздутие, метеоризм. Расстройства стула чаще всего протекают в виде запоров, но может отмечаться и чередование запоров и поносов. Для хронических колитов характерен понос с выделением водянистого кала с прожилками слизи (иногда может отмечаться кровь). Могут возникать тенезмы – ложные позывы к дефекации. Иногда позыв к дефекации заканчивается выделением слизи. При остром воспалительном процессе все перечисленные выше симптомы выражены более ярко, диарея преобладает над запорами. Воспаление толстого кишечника чаще всего развивается в ее терминальных отделах (проктит и проктосигмоидит). Зачастую причиной колита в таких случаях является острая кишечная инфекция (дизентерия) или хронические запоры. Кроме того, проктосигмоидит является нередким результатом злоупотребления очищающими и лечебными клизмами, приема слабительных средств. При этой форме колита боль локализуется с левой подвздошной области, возникают частые и болезненные тенезмы, особенно по ночам. Стул, как правило, скудный, может быть наподобие овечьего кала, содержать в больших количествах слизь, реже кровь и гной. При пальпации живота отмечают болезненность в области проекции сигмовидной кишки. Иногда пальпируется врожденная аномалия развития – дополнительная петля сигмы.
Анатомические и функциональные особенности толстого кишечника визуализируются его при контрастной ирригоскопии. Колоноскопия позволяет досконально изучить состояние слизистой на всем протяжении толстой кишки. Кроме того, проведение колоноскопии позволяет взять биоптаты слизистой кишечной стенки для дальнейшего гистологического исследования. Для исключения геморроя, анальной трещины, парапроктита и других патологий показан осмотр проктолога с пальцевым исследованием заднего прохода. Дифференциальная диагностика хронических колитов проводится с дискинезией толстого кишечника. Однако, необходимо помнить, что продолжительно существующее расстройство моторики кишечника может осложниться воспалительным процессом. Довольно часто клиническая картина колита может сопровождать развивающуюся опухоль толстого кишечника. Для исключения злокачественных образований производят биопсию всех подозрительных участков стенки кишечника. Кроме того, производят дифференциацию колитов и энтеритов. Иногда имеет место воспаление обоих отделов кишечника. Данные для дифференциальной диагностики хронического колита и заболеваний верхних отделов пищеварительного тракта дают эндоскопические исследования (колоноскопия, фиброгастродуоденоскопия), УЗИ органов брюшной полости и функциональные пробы для выявления маркеров воспаления печени и поджелудочной железы. Колит может привести к перфорации кишечной стенки с развитием перитонита (характерное осложнение тяжело протекающего неспецифического язвенного колита), кишечному кровотечению, которое способствует развитию анемии, непроходимости кишечника в результате формирования спаек, стриктур, рубцов. Хронический колит в период обострения целесообразно лечить в стационаре, в отделении проктологии. Колиты инфекционной природы лечат в специализированных инфекционных отделениях. Значительным элементом в лечении хронического колита является соблюдение лечебной диеты. При этом из рациона исключают все продукты, которые могут механически или химически раздражать слизистую оболочку кишечника, пищу употребляют в протертом виде, с частотой не менее 4-5 раз в день. Кроме того, для исключения молочнокислого брожения больным рекомендуют отказаться от молока, с целью снижения газообразования ограничивают капусту, бобовые. Из хлебобулочных изделий разрешен подсушенный пшеничный несладкий хлеб. Мясо и рыбу нежирных сортов желательно употреблять приготовленными на пару. При стихании выраженной клинической симптоматики диету постепенно расширяют. Для борьбы с запорами рекомендуют включение в рацион вареных овощей, фруктовых пюре (киселя), хлеба с отрубями. Улучшению прохождения кишечных масс способствует растительное масло и достаточное количество употребляемой в сутки жидкости. Употреблять фрукты и овощи в сыром виде в острый период заболевания нежелательно. Также стоит отказаться от охлажденных блюд, молочнокислых продуктов и пищи с высоким содержанием кислоты. Для регуляции секреции жидкости в кишечнике ограничивают употребление поваренной соли. В случае инфекционной природы колита и для подавления патогенной бактериальной флоры, развившейся в результате дисбактериоза, назначают антибиотикотерапию короткими курсами (препараты ципрофлоксацин, Нифуроксазид, рифаксимин). Назначения лекарственных средств производится только специалистом. Выявления яиц глистов является показанием к назначению противогельминтных средств. Для облегчения болевого синдрома назначают спазмолитические средства (дротаверин, папаверин). При лечении проктосигмоидита полезна местная терапия: микроклизмы с отварами ромашки, календулы, с танином или протарголом. При проктите назначают ректальные суппозитории с белладонной, анестезином для снятия выраженной болезненности, вяжущие средства (окись цинка, ксероформ). При поносах вяжущие и обволакивающие средства назначаются внутрь (танин+альбумин, нитрат висмута, белая глина, отвар коры дуб, другие отвары и настои сборов, содержащие дубильные компоненты). При запорах показано проведение гидроколонотерапии. Сильные спазмы при колите могут стать показанием для назначения холинолитиков. Помимо вышеперечисленных средств, при колитах могут назначать энтеросорбенты (для борьбы с метеоризмом), ферментные препараты (при нарушении пищеварения в результате ферментных недостаточностей), эубиотики (для коррекции дисбиоза). Хороший эффект при терапии хронических колитов дает регулярное санаторно-курортное лечение, бальнеотерапия. В комплекс профилактических мер для предотвращения колитов входит сбалансированная рациональная диета, своевременное выявление и лечение заболеваний пищеварительной системы, меры санитарно-гигиенического режима и соблюдение правил техники безопасности на производствах, связанных с опасными химическими ядами. Профилактика обострений у лиц, страдающих хроническими заболеваниями толстого кишечника, кроме того, включают регулярное диспансерное наблюдение специалиста в области клинической проктологии. Трудоспособность больных с данной патологией ограничена, им стоит избегать избыточных физических нагрузок, психо-эмоциональных стрессов и деятельности, связанной с частыми командировками и способствующей нарушению режима питания. Прогноз при своевременном выявлении и соблюдении врачебных рекомендаций по лечению хронического колита благоприятный. источник Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам. У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования. Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter. Причины развития хронического колита
источник Колит представляет собой острый или хронический воспалительный процесс, протекающий в толстом кишечнике, который возникает по причине токсического, ишемического или инфекционного поражения органа. В представлении среднестатистического обывателя без особых медицинских знаний колит ассоциируется с кишечной коликой. Однако два этих состояния далеко не одинаковы. Кишечная колика — это дискомфортное приступообразное болевое ощущение в нижней части живота. Колика — всего лишь симптом, характеризующий огромное число заболеваний и патологий, от банального метеоризма до онкологических процессов. Колит же, в свою очередь, самостоятельное заболевание, отличающееся собственной этиологией, симптоматикой и особенностями протекания. Чтобы лучше понять, что собой представляет эта патология, необходимо обратиться к основам анатомии желудочно-кишечного тракта. Кишечник подразделяется на два отдела: толстый кишечник и тонкий кишечник. Каждый обладает собственными пищеварительными функциями. Тонкий отдел начинается сразу же после желудка и в нем происходят основные пищеварительные процессы (в том числе окончательная переработка пищи, выделение питательных веществ и транспортировка их в кровеносное русло через стенки органа). От толстого кишечника тонкий отделен слизистой мембраной. Благодаря ей, отходы жизнедеятельности и микроорганизмы из толстого кишечника не поступают в предыдущий отдел. В толстом кишечнике происходит окончательная переработка пищи и всасывание жидкости. Не последнюю роль в этом процессе играют особые бактерии (в толстой кишке их объем достигает порядка 1,5 кг или даже больше). В толстой кишке помимо «полезных» бактерий (которые способствуют переработке остатков пищи) обитают также и патогенные организмы. Эти микроорганизмы в ходе жизнедеятельности вырабатывают огромное количество активных веществ, обладающих высоким токсическим потенциалом. Если в результате потребления некачественной пищи или по иным причинам концентрация патогенной микрофлоры в органе растет, слизистая толстой кишки воспаляется. Так проявляется иммунная реакция, дабы предотвратить проникновение токсинов в кровеносное русло. Развивается колит. В ряде случаев патогенная микрофлора может проникнуть в тонкую кишку, в таком случае развивается ещё более тяжелая форма патологии — энтероколит. Нужно заметить, если в тонкий кишечник попадет условно полезная микрофлора, энтероколит не разовьется и все ограничится дискомфортными ощущениями и вздутием живота. Этиология колита не ограничивается инфекцией. Тем же эффектом обладают некоторые медикаменты (побочный эффект), также колит может сопутствовать некоторым другим патологическим процессам. Первые признаки острого и хронического колита существенно отличаются по интенсивности и степени нарастания симптоматики. Колит в острой фазе отличается стремительным нарастанием проявлений и их высокой интенсивностью. Однако это не аксиома, и многое зависит от индивидуальных особенностей организма больного (в частности особенностей иммунной системы). У одних пациентов симптомы проявляются ярко, болезнь протекает тяжело. У других же отмечается незначительный дискомфорт, и патология характеризуется вялым течением. Важными факторами помимо особенностей иммунной системы являются: возраст больного, степень токсического, инфекционного или ишемического поражения кишечника, наличие иных сопутствующих патологий. Среди симптомов наиболее характерны следующие: Дискомфортные и болевые ощущения . Часто сопровождают заболевание, усиливаются после терапевтических процедур (клизм), приема пищи, механического воздействия (например, тряски в транспорте), ходьбы или бега. Расстройство и нестабильность стула. Это проявление нельзя назвать основным или характерным только для колита кишечника. Поносы и запоры, а также их попеременное чередование характеризует большинство расстройств ЖКТ, от холецистита до отравления ботулотоксином. Главное отличие стула при колите — наличие в нем бесцветных или зеленоватых слизистых прожилок или примесей крови. Ложные позывы к дефекации (т.н. тенезмы). Характерны не только для колита, но также и для ряда других заболеваний, таких как, например, проктосигмоидит (воспаление сигмовидной и тонкой кишки) или проктит. Выделения скудные, слизистые. При развитии колита в толстой кишке — позывы относительно редки, беспокоят пациентов не чаще 2-3 раз в день. Однако если процесс локализуется в прямой, либо сигмовидной кишке — позывы более мучительны, чаще возникают ночью и оканчиваются малым количеством выделяемых каловых масс (по типу «овечий кал») с обильными примесями крови, слизи, гноя. Если лечение было начато несвоевременно, либо проведено неправильно, болезнь может затихнуть, перейдя в хроническую форму. Обострения могут возникать до нескольких раз в год. Симптоматика схожа с острым колитом. Даже на стадии ремиссии в 35-40% случаев наблюдаются вялые проявления. Метеоризм (повышенное газообразование). Проблемы со стулом. В 80% случаев речь идёт о тяжелых спастических запорах, что связано с недостатком «полезной» микрофлоры и нарушением перистальтики кишечника. Урчание в животе, возникающее спустя несколько часов после приема пищи. Слабо выраженные болевые ощущения в животе после физической нагрузки или стресса. — Кожная сыпь, обусловленная токсическим поражением организма из-за нарушений выведения кала. Симптоматика усиливается в периоды обострений. Частным случаем колита кишечника выступает язвенный колит. Его главное отличие — наличие язвенных дефектов на стенках слизистых оболочек (вплоть до перфорации), что обуславливает куда более тяжелое течение патологии. Язвенный колит отличается особой симптоматикой. Частые ложные позывы к дефекации . В начале процесса — скудные поносы (до 15-20 раз в день), невозможность удержать стул. Симптом наблюдается более чем у половины больных (55-60%). Посторонние примеси в стуле . Кровь, зеленоватая слизь, ленты гноя. Выделение крови варьируется от незначительного (обнаруживается только на туалетной бумаге) до обильного, видного невооруженным глазом в кале. Внезапные запоры , свидетельствующие о воспалении отделов тонкого кишечника. Встречается, примерно, у четверти пациентов. Проявления интоксикации организма . Проявления схожи с ОРВИ. При тяжелых поражениях наблюдается усиленное сердцебиение (тахикардия), общая слабость, повышение температуры тела, тошнота, рвота, пониженный аппетит. Поносы также могут привести к обезвоживанию организма. В некоторых случаях могут развиваться симптомы, не связанные с поражениями желудочно-кишечного тракта . Нарушения зрения, кожная сыпь, зуд слизистых, образование тромбов, боли в суставах. Кроме того, могут страдать печень и желчный пузырь. Болевые ощущения при колите толстой кишки носят ноющий либо тупой характер. Иногда пациенты жалуются на распирающие боли. Неприятные ощущения могут быть стойкими и мучительными, однако чаще всего боли проявляются периодами (схваткообразность). Локализация боли различается от случая к случаю. Часто локализацию определить невозможно, боль разливается по всему животу или блуждает. На начальном периоде дискомфорт возникает в нижней левой части живота. Боль иррадиирует в спину, крестец, левую часть грудной клетки. По этой причине часто пациент не может самостоятельно определить источник боли, принимая колит за проблемы с позвоночником или сердцем. После приема препаратов (спазмолитических, холинолитических), отхождения кишечных газов, дефекации, согревания пораженного места боли ослабевают, однако спустя некоторый период времени вновь возвращаются. У некоторых больных отхождение газов, наоборот, приводит к усилению болевых ощущений. В данный момент причины колита кишечника до конца неизвестны. Проводятся многочисленные научные исследования, однако ученые до сих пор не пришли к единому мнению. Несмотря на это, можно назвать ряд провоцирующих факторов. Они выступают триггерами, инициирующими начало патологического процесса. Инфекционные поражения организма . Вполне тривиальна ситуация, когда человек потребляет некачественные просроченные продукты питания. Пищевые отравления вызываются патогенной микрофлорой, которая активно размножается в кишечнике. Кроме того, при иных условиях человек может стать носителем кишечной инфекции, холерного вибриона, дизентерийной амебы, сальмонеллы, иных инфекционных агентов. Такими агентами могут стать бактерии туберкулеза, шигеллеза. Во всех случаях патогенные микроорганизмы выделяют токсины, раздражающие стенки кишечника и вызывающие специфические симптомы. Несмотря на происхождение заболевания в данном случае, колит, вызванный инфекцией, считается незаразным. Нарушение питания (алиментарные причины развития колита). На бытовом уровне колит, вызванный нарушением режима потребления пищи, называется «расстройство желудка». Алиментарный колит вызывается избыточным потреблением фаст-фуда, нерегулярным питанием, злоупотреблением алкоголя, недостатком потребляемой клетчатки, недостаточным употреблением «полезной» пищи (овощей, фруктов, натуральных мясных продуктов) и т.д. Генетические факторы . Некоторые генетические мутации могут обусловить врожденные нарушения работы кишечника. Наличие сопутствующих патологий . Холецистит, гепатит, панкреатит, различные формы гастрита способствуют нарушению работы кишечника и развитию колита. Тот же эффект производит снижение иммунитета и ослабление организма после перенесенных вирусных заболеваний. Прием медикаментов. Многие лекарства негативно воздействуют на кишечную микрофлору и снижают перистальтику кишечника. Антибиотики, противовоспалительные препараты, аминогликозоидные препараты, слабительные, препараты для контрацепции и др. Токсические отравления . Могут носить как экзогенный характер (отравления солями ртути, фосфором, мышьяком), так и эндогенный (например, отравление солями-уратами при подагрическом поражении). Аллергическая реакция . Пищевые и иные формы аллергии способствуют нарушению работы кишечника. Механическое воздействие . Злоупотребление очистительными клизмами или свечами приводит к нарушению работы кишечника по причине постоянного раздражения слизистой оболочки кишечника. Острая форма колита кишечника вызывается одной из названных выше причин и протекает в большинстве случаев стремительно с постепенным нарастанием характерных симптомов. Чаще всего острый колит провоцируется пищевым отравлением, аллергической реакцией (в результате которой разрушаются тучные клетки-базофилы и в большом количестве выделяется гистамин, нарушающий целостность клеток слизистой оболочки кишечника, в результате чего кишечник раздражается) или избыточным приемом некоторых медикаментов. Заболевание начинается с развития гипертермии (температура повышается до отметок 37.2-38.1 градус). Больной испытывает слабость, следом за температурой возникают схваткообразные боли и спазмы в животе. Толстая кишка по всей длине болезненна и при надавливании отзывается тупой болью. Позывы к дефекации частые, сопровождаются скудными выделениями слизи или небольшого количества жидкого кала. Болевые приступы сопровождаются потливостью, головокружением, бледностью кожных покровов. Наблюдается картина интоксикации организма. Помимо специфической симптоматики наблюдаются и общие явления со стороны организма. Резкое падение массы тела на 2-6 кг. Периодическое повышение температуры тела. Сонливость и утомляемость. Эти явления могут сохраняться достаточно длительный срок после перенесенного острого колита (до 10-25 дней). Если адекватное лечение патологии не было проведено с первых же дней — колит может перейти в хроническую форму с периодическими рецидивами. При переходе заболевания в иную форму симптомы также ослабевают и исчезают сами собой. Гастроэнтерологи сходятся во мнении, что основной причиной колита кишечника выступает нарушение рациона питания. Поэтому среди лиц в возрасте от 25 до 40 лет колит распространен гораздо шире, чем можно предположить. В ряде случаев в хроническую форму переходят колиты, вызванные: Осложнениями перенесенных инфекционных заболеваний кишечника (сальмонеллеза, холеры, кишечной формы гриппа и т.д.); Длительным воздействием на организм солей тяжелых металлов и токсичных неметаллов (характерно для лиц, работающих на вредных промышленных предприятиях); Дисбактериозом, в результате которого нарушается концентрация полезной микрофлоры и перистальтика кишечника; Ферментативной недостаточностью в результате заболеваний желчного пузыря, поджелудочной железы и желудка. Однако первичной причиной остается неправильное питание. Недостаток клетчатки в рационе приводит к снижению секреции слизи и нарушению нормальной эвакуации каловых масс из толстой кишки. Застой кала в кишечнике приводит к раздражению и воспалению слизистой. Существенную роль в развитии колита играет неправильная диета (потому дополнительно особую группу риска составляют женщины). Хронической форме не обязательно предшествует ярко выраженная острая фаза. Возможна ситуация, при которой будет наблюдаться один единственный симптом острой формы, и то очень вялый. В других случаях симптомов может вовсе не быть, тогда патология протекает в обратном порядке. Яркое и тяжелое течение хронического колита возможно только на запущенном этапе. Первые симптомы, на которые следует незамедлительно обратить внимание: Если не провести необходимое лечение, заболевание сформируется окончательно, а проявления стихнут. Внезапно и из ниоткуда хронический кишечный колит не появляется. Чтобы болезнь проявилась «во всей красе» нужен триггер, спусковой механизм. Таким триггером может стать пищевое отравление, инфекция, травма, приступ аллергии и др. Только у 10-12% от всего числа пациентов после развития триггера колит не проявляется, а затихает и постепенно самопроизвольно излечивается, в остальных случаях эта неприятная патология становится пожизненным спутником человека. В периоды обострения налицо картина острой формы патологии, однако, как было сказано, специфические симптомы (хоть и в ослабленном виде) сопровождают больного даже в период ремиссии. Язвенный колит кишечника представляет собой воспаление слизистой оболочки толстой кишки, сопровождающееся изъязвлениями её поверхности, отеком и дегенеративными изменениями эпителия оболочки. В группу повышенного риска входят молодые люди в возрасте от 20 до 40 лет, а также лица старшего возраста (после 50-55). Для патологического процесса характерно изъязвление стенок толстого кишечника на всем протяжении органа. Этиология данного типа колита до конца неизвестна, в данный момент выдвигается ряд теорий: Инфекционная. Основывается на том, что язвенный колит кишечника — вызывается вирусом либо бактерией. Точный штамм, однако, неизвестен. Генетическая. Гласит, что язвенный колит представляет собой аутоимунное заболевание, при котором клетки выделяют антитела, разрушающие клетки эпителия слизистой кишечника (наподобие того, как вырабатываемые антитела против йодосодержащих веществ разрушают клетки-тиреоциты щитовидной железы при аутоимунном тиреодите Хашимото). Наследственная. Согласно данной теории язвенный колит передается по наследству и обусловлен агрессивными факторами внешней среды, воздействовавшей на родителей. Заболевание вызывается следующими триггерами: Рацион, богатый углеводами; Недостаток клетчатки в рационе; Заболевание протекает в трех основных формах: легкой, средней и тяжелой. При легкой степени поражения, стенки кишечника не подвергаются серьёзному изъязвлению. Болезнь практически ничем не даёт о себе знать, кроме небольших прожилок слизи и крови в стуле. Симптоматика, специфическая для колита, может отсутствовать вообще. Средняя степень протекания патологии характеризуется повышением температуры тела (максимум до 38.1), схваткообразными болевыми ощущениями и общим недомоганием. Позывы к дефекации возникают 4-6 раз в сутки, преимущественно в ночное время. Тяжелая степень протекает при высокой температуры (свыше 38.1) на фоне расстройств сердечнососудистой системы (тахикардия). Наблюдается бледность кожи, неровность дыхания. Боли в животе сильные, схваткообразные. Позывы не реже 7-10 раз в день. Боли особенно выраженные непосредственно перед актом. В особо тяжелых случаях возможно развитие перфорации кишечника с последующим сепсисом, перитонитом и массивным кровотечением. Спастический колит отличается от иных типов данной патологии значительно сниженной функцией толстой кишки по причине недостаточной перистальтики. В отличие от язвенного колита, спастический тяжелой патологией не считается и относится, скорее, к расстройству функций кишечника. В норме акты дефекации происходят с определенной частотой. Для кого-то нормой считается 1 раз в день, для других — 1 раз в неделю. При спастическом колите основным симптомом является стойкий запор. Тяжесть протекания заболевания всё же сугубо индивидуальна и у двух пациентов симптоматика будет абсолютно различной. Симптоматика, в целом, схожа с иными формами и включает в себя: Резкое чередование запоров и поносов с преобладанием последних; Большую часть времени сохраняется запор; повышенная продукция газов. Спастический кишечный колит проходит легче, потому состояние пациентов можно охарактеризовать как удовлетворительное. При пальпации толстой кишки, а также проведении ультразвуковой диагностики хорошо видны спазмированные участки толстой кишки. Для данного типа заболевания характерны изменения кишечника. В одних участках он чрезмерно расширен, в других — напротив, сужен. Длительное заболевание вызывает постепенные атрофические изменения гладкой мускулатуры толстой кишки, вызванные снижением работы. Тонус кишечника падает, по всей протяженности органа наблюдается выделение слизи, отечность. Данные признаки обнаруживаются при ректороманоскопии. Если обнаружены дегенеративные или атрофические процессы, необходима более тщательная диагностика, поскольку в этом случае стенки кишечника становятся сухими, начинают трескаться. Трещины можно принять за язвы, отличающие язвенный колит. По этой причине важно учитывать комплекс симптомов и факторов в совокупности с данными инструментальной диагностики для точной постановки диагноза. Катаральный колит — скорее не самостоятельный тип данной патологии, а этап в её развитии. Катаральный колит представляет собой начальный этап формирования патологического процесса. По длительности катаральный тип протекает в 2-3 дня сроком и отличается выраженной симптоматикой. Кроме того, катаральный колит может быть не началом заболевания, а всего лишь проявлением (например, пищевого отравления) который при грамотном лечение сойдет на нет и не перейдет в хроническую форму. Симптомы данного типа колита: Постепенное воспаление слизистой оболочки кишечника вызывает нарастающее чувство дискомфорта в подвздошной области, в левой нижней части живота или в области лобка. Воспаленный кишечник увеличивается в размерах, в связи с чем больной ощущает сильную тяжесть и вздутие живота. В стуле обнаруживается большое количество кровянистых выделений, что свидетельствует о процессе дегенерации слизистой. Поврежденные участки подвергаются некрозу, потому даже по окончании острой фазы дисфункции кишечника, а также болевые ощущения будут сохраняться. Для катарального колита, как и любого иного типа характерны общие проявления, вроде симптомов интоксикации (слабость, головная боль, раздражительность и усталость, сонливость и др.), запоров или поносов, частых тенезмов, болевых ощущений и др. Катаральный колит легко выявить даже неспециалисту без медицинской подготовки, поэтому особых диагностических манипуляций кроме сбора анамнеза для постановки общего диагноза не требуется. Следует внимательно отнестись к лечению катарального типа патологии, поскольку она склонна к быстрому прогрессированию и спустя 8-10 дней переходит в фибринозный тип, а ещё через неделю-полторы может начать переходить в язвенный тип. Атрофический колит часто идёт рука об руку со спастическим колитом и развивается на более поздних стадиях. Суть патологического процесса заключается в атрофии гладкой мускулатуры толстой кишки по причине длительного застойного процесса. Нужно отметить важный момент. Если иные типы колита кишечника поражают как толстый, так и тонкий кишечник, атрофический колит характерен только для толстой кишки. Часто вместе с атрофическим колитом диагностируется гастрит, однако неизвестно, если ли между данными заболеваниями причинно-следственная связь. Симптоматика схожа с иными типами и не имеет особых проявлений. С течением времени атрофический колит может перейти в язвенную форму, поскольку слизистая оболочка толстой кишки с течением времени истончается, а количество патологических микроорганизмом в органе не снижается, что может привести к быстрой дегенерации эпителиальной ткани. В особо запущенных случаях все может закончиться перфорацией толстой кишки и тяжелыми осложнениями, вроде сепсиса или сильного кровотечения. Сложность данного заболевания заключается в сложности диагностических мероприятий. Только грамотный и внимательный врач-специалист способен верно дифференцировать диагноз. Эрозивный колит не всегда выделяется специалистами в качестве отдельного типа. Вернее было бы говорить о данном типе, как о начальной стадии развития язвенного колита. Единственное и главное отличие — эрозивные изменения носят незначительный характер и не оканчиваются перфорацией, однако симптоматика достаточно характерна, чтобы выделить эрозивный колит без особых сложностей. Практически всегда, независимо от индивидуальных особенностей организма эрозивный колит представлен всем комплексом типичных проявлений, среди которых: Тошнота (пациента «мутит»), возможна рвота. Тяжесть в животе (локализуется, преимущественно, в области желудка). Боли в желудке. Неопытный врач из-за этого симптома может принять эрозивный колит за одну из форм гастрита и назначить в корне не верное лечение. Металлический кисловатый привкус во рту. Отрыжка и изжога (также обычно характерны для гастрита с повышенной кислотностью). Кроме комплекса симптомов, которыми сопровождается эрозивный колит, заболеванию сопутствуют и типичные для любого колита симптомы, вроде нарушения стула и т.д. Диффузный колит кишечника чаще всего затрагивает сразу оба отдела, протекая тяжело. Поскольку колит поражает и толстый, и тонкий кишечник, симптомы ярко проявляются с первого же дня. В симптоматике присутствуют как признаки гастрита, так и признаки энтерита. Диагностировать диффузный колит, как правило, не так сложно при наличии минимальной медицинской подготовки. Данный тип патологии отличается рядом симптомов: Болевые ощущения. Боли при диффузном типе колита не локализуются в каком-либо одном участке, а разливаются по всему животу. Часто наблюдается перемещение неприятных ощущений из одной части живота в другую (блуждающая боль). В ряде случаев на второй-третий день боли приобретают различимый характер и располагаются в нижней левой или нижней правой части живота. В последнем случае следует дополнительно провести функциональные пробы на аппендицит. Боли ноющие или тупые, носят коликообразный характер. Боль может иррадиировать в область сердца. Вкупе с сердцебиением это даёт основания пациенту предполагать патологии сердца, а не ЖКТ. Часто при выявлении диффузного типа наблюдается не снижение аппетита, а его полное отсутствие. Очень частые тенезмы. В первый день — обильный понос с характерными примесями. После акта дефекации болевые ощущения усиливаются, однако не сразу, а спустя 1.5-2 часа. На 2-3 день понос продолжается. Выделяется незначительное количество жидкого с крайне неприятным запахом кала. Почти всегда понос начинается в ночное время суток, обычно — 5-7 часов утра (т.н. «понос-будильник»). Тошнота, рвота. Позывы к рвоте сохраняются даже при пустом желудке. Клиническая картина противоречива. На рентгенологическом исследовании с контрастным веществом видны как участки сужения, так и патологического расширения кишечника. Перистальтика может как в разы ускориться, так и быть угнетенной. Язык больного обложен серым или желтоватым налетом. При пальпации отмечаются жесткие, спазмированные участки, при пальпации больные указывают на болевые ощущения. Колит кишечника, несмотря на несерьезные на первый взгляд проявления, а также относительную легкость лечения способен вызывать грозные осложнения. Острый колит, как было сказано, в отсутствии должной терапии в 90% случаев переходит в хроническую неизлечимую форму и на протяжении всей жизни преследует пациента.
У взрослых людей и острый, и хронический колит могут стать причиной развития четырех тяжелых последствий: Язвы формируются преимущественно при застарелой форме хронического колита, когда агрессивный агент постоянно воздействует на слизистую стенку кишечника. Язвы могут привести к перфорации стенки и выходу содержимого кишечника за его пределы. В результате перфорации быстро развивается обильное внутреннее кровотечение, требующее незамедлительного хирургического вмешательства. Без медицинской помощи пациент рискует погибнуть от потери крови. Кроме того, в результате перфорации содержимое кишечника оказывается в брюшной полости и вызывает инфекционное заражение, также способное привести к летальному исходу. Сепсис. Кишечник имеет развитую и сложную кровеносную систему, потому любое повреждение стенок органа влечет одновременно и повреждение кровеносных сосудов. Каловые массы богаты вредными веществами и патогенными организмами, которые, попав в кровь, могут вызвать её заражение. Особенно высок риск сепсиса при инфекционной причине кишечного колита. Кроме того, колит, в особенности хронический, всегда сопровождается застойными процессами в толстом кишечнике. Как итог — вредные вещества вовремя из организма не выводятся и всасываются обратно в кровь, отравляя организм. У больных постоянно наблюдаются признаки интоксикации: слабость, головная боль, нарушения аппетита и др. Также колит способен привести к обезвоживанию организма, поскольку большая часть воды не успевает усвоиться в толстом кишечнике и выходит с частыми поносами. Достаточно частым и опасным последствием колита является кишечная непроходимость. Поскольку перистальтика кишечника ослабевает, каловые массы не эвакуируются из организма и приобретают каменистую структуру. Постепенно накапливаясь, они способны вызвать полное закрытие просвета кишечника. В этом случае без оперативного вмешательства в кротчайшие сроки не обойтись. Современная медицина обладает широким спектром лабораторных и инструментальных методов исследования. С их помощью можно определить наличие патологии, её стадию и форму. К лабораторным методам дифференциальной диагностики колита относят: Общий анализ крови. Клиническая картина кишечного колита характеризуется воспалительным процессом, а это значит в крови будет определяться высокая скорость оседания эритроцитов (СОЭ), значительная концентрация тромбоцитов, лейкоцитоз, низкий уровень гемоглобина. Анализ кала (копрограмма). В кале может наблюдаться содержание крови, лейкоцитов и эритроцитов. Посевы испражнений на инфекционные и бактериальные агенты (дизентерия, холера, туберкулез и др.). Диагностика ПЦР. Позволяет выявить гельминтоз, а также вирусные поражения кишечника. Анализ на наличие специфических антител к цитоплазме клеток-нейтрофилов (pANCA) позволяет определить наличие генетических аутоиммунных патологий, которые снижают эффективность работы кишечника. Анализ на фекальный кальпротектин. Проводится с целью выявления Болезни Крона, вторичным признаком которой может выступать колит. К инструментальным методам дифференциальной диагностики колита относят: Контрастная ирригоскопия. В ходе исследования в прямую кишку больного вводится контрастное вещество. Через некоторое время проводится рентгенография, позволяющая оценить степень функциональных нарушений органа. Ирригоскопия даёт возможность исключить разрастание опухолей, стеноз стенок кишечника и т.д. Фиброилеоколоноскопия . Эндоскопический осмотр кишечника. Позволяет определить дислокацию патологического процесса, его характер и стадию, а также взять биологический материал на исследование (чтобы исключить злокачественные новообразования и возможность их формирования) . Ультразвуковое исследование. Проводится с целью выявить изменения просвета кишки или стенок органа. Осмотр проктолога с пальцевым исследованием ануса и прямой кишки. Проводится с целью исключить патологии прямой кишки: парапроктит, а также анальные трещины и геморрой. Ультразвуковое исследование органов брюшной полости и функциональные пробы печени выявляют воспаление печени, поджелудочной железы и желчного пузыря. Биопсия. Симптомы и клиническая картина колита очень схожи с симптоматикой различных злокачественных новообразований. Подозрительные фрагменты кишечника необходимо подвергать биопсии, чтобы исключить онкологию. Для того, чтобы назначить лечение или распознать колит, необходимо обратиться к врачу-гастроэнтерологу или к врачу-колопроктологу. Главным звеном в цепочке лечения колита является специальная диета. Лечение колита, в отличие от лечения многих других заболеваний характеризуется тем, что диета является неотъемлемым элементом терапии. Поскольку слизистая толстой (а возможно и тонкой) кишки раздражена, ни в коем случае не следует раздражать её ещё больше. Поэтому цель диеты — сократить до минимума нагрузку на кишечник, сохраняя при этом оптимальный режим питания, богатого всем необходимым. Из рациона временно исключаются продукты, богатые клетчаткой: Все соленые, кислые и сладкие продукты питания Пища должна быть мягкой, поэтому при термической обработке предпочтение отдается тушению на пару, варке. Питание должно быть дробное, 4-6 раз в день, чтобы избежать лишней нагрузки на ЖКТ. Продукты, улучшающие перистальтику кишечника и обладающие послабляющим эффектом также употреблять в пищу не стоит. Это касается чернослива, молока, тыквы, капусты и т.д. Лучше всего есть протертую пищу. При колите следует пить достаточное количество жидкости, поскольку организм быстро обезвоживается. Перечислим также ряд мер, которые могут применяться в ходе лечения: Антибиотики и противомикробные препараты. Назначаются если выявлена инфекционная этиология заболевания. Назначаются препараты Энтерофурил, Альфа Нормикс (Рифаксимин), Цифран. Курс лечения краткий, 3-5 дней строго по показаниям и под контролем лечащего врача. Гельминтоз. Если причина кишечного колита заключается в гельминтозе (паразитарном поражении кишечника), назначаются специализированные противогельминтные медикаменты (конкретные наименования зависят от типа гельминта и степени поражения). Снятие болевого синдрома. Ярко выраженный болевой синдром снимается препаратами-спазмолитиками, такими как Но-шпа, Папаверин. В более тяжелых случаях к спазмолитикам добавляются холинолитические лекарственные средства. Лечение сопутствующих осложнений. При колите кишечника нередко формируется проктит или проктосигмоидит. Для устранения данных последствий колита проводят специфическую местную терапию с применением свечей (ректально вводят препараты, на основе беладонны, анестезина, вводятся вяжущие средства), а также клизм (фитотерапевтические с календулой, ромашкой, либо препараты танин, проторгол). Устранение нарушений стула. Запоры и поносы устраняются разными способами. Для прекращения поноса рекомендуются вяжущие средства (дубовая кора, нитратная соль висмута, танальбин, белая глина и др.), для устранения запора проводится очистительная клизма. Нормализация микрофлоры. Нормальная и стабильная перистальтика невозможна без полезной микрофлоры. В результате поноса или запора микрофлора гибнет. Если проводились очистительные мероприятия — бактерии вымываются, в результате чего может начаться затяжной запор. Назначаются специальные препараты-пробиотики, такие как Линекс, ферменты (если болезнь протекает на фоне их недостататочности), энтеросорбенты (полисорб, уголь активированный, Полифепан, Энтеросгель, Фильтрум и др.). Язвенный колит кишечника поддается лечению сложнее. Требуется более интенсивная терапия, а значит более долгая и дорогостоящая. Препараты для лечения данного типа патологии не только дорогие, но и обладают массой побочных эффектов, потому применяются строго по предписанию специалиста. Выпускаются они в форме ректальных свечей, клизм, в таблетированной форме (Салофальк, Пентаса, Мезавант, Месакол). В ряде случаев прибегают к использованию препаратов биологической терапии, вроде препаратов Хумир (Адалимумаб), Ремикейд (Инфликсимаб). В наиболее тяжелых случаях допустимо использование кортикостероидых медикаментов (Преднизолон, Метилпреднизолон, Гидрокортизон). Препараты выпускаются в виде ректальных капельниц, свечей, таблеток. Если причина заболевания в аутоимунном заболевании или аллергической реакции назначаются имуннодепрессоры (Циклоспорин, Азатиоприн, Метотрексат). Также при хроническом колите рекомендуется санаторно-курортное лечение. Автор статьи: Горшенина Елена Ивановна | Врач-гастроэнтеролог Образование: Диплом по специальности «Лечебное дело» получен в РГМУ им. Н. И. Пирогова (2005 г.). Аспирантура по специальности «Гастроэнтерология» — учебно-научный медицинский центр. источник |
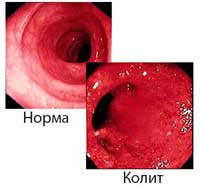


 В комплекс обязательных диагностических мероприятий при подозрении на колит входит макро- и микроскопия кала, копрограмма, выявления яиц гельминтов, бакпосев каловых масс. Производят общий анализ крови для определения наличия признаков воспаления.
В комплекс обязательных диагностических мероприятий при подозрении на колит входит макро- и микроскопия кала, копрограмма, выявления яиц гельминтов, бакпосев каловых масс. Производят общий анализ крови для определения наличия признаков воспаления. [1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12]
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12]