СРЕДСТВА, ВЛИЯЮЩИЕ НА КРОВЕТВОРЕНИЕ. ПРОТИВОАНЕМИЧЕСКИЕ СРЕДСТВА
КЛАССИФИКАЦИЯ СРЕДСТВ, ВЛИЯЮЩИХ НА КРОВЕТВОРЕНИЕ
Препараты железа
Препараты железа для приёма внутрь
1.1.1. Препараты железа закисного (Fe 2+ ) сульфата короткого действия
· Железа сульфат+серин (Актиферрин)
· Железа сульфат+серин+кислота фолиевая (Актиферрин композитум)
· Железа сульфат+поливитамины (Фенюльс)
· Железа сульфат+фолиевая кислота+цианокобаламин (Ферро-фольгамма)
1.1.2. Препараты железа закисного (Fe 2+ ) сульфата длительного действия
· Железа сульфат+кислота аскорбиновая(Сорбифе Дурулес)
· Аскорбиновая кислота+железа сульфат+мукопротеоза+фолиевая кислота (Гино-Тардиферон)
1.1.3. Препараты железа закисного (Fe 2+ ) хлорида
1.1.4. Другие препараты железа закисного (Fe 2+ )
· Протеин сукцинат железа (Ферлатум)
1.1.5. Неионные препараты железа окисного (Fe 3+ )
· Железа [III] гидроксид полимальтозат (Мальтофер, Тотема, Феррум Лек)
1.2. Препараты железа окисного (Fe 3+ ) для введения в мышцы
· Железа [III] гидроксид полимальтозат (Феррум Лек)
1.3. Препараты железа окисного (Fe 3+ ) для введения в вену
· Железа [III] гидроксид полимальтозат (Венофер)
Антидот препаратов железа
Гемопоэтические факторы роста
Эритропоэтины
· Дарбэпоэтин альфа (Аранесп)
· Метоксиполиэтиленгликоль-эпоэтин бета (Мирцера)
Гранулоцитарный и гранулоцитарно-макрофагальный колониестимулирующие факторы
Тромбопоэтиновые миметики
Неспецифические регуляторы гемопоэза
· Дезоксирибонуклеат натрия (Деринат)
Препараты разных групп, стимулирующие лейпоэз
Ромипластим — представитель класса тромбопоэтиновых миметиков. Увеличивает продукцию тромбоцитов путем связывания и активации тромбопоэтинового рецептора, механизм этого процесса аналогичен эндогенному тромбопоэтину. Тромбопоэтиновый рецептор преимущественно экспрессируется на клетках миелоидного ростка, таких как клетки-предшественники мегакариоцитов, мегакариоциты и тромбоциты.
Показания: Лечение тромбоцитопении при хронической идиопатической тромбоцитопенической пурпуре.
Побочное действие: анемия; тошнота, диарея, кровоточивость десен; инфекции верхних дыхательных путей, кашель; артралгия, миалгия; головокружение, бессонница; петехии; гематомы; слабость, повышение температуры тела, астения, периферические отеки.
Противопоказания: повышенная чувствительность к ромиплостиму, продуктам жизнедеятельности Escherichia coli.
Дезоксирибонуклеат натрия —иммуномодулятор, влияющий на клеточный и гуморальный иммунитет. Деринат стимулирует репаративные процессы, обладает противовоспалительным действием, нормализует состояние тканей при дистрофических изменениях сосудистого генеза. Препарат активизирует противовирусный, противогрибковый и противомикробный иммунитет, обладает высоким репаративным и регенераторным действием. При наружном применении Деринат способствует заживлению трофических язв, инфицированных ран и глубоких ожогов, значительно ускоряя эпителизацию. Под действием Дерината происходит безрубцовое заживление язвенных дефектов на слизистой оболочке. При гангренозных процессах под воздействием препарата отмечается самопроизвольное отторжение некротических масс в очагах поражения (например, на фалангах пальцев).
Показания:ОРВИ, ОРЗ, риниты, синуситы, облитерирующие заболевания нижних конечностей, трофические язвы, гангрена, инфицированные и длительно незаживающие раны, ожоги, воспалительные заболевания слизистой оболочки полости рта, глаз, носа, влагалища, прямой кишки, геморрой.
Побочные действия: При наружном и местном применении препарата побочных эффектов выявлено не было.
СРЕДСТВА, ВЛИЯЮЩИЕ НА ЭРИТРОПОЭЗ
Средства, стимулирующие эритропоэз
Препараты данной группы используют для лечения анемий.
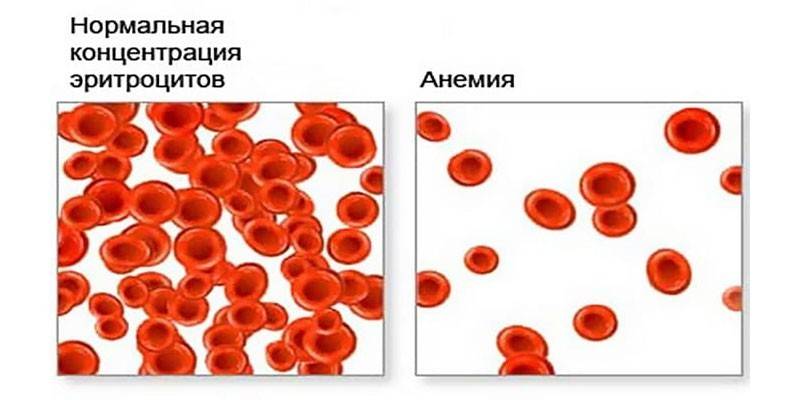
Анемия — состояние, при котором снижается способность крови переносить кислород, так как транспорт кислорода зависит от количества эритроцитов и содержания гемоглобина в них, то анемия сопровождается уменьшением количества эритроцитов и (или) уменьшением количества гемоглобина в единице объема.
Анемии могут развиваться вследствие массивной острой или хронической кровопотери (постгеморрагические анемии), при повышенном разрушении эритроцитов в периферической крови (гемолитические анемии); вследствие нарушения кроветворения: нормобластическая железодефицитная (гипохромная); мегалобластическая гиперхромная (при недостаточности витамина В12 или фолиевой кислоты).
В зависимости от вида анемий используют различные ЛС.
Препараты, применяемые при гипохромных (железодефицитных) анемиях
Эти анемии характеризуются продукцией нормальных эритроцитов, в уменьшенном количестве и с малым содержанием гемоглобина (гипохромные). Гипохромная анемия развивается вследствие недостаточного снабжения кроветворных органов железом. При этом снижается синтез гемоглобина эритробластами костного мозга. Основной причиной является дефицит железа при недостаточном поступлении с пищей, нарушенном всасывании (низкая кислотность желудочного сока, воспалительные процессы в кишечнике), при повышенной потребности (беременность), усиленном выведении из организма (кровопотеря).
Всасывание железа происходит преимущественно в верхних отделах тонкого кишечника. В кишечнике взрослого человека из пищи всасывается порядка 1-1,5 мг железа в сутки, что соответствует физиологическим потребностям. Общая потеря железа составляет порядка 1 мг в сутки.
С пищей и лекарственными препаратами железо может поступать в виде неионизированного и ионизированного: закисного (Fe 2+ ) и окисного (Fe 3+ ) железа. В ЖКТ всасываются только ионизированные формы железа — главным образом закисное железо (Fe 2+ ), которое транспортируется через клеточные мембраны слизистой оболочки кишечника. Для нормального всасывания железа необходимы хлористоводородная кислота и пепсин желудочного сока, которые высвобождают железо из соединений и переводят его в ионизированную форму, а также аскорбиновая кислота, которая восстанавливает трехвалентное железо в двухвалентное. В слизистой оболочке кишечника железо с белком апоферритином образует комплекс ферритин, который обеспечивает прохождение железа через кишечный барьер в кровь.
Транспорт поступившего в кровь железа осуществляется с помощью белка трансферрина, синтезируемого клетками печени и относящегося к β-глобулинам. Этот транспортный белок доставляет железо к различным тканям.
Основная часть железа используется для биосинтеза гемоглобина в костном мозге, часть железа — для синтеза миоглобина и ферментов, оставшееся железо депонируется в костном мозге, печени, селезенке.
Железо из организма выводится со слущенным эпителием слизистой оболочки ЖКТ (невсосавшаяся часть железа), с желчью, а также почками и потовыми железами. Женщины теряют больше железа, что связано с его потерей во время менструаций, а также потерей с молоком во время лактации.
источник
Препараты, регулирующие эритропоэз, подразделяют на следующие группы.
1. Применяемые при гипохромной анемии:
1.1. При железодефицитной анемии:
- Препараты железа:
- Для энтерального введения (внутрь):
- Монокомпонентные: железа закисного сульфат, ферро-градумет, ферроцерон, темофер пролонгатум, актиферрин, железа закисного лактат, ферроград, ферронал (железа глюконат), хеферол (железа фумарат), гемофер (железа хлорид), мальтофер/феррум лек (железа гидроксид полимальтозный комплекс), железа протеин сукцинилат, ферамид;
- Комбинированные препараты железа: фенотек, ферретаб, тардиферон, фенюльс, гемостимулин (+медь), ферроплекс (+аскорбиновая кислота), феррокаль (+церебролецитин +кальция фруктозодифосфат), мальтоферфол (+фолиевая кислота);
- Для парентерального применения:
- В вену: ферковен, венофер, железа глюконат, феррлецит;
- В мышцы: жектофер (железосорбитоловый комплекс), фербитол;
- В вену и в мышцы: феррум лек;
- Для энтерального введения (внутрь):
- Препараты кобальта: коамид;
1.2. При анемии, возникающей при некоторых хронических заболеваниях: репоэтин (рекомбинантный эритропоэтин человека), эпоэтин альфа, эпоэтин бета;
2. Применяемые при гиперхромной анемии: цианокобаламин, оксикобаламин, кобамамид, витогепат, фолиевая кислота;
Средства, угнетающие эритропоэз: раствор натрия фосфата, меченного фосфором-32.
При гиперхромной анемии применяют цианокобаламин и кислоту фолиевую, участвующие в синтезе нуклеиновых кислот.
Цианокобаламин (витамин В12) назначают при злокачественной (пернициозной) анемии. Суточная потребность — 2-5 мкг. При дефиците цианокобаламина эритропоэз протекает по мегалобластическому типу: эритробласт → гиперхромный мегалобласт → мегалоцит.
Дефицит при: ↓ содержания фактора Касла (аутоантитела к нему, резекция желудка, хронический гастрит) — в обычных условиях он вырабатывается слизистой оболочкой желудка и обеспечивает всасывание цианокобаламина в тонкой кишке; заболеваниях кишечника, панкреатите, заражении лентецом широким и др.
Фармакокинетика:
- Всасывание: По всей длине тонкого кишечника и в дистальном отделе слепой кишки в связанной форме со специфическим внутренним фактором Касла (гликопротеин, синтезируемый париетальными клетками желудка) транспортируется в кровь пиноцитозом через рецептор на энтероцитах, активность которого зависит от нормальной функции слизистой, поддерживаемой Вс; при избытке — простой диффузией;
- Распределение: Транспортируются в крови транскобаламинами II в печень, костный мозг и селезёнку; транскобаламины I и III участвуют в депонировании;
- Депонирование: В печени содержится 1-10 мг (запас на 2-5 лет), ежедневно используется 0,5-8,0 мкг;
- Выведение: С желчью в кишечник — ежедневно секретируется 3 мкг; энтерогепатическая циркуляция (50-60 % всасываются обратно); также почками (особенно при избытке).
Фармакодинамика.
Основные реакции:
1. Дезоксиаденозилкобаламин (кобаламин) катализирует метилмалонил-КоА-мутазу в реакции: метилмалонил-КоА → сукцинил-КоА (метилмалоновая → янтарная кислота) ⇒ метаболизм жирных кислот, изолейцина и валина ⇒ при дефиците ↑ содержания метилмалоновой кислоты, подавляющей продукцию миелина ⇒ неврологические расстройства;
2. Метилкобаламин, участвуя в реакции деметилирования тетрагидрофолиевой кислоты, регулирует:
- Синтез ДНК: через превращение 5СН3-Н4-фолата (пищевого и депонированного) в Н4-фолат ⇒ при дефиците нарушение гемопоэза (репликации ДНК, созревание ядра эритроцитов ⇒ мегалобласты);
- Синтез метионина: под действием метилтетрагидрофолата цианогруппа В12 замещается на метил с образованием метилкобаламина, который метилирует гомоцистеин с образованием метионина ⇒ синтез белков, фосфолипидов, бетаина, холина.
Действие:
- Анаболическое действие: ↑ обмена белков и нуклеиновых кислот;
- Липотропное: ↑ обмен углеводов и липидов, ↓ содержание холестерина в крови;
- Активирует эритропоэз (с Вс): репликация ДНК, завершение созревания эритроцитов, предотвращение гемолиза за счёт накопления в эритроцитах сульфгидрильных соединений;
- Стимуляция иммунитета: ↑ фагоцитарную активность лейкоцитов, деятельность ретикулоэндотелиальной системы;
- Стимулирует свертывающую систему крови;
- Стимулирует регенерацию тканей;
- Гепатозащитная функция;
- Нейропротекция, участие в познавательной и эмоциональной сфере;
- Репродукция (↑ содержание сперматозоидов).
Цианокобаламин при злокачественной анемии нормализует картину крови, а также устраняет или ослабляет неврологические нарушения и поражения слизистой оболочки языка. Ахлоргидрия желудочного сока сохраняется.
Побочное действие:
- Нервное возбуждение;
- Боли в области сердца, тахикардия, аритмия (↓ К+);
- ↑ свертывания крови, ↑ тромбоцитов, лейкоцитов, эритроцитов в крови;
- Анафилактический шок (редко).
Взаимодействие с другими лекарствами:
- Нарушение всасывания при применении препаратов калия, гиполипидемических, противотуберкулезных средств, больших доз аскорбиновой кислоты, недостатке фолиевой кислоты, хроническом употреблении алкоголя;
- Дефицит при приеме нейролептиков, глюкокортикоидов;
- Не рекомендовано в одном шприце с тиамином и пиридоксином;
- ↑ аллергизирующего действия витамина В1 ⇒ их комбинация нецелесообразна.
Кислоту фолиевую (витамин Вс) назначают при макроцитарной анемии. Суточная потребность — 50 мкг, при беременности — 400-800 мкг, дети 2–12 лет — 200 мкг. При дефиците кислоты фолиевой образуются макроциты: эритробласт → гиперхромный макронормобласт → макроцит.
Фармакокинетика:
- Всасывание: Фолаты пищи — это, в основном, полиглутаматные формы 5-СН3-тетрагидрофолата (ТГФ); для всасывания в кишечнике должны гидролизоваться в моноглутамат глутаматтрансферазой (конъюгазой); её активность ↓ при алкоголизме, спру; моноглутамат-5-СН3-ТГФ всасывается в проксимальном отделе тонкого кишечника активным или пассивным транспортом; горячая обработка ↓ содержание фолатов на 50–95 %; лучшее всасывание — из печени, яичных желтков, пивных дрожжей;
- Связь с белками: 60-70%;
- Концентрация в крови: 4-20 нг/мл;
- Распределение: В печени, спинномозговой жидкости наибольшее количество; общее содержание — 5-10 мг; активно транспортируется через плаценту (в 2 и 5 раз ↑ концентрация в эритроцитах и плазме крови соответственно, чем у матери);
- Выведение: Почками, а также с грудным молоком (50-60 мкг/л).
Фармакодинамика.
Основная функция тетрагидрофолиевой кислоты и её производных — перенос (акцептор) одноуглеродных групп, например метильных и формильных, от одних органических соединений к другим.
Основные коферментные формы тетрагидрофолата: МетилТГФ, фолиниевая кислота (цитрофорум-фактор).
Основные реакции:
1. Трансформация серина в глицин;
2. Метаболизм гистидина;
3. Включение атомов углерода в кольцо пуриновых оснований;
4. Превращение гомоцистеина в метионин с В12 как кофактора.
Действие: ↑ эритро-, лейко-, тромбоцитоз, пластические и регенеративные процессы во всех органах.
Кислоту фолиевую используют при алиментарной и медикаментозной макроцитарной анемии, спру (хроническое заболевание, проявляющееся диареей, глосситом, анемией, общим истощением и гипофункцией эндокринных желез), анемии беременных. Для лечения злокачественной анемии кислоту фолиевую отдельно не назначают, так как она не только не устраняет патологические изменения со стороны нервной системы, но даже усиливает их. Нормализуется лишь картина крови. В связи с этим при злокачественной анемии кислота фолиевая комбинируется с цианокобаламином.
Побочное действие:
- Диспепсия;
- В больших дозах ↑ возбудимости ЦНС, вплоть до судорог (↓ активности ГАМК), ↓ функции почек;
- Аллергические реакции.
Взаимодействие с другими лекарствами:
- Нарушение всасывания при применении оральных контрацептивов, изониазида, хроническом употреблении алкоголя, противоэпилептических средств (дифенин, фенобарбитал, гексамидин);
- Нарушение метаболизма (↓ активности дигидрофолат-редуктазы) на фоне метотрексата, сульфаниламидов, триметоприма, ПАСК, цитостатиков и др.;
- Нельзя вводить в одном шприце с витаминами В12, С, местноанестезирующими (разрушение); вместе с минеральными кислотами, щелочными веществами, восстановителями (инактивация Вс);
- ↑ эффекты сердечных гликозидов; с В12 для лечения мегалобластических анемий; с Fe, витаминами В2, В6 — гипохромных анемий.
источник
Обязательное посещение аудиторных занятий, активность в аудитории, предварительная подготовка к занятиям, качественное и своевременное выполнение СРО, участие во всех видах контроля.
Все задания должны выполняться к установленному времени. Несвоевременное предоставление работ приводит к снижению его итоговой оценки.
В случае нарушения студентом академического поведения и правил этики итоговая оценка также снижается.
Разработчик ___________ ______Тлесова Э.Б.___
(подпись) (Ф.И.О.)
Рассмотрено на заседании кафедры____Экономика___
протокол № ______ от «______» __________2014 г.
СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ГИПЕРХРОМНЫХ АНЕМИЙ
ВИТАМИНОВ В 12 И ФОЛИЕВОЙ КИСЛОТЫ
Витамин В 12 и фолиевая кислота необходимы для биосинтеза ДНК. Их дефицит приводит к аномальному созреванию и функционированию образующихся клеток.
Основное проявление недостатка витамина В 12 и фолиевой кислоты — тяжелая анемия.
При дефиците витамина В 12 могут наблюдаться неврологические нарушения
ПРЕПАРАТЫ ДЛЯ ЛЕЧЕНИЯ ПЕРНИЦИОЗНОЙ
Суть патологии состоит в нарушении нуклеинового обмена эритроидных клеток, в результате чего в кровь поступают незрелые формы с высоким содержанием железа (гиперхромные мегалоциты), но с резко сниженной способностью к переносу кислорода.
Эти расстройства эритропоэза вызываются дефицитом витамина В 12 и фолиевой кислоты.
В 12 — дефицитная анемия развивается при нарушении всасывания витамина.
Париетальные клетки слизистой желудка секретируют особый гликопротеид, который специфически связывает поступивший с пищей витамин В 12 в комплекс, процесс происходит в желудке и 12-перстной кишке. Затем комплекс проходит почти через весь кишечник и всасывается в дистальном отделе слепой кишки с помощью специфического транспортного механизма.
Дефицит витамина может быть обусловлен и повреждением транспортного механизма (инвазия широким лентецом, хронический воспалительный процесс в толстом кишечнике).
При недостатке витамина В 12 развивается следующая патология (три А):
1. АНЕМИЯ — гиперхромная, так как нарушен процесс созревания эритроцитов, гемолиз эритроцитов.
2. АТАКСИЯ — неврологические расстройства, так как нарушен синтез миелиновых оболочек (комбинированные расстройства двигательного тракта спинного мозга и психических функций).
Цианкобаламин контролирует в клетках:
1) превращение метилмалоновой кислоты в янтарную
Нарушение этой реакции ведет к образованию и встраиванию аномальных жирных
кислот в мембраны клеток с повреждением их функции и процесса формирования
миелиновых оболочек нервных волокон, в первую очередь в ЦНС.
2) гомоцистеина в метионин (сопряжено с фолиевой кислотой)
Нарушение этой реакции сопровождается накоплением гомоцистеина и выведением
фолиевой кислоты из его оборота в биохимических реакциях синтеза ДНК.
В последнее время с нарушением обезвреживания гомоцистеина связывают
первичные повреждения эндотелия сосудов, которые сопровождаются
последующим отложением холестерина и Са++ с формированием склеротических
Неврологические нарушения более тяжелые, чем гематологические.
3. АХИЛИЯ — снижение секреции желудком соляной кислоты.
Эти проявления сопровождаются дегенерацией эпителия (в области ротовой полости и желудочно-
Так как дефицит витамина В 12 в основном связан с нарушением его всасывания, для лечения необходимо парентеральное введение препаратов.
Парентеральное введение витамина В 12 уже в течение нескольких дней приводит к нормализации числа эритроцитов, лейкоцитов и тромбоцитов в крови. Быстро исчезают изменения эпителия в ЖКТ, за исключением атрофии слизистой оболочки желудка и ахилии.
Восстановление неврологических нарушений длится годами, причем некоторые из них уже необратимы.
В клетках слизистой кишечника содержится фермент редуктаза фолиевой кислоты, которая восстанавливает витамин в тетрагидрофолиевую кислоту. При нарушении этого процесса всасывание страдает.
Фолиевая кислота в форме тетрагидрофолиевой кислоты выполняет важнейшую роль в процессах физиологической и репаративной регенерации, в синтезе белков, оснований нуклеиновых кислот и макроэргов, что особенно заметно на быстропролиферирующих тканях. Поэтому при дефиците фолиевой кислоты в первую очередь страдает клеточное деление и созревание клеток кроветворной системы и развивается макроцитарная анемия, лейкопения, нарушаются регенерация слизистой желудка и кишечника. Процессы всасывания (в том числе — железа), могут развиваться глубокие дистрофические изменения слизистых.
Кислота фолиевая с цианкобаламином
Дефицит фолиевой кислоты является причиной мегалобластной анемии ( морфологически не отличается от пернициозной, однако отсутствуют повреждения в кишечном тракте и видимые неврологические нарушения). Во время беременности может приводить к уродствам плода.
Фолиевая кислота самостоятельно не обладает метаболической активностью, а восстанавливается в тетрагидрофолиевую кислоту, которая ответственна за все биохимические реакции в организме, связанные с переносом С 1 атома.
Дефицит фолиевой кислоты в отличие от дефицита витамина В 12 наступает при нерациональном питании ( отсутствие в диете овощей, яиц, мяса), в старческом возрасте, при алкоголизме. Также при лечении некоторыми противосудорожными средствами (дифенин, фенобарбитал), изониазидом, при пользовании гормональными контрацептивными препаратами.
Метаболизм и утилизация витамина В 12 и фолиевой кислоты тесно связаны друг с другом. На основании картины периферической крови нельзя заключить имеется дефицит того или другого витамина.
Поступление только фолиевой кислоты не устраняет тяжелых неврологических нарушений, которые наступают в результате дефицита витамина В 12. Из-за угрожающих осложнений начинают терапию обоими витаминами.
Применяют фолиевую кислоту энтерально в течение 3-4 недель. Парентеральное применение целесообразно только при синдроме недостаточного всасывания.
СРЕДСТВА, ВЛИЯЮЩИЕ НА ГЕМОСТАЗ
Дата добавления: 2015-03-11 ; просмотров: 1702 . Нарушение авторских прав
источник
1. Цианокобаломин (витамин В12) назнач. при злокачественной анемии. При его дефиците эритропоэз протекает по мегалобластич. типу: эритробласт→гиперхромный мегалобласт→мегалоцит. Возникновение злокач. анемии связано с нарушением всасывания цианокобаломина из-за отсутствия фактора Касла. В обычных усл. он вырабатывается в тонкой кишке.
2. Кислота фолиевая (витамин Вс)назнач. при макроцитарной анемии. При ее дефиците образуются макроциты: эритробласт→гиперхромный макронормобласт→макроцит. В организме фол. к-та превращается в фолиниевую, которая и обладает физиологической активностью.
Для предупреждения приступов стенокардии препараты нитроглицерина пролонгированного действия. Сустак – нитроглицерин в виду постепенно растворяющихся таблеток, начинает действ. через 10-15 мин., длится около 4 часов. Тринитротролонг – полимерная пластинка на десну. Нитронг – внутрь, в таблетках (7-8 часов). Мазь нитроглицерина 2% — через 15-30 минут, до 5 часов. Пластырь — 8-10 часов, чтобы не вызвать привыкания к нитроглицерину.
+ Нитросорбид (изосорбида динитрат), эринит (нитропентон) , изосорбида мононитрат ( моночинкве) Их эффективность несколько ниже, через 30 мин, 1-4 часа.
Мочегонные средства предназначены в основном для выведения из организма избыточного кол-ва воды и устранения отеков. Их также используют для снижения АД.
Вещества, оказывающие прямое влияние на функцию эпителия почечных канальцев.
Вещества, содержащие сульфаниламидную группировку
Тиазиды (дихлотиазид, циклометиазид)
Соединения «нетиазидной» структуры (фуросемид, клопамид, оксодолин)
Производные дихлорфеноксиуксусной кислоты (этакриновая к-та)
Производные птеридина (триамтерен)
Производные пиразиноилгуанидина (амилорид)
Антагонисты альдостерона (спиронолактон)
Осмотически активные диуретики (маннит, мочевина)
Препараты, стимулирующие деятельность сердца, подразделяются на:
Сердечные гликозиды – вещ-ва растительного происхождения, исп. для лечения сердечной недостаточности, связанной с дистрофией миокарда. Повышают работоспособность миокарда, обеспечивают эффективную деятельность сердца.
Наиболее часто используют: дигитоксин (из наперстянки пурпуровой), дигоксин, целанид (наперстянка шерстистая), строфантин К (строфант Комбе), коргликон (ландыш), настой травы горицвета.
Кардиотонические средства негликозидной структуры – стимулирующим влиянием на сердце также обладают адреномиметики, дофамин, глюкагон, метилксантины. Но вызывают многие нежелательные эффекты.
2.1.Средства, стимулирующие β1-адренорецепторы (дофамин, добутамин)
2.2. Ингибиторы фосфодиэстеразы (амринон, милринон).
Антиангинальные – средства, применяемые для лечения стенокардии. Коронарная недостаточность возникает при несоответствии между потребностью сердца в кислороде и его кровоснабжением. Отсюда два принципа действияэффективных веществ: либо уменьшение работы сердца(и снижение его потребности в ксилороде), либо повышение кровоснабжения сердца.
Средства, понижающие потребность миокарда в кислороде и улучшающие его кровоснабжение.
Органические нитраты (нитроглицерин, нитронг, тринитролонг)
Средства, блокирующие кальциевые каналы (нифедипин, верапамил, амлодипин)
Активаторы калиевых каналов (пинацидил, никорандил)
Разные средства с антиангинальной активностью (амиодарон)
Средства, понижающие потребность миокарда в кислороде
β1-адреноблокаторы (талинолол, метопролол, атенолол)
брадикардические препараты(алинидин, фалипамил)
Средства, повышающие доставку кислорода к миокарду
3.1. Коронарорасширяющие средства миотропного действия (дипиридамол)
3.2. Средства рефлекторного действия, устраняющие коронароспазм (валидол)
Кардиопротекторные препараты (предуктал МВ)
источник
К стимуляторам эритропоэза относятся эпоэтины, цианокобаламин, фолиевая кислота, препараты железа.
Эпоэтин альфа (Epoetin alfa) и эпоэтин бета (Epoetin beta; эритростим, рекормон) – рекомбинантные препараты эритропоэтина человека. Применяют при анемиях, связанных с поражением костного мозга, хронической почечной недостаточностью. Вводят под кожу или внутривенно.
Цианокобаламин (витамин В12) применяют при пернициозной (злокачественной) анемии, связанной с отсутствием в желудке внутреннего фактора Касла, который способствует всасыванию цианокобаламина. Препарат вводят под кожу, внутримышечно или внутривенно.
Фолиевая кислота (витамин Вс) эффективна при макроцитарной (фолиеводефицитной) анемии. Препарат назначают внутрь.
Препараты железа применяют для лечения железодефицитных гипохромных анемий, то есть анемий, при которых в эритроцитах снижается содержание гемоглобина. Гипохромные анемии обычно связаны с недостаточным усвоением железа, которое входит в состав гемоглобина.
Железа глюконат (Ferrous gluconate), железа лактат (Ferrous lactate), железа сульфат (Ferrous sulfate), железа фумарат (Ferrous fumarate) назначают внутрь. Железа глюконат, кроме того, вводят внутривенно.
Побочные эффекты препаратов железа:
СРЕДСТВА, ИСПОЛЬЗУЕМЫЕ ПРИ ГИПОХРОМНЫХ АНЕМИЯХ
Чаще всего гипохромные анемии — железодефицитного генеза. Дефицит железа может быть следствием:
• недостаточного поступления железа в организм плода и ребенка;
• плохого всасывания из кишечника (синдром мальабсорбции, воспалительные заболевания кишечника, прием тетрациклинов и других антибиотиков);
• избыточные кровопотери (глистная инвазия, носовые и геморроидальные кровотечения);
• повышенного расхода железа (интенсивный рост, инфекции).
Железо является важнейшим компонентом ряда ферментов как геминовой, так и негиминовой структуры.
Геминовые ферменты : — гемо- и миоглобин;
Негеминовые ферменты : — сукцинатдегидрогеназа;
При недостатке железа снижается содержание гемоглобина (цветовой показатель меньше единицы), а также активность дыхательных ферментов в тканях (гипотрофия).
Железо всасывается в двенадцатиперстной кишке, а также в других отделах тонкой кишки. Двухвалентное железо всасывается хорошо. Поступившее с пищей трехвалентное железо под влиянием соляной кислоты желудка переходит в двухвалентное. Кальций, фосфаты, содержащиеся в молоке, особенно коровьем, фитиновая кислота, тетрациклины препятствуют всасыванию железа. Максимальное количество железа (двухвалентного, которое может поступить в организм за сутки, равно 100 мг).
Железо всасывается в два этапа:
I этап : железо захватывается клетками слизистой.
Поддерживается этот процесс фолиевой кислотой.
II этап : транспортировка железа через клетку слизистой и отдача его в кровь. В крови железо окисляется до трехвалентного, связывается с трансферрином.
Чем тяжелее железодефицитная анемия, тем менее насыщен этот белок и тем больше его емкость и способность связывать железо. Трансферрин транспортирует железо в органы кроветворения (костный мозг) или депонирования (печень, селезенка).
Для лечения больных с гипохромной анемией используют препараты, назначаемые как внутрь, так и в инъекциях.
Внутрь применяют преимущественно препараты двухвалентного железа, так как оно лучше всасывается и меньше раздражает слизистую.
Препараты железа
Препараты железа закисного (Fe2+) для приема внутрь
Ферроплекс (железа сульфат, аскорбиновая кислота)
Актиферрин (железа сульфат, глюкоза, фруктоза)
Ферроградумет (железа сульфат на синтетическом носителе)
Тардиферон железа сульфат, аскорбиновая кислота, мукопротеоза)
Препараты железа закисного (Fe3+) для внутримышечного введения
Ферковен (железа сахарат, кобальта глюконат, раствор углеводов)
Феррум лек (трехосновное железо в виде комплекса с мальтозой)
Препараты железа закисного (Fe3+) для внутривенного введения
Последнее изменение этой страницы: 2017-01-19; Нарушение авторского права страницы
источник
Гиперхромные анемии развиваются в результате нарушения эритропоэза и характеризуются поступлением в периферическую кровь незрелых предшественников эритроцитов — мегалобластов, содержащих большое количество железа, но обладающих резко сниженной способностью к переносу кислорода.
Появление этих гигантских клеток в периферической крови обусловлено дефицитом в организме витамина В12 и/или фолиевой кислоты (витамина Вc), необходимых для нормального созревания эритроцитов. В организме дефицит витамина В12 развивается в результате уменьшения или прекращения секреции париетальными клетками желудка специфического гликомукопротеида, который получил название «внутренний (антианемический) фактор Кастла», который образует с витамином В12(внешний фактор Кастла) комплекс, защищающий витамин В12 от разрушения в кишечнике и обусловливающий его нормальное всасывание.
Не менее важна в организме и фолиевая кислота, недостаток которой тормозит переход мегалобластической фазы кроветворения в нормобластную. Помимо этого фолиевая кислота совместно с витамином В12 регулирует синтез нуклеиновых кислот (ДНК и РНК). Нарушение синтеза нуклеиновых кислот влечет за собой замедление деления стволовых клеток костного мозга на фоне практически не сниженной скорости их роста, в результате в периферической крови появляются незрелые предшественники эритроцитов — «гигантские» гиперхромные мегалобласты и мегалоциты.
При недостатке в организме витамина В12 процесс образования зрелых эритроцитов обрывается на этапе: эритробласт → гиперхромный мегалобласт → мегалоцит. Такая анемия носит название «мегалобластная анемия».
При дефиците фолиевой кислоты эритробласты дифференцируются до макроцитов (эритробласт → гиперхромный макронормобласт → макроцит). Этот вид анемии носит название «макроцитарная анемия».
Для лечения гиперхромной мегалобластной анемии в клинической практике используют получаемый путём микробиотического синтеза витамин В12 — цианокобаламин, а для лечения макроцитарной анемии — фолиевую кислоту.
При гиперхромной мегалобластной анемии цианокобаламин восстанавливает нормальную картину крови, одновременно с этим уменьшая сопутствующие дефициту витамина В12 изменения слизистой оболочки языка, а также неврологические нарушения, т. е. купирует симптомы болезни Аддисона — Бирмера.
Фолиевую кислоту используют для лечения как алиментарной (макроцитарной анемии новорожденных), так и медикаментозной (вторичной) макроцитарной анемии (возникающей на фоне приема противосудорожных препаратов — фенитоина, примидона, фенобарбитала, а также противозачаточных и других лекарственных средств), анемии беременных, спру (от англ. sprue — язвенный грибковый стоматит, молочница — заболевание неясной этиологии, развивающееся в результате нарушения всасывания в кишечнике витаминов, жиров, глюкозы и проявляющееся стоматитом, диареей, анемией). Однако в отличие от витамина В12 фолиевую кислоту для лечения гиперхромной анемии самостоятельно не используют, так как на фоне ее приема сопутствующая неврологическая патология не устраняется, поэтомy фолиевую кислоту назначают совместно с цианокобаламином.
Краткое описание фармакологической группы. Лекарственные средства для лечения железодефицитных анемий цианокобаламином и фолиевой кислотой.
источник
Гиперхромные анемии развиваются при недостатке в организме витамина В12 или фолиевой кислоты. При дефиците витамина В12 развивается пернициозная (злокачественная) анемия, которая кроме гематологических нарушений характеризуется возникновением неврологической симптоматики вследствие поражения нервной системы. Витамин В12 в двенадцатиперстной кишке образует комплекс с внутренним фактором Касла (гликопротеин, секретируемый париетальными клетками желудка) и таким образом всасывается в кровь. В плазме крови витамин В12 связывается с белками-транскобаламинами, передающими его клеткам костного мозга. Суточная потребность в витамине составляет 3-7 мкг, за сутки организм теряет 2—5 мкг витамина В12. Поскольку содержание витамина В12в организме здорового человека составляет 2—5 мг, дефицит витамина В12 развивается только через несколько лет после прекращения его поступления.
В результате метаболических превращений витамина В]2 в организме образуется его коферментная форма — метилкобаламин, которая необходима для образования тетрагидрофолиевой кислоты, активной формы фолиевой кислоты.
Тетрагидрофолиевая кислота участвует в синтезе дезокситимидина, который в виде монофосфата включается в ДНК. Поэтому при недостаточности цианокобалами-на, а также при недостаточности фолиевой кислоты нарушается синтез ДНК. При нарушении синтеза ДНК в первую очередь страдает костный мозг, в котором идет активный процесс деления клеток. В результате нарушения клеточного деления эритробласты увеличиваются в размерах, превращаясь в мегалобласты, образуются крупные эритроциты с большим содержанием гемоглобина (дефицит эритроцитов преобладает над дефицитом гемоглобина, цветовой показатель больше 1). Развивается мегалобластная анемия.
Кроме того, витамин В12 участвует в синтезе миелина, поэтому при недостаточности витамина В]2 нарушается синтез миелина и возникают неврологические нарушения, связанные с поражением нервной системы (пернициозная анемия). Пернициозная (злокачественная) анемия возникает при нарушении всасывания цианокобаламина из-за отсутствия внутреннего фактора Касла при патологии желудка (атрофический гастрит, опухолевые заболевания и др.). Для устранения неврологической симптоматики при пернициозной анемии эффективен только цианокобаламин.
Цианокобаламин вводят внутримышечно, подкожно или внутривенно при пернициозной анемии (по 0,1—0,2 мг 1 раз в 2 дня). Из побочных эффектов наблюдаются аллергические реакции, нервное возбуждение, боли в области сердца, тахикардия. Цианокобаламин противопоказан при острой тромбоэмболии, эритроцитозе.
При дефиците фолиевой кислоты развивается макроцитарная гиперхромная анемия. Это может быть связано с недостаточным поступлением фолиевой кислоты в организм (недостаточное содержание в рационе, нарушение всасывания при синдроме мальабсорбции и др.), с применением антагонистов фолиевой кислоты (метотрексат, триметоприм, триамтерен, пириметамин и др.), повышенной потребностью ее (беременность) и др. В этих случаях назначают фолиевую кислоту. Кроме того фолиевую кислоту применяют вместе с витамином В12 при пернициозной анемии (при этом фолиевая кислота не может быть использована без цианокобаламина, поскольку она не устраняет неврологическую симптоматику пернициозной анемии, патологические изменения со стороны нервной системы могут даже усилиться).
Фолиевая кислота назначается внутрь по 0,005 г в сутки. Продолжительность курса лечения 20—30 дней. Возможны аллергические реакции. Подробнее о фолиевой кислоте и витамине В|2 см. в гл. 32 «Витамины».
Не нашли то, что искали? Воспользуйтесь поиском:
источник
26.1.1.2. Препараты, применяемые при гиперхромных анемиях
Гиперхромные анемии развиваются при недостатке в организме витамина В 12 или фолиевой кислоты. При дефиците витамина В 12 развивается пернициозная (злокачественная) анемия, которая кроме гематологических нарушений характеризуется возникновением неврологической симптоматики вследствие поражения нервной системы. Витамин В 12 в двенадцатиперстной кишке образует комплекс с внутренним фактором Касла (гликопротеин, секретируемый париетальными клетками желудка) и таким образом всасывается в кровь. В плазме крови витамин В 12 связывается с белками-транскобаламинами, передающими его клеткам костного мозга. Суточная потребность в витамине составляет 3-7 мкг, за сутки организм теряет 2—5 мкг витамина В 12 . Поскольку содержание витамина В 12 в организме здорового человека составляет 2—5 мг, дефицит витамина В 12 развивается только через несколько лет после прекращения его поступления.
В результате метаболических превращений витамина В ]2 в организме образуется его коферментная форма — метилкобаламин, которая необходима для образования тетрагидрофолиевой кислоты, активной формы фолиевой кислоты.
Тетрагидрофолиевая кислота участвует в синтезе дезокситимидина, который в виде монофосфата включается в ДНК. Поэтому при недостаточности цианокобалами-на, а также при недостаточности фолиевой кислоты нарушается синтез ДНК. При нарушении синтеза ДНК в первую очередь страдает костный мозг, в котором идет активный процесс деления клеток. В результате нарушения клеточного деления эритробласты увеличиваются в размерах, превращаясь в мегалобласты, образуются крупные эритроциты с большим содержанием гемоглобина (дефицит эритроцитов преобладает над дефицитом гемоглобина, цветовой показатель больше 1). Развивается мегалобластная анемия.
Кроме того, витамин В 12 участвует в синтезе миелина, поэтому при недостаточности витамина В ]2 нарушается синтез миелина и возникают неврологические нарушения, связанные с поражением нервной системы (пернициозная анемия). Пернициозная (злокачественная) анемия возникает при нарушении всасывания цианокобаламина из-за отсутствия внутреннего фактора Касла при патологии желудка (атрофический гастрит, опухолевые заболевания и др.). Для устранения неврологической симптоматики при пернициозной анемии эффективен только цианокобаламин.
Цианокобаламин вводят внутримышечно, подкожно или внутривенно при пернициозной анемии (по 0,1—0,2 мг 1 раз в 2 дня). Из побочных эффектов наблюдаются аллергические реакции, нервное возбуждение, боли в области сердца, тахикардия. Цианокобаламин противопоказан при острой тромбоэмболии, эритроцитозе.
При дефиците фолиевой кислоты развивается макроцитарная гиперхромная анемия. Это может быть связано с недостаточным поступлением фолиевой кислоты в организм (недостаточное содержание в рационе, нарушение всасывания при синдроме мальабсорбции и др.), с применением антагонистов фолиевой кислоты (метотрексат, триметоприм, триамтерен, пириметамин и др.), повышенной потребностью ее (беременность) и др. В этих случаях назначают фолиевую кислоту. Кроме того фолиевую кислоту применяют вместе с витамином В 12 при пернициозной анемии (при этом фолиевая кислота не может быть использована без цианокобаламина, поскольку она не устраняет неврологическую симптоматику пернициозной анемии, патологические изменения со стороны нервной системы могут даже усилиться).
Фолиевая кислота назначается внутрь по 0,005 г в сутки. Продолжительность курса лечения 20—30 дней. Возможны аллергические реакции. Подробнее о фолиевой кислоте и витамине В |2 см. в гл. 32 «Витамины».
26.1.1.3. Препараты эритропоэтина
Эритропоэтин — гликопротеин, который является фактором роста, регулирующим эритропоэз. Эритропоэтин стимулирует пролиферацию и дифференциров-ку эритроидных клеток-предшественников, способствует высвобождению рети-кулоцитов из костного мозга в кровь. Эритропоэтин в основном образуется в перитубулярных клетках почек (90%) и в меньшем количестве в печени (10%). Образование эритропоэтина значительно усиливается при гипоксии тканей. Синтез эритропоэтина нарушается при хронических заболеваниях почек.
В клинической практике используются рекомбинантные препараты эритропоэтина человека, полученные методом генной инженерии — эпоэтинос (Эп-рекс, Эпоген), эпоэтин-р (Рекормон). Применяются при анемиях, связанных с хронической почечной недостаточностью, поражениями костного мозга, хро-
ническими воспалительными заболеваниями, СПИДом, злокачественными опухолями, при анемии у недоношенных детей. Препараты вводят подкожно и внутривенно. Дозируются в МЕ/кг массы тела. Эффект развивается через 1—2 нед, кроветворение нормализуется через 8—12 нед. При применении препаратов возможны боли в грудной клетке, отеки, повышение артериального давления, ги-пертензивный криз с явлениями энцефалопатии (головная боль, головокружение, спутанность сознания, судороги), тромбозы.
26.1.2. Средства, угнетающие эритропоэз
Раствор натрия фосфата, меченного фосфором-32 (Na 2 H 32 P0 4 ), применяется при полицитемии (эритремии).
В основе эритремии лежит повышенная пролиферация всех ростков кроветворения, особенно эритроидного ростка, что сопровождается значительным увеличением числа эритроцитов в периферической крови. Радиоактивный 32 Р из Na 2 H 32 P0 4 накапливается в костномозговой ткани и нарушает образование эритроцитов. Применение препарата приводит не только к снижению числа эритроцитов, но и тромбоцитов. Препарат вводится внутрь или внутривенно и дозируется в милликюри. Лечение проводят под тщательным гематологическим контролем.
Противопоказаниями являются анемия, лейкопения, тромбоцитопения, сердечная недостаточность, нарушения функции печени и почек.
26.2. СРЕДСТВА, ВЛИЯЮЩИЕ НА ЛЕИКОПОЭЗ 26.2.1. Средства, стимулирующие леикопоэз
Эти средства используются для лечения лейкопении и агранулоцитоза.
Лейкопения — уменьшение числа лейкоцитов в периферической крови ниже 4000 в 1 мкл. Агранулоцитоз — состояние, обусловленное резким снижением в крови числа гранулоцитов и общего количества лейкоцитов.
Эти патологические состояния могут возникнуть при действии на организм ионизирующей радиации, в том числе при проведении рентгено- и радиотерапии, воздействии токсических веществ и некоторых лекарственных препаратов. При уменьшении числа лейкоцитов в крови снижается устойчивость организма к инфекциям, что требует назначения средств, стимулирующих леикопоэз.
В качестве стимуляторов лейкопоэза используют факторы роста, регулирующие леикопоэз, среди которых выделяют четыре колониестимулирующих фактора: гранулоцитарный (стимулирует продукцию нейтрофилов), макрофаг гальный (стимулирует продукцию моноцитов, которые в тканях превращаются в макрофаги), гранулоцитарно-макрофагальный (стимулирует продукцию нейтрофилов, эозинофилов, базофилов, моноцитов), интерлейкин-3 (универсальный ко-лониестимулирующий фактор роста). Получены рекомбинантные препараты некоторых из этих факторов.
Молграмостим (Лейкомакс) — рекомбинантный препарат человеческого гранулоцитарно-макрофагального колониестимулирующего фактора. Представляет собой гликопротеин. Молграмостим стимулирует пролиферацию и диффе-ренцировку гемопоэтических клеток-предшественников, что приводит к образованию гранулоцитов, моноцитов/макрофагов. Молграмостим в небольшой степени стимулирует пролиферацию эозинофилов и образование эритроцитов (является кофактором эритропоэтина).
Применяется: при угнетении лейкопоэза, вызванного противоопухолевыми средствами; при временной лейкопении после трансплантации костного мозга; при-миелодиспластическом синдроме, апластической анемии; при лейкопении, связанной с инфекционными заболеваниями (в том числе с ВИЧ). Вводят подкожно и внутривенно. Максимальная плазменная концентрация при подкожном введении достигается через 3—4 ч. Побочные эффекты: лихорадка, озноб, одышка, мышечно-скелетные боли, астения, тошнота, рвота, анорексия, диарея, головная боль, головокружение, сыпь, зуд, болезненность в месте введения. Аналогичными фармакологическими свойствами обладает другой рекомбинантный препарат человеческого гранулоцитарно-макрофагального колониестимулирую-щего фактора сарграмостим (Лейкин).
Филграстим (Нейпоген) — рекомбинантный препарат человеческого гра-нулоцитарного колониестимулирующего фактора. Регулирует продукцию нейт-рофилов и их выход в кровь из костномозговой ткани, а также активирует фагоцитарную и хемотаксическую активность нейтрофилов. Вводят подкожно и внутривенно капельно. Вызывает заметное увеличение количества нейтрофилов в течение 24 ч и незначительное увеличение моноцитов. Применяют при лейкопении, связанной с химиотерапией злокачественных заболеваний и др. Из побочных эффектов отмечаются костно-мышечные боли, дизурия, транзиторная артериальная гипотензия.
При легких формах лейкопении применяют метилурацил и пентоксил.
Метилурацил и пентоксил являются производными пиримидина. Стимулируют лейкопоэз, оказывают противовоспалительное действие, ускоряют процессы клеточной регенерации и способствуют заживлению ран. Принимают внутрь. Пентоксил обладает раздражающим действием и может вызвать диспеп-тические расстройства. Метилурацил таким действием не обладает. В качестве стимуляторов лейкопоэза применяют также лейкоген, батилол и этаден.
26.2.2. Средства, угнетающие лейкопоэз
Эти средства применяются при злокачественных поражениях кроветворной системы — лейкозах и лимфогранулематозе (см. гл. 42 «Противоопухолевые средства»).
Взаимодействие средств, влияющих на кроветворение, с другими лекарственными средствами
Взаимодействующий препарат (группа препаратов)
Железа закисного сульфат и его комбинированные препараты
Антациды, содержащие алюминий, магний, кальций
Нарушение всасывания железа за счет образования комплексов
Противомикробные средства из группы хинолонов
Антибиотики группы тетрациклина
Блокаторы Н 2 -гистаминовых рецепторов
Нарушение всасывания взаимодействующих препаратов за счет образования комплексов
Фолиевая кислота (длительный прием больших доз)
Снижение плазменной концентрации витамина В 12
Витамины В, и В 6 (в одном шприце)
Разрушение витаминов В, и В 6
Усиление аллергических реакций
Международное непатентованное название
Патентованные (торговые) названия
Железа закис-ного сульфат (Ferrosi sulfas)
Принимают за 1 ч до еды. Кофе, яйца, пища, содержащая гидрокарбонаты и карбонаты, оксалаты и фосфаты, молоко и молочные продукты, чай (танин), хлебные продукты, содержащие фитиновую кислоту, уменьшают всасывание железа за счет образования невсасывающихся комплексов. Запивать препараты железа рекомендуется полным стаканом воды или фруктового сока
Ампулы по 2 мл для внутримышечного введения и по 5 мл для внутривенного введения
Нельзя применять внутривенно препарат, предназначенный для внутримышечного введения
Ампулы по 1 мл 0,003%; 0,01%; 0,02%; 0,05% раствора
При стенокардии применять с осторожностью и в меньших дозах
Кислота фолиевая (Acidum folicum)
Принимают натощак, запивают достаточным количеством воды. Пропущенную дозу следует принять как можно скорее и не принимать ее вообще, если до приема последующей дозы не осталось времени; не принимать двойных доз
Порошок; таблетки, покрытые оболочкой, по 0,025 и 0,2 г
Препарат применяется только под наблюдением врача
Лиофилизированный порошок во флаконах, содержащих по 50, 150, 400, 500, 700, 1500 мкг
Препарат применяется только под наблюдением врача
СРЕДСТВА, ВЛИЯЮЩИЕ НА ТРОМБООБРАЗОВАНИЕ
Образование тромбов является защитной реакцией, которая обеспечивает остановку кровотечения (гемостаз) при повреждении сосудистой стенки. После повреждения сосудистой стенки возникает спазм сосудов. Эта немедленная реакция на травму может остановить кровотечение только при незначительных повреждениях мелких сосудов. В основном гемостаз достигается благодаря образованию тромбов (гемостатических пробок), которые закрывают просвет поврежденного сосуда и таким образом препятствуют кровопотере. Частой причиной образования тромбов могут быть патологические изменения эндотелия, включая его повреждения, связанные с атеросклерозом сосудов.
Тромбообразование происходит при участии двух основных процессов — агрегации тромбоцитов и свертывания крови (гемокоагуляции).
Агрегация тромбоцитов — это объединение тромбоцитов в конгломераты (агрегаты) разной величины и плотности. Этот процесс инициируется при повреждении сосудистой стенки. В месте повреждения тромбоциты связываются с фактором Виллебранда и с коллагеном субэндотелиального слоя, что стимулирует их агрегацию. При этом сами тромбоциты становятся источниками веществ, стимулирующих агрегацию, таких как тромбоксан А 2 , АДФ, серотонин. Тромбин, который высвобождается из тромбоцитов и образуется локально в процессе свертывания крови, также является индуктором агрегации тромбоцитов. Кроме того, агрегацию индуцируют катехоламины, фактор активации тромбоцитов и некоторые другие эндогенные вещества.
Агрегации тромбоцитов препятствуют простациклин и эндотелиальный релак-сирующий фактор, которые образуются клетками эндотелия сосудов и высвобождаются в кровоток. Однако при повреждении эндотелиальных клеток синтез этих веществ снижается и на таком фоне действие веществ, стимулирующих агрегацию, становится доминирующим. В результате тромбоциты объединяются в агрегаты, из которых формируется тромбоцитарный тромб.
Тромбоцитарный тромб становится более прочным благодаря нитям фибрина, который образуется в процессе свертывания крови. Основными участниками этого процесса являются белки плазмы крови, называемые факторами свертывания крови.
Плазменные факторы свертывания синтезируются в печени и циркулируют в крови в неактивной форме. При повреждении сосудистой стенки происходит быстрая активация фактора VII при участии тканевого фактора, который синтезируется эндотелиальными клетками, но в норме не контактирует с кровью. Экспрессия тканевого фактора на поверхности поврежденных эндотелиальных клеток значительно ускоряет активацию фактора VII (образование фактора Vila) в присутствии ионов Са 2+ . Под действием фактора Vila происходит последовательная активация других факторов свертывания крови (IX и X) в сложной аутокаталитической системе, называемой каскадом свертывания крови. В результате образуется тромбин (фактор Па), который превращает .циркулирующий в крови растворимый белок фибриноген (фактор I) в нерастворимый фибрин. Фибрин заполняет пространство между тромбоцитами и укрепляет тромбоцитарный тромб. Фибриновые нити образуют сеть, которая задерживает циркулирующие в крови эритроциты. Формируется так называемый красный тромб.
Свертыванию крови противодействуют вещества, которые являются естественными ингибиторами факторов свертывания крови. Активации фактора X под действием фактора Vila препятствует ингибитор пути тканевого фактора, синтезируемый эндотелиальными клетками. Ингибитором тромбина и некоторых других факторов свертывания (за исключением фактора VII) является антитромбин III -белок плазмы крови, действующий в комплексе с гепарином. Эти вещества являются компонентами противосвертывающей системы, которая способствует поддержанию крови в жидком состоянии даже при локальном образовании тромбов в месте повреждения сосуда.
Агрегация тромбоцитов и свертывание крови — взаимосвязанные процессы. Преобладание того или иного процесса в механизме тромбообразования зависит от калибра сосуда и скорости кровотока. Агрегация тромбоцитов имеет большее значение для формирования тромбов при высокой скорости кровотока, т.е. в артериях. В венозных сосудах, где скорость кровотока невелика, преобладает процесс свертывания крови.
Последующая судьба образовавшегося тромба зависит от активности фибри-
нолитической системы. Если эта система функционирует нормально, происхо
дит постепенное растворение фибрина (фибринолиз) при участии фермента пл$з-
мина (фибринолизина), который образуется из неактивного плазминогена под
влиянием активаторов плазминогена. Действию плазмина препятствуют цирку
лирующие в крови антиплазмины. Активаторы плазминогена нейтрализуются
специфическими ингибиторами. уНарушение процессов агрегации тромбоцитов и свертывания крови, а также повышение активности фибринолитической системы могут привести к кровоточивости, а чрезмерная активация этих процессов или угнетение фибринолиза — к возникновению тромбов (тромбозу). В результате тромбоза артериальных сосудов уменьшается приток крови к тканям, развивается ишемия тканей. Следствием ишемии является гибель клеток — некроз. Тромбозы могут быть причиной таких тяжелых осложнений, как инфаркт миокарда (тромбоз коронарных артерий), ишемический инсульт (тромбоз сосудов мозга) и т.д. Венозные тромбозы могут быть причиной эмболии легочной артерии.
Для предупреждения тромбозов используют вещества, которые ингибиру-ют агрегацию тромбоцитов и свертывание крови и таким образом препятствуют образованию тромбов. Кроме того, при тромбозах используют вещества, которые вызывают лизис образовавшихся тромбов — тромболитические (фибринолити-ческие) средства.
Для остановки кровотечений в основном применяют средства, повышающие свертывание крови и средства, угнетающие фибринолиз. Выбор тех или иных средств зависит от причины возникновения кровотечения.
Практическое значение имеют следующие группы средств, влияющих на тромбообразование.
Средства, снижающие агрегацию тромбоцитов (антиагреганты).
Средства, влияющие на свертывание крови:
средства, понижающие свертывание крови (антикоагулянты);
средства, повышающие свертывание крови (гемостатики). Средства, влияющие на фибринолиз:
фибринолитические (тромболитические средства);
антифибринолитические средства (ингибиторы фибринолиза).
источник
Понижение уровня гемоглобина в крови, преимущественно на фоне падения числа эритроцитов, в медицине известно как анемия – заболевание, являющееся симптомом разных патологических состояний. Одной из разновидностей анемии является гиперхромная, особенно часто поражающая лиц зрелого и преклонного возраста. Почему она возникает и как ее лечить?
Заболевание, известное большинству людей как малокровие, в официальной медицине названное «анемия», связано с падением уровня гемоглобина. При гиперхромной форме одновременно с этим снижается количество здоровых эритроцитов и появляются дефектные: содержащие в себе избыток железа. Благодаря этому веществу кровяные тельца становятся пресыщены гемоглобином, поэтому срединное просветление у них закрыто алым цветом (это видно при лабораторном исследовании анализов). Существует 2 вида анемии гиперхромной:
- Мегалобластная (макроцитарная) – характеризуется нарушением синтеза ДНК и РНК, что приводит к появлению очень крупных эритроцитов (мегалобластов и мегалоцитов) в костном мозге. Такая анемия может передаться по наследству.
- Немегалобластная – синтез ДНК в норме, костный мозг не продуцирует мегалобласты, но дефектные эритроциты присутствуют.
Большинство врачей не считают анемию самостоятельным заболеванием, поскольку она может развиться на фоне первичного поражения системы крови или при иных патологиях, никак с этим не связанных. По этой причине отсутствует строгая нозологическая классификация и, помимо уже упомянутого деления гиперхромного типа на 2 вида, существует группировка по состояниям, которым она соответствует:
- Витамин В12-дефицитная (пернициозная) анемия – болезнь Аддисона-Бирмера, злокачественное малокровие, обусловленное нехваткой витамина В12. Характеризуется образованием в костном мозге незрелых мегалобластов, может проявляться неврологическими расстройствами.
- Фолиеводефицитная анемия – тоже пернициозная, только возникает при дефиците фолиевой кислоты.
- Миелодиспластический синдром – характеризуется цитопенией (дефицит 1-ого или нескольких видов кровяных телец) в периферической крови, дисплазией (неправильным развитием) костного мозга. Заболевание склонно к переходу в острую форму лейкоза (недоброкачественное поражение системы кроветворения), тяжело поддается лечению (преимущественно проводится поддерживающая терапия). По официальной статистике 80% пациентов с миелодиспластическим синдромом старше 60-ти лет.
Дефицит витамина В12 (цианокобаламин) и фолиевой кислоты являются самыми распространенными отправными точками к развитию анемии гиперхромного типа, но эти состояния могут возникать под воздействием целого ряда факторов. Конкретный перечень причин для каждой ситуации свой. Нехватку цианокобаламина провоцируют:
- патологические процессы в подвздошной кишке, при которых происходит нарушение усвояемости питательных веществ за счет плохого всасывания ее стенками;
- инфекционные патологии кишечника, тоже нарушающие процесс всасывания витаминов;
- глисты – ленточные черви и бактерии активно поглощают витамин В12;
- атрофический гастрит, при котором в париетальных клетках желудка наблюдается недостаточный синтез внутреннего фактора Касла (фермент, который переводит цианокобаламин из неактивной формы в усваивающуюся).
У анемии гиперхромного типа, которая возникает как результат дефицита фолиевой кислоты, провоцирующие факторы выглядят иначе. Зачастую с таким состоянием сталкиваются женщины во время беременности, поскольку вся фолиевая кислота идет на строительство нервной трубки плода. Влияние могут оказывать и:
- алкоголизм;
- заболевания печени (особенно гепатит, цирроз, печеночная недостаточность).
Отдельно врачами упоминается гиперхромная макроцитарная анемия, которая носит наследственный характер (аутосомно-рецессивная передача – от родителей) и развивается на фоне генетических мутаций, а у женщин предпосылкой к ее возникновению является и прием гормональных препаратов. Если не рассматривать отдельные разновидности анемии, при которой у эритроцитов появляются гиперхромные ядра, в число общих причин можно включить:
- длительное голодание или нерациональное питание (с дефицитом витаминов и микроэлементов в пище);
- курение;
- наличие опухолей;
- инфекции (особенно ВИЧ) и вирусы;
- регулярная большая потеря крови во время менструации;
- рак желудка, гастрэктомия (его полное вырезание);
- гипотиреоз (дефицит гормонов щитовидной железы);
- прием лекарственных препаратов (Метформин, Неомицин, Дифенин);
- частые расстройства кишечника.
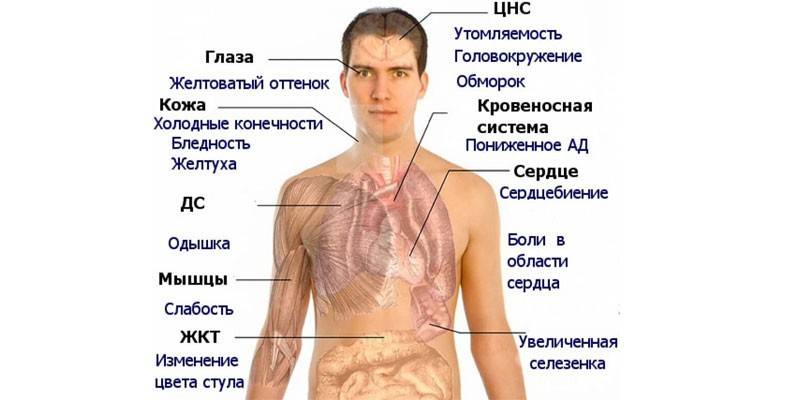
Заболевание имеет внешние и внутренние проявления: последние подразумевают изменения общего самочувствия, которые не всегда специфичны и не дают возможности поставить точный диагноз. К таким симптомам гиперхромного малокровия относятся:
- повышенная сонливость, усталость;
- снижение работоспособности;
- потеря концентрации внимания.
Данная клиническая картина характерна большинству случаев анемии, поэтому болезнь распознается исключительно после проведения лабораторных исследований. Если течение более тяжелое, могут добавиться:
- тахикардия (учащенный пульс);
- одышка при минимальных физических нагрузках (даже после быстрой ходьбы);
- шум в ушах (не постоянный);
- нарушения сна;
- потеря аппетита;
- головные боли;
- снижение либидо (полового влечения).
Почти во всех случаях гиперхромного малокровия можно наблюдать изменения во внешности: кожные покровы бледнеют, кожа истончается, становится сухой, на руках может приобрести желтоватый оттенок. В волосах появляется ранняя седина. Общая клиническая картина выраженной анемии дополняется следующими симптомами:
- потеря веса;
- расстройство зрения и слуха;
- тошнота, рвота;
- потеря вкуса, отсутствие влечения к ранее любимым продуктам и блюдам;
- мышечная слабость;
- онемение нижних конечностей;
- чувство зябкости;
- покраснение языка до малинового цвета, поверхность становится блестящей.
Лица, у которых гиперхромная анемия сочетается с миелопластическим синдромом, часто испытывают головокружения, повышенную утомляемость. Не исключены боли за грудиной при сильном сердцебиении и одышке. При сильном поражении нервной системы у пациента нарушается чувствительность пальцев (на ногах и руках), могут случаться потеря сознания, судороги. Артериальное давление преимущественно пониженное, печень увеличена (прощупывается при пальпации).
Авитаминоз по фолиевой кислоте для будущей матери – распространенное явление, поскольку этот элемент (вместе с цианокобаламином) требуется для полноценной жизнедеятельности плода. Потребность в витаминах В9 и В12 у беременной вырастает в 2 раза. При стремительном развитии и тяжелом течении анемия может спровоцировать преждевременные роды, недостаточный вес новорожденного, отслоение плаценты, внутриутробные кровотечения.
У детей анемия, при которой наблюдается гиперхромия эритроцитов, может привести к отставанию в развитии умственном и физическом, снижении защитных сил организма (ребенок будет часто подхватывать ОРВИ, тяжело переносить даже простуду). У взрослых распространенным осложнением анемии являются дефицит кислорода в крови, поражения нервной системы, на фоне чего возникают:
- гипоксия (кислородное голодание) мозга;
- ухудшение памяти и мышления;
- отмирание клеток головного мозга и нарушения работы его сосудов;
- сердечная недостаточность (может окончиться летальным исходом).
Отсутствие специфической клинической картины для анемии любого типа повышает значимость диагностических мероприятий для уточнения заболевания. Общий анализ крови является первичной проверкой, по результатам которой можно увидеть изменения в структуре эритроцитов (форма и размеры клеток), обнаружить ядерные тельца Жолли. При наличии подозрений на гиперхромное малокровие врач дополнительно назначает:
- биохимическое исследование крови – для определения уровня билирубина, сывороточного уровня железа;
- рентгеноскопию ОБП (органов брюшной полости);
- УЗИ органов пищеварения;
- иммунологическое исследование – помогает выявить антитела, которые специфичны против антигенов цитоплазмы париетальных клеток желудка и внутреннего фактора Касла.
Для легких форм гиперхромного малокровия основу терапевтической схемы составляет коррекция рациона питания, особенно если проблема кроется в дефиците фолиевой кислоты или витамина В12. Дополнительно за день важно принимать с едой 8 мг железа. Меню базируется на следующих продуктах:
- печень куриная, говяжья (2-3 раза в неделю);
- гречневая крупа;
- рыба (особенно треска);
- мясо (желательно ввести в рацион кролика);
- куриные яйца;
- сыры;
- бобовые культуры.
Обязательно употребление свежих овощей и фруктов, дополняющих список полезных при анемии продуктов. От острой и жареной пищи стоит отказаться, поскольку она раздражает пищеварительную систему. Кофеин тоже исключен, поскольку он мешает усваиваться железу. Такой диеты следует придерживаться несколько месяцев (в некоторых случаях – больше года), она актуальна для всех стадий заболевания, но не исключена индивидуальная коррекция рациона под конкретную клиническую картину. Медикаментозное лечение зависит от причин анемии и ее течения:
- Терапия легких дефицитных состояний начинается с назначения Цианокобаламина: синтетического аналога витамина В12, который принимается перорально или вводится внутримышечно. Если спустя 1-1,5 недели после начала его использования положительной динамики не наблюдается, врач выписывает Фолиевую кислоту (таблетки), Фемибион. В некоторых случаях проводится одновременное лечение обоими препаратами.
- При средней степени выраженности анемии Цианокобаламин или Оксикобаламин (более сильный препарат для тяжелых случаев) вводятся внутривенно и на 5-8 день отслеживается уровень ретикулоцитов: их количество должно возрасти на 20-30%.
- По необходимости назначаются препараты железа – Мальтофер, Гемофер (таблетки, инъекции), особенно если заболевание диагностировано у ребенка.
- Во время беременности (или после родов, если состояние не улучшается) врач может назначить пациентке внутривенное введение витаминных препаратов, начиная с больших доз. После они уменьшаются, а инъекционная форма заменяется на пероральную.
Восстановление показателей крови происходит быстро: уже через месяц можно видеть результат, а неврологические нарушения устраняются медленнее и могут требовать дополнительных препаратов. Если начальную (легкую) форму гиперхромного малокровия можно лечить амбулаторно (дома), то средняя и тяжелая требуют помещения пациента в стационар, где ему будут делать инъекции лекарственных средств и постоянно отслеживать состояние. Несколько моментов лечения таких случаев анемии:
- Резкое нарушение гемодинамики, падение гемоглобина ниже 70 г/л (тяжелая форма анемии) требуют немедленной гемотрансфузии – переливания крови.
- При миелодиспластическом синдроме обязательны госпитализация, гемотрансфузия (переливаются эритроцитарная и тромбоцитарная массы, зачастую с замещением клеток) и внутривенное введение препаратов, ускоряющих деление кровяных телец, чтобы предотвратить лейкоз.
- Если лечение подразумевает инъекционное введение лекарственных средств одновременно с приемом таблеток, такой курс длится 2-3 месяца. После раз в неделю делают 1 укол, оставляя таблетки, а через 2 месяца их ставят с частотой 1 раз в 14 дней. Основной формой лечения не тяжелых состояний являются таблетки.
Лечение анемии гиперхромной длится от полугода до года, дефицитные состояния за этот срок полностью устраняются. При миелодиспластическом синдроме терапия стационарная, прогноз неутешительный, поскольку препараты только способствуют увеличению срока жизни и сдвигают момент ремиссии. Шансы на исключение летального исхода возникают только при пересадке костного мозга.
Соблюдение принципов здорового питания, поддержание хорошего уровня витаминов В9 и В12, железа – самый простой и важный способ защиты от гиперхромного малокровия, особенно для беременных. Диета, используемая для его лечения, одновременно носит и профилактический характер. Дополнительно стоит:
- регулярно посещать гастроэнтеролога;
- заниматься спортом;
- отказаться от курения;
- не контактировать с ядохимикатами;
- гулять на свежем воздухе;
- своевременно лечить инфекционные заболевания, выводить паразитов;
- принимать витаминно-минеральные комплексы.
источник