Лабораторно-диагносточеский подход при синдроме анемии. Приведенная ниже патогенетическая классификация составляет основной материал в деле диагностирования анемии. Группировка анемий по морфологический критериям в результате гематологических исследований представляет собой одно из диагностических направлений, которое, однако, следует связать с этиопатогенетическими механизмами.
Диагноз этиопатогенетической формы осуществляется классическими исследованиями периферической крови и костного мозга во взаимосвязи с данными частных биологических исследований. Хорошо ориентирующийся в проблеме этиопатогенеза анемий клиницист запрашивает в лаборатории поэтапное проведение исследований при сопоставлении результатов которых уточняется правильное диагностическое определение.
Целью поэтапного исследования является, в первую очередь, определение синдрома анемии, как такового, затем ее этиопатогенетическую форму, тяжесть и течение.
Диагностирование синдрома анемии проводится на основе известных исследований периферической крови, таких как, определение гемоглобина, массы красных кровяных телец путем их подсчета, или, особенно, уточнением гематокрита. Это перечисление следует дополнить частными исследованиями красных кровяных телец и определением их показателей, в том числе диаметра, объема, количества гемоглобина на каждое красное кровяное тельце, процент нагрузки гемоглобином.
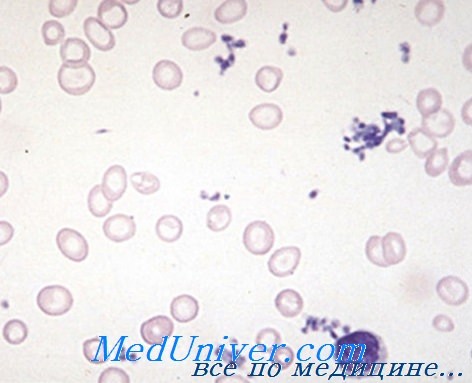
Морфологические сдвиги, уточненные исследованием окрашенных по Май-Грюнвальду-Гимза мазков, представляют особую ценность. Морфология эритроцитов указывает на быстроту их восстановления, нагрузку гемоглобином, а в отдельных случаях и на наличие патологического гемоглобина, как, например, при талассемии, дрепаноцитозе и т.д.
Патогенетическая классификация анемий
Довольно четко выделяются следующие виды анемии:
1) регенеративная — с молодыми красными кровяными тельцами, полихроматофилией, анизохромией, кольцами Кабо, базофильными точками; при этом рост ретикулоцитов более 2,5—3% составляет признак анемии по периферической причине, за счет геморрагии или гемолиза;
2) гипорегенеративная — за счет аплазии костного мозга, при которой выявляются состарившиеся красные кровяные тельца, в принципе нормохромные и нормоцитные, без признаков регенерации и заниженным ретикулоцитозом;
3) группа классических анемий, за счет недостатка созревания, по виду бирмеровской или железодефицитной анемии, которые, с точки зрения кроветворения также гипорегенеративные. Периферическое исследование выявляет особую характеристику красных кровяных телец мегалобластической группы с наличием макрофагов и мегалоцитов, пойкилоцитоза, а в отдельных случаях почти патогномоничное присутствие мегалобластов.
В отношении гипохромной анемии, независимо от причины, вообще обнаруживаются микроциты с анизоцитозом, также характерное наличие аннулоцитов с периферическим расположением гемоглобина. Эритроцитные показатели свидетельствуют о небольшом содержании гемоглобина, в то время как заниженный ретикулоцитоз составляет признак гипорегенерации. Наличие пигмента железа в красных кровяных тельцах отличает гипосидеремическую гипохромную анемию от сидероакктрестической.
Морфологическое исследование костного мозга уточняет следующие виды миелограммы:
1) апластический или гипопластический костный могз, характерный апластичеокой анемии;
2) гиперпластический костный могз, охватывающий два вида:
а) активный регенеративный гиперпластический костный мозг со всей эритробластической филиацией и явными признаками созревания по виду ретикулоцитов — характерный гемолитической анемии всех видов и анемии с острыми кровотечениями (анемии периферической природы);
б) гиперпластический костный мозг с множеством молодых клеток, преобладание которых указывает на недостаточность созревания; при этом различаются макромегалобластический или мегалобластический вид — подобно анемии Бирмера, эритробласти-ческий вид — как при гипохромной анемии,
Следует отметить, что макробластические отклонения наблюдаются при отдельных острых или хронических гемолитических анемиях за счет расхода факторов созревания, в то время как мегалобластические — при ночной пароксизмальной гемоглобинурии, сидероаккрестических и прочих анемиях сложной зтиологии, описанных под названием дисэритропоэтических анемий с гигантскими мегалобластами.
Специальные биологические исследования составляют обязательный этап в процессе постановки этиопатогенетического диагноза отдельных видов анемии. Эти исследования проводятся комплексными методами путем сотрудничества клинициста, морфолога, биохимика и иммунолога. В каждой группе преобладает тот или иной вид частных исследований.
Как уже говорилось, во многих анемиях морфологические периферические и центральные исследования достаточны для постановки диагноза, как, например, при апластической анемии, с дополнительной биопсией костного мозга. Некоторые исследования общего характера, организуемые на основе данных анамнеза, стремятся уточнить этиологическую — токсическую, инфекционную, раковую или пр. природу аплазии костного мозга.
Так, исследование интенсивности и скорости метаболизма железа предоставляет ценный материал, по которому определяется неспособность костного мозга использовать железо и откладывать его в отдельные органы.
При других анемиях, как описано ниже, частные исследования необходимы для уточнения их этиопатогенетической природы.
1) Диагностика гемолитической анемии. На первом этапе при помощи исследования расплавления крови, уточняются: гипербилирубинемия, уробилинурия, повышенный показатель стеркобилина, гиперсидеремия, с увеличенными интенсивностью и скоростью метаболизма железа; иногда невысокая устойчивость кровяных клеток — как, например, при микросфероцитозе и повышенном аутогемолизе; при этом продолжительность жизни красных кровяных клеток невелика в любом из видов гемолитической анемии.
На следующем этапе частные исследования стремятся уточнить природу расплавления крови (путем эндо- или экзоэри-троцитного механизма). Так, уточняется диагностика микросфероцитоза, гемоглобинопатии или энзимопатии сопоставлением морфологических периферических сдвигов и осмотической устойчивости, аутогемолиза, методами определения гемоглобина и прямыми или косвенными испытаниями, уточняющими ферментативную недостаточность.
Наличие телец Гейнца, характерно гемолитическим анемиям за счет гемоглобинопатии, отдельных энзимопатии или токсических факторов окислительного действия на гемоглобин. Среди гемолитических экзоэритроцитных анемий особую характеристику представляют те из них, которые обусловлены свинцовым отравлением. Особо важную группу составляют изоиммунные и аутоиммунные гемолитические анемии, которые исследуются правильным применением прямой или косвенной техники Кумбса с сыворотками антигамма и антинонгамма, в теплых и холодовых условиях.
Специальные методы требуются в постановке диагноза гемолитической анемии за счет сенсибилизации к медикаментам, что определяется тестами гемолиза, в том числе реакцией Кумбса, в присутствии сенсибилизирующих препаратов.
2) Диагностика анемии за счет острого кровотечения предполагает общее исследование для уточнения внутреннего кровотечения по местным, висцеральным (язва или рак желудка, разрыв аневризмы) или общим (в рамках геморрагического, фибриногенопенического, воротногипертензивного и пр. синдромов) причинам.
3) Группа анемий за счет недостаточности созревания. Когда морфологические исследования оказываются недостаточными, необходимо прибегнуть к частным исследованиям. Так, в бирмеровской и парабирмеровской группах анемии подвергаются исследованию недостаточность выделения желудочного сока, отсутствие фактора Castle с помощью реакции Шиллинга.
В хорошо оснащенных лабораториях высокая точность диагноза достигается биологическими или радиохимическими методами в целях определения циркуляции витамина В12 и фолиегой кислоты.
4) Гипохромная анемия. Помимо текущих исследований в отдельных случаях необходимо использование и частных методов определения механизма гипохромии. Так, проводится исследование интенсивности и скорости метаболизма железа, уточняется плазматический раздел с определением трансферина, предельной насыщаемости, способности резорбции слизистой оболочкой желудка.
Затем определяются загрузка железом и его отложения в РЭС или сидеробластах, используя на то метод прямой окраски в костном мозге или радиоактивные способы.
Поэтапное проведение этих исследований входит в обязанности обычных гематологических лабораторий, которые уточняют диагностику значительного числа анемий, включительно гемолитических аутоиммунных, а косвенными способами даже гемолитических, обусловленных гемоглобине- и энзимопатией.
Применение частных способов, таких как определение продолжительности жизни, интенсивности и скорости метаболизма железа, электрофоретическая характеристика определенного патологического гемоглобина, недостаточности отдельных эритроцитных ферментов, циркуляции витамина В12 и фолиевой кислоты — возлагаются на высокоспециализированные лаборатории. Перед назначением специфической терапии рекомендуется использовать все виды исследования в целях устранения любой возможной нечеткости.
Неоправдывающие себя лечения витамином В12 и фолиевой кислотой, равно как и кортизонотерапия или лечение иммуносупрессорными средствами при предполагаемых аутоиммуных анемиях в значительной мере способствуют не правильному диагностированию заболевания.
источник
23. Лабораторная диагностика гемолитических анемий. Виды гемолиза. Компенсированный и субкомпенсированный гемолиз.
Гемолитические анемии — большая группа наследственных и приобретенных заболеваний, при которых процессы кроворазрушения преобладают над процессами кровообразования. При них снижена продолжительность жизни эритроцитов. Разрушение эритроцитов (гемолиз) может развиться под влиянием эндодогенных и экзогенных причин. К эндогенным причинам относят нарушения структуры гемоглобина или эритроцитов. К экзогенным — воздействие различных токсических веществ, антител, механических повреждений на эритроциты с неизменными морфологическими свойствами и функциональной активностью Гемолиз может быть компенсированным и декомпенсированным. При компенсированном гемолизе анемия не развивается так как снижение числа эритроцитов, обусловленное их гемолн зом, компенсируется выходом новых эритроцитов из костного мозга. Костный мозг при необходимости может повысить свою кроветворную функцию в 6—8 раз. Если у больного на фоне снижения продолжительности жизни эритроцитов наблюдается и длительный гемолиз, то компенсаторные возможности красного ростка костного мозга снижены и он не может восполнить количество разрушенных эритроцитов, в результате чего развивается анемия (декомпенсированный гемолиз).
Клиническая картина гемолитических анемий вариабельна, зависит от этиологии, патогенеза, продолжительности заболевания и степени компенсации гемолитического процесса. Клинически гемолиз эритроцитов может протекать в виде: 1) периодически возникающих гемолитических кризов, вне кризов больные чувствуют себя здоровыми; 2) хронического течения, которое периодически осложняется гемолитическими кризами.
Продолжительность жизни эритроцитов составляет 90—120 дней. Около 90% состарившихся эритроцитов разрушается в макрофагах селезенки с образованием желчных пигментов; 10% эритроцитов разрушается в капиллярах сосудистого русла с выделением свободного гемоглобина, который в норме составляет 10—40 мг/л. Свободный гемоглобин связывается с белком плазмы гаптоглобином. Гаптоглобин может связать не более 1 г/л свободного гемоглобина. Связанный с гаптоглобином свободный гемоглобин не проходит через почечный фильтр. Процессы физиологического разрушения старых и образования новых эритроцитов в организме уравновешены. При гемолитических анемиях процессы разрушения эритроцитов преобладают над процессами их образования.
Различают гемолитические анемии с внутриклеточным и с вну- трисосудистым гемолизом. Гемолитические анемии, обусловленные внутриклеточным гемолизом эритроцитов, — чаще наследственные заболевания, имеющие хроническое течение. Для них характерно нарушение мембран эритроцитов, приводящее к повышению их проницаемости для ионов натрия и воды, в результате чего эритроциты приобретают форму сфероцитов. Нормальные эритроциты, имеющие форму двояковогнутого диска, обладают способностью изменять ее, уплощаться, что позволяет им легко проходить через синусы селезенки, в самые узкие места кровотока. Эритроциты в форме сфероцитов задерживаются в синусах селезенки, разрушаются, фагоцитируются клетками системы фагоцитирующих мононуклеаров. Если в селезенке разрушается много эритроцитов, она увеличивается в размерах вплоть до спленомегалии. Внутриклеточный гемолиз еще называют селезеночным. Гемолиз эритроцитов сопровождается образованием желчных пигментов.
Клинические признаки гемолитических анемий с внутриклеточным гемолизом: анемия, желтуха, спленомегалия. Лабораторные признаки внутриклеточного гемолиза: билирубинемия за счет свободного билирубина, увеличение стеркобилиногена в кале (кал приобретает темно-коричневую окраску), уробилинурия (за счет всасывания больших количеств стеркобилиногена), снижение осмотической резистентности эритроцитов.
Гемолитические анемии с внутрисосудистым гемолизом — приобретенные заболевания. Развиваются остро, часто возникновение гемолиза связано с воздействием неблагоприятных факторов: токсинов, приемом лекарств и др. Гемолиз происходит в капиллярах почек, его называют почечным гемолизом. При разрушении эритроцитов появляется свободный гемоглобин. Если его содержание превышает 1 г/л, то он не весь свяжется с гаптоглобином. Избыток свободного гемоглобина будет проходить через почечный фильтр, он появляется в моче, за счет чего она становится темно- коричневого или черного цвета (гемоглобинурия). Уровень гемогло- бинурии зависит от содержания свободного гемоглобина и уровня гаптоглобина в плазме. При прохождении через канальцы почек свободный гемоглобин частично разрушается, откладывается в эпителии канальцев, появляется в моче в виде гемосидерина (гемосидеринурия). Если уровень свободного гемоглобина плазмы значительно возрастает, образуется метальбумин плазмы, за счет которого кровь при остром внутрисосудистом гемолизе приобретает лаковый, коричневатый цвет.
Лабораторные признаки острого внутрисосудистого гемолиза: гемоглобинемия, гемоглобинурия за счет свободного гемоглобина, гемосидеринурия.
Для выработки тактики лечения нужно правильно определить место гемолиза. При внутриклеточном гемолизе рекомендована спленэктомия, при внутрисосудистом она не показана.
При диагностике гемолитических анемий используются лабораторные признаки гемолиза: ретикулоцитоз, снижение осмотической резистентности эритроцитов, билирубинемия за счет свободного билирубина, увеличение стеркобилиногена в кале, уробилинурия, изменение морфологии эритроцитов (микросфероцитоз, овалоцитоз и др.), гемоглобинемия, гемоглобинурия за счет свободного гемоглобина, гемосидеринурия, появление в эритроцитах телец Гейнца, обнаружение нестабильных гемоглобинов, увеличение гемоглобина Аг, положительные пробы на аутогемолиз эритроцитов, прямая проба Кумбса, дефицит глюкозо-6-фосфатдегидрогеназы и других ферментов в эритроцитах, характер антител, раздражение красного ростка костного мозга. Перечисленные лабораторные признаки гемолиза используют дифференцированно при диагностике различных форм гемолитических анемий.
источник
Анемия – состояние, характеризующееся снижением гемоглобина и почти всегда эритроцитов в крови. У мужчин анемия возникает при уровне гемоглобина менее 130 г/л, эритроцитов – 4 *1012/л. У женщин аналогичные показатели составляют – 120 г/л и 3,8 * 1012/л соответственно.
В основу клинических проявлений положен дефицит эритроцитов и гемоглобина. Нехватка этого белка приводит к неспособности поддерживать газообмен крови на необходимом уровне.
Анемия может быть относительной и абсолютной. Абсолютная вызвана снижением уровня красных кровяных клеток. Относительная – является результатом процесса, происходящего в организме. Одним из таких может быть:
- увеличение объёма плазмы;
- беременность;
- недостаточность сердца;
- острая потеря крови;
- переливание кровезаменителей.
Для того чтобы немножко разбираться в анемии, разберём её основную классификацию.
- гипохромные – цветовой показатель ниже нормы (менее 0,85). Характерно для железодефицитной анемии и талассемии;
- нормохромные – цветовой показатель в пределах нормы;
- гиперхромные – повышен цветовой показатель (более 1,1). Характерно для мегалобластных анемий.
Цветовой показатель показывает степень насыщения эритроцита гемоглобином. В норме составляет 0,85 – 1,05. Высчитывается он следующим образом:
Цветовой показатель = (гемоглобин * 3)/ первые три цифры показателя уровня эритроцитов.
Например, гемоглобин составляет 140 г/л, а число эритроцитов – 4,5*1012/л. Тогда цветовой показатель будет равен 140 * 3/450 = 0,93. Это соответствует нормальному значению.
- лёгкая степень – уровень гемоглобина не опускается ниже 90 г/л;
- средняя степень – концентрация гемоглобина составляет 70 – 90 г/л;
- тяжёлая степень – содержание гемоглобина в крови менее 70 г/л.
- арегенераторная – характерно отсутствие ретикулоцитов в крови, такое может быть, например, при апластической анемии;
- гипорегенераторная – низкое содержание ретикулоцитов в крови. Наблюдается при железодефицитной анемии;
- норморегенераторная – уровень ретикулоцитов в пределах нормы;
- гиперрегенераторная – количество ретикулоцитов выше нормы, характерно для гемолитической анемии.
Регенераторная способность костного мозга оценивается по уровню ретикулоцитов крови. В норме их содержание в крови составляет 2 – 12‰ или 0,2 – 1,2%.
- в результате потери эритроцитов. Анемия возникает при кровопотере (острой или хронической);
- в результате повышенного разрушения красных кровяных клеток. Это приводит к развитию гемолитической анемии;
- вследствие нарушения образования эритроцитов и гемоглобина. Примером такого механизма развития является мегалобластная анемия.
Микросфероцитарная гемолитическая анемия (болезнь Минковского — Шоффара)
В основе данной патологии лежит дефект, в результате которого нарушается взаимодействие спектрина и анкирина – белков мембраны эритроцита, что приводит к нарушению её проницаемости.
Микросфероцитарная гемолитическая анемия наследуется по аутосомно-доминантному типу. Заподозрить это заболевание можно по проявлению гемолитического синдрома (желтуха, спленомегалия), развитию анемии. При развитии микросфероцитоза в детском возрасте могут быть деформации костей скелета, отставание в развитии. Может манифестировать и лёгкая форма без ярко-выраженных клинических признаков.
Явным диагностическим признаком наличия у пациента болезни Минковского — Шоффара является:
- микросфероцитарная форма эритроцитов;
- низкая осмотическая резистентность эритроцитов;
- присутствует ретикулоцитоз – повышение уровня ретикулоцитов.
Данная патология может сопровождаться гемолитическим кризом.
Овалоцитарная гемолитическая анемия
Наследственный овалоцитоз, эллиптоцитоз – другие названия овалоцитарной гемолитической анемии. Это редко встречаемая форма, при которой снижается стабильность мембраны эритроцитов.
По большей части овалоцитоз протекает без каких-либо симптомов, лишь у 10% возможно развитие более тяжёлого состояния.
Клинически проявления ничем не отличаются от болезни Минковского — Шоффара. Дифференциальная диагностика между овалоцитозом и микросфероцитозом проводится в основном по форме эритроцитов.
Акантоцитоз – заболевание, которое наследуется по аутосомно-рецессивному типу. Обычно такое состояние возникает при абеталипопротеинемии. При данной патологии снижается уровень триглицеридов, холестерина, что сказывается на строении мембраны эритроцитов. При акантоцитозе красные кровяные клетки принимают форму листа аканта. Эритроциты разрушаются внутриклеточно в селезёнке.
К клиническим симптомам помимо признаков анемии и гемолитического синдрома добавляется пигментный ретинит (заболевание глаз), тремор рук, атаксия.
Особенностью акантоцитоза являются форма эритроцитов при микроскопии – клетки с зубчатым контуром.
Дефицит глюкозо-6-фосфатдегидрогеназы
Дефицит глюкозо-6-фосфатдегидрогеназы приводит к гемолизу эритроцитов. Этот фермент катализирует реакцию образования НАДФН. При дефиците НАДФН эритроцит и гемоглобин разрушаются.
Дефицит глюкозо-6-фосфатдегидрогеназы является наиболее распространённой гемолитической анемией, связанной с дефектом фермента.
Провоцирующим фактором являются инфекционные заболевания, вдыхание пыльцы растений, употребление конских бобов, некоторых лекарственных средств (их список представлен ниже).
Первыми признаками развития гемолитической анемии при приёме лекарств является пожелтение склер и потемнение мочи. Если не прекратить их употребление, то в дальнейшем может развиться гемолитический криз.
Гемолиз внутри сосудов может привести к поражению микроциркуляции, образованию тромбов и, как следствие, поражению почек.
Диагноз дефицита глюкозо-6-фосфатдегидрогеназы подтверждается определением уровня этого фермента в крови.
Дефицит пируваткиназы
Пируваткиназа катализирует реакцию, в ходе которой образуется АТФ (аденозинтрифосфат), являющийся энергетическим субстратом. АТФ обеспечивает много процессов клетке, например, поддерживает необходимую концентрацию ионов внутри клетки.
При дефиците пируваткиназы снижается уровень АТФ, нарушается электролитный состав клетки, что приводит к сморщиванию эритроцита. В таком виде клетки с трудом выполняют свои функции по транспорту газов в крови.
Чаще всего клинические симптомы появляются при возникновении тяжёлых форм дефицита пируваткиназы, которые проявляются с рождения. Часто бывают гемолитические кризы.
При кризах в крови:
- повышен непрямой билирубин;
- ретикулоцитоз до 70%.
Криз может быть спровоцирован беременностью или инфекционным процессом.
Диагноз также подтверждается уровнем фермента в крови.
Изменение структуры гемоглобина также может являться причиной развития гемолитической анемии. Выделяют качественные и количественные гемоглобинопатии.
К количественным относится талассемия, обусловленная генетическим дефектом строения цепей гемоглобина. В результате нарушается процесс переноса кислорода к тканям. Различают альфа-талассемию и бета-талассемию. Бывают также лёгкие бессимптомные и тяжёлые формы.
При талассемиях изменяется состав фракций гемоглобина, превалирует фетальный (HbF). Вовремя назначенное лечение снижает риск развития неблагоприятного исхода.
К качественным гемоглобинопатиям относится серповидноклеточная анемия. Это заболевание распространено в станах Африки, Индии, Азии. Дефект в строении молекулы гемоглобина приводит к изменению формы эритроцитов на серповидные. Продолжительность таких видоизменённых красных кровяных клеток составляет 17 дней.
Для лиц с серповидноклеточной анемией характерна устойчивость к воздействию малярийного плазмодия. Эритроциты так изменены, что паразит просто не может проникнуть в них.
Характерными симптомами серповидноклеточной анемии являются боли в суставах, их симметричное опухание, боли в животе, увеличение селезёнки, пожелтение кожи.
Диагноз подтверждается по наличию HbS и серповидной формы эритроцитов.
Данная группа заболеваний обусловлена возникновением антител против собственных эритроцитов крови, в результате чего они агглютинируют и разрушаются. Существует подразделение аутоиммунной гемолитической анемии на:
- аутоиммунная гемолитическая анемия, при которой образуются неполные тепловые агглютинины;
- аутоиммунная гемолитическая анемия с образованием тепловых гемолизинов;
- аутоиммунная гемолитическая анемия с образованием полных холодовых агглютининов;
- аутоиммунная гемолитическая анемия с двухфазными гемолизинами.
Чаще всего аутоиммунная гемолитическая анемия развивается у детей до 10 лет или у взрослых после 40.
Диагностика аутоиммунной анемии должна включать проведение прямой и непрямой пробы Кумбса.
В таблице 2 представлена краткая характеристика разновидности аутоиммунной гемолитической анемии.
| Разновидность | Иммунный фактор | Клинические проявления |
| Аутоиммунная гемолитическая анемия, развитие которой обусловлено неполными тепловыми агглютининами | Тепловые агглютинины, которые могут появиться при антибиотикотерапии. | Анемический синдром, |
Гемолитический синдром
Гемолитическая болезнь плода и новорождённого
Данное заболевание является разновидностью аутоиммунной гемолитической анемии. Развивается при несовместимости матери и плода по резус-фактору: мама резус-отрицательная, а ребёнок резус-положительный.
Кровь ребёнка, так или иначе, попадает в организм матери. В результате этого начинают вырабатываться антитела против эритроцитов ребёнка. Они попадают в организме плода, вызывают гемолиз эритроцитов.
Гемолитическая анемия у детей в первые дни будет сопровождаться такими симптомами, как гемолитическая желтуха, повышение непрямого билирубина в крови, стеркобилина в кале и уробилина в моче, увеличение печени и селезёнки, увеличение ретикулоцитов.
Основными причинами гемолитической анемии могут быть инфекции, лекарственные средства, токсины.
Обусловленные инфекцией
Малярийный плазмодий в процессе своего жизненного цикла в эритроцитах способен вызывать их гемолиз.
Гемолитико-уремический синдром – патологическое состояние, для которого характерно развитие тромбоцитопении, азотемии и гемолитической анемии. Чаще всего данная патология развивается у детей. Опасно при этом поражение почек. Причиной развития этого синдрома является кишечная инфекция (E. coli).
Обусловленные механическим повреждением эритроцитов
- Травма с микроангиопатическим гемолизом. Причина травмирования эритроцитов может быть различной:
- маршевая гемоглобинурия;
- дефект протезов клапана сердца или развитие стеноз аортального клапана;
- ДВС-синдром;
- злокачественная артериальная гипертензия.
В анализах крови наблюдается повышенный уровень лейкоцитов, низкий уровень тромбоцитов, факторов свёртывания, MCV.
- Маршевая гемоглобинурия. Механическое разрушение эритроцитов происходит в капиллярах стоп. Основным клиническим проявлением является появление чёрной мочи после длительной ходьбы. После прекращения ходьбы моча приобретает нормальный цвет. Такая форма гемолитической анемии встречается редко. Из всех выявленных случаев чаще всего болели мужчины, у которых имелась значительная нагрузка на ноги – ходьба, марш, бег.
- Химические вещества. Эти вещества могут вызывать окисление гемоглобина, также приводят к образованию радикалов и перекиси водорода, что в дальнейшем может привести к кислородному взрыву и гемолизу клеток. Гемолиз эритроцитов могут вызывать:
- сапонин;
- фенилгидразин;
- мышьяк;
- свинец;
- токсины грибов;
- и другие.
- Ожоговая болезнь. При ожоговой болезни может отмечаться гемолиз эритроцитов. Его проявления видны не сразу. В послешоковом периоде происходит снижение уровня гемоглобина, эритроцитов, иногда появляется желтуха. В моче может присутствовать гемоглобин при тяжёлых случаях.
- Тромботическая тромбоцитопеническая пурпура (болезнь Мошковица).Заболевание развивается внезапно и его основными признаками могут быть:
- снижение уровня тромбоцитов в крови;
- геморрагический синдром (кровотечения различной локализации);
- снижение гемоглобина;
- нарушения сознания;
- судороги;
- лихорадка;
- поражение почек;
- ретикулоцитоз;
- повышение билирубина;
- наличие шизоцитов в крови (1 – 18%).
Гемолитическая анемия симптомы имеет общие для всех её разновидностей. Клинические проявления гемолитической анемии обширны. Но основными являются анемический и гемолитический синдромы.
Проявления анемического синдрома:
- бледная кожа и слизистые оболочки;
- головокружение;
- слабость;
- быстрая утомляемость;
- наличие одышки при физической нагрузке;
- учащённое сердцебиение.
Проявления гемолитического синдрома:
- спленомегалия – увеличение селезёнки в размерах;
- потемнение мочи;
- кожа и слизистые приобретают жёлтый окрас.
Клинические симптомы характерные для конкретной формы гемолитической анемии мало отличаются между собой.
К осложнениям, которые могут развиться при гемолитической анемии, относятся:
- появление сердечной недостаточности;
- появление почечной недостаточности;
- разрыв селезёнки;
- гемолитический криз.
Диагностические мероприятия по выявлению гемолитической анемии подразделяются на две составляющие:
- диагностика процесса гемолиза;
- выявление источника разрушения эритроцитов.
Разрушение эритроцитов может происходить внутри клеток путём переваривания неправильных эритроцитов фагоцитами. Обычно это происходит в селезёнке. Также гемолиз красных кровяных клеток может происходить внутри сосудистого русла под действием циркулирующих, например, антител.
Как узнать, каким образом происходит разрушение эритроцитов, помогут следующие показатели, представленные в таблице 3.
Таблица 3. Лабораторные показатели, свидетельствующие о внутриклеточном и внутрисосудистом гемолизе
| Вид гемолиза | Лабораторный показатель |
| Внутриклеточный | Обнаружение гемосидерина (продукт окисления избытка свободного гемоглобина) в моче. Обнаружение гемоглобина в моче (вследствие быстрого разрушения эритроцитов). |
| Внутрисосудистый | Снижение эритроцитов, гемоглобина, повышение ретикулоцитов. Увеличение непрямого билирубина. Патологические эритроциты могут встречаться в мазках крови. |
После того, как по анализам крови понятно, что в организме происходит разрушение красных кровяных клеток, необходимо найти причину.
Важно собрать полную информацию о жизни пациента: где жил, что ел, кем работал. Пациент рассказывает, какие симптомы у него появились сначала, прогрессировали ли они.
Врач проводит осмотр кожи и слизистой оболочки пациента, пальпацию печени и селезёнки.
Лабораторные анализы, назначенные врачом, для диагностики причины гемолиза:
- прямая проба Кумбса – обнаружение антител, фиксированных на эритроцитах;
- непрямая проба Кумбса – выявление циркулирующих в крови антител к эритроцитам;
- определение ЦИК (циркулирующих иммунных комплексов) в крови;
- определение осмотической резистентности эритроцитов – понижена при сфероцитозе, овалоцитозе и акантоцитозе;
- определение эритроцитов с тельцами Гейнца;
- определение активности ферментов в эритроцитах, например, глюкозо-6-фосфатдегидрогеназы и пируваткиназы;
- определение фракций гемоглобина путём электрофореза – для диагностики гемоглобинопатии (талассемии и серповидноклеточной анемии);
- исследование эритроцитов на серповидность;
- исследование крови на наличие паразитов – «толстая капля» помогает обнаружить малярийного плазмодия;
- пробы Хема и Хартмана – определение длительности жизни эритроцитов при добавлении кислоты или сахара;
- миелограмма – результат пункции костного мозга.
Кроме лабораторных анализов могут быть назначены инструментальные методы исследования, например, УЗИ для оценки состояния селезёнки и печени.
Гемолитическая анемия лечение имеет, которое является нелёгким процессом, и зависит от различных факторов.
Если в процессе диагностики удалось выяснить, что служит причиной разрушения эритроцитов, то пытаются устранить этот фактор.
При подтверждении аутоиммунной природы патологии назначаются глюкокортикоиды в качестве подавителя иммунных реакций. Напомню, что аутоиммунная гемолитическая анемия возникает при выработке антител к эритроцитам, в результате чего они подвергаются гемолизу.
Если же процесс разрушения эритроцитов протекает остро, то назначается переливание эритроцитарной массы.
При гемоглобинопатиях тяжёлых форм, которым зачастую требуются частые переливания крови, назначаются препараты, связывающие и выводящие из организма избыток железа. Таким образом, не допускается откладывание избытка железа в органах и тканях.
В ситуациях, когда гемолитическая анемия является осложнением какого-либо состояния, важная роль отводится лечению основного заболевания. После выздоровления обычно признаки гемолитической анемии исчезают.
Имеется ряд ситуаций, когда проводится оперативное вмешательство, например, удаление селезёнки. Чаще всего спленэктомия применяется как метод лечения мембранопатий и гемоглобинопатий.
Пересадка костного мозга также является одним из способов лечения гемолитической анемии.
Исход заболевания будет зависеть от причин возникновения гемолитической анемии, её формы и степени течения. Если не брать во внимание наследственные формы, характеризующиеся внутриутробной гибелью плода, то прогноз в целом благоприятный при правильном вовремя назначенном лечении.
Имеется ряд профилактических мероприятий, направленных на предотвращение возникновения приобретённых аутоиммунных гемолитических анемий:
- избегать змеиных укусов;
- избегать длительного нахождения в среде с высоким содержанием тяжёлых металлов и токсических веществ;
- при наличии холодовых антител в организме избегать пребывания в среде с низкими температурными условиями.
Также необходимо быть аккуратнее с приёмом таких лекарственных средств, как:
- противомалярийные средства;
- ацетилсалициловая кислота (аспирин);
- сульфаниламиды;
- антибактериальные препараты;
- противотуберкулёзные средства.
Эти препараты могут вызывать гемолиз при недостаточности глюкозо-6-фосфатдегидрогеназы в эритроцитах.
Анемия гемолитическая у детей протекает обычно наиболее выражено, чем у взрослых, так как в таком возрасте симптомы указывают на среднюю или тяжёлую форму заболевания.
Заподозрить гемолитическую анемию можно по следующим симптомам:
- раздражительность;
- плаксивость;
- быстрая утомляемость;
- бледность кожи и слизистых оболочек;
- пожелтение кожи и слизистых оболочек;
- одышка;
- увеличение печени и селезёнки в размерах (крупный живот);
- деформация костей при наличии врождённой формы заболевания (укорочение фаланг пальцев, изменение большеберцовых костей, башенный череп, узкие глазницы).
КЛИНИКО-ЛАБОРАТОРНАЯ ДИАГНОСТИКА АНЕМИЙ
Анемия — это гематологический синдром или самостоятельное заболевание, для которого характерно уменьшение количества эритроцитов и / или содержания гемоглобина в единице объема крови, что приводит к развитию гипоксии тканей.
Патогенетическая классификация анемий .
1. Анемии вследствие кровопотери (постгеморрагические):
2. Анемии вследствие нарушения образования эритроцитов и гемоглобина:
2.1 Анемии, связанные с нарушением образования Нb
— Н арушение реутилизации железа;
2.2 М егалобластн ые анеми и , связанные с нарушением синтеза ДНК или РНК ( В 12-фолиево-дефицитн ые анемии вследствие наследственного дефицита ферментов, участвующих в синтезе пуриновых и пиримидиновых оснований);
— Гипопролиферативн ые анемии
-Анемии, связанные с костномозговой недостаточностью (гипоапластичн ые , рефрактерные анемии при миелодиспластическо м синдроме)
— Метапластические анемии (при гемобластозах, метастазах рака в костный мозг);
— Наследственные (мембранопатии — Миньковского-Шафар а , овалоцитоз; ферментопатии — дефицит глюкозо-6-фосфатдегидрогеназы, пируваткиназы, глутатион-редуктазы; гемоглобинопатии — талассемия, серповидно-клеточная анемия);
-Приобретенные (аутоиммунные, пароксизмальная ночная гемоглобинурия, медикаментозные, травматические и микроангиопатическ ие , в результате отравления гемолитическими ядами и бактериальными токсинами).
Морфологическая классификация (по размерам эритроцитов).
1. Макроцитарная анемия (MCV — mean corpuscular volume-средний объем эритроцита> 100 мкм3, диаметр эритроцита> 8 мкм);
— Мегалобластические (дефицит витамина В12 и фолиевой кислоты, врожденные нарушения синтеза ДНК, лекарственно-индуцированные нарушения синтеза ДНК);
— Немегалобластич еские (ускоренный эритропоэз при гемолитической анемии, увеличение поверхности эритроцитарной мембраны в ответ на кровопотерю, при заболеваниях печени, механической желтухе, после спленэктомии, при микседеме, гипо-апластической анемии, при хронических обструктивных заболеваниях легких, алкоголизме, миелодиспластическ ом синдроме).
2. Микроцитарная анемия (MCV
— Нарушение синтеза гемоглобина (талассемия, гемоглобинопатии);
— Нарушение синтеза порфирина и гема;
— Другие нарушения обмена железа.
3. Нормоцитарная анемия (MCV 81-99 мкм3, диаметр эритроцита 7,2-7,5 мкм):
— Значительное увеличение объема плазмы (беременность, гипергидратация)
— Гипо-, апластические анемии;
— Инфильтративные изменения в костном мозге (лейкемии, множественные миеломы, миелофиброз);
— Эндокринная патология (гипотиреоз, надпочечниковая недостаточность);
По регенераторной способност и красного костного мозга
— Регенераторные (например, острая постгеморрагическая анемия);
— Гиперрегенераторна я (например, приобретенная гемолитическая анемия);
— Гипорегенераторн ая (например, железодефицитная анемия);
— Арегенераторна я (например, апластическая анемия).
1 . Н ормохромная ( Ц П — 0,85-1,05):
— При хронической почечной недостаточности;
— При гипофизарной недостаточности;
— Гипопластическая (апластическая) анемия;
— Анемия при миелодиспластическ м синдроме
— Медикаментозная и лучевая цитостатическая болезнь;
— Анемии при злокачественных новообразованиях, гемобластозах;
— При системных заболеваниях соединительной ткани;
— При хроническом активном гепатите и циррозе печени (кроме хронической постгеморрагической)
— Гемолитические (кроме талассемии);
— Острая постгеморрагическая анемия.
— Фолиево-дефицитная анеми я .
— Анемии с э ритробластичн ы м типом кроветворения (например, железодефицитная анемия);
— Анемии с мегалобластн ым типом кроветворения (например, В-12 и / или фолиево-дефицитная анемия).
— Острые (например, анемии после гемотрансфузионного шока);
— Хронические (например, апластическая анемия).
Железодефицитн ая анеми я
Железодефицитная анемия обусловлена дефицитом железа в сыворотке крови, костном мозге и депо, в результате чего нарушается образование гемоглобина, а затем и эритроцитов.
Этиология. В зависимости от причин, вызывающих дефицит железа, выделяют 5 групп ЖДА.
1 Хронические постгеморрагические ЖДА.
2 ЖДА, связанные с нарушением всасывания и / или недостаточным поступлением в организм с пищей.
3 ЖДА, связанные с недостаточным исходным уровнем железа в организме (чаще у детей).
4 ЖДА, связанные с повышенной потребностью в железе (без кровопотери).
5 ЖДА, связанные с нарушением транспорта железа.
Патогенез. В организме здорового человека в среднем содержится 3 — 5 г железа, 72,9% которого входит в состав гемоглобина (Hb), 3,3% — миоглобина и 16,4% находится в запасах (депо) в виде ферритина (80%) и гемосидерина. Физиологические потери железа составляют 0,6-1,2 мг / сут у мужчин и 1,5- 2 г / сут у женщин и компенсируются за счет железа, попадает с пищей. В пище при обычном питании содержится около 14 мг железа или в виде составляющей гема. (Мясо, рыба), или негемового железа (овощи, фрукты). Стенки кишок содержат фермент гемоксигеназы, который расщепляет гем пищевых продуктов на билирубин, оксид углерода (II) и ионы железа. Органическое железо (Fe +2) хорошо всасывается (до 20-30%), а неорганическое — (Fe +3) — не более 5%. Всего за сутки в верхних отделах тонкой кишки абсорбируется 1-2 мг железа, или 8-15% от того, что содержится в пище. Всасывание железа регулируется клетками кишечника-энтероцитами: увеличивается при дефиците железа и неэффективном эритропоэза и блокируется при избытке железа в организме. Улучшают процесс всасывания аскорбиновая кислота, фруктоза. Абсорбция железа из просвета кишечника происходит с помощью белка — мукозные апотрансферину, который синтезируется в печени и поступает в энтероциты. С энтероцитов выделяется в просвет кишечника, в котором соединяется с железом и снова попадает в энтероцитов. Транспорт от кишечной стенки до предшественников эритроцитов и клеток-депо происходит с помощью белка плазмы — трансферрина. Небольшая часть железа в энтероцитов сочетается с ферритином, который можно считать пулом железа в слизистой тонкой кишки, медленно обменивается. В крови железо циркулирует в комплексе с плазменным белком трансферрином, который синтезируется преимущественно в печени, в небольшом количестве в лимфоидной ткани, молочной железе, тестикулах и яичниках. Трансферрин захватывает железо из энтероцитов, из депо в печени и селезенке и переносит его к рецепторам на еритрокариоцитах костного мозга. Каждая молекула трансферрина может связать два атома железа. У здоровых лиц трансферрин насыщен железом только на одну треть. Мерой количества свободного трансферрина в плазме, который способен полностью насыщаться железом, есть общая железосвязывающая способность. Ненасыщенная железом часть трансферрина обозначается как латентная железосвязывающая способность. Основные запасы железа в организме в течение наиболее длительного времени находятся в печени (в виде ферритина). Также депо есть в селезенке (фагоцитирующими макрофаги), в костном мозге и в незначительном количестве в эпителии кишечника.
Расходы железа на эритропоэз составляют 25 мг в сутки, что значительно превышает возможности всасывания в кишечнике. Поэтому для гемопоэза постоянно используется железо, освободившееся при распаде эритроцитов в селезенке.
Другой формой депонированного железа является гемосидерин-малорастворимое производная ферритина с более высокой концентрацией железа без апоферитиновои оболочки. Гемосидерин накапливается в макрофагах костного мозга, селезенки, купферовських клетках печени.
Таким образом, в организме человека железо распределяется так:
-Железо еритрону (в составе гемоглобина эритроцитов костного мозга и тех, которые циркулируют в крови, -2,8- 2,9 г );
-Железо депо (в составе ферритина и гемосидерина — 0,5- 1,5 г );
-Железо тканевое (миоглобин, цитохромы, ферменты — 0,125 — 0,140 г );
-Железо транспортное (связано с белком крови — трансферрином — 0,003 — 0,004 г ).
Итак, патогенез ЖДА схематично можно отобразить следующим образом:
1) дефицит железа нарушение синтеза гема и гемоглобина анемия
2) дефицит железа нарушение синтеза гема нарушение образования цитохромов нарушения клеточного дыхания (нарушение утилизации кислорода) тканевая гипоксия;
3) дефицит железа нарушение синтеза гема уменьшение активности каталазы нарушения функции антиоксидантных систем активация свободнорадикального окисления повреждения клеток гемолиз эритроцитов и развитие дистрофических изменений в клетках;
4) дефицит железа нарушение синтеза гема уменьшения синтеза миоглобина ухудшение приспособления клеток к гипоксии.
Лабораторная диагностика ЖДА
Диагностика ЖДА основана на анализе данных клинических и лабораторных исследований.
Общий анализ крови с определением количества тромбоцитов и ретикулоцитов, а также определение:
-Среднего объема эритроцита — MCV (mean corpuscular volume-N 75-95мкм3),
— Среднего содержания гемоглобина в эритроцитах-MCH (mean corpuscular hemoglobin-N 24-33 пг),
— Средней концентрации гемоглобина в эритроцитах — MCHC (mean corpuscular hemoglobin concentration — N 30-38%),
— Гистограммы объема эритроцитов, оценивает степень Анизоцитоз — RDW (red cell distribution width).
2. Биохимические исследования.
Определение железа в сыворотке крови, общей железосвязывающей способности сыворотки крови, насыщение железом трансферрина, содержание трансферрина, ферритина в сыворотке крови, Десфераловый тест.
Вычисление показателей миелограммы, определение костномозговых индексов, количества сидеробластов.
4. Исследование свободного протопорфирина в эритроцитах.
В начале заболевания количество эритроцитов не уменьшается, но они уменьшены по размерам (микроциты) и недостаточно насыщены гемоглобином (гипохромия). Уровень снижения гемоглобина опережает уменьшение эритроцитов. Наблюдается низкий цветной показатель (0,7-0,5) и уменьшение MCHС. В мазках крови преобладают небольшие гипохромные эритроциты, анулоциты (эритроциты с отсутствующим гемоглобином в центре в виде колец), неодинакового размера и формы (анизоцитоз, пойкилоцитоза). При тяжелой анемии могут появляться эритробласты. Количество ретикулоцитов не меняется. Но если анемия вызвана острым кровотечением, непосредственно после нее уровень ретикулоцитов повышается, что является важным признаком кровотечения. Осмотическая резистентность эритроцитов мало изменяется или несколько повышена.
Количество лейкоцитов имеет нерезко выраженную тенденцию к снижению, но лейкоцитарная формула не меняется. Уровень тромбоцитов не меняется, только при кровотечениях несколько повышается.
Уровень ферритина сыворотки крови определен радиоиммунным методом, уменьшается уже на прелатентний стадии ЖДА. В норме его содержание составляет 85-130 мкг / л у мужчин и 58-150 мкг / л у женщин.
Уровень железа в сыворотке крови здоровых людей, определяемый по методу Henry, составляет 0,7-1,7 мг / л, или 12,5-30,4 мкмоль / л, при ЖДА он уменьшается до 1,8-5,4 мкмоль / л. Общая железосвязывающая способность плазмы крови (или общий трансферрин сыворотки) увеличивается (N-1,7-4,7 мг / л, или 30,6 -84,6 мкмоль / л). Около трети (30-35%) всего трансферрина сыворотки крови связано с железом (показатель насыщения трансферрина железом). Остальные трансферрина свободная и характеризует скрытую железосвязывающей способность сыворотки крови. У больных ЖДА процент насыщения трансферрином уменьшается до 10-20, при этом увеличивается скрытая железосвязывающая способность плазмы.
В костном мозге — еритробластична реакция с задержкой созревания и гемоглобинизации эритробластов на уровне полихроматофильного нормоцита (количество последних увеличивается). Количество сидеробластов резко уменьшается —
Больным ЖДА проводят Десфераловый тест — определяют количество железа, которое выделяется с мочой после введения 500 мг Десферала (комплексон, продукт жизнедеятельности актиномицетов, который связывает железо). Этот тест позволяет определить депо железа в организме. У здоровых лиц с мочой после введения Десферала выделяется 0,8-1,8 мг железа в сутки. У больных ЖДА этот показатель уменьшается до 0,4 мг и меньше уже на прелатентний стадии дефицита железа. Если же показатель остается нормальным при наличии клинических признаков ЖДА, скорее всего причиной патологического состояния может быть инфекционный или иной воспалительный процесс в организме. Увеличение количества выделенного железа с мочой при наличии анемии свидетельствует о наличии железа в депо без его реутилизации (гемосидероз внутренних органов).
Для установления причин и факторов ЖДА необходимо провести дополнительное обследование:
-Исследовании кислотности желудочного сока (рН-метрия);
-Исследование кала на наличие паразитов;
-Исследование кала на скрытую кровь;
-Рентгенологическое и эндоскопическое (ФЭГДС, при необходимости — ирригоскопия, ректороманоскопия, колоноскопия) исследование пищеварительного тракта;
-Гинекологическое и урологическое обследование больных.
-Наличие анемического и сидеропеничного синдромов;
-Низкий цветной показатель (
-Микроцитоз, пойкилоцитоза, анизоцитоз эритроцитов (в мазке периферической крови);
-Уменьшение средней концентрации Hb в эритроците;
-Уменьшение содержания железа в сыворотке крови;
-Увеличение общей железосвязывающей способности сыворотки
-Увеличение ненасыщенной железосвязывающей способности сыворотки крови;
-Уменьшение количества сидеробластов в костном мозге.
Изменения в полости рта. Основным признаком железодефицитной анемии являются бледность слизистой оболочки. Кроме того, эпителиальные клетки становятся атрофические, с потерей нормального ороговения. Язык может стать гладким в связи с атрофией нитевидных сосочков. В запущенных случаях может развиваться стриктура пищевода, в результате дисфагии. Недавние клинические исследования показали, языковые признаки и симптомы гораздо менее распространены, чем считалось ранее. Гистологическое исследование слизистой оболочки языка показывает уменьшение толщины эпителия, с уменьшением количества клеток, несмотря на увеличение слоя клеток-предшественников. Эти изменения слизистой оболочки могут происходить при отсутствии других явных клинических проявлений.
Мегалобластические анемии — группа анемий, вызванных нарушением синтеза ДНК и РНК в клетках, в результате чего нарушается их размножения; характеризуется мегалобластную типом кроветворения.
Витамин В12 (цианокобаламин) содержится в продуктах животного происхождения — мясе, яйцах, сыре, печени, молоке, почках. В них цианокобаламин связан с белком. При кулинарной обработке, а также в желудке витамин В12 освобождается от белка (в последнем случае — под действием протеолитических ферментов). Недостаток витамина В12 в продуктах, голодание или отказ от употребления продуктов животного происхождения (вегетарианство) нередко обусловливает развиток 12 — дефицитной анемии. Витамин В12, поступающего с пищей, по предложению Кастла (1930), называют «внешним фактором» развития анемии. Париетальные клетки желудка синтезируют термолабильный лужностийкий фактор (его обозначают как «внутренний фактор» Кастла), который представляет собой гликопротеин с молекулярной массой 50 000 — 60 000. Комплекс витамина и гликопротеина связывается со специфическими рецепторами клеток слизистой оболочки средней и нижней частей подвздошной кишки и далее поступает в кровь.
Этиология. Причины, вызывающие развитие названной анемии, могут быть разделены на три группы:
нарушения всасывания витамина В12 в организме:
-Атрофия желез фундального отдела желудка (болезнь Аддисона-Бирмера):
-Опухоли желудка (полипоз, рак);
-Заболевания кишечника (терминальный илеит, дивертикулы, опухоли);
-Оперативные вмешательства на желудке, кишечнике (резекция, гастроктомия)
• повышенные затраты витамина и нарушение утилизации в костном мозге:
-Кишечные паразиты (дифилоботриоз)
-Гемобластозы (острый лейкоз, эритромиелоз, остеомиелофиброз)
• недостаточное поступление витамина В12 в организм с продуктами питания (достаточно редко).
Патогенез. В клетках с витамина В12 образуются две его коферментные формы: метилкобаламин и 5 — дезоксиаденозилкобаламин. Метилкобаламин участвует в обеспечении нормального, еритробластичного кроветворения. Дефицит витамина В12, а в дальнейшем метилкобаламин, приводит к нарушению созревания эпителиальных клеток пищеварительного тракта (они также быстро делятся), что способствует развитию атрофии слизистой оболочки желудка и тонкой кишки с соответствующей симптоматикою.Другий кофермент витамина В12 — 5-дезоксиаденозилкобаламин участвует в обмене жирных кислот путем катализации образования янтарной кислоты с метилмалоновой. Вследствие дефицита витамина В12 образуется избыток метилмалоновой кислоты, которая является токсичной для нервных клеток. Это приводит к нарушению образования миелина в нейронах головного и спинного мозга (особенно задних и боковых его столбов) с последующим расстройством в нервной системе.
Клиника. Наблюдаются 3 основные синдромы:
-Синдром Макроцитарная-мегалобластической анемии.
В периферической крови значительно снижено число эритроцитов, иногда до 0,7 — 0,8 x1012 / л. Они большого размера — до 10 — 12 мкм, часто овальной формы, без центрального просветления. Обычно наблюдаются мегалобласты. Во многих эритроцитах наблюдаются остатки ядра (тельца Жолли) и нуклеолемы (кольца Кебота). Характерные анизоцитоз (преобладают макро-и мегалоциты), пойкилоцитоза, полихроматофилия, базофильная пунктация цитоплазмы эритроцитов. Эритроциты в избытке насыщенные гемоглобином. Цветной показатель повышен более чем на 1,1 — 1,3. Однако общее содержание гемоглобина в крови существенно уменьшается за счет значительного снижения количества эритроцитов. Количество ретикулоцитов обычно уменьшена, реже — нормальная. Наблюдается лейкопения (за счет нейтрофилов), сочетающаяся с полисегментованимы, гигантских размеров нейтрофилами, а также тромбоцитопения. В связи с повышенным гемолизом эритроцитов (всего в кистовому мозга) развивается билирубинемия.
В костном мозге наблюдаются мегалобласты диаметром до 15 мкм, а также мегалокариоциты. Мегалобласты характеризуются десинхронизацией созревания ядра и цитоплазмы. Быстрое образование гемоглобина (уже в мегалобластов) сочетается с опозданием дифференциации ядра. Названные изменения в клетках еритрону сочетаются с нарушением дифференциации и других клеток миелоидного ряда: мегакариобласты, миелоциты, метамиелоциты, Стилус и сегментоядерные лейкоциты, также увеличены по размерам, их ядра имеют более нежную, чем в норме, структуру хроматина.
Следует отметить, что мегалобласты при В12-дефицитной анемии не является особой популяцией клеток, поскольку способны при наличии соответствующей Коферментные формы дифференцировать в обычные еритрокариоциты течение нескольких часов. Это означает, что одна инъекция витамина В12 в состоянии полностью изменить морфологическую картину костного мозга, что иногда приводит к усложнению диагностики заболевания, появления стертой клинической картины.
•-атрофический гастрит (гунтеровський глоссит, лакированный язык);
•-признаки поражения нервной системы (фуникулярный миелоз);
•-снижение количества эритроцитов и Нb;
•-высокий цветной показатель;
•-нормобласты в крови, тельца Жолли и кольца Кебота;
•-ретикулоцитопения (при отсутствии лечения витамином В12);
•-нейтрофилоцитопения, гиперсегментация нейтрофилов;
•-повышенное содержание сывороточного железа, билирубина;
•-признаки мегалобластического кроветворения в миелограмме (мегалобласты в большом количестве, полисегментарнисть нейтрофилов).
В специализированных лабораториях с диагностической целью можно определить: уровень цианокобаламина в сыворотке крови, оценить его функцию всасывания; активность гастрогликопротеиду и найти антитела к нему; повышенный уровень выделения метилмалоновой кислоты с мочой после нагрузки гистидина. Необходимо также провести дополнительные обследования для установления диагноза (ФЭГДС с биопсией для подтверждения атрофии слизистой, при необходимости-колоноскопию, УЗИ ограни брюшной полости).
Фолиевая кислота состоит из птерилинового кольца, парааминобензойной и глутаминовой кислот. Ее запасы в организме составляют 5-20 мг. В отличие от цианокобаламина, запасы которого истощаются при нарушении поступления в организм только через несколько лет, запасы фолиевой кислоты исчерпываются течение 4-5 месяцев.
Этиология. Причины развития фолиево-дефицитной анемии, так же как и В12-дефицитной анемии следует разделить на три группы:
• нарушение всасывания фолиевой кислоты в организме (понос, кишечные инфекции, резекция тонкой кишки, синдром слепой петли, алкоголизм);
• повышенные затраты (беременность, период повышенного роста) и нарушение утилизации в костном мозге (принятие медикаментов, которые являются аналогами или антагонистами фолиевой кислоты — противоэпилептические, химиопрепараты, гемолитические анемии с частыми кризами);
• недостаточное поступление фолиевой кислоты в организм с продуктами питания (у недоношенных новорожденных, при однообразном кормлении порошковым или козьим молоком).
Патогенез. Фолиевая кислота хорошо всасывается преимущественно в верхнем отделе тонкой кишки и превращается в конечном этапе в тетрагидрофолиевую кислоту. Именно последняя является метаболически активной (Коферментные) формой фолиевой кислоты и трансформируется в полиглютаминовий тетрафолиат. Она необходима для регуляции образования тимидинмонофосфату с уридинфосфату (вместе с витамином В12), синтеза пуринов и пиримидинов, т.е. синтеза не только ДНК, но и РНК. Участвует в образовании глютаминовой кислоты из гистидина.
Дефицит фолиевой кислоты приводит к таким же морфологических изменений, как и дефицит витамина В12, т.е. мегалобластического типа кроветворения.
На фолиево-дефицитную анемию чаще страдают лица молодого возраста, беременные женщины. В клинике фолиево-дефицитной анемии так же, как и при В12-дефицитной анемии, выделяют гастроэнтерологический синдром и синдром Макроцитарная-мегалобластической анемии. Симптомы макроцитарной анемии преобладают. Патологические изменения в пищеварительном тракте по сравнению с В12-дефицитной анемией менее выражены.
Диагностическое и дифференциально-диагностическое значение имеют следующие тесты:
• определение содержания фолиевой кислоты в сыворотке крови и эритроцитах (микробиологическим и радиоиммунным методами): в норме содержание фолиевой кислоты в сыворотке колеблется в пределах 3,0-25нг / мл (в зависимости от методики определения), в эритроцитах -100-420 нг / мл . При дефиците фолиевой кислоты ее содержание уменьшается как в сыворотке, так и в эритроцитах, тогда как при В12-дефицитной анемии содержание фолиевой кислоты в сыворотке повышается;
• тест с гистидина: у здоровых лиц основная часть гистидина образует глютаминовую кислоту с мочой выводится 1-18 мг формиминглютаминовои кислоты. Через 8 часов после принятия 15 г гистидина при фолиево-дефицитной анемии с мочой выделяется от 20 до 1500 мг формиминглютаминовои кислоты, что значительно выше, чем при В12-дефицитной анемии. Особенно ее много выделяется у лиц, принимающих метотрексат;
• определение содержания метилмалоновой кислоты в моче: не изменяется при фолиево-дефицитной анемии и значительно увеличивается при В12-дефицитной;
• окраска костного мозга ализарин красным предложено кассу: окрашиваются в красный цвет только мегалобласты, связанные с В12-дефицитной анемией, мегалобласты при дефиците фолиевой кислоты остаются желтыми;
• пробное лечение витамином В12: отсутствие эффекта при фолиево-дефицитной анемии.
Острая постгеморрагическая анемия
Возникает вследствие разрыва или разъедание сосудистой стенки при механической травме, язвенной болезни желудка, туберкулезе легких, бронхоэктатической болезни, злокачественных опухолях, портальной гипертензии.
Картина крови в различные фазы заболевания неодинакова.
Первая фаза — Рефлекторная компенсация (1-2 ч после кровотечения) в связи с поступлением депонированной крови в сосудистое русло и уменьшением ее объема вследствие рефлекторного сужения большого числа капилляров характеризуется нормальными показателями содержания гемоглобина, числа эритроцитов, цветового и других показателей периферической крови.
Ранними признаками кровопотери является тромбоцитоз и лейкоцитоз
Вторая фаза — Гидремична компенсация (первые 1-2 дня) характеризуется восстановлением первоначального объема циркулирующей крови за счет поступления в периферическое сосудистое русло большого количества тканевой жидкости, плазмы. В этой фазе проявляют истинную анемизации без снижения цветового показателя. Наблюдается практически одинаковое снижение содержания гемоглобина, числа эритроцитов, а также уменьшение гематокрита
Третья фаза — Костномозговая фаза компенсации (4-5 суток от начала кровотечения). Наряду со снижением содержания гемоглобина и числа эритроцитов, хранящейся в периферической крови наблюдается ретикулоцитоз. Одновременно может определяться умеренный лейкоцитоз, большое количество молодых форм нейтрофилов (палочкоядерных, метамиелоцитов, иногда — миелоцитов), сдвиг лейкоцитарной формулы влево, а также кратковременный тромбоцитоз.
Итак, острая постгеморрагическая анемия при лабораторными признаками нормохромная, нормоцитарная, гиперрегенераторна.
Хроническая постгеморрагическая анемия
Возникает как следствие длительных повторных кровопотерь у больных с язвенной болезнью желудка и двенадцатиперстной кишки, раком желудка, геморроем, гемофилией, у женщин с маточными кровотечениями.
В костном мозге наблюдаются явления выраженной регенерации, появляются очаги экстрамедуллярного кроветворения. Вследствие истощения запасов железа анемия постепенно приобретает гипохромной характера. В кровь выбрасываются гипохромные эритроциты и микроциты. Со временем еритропоетична функция костного мозга подавляется, и анемия становится гипорегенераторною.
Гемолитические анемии делятся на наследственные (врожденные) и приобретенные.
Наследственные гемолитические анемии
а) мембранопатии (еритроцитопатии) — связанные с нарушением структуры и обновление белковых и липидных компонентов мембран эритроцитов (микросфероцитарна анемия — болезнь Минковского-Шоффара);
б) ферментопатии — связанные с дефицитом эритроцитарных ферментов, обеспечивающих пентозо-фосфатный цикл, гликолиз, синтез АТФ и порфиринов;
в) гемоглобинопатии — связанные с нарушением структуры или синтеза цепей гемоглобина (талассемия, серповидно-клеточная анемия).
Этиология. Генетический дефект мембраны эритроцитов.
Патогенез. Мембранный дефект заключается в высокой проницаемости эритроцитарных оболочек для ионов натрия. Несмотря на активацию калий-натриевого насоса, они пассивно диффундируют внутрь эритроцита и повышают осмотическое давление внутриклеточной среды. В эритроциты направляется вода, и они набирают сферической формы.
Картина крови. Имеет циклическое течение с обострениями и ремиссиями. При гемолитического кризис гемоглобин и эритроциты значительно уменьшаются. КП в норме. Это микроцитарная, нормохромная, гиперрегенераторна анемия. Анизоцитоз, пойкилоцитоза: эритроциты сферической формы, уменьшенные в диаметре, равномерно окрашенные, без зоны просветления. Содержание ретикулоцитов резко повышен. В период обострения — лейкоцитоз с нейтрофилезом, СОЭ ускорена. Осмотическая резистентность эритроцитов снижена. Характерно повышение количества непрямого билирубина в крови.
Кроме микросфероцитоза, в группу мембранопатий относят
1. наследственный елиптоцитоз,
2. наследственный пиропойкилоцитоз, наследственный стоматоцитоз,
3. наследственный акантоцитоз,
4. наследственный ехиноцитоз.
Примером ферментопатии может служить анемия на почве дефицита глюкозо-6-фосфатдегидрогеназы. Болезнь наследуется доминантно, сцеплено с Х-хромосомой. Постоянная анемия наблюдается редко. Как правило, болезнь проявляется гемолитическими кризами после приема некоторых лекарств-сульфаниламидных препаратов (норсульфазола, сульфодиметоксину, этазол, бисептола), противомалярийных (хинина, Акрихин) и противотуберкулезных средств (тубазид, фтивазида, ПАСК). Все названные препараты способны окислить гемоглобин и исключить его из дыхательной функции. У здоровых лиц этого не происходит благодаря существованию антиоксидантной системы, важным компонентом которой является восстановленный глутатион. При дефиците глюкозо-6-фосфатдегидрогеназы количество восстановленного глутатиона уменьшается. Поэтому медикаменты с окислительными свойствами даже в терапевтических дозах окисляют и разрушают гемоглобин. От его молекулы отрывается гем, а цепи глобина выпадают в осадок (тельца Гейнца). Эти включения элиминируются в селезенке, но в процессе их удаления теряется часть поверхности эритроцита, который затем быстро распадается в кровеносном русле. Такую же провоцирующую роль могут сыграть некоторые инфекционные болезни — грипп, вирусный гепатит, сальмонеллез. В отдельных лиц гемолитические кризы возникают после употребления конских бобов или вдыхание пыльцы этого растения (фавизм). Активные факторы конских бобов (Вицин, конвицин) окисляют восстановленный глутатион, уменьшая мощность антиоксидантной системы.
С гемоглобинопатий наиболее распространенная серповидно-клеточная анемия. У таких больных вместо гемоглобина А синтезируется гемоглобин S. Отличается он тем, что глутаминовая кислота в нем замещена валином в шестом положении -цепи. Эта замена резко снижает растворимость гемоглобина в условиях гипоксии. Восстановленный гемоглобин S в 100 раз менее растворим, чем окисленный, и в 50 раз менее растворим от гемоглобина А. В кислой среде он выпадает в осадок в виде кристаллов и деформирует эритроциты, предоставляя им серповидной формы. Мембрана их теряет прочность, и наступает внутрисосудистый гемолиз.
Изменения в полости рта при серповидно-клеточной анемии. Помимо желтухи и бледности слизистой оболочки полости рта, пациенты часто указывают на задержка прорезывания и гипоплазию зубов наряду с общей задержкой. Из-за хронической повышенную активность эритропоэза и гиперплазию костного мозга, которые являются попытками компенсировать гемолиз, повышение просветления в результате уменьшения числа трабекул видно на стоматологических рентгенограммах. Это изменение чаще наблюдается особенно в альвеолярном отростке между корнями зубов, где трабекулы могут отображаться в виде горизонтальных рядов
Картина крови. Серповидно-клеточная анемия.
Когда заторможен синтез — или -цепей гемоглобина, развивается талассемия. Для нее характерны мишенеподибни еритроцити.У гетерозигот развивается так называемая малая талассемия, у гетерозигот — большая талассемия Шары с высшей степенью гемолиза эритроцитов.
Изменения в полости рта при талассемии. При тяжелых формах заболевания разрастаются кости верхней челюсти с участками выпячивание костной ткани вокруг скул, очень бледную кожу. Раннее начало гемолиза, который сопровождается резкой гиперплазией (увеличением массы) костного мозга, приводит к грубым нарушениям в строении лицевой части черепа, нос приобретает седловидной формы, нарушается прикус и расположение зубив.Рентгенографични изменения заметны и в челюстях включая просветление альвеолярных отростков, истончение кортикальной кости , увеличения пространства мозга и грубых трабекул, которые похожи на изменения, наблюдаемые при серповидно-клеточной анемии пациентов. Высокая концентрация железа объясняет изменение цвета зубов у пациентов с β-талассемии.
1. Выраженный анизоцитоз и пойкилоцитоза
2. базофильная зернистость
3. Спорадические клетки-мишени
> 3. Полихроматический эритроциты
> Приобретенные гемолитические анемии
Токсичные гемолитические анемии вызываются гемолитическими ядами. Нитробензол, фенилгидразин, фосфор, соли свинца окисляющие липиды или денатурируют белки оболочек и частично стромы эритроцитов, что ведет к их распаду. Яды биологического происхождения (пчелиный, змеиный, грибная, стрепто-и стафилолизины) имеют ферментативную активность и расщепляют лецитин эритроцитарных мембран.
Иммунные гемолитические анемии возникают вследствие действия антиэритроцитарных антител, вызывающих повреждения и повышенный гемолиз эритроцитов. В зависимости от характера антигена, действующего различают изоиммунные, гетеро иммунные и аутоиммунные гемолитические анемии.
Во изоиммунного анемиями понимают такие, когда в организм извне проникают антитела против эритроцитов или же эритроциты, против которых у больного есть собственные антитела. Пример — гемолитическая анемия плода и новорожденного. Еще один пример изоиммунной гемолитической анемии — гемолиз после трансфузии групповых-или резус-несовместимых эритроцитов.
Картина крови. Содержание гемоглобина и эритроцитов снижен о . Анемия нормохромного типа. Отмечается анизоцитоз эритроцитов, ретикулоцитоз. Осмотическая резистентность эритроцитов снижена. Количество лейкоцитов в норме. СОЭ ускорена.
Гетероимуннимы гемолитическими анемиями называют такие, которые связаны с появлением на поверхности эритроцита нового антигена, который представляет собой комплекс «гаптен-эритроцит». Чаще всего такие комплексные антигены образуются вследствие фиксации на эритроцитах медикаментозных препаратов — пенициллина, цепорин, фенацетина, хлорпромазина, ПАСК. Гаптенами могут быть и вирусы.
При аутоиммунных гемолитических анемиях антитела вырабатываются против собственных неизмененных эритроцитов. Гемолизом усложняются такие болезни, как хронический лимфолейкоз, лимфосаркома, миеломная болезнь, системная красная волчанка, ревматоидный полиартрит, злокачественные опухоли. Эти формы анемии называют симптоматическими, поскольку они возникают на фоне других заболеваний.
Изменения в полости рта. Есть определенные признаки, которые являются общими для всех гемолитических анемий. Следствием гемолиза является анемия-как результат бледность слизистых. Чаще бледность наблюдается на ногтевой пластине и конъюнктиве глаза. Бледность слизистой оболочки полости рта, особенно на мягком небе, языке, и подъязычных тканях наблюдается если анемия прогрессирует. В отличие от некоторых анемий при гемолитической анемии отмечается желтуха вызвана гипербилирубинемией, которая наблюдается при разрушении эритроцитов. Это лучше всего видно в склере, однако и слизистая неба и тканей дна полости рта также становятся желтушные, когда в сыворотке крови увеличивается билирубин.
Апластическая анемия характеризуется недостаточностью кроветворения — гипоклитинним костным мозгом и панцитопенией в периферической крови.
Этиологические факторы апластических анемий:
2. Цитотоксические химические агенты (алкилирующие, бензол и др..). Химические вещества, лекарства (вследствие иммунологически-опосредованного механизма и идиосинкразии (левомицитин, сульфаниламиды, антитиреоидные, антигистаминные препараты, золото, бутадион и др.).
3. Инфекционные вирусные гепатиты В, С, краснуха, инфекционный мононуклеоз, эпидемический паротит, грипп и др.)., Бактериальные инфекции, микозы, паразитарные инвазии (вследствие прямого и иммунологически-опосредованной цитотоксичности)
4. Аутоиммунная деструкция стволовых клеток.
5. Наследственный (генетический) дефект стволовых клеток.
Патогенез. Резкое снижение численности стволовых клеток в костном мозге приводит к дефициту пула созревающих и зрелых форм, проявлением чего является панцитопения в периферической крови, гипоклитиннисть и жировая инфильтрация костного мозга.
Ст е пен и тяжести апластич еской анем ии
источник
