Воробьев С.А. Морфологические особенности и секреторная функция желудка у больных хроническим гастритом на фоне В12-дефицитной анемии. Эксперементальная и клиническая гастроэнтерология. – 2006. – № 4. – с. 11–16.
Морфологические особенности и секреторная функция желудка у больных хроническим гастритом на фоне В12-дефицитной анемии
Известно, что у больных В12-дефицитной анемией нередко наблюдается хронический гастрит, характеризующийся развитием атрофии слизистой оболочки преимущественно в теле желудка и выраженным снижением продукции соляной кислоты вплоть до анацидного состояния [4,8,11,13]. Это связывается с появлением антител к париетальным клеткам желудка и запуском аутоиммунного воспаления [2,7,12]. На основании выявления противожелудочных антител принято обозначать этот гастрит как аутоиммунный или гастрит типа А [17].
Однако, как известно, В12-дефицитная анемия не является однородным по этиологии и патогенезу заболеванием [3,5,14]. В ее развитии, помимо наследственного дефицита внутреннего фактора Кастла и аутоиммунных процессов, имеют значение алиментарный дефицит цианкобаламина, заболевания кишечника, глистная инвазия, препятствующие достаточному поступлению витамина в организм [4,6,11].
Остается до конца не решенным вопрос, является ли наличие аутоантител к париетальным клеткам и внутреннему фактору Кастла у больных В12-дефицитной анемией причиной атрофии слизистой оболочки желудка или же ее следствием [1,2,7,12]. По данным А.Б. Островского [9], лишь у 50% пациентов с В12-дефицитной анемией имеются в крови антитела к париетальным клеткам слизистой оболочки желудка, а ряд исследователей находили их у больных атрофическим гастритом без пернициозной анемии и даже у здоровых людей [7,12,16].
В литературе мы не встретили сведений, касающихся состояния секреторной функции желудка у больных с В12-дефицитной анемией различной этиологии.
С учетом изложенного возникает необходимость дальнейшего детального изучения различных факторов, участвующих в формировании атрофии слизистой оболочки и секреторной недостаточности желудка у больных мегалобластной анемией.
В связи с этим целью работы было выяснение особенностей морфологического состояния, кислото-, пепсиногено-, гастромуко-протеидообразующей функций желудка у больных хроническим гастритом, ассоциированным с В12-дефицитной анемией различной этиологии.
Обследованы 45 больных хроническим гастритом, лечившихся в терапевтическом отделении 4-й городской больницы Твери, и 15 здоровых лиц (добровольцев) для отработки собственных нормативов.
У 25 пациентов (21 женщина и 4 мужчин, средний возраст — 68,5 ± 77 года) хронический гастрит сочетался с В12-дефицитной анемией, а у 20 (17 женщин и 3 мужчин, средний возраст — 66,4 ± 8,4 года) — с железодефицитной анемией.
Больные железодефицитной анемией были обследованы как контрольная группа сравнения для выяснения влияния характера анемического синдрома на морфофункциональное состояние желудка. Учитывая, что у всех больных В12-дефицитной анемией имелся атрофический гастрит, в группу сравнения включались пациенты с железодефицитной анемией, у которых при эндоскопическом и гистологическом исследовании биоптатов слизистой оболочки желудка выявлялось ее атрофическое поражение.
Пациенты с В12-дефицитной анемией в зависимости от возможных этиологических особенностей были разделены на 3 группы: 10 больных имели в анамнезе указание на алиментарный дефицит B12 (строгое соблюдение постов и материальный недостаток). У 8 пациентов — болезнь, вероятнее всего, имела аутоиммунную природу, поскольку клинически проявлялась ярко выраженной типичной триадой симптомов (анемия, гастрит, фуникулярный миелоз) и сочеталась с такими аутоиммунными заболеваниями, как тиреоидит, ревматоидный артрит. У 7 обследованных при колоноскопии была выявлена патология кишечника (у 2 — доброкачественные полипы сигмовидной кишки, у 5 — дивертикулез толстого кишечника).
Диагноз анемии выставлялся с учетом данных клинического анализа крови, оценки эритроцитарных индексов, определения сывороточного железа и общей железосвязывающей способности сыворотки крови, наличия признаков мегалобластного кроветворения в стернальном пунктате.
Данные исследования клинического анализа крови у больных с анемическим синдромом приведены в табл.1.
Таблица 1. Показатели клинического анализа крови у обследованных больных хроническим гастритом с сопутствующим анемическим синдромом
| Показатели | Здоровые | В12-дефицитная анемия | р | Железодефицитная анемия | р1 |
| Лейкоциты, 10 9 /л | 6,2±1,6 | 4,5±1,3 | 6,5±2,1 | 0,001 | |
| Эритроциты, 10 12 /л | 4,6±0,5 | 2,2±0,6 | 3,5±0,6 | ||
| Гемоглобин, г/л | 136±15,2 | 79,5±17,2 | 79,3±13,1 | >0,05 | |
| Гематокрит, % | 41,2±3,2 | 22,1±4,4 | 26,3±4,3 | ||
| Тромбоциты, 10 9 /л | 280±44,1 | 202,2±50,4 | 306,7±81,9 | ||
| Средний размер эритроцита, фл | 88,2±7,3 | 11,5±7,4 | 65,7±4,5 | ||
| Среднее содержание гемоглобина в эритроците, пг | 29,3±2,5 | 37,5±6,5 | 24,7±2,7 | ||
| Средняя концентрация гемоглобина в эритроците, г/дл | 35,1±1,7 | 38,7±1,2 | 29,5±1,3 | ||
| Цветной показатель | 0,91±0,1 | 1,2±0,2 | 0,7±0,1 | ||
| СОЭ, мм/ч | 8,3±4,2 | 21,7±16,5 | 22,5±16,9 | >0,05 |
Примечание: р — достоверность различий со здоровыми лицами; р1 — достоверность различий между группами.
Из данных табл. 1 следует, что в обеих группах у больных подтверждался анемический синдром, имеющий особенности в зависимости от характера заболевания.
Помимо общеклинического обследования, всем больным проводились фиброгастроскопия с прицельной биопсией и гистологическим изучением биоптатов слизистой желудка по визуально-аналоговой шкале Сиднейской модифицированной системы [1], исследование обсемененности слизистой оболочки желудка Helicobacter pylori (HP) и другими микроорганизмами в мазках-отпечатках, окрашенных по Граму, ставился уреазный тест.
Исследование кислотообразующей функции желудка проводили методом внутрижелудочной рН-метрии по В.Н. Чернобровому [15] с использованием аппарата ИАГМ-1 с помощью стандартных рН-зондов и титровочных растворов фирмы «Исток-система».
Результаты рН-метрии по протяженности желудка распределяли в соответствии с функциональными интервалами (ФИ рН) базальной рН-граммы желудка: рН 7,0-7,5 (анацидность — ФИ рН6), рН 3,6-6,9 (выраженная гипоацидность — ФИ рН5), рН 2,3-3,5 (гипоацидность — ФИ рН4), рН 1,6-2,2 (нормоацидность — ФИ рН3), рН 1,3-1,5 (гиперацидность — ФИ рН2), рН 0,9-1,2 (выраженная гиперацидность — ФИ pH1).
При анализе рН-метрии выделяли ФИ рН, на который приходится наибольшее количество точек замера рН по протяженности желудка, так называемый доминирующий функциональный интервал рН-ДФИ.
О пепсиногенобразующей функции желудка судили по содержанию пепсиногена (методика В.Н. Туголукова), а гастромукопротеидобразующей — фукомукопротеидов в сыворотке крови [10]. Забор крови поводили непосредственно перед проведением рН-метрии. Показатели выражали в единицах системы СИ.
Для статистической обработки данных применяли критерий Стьюдента, однофакторный дисперсионный анализ и критерий z (для процентных соотношений). В работе использовали пакет программ «Biostatics» и «Microsoft Office Excel XP».
Установлено, что у всех больных В12-дефицитной анемией при фиброгастроскопии и последующем гистологическом исследовании биоптатов слизистой оболочки желудка выявлен атрофический гастрит. Гастрит на фоне В12-дефицитной анемии характеризовался сочетанным поражением антрального и фундального отделов желудка, в то время как у пациентов на фоне железодефицитной анемии атрофия была менее выражена и в 70% случаев локализовалась только в антральном его отделе (рис. 1).
При микроскопическом исследовании биопатов слизистой оболочки желудка (по визуально-аналоговой шкале Сиднейской модифицированной системы) у больных хроническим гастритом на фоне железодефицитной анемии наблюдалась выраженная лимфоплазмоцитарная и слабая, реже умеренная, нейтрофильная инфильтрация собственной пластинки, слабая и умеренная атрофия желез, в единичных случаях (15%) — кишечная метаплазия. В мазках-отпечатках выявлялась очень низкая обсемененность слизистой оболочки микрофлорой с преимущественным выявлением единичных скоплений стрептококков, стафилококков, энтеробактерий. HP регистрировался в 25% случаев. Уреазный тест был положительным у 30% пациентов.
Хронический гастрит на фоне В12-дефицитной анемии гистологически отличался умеренной или выраженной атрофией, частым (44%) выявлением кишечной метаплазии, слабой, реже умеренной, как лимфоплазмоцитарной, так и нейтрофильной инфильтрацией. В мазках-отпечатках отмечалась низкая обсемененность слизистой оболочки микрофлорой с выявлением единичных скоплений стрептококков, стафилококков, энтеробактерий, лактобактерий, лептотрихий. HP регистрировался в 16% случаев. Уреазный тест был положительным у 24% пациентов. По данным других исследователей [1,16], HP при хроническом гастрите на фоне железодефицитной анемии встречается в 76,9% случаев, а на фоне B12-дефицитной — в 6,5% случаев.
Изучение кислотообразующей функции желудка по анализу результатов интрагастральной рН-метрии показало (рис. 2), что в обеих группах больных хроническим гастритом на фоне анемического синдрома, по сравнению со здоровыми лицами, доминирующие ФИ рН достоверно (р 0,05).
Таблица 2. Пепсиноген плазмы и фукомукопротеиды сыворотки крови у больных атрофическим гастритом на фоне В12— и железодефицитной анемии
| Показатели | Здоровые лица | анемия | р | Железодефицитная анемия | р | р1 |
| Пепсиноген плазмы, мг/л | 75,2±17 ,91 | 29,2±10,2 | 52,7±7,2 | |||
| Фукомукопротеиды сыворотки крови, мг/л | 150,2±32 | 68,0±18,1 | 102,1±22,7 |
Примечание: р — достоверность различий со здоровыми; р1 — между группами больных.
Суммируя изложенное, следует констатировать, что хронический гастрит на фоне В12-дефицитной анемии во всех случаях носил атрофический характер и в большинстве случаев одновременно поражал антральный и фундальный отделы желудка.
Заболевание протекало с существенным снижением кислото-, пепсиногено- и гастромукопротеидообразующей функции желудка, которое имело незначительные особенности в зависимости от этиологии В12-дефицитной анемии.
Только аутоиммунными механизмами трудно объяснить развитие выраженного атрофического процесса и глубокое снижение секреторной функции слизистой оболочки желудка при В12-дефицитной анемии, так как оно имело место и при алиментарном дефиците цианкобаламина и при патологии кишечника.
По-видимому, в развитии гастрического процесса на фоне В12-дефицитной анемии, помимо аутоиммунных механизмов, имеют значение действия различных эндогенных и экзогенных факторов, в том числе влияние гемической гипоксии, нарушения синтеза ДНК и клеточного обновления из-за дефицита цианкобаламина, изменения вегетативной регуляции при фуникулярном миелозе, а также расстройства системного гемостаза и микро-циркуляции. Это позволяет объяснить сходные морфофункциональные нарушения желудка при В12-дефицитной анемии различной этиологии.
Полученные данные указывают на необходимость дальнейшего детального исследования особенностей морфологических и функциональных изменений желудка при хроническом гастрите, протекающем на фоне анемии, в зависимости от ее характера, длительности и степени тяжести, а также с учетом нарушения гемостаза и микрогемоциркуляции.
1. Хронический атрофический гастрит на фоне В12-дефицитной анемии в 68% случаев характеризуется одновременным поражением антрального и фундального отделов желудка, а атрофические изменения на фоне железодефицитной анемии в 70% случаев происходят только в антральном его отделе. Степень выраженности атрофии больше при мегалобластной анемии.
2. Хронический гастрит на фоне В12-дефицитной анемии сопровождается существенным снижением кислото-, пепсиногено- и гастромукопротеиодообразования, более выраженным, чем при сочетании гастрического процесса с железодефицитной анемией.
3. Более выраженное снижение секреторной функции желудка у больных хроническим гастритом на фоне В12-дефицитной анемии, по сравнению с заболеванием, ассоциированным с железодефицитной анемией, может быть обусловлено большей степенью атрофического процесса в слизистой оболочке желудка и частым одновременным поражением его антрального и фундального отделов.
4. Полученные данные следует учитывать при ведении данного контингента больных, выборе лечебного питания и медикаментозной терапии.
1. Аруин Л.И. Морфологическая диагностика болезней желудка и кишечника / Л.И. Аруин, Л.Л. Капуллер, В.А. Исаков. — М.: Триада-Х, 1998. — 496 с.
2. Аруин Л.И. Иммуноморфология желудка / Л.И. Аруин, О.Л. Шаталова // Клин. мед. 1981. № 7. С. 8-14.
3. Григорьев П.Я. Клиническая гастроэнтерология / П.Я. Григорьев, А.В. Яковенко. — М.: МИА, 2001. — 704 с.
4. Демидова А.В. Вопросы диагностики и терапии B12-дефицитной анемии / А.В. Демидова, НА. Сысоева // Клин. мед. 1996. № 1. С. 59-60.
5. Долгов В.В. Лабораторная диагностика анемий / В.В. Долгов, СА. Луговская, В.Т. Морозова, М.Н. Почтарь. — Тверь: Губернская медицина, 2001. — 88 с.
6. Идельсон Л.И. Ошибки в диагностике В12— и фолиеводефицитной анемии / Л.И. Идельсон // Тер. арх. 1986. № 9. С. 144-150.
7. Kиpeeвa O.B. Аутоимунные процессы у больных хроническим гастритом / О.В. Киреева, A.M. Раскин, Б.Г. Лисочкин // Тер. архив. 1974. № 11. С. 104-107.
8. Логинов А.С. Хронический гастрит. Современные аспекты (обзор литературы) / А.С. Логинов, В.Ф. Алексеев, О.С. Радбиль. — М. 1987. — 56 с.
9. Островский А.Б. Иммунопатология хронического гастрита при В12-дефицитной анемии / А.Б. Островский // Тер. архив. 1984. № 10. С. 49-52.
10. Рабинович П.Д. Содержание некоторых Сахаров, связанных с биополимерами в секрете тканей желудка, сыворотке крови и моче при язвенной болезни. / П.Д. Рабинович, СИ. Вайстух, Н.М. Лошакова и др. // Вопр. мед. химии. 1972. № 6. С. 52-58.
11. Рысс Е.С. Анемии и желудочно-кишечный тракт / Е.С. Рысс — М.: Медицина, 1972. — 192 с.
12. Салупере В.П. Проблема хронического гастрита / В.П. Салупере. — Таллин: Валгус, 1978. — 143 с.
13. Циммерман Я.С. Хронический гастрит и язвенная болезнь (Очерки клинической гастроэнтерологии) / Я.С. Циммерман. — Пермь: Изд-во Перм. гос. мед. академии, 2000. — 256 с.
14. Циммерман Я.С. Анемии (вопросы этиологии, классификации, диагностики и дифференцированного лечения) / Я.С. Циммерман, Г.Д. Бабушкина. — Пермь: Изд-во Перм. гос. мед. академии, 2004. — 125 с.
15. Чернобровый В.Н. Экспресс-методика внутрижелудочной рН-метрии / В.Н. Чернобровый // Лаб. дело. 1990. № 3. С. 113-117.
16. Шамгунова Б.А. Клинико-морфологические особенности хронического геликобактерного гастрита у больных железодефицитной и смешанной (железо- и В12-дефицитной) анемией / БА. Шамгунова // Дисс. . канд. мед. наук. — Астрахань. 2001. С. 23.
17. Hamashinma V. Immunohistopathology / V. Hamashinma. — Stuttgart. 1976.
18. Strickland, R.G. / R.G. Strickland, J.R. Mackay // Am. J. Dig. Dis. 1973. Vol. 18. P. 426-440.
Морфологические особенности и секреторная функция желудка у больных хроническим гастритом на фоне В12-дефицитной анемии.
Тверская медицинская академия.
Эксперементальная и клиническая гастроэнтерология. 2006, № 4, с. 11-16.
источник
«ФАРМАТЕКА»; Актуальные обзоры; № 13; 2012; стр. 9-14.
Д.Т. Абдурахманов
Кафедра терапии и профболезней ГБОУ ВПО «Первый МГМУ им. И.М. Сеченова» Минздравсоцразвития РФ, Москва
Обсуждается проблема железодефицитной анемии (ЖДА), развивающейся в т. ч. при заболеваниях желудочно-кишечного тракта. Представлены сведения, касающиеся причин возникновения ЖДА, патогенеза, симптоматики, диагностики и лечения данной патологии. Особое внимание уделено препарату Феринжект (железа карбоксимальтозат), который применяется в комплексной терапии пациентов с ЖДА, обусловленной воспалительными заболеваниями кишечника.
Ключевые слова: железодефицитная анемия, дефицит железа, ферротерапия, железа карбоксимальтозат
The article discusses the problem of iron deficiency anemia (IDA), which develops against the background of many diseases, including gastrointestinal diseases. The data on the causes of IDA, pathogenesis, symptoms, diagnosis and treatment of this disease are presented. Particular attention is paid to the drug Ferinject (ferric carboxymaltosate) used for the treatment of IDA in patients with inflammatory bowel diseases.
Key words: iron deficiency anemia, iron deficiency, ferrotherapy, ferric carboxymaltosate
Наиболее частая в популяции причина анемии — дефицит железа в организме. По данным отчета Всемирной организации здравоохранения (ВОЗ) о состоянии здоровья за 2002 г., железодефицитная анемия (ЖДА) входит в десятку глобальных факторов риска развития нетрудоспособности. Так, показано, что ЖДА встречается среди 30 % населения планеты [1]. В США ЖДА наблюдается среди 5-12 % небеременных женщин и 1-5 % мужчин [2].
Метаболизм железа в организме
Общее количество железа в организме взрослого человека составляет около 3,5-4,0 г, в среднем 50 и 40 мг/кг у мужчин и женщин соответственно. Основная часть железа входит в состав гемоглобина эритроцитов (около 2,5 г), значительная часть железа (около 0,5—1,0 г) депонируется в составе ферритина или входит в состав гемсодержащих и других ферментов (миоглобина, каталазы, цитохромов) организма (около 0,4 г) и небольшая часть железа (0,003—0,007 г) находится в связанном с трансферрином состоянии в крови.
Баланс железа в организме поддерживается соответствием количества поступающего железа его потерям. В пище железо присутствует в составе гема или как негемовое железо. Ежедневно с пищей (стандартный пищевой рацион) в организм человека поступает 10—20 мг железа, из которого в норме в кишечнике всасывается около 10 % (от 3 до 15 %), что компенсирует суточные потери железа, главным образом при слущивании эпителиальных клеток. Организм обеспечивает баланс железа в организме, регулируя процесс его всасывания в кишечнике. В случае развития дефицита железа организм увеличивает процент всасываемого железа (может достигать 25 %), при избытке — уменьшает [3]. В этом процессе ключевое значение придают гепсидину — белку, который синтезируется в печени. Поступление с пищей или выведение железа, как правило, вне контроля организма.
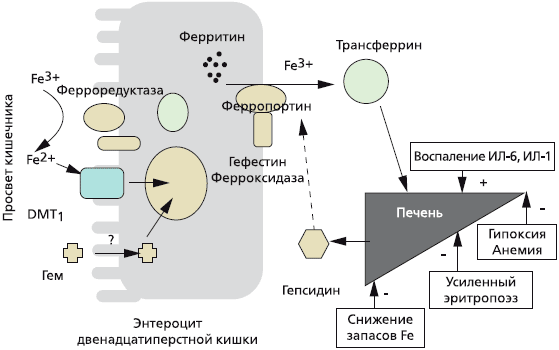
Около 25—30 мг железа ежедневно реутилизируется после разрушения (вследствие старения) эритроцитов в селезенке и поступает снова в костный мозг для синтеза новых эритроцитов. Железо, которое всасывается в кишечнике, предварительно на поверхности энтероцита восстанавливается с участием ферроредуктаз из трехвалентного (Fe 3+ ) в двухвалентнтное (Fe 2+ ), затем с помощью специфического переносчика — транспортера двухвалентных металлов (DMT1) поступает в цитоплазму [4]. Железо в составе гема (содержится в мясе, рыбе) всасывается напрямую. В дальнейшем двухвалентное железо с помощью другого переносчика, ферропортина (также мобилизует железо из ферритина), секретируется в кровь, где снова окисляется до трехвалентного (при участии белка гефестина) и связывается с плазменным белком трансферрином [5]. Трансферрин осуществляет транспорт железа в костный мозг, где оно утилизируется для синтеза эритроцитов, или преимущественно в печень, где железо депонируется в составе ферритина (рис. 1) [6].
При снижении запасов железа, гипоксии, анемии, усиленном эритропоэзе в печени снижается синтез гепсидина, что усиливает всасывание железа в кишечнике, при хроническом воспалении синтез гепсидина в печени увеличивается и, соответственно, всасывание железа в кишечнике снижается.
Рис 1. Регуляция всасывания железа в кишечнике [Guidi G.C., Santonastaso C.L., 2010]
Ферритин — ключевой белок, отражающий запасы железа в организме. Он депонирует железо в нетоксической форме, которое при необходимости мобилизуется. В среднем одна молекула ферритина содержит до 4500 атомов железа. Главным образом железо депонируется в печени, костном мозге и селезенке. Снижение уровня ферритина в сыворотке крови является достаточно надежным показателем дефицита железа в организме, его увеличение, как правило, указывает на перегрузку организма железом. В то же время необходимо помнить, что ферритин относится к белкам острой фазы воспаления, поэтому увеличение его содержания в крови может быть следствием активного воспалительного процесса, а не телько избытка железа. В ряде случаев некоторые злокачественные опухоли обладают способностью синтезировать и секретировать в кровь большое количество ферритина (в рамках паранеопластического синдрома). В норме содержание ферритина в сыворотке крови составляет 30-300 нг/мл.
Причины железодефицитной анемии
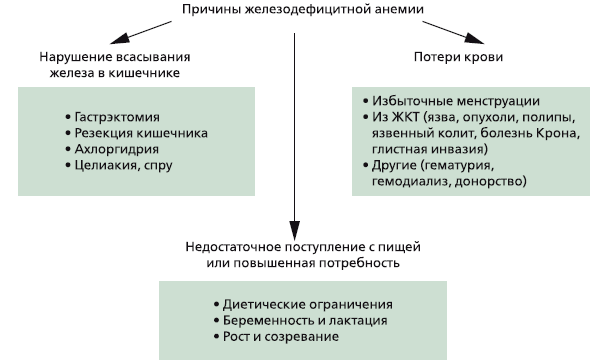
Выделяют три глобальные причины развития дефицита железа в организме (рис. 2):
1. Недостаточное поступление с пищей или повышенная потребность.
2. Нарушение всасывания железа в кишечнике.
3. Хронические потери крови.
Рис 2. Основные причины железодефицитной анемии
В популяции наиболее частой причиной ЖДА является недостаточное поступление с пищей: по данным ВОЗ, от четверти до трети населения в мире хронически голодают из-за нехватки продуктов питания, особенно мясной пищи. Однако в клинической практике среди основных причин ЖДА выделяют хронические потери крови, прежде всего из желудочно-кишечного тракта.
Клиническая картина
При ЖДА наблюдаются общие для всех анемий проявления циркуляторно-гипоксического синдрома:
Кроме того могут встречаться специфические признаки тканевого дефицита железа:
Диагностика
Лабораторная диагностика ЖДА основана на изучении обмена железа и выявлении его дефицита. Выделяют ряд признаков, указывающих на железодефицитный характер анемии (табл. 1).
Лабораторные признаки дефицита железа и ЖДА
| Параметры | Значения при ЖДА | Норма | |
| Железо сыворотки, мкг/дл | 3 | 5 | Примечание. НПВС — нестероидные противовоспалительные средства. Среди причин ЖДА (почти 30-50 % всех случаев) прежде всего рассматривают острые или хронические кровопотери из ЖКТ. Основной причиной ЖДА у женщин до менопаузы являются беременность и менструации, у женщин после менопаузы и у мужчин — хронические (латентные) потери крови из ЖКТ. Анализ кала на скрытую кровь — основной скрининговый метод выявления скрытого желудочно-кишечного кровотечения (тест положительный при выделении не менее 10 мл крови в сутки). При потере не менее 30 мл крови в сутки тест на скрытую кровь бывает положительным в 93 % случаев [8]. Наиболее часто при хронической ЖДА и особенно в случаях положительного результата кала на скрытую кровь выполняют эзофагогастродуодено- (ЭФГДС) и колоноскопию. В 5-10 % случаев анемий, связанных с заболеваниями ЖКТ, при ЭФГДС и колоноскопии не удается выявить очага поражения [9]. В 25 % случаев это обусловлено небольшим размером пораженного участка, который обнаруживается при повторном осмотре, в остальных случаях необходимо обследование тонкой кишки. В последние годы наиболее часто для выявления источника кровотечения из тонкой кишки используется беспроводная капсульная эндоскопия. В 10-17 % случаев причиной ЖДА у мужчин и женщин старше 40 лет являются онкологические заболевания ЖКТ; прежде всего колоректальный рак. ЖДА в течение длительного времени может быть единственным проявлением рака толстой кишки правосторонней локализации, при этом размер опухоли обычно превышает 3 см. Другая наиболее частая причина ЖДА -язвенная болезнь желудка и двенадцатиперстной кишки. При скрытых кровопотерях, обусловленных поражением тонкой кишки, наиболее часто в возрасте до 40 лет выявляют опухоли (лимфому, карциноид, аденокарциному, полипоз), ангиоэктазию артерий (Dieulafoy’s поражение), целиакию и болезнь Крона, в возрасте старше 40 лет -патологию сосудов различной природы и прием НПВС. У трети больных воспалительными заболеваниями кишечника (болезнь Крона, язвенный колит) выявляется анемия, имеющая сложный генез (сочетание ЖДА и анемии хронических заболеваний). При этом дефицит железа становится следствием нескольких причин: Лечение Суточная терапевтическая доза элементарного железа при лечении ЖДА для взрослых составляет в среднем 100— 200 мг в 2—3 приема. Поливитаминные комплексы, содержащие железо, не рекомендуют в качестве лечения ЖДА, т. к. они содержат недостаточное количество железа либо оно плохо всасывается в кишечнике. При адекватном лечении уже в течение первых 3 суток наблюдается увеличение числа ретикулоцитов в крови, на 7—10-й день отмечается ретикулоцитарный криз (пик ретикулоцитоза). К 3—4-й неделе лечения имеет место увеличение уровня гемоглобина на 20 г/л. Прием препаратов железа необходимо продолжать еще в течение 3—6 месяцев после нормализации уровня гемоглобина — пока насыщение трансферрина железом не превысит 30 % и концентрация ферритина не достигнет 50 нг/мл (показатель восстановления тканевых запасов железа). Среди 20—30 % пациентов в результате приема препаратов железа отмечаются различные диспептические расстройства (тошнота, дискомфорт в эпигастрии, диарея или запор). Риск развития желудочно-кишечных расстройств можно снизить, принимая препарат во время еды или на ночь, а также при постепенном увеличении дозы. Среди причин неэффективности пероральных форм железа рассматривают целый ряд факторов [10]: недостаточное поступление железа; Нарушение всасывания железа: Продолжающиеся потери крови или повышенная потребность в железе: Сопутствующие заболевания или состояния: Неправильный диагноз или наличие других причин анемии: Выделяют следующие показания к парентеральному введению, преимущественно внутривенному, препаратов железа: Основная опасность при парентеральном введении железа — развитие тяжелых аллергических реакций, включая анафилактических шок с летальным исходом, которые наблюдаются в 0,6—1,0 % случаев. Данные реакции, в основном, характерны для препаратов железа, содержащих декстран. Среди парентеральных препаратов железа широкое распространение, особенно в комплексной терапии воспалительных заболеваний кишечника, получили сахарат железа и железа карбоксимальтозат (Феринжект), которые в отличие от декстрана железа ассоциируются с минимальным риском развития анафилактических и других аллергических реакций [11—13]. Так, в 2011 г. были опубликованы результаты рандомизированного контролируемого исследования применения железа карбоксимальтозата пациентами с железодефицитной анемией, обусловленной воспалительными заболеваниями кишечника (FERGIcor — a Randomized Controlled Trial on Ferric Carboxymaltose for Iron Deficiency Anemia in Inflammatory Bowel Disease) [14]. В исследовании сравнивали эффективность и безопасность нового режима фиксированной дозы железа карбоксимальтозата (Феринжекта) и индивидуально рассчитываемых доз сахарата железа (СЖ) для пациентов с воспалительными заболеваниями кишечника и ЖДА. В исследование были включены 485 пациентов с ЖДА (уровень ферритина ЛИТЕРАТУРА источник Хронический гастрит в России является одним из наиболее частых заболеваний. Мы традиционно понимаем под термином гастрит наличие какого – либо воспалительного процесса в желудке. Однако это воспаление, во – первых, может иметь различные причины, а во – вторых, может иметь разную интенсивность. Поэтому не все гастриты «одинаково полезны». Некоторые виды гастрита, например атрофический гастрит, очень опасны и могут сопровождаться такими состояниями, как анемия или дефицит железа. При «обычных» видах гастрита, которые встречаются в 80% случаев, стенка желудка становится красной, отечной, толстой, болезненной. Эти виды гастритов раньше называли гастритами с повышенной кислотностью. В таких случаях мы применяем лекарства, уменьшающие воспаление в желудке и снижающие выработку соляной кислоты. Это необходимо, чтобы уменьшить повреждение желудка и восстановить его. И именно в таких ситуациях мы рекомендуем ограничения в питании, исключение жирного, жареного, острого и некоторых других продуктов. А вот у каждого пятого может встречаться противоположная ситуация, которая называется атрофия. При этом стенка желудка становится тоненькой, слабенькой, жиденькой, плохо вырабатывает желудочный сок. Раньше такой гастрит называли гастритом с пониженной кислотностью. Именно атрофический гастрит в течение длительного времени может перерождаться в рак желудка. Именно при атрофическом гастрите очень часто развивается анемия и дефицит железа. Конечно, при любом гастрите может развиться анемия, но при атрофическом гастрите это происходит практически всегда. Самостоятельно по симптомам не всегда возможно отличить один вид гастрита от другого. Для определения типа гастрита необходимо сделать биопсию, то есть забрать очень маленький кусочек слизистой оболочки из желудка и изучить его под микроскопом. Иногда для выявления атрофии можно использовать анализ крови и определение гормонов желудка. Раньше применяли забор желудочного сока или определение кислотности через специальный зонд с датчиками. Сейчас эти методы практически не используются, так как дают очень мало информации. Заподозрить наличие гастрита можно по появлению дискомфорта или болей вверху живота, тяжести, переполненности в желудке, резкому возрастанию аппетита или полному его исчезновению, а в некоторых случаях может появляться изжога или отрыжка. В такой ситуации необходим осмотр живота. При этом атрофический гастрит может быть и вовсе без симптомов! Также как и дефицит железа и анемия могут сопровождаться усталостью, утомляемостью, проблемной кожей, волосами и ногтями, а могут не выдавать себя симптомами. Если при гастрите развилась анемия, это означает, что нужно лечить и анемию, и гастрит. Для восполнения уровня железа в организме используются препараты железа. Практически все препараты, существовавшие до настоящего времени, к сожалению, имели побочное действие на желудок и усиливали в нем воспаление. Поэтому лечить анемию у людей с гастритом было сложной задачей. К счастью, наука не стоит на месте и сейчас уже появились новые препараты, решающие эту проблему. Например, Сидерал Форте. Этот препарат железа не имеет побочных эффектов на желудок, а все железо полностью попадает в организм. Поэтому при анемии и заболеваниях желудочно – кишечного тракта он является главным лекарством. Восполнять железо в организме и лечить гастрит нужно одновременно. Чаще всего к развитию именно атрофического гастрита приводит бактерия хеликобактер. Даже если сейчас у вас ее нет, но она была раньше, дсо временем она могла вызвать атрофию. Лечится хеликобактер с помощью антибиотиков, их назначает врач. Другой частой причиной развития атрофического гастрита является так называемый билиарный рефлюкс, то есть заброс желчи из двенадцатиперстной кишки в желудок. Это сложный для понимания момент, поскольку повреждает желудок в этой ситуации не щелочность желчи, а содержащиеся в ней токсичные желчные кислоты. Чтобы заброс желчи в желудок не происходил необходимо восстановить нормальные сокращения желчного пузыря, его протоков, двенадцатиперстной кишки и, собственно, самого желудка. Для этого используется прокинетик Итомед. Кроме того, важно изменение состава самой желчи и нейтрализация токсичных желчных кислот с помощью Урсосана. Если у вас появились тревожные симптомы нужно сделать общий анализ крови и анализ кала на хеликобактер и обратиться к врачу. Он определит, есть ли необходимость проводить гастроскопию и подберет лечение. Автор: Сергей Вялов, врач – гастроэнтеролог в GMS Clinic, к. м.н. Член Американской гастроэнтерологической ассоциации ( AGA ) и Российской гастроэнтерологической ассоциации ( РГА ) источник Под атрофическим гастритом понимают атрофию клеток секреторных желез и их перерождение. В итоге вместо желудочного сока они синтезируют слизь. Это и объясняет главный признак болезни — воспаление с пониженной кислотностью. Основная опасность данного недуга скрывается в повышенном риске ракового перерождения. Нормальная регенерация клеток регулируется гормонами, ферментами, иммунными реакциями и многими другими регулирующими факторами. Если образование зрелых клеток и их нормальное функционирование нарушается, как это происходит при атрофическом гастрите, вероятность дальнейшего морфологического изменения и малигнезации значительно возрастает. Первый этап заболевания — воспалительный (неатрофический) процесс с повышенной кислотностью (незначительной) — обусловлен усиленным размножением в желудке кислотоустойчивых бактерий Helicobacter pylori. Далее под действием аутоиммунных процессов нарушается формирование зрелых клеток секреторных желез, которые в итоге теряют свою специализацию, а процесс синтеза соляной кислоты постепенно снижается. Хотя вырабатываемая слизь защищает стенки желудка, в процессе пищеварения она никакой роли не играет. До сих пор ученые не смогли установить точную причину активации атрофических процессов в желудке. Достоверно установлены факторы, провоцирующие патологический процесс:
О негативном влиянии несбалансированного питания, злоупотребления жирной/острой пищей и специями, чрезмерного употребления кофе и газированных напитков написано много. Однако многие люди не придают этому значения, подвергая серьезному риску свой организм. Алкогольные напитки, их чрезмерное употребление и никотиновая зависимость — первые враги желудочно-кишечного тракта. Их негативное влияние в первую очередь нацелено на желудок и печень. Это объясняет распространенность процесса среди мужчин, у женщин атрофические изменения встречаются реже. Люди, чьи близкие родственники в предыдущем поколении страдали хроническими заболеваниями ЖКТ, имеют более высокий риск развития атрофического гастрита. Постоянное поступление в организм токсических веществ, включая вредное химическое производство, инактивирует секреторную функцию желудка. Старение организма и угасание всех функций никто не отменял. В патогенезе атрофии слизистой желудка немаловажную роль играет возрастное угасание регенеративной способности клеток. Этим объясняется большинство (60%) зарегистрированных случаев заболевания в возрасте старше 50 лет. Различают несколько видов атрофического гастрита по степени его прогрессирования.
Крайне редко диагностируется смешанный тип гастрита, характеризующийся жировой дегенерацией или формированием кистозных образований в желудке. Выявить атрофическую дегенерацию слизистой желудка на начальном этапе развития болезни достаточно сложно из-за отсутствия яркой симптоматики. Выраженность симптомов нарастает с распространением процесса на все отделы желудка. Зачастую анемия — единственный признак начала атрофии желудочной слизистой. Это связано с отмиранием париетальных клеток, синтезирующих ферменты для нормального пищеварения (пепсиноген, гастромукопротеин, соляную кислоту). Вследствие уменьшения продукции гастромукопротеина снижается всасываемость витамина В12. Анемия сопровождается общей слабостью, головокружениями, головной болью и повышенной утомляемостью. Сопутствующий недостаток витамина С выражается в снижении иммунной защиты и кровоточивости десен, а недостаточность витамина А провоцирует ухудшение зрения и негативно сказывается на состоянии кожи, волос и ногтей. Головокружение, слабость и повышенное потоотделение зачастую возникают после приема пищи, насыщенной углеводами. Тяжесть в области желудка пациент ощущает практически постоянно, при этом дискомфорт становится все более выраженным с развитием заболевания. Отрыжка воздухом, сухость во рту и горький привкус — частые признаки атрофии секреторных желез. С развитием процесса и уменьшением кислотного синтеза отрыжка вызывает тухлый привкус, обусловленный неперевариванием пищи в желудке. Отрыжка и тошнота возникают после каждого приема пищи. При длительно развивающейся атрофии наблюдается специфический признак — «полированный» язык. Обострение симптоматики сопровождается обложенностью языка плотной белой пленкой. Снижение аппетита обусловлено низким уровнем pH, пациенты отмечают быструю насыщаемость и потерю веса. Сбой процесса пищеварения в желудке приводит к появлению метеоризма. Больной жалуется на урчание в животе и частые поносы/запоры. Во время обострения нередко наблюдается обострение температуры, возникают боли в желудке, рвота и понос. Нередки обмороки, спутанность сознания. Хронизация процесса чревата распространением атрофии на 12-перстную кишку, нарушением работы пищевода (рефлюкс), печени, поджелудочной железы, нервной системы и эндокринных желез. Обследование ЖКТ играет важную роль в выявлении атрофических изменений в желудке.
Лечебная тактика при атрофии слизистой желудка подбирается индивидуально и определяется микроструктурными изменениями слизистой, распространенностью процесса и выраженностью клинических проявлений. Возникает вопрос: можно ли вылечить гастрит атрофического типа? Квалифицированные гастроэнтерологи сходятся во мнении: уже сформировавшуюся атрофию секреторных желез желудка излечить нельзя. Однако разработаны достаточно эффективные лечебные схемы, способные предотвратить дальнейшую атрофию и остановить патологический процесс. Обобщенная схема лечения:
Своевременная диагностика, полноценное лечение в виде повторных курсов и строгая диета — неотъемлемые компоненты успешного лечения атрофического гастрита, предотвращающего развитие онкологии. Как лечить атрофическую патологию желудка, дозировку и длительность приема препаратов определяет квалифицированный гастроэнтеролог. Рентгеноскопия желудка – один из методов диагностики различных заболеваний и функциональных расстройств желудочно-кишечного тракта. Рентгеноскопия показана при наличии симптомов заболевания желудочно-кишечной системы:
Также контрастная рентгеноскопия желудка с барием может назначаться при наличии диагностированных заболеваний ЖКТ для определения динамики их течения (язва желудка, доброкачественные и злокачественные опухоли, ахалазия пищевода, пилоростеноз и др.).
Эти противопоказания относительны, так как после улучшения состояния и прекращения кровотечения возможно проведение рентгеноконтрастного исследования желудка. При необходимости рентгеноскопия проводится во II и III семестрах беременности после согласования с акушером-гинекологом. Рентгеноскопия осуществляется лишь в тех случаях, когда невозможно провести эзофагогастроскопию или ее данных недостаточно для постановки диагноза. Подготовка к рентгеноскопии желудка не требует каких-то особых мероприятий. Сначала выполняется обзорная рентгенография грудной и брюшной полости, которая позволяет выявить грубые патологические изменения.
Если предполагается исследовать нижние отделы кишечника, то снимки повторяют через определенные промежутки времени в течение дня.
Расшифровку результатов рентгеноскопии желудка осуществляют рентгенолог и гастроэнтеролог, иногда хирург.
Перечисленные симптомы при их обнаружении не всегда являются основанием для постановки диагноза. Данные рентгеноскопии оцениваются с учетом жалоб, данных объективного обследования, результатов лабораторных и инструментальных методов диагностики.
Рекомендуем прочитать историю Ольги Кировцевой, как она вылечила желудок… Читать статью >> Последние несколько десятилетий колоссальное число людей перестали следить за тем, что они употребляют в пищу. Обилие фаст-фуда и, так называемого, гастрономического мусора не даёт шанса большинству населению России и стран СНГ сделать выбор в пользу здорового и правильного питания, ведь гораздо легче за небольшие деньги и достаточно быстро перекусить в кафе едой не всегда высокого качества. Введение подобной политики питания отрицательно сказывается на состоянии и функционировании желудочно-кишечного тракта (ЖКТ). В большинстве случаев наблюдается проблема отхождения от нормы уровня кислотности желудка. Заболеваний, её вызывающих, достаточно много, однако с уверенностью можно сказать, что устранять недуг надо и это вполне осуществимо своими силами. Пониженный уровень кислотности в ЖКТ свидетельствует о частично или полной дисфункции узлов секреции (как правило, желёз), участвующих в процессе расщепления пищи. Слабая активность продуцирования ферментов пищеварения, расщепляющих кислот и пепсинных соединений – основные признаки плохо работающей секреционной системы желудка. Данное явление негативно влияет на состояние организма. Систематично низкий уровень кислотности в желудке непременно приведёт к чрезмерному накоплению не переварившихся веществ сложной структуры в теле человека, что отрицательно сказывается на его общем самочувствии. Исходя из этого, стоит отметить важность своевременной диагностики и лечения патологии. Нарушенный процесс пищеварения, связанный с низким содержанием соляных кислот в желудочном соке, делает невозможным процесс стабильного обеззараживания пищи от неблагоприятной микрофлоры. Впоследствии это чревато тем, что начинается развитие различных воспалений в ЖКТ.
Наиболее часто пониженный уровень кислотности наблюдается при гастрите определённой этиологии. Понаблюдав и обнаружив у себя указанные выше симптомы, необходимо обратиться к врачу. Для получения полной картины заболевания в каждом индивидуальном случае может потребоваться сделать определённый вид исследования и определения уровня кислотности. Игнорировать подобные мероприятия не стоит, так как помимо обычного гастрита низкий уровень кислотности наблюдается при таких тяжёлых недугах как рак ЖКТ и анацидные гастриты высокой тяжести. Только удостоверившись в диагнозе, можно начинать какие-либо лечебные процедуры, о которых пойдёт речь ниже. Первое, что должен сделать любой человек, страдающий от пониженной кислотности желудка, пересмотреть свой привычный рацион питания и основные его принципы. Важно понимать, что существует огромное количество продуктов, стимулирующих секрецию кислот желудочного сока. К примеру, увеличив приём в пищу варёного кофе, перца чили или корня хрена, можно за короткий период времени повысить кислотность ЖКТ. Однако стоит понимать, что они также отрицательно влияют на состояние желудка, так как могут вызвать усиление симптоматики гастрита или даже язву. Исходя из этого, можно выделить наиболее эффективные и безопасные для систематичного приёма в пищу продукты, которые помогут в борьбе с нестабильностью кислотности вашего ЖКТ. Перечень продуктов таков:
Стоит понимать, что указанные выше продукты окажут реальную помощь лишь в том случае, если общий рацион питания будет правильным и полезным. Важно не принимать в пищу много жирной еды, фаст-фуда и прочего гастрономического мусора. В противном случае эффекта ждать не стоит – неприятная симптоматика останется. Ряд случаев у пациентов с пониженной кислотностью желудка предполагает лечение патологии народным средствами. Однако важно понимать всю серьёзность данного мероприятия, так как только врач в полной мере сможет определить: рациональна ли она в определённом случае или нет. Реального эффекта от лечения при помощи народных средств можно добиться лишь с соблюдением правильного питания. Наиболее эффективные рецепты из народа представлены ниже:
Наилучшим дополнением к любому из видов терапии по повышению уровня кислотности в желудке является систематичный приём минеральной воды. При патологии ЖКТ подобного рода воду необходимо пить медленно за 10-20 минут до еды или же аналогичным образом непосредственно в самом процессе. Прежде чем организовать приём минеральных вод, желательно проконсультироваться с лечащим специалистом, дабы избежать каких-либо проблем. Лечение, как правило, осуществляется некоторыми видами минеральных вод (МВ), а точнее:
Некоторым людям нельзя принимать минеральные воды или делать это можно, но только в небольшом количестве, именно поэтому консультация с врачом — достаточно важное мероприятие. Наибольший терапевтический эффект можно добиться, работая в паре с лечащим специалистом. В заключении, стоит констатировать всю опасность и серьёзность пониженной кислотности ЖКТ. Только своевременная диагностика и правильно организованная терапия помогут вам избежать потенциальных осложнений. Важно понимать, что даже обычный гастрит может трансформироваться в более серьёзные патологии. Указанная выше информация в полной мере даст ответ на вопрос о том, как повысить кислотность желудка народными средства и в целом своими силами. Используя её, каждому под силу побороть неприятную патологию. Здоровья вам! О пониженной кислотности желудка — в видеосюжете: Расскажите друзьям! Расскажите об этой статье своим друзьям в любимой социальной сети с помощью социальных кнопок. Спасибо! источник |